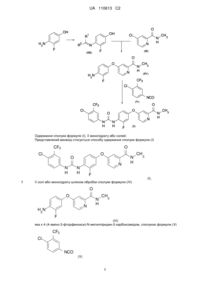
Спосіб одержання 4-{4-[({[4-хлор-3-(трифторметил)феніл]аміно}карбоніл)аміно]-3-фторфенокси}-n-метилпіридин-2-карбоксаміду, його солей і моногідрату
Номер патенту: 110613
Опубліковано: 25.01.2016
Автори: Льогерс Міхаель, Готтфрід Міхаель, Хайльманн Вернер, Резе Йоахім, Штіль Юрген, Віхманн Саскіа
Формула / Реферат
1. Спосіб одержання моногідрату сполуки формули (І)
 , (I)
, (I)
в якому здійснюють обробку сполуки формули (IV)
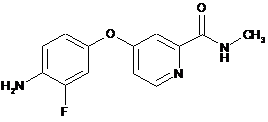 (IV)
(IV)
сполукою формули (V)
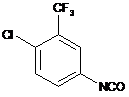 (V)
(V)
у реакційній суміші у прийнятному органічному розчиннику при температурі від 15 °C до 70 °C, і потім розчинену сполуку формули (І) обробляють кислотою, одержуючи сіль сполуки формули (І), яку осаджують з розчину, що містить розчинену сполуку формули (І), а потім вказану сіль сполуки формули (І) обробляють водним розчином основи, осаджуючи моногідрат сполуки формули (І).
2. Спосіб за п. 1, в якому моногідрат сполуки формули (І) осаджують при температурі від 35 °C до 45 °C.
3. Спосіб за п. 1 або 2 одержання сполуки формули (І), в якому моногідрат сушать при пониженому тиску, доки не одержують сполуку формули (І).
4. Спосіб за будь-яким з пп. 1-3, в якому кислоту одержують in situ у реакційній суміші після одержання сполуки формули (І), шляхом додавання до реакційної суміші протонвмісної речовини і прекурсору кислоти.
5. Спосіб за п. 4, в якому кислоту одержують in situ у реакційній суміші після одержання сполуки формули (І), шляхом додавання до реакційної суміші спирту і ацилхлориду.
6. Спосіб за п. 5, в якому спиртом є етанол, а ацилхлоридом є ацетилхлорид.
7. Спосіб за будь-яким з пп. 1-6, в якому сполуку формули (IV) одержують шляхом взаємодії сполуки формули (III)
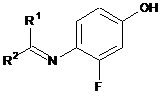 , (III)
, (III)
в якій R1 і R2 незалежно вибрані з групи, що включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, втор-бутил, трет-бутил, н-пентил, 2-пентил, 3-пентил, неопентил, н-гексил, 2-гексил та 3-гексил, або
R1 і R2 з'єднані і взяті разом з атомом вуглецю, до якого вони приєднані, утворючи 4-7-членне циклоалкільне кільце,
зі сполукою формули (II)
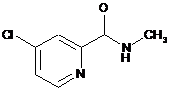 (II)
(II)
у присутності основи, з наступним додаванням кислоти, вивільнюючи сполуку формули (IV).
8. Спосіб за п. 7, в якому сполуку формули (III) використовують у розчині прийнятного органічного розчинника і одержують шляхом взаємодії 4-аміно-3-фторфенолу зі сполукою формули (VI)
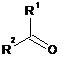 , (VI)
, (VI)
в якій R1 і R2 незалежно вибирають з групи, що включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, втор-бутил, трет-бутил, н-пентил, 2-пентил, 3-пентил, неопентил, н-гексил, 2-гексил та 3-гексил, або
R1 і R2 з'єднані і взяті разом з атомом вуглецю, до якого вони приєднані, утворючи 4-7-членне циклоалкільне кільце.
9. Спосіб за п. 7 або 8, в якому сполуку формули (II) використовують у розчині прийнятного органічного розчинника, де розчин одержують шляхом нейтралізації солі хлорводневої кислоти сполуки формули (II) основою.
10. Спосіб за будь-яким з пп. 7-9, в якому сполуку формули (II) розчиняють у прийнятному органічному розчиннику, обробляють кислотою, яку одержують in situ шляхом додавання протонвмісної речовини і прекурсору кислоти, осаджують у вигляді солі сполуки формули (II) і нейтралізують шляхом додавання водного розчину основи.
11. Спосіб за п. 10, в якому протонвмісною речовиною є спирт, а прекурсором кислоти є ацилхлорид.
12. Суміш сполуки формули (І)
 (I)
(I)
або її моногідрату з однією або більше аніліновими речовинами, кожна у кількості від 0,0001 мас. % до максимального значення 0,05 мас. % у перерахунку на кількість сполуки формули (І).
13. Суміш за п. 12, де анілінова речовина є 4-аміно-3-фторфенолом та/або метиламідом 4-(4-аміно-3-фторфенокси)піридин-2-карбонової кислоти, кожна у кількості від 0,0001 мас. % до максимального значення 0,05 мас. % у перерахунку на кількість сполуки формули (І).
14. Суміш за п. 12, де анілінова речовина є метиламідом 4-(4-аміно-3-фторфенокси)-піридин-2-карбонової кислоти у кількості від 0,0001 мас. % до максимального значення 0,05 мас. % у перерахунку на кількість сполуки формули (І).
Текст
Реферат: Представлений винахід стосується способу одержання 4-{4-[({[4-хлор-3(трифторметил)феніл]аміно}карбоніл)аміно]-3-фторфенокси}-N-метилпіридин-2-карбоксаміду, його солі і моногідрату. UA 110613 C2 (12) UA 110613 C2 UA 110613 C2 5 Представлений винахід стосується способу одержання 4-{4-[({[4-хлор-3(трифторметил)феніл]аміно}карбоніл)аміно]-3-фторфенокси}-N-метилпіридин-2-карбоксаміду, його солей і моногідрату. 4-{4-[({[4-хлор-3-(трифторметил)феніл]аміно}карбоніл)аміно]-3-фторфенокси}-Nметилпіридин-2-карбоксамід зазначений у документі WO 05/009961 і відповідає сполуці формули (I): CF3 O Cl N H 10 O O N N H N H CH 3 F (I) Моногідрат сполуки формули (I) зазначений у документі WO 08/043446. Крім того, солі сполуки формули (I), такі як її гідрохлорид, мезилат та фенілсульфонат зазначені у документі WO 05/009961 і можуть бути утворені обробкою сполуки формули (I) відповідною кислотою. Сполука формули (I) описана для лікування гіперпроліферативних розладів, таких як рак, пухлини, лімфома, саркома та лейкемія. У документі WO 05/009961 описаний спосіб одержання сполуки формули (I), який проілюстрований на наступній схемі: OH O O Cl N N H CH 3 O H N 2 F N H N H N CH 3 2 F CF3 Cl O CF3 Cl NCO N H 15 20 25 30 O O N H N N H CH 3 F У першій стадії 4-аміно-3-фторфенол обробляли трет-бутоксидом калію і додавали 4-хлорN-метил-2-піридинкарбоксамід у N,N-диметилацетаміді, одержуючи метиламід 4-(4-аміно-3фторфенокси)піридин-2-карбонової кислоти, який після виділення, остаточно обробляли 4-хлор3-(трифторметил)фенілізоціанатом у толуолі, одержуючи метиламід 4{4-[3-(4-хлор-3трифторметилфеніл)уреїдо]-3-фторфенокси}піридин-2-карбонової кислоти, який є сполукою формули (I). Хоча способи, розкриті у попередньому рівні техніки, є per se ефективними для одержання сполуки формули (I), її моногідрату, гідрохлориду, мезилату та фенілсульфонату, фактори, такі як чистота, вихід продуктів, ефективність процесу, безпека та економічність залишаються дуже значущими для процесу виробництва фармацевтичного продукту у промислових масштабах. Задача представленого винаходу полягає в забезпеченні способу одержання сполуки формули (I), її солей і моногідрату у промисловому масштабі (в діапазоні від кілограмів до метричних тон), який задовольняє критеріям, які застосовуються у виробництві, і забезпечує покращення у чистоті, сумісність з оточуючим середовищем, промислову придатність, питання забезпечення безпеки та обсяги виходу продукту. При одержанні фармацевтичних препаратів, особлива увага приділяється чистоті і питанням забезпечення безпеки. Ця задача вирішується представленим винаходом. Одержання згідно з винаходом сполуки формули (I) показано у наступній схемі: 1 UA 110613 C2 O OH OH 1 R H N 2 R 2 Cl N H N N F F (III) CH 3 (II) O O N H N H N CH 3 (IV) 2 CF3 F Cl NCO (V) CF3 Cl O O N H O N N H N H CH 3 (I) F Одержання сполуки формули (I), її моногідрату або солей: Представлений винахід стосується способу одержання сполуки формули (I) CF3 O Cl O O N H N N H N H CH 3 F (I), 5 її солі або моногідрату шляхом обробки сполуки формули (IV) O O N H N N H CH 3 2 F (IV) яка є 4-(4-аміно-3-фторфенокси)-N-метилпіридин-2-карбоксамідом, сполукою формули (V) CF3 Cl NCO (V) 2 UA 110613 C2 5 10 15 20 25 30 35 40 45 50 55 яка є 4-хлор-3-трифторметилфенілізоціанатом у реакційній суміші, і потім, розчинену сполуку формули (I) обробляють кислотою, одержуючи сіль сполуки формули (I), яка осаджується з розчину, що містить розчинену сполуку формули (I), при необхідності, сіль сполуки формули (I) потім обробляють водним основним розчином, осаджуючи моногідрат сполуки формули (I) і, при необхідності, моногідрат сушать при пониженому тиску, до тих пір, доки не одержують сполуку формули (I). Сіль сполуки формули (I) може бути одержана шляхом обробки сполуки формули (IV) сполукою формули (V) у реакційній суміші і потім розчинену сполуку формули (I) обробляють кислотою, одержуючи сіль сполуки формули (I), яка осаджується з розчину, що містить розчинену сполуку формули (I). Моногідрат сполуки формули (I) може бути одержаний шляхом обробки сполуки формули (IV) сполукою формули (V) у реакційній суміші і потім розчинену сполуку формули (I) обробляють кислотою, одержуючи сіль сполуки формули (I), яка осаджується з розчину, що містить розчинену сполуку формули (I), сіль сполуки формули (I) потім обробляють водним основним розчином, осаджуючи моногідрат сполуки формули (I), переважно при температурі 35 °C-45 °C, більш переважно 38 °C-42 °C. Cполука формули (I) може бути одержана шляхом обробки сполуки формули (IV) сполукою формули (V) у реакційній суміші і потім розчинену сполуку формули (I) обробляють кислотою, одержуючи сіль сполуки формули (I) яка осаджується з розчину, що містить розчинену сполуку формули (I), сіль сполуки формули (I) потім обробляють водним основним розчином, осаджуючи моногідрат сполуки формули (I) і моногідрат сушать при пониженому тиску, до тих пір, доки не одержують сполуку формули (I), переважно при температурі 85 °C-120 °C і переважно при тиску нижче 30 мбар. Відповідно до способів, описаних вище, розчин, що містить розчинену сполуку формули (I) і осаджену сіль сполуки формули (I), може бути переважно реакційною сумішшю або може бути окремим розчином, що містить сполуку формули (I). Окремий розчин може бути одержаний після відокремлення сполуки формули (I) від реакційної суміші, наприклад, за допомогою стандартних процедур розділення продукту, як описано, наприклад, у документі WO 05/009961 і розчинення сполуки формули (I) у прийнятному органічному розчиннику. У переважному втіленні способу одержання сполуки формули (I), її моногідрату або солі, як описано вище, кислоту одержують in situ у розчині, що містить розчинену сполуку формули (I), шляхом додавання до реакційної суміші протонвмісної речовини і прекурсору кислоти. У більш переважному способі одержання сполуки формули (I), її моногідрату або солі кислоту одержують in situ у реакційній суміші після одержання сполуки формули (I) шляхом додавання до реакційної суміші спирту прекурсору кислоти. У найбільш переважному способі одержання сполуки формули (I), її моногідрату або солі кислоту одержують in situ у реакційній суміші після одержання сполуки формули (I) шляхом додавання до реакційної суміші спирту і ацилхлориду, переважно ацетилхлориду. У способі одержання сполуки формули (I), її моногідрату або солі, реакцію сполуки формули (IV) з сполукою формули (V) здійснюють у прийнятному органічному розчиннику, наприклад, у тетрагідрофурані, при температурі вище 15 °C і нижче 70 °C, переважно при температурі 15 °C60 °C, більш переважно 15 °C-50 °C, більш переважно при кімнатній температурі. Перевага надається спочатку завантаженню сполуки формули (IV) у прийнятний органічний розчинник, наприклад, у тетрагідрофуран і примішуванню протягом 30-300 хвилин, переважно протягом 60150 хвилин, більш переважно протягом 80-100 хвилин сполуки формули (V), переважно розчиненої або суспендованої у прийнятному органічному розчиннику, наприклад, толуолі, який може відрізнятись від первинного прийнятного органічного розчинника. Після одержання сполуки формули (I) до реакційної суміші додають кислоту. Переважним чином кислоту одержують in situ у реакційній суміші шляхом додавання протонвмісної речовини, наприклад, води та/або спирту, переважно спирту та прекурсору кислоти, переважно ацилхлориду, протягом, наприклад, 5-60 хвилин, переважно протягом 10-30 хвилин, для утворення відповідної кислоти in situ. Переважним чином протонвмісну речовину додають першою. Сіль сполуки формули (I) може бути виділена шляхом осадження. Для одержання моногідрату сполуки формули (I), сіль сполуки формули (I) додатково обробляють водним основним розчином, переважно сумішшю органічного розчинника і водного основного розчину. Моногідрат сполуки формули (I) може бути виділений шляхом осадження, переважно при температурі 35 °C-45 °C, більш переважно 38 °C-42 °C. Для одержання сполуки формули (I) моногідрат сполуки формули (I) сушать переважно при температурі 85 °C-120 °C і при пониженому тиску, більш переважно при тиску нижче 30 мбар. 3 UA 110613 C2 5 10 15 20 25 30 35 40 45 50 55 60 Прийнятні кислоти у способі одержання сполуки формули (I), її моногідрату або солі включають, але не обмежуються ними, мінеральні кислоти, карбонові кислоти та сульфонові кислоти, наприклад, хлорводневу кислоту, бромводневу кислоту, сірчану кислоту, фосфорну кислоту, метансульфонову кислоту, трифторметансульфонову кислоту, етансульфонову кислоту, толуолсульфонову кислоту, бензолсульфонову кислоту, нафталендисульфонову кислоту, оцтову кислоту, пропіонову кислоту, молочну кислоту, винну кислоту, яблучну кислоту, лимонну кислоту, фумарову кислоту, малеїнову кислоту та бензойну кислоту. Перевага надається хлорводневій кислоті, бромводневій кислоті, сірчаній кислоті, фосфорній кислоті, метансульфоновій кислоті, трифторметансульфоновій кислоті, етансульфоновій кислоті, толуолсульфоновій кислоті, бензолсульфоновій кислоті та нафталендисульфоновій кислоті, більша перевага надається хлорводневій кислоті, бензолсульфоновій кислоті, толуолсульфоновій кислоті або метансульфоновій кислоті, найбільша перевага надається хлорводневій кислоті. Солі сполуки формули (I), які є фармацевтично прийнятними солями, включають, але не обмежуються ними, кислотно-адитивні солі мінеральних кислот, карбонових кислот та сульфонових кислот, наприклад, солі хлорводневої кислоти, бромводневої кислоти, сірчаної кислоти, фосфорної кислоти, метансульфонової кислоти, трифторметансульфонової кислоти, етансульфонової кислоти, толуолсульфонової кислоти, бензолсульфонової кислоти, нафталендисульфонової кислоти, оцтової кислоти, пропіонової кислоти, молочної кислоти, винної кислоти, яблучної кислоти, лимонної кислоти, фумарової кислоти, малеїнової кислоти та бензойної кислоти. Перевага надається солям хлорводневої кислоти, бромводневої кислоти, сірчаної кислоти, фосфорної кислоти, метансульфонової кислоти, трифторметансульфонової кислоти, етансульфонової кислоти, толуолсульфонової кислоти, бензолсульфонової кислоти та нафталендисульфонової кислоти, більш переважно солям хлорводневої кислоти, бензолсульфонової кислоти, толуолсульфонової кислоти або метансульфонової кислоти, найбільш переважно солі хлорводневої кислоти. Відповідно до представленого винаходу, спирти є органічними речовинами, що несуть щонайменше одну гідроксильну групу. Спирти включають, але не обмежуються ними, метанол, етанол, н-пропанол, ізопропанол, н-бутанол, втор-бутанол, ізобутанол, н-пентанол, гліцерин або їх суміші. У представленому способі як спирти переважно використовують метанол, етанол та ізопропанол. Для одержання кислоти in situ прийнятні прекурсори кислоти включають, але не обмежуються ними, галогеніди органічних кислот, переважно ацилгалогеніди, такі як ацилхлориди і ацилброміди, більш переважно ацетилхлорид, ацетилбромід, пропіонілхлорид або пропіонілбромід, більш переважно ацетилхлорид. Перевага надається способу, описаному вище, в якому кислоту одержували in situ без води. Прийнятні органічні розчинники у способі одержання сполуки формули (I), її моногідрату або солі включають, але не обмежуються ними, тетрагідрофуран, толуол, етилацетат, діоксан, метил трет-бутиловий етер, диметоксиетан, диметилсульфоксид, диметилформамід, 1-метил-2піролідинон або суміші зазначених розчинників. Більш переважно використовують тетрагідрофуран, толуол і їх суміші. Прийнятні водні основні розчинники у способі одержання моногідрату сполуки формули (I) включають, але не обмежуються ними, водні розчинники гідроксидів лужних металів, гідроксидів лужно-земельних металів, алкоксидів лужних металів, алкоксидів лужно-земельних металів, органічних амінів та амонію, переважно гідроксиду натрію і гідроксиду калію, більш переважно водний розчин гідроксиду натрію. Водний основний розчин може бути змішаний з органічним розчинником, таким як ацетон, етилацетат, тетрагідрофуран, переважно з ацетоном. Відповідно до представленого способу передбачувані побічні продукти, зокрема, анілінові побічні продукти, такі як вихідні сполуки 4-аміно-3-фторфенол і сполука формули (IV), що можуть бути виділені, дуже ефективно утворюють сіль сполуки формули (I), переважно сіль хлорводневої кислоти, тому що солі анілінових побічних продуктів, зокрема, солі сполуки формули (IV), переважно сіль хлорводневої кислоти сполуки формули (IV), не осаджуються за умов згідно з представленим способом і залишаються у фільтраті. Крім того, у випадку, коли кислоту одержують in situ, використовуючи ацилгалогеніди, відповідні ацильовані похідні анілінових побічних продуктів, зокрема, сполуки формули (IV), можуть бути легко виділені із солі сполуки формули (I), переважно із солі хлорводневої кислоти, тому що ацильовані похідні не осаджуються за умов згідно з представленим способом і залишаються у фільтраті. Таким чином, сполука формули (I), її солі та її моногідрат можуть бути одержані дуже високої чистоти. Іншим втіленням представленого винаходу є сполука формули (I), її моногідрат або сіль дуже високої чистоти, що містять або забруднені однією або більше аніліновими речовинами, 4 UA 110613 C2 5 10 15 20 25 30 будь-якою, у кількості, що дорівнює або менше, ніж 0,05 мас. %, що означає від 0,0001 мас. % до максимального значення 0,05 мас. %, переважно будь-якою у кількості, що дорівнює або менше, ніж 0,025 мас %, що означає від 0,0001 мас. % до максимального значення 0,025 мас. %, більш переважно, будь-якою, у кількості, що дорівнює або менше, ніж 0,01 мас. %, що означає від 0,0001 мас. % до максимального значення 0,01 мас. % у перерахунку на кількість сполуки формули (I). Іншими словами, іншим втіленням є суміш сполуки формули (I), її моногідрату або солі з однією або більше аніліновими речовинами, будь-якою, у кількості, що дорівнює або менше, ніж 0,05 мас. %, що означає від 0,0001 мас. % до максимального значення 0,05 мас. %,переважно, будь-якою, у кількості, що дорівнює або менше, ніж 0,025 мас. %, що означає від 0,0001 мас. % до максимального значення 0,025 мас. %, більш переважно, будьякою, у кількості, що дорівнює або менше, ніж 0,01 %, що означає від 0,0001 мас. % до максимального значення 0,01 мас. % у перерахунку на кількість сполуки формули (I). Анілінові речовини включають, але не обмежуються ними, 4-аміно-3-фторфенол, 4-хлор-3трифторметиланілін, метиламід 4-(4-аміно-3-фторфенокси)піридин-2-карбонової кислоти, який є сполукою формули (IV). Перевага надається сполуці формули (I), її моногідрату або солі, що містять або забруднені 4-аміно-3-фторфенолом та/або метиламідом 4-(4-аміно-3-фторфенокси)піридин-2-карбонової кислоти, кожним, у кількості, що дорівнює або менше ніж 0,05 мас. %, що означає від 0,0001 мас. % до максимального значення 0,05 мас. %, переважно, кожним, у кількості, що дорівнює або менше ніж 0,025 мас. %, що означає від 0,0001 мас. % до максимального значення 0,025 мас. %, більш переважно, кожним, у кількості, що дорівнює або менше ніж 0,01 мас. %, що означає від 0,0001 мас. % до максимального значення 0,01 мас. % у перерахунку на кількість сполуки формули (I). Іншими словами, перевага надається суміші сполуки формули (I), її моногідрату або солі з 4-аміно-3-фторфенолом та/або метиламідом 4-(4-аміно-3фторфенокси)піридин-2-карбонової кислоти, кожною аніліновою речовиною, у кількості, що дорівнює або менше, ніж 0,05 мас. %, що означає від 0,0001 мас. % до максимального значення 0,05 мас. %, переважно, кожною, у кількості, що дорівнює або менше ніж 0,025 мас. %, що означає від 0,0001 мас. % до максимального значення 0,025 мас. %, більш переважно, кожною у кількості, що дорівнює або менше ніж 0,01 мас. %, що означає від 0,0001 мас. % до максимального значення 0,01 мас. % у перерахунку на кількість сполуки формули (I). Одержання сполуки формули (IV): Представлений винахід також стосується способу одержання сполуки формули (IV) шляхом взаємодії сполуки формули (III) OH 1 R 2 R N F 35 40 (III) 1 2 в якій R і R незалежно вибрані з групи, що включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, втор-бутил, трет-бутил, н-пентил, 2-пентил, 3-пентил, неопентил, нгексил, 2-гексил та 3-гексил, або 1 2 R і R з'єднані і, взяті разом з атомом вуглецю, до якого вони приєднані, утворюють 4- - 7членне циклоалкільне кільце. з сполукою формули (II) O Cl N 45 N H CH 3 (II) яка є 4-хлор-N-метил-2-піридинкарбоксамідом, у присутності основи, з наступним додаванням кислоти, вивільнюючи сполуку формули (IV). У переважному втіленні способу одержання сполуки формули (IV), сполуку формули (III) використовують у розчині прийнятного органічного розчинника і одержують шляхом взаємодії 4аміно-3-фторфенолу з сполукою формули (VI) 5 UA 110613 C2 1 R 2 R 5 10 15 20 25 30 35 40 45 50 55 O (VI) 1 2 в якій R і R незалежно вибрані з групи, що включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, втор-бутил, трет-бутил, н-пентил, 2-пентил, 3-пентил, неопентил, нгексил, 2-гексил та 3-гексил, або 1 2 R і R з'єднані і, взяті разом з атомом вуглецю, до якого вони приєднані, утворюють 4- - 7членне циклоалкільне кільце. У ще одному переважному втіленні способу одержання сполуки формули (IV), сполуку формули (II) використовують у розчині прийнятного органічного розчинника, де розчин одержують шляхом нейтралізації солі хлорводневої кислоти сполуки формули (II) основою, переважно гідроксидом натрію, більш переважно водним розчином гідроксиду натрію. У способі одержання сполуки формули (IV) 4-аміно-3-фторфенол взаємодіє зі сполукою формули (VI) при температурі від 20 °C до температури кипіння, переважно від 50 °C до температури кипіння, більш переважно при температурі кипіння сполуки формули (VI), яка може використовуватись у надлишку та як розчинник. Необов'язково може бути доданий додатково інший розчинник, такий як толуол, етилацетат, циклогексан або їх суміші. Леткі реакційні компоненти можуть бути видалені шляхом азеотропної перегонки, необов'язково при пониженому тиску. Одержана сполука формули (III) може використовуватись у розчині прийнятного органічного розчинника, переважно у розчині 1-метил-2-піролідинону, і оброблена 4-хлор-N-метил-2-піридинкарбоксамідом, переважно використовуваним у розчині прийнятного органічного розчинника, більш переважно у розчині 1-метил-2-піролідинону, у присутності основи. Реакційну суміш нагрівають до температури від 50 °C до 150 °C, переважно від 80 °C до 120 °C. Через 1-5 годин, переважно 2-4 години, температуру доводять від 50 °C до 90 °C, переважно від 70 °C до 90 °C, і додають кислоту, переважно оцтову кислоту у воді. Після охолодження, переважно до температури від 0 °C до 10 °C, і необов'язково вносять затравку кристалами сполукиформули (IV), сполука формули (IV) може бути виділена шляхом осадження. 1 2 Перевага надається сполуці формули (VI), в якій R і R незалежно вибрані з метилу, етилу, 1 2 н-пропілу, ізопропілу, н-бутилу, ізобутилу, втор-бутилу або R і R з'єднані і, взяті разом з атомом вуглецю, до якого вони приєднані, утворюють 4- - 7- членне циклоалкільне кільце. Більш переважно сполуку формули (VI) вибирають з групи, що включає 4-метил-2-пентанон, 3-метил2-бутанонон, 2-бутанонон, 2-пентанон, 4-гептанон, 2,4-диметил-3-пентанон та циклогексанон. Прийнятні органічні розчинники у способі одержання сполуки формули (IV) включають, але не обмежуються ними, 1-метил-2-піролідинон, диметилформамід, N,N-диметилацетамід, диметилсульфоксид, сульфолан або суміші зазначених розчинників. Перевага надається використанню 1-метил-2-піролідинону та/або диметилформаміду. У способі одержання сполуки формули (IV) прийнятними основами є гідроксиди лужних металів і алкоксиди лужних металів. Перевага надається трет-бутоксиду калію. трет-Бутоксид калію переважно використовують у розчині, більш переважно у розчині тетрагідрофурану. Для забезпечення високоочищеного варіанту сполуки формули (II), її розчиняють у прийнятному органічному розчиннику, обробляють кислотою, яку одержують in situ шляхом додавання протонвмісної речовини і прекурсору кислоти, осаджують у вигляді солі сполуки формули (II), переважно солі хлорводневої кислоти сполуки формули (II), і нейтралізують шляхом додавання водного розчину основи. Для цієї цілі, вихідну сполуку, 4-хлор-N-метил-2-піридинкарбоксамід розчиняють у прийнятному органічному розчиннику, переважно у толуолі, і обробляють кислотою, яку одержують in situ, шляхом додавання протонвмісної речовини, наприклад, води та/або спирту, переважно спирту, і прекурсору кислоти, переважно ацилхлориду, наприклад, протягом 5-60 хвилин, переважно протягом 10-30 хвилин, для одержання відповідної кислоти in situ. Переважно протонвмісну речовину додають першою. Сіль 4-хлор-N-метил-2піридинкарбоксаміду, переважно сіль хлорводневої кислоти 4-хлор-N-метил-2піридинкарбоксаміду, може бути виділена шляхом осадження. Таку очищену сіль 4-хлор-Nметил-2-піридинкарбоксаміду розчиняють у прийнятному органічному розчиннику, переважно у толуолі, і нейтралізують шляхом додавання водного розчину основи, переважно водного розчину гідроксиду натрію. Після відокремлення органічних фаз, органічну фазу необов'язково 6 UA 110613 C2 5 10 15 20 25 30 35 40 45 концентрують при пониженому тиску і додають прийнятний органічний розчинник, переважно 1метил-2-піролідинон, одержуючи розчин, який може безпосередньо використовуватись для одержання сполуки формули (IV), як описано вище. Прийнятні органічні розчинники у способі одержання 4-хлор-N-метил-2-піридинкарбоксаміду включають, але не обмежуються ними, тетрагідрофуран, толуол, етилацетат, діоксан, метил трет-бутиловий етер, диметоксиетан, диметилсульфоксид, диметилформамід, 1-метил-2піролідинон або суміші зазначених розчинників. Більш переважно використовують тетрагідрофуран, толуол і їх суміші. Відповідно до представленого винаходу, спирти є органічними речовинами, що несуть щонайменше одну гідроксильну групу. Спирти включають, але не обмежуються ними, метанол, етанол, н-пропанол, ізопропанол, н-бутанол, втор-бутанол, ізобутанол, н-пентанол, гліцерин або їх суміші. У представленому способі як спирти переважним чином використовують метанол, етанол, ізопропанол. Для одержання кислоти in situ прийнятні прекурсори включають, але не обмежуються ними, галогеніди органічних кислот, переважно ацилгалогеніди, такі як ацилхлориди і ацилброміди, більш переважно ацетилхлорид, ацетилбромід, пропіонілхлорид або пропіонілбромід, більш переважно ацетилхлорид. Перевага надається одержанню кислоти in situ без води. Альтернативно, сполука формули (II) і її сіль хлорводневої кислоти можуть бути одержані, як описано у документі WO 05/009961 або у Bankston et al. (Organic Process Research & Development, 2002, 6, 777-781). Сполука формули (V), яка є 4-хлор-3-трифторметилфенілізоціанатом, може бути одержана, як описано у документі WO 00/42012. Скорочення: ДХІ Десорбційна (пряма) хімічна іонізація (у МС) ДМФ диметилформамід ДМСО диметилсульфоксид ЕУ іонізація електронним ударом (у МС) ESI іонізація методом електророзпилення (у МС) год. година(и) хв. хвилина(и) т.п. Температура плавлення МС Масспектрометрія ЯМР спектроскопія протонним ядерним резонансом ТГФ тетрагідрофуран Робочі приклади: 1 H-ЯМР спектри реєстрували при кімнатній температурі, використовуючи спектрометри від фірми Bruker. Дейтерій диметилсульфоксид використовували як розчинник, що включає тетраметилсилан як внутрішній стандарт (якщо не зазначено інше). МС спектри реєстрували, використовуючи спектрометри від Waters і Applied Biosystems. Встановлювали відносну інтенсивність сигналу (у відсотках на основі базисного піку). ВЕРХ здійснювали, використовуючи HP 1100 від фірми Hewlett Packard. Певні умови викладені у відповідних робочих прикладах. Одержання 4-{4-[({[4-хлор-3-(трифторметил)феніл]аміно}карбоніл)аміно]-3-фторфенокси}-Nметилпіридин-2-карбоксаміду, його гідрохлориду та його моногідрату Стадія 1: гідрохлорид 4-хлор-N-метилпіридин-2-карбоксаміду: 420 г розчину 4-хлор-N-метилпіридин-2-карбоксаміду (одержаного відповідно до документу WO2006/034796) у толуолі (приблизно 30 % мас./мас.) і 48,8 г етанолу поміщали до реакційної колби. Додавали 67,2 г ацетилхлориду, перемішуючи до такого ступеню, щоб температура реакційної суміші не перевищувала 30 °C. Після додаткового перемішування при кімнатній температурі протягом 1,5 год., продукт відфільтровували, промивали толуолом (212 г) і сушили при пониженому тиску (30 °C, 80 мбар). Таким чином, одержували 156 г (кількісний вихід) гідрохлориду 4-хлор-N-метилпіридин-2-карбоксаміду. т.п. 173,5-174,5 °C 1 H-ЯМР (500 МГц, ДМСО-d6): δ [млн. ч.] = 2,93 (д, 3H), 7,79 – 7,97 (м, 1H), 8,13 – 8,26 (м, 1H), 8,71 (д, 1H), 9,03 (ш с, 1H), 13,16 (ш с, 1H). + МС [ДХІ, NH3]: m/e=171 [M+H] (M = вільна основа). ВЕРХ: нерухома фаза: наповнювач Nucleodur Gravity C18 (довжина 150 мм, 3 мм ВД, розмір частинок 3,0 мкм); рухома фаза A: 1,15 г діамонийгідрофосфату + 0,68 мл o-фосфорної кислоти 7 UA 110613 C2 5 10 15 20 25 30 35 40 45 50 55 60 (85 % у воді) / 1 л води; рухома фаза B: ацетонітрил; УФ виявлення при 254 нм; температура печі: 45 °C, об'єм впорскування: 3 мл, потік: 0,5 мл/хв.; лінейний градієнт: 5 % B → 80 % B (20 хв.), час утримання 10 хвилин при 80 % B; чистота: >98 % (Rt=17,9 хв.). Стадія 2: 4-(4-аміно-3-фторфенокси)-N-метилпіридин-2-карбоксамід Спосіб 2a: До реакційної колби з мішалкою поміщали 41,4 г гідрохлориду 4-хлор-N-метилпіридин-2карбоксаміду і 100 г толуолу як розчинника. Після додавання 68,4 г води і 19,6 г водного розчину гідроксиду натрію (45 % мас./мас.), реакційну суміш перемішували протягом 30 хвилин. Виділяли дві фази і водний шар відкидали. Органічний шар концентрували шляхом перегонки під вакуумом і замінювали толуол 1-метил-2-піролідиноном (70 г), одержуючи розчин 4-хлор-Nметилпіридин-2-карбоксаміду у 1-метил-2-піролідиноні. До другої реакційної колби з мішалкою поміщали 26,7 г 4-аміно-3-фторфенолу і 100 г 4метил-2-пентанону. При нагріванні до кипіння зі зворотним холодильником і при додатковому перемішуванні протягом 1 години, шляхом азеотропної перегонки видаляли воду. Потім надлишок 4-метил-2-пентанону видаляли шляхом перегонки під вакуумом і замінювали 1метил-2-піролідиноном (70 г), одержуючи розчин, що містить імін, сполуку відповідно до формули (III). До одержаної реакційної суміші додавали розчин 4-хлор-N-метилпіридин-2карбоксаміду у 1-метил-2-піролідиноні. Реакційну суміш нагрівали до приблизно 100 °C. Додавали краплями 123,2 г калій-т-бутоксиду у тетрагідрофурані (20 % мас./мас.) (протягом приблизно 70 хвилин), поки видаляли перегонкою тетрагідрофуран. Після цього реакційну суміш перемішували протягом додаткових 3 годин при 100 °C - завершуючи реакцію. Після доведення до 80 °C, додавали 350 мл толуолу, 392 мл води та 8 г оцтової кислоти. Суміш перемішували протягом 10 хвилин при 80 °C, охолоджували до 50 °C і вносили затравку кристалами 4-(4-аміно-3-фторфенокси)-N-метилпіридин-2-карбоксаміду. Після охолодження до 0 °C суспензію перемішували протягом приблизно 30 хвилин. Продукт відфільтровували, промивали сумішшю метанол / вода (1:3 о/о, 144 мл) і сушили при пониженому тиску (30 °C, 80 мбар). Таким чином, одержували 40,7 г (78 % від теоретичної кількості) 4-(4-аміно-3фторфенокси)-N-метилпіридин-2-карбоксаміду у вигляді коричневих кристалів. т.п. 140,5-141,2 °C 1 H-ЯМР (400 МГц, ДМСО-d6): δ [млн. ч.] = 2,86 (д, 3H), 5,24 – 5,35 (с, 2H), 6,80-6,86 (м, 1H), 6,89 – 6,99 (м, 1H), 7,01-7,09 (м, 1H), 7,09 – 7,15 (м, 1H), 7,45 (д, 1H), 8,49 (д, 1H), 8,75-8,85 (м, 1H). + МС [ES]: m/e=262 [M+H] ВЕРХ: нерухома фаза: наповнювач Agilent Zorbax SB-AQ (довжина 150 мм, 3 мм ВД, розмір частинок 3,5 мкм); рухома фаза A: 1,40 г дикалійгідрофосфату + 5,8 мл o-фосфорної кислоти (8,5 % у воді) / 1 л води; рухома фаза B: ацетонітрил; УФ виявлення при 268 нм; температура печі: 50 °C, об'єм впорскування: 3 мл, потік: 0,8 мл/хв.; лінейний градієнт у дві стадії: (10 хв.), 37 % B → 80 % B (10 хв.), час утримання 10 хвилин при 80 % B; чистота: >97 % (Rt=9,2 хв.). Спосіб 2b: До реакційної колби з мішалкою поміщали 41,4 г гідрохлориду 4-хлор-N-метилпіридин-2карбоксаміду і 100 г толуолу як розчинника. Після додавання 68,4 г води і 19,6 г водного розчину гідроксиду натрію (45 % мас./мас.), реакційну суміш перемішували протягом 30 хвилин. Виділяли дві фази і водний шар видаляли. Органічний шар концентрували шляхом перегонки під вакуумом і толуол замінювали 1-метил-2-піролідиноном (70 г), одержуючи розчин 4-хлор-Nметилпіридин-2-карбоксаміду у 1-метил-2-піролідиноні. До другої реакційної колби з мішалкою поміщали 26,7 г 4-аміно-3-фторфенолу і 100 г 3метил-2-бутанонону. При нагріванні до кипіння зі зворотним холодильником і при додатковому перемішуванні протягом 3 годин, шляхом азеотропної перегонки видаляли воду. Потім видаляли надлишок 3-метил-2-бутанонону шляхом перегонки під вакуумом і замінювали 1метил-2-піролідиноном (70 г), одержуючи розчин, що містить імін, сполуку відповідно до формули (III). До одержаної реакційної суміші додавали розчин 4-хлор-N-метилпіридин-2карбоксаміду у 1-метил-2-піролідиноні. Реакційну суміш нагрівали до приблизно 100 °C. Додавали краплями 123,2 г калій-т-бутоксиду у тетрагідрофурані (20 % мас./мас.) (протягом приблизно 3 години), поки видаляли перегонкою тетрагідрофуран. Потім реакційну суміш перемішували протягом додаткових 2,5 годин при 100 °C – завершуючи реакцію. Після доведення до 80 °C додавали 350 мл толуолу, 392 мл води та 8 г оцтової кислоти. Суміш перемішували протягом 10 хвилин при 80 °C, охолоджували до 50 °C і вносили затравку кристалами 4-(4-аміно-3-фторфенокси)-N-метилпіридин-2-карбоксаміду. Після охолодження до 0 °C, суспензію перемішували протягом приблизно 30 хвилин. Продукт відфільтровували, 8 UA 110613 C2 5 10 15 20 25 30 35 40 45 50 55 60 промивали сумішшю метанол / вода (1:3 о/о, 144 мл) і сушили при пониженому тиску (30 °C, 80 мбар). Таким чином, одержували 44,4 г (84 % від теоретичної кількості) 4-(4-аміно-3фторфенокси)-N-метилпіридин-2-карбоксаміду у вигляді світло-коричневих кристалів. т.п. 142,2-142,8 °C 1 H-ЯМР (400 МГц, ДМСО-d6): δ [млн. ч.] = 2,83 (д, 3H), 5,27 (с, 2H), 6,78-6,85 (м, 1H), 6,866,94 (м, 1H), 7,01-7,07 (м, 1H), 7,09-7,14 (м, 1H), 7,41 (д, 1H), 8,49 (д, 1H), 8,71-8,87 (м, 1H). + МС [ES]: m/e=262 [M+H] ВЕРХ: нерухома фаза: наповнювач Agilent Zorbax SB-AQ (довжина довжина 150 мм, 3 мм ВД, розмір частинок 3,5 мкм); рухома фаза A: 1,40 г дикалійгідрофосфату + 5,8 мл o-фосфорної кислоти (8,5 % у воді) / 1 л води; рухома фаза B: ацетонітрил; УФ виявлення при 268 нм; температура печі: 50 °C, об'єм впорскування: 3 мл, потік: 0,8 мл/хв.; лінейний градієнт у дві стадії: 10 % B → 37 % B (10 хв.), 37 % B → 80 % B (10 хв.), час утримання 10 хвилин при 80 % B; чистота: >99 % (Rt=9,1 хв.). Спосіб 2c: До реакційної колби з мішалкою поміщали 41,4 г гідрохлориду 4-хлор-N-метилпіридин-2карбоксаміду і 100 г толуолу як розчинника. Після додавання 68,4 г води і 19,6 г водного розчину гідроксиду натрію (45 % мас./мас.), реакційну суміш перемішували протягом 30 хвилин. Виділяли дві фази і водний шар відкидали. Органічний шар концентрували шляхом перегонки під вакуумом і толуол замінювали 1-метил-2-піролідиноном (70 г), одержуючи розчин 4-хлор-Nметилпіридин-2-карбоксаміду у 1-метил-2-піролідиноні. До другої реакційної колби з мішалкою поміщали 26,7 г 4-аміно-3-фторфенолу, 73 г циклогексану та 20,6 г циклогексанону. При нагріванні до кипіння зі зворотним холодильником і при додатковому перемішуванні протягом 3 годин, шляхом азеотропної перегонки видаляли воду. Потім розчинник циклогексан і надлишковий циклогексанон видаляли шляхом перегонки під вакуумом і замінювали 1-метил-2-піролідиноном (70 г), одержуючи розчин, що містить імін, сполуку відповідно до формули (III). До одержаної реакційної суміші додавали розчин 4-хлор-Nметилпіридин-2-карбоксаміду у 1-метил-2-піролідиноні. Реакційну суміш нагрівали до приблизно 100 °C. Додавали краплями 126 г калій-т-бутоксиду у тетрагідрофурані (20 % мас./мас.) (протягом приблизно 40 хвилин), під час видалення перегонкою тетрагідрофурану. Після цього реакційну суміш перемішували протягом додаткових 3 годин при 100 °C – завершуючи реакцію. Після доведення до 80 °C, додавали 350 мл толуолу, 392 мл води та 8 г оцтової кислоти. Суміш перемішували протягом 10 хвилин при 80 °C, охолоджували до 50 °C і вносили затравку кристалами 4-(4-аміно-3-фторфенокси)-N-метилпіридин-2-карбоксаміду. Після охолодження до 3 °C, суспензію перемішували протягом приблизно 30 хвилин. Продукт відфільтровували, промивали сумішшю метанол / вода (1:3 о/о, 144 мл) і сушили при пониженому тиску (30 °C, 80 мбар). Таким чином, одержували 40,2 г (76 % від теоретичної кількості) 4-(4-аміно-3фторфенокси)-N-метилпіридин-2-карбоксаміду у вигляді світло-коричневих кристалів. т.п. 141 °C 1H-ЯМР (400 МГц, ДМСО-d6): δ [млн. ч.] = 2,83 (д, 3H), 5,27 (с, 2H), 6,78-6,85 (м, 1H), 6,866,94 (м, 1H), 7,01-7,07 (м, 1H), 7,09-7,14 (м, 1H), 7,41 (д, 1H), 8,49 (д, 1H), 8,71-8,87 (м, 1H). МС [ES]: m/e=262 [M+H]+ ВЕРХ: нерухома фаза: наповнювач Agilent Zorbax SB-AQ (довжина 150 мм, 3 мм ВД, розмір частинок 3,5 мкм); рухома фаза A: 1,40 г дикалійгідрофосфат + 5,8 мл o-фосфорну кислоту (8,5 % у воді) / 1 л води; рухома фаза B: ацетонітрил; УФ виявлення при 268 нм; температура печі: 50 °C, об'єм впорскування: 3 мл, потік: 0,8 мл/хв.; лінейний градієнт у дві стадії: 10 % B → 37 % B (10 хв.), 37 % B → 80 % B (10 хв.), час утримання 10 хвилин при 80 % B; чистота: >98 % (Rt=9,1 хв.). Стадія 3: моногідрат 4-{4-[({[4-хлор-3-(трифторметил)феніл]аміно}карбоніл)аміно]-3-фторфенокси}-Nметилпіридин-2-карбоксаміду До реакційної колби з мішалкою поміщали 20,0 г 4-(4-аміно-3-фторфенокси)-Nметилпіридин-2-карбоксаміду і 180 г тетрагідрофурану як розчинника. Додавали краплями розчин 18,7 г 4-хлор-3-трифторметилфенілізоціанату і 21,1 г толуолу протягом приблизно 90 хвилин при кімнатній температурі. Одержаний розчин перемішували протягом 3 годин, завершуючи реакцію. Потім до реакційної суміші додавали 30 г тетрагідрофурану і 7,8 г метанолу. До реакційної суміші краплями додавали наступні 9,0 г ацетилхлориду протягом 15 хвилин. Після додаткового перемішування протягом приблизно 2 годин, суспензію фільтрували, тверду речовину промивали тетрагідрофураном (18,2 г) і ацетоном (136,4 г). Тверду речовину додавали до суміші ацетону (268,6 г), води (55,8 г) і водного розчину гідроксиду натрію (8,2 г, 45 % мас./мас.) при 40 °C. Суміш перемішували протягом додаткових 30 хвилин. Потім 9 UA 110613 C2 5 10 15 20 25 30 35 40 45 50 55 60 ініціювали кристалізацію шляхом внесення затравочних кристалів моногідрату 4-{4-[({[4-хлор-3(трифторметил)феніл]аміно}карбоніл)аміно]-3-фторфенокси}-N-метилпіридин-2-карбоксаміду. Після охолодження до 20 °C, додавали 31,6 г води. Суспензію охолоджували до приблизно 3 °C і перемішували протягом 30 хвилин. Продукт відфільтровували, промивали холодною сумішшю ацетону (106 г) і води (44 г), і сушили при пониженому тиску (30 °C, 80 мбар). Таким чином, одержували 31,8 г (83 % від теоретичної кількості) моногідрату 4-{4-[({[4-хлор-3(трифторметил)феніл]аміно}карбоніл)аміно]-3-фторфенокси}-N-метилпіридин-2-карбоксаміду у вигляді білих кристалів. 1H-ЯМР (500 МГц, МЕТАНОЛ-d4): δ [млн. ч.] = 2,94 (с, 3H), 6,96-7,01 (м, 1H), 7,05-7,11 (м, 2H), 7,49 – 7,53 (м, 1H), 7,56-7,59 (м, 1H), 7,61-7,65 (м, 1H), 8,00-8,03 (м, 1H), 8,15-8,20 (м, 1H), 8,46-8,51 (м, 1H). + МС [ES]: m/e=483 [M+H] ВЕРХ: нерухома фаза: наповнювач Eclipse XDB-C8 (довжина 150 мм, 2,1 мм ВД, розмір частинок 3,5 мкм); рухома фаза A: 1,0 г натрієвої солі гексан-1-сульфонової кислоти + 1,0 мл трифтороцтової кислоти / 1 л води; рухома фаза B: ацетонітрил; УФ виявлення при 232 нм; температура печі: 43 °C, об'єм впорскування: 3 мл, потік: 0,5 мл/хв.; лінейний градієнт у 3 стадії: 5 % B → 36 % B (14,5 хв.), 36 % B → 44 % B (6 хв.), 44 % B → 80 % B (9,5 хв.), час утримання 10 хвилин при 80 % B; чистота: >99,5 % (Rt=25,7 хв.), характерні передбачувані побічні продукти: 4аміно-3-фторфенол при RRT (відносний час утримання) 0,10: типово < 0,01 % (2,6 хв.), 4-(4аміно-3-фторфенокси)-N-метилпіридин-2-карбоксамід RRT 0,37: типово < 0,01 % (9,5 хв.); RRT 0,46 (4-(3-фтор-4-{[2-(метилкарбамоїл)піридин-4-іл]аміно}фенокси)-N-метилпіридин-2карбоксамід): типово < 0,15 % (11,7 хв.); RRT 0,69 (4-(3-фтор-4-{[(2-фтор-4-{[2(метилкарбамоїл)піридин-4-іл]окси}феніл)карбамоїл]аміно}фенокси)-N-метилпіридин-2карбоксамід): типово 99,5 % (Rt=25,2 хв.), характерні передбачувані побічні продукти: 4аміно-3-фторфенол при RRT (відносний час утримання) 0,10: типово < 0,01 % (2,5 хв.), 4-(4аміно-3-фторфенокси)-N-метилпіридин-2-карбоксаміду RRT 0,36: типово < 0,01 % (9,1 хв.); RRT 0,46 (4-(3-фтор-4-{[2-(метилкарбамоїл)піридин-4-іл]аміно}фенокси)-N-метилпіридин-2 10 UA 110613 C2 5 10 15 карбоксаміду): типово < 0,15 % (11,3 хв.); RRT 0,69 (4-(3-фтор-4-{[(2-фтор-4-{[2(метилкарбамоїл)піридин-4-іл]окси}феніл)карбамоїл]аміно}фенокси)-N-метилпіридин-2карбоксаміду): типово < 0,15 % (17,2 хв.). ВЕРХ (метод аналізу слідів мікродомішок для визначення кількості 4-аміно-3-фторфенолу): нерухома фаза: наповнювач X-Bridge Shield C18 (довжина 150 мм, 3,0 мм ВД, розмір частинок 3,5 мкм); рухома фаза A: 1,5 г дигідрофосфату калію + 0,5 г дикалійгідрофосфат /1 л води; рухома фаза B: ацетонітрил; УФ виявлення при 228 нм; температура печі: 50 °C, об'єм впорскування: 3 мл, потік: 1,0 мл/хв.; час утримання 5 хвилин при 5 % B, лінейний градієнт у 1 стадію: 5 % B → 80 % B (10 хв.), RT 4-аміно-3-фторфенол: 1,7 хв., кількість визначали, використовуючи як зовнішній стандарт 4-аміно-3-фторфенол. ВЕРХ (метод аналізу слідів мікродомішок для визначення кількості 4-(4-аміно-3фторфенокси)-N-метилпіридин-2-карбоксамід): нерухома фаза: наповнювач X-Bridge Shield C18 (довжина 150 мм, 3,0 мм ВД, розмір частинок 3,5 мкм); рухома фаза A: 1,5 г дигідрофосфату калію + 0,5 г дикалійгідрофосфат /1 л вода; рухома фаза B: ацетонітрил; УФ виявлення при 228 нм; температура печі: 50 °C, об'єм впорскування: 3 мл, потік: 1,0 мл/хв.; лінейний градієнт у 1 стадію: 8 % B → 80 % B (15 хв.), RT 4-(4-аміно-3-фторфенокси)-N-метилпіридин-2-карбоксаміду: 7,0 хв., кількість визначали, використовуючи як зовнішній стандарт 4-(4-аміно-3-фторфенокси)N-метилпіридин-2-карбоксамід. 11 UA 110613 C2 ФОРМУЛА ВИНАХОДУ 1. Спосіб одержання моногідрату сполуки формули (І) CF3 O Cl O O N H N H CH3 N N H F 5 , (I) в якому здійснюють обробку сполуки формули (IV) O O N H CH3 N H2 N F (IV) сполукою формули (V) CF3 Cl NCO (V) 10 15 20 25 у реакційній суміші у прийнятному органічному розчиннику при температурі від 15 °C до 70 °C, і потім розчинену сполуку формули (І) обробляють кислотою, одержуючи сіль сполуки формули (І), яку осаджують з розчину, що містить розчинену сполуку формули (І), а потім вказану сіль сполуки формули (І) обробляють водним розчином основи, осаджуючи моногідрат сполуки формули (І). 2. Спосіб за п. 1, в якому моногідрат сполуки формули (І) осаджують при температурі від 35 °C до 45 °C. 3. Спосіб за п. 1 або 2 одержання сполуки формули (І), в якому моногідрат сушать при пониженому тиску, доки не одержують сполуку формули (І). 4. Спосіб за будь-яким з пп. 1-3, в якому кислоту одержують in situ у реакційній суміші після одержання сполуки формули (І), шляхом додавання до реакційної суміші протонвмісної речовини і прекурсору кислоти. 5. Спосіб за п. 4, в якому кислоту одержують in situ у реакційній суміші після одержання сполуки формули (І), шляхом додавання до реакційної суміші спирту і ацилхлориду. 6. Спосіб за п. 5, в якому спиртом є етанол, а ацилхлоридом є ацетилхлорид. 7. Спосіб за будь-яким з пп. 1-6, в якому сполуку формули (IV) одержують шляхом взаємодії сполуки формули (III) R R 2 OH 1 N F , (III) в якій R і R незалежно вибрані з групи, що включає водень, метил, етил, н-пропіл, ізопропіл, нбутил, ізобутил, втор-бутил, трет-бутил, н-пентил, 2-пентил, 3-пентил, неопентил, н-гексил, 2гексил та 3-гексил, або 1 2 R і R з'єднані і взяті разом з атомом вуглецю, до якого вони приєднані, утворючи 4-7-членне циклоалкільне кільце, зі сполукою формули (II) 1 30 2 12 UA 110613 C2 O Cl N H CH3 N 5 (II) у присутності основи, з наступним додаванням кислоти, вивільнюючи сполуку формули (IV). 8. Спосіб за п. 7, в якому сполуку формули (III) використовують у розчині прийнятного органічного розчинника і одержують шляхом взаємодії 4-аміно-3-фторфенолу зі сполукою формули (VI) R 2 R 1 O , (VI) 1 10 15 20 2 в якій R і R незалежно вибирають з групи, що включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, втор-бутил, трет-бутил, н-пентил, 2-пентил, 3-пентил, неопентил, нгексил, 2-гексил та 3-гексил, або 1 2 R і R з'єднані і взяті разом з атомом вуглецю, до якого вони приєднані, утворючи 4-7-членне циклоалкільне кільце. 9. Спосіб за п. 7 або 8, в якому сполуку формули (II) використовують у розчині прийнятного органічного розчинника, де розчин одержують шляхом нейтралізації солі хлорводневої кислоти сполуки формули (II) основою. 10. Спосіб за будь-яким з пп. 7-9, в якому сполуку формули (II) розчиняють у прийнятному органічному розчиннику, обробляють кислотою, яку одержують in situ шляхом додавання протонвмісної речовини і прекурсору кислоти, осаджують у вигляді солі сполуки формули (II) і нейтралізують шляхом додавання водного розчину основи. 11. Спосіб за п. 10, в якому протонвмісною речовиною є спирт, а прекурсором кислоти є ацилхлорид. 12. Суміш сполуки формули (І) CF3 O Cl O O N H N H CH3 N N H F 25 30 (I) або її моногідрату з однією або більше аніліновими речовинами, кожна у кількості від 0,0001 мас. % до максимального значення 0,05 мас. % у перерахунку на кількість сполуки формули (І). 13. Суміш за п. 12, де анілінова речовина є 4-аміно-3-фторфенолом та/або метиламідом 4-(4аміно-3-фторфенокси)піридин-2-карбонової кислоти, кожна у кількості від 0,0001 мас. % до максимального значення 0,05 мас. % у перерахунку на кількість сполуки формули (І). 14. Суміш за п. 12, де анілінова речовина є метиламідом 4-(4-аміно-3-фторфенокси)-піридин-2карбонової кислоти у кількості від 0,0001 мас. % до максимального значення 0,05 мас. % у перерахунку на кількість сполуки формули (І). Комп’ютерна верстка О. Гергіль Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 13
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of 4-{4-[({[4-chloro-3-(trifluoromethyl)-phenyl]amino}carbonyl)amino]-3-fluorophenoxy}-n-methylpyridine-2-carboxamide, its salts and monohydrate
Автори англійськоюStiehl, Juergen, Heilmann, Werner, Loegers, Michael, Rehse, Joachim, Gottfried, Michael, Wichmann, Saskia
Автори російськоюШтиль Юрген, Хайльманн Вернер, Лёгерс Михаэль, Резе Йоахим, Готтфрид Михаэль, Вихманн Саскиа
МПК / Мітки
МПК: C07D 213/81
Мітки: моногідрату, одержання, спосіб, солей, 4-{4-[({[4-хлор-3-(трифторметил)феніл]аміно}карбоніл)аміно]-3-фторфенокси}-n-метилпіридин-2-карбоксаміду
Код посилання
<a href="https://ua.patents.su/15-110613-sposib-oderzhannya-4-4-4-khlor-3-triftormetilfenilaminokarbonilamino-3-ftorfenoksi-n-metilpiridin-2-karboksamidu-jjogo-solejj-i-monogidratu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 4-{4-[({[4-хлор-3-(трифторметил)феніл]аміно}карбоніл)аміно]-3-фторфенокси}-n-метилпіридин-2-карбоксаміду, його солей і моногідрату</a>
Попередній патент: Похідні 1-аміно-2-циклопропілетилборонової кислоти
Наступний патент: Пристрій для обробки даних та спосіб обробки даних
Випадковий патент: Глибокорозпушувач ґрунту