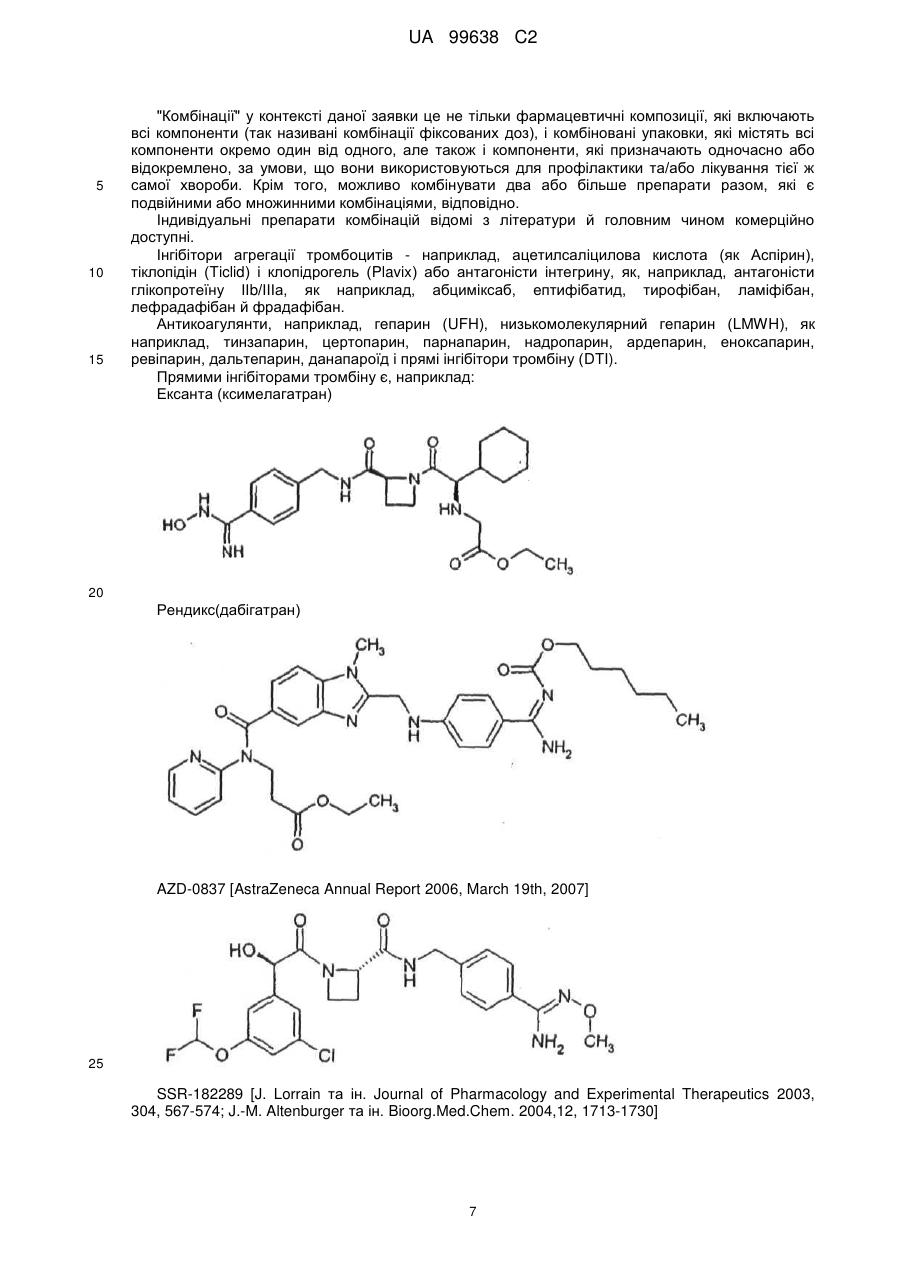
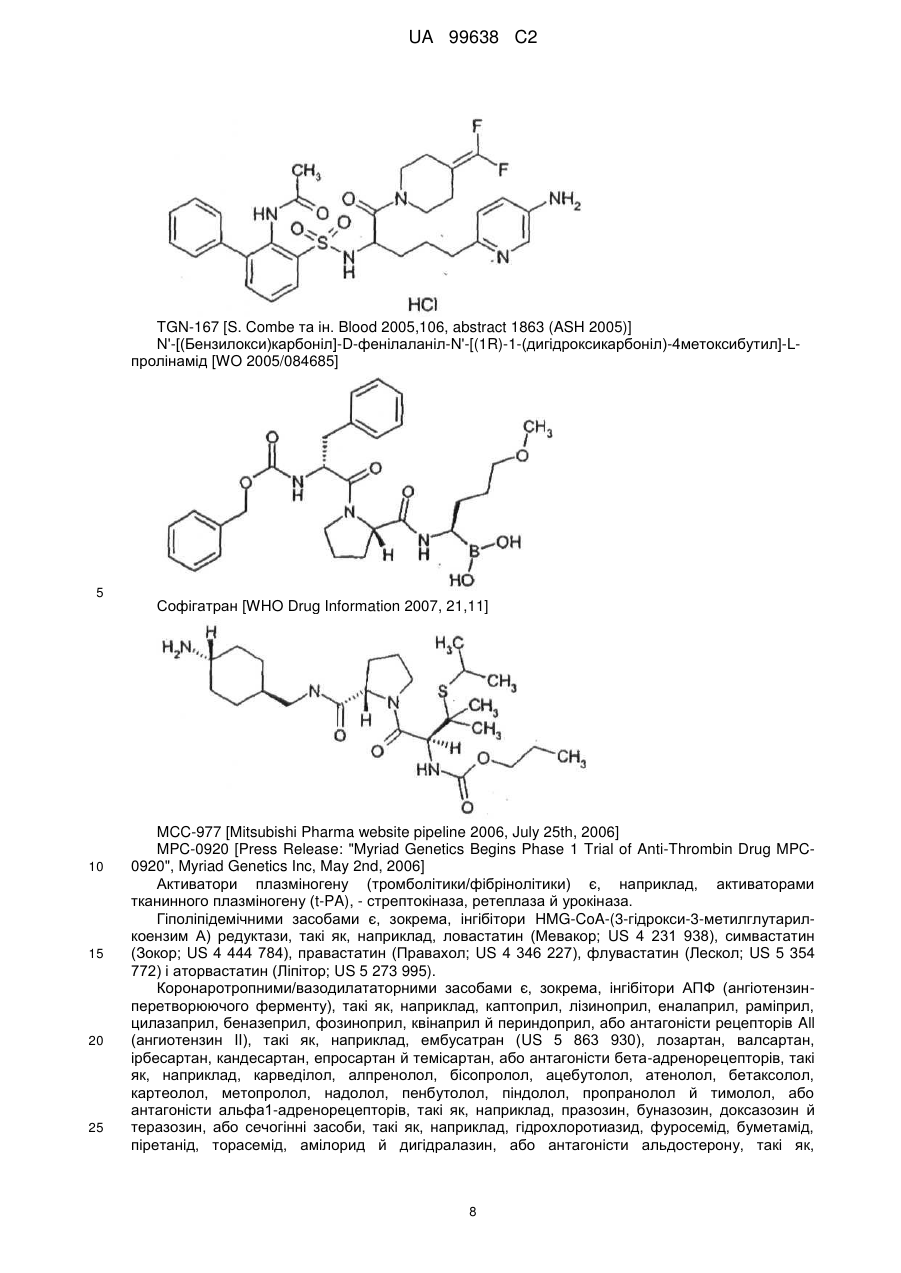
Оксазолідинони для лікування та/або профілактики серцевої недостатності
Номер патенту: 99638
Опубліковано: 10.09.2012
Автори: Каллабіс Харальд, Махал Джіт, Спіро Теодоре, Перцборн Елізабет, Кубітца Дагмар, Рьоріг Сусанне, Хаскелл Ллойд, Тілеманн Вольфганг
Формула / Реферат
1. Застосування сполуки формули (І)
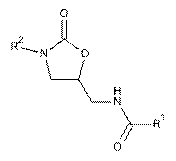 (I),
(I),
де
R1 є 2-тіофен, заміщений у 5 положенні радикалом із групи: хлор, бром, метил або трифторметил,
R2 є D-A-:
де:
радикал "А" є фенілен;
де:
група "А", визначена вище, може необов'язково бути заміщена один раз або двічі у мета-положенні, відносно зв'язку з оксазолідиноном, радикалом із групи: фтор, хлор, нітро, аміно, трифторметил, метил або ціано,
радикал "D" є насичений 5- або 6-членний гетероцикл, який зв'язаний через атом азоту з "А", що має карбонільну групу в безпосередній близькості із з'єднувальним атомом азоту, і в якому кільцевий атом вуглецю може бути замінений на гетероатом, вибраний із групи: S, N, О;
і її фармацевтично прийнятних солей, сольватів і сольватів солей для одержання медикаментів або фармацевтичних композицій для лікування та/або профілактики серцевої недостатності.
2. Застосування за п. 1, яке відрізняється тим, що сполукою формули (І) є 5-хлор-N-({(5S)-2-оксо-3-[4-(3-оксо-4-морфолініл)феніл]-1,3-оксазолідин-5-іл}метил)-2-тіофенкарбоксамід
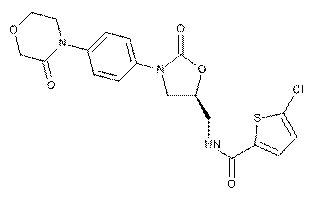 ,
,
або його фармацевтично прийнятні солі, сольвати і сольвати солей.
3. Застосування сполуки формули (І) за п. 1 або 2, яке відрізняється тим, що серцевою недостатністю є серцева недостатність, хронічна серцева недостатність, застійна серцева недостатність, застійна кардіальна недостатність, гостра серцева недостатність, гостра декомпенсована серцева недостатність, систолічна серцева недостатність, діастолічна серцева недостатність, правостороння серцева недостатність, лівостороння серцева недостатність, серцевий дефіцит, кардіальний дефіцит, хронічний серцевий дефіцит, серцева декомпенсація, високопродуктивна серцева недостатність, низькопродуктивна серцева недостатність, кардіоміопатія, дилатаційна кардіоміопатія і/або гіпертрофічна кардіоміопатія.
Текст
Реферат: Винахід стосується застосування сполуки формули (І) для лікування та/або профілактики серцевої недостатності. UA 99638 C2 (12) UA 99638 C2 UA 99638 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід відноситься до застосування селективних інгібіторів коагуляційного фактора Ха, зокрема оксазолідинонів формули (І), для лікування та/або профілактики серцевої недостатності та/або розладів, пов'язаних із серцевою недостатністю, так само як їх застосування для одержання фармацевтичних препаратів для лікування та/або профілактики серцевої недостатності та/або розладів, пов'язаних із серцевою недостатністю. Оксазолідинони формули (І) відомі з WO-A-01/047919 і діють, зокрема, як селективні інгібітори коагуляційного фактора Ха й як антикоагулянти. Оксазолідинони формули (І) селективно інгібують фактор коагуляції Ха. Було можливо продемонструвати антитромботичний ефект інгібіторів фактора Ха у численних моделях тварин (див. U. Sinha, P. Ku, J. Malinowski, В. Yan Zhu, R.M. Scarborough, C.K. Marlowe, P.W. Wong, P. Hua Lin, SJ. Hollenbach, Antithrombotic and hemostatic capacity of factor Xa versus thrombin inhibitors in models of venous and arteriovenous thrombosis, European Journal of Pharmacology 2000, 395, 51-59; A. Betz, Recent advances in Factor Xa inhibitors, Expert Opin. Ther Patents 20001,11, 1007; K. Tsong Tan, A. Makin, G.Y.H. Lip, Factor X inhibitors, Exp. Opin. Investig. Drugs 2003,12, 799; J. Ruef, H.A. Katus, New antithrombotic drugs on the horizon, Expert Opin. Investig. Drugs 2003, 12, 781; M.M. Samama, Synthetic direct and indirect factor Xa inhibitors, Thrombosis Research 2002, 106, V267; M.L. Quan, J.M. Smallheer, The race to an orally active Factor Xa inhibitor, Recent advances, J. Current Opinion in Drug Discovery & Development 2004, 7, 460-469) та в клінічних дослідженнях на пацієнтах (The Ephesus Study, Blood 2000, 96, 490a; The Penthifra Study, Blood 2000, 96, 490a; The Pentamaks Study, Blood 2000, 96, 490a-491a; The Pentathlon Study, Blood 2000, Vol 96, 491a). Інгібітори фактору Ха тому можуть використовуватися переважно в медикаментах для профілактики та/або лікування тромбоемболійних розладів. Селективні інгібітори фактору Ха показують широкий терапевтичний коридор. Було можливо продемонструвати в численних моделях тварин, що селективні інгібітори фактору Ха показують антитромботичний ефект без або тільки з незначно пролонгованим часом кровотечі (див. RJ Leadly, Coagulationfactor Xa inhibition: biological background and rationale, Curr. Top. Med. Chem. 2001, 1, 151-159). Тому, індивідуальне дозування для антикоагулянтів класу селективних інгібіторів фактора Ха не потрібно. Серцева недостатність, синонім - застійна серцева недостатність (ЗСН) або кардіальна недостатність, або гостра і хронічна серцева недостатність, є патофізіологічним станом, при якому серце не здатне перекачувати кров при швидкості, що відповідає вимогам метаболізму тканин, або здатне тільки при підвищеному тиску наповнення (W S Colucci, E.Braunwald. Pathophysiology of Heart Failure page 394-420 in Heart Disease, A Textbook of Cardiovascular Medicine, ed. E. Braunwald, WB Saunders Company, 5™ edition). Це звичайно спричиняється дефектом міокардіальної контракції, тобто внаслідок інфаркту міокарду або гіпертонії. За наявності порушення в міокардіальній контрактильності або надлишковому гемодинамічному навантаженні на шлуночок, або в обох випадках, серцевий м'яз залежить від ряду адаптивних механізмів для підтримки його насосної функції. Один з важливих механізмів є, наприклад, процес ремоделювання серця у відповідь на початковий патологічний випадок, що може привести до прогресивного погіршення серцевої функції. Патофізіологічні ознаки серцевої недостатності включають хронічний прокоагуляційний стан крові зі схильністю до тромбоемболізму. Клінічні дослідження продемонстрували збільшення інцидентів венозного й артеріального тромбозу у суб'єктів з ЗСН [White RH. The epidemiology of venous thromboembolism. Circulation 2003; 107 (23 suppl 1); 14-18]. Є достовірні докази взаємозв'язку підвищеного рівня маркерів гіперкоагуляційності та випадків тромбозу з несприятливими наслідками у пацієнтів, і збільшення ступеня захворюваності та смертності. Активована коагуляційна активність є ознакою збільшеного TNF, тромбін-антитромбінового комплексу (ТАТ), D-димеру, протромбінового фрагменту F1+2, фібрінопептиду A, IL-6 (Garg RK та ін. Prog Cardiovasc Dis. 1998; 41:225-236. Davis CJ та ін. Int J Cardiol 2000; 75:15-21). Гіперкоагуляція, венозний й артеріальний тромбоз, включаючи, наприклад, легеневу емболію (ЛЕ), інфаркт міокарду, інсульт, можуть погіршити серцеву функцію, викликати декомпенсацію й можуть зашкодити іншим органам і тканинам у людей з ЗСН, таким чином, збільшуючи захворюваність і смертність. Крім того, ЗСН може впливати на клінічний результат пацієнтів із тромбозом і ЛЕ, і обидва стани погіршують результат. На додаток до їхньої важливої ролі в активації коагуляційної системи, що призводить до гіперкоагуляції і тромбозу, фактор Ха і тромбін, як відомо, виявляють різні плейотропні ефекти. Таким чином, вони є потужними мітогенами, які індукують проліферацію. Вони викликають та/або посилюють вазоконстрикцію. Передача сигналів тромбіном приводить до вивільнення прозапальних цитокінів. Лікування інгібіторами FXa, окрім інгібування гемокоагуляції, може 1 UA 99638 C2 5 10 15 20 25 30 35 40 супресувати мітогенні, вазоконстриктивні і запальні стимули FXa і тромбіну, останній інгібуванням утворення тромбіну. Антитромботична терапія або з аспірином, або з варфарином привела до зменшення частоти клінічних випадків у порівнянні із суб'єктами, які не одержували антитромботичні препарати. Антикоагуляційна терапія з варфарином також зменшувала частоту госпіталізації пацієнтів з ЗСН, але за рахунок збільшення кровоточивості. Застосування аспірину може збільшити ризик госпіталізації пацієнтів з ЗСН. [1] Dunkman WB, Johnson GR, Carson PE, Bhat G, Farrell L, Cohn JN. Incidence of thromboembolic events in congestive heart failure. The V-HEFT VA Cooperative Studies Group. Circulation 1993; 87 (6 Suppl): V194-V1101.2) Loh E, Sutton MS, Wun CC, та ін. Ventricular dysfunction and risk of stroke after myocardial infarction. N Engl J Med 1997; 336; 251-257. 3) The CONSENSUS Trial Study Group. Effect of enalapril on mortility in severe congestive heart failure. Results of Cooperative North Scandinavian Enalapril Survival Study (CONSENSUS). N Engl J Med 1987, 316:1429-1435. 4) Dries DL, Rosenberg YD, Waclawiw MA, Domanski MJ. Ejection fraction and risk of thromboembolic events in patients with systolic dysfunction and sinus rhythm: evidence for gender differences in the studies of left ventricular dysfunction trials. J Am Coll Cardiol 1997; 29: 1074-1080]. Тепер несподівано було виявлено, що селективні інгібітори коагуляційного фактора Ха, зокрема оксазолідинони формули (І), є також прийнятними для профілактики та/або лікування серцевої недостатності та/або розладів, пов'язаних із серцевою недостатністю. Таким чином, даний винахід відноситься до застосування селективних інгібіторів фактора Ха для одержання медикаментів або фармацевтичних композицій для лікування та/або профілактики серцевої недостатності та/або розладів, пов'язаних із серцевою недостатністю. Зокрема, даний винахід відноситься до застосування сполук формули (І) де 1R 2-тіофен, заміщений у 5 положенні радикалом із групи: хлор, бром, метил або трифторметил, 2 R -D-A-: де: радикал "А" - фенілен; де: група "А", визначена вище, може довільно бути заміщена один раз або двічі у метаположенні відносно зв'язку з оксазолідиноном, радикалом із групи: фтор, хлор, нітро, аміно, трифторметил, метил або ціано, радикал "D" - насичений 5-або 6-членний гетероцикл, що зв'язаний через атом азоту з "А", що має карбонільну групу в безпосередній близькості із з'єднувальним атомом азоту, і в якому вуглецевий атом кільця може бути заміщений гетероатомом із групи S, N і О; і їх фармацевтично прийнятних солей, сольватів й сольватів солей для одержання медикаментів або фармацевтичних композицій.для лікування та/або профілактики серцевої недостатності та/або розладів, пов'язаних із серцевою недостатністю. Дуже конкретна перевага також надається у цьому зв'язку застосуванню сполуки 5-хлор-N({(5S)-2-оксо-3-[4-(3-оксо-4-морфолініл)феніл]-1,3-оксазолідин-5-іл}метил)-2-тіо-фенкарбоксамід (ривароксабан; приклад 1), що має наступну формулу: 2 UA 99638 C2 5 10 15 20 25 30 35 40 45 і його фармацевтично прийнятним солям, сольватам й сольватам солей для одержання медикаментів або фармацевтичних композицій для лікування та/або профілактики серцевої недостатності та/або розладів, пов'язаних із серцевою недостатністю. Дотепер оксазолідинони були описані по суті тільки як антибіотики, і в декількох випадках також як інгібітори МАО й антагоністи фібриногену (Review: В. Riedl, R. Endermann, Exp. Opin. Ther. Patents 1999, 9, 625), і невелика група 5-[ациламінометил] (переважно 5[ацетиламінометил]), здається, є суттєвою для антибактеріального ефекту. Заміщені арил- і гетероарилфенілоксазолідинони, в яких монозаміщений або полізаміщений фенільний радикал може бути зв'язаний з N атомом кільця оксазолідинону, та у яких може бути в положенні 5 кільця оксазолідинону незаміщений залишок N-метил-2-тіофенкарбоксамід, і їх застосування як речовин з антибактеріальною активністю, розкриті у патентах США: US 5 929 248, US 5 801 246, US 5 756 732, US 5 654 435, US 5 654 428 і US 5 565 571. Крім того, оксазолідинони, що містять бензамідин, є відомими як синтетичні проміжні сполуки в синтезі інгібіторів фактора Ха або антагоністів фібриногену (WO-A-99/31092, ЕР-А623615). Сполуки винаходу це сполуки формули (І) та їх солі, сольвати й сольвати їх солей, сполуки формул, згаданих нижче, що охоплюються формулою (І) та їх солі, сольвати і сольвати їх солей та сполуки, згадані нижче, як ґірактичні приклади, що охоплюються формулою (І) та їх солі, сольвати і сольвати їх солей, оскільки сполуки формул, згаданих нижче, що охоплюються формулою (І), уже не є солями, сольватами і сольватами солей. Залежно від їхньої структури сполуки винаходу можуть існувати в стереоізомерних формах (енантіомери, діастереомери). Тому даний винахід включає енантіомери або діастереомери і відповідні їх суміші. З таких сумішей енантіомерів та/або діастереомерів, стереоізомерні гомогенні компоненти можуть бути виділені відомим способом. Оскільки сполуки винаходу можуть зустрічатися в таутомерних формах, даний винахід включає всі таутомерні форми. Як солі в контексті представленого винаходу, переважними є ізіологічно безпечні солі сполук відповідно до винаходу. Також включені солі, які не є самостійно прийнятними для фармацевтичного застосування, але можуть, наприклад, використовуватися для виділення або очищення сполук відповідно до винаходу. Фізіологічно безпечні солі сполук відповідно до винаходу включають кислотно-адитивні солі неорганічних кислот, карбонових кислот і сульфокислот, наприклад, солі соляної кислоти, бромводневої кислоти, сірчаної кислоти, фосфорної кислоти, метансульфонової кислоти, етансульфонової кислоти, толуолсульфонової кислоти, бензолсульфонової кислоти, нафталенедисульфонової, оцтової кислоти, трифтороцтової кислоти, пропіонової кислоти, молочної кислоти, винної кислоти, яблучної кислоти, лимонної кислоти, фумарової кислоти, малеїнової й бензойної кислоти. Фізіологічно безпечні солі сполук відповідно до винаходу також включають солі звичайних основ, таких як, наприклад і переважно, солі лужних металів (наприклад, солі натрію і калію), солі лужно-земельних металів (наприклад, солі кальцію і магнію) і солі амонію, одержані з аміаку або органічних амінів з 1-16 атомами С, такі як, наприклад і переважно: етиламін, діетиламін, триетиламін, етилдіізопропіламін, моноетаноламін, діетаноламін, триетаноламін, дициклогексиламін, диметиламіноетанол, прокаїн, дибензиламін, N-метилморфолін, аргінін, лізин, етилендіамін й N-метилпіперидин. У контексті винаходу ті форми сполук відповідно до винаходу, які у твердому або рідкому стані утворюють комплекс координацією з молекулами розчинника, описані як сольвати. Гідрати - певна форма сольватів, де координація відбувається з водою. Гідрати є переважними сольватами в контексті представленого винаходу. 3 UA 99638 C2 5 10 15 20 25 Крім того, даний винахід також включає прекурсори сполук відповідно до винаходу. Термін "прекурсори" включає сполуки, які можуть самостійно бути біологічно активними або неактивними, але перетворюються в сполуки винаходу (наприклад, метаболічно або гідролітично) під час їх перебування в організмі. У контексті представленого винаходу, якщо інакше не визначено, замісники мають наступні значення: Насичений 5-або 6-членний гетероцикл, який зв'язаний через атом азоту з "А", що має карбонільну групу в безпосередній близькості із з'єднувальним атомом азоту, і в якому кільцевий атом вуглецю може бути замінений на гетероатом, вибраний із групи: S, N, О, може бути згаданий, наприклад, як: 2-оксопіролідин-1-іл, 2-оксопіперидин-1-іл, 2-оксопіперазин-1-іл, 2оксоморфолін-1-іл, 3-оксотіоморфолін-4-іл, 2-оксо-1,3-оксазолідин-1-іл, 2-оксо-1,3-оксазинан-1іл, 2-оксоімідазолідин-1-іл і 2-оксотетрагідропіримідин-і-іл. Сполуки формули (І) можуть бути одержані також, альтернативним способом, [А] реакцією сполук загальної формули (II) де 2 радикал R має вищевказане значення, з карбоновими кислотами загальної формули (III) де 1 радикал R має вищевказане значення, або, крім того, з відповідними карбонілгалоїдами, переважно карбонілхлоридами, або, крім того, з відповідними симетричними або змішаними ангідридами карбонових кислот загальної формули (III), визначеної вище в інертних розчинниках, якщо прийнятно, в присутності активувального або сполучного реагента та/або основи з одержанням сполук загальної формули (І) або, крім того, альтернативним способом [В] перетворенням сполук загальної формули (IV) 30 де 1 радикал R має вищевказане значення, з прийнятним селективним окислювачем в інертному розчиннику у відповідний епоксид загальної формули (V) 35 де 1 радикал R має вищевказане значення, і взаємодією в інертному розчиннику, якщо прийнятно в присутності каталізатора, з аміном загальної формули (VI) 2 R -NH2 (VI), де 2 радикал R має вищевказане значення, спочатку одержуючи сполуки загальної формули (VII) 40 4 UA 99638 C2 5 10 15 20 25 30 35 40 45 50 55 де 1 2 радикали R й R мають вищевказане значення, та згодом, циклізуючи в інертному розчиннику в присутності фосгену або еквівалентів фосгену, таких як, наприклад, карбонілдіімідазол (КДІ), до сполук загальної формули (І). Розчинниками, прийнятними для способів, описаних вище, є у випадку органічних розчинників - розчинники, що є інертними в умовах реакції. Вони включають галоїдзаміщені вуглеводні, такі як дихлорметан, хлороформ, тетрахлорметан, 1,2-дихлоретан, трихлоретан, тетрахлоретан, 1,2-дихлоретилен або трихлоретилен, етери, такі як діетиловий етер, діоксан, тетрагідрофуран, диметиловий етер гліколю або диметиловий етер діетиленгліколю, спирти, такі як метанол, етанол, н-пропанол, ізопропанол, н-бутанол або трет-бутанол, вуглеводні, такі як бензол, ксилол, толуол, гексан або циклогексан, диметилформамід, диметилсульфоксид, ацетонітрил, піридин, гексаметил-фосфорний триамід, або вода. Аналогічно, можливо використовувати суміш розчинників, що складаються з вищезгаданих розчинників. Активувальні або сполучні реагенти, прийнятні для способів, описаних вище, є у цих випадках реактивами, звичайно використовуваними в цих цілях, наприклад, N'-(3диметиламінопропіл)-N-етилкарбодіімід • НСL, N,N'-дициклогексилкарбодіімід, 1-гідрокси-1 Нбензотріазол • Н2О та подібні. Прийнятними основами є звичайні неорганічні або органічні основи. Вони переважно включають гідроксид лужного металу такий, як, наприклад, гідроксид натрію або калію, або карбонати лужного металу, такі як карбонат натрію або калію, або натрію або калію метанолат, або натрію або калію етанолат, або трет-бутоксид калію, або аміди, такі як амід натрію, літій біс(триметилсиліл)амід або діізопропіламід літію, або аміни, такі як триетиламін, діізопропілетиламін, діізопропіламін, 4-N,N'-диметиламінопіридин або піридин. Основа може використовуватися в цих випадках у кількості від 1 до 5 моль, переважно від 1 до 2 моль, виходячи з 1 моль сполук загальної формули (II). Реакції взагалі відбуваються в діапазоні температур від -78 °C до температури кипіння, переважно в діапазоні від 0 °C до температури кипіння. Реакції можуть бути виконані при атмосферному, підвищеному або зменшеному тиску (наприклад, у діапазоні від 0,5 до 5 бар), взагалі при атмосферному тиску. Придатними селективними окислювачами як для одержання епоксидів, так і для окислення, яке необов'язково здійснюють до сульфону, сульфоксиду або N-оксиду, є, наприклад, мхлорпербензойна кислота (МХПБК), натрію метаперіодат, N-метилморфолін N-оксид (NMO), монопероксифталева кислота або тетраоксид осмію. Умови, використовувані для одержання епоксидів, є загальноприйнятими для такого одержання. Для деталізованих умов процесу окислювання, яке здійснюють, якщо прийнятно, до сульфону, сульфоксиду або N-оксиду, посилання може бути зроблене на наступну літературу: M.R. Barbachyn et al. J. Med. Chem. 1996, 39, 680 and WO-A-97/10223. Сполуки формул (II), (III), (IV) і -(VI) відомі фахівцям або можуть бути одержані загальноприйнятними способами. Для оксазолідинонів, зокрема, 5-(амінометил)-2оксооксазолідинів необхідні способи, як описані в: WO-A-98/01446; WO-A-93/23384; WO-A97/03072; J.A. Tucker та ін., J. Med. Chem. 1998, 41, 3727; S.J. Brickner та ін. J. Med. Chem. 1996, 39, 673; W.A. Gregory та ін. J. Med. Chem. 1989, 32, 1673. Спосіб синтезу сполук загальної формули (І) описаний докладно в WO-A-01/047919. Для цілей представленого винаходу "серцева недостатність" включає, зокрема серйозні розлади, такі як кардіальна недостатність, хронічна серцева недостатність, застійна серцева недостатність, застійна кардіальна недостатність, гостра серцева недостатність, гостра декомпенсована серцева недостатність, систолічна серцева недостатність, діастолічна серцева недостатність, правостороння серцева недостатність, лівостороння серцева недостатність, серцевий дефіцит, кардіальний дефіцит, хронічний серцевий дефіцит, серцева декомпенсація, високопродуктивна серцева недостатність, низькопродуктивна серцева недостатність, кардіоміопатія, дилатаційна кардіоміопатія й гіпертрофічна кардіоміопатія. 5 UA 99638 C2 5 10 15 20 25 30 35 40 45 50 55 Для цілей представленого винаходу "розлади, пов'язані із серцевою недостатністю", включають, зокрема, наступні: прогресивна декомпенсація серцевої функції, серцева декомпенсація й пошкодження інших органів і тканин, гіперкоагуляція, артеріальні і венозні тромбоемболії, легенева емболія (ЛЕ), інфаркт міокарду й інсульт. Крім того, даний винахід відноситься до способу лікування та/або профілактики серцевої недостатності та/або розладів, пов'язаних із серцевою недостатністю, людини або тварини з застосуванням ефективної кількості селективного інгібітора фактора Ха або медикамента, що включає принаймні один селективний інгібітор фактора Ха у комбінації з одним або більше фармакологічно прийнятними допоміжними засобами або ексціпієнтами. Крім того, даний винахід відноситься до способу лікування та/або профілактики серцевої недостатності та/або розладів, пов'язаних із серцевою недостатністю, людини або тварини з застосуванням ефективної кількості принаймні однієї сполуки формули (І) або медикамента, що включає принаймні одну сполуку формули (І) у комбінації з одним або більше фармакологічно прийнятними допоміжними засобами або ексціпієнтами. Крім того, даний винахід відноситься до способу лікування та/або профілактики серцевої недостатності та/або розладів, пов'язаних із серцевою недостатністю, людини або тварини з застосуванням ефективної кількості принаймні сполуки 5-хлор-N-({(5S)-2-оксо-3-[4-(3-оксо-4морфолініл)феніл]-1,3-оксазолідин-5-іл}метил)- 2-тіофенкарбоксаміду або медикаментів, що включають принаймні сполуку 5-хлор-N-({(5S)-2-оксо-3-[4-(3-оксо-4-морфолініл)феніл]-1,3оксазолідин-5-іл}метил)-2-тіофенкарбоксамід у комбінації з одним або більше фармакологічно прийнятними допоміжними засобами або ексціпієнтами. Даний винахід, крім того, стосується медикаментів та фармацевтичних композицій, що включають принаймні одну сполуку формули (І) відповідно до винаходу разом з одним або більше фармакологічно прийнятними допоміжними засобами або ексціпієнтами, причому медикаменти й фармацевтичні композиції можуть використовуватися при згаданих вище показаннях. В одному з втілень винахід стосується способу профілактики тромбоутворення у мікросудинах й макросудинах, причому спосіб включає довготривале призначення ссавцю терапевтично ефективної кількості принаймні однієї сполуки формули (І), такої як ривароксабан. В іншому втіленні спосіб забезпечує поліпшену тривалість життя у ссавців, причому спосіб включає стадію довготривалого призначення ссавцю терапевтично ефективної кількості принаймні однієї сполуки формули (І), такої як ривароксабан, де частота раніше зазначених випадків зменшена щодо частоти, установленої за визнаним стандартом догляду. В іншому втіленні сполуки формули (І) є прийнятними, щоб зменшити захворюваність і смертність широкого спектру індивідуумів із серцевою недостатністю, що також включає пацієнтів із серцевою недостатністю з і без штучних серцевих клапанів, пацієнтів із фібріляцією передсердя, ішемічною хворобою серця, госпіталізованих пацієнтів внаслідок їх захворювань (з медичної точки зору - хворі пацієнти). В іншому втіленні ривароксабан є прийнятним, щоб зменшити захворюваність і смертність широкого спектру індивідуумів із серцевою недостатністю, що також включає пацієнтів із серцевою недостатністю з і без штучних серцевих клапанів, пацієнтів із фібріляцією предсердя, ішемічною хворобою серця, госпіталізованих пацієнтів внаслідок їх захворювань (з медичної точки зору хворі пацієнти). В іншому втіленні спосіб забезпечує зменшення кількості госпіталізацій, необхідних для догляду за індивідуумом, спосіб, що включає стадію довготривалого призначення ссавцю терапевтично ефективної кількості принаймні однієї сполуки формули (І), такої як ривароксабан, де частота раніше зазначених випадків зменшена щодо частоти, установленої за визнаним стандартом догляду. В іншому втіленні спосіб забезпечує замісну терапію у ссавця іншим антикоагулянтом і дезагрегантом, які представлені сучасними рекомендаціями на основі стандартів догляду, спосіб, що включає стадію довготривалого призначення ссавцю терапевтично ефективної кількості принаймні однієї сполуки формули (І), такої як ривароксабан. Частота випадків, які спостерігаються у ссавців, дорівнює або зменшена щодо частоти, установленої за визнаним стандартом замісного догляду. В іншому втіленні даний винахід також відноситься до комбінацій: A) сполуки формули (І) разом з B) іншими фармацевтичними препаратами, особливо з інгібіторами агрегації тромбоцитів, антикоагулянтами, фібрінолітиками, гіполіпідемічними, коронаротропними та/або вазодилататорами. 6 UA 99638 C2 5 10 15 "Комбінації" у контексті даної заявки це не тільки фармацевтичні композиції, які включають всі компоненти (так називані комбінації фіксованих доз), і комбіновані упаковки, які містять всі компоненти окремо один від одного, але також і компоненти, які призначають одночасно або відокремлено, за умови, що вони використовуються для профілактики та/або лікування тієї ж самої хвороби. Крім того, можливо комбінувати два або більше препарати разом, які є подвійними або множинними комбінаціями, відповідно. Індивідуальні препарати комбінацій відомі з літератури й головним чином комерційно доступні. Інгібітори агрегації тромбоцитів - наприклад, ацетилсаліцилова кислота (як Аспірин), тіклопідін (Ticlid) і клопідрогель (Plavix) або антагоністи інтегрину, як, наприклад, антагоністи глікопротеїну ІІb/ІІІа, як наприклад, абциміксаб, ептифібатид, тирофібан, ламіфібан, лефрадафібан й фрадафібан. Антикоагулянти, наприклад, гепарин (UFH), низькомолекулярний гепарин (LMWH), як наприклад, тинзапарин, цертопарин, парнапарин, надропарин, ардепарин, еноксапарин, ревіпарин, дальтепарин, данапароїд і прямі інгібітори тромбіну (DTI). Прямими інгібіторами тромбіну є, наприклад: Ексанта (ксимелагатран) 20 Рендикс(дабігатран) AZD-0837 [AstraZeneca Annual Report 2006, March 19th, 2007] 25 SSR-182289 [J. Lorrain та ін. Journal of Pharmacology and Experimental Therapeutics 2003, 304, 567-574; J.-M. Altenburger та ін. Bioorg.Med.Chem. 2004,12, 1713-1730] 7 UA 99638 C2 TGN-167 [S. Combe та ін. Blood 2005,106, abstract 1863 (ASH 2005)] N'-[(Бензилокси)карбоніл]-D-фенілаланіл-N'-[(1R)-1-(дигідроксикарбоніл)-4метоксибутил]-Lпролінамід [WO 2005/084685] 5 10 15 20 25 Софігатран [WHO Drug Information 2007, 21,11] MCC-977 [Mitsubishi Pharma website pipeline 2006, July 25th, 2006] MPC-0920 [Press Release: "Myriad Genetics Begins Phase 1 Trial of Anti-Thrombin Drug MPC0920", Myriad Genetics Inc, May 2nd, 2006] Активатори плазміногену (тромболітики/фібрінолітики) є, наприклад, активаторами тканинного плазміногену (t-PA), - стрептокіназа, ретеплаза й урокіназа. Гіполіпідемічними засобами є, зокрема, інгібітори HMG-CoA-(3-гідрокси-3-метилглутарилкоензим А) редуктази, такі як, наприклад, ловастатин (Мевакор; US 4 231 938), симвастатин (Зокор; US 4 444 784), правастатин (Правахол; US 4 346 227), флувастатин (Лескол; US 5 354 772) і аторвастатин (Ліпітор; US 5 273 995). Коронаротропними/вазодилататорними засобами є, зокрема, інгібітори АПФ (ангіотензинперетворюючого ферменту), такі як, наприклад, каптоприл, лізиноприл, еналаприл, раміприл, цилазаприл, беназеприл, фозиноприл, квінаприл й периндоприл, або антагоністи рецепторів All (ангиотензин II), такі як, наприклад, ембусатран (US 5 863 930), лозартан, валсартан, ірбесартан, кандесартан, епросартан й темісартан, або антагоністи бета-адренорецепторів, такі як, наприклад, карведілол, алпренолол, бісопролол, ацебутолол, атенолол, бетаксолол, картеолол, метопролол, надолол, пенбутолол, піндолол, пропранолол й тимолол, або антагоністи альфа1-адренорецепторів, такі як, наприклад, празозин, буназозин, доксазозин й теразозин, або сечогінні засоби, такі як, наприклад, гідрохлоротиазид, фуросемід, буметамід, піретанід, торасемід, амілорид й дигідралазин, або антагоністи альдостерону, такі як, 8 UA 99638 C2 5 10 15 20 25 30 35 40 45 50 55 60 наприклад, спіронолактон й еплеренон, або позитивні інотропи, такі як, наприклад, дігоксин, або блокатори кальцієвих каналів, такі як, наприклад, верапаміл й ділтіазем, або похідні дигідропиридину, такі як, наприклад, ніфедипін (Адалат) і нітрендипін (Байотензин), або донори оксиду азоту, такі як, наприклад, ізосорбід-5-мононітрат, ізосорбіду-динітрат й нітрогліцерин, або сполуки, які мають ефект збільшення циклічного гуанозин-монофосфату (cGMP), такі як, наприклад, стимулятори солюбільної гуанілатциклази (WO 98/16223, WO 98/16507, WO 98/23619, WO 00/06567, WO 00/06568, WO 00/06569, WO 00/21954, WO 00/66582, WO 01/17998, WO 01/19776, WO 01/19355, WO 01/19780, WO 01/19778, WO 07/045366, WO 07/045367, WO 07/045369, WO 07/045370, WO 07/045433). Крім того, даний винахід відноситься до препаратів, які включають принаймні одну сполуку винаходу, разом з одним або більше інертним, нетоксичним і фармацевтично прийнятним ад'ювантом, так само як до їх застосування у вищезгаданих цілях. Крім того, даний винахід відноситься до препаратів, які включають принаймні одну сполуку винаходу, разом з одним або більше комбінованим препаратом, особливо для застосування для профілактики та/або лікування вищезгаданих хвороб. Сполуки винаходу можуть діяти системно та/або локально. Із цією метою, вони можуть призначатися прийнятним способом, таким, як наприклад, оральний, парентеральний, легеневий, назальний, сублінгвальний, лінгвальний, букальний, ректальний, дермальний, трансдермальний, кон'юнктивальний або ауральний, або як імплантант або стент. Для цих шляхів введення сполуки винаходу можна призначати в прийнятних формах введення. Для перорального призначення сучасні дозовані форми, що вивільняють сполуку винаходу швидко та/або модифікованим способом, містять сполуки винаходу в кристалічній формі та/або аморфній, та/або розчиненій формі, такій як, наприклад, таблетки (безоболонкові або оболонкові таблетки, наприклад, резистентні до шлункового соку або уповільненого розчинення, або несолюбільні оболонки, які контролюють вивільнення сполуки винаходу), таблетки, що швидко розпадаються в порожнині рота або плівки/пластинки, плівки/ліофілізат, капсули (наприклад, тверді або м'які желатинові капсули), драже, гранули, таблетки, порошки, емульсії, суспензії, аерозолі або розчини, є прийнятними. Парентеральне введення може бути здійснене, опускаючи стадію абсорбції (наприклад, внутрішньовенне, внутрішньоартеріальне, внутрішньо серцеве інтраспінальне або інтралюмбальне введення) або включаючи абсорбцію (наприклад, внутрішньом'язове, підшкірне, внутрішньошкірне, або інтраперитонеальне введення). Прийнятні дозовані форми для перентерального введення включають ін'єкційні та інфузійні препарати у формі розчинів, суспензій, емульсій, ліофілізатів або стерильних порошків. Для інших шляхів введення, прийнятними є, наприклад, інгаляційні композиції (включаючи порошкові інгалятори й небулайзери), назальні краплі, розчини або спреї, таблетки для язиковий, таблетки для лінгвального, сублінгвального, букального введення, таблетки, плівки/пластинки або капсули, супозиторії, оральні або офтальмологічні препарати, вагінальні капсули, водні суспензії (лосьйони, мікстури), ліпофільні суспензії, мазі, мазі, трансдермальні терапевтичні системи (наприклад, пластири), молочко, пасти, піни, присипки, імплантанти або стенти. Перевага надається оральному або парентеральному введенню, зокрема, оральному і внутрішньовенному введенню. Сполуки винаходу можуть бути перетворені у встановлені дозовані форми. Це може бути зроблене відомим способом безпосереднього змішування із інертним, нетоксичним, фармацевтично прийнятним ад'ювантом. Ці ад'юванти включають носії (наприклад, мікрокристалічну целюлозу, лактозу або маніт), розчинники (наприклад, рідкі поліетиленгліколи), емульгатори й диспергатори або змочувальні речовини (наприклад, натрію додецилсульфат, поліоксисорбітану олеат), зв'язуючі (наприклад, полівінілпіролідон), синтетичні й природні полімери (наприклад, альбумін), стабілізатори (наприклад, антиоксиданти, такі як, наприклад, аскорбінова кислота), барвники (наприклад, неорганічні пігменти наприклад, оксид заліза) і смакові добавки і ароматизатори. Взагалі, щоб досягти ефективних результатів при перентеральному введенні, були визначені переважні кількості для введення - приблизно від 0,001 до 30 мг/кг, переважно приблизно від 0,01 до 1 мг/кг. При оральному введенні дозування становить приблизно від 0,01 до 100 мг/кг, переважно приблизно від 0,01 до 30 мг/кг і найбільш переважно 1 - 30 мг/кг. Проте інколи може бути необхідним відхилення від згаданих кількостей, а саме: залежно від маси тіла, шляху введення, індивідуальної реакції на активну речовину, природи препарату й часу або інтервалу введення. Таким чином, у деяких випадках може бути достатньою менша, 9 UA 99638 C2 5 10 ніж вищесказана мінімальна кількість, у той час як в інших випадках установлена верхня межа може бути перевищена. У випадку введення більших кількостей, бажано розділити їх на кілька окремих введень протягом дня. Даний винахід проілюстрований прикладами нижче; однак, ці приклади у жодному разі не призначені для обмеження винаходу. Відсотки в наступних тестах і прикладах, якщо інакше не вказано, є ваговими відсотками; а частини є ваговими частинами. Співвідношення розчинників, ступінь розведення й концентрації, наведені для рідин/рідких розчинів, є об'ємними величинами. Приклади А Приклади Одержання Вихідні речовини Синтези вихідних матеріалів детально описані в WO-A-01/047919. Приклади синтезу Приклад 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 А-В-С СН2ОСН2СН2 СН2СН2СН2 СН2СН2СН2 СН2СН2СН2 СН2ОСН2СН2 СН2ОСН2СН2 ОСН2СН2 СН2СН2СН2 СH2СН2СH2 ОСН2СH2СH2 СН2СН2СН2 CH2OCH2CH2 СН2СН2СН2 СН2ОСН2СН2 CH2OCH2CH2 СН2ОСН2СН2 СН2ОСН2СН2 СН2СН2СН2 СН2ОСН2СН2 СН2ОСН2СН2 СН2ОСН2СН2 СН2СН2СH2 СН2СН2СH2СН2 СН2СН2СН2 СН2ОСН2СН2 СH2СН2СH2СH2 D Н Н Н Н Н Н Н Н Н Н F Н CF3 СІ CF3 СН3 CN СІ СН3 NH2 F F Н F F H Е D' Н Н Н Н Н Н Н Н Н Н Н H H H H H H H СН3 H H H H H H H СІ СІ СН3 Вr СН3 Вr СІ Вr CH3 СІ СІ Cl Cl Cl Cl Cl Cl Cl Cl Cl Br Br Br Cl Cl Cl 15 20 Синтези прикладів сполук детально описані в WO-A-01/047919. В. Оцінка фізіологічної активності 1. Фізіологічна активність сполук Формули (І) Сполуки формули (І) діють, зокрема, як селективні інгібітори коагуляційного фактора Ха і не інгібують або інгібують тільки при більш високих концентраціях інші серинпротеази, такі як, плазмін або трипсин. Інгібітори коагуляційного фактора Ха згадуються також як "селективні", коли їх значення IC50 для фактора інгібування Ха є в 100 разів, переважно в 500 разів, зокрема, в 1000 разів, 10 UA 99638 C2 5 10 15 20 25 30 35 40 45 50 55 меншими за значення ІС50 для інгібування інших серинпротеаз, особливо плазміну і трипсину, посилаючись на тестові способи селективності Прикладів А.а.1) і А.2), описані нижче. Особливо переважні біологічні властивості сполук формули (І) можуть бути встановлені наступними способами. а) Опис тесту in vitro а.1) Вимірювання фактора інгібування Ха Ферментативна активність людського фактора Ха (FXa) була визначена перетворенням FXa-специфічного хромогенного субстрату. У цьому випадку, фактор Ха елімінує п-нітроанілін з хромогенного субстрату. Визначення були виконані на мікротитрованих планшетах наступним чином. Досліджувані речовини розчиняли при різних концентраціях у диметилсульфоксиді та інкубували з людським FXa (0,5 нмоль/л, розчинені в 50 ммоль/л трис-буфера [С,С,С-трис(гідроксиметил)-амінометан], 150 ммоль/л NaCI, 0,1 % BSA (альбумін бичачої сироватки, рН= 8,3) при 25 °C протягом 10 хвилин. Чистий диметилсульфоксид служить контролем. Потім додавали хромогенний субстрат (150 мкмоль/л Pefachrome® FXa від Pentapharm). Після інкубування при 25 °C протягом 20 хвилин визначали екстинкцію при 405 нм. Екстинції випробуваних сумішей з досліджуваною речовиною порівнювали з контрольними сумішами без досліджуваної речовини, і розраховували значення ІС50. а.2) Визначення селективності Селективне інгібування FXa було продемонстровано дослідженням інгібування досліджуваними речовинами інших людських серинпротеаз, таких як трипсин, плазмін. Ферментативну активність трипсину (500 мОд./мл) і плазміну (3,2 нмоль/л) визначали, розчиняючи ці ферменти в трис-буфері (100 ммоль/л, 20 ммоль/л СаСІ2, pH=8,0) і інкубуючи з досліджуваною речовиною або розчинником протягом 10 хвилин. Потім ферментативну реакцію ініціювали шляхом додавання придатного специфічного хромогенного субстрату (Chromozym Trypsin® від Boehringer Mannheim, Chromozym Plazmin® від Boehringer Mannheim), і екстинкцію визначали при 405 нм через 20 хвилин. Всі визначення здійснювали при 37 °C. Екстинції випробуваних сумішей з досліджуваною речовиною порівнювали з еталонними зразками без досліджуваної речовини, і розраховували значення ІС50. а.3) Визначення антикоагулянтного ефекту Антикоагулянтний ефект досліджуваних речовин був визначений in vitro в людській плазмі. Із цією метою, людську кров збирали в 0,11 молярний розчин цитрату натрію при співвідношенні цитратнатрію/кров - 1/9. Кров ретельно змішували після збору й центрифугували приблизно при 2000 об./хвил. протягом 10 хвилин. Супернатант вилучали піпеткою. Протромбіновий індекс (РТ, синонім: тест Quick's), визначали у присутності змінюваних концентрацій досліджуваної речовини або відповідного розчинника, використовуючи комерційно доступний тестовий комплект (Neoplastin® від Boehringer Mannheim). Досліджувані сполуки інкубували із плазмою при 37 °C протягом 10 хвилин. Потім індукували коагуляцію, додаючи тромбопластин, і визначали час початку коагуляції. Визначали концентрацію досліджуваної речовини, що викликає подвоєння протромбінового часу. b) Визначення антитромбічного ефекту (in vivo) b) Модель артеріовенозного шунта (пацюк) Голодні пацюки чоловічої статі (штам: HSD CPB:WU), вагою 200-250 г були анестезовані розчином Rompun/Ketavet (12 мг/кг/50 мг/кг). Тромбоутворення індукували в артеріовенозному шунті способом, заснованим на описаному Christopher N. Berry та ін., Br. J. Pharmacol. (1994), 113, 1209-1214. Із цією метою ліва яремна вена й права каротидна артерія були піддані втручанню. Екстракорпоральний шунт формували між цими двома судинами, використовуючи 10 см поліетиленову трубку (ПЕ 60). Ця поліетиленова трубка була в середині, зв'язуючи додаткову 3 см поліетиленову трубку (ПЕ 160), що містить шорсткувату нейлонову нитку, що утворює петлю для утворення тромбогенної поверхні. Екстракорпоральну циркуляцію підтримували протягом 15 хвилин. Шунт потім вилучали і негайно зважували нейлонову нитку з тромбом. Чисту вагу нейлонової нитки визначали перед початком експерименту. Досліджувані речовини призначали або внутрішньовенно через вену хвоста, або перорально через зонд неанестезованим тваринам перед проведенням екстракорпоральної циркуляції. С Практичні Приклади Фармацевтичних Композицій Сполуки відповідно до винаходу можуть бути перетворені у фармацевтичні препарати наступним чином: Таблетка: Композиція: 11 UA 99638 C2 5 10 15 20 25 30 100 мг сполуки винаходу, 50 мг лактози (моногідрат), 50 мг кукурудзяного крохмалю (нативний), 10 мг полівінілпіролідону (PVP 25) (BASF Co., Людвигсхафен, Німеччина) і 2 мг стеарату магнію. Вага таблетки 212 мг, діаметр 8 мм, радіус кривизни 12 мм. Виробництво: Суміш сполук відповідно до винаходу, лактозу й крохмаль гранулювали з 5 %-им розчином (ваг/ваг) PVP у воді. Після сушіння гранулят змішували із стеаратом магнію протягом 5 хвилин. Цю суміш пресували нормальним таблетувальним пресом (формат таблетки: див. вище). Як норматив, застосовується сила компресії 15 kN. Дозована суспензія для орального застосування: Композиція: 1000 мг сполуки винаходу, 1000 мг етилового спирту (96 %), 400 мг Rhodigel® (ксантанова камедь від FMC Co., Пенсільваняї, США), і 99 г. води. 10 мл оральної суспензії відповідають однократній дозі 100 мг сполуки винаходу. Виробництво: Rhodigel суспендували в етиловому спирті, і сполуку винаходу додавали до суспензії. Воду додавали при перемішуванні. Суміш перемішували протягом приблизно 6 годин до завершення набрякання Rhodigel. Дозований розчин для орального застосування: Композиція: 500 мг сполуки винаходу, 2.5 г полісорбату й 97 г поліетиленгліколю 400. 20 г орального розчину відповідають однократній дозі 100 мг сполуки винаходу. Виробництво: Композицію винаходу суспендували при перемішуванні у суміші поліетиленгліколю й полісорбату. Процес перемішування продовжували до повного розчинення сполуки винаходу. Внутрішньовенний Розчин: Композицію винаходу розчиняли у фізіологічно сумісному розчиннику (наприклад, ізотонічний розчин натрію хлориду, 5 %-ий розчин глюкози та/або 30 % розчин PEG 400) при концентрації нижче насиченості. Розчин стерильно фільтрували й заповнювали у стерильні й апірогенні ін'єкційні контейнери. ФОРМУЛА ВИНАХОДУ 1. Застосування сполуки формули (І) 35 40 45 50 (I), де 1 R є 2-тіофен, заміщений у 5 положенні радикалом із групи: хлор, бром, метил або трифторметил, 2 R є D-A-: де: радикал "А" є фенілен; де: група "А", визначена вище, може необов'язково бути заміщена один раз або двічі у метаположенні, відносно зв'язку з оксазолідиноном, радикалом із групи: фтор, хлор, нітро, аміно, трифторметил, метил або ціано, радикал "D" є насичений 5- або 6-членний гетероцикл, який зв'язаний через атом азоту з "А", що має карбонільну групу в безпосередній близькості із з'єднувальним атомом азоту, і в якому кільцевий атом вуглецю може бути замінений на гетероатом, вибраний із групи: S, N, О; і її фармацевтично прийнятних солей, сольватів і сольватів солей для одержання медикаментів або фармацевтичних композицій для лікування та/або профілактики серцевої недостатності. 12 UA 99638 C2 2. Застосування за п. 1, яке відрізняється тим, що сполукою формули (І) є 5-хлор-N-({(5S)-2оксо-3-[4-(3-оксо-4-морфолініл)феніл]-1,3-оксазолідин-5-іл}метил)-2-тіофенкарбоксамід 5 10 , або його фармацевтично прийнятні солі, сольвати і сольвати солей. 3. Застосування сполуки формули (І) за п. 1 або 2, яке відрізняється тим, що серцевою недостатністю є серцева недостатність, хронічна серцева недостатність, застійна серцева недостатність, застійна кардіальна недостатність, гостра серцева недостатність, гостра декомпенсована серцева недостатність, систолічна серцева недостатність, діастолічна серцева недостатність, правостороння серцева недостатність, лівостороння серцева недостатність, серцевий дефіцит, кардіальний дефіцит, хронічний серцевий дефіцит, серцева декомпенсація, високопродуктивна серцева недостатність, низькопродуктивна серцева недостатність, кардіоміопатія, дилатаційна кардіоміопатія і/або гіпертрофічна кардіоміопатія. Комп’ютерна верстка Л.Литвиненко Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 13
ДивитисяДодаткова інформація
Назва патенту англійськоюOxazolidinones for the treatment and/or prophylaxis of heart failure
Автори англійськоюKallabis, Harald, Thielemann, Wolfgang, Perzborn, Elisabeth, Rohrig, Susanne, Kubitza Dagmar, Spiro, Theodore, Haskell, Lloyd, Mahal, Jeet
Назва патенту російськоюОксазолидиноны для лечения и/или профилактики сердечной недостаточности
Автори російськоюКаллабис Харальд, Тилеманн Вольфганг, Перцборн Элизабет, Рериг Сусанне, Кубитца Дагмар, Спиро Теодоре, Хаскелл Ллойд, Махал Джит
МПК / Мітки
МПК: A61P 7/02, A61P 9/00, A61K 31/5377
Мітки: лікування, серцевої, недостатності, профілактики, оксазолідинони
Код посилання
<a href="https://ua.patents.su/15-99638-oksazolidinoni-dlya-likuvannya-ta-abo-profilaktiki-sercevo-nedostatnosti.html" target="_blank" rel="follow" title="База патентів України">Оксазолідинони для лікування та/або профілактики серцевої недостатності</a>
Попередній патент: Похідні піридину, заміщені гетероциклічним кільцем і фосфоноксиметильною групою, і протигрибковий засіб, що їх містить
Наступний патент: Матричний декодер
Випадковий патент: Спосіб визначення впливу порушення метаболізму вітаміну в1 його антагоністом окситіаміном на скоротливую активність діафрагмального м'яза