Хімічний спосіб
Номер патенту: 107443
Опубліковано: 12.01.2015
Автори: Васс Джек, Уіттон Алан Джон, Бойд Еван Кемпбелл
Формула / Реферат
Спосіб одержання сполуки формули (IV)
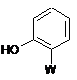 , (IV)
, (IV)
де W являє собою метил-(Е)-2-(3-метоксі)акрилатну групу, який включає стадії:
(і) взаємодії сполуки формули (IV), де W являє собою метил-2-(3,3-диметокси)пропаноатну групу, з реагентом, який буде захищати гідроксильну групу цієї сполуки від вступу в реакцію під час наступного деметанолізу;
(іі) відщеплення метанолу від гідроксилзахищеної сполуки, утвореної на стадії (і); і
(ііі) зняття групи, яка захищає гідроксильну групу, утвореної на стадії (і), з утворенням сполуки формули (IV), де W являє собою метил-(Е)-2-(3-метоксі)акрилатну групу.
Текст
Реферат: Даний винахід, зокрема, належить до способу одержання сполуки формули (IV) HO W , (IV) де W являє собою метил-(Е)-2-(3-метоксі)акрилатну групу. UA 107443 C2 (12) UA 107443 C2 UA 107443 C2 5 10 15 Даний винахід належить до способу одержання стробілуринового фунгіциду метил-(Е)-2-{2[6-(2-ціанофенокси)піримідин-4-ілокси]феніл}-3-метоксіакрилату (азоксистробіну), а також до його нових попередників. Способи одержання азоксистробіну описані в публікації WO 92/08703. У одному зі способів азоксистробін одержують реакцією 2-ціанофенолу з метил-(Е)-2-[2-(6-хлорпіримідин-4ілокси)феніл]-3-метоксиакрилатом. У публікації WO 01/72719 розкритий спосіб одержання з високим виходом похідних асиметричного 4,6-біс(арилокси)піримідину, в якому 6-хлор-4-арилоксипіримідин вводять в реакцію з фенолом, необов'язково в присутності розчинника і/або основи з додаванням від 2 до 40 % мол. 1,4-діазабіцикло[2.2.2]октану (DABCO). Даний винахід заснований на встановленні факту, що при одержанні азоксистробіну або нового ацетального попередника азоксистробіну з використанням DABCO як каталізатора можуть бути використані значно більш низькі кількості відносно дорогого каталізатора, ніж передбачається в публікації WO 01/72719, без зниження виходу. Крім зниження вартості є додаткова перевага з точки зору забруднення навколишнього середовища, оскільки зменшується кількість каталізатора, що виводиться з водними вихідними потоками процесу. Таким чином, відповідно до даного винаходу пропонується спосіб одержання сполуки формули (І): N N O O CN 20 W (I), де W являє собою метил-(Е)-2-(3-метоксі)акрилатну групу С(СО2СН3)=СНОСН3 або метил-2(3,3-диметокси)пропаноатну групу С(СО2СН3)СН(ОСН3)2, або суміш двох груп, і спосіб включає або: (а) взаємодію сполуки формули (II): N N Cl O W 25 (ІІ), де W має наведені вище значення, з 2-ціанофенолом або його сіллю (переважно з 2ціанофеноксидом калію) в присутності від 0,1 до 2 % мол. 1,4-діазабіцикло[2.2.2]октану, або (b) взаємодію сполуки формули (III): N N O Cl CN (ІІІ) із сполукою формули (IV): HO 30 W (IV), де W має наведені вище значення, в присутності від 0,1 до 2 % мол. 1,4діазабіцикло[2.2.2]октану. У переважному варіанті здійснення спосіб винаходу включає взаємодію сполуки формули (II): N Cl 35 N O W (II), де W має наведені вище значення, з 2-ціанофенолом або його сіллю (переважно з 2ціанофеноксидом калію) в присутності від 0,1 до 2 % мол. 1,4-діазабіцикло[2.2.2]октану. 1 UA 107443 C2 5 10 15 20 25 30 35 40 45 50 55 60 Сполука формули (І), де W являє собою метил-2-(3,3-диметокси)пропаноатну групу С(СО2СН3)СН(ОСН3)2 [тобто, сполуку метил-2-{2-[6-(2-ціанофенокси)піримідин-4-ілокси]феніл}3,3-диметоксипропаноат (звану далі "азоксистробінацеталь")], являє собою нову сполуку і складає частину даного винаходу. Зокрема, винахід включає виділений азоксистробінацеталь по суті в чистій формі [тобто, в формі продукту, що містить від 85 до 100 % мас., переважно від 90 до 100 % мас. азоксистробінацеталю]. Коли спосіб даного винаходу проводять з використанням сполуки формули (II), де W являє собою 2-(3,3-диметокси)пропаноатну групу, або з використанням сполуки формули (IV), де W являє собою 2-(3,3-диметокси)пропаноатну групу, одержаний продукт може містити деяку частку сполуки формули (І), де W являє собою метил-(Е)-2-(3-метоксі)акрилатну групу. Це відбувається, оскільки, мабуть, в умовах процесу метанол відщеплюється від метил-2-(3,3диметокси)пропаноатної групи. По тій же причині, якщо процес проводять з використанням сполуки формули (II) або сполуки формули (IV), де W являє собою суміш метил-2-(3,3диметокси)пропаноатної групи і метил-(Е)-2-(3-метоксі)акрилатної групи (а винахід включає такий процес), одержуваний продукт буде являти собою сполуку формули (І), де W являє собою суміш метил-2-(3,3-диметокси)пропаноатної групи і метил-(Е)-2-(3-метоксі)акрилатної групи; однак, продукт може містити більш високу частку сполуки формули (І), де W являє собою метил-(Е)-2-(3-метоксі)акрилатну групу, ніж очікується, виходячи з частки метил-(Е)-2-(3метоксі)акрилатної групи у вихідній суміші внаслідок такого можливого відщеплювання метанолу. Це не призводить до значущих наслідків, оскільки звичайно буде необхідно перетворити продукт формули (І), де W являє собою метил-2-(3,3-диметокси)пропаноатну групу, на сполуку формули (І), де W являє собою метил-(Е)-2-(3-метоксі)акрилатну групу, шляхом відщеплювання метанолу, як обговорювалося вище. Звичайно спосіб даного винаходу проводять у придатному інертному розчиннику або розріджувачі. Такі розчинники являють собою, наприклад, аліфатичні, аліциклічні і ароматичні вуглеводні, такі як петролейний ефір, гексан гептан, циклогексан, метилциклогексан, бензол, толуол, ксилол і декалін; галогеновані вуглеводні, такі як хлорбензол, дихлорбензол, дихлорметан, хлороформ, тетрахлорид вуглецю, дихлоретан і трихлоретан; гетероароматичні розчинники, такі як піридин або заміщений піридин, наприклад, 2,6-диметилпіридин; прості ефіри, такі як діетиловий ефір, діізопропіловий ефір, метил-трет-бутиловий ефір, метил-третаміловий ефір, діоксан, тетрагідрофуран, 1,2-диметоксіетан, 1,2-діетоксіетан і анізол; кетони, такі як ацетон, бутанон, метилізобутилкетон і циклогексанон; нітрили, такі як ацетонітрил, пропіонітрил, н-і ізо-бутиронітрил і бензонітрил; аміди, такі як N,N-диметилформамід, N-Nдиметилацетамід, N-метилформамід, N-метилпіролідон і триамід гексаметилфосфорної 1 2 3 1 2 3 кислоти; третинні аміни, зокрема аміни формули R R R N, де R , R і R кожний незалежно один від одного являє собою С 1-10-алкіл (особливо С1-8-алкіл), С3-6-циклоалкіл, арил (особливо феніл) 1 2 3 і арил(С1-4)алкіл (особливо бензил); або два або три замісники R , R і R об'єднані з атомом азоту, до якого вони приєднані, з утворенням одного, двох або трьох 5-, 6- або 7-членних аліциклічних кілець, які необов'язково конденсовані і необов'язково містять другий атом азоту в кільці, причому прикладами придатних третинних амінів є N,N-діізопропілетиламін (основа Ханіга), N,N-диметиланілін, триетиламін, трет.-бутилдиметиламін, N,N-діізопропілметиламін, N,N-діізопропілізобутиламін, N,N-діізопропіл-2-етилбутиламін, три-н-бутиламін, N,Nдициклогексилметиламін, N,N-дициклогексилетиламін, N-трет-бутилциклогексиламін, N,Nдиметилциклогексиламін, 1,5-діазабіцикло[4.3.0]нон-5-ен, 1,8-діазабіцикло[5.4.0]ундец-7-ен або 2-диметиламінопіридин; складні ефіри, такі як метилацетат, етилацетат і ізопропілацетат; сульфоксиди, такі як диметилсульфоксид; сульфони, такі як сульфолан; і суміші таких розчинників і розріджувачів і суміші одного або декількох з них з водою. Особливо придатними розріджувачами є кетони [такі як метилізобутилкетон і циклогексанон], складні ефіри [такі як ізопропілацетат], третинні аміни [такі як N,N-діізопропілетиламін (основа Ханіга)] і аміди [такі як N,N-диметилформамід]. У конкретному аспекті даного винаходу як розріджувач використовується метилізобутилкетон. У ще одному аспекті даного винаходу як розріджувач використовується циклогексанон. У ще одному аспекті даного винаходу як розріджувач використовується ізопропілацетат. У ще одному аспекті даного винаходу як розріджувач використовується N,N-диметилформамід. У ще одному аспекті даного винаходу як розріджувач використовується N,N-діізопропіл етил амін (основа Ханіга). Найбільш переважно розріджувач, що використовується в даному винаході, являє собою N,N-диметилформамід. У ще одному варіанті здійснення даного винаходу спосіб проводять у водній двофазній системі розчинника. Переважно в цьому варіанті, коли сполуку формули (II) вводять в реакцію з 2-ціанофенолом, 2-ціанофенол присутній у вигляді солі. Найбільш переважно сіль являє собою 2-ціанофеноксид калію. Переважно воду видаляють протягом всієї реакції. Придатними 2 UA 107443 C2 5 10 15 20 25 30 35 40 45 50 55 60 співрозчинниками для використання в такому водному процесі є розчинники, які являють собою щонайменше частково незмішувані з водою розчинники, такі як циклогексанон, метилізобутилкетон і ізопропілацетат. Найбільш переважно при використанні такої водної системи сіль 2-ціанофенолу являє собою 2-ціанофеноксид калію і розріджувачем є циклогексанон, метилізобутилкетон або ізопропілацетат. Потрібно зазначити, що, коли 2ціанофенол додають в процес у вигляді водного розчину 2-ціанофеноксиду калію, можна зменшити кількість використовуваного акцептора кислоти (див. нижче). Крім того, спосіб даного винаходу звичайно проводять в присутності акцептора кислоти. Придатними акцепторами кислоти є всі звичайні неорганічні і органічні основи. До них належать, наприклад, гідроксиди лужноземельних і лужних металів, ацетати, карбонати, бікарбонати і гідриди [такі як гідроксид натрію, гідроксид калію, ацетат натрію, ацетат калію, карбонат натрію, карбонат калію, бікарбонат натрію, бікарбонат калію, гідрид кальцію, гідрид натрію і гідрид калію], гуанідини, фосфазини (див., наприклад, Liebigs Ann., 1996, 1055-1081), фосфосфатрани (див., наприклад, JACS, 1990, 9421-9422) і третинні аміни [такі як аміни, які описані вище як можливі розчинники або розріджувачі]. Особливо переважними акцепторами кислоти є карбонати лужноземельних металів і лужних металів, особливо карбонат калію і карбонат натрію, і третинні аміни 1,5-діазабіцикло[4.3.0]нон-5-ен і 1,8-діазабіцикло[5.4.0]ундец-7-ен. Більш переважно акцептор кислоти являє собою карбонат калію. Більш переважно даний винахід проводять в присутності метилізобутилкетону, циклогексанону, ізопропілацетату, N,Nдіізопропілетиламіну (основа Ханіга) або N,N-диметилетилформаміду з карбонатом калію як акцептором кислоти. Спосіб даного винаходу проводять в присутності від 0,1 до 2 % мол. 1,4діазабіцикло[2.2.2]октану (DABCO), тобто в присутності більше ніж 0,1, але менше ніж 2 % мол. DABCO. Переважно спосіб проводять в присутності від 0,2 до 2 % мол. DABCO. Будь-яка кількість DABCO від 0,1 або 0,2 до 2, від 0,1 або 0,2 до 1,9, від 0,1 або 0,2 до 1,8, від 0,1 або 0,2 до 1,7, від 0,1 або 0,2 до 1,6 і від 0,1 або 0,2 до 1,5 % мол. прийнятна, але винахід має особливу перевагу в тому, що кількість використовуваного DABCO може складати від 0,2 до 1,4 % мол. Звичайно ця кількість буде складати від 0,5 до 1,4 % мол., звичайно від 0,8 до 1,2 % мол., наприклад, приблизно 1 % мол. У конкретному варіанті винаходу спосіб проводять в присутності приблизно 1 % мол. DABCO з метилізобутилкетоном, циклогексаноном, ізопропілацетатом, N,Nдіізопропілетиламіном (основа Ханіга) або N,N-диметилформамідом як розріджувачем. Найбільш переважно розріджувач являє собою N,N-диметилформамід. Переважно акцептором кислоти буде карбонат калію. При проведенні способу даного винаходу температура реакції може мінятися в межах відносно широкого інтервалу. Вибрана температура буде залежати від природи розчинника або розріджувача, наприклад, від його температури кипіння і/або його ефективності промотування цільової реакції і від швидкості, при якій реакція повинна бути проведена. У будь-якому конкретному розчиннику або розріджувачі реакція буде мати тенденцію протікати більш повільно при більш низьких температурах. У загальному випадку реакція може бути проведена при температурі від 0 до 120 °C, переважно при температурі від 40 до 100 °C, і звичайно при температурі від 45 до 95 °C, наприклад, від 60 до 85 °C. При проведенні способу даного винаходу звичайно на моль сполуки формули (II) використовується від 0,8 до 4 молів, звичайно від 0,95 до 1,2 моль 2-ціанофенолу; і аналогічні кількості (від 0,8 до 4 молів, звичайно від 0,95 до 1,2 моль) сполуки формули (IV) використовується на моль сполуки формули (III). Звичайно спосіб даного винаходу проводять шляхом змішування одного з компонентів реакції, переважно в присутності розчинника або розріджувача, з основою. Потім додають інший компонент, якщо необхідно в присутності розчинника або розріджувача, і суміш перемішують, звичайно при підвищеній температурі. Каталізатор DABCO може бути доданий на будь-якій стадії, але переважно його додають як останній компонент, оскільки це сприяє більш високому виходу продукту. Після підтвердження закінчення реакції реакційну суміш обробляють, і продукт виділяють з використанням звичайних методик, добре відомих кваліфікованому хіміку. 2-Ціанофенол являє собою комерційно доступний матеріал. Сполука формули (II), де W являє собою метил-(Е)-2-(3-метоксі)акрилатну групу С(СО2СН3)=СНОСН3, і сполука формули (II), де W являє собою метил-2-(3,3диметокси)пропаноатну групу С(СО2СН3)СН(ОСН3)2, можуть бути одержані, як описано в публікації WO 92/08703, за реакцією 3-(а-метокси)метиленбензофуран-2-(3Н)-ону (одержаного з бензофуран-2(3Н)-ону) з 4,6-дихлорпіримідином. Сполука формули (II), де W являє собою метил-(Е)-2-(3-метоксі)акрилатну групу, також може бути одержана шляхом відщеплювання 3 UA 107443 C2 5 10 15 20 25 метанолу (тобто, шляхом деметанолізу) від сполуки формули (II), де W являє собою метил-2(3,3-диметокси)пропаноатну групу, як описано в публікації WO 92/08703 або WO 98/07707. Сполука формули (II), де W являє собою метил-2-(3,3-диметокси)пропаноатну групу, може бути одержана, як описано в публікації GB-A-2291874, шляхом введення в реакцію сполуки формули (IV), де W являє собою метил-2-(3,3-диметокси)пропаноатну групу, з 4,6-дихлорпіримідином. Сполука може бути обчищена перед використанням за допомогою відомих методик або може бути використана в неочищеному стані з попередньої реакції, наприклад, в реакції "одного горщика". Сполука формули (IV), де W являє собою метил-2-(3,3-диметокси)пропаноатну групу, може бути одержана, як описано в публікації GB-A-2291874, з 3-(а-метокси)метиленбензофуран2(3H)-ону. Сполука формули (IV), де W являє собою метил-(Е)-2-(3-метоксі)акрилатну групу, може бути одержана деметанолізом сполуки формули (IV), де W являє собою метил-2-(3,3диметокси)пропаноатну групу. У цьому випадку фенольну групу перед деметанолізом необхідно захищати, наприклад, бензилуванням, а потім знімати захист. У ще одному аспекті даний винахід включає спосіб одержання сполуки формули (IV), де W являє собою метил-(Е)-2-(3-метоксі)акрилатну групу, який включає стадії: (і) взаємодії сполуки формули (IV), де W являє собою метил-2-(3,3-диметокси)пропаноатну групу, з реагентом, який буде захищати гідроксильну групу цієї сполуки від вступання в реакцію під час подальшого деметанолізу; (іі) відщеплювання метанолу від гідроксилзахищеної сполуки, утвореної на стадії (і); і (ііі) зняття групи, що захищає гідроксильну групу, утвореної на стадії (і), з утворенням сполуки формули (IV), де W являє собою метил-(Е)-2-(3-метоксі)акрилатну групу. На стадії (і) способу сполуку формули (IV), де W являє собою метил-2-(3,3диметокси)пропаноатну групу, вводять в реакцію зі стандартним захисним реагентом, таким як бензилгалогенід або заміщений бензилгалогенід [таким як 2-нітробензилгалогенід], наприклад, з бензилбромідом або 2-нітробензилбромідом, звичайно у придатному розчиннику, такому як N,Nдиметилформамід, і з придатною основою, такою як карбонат калію, з утворенням сполуки формули (V): O O O O O Q 30 35 40 45 50 (V), де Q являє собою захисну групу, таку як бензил або 2-нітробензил. На стадії (іі) способу метанол відщеплюють за допомогою будь-якого придатного фізичного або хімічного засобу, наприклад, як описано в публікаціях WO 92/08703 або WO 98/07707. Звичайно метанол відщеплюють шляхом обробки сполуки формули (V) метансульфоновою кислотою в присутності оцтового ангідриду при температурі в інтервалі, наприклад, від 20 до 110 °C, звичайно від 20 до 80 °C, переважно від 30 до 60 °C, наприклад, приблизно при 40 °C. На стадії (ііі) способу даного винаходу захисна група може бути видалена будь-якою стандартною методикою, наприклад, шляхом відновлення з використанням водню з каталізатором 10 % паладію/вугілля в етилацетаті при кімнатній температурі. Винахід також включає нові проміжні сполуки формули (V), де Q являє собою захисну групу, і переважна проміжна сполука формули (V), де Q являє собою бензил [тобто, сполука метил-2(2-бензилокси)феніл-3,3-диметоксипропаноат]. Більш переважно, винахід включає виділений метил-2-(2-бензилокси)феніл-3,3-диметоксипропаноат по суті в чистій формі [тобто, в ізольованій формі, яка містить від 85 до 100 % мас, переважно від 90 до 100 % мас. метил-2-(2бензилокси)феніл-3,3-диметоксипропаноату]. Подальші приклади ілюструють винахід. У всіх прикладах використовуються наступні скорочення: ДМФА = диметилформамід; МІБК (МІВК) = метилізобутилкетон; МГц = Мегагерц; Ar = арил; DABCO=1,4-діазабіцикло[2.2.2]октан; ЯМР = ядерний магнітний резонанс; Ру = піримідин. Приклади. 4 UA 107443 C2 5 10 15 20 25 30 35 40 45 50 55 Приклад 1. Наведені приклади описують послідовність дослідів, спланованих так, щоб показати вплив зниження концентрації DABCO. а) Сполучання метил-(Е)-2-{2-[6-хлорпіримідин-4-ілокси]феніл}-3-метоксіакрилату з 2ціанофенолом в ДМФА з 2 % мол. DABCO. Суспензію, що містить метил-(Е)-2-{2-[6-хлорпіримідин-4-ілокси]феніл}-3-метоксіакрилат (80,9 г при 99 %, 0,25 моль), карбонат калію (52,8 г при 98 %, 0,375 моль) і 2-ціанофенол (33,6 г при 97,5 %, 0,275 моль) в ДМФА (130 мл) нагрівають приблизно до 60 °C. Додають розчин DABCO (0,56 г, 0,005 моль) в ДМФА (10 мл). Суміш нагрівають до 80 °C і витримують при цій температурі протягом 60 хвилин. Видаляють ДМФА шляхом вакуумної відгонки. До залишку після відгонки додають толуол (160 мл) і воду (265 мл) і двофазну суміш нагрівають до 70-80 °C. Суміш перемішують протягом 40 хвилин, потім відстоюють і нижню водну фазу відділяють. Толуольний розчин (237,8 г) містить метил-(Е)-2-{2-[6-(2-ціанофенокси)піримідин-4ілокси]феніл}-3-метоксіакрилат (41,3 % мас/мас), 97,5 % від теорії. b) Сполучання метил-(Е)-2-{2-[6-хлорпіримідин-4-ілокси]феніл)-3-метоксіакрилату з 2ціанофенолом в ДМФА з 1 % мол. DABCO. Суспензію, що містить метил-(Е)-2-{2-[6-хлорпіримідин-4-ілокси]феніл}-3-метоксіакрилат (80,9 г при 99 %, 0,25 моль), карбонат калію (52,8 г при 98 %, 0,375 моль) і 2-ціанофенол (33,6 г при 97,5 %, 0,275 моль) в ДМФА (130 мл) нагрівають приблизно до 60 °C. Додають розчин DABCO (0,28 г, 0,0025 моль) в ДМФА (10 мл). Суміш нагрівають до 80 °C і витримують при цій температурі протягом 60 хвилин. Видаляють ДМФА шляхом вакуумної відгонки. До залишку після відгонки додають толуол (160 мл) і воду (265 мл) і двофазну суміш нагрівають до 70-80 °C. Суміш перемішують протягом 40 хвилин, потім відстоюють і нижню водну фазу відділяють. Толуольний розчин (227,9 г) містить метил-(Е)-2-{2-[6-(2-ціанофенокси)піримідин-4ілокси]феніл}-3-метоксіакрилат (43,6 % мас/мас), 98,7 % від теорії. с) Сполучання метил-(Е)-2-{2-[6-хлорпіримідин-4-ілокси]феніл}-3-метоксіакрилату з 2ціанофенолом в ДМФА з 0,2 % мол. DABCO. Суспензію, що містить метил-(Е)-2-{2-[6-хлорпіримідин-4-ілокси]феніл}-3-метоксіакрилат (80,9 г при 99 %, 0,25 моль), карбонат калію (52,8 г при 98 %, 0,375 моль) і 2-ціанофенол (33,6 г при 97,5 %, 0,275 моль) в ДМФА (130 мл) нагрівають приблизно до 60 °C. Додають розчин DABCO (0,056 г, 0,0005 моль) в ДМФА (10 мл). Суміш нагрівають до 80 °C і витримують при цій температурі протягом 300 хвилин. Видаляють ДМФА шляхом вакуумної відгонки. До залишку після відгонки додають толуол (160 мл) і воду (265 мл) і двофазну суміш нагрівають до 70-80 °C. Суміш перемішують протягом 40 хвилин, потім відстоюють і нижню водну фазу відділяють. Толуольний розчин (243,1 г) містить метил-(Е)-2-{2-[6-(2-ціанофенокси)піримідин-4ілокси]феніл}-3-метоксіакрилат (38,6 % мас/мас), 93,1 % від теорії. d) Сполучання метил-(E)-2-{2-[6-хлорпіримідин-4-ілокси]феніл}-3-метоксіакрилату з 2ціанофенолом в ДМФА з 0.1 % мол. DABCO. Суспензію, що містить метил-(Е)-2-{2-[6-хлорпіримідин-4-ілокси]феніл}-3-метоксіакрилат (80,9 г при 99 %, 0,25 моль), карбонат калію (52,8 г при 98 %, 0,375 моль) і 2-ціанофенол (33,6 г при 97,5 %, 0,275 моль) в ДМФА (130 мл) нагрівають приблизно до 60 °C. Додають розчин DABCO (0,028 г, 0,00025 моль) в ДМФА (10 мл). Суміш нагрівають до 80 °C і витримують при цій температурі протягом 300 хвилин. Видаляють ДМФА шляхом вакуумної відгонки. До залишку після відгонки додають толуол (160 мл), підтримуючи температуру 70-80 °C, потім додають воду (265 мл), яка нагріта до 60 °C. Суміш перемішують протягом 40 хвилин, потім відстоюють і нижню водну фазу відділяють. Толуольний розчин (226,7 г) містить метил-(Е)-2-{2-[6-(2ціанофенокси)піримідин-4-ілокси]феніл}-3-метоксіакрилат (41,5 % мас/мас), 93,4 % від теорії. e) Сполучання метил-(Е)-2-(2-[6-хлорпіримідин-4-ілокси]феніл}-3-метоксіакрилату з 2ціанофенолом в ДМФА за відсутності DABCO. Суспензію, що містить метил-(Е)-2-{2-[6-хлорпіримідин-4-ілокси]феніл}-3-метоксіакрилат (80,9 г при 99 %, 0,25 моль), карбонат калію (52,8 г при 98 %, 0,375 моль) і 2-ціанофенол (33,6 г при 97,5 %, 0,275 моль) в ДМФА (130 мл) нагрівають приблизно до 80 °C і витримують при цій температурі протягом 8 годин. Видаляють ДМФА шляхом вакуумної відгонки до максимальної температури 100 °C. До залишку після відгонки додають толуол (160 мл), підтримуючи температуру 60-70 °C, потім додають воду (265 мл), яка нагріта до 60 °C, знов підтримуючи температуру 60-70 °C. Суміш перемішують протягом 40 хвилин при 80 °C, потім відстоюють і нижню водну фазу відділяють. Толуольний розчин (223,3 г) містить метил-(Е)-2-{2-[6-(2ціанофенокси)піримідин-4-ілокси]феніл}-3-метоксіакрилат (38,8 % мас/мас), 86,6 % від теорії. Одержані результати даних дослідів наведені в наступній таблиці. 60 5 UA 107443 C2 Таблиця 1 Концентрація DABCO 2,0 % мол. 1,0 % мол. 0,2 % мол. 0,1 % мол. Нуль 5 10 15 20 25 30 35 40 45 50 Виділений азоксистробін (% від теорії) 97,5 98,7 93,1 93,4 86,6 Як можна побачити, несподівано вихід азоксистробіну, що утворюється в способі, не знижується значною мірою, коли концентрація DABCO знижується нижче 2 % мол.; навіть концентрації DABCO до 0,1 % мол. досить, щоб одержати вихід 93,4 % від теоретичного виходу. Крім того, видно, що дослід за відсутності DABCO не тільки дає набагато більш низький вихід, але також вимагає 8 годин для досягнення вказаної точки в порівнянні з 5 годинами у випадку концентрації 0,1 % мол. і 0,2 % мол. DABCO і 60 хвилин у випадку концентрації 1,0 % мол. і 2,0 % мол. DABCO (в зв'язку з цим також можна зазначити, що дослід із вмістом 1,0 % DABCO несподівано дає аналогічний вихід при тому ж часі, що і дослід із вмістом 2,0 % мол. DABCO). Приклад 2. Додаткові окремі досліди проведені для вивчення виходу, одержуваного при низьких рівнях DABCO, коли використовуються різні розчинники. Крім того, в прикладі 2с) наведені характерні дані для метил-2-{2-[6-(2-ціанофенокси)піримідин-4-ілокси]феніл}-3,3-диметоксипропаноату. a) Одержання азоксистробіну шляхом сполучання 2-ціанофенолу і метил-(Е)-2-{2-[6хлорпіримідин-4-ілокси]феніл}-3-метоксіакрилату в ДМФА з 1 % мол. DABCO. До розчину метил-(Е)-2-{2-[6-хлорпіримідин-4-ілокси]феніл}-3-метоксіакрилату (96,2 г, одержаний, як описано в публікації WO 92/08703) в ДМФА (приблизно 100 г) додають розчин 2ціанофенолу в ДМФА (78,5 г при 50 % мас/мас. 2-ціанофенолу), після чого додають карбонат калію (63,5 г) і DABCO (0,34 г). Суміш нагрівають до 80 °C і витримують протягом 75 хвилин. ДМФА видаляють вакуумною відгонкою до кінцевої температури 100 °C. Толуол (165,8 г) додають до залишку після відгонки і температуру підіймають до 75 °C, потім додають гарячу воду (318,6 г) і перемішують 30 хвилин при 80 °C. Водну фазу видаляють і потім відбирають зразок толуольного шару і аналізують. Вихід розчину метил-(Е)-2-{2-[6-(2ціанофенокси)піримідин-4-ілокси]феніл}-3-метоксіакрилату (азоксистробіну) становить 90,0 %. Толуол відганяють у вакуумі. До залишку після відгонки додають метанол (88 г) і суміш охолоджують до
ДивитисяДодаткова інформація
Автори англійськоюWhitton Alan John, Boyd Ewan Campbell, Vass Jack
Автори російськоюУиттон Алан Джон, Бойд Эван Кемпбелл, Васс Джек
МПК / Мітки
МПК: C07C 69/734, C07C 67/31
Код посилання
<a href="https://ua.patents.su/16-107443-khimichnijj-sposib.html" target="_blank" rel="follow" title="База патентів України">Хімічний спосіб</a>
Попередній патент: Суміш жирних кислот та її застосування
Наступний патент: Інгібітори seh та їх застосування
Випадковий патент: Спосіб корекції больового синдрому при порушенні функції підшлункової залози у дітей з хронічною гастродуоденальною патологією