Сполуки бензотіадіазепіну, спосіб їх одержання і фармацевтичні композиції, які їх містять
Номер патенту: 100477
Опубліковано: 25.12.2012
Автори: Лєстаж П'єр, Корді Алексіс, Десос Патріс, Данобер Лоранс
Формула / Реферат
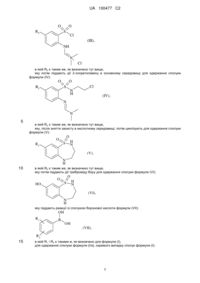
1. Сполука формули (І):
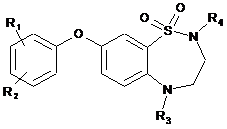 , (I)
, (I)
в якій:
R1 і R2, які можуть бути однаковими або відрізнятись, кожний являє собою атом водню; лінійну або розгалужену (С1-С6)алкільну групу, не заміщену або заміщену одним або більше атомами галогену; лінійну або розгалужену (С1-С6)алкоксигрупу; лінійну або розгалужену (С1-С6)алкілтіогрупу; лінійну або розгалужену (С1-С6)алкоксикарбонільну групу; карбоксигрупу; лінійну або розгалужену (С1-С6)ацильну групу; гідроксигрупу; лінійну або розгалужену (С1-С6)гідроксіалкільну групу; ціаногрупу, нітрогрупу; аміногрупу, не заміщену або заміщену однією або декількома лінійними або розгалуженими (С1-С6)алкільними групами; аміногрупу, заміщену лінійною або розгалуженою (С1-С6)ацильною групою; амінокарбонільну групу, не заміщену або заміщену однією або декількома лінійними або розгалуженими (С1-С6)алкільними групами; аміносульфонільну групу, не заміщену або заміщену однією або декількома лінійними або розгалуженими (С1-С6)алкільними групами; (С1-С6)алкілсульфоніламіно(С1-С6)алкільну групу, в якій алкільні частини є лінійними або розгалуженими; N-гідроксикарбоксімідамідну групу або бензилоксигрупу,
R3 являє собою атом водню, лінійну або розгалужену (С1-С6)алкільну групу, (С3-С8)циклоалкільну групу або (С3-С8)циклоалкіл(С1-С6)алкільну групу, в якій алкільна частина є лінійною або розгалуженою,
R4 являє собою атом водню або лінійну або розгалужену (С1-С6)алкільну групу, не заміщену або заміщену одним або більше атомами галогену, її оптичні і позиційні ізомери, а також її адитивні солі з фармацевтично прийнятною кислотою або основою.
2. Сполука формули (І) за п. 1, яка відрізняється тим, що група R1 являє собою атом водню або гідроксигрупу, гідроксиметильну групу, етоксикарбонільну групу, аміногрупу або N-метиламінокарбонільну групу.
3. Сполука формули (І) за п. 1 або п. 2, яка відрізняється тим, що група R1 знаходиться у мета- або пара-положенні.
4. Сполука формули (І) за будь-яким з пп. 1-3, яка відрізняється тим, що групи R2 і R4 являють собою атоми водню.
5. Сполука формули (І) за будь-яким з пп. 1-4, яка відрізняється тим, що група R3 являє собою атом водню або метильну групу.
6. Сполука формули (І) за п. 1, яка вибрана з групи:
8-фенокси-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепіну 1,1-діоксид;
етил-3-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-іл)окси]бензоат;
3-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-іл)окси]-N-метилу бензамід;
{3-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-іл)-окси]феніл}метанол;
4-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-іл)окси]фенол;
4-[(5-метил-1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-іл)окси]фенол;
4-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-іл)оксі]анілін,
а також її адитивні солі з фармацевтично прийнятною кислотою або основою.
7. Спосіб одержання сполуки формули (І), вказаної у п. 1, який відрізняється тим, що як вихідний матеріал використовують сполуку формули (II):
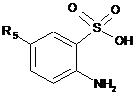 , (II)
, (II)
в якій R5 являє собою лінійну або розгалужену (С1-С6)алкоксигрупу,
яку піддають реакції з тіонілхлоридом у присутності диметилформаміду для одержання сполуки формули (III):
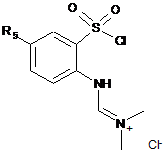 , (III)
, (III)
в якій R5 є таким же, як визначено тут вище,
яку потім піддають дії 2-хлоретиламіну в основному середовищі для одержання сполуки формули (IV):
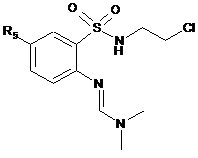 , (IV)
, (IV)
в якій R5 є таким же, як визначено тут вище,
яку, після зняття захисту в кислотному середовищі, потім циклізують для одержання сполуки формули (V):
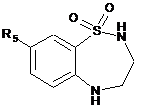 , (V)
, (V)
в якій R5 є таким же, як визначено тут вище,
яку потім піддають дії триброміду бору для одержання сполуки формули (VI):
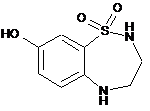 , (VI)
, (VI)
яку піддають реакції зі сполукою боронової кислоти формули (VII):
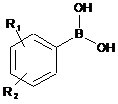 , (VII)
, (VII)
в якій R1 і R2 є такими ж, як визначено для формули (І),
для одержання сполуки формули (І/а), окремого випадку сполук формули (І):
 , (I/a)
, (I/a)
в якій R1 і R2 є такими ж, як визначено тут вище,
варіант одержання сполуки формули (І/а), який включає застосування - після проведення етапу зв'язування зі сполукою формули (VI) - звичайних хімічних реакцій, щоб згодом модифікувати замісники сполуки боронової кислоти,
сполуку формули (І/а) можуть потім, якщо бажано, піддавати:
або подвійному алкілуванню на атомах азоту у положеннях 2 і 5 шляхом дії сильної основи у присутності алкілуючого агента R'-X, де R' являє собою лінійну або розгалужену (С1-С6)алкільну групу і X являє собою атом галогену,
для одержання сполуки формули (І/b), окремого випадку сполук формули (І):
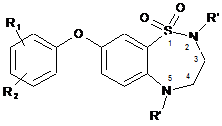 , (I/b)
, (I/b)
в якій R1, R2 і R' є такими ж, як визначено тут вище,
або алкілуванню на атомі азоту у положенні 2 шляхом дії основи у присутності алкілуючого агента R'4-X, в якому R'4 являє собою лінійну або розгалужену (С1-С6)алкільну групу, не заміщену або заміщену одним або більше атомами галогену, і X являє собою атом галогену,
для одержання сполуки формули (І/с), окремого випадку сполук формули (І):
 , (I/c)
, (I/c)
в якій R1, R2 і R'4 є такими ж, як визначено тут вище,
яку можуть необов'язково піддавати алкілуванню на атомі азоту у положенні 5 шляхом дії основи у присутності алкілуючого агента R'3-X, в якому R'3 являє собою лінійну або розгалужену (С1-С6)алкільну групу, (С3-С8)циклоалкільну групу або (С3-С8)циклоалкіл(С1-С6)алкільну групу, в якій алкільна частина є лінійною або розгалуженою, а X являє собою атом галогену,
для одержання сполуки формули (І/d):
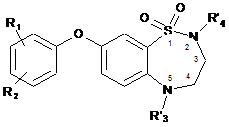 , (I/d)
, (I/d)
в якій R1, R2, R'3 і R'4 є такими ж, як визначено тут вище,
або альтернативно алкілуванню на атомі азоту у положенні 5 за допомогою відновного амінування, використовуючи відновлювальний агент, такий як триацетоксиборгідрид або ціаноборгідрид натрію у присутності:
або [(1-етоксициклопропіл)окси]триметилсилану,
або сполуки формули (VIII):
R"3-CHO, (VIII)
в якій R"3 являє собою атом водню або лінійну або розгалужену (С1-С5)алкільну групу, (С3-С8)циклоалкільну групу або (С3-С8)циклоалкіл(С1-С5)групу, в якій алкільна частина є лінійною або розгалуженою,
або альтернативно сполуки формули (IX):
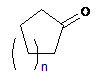 , (IX)
, (IX)
в якій 0 £ n £ 4,
для одержання сполуки формули (І/е), окремого випадку сполук формули (І):
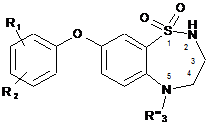 , (I/e)
, (I/e)
в якій R'"3 являє собою лінійну або розгалужену (С1-С6)алкільну групу, (С3-С8)циклоалкільну групу або (С3-С8)циклоалкіл(С1-С6)групу, в якій алкільна частина є лінійною або розгалуженою, і R1 і R2 є такими ж, як визначено тут вище,
яку можуть необов'язково піддавати алкілуванню на атомі азоту у положенні 2 шляхом дії основи у присутності алкілуючого агента R"4-X, в якому R"4 являє собою лінійну або розгалужену (С1-С6)алкільну групу, яка є не заміщеною або заміщеною одним або декількома атомами галогену, і X являє собою атом галогену,
для одержання сполуки формули (І/f):
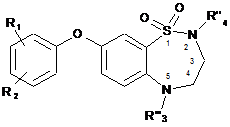 , (I/f)
, (I/f)
в якій R1, R2, R'"3 і R"4 є такими ж, як визначено тут вище,
сполуки формул (І/а)-(І/f), які складають сукупність сполук формули (І), можуть потім бути очищені відповідно до звичайної методики розділення, перетворені, якщо бажано, в їх адитивні солі з фармацевтично прийнятною кислотою або основою і розділені, коли прийнятно, на їх оптичні і позиційні ізомери, якщо вони існують, відповідно до звичайної методики розділення.
8. Сполука формули (VI), вказана у п. 7:
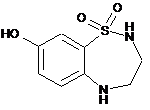 , (VI)
, (VI)
яка відрізняється тим, що вона призначена для використання як проміжної сполуки в синтезі сполук формули (І).
9. Фармацевтична композиція, яка містить як активний інгредієнт сполуку, вказану у будь-якому з пп. 1-6, у поєднанні з одним або більше фармацевтично прийнятними, нетоксичними, інертними носіями.
10. Фармацевтична композиція за п. 9 для застосування у виробництві лікарських засобів для використання як модуляторів рецептора АМРА і антагоністів рецептора NMDA.
11. Фармацевтична композиція за п. 9 для застосування у виробництві лікарських засобів для використання у лікуванні або попередженні прогресуючих нейродегенеративних захворювань, хвороби Альцгеймера, хвороби Паркінсона, атрофії Піка, хореї Хангтінгтона, корсаківського психозу, шизофренії, гострих нейродегенеративних захворювань, деменції лобової частки і підкоркової деменції, судинної деменції, епілепсії, інсультів, а також депресивних і тривожних станів.
Текст
Реферат: Сполука формули (І): R1 R2 O O O S R4 N N R3 , (I) в якій: R1 і R2, які можуть бути однаковими або відрізнятись, кожний являє собою атом водню або алкільну, алкокси, алкілтіо, ацильну, алкоксикарбонільну, карбокси, гідрокси, гідроксіалкільну, ціано, нітро, аміно, заміщену або незаміщену амінокарбонільну, аміносульфонільну, алкілсульфоніламіноалкільну, N-гідроксикарбоксімідамідну або бензилоксигрупу, R3 являє собою атом водню або алкільну, циклоалкільну або циклоалкілалкільну групу, R4 являє собою атом водню або заміщену або незаміщену алкільну групу. UA 100477 C2 (12) UA 100477 C2 Лікарські засоби. UA 100477 C2 5 10 15 20 25 30 35 40 45 Даний винахід стосується нових сполук бензотіадіазепіну, способу їх одержання, фармацевтичних композицій, які їх містять, а також їх застосування як позитивних алостеричних модуляторів рецепторів АМРА і антагоністів рецепторів NMDA. На сьогоднішній день визнано, що збуджувальні амінокислоти, особливо глутамат, відіграють вирішальну роль у фізіологічних процесах нейронної пластичності і в механізмах, що лежать в основі навчання і запам’ятовування. Патофізіологічні дослідження чітко продемонстрували, що дефіцит у глутаматергічній нейротрансмісії тісно пов’язаний з розвитком хвороби Альцгеймера (Neuroscience and Biobehavioral reviews, 1992, 16, 13-24 ; Progress in Neurobiology, 1992, 39, 517-545). Крім того, деякі роботи продемонстрували існування підтипів рецепторів збуджувальних амінокислот і їх функціональних взаємодій (Molecular Neuropharmacology, 1992, 2,15-31). Серед таких рецепторів, рецептор AMPА (α-аміно-3-гідрокси-5-метил-4-ізоксазол-пропіонова + + кислота) являє собою рецептор-канал для глутамату, який є проникним для Na і K і має низьку 2+ проникність для Ca . Рецептор AMPА, очевидно, залучений найбільшим чином у явища фізіологічної збуджувальної синаптичної передачі і, особливо, в ті явища, які залучені до процесів запам’ятовування. Наприклад, було виявлено, що навчання пов’язане зі зростанням кількості рецепторів AMPА у синаптичних контактах в гіпокампусі, одній з ділянок мозку, суттєвих для процесів запам’ятовування і пізнавання. Також, ноотропні агенти, такі як анірацетам, нещодавно були описані як такі, що модулюють AMPA рецептори нейронних клітин позитивним чином (Journal of Neurochemistry, 1992, 58, 1199-1204). Другий рецептор, рецептор NMDA (N-метил-D-аспартат), також належить до одного з трьох кластів рецепторів-каналів глутамату. Зв’язування глутамату і його спів-агоністу, гліцину, є 2+ необхідним для досягнення відкриття каналу і надання можливості Ca увійти у клітину (Progress in Neurobiology, 1998, 54, 581-618; Handb. Exp. Pharmacol., 2005, 169, 249-303). Рецептори NMDA подібним чином відіграють важливу фізіологічну роль у процесі навчання і запам’ятовування. Не дивлячись на це, надмірна активація цих рецепторів, яка може статись при церебральній ішемії і аноксії головного мозку, приступах епілепсії, емоційних травмах або 2+ нейродегенеративних захворюваннях, приводить до входження надмірної кількості Ca у клітину, що потенційно може призвести до смерті клітини через явище ексайтотоксичності (Progress in Neurobiology, 1998, 54, 369-415; J. Pharmacol. Exp. Ther., 2002, 300, 717-723). Було доведено, що деякі форми нейротоксичності, викликані глутаматом, залежать від акумулювання 2+ Ca у клітині, що призводить до збільшення метаболічного стресу в мітохондрії і до збільшення у продукуванні вільних радикалів. З цих причин було розроблено антагоністи рецепторів NMDA, через їх нейропротективні властивості, включаючи мемантин, який на даний момент призначають для лікування від помірно тяжкої до тяжкої форм хвороби Альцгеймера (Neuropharmacology, 1999, 38, 735-767; Dement. Geriatr. Cogn. Disord., 2005, 19, 229- 245). В літературі лише декілька сполук, які мають бензотіадіазинову структуру, було описано як такі, що являють собою позитивні модулятори рецепторів АМРА, які також мають активність як антагоністи рецепторів NMDA (Neuropharmacology, 2004, 46, 1105-1113). Сполука IDRA-21, зокрема, здатна покращувати роботу пам’яті. Опис патенту WO 99/42456, серед іншого, розкриває сполуки бензотіадіазину і бензотіадіазепіну як модулятори рецепторів АМРА. Сполуки бензотіадіазепіну за даним винаходом окрім того, що вони є новими, також проявляють фармакологічну активність по відношенню як до рецептора АМРА, так і до рецептора NMDA, яка є значно кращою, ніж активність сполук, що мають подібну структуру, розкриту у попередньому рівні техніки. Більш конкретно, даний винахід стосується сполук формули (І): O O R1 S O R4 N (I), R2 N R3 50 в якій: - R1 і R2, які можуть бути однаковими або відрізнятись, кожний являє собою атом водню; лінійну або розгалужену (C1-C6)алкільну групу, не заміщену або заміщену одним або більше атомами галогену; лінійну або розгалужену (C1-C6)алкоксигрупу; лінійну або розгалужену (C1 1 UA 100477 C2 5 10 15 20 25 30 35 40 45 C6)алкілтіогрупу; лінійну або розгалужену (C1-C6)алкоксикарбонільну групу; карбоксигрупу; лінійну або розгалужену (C1-C6)ацильну групу; гідроксигрупу; лінійну або розгалужену (C 1C6)гідроксіалкільну групу; ціаногрупу, нітрогрупу; аміногрупу, не заміщену або заміщену однією або декількома лінійними або розгалуженими (C 1-C6)алкільними групами; аміногрупу, заміщену лінійною або розгалуженою (C1-C6)ацильною групою; амінокарбонільну групу, не заміщену або заміщену однією або декількома лінійними або розгалуженими (C1-C6)алкільними групами; аміносульфонільну групу, не заміщену або заміщену однією або декількома лінійними або розгалуженими (C1-C6)алкільними групами; (C1-C6)алкілсульфоніламіно(C1-C6)алкільну групу, в якій алкільні частини є лінійними або розгалуженими; N-гідроксикарбоксимідамідну групу; або бензилоксигрупу, - R3 являє собою атом водню, лінійну або розгалужену (C 1-C6)алкільну групу, (C3C8)циклоалкільну групу або (C3-C8)циклоалкіл(C1-C6) алкільну групу, в якій алкільна частина є лінійною або розгалуженою, - R4 являє собою атом водню або лінійну або розгалужену (C 1-C6)алкільну групу, не заміщену або заміщену одним або більше атомами галогену, їх оптичних і позиційних ізомерів, коли вони існують, а також їх адитивних солей з фармацевтично прийнятною кислотою або основою. Серед фармацевтично прийнятних кислот можуть бути згадані, без будь-якого обмеження, хлористоводнева кислота, бромистоводнева кислота, сірчана кислота, фосфорна кислота, оцтова кислота, трифтороцтова кислота, молочна кислота, піровиноградна кислота, малонова кислота, янтарна кислота, глутарова кислота, фумарова кислота, винна кислота, малеїнова кислота, лимонна кислота, аскорбінова кислота, щавлева кислота, метансульфонова кисла, бензолсульфонова кислота і камфорна кислота. Серед фармацевтично прийнятних основ можуть бути згадані, без будь-якого обмеження, гідроксид натрію, гідроксид калію, триетиламін і трет-бутиламін. Група R1 переважно являє собою атом галогену або гідроксигрупу; лінійну або розгалужену (C1-C6)гідроксіалкільну групу і, більш конкретно, гідроксиметильну групу; лінійну або розгалужену (C1-C6)алкоксикарбонільну групу і, переважно, етоксикарбонільну групу; аміногрупу, або амінокарбонільну групу, заміщену лінійною або розгалуженою (C 1-C6)алкільною групою і, більш конкретно, N-метил-амінокарбонільну групу. Перевага надається групі R 1, яка знаходиться у мета- або пара-положенні. R1 зокрема переважно являє собою атом водню. Групи R2 і R4 кожна переважно являє собою атом водню. R3 переважно являє собою атом водню або метильну групу. Переважні сполуки за даним винаходом являють собою: - 8-фенокси-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепіну 1,1-діоксид; - етил 3-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-іл)окси]бензоат; - 3-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-іл)окси]-N-метилу бензамід; - {3-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-іл)-окси]феніл}метанол; - 4-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-іл)окси]-фенол; - 4-[(5-метил-1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-іл)окси]фенол; - 4-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-іл)окси]-анілін. Адитивні солі з фармацевтично прийнятною кислотою або основою переважних сполук даного винаходу утворюють невід’ємну частину даного винаходу. Даний винахід стосується також способу одержання сполук формули (І), який відрізняється тим, що як вихідний матеріал використовують сполуку формули (ІІ): O R5 O S OH (II), NH2 в якій R5 являє собою лінійну або розгалужену (C1-C6)алкоксигрупу, яку піддають реакції з тіонілхлоридом у присутності диметилформаміду для одержання сполуки формули (III): 2 UA 100477 C2 O O S R5 Cl (III), NH N+ Cl в якій R5 є таким же, як визначено тут вище, яку потім піддають дії 2-хлоретиламіну в основному середовищі для одержання сполуки формули (IV): O O Cl S R5 N H (IV), N N 5 в якій R5 є таким же, як визначено тут вище, яку, після зняття захисту в кислотному середовищі, потім циклізують для одержання сполуки формули (V): O O S R5 H N (V), N H 10 в якій R5 є таким же, як визначено тут вище, яку потім піддають дії триброміду бору для одержання сполуки формули (VI): O O S HO H N (VI), N H яку піддають реакції зі сполукою боронової кислоти формули (VII): OH R1 B OH (VII), R2 15 в якій R1 і R2 є такими ж, як визначено для формули (I), для одержання сполуки формули (I/a), окремого випадку сполук формули (I): 3 UA 100477 C2 O O R1 H N S O 1 2 3 5 N H R2 5 10 (I/a), 4 в якій R1 і R2 є такими ж, як визначено для формули (I), варіант одержання сполуки формули (I/a), який включає застосування - після проведення етапу зв’язування зі сполукою формули (VI) - звичайних хімічних реакцій, щоб згодом модифікувати замісники сполуки боронової кислоти, сполуку формули (I/a) можуть потім, якщо бажано, піддавати: - або подвійному алкілуванню на атомах азоту у положеннях 2 і 5, шляхом дії сильної основи у присутності алкілуючого агента R’-X, де R' являє собою лінійну або розгалужену (C 1-C6)алкільну групу і X являє собою атом галогену, для одержання сполуки формули (I/b), окремого випадку сполук формули (I): O O R1 R' S O 1 N 2 3 5 (I/b), 4 N R2 R' 15 в якій R1, R2 і R' є такими ж, як визначено тут вище, - або алкілуванню на атомі азоту у положенні 2, шляхом дії основи у присутності алкілуючого агента R'4-X, в якому R'4 являє собою лінійну або розгалужену (C1-C6)алкільну групу, не заміщену або заміщену одним або більше атомами галогену, і X являє собою атом галогену, для одержання сполуки формули (I/c), окремого випадку сполук формули (I): O O R1 S O R'4 N 1 2 3 5 N H R2 20 (I/c), 4 в якій R1, R2 і R'4 є такими ж, як визначено тут вище, яку можуть необов’язково піддавати алкілуванню на атомі азоту у положенні 5, шляхом дії основи у присутності алкілуючого агента R'3-X, в якому R'3 являє собою лінійну або розгалужену (C1-C6)алкільну групу, (C3-C8)циклоалкільну групу або (C3-C8)циклоалкіл(C1-C6)алкільну групу, в якій алкільна частина є лінійною або розгалуженою, а X являє собою атом галогену, для одержання сполуки формули (I/d): R1 O O S O 1 R'4 N 2 3 5 R2 (I/d), 4 N R'3 25 в якій R1, R2, R'3 і R'4 є такими ж, як визначено тут вище, - або альтернативно алкілуванню на атомі азоту у положенні 5, за допомогою відновного амінування, використовуючи відновлювальний агент, такий як триацетоксиборгідрид або ціаноборгідрид натрію у присутності: - або [(1-етоксициклопропіл)окси]триметилсилану, 4 UA 100477 C2 5 - або сполуки формули (VIII): R''3-CHO (VIII), в якій R''3 являє собою атом водню або лінійну або розгалужену (C 1-C5)алкільну групу, (C3C8)циклоалкільну групу або (C3-C8)циклоалкіл(C1-C5)групу, в якій алкільна частина є лінійною або розгалуженою, - або альтернативно сполуки формули (IX): O (IX), n в якій 0 n 4, для одержання сполуки формули (I/e), окремого випадку сполук формули (I): O O R1 H N S O 1 2 3 N R2 10 15 (I/e), 4 5 R'''3 в якій R'''3 являє собою лінійну або розгалужену (C 1-C6)алкільну групу, (C3-C8)циклоалкільну групу або (C3-C8)циклоалкіл(C1-C6)групу, в якій алкільна частина є лінійною або розгалуженою, і R1 і R2 є такими ж, як визначено тут вище, яку можуть необов’язково піддавати алкілуванню на атомі азоту у положенні 2, шляхом дії основи у присутності алкілуючого агента R'' 4-X, в якому R''4 являє собою лінійну або розгалужену (C1-C6)алкільну групу, яка є не заміщеною або заміщеною одним або декількома атомами галогену, і X являє собою атом галогену, для одержання сполуки формули (I/f): O O R1 S O 1 R''4 N 2 3 5 R2 (I/f), 4 N R'''3 20 25 30 35 в якій R1, R2, R'''3 і R''4 є такими ж, як визначено тут вище, сполуки формул (I/a) - (I/f), які складають сукупність сполук формули (I), можуть бути очищені відповідно до звичайної методики розділення, перетворені, якщо бажано, в їх адитивні солі з фармацевтично прийнятною кислотою або основою і розділені, коли прийнятно, на їх оптичні і позиційні ізомери, якщо вони існують, відповідно до звичайної методики розділення. Сполуки формул (II) і (VII) є комерційно доступними або їх легко одержати фахівцю в даній галузі техніки, використовуючи звичайні хімічні реакції або хімічні реакції, розкриті в літературі. Сполука формули (VI) є новою і як проміжна сполука синтезу сполук формули (I) також утворює частину даного винаходу. Сполуки формули (I) за даним винаходом мають властивості щодо активації рецептора AMPA і властивості як антагоніста рецептора NMDA, що робить їх корисними у лікуванні або попередженні прогресуючих нейродегенеративних захворювань, хвороби Альцгеймера, хвороби Паркінсона, атрофії Піка, хореї Хангтінгтона, корсаковсього психозу, шизофренії, гострих нейродегенеративних захворювань, деменції лобової частки і підкоркової деменції, судинної деменції, епілепсії, інсультів, а також депресивних і тривожних станів. Винахід також стосується фармацевтичних композицій, які містять як активний інгредієнт щонайменше одну сполуку формули (I) з одним або більше прийнятним, інертним, нетоксичним наповнювачем. Серед фармацевтичних композицій за даним винаходом можуть бути згадані більш конкретно ті, які придатні для орального, парентерального (внутрішньовенного або підшкірного), назального, перкутанного, транскутанного, ректального, під’язикового, очного і респіраторного введення і, особливо, таблетки або драже, під’язикові таблетки, саше, пакетики, 5 UA 100477 C2 5 10 15 20 25 30 35 40 45 50 55 капсули, коржики, таблетки для повільного розчинення під язиком, супозиторії, креми, мазі, шкірні гелі, препарати для ін’єкцій і питні суспензії. Корисне дозування змінюється в залежності від природи і тяжкості розладу, шляху введення, а також ваги і віку пацієнта, і знаходиться в діапазоні від 0,01 мг до 1 г на день за одне або більше введень. Наступні приклади ілюструють даний винахід, але не обмежують його жодним чином. Використані вихідні матеріали являють собою або відомі продукти, або продукти, які одержують відповідно до відомих методик. Структури сполук, розкритих у Прикладах, визначають відповідно до звичайних спектрофотометричних методик (інфрачервоний, ЯМР, мас-спектрометрія). ПРИКЛАД 1: 8-фенокси-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепіну 1,1-діоксид Стадія A: N-[[[2-(хлорсульфоніл)-4-метоксифеніл]аміно]метилен]-N-метил-метанамінію хлорид Диметилформамід (0,152 моль) додають краплями до суспензії 2-аміно-5метоксибензолсульфонової кислоти (0,152 моль) в тіонілхлориді (0,763 моль). Реакційну суміш нагрівають поступово до 70°C і підтримують при цій температурі протягом 1,5 години. Після охолодження, перемішаний реакційний розчин обробляють шляхом додавання 20 мл толуолу. Утворюється осад, який швидко відфільтровують, промивають толуолом і потім висушують при 40°C у вакуумі у присутності гранул KOH, для одержання вказаного у заголовку продукту. Стадія B: N-(2-хлоретил)-2-{[(1E)-(диметиламіно)метилен]аміно}-5метоксибензолсульфонамід Триетиламін (0,517 моль) додають краплями до суспензії суміші продукту зі Стадії, розкритої вище, (0,152 моль) і 2-хлоретиламін гідрохлориду (0,182 моль) у 470 мл дихлорметану, підтримуючи температуру реакційної суміші нижче 30°C. Після перемішування протягом 2 годин, реакційну суміш розбавляють дихлорметаном і органічну фазу промивають двічі водою і потім насиченим розчином NaCl. Органічну фазу висушують над MgSO4 і випаровують під зниженим тиском. Залишок затверджують в етиловому ефірі для одержання, після фільтрування, вказаного у заголовку продукту. Точка плавлення: 89°C Елементний мікроаналіз: C H N S Cl теоретично % 45,07 5,67 13,14 10,03 11,09 експериментально % 44,93 5,63 13,07 10,19 11,82 Стадія C: 2-аміно-N-(2-хлоретил)-5-метоксибензолсульфонамід Весь продукт зі Стадії, розкритої вище, суспендують в суміші 130 мл діоксану і 110 мл 5M HCl. Реакційну суміш перемішують при 110°C протягом 16 годин. Після випаровування діоксану, реакційну суміш розбавляють водою і потім нейтралізують шляхом додавання 10 % розчину NaHCO3. При нейтральному pH, водну фазу екстрагують тричі етилацетатом. Органічні фази збирають, промивають насиченим розчином NaCl і потім висушують над MgSO4 для одержання, після випаровування під зниженим тиском, вказаного у заголовку продукту у формі олії. Стадія D: 8-метокси-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепіну 1,1-діоксид В 1-літровому автоклавному реакторі PAAR зі скляним корпусом весь продукт зі Стадії, розкритої вище, суспендують у 300 мл етанолу. Реакційну суміш нагрівають при 150°C протягом 8 годин. Після того, як охолодження завершене, тверду речовину відфільтровують для одержання вказаного у заголовку продукту. Точка плавлення: 126°C Стадія E: 2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-олу 1,1-діоксид До суспензії продукту зі Стадії, розкритої вище, (12,3 ммоль) у 30 мл дихлорметану додають краплями 1M розчин триброміду бору в дихлорметані (37 мл), підтримуючи температуру реакційної суміші нижче 30°C. Гетерогенну суміш перемішують протягом 20 годин при температурі навколишнього середовища і виливають на приблизно 100 г льоду. Розчин потім нейтралізують шляхом додавання 10 % розчину Na2CO3. Після випаровування водної фази досуха, залишок порошкують в ацетоні Солі фільтрують декілька разів і різні фільтрати (які містять очікуваний продукт, а також вихідний матеріал) збирають. Їх абсорбують на кремнезем для одержання, після хроматографування елююванням з градієнтом дихлорметан/ацетон від 96/4 до 90/10 і затверджують в етиловому ефірі, вказаного у заголовку продукту у формі порошку білого кольору. Точка плавлення: 183-188°C Стадія F: 8-фенокси-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепіну 1,1-діоксид Суспензію фенілборонової кислоти (8,36 ммоль), продукту зі Стадії, розкритої вище, (5,60 6 UA 100477 C2 5 10 15 20 25 30 35 ммоль), Cu(OAc)2 (8,42 ммоль), піридину (16,8 ммоль) і 12 г молекулярного сита у 200 мл дихлорметану перемішують протягом ночі на повітрі при температурі навколишнього середовища. Потім додають ацетон і потім реакційну суміш фільтрують над фритою. Фільтрат випаровують, вміщують у дихлорметан і хроматографують на колонці кремнезему, елююючи сумішшю дихлорметан/ацетон 96/4, дляодержання, після затверджування в етиловому ефірі, вказаного у заголовку продукту у формі порошку білого кольору. Точка плавлення: 146-149°C Елементний мікроаналіз: C H N S теоретично % 57,92 4,56 9,65 11,04 експериментально % 57,90 5,00 9,78 11,08 Продукти Прикладів 2-9, які наведені нижче, одержують відповідно до методики Стадії F Прикладу 1, починаючи з проміжної сполуки 2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-ол 1,1діоксиду (Стадія E Прикладу 1) і відповідної боронової кислоти як зазначено вище. ПРИКЛАД 2: N-{4-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіа-зепін-8іл)окси]бензил}метансульфонамід Реакція з (4-{[(метилсульфоніл)аміно]метил}феніл)бороновою кислотою. Точка плавлення: 115-117°C Елементний мікроаналіз: C H N S теоретично % 48,35 4,82 10,57 16,13 експериментально % 48,60 4,93 10,50 16,20 ПРИКЛАД 3: 8-(4-фторфенокси)-2,3,4,5-тетрагідро-1,2,5-бензотіа-діазепіну 1,1-діоксид Реакція з (4-фторфеніл)бороновою кислотою. Точка плавлення: 153-156°C Елементний мікроаналіз: C H N S теоретично % 54,54 4,25 9,09 10,40 експериментально % 54,14 4,41 9,04 10,08 ПРИКЛАД 4: 8-(3-фторфенокси)-2,3,4,5-тетрагідро-1,2,5-бензотіа-діазепіну 1,1-діоксид Реакція з (3-фторфеніл)бороновою кислотою. Точка плавлення: 128 °C Елементний мікроаналіз: C H N S теоретично % 54,54 4,25 9,09 10,40 експериментально % 54,39 4,17 8,99 9,98 ПРИКЛАД 5: 8-(3,5-дифторфенокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепіну 1,1діоксид Реакція з (3,5-дифторфеніл)бороновою кислотою. Точка плавлення: 90-95°C Елементний мікроаналіз: C H N S теоретично % 51,53 3,71 8,58 9,83 експериментально % 51,44 3,86 8,50 9,65 ПРИКЛАД 6: 3-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіа-зепін-8іл)окси]бензонітрил Реакція з (3-ціанофеніл)бороновою кислотою. Точка плавлення: 172-174°C Елементний мікроаналіз: C H N S теоретично % 57,13 4,15 13,33 10,17 експериментально % 56,41 4,12 13,15 10,61 ПРИКЛАД 7: етил 3-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8іл)окси]бензоат Реакція з [3-(етоксикарбоніл)феніл]бороновою кислотою. Точка плавлення: 110°C Елементний мікроаналіз: C H N S теоретично % 56,34 5,01 7,73 8,85 експериментально % 55,70 4,95 7,76 9,03 7 UA 100477 C2 5 10 15 20 25 30 35 40 45 50 ПРИКЛАД 8: 8-[4-(бензилокси)фенокси]-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепіну 1,1діоксид Реакція з [4-(бензилокси)феніл]бороновою кислотою. Точка плавлення: 134°C ПРИКЛАД 9: 8-(4-нітрофенокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіа-зепіну 1,1-діоксид Реакція з (4-нітрофеніл)бороновою кислотою. Точка плавлення: 162°C ПРИКЛАД 10: 3-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіа-діазепін-8-іл)окси]-N'гідроксибензолкарбоксімідамід До 750 мкл DMSO додають гідроксиламіну гідрохлорид (1,90 ммоль), а потім триетиламін (1,90 ммоль). Утворюється рясний осад білого кольору, його розбавляють шляхом додавання 3 мл THF і перемішування проводять протягом 25 хвилин при температурі навколишнього середовища. THF випаровують під зниженим тиском і суспензію фільтрують. Продукт Прикладу 6 (0,317 ммоль) додають до фільтрату і розчин перемішують протягом ночі при температурі навколишнього середовища. Після додавання води до реакційної суміші, утворюється смола, яку затверджують шляхом додавання дихлорметану і етилового ефіру. Тверду речовину відфільтровують і промивають водою і етиловим ефіром для одержання вказаного у заголовку продукту. Точка плавлення: 197°C Елементний мікроаналіз: C H N S теоретично % 51,71 4,63 16,08 9,20 експериментально % 51,38 4,58 15,61 8,84 ПРИКЛАД 11: 3-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіа-зепін-8-іл)окси]бензойна кислота Суспензію складного ефіру Прикладу 7 (0,55 ммоль) у 5 мл 1N розчину гідроксиду натрію перемішують протягом 30 хвилин при 80°C. Реакційну суміш потім нейтралізують, використовуючи 1N розчин HCl, екстрагують етилацетатом, промивають (насиченим розчином NaCl), висушують (MgSO4), фільтрують і потім випаровують під зниженим тиском для одержання, після порошкування залишку в етиловому ефірі і фільтрування, вказаного у заголовку продукту. Точка плавлення: 212-217°C Елементний мікроаналіз: C H N S теоретично % 53,89 4,22 8,38 9,59 експериментально % 53,41 4,23 8,35 9,82 ПРИКЛАД 12: 3-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіа-діазепін-8-іл)окси]-Nметилбензамід Кислоту Прикладу 11 (0,66 ммоль) перемішують протягом ночі при температурі навколишнього середовища у 50 мл дихлорметану у присутності 2-(1H-бензотриазол-1-іл)1,1,3,3-тетраметилуроній тетрафторборату (0,80 ммоль), діізопропілетиламіну (0,80 ммоль) і 2M розчину метиламіну у THF (1,32 ммоль). Реакційну суміш потім нейтралізують 1N розчином HCl, екстрагують етилацетатом, промивають (насиченим розчином NaCl), висушують (MgSO4), фільтрують і потім випаровують під зниженим тиском для одержання, після порошкування залишку в суміші дихлорметан/метанол і фільтрування, вказаного у заголовку продукту. Точка плавлення: 205 °C Елементний мікроаналіз: C H N S теоретично % 55,32 4,93 12,10 9,23 експериментально % 54,79 4,88 11,88 9,20 ПРИКЛАД 13: {3-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіа-зепін-8іл)окси]феніл}метанол Складний ефір Прикладу 7 (0,805 ммоль) розчиняють у 10 мл THF і додають невеликими порціями LiAlH4 (2,43 ммоль). Після перемішування протягом 30 хвилин, до реакційної суміші послідовно додають 1 мл ізопропанолу і 1 мл розсолу. Суспензію фільтрують і фільтрат, після випаровування під зниженим тиском, хроматографують на колонці кремнезему (98/2 дихлорметан/метанол) для одержання вказаного у заголовку продукту. Точка плавлення: 146°C ПРИКЛАД 14: 4-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіа-діазепін-8-іл)окси]фенол Продукт Прикладу 8 (0,76 ммоль) гідрогенізують протягом 1 години при атмосферному тиску 8 UA 100477 C2 5 10 15 20 25 30 35 40 45 50 у 60 мл етанолу у присутності 30 мг 10 % паладію-на-вуглеці і 2 крапель 4N розчину HCl в діоксані. Каталізатор видаляють шляхом фільтрування і фільтрат випаровують досуха. Залишок вміщують в гарячому стані в етилацетат. Органічну фазу промивають 1 % розчином NaHCO3 і потім насиченим розчином NaCl, висушують (MgSO 4), фільтрують і випаровують. Залишок порошкують в суміші етилацетат/етиловий ефір для одержання, після фільтрування, вказаного у заголовку продукту. Точка плавлення: 175°C Елементний мікроаналіз: C H N S теоретично % 54,89 4,61 9,14 10,47 експериментально % 54,96 4,74 8,89 10,39 ПРИКЛАД 15: 8-[4-(бензилокси)фенокси]-5-метил-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепіну 1,1-діоксид Водний формальдегід 37 % (12,6 ммоль) додають до суспензії продукту Прикладу 8 (2,52 ммоль) в 10 мл ацетонітрилу. Суспензію перемішують протягом 1 години при температурі навколишнього середовища. Послідовно додають на кінчику шпателю бромкрезоловий зелений і ціаноборгідрид натрію (7,56 ммоль). Реакційну суміш доводять до кислотного pH шляхом додавання 4N розчину HCl в діоксані. Реакційну суміш перемішують протягом ночі при температурі навколишнього середовища і потім нейтралізують шляхом додавання 10% розчину NaHCO3. Після розбавлення реакційної суміші водою, утворюється осад, який відфільтровують. Очищення вказаного у заголовку продукту проводять за допомогою хроматографії на кремнеземі, елююючи сумішшю дихлорметан/етилацетат 96/4. Точка плавлення: 168-172°C ПРИКЛАД 16: 4-[(5-метил-1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8іл)окси]фенол Сполуку одержують шляхом каталітичної гідрогенізації продукту Прикладу 15 відповідно до методики Прикладу 14. Очищення проводять за допомогою хроматографії на кремнеземі, елююючи сумішшю дихлорметан/ацетон 95/5. Точка плавлення: 128-130°C Елементний мікроаналіз: C H N S теоретично % 56,24 5,03 8,74 10,01 експериментально % 56,30 5,03 8,67 10,24 ПРИКЛАД 17: 4-[(1,1-Діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіа-діазепін-8-іл)окси]аніліну дигідрохлорид Продукт Прикладу 9 (0,51 ммоль) гідрогенізують протягом 2 годин при атмосферному тиску у 30 мл метанолу у присутності 20 мг 10% паладію-на-вуглеці. Каталізатор видаляють шляхом фільтрування і фільтрат випаровують досуха. Залишок вміщують у гарячому стані в метанол і суміш підкислюють 4N розчином HCl в діоксані. Після випаровування досуха, залишок порошкують в ацетонітрилі для одержання, після фільтрування, вказаного у заголовку продукту. Точка плавлення: 128-134°C Продукти Прикладів 18-21, наведені далі, одержують шляхом відновного амінування сполуки Прикладу 1. ПРИКЛАД 18: 5-(Циклопропілметил)-8-фенокси-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін 1,1діоксиду гідрохлорид До розчину продукту Прикладу 1 (1,38 ммоль) у 50 мл CH 2Cl2 додають циклопропанкарбальдегід (4,17 ммоль), оцтову кислоту (4,17 ммоль) і триацетоксиборгідрид натрію (4,17 ммоль). Реакційну суміш перемішують протягом ночі при температурі навколишнього середовища і потім нейтралізують шляхом додавання 10% розчину NaHCO 3. Після екстрагування дихлорметаном, органічні фази збирають, промивають (насиченим розчином NaCl), висушують (MgSO4) і потім випаровують. Сирий продукт очищують за допомогою хроматографії на кремнеземі (дихлорметан/метанол 98/2) і продукт перетворюють у сіль в етанолі шляхом додавання 4N розчину HCl в діоксані для одержання вказаного у заголовку продукту. Точка плавлення: 62°C (меренга) ПРИКЛАД 19: 5-циклобутил-8-фенокси-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепіну 1,1діоксид Методика є такою ж, як і методика Прикладу 18, але реакційну суміш перемішують при 70°C в дихлоретані, використовуючи циклобутанон замість циклопропанкарбальдегіду. Сирий продукт очищують за допомогою хроматографії на кремнеземі, елююючи сумішшю 9 UA 100477 C2 5 10 15 20 25 30 35 40 45 етилацетат/циклогексан 2/8, для одержання, після випаровування, вказаного у заголовку продукту. Точка плавлення: 55°C (меренга) Елементний мікроаналіз: C H N S теоретично % 62,77 5,85 8,13 9,31 експериментально % 62,81 5,90 7,98 9,34 ПРИКЛАД 20: 5-метил-8-фенокси-2,3,4,5-тетрагідро-1,2,5-бензотіа-діазепіну 1,1-діоксид Методика є такою ж, як і методика Прикладу 18, використовуючи водний формальдегід 37% замість циклопропанкарбальдегіду. Сирий продукт очищують за допомогою хроматографії на кремнеземі, елююючи сумішшю дихлорметан/метанол 98/2, для одержання вказаного у заголовку продукту. Точка плавлення: 128-131°C Елементний мікроаналіз: C H N S теоретично % 59,19 5,30 9,20 10,54 експериментально % 59,35 5,30 9,07 10,52 ПРИКЛАД 21: 5-етил-8-фенокси-2,3,4,5-тетрагідро-1,2,5-бензотіа-діазепіну 1,1-діоксид Методика є такою ж, як і методика Прикладу 18, використовуючи ацетальдегід замість циклопропанкарбальдегіду. Сирий продукт очищують за допомогою хроматографії на кремнеземі, елююючи сумішшю дихлорметан/метанол 98/2, для одержання вказаного у заголовку продукту. Точка плавлення: 138°C Елементний мікроаналіз: C H N S теоретично % 60,36 5,70 8,80 10,07 експериментально % 60,25 5,65 8,70 10,18 ПРИКЛАД 22: 5-циклопропіл-8-фенокси-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепіну 1,1-діоксид Методика є такою ж, як і методика Прикладу 18, але реакційну суміш перемішують при 70°C в дихлоретані, використовуючи [(1-етоксициклопропіл)окси]триметилсилан замість циклопропанкарбальдегіду. Сирий продукт очищують за допомогою хроматографії на кремнеземі, елююючи сумішшю циклогексан/етилацетат 70/30, для одержання вказаного у заголовку продукту. Точка плавлення: 119°C Елементний мікроаналіз: C H N S теоретично % 61,80 5,49 8,48 9,71 експериментально % 61,15 5,53 8,25 9,60 ПРИКЛАД 23: 2,5-диметил-8-фенокси-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепіну 1,1-діоксид Гідрид натрію 60% в мінеральній олії (3,05 ммоль) додають до суспензії продукту Прикладу 1 (1,016 ммоль) у 3 мл диметилформаміду. Після перемішування протягом 10 хвилин, додають краплями 2M розчин метил йодиду в метил трет-бутиловому ефірі (3,05 ммоль). Реакційну суміш перемішують протягом ночі при температурі навколишнього середовища і потім розбавляють водою, екстрагують етилацетатом, промивають (насиченим розчином NaCl), висушують (MgSO4), фільтрують і потім випаровують досуха. Залишок хроматографують на кремнеземі, елююючи сумішшю дихлорметан/ацетон, для одержання вказаного у заголовку продукту. Точка плавлення: 130-131°C Елементний мікроаналіз: C H N S теоретично % 60,36 5,70 8,80 10,07 експериментально % 60,58 5,75 8,64 10,31 ПРИКЛАД 24: 2-(2-фторетил)-8-фенокси-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепіну 1,1діоксид Суспензію продукту Прикладу 1 (2,06 ммоль) у 100 мл ацетонітрилу перемішують протягом 24 годин у присутності карбонату цезію (4,12 ммоль) і 1-бром-2-фторетану (4,12 ммоль). Реакційну суміш потім фільтрують і фільтрат випаровують досуха. Сирий продукт хроматографують на кремнеземі, елююючи сумішшю дихлорметан/метанол 98/2. Продукт перетворюють у сіль в етанолі шляхом додавання 4N розчину HCl в діоксані для одержання вказаного у заголовку продукту у формі гідрохлориду. 10 UA 100477 C2 5 10 15 20 25 30 35 40 45 50 55 60 Точка плавлення: 95-98°C ФАРМАКОЛОГІЧНІ ДОСЛІДЖЕННЯ ПРИКЛАД A: Дослідження впливу сполук на деполяризацію мембрани, викликану АМРА у первинних культурах нейронів щурів Дослідження включає in vitro вимірювання, за допомогою флюоресценції, деполяризації мембрани, викликаної у культурованих щурячих ембріональних нейронах сумісною дією AMPA і досліджуваної сполуки, у порівнянні з дією AMPA самого по собі. Клітини мозку вміщують в культуру і утримують в інкубаторі для клітинних культур протягом 18. Після інкубування, культуральне середовище видаляють і заміщують середовищем з флуоресцентними зондами для вимірювання мембранного потенціалу (20 мкл; набір для вимірювання мембранного потенціалу від Molecular Devices) і залишають при температурі навколишнього середовища на 1 годину. Зчитують базову флуоресценцію ямок (прилад FDSS від Hamamatsu) і в клітини потім ін’єктують AMPA (20 мкл; діапазон концентрації: від 3 до 100 мкM) і дію AMPA вимірюють кінетично. Досліджувану сполуку потім вміщують в ямки (20 мкл; при діапазоні концентрації, що перехрещується з діапазоном концентрації AMPA) і дію сполуки вимірюють кінетично. В кінці кожного з двох періодів кінетичного вимірювання, результат для кожної ямки являє собою середнє зчитування протягом кінцевих 15 секунд періоду вимірювання. На криві нанесені впливи AMPA при різних концентраціях сполуки. Для кожної концентрації сполуки, результат являє собою ділянку під кривою AMPA при цій концентрації, і підраховують EC 2X (концентрація сполуки, яка подвоює мембранний потенціал, викликаний AMPA). Сполуки за даним винаходом суттєво потенціюють збуджувальний вплив AMPA. Як приклад, сполука Прикладу 1 має EC2X зі значенням 25 мкM. ПРИКЛАД B: Тест на розпізнавання об’єктів на миші CD1 Тест на розпізнавання об’єктів (Behav. Brain Res., 1988, 31, 47-59) ґрунтується на мимовільній дослідницькій активності тварини і має характеристики епізодичної пам'яті у людини. Цей тест на запам’ятовування є чутливим до старіння (Eur. J. Pharmacol., 1997, 325, 173-180) і до холінергічних дисфункцій (Pharm. Biochem. Behav., 1996, 53(2), 277-283) і ґрунтується на відмінностях в дослідженні двох об'єктів фактично подібної форми - один добре знайомий, інший - новий. Методика дослідження, яку було адаптовано для миші CD1, включає 3 фази, які відбуваються в одній і тій же огородженій ділянці даного дослідження. Під час першої фази, яка триває 40 хвилин, мишей привчають до оточення. Під час другої фази, яка відбувається наступного дня, в огороджену ділянку вміщують об’єкт, і миша може вільно досліджувати його. Як тільки тривалість вивчання досягає 20 секунд, мишу виймають з огородженої ділянки. В ході третьої фази (5 хвилин), через 24 години, представляють той же об’єкт (який набув статусу "знайомого" об’єкту), а також новий об’єкт. Вимірюють тривалість вивчання, виражену в секундах, для кожного з двох об’єктів. Контрольні тварини, заздалегідь оброблені носієм оральним шляхом за 60 хвилин перед кожною з трьох фаз, досліджують “знайомий” об'єкт і “новий” об'єкт однаковим чином, що вказує на те, що об'єкт, представлений раніше, був забутий. Тварини, оброблені сполукою, яка сприяє процесу запам’ятовування, переважно досліджують новий об'єкт, що вказує на те, що об'єкт, представлений раніше, було запам'ятовано. При дослідження відповідно до методики Прикладу В, сполуки формули (І) відповідно до даного винаходу проявляють себе як такі, що є дуже ефективними у покращенні процесу запам’ятовування. Наприклад, результати, одержані для сполуки Прикладу 1 за даним винаходом, показують, що новий об’єкт досліджується значно більше, ніж знайомий об’єкт, при дозуванні 1 і 3 мг/кг перорально. ПРИКЛАД C: Вплив сполук на струм, індукований NMDA в ооцитах Xenopus laevis, в які + ін’єктовано полі(A ) mRNA з кори головного мозку щура Електрофізіологічні зчитування проводять на ооцитах Xenopus laevis, в які ін’єктовано + полі(A ) mRNA з кори головного мозку щура і які експресують, серед іншого, глутаматні рецептори NMDA-типу з кори головного мозку щура, у плексигласовій реєструючій камері, в яку постійно заливають OR2 розчин, який не містить магнію, (який блокує відкривання каналу рецептора NMDA) і при температурі навколишнього середовища. Вхідний струм, індукований шляхом введення NMDA, реєструють при потенціалі спокою -60 мВ, використовуючи стандартну -4 методику двохелектродного режиму фіксації потенціалу. NMDA (3x10 M) вводять з -5 перфузійним розчином у присутності 3x10 M гліцину протягом 30 секунд кожні 5 хвилин, при постійній швидкості перфузії 3 мл/хв. Амплітуду струму, індукованого NMDA, вимірюють на піку струму. Досліджувані сполуки вводять при підвищених дозах в той же ооцит в перфузійному -4 розчині за 45 секунд, протягом 30 секунд і через 30 секунд після введення 3x10 M NMDA у -5 присутності 3x10 M гліцину кожні 5 хвилин. Амплітуду струму, індукованого NMDA у присутності 11 UA 100477 C2 5 сполуки, нормалізують і виражають як процент струму, індукованого в тому ж ооциті за відсутності продукту, що відповідає 100 % відповіді. Значення IC 50, яке відповідає концентрації продукту, яка інгібує струм, індукований NMDA, на 50 %, визначають за допомогою нелінійної регресії, використовуючи сигмоподібну модель концентрація-відповідь зі змінною крутизною. Сполуки за даним винаходом суттєво інгібують вплив NMDA. Як приклад, сполука Прикладу 1 має значення IC50 на рівні 9 мкM. ПРИКЛАД D: Фармацевтична композиція Формула для одержання 1000 таблеток, кожна з яких містить 10 мг 8-фенокси-2,3,4,5-тетрагідро1,2,5-бензотіадіазепіну 1,1-діоксиду (Приклад 1) 10 г Гідроксипропілцелюлоза 2г Пшеничний крохмаль 10 г Лактоза 100 г Стеатар магнію 3г Тальк 3г ФОРМУЛА ВИНАХОДУ 10 1. Сполука формули (І): R1 R2 O O O S R4 N N R3 15 20 25 30 35 40 45 , (I) в якій: R1 і R2, які можуть бути однаковими або відрізнятись, кожний являє собою атом водню; лінійну або розгалужену (С1-С6)алкільну групу, не заміщену або заміщену одним або більше атомами галогену; лінійну або розгалужену (С1-С6)алкоксигрупу; лінійну або розгалужену (С1С6)алкілтіогрупу; лінійну або розгалужену (С1-С6)алкоксикарбонільну групу; карбоксигрупу; лінійну або розгалужену (С1-С6)ацильну групу; гідроксигрупу; лінійну або розгалужену (С1С6)гідроксіалкільну групу; ціаногрупу, нітрогрупу; аміногрупу, не заміщену або заміщену однією або декількома лінійними або розгалуженими (С 1-С6)алкільними групами; аміногрупу, заміщену лінійною або розгалуженою (С1-С6)ацильною групою; амінокарбонільну групу, не заміщену або заміщену однією або декількома лінійними або розгалуженими (С 1-С6)алкільними групами; аміносульфонільну групу, не заміщену або заміщену однією або декількома лінійними або розгалуженими (С1-С6)алкільними групами; (С1-С6)алкілсульфоніламіно(С1-С6)алкільну групу, в якій алкільні частини є лінійними або розгалуженими; N-гідроксикарбоксімідамідну групу або бензилоксигрупу, R3 являє собою атом водню, лінійну або розгалужену (С 1-С6)алкільну групу, (С3С8)циклоалкільну групу або (С3-С8)циклоалкіл(С1-С6)алкільну групу, в якій алкільна частина є лінійною або розгалуженою, R4 являє собою атом водню або лінійну або розгалужену (С 1-С6)алкільну групу, не заміщену або заміщену одним або більше атомами галогену, її оптичні і позиційні ізомери, а також її адитивні солі з фармацевтично прийнятною кислотою або основою. 2. Сполука формули (І) за п. 1, яка відрізняється тим, що група R1 являє собою атом водню або гідроксигрупу, гідроксиметильну групу, етоксикарбонільну групу, аміногрупу або Nметиламінокарбонільну групу. 3. Сполука формули (І) за п. 1 або п. 2, яка відрізняється тим, що група R1 знаходиться у метаабо пара-положенні. 4. Сполука формули (І) за будь-яким з пп. 1-3, яка відрізняється тим, що групи R2 і R4 являють собою атоми водню. 5. Сполука формули (І) за будь-яким з пп. 1-4, яка відрізняється тим, що група R3 являє собою атом водню або метильну групу. 6. Сполука формули (І) за п. 1, яка вибрана з групи: 8-фенокси-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепіну 1,1-діоксид; етил-3-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-іл)окси]бензоат; 12 UA 100477 C2 5 3-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-іл)окси]-N-метилу бензамід; {3-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-іл)-окси]феніл}метанол; 4-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-іл)окси]фенол; 4-[(5-метил-1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-іл)окси]фенол; 4-[(1,1-діоксидо-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін-8-іл)оксі]анілін, а також її адитивні солі з фармацевтично прийнятною кислотою або основою. 7. Спосіб одержання сполуки формули (І), вказаної у п. 1, який відрізняється тим, що як вихідний матеріал використовують сполуку формули (II): O O S R5 OH NH2 10 , (II) в якій R5 являє собою лінійну або розгалужену (С1-С6)алкоксигрупу, яку піддають реакції з тіонілхлоридом у присутності диметилформаміду для одержання сполуки формули (III): O O S R5 Cl NH N+ Cl 15 , (III) в якій R5 є таким же, як визначено тут вище, яку потім піддають дії 2-хлоретиламіну в основному середовищі для одержання сполуки формули (IV): O O Cl S R5 N H N N 20 , (IV) в якій R5 є таким же, як визначено тут вище, яку, після зняття захисту в кислотному середовищі, потім циклізують для одержання сполуки формули (V): O R5 O S H N N H , (V) в якій R5 є таким же, як визначено тут вище, яку потім піддають дії триброміду бору для одержання сполуки формули (VI): 13 UA 100477 C2 O HO O S H N N H , (VI) яку піддають реакції зі сполукою боронової кислоти формули (VII): OH R1 B OH R2 5 , (VII) в якій R1 і R2 є такими ж, як визначено для формули (І), для одержання сполуки формули (І/а), окремого випадку сполук формули (І): R1 O O N H R2 10 15 H N S O , (I/a) в якій R1 і R2 є такими ж, як визначено тут вище, варіант одержання сполуки формули (І/а), який включає застосування - після проведення етапу зв'язування зі сполукою формули (VI) - звичайних хімічних реакцій, щоб згодом модифікувати замісники сполуки боронової кислоти, сполуку формули (І/а) можуть потім, якщо бажано, піддавати: або подвійному алкілуванню на атомах азоту у положеннях 2 і 5 шляхом дії сильної основи у присутності алкілуючого агента R'-X, де R' являє собою лінійну або розгалужену (С1-С6)алкільну групу і X являє собою атом галогену, для одержання сполуки формули (І/b), окремого випадку сполук формули (І): R1 O O R' S O N 1 2 5 4 3 N R2 R' 20 , (I/b) в якій R1, R2 і R' є такими ж, як визначено тут вище, або алкілуванню на атомі азоту у положенні 2 шляхом дії основи у присутності алкілуючого агента R'4-X, в якому R'4 являє собою лінійну або розгалужену (С1-С6)алкільну групу, не заміщену або заміщену одним або більше атомами галогену, і X являє собою атом галогену, для одержання сполуки формули (І/с), окремого випадку сполук формули (І): O R1 O O S R' 4 N 1 2 5 4 3 R2 25 N H , (I/c) в якій R1, R2 і R'4 є такими ж, як визначено тут вище, яку можуть необов'язково піддавати алкілуванню на атомі азоту у положенні 5 шляхом дії основи у присутності алкілуючого агента R'3-X, в якому R'3 являє собою лінійну або розгалужену (С1-С6)алкільну групу, (С3-С8)циклоалкільну групу або (С3-С8)циклоалкіл(С1-С6)алкільну групу, в якій алкільна частина є лінійною або розгалуженою, а X являє собою атом галогену, для одержання сполуки формули (І/d): 14 UA 100477 C2 O R1 O O R' 4 S N 1 2 5 4 3 N R2 R' 3 5 10 , (I/d) в якій R1, R2, R'3 і R'4 є такими ж, як визначено тут вище, або альтернативно алкілуванню на атомі азоту у положенні 5 за допомогою відновного амінування, використовуючи відновлювальний агент, такий як триацетоксиборгідрид або ціаноборгідрид натрію у присутності: або [(1-етоксициклопропіл)окси]триметилсилану, або сполуки формули (VIII): R"3-CHO, (VIII) в якій R"3 являє собою атом водню або лінійну або розгалужену (С 1-С5)алкільну групу, (С3С8)циклоалкільну групу або (С3-С8)циклоалкіл(С1-С5)групу, в якій алкільна частина є лінійною або розгалуженою, або альтернативно сполуки формули (IX): O n 15 , (IX) в якій 0 n 4, для одержання сполуки формули (І/е), окремого випадку сполук формули (І): R1 O O O H N S 1 2 3 4 5 N R2 R''' 3 20 , (I/e) в якій R'"3 являє собою лінійну або розгалужену (С1-С6)алкільну групу, (С3-С8)циклоалкільну групу або (С3-С8)циклоалкіл(С1-С6)групу, в якій алкільна частина є лінійною або розгалуженою, і R1 і R2 є такими ж, як визначено тут вище, яку можуть необов'язково піддавати алкілуванню на атомі азоту у положенні 2 шляхом дії основи у присутності алкілуючого агента R"4-X, в якому R"4 являє собою лінійну або розгалужену (С1-С6)алкільну групу, яка є не заміщеною або заміщеною одним або декількома атомами галогену, і X являє собою атом галогену, для одержання сполуки формули (І/f): R1 O O O R'' 4 S 1 N 2 3 5 R2 25 30 4 N R''' 3 , (I/f) в якій R1, R2, R'"3 і R"4 є такими ж, як визначено тут вище, сполуки формул (І/а)-(І/f), які складають сукупність сполук формули (І), можуть потім бути очищені відповідно до звичайної методики розділення, перетворені, якщо бажано, в їх адитивні солі з фармацевтично прийнятною кислотою або основою і розділені, коли прийнятно, на їх оптичні і позиційні ізомери, якщо вони існують, відповідно до звичайної методики розділення. 8. Сполука формули (VI), вказана у п. 7: 15 UA 100477 C2 O HO O S N H 5 10 15 H N , (VI) яка відрізняється тим, що вона призначена для використання як проміжної сполуки в синтезі сполук формули (І). 9. Фармацевтична композиція, яка містить як активний інгредієнт сполуку, вказану у будь-якому з пп. 1-6, у поєднанні з одним або більше фармацевтично прийнятними, нетоксичними, інертними носіями. 10. Фармацевтична композиція за п. 9 для застосування у виробництві лікарських засобів для використання як модуляторів рецептора АМРА і антагоністів рецептора NMDA. 11. Фармацевтична композиція за п. 9 для застосування у виробництві лікарських засобів для використання у лікуванні або попередженні прогресуючих нейродегенеративних захворювань, хвороби Альцгеймера, хвороби Паркінсона, атрофії Піка, хореї Хангтінгтона, корсаківського психозу, шизофренії, гострих нейродегенеративних захворювань, деменції лобової частки і підкоркової деменції, судинної деменції, епілепсії, інсультів, а також депресивних і тривожних станів. Комп’ютерна верстка А. Крулевський Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 16
ДивитисяДодаткова інформація
Назва патенту англійськоюBenzothiadiazepine compounds, process for the preparation thereof and pharmaceutical compositions comprising thereof
Автори англійськоюCordi, Alexis, Desos, Patrice, Lestage, Pierre, Danober, Laurence
Назва патенту російськоюСоединения бензотиадиазепина, способ их получения и фармацевтические композиции, которые их содержат
Автори російськоюКорди Алексис, Десос Патрис, Лестаж Пьер, Данобер Лоранс
МПК / Мітки
МПК: C07D 285/36, A61P 25/00, A61K 31/554
Мітки: спосіб, сполуки, одержання, містять, фармацевтичні, бензотіадіазепіну, композиції
Код посилання
<a href="https://ua.patents.su/18-100477-spoluki-benzotiadiazepinu-sposib-kh-oderzhannya-i-farmacevtichni-kompozici-yaki-kh-mistyat.html" target="_blank" rel="follow" title="База патентів України">Сполуки бензотіадіазепіну, спосіб їх одержання і фармацевтичні композиції, які їх містять</a>
Попередній патент: Кристалічна форма vi агомелатину, спосіб її одержання і застосування
Наступний патент: Перетворювач частоти для двигуна змінного струму
Випадковий патент: Спосіб охорони підготовчих виробок