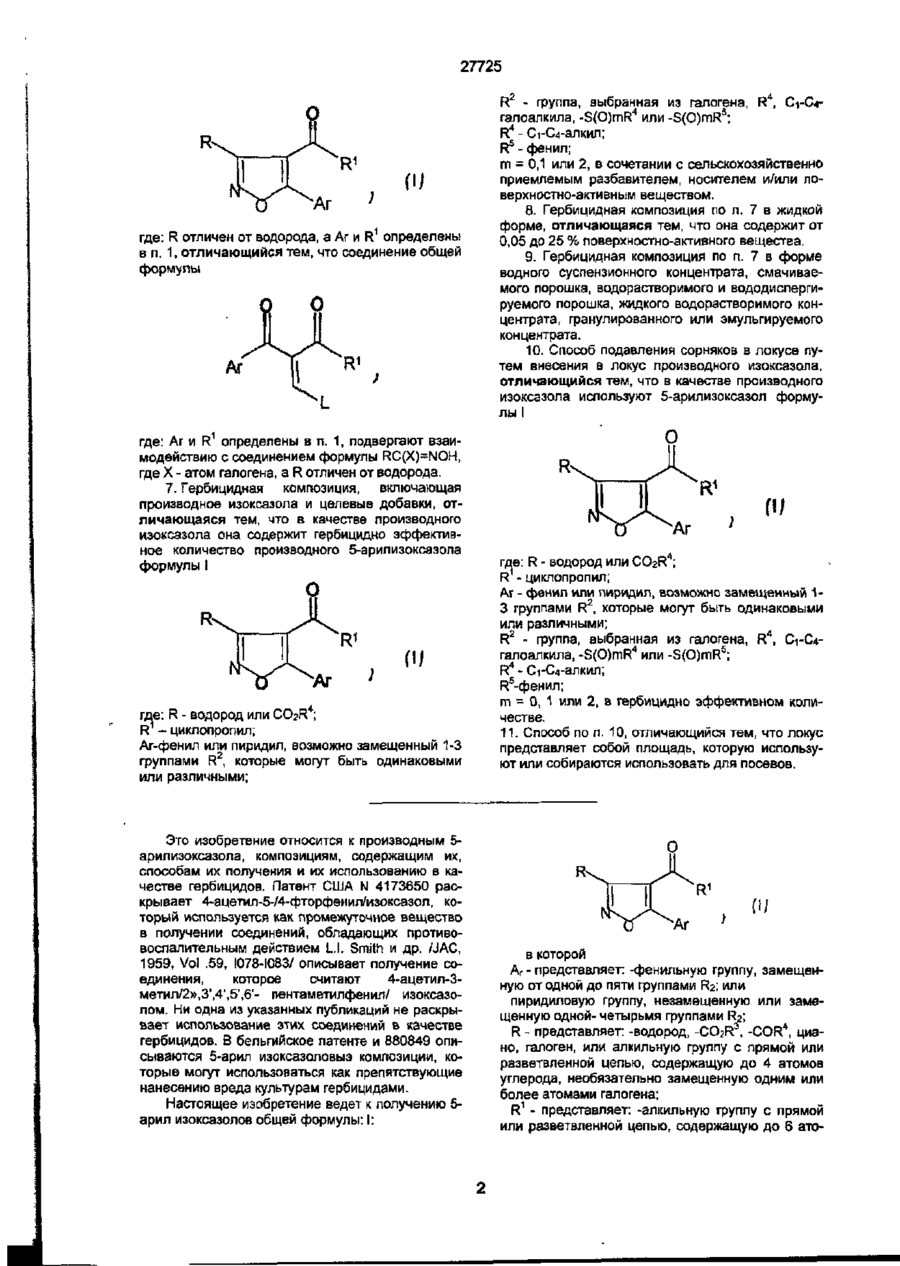
Похідні 5-арилізоксазолу, спосіб їх одержання (варіанти) і гербіцидна композиція на їх основі та спосіб пригнічення бур’янів в локусі
Номер патенту: 27725
Опубліковано: 16.10.2000
Автори: Ламберт Клод, КЕЙН Пол Альфред, Кремп Сьюзан Мері
Текст
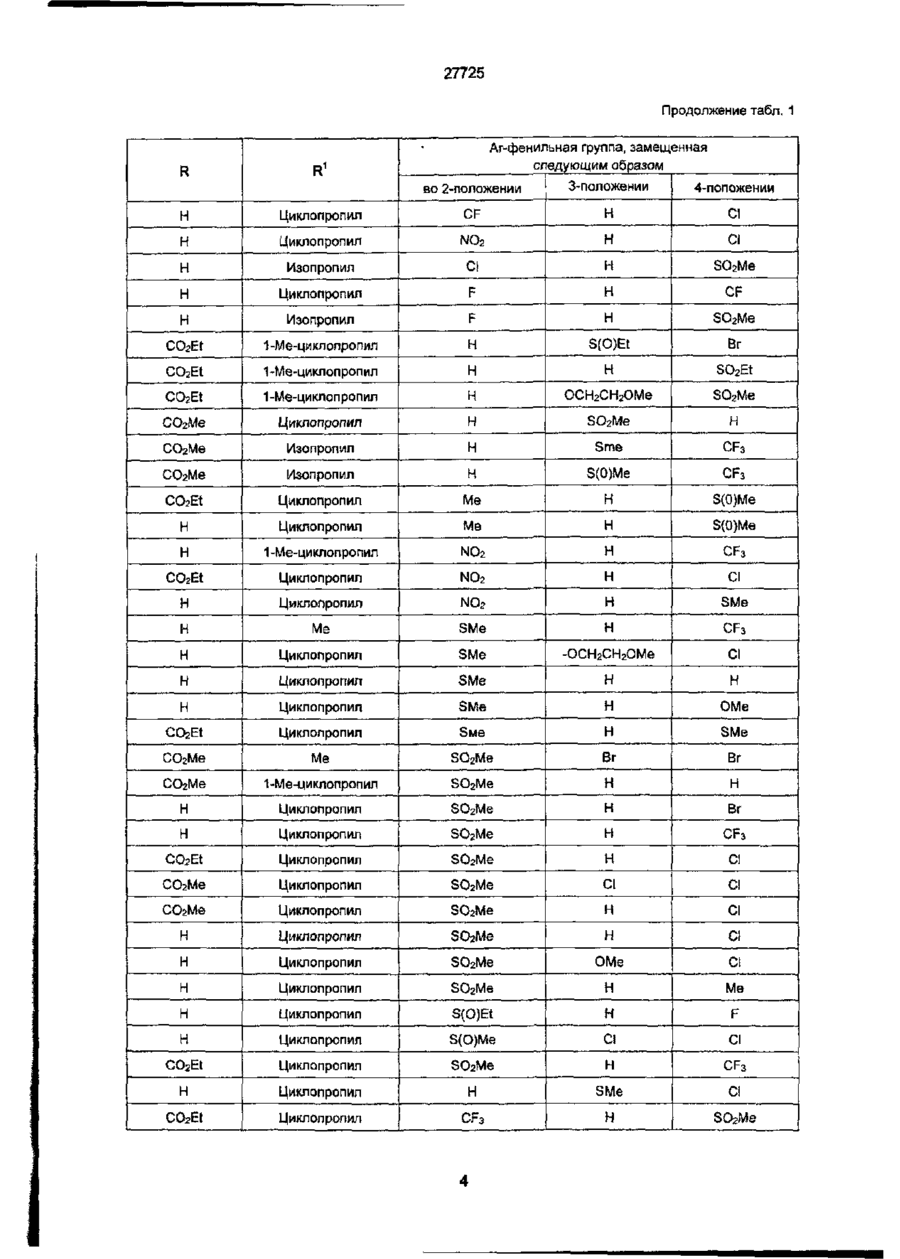
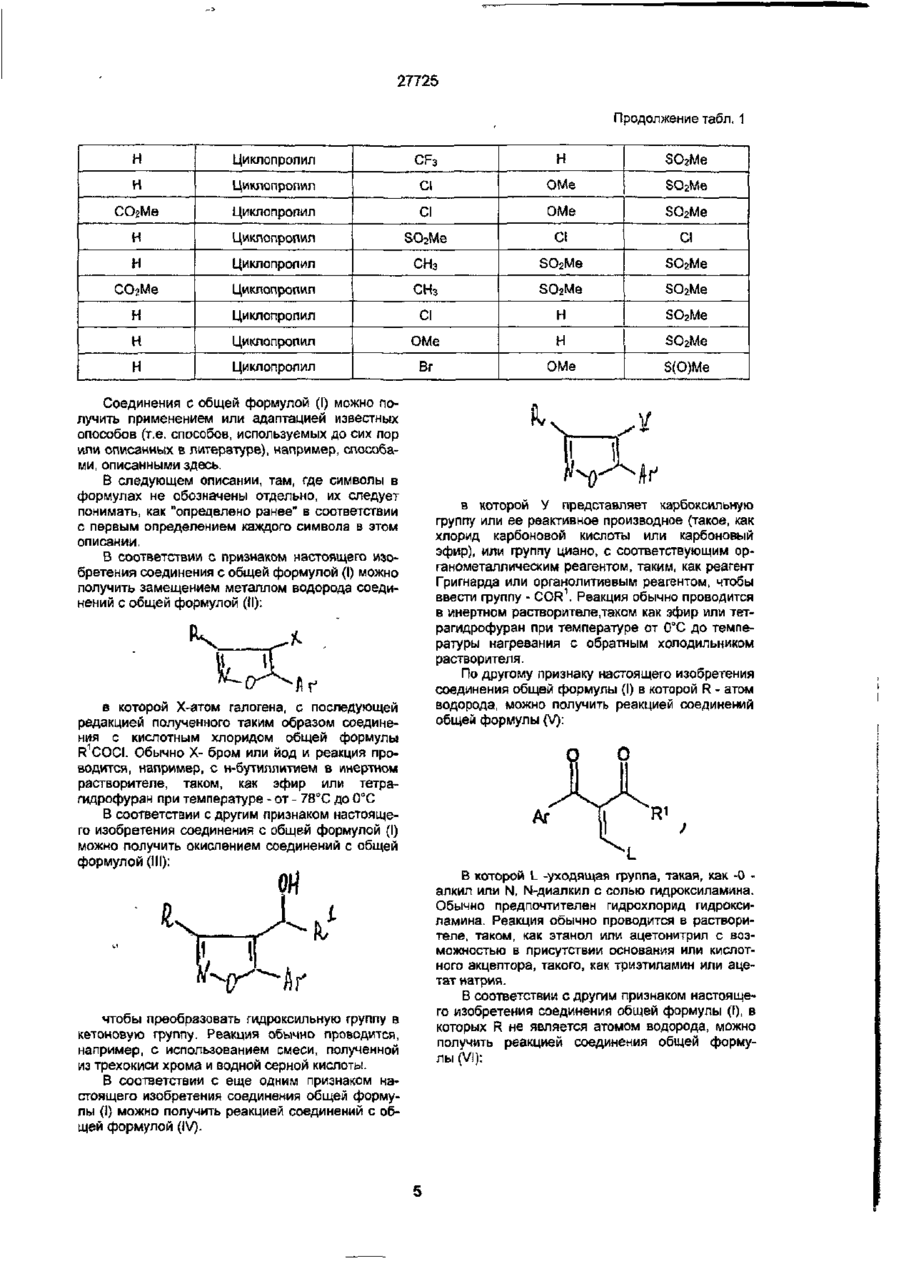
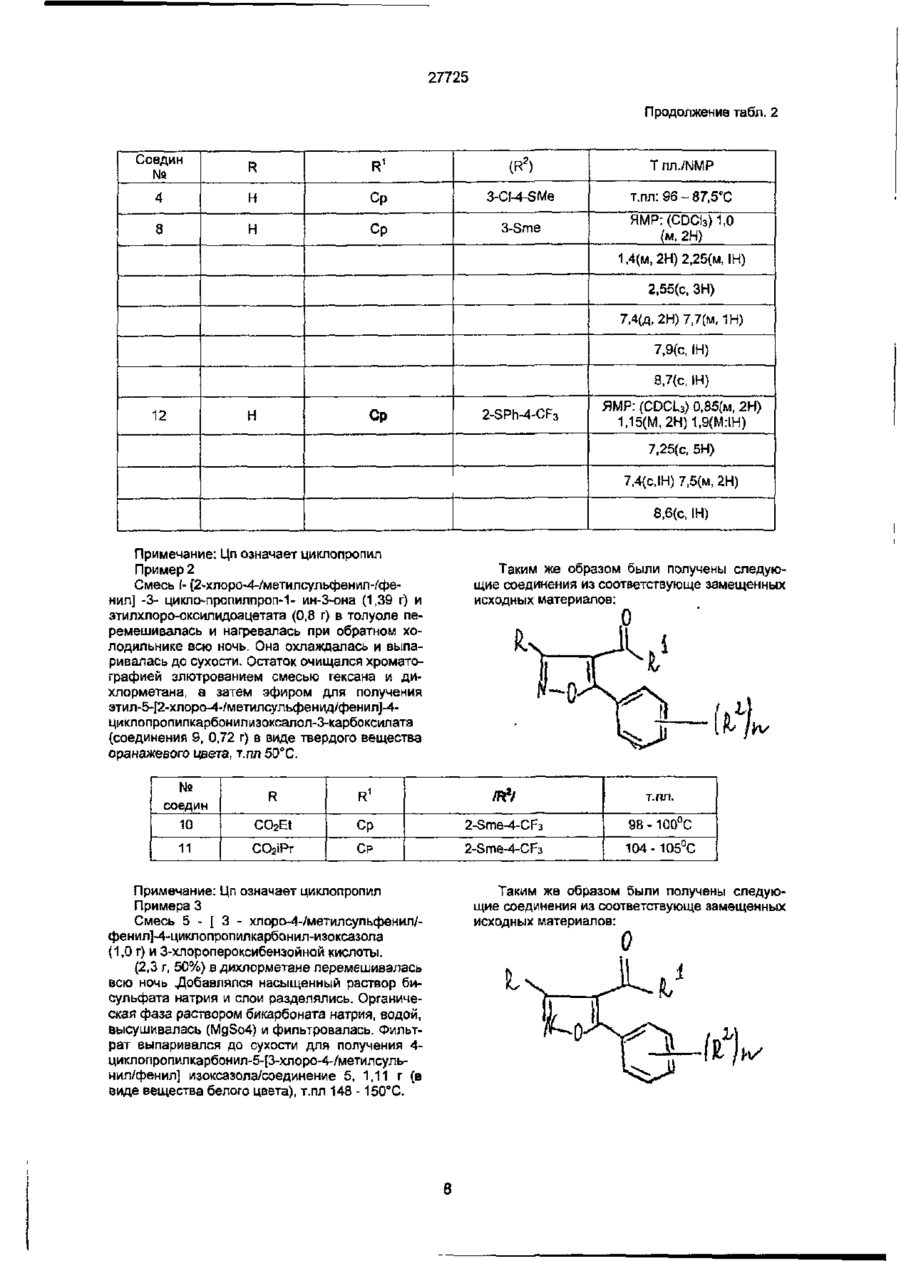
1. Производные 5-арилизоксазола формулы I где R - водород или CO2R ; R - циклопропил; Аг - фенил или пиридил, возможно замещенный 1-3 группами R2, которые могут быть одинаковы или различны; 2 4 R - группа, выбранная из галогена, R , С1-С4A 5 галоалкила, -S(O)m R или -S(O)m R ; R 4 - Сі-С4-апкил; R 5 -фенил, m = 0,1 или 2 2 Соединение по п. 1, где Аг-фенил, замещенный одной или двумя группами, выбранными из галогена, FT, -S(O)mR4 или -S(O)m R5 или Агпиридил, замещенный группой -S(O)m R4. 3 Соединение по одному любому из пп 1-2, представляющее собой. 4-ци клопропил карбон ил-5-(2 -фторо-4метилсул ьфонил фен ил )изоксазол; 4-ци клопропил карбон ил-5- (3,4дихлорфенил)изоксазол, 4-ци клопропил карбон и л-5-[4-(мети л сул ьфен ил )фенил]изо ксззол, 4-ци клопропил карбон и л-5-[3-хл о ро-4(метилсульфенил)фенил]изоксазол, 4-ци клопропил карбон ил-5-[3-хл о ро-4(метилсульфонил)фенил]изоксазол, 4-ци клопропил карбон и л-5-[4-(ыетилсул ьфонил > фенил]изоксазол, 4- циклопропил карбон и л-5-[4-(метил сул ьфен ил )фенил]изоксазол; 4-ци клопропил карбон ил-5-[3-(метил сул ьфен ил }фенил]изоксазол, этил-5-[2-хлоро-4-(метилсульфенил)фенил]-4ци-кло пропилка рбон и л изоксазол-3- карбокси лат; этил-4-циклопропил карбон лл-5-[2-{метил сул faфен ил }-4-трифторметил фени л]изоксазол-3-карбоксилат, 1-метилэтил-4-циклопропилкарбонил-5-[-2(метил-сульфенил)-4-трифторметилфенил]-изоксазол-3-карбоксилат; 4-циклоп ропи л карбон ил-5-[2- (фен илсул ьфен ил)4-трифторметилфенил]изоксазол; или 4-циклопропилкэрбонил-5-[5-(метилсульфенил)п и рид-2-ил]изоксазол. 4. Способ получения производных 5-арилизоксазола формулы I, где R - группа -SOR4 или SO2R4, отличающийся тем, что осуществляют окисление соответствующего соединения формулы I, где R2 - группа -SR . 5. Способ получения производных 5-арилизоксазола формулы I R R1 Аг где: R - водород, а Аг и R' определены в п 1, отличающийся тем, что соединение общей формулы где' L- - уходящая группа, а Аг и R1 определены в п. 1, подвергают взаимодействию с солью гидроксиламина 6. Способ получения производных 5-арилизоксазола формулы I О4 О Ю СМ h CM 27725 R R1 Аг ("і где: R отличен от водорода, а Аг и R1 определены s п. 1, отличающийся тем, что соединение общей формулы где: Аг и R1 определены в п. 1, подвергают взаимодействию с соединением формулы RC(X)=NOH, где X - атом галогена, a R отличен от водорода. 7. Гербицидная композиция, включающая производное изоксазола и целевые добавки, отличающаяся тем, что в качестве производного изоксазола она содержит гербицидно эффективное количество производного 5-а рил изоксазола формулы I R X. Аг где: R - водород или CO2R4; R - циклопропил; Ar-фенил или пиридил, возможно замещенный 1-3 группами R2, которые могут быть одинаковыми или различными; Это изобретение относится к производным 5арилизоксазола, композициям, содержащим их, способам их получения и их использованию в качестве гербицидов. Патент США N 4173650 раскрывает 4-ацетил-5-/4-фторфенил/изоксазол, который используется как промежуточное вещество в получении соединений, обладающих противовоспалительным действием L.I. Smith и др. /JAC, 1959, Vol .59, I078-I083/ описывает получение соединения, которое считают 4-ацетил-Зметил/2»,3',4',5',6'- пентаметилфенил/ изоксазолом. Ни одна из указанных публикаций не раскрывает использование этих соединений в качестве гербицидов. В бельгийское патенте и 880849 описываются 5-арил изоксазоловыэ композиции, которые могут использоваться как препятствующие нанесению вреда культурам гербицидами. Настоящее изобретение ведет к получению 5арил изоксазолов общей формулы:!: R2 - группа, выбранная из галогена, R4, Сі-Сдгалоалкила, -S(O)mR4 или -S(O)mR5; R4 - Сі-С4-алкил; R5 - фенил; m = 6,1 или 2, в сочетании с сельскохозяйственно приемлемым разбавителем, носителем и/или поверхностно-активным веществом. 8. Гербицидная композиция по п. 7 в жидкой форме, отличающаяся тем, что она содержит от 0,05 до 25 % поверхностно-активного вещества. 9. Гербицидная композиция по п. 7 в форме водного суспензионного концентрата, смачиваемого порошка, водорастворимого и вододиспергируемого порошка, жидкого водорастворимого концентрата, гранулированного или эмульгируемого концентрата. 10. Способ подавления сорняков в локусе путем внесения в локус производного изоксазола, отличающийся тем, что в качестве производного изоксазола используют 5-арилизоксазол формулы I Аг где: R - водород или CO2R ; R - циклопропил; Аг - фенил или пиридил, возможно замещенный 13 группами R2, которые могут быть одинаковыми или различными; R2 - группа, выбранная из галогена, R4, СгСдгалоалшла, -S(O)mR4 или -S(O)mR5; R4 - Сі-С4-алкил; R5-фeнил; m = 0, 1 или 2, в гербицидно эффективном количестве. 11. Способ по п. 10, отличающийся тем, что локус представляет собой площадь, которую используют или собираются использовать для посевов. П / в которой Аг - представляет: -фенильную группу, замещенную от одной до пяти группами R2; или пиридиловую группу, незамещенную или замещенную одной- четырьмя группами R^; R - представляет: -водород, -CO2R3, -COR4, циано, галоген, или алкильную группу с прямой или разветвленной цепью, содержащую до 4 атомов углерода, необязательно замещенную одним или более атомами галогена; R1 - представляет: -алкильную группу с прямой или разветвленной цепью, содержащую до 6 ато 27725 a) R представляет: -группу выбранную из водорода CO2R3 или - COR4; и/или в) Аг представляет фенильную группу, замещенную одной-тремя группами R2. Еще одним предпочтительным классом соединений с общей формулой (1) являются те, в которых. Аг представляет: -фенильную группу, замещенную одной или двумя группами R2 и, или пиридиловую группу, замещенную группой S/0/mR4; R - представляет водород или - CO2R3; R1 - представляет циклопропил; R2 представляет группу выбранную из галогена, R4, -S/0/mR4 и -S/0/mR5. Наиболее важные соединения включают следующие І.4-циклопрогмлкарбонил5-/2-фторо-4-метилсульфо нил фени л/изоксазол; 2. 4-циклопропилкарбонил-5-/3,4-дихлорфенид-/ -изоксазол; 3.4-циклопропилкарбонил-5[4-/метилсульфенил/фенил] изоксазол; 4.4-циклопропипкарбонілп-5-[3-хлоро-4-/метилсульфенил/фенил] изоксазол, 5.4-циклопропипкарбонип-5[3-хпоро-4-/метипсульфонил/фенид] изоксазол; 6.4-циклопропипкарбокил-5-[4-/метипсупьфанил/фенил] изоксазол, 7,4-циклопропилкарбонил-5-[4-/метилсульфонил/фенил] изоксазол; 8. 4-ци клоп роп ил карбон ил-5-[3-/метил сул ьфенил/фенил] изоксазол; 9. этил 5-[2-хлоро-4-/метилсульфенил/фенил1-4циклопропил-карбоиилизоксазол-3-карбоксилат; 10. этил 4-циклопропилкар6онил-5-[2-/метилосульфенил/-4-три-фторметилфенил] изоксазол-3карбоксилат; 11. I- метил этил-4-ци клоп роп ил карбонил-5-[2/метилсульфенид/-4-трифтордетилфенил] изоксазол-3- карбоксидат; 12. 4-циклопропилкарбонил-5-[2-/фенилсуль-феНИЛ/-4- трифторметилфенил] изоксазол ;и 13. 4- циклопропилкарбонил-5-[5-/метилсульфенил/пирид-2-ил] изоксазол. Номера 1-13 присвоены указанным соединениям для идентификации и ссылок. Описанными в последующем способами можно также получить следующие соединения с общей формулой (1), которые также представляют интерес: мов углерода, которые могут замещаться одним или более атомами галогена или циклоалкильной группой, содержащей от 3 до 6 атомов углерода, или циклоалкильную группу, содержащую от 3 до 6 атомов углерода, необязательно замещенную одной или более группами R4 или одним или более атомами галогена; R2 представляет -атом галогена, R4, нитро-. CO 2 R 3 , -OR4, -S/O/mR4, - ЭЮ/тР^О-ЮНг/р -OR4 или алкильную группу с прямой или разветвленной цепью, содержащую до 6 атомов углерода, замещенную -OR4, R3 и R , которые могут быть одинаковыми или разными, каждый представляет : -алкильную группу с прямой или разветвленной цепью, содержащую до 6 атомов углерода, необязательно замещенную одним или несколькими атомами галогена; R5 представляет фенильную группу необязательно замещенную одной-пятью группами, выбранными из галогена, нитро, R4 и -OR4, представляет целое число от 1 до 3 , и р представляет 0,1 или 2, m при условии, что: а) если R представляет водород и R1 представляет метил, Аг не является 4-фторфенилом; и а) если R и R1 оба представляют метил, Аг не является 2,3,4,5,6-пентаметилфенилом, которое обладает ценными гербицидными свойствами. В некоторых случаях заместители R, R1, R2, R3 и R4, улучшают оптическую изомерию и/или стереомерию. Все такие формы охвачены настоящим изобретением. Соединения, в которых R представляет водород, R1 представляет метил и Аг представляет 4фгорфенил, и в которых R, и R1 представляют метил и Аг представляет 2,3,4,5,6- пентаметилфенил, не считаются как таковые, частью изобретения, но композиции, содержащие их, и их использование в качестве гербицидов, считаются частью изобретения. Предпочтительным классом соединений формулы (I), благодаря их гербицидным свойствам, являются те, в которых: Аг представляет: фенильную группу, замещенную одной-пятью группами R2; и R2 представляет, -атом галогена R4,HHTPO.CO2R3, -OR4, -S/O/mR4, -0-/CH2/p-0R4 ИЛИ алкильную группу с прямой или разветвленной цепью, содержащую до 6 атомов углерода, которые замещаются - OR4. Другим предпочтительным классом соединений формулы (і), благодаря их гербицидным свойствам являются те, в которых' Таблица 1 Ar-фенильная группа, замещенная следующим образом R1 R во 2-положении 3-положении 4-положении Н Циклопропил Вг н S(0)Me CO2Et Циклопропил CF 3 Н S(O)Et Me CF3 Н SO2Me Н 27725 Продолжение табл. 1 R Ar-фенильная группа, замещенная следующим образом 1 R во 2-положении 3-положении 4-положении Н Циклопропил CF H Cl н н Циклопропил NO2 H Cl Изопропил СІ H SO2Me н Циклопропил F H CF н Изопропил F H SO2Me седа 1 -Ме-циклопропил н S(O)Et Br CO2Et 1 -Ме-циклопропил н H SO2Et CO2Et 1-Ме-циклопропил OCH2CH2OMe SO2Me СО2Ме Циклопропил SO2Me H СО2Ме Изопропил Sme CF3 СО2Ме Изопропил н н н н S(0)Me CF3 ССШ Циклопропил Me H S(0)Me н н Циклопропил Me H S(0)Me 1 -Ме-циклопропил NO2 H CF3 CO2Et Циклопропил NO2 H Cl н н н н н Циклолролил NO? H SMe Me SMe H CF3 Циклопропил SMe -OCH2CH2OMe Cl Циклопропил SMe H H Циклопропил SMe H OMe CO2Et Циклопропил SMe H SMe СО2Ме Me SO2Me Br Br СО2Ме 1-Ме-циклопропил SO2Me H H Н Циклопропил SO2Me H Br Н Циклопропил SO2Me H CF3 CO2Et Циклопропил SO2Me H Cl СОгМе Циклопропил SO2Me Cl Cl СО2Ме Циклопропил SO2Me H Cl Н Циклопропил SO2Me H C! Н Циклопропил SO2Me OMe Cl н н н Циклопропил SO2Me H Me Циклопропил S(O)Et H F Циклопропил S(O)Me Cl Cl CO2Et Циклопропил SO2Me H CF3 н Циклопропил H SMe Cl ссш Циклопропил CF3 H SO2Me 27725 Продолжение табл, 1 н н Циклопропил CF3 Н SO2Me Циклопропил CI ОМе SO2Me СО2Ме Циклопропил CI ОМе SO2Me н Циклопропил SO2Me CI СІ и Циклопропил СНз SO2Me SO2Me СО2Ме Циклопропип СНз SO2Me SO2Me н н Циклопропил CI Н SO2Me Циклопропил ОМе н SO2Me н Циклопропил Вг ОМе S(O)Me Соединения с общей формулой (I) можно получить применением или адаптацией известных опособов (т.е. способов, используемых до сих пор или описанных в литературе), например, способами, описанными здесь. В следующем описании, там, где символы в формулах не обозначены отдельно, их следует понимать, как "определено ранее" в соответствии с первым определением каждого символа в этом описании, В соответствии с признаком настоящего изобретения соединения с общей формулой (I) можно получить замещением металлом водорода соединений с общей формулой (II): I в которой Х-атом галогена, с последующей редакцией полученного таким образом соединения с кислотным хлоридом общей формулы R1COCI. Обычно Х- бром или йод и реакция проводится, например, с н-бутиллитием в инертном растворителе, таком, как эфир или тетрагидрофуран при температуре - от - 78°С до 0°С В соответствии с другим признаком настоящего изобретения соединения с общей формулой (I) можно получить окислением соединений с общей чтобы преобразовать гидроксильную группу в кетоновую группу. Реакция обычно проводится, например, с использованием смеси, полученной из трехокиси хрома и водной серной кислоты. В соответствии с еще одним признаком настоящего изобретения соединения общей формулы (I) можно получить реакцией соединений с общей формулой (IV). в которой У представляет карбоксильную группу или ее реактивное производное (такое, как хлорид карбоновой кислоты или карбоновый эфир), или группу циано, с соответствующим органометаллическим реагентом, таким, как реагент Григнарда или органолитиевым реагентом, чтобы ввести группу - COR1. Реакция обычно проводится в инертном растворителе .таком как эфир или тетрагидрофуран при температуре от 0°С до температуры нагревания с обратным холодильником растворителя. По другому признаку настоящего изобретения соединения общей формулы (I) в которой R - атом водорода, можно получить реакцией соединений общей формулы (V): В которой L -уходящая группа, такая, как -0 алкил или N, N-диалкил с солью гидроксиламина. Обычно предпочтителен гидрохлорид гидроксиламина. Реакция обычно проводится в растворителе, таком, как этанол или ацетонитрил с возможностью в присутствии основания или кислотного акцептора, такого, как триэтиламин или ацетат натрия. В соответствии с другим признаком настоящего изобретения соединения общей формулы (I), в которых R не является атомом водорода, можно получить реакцией соединения общей формулы (VI): 27725 (L 7 где R-уходящая группа, такая, как N, N- диалкил или S-алкил, с соединением общей формулы RC7X/ = N-OH, где X - как определено выше и R не водород. Обычно Х-хлор или бром Реакция обычно проводится в инертном растворителе, таком, как толуол или дихлорметан, либо в присутствии основания, такого, как триэтиламин, либо катализатора, такого, как 4А молекулярное сито или ион фторида. По другому признаку настоящего изобретения соединения общей формулы (І), в которой R- не водород, можно получить реакцией соединений общей формулы (VII): о II Аг — С = С ~ CR1 -(VH) с соединением общей формулы RC/X/ = N-OH, где X - как определено ранее и R - не водород. Обычно Х-хлор или бром. Реация обычно проводится в инертном растворителе, таком, как толуол или дихлор-метан. Возможно в присутствии основания, такого, как триэтиламин или катализатора, такого, как 4А молекулярное сито или ионфторида. В соответствии с еще одним признаком настоящего изобретения соединения общей формулы (I), в которой R - не водород, можно получить реакцией соли соединений общей формулы (VIII): О О с соединением общей формулы RC/X/ = NOH, где Х- как определено выше и R - не водород. Обычно Х-хлор или бром. Предпочтительные соли включают соли натрия и магния. Промежуточные соединения, используемые в получении соединений общей формулы (I), можно получить применением или адаптацией известных способов, например, способов, описанных ранее. Соединения общей формулы (II!) можно получить замещенном металлом водорода в соединениях общей формулы (II), например, нбутиллитием в инертном растворителе, таком, как эфир или тетра-гидрофуран при температуре от 78°С до 0°С с последующей реакцией с альдегидом общей формулы R1CHO. Соединения общей формулы (Y), в которой R атом водорода, и У-СОг-алкил или -CN, можно получить реакцией соединений общей формулы (IX): такой, как гидрохлорид гидроксиламина в растворителе, таком как этанол или ацетонитрил, возможно в присутствии основания или кислотного акцептора, такого, как триэтиламин или ацетат натрия. Соединения общей формулы (IV), в которых У представляет карболовую кислоту или хлорид карбоновой кислоты, можно получить из соответствующего соединения общей формулы (IV), в которой У представляет группу карбонового эфира, гидролизом указанной эфирной группы и преобразованием полученной таким образом кислоты в кислотный хлорид, например, нагреванием с тионилхлоридом. Соединения общей формулы (IX) можно подучить реакцией кето-эфира или кетонитрила общей формулы (X): о где У - как определено ранее, либо с триалкил ортоформа том (например, триэтилорформатом) в присутствии уксусного ангидрида при температуре нагревания с обратным холодильником смеси, либо с диалкилформамиддиалкилацеталем (например диметипформамиддиметилацеталем) в инертном растворителе, таком, как толуол при температуре от комнатной до темературы нагревания с обратным холодильником смеси. Соединения общей формулы (IV), в которой R - не водород, можно получить реакцией соединений общей формулы (X) с соединением общей формулы RC/X/ - N-OH, где X - как определено ранее и R - не водород. Обычно X - хлор или бром. Соединения общей формулы (V) можно получить реакцией соединений общей формулы (Vili) либо с триал кил ортофортл атом (например, триэтилортоформатом) в присутствии уксусного ангидрида при температуре нагревания с обратным холодилником смеси, либо с диальформамиддиалкилацеталем (например, диметилсрома миддиметилацетапем) в инертном растворителе, таком, как толуол при температуре от комнатной до температуры нагревания с обратным холодильником смеси. Соединения общей формулы (VI) можно получить реакцией соединения общей формулы (Xi): где R- как определено ранее, с кислотным хлоридом общей формулы R1COCI в инертном растворителе, таком, как дихлорметан или толуол в присутствии основания, такого, как триэтиламин. Соединения общей формулы (VII) можно получить металлированием соответствующего ацетилена общей формулы (XII): Аг-С 1 где У - представляет -С02-алкил или -CN; и L как определено ранее, с солью гидроксиламина, = С-Х1 /Ш/ где X представляет водород или галоген (например, бром) с использованием, например, нбутиллития в инертном растворителе, таком, как 27725 эфир или тетрагидрофуран при температуре от 78 С до 0°С с последующей обработкой хлоридом кислоты общей формулы R1COCL. Соединения общей формулы (II) можно получить галогенированием соединений общей формулы (XIII): например нагреванием с бромом или йодом в присутствии концентрированной азотной кислоты. Соединения общей формулы (XIII) можно получить реакцией соединений общей формулы (XIV): с солью гидроксиламина, такой, как гидроксиламин гидрохлорид в растворителе, таком, как этанол или ацетонитрил необязательно в присутствии основания или кислотного акцептора, такого, как к триэтиламин или ацетат натрия Соединения общей формулы (VIII), (IX), (X), (XI), (XII) и (XIV) можно получить применением или адаптацией известных способов. Специалистам данной области известно, что некоторые соединения общей формулы (I) можно получить взаимным преобразованием других соеднений общей формулы (I) и такие взаимные преобразования составляют другие признаки настоящего изобретения. Примеры таких взаимных преобразований описываются ниже. Соединения, в которых R представляет циано группу, можно получить из соединений, в которых R представляет эфирную группу - CO2R3, где R3 как определено выше, через гидролиз в соответствующую карбоновую кислоту, преобразованием в соответствующий кислотный хлорид реакцией, например, с тионилхлоридом, обработкой аммиаком чтобы получить амид и дегидрованием, например, хлорокисью фосфора. Соединения, в которых R2 представляет группу -SOR4 или -SO2R4, можно получить окислением соединений, в которых R2 представляет группу R4 с использованием, например, 3-хлоропербензойной кислоты в инертном растворителе, таком, как ди хлорметан при температуре от - 40°С до 0°С. Следующие примеры иллюстрируют получение соединений общей формулы (I). Если не указано иначе проценты даются в весовых частях Пример 1 Ацетат натрия (7,4 г) добавлялся к смеси гидроксидамин гидрохлорида (6,3 г) и 3-пиклопропил2-этоксиметилен-1/2-фторо-4-метилсульфонилфенил/-пропан-1,3-диона (29,0 г) в этаноле. Смесь перемешивалась при комнатной температуре всю ночь. Растворитель выпаривался и остаток разделялся между этилацетатом и водой. Органическая фаза промывалась водой, высушивалась (безводный сульфат магния), фильтровалось и выпаривала до сухости Остаток растирался в порошок с эфиром и фильтровался Полученное твердое вещество рекристаллизовалось из метанола. Маточные жидкости из рекристаллизации соединялись и выпаривались до сухости Остаток очищался колонной хроматографией на силикагеле для получения 4-ци кклопроп ил карбони л-5-/2-фторо-4метилсульфонилфенилАизоксазола (соединение І) в виде твердого вещества белого цвета, т. пл 129-130,5°С. Таким же образом из соответствующе замещенных исходных материалов были получены следующие соединения: Таблица 2 Соедин № R R1 (R2) Т.пл./NMP 2 Н Ср 3,4 - С12 ЯМР. (CDCU) 1,1(м, 2Н) 1,35 (м, 2Н)2 3(м, IH) 7,6(д, IH) 7,95(д, ІН)8,2б(с, ІН) 8,75(с, IH) 3 Н Ср 4-Sme т.лл. 94 - 86°С 27725 Продолжение табл. 2 Соедин № R R1 (R2) Т пл./NMP 4 Н Ср З-Сі-4-SMe т.пл: 96 - 87,5°С 8 Н Ср 3-Sme ЯМР:(СОС1з)1,0 (м, 2Н) 1,4(м, 2Н) 2,25(м, IH) 2,55(0. ЗН) 7,4(д,2Н)7,7(м ( 1Н) 7,9{с, IH) S,7(c, IH) н 12 Ср 2-SPh-4-CF3 ЯМР: (CDCLs) 0,85(м, 2Н) 1,15(М,2Н)1,9(М:1Н) 7,25{с, 5Н) 7,4(с,ІН)7,5(м, 2Н) 8,6(с, IH) Примечание: Цп означает циклопропил Пример 2 Смесь I- [2-хлоро-4-/метилсульфенил-/фенил] -3- цикло-пропилпроп-1- ин-3-она (1,39 г) и этилхлоро-оксилидоацетата (0,8 г) в толуоле перемешивалась и нагревалась при обратном холодильнике всю ночь. Она охлаждалась и выпаривалась до сухости. Остаток очищался хроматографией элютрованием смесью гексана и дихлорметана, а затем эфиром для получения зтил-5-[2-хл оро-4-/метил сул ьфен ид/фен и л]-4циклопропилкарбонилизоксалол-3-карбоксилата (соединения 9, 0,72 г) в виде твердого вещества оранажевого цвета, т.пл 50°С. Таким же образом были получены следующие соединения из соответствующе замещенных исходных материалов; № соедин 10 R R1 /R2/ т.пл. CO2Et Ср 2-Sme-4-CF3 98 -100°С 11 ССЫРг СР 2-Sme-4-CF3 104- 105°С Примечание: Цп означает циклопропил Примера 3 Смесь 5 - [ 3 - хлоро-47метилсупьфенил/фенил]-4-цикпопропилкарбонил-изоксазола (1,0 г) и 3-хлоропероксибензойной кислоты. (2,3 г, 50%) в дихлорметане перемешивалась всю ночь .Добавлялся насыщенный раствор бисульфата натрия и слои разделялись. Органическая фаза раствором бикарбоната натрия, водой, высушивалась (MgSo4) и фильтровалась. Фильтрат выпаривался до сухости для получения 4циклопропил карбон ил-5-[3-хлоро-4-/мети л сул ьнил/фенил] изоксазола/соединение 5, 1,11 г (в виде вещества белого цвета), т.пл 148 - 150"С. Таким же образом были получены следующие соединения из соответствующе замещенных исходных материалов: 27725 № соедин 6 R R1 /R2/n Т.пп. Н Цп 4-SO2Me 102 - 104°C Цп 4-SOMe 97 - 99°C 7 Примечание Цп означает циклопропил Пример 4 Ацетат натрия (1,1 г) добавлялся к раствору гидроксиламин гидрохлорида (0,9 г) и 3- циклоnponnn-2-/N, N- диметиламинометилен/- 1- [5/метилсульфенил/-лирид-2- ил]пропан-1,3- диона (ЗЮ24 г) в этаноле. Смесь перемешивалась 1 час, затем охлаждалась и фильтровалась. Твердое вещество промывалось холодным этанолом и фильтрат частично выпаривался. Добавлялась вода и смесь перемешивалась при 0° 0,5 часа. Она экстрагировалась дихлорметэном, промывалась водой, высушивалась (Na2SO4) и фильтровалась. Фильтрат выпаривался до сухости и остаток очищался хроматографией с элюированием смесью этилацетата и гексана для получения 4- циклопропилкарбонил- 5- [5-/ метилсульфенил/пирид-2-ил] изоксаэола (соединение 13, 0,41 г) в виде твердого вещества белого цвета.т.пл 103- 104°С. Ссылочный пример 1 Смесь 3- циклопропил-1- /2- фторо- 4- метилсульфон ил фенил/- пропан-1,3-диона (7,4 г), триэтипортоформата (8,5 г) и уксусного ангидрида перемешивалась и нагревалась с обратным холодильником 4 часа. Смесь выпаривалась до сухости. Добавлялся ксилен и смесь повторно выпаривалась для получения З-цаклопропил-2этоксиметилен-1-/2-фторо-4-метилсульфонилфенид/-пропан-1,3-диона (8,8 г) в виде масла красного цвета, которое более не очищалось Подобным же образом были получены следующие соединения из соответствующе замещенных исходных материалов: о о R1 /R2/n Циклопропил 3,4 - С12 Циклопропил 4-SMe Циклопропил 3 - СІ - 4 - SMe Циклопропил 3-SMe Циклопропил 2 -SPh-4-CF3 Ссылочный пример 2 Смесь т-бутил -3- циклопропил -272- фторо4- метилсульфонил-бензоид/- 3-оксопропионата (10,5 г) и п-толуолсульфокислоты (2,0 г) в толуоле перемешивалась и нагревалась с обратный холодильником 4 часа. Смесь промывалась водой, высушивалась (безводный сульфат магния) и фильтровалась. Фильтрат выпаривался до су хости для получения 3- циклопропил-1-/2- фторо4- метилсульфонилфенил/-пропан-1,3диона (7,4 г) в воде смолы красного цвета. ЯМР /CDC13/A9-1.3/M, 4Н/, 1,8-2,1/М. 1Н/, 3,Vc, ЗН/, 6,3/с, 1Н/ 7,5-8,0/М. ЗН/. Таким же образом 3-циклопропил-1-/3,4- дихлорфенил/-пропан-1,3-дион был получен из соответствующе замещенного исходного материала. _Ссылочный примеру Смесь магния (0,7 г) и т-бутил 3- циклопропил-3- оксопропио-ната (4,9? г) в метаноле перемешивалась и добавлялся тетрахлор-метан (1 мл). Смесь перемешивалась 1 час и выпаривалась до сухости. Добавлялся толуол и смесь повторно вываривалась до сухости. Остаток растворялся в ацетонитриле и добавлялся 2- фторо4- метил сул ьфон и л-бензоил хлорид (6,5 г). Смесь перемешивалась 4 часа, выпаривалась до сухости и растворялась в этилацетате, промывалась разбавленной хлористоводородной кислотой, высушивалась (безводный сульфат магния) и фильтровалась. Фильтрат выпаривался до сухости для получения т-бутил-3- циклопропил 12фторо-4- метил-сульфонилбензоид/-3- оксопропионата (10,5 г) в виде смолы красного цвета, которая более не очищалась. Подобным же образом (с заменой ацетонитрила толуолом в качестве растворителя реакции) из соответствующе замещенного исходного материала был получен/3-цикло-пропил -/3,4- дихлорбензоидАЗ- оксо-пропионат. Ссылочные пример 4 Смесь 2-фторо- 4 - метилсул ьфон ил бензойной кислоты (6,0 г) и тион ил хлорида перемешивалась и нагревалась с обратным холодильником 2 часа. Смесь охлаждалась л выпаривалась до сухости. Добавлялся толуол и растворитель повторно выпаривался для получения 2-фторо-4~ глетил-сульфонилбензойхлорида (6,5 г) в виде твердого вещества коричневого цвета, которое далее не очищалось. Ссылочный пример 5 2- фторо- 4 /метилсульфенил/-толуол (25,4 т) суспендировался в воде и суспензия нагревалась до 100°С. Перманганат калия (110,2 г) добавлялся с такой скоростью, чтобы поддержать температуру около 100°С. Полученная суспензия фильтровалась и твердое вещество промывалось горячей водой. Охлажденный фильтрат экстрагировался этилацетатом. Водный слой окислялся до рН I и экстрагировался этилацетатом. Органическая фаза высушивалась (безводный сульфат магния) и фильтровалась. Фильтрат выпаривался до сухости для получения 2- фторо4- метилсульфонилбензойной кислоты (15,9 г) в виде твердого вещества оранжевого цвета, т.пл 187-188°С. Ссылочный пример 6 Смесь 3- фторо-4- метиланилина (25 г) .диметилд и сульфида (375 г) и т-бутил нитрита 27725 (30 мл) в 1,2- дихлорэтане согревалась до начала реакции. Раствор 3- фторо-4- метиланилина (225 г) в 1,2- дихлорэтане добавлялся по каплям одновременно с т-6утил-нитритом (24І мл) с такой скоростью, чтобы поддерживать температуру ниже 60°С. Смесь перемешивалась 2 часа, затем добавлялась вода. Органический слой промывался водой, хлористоводородной кислотой, высушивался (безводный сульфат магния) и фильтровался. Фильтрат выпаривался до сухости и остаток подвергался дистилляции, чтобы получить 2- фторо-4-/метилсульфенилАтолуол (164 г) в виде желтого масла, ЯМР /ацетон - oV, 2,2/ЗН, d/2,5/3H, с/,7,05/ЗН,МУ Ссылочный пример 7 Смесь 3- циклопропил-1- [5- /метилсульфенид/ - пирид-2- ил] пропан-1,3- диона (2,9 г), диметилформадлид диметилацетата и диоксана перемешивалась при комнатной температуре всю ночь. Она выпаривалась до сухости и остаток растирался в порошок с эфиром и фильтровался с тем, чтобы получить 3- циклопропил-2/ N, N диметиламинометилен/-1-5/- метилсульфенил/-пирид-2- ил пропан-1,3- дион (3,24 г) в виде твердого вещества коричневого цвета, которое использовалось без дальнейшей характеристики. Ссылочный пример 8 Циклопропилметилкетон (0,84 г) добавлялся к суспензии гидрида натрия (80%, 0,3 г) в диоксане. Смесь перемешивалась 20 минут и добавлялся этил 4-/метилсульфенид/бензоат (1,0 г). Смесь перемешивалась и нагревалась при 45"С 1,5 часа и при 60°С 2 часа. Она выстаивалась при комнатной температуре всю ночь. Добавлялись хлористоводородная кислота (2М) и смесь экстрагировалась зтилацетатом, промывалась, высушивалась (MgSO4) и фильтровалась. Фильтрат выпаривался до сухости и остаток очищался хроматографией с элюированием смесью этилацетата и гексана до получения 3- циклопропил-1 -[4- /метилсульфонид/-фэнил]-пропан/-1,3- диона (0,59 г) в качестве твердого вещества оранжевого цвета, ЯМР /СОСУ 1,0/м, 2Н/, 1,2/м, 2Н/, 1,87м, IH/ 2,5/с, ЗН/, 76,25/с, Ш/, 7,25/д, 2Н/, 16,35/ширсІН/. С помощью такого же способа следующие соединения были получены из соответствующе замещенных исходных материалов с использованием описанного растворителя для проведения реакции: г /R2/n Растворитель ЯМР/т.пл Циклолропил СИ З-СИ-SMe Эфир 102- 105°С Циклопролил сн 3-SMe ТГФ 1 Цшслопррпил сн 2-SPh-4-CI3 ТГФ 2 Циклопропил N 5-SMe Эфир 85 - 87°С R1 Примечание: 1. ЯМР /CDCI3/: 0,8 -1,5 /м, 4Н/, 1,7 2,55/с, ЗН/, 6,25 /с, IH/, 7,2 - 7,85 /М, 4Н/. 2. ЯМР /CDCW: 0,95/м, 2Н/, 1,2/м, 2Н/, 1,7/м, IH/, 6,05/с, IH/, 7,15/с, !Н/, 7,3-7,5/м, 6Н/, 7,6/д, IH/. 2,1/м, !Н/, Ссылочный пример.9 Раствор 2-І фениясульфенил/-4- трифторметилбензойной кислоты (11,5 г) и тионилхлорида (11,4 г) в дихлорметане, содержащей несколько капель ДМФ, нагревался с обратным холодильником 2 часа. Смесь выпаривалась до сухости и добавлялся метанол. Смесь нагревалась с обратным холодильником 1 час и выпаривалась до сухости Она обрабатывалась водой и экстрагировалась эфиром, промывалась раствором карбоната натрия (2М), водой, высушивалась (Na2O4) и фильтровалась. Фильтрат выпаривался до сухости и остаток растирался в порошок с циклогексаном и фильтровался для получения метил 2-/фенил-сульфенил/-4- трифторметилбензоата (10,5 г) в виде твердого вещества белого цвета, т пл 55 - 60"С. Ссылочный пример 10 Смесь 2-/фенилсульфенил/-4- трифторметибензонитрила (90 г) серной кислоте (50%) перемешивалась и нагревалась с обратным холодильником 10 часов. После охлаждения она разбавляется водой и экстрагируется ДХМ. Органи чески и слой экстрагировался водным гидроксидом натрия (2М) и водная фаза окислялась до рН 1, экстрагировалась ДХМ, высушивалась (Na2SO4) и фильтровалась. Фильтрат выпаривался до сухости для получения 2-І фенилсультенил/-4- трифторметнлбензойной кислоты (75 г) в виде твердого вещества желтого цвета, т.пл161-164 е С. Ссылочный пример 11 Смесь 2- нитро-4- трифторнетил-бензонитрила (8,63 г), тиофенола (4,4 г) и карбоната калия (6,9 г), а в ацетонитриле перемешивалась при комнатной температуре 1 час, затем нагревалась с обратным холодильником 9 часов. Добавлялся тиофенол (0,3 мл) и смесь перемешивалась и нагревалась с обратным холодильником 1 час. Добавлялась вода и смесь экстрагировалась дихлорметаном высушивалась (MgSO4) и фильтровалась. Фильтрат выпаривался до сухости и остаток рекристаллизовался из н-гексана для получения 2-/фенилсульфенилЛ4- трифгорметилбензонитрила (9,5 г) в виде твердого вещества белого цвета, т.пл 51 °С. 10 27725 Ссылочный пример 12 Раствор н-бутиллития в гексане (4,4 мл) добавлялся к перемешанному раствору -2-хлоро-4Л метил сул ьфени л/фенил ацетилена (2,0 г) в ТГФ при поддержании температуры - 70°С. Смесь перемешивалась 5 минут и добавлялся циклопропанкарбонилхлорид (2,4 г). Смесь подогревалась до комнатной температуры и выливалась на водный раствор хлорида натрия. Водный слой экстрагировался эфиром и соединенные органичесткие слои высушивались (MgSCU) и фильтровались. Фильтр выпаривался до сухости и остаток растворялся в метаноле и нагревался с обратным холодильником 5 минут. Добавлялся толуол и смесь выпаривалась до сухости. Остаток очищался хроматографией с элюированием смесью гексана и эфира для получения 1-[2- хлоро4-/метилсульфенил/ фенил] -3- циклопропилпроп-1- ин-3- она в виде масла желтого цвета, которое кристаллизовалось при стоянии, т.пл 46 50°С. 2-Хлоро-4-/ метилсульфен ил/фен ил ацетилен был получен реакцией 1-бромо-2-[2 -хлоро4-1 метилсульфен ил/фенил] ацетилена с -нбутиллитием и влажным хлоридом цинка в ТГФ при - 70°С. щей непрореагированный 1,1- дибромо-2- [метилсульфен ил-4- трифторметилфенил] этилен. Ссылочный пример 15 Трифенилфосфин (2,5 г) добавлялся к перемешанному раствору тетрабромметана с поддержанием температуры при 0°С. Смесь перемешивалась 0,5 часа и добавлялся 2-хлоро-4-/ сульфенил-бензальдегид (1,0 г). Смесь перемешивалась 0,5 часа и выливалась в гексан. Полученное твердое вещество отфильтровывалось и промывалось эфиром. Объединенные фильтраты выпаривались до сухости и остаток очищался хроматографией с элюированием гексаном для получения 1,1-дибромо-2-[2хлоро-4-/метилсульфенил/фенил]-этилена (0,96 г) в виде твердого вещества белого цвета, ЯМР /СОСЫ 2,45 /с, ЗН/, 7,15 /д, !Н/, 7,25/с, ІН/, 7,55 /с, ІН/, 7,6/д, ІН/. Таким же способом из соответствующе замещенного исходного материала было получено следующее соединение. 1,1- Дибромо-2-[2-/метилсульфенил/-4- трифторметилфенил] этилен в виде твердого вещества белого цвета, ЯМР /CDCIa/ 2,5/с, ЗН/, 7,4-7,7 /м, 4Н/. Ссылочный пример 16 Смесь 2- хлоро-4- /метилсульфенид/-бензоил хлорида (1,0 г) трифенил фосфина (2,47 г) и бис/ трифенилфосфин/медь (1) борогидрида (1,0 г) а ацетоне перемешивалась при ОТ 1 час. Потом добавлялся бис/ трифенилфосфин/медь (1) борогидрид (1,5 г) и смесь перемешивалась 2 часа. Смесь фильтровалась и фильтрат выпаривался до сухости. Остаток растворялся в хлороформе и обрабатывался бромидом меди (1) (2,1 г). Фильтрат выпаривался до сухости и фильтрат очищался хроматографией с элюированием смесью этипацетата и гексана для получения 2- хлоро-4/метилсульфенил/- бензальдегида (0,83 г) в вида твердого вещества белого цвета, т пл 76 - 77СС. Ссылочный пример 13 н- бутиллитий (2,5 М, 1,45 мл) добавлялся к перемешанному холодному раствору 1 - бромо-22-/метилсульфенил/-4-трифторметилфенил ацетилена и 1,1- дибромо-2-2-/метилсуль-фенил/-4трифторметилфенил этилена (1,0 г) в ТГФ с поддержанием температуры ниже -70°С. Смесь перемешивалась 80 минут и добавлялся хлорид циклопропанкарбонила (0,75 г). Когда температура достигала комнатной, смесь перемешивалась 2 часа. Добавлялся водный хлорид аммония и смесь экстрагировалась эфиром, высушивалась и фильтровалась. Фильтрат выпаривался до сухости и остаток очищался хроматографией с элюированием смесью гексана и эфира для получения 3- циклопропил-1-[2-/метилосуль-фенил/-4-трифтор-метилфенил] - проп-1- ин-3- она (0,64 г) в виде желтого масла, ЯМР /CDCW 1,15 /м, 2Н/, 1,45/м, 2Н/, 2,2/м, IH/, 2,6 /с, IH/, 7,35/ д, Н/, 7,4/с, IH/, 7,р/д, IH/. Таким же способом был получен 2-/ метилсульфенил/-4- три-фторметилбензальдегид из соответствующе замещенного исходного материала. Ссылочный матриал 17 н-Бутиллитий (2,5 М Б гексане ,25 мл) добавлялся в инертной атмосфере к перемешанному раствору 4-бромо-З- /метилсульфенид/ бензотрифторида (16,4 г) в эфире при поддержании температуры ниже -70°С 2 часа. Смесь выпивалась на твердые гранулы двуокиси углерода, перемешивалась 10 минут и добавлялась водная хлористо-водородная кислота. Слои разделялись и водный слой экстрагировался эфиром. Соединенные органические слои промывались водой, высушивались (MgSO-O и фильтровались. Фильтрат выпаривался и остаток растирался в порошок с циклогексаном и фильтровался для получения 2-І метилоульфенил/-4- трифторметилбензойной кисдоты (12,4 г) в виде твердого вещества белого цвета, ЯМР /CDCI3+DMSO-d6/: 2,45/с, ЗН/, 7,2/д, ІН/, 7,3/с, ІН/, 8,0/д, ІН/, 10,7-11/шир.сІН/. Ссылочный пример 18 т-бутилнитрит /3 мл/ добавлялся к смеси 3амино-4- бромо-бензотрифторида (4 г) и диметиддисульфида (15 мл) г хлороформе. Смесь согревалась до начала реакции, когда одновре Ссылочный пример 14 Суспензия Triton ВАговарный знак Reg бензилтри метила ммонийгидроксид, 40% в метаноле, (1,8 г) в толуоле добавлялась к раствору 1,1- дибромо -2-[2- хлоро-4-/ метил-сульфенил/фенил] этилену (0,96 г) в толуоле. Смесь перемешивалась 15 минут. Добавлялась серная кислота (2м) и полученные слои разделялись. Органический слой промывался водой, высушивался (MgSOi) и фильтровался. Фильтрат выпаривался до сухости и остаток очищался хроматографией с элюированнем смесью гексана и дихлорметана для получения 1- бромо -2- [2- хлоро-4-/ метилсульфен ил/ фенил] ацетилена (90,78 г) в виде масла желтого цвета, ЯМР /CDCb/ 2,5 /с, ЗН/, 7,05/Д, IH/, 7,3/с, ІН/,7,35/Д, ІН/. С помощью такого же способа было получено следующее соединение из соответствующе замещенного исходного материала. 1- бромо-2-[2-/гл етил сул ьфенид/-4- трифторметилфенил] ацетилен в виде смеси, содержа 11 27725 менно добавлялись т-бутилнитрит (11 мл) и раствор 3- амино -4- бромбензотрифторида (16 г) в хлороформе. Полученнная смесь перемешивалась 24 часа, промывалась водой, хлористоводородной кислотой (2М) водой, высушивалась (MgS04) и фильтровалась. Фильтрат выпаривался до сухости и остаток подвергался дистилляции для получения 4-бромо-З- /метилсульфенил/-бензотрифторида (16,4 г) в виде желтого масла, т.кип. 84 - 88°С при 2 мм рт.ст. В соответствии с признаком настоящего изобретения предлагается способ борьбы с ростом сорняков (т.е. нежелательной вегетации) в очаге, который включает применение к очагу гербицидно эффективного количества по меньшей мере одного из производных 5- арил изоксазола с общей формулой (1). Для этой цели производные 5 -арил изоксазола обычно используются в виде гербицидных композиций (т.е. вместе с совместимыми разбавителями или носителями и/или поверхностно-активными агентами, пригодными для использования в гербицидных композициях), например, описанных далее. сорняков, например, для контроля роста тех видов, которые были упомянуты ранее применением до или после всхожести непосредственно или опосредованно, как, например, прямым или непрямым распылением очага заражения сорняками, который используется для выращивания культур, например, зерновых: - пшеницы, ячменя, овса, кукурузы и риса, соевых бобов, полевых и карликовых бобов, гороха люцерны, хлопка, земляного ореха, льна, лука, моркови, капусты, редьки, подсолнечника, сахарной свеклы и постоянных или культурных пастбищ до ипи после высевания культуры или до или после всхожести культуры. Для селективного контроля сорняков в очаге, предназначенного или используемого для выращивания культур, например, упомянутых выше, наиболее приемлемыми являются нормы применения между 0,01 и 4,0 кг, а лучше между 0,01 кг и 2,0 кг активного материала на гектар Соединения общей формулы (1) можно также использовать для контроля роста сорняков, в частности, упомянутых выше, применением до или после всхожести в рощах и других дереворастущих площадях, например, лесах, парках и плантациях, например, сахарного тростника, масличной пальмы и каучуковых, плантациях. Для этой цели их можно применять непосредственно или опосредованно (прямым) непрямым распылением на сорняки или в почву, в которой они находятся до или после высаживания деревьев или плантаций с нормами применения между 0,25 кг и 5,0 кг, а предпочтительно между 0,5 кг и 4,0 кг, активного материала на гектар. Соединения общей формулы (1) демонстрируют гербицидную активность против двудольных (т.е. широколистных) и однодольных (т.е. травяных) сорняков применением до -и /или после всхожести. Под термином «применение до всхожести» понимается применение в почву, в которой семена или ростки сорняков присутствуют до появления сорняков над поверхностью почвы. Под термином "применение после всхожести" понимается применение к открытым частям сорняков, которые появились над поверхностью почвы. Например, соединения общей формулы (1) можно использовать для борьбы с ростом: - широколистных сорняков например Abutilon theophrasti Amaranthus retroflexus, Bides pilosa, Chenipodium album Galium aparine. Ipomola spp. Например Ipomela purpurea, Sesbania exaltata, Sinapis arvensis, Solanum nigrum and Xanthium strumarium; и -травяных сорняков, например, Alopucurus myosuroides, Arena fatua, Digitaria sanguinlis, Echinochloa crusgalli, Eleusine indica u Setaria faben'i илиЄеіала viridis; и - осок, например, Cuperus esculentus. Количество применяемых соединений общей формулы (1) зависит от природы сорняков, используемых композиций, времени применения, климатических и природных условий и (при использовании для борьбы с ростом сорняков на площади выращивания культур) - от вида культур. При использовании на площади выращивания культур норма применения должна быть достаточной для контроля роста сорняков, но не должна наносить вред урожаю. В общем, с учетом этих факторов нормы применения между 0,01 кг и 5 кг активного материала на гектар дают хорошие результаты. Однако следует понимать, что могут использоваться более высокие или низкие нормы применения в зависимости от конкретной поставленной задачи борьбы с сорняками. Соединения общей формулы (1) можно также использовать для борьбы с сорняками в очагах, не являющихся площадями для выращивания культур, но в которых борьба с сорняками желательна. Примерами таких очагов являются аэродромы, индустриальные районы, жапезные дороги, обочины дорог, берега рек, ирригационные и другие каналы, кустарники, пустыри или не культивируемая земля, в частности, где необходимо уменьшить риск пожаров. При использовании в таких целях, когда часто требуется полный гербицидный эффект, активные соединения используются в более высоких дозировках и точная дозировка зависит от характера уничтожаемой растительности и искомого эффекта. Применение до всхожести или после ее, а лучше до всхожести прямым или опосредованным распылением при нормах применения между 1,0 кг и 20,0 кг, а предпочтительно между 5,0 и 10,0 кг активного материала на гектар особенно приемлемо для этой цели. При использовании для борьбы с ростом сорняков до всхожести соединения общей формулы (1) можно вводить в почву, в которой предполагается появление сорняков. Когда соединения формулы (1) используются после всхожести, они входят в контакт с почвой и могут затем осуществлять контроль всхожести сорняков, прорастающих позднее. При необходимости более длительного контроля применение может быть повторено. Соединения общей формулы (1) могут использоваться для селективного контроля роста 12 27725 В соответствии с другим признаком настоящего изобретения предлагаются композиции, пригодные для гербицидного использования, включающие одно или несколько производных 5арил изокса-зола общей формулы (1) вместе с одним или несколькими совместимыми сельскохозяйственно приемлемыми разбавителями или носителями и/или ПАВ, а лучше гомогенно диспергированными в этих носителях т.е. разбавителями или носителями и/или ПАВ типа, известного в области техники и пригодных для использования в гербицидных соединениях и композициях и совместимых с соединениями общей формулы (1).Термин «гомогенно диспергированные» используется для вручения композиций, в которых соединения общей формулы (1) растворены в других компонентах. Термин "гербицидные композиции" используется в широком смысле для включения не только композиций, которые готовы для применения в качестве гербицидов, но также концентратов, которые должны разбавляться перед использованием. Предпочтительно композиции содержат от 0,05 до 90 вес.% одного или нескольких соединений общей формулы (1). рованные формации можно готовить абсорбцией соединений общей формулы (1) растворенных в подходящих растворителях, которые при желании могут быть летучими на твердые разбавители или носители в гранулированной форме и, при желании, испарением растворителей, или гранулированием композиций в порошкообразной форме, полученных как описано выше. Твердые гербицидные композиции, особенно самчивающие порошки и гранулы, могут содержать смачивающие или диспергирующие агенты, которые в твердом состоянии могут служить разбавителями или растворителями. Жидкие композиции по изобретению могут принимать форму водных, органических или водо-органических растворов, суспензий и эмульсий, которые включают ПАВ. Приемлемые жидкие разбавители для включения в жидкие композиции-вода, гликоли, тотрагад-рофурфуриловый спирт, ацетофенон, циклогексанон, изофорон, толуол, ксилен, руда, животные и растительные жиры и легкие ароматические и нафтеновые фракции нефти (и смеси этих разбавителей ПАВ в жидких композициях могут быть ионными и неионными), например, типов, описанных выше и в жидких состояниях могут также служить разбавителями или носителями. Гербицидные композиции могут содержать и разбавитель или носитель, и ПАВ (например, смачивающее, диспергирующее или эмульгирующее вещество или агент, ПАВ, присутствующие в гербицидных композициях настоящего изобретения, могут быть ионного или неионного видов, например, сульфоркцинолеаты, производные четвертичного аммония, продукты, основанные на конденсатах этиленоксида с алкиловыми или полиариловыми фенолами, например, нонил - или октил-фенолы или эфиры ангидросорбитов карбоновой кислоты, которые делаются растворимыми этерификацией свободных гидроксильных групп конденсацией с этиленоксидом, соли щелочных и щелочно-земельных металлов эфиров серной кислоты и сульфокислот, такие, как динонил- и диоктилнатрий сульфоносукцинаты и соли щелочных и щелочно-земельных металлов производных сульфокислоты с высокой молекулярной массой такие, как лигносульфонаты натрия и кальция и алкилбензол сульфонаты натрия и кальция. Порошка, диспергируемые гранулы и жидкие композиции в форме концентратов могут разбавляться водой или другими подходящими разбавителями, например, минеральными или растительными маслами, особенно в случае, если в жидких концентратах разбавителем или носителем является масло. При желании жидкие композиции могут использоваться в форме самоэмульгирущихся концентратов, содержащих активные вещества, растворенные в эмульгирущих агентах или в растворителях, содержащих эмульгирущие агенты совместимые с активными веществами, простое добавление воды к таким коцентратам дает композиции готовые для использования, жидкие концентраты, в которых разбавитель или носитель-масло, могут применяться без дальнейшего разбавления с использованием техники электростатического распыления. Гербицидные композиции по настоящему изобретению могут также включать при желании обычные препараты, усиливающие действие, такие, как клеи, защитные коллоиды, сгустители, пенетрирующие агенты, стабилизаторы, пассиваторы, антиспекающие агенты и ингибиторы коррозии. Эти препараты могут также служить носителями или разбавителями. Если не указано иначе следующие проценты даются по весу. Предпочтительными гербицидными композициями по настоящему изобретению являются водные суспензионные концентраты, включающие от 10 до 70 % одного или нескольких соединений общей формулы (1), от 2 до 10% ПАВ, от 0.1 до 5% сгустителя и от 15 до 87,9 % воды: - смачиваемые порошки, включающие от 10 до 90% одного или нескольких соединений общей формулы (1), от 2 до 10% ПАВ и от 8 до 88% твердого разбавителя или носителя; Гербицидпые композиции по настоящему изобретенияю могут включать до 10% по весу, например, от 0,05 до 10% ПАВ, но при желании даже более высокие пропорции ПАВ, например, до 15 вес.% в концентратах жидкой эмульсионной суспензии и до 25 вес,% в жидких водорастворимых концентратах. Примеры подходящих твердых разбавителей или носителей-силикат алюминия, тальк, кальцинированная магнезия, кизельгур, трикальций фосфат, порошковая пробка, абсорбентный черный уголь и глины, такие, как каолин и бентонит Твердые композиции (которые имеют форму пылей, гранул или смачиваемых порошков) готовятся измельчением соединений общей формулы (1) с твердыми разбавителями или насыщением твердых разбавителей или носителей растворами соединений общей формулы{1) в летучих растворителях выпариванием растворителей, и, при необходимости, измельчением продуктов с тем, чтобы получить порошки. Гранули 13 27725 тетические пиретроиды, перметрин и циперметрин и фунгициды, например, карбаматы-метил N/1- бутил-карбамоил-бензимидазол -2- ил/карбамат, и триазолы, например, 1-/4- хлорофенокси/-3,3- диметил-1- /1,2,4- триазол -1- ил/бутан -2-он. Пестицидно активные соединения и другие биологически активные материалы, которые могут включаться или использоваться вместе с соединениями настоящего изобретения, и которые представляют собой кислоты, при желании могут применяться в форме обычных производных, например, солей щелочных металлов и амина и эфиров. В соответствии с еще одним признаком настоящего изобретения предлагается продукт, включающий по меньшей мере одно производное 5- арил изоксазола общей формулы (I) или гербицидная композиция, описанная выше, а предпочтительно гербицидный концентрат, который должен разбавляться перед применением, включающий по меньшей мере одно из производных 5-арил изоксазола общей формулы (1) внутри контейнера и инструкции к этому контейнеру, излагающие способ использования указанного производного или гербицидной композиции, содержащейся внутри для борьбы с ростом сорняков. Контейнеры представляют собой те, которые обычно используются для хранения химических веществ в твердом состоянии при обычных температурах окружающей среды и гербицидных композиций, в частности, в форме концентратов, например, металлические банки и бочки, которые изнутри могут быть покрыты лаком, или выполненные из пластика, бутылки из пластика или стекла, и если содержимое контейнера твердое вещество, например, гранулированное, это могут быть коробки из картона, пластика и металла, или мешки. Контейнеры обычно бывают достаточной емкости с тем, чтобы содержать достаточное количество гербицида для обработки хотя бы одного акра земли, но не превышать размера удобного в обращении. Инструкции должны быть физически связаны с контейнером, например, напечатаны на нем либо на специальной наклейке или ярлыке, прикрепленном к контейнеру. Там обычно указывается содержимое контейнера, которое после разбавления, при необходимости, применяется для борьбы с ростом сорняков с нормой применения между 0,01 кг и 20 кг активного материала на гектар определенным способом. - водорастворимые или вододиспергируемые порошки, включающие от 10 до 90% одного или нескольких соединений общей формулы (1), от 2 до 40% карбоната натрия и от 0 до 88% твердого разбавителя, -жидкие водорастворимые концентраты, включающие от 5 до 50%, например, 10-30 % одного или нескольких соединений общей формулы (1), от 5 до 25% ПАВ и от 25 до 90%, например. 4585% водоемешиваемого растворителя, например, диметилформамида или смеси водосмешиваемого растворителя и воды; - концентраты жидкой эмульсионной суспензии, включающие от 10 до 70% одного или нескольких соединений общей формулы (1), от 5 до 15% ПАВ, от 0,1 до 5% сгустителя и от 10 до 84,9% органического растворителя, - гранулы, включающие от 1 до 90%, например, 2-10% одного или нескольких соединений общей формулы (1), от 0,5 до 7%, например, 0,5-2% ПАВ, и от 3 до 98,5%, например, 88-97,5% гранулированного носителя,и - эмульсионные концентраты, включающие 0,05-90%, а предпочтительно от 1 до 60% одного или нескольких соединений общей формулы (1) от 0,01 до 10%, а лучше от 1 до 10% ПАВ, и от 9,99 до 99,94%, а лучше от 39 до 98,99% органического растворителя. Гербицидные соединения по настоящему изобретению могут также содержать соединения общей формулы (1) вместе с одним или несколькими другими пестицидно активными соединениями или диспергироваться в них, и кроме того, один или несколько совместимых пестицидно приемлемых разбавителей или носителей ДАВ, и препаратов, усиливающих действие Примеры других включенных в данные композиции пестицидно активных соединений включают гербициды, например, увеличивающие диапазон видов сорняков: алахлор[2- хлоро-2,6"-э диэтил -N- /метоксиметил/-ацетанилид], атразин [2- хлоро-4- этиламино-6- изопропиламино-1,3,5- триазин], бромоксинил [3,5- дибромо-4- гидроксибенэонитрил], хлортолурон N" -хлоро-4- метилфенил/-М,М- диметилмочевина цианазин, [2- хлоро-4-/1- циано-1- метил этилам ино/-6этиламино-1,3,5-триазин], 2,4 D[2,4- дихлорофенокси-уксусная кислота], дикамба [3,6- дихлоро2- метоксибензойная кислота] дифензохат [1,2диметил-3,5дифенил-пиразолиевые соли], флампропметил [метил N-2-N- бензоил -З- хлоро4- фтороанилино /-пропинат] фторметурон [N" /3- трифторо-метилфенил/-М,М- диметилмочевина], изопротурон [N'-/4- изопропилфенил /-N.Nди метил мочевина, инсектициды, например, син Следующие примеры иллюстрируют гербицидные композиции в соответствии с настоящим изобретением ПримерС1 Растворимый концентрат формируется изАктивного ингредиента (соединение 1) 20% вес/об 33% вес/об раствора гидроокиси калия 10% об/об Тетрагидрофурфурилового спирта ЛТФС/ 10% об/об Воды до 100 объемов 14 27725 Подобные растворимые концентраты можно приготовить как описано выше заменой изоксазола (соединения 1) другими соединениями общей формулы (1). перемешиванием ТГФС, активного ингредиента (соединения 1) и 90% объема воды и медленным добавлением раствора гидроокиси калия до достижения постоянного рН 7-8, и затем доведением до нужного объема водой. Пример С2 Смачиваемый порошок формируется из: Активного ингредиента (соединение 1) 50% вес/вес Натрий додецилбензол сульфоната 3% вес/вес Лигносульфоната натрия 5% вес/вес Натрий формальдегид алкилнафталин сульфоната 2% вес/вес Сильно измельченного диоксида кремния 3% вес/вес Фарфоровой глины 37% вес/вес Подобные смачиваемые порошки можно приготовить как описано выше заменой изоксазола (соединения 1) другими соединениями общей формулы (1). смешиванием вышеуказанных ингредиентов вместе и измельчением смеси в реактивной мельнице. Пример СЗ Водорастворимый порошок формируется из: Активного ингредиента /соединение 1/ 50% вес/вес Натрий додецилбензолсульфонат 1% вес/вес Сильно измельченного диоксида кремния 2% вес/вес Бикарбоната натрия 47% вес/вес Соответствующие количества соединений, используемых для обработки растений, растворялись в ацетоне для получения растворов эквивалентных нормам применения до 4000 г испытуемого соединения на гектар /г/га/. Эти растворы подавались из стандартного лабораторного распылителя с подачей 290 литров распыдительной жидкости на гектар в). Контроль сорняков: до всхожести Семена высевались в квадратные пластиковые горшочки размером 70 мм и глубиной 75 мм в нестерильную почву. Количество семян на горшок было следующим: смешиванием вышеуказанных ингредиентов и измельчением указанной смеси в молотковой мельнице. Подобные водорастворимые порошки можно приготовить как описано выше заменой изоксазола (соединения 1) другими соединениями общей формулы (1). Представленные соединения изобретения использовались в гербицидных применениях в соответствии со следующими процедурами Способ использования гербицидных соединений а). Общая часть Виды соря ков 1) Широколистные сорняки Abutilon theophrasti Amaranthus retroflexus Galium aparine Ipomea purpurea Sinapis arvensis Xantium strumarium 2) Травянистые сорняки Alopecurus myosuroides Avena fatua Echinochloa crus-galli Setaria viridis 3) Осоки Cyparus esculentus Культура 1) Широколистная Приблизительное число семян/горш 10 20 10 10 15 2 15 10 15 20 3 15 27725 3 3 Хлопок Соя 2/Травянистая Кукуруза Рис Пшеница 2 6 6 Соединение изобретения применялось к поверхности почвы, содержащей семена, как описано в /а/. Каждый горшочек каждой культуры и каждого сорняка подвергался каждой обработке, контрольные горшочки не подвергались распылению, а другие контрольные подвергались распылению только ацетоном. После обработки горшочки помещались, на капилярную подстилку в оранжерею и поливались сверху. Визуальная оценка повреждения культуры делалась спустя 20-24 дня после распыления. Результаты выражались в процентном снижении роста или повреждении культуры или 1) Широколистные сорняки Abutilon theophrasti Amaranthus retraflexus Galium aparine Ipomea purpurea Sinapis arvensis Xantium strumarium 2) Травянистые сорняки Alopecurus myosuroides Avena fatua Echinochloa crus-galli Setaria viridis 3) Осоки Cyparus esculentus Культура 1) Широколистная Хлопок сорняков по сравнению с растениями в контрольных горшочках. с). Контроль сорняков: после всхожести Сорняки и культуры высеивались непосредственно в компост для горшочков глубиной 75 мм, размером 70 мм квадратной форы, за исключением, который был на стадии ростка и перенесен в горшки за неделю до распыления. Затем растения выращивались в оранжерее до готовности к распылению соединениями, используемыми для обработки растений. Число растений на горшок было следующим: Число растений на горшок 3 4 3 3 4 1 Стадия роста 1-2 листа 1-2 листа 1-я мутовка 1-2 листа 2 листа 2-3 листа 8-12 12-18 4 15-25 3 2 Соединение, используемое для обработки растений, применялось к растениям как описано в (а). Каждый горшок каждой культуры и вида сорняков подвергался каждой обработке, контрольные горшочки не подвергались распылению, а другие контрольные горшочки подвергались распылению только ацетоном. После обработки горшочки помещались на капилярную подстилку в оранжерею и поливали сверху один раз спустя 24 часа и затем контролируемом ирригацией Визуальная оценка повреждения культур и контроля сорняков делалась через 20-24 дня после распыления. Результаты выражались в процентном снижении роста или повреждении культуры или сорняков по 1 лист 2 листа 2 4 5 2) Травянистая Кукуруза Рис Пшеница Элиста 2 Соя 1-2 листа 1 -2 листа 1-2 листа 1-2 листа 2-3 листа 2-3 листа 2-3 листа сравнению с растениями в контрольных горшочках. Соединения изобретения, используемые с дозировкой 4 кг/га или меньше показали отличный уровень гербицидной активности вместе с толерантностью культуры к сорнякам используемым в предшествующих экспериментах. При применении до всхожести с нормой 1000 г/га соединений 1-13 произошло снижение роста на 90% одного или нескольких видов сорняков. Применение после всхожести с дозировкой 1000 г/га дало снижение роста на 90% одного или нескольких видов сорняков с селективностью по меньшей мере в одном виде культуры. 16 27725 ДП "Український інститут промислової' власності" (Укрпатент) Україна, 01133, Київ-133, бульв. Лесі Українки, 26 (044) 295-81-42, 295-61-97 Підписано до друку ^ - ^ 5 ^ 2 0 0 1 р. Формат 60x84 1/8. Обсяг
ДивитисяДодаткова інформація
Автори англійськоюKramp Suzanne Mary
Автори російськоюКремп Сьюзан Мери
МПК / Мітки
МПК: C07D 261/18, C07D 413/04, A01N 43/80, C07D 261/08
Мітки: похідні, одержання, 5-арилізоксазолу, варіанти, бур'янів, гербіцидна, композиція, спосіб, пригнічення, локусі, основі
Код посилання
<a href="https://ua.patents.su/18-27725-pokhidni-5-arilizoksazolu-sposib-kh-oderzhannya-varianti-i-gerbicidna-kompoziciya-na-kh-osnovi-ta-sposib-prignichennya-buryaniv-v-lokusi.html" target="_blank" rel="follow" title="База патентів України">Похідні 5-арилізоксазолу, спосіб їх одержання (варіанти) і гербіцидна композиція на їх основі та спосіб пригнічення бур’янів в локусі</a>
Попередній патент: Передавальна схема
Наступний патент: Спосіб біокаталітичного одержання одного з енантіомерів хіральної 2-арилалканової кислоти
Випадковий патент: Спосіб контролю дефектності матеріалу