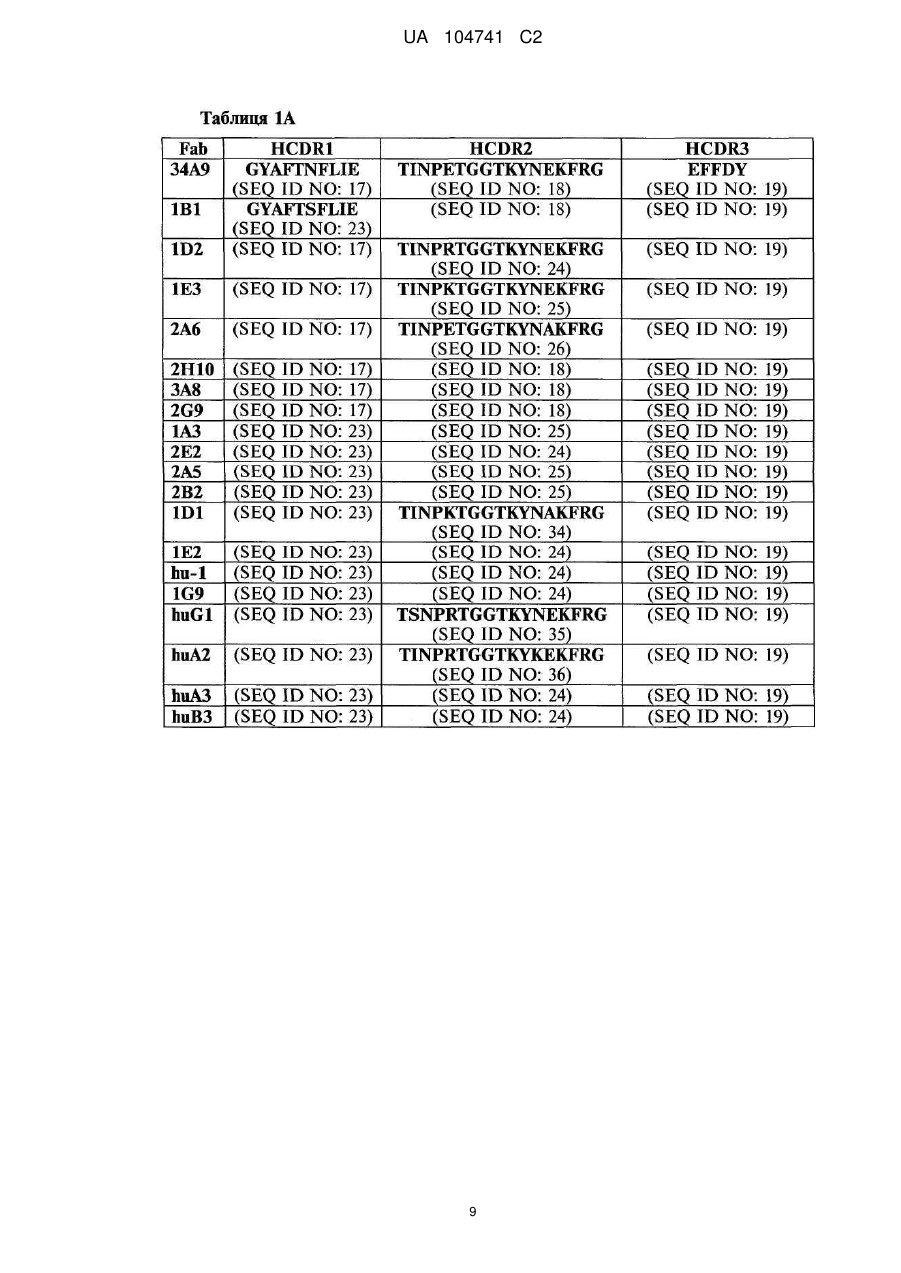
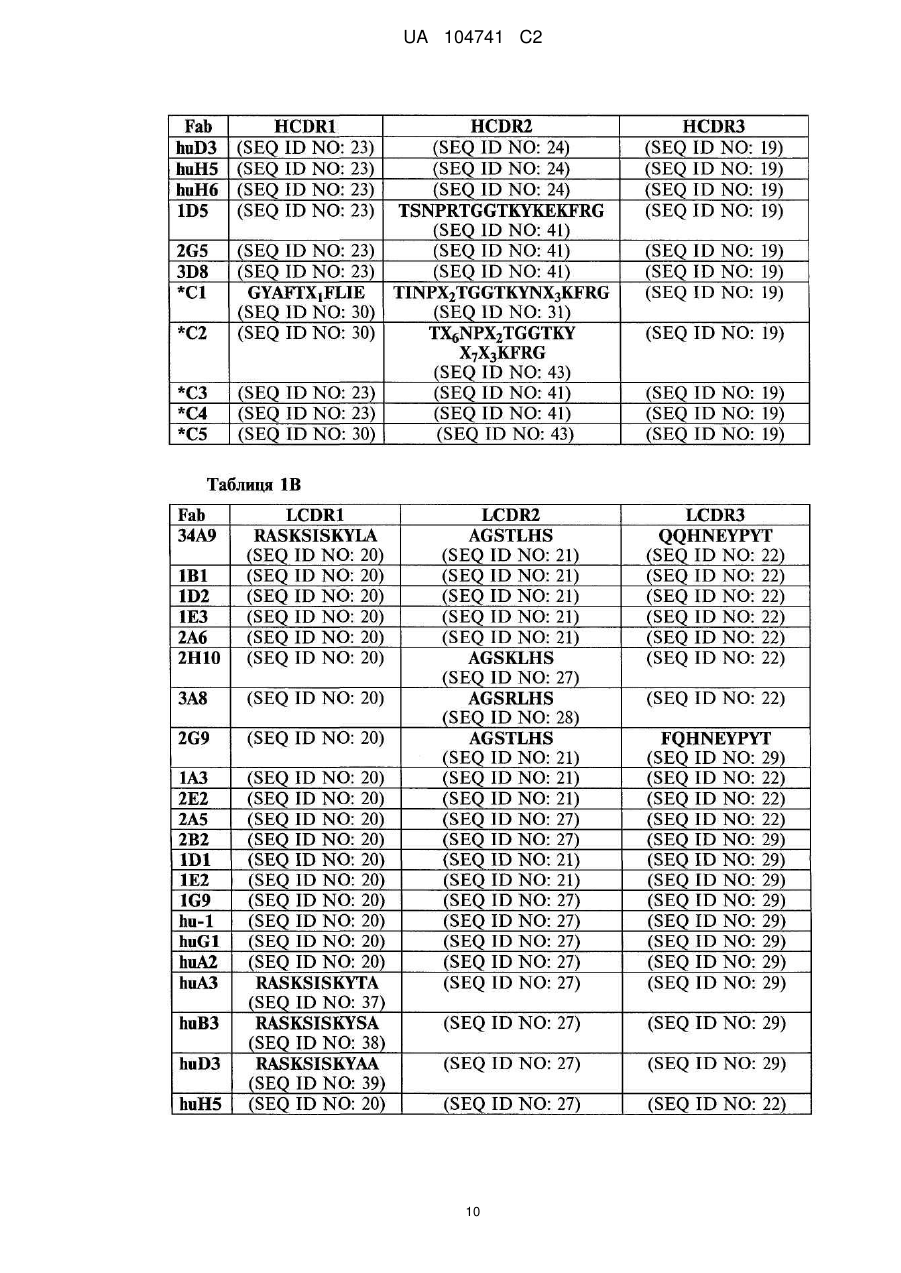
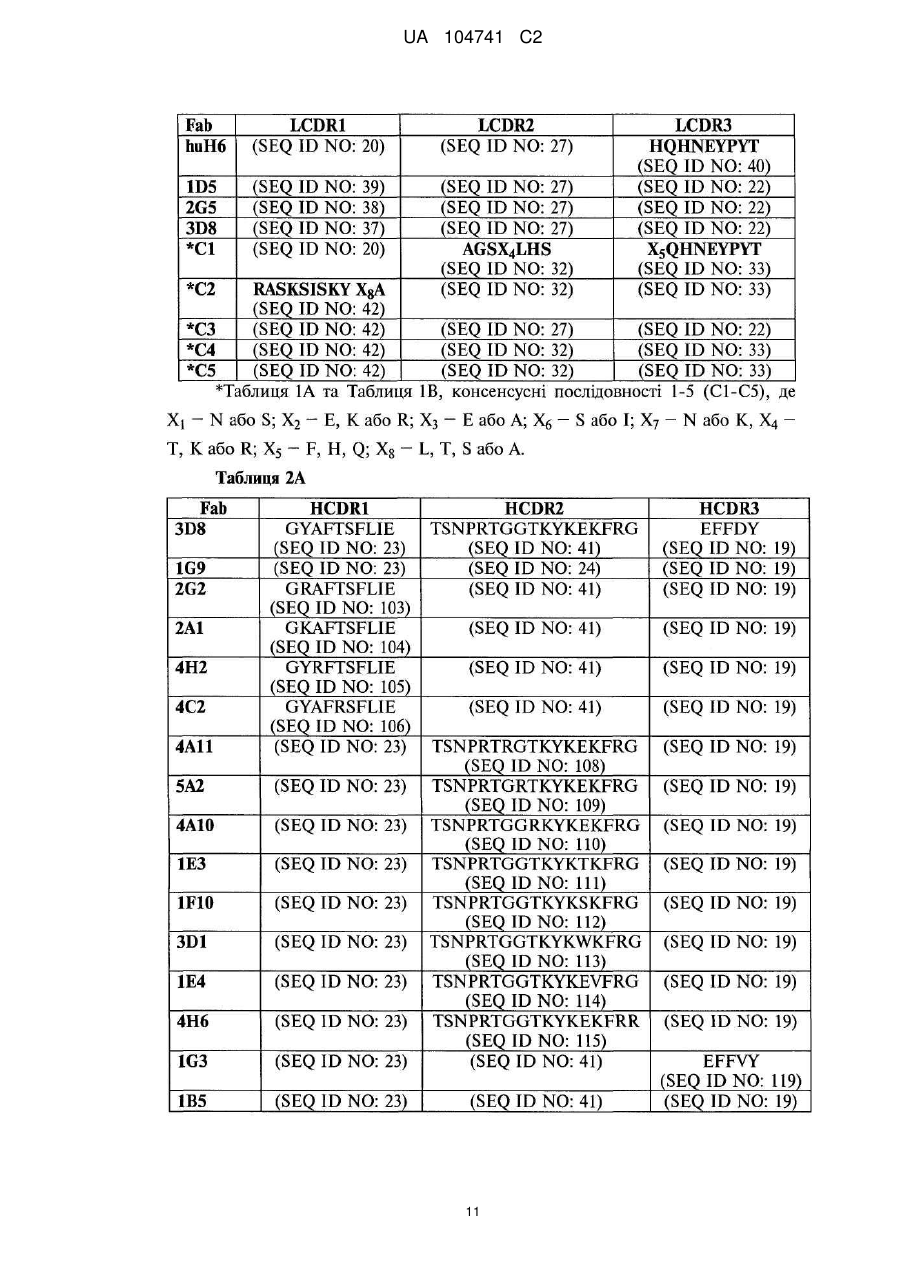
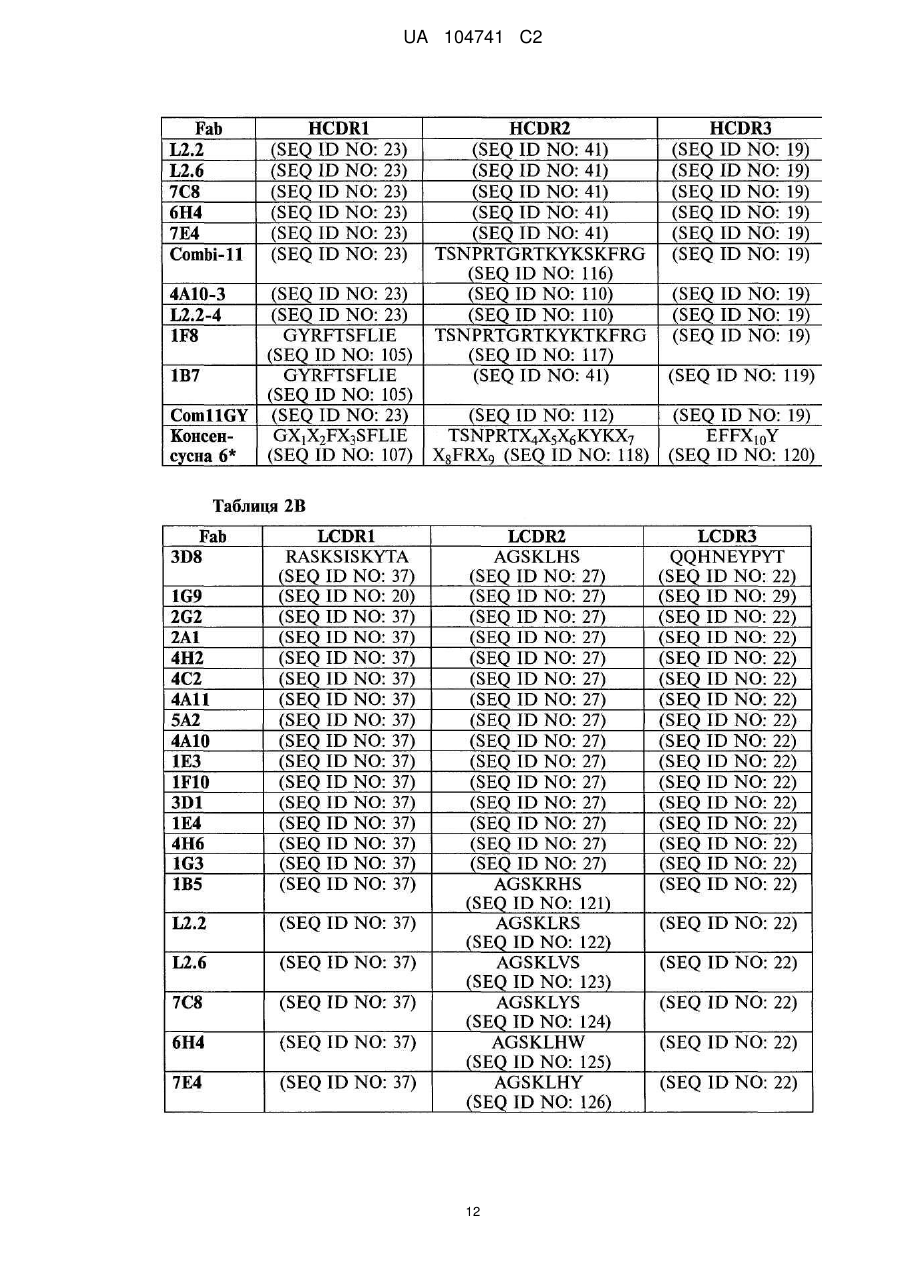
Моноклональні антитіла проти феропортину 1 та варіанти їх застосування
Номер патенту: 104741
Опубліковано: 11.03.2014
Автори: Тань Їнь, Луань Пен, Льюнг Донмайєнн Дон Мун, Манетта Джозеф Вінсент, Уітчер Деррік Райан
Формула / Реферат
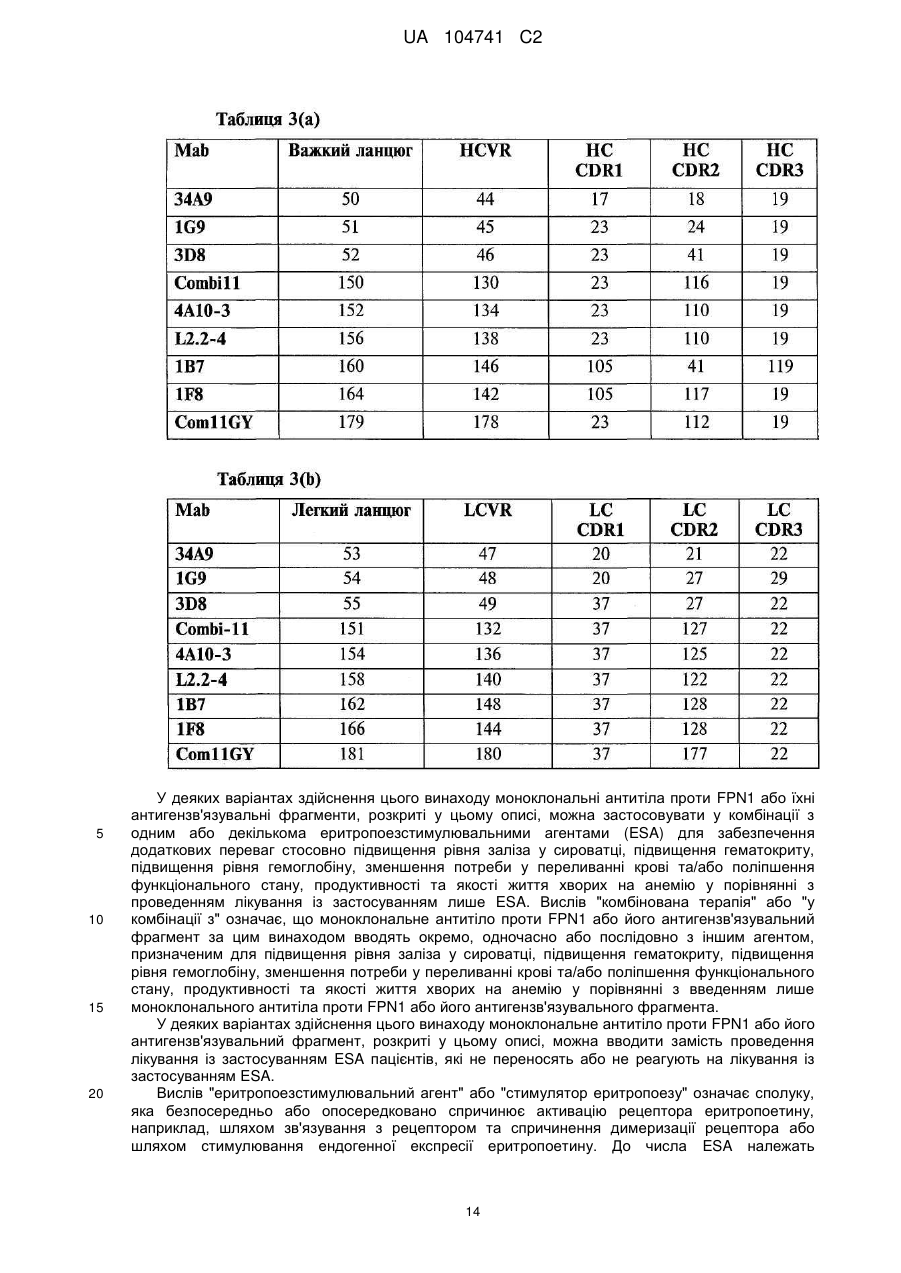
1. Моноклональне антитіло або його антигензв'язувальний фрагмент, що має LCDR1, LCDR2, LCDR3, HCDR1, HCDR2 та HCDR3, які містять амінокислотні послідовності, представлені послідовностями:
a) SEQ ID NO:37, 125, 22, 23, 110 та 19, відповідно; або
b) SEQ ID NO:37, 122, 22, 23, 110 та 19, відповідно;
який зв'язує людський феропортин 1, до складу якого входить амінокислотна послідовність, представлена послідовністю SEQ ID NO:1.
2. Моноклональне антитіло або антигензв'язувальний фрагмент за п. 1, що має варіабельну ділянку легкого ланцюга та варіабельну ділянку важкого ланцюга, представлені послідовностями:
a) SEQ ID NO: 136 та SEQ ID NO:134, відповідно; або
b) SEQ ID NO: 140 та SEQ ID NO:138, відповідно.
3. Моноклональне антитіло або антигензв'язувальний фрагмент за будь-яким із пп. 1-2, що має:
a) легкий ланцюг і важкий ланцюг, представлені послідовністю SEQ ID NO:154 та послідовністю SEQ ID NO:152, відповідно; або
b) легкий ланцюг і важкий ланцюг, представлені послідовністю SEQ ID NO:158 та послідовністю SEQ ID NO:156, відповідно.
4. Моноклональне антитіло за будь-яким із пп. 1-3, що має два поліпептиди легкого ланцюга і два поліпептиди важкого ланцюга, причому кожен з поліпептидів легкого ланцюга має амінокислотну послідовність, представлену послідовністю SEQ ID NO:154, і кожен з поліпептидів важкого ланцюга має амінокислотну послідовність, представлену послідовністю SEQ ID NO:152.
5. Моноклональне антитіло за будь-яким із пп. 1-3, що має два поліпептиди легкого ланцюга і два поліпептиди важкого ланцюга, причому кожен з поліпептидів легкого ланцюга має амінокислотну послідовність, представлену послідовністю SEQ ID NO:158, і кожен з поліпептидів важкого ланцюга має амінокислотну послідовність, представлену послідовністю SEQ ID NO:156.
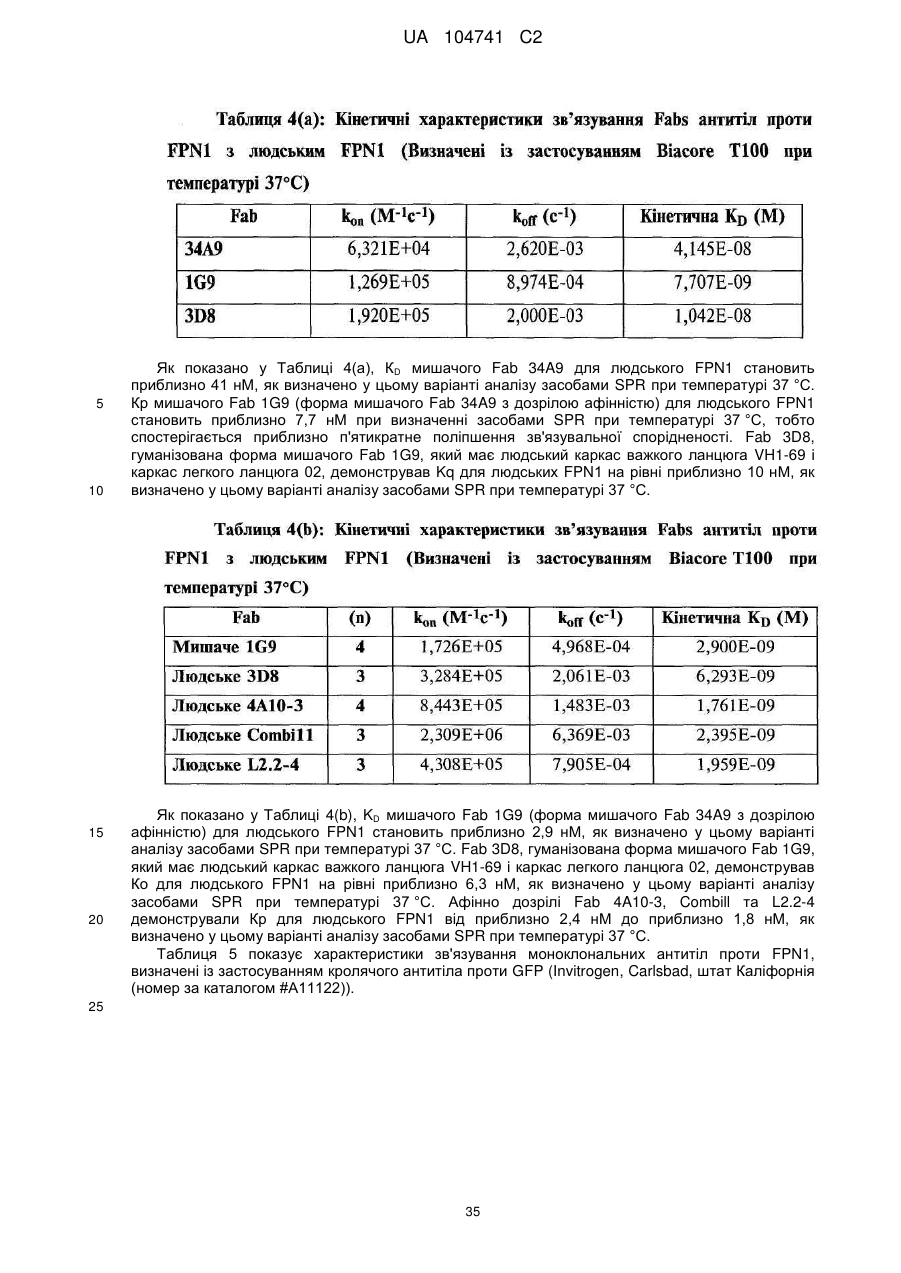
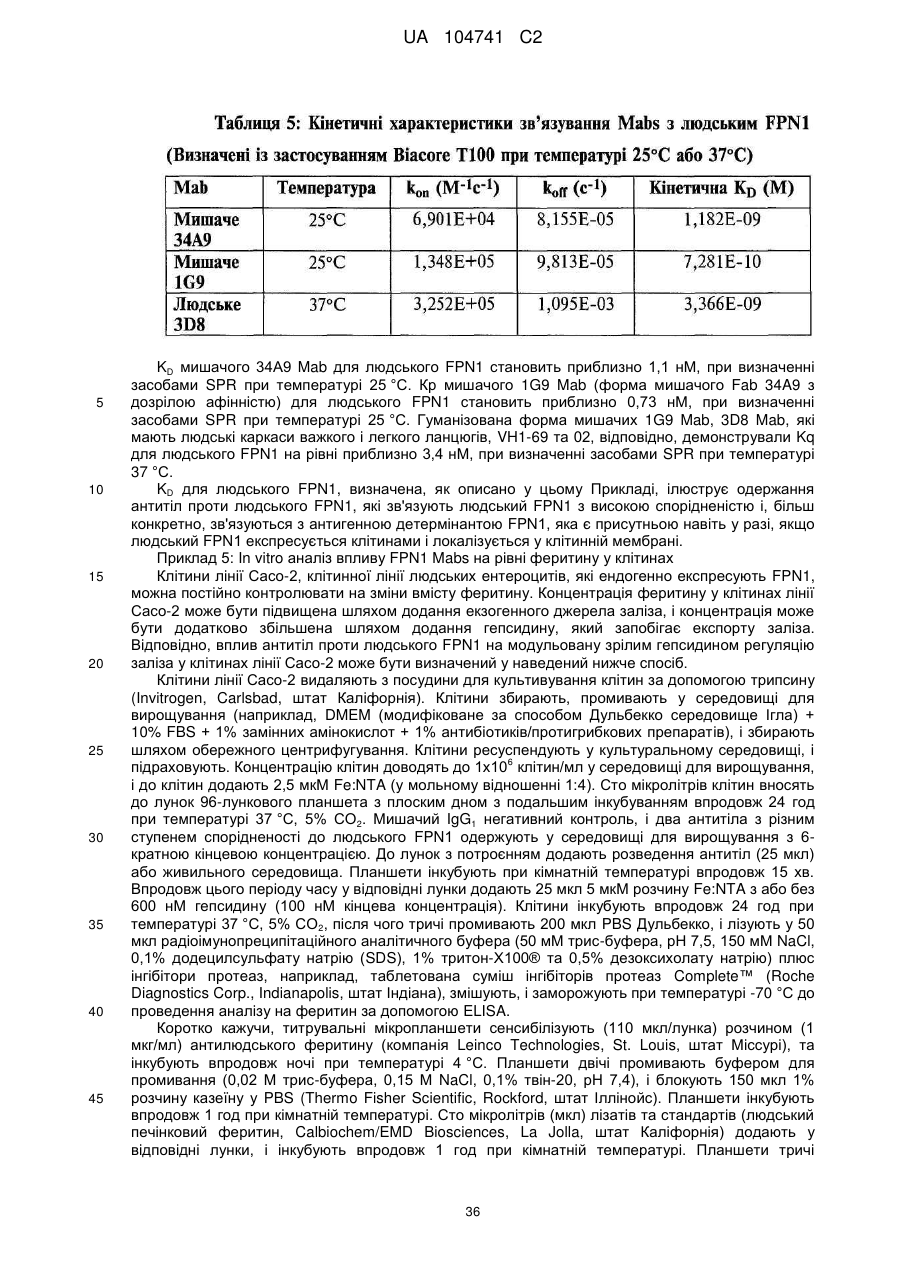
6. Моноклональне антитіло або антигензв'язувальний фрагмент за будь-яким із пп. 1-5, що зв'язує людський феропортин 1 з KD, меншою за приблизно 10 нМ, при визначенні засобами поверхневого плазмонного резонансу при температурі 25 °С.
7. Моноклональне антитіло або антигензв'язувальний фрагмент за будь-яким із пп. 1-6, що зв'язується з одним або декількома пептидами, вибраними з:
а) 403SPFEDIRSRFIQGESITPTK422 (SEQ IDNO:12);
b) 406EDIRSRFIQGESIT419 (SEQ ID NO:13);
c) 409RSRFIQGESITPTK422 (SEQ ID NO:14);
d) 403SPFEDIRSRFIQG415 (SEQ ID NO:15);
e) 409RSRFIQGESIT419 (SEQ ID NO:16); та
f) 409RSRFIQG415 (SEQ ID NO:95).
8. Моноклональне антитіло або антигензв'язувальний фрагмент за будь-яким із пп. 1-7 для застосування у терапії.
9. Моноклональне антитіло або антигензв'язувальний фрагмент за будь-яким із пп. 1-7 для застосування при лікуванні у суб'єкта анемії або при її запобіганні.
10. Застосування моноклонального антитіла або антигензв'язувального фрагмента за будь-яким із пп. 1-7 для одержання лікарського засобу для лікування або запобігання у суб'єкта анемії.
11. Спосіб підвищення рівня заліза у сироватці, кількості ретикулоцитів, кількості еритроцитів, рівня гемоглобіну та/або гематокриту, який включає введення в організм суб'єкта ефективної кількості моноклонального антитіла або антигензв'язувального фрагмента за будь-яким із пп. 1-7.
12. Спосіб лікування анемії у суб'єкта, який включає введення в організм згаданого суб'єкта ефективної кількості моноклонального антитіла або антигензв'язувального фрагмента за будь-яким із пп. 1-7.
13. Спосіб за будь-яким із пп. 11-12, який додатково включає введення в організм згаданого суб'єкта еритропоезстимулювального агента або іншого терапевтичного агента, що традиційно застосовується для підвищення у суб'єкта рівня заліза у сироватці, кількості ретикулоцитів, кількості еритроцитів, рівня гемоглобіну та/або гематокриту.
14. Фармацевтична композиція, яка містить моноклональне антитіло або антигензв'язувальний фрагмент за будь-яким із пп. 1-7 та фармацевтично прийнятний носій, розріджувач або допоміжну речовину.
15. Фармацевтична композиція за п. 14, яка додатково містить еритропоезстимулювальний агент або інший терапевтичний агент, що традиційно застосовується для підвищення у суб'єкта рівня заліза у сироватці, кількості ретикулоцитів, кількості еритроцитів, рівня гемоглобіну та/або гематокриту.
Текст
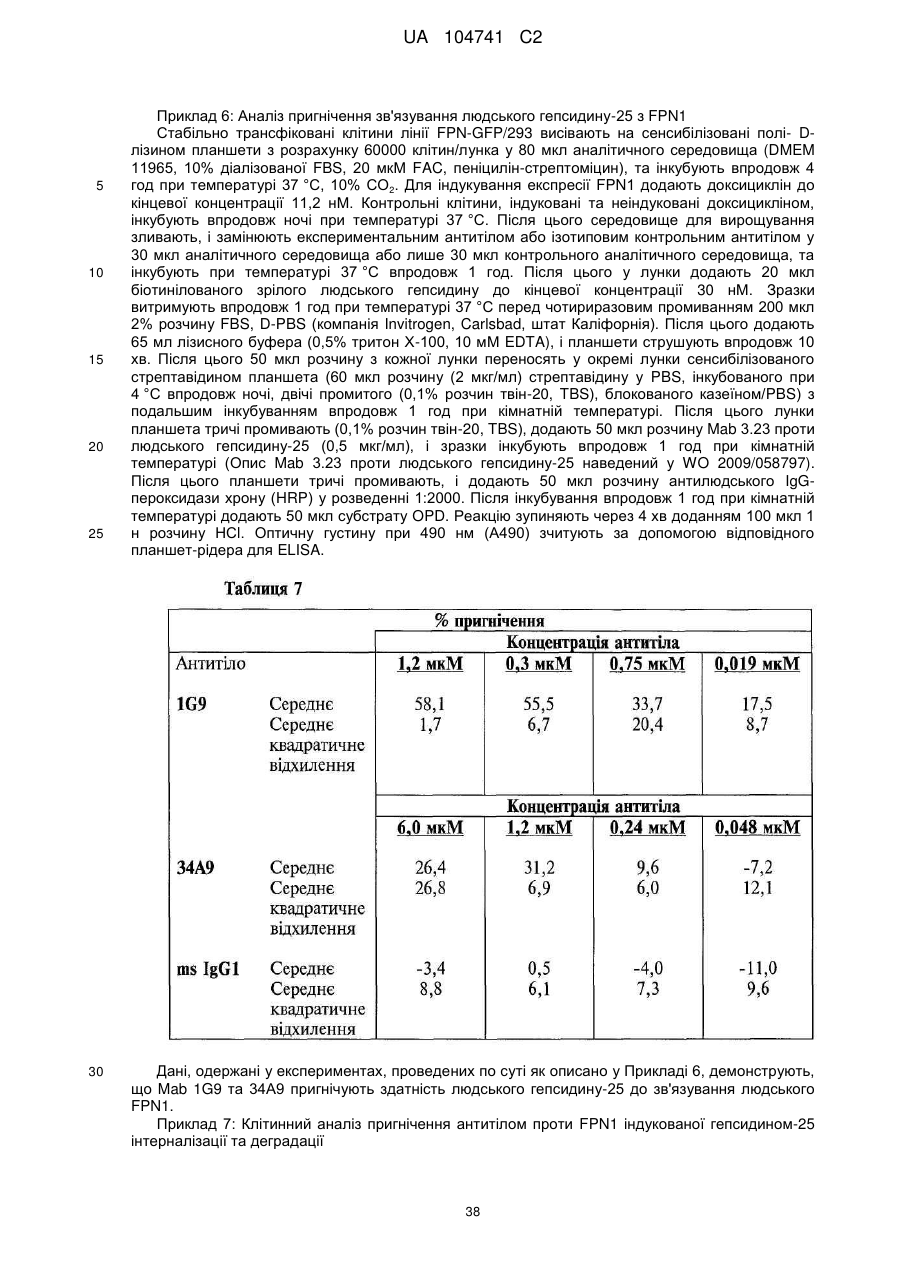
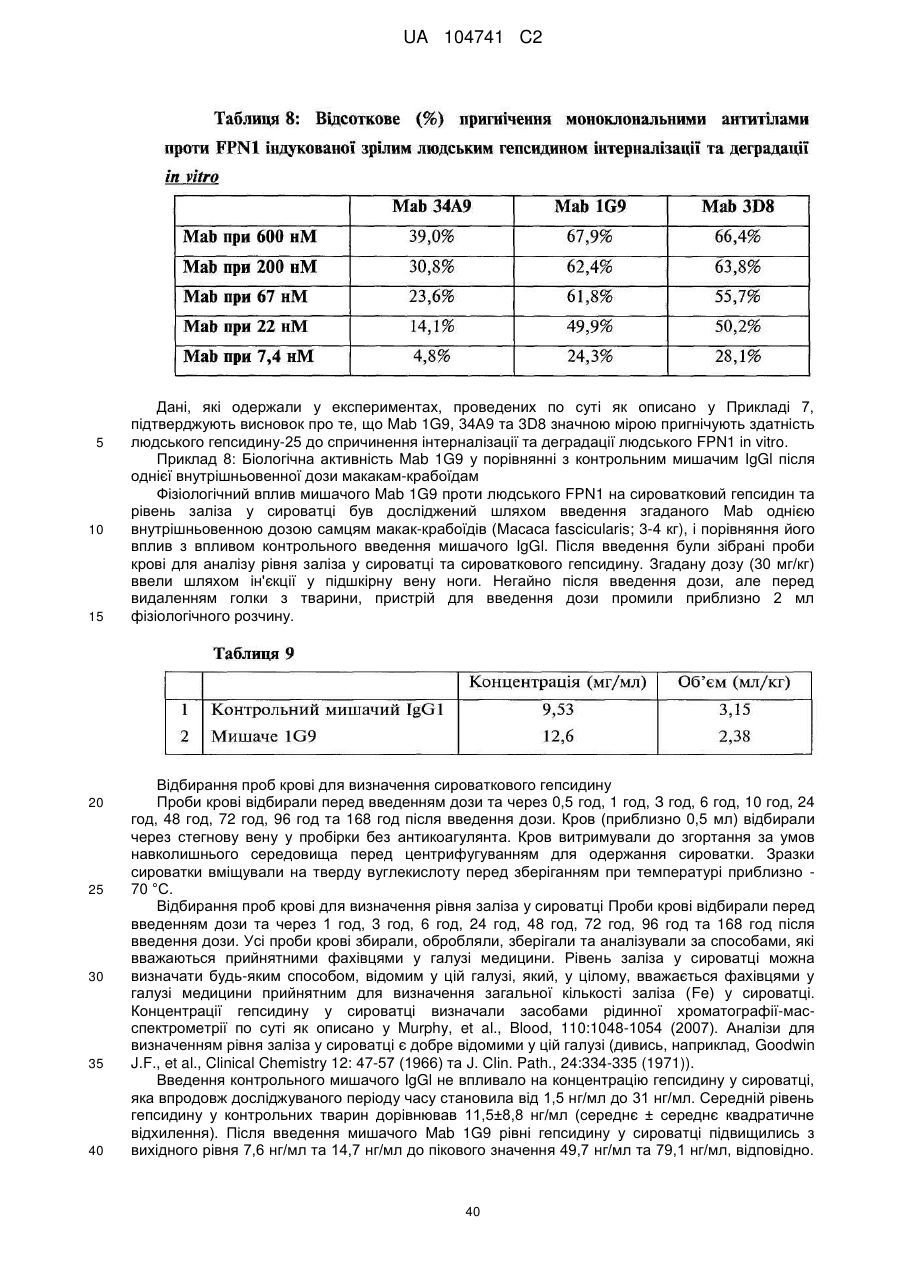
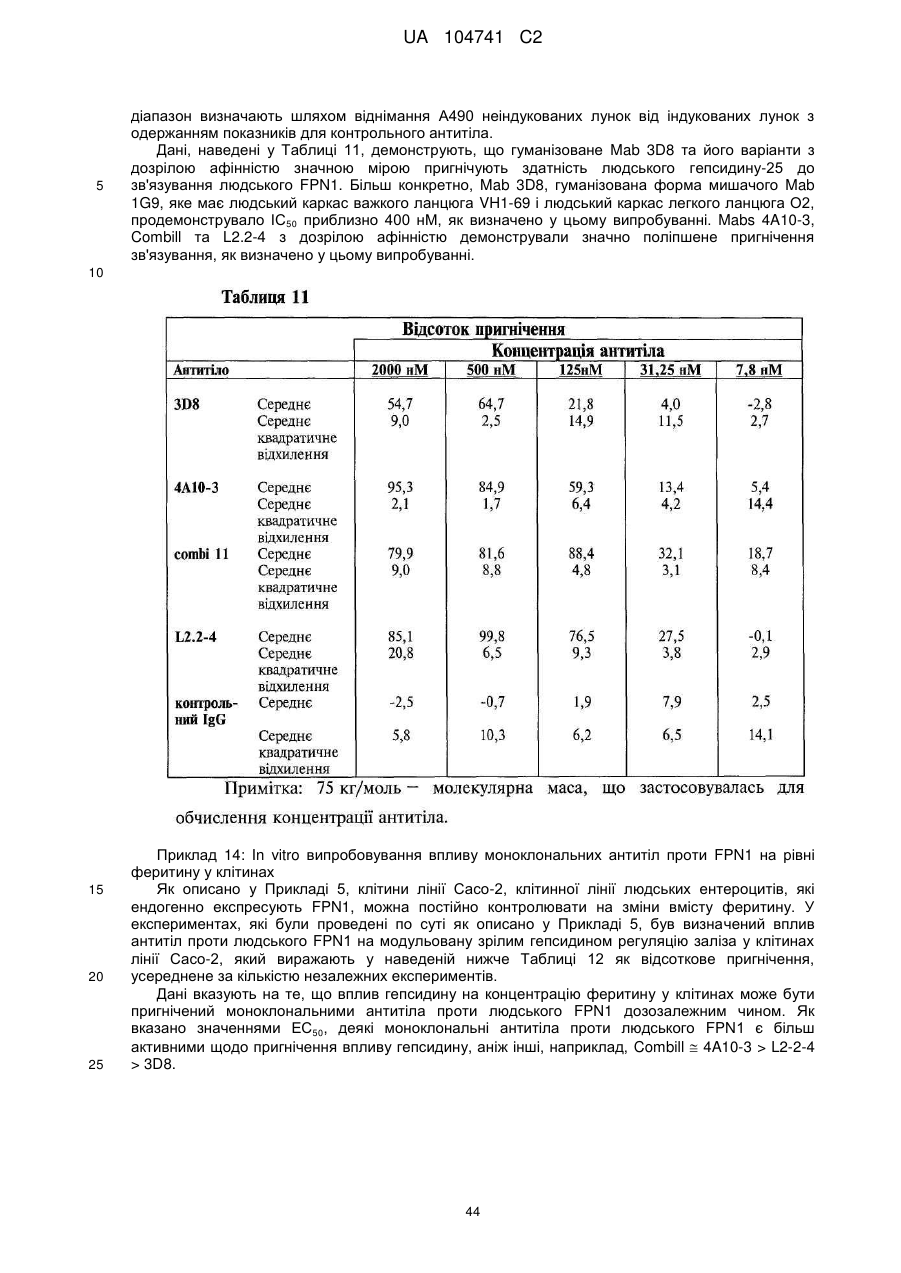
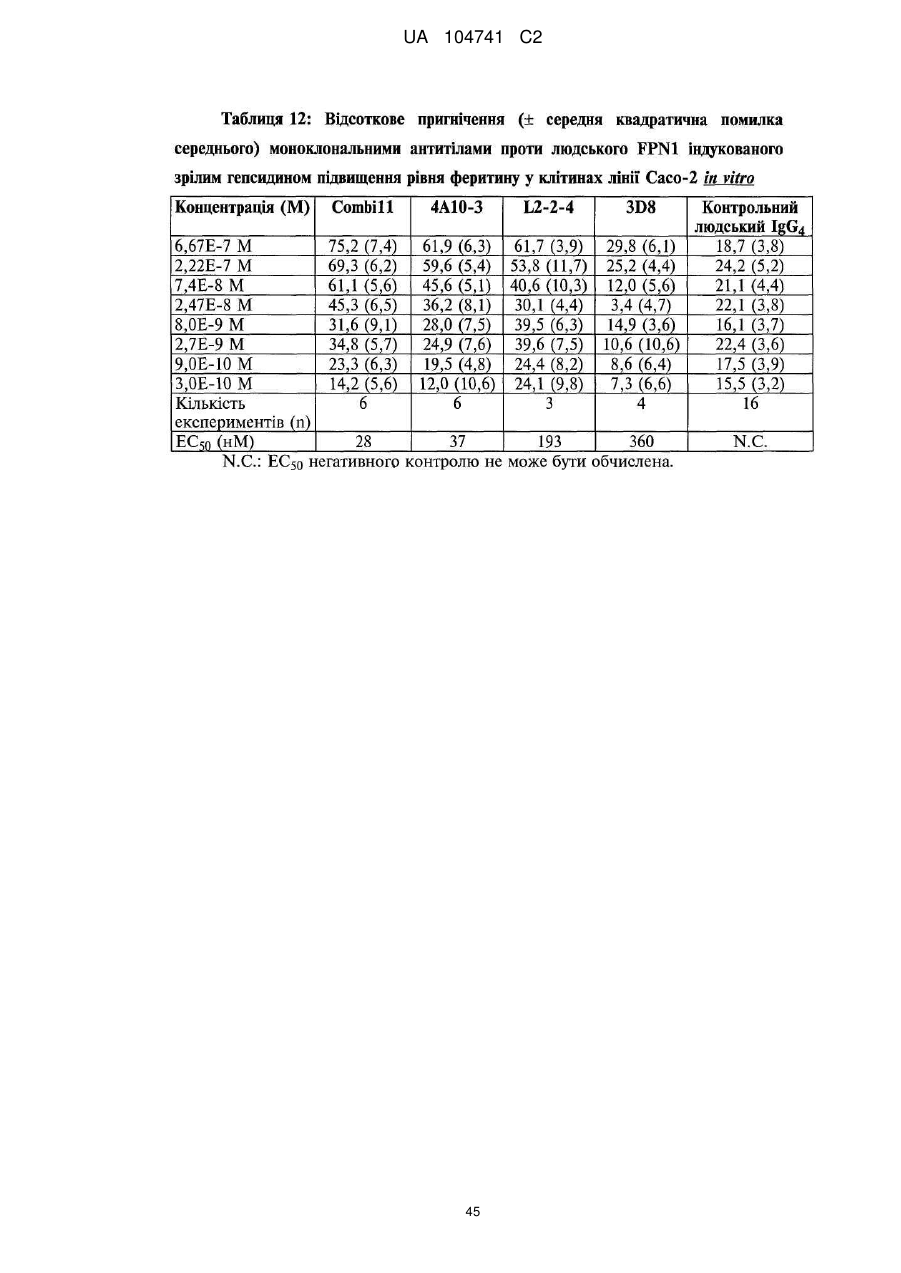
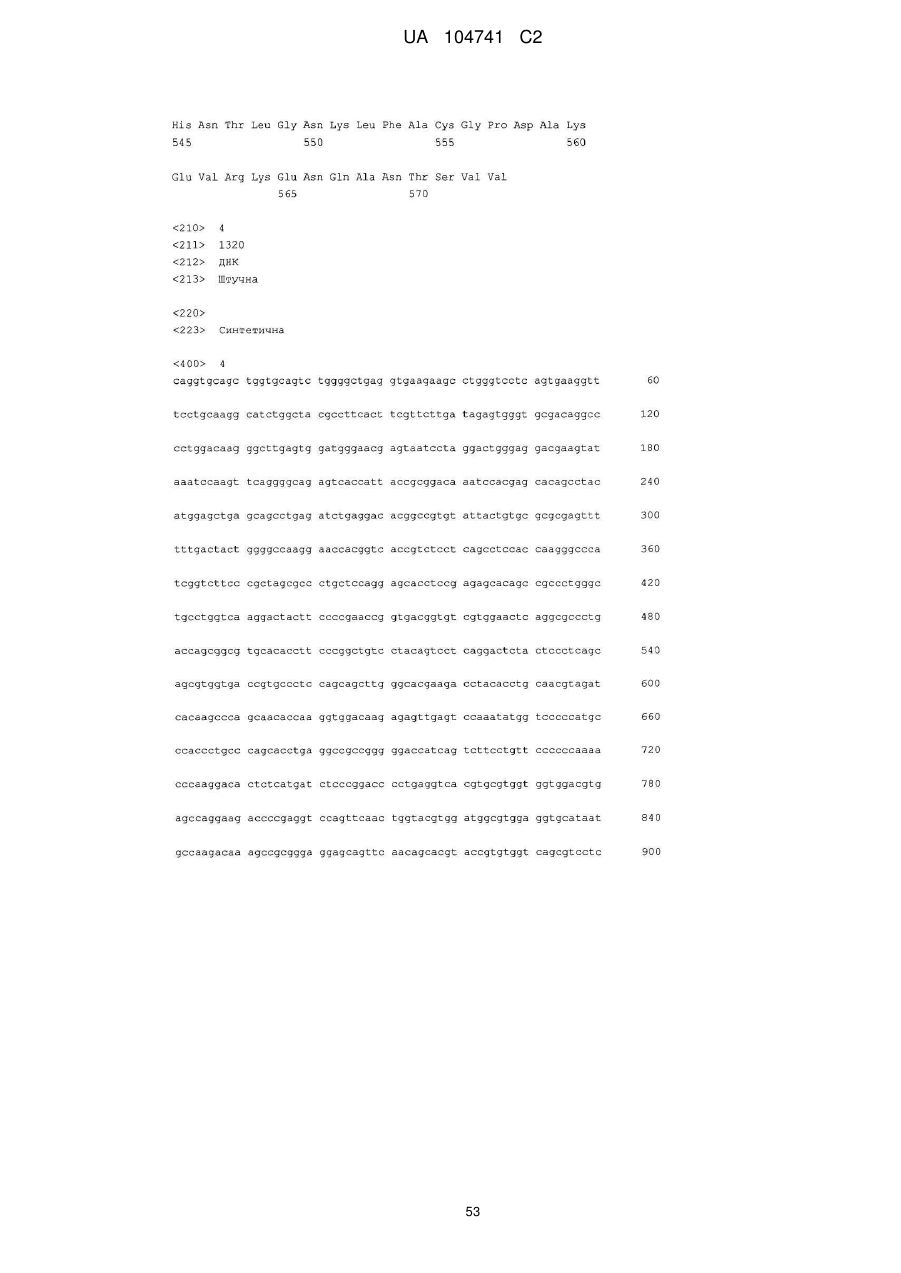
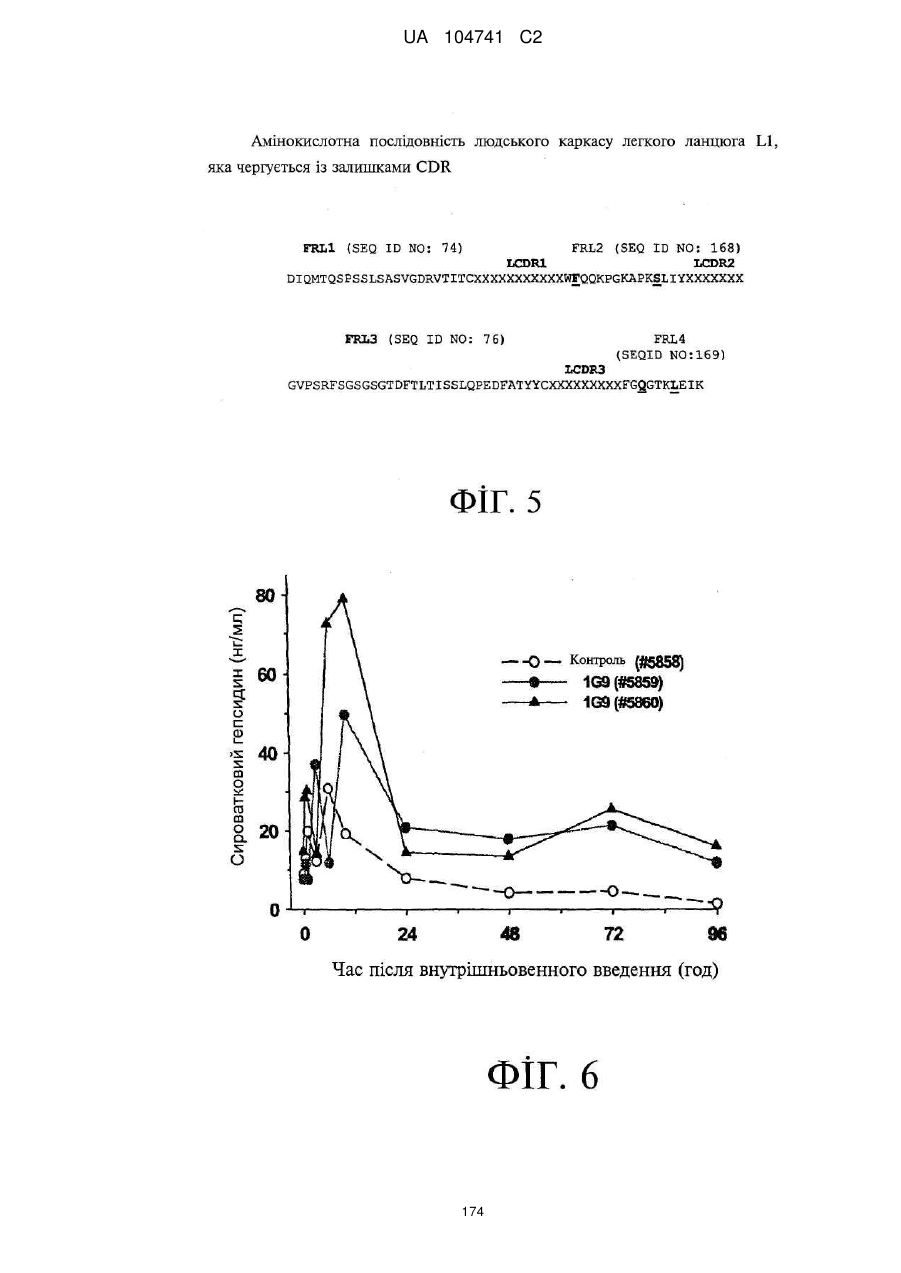
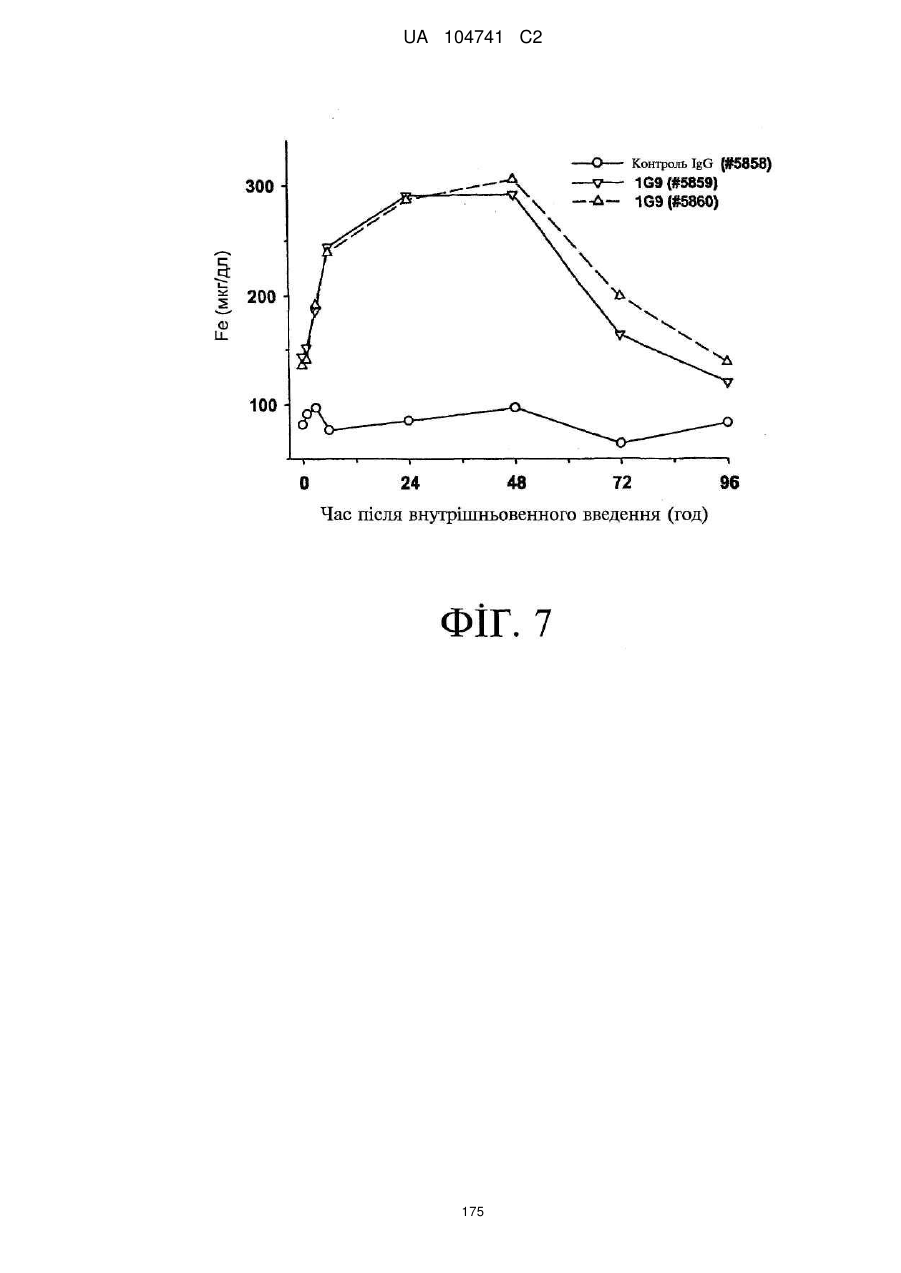
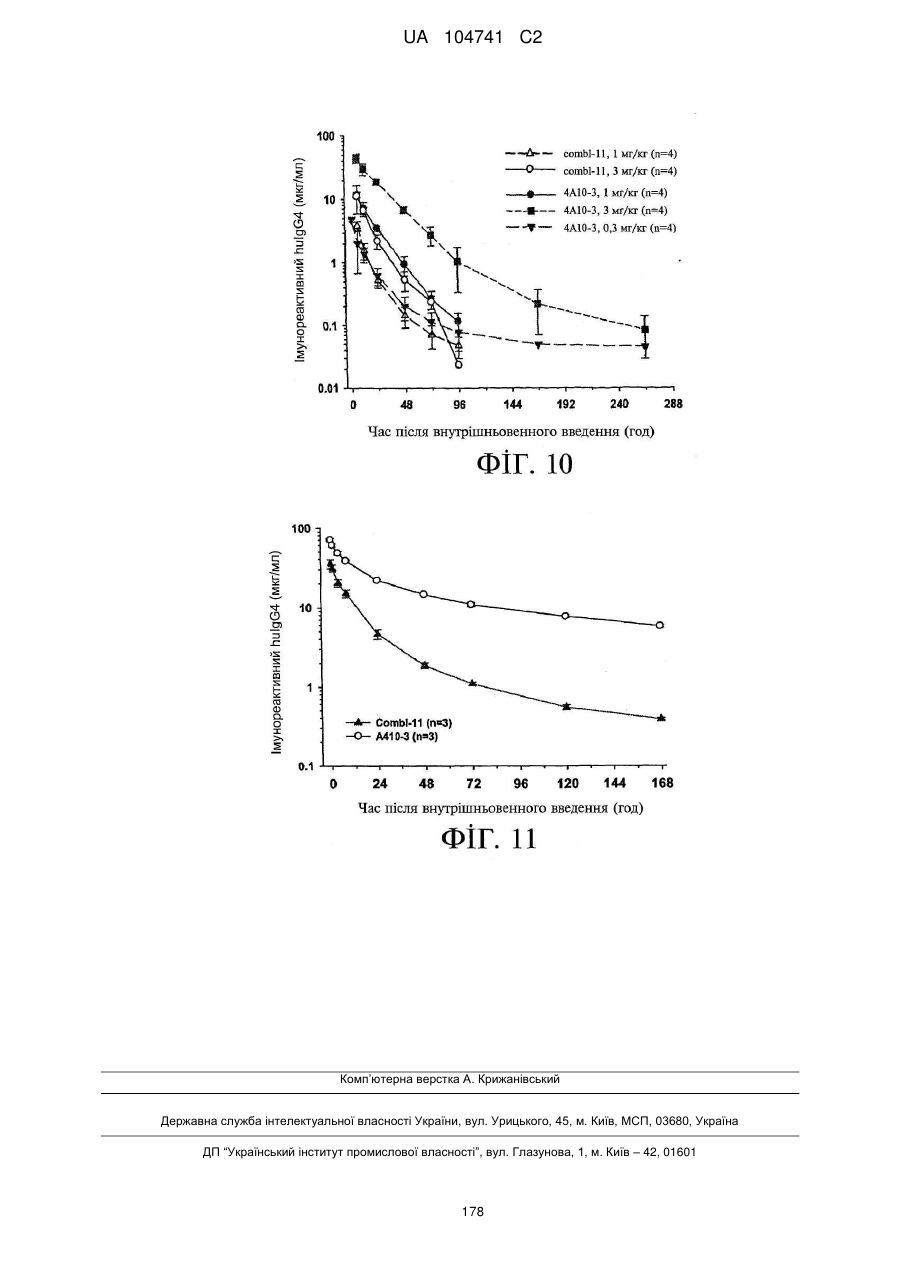
Реферат: Винахід стосується моноклональних антитіл або їх антигензв'язувальних фрагментів, які зв'язують людський феропортин 1 (FPN1) та пригнічують активність людського FPN1 і які є ефективними щодо підтримання або підвищення транспорту заліза з клітин ссавців та/або підтримання або підвищення рівня заліза у сироватці, кількості ретикулоцитів, кількості еритроцитів, рівня гемоглобіну та/або гематокриту у суб'єкта in vivo. UA 104741 C2 (12) UA 104741 C2 UA 104741 C2 5 10 15 20 25 30 35 40 45 50 55 60 Цей винахід стосується антитіл, які зв'язують феропортин 1 (FPN1), та їх застосування при лікуванні анемії. Залізо є найважливішим мікроелементом, необхідним для численних клітинних функцій. У ссавців постачання заліза до організму регулюється таким чином, щоб узгоджуватись із потребами організму у залізі на рівні адсорбції заліза ентероцитами дванадцятипалої кишки. Вважають, що транспорт заліза через базолатеральну мембрану ентероцита опосередковується феропортином 1 (відомим також як залізорегулювальний транспортер 1 (IREG-1), метал-транспортувальний білок 1 (МТР1) та SLC40A1), який у подальшому позначений як FPN1. Зараз відомо, що FPN1 є рецептором гепсидину, поліпептидного гормону, який продукується печінкою у відповідь на накопичення заліза та запалення. Зв'язування зрілого гепсидину з FPN1 призводить до інтерналізації та деградації FPN1, запобігання експорту заліза з клітин, і являє собою головний контролюючий фактор системного гомеостазу заліза. У патенті США № 7,166,448 розкриті, inte alia, нуклеотидні послідовності, які кодують людський білок FPN1, людський білок FPN1, який має залізотранспортувальну функцію, і кролячу поліклональну антисироватку, яку одержали проти пептиду, до складу якого входять 19 С-кінцевих амінокислот людського FPN1. Публікація міжнародної заявки на патент WO2009/094551 описує моноклональні антитіла (Mab) проти феропортину та способи їхнього застосування для лікування розладів гомеостазу заліза. Більш конкретно, WO2009/094551 описує моноклональні антитіла гризунів та повністю людські моноклональні антитіла до різних антигенних детермінант людського білка FPN1. Зважаючи на участь FPN1 у транспорті заліза та зв'язок мутацій FPN1 із захворюваннями, обумовленими порушенням гомеостазу заліза, існує потреба у терапевтично прийнятних антагоністах FPN1, які зв'язуються з високою спорідненістю з екстрацелюлярною антигенною детермінантою FPN1, а після зв'язування пригнічують опосередковану зрілим гепсидином інтерналізацію FPN1, підтримуючи або посилюючи тим самим експорт заліза з внутрішньоклітинних депо. Крім того, терапевтичне спрямування моноклонального антитіла (або його антигензв'язувального фрагмента) проти FPN1 з метою пригнічення зв'язування зрілого гепсидину з екстрацелюлярною антигенною детермінантою FPN1, повинно здійснюватись із достатньо високою точністю для того, щоб це антитіло не викликало значного порушення відтоку заліза з клітин та/або індукувало інтерналізацію у разі зв'язування зі своєю мішенню. Крім того, антитіла проти FPN, призначені для застосування у медицині, мають демонструвати достатні фармакокінетичні та фармакодинамічні характеристики, у тому числі, in vivo стабільність та/або період напіввиведення, які б уможливлювали їх терапевтичне застосування. Одне або декілька антитіл проти людського FPN1, розкрите(-і) у цьому описі, специфічно зв'язує(-ють) людський FPN1, у тому числі щонайменше один з його пептидних фрагментів, вибраний з групи, яку складають: a) 403SPFEDIRSRFIQGESITPTK422 (SEQ ID NO: 12); b) 406EDIRSRFIQGESIT419 (SEQ ID NO: 13); c) 409RSRFIQGESITPTK422 (SEQ ID NO: 14); d) 403SPFEDIRSRFIQG415 (SEQ ID NO: 15); e) 409RSRFIQGESIT419 (SEQ ID NO: 16); та і) 409RSRFIQG415 (SEQ ID NO: 95), блокує(-ють) зв'язування гепсидину із феропортином, активно пригнічує(-ють) активність гепсидину in vitro, підвищує(-ють) рівень заліза у сироватці дозозалежним чином in vivo та має(-ють) прийнятну розчинність, in vivo стабільність та характеристики періоду напіввиведення, які роблять його(їх) прийнятним(-и) засобом(-ами) для лікування та/або запобігання анемії у суб'єкта, який потребує такого лікування, шляхом внутрішньовенного вливання або навіть шляхом підшкірної ін'єкції. Таким чином, разом з іншими аспектами, цей винахід пропонує: Моноклональні антитіла або їхні антигензв'язувальні фрагменти, які специфічно зв'язуються з людським феропортином 1, до складу якого входить амінокислотна послідовність, представлена послідовністю SEQ ID NO: 1, на антигенній детермінанті, яка містить амінокислоти, локалізовані у складі однієї або декількох амінокислотних послідовностей, вибраних із групи, яку складають: a. 403SPFEDIRSRFIQGESITPTK422 (SEQ ID NO: 12); b. 406EDIRSRFIQGESIT419 (SEQID NO: 13); с. 409RSRFIQGESITPTK422 (SEQ ID NO: 14); d. 403SPFEDIRSRFIQG415 (SEQ ID NO: 15); e. 409RSRFIQGESIT419 (SEQ ID NO: 16); та f. 409RSRFIQG415 (SEQ ID NO: 95). 1 UA 104741 C2 5 10 15 20 25 30 35 40 45 50 55 У деяких варіантах здійснення цей винахід пропонує моноклональні антитіла або їхні антигензв'язувальні фрагменти, які містять LCDR1, LCDR2, LCDR3, HCDR1, HCDR2 та HCDR3, що містять амінокислотну послідовність, представлену послідовностями SEQ ID NO: 37, 129, 22, 107, 118 та 120, відповідно, і моноклональне антитіло або його антигензв'язувальний фрагмент, що зв'язує людський FPN 1, який містить амінокислотну послідовність, представлену послідовністю SEQ ID NO: 1, на антигенній детермінанті, яка містить амінокислоту або амінокислоти, локалізовані у складі амінокислотної послідовності, представленої послідовністю SEQ ID NO: 12, з KD приблизно 100 нМ або менше, при визначенні поверхневим плазмонним резонансом (SPR), за варіантом, якому віддають перевагу, при температурі 25 °C для моноклональних антитіл і температурі 37 °C для антигензв'язувальних фрагментів. У деяких варіантах здійснення цього винаходу моноклональне антитіло або його антигензв'язувальний фрагмент містить шість гіперваріабельних ділянок (CDR), вибраних із групи, яку складають: (і) LCDR1, LCDR2, LCDR3, HCDR1, HCDR2 та HCDR3, які містять амінокислотні послідовності, представлені послідовностями SEQ ID NO: 20, 32, 33, 30, 31 та 19, відповідно; (іі) LCDR1, LCDR2, LCDR3, HCDR1, HCDR2 та HCDR3, які містять амінокислотні послідовності, представлені послідовностями SEQ ID NO: 42, 32, 33, ЗО, 43 та 19, відповідно; (ііі) LCDR1, LCDR2, LCDR3, HCDR1, HCDR2 та HCDR3, які містять амінокислотні послідовності, представлені послідовностями SEQ ID NO: 42, 27, 22, 23, 41 та 19, відповідно; (iv) LCDR1, LCDR2, LCDR3, HCDR1, HCDR2 та HCDR3, які містять амінокислотні послідовності, представлені послідовностями SEQ ID NO: 42, 32, 33, 23, 41 та 19, відповідно; (v) LCDR1, LCDR2, LCDR3, HCDR1, HCDR2 та HCDR3, які містять амінокислотні послідовності, представлені послідовностями SEQ ID NO: 20, 21, 22, 17, 18 та 19, відповідно; (vi) LCDR1, LCDR2, LCDR3, HCDR1, HCDR2 та HCDR3, які містять амінокислотні послідовності, представлені послідовностями SEQ ID NO: 20, 27, 29, 23, 24 та 19, відповідно; (vii) LCDR1, LCDR2, LCDR3, HCDR1, HCDR2 та HCDR3, які містять амінокислотні послідовності, представлені послідовностями SEQ ID NO: 37, 27, 22, 23, 41 та 19, відповідно; (viii) LCDR1, LCDR2, LCDR3, HCDR1, HCDR2 та HCDR3, які містять амінокислотні послідовності, представлені послідовностями SEQ ID NO: 170, 171, 172, 182, 173 та 19, відповідно; (іх) LCDR1, LCDR2, LCDR3, HCDR1, HCDR2 та HCDR3, які містять амінокислотні послідовності, представлені послідовностями SEQ ID NO: 37, 127, 22, 23, 116 та 19, відповідно; (х) LCDR1, LCDR2, LCDR3, HCDR1, HCDR2 та HCDR3, які містять амінокислотні послідовності, представлені послідовностями SEQ ID NO: 37, 125, 22, 23, 110 та 19, відповідно; (хі) LCDR1, LCDR2, LCDR3, HCDR1, HCDR2 та HCDR3, які містять амінокислотні послідовності, представлені послідовностями SEQ ID NO: 37, 122, 22, 23, ПО та 19, відповідно; (хіі) LCDR1, LCDR2, LCDR3, HCDR1, HCDR2 та HCDR3, які містять амінокислотні послідовності, представлені послідовностями SEQ ID NO: 37, 129, 22, 107, 118 та 120, відповідно; (xiii) LCDR1, LCDR2, LCDR3, HCDR1, HCDR2 та HCDR3, які містять амінокислотні послідовності, представлені послідовностями SEQ ID NO: 37, 128, 22, 105, 41 та 119, відповідно; (xiv) LCDR1, LCDR2, LCDR3, HCDR1, HCDR2 та HCDR3, які містять амінокислотні послідовності, представлені послідовностями SEQ ID NO: 37, 174, 22, 175, 176 та 120, відповідно; (xvi) LCDR1, LCDR2, LCDR3, HCDR1, HCDR2 та HCDR3, які містять амінокислотні послідовності, представлені послідовностями SEQ ID NO: 37, 128, 22, 105, 117 та 19, відповідно; і (xvii) LCDR1, LCDR2, LCDR3, HCDR1, HCDR2 та HCDR3, які містять амінокислотні послідовності, представлені послідовностями SEQ ID NO: 37, 177, 22, 23, 112 та 19, відповідно, і зв'язує людський FPN1, який містить амінокислотну послідовність, представлену послідовністю SEQ ID NO: 1, на антигенній детермінанті, яка по суті складається або містить амінокислоту або амінокислоти, локалізовані у складі амінокислотної послідовності, вибраної з групи, яку складають: a) 403SPFEDIRSRFIQGESITPTK422 (SEQ ID NO: 12); b) 406EDIRSRFIQGESIT419 (SEQ ID NO: 13); c) 409RSRFIQGESITPTK422 (SEQ ID NO: 14); d) 403SPFEDIRSRFIQG415 (SEQ ID NO: 15); e) 409RSRFIQGESIT419 (SEQ ID NO: 16); та f) 409RSRFIQG415 (SEQ ID NO: 95), 2 UA 104741 C2 5 10 15 20 25 30 35 40 45 50 55 60 з KD, меншою ніж приблизно 100 нМ, при визначенні засобами SPR, за варіантом, якому віддається перевага, при температурі 25 °C для моноклональних антитіл і температурі 37 °C для антигензв'язувальних фрагментів. У конкретних варіантах здійснення моноклональні антитіла або їхні антигензв'язувальні фрагменти за цим винаходом пригнічують індуковану гепсидином інтерналізацію та/або деградацію людського FPN1, таким чином підтримуючи або підвищуючи: 1) транспорт заліза з клітин, 2) рівень заліза у сироватці, 3) кількість ретикулоцитів, 4) кількість еритроцитів, 5) рівень гемоглобіну та/або 6) гематокрит у суб'єкта, за варіантом, якому віддається перевага, людини, на щонайменше приблизно 10% у порівнянні з відповідними показниками у згаданого суб'єкта за відсутності згаданого моноклонального антитіла або його антигензв'язувального фрагмента. За іншим аспектом запропоновані полінуклеотиди, які містять нуклеотидну послідовність, яка кодує моноклональні антитіла або їхні антигензв'язувальні фрагменти за цим винаходом проти людського FPN1. За іншим аспектом запропоновані фармацевтичні композиції, які містять будь-яке з моноклональних антитіл або його антигензв'язувальні фрагменти, розкриті у цьому описі, та фармацевтично прийнятний носій, розріджувач або наповнювач. Запропоновані також 1) застосування моноклональних антитіл або їхніх антигензв'язувальних фрагментів, розкритих у цьому описі, у терапії, за варіантом, якому віддається перевага, у терапії для лікування або запобігання анемії, 2) застосування моноклональних антитіл або їхніх антигензв'язувальних фрагментів, розкритих у цьому описі, у комбінованій терапії, за варіантом, якому віддається перевага, у комбінованій терапії для лікування або запобігання анемії, 3) застосування моноклональних антитіл або їхніх антигензв'язувальних фрагментів, розкритих у цьому описі, для лікування або запобігання анемії, підтримання або підвищення рівня заліза у сироватці, кількості ретикулоцитів, кількості еритроцитів, рівня гемоглобіну та/або гематокриту у суб'єкта, за варіантом, якому віддається перевага, у людини, 4) застосування моноклональних антитіл або їхніх антигензв'язувальних фрагментів, розкритих у цьому описі, для виготовлення лікарського засобу для лікування або запобігання анемії, підтримання або підвищення рівня заліза у сироватці, кількості ретикулоцитів, кількості еритроцитів, рівня гемоглобіну та/або гематокриту у суб'єкта, за варіантом, якому віддається перевага, у людини, та 5) застосування моноклональних антитіл або їхніх антигензв'язувальних фрагментів, розкритих у цьому описі, для виготовлення лікарського засобу для застосування у комбінованій терапії для лікування або запобігання анемії, підвищення рівня заліза у сироватці, кількості ретикулоцитів, кількості еритроцитів, рівня гемоглобіну та/або гематокриту у людини, причому згаданий лікарський засіб має застосовуватись у комбінації з одним або декількома еритропоезстимулювальними агентами (ESA) або іншим терапевтичним агентом або терапевтичним лікуванням, яке традиційно застосовують для лікування анемії, підтримання або підвищення рівня заліза у сироватці, кількості ретикулоцитів, кількості еритроцитів, рівня гемоглобіну та/або гематокриту у людини. За ще одним аспектом запропоновані способи 1) підтримання або підвищення рівня заліза у сироватці, кількості ретикулоцитів, кількості еритроцитів, рівня гемоглобіну та/або гематокриту у суб'єкта, за варіантом, якому віддається перевага, у людини, які включають введення в організм суб'єкта, який цього потребує, ефективної кількості моноклонального антитіла або його антигензв'язувального фрагмента, розкритого у цьому описі, 2) лікування або запобігання анемії, у тому числі, але без обмеження, анемії хронічних захворювань, ракової анемії та запальної анемії, які включають введення в організм суб'єкта, за варіантом, якому віддається перевага, в організм людини, яка цього потребує, ефективної кількості моноклонального антитіла або його антигензв'язувального фрагмента, розкритого у цьому описі, 3) спосіб лікування або запобігання анемії, у тому числі, але без обмеження, анемії хронічних захворювань, ракової анемії та запальної анемії, який включає введення в організм суб'єкта, за варіантом, якому віддається перевага, в організм людини, яка цього потребує, ефективної кількості комбінації моноклональних антитіл або їхніх антигензв'язувальних фрагментів, розкритих у цьому описі, або суміші щонайменше одного моноклонального антитіла і щонайменше одного його антигензв'язувального фрагмента, розкритих у цьому описі, та 4) будь-який з вищезгаданих способів 1-3, що додатково включає введення в організм згаданої людини ESA або іншого терапевтичного агента чи здійснення терапевтичного лікування, що вводиться (здійснюється) для підтримання або підвищення рівня заліза у сироватці, кількості ретикулоцитів, кількості еритроцитів, рівня гемоглобіну та/або гематокриту у людини. За ще одним аспектом запропоновані способи пригнічення індукованої зрілим гепсидином інтерналізації та деградації FPN1, які включають введення в контакт згаданого FPN1 та 3 UA 104741 C2 5 10 15 20 25 30 35 40 45 50 55 60 ефективної кількості щонайменше одного моноклонального антитіла або його антигензв'язувального фрагмента, розкритого у цьому описі. Запропонований також спосіб зниження зв'язування зрілого людського гепсидину з людським FPN1, який включає введення в контакт згаданого людського FPN1 та ефективної кількості щонайменше одного моноклонального антитіла та/або його антигензв'язувального фрагмента, розкритого у цьому описі. Запропонований також спосіб зменшення кількості білка FPN1, що інтерналізується клітиною, яка експресує білок FPN1, який включає введення в організм людини, яка цього потребує, ефективної кількості щонайменше одного з моноклональних антитіл та/або його антигензв'язувального фрагмента, розкритих у цьому описі. Фіг. 1 відображає послідовності різних пептидів, які містять фрагменти імуногену, який був застосований для одержання антитіл проти FPN1, і результати експериментів зі зв'язування пептиду-антитіла із застосуванням згаданих пептидів для визначення антигенної детермінанти Mab 34A9 проти FPN1. Підкреслені амінокислоти означають фактичні послідовності феропортину. Mab 34A9 зв'язується з пептидами FpnE3a, 060719Z, 0708L4C та 0708L4D, усі з яких містять спільну амінокислотну послідовність RSRFIQG (послідовність SEQ ID NO: 95). Фіг. 2А показує амінокислотні послідовності повністю людської каркасної ділянки 02 легкого ланцюга, які чергуються з CDR. Чотири каркасні ділянки позначені як FRL1, 2, 3 та 4 (послідовності SEQ ID NO: 74, 75, 76 та 77, відповідно). Фіг. 2В показує амінокислотні послідовності людської каркасної ділянки VH1-69 важкого ланцюга, які чергуються з CDR. Чотири каркасні ділянки позначені як FRH1-4 (послідовності SEQ ID NO: 78-81, відповідно). Фіг. 3А показує амінокислотні послідовності людської каркасної ділянки 018 легкого ланцюга, які чергуються з CDR. Чотири каркасні ділянки позначені як FRL1, 2, 3 та 4 (послідовності SEQ ID NO: 74, 75, 82 та 77, відповідно). Залишки, які відрізняються від залишків 02, виділені жирним шрифтом та підкреслені. Фіг. 3В показує амінокислотні послідовності людської каркасної ділянки VH1-18 важкого ланцюга, які чергуються з CDR. Чотири каркасні ділянки позначені як FRH1, 2, 3 та 4 (послідовності SEQ ID NO: 83, 79, 84 та 81, відповідно). Залишки, які відрізняються від залишків VH1-69, виділені жирним шрифтом та підкреслені. Фіг. 4А показує амінокислотні послідовності людської каркасної ділянки L12 легкого ланцюга, які чергуються з CDR. Чотири каркасні ділянки позначені як FRL1, 2, 3 та 4 (послідовності SEQ ID NO: 85, 75, 86 та 77, відповідно). Залишки, які відрізняються від залишків 02, виділені жирним шрифтом та підкреслені. Фіг. 4В показує амінокислотні послідовності людської каркасної ділянки VH1-46 важкого ланцюга, які чергуються з CDR. Чотири каркасні ділянки позначені як FRH1, 2, 3 та 4 (послідовності SEQ ID NO: 83, 79, 87 та 81, відповідно). Залишки, які відрізняються від залишків VH1-69, виділені жирним шрифтом та підкреслені. Фіг. 5 показує амінокислотні послідовності людської каркасної ділянки L1 легкого ланцюга, які чергуються з CDR. Чотири каркасні ділянки позначені як FRL1, 2, 3 та 4 (послідовності SEQ ID NO: 74, 168, 76 та 169, відповідно). Залишки, які відрізняються від залишків 02, виділені жирним шрифтом та підкреслені. Зародкова послідовність ділянки FR1 людської каркасної ділянки L12 легкого ланцюга відповідає послідовності, представленій послідовністю SEQ ID NO: 85; за деякими прикладами здійснення цього винаходу передбачається варіант, в якому амінокислотна послідовність ділянки FR1 людської каркасної ділянки L1 легкого ланцюга відповідає послідовності, представленій послідовністю SEQ ID NO: 74. Фіг. 6 показує графік рівня гепсидину у сироватці самців макак-крабоїдів після введення контрольного мишачого IgGl або мишачого Mab 1G9 однією внутрішньовенною дозою (30 мг/кг). Наведені дані від окремих тварин. Фіг. 7 показує графік рівня заліза у сироватці самців макак-крабоїдів після введення контрольного мишачого IgGl або мишачого Mab 1G9 однією внутрішньовенною дозою (30 мг/кг). Наведені дані від окремих тварин. Фіг. 8 показує амінокислотні послідовності та консенсусну амінокислотну послідовність варіабельних ділянок важкого ланцюга антитіл та їхніх антигензв'язувальних фрагментів за цим винаходом, яким віддається перевага. Крапка (.) вказує, що амінокислота у цьому положенні є ідентичною відповідній амінокислоті послідовності № 1. CDR послідовності № 1 підкреслені та виділені жирним шрифтом. Фіг. 9 показує амінокислотні послідовності та консенсусну амінокислотну послідовність варіабельних ділянок легкого ланцюга антитіл та їхніх антигензв'язувальних фрагментів за цим винаходом, яким віддається перевага. Крапка (.) вказує, що амінокислота у цьому положенні є 4 UA 104741 C2 5 10 15 20 25 30 35 40 45 50 55 60 ідентичною відповідній амінокислоті послідовності № 1. CDR послідовності № 1 підкреслені та виділені жирним шрифтом. Фіг. 10 відображає концентрації Mab 4A10-3 та Mab Combill у сироватці макак-крабоїдів після однієї внутрішньовенної ударної дози (0,3 мг/кг, 1,0 мг/кг або 3,0 мг/кг). Концентрації Mab Combill у сироватці для дози 0,3 мг/кг знаходились нижче межі визначення цього аналізу (
ДивитисяДодаткова інформація
Назва патенту англійськоюAnti-ferroportin 1 monoclonal antibodies and uses thereof
Автори англійськоюLeung, Donmienne, Doen, Mun, Luan, Peng, Manetta, Joseph Vincent, Tang, Ying, Witcher, Derrick, Ryan
Автори російськоюТань Инь, Уитчер Деррик Райан
МПК / Мітки
МПК: C07K 16/28, A61P 7/06, A61K 39/395
Мітки: моноклональні, антитіла, варіанти, застосування, феропортину
Код посилання
<a href="https://ua.patents.su/180-104741-monoklonalni-antitila-proti-feroportinu-1-ta-varianti-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Моноклональні антитіла проти феропортину 1 та варіанти їх застосування</a>
Попередній патент: Контейнер з відкидною кришкою
Наступний патент: Похідні арилциклопропілацетаміду, застосовні як активатори глюкокінази
Випадковий патент: Спосіб визначення струму однофазного замикання на землю в мережі з ізольованою нейтраллю