Застосування похідних бензоімідазолу-проліну
Номер патенту: 116053
Опубліковано: 25.01.2018
Автори: Хейдманн Бібія, Штайнер Мішель, Вілльямс Джоді Т., Сіфферлен Тьєрі, Рох Катерін, Бротші Христина, Єнк Франсуа, Босс Крістоф, Гуде Маркус
Формула / Реферат
1. Застосування сполуки формули (І)
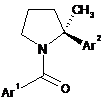 Формула (І)
Формула (І)
або її фармацевтично прийнятної солі
для приготування лікарського засобу для попередження або лікування вечірньої сплутаності;
де сполука формули (І) знаходиться у абсолютній конфігурації (S);
Аr1 являє собою
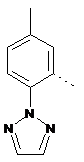 ,
,  або
або  ;
;
та Аr2 являє собою
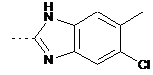 ,
, 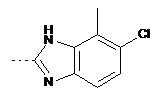 ,
,  ,
, 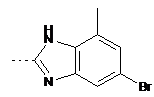 ,
, 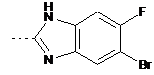 ,
, 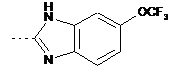 ,
, 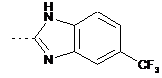 ,
, 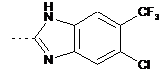 aбо
aбо  .
.
2. Застосування за п. 1, у якому сполука являє собою:
[(S)-2-(5-хлор-4-метил-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метил-2-піримідин-2-ілфеніл)-метанон;
[(S)-2-(5-бром-7-метил-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метил-2-[1,2,3]триазол-2-ілфеніл)-метанон;
[(S)-2-(5-бром-7-метил-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метил-2-піримідин-2-ілфеніл)-метанон;
[(S)-2-(5-хлор-4-метил-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метокси-2-[1,2,3]триазол-2-ілфеніл)-метанон;
[(S)-2-(6-бром-5-фтор-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метил-2-[1,2,3]триазол-2-ілфеніл)-метанон;
[(S)-2-(5,6-диметокси-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метил-2-[1,2,3]триазол-2-ілфеніл)-метанон;
[(S)-2-(5,6-диметокси-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метил-2-піразол-1-ілфеніл)-метанон;
[(S)-2-(5,6-диметокси-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метокси-2-[1,2,3]триазол-2-ілфеніл)-метанон;
[(S)-2-(6-хлор-5-трифторметил-1H-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метил-2-[1,2,3]триазол-2-ілфеніл)-метанон;
(5-метил-2-[1,2,3]триазол-2-ілфеніл)-[(S)-2-метил-2-(5-трифторметил-1Н-бензоімідазол-2-іл)-піролідин-1-іл]-метанон або
(5-метил-2-[1,2,3]триазол-2-ілфеніл)-[(S)-2-метил-2-(5-трифторметокси-1Н-бензоімідазол-2-іл)-піролідин-1-іл]-метанон,
або його фармацевтично прийнятну сіль.
3. Застосування за п. 1, у якому сполука являє собою:
[(S)-2-(5-бром-7-метил-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метил-2-піримідин-2-ілфеніл)-метанон або його фармацевтично прийнятну сіль.
4. Застосування за п. 1, у якому сполука являє собою:
[(S)-2-(5-хлор-4-метил-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метокси-2-[1,2,3]триазол-2-ілфеніл)-метанон або його фармацевтично прийнятну сіль.
5. Застосування за будь-яким з пп. 1-4, у якому лікарський засіб призначений для попередження або лікування вечірньої сплутаності у пацієнта, який має деменцію типу Альцгеймера.
6. Застосування за п. 5, у якому пацієнт має помірну стадію деменції Альцгеймера.
7. Застосування за будь-яким з пп. 1-6, у якому вечірня сплутаність являє собою післяобідню вечірню сплутаність.
8. Застосування за будь-яким з пп. 1-7, у якому лікують підвищене збудження.
Текст
Реферат: Даний винахід стосується сполук формули (І) CH3 Ar Ar 1 O 2 , Формула (І) UA 116053 C2 (12) UA 116053 C2 1 2 де Аr та Аr приймають значення, як зазначено у описі, та їх застосування як лікарських засобів для лікування вечірньої сплутаності. Винахід також стосується приготування таких сполук та їх фармацевтично прийнятних солей. UA 116053 C2 5 10 15 20 25 30 35 40 45 50 55 Даний винахід відноситься до нових похідних бензімідазол-проліну формули (I) та до їх застосування як лікарські засоби для лікування вечірньої сплутаності. Винахід також охоплює споріднені аспекти, включаючи способи одержання сполук та фармацевтичних композицій, що містять одну або декілька сполук формули (I). Вечірня сплутаність являє собою добовий синдром другої половини дня підвищення дезорієнтації та неспокою, як правило, у пацієнтів з деяким ступенем деменції. Кардинальні клінічні ознаки включають підвищене збудження, загальну сплутаність та перепади настрою, які типово розвиваються, коли природне освітлення починає зменшуватися. Цей поведінковий розлад, який погіршується у кінці дня або на початку вечора серед пацієнтів з деменцією або госпіталізованих пацієнтів похилого віку, було описано у медичній літературі впродовж більше 60 років (Bachman & Rabins, Annu. Rev. Med. 2006. 57:499–511). Терміни, використовувані для опису цього феномену, включають вечірню сплутаність, післяобідню вечірню сплутаність, синдром сплутаності вечором або синдром вечірньої сплутаності. На відміну від делірію, який звичайно має гострий початок та коливання впродовж дня, вечірня сплутаність визначається тимчасовою картиною (початок та закінчення до кінця другої половини дня). Вважають, що вечірня сплутаність більш часто проявляється при помірних стадіях деменції Альцгеймера. Пацієнти у цілому здатні розуміти, що характер їх поведінки ненормальний. Вважають, що вечірня сплутаність послаблюється при прогресуванні деменції у пацієнтів. Приблизно половина деменцій (44 %) є альцгеймерівського типу, включаючи деменцію Альцгеймера (пресенільна деменція або сенільна деменція), підкоркову деменцію, деменцію дифузних тілець Леві та лобно-скроневу деменцію. Приблизно у 20–45 % пацієнтів типу Альцгеймера будуть відчувати у деякому ступені неспокій вечором. Інші 47 % деменцій є судинного типу, включаючи судинну деменцію, мультиінфарктну деменцію, деменцію Бінсвангера, деменцію боксерів та артеріосклеротичну деменцію. Решта типів деменції (9 %) має інші етіології, такі як паралітична деменція, індукована речовиною персистуюча деменція, діалізна деменція, гідроцефалічна деменція, пухлини, субдуральна гематома, нормотензивна гідроцефалія, васкуліт, гіповітаміноз, або ендокринне та метаболічне захворювання. Можлива етіологія вечірньої сплутаності включає конкретні гістопатологічні ознаки дегенерації, які описані у вентролатеральній преоптичній області (VLPO) та супрахіазмальному ядрі (SCN) при деменції. SCN пейсмекер значно уражений при хворобі Альцгеймера, у той час як шишковидний по суті не уражений (Swaab DF, Fliers E, Partiman TS. "The suprachiasmatic nucleus of the human brain in relation to sex, age and senile dementia". Brain Res 1985; 342: 37–44; Zhou JN, Hofman MA, Swaab DF. "VIP neurons in the human SCN in relation to sex, age, and Alzheimer's disease". Neurobiol Aging 1995; 16: 571–576; Swaab DF, Grundke-Iqbal I, Iqbal Ket al. "Tau and ubiquitin in the human hypothalamus in aging and Alzheimer's disease". Brain Res 1992; 590: 239–249; Stopa EG, Volicer L, Kuo-Leblanc Vet al. "Pathologic evaluation of the human suprachiasmatic nucleus in severe dementia". J Neuropathol Exp Neurol 1999; 58: 29–39). SCN зв'язаний з регулюванням фаз неспання та сну шляхом підтримання добових ритмів. Ці ритми синхронізуються із зовнішніми сигналами світло-темрява та залучають комплекс нейробіологічної регуляції у головному мозку. Гістопатологічні ознаки старечих ушкоджень у циркадних осциляторах у головному мозку, таких як SCN, спостерігаються у ссавців декількох видів. Найбільш широко призначуване фармакологічне лікування вечірньої сплутаності - атипові нейролептики – мають помірні, але достовірні сприятливі ефекти при короткостроковому лікуванні (впродовж 6–12 тижнів) агресії, менш відчутне на симптоми збудження, та мають обмежені переваги при більш тривалій терапії. Проблеми зростають відносно можливих важких побічних ефектів при такому лікуванні, включаючи інсульт та смерть (Ballard та ін., Nat. Rev. Neurol. 5, 245–255, 2009). Були опубліковані раніше проведені клінічні дослідження та була описана медична технологія з протоколами для оцінки ефективності лікарських засобів у пацієнтів з вечірньою сплутаністю; огляд клінічних випробувань та методології при збудженні та агресії при деменції можна знайти у Ballard та ін., Nat. Rev. Neurol. 5, 245–255, 2009 (див., особливо таблицю 1). Опублікованими роботами є, наприклад: a) Cohen-Mansfield J, Garfinkel D, Lipson S. Melatonin for treatment of sundowning in elderly persons with dementia – a preliminary study. Arch Gerontol Geriatr 2000; 31: 65–76. b) Brusco LI, Marquez M, Cardinali DP. Melatonin treatment stabilizes chronobiologic and cognitive symptoms in Alzheimer's disease. Neuroendocrinol Lett 2000; 21: 39–42. 1 UA 116053 C2 5 10 15 20 25 30 35 40 45 50 55 60 c) de Jonghe A, Korevaar JC, van Munster BC, de Rooij SE. Effectiveness of melatonin treatment on circadian rhythm disturbances in dementia. Are there implications for delirium? A systematic review. Int J Geriatr Psychiatry. 2010 Dec; 25(12):1201-8. d) Falsetti AE. Risperidone for control of agitation in dementia patients. Am J Health Syst Pharm. 2000 May 1;57(9):862-70. Були описані частинні ефективності мелатоніну або впливу яскравого світла для зниження поведінкових симптомів при вечірній сплутаності. Погоджений режим сну та розпорядок дня також можуть знижувати замішання та агресію. Рекомендується зменшення денної тихої години, тому що ненавмисне бажання поспати занадто багато, буде негативно впливати на нічний сон. Рекомендується зменшення вживання кофеїну у пацієнтів з вечернею сплутаністю. Нейронна аферентація та еферентація з'єднує гіпоталамічні орексинові нейрони з областями головного мозку, задіяні у регуляцію добового ритму (отримуючи сигнали день-ніч) та у коркову активацію (індукуючи та підтримуючи активність); орексинові нейрони також отримують аферентні фізіологічні та емоційні вхідні сигнали лімбічного та метаболічного походження. Таким чином, активовані орексинові нейрони регулюють готовність до адаптації організму до вимог навколишнього середовища та добових вимог та до точної підтримки гомеостазу (Saper та ін., Nature 437: 1257, 2005). Вентролатеральна преоптична область (VLPO) та супрахіазмальне ядро (SCN) є важливими годинними ділянками головного мозку, які проявляють основне інгібування на активність орексинових нейронів під час нічної фази. Існує гіпотеза, що аномально гіперактивні орексинові нейрони значно впливають на перезбудження кори головного мозку, що опосередковує гіперактивність у цей момент часу у добовому циклі. Патологічна орексинова гіперактивність може розвиватися внаслідок недостатнього інгібування вхідних сигналів з VLPO та SCN, які повинні починати поступово встановлюватися наприкінці дня. Введення кофеїну підвищує рівні орексину у головному мозку щурів. Кофеїн можна використовувати як засоби для експериментальної стимуляції недостатнього інгібування VLPOSCN вхідних сигналів на гіпоталамічні орексинові нейрони. Фармакологічна дія кофеїну, антагоністу рецептору аденозину A1 та A2A, полягає у блокуванні аденозинергічного інгібування, що роблять аденозинергічні нейрони на орексинові нейрони. Антагоністи орексинового рецептору у відповідності з даним винаходом можуть усувати збудження наприкінці дня, що стимулюється у тварин шляхом післяобіднього введення кофеїну. Електроенцефалографічні записи підтверджують поведінкові симптоми збудження, які зменшуються двома розкритими у заявці сполуками при введенні перорально щурам та/ або собакам. Короткий опис фігур: На фігурі 1 показаний вплив сполуки з прикладу 7 на моделі збудження, індукованого кофеїном, у щурів. На фігурі 2 показаний вплив сполуки з прикладу 11 на моделі збудження, індукованого кофеїном, у щурів. На фігурі 3 показаний вплив сполуки з прикладу 7 на моделі збудження, індукованого кофеїном, у собак. Антагоністи орексинового рецептору, що містять 2-заміщені насичені циклічні амідні похідні (такі як 2-заміщені піролідин-1-карбоксаміди) відомі, наприклад, з WO2008/020405, WO2008/038251, WO2008/081399, WO2008/087611, WO2008/117241, WO2008/139416, WO2009/004584, WO2009/016560, WO2009/016564, WO2009/040730, WO2009/104155, WO2010/004507, WO2010/038200, WO2001/096302, WO2002/044172, WO2002/089800, WO2002/090355, WO2003/002559, WO2003/032991, WO2003/041711, WO2003/051368, WO2003/051873, WO2004/026866, WO2004/041791, WO2004/041807, WO2004/041816, WO2009/003993, WO2009/003997, WO2009/124956, WO2010/060470, WO2010/060471, WO2010/060472, WO2010/063662, WO2010/063663, WO2010/072722, WO2010/122151, та WO2008/150364. Переважна піролідинова похідна сполука розкрита у Langmead та ін., Brit. J. Pharmacol. 2004, 141, 340-346 як високо селективна до орексину-1. У WO2003/002561 описані певні похідні N-ароїл циклічного аміну, що охоплюють похідні бензімідазол-2-іл-метилзаміщеного піролідину, як антагоністи орексинового рецептору. У WO2003/002561 не згадується вечірня сплутаність. Незважаючи на велику кількість описаних у рівні техніки сполук антагоністів орексинового рецептору та їх високу структурну різноманітність, усі сполуки мають загальну загальноприйняту характерну структурну особливість, тобто у положенні 2 насиченого циклічного аміду лінкерна група, така як щонайменше метиленова група (або більш довгі групи, такі як -CH2-NH-CO-, -CH2-NH-, -CH2-O-, -CH2-S-, та ін.) зв'язують циклічний амід з відповідним замісником ароматичної кільцевої системи. Наразі неочікувано було виявлено, що, незважаючи 2 UA 116053 C2 5 на значні конформаційні зміни, які можна очікувати від видалення лінкеру між двома ригідними структурними елементами, сполуки у відповідності з даним винаходом, які мають бензімідазольне кільце, приєднане безпосередньо до піролідинового аміду у положенні 2, є ефективними антагоністами орексинового рецептору. Зараз даний винахід забезпечує певні похідні бензімідазол-проліну, які є ефективними непептидними антагоністами орексинових рецепторів людини для застосування для попередження або лікування вечірньої сплутаності. 1) Перший аспект винаходу відноситься до сполук формули (I): Формула (I) 10 для застосування для попередження або лікування вечірньої сплутаності; де сполуки формули (I) знаходяться у абсолютній конфігурації (S); 1 Ar являє собою 15 , або , ; 2 та Ar являє собою 20 , , , 25 30 35 40 , , , або , , . 2) Другий варіант здійснення винаходу відноситься до сполук формули (I) у відповідності з варіантом здійснення 1) для застосування у відповідності з варіантом здійснення 1), де сполука являє собою: [(S)-2-(5-Хлор-4-метил-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метил-2-піримідин2-іл-феніл)-метанон; [(S)-2-(5-Бром-7-метил-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метил-2[1,2,3]триазол-2-іл-феніл)-метанон; [(S)-2-(5-Бром-7-метил-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метил-2-піримідин2-іл-феніл)-метанон; [(S)-2-(5-Хлор-4-метил-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метокси-2[1,2,3]триазол-2-іл-феніл)-метанон; [(S)-2-(6-Бром-5-фтор-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метил-2[1,2,3]триазол-2-іл-феніл)-метанон; [(S)-2-(5,6-Диметокси-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метил-2[1,2,3]триазол-2-іл-феніл)-метанон; [(S)-2-(5,6-Диметокси-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метил-2-піразол-1-ілфеніл)-метанон; [(S)-2-(5,6-Диметокси-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метокси-2[1,2,3]триазол-2-іл-феніл)-метанон; [(S)-2-(6-Хлор-5-трифторметил-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метил-2[1,2,3]триазол-2-іл-феніл)-метанон; 3 UA 116053 C2 5 10 15 20 25 (5-Метил-2-[1,2,3]триазол-2-іл-феніл)-[(S)-2-метил-2-(5-трифторметил-1H-бензоімідазол-2іл)-піролідин-1-іл]-метанон; або (5-Метил-2-[1,2,3]триазол-2-іл-феніл)-[(S)-2-метил-2-(5-трифторметокси-1H-бензоімідазол-2іл)-піролідин-1-іл]-метанон. 3) Третій варіант здійснення винаходу відноситься до сполук у відповідності з варіантом здійснення 1) для застосування у відповідності з варіантом здійснення 1), де сполука являє собою: [(S)-2-(5-Бром-7-метил-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метил-2-піримідин2-іл-феніл)-метанон. 4) Четвертий варіант здійснення винаходу відноситься до сполук у відповідності з варіантом здійснення 1) для застосування у відповідності з варіантом здійснення 1), де сполука являє собою: [(S)-2-(5-Хлор-4-метил-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метокси-2[1,2,3]триазол-2-іл-феніл)-метанон. Сполуки формули (I) містять щонайменше один стереогенний центр, який розташований у положенні 2 піролідинового компоненту. Абсолютна конфігурація піролідинового компоненту сполук у відповідності з даним винаходом представлена у формулі (I); тобто зазначений хіральний центр знаходиться у абсолютній (S) конфігурації. 2 Додатково, добре відомо, що бензімідазольний компонент Ar сполук у відповідності з даним винаходом має таутомерні форми. Таким чином, замісники бензімідазольного компоненту можуть бути приєднані у положенні(ях) орто до атомів у голові містку (тобто приєднані у положенні(ях) 4 та/або 7), та/або у положенні(ях) мета до атомів у голові містку, (тобто приєднані у положенні(ях) 5 та/або 6). Мається на увазі, що два орто, та, відповідно, два мета положення розглядаються як еквівалент. Наприклад, група 5-хлор-4-метил-1H-бензоімідазол-2іл мається на увазі як така, що позначує таку ж групу, що і 6-хлор-7-метил-1H-бензоімідазол-2іл, 5-хлор-4-метил-3H-бензоімідазол-2-іл та 6-хлор-7-метил-3H-бензоімідазол-2-іл. У цій патентній заявці, пунктирна лінія показує точку приєднання зображеного радикалу. Наприклад, радикал, зображений нижче 30 35 40 45 50 55 являє собою 5-метил-2-(2-триазоліл)-фенільну групу. Якщо використовується форма множини для сполук, солей, фармацевтичних композицій, захворювань та т.п., тоді це також призначене для позначення форми однини сполуки, солі або т.п. Будь-яке посилання на сполуки формули (I) розуміється як таке, що відноситься також до солей (і особливо фармацевтично прийнятних солей) таких сполук, якщо це є підходящим та доцільним. Термін "фармацевтично прийнятні солі" відноситься до солей, які зберігають бажану біологічну активність даної сполуки та проявляють мінімальні небажані токсикологічні ефекти. Такі солі включають солі приєднання неорганічнихабо органічних кислот та/або основ залежно від присутності лужних та/або кислотних груп у даній сполуці. Для довідки, див, наприклад, "Handbook of Pharmaceutical Salts. Properties, Selection and Use.”, P. Heinrich Stahl, Camille G. Wermuth (Eds.), Wiley-vch, 2008; та "Pharmaceutical Salts and Co-crystals", Johan Wouters and Luc Quéré (Eds.), RSC Publishing, 2012. Кращою фармацевтично прийнятною сіллю є сіль соляної кислоти. Вечірня сплутаність визначається як циркадний синдром другої половини дня (тобто післяобідніх та/ або вечірніх годин, особливо післяобідніх годин) підвищеного занепокоєння та дезорієнтації у пацієнта, де у цілому зазначений пацієнт має деяку форму деменції. Основні клінічні ознаки включають підвищене збудження, загальне занепокоєння та перепади настрою, які типово розвиваються при зменшенні природного світла. Термін "у другій половині дня", використовуваний у даній заявці, відноситься до післяобіднього періоду та вечора, особливо, часу приблизно між заходом сонця та пізніше (але не включаючи ніч / час сну); наприклад, час від приблизно 16.00 до приблизно 22.00, особливо від приблизно 16.00 до приблизно 21.00. У одному підваріанті здійснення, термін відноситься до післяобіднього періоду, особливо від приблизно 16.00 до приблизно 19.00; у іншому підваріанті здійснення термін відноситься до вечора, особливо від приблизно 19.00 до приблизно 22.00. 4 UA 116053 C2 5 10 15 20 25 30 35 40 45 50 55 60 Деменції включають особливо, деменції типу Альцгеймера, включаючи: деменцію Альцгеймера (пресенільну деменцію або сенільну деменцію), підкіркову деменцію, деменцію дифузійних тілець Леві та лобно-скроневу деменцію. Деменції далі включають деменції судинних типів, такі як: судинна деменція, мультиінфарктна деменція, деменція Бінсвангера, деменція боксерів, артеріосклеротична деменція. Решта типів деменції (9 %) мають інші етіології, такі як паралітична деменція, індукована речовиною персистуюча деменція, діалізна деменція, гідроцефалічна деменція, та деменції внаслідок пухлин, субдуральної гематоми, нормотензивної гідроцефалії, васкуліту, гіповітамінозу, або ендокринного або метаболічного захворювання. У контексті даного винаходу, термін переважно відноситься до деменцій типу Альцгеймера, особливо деменції Альцгеймера. Мається на увазі, що термін деменція також включає будь-яку комбінацію перерахованих вище типів деменцій. У підваріанті здійснення, деменція особливо відноситься до помірних стадій деменцій типу Альцгеймера (особливо до помірних стадій деменції Альцгеймера), у яких стадії вечірньої сплутаності починають проявлятися більш часто та/або змішаної деменції [форми деменції, що комбінує нейропатологічні відкладення пептидів (зв'язані з деменцією Альцгеймера) з деменцією судинного типу]. У кращому підваріанті здійснення, деменція відноситься до помірних стадій деменцій типу Альцгеймера (особливо до помірних стадій деменції Альцгеймера). Стадії деменції типу Альцгеймера можуть бути визначені у такий спосіб (де вищевказані помірні стадії деменцій типу Альцгеймера (особливо помірні стадії деменції Альцгеймера) відносяться до стадій 3-6, переважно до стадій 3-5, зокрема до стадій 3 та 4, як визначено нижче, та де пре-сенільна деменція може бути визначена як така, що відповідає стадіям 1-4, зокрема стадіям 3 та 4, нижче): Стадія 1: Немає ушкодження (нормальна функція); Особа не відчуває яких-небудь проблем з пам'яттю. При співбесіді із кваліфікованим лікарем не виявляються які-небудь докази симптомів деменції. Стадія 2: Дуже незначне зниження когнітивних здатностей (можуть бути нормальні вікові зміни або самі ранні ознаки деменції, наприклад, типу Альцгеймера): Особа може відчувати, як він або вона має провали у пам'яті (наприклад, забування знайомих слів або розташування побутових предметів). Але на цій стадії можна не виявити симптомів деменції при медичному дослідженні або друзями, членами родини або колегами по роботі. Стадія 3: Помірне зниження когнітивних здатностей (деменція, наприклад, типу Альцгеймера може бути діагностовано у деяких, але не в усіх, індивідуумів із цими симптомами): Друзі, члени родини або колеги по роботі починають зауважувати складності. При більш докладній медичній співбесіді, лікарі можуть виявити проблеми у пам'яті або концентрації. Загальноприйнята стадія 3 утруднень включає: помітні проблеми добору правильного слова або назви; складності запам'ятовування імен при знайомстві з новими людьми; наявність помітних складностей виконання завдань у соціальній або робочій обстановці; забування матеріалу, який хто-небудь тільки що прочитав; втрата або розміщення на неправильне місце цінних об'єктів; підвищення труднощів із плануванням або організацією. Стадія 4: Середньо-важке зниження когнітивних здатностей: На цій стадії ретельна медична співбесіда повинна визначити чіткі симптоми у деяких областях: забудькуватість нещодавніх подій; порушена здатність виконувати розумову арифметику; великі складності виконання складних завдань, таких як планування обіду для гостей, оплата рахунків або керування фінансами; забудькуватість про чиюсь особисту історію; перетворення у сумовиту або замкнену особистість, особливо у соціальних або розумових напружених ситуаціях. Стадія 5: Помірна вага зниження когнітивних здатностей: пробіли у пам'яті та мисленні стають помітними, та особини починають потребувати допомоги виконання повсякденних активностей. На цій стадії, люди з деменцією, наприклад, типу Альцгеймера, можуть бути нездатні назвати їхню власну адресу або номер телефону або вищий навчальний заклад або коледж, який вони закінчили; приходять у замішання про те, де вони або який день; мають проблеми з розумовою арифметикою невеликої складності; потребують допомоги вибору належного одягу для сезону або події; усе ще пам'ятаючи істотні деталі про них самих та їх родичів; ще не потребуючи допомоги при прийманні їжі або використанні туалету. Стадія 6: Важке зниження когнітивних здатностей: Пам'ять продовжує погіршуватися, відбуваються зміни особистості та особи потребують значної допомоги при побутових активностях. На цій стадії, особи можуть втрачати компетентність щодо нещодавно отриманого досвіду, а також про їхнє оточення; пам'ятають свої імена, але мають складності з їх особистою історією; розрізняють рідні та нерідні особи, але мають складності запам'ятовування імені дружини або опікуна; потребують допомоги для вдягання належним чином та можуть, без контролю, робити помилки, такі як вдягання піжам поверх денного одягу або взуття на неправильну ногу; переживання значних змін характеру сну (наприклад, сон впродовж дня та виникнення занепокоєння вночі); 5 UA 116053 C2 5 10 15 20 25 30 35 40 45 50 55 60 потребують допомоги при користуванні туалетом; мають зростаючі складності контролювання їх сечового міхура або кишечнику; відчувають значні особистісні та поведінкові зміни, включаючи підозрілість та манії (такі як припущення, що їх опікун є ошуканцем) або компульсивну поведінку, що повторюється, таку як заламування рук або кришіння паперу; прагнення бродити або загубитися. Стадія 7: Надзвичайно важке зниження когнітивних здатностей: На кінцевій стадії, наприклад, деменції Альцгеймера, особи втрачають здатність відповідати на їхнє навколишнє середовище, розмовляти та, в остаточному підсумку, контролювати рух. Вони все ще можуть говорити слова або фрази. На цій стадії, особи потребують допомоги для більшої частини щоденної особистої гігієни, включаючи харчування або користування туалетом. Вони також можуть втрачати здатність посміхатися, сидіти без підтримки та утримувати голову вертикально. Рефлекси стають аномальними, м'язи стають ригідними, порушується ковтання. 5) Таким чином, п'ятий варіант відноситься до сполук у відповідності з будь-яким з варіантів здійснення 1) - 4) для застосування у відповідності з варіантом здійснення 1), де сполуку використовують для попередження або лікування вечірньої сплутаності у пацієнта, який має деяку форму деменції. Медичні фактори, які можуть сприяти розвитку вечірньої сплутаності у зазначених пацієнтів, що виявляють деяку форму деменції, можуть являти собою хронічний біль (наприклад, внаслідок артриту або злоякісного новоутворення), системне порушення органів (наприклад, застійна серцева недостатність, ішемічна хвороба серця, астма, хронічне обструктивне захворювання легенів, гастроезофагеальний рефлюкс, нетримання сечі, доброякісна гіпертрофія передміхурової залози), психіатричні умови (наприклад, депресія, тривожність, психоз), та ефекти медикаментозного лікування. 6) Подальший варіант здійснення винаходу відноситься до сполук у відповідності з будьяким з варіантів здійснення 1) - 4) для застосування у відповідності з варіантом здійснення 5), де зазначений пацієнт має деменцію типу Альцгеймера. 7) Подальший варіант здійснення винаходу відноситься до сполук у відповідності з будьяким з варіантів здійснення 1) - 4) для застосування у відповідності з варіантом здійснення 5), де зазначений пацієнт має деменцію Альцгеймера. 8) Подальший варіант здійснення винаходу відноситься до сполук у відповідності з будьяким з варіантів здійснення 1) - 4) для застосування у відповідності з варіантом здійснення 5), де зазначений пацієнт має помірну стадію деменції типу Альцгеймера (особливо помірну стадію деменції Альцгеймера). 9) Подальший варіант здійснення винаходу відноситься до сполук у відповідності з будьяким з варіантів здійснення 1) - 4) для застосування у відповідності з будь-яким з варіантів здійснення 1) - 8), де зазначена вечірня сплутаність являє собою післяобідню вечірню сплутаність (де друга половина дня особливо визначається як інтервал від приблизно 16.00 до приблизно 19.00). 10) Подальший варіант здійснення винаходу відноситься до сполук у відповідності з будьяким з варіантів здійснення 1) - 4) для застосування у відповідності з будь-яким з варіантів здійснення 1) - 8), де зазначена вечірня сплутаність являє собою вечірню сплутаність після заходу сонця (де друга половина дня особливо визначається як інтервал від приблизно 19.00 до приблизно 22.00). Таким чином, винахід відноситься до сполук формули (I), як визначено у варіанті здійснення 1), або до таких сполук, які у подальшому обмежені характеристиками будь-якого з варіантів здійснення 2) - 4), що розглядаються з урахуванням їх відповідних залежностей; до їх фармацевтично прийнятних солей; та до застосування таких сполук як лікарські засоби для лікування вечірньої сплутаності у відповідності з будь-яким з варіантів здійснення 1) - 10). Для уникнення якої-небудь невизначеності, наступні варіанти здійснення винаходу, відповідно, можливі та призначені й, таким чином, специфічно розкриті у індивідуалізованій формі: 1, 2+1, 3+1, 4+1, 5+1, 5+2+1, 5+3+1, 5+4+1, 6+5+1, 6+5+2+1, 6+5+3+1, 6+5+4+1, 7+5+1, 7+5+2+1, 7+5+3+1, 7+5+4+1, 8+5+1, 8+5+2+1, 8+5+3+1, 8+5+4+1, 9+1, 9+2+1, 9+3+1, 9+4+1, 9+5+1, 9+5+2+1, 9+5+3+1, 9+5+4+1, 9+6+5+1, 9+6+5+2+1, 9+6+5+3+1, 9+6+5+4+1, 9+7+5+1, 9+7+5+2+1, 9+7+5+3+1, 9+7+5+4+1, 9+8+5+1, 9+8+5+2+1, 9+8+5+3+1, 9+8+5+4+1, 10+1, 10+2+1, 10+3+1, 10+4+1, 10+5+1, 10+5+2+1, 10+5+3+1, 10+5+4+1, 10+6+5+1, 10+6+5+2+1, 10+6+5+3+1, 10+6+5+4+1, 10+7+5+1, 10+7+5+2+1, 10+7+5+3+1, 10+7+5+4+1, 10+8+5+1, 10+8+5+2+1, 10+8+5+3+1, 10+8+5+4+1. До переліку, представленого вище, номери відносяться до варіантів здійснення винаходу у відповідності з їх нумерацією, зазначеною у даній заявці вище, у той час як “+” вказує залежність від іншого варіанту здійснення. Різні індивідуалізовані варіанти здійснення розділені комами. Іншими словами, "10+7+5+1", наприклад, відноситься до варіанту здійснення 10), 6 UA 116053 C2 5 10 15 20 25 30 35 40 45 50 55 залежного від варіанту здійснення 7), залежного від варіанту здійснення 5), залежного від варіанту здійснення 1), тобто варіант здійснення "10+7+5+1" відноситься до сполук формули (I) у відповідності з варіантом здійснення 1), додатково обмежених всіма характерними ознаками варіантів здійснення 5), 7), та 10). Сполуки формули (I) у відповідності з будь-яким з варіантів здійснення 1) - 4) та їх фармацевтично прийнятні солі можна використовувати як лікарські засоби для попередження або лікування вечірньої сплутаності, наприклад, у формі фармацевтичних композицій для ентерального (такого як, особливо, пероральне) або парентерального введення (включаючи місцеве введення або інгаляцію). Одержання фармацевтичних композицій можна здійснювати таким чином, який буде відомий будь-якому кваліфікованому спеціалісту у даній галузі техніки (див., наприклад, Remington, The Science and Practice of Pharmacy, 21-е видання (2005), Частина 5, "Pharmaceutical Manufacturing" [опубліковане Lippincott Williams & Wilkins]) шляхом перетворення описаних сполук формул (I), (II) та (III) або їх фармацевтично прийнятних солей, необов'язково у комбінації з іншими терапевтично цінними речовинами, у галенову форму для введення разом з підходящими, нетоксичними, інертними, терапевтично сумісними твердими або рідкими матеріалами-носіями та, якщо це є бажаним, звичайними фармацевтичними ад'ювантами. Даний винахід також відноситься до способу лікування розладу, зазначеного у даній заявці, який включає введення суб'єкту фармацевтично активної кількості СПОЛУКИ формули (I), як визначено у будь-якому з варіантів здійснення винаходу 1) - 4). У переважному варіанті здійснення винаходу, кількість такої сполуки формули (I), що вводиться, у відповідності з будь-яким з варіантів здійснення 1) - 4) знаходиться у діапазоні від 1 мг до 1000 мг на добу, переважно у діапазоні 5 мг та 400 мг на добу, більш переважно у діапазоні 5 мг та 200 мг на добу. Кожен раз, коли слово "у діапазоні" використовується для опису області числових значень, тоді мається на увазі, що кінцеві точки зазначеного діапазону однозначно включені у діапазон. Наприклад: якщо температурний інтервал описаний як у діапазоні 40 ºC та 80 ºC, тоді це означає, що кінцеві точки 40 ºC та 80 ºC включені у інтервал; або якщо перемінна величина визначена як ціле число у діапазоні 1 та 4, тоді це означає, що перемінна величина являє собою ціле число 1, 2, 3, або 4. Термін "приблизно", зазначений перед числовим значенням "X", відноситься у даній заявці до інтервалу, що включає у себе від X мінус 10 % X до X плюс 10 % X, та переважно до інтервалу, що включає у себе від X мінус 5 % X до X плюс 5 % X. У окремому випадку температур, термін "приблизно", розташований перед температурою "Y", відноситься у даній заявці до інтервалу, що включає у себе від температури Y мінус 10ºC до Y плюс 10ºC, та переважно до інтервалу, що включає у себе від Y мінус 5ºC до Y плюс 5ºC. Крім того, термін "кімнатна температура", як використовується у даній заявці, відноситься до температури приблизно 25 °C. У конкретному випадку часових точок, термін "приблизно", розташований перед певною часовою точкою "Y", відноситься у даній заявці до інтервалу, що включає у себе від часової точки Y мінус 1 година до Y плюс 1 година, та переважно до інтервалу, що включає у себе від Y мінус 30 хвилин до Y плюс 30 хвилин. Для уникнення якої-небудь невизначеності, якщо сполуки описані як придатні для попередження або лікування певних захворювань, тоді такі сполуки також придатні для застосування для одержання лікарського засобу для попередження або лікування таких захворювань. Одержання сполук формули (I): Сполуки формули (I) можуть бути отримані за допомогою способів, описаних нижче, за допомогою способів, описаних у експериментальній частині нижче або за допомогою аналогічних способів. Оптимальні умови реакцій можуть змінюватися залежно від конкретних використовуваних реагуючих речовин або розчинників, але такі умови можуть бути визначені кваліфікованим спеціалістом у даній галузі техніки за допомогою загальноприйнятих оптимізованих процедур. У деяких випадках, кінцевий продукт може бути надалі модифікований, наприклад, шляхом перетворення замісників, одержуючи новий кінцевий продукт. Ці перетворення можуть включати, але не обмежуючись тільки ними, реакції відновлення, окиснення, алкілування, ацилювання, та гідролізу, які добре відомі кваліфікованому спеціалісту у даній галузі техніки. У деяких випадках, порядок здійснення наступних схем реакцій, та/або стадій реакцій, може змінюватися для полегшення реакції або для запобігання небажаних продуктів реакції. 7 UA 116053 C2 5 10 15 20 Сполуки формули (I) у відповідності з даним винаходом можуть бути приготовлені у 1 2 відповідності із загальною послідовністю реакцій, викладених нижче, де Ar та Ar приймають значення, як визначено для формули (I). Родовий замісник (R) n відноситься до замісників 2 бензімідазольної групи Ar , як визначено для сполук формули (I). Існують два загальні синтетичні підходи для сполук формули (I). Перший синтетичний підхід 1 може починатися з Boc-захисту відповідної пролінової похідної a у стандартних умовах, наприклад, шляхом розчинення проліну a у розчиннику, такому як ДХМ або ТГФ, та додавання основи до розчину, наприклад DIPEA, TEA або водн. Na 2CO3 з наступним додаванням Boc2O. Реакцію здійснюють при кт та звичайно завершують впродовж декількох годин та отримують Boc-захищену пролінову похідну b. Після цього захищену пролінову похідну b (яка також є комерційно доступною) сполучають у стандартних умовах амідного сполучення з підходящою похідною фенілен-діаміну, наприклад, у розчиннику, такому як ТГФ, ДХМ або ДМФА у присутності зв'язуючого реагенту, такого як HBTU або TBTU або т.п., та основи, наприклад, DIPEA або TEA, отримуючи сполуку c. Замикання кільця для одержання бензімідазольної похідної d здійснюють, наприклад, шляхом розчинення попереднику c у AcOH та нагрівання при 100 °C впродовж 1 год. Зі сполуки d знімають Boc-захист у стандартних кислотних умовах, таких як 4M HCl у діоксані, або TFA у ДХМ, отримуючи попередник e, який 1 перетворюють у кінцеву сполуку f шляхом реакції амідного сполучення з Ar -COOH, наприклад, у розчиннику, такому як ТГФ, ДМФА або ДХМ у присутності зв'язуючого реагенту, такого як TBTU, HBTU, HATU, EDC або т.п. та основи, такої як DIPEA, TEA або N-метилморфолін. 25 30 Альтернативний синтетичний підхід 2 може починатися з естерифікації (звичайно утворення складного метилового ефіру) пролінової похідної a, наприклад, шляхом розчинення вихідної речовини у ТГФ та додавання 5 еквівалентів відповідного спирту (звичайно MeOH) з наступним додаванням EDC та DMAP. Після цього похідну метил-складного ефіру g (яка також є 1 комерційно доступною) ацилюють за допомогою Ar -COOH, використовуючи стандартні умови амідного сполучення, такі як ті, які описані вище, що приводить до одержання проміжної сполуки h. Гідроліз складного ефіру у стандартних умовах, наприклад, шляхом розчинення складноефірної похідної h у ТГФ / MeOH=1 / 1 з наступним додаванням 2 екв. водн. 1M розчину 8 UA 116053 C2 5 10 15 20 25 30 35 40 45 50 55 60 NaOH приводить до одержання похідної карбонової кислоти i. Кінцеві сполуки f отримують за допомогою попереднику j шляхом застосування таких же умов, що і описано для амідного сполучення та циклізації у синтетичному підході 1. Кожен раз, коли сполуки формули (I) отримують у формі суміші стереоізомерів, таких як, особливо енантіомери, тоді стереоізомери можна розділяти, використовуючи методи, які добре відомі кваліфікованому спеціалісту у даній галузі техніки: наприклад, шляхом утворення та розділення діастереомерних солей або шляхом ВЕРХ через хіральну нерухому фазу, таку як Daicel ChiralPak AD-H (5 мкм) колонка, Daicel ChiralCel OD-H (5 мкм) колонка, Daicel ChiralCel OD (10 мкм) колонка, Daicel ChiralPak IA (5 мкм) колонка, Daicel ChiralPak IB (5 мкм) колонка, Daicel ChiralPak IC (5 мкм) колонка, або (R, R)-Whelk-01 (5 мкм) колонка. Типові умови хіральної ВЕРХ являють собою ізократичну суміш елюенту A (EtOH, у присутності або за відсутності основи, такої як TEA та/або діетиламін, або солі, такої як TFA) та елюенту B (гептан). Наступні приклади призначені для ілюстрації винаходу. Ці приклади є тільки ілюстративними та не повинні розглядатися, як яким-небудь чином обмежуючі винахід. Експериментальна частина Скорочення (як використовується у даній заявці далі та у описі вище): Ac ацетил (такої як у OAc = ацетат) AcOH оцтова кислота безв. безводний водн. водний водн атмосфера Boc трет-Бутоксикарбоніл Boc2O ди-трет-бутил дикарбонат BSA бичачий сироватковий альбумін Bu бутил, такий як у tBu = трет-бутил = третинний бутил КХ колонкова хроматографія через силікагель CHO яєчники китайського хом'ячку конц. концентрований DCE 1,2-дихлоретан ДХМ дихлорметан DEA діетиламін DIPEA діізопропілетиламін ДМФА N, N-диметилформамід ДМСО диметилсульфоксид EDC 3-(етилімінометиленаміно)-N, N-диметилпропан-1-амін ELSD детектування за світлорозсіянням випареного зразку екв. еквівалент(и) ES електророзпилення Et етил Et2O діетиловий ефір EtOAc етилацетат EtOH етанол Пр. приклад (сполука з прикладу) FC колонкова флеш-хроматографія на силікагелі FCS фетальна теляча сироватка FLIPR спектрофотометр для читання планшетів для візуалізації флуоресценції год. година(и) HATU 1-[біс(диметиламіно)метилен]-1H-1,2,3-триазолo[4,5-b]піридиній 3-оксид гексафторфосфат HBSS збалансований сольовий розчин Хенкса HBTU N, N,N′,N′-тетраметил-O-(1H-бензотриазол-1-іл)уроній гексафторфосфат HEPES 4-(2-гідроксиетил)-піперазин-1-етансульфонова кислота 1 H-ЯМР ядерний магнітний резонанс протону ВЕРХ високоефективна рідинна хроматографія РХ-МС рідинна хроматографія – мас-спектроскопія Літ. література M точна маса (як використовується для РХ-МС) Me метил MeCN ацетонітрил MeOH метанол 9 UA 116053 C2 5 10 15 20 25 30 35 40 45 50 55 60 MeI метил-йодид МГц мегагерц мкл мікролітр хвил. хвилина(и) МС мас-спектроскопія N нормальність Pd(OAc)2 діацетат паладію Pd(PPh3)4 тетракіс(трифенілфосфін)паладій(0) PL-HCO3 гідрокарбонат на полімерній підкладці Ph феніл PPh3 трифенілфосфін преп. препаративний КТ кімнатна температура нас. насичений TBTU O-(бензотриазол-1-іл)-N, N,N',N'-тетраметилуроній тетрафторборат TEA триетиламін TFA трифтороцтова кислота Tf трифторметансульфоніл ТГФ тетрагідрофуран tR час утримання УФ ультрафіолет I-Хімія Усі температури зазначені у°C. Комерційно доступні вихідні речовини використовували у отриманому вигляді без додаткового очищення. Сполуки очищали шляхом колонкової флешхроматографії через силікагель (FC), колонкової хроматографії через силікагель (КХ) або шляхом препаративної ВЕРХ. Сполуки, описані у винаході, характеризували за допомогою РХМС (час утримання tR представлено у хвил.; молекулярна маса, отриманий з мас-спектру, представлена у г/моль, використовуючи умови, перераховані нижче). Якщо масу неможливо 1 визначити, тоді сполуки також характеризували за допомогою H-ЯМР (400 МГц: Bruker; хімічні зсуви представлені у част. на млн. відносно використовуваного розчиннику; мультиплетність: s = синглет, d = дублет, t = триплет; p = пентуплет, hex = гексет, hept = гептет, m = мультиплет, br = широкий, константи зв'язку представлені у Гц). Препаративна ВЕРХ для очищення сполук (умови C) Колонка: Waters XBridge (10 мкм, 75 × 30 мм). Умови: MeCN [елюент A]; вода + 0,5 % NH4OH (25 % водн.) [елюент B]; Градієнт: 90 % B 5 % B впродовж 6,5 хвил. (потік: 75 мл/хвил.). Детектування: УФ + ELSD. Препаративна ВЕРХ для очищення сполук (умови D) Колонка: Waters Atlantis T3 OBD (10 мкм, 75 × 30 мм). Умови: MeCN [елюент A]; вода + 0,5 % HCOOH [елюент B]; Градієнт: 90 % B 5 % B впродовж 6,4 хвил. (потік: 75 мл/хвил.). Детектування: УФ + ELSD. РХ-МС з кислотними умовами Прилад: Agilent 1100 серії з мас-спектроскопічним детектуванням (МС: Finnigan одиничний квадруполь). Колонка: Agilent Zorbax SB-Aq, (3,5 мкм, 4,6 × 50 мм). Умови: MeCN [елюент A]; вода + 0,04 % TFA [елюент B]. Градієнт: 95 % B 5 % B впродовж 1,5 хвил. (потік: 4,5 мл/хвил.). Детектування: УФ + МС. 1) Синтез 5-метокси-2-(2H-1,2,3-триазол-2-іл)бензойної кислоти 2-Йод-5-метокси-бензойну кислоту (15,0 г; 53,9 ммоль) розчиняли у безводному ДМФА (45 мл) з наступним додаванням 1H-1,2,3-триазолу (7,452 г; 108 ммоль) та карбонату цезію (35,155 г; 108 ммоль). Шляхом додавання карбонату цезію температуру реакційної суміші підвищували до 40 °C та газ виділявся з реакційної суміші. Додавали йодид міді (I) (514 мг; 2,7 ммоль). Це запускало сильну екзотермічну реакцію та температура реакційної суміші досягала 70 °C впродовж декількох секунд. Продовжували перемішувати впродовж 30 хвилин. Після цього ДМФА упарювали при зниженому тиску з наступним додаванням води (170 мл) та EtOAc (90 мл). Суміш інтенсивно перемішували та шляхом додавання моногідрату лимонної кислоти pH доводили до 3-4. Осад відфільтровували та промивали водою та EtOAc та відкидали. Фільтрат виливали на ділильну лійку та фази розділяли. Водну фазу знову екстрагували за допомогою EtOAc. Об'єднані органічні шари знову висушували над MgSO4, фільтрували та розчинник упарювали, отримуючи 7,1 г 5-метокси-2-(2H-1,2,3-триазол-2-іл)бензойної кислоти у вигляді білого порошку з чистотою 94 % (6 % домішки являли собою регіоізометрично N1-зв'язану + триазолo-похідну); tR [хвил.] = 0,60; [M+H] = 220,21. 10 UA 116053 C2 5 10 15 20 25 30 35 40 45 50 55 60 2) Синтез (S)-1-(трет-бутоксикарбоніл)-2-метилпіролідин-2-карбонової кислоти 2-Метил-L-пролін гідрохлорид (99,7 г; 602 ммоль) розчиняли у 1/1-суміші MeCN та води (800 мл) та додавали триетиламін (254 мл; 1810 ммоль). Температуру реакційної суміші незначно підвищували. Реакційну суміш охолоджували до 10 °C до 15 °C з наступним обережним додаванням розчину Boc2O (145 г; 662 ммоль) у MeCN (200 мл) впродовж 10 хвилин. Перемішування при кт продовжували впродовж 2 годин. MeCN упарювали при зниженому тиску та водн. NaOH розчин (2M; 250 мл) додавали до залишкової водн. частини реакційної суміші. Водний шар промивали за допомогою Et2O (2 × 300 мл), потім охолоджували до 0 °C з наступним повільним та обережним додаванням водн. HCl (25 %) для доведення pH до 2. При цій процедурі утворювалась суспензія. Осад відфільтровували та висушували при ВВ, отримуючи 110,9 г зазначеної у заголовку сполуки у вигляді бежевого порошку; t R [хвил.] = 0,68; + [M+H] = 230,14. 3) Синтез (S)-трет-бутил 2-((2-аміно-4-хлор-3-метилфеніл)карбамоїл)-2-метилпіролідин-1карбоксилату (S)-1-(трет-бутоксикарбоніл)-2-метилпіролідин-2-карбонову кислоту (60 г; 262 ммоль) та HATU (100 г; 264 ммоль) суспендували у ДХМ (600 мл) з наступним додаванням DIPEA (84,6 г; 654 ммоль) та 6-хлор-2,3-діамінотолуолу (41 г; 262 ммоль). Реакційну суміш перемішували при кт впродовж 14 годин, після цього концентрували при зниженому тиску та до залишку додавали воду з наступною екстракцією продукту за допомогою EtOAc (3x). Об'єднані органічні шари промивали сольовим розчином, висушували над MgSO 4, фільтрували та розчинник упарювали при зниженому тиску, отримуючи 185 г зазначеної у заголовку сполуки у вигляді темнокоричнюватого масла, яке використовували на наступній стадії без додаткового очищення; t R + [хвил.] = 0,89; [M+H] = 368,01. 4) Синтез (S)-трет-бутил 2-(5-хлор-4-метил-1H-бензо[d]імідазол-2-іл)-2-метилпіролідин-1карбоксилату (S)-трет-бутил 2-((2-аміно-4-хлор-3-метилфеніл)карбамоїл)-2-метилпіролідин-1-карбоксилат (185 г; 427 ммоль) розчиняли у AcOH (100 %; 611 мл), нагрівали до 100 °C та продовжували перемішувати впродовж 90 хвилин. AcOH упарювали при зниженому тиску та залишок розчиняли у ДХМ з наступним обережним додаванням насиченого розчину бікарбонату натрію. Фази розділяли, водн. фазу екстрагували ще один раз за допомогою ДХМ, об'єднані водн. фази знову висушували над MgSO4, фільтрували та розчинник упарювали при зниженому тиску, отримуючи 142,92 г зазначеної у заголовку сполуки у вигляді темно-коричневого масла, яке + використовували на наступній стадії без додаткового очищення; tR [хвил.] = 0,69; [M+H] = 350,04. 5) Синтез (S)-5-хлор-4-метил-2-(2-метилпіролідин-2-іл)-1H-бензо[d]імідазолу гідрохлориду (S)-трет-бутил 2-(5-хлор-4-метил-1H-бензо[d]імідазол-2-іл)-2-метилпіролідин-1-карбоксилат (355,53 г; 1,02 моль) розчиняли у діоксані (750 мл) з наступним обережним додаванням розчину HCl у діоксані (4M; 750 мл; 3,05 моль). Реакційну суміш перемішували впродовж 3 годин з наступним додаванням Et2O (800 мл), який запускав осадження продукту. Тверду речовину відфільтровували та висушували при високому вакуумі, отримуючи 298,84 г зазначеної у + заголовку сполуки у вигляді рудуватого порошку; tR [хвил.] = 0,59; [M+H] = 250,23. 6) Синтез [(S)-2-(5-хлор-4-метил-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метокси2-[1,2,3]триазол-2-іл-феніл)-метанону (S)-5-хлор-4-метил-2-(2-метилпіролідин-2-іл)-1H-бензо[d]імідазол гідрохлорид (62,8 г; 121 ммоль) розчиняли у ДХМ (750 мл) з наступним додаванням 5-метокси-2-(2H-1,2,3-триазол-2іл)бензойної кислоти (62,8 г; 121 ммоль) та DIPEA (103 мл; 603 ммоль). Продовжували перемішувати впродовж 10 хвилин з наступним додаванням HATU (47 г; 124 ммоль). Реакційну суміш перемішували впродовж 16 годин при кт. Розчинники упарювали при зниженому тиску та залишок розчиняли у EtOAc (1000 мл) та промивали водою (3 × 750 мл). Органічну фазу висушували над MgSO4, фільтрували та розчинник упарювали при зниженому тиску. Залишок очищали шляхом КК за допомогою EtOAc / гексан = 2 / 1, отримуючи 36,68 г зазначеної у + заголовку сполуки у вигляді аморфного білого порошку. tR [хвил] = 0,73; [M+H] = 450,96. Зазначену у заголовку сполуку переведено у відповідну сіль соляної кислоти, використовуючи стандартні умови, такі як ізопропанол / HCl у ізопропанолі. 7) Синтез метил 2-йод-5-метилбензоaту 2-Йод-5-метилбензойної кислоти (101 г; 387 ммоль) розчиняли у MeOH (700 мл) з наступним додаванням концентрованої сірчаної кислоти (97 %; 10,4 мл; 193 ммоль). Реакційну суміш нагрівали до 83 °C впродовж 16 годин, знову охолоджували до КТ з наступним повільним та обережним додаванням водн. 1M розчину NaOH до досягнення pH 8. MeOH упарювали при зниженому тиску та решту водн. фази екстрагували за допомогою ДХМ (2 × 350 мл). Об'єднані 11 UA 116053 C2 5 10 15 20 25 30 35 40 45 50 55 60 органічні шари промивали водою (400 мл), висушували над MgSO 4, фільтрували та розчинник упарювали при зниженому тиску, отримуючи 104,13 г зазначеної у заголовку сполуки у вигляді + жовтої рідини. tR [хвил] = 0,89; [M+H] = не виявлено. 8) Синтез метил 5-метил-2-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)бензоaту Метил 2-йод-5-метилбензоaт (104,13 г; 358 ммоль) розчиняли у ТГФ (500 мл) у інертній атмосфері азоту з наступним додаванням триетиламіну (150 мл; 1,07 моль) та 4,4,5,5тетраметил-1,3,2-діоксаборолану (68,8 г; 537 ммоль). Суміш додатково дегазували шляхом барботування газоподібного азоту впродовж 5 хвил. Після цього додавали три-(o-толіл)-фосфін (5,45 г; 17,9 ммоль) та ацетат паладію (II) (2,01 г; 8,96 ммоль) та суміш нагрівали до 75 °C впродовж 1 години. Реакційну суміш охолоджували до 0 °C з наступним обережним додаванням нас. водн. розчин NH4Cl (до точки, коли більше не відбувалося виділення газу). Чорну суспензію фільтрували, фільтрат концентрували при зниженому тиску та воду додавали до залишку. Продукт екстрагували за допомогою EtOAc (2 × 200 мл). Об'єднані EtOAc шари знову висушували над MgSO4, фільтрували та розчинник упарювали при зниженому тиску. Залишок очищали шляхом КК за допомогою гептан / EtOAc=95 / 5, отримуючи 82,7 зазначеної у + заголовку сполуки у вигляді світло-помаранчевої твердої речовини; tR [хвил] = 0,92; [M+H] = 277,22. 9) Синтез метил 5-метил-2-(піримідин-2-іл)бензоaту 5-Метил-2-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)бензоaт (165,45 г; 599 ммоль) розчиняли у 2-метли-тетрагідрофурані (900 мл). Додавали 2-хлорпіримідин (82,3 г; 719 ммоль), твердий карбонат натрію (159 г, 1,5 моль) та воду (275 мл) та реакційну суміш дегазували шляхом барботування газоподібного азоту впродовж 5 хвилин з наступним додаванням [1,1′біс(дифенілфосфіно)фероцен]дихлорпаладій (II), комплекс з ДХМ (CAS: 95464-05-4; Pd(dppf)Cl2 x ДХМ; 39,1 мг; 47,9 ммоль). Реакційну суміш нагрівали до внутрішньої температури 75 °C впродовж 40 годин, потім охолоджували до КТ, фільтрували та до фільтрату додавали воду з наступною екстракцією продукту за допомогою EtOAc (2 × 700 мл). Об'єднані органічні шари знову висушували над MgSO4, фільтрували та розчинник упарювали при зниженому тиску. Залишок очищали шляхом КК за допомогою гептан / EtOAc=2 / 1, отримуючи 86,13 г зазначеної + у заголовку сполуки у вигляді світло-жовтої твердої речовини; tR [хвил] = 0,72; [M+H] = 229,17. 10) Синтез 5-метил-2-(піримідин-2-іл)бензойної кислоти Метил 5-метил-2-(піримідин-2-іл)бензоaт (86,1 г; 377 ммоль) розчиняли у ТГФ (350 мл) з наступним додаванням води (350 мл) та водн. NaOH (190 мл; 4M). Реакційну суміш нагрівали до 70 °C впродовж 4 годин. Органічний розчинник відганяли при зниженому тиску та водн. фазу екстрагували за допомогою ДХМ. Після цього водн. фазу охолоджували до 0 °C та значення pH доводили до pH=1 шляхом обережного додавання водн. 2M розчину соляної кислоти, що приводило до утворення суспензії. Тверду речовину відфільтровували та висушували при високому вакуумі, отримуючи 59,98 г зазначеної у заголовку сполуки у вигляді бежевої твердої + речовини; tR [хвил] = 0,58; [M+H] = 215,14. 11) Синтез (S)-трет-бутил 2-((2-аміно-5-бром-3-метилфеніл)карбамоїл)-2-метилпіролідин-1карбоксилату (S)-1-(трет-бутоксикарбоніл)-2-метилпіролідин-2-карбонову кислоту (2,5 г; 10,9 ммоль) розчиняли у ДХМ (25 мл) та додавали HATU (4,2 г; 11 ммоль). До цієї суміші додавали DIPEA (5,6 мл, 32,7 ммоль) та 5-бром-3-метилбензол-1,2-діамін. Реакційну суміш перемішували при кт впродовж 16 годин. Розчинники упарювали при зниженому тиску та залишок розчиняли у EtOAc (200 мл) та промивали водою (3 × 150 мл). Органічний шар висушували над MgSO4, фільтрували та розчинник упарювали при зниженому тиску. Залишок висушували при високому + вакуумі, отримуючи 5 г зазначеної у заголовку сполуки; tR [хвил] = 0,90; [M+H] = 414,25. 12) Синтез (S)-трет-бутил 2-(5-бром-7-метил-1H-бензо[d]імідазол-2-іл)-2-метилпіролідин-1карбоксилату (S)-трет-бутил 2-((2-аміно-5-бром-3-метилфеніл)карбамоїл)-2-метилпіролідин-1-карбоксилат (4,97 г; 12,1 ммоль) розчиняли у AcOH (100 %; 41 мл) та суміш нагрівали до 100 °C та продовжували перемішувати впродовж 1 год. AcOH упарювали при зниженому тиску та до залишку повільно та обережно додавали нас. водн. розчин NaHCO 3 (250 мл). Продукт екстрагували за допомогою EtOAc (2 × 250 мл). Об'єднані органічні шари знову висушували над MgSO4, фільтрували та розчинник упарювали при зниженому тиску. Залишок висушували при + високому вакуумі, отримуючи 4,3 г зазначеної у заголовку сполуки; t R [хвил] = 0,71; [M+H] = 394,27. 13) Синтез (S)-5-бром-7-метил-2-(2-метилпіролідин-2-іл)-1H-бензо[d]імідазолу гідрохлориду (S)-трет-бутил 2-(5-бром-7-метил-1H-бензо[d]імідазол-2-іл)-2-метил-піролідин-1-карбоксилат (4,26 г; 10,8 ммоль) розчиняли у діоксані (31 мл) та додавали розчин соляної кислоти у діоксані 12 UA 116053 C2 5 10 15 20 (4M; 31 мл; 130 ммоль) з наступним додаванням MeOH (5 мл). Продовжували перемішувати впродовж 2 годин з наступним додаванням Et2O (250 мл), що приводило до осадження білого порошку, який відфільтровували та промивали за допомогою Et 2O (25 мл). Коричнюватий порошок розчиняли у MeOH (50 мл) та додавали 1 г активованого вугілля (Norit) та продовжували перемішувати впродовж 5 хвилин після цього вугілля відфільтровували через целіт та розчинник упарювали при зниженому тиску та залишок висушували при високому вакуумі, отримуючи 3,9 г зазначеної у заголовку сполуки у вигляді світло-рудуватого порошку; tR + [хвил] = 0,61; [M+H] = 294,09. 14) Синтез [(S)-2-(5-Бром-7-метил-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метил-2піримідин-2-іл-феніл)-метанону 5-Метил-2-(піримідин-2-іл)бензойну кислоту (1,47 г; 6,86 ммоль) розчиняли у ДХМ (50 мл) та додавали диметиламінопіридин (168 мг, 1,37 ммоль) та EDC (1,45 г; 7,55 ммоль). Продовжували перемішувати впродовж 30 хвилин з наступним додаванням гідрохлориду (S)-5-бром-7-метил-2(2-метилпіролідин-2-іл)-1H-бензо[d]імідазолу (2,27 г; 6,86 ммоль). Перемішування при кт продовжували впродовж 16 годин. До реакційної суміші додавали етилацетат (150 мл) та нас. розчин гідрокарбонату натрію (100 мл). Фази розділяли та водн. фазу екстрагували за допомогою EtOAc (50 мл). Об'єднані органічні шари висушували за допомогою MgSO4, фільтрували та розчинник упарювали при зниженому тиску. Продукт очищали шляхом препаративної ВЕРХ (умови C), отримуючи 2,07 г зазначеної у заголовку сполуки у вигляді + білого порошку; tR [хвил] = 0,73; [M+H] = 492,14. Аналогічно процедурам, описаним у даній заявці вище, готували наступні приклади. Таблиця 1 Пр. 1 2 3 4 5 6 7 8 9 10 11 25 30 Назва сполуки. РХ-МС (5-Метил-2-[1,2,3]триазол-2-іл-феніл)-[(S)-2-метил-2-(5-трифторметил-1H-бензоімідазол+ 2-іл)-піролідин-1-іл]-метанон. РХ-МС: tR=0,83; [M+H] = 455,3 [(S)-2-(5-Бром-7-метил-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метил-2+ [1,2,3]триазол-2-іл-феніл)-метанон. РХ-МС: tR=0,82; [M+H] = 479,2 (5-Метил-2-[1,2,3]триазол-2-іл-феніл)-[(S)-2-метил-2-(5-трифторметокси-1H+ бензоімідазол-2-іл)-піролідин-1-іл]-метанон. РХ-МС: tR=0,82; [M+H] = 471,2 [(S)-2-(5,6-Диметокси-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метил-2+ [1,2,3]триазол-2-іл-феніл)-метанон. РХ-МС: tR=0,68; [M+H] = 447,4 [(S)-2-(6-Бром-5-фтор-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метил-2+ [1,2,3]триазол-2-іл-феніл)-метанон. РХ-МС: tR=0,82; [M+H] = 483,2 [(S)-2-(6-Хлор-5-трифторметил-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метил+ 2-[1,2,3]триазол-2-іл-феніл)-метанон. РХ-МС: tR=1,01; [M+H] = 489,2 [(S)-2-(5-Хлор-4-метил-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метокси-2+ [1,2,3]триазол-2-іл-феніл)-метанон. РХ-МС: tR=0,78; [M+H] = 451,3 [(S)-2-(5,6-Диметокси-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метокси-2+ [1,2,3]триазол-2-іл-феніл)-метанон. РХ-МС: tR=0,64; [M+H] = 463,3 [(S)-2-(5,6-Диметокси-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метил-2-піразол+ 1-іл-феніл)-метанон. РХ-МС: tR=0,67; [M+H] = 446,3 [(S)-2-(5-Хлор-4-метил-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метил-2+ піримідин-2-іл-феніл)-метанон. РХ-МС: tR=77; [M+H] = 446,2 [(S)-2-(5-Бром-7-метил-1H-бензоімідазол-2-іл)-2-метил-піролідин-1-іл]-(5-метил-2+ піримідин-2-іл-феніл)-метанон. РХ-МС: tR=0,84; [M+H] = 490,3 II-Біологічні дослідження Антагонічні активності на обох орексинових рецепторах вимірювали для кожної сполуки з прикладу, використовуючи наступну процедуру: In vitro аналіз: вимірювання внутрішньоклітинного кальцію: Клітини яєчника китайського хом'ячка (CHO), що експресують орексин-1 рецептор людини та орексин-2 рецептор людини, відповідно, вирощували у культуральному середовищі (Ham F-12 з L-глутаміном), яке містить 300 мкг/мл G418, 100 Од/мл пеніциліну, 100 мкг/мл стрептоміцину та 10 % інактивованої нагріванням фетальної телячої сироватки (FCS). Клітини висівали при щільності 20 тис. клітин / лунку у чорні стерильні планшети на 384 лунки з прозорим дном (Greiner). Висіяні планшети інкубували впродовж ночі при 37 °C у 5 % CO2. 13 UA 116053 C2 5 10 15 20 25 Орексин-A людини як агоніст готували у вигляді 1 мM маточного розчину у MeOH: воді (1:1), розведеному у HBSS, що містить 0,1 % бичачий сироватковий альбумін (BSA), NaHCO 3: 0,375 г/л та 20 мM HEPES для застосування у дослідженні при кінцевій концентрації 3 нM. Антагоністи готували у вигляді 10 мM маточного розчину у ДМСО, потім розводили у планшетах на 384 лунки, використовуючи ДМСО, з наступним переносом розведень у HBSS, що містить 0,1 % бичачий сироватковий альбумін (BSA), NaHCO 3: 0,375 г/л та 20 мM HEPES. У день дослідження, 50 мкл забарвлюючого буферу (HBSS, що містить 1 % FCS, 20 мM HEPES, NaHCO3: 0,375 г/л, 5 мM пробенециду (Sigma) та 3 мкМ флуоресцентного індикатору кальцію fluo-4 AM (1 мM маточного розчину у ДМСО, що містить 10 % плюроніку) додавали у кожну лунку. Клітинні планшети на 384 лунки інкубували впродовж 50 хвил. при 37° C у 5 % CO2, потім урівноважували при кт впродовж 30 хвилин перед вимірюванням. У спектрофотометрі для читання планшетів для візуалізації флуоресценції (FLIPR Tetra, Molecular Devices), антагоністи додавали у планшет у об'ємі 10 мкл/лунку, інкубували впродовж 120 хвил. та на завершення додавали 10 мкл/лунку агоністу. Флуоресценцію вимірювали для кожної лунки з інтервалами 1 секунда, та висоту кожного флуоресцентного піку порівнювали з висотою флуоресцентного піку, що індукує приблизно EC70 (наприклад, 5 нM) орексину-A з носієм замість антагоністу. IC50 значення (концентрацію сполуки, необхідну для інгібування 50 % агоністичної відповіді) визначали та можна нормалізувати, використовуючи отримане IC 50 значення порівняльної сполуки для планшету. Оптимізовані умови досягали шляхом доведення швидкості піпетування та схеми секціонування клітин. Розраховані IC 50 значення можуть коливатися в залежності від добового виконання клітинного аналізу. Коливання такого типу відомі кваліфікованому спеціалісту у даній галузі техніки. Усереднені IC 50 значення з декількох вимірювань представляли у вигляді середніх значень. Антагонічні активності зі сполук з прикладів по відношенню до рецепторів Ox 1 та Ox2 представлені у Таблиці 2. Таблиця 2 Номер прикладу Пр. 1 Пр. 4 Пр. 7 Пр. 10 30 35 40 45 50 IC50 Ox1 IC50 Ox2 Номер [нM] [нM] прикладу 8 81 Пр. 2 22 18 Пр. 5 2 3 Пр. 8 2 4 Пр. 11 IC50 Ox1 IC50 Ox2 Номер [нM] [нM] прикладу 9 20 Пр. 3 15 80 Пр. 6 27 23 Пр. 9 6 21 IC50 Ox1 [нM] 19 2 27 IC50 Ox2 [нM] 161 9 15 Вплив сполук з прикладів на збудження, індуковане кофеїном у щурів та собак Нейробіологічні та нейрофармакологічні логічні обґрунтування: Кофеїн використовували як засіб для стимуляції недостатнього інгібування VLPO-SCN вхідного сигналу на гіпоталамічні орексинові нейрони. Аденозинові рецептори (головним чином рецептори аденозин A1 та A2A) негативно регулюють збудження орексинових нейронів, які опосередковують неспання шляхом підкріплення висхідної пробуджуючої моноамінергічної медіо-кортикальної системи. Впродовж дня, ендогенний аденозин накопичується з метаболізму АТФ та поступово сприяє, з ГАМК та мелатоніном, підвищенню тиску сну шляхом VLPOопосередкованого інгібування орексину у середньому мозку та моноамінових нейронів. Кофеїн, антагоніст рецептору аденозину A1 та A2A, блокує аденозинергічне інгібування на орексинових нейронах, таким чином посилюючи орексинергічну активацію та підвищуючи пильність. Це по суті являє собою один з нейробіологічних механізмів властивостей кофеїну попереджувати від небезпеки та пробуджувати. Гостре пероральне введення кофеїну у кінці дня (у денних видів) використовували для експериментальної симуляції VLPO та SCN деаферентації, що приводить до вечірнього збудження; це має встановлену орексинeргічну активацію та підвищену активність. Висока доза кофеїну, як правило, необхідна для індукування збудження та гіперактивності у здорових тварин з нормальним аденозиновим тоном та рецепторами. Споживання кофеїну протипоказано у пацієнтів похилого віку, що страждають на вечірню сплутаність. Вважають, що кофеїн-вмісні напої загострюють збуджуючі симптоми у пацієнтів з вечірньою сплутаністю. VLPO та SCN деафферентація, а також низький ендогенний аденозиновий тон (внаслідок ослабленого метаболізму АТФ) може приводити до нерегульованих (гіперчутливих) аденозинових рецепторів. Протоколи збудження, індукованого кофеїном у щурів та собак: 14 UA 116053 C2 5 10 15 20 25 30 Сигнали електроенцефалографії (ЕЕГ) та електроміографії (ЕМГ) вимірювали шляхом телеметрії, використовуючи радіотелеметричні імплантати (Data Science Int.). (1) У щурів (нічні види): Сполуку з Пр. 7, сполуку з Пр. 11 та кофеїн дозували п.о. шляхом примусового годування через зонд у зазначеній дозі та момент часу. Умови були наступними: Освітлення вимикали у 11 годин, лікарський засіб або носій 16:30, кофеїн або носій у 17.00, освітлення вмикали у 23 години, онлайн безперервні радіотелеметричні записи ЕЕГ, ЕМГ, терморегуляції та локомоторної активності впродовж декількох добових циклів. Послаблюючі ефекти антагоністів орексинового рецептору визначали кількісно для сили, ефективності, початку ефектів на електрофізіологічних маркерах. На фігурі 1 показана активність (імпульси на хвилину, n=8 тварин) в залежності від часу (сіра зона представляє нічний активний період). Дозування лікарського засобу або носія зазначено у (1), 30 хвилин перед дозуванням кофеїну або носія, зазначених у (2). Криві показують: (A): носій у (1) та носій у (2); (B): сполука з Пр. 7-HCl сіль (108 мг/кг п.о.) у (1) та носій у (2); (C): носій у (1) та кофеїн у (2); та (D): сполука з Пр. 7-HCl сіль (108 мг/кг п.о.) у (1) та кофеїн у (2). На фігурі 2 показана активність (імпульси на хвилину, n=8 тварин) в залежності від часу (сіра зона представляє нічний активний період). Дозування лікарського засобу або носія зазначено у (1), 30 хвилин перед дозуванням кофеїну або носія, зазначених у (2). Криві показують: (A): носій у (1) та носій у (2); (B): сполука з Пр. 11 (100 мг/кг п.о.) у (1) та носій у (2); (C): носій у (1) та кофеїн у (2); та (D): сполука з Пр. 11 (100 мг/кг п.о.) у (1) та кофеїн у (2). (2) У собак (денні види): Сполуку з Пр. 7 та кофеїн дозували п.о. шляхом примусового годування через зонд у зазначеній дозі та момент часу. Умови були наступними: Освітлення вимикали у 7 годин ранку, лікарський засіб або носій у 13:30, кофеїн або носій у 14 год., освітлення вмикали у 19 год. вечора, онлайн 24 год. радіотелеметричні записи (10 год. ранку -10 год. ранку) ЕЕГ, ЕМГ, терморегуляції та локомоторної активності. Ефекти тестуємої сполуки визначали кількісно відносно сили, ефективності, початку та тривалості ефектів на електрофізіологічні та клінічні маркери збудження кофеїном та гіперактивності у собак. На фігурі 3 представлений час, проведений у активному неспанні (% загального часу, n=8 тварин) у залежності від часу (з 13.00 до 7 год. ранку, сіра зона являє нічний неактивний період з 19.00 до 7 год. ранку). Дозування лікарського засобу або носія зазначено у (1), 30 хвилин перед дозуванням кофеїну або носія, зазначених у (2). Криві показують: (A): носій у (1) та носій у (2); (B): сполука з Пр. 7 (90 мг/собаку) у (1) та носій у (2); (C): носій у (1) та кофеїн у (2); та (D): сполука з Пр. 7 (90 мг/собаку) у (1) та кофеїн у (2). ФОРМУЛА ВИНАХОДУ 35 1. Застосування сполуки формули (І) CH3 Ar N Ar 40 1 2 O Формула (І) або її фармацевтично прийнятної солі для приготування лікарського засобу для попередження або лікування вечірньої сплутаності; де сполука формули (І) знаходиться у абсолютній конфігурації (S); 1 Аr являє собою O N N N N N N , 2 та Аr являє собою N або N ; 15 UA 116053 C2 H N N H N Cl N , N H N N 5 10 15 20 25 30 35 H N CF3 F N Br , N , H N H N H N Cl Br CF3 N H N OCF3 N , H N N Cl , , O Cl O , aбо . 2. Застосування за п. 1, у якому сполука являє собою: [(S)-2-(5-хлор-4-метил-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метил-2-піримідин-2ілфеніл)-метанон; [(S)-2-(5-бром-7-метил-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метил-2-[1,2,3]триазол2-ілфеніл)-метанон; [(S)-2-(5-бром-7-метил-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метил-2-піримідин-2ілфеніл)-метанон; [(S)-2-(5-хлор-4-метил-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метокси-2[1,2,3]триазол-2-ілфеніл)-метанон; [(S)-2-(6-бром-5-фтор-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метил-2-[1,2,3]триазол-2ілфеніл)-метанон; [(S)-2-(5,6-диметокси-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метил-2-[1,2,3]триазол-2ілфеніл)-метанон; [(S)-2-(5,6-диметокси-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метил-2-піразол-1ілфеніл)-метанон; [(S)-2-(5,6-диметокси-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метокси-2-[1,2,3]триазол2-ілфеніл)-метанон; [(S)-2-(6-хлор-5-трифторметил-1H-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метил-2[1,2,3]триазол-2-ілфеніл)-метанон; (5-метил-2-[1,2,3]триазол-2-ілфеніл)-[(S)-2-метил-2-(5-трифторметил-1Н-бензоімідазол-2-іл)піролідин-1-іл]-метанон або (5-метил-2-[1,2,3]триазол-2-ілфеніл)-[(S)-2-метил-2-(5-трифторметокси-1Н-бензоімідазол-2-іл)піролідин-1-іл]-метанон, або його фармацевтично прийнятну сіль. 3. Застосування за п. 1, у якому сполука являє собою: [(S)-2-(5-бром-7-метил-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метил-2-піримідин-2ілфеніл)-метанон або його фармацевтично прийнятну сіль. 4. Застосування за п. 1, у якому сполука являє собою: [(S)-2-(5-хлор-4-метил-1Н-бензоімідазол-2-іл)-2-метилпіролідин-1-іл]-(5-метокси-2[1,2,3]триазол-2-ілфеніл)-метанон або його фармацевтично прийнятну сіль. 5. Застосування за будь-яким з пп. 1-4, у якому лікарський засіб призначений для попередження або лікування вечірньої сплутаності у пацієнта, який має деменцію типу Альцгеймера. 6. Застосування за п. 5, у якому пацієнт має помірну стадію деменції Альцгеймера. 7. Застосування за будь-яким з пп. 1-6, у якому вечірня сплутаність являє собою післяобідню вечірню сплутаність. 8. Застосування за будь-яким з пп. 1-7, у якому лікують підвищене збудження. 16 UA 116053 C2 Комп’ютерна верстка Л. Ціхановська Міністерство економічного розвитку і торгівлі України, вул. М. Грушевського, 12/2, м. Київ, 01008, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 17
ДивитисяДодаткова інформація
Назва патенту англійськоюUse of benzimidazole-proline derivatives
Автори англійськоюBoss, Christoph, Roch, Catherine, Brotschi, Christine, Gude, Markus, Heidmann, Bibia, Jenck, Francois, Sifferlen, Thierry, Steiner, Michel, Williams, Jodi T.
Автори російськоюБосс Кристоф, Рох Катерин, Бротши Христина, Гудэ Маркус, Хэйдманн Бибия, Енк Франсуа, Сифферлен Тьери, Штайнер Мишель, Вилльямс Джоди Т.
МПК / Мітки
МПК: A61K 31/506, A61K 31/4178, C07D 403/14, A61K 31/4192
Мітки: бензоімідазолу-проліну, похідних, застосування
Код посилання
<a href="https://ua.patents.su/19-116053-zastosuvannya-pokhidnikh-benzoimidazolu-prolinu.html" target="_blank" rel="follow" title="База патентів України">Застосування похідних бензоімідазолу-проліну</a>
Попередній патент: Аеротермоенергетична установка
Наступний патент: Спосіб комплексного лікування хвороби альцгеймера з включенням препаратів з матеріалу ембріофетального походження та виділених з нього клітин
Випадковий патент: Плоский електронагрівник