Похідні фосфоліпідів, що мають протипухлинну та/або антипротозойну активність, спосіб їх одержання, фармацевтична композиція на їх основі та спосіб одержання фармацевтичної композиції
Номер патенту: 39163
Опубліковано: 15.06.2001
Автори: Енгел Юрген, СТЕКАР Юрій, ХІЛГАРД Петер, НЬОСНЕР Герхард, КУТШЕР Бернхард
Формула / Реферат
1. Производные фосфолипидов общей формулы (I):
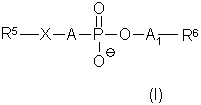
где R5 обозначает линейный или разветвленный (С10-С24)алкильный остаток, который может содержать также от одной до трех двойных и/или тройных связей,
А обозначает простую связь или одну из групп формул (II) - (VI):
-CH2-CH2-CH2-O- (II)
-CH2-CH2-O- (III)
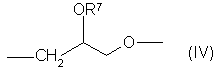
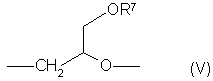
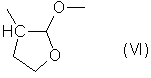
причем R7 обозначает линейную (С1-С4) алкильную группу, и группы (II) - (VI) ориентированы так, что атом кислорода связан с атомом фосфора соединения (I),
Χ обозначает атом кислорода или серы,
Α1 обозначает линейный или разветвленный (С2-С10)алкильный остаток,
R6 обозначает
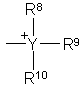
где R8, R9, R10 - одинаковые или различные, обозначают независимо друг от друга водород, линейный, разветвленный или циклический (C1-С6)алкильный остаток, или два остатка могут образовывать цикл, при этом Υ обозначает Р, As, Sb, обладающие противоопухолевой и/или антипротозойной активностью.
2. Производные по п. 1, отличающиеся тем, что они обладают противоопухолевой и/или противолейшманиозной активностью.
3. Способ получения производных формулы (I):
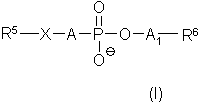
где R5 обозначает линейный или разветвленный (С10-С24)алкильный остаток, который может содержать также от одной до трех двойных и/или тройных связей,
А обозначает простую связь или одну из групп формул (II) - (VI):
-CH2-CH2-CH2-O- (II)
-CH2-CH2-O- (III)



причем R7 обозначает линейную (С1-С4)алкильную группу, и группы (II) - (VI) ориентированы так, что атом кислорода связан с атомом фосфора соединения (I),
Χ обозначает атом кислорода или серы,
A1 обозначает линейный или разветвленный (С2-С10) aлкильный остаток,
R6 обозначает

где R8, R9, R10 - одинаковые или различные, обозначают независимо друг от друга водород, линейный, разветвленный или циклический (С1-С6) алкильный остаток, или два остатка могут образовывать цикл, при этом Υ обозначает Р, As, Sb,
отличающийся тем, что взаимодействию подвергают соединение общей формулы (VII):
R5-X-A-H (VII)
где R5 обозначает линейный или разветвленный (С10-С24) алкильный остаток, который может содержать также от одной до трех двойных и/или тройных связей,
Χ обозначает атом кислорода или серы,
А обозначает простую связь или одну из групп формул (II) - (VI):
-CH2-CH2-CH2-O- (II)
-CH2-CH2-O- (III)



причем R7 обозначает линейную (С1-С4) алкильную группу, с оксихлоридом фосфора в среде растворителя или в его отсутствии, полученный продукт далее подвергают взаимодействию с соединением общей формулы (VIII):
HO-A1-R6 (VIII)
где Α1 обозначает линейный или разветвленный (С2-С10) алкильный остаток,
R6 обозначает линейный или разветвленный (С10-С24) алкильный остаток, который может содержать также от одной до трех двойных и/или тройных связей, а затем осуществляют гидролиз.
4. Способ по п. 3, отличающийся тем, что полученный продукт обрабатывают Н-ОН-ионообменником (совместная Н-ОН-ионизация) или одновременно или последовательно кислым и/или основным ионообменником.
5. Фармацевтическая композиция, содержащая активное начало, добавки и обладающая противоопухолевым и/или противолейшманиозным действием, отличающаяся тем, что в качестве активного начала она содержит эффективное количество, по крайней мере, одного производного формулы (I):
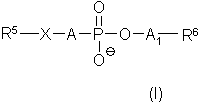
где R5 обозначает линейный или разветвленный (С10-С24) алкильный остаток, который может содержать также от одной до трех двойных и/или тройных связей,
А обозначает простую связь или одну из групп формул (II) - (VI):
-CH2-CH2-CH2-O- (II)
-CH2-CH2-O- (III)



причем R7 обозначает линейную (С1-С4)алкильную группу, и группы (II) - (VI) ориентированы так, что атом кислорода связан с атомом фосфора соединения (I),
Χ обозначает атом кислорода или серы,
Α1 обозначает линейный или разветвленный (С2-С10)алкильный остаток,
R6 обозначает

где R8, R9, R10 - одинаковые или различные, обозначают независимо друг от друга водород, линейный, разветвленный или циклический (С1-С6) алкильный остаток, или два остатка могут образовывать цикл, при этом Υ обозначает Р, As, Sb.
6. Способ получения фармацевтической композиции, обладающей противоопухолевым и/или противолейшманиозным действием, включающий смешивание фосфолипида и добавок и последующую переработку полученной смеси в обычные лекарственные формы, отличающийся тем, что в качестве фосфолипида берут эффективное количество одного или более соединений общей формулы (I):
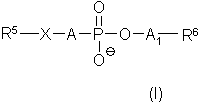
где R5 обозначает линейный или разветвленный (С10-С24)алкильный остаток, который может содержать также от одной до трех двойных и/или тройных связей,
А обозначает простую связь или одну из групп формул (II) - (VI):
-CH2-CH2-CH2-O- (II)
-CH2-CH2-O- (III)



причем R7 обозначает линейную (С1-С4) алкильную группу, и группы (II) - (VI) ориентированы так, что атом кислорода связан с атомом фосфора соединения (I),
Χ обозначает атом кислорода или серы,
Α1 обозначает линейный или разветвленный (С2-С10) алкильный остаток,
R6 обозначает

где R8, R9, R10 - одинаковые или различные, обозначают независимо друг от друга водород, линейный, разветвленный или циклический (С1-С6) алкильный остаток, или два остатка могут образовывать цикл, при этом Υ обозначает Р, As, Sb.
Текст
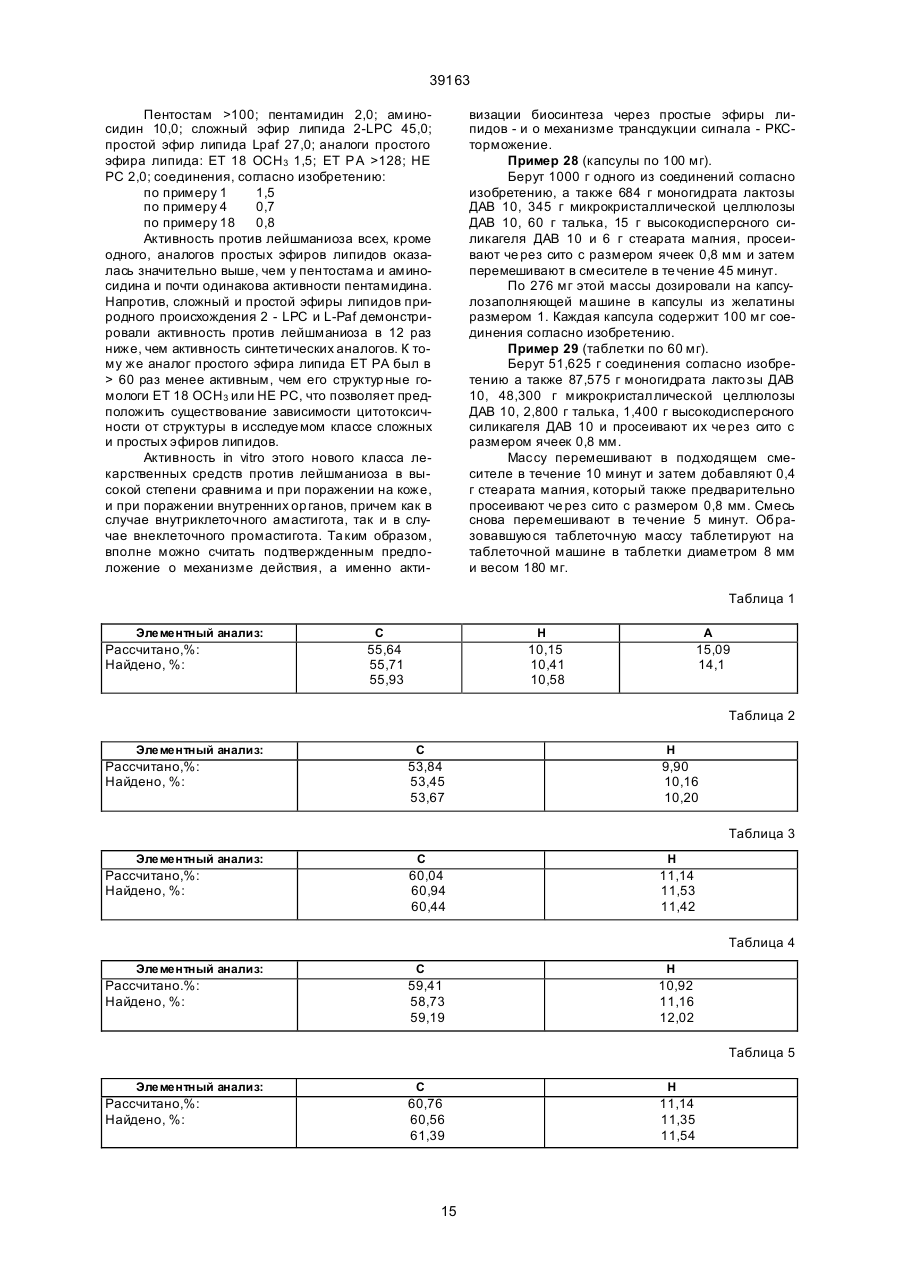
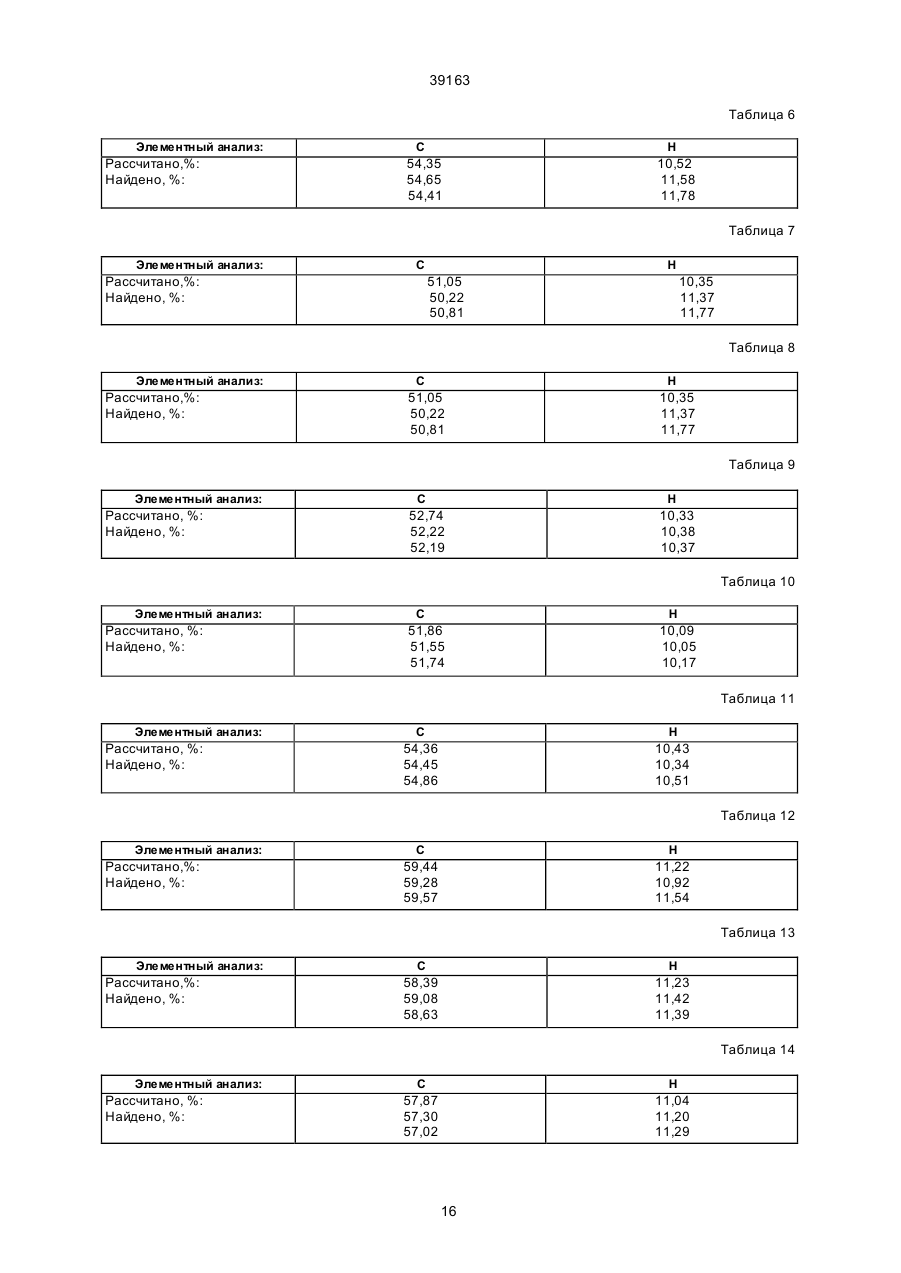
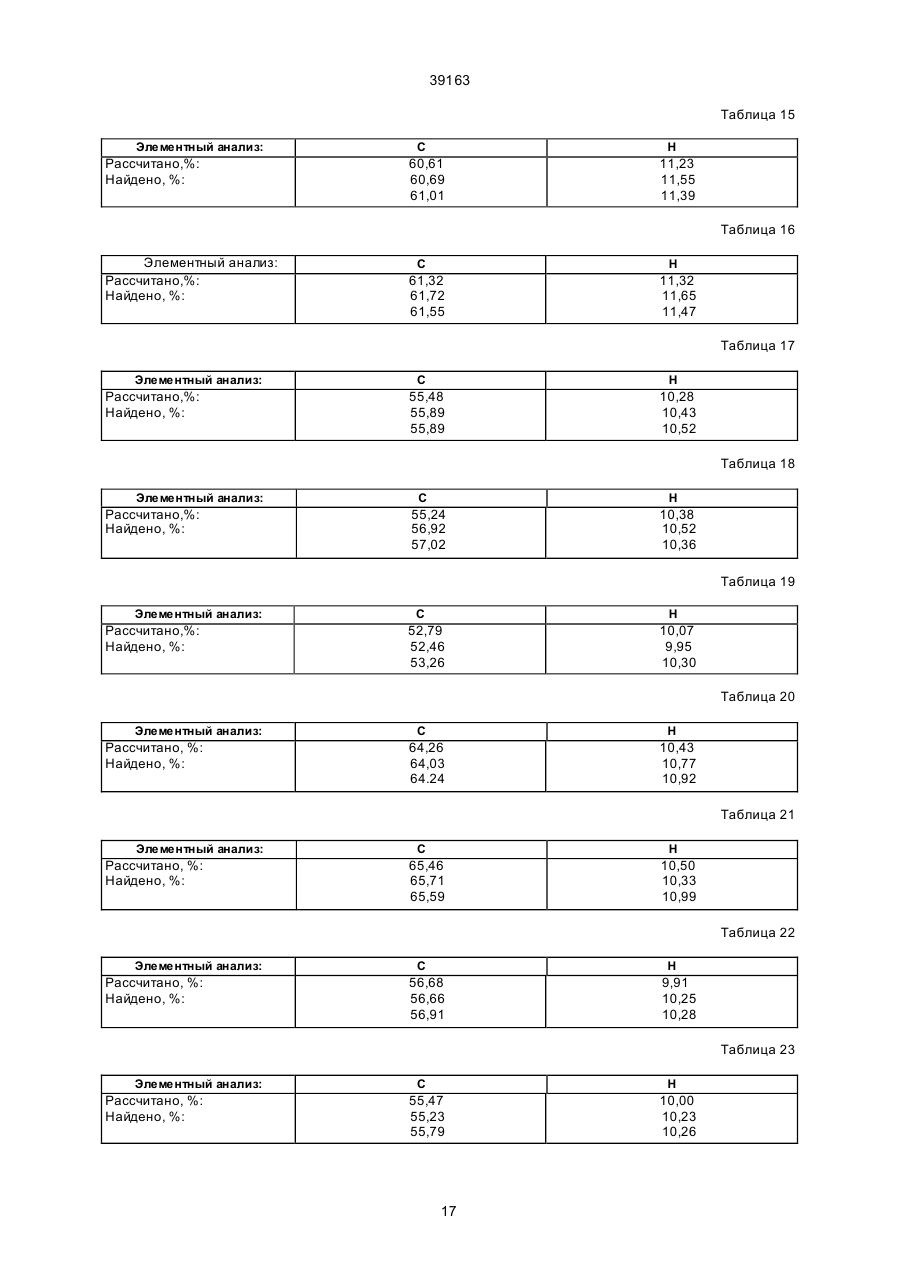
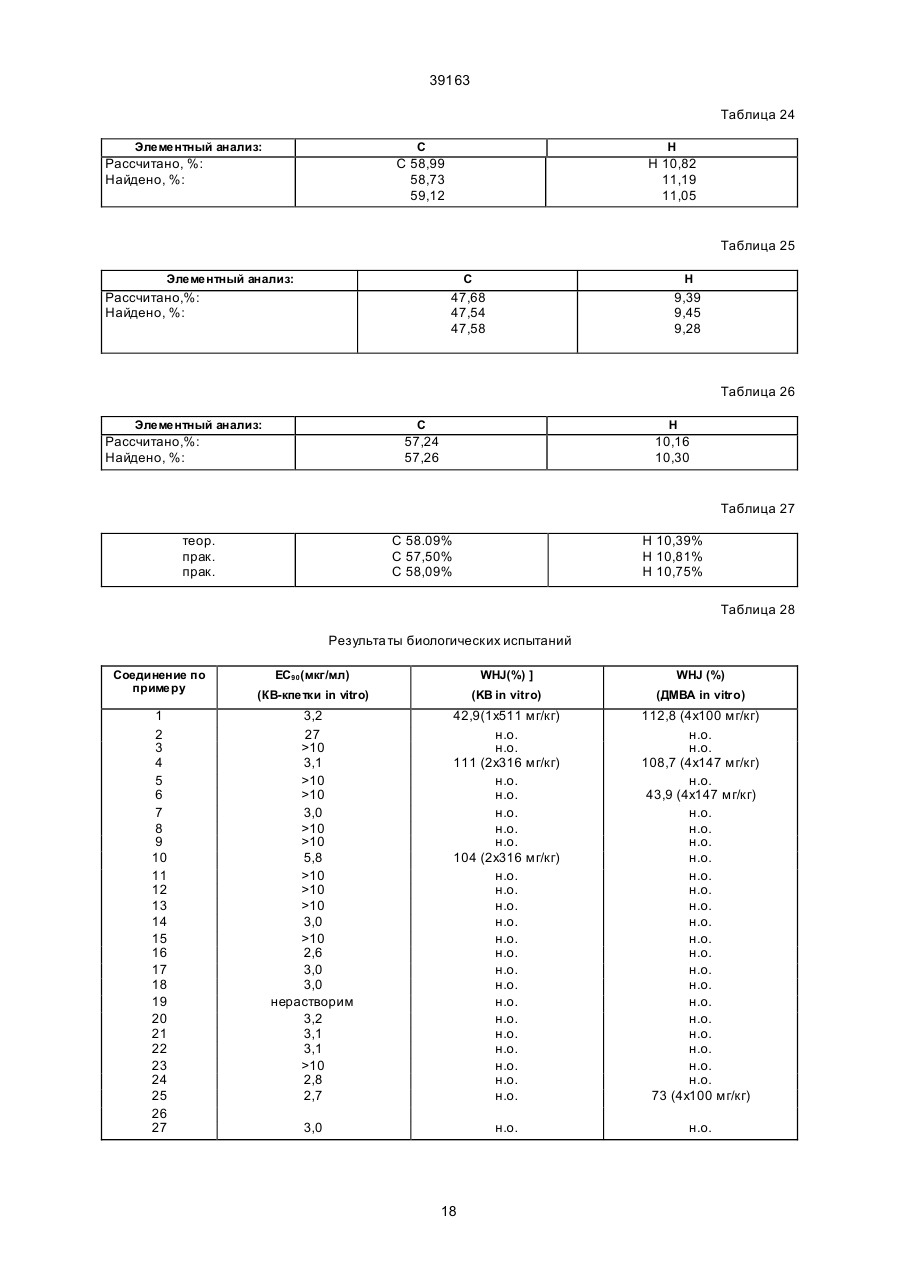
1. Производные фосфолипидов общей формулы (I): 39163 OR 7 OR7 O CH2 CH2 (IV) O (VI) O OR7 HC CH2 O O (VI) (V) причем R7 обозначает линейную (С1-С4) алкильную группу, с оксихлоридом фосфора в среде растворителя или в его отсутствии, полученный продукт далее подвергают взаимодействию с соединением общей формулы (VIII): O HC O HO-A1-R 6 (IV) R10 R9 , где R8, R9, R10 - одинаковые или различные, обозначают независимо друг от друга водород, линейный, разветвленный или циклический (С1-С6) алкильный остаток, или два остатка могут образовывать цикл, при этом Υ обозначает Р, As, Sb, отличающийся тем, что взаимодействию подвергают соединение общей формулы (VII): 5 R -X-A-H O R5 X A P O A1 O (VII) R6 , (I) где R5 обозначает линейный или разветвленный (С10-С24) алкильный остаток, который может содержать также от одной до трех двойных и/или тройных связей, А обозначает простую связь или одну из групп формул (II) - (VI): где R5 обозначает линейный или разветвленный (С10-С24) алкильный остаток, который может содержать также от одной до трех двойных и/или тройных связей, Χ обозначает атом кислорода или серы, А обозначает простую связь или одну из групп формул (II) - (VI): -CH2-CH2-CH2-O (VIII) где Α1 обозначает линейный или разветвленный (С2-С10) алкильный остаток, R6 обозначает линейный или разветвленный (С10С24) алкильный остаток, который может содержать также от одной до трех двойных и/или тройных связей, а затем осуществляют гидролиз. 4. Способ по п. 3, отличающийся тем, что полученный продукт обрабатывают Н-ОН-ионообменником (совместная Н-ОН-ионизация) или одновременно или последовательно кислым и/или основным ионообменником. 5. Фармацевтическая композиция, содержащая активное начало, добавки и обладающая противоопухолевым и/или противолейшманиозным действием, отличающаяся тем, что в качестве активного начала она содержит эффективное количество, по крайней мере, одного производного формулы (I): причем R7 обозначает линейную (С1-С4)алкильную группу, и гр уппы (II) - (VI) ориентированы так, что атом кислорода связан с атомом фосфора соединения (I), Χ обозначает атом кислорода или серы, A1 обозначает линейный или разветвленный (С2С10) aлкильный остаток, R6 обозначает R8 + Y , -CH2-CH2-CH2-O-CH2-CH2-O (II) (II) (III) OR7 -CH2-CH2-O (III) OR 7 CH2 O CH 2 (IV) OR7 O (IV) CH2 2 O (V) 39163 А обозначает простую связь или одну из групп формул (II) - (VI): O HC -CH2-CH2-CH2-O(IV) (II) -CH2-CH2-O O (III) 7 причем R обозначает линейную (С1-С4)алкильную группу, и гр уппы (II) - (VI) ориентированы так, что атом кислорода связан с атомом фосфора соединения (I), Χ обозначает атом кислорода или серы, Α1 обозначает линейный или разветвленный (С2С10) алкильный остаток, R6 обозначает OR7 R9 CH2 R 10 O (V) HC O (VI) причем R7 обозначает линейную (С1-С4) алкильную гр уппу, и гр уппы (II) - (VI) ориентированы так, что атом кислорода связан с атомом фосфора соединения (I), Χ обозначает атом кислорода или серы, Α1 обозначает линейный или разветвленный (С2С10) алкильный остаток, R6 обозначает R8 O X A P O A1 O O где R8, R9, R10 - одинаковые или различные, обозначают независимо друг от друга водород, линейный, разветвленный или циклический (С1-С6) алкильный остаток, или два остатка могут образовывать цикл, при этом Υ обозначает Р, As, Sb. 6. Способ получения фармацевтической композиции, обладающей противоопухолевым и/или противолейшманиозным действием, включающий смешивание фосфолипида и добавок и последующую переработку полученной смеси в обычные лекарственные формы, отличающийся тем, что в качестве фосфолипида берут эффективное количество одного или более соединений общей формулы (I): R5 (IV) OR7 R8 +Y O CH 2 + Y R6 , R9 R10 (I) , где R8, R9, R10 - одинаковые или различные, обозначают независимо друг от друга водород, линейный, разветвленный или циклический (С1-С6) алкильный остаток, или два остатка могут образовывать цикл, при этом Υ обозначает Р, As, Sb. где R5 обозначает линейный или разветвленный (С10-С24)алкильный остаток, который может содержать также от одной до трех двойных и/или тройных связей, ______________________________ где R1 обозначает алифатический углеводородный остаток с 8-30 С-атомами, остатки R2, R3 и R 4 являются одинаковыми или разными и обозначают водород или низшие алкильные остатки, или где группа NR2 R3 R4 обозначает циклическую аммониевую груп пу; а n обозначает 0 или 1. Для этих соединений указывается противоопухолевое действие, а также противогрибковое действие. Согласно изобретению предлагаются производные фосфолипидов общей формулы I Данное изобретение относится к области фармацевтически ценных веществ и касается обладающи х вы сокой фармацевти ческой активностью производных фосфолипидов, способа их получе ния, содержащей их фармацевтической композиции и способа получе ния этой композиции. Длинноцепочные алкилфосфохоли ны с антимикробной активностью описываются Капе aп и др. Nippon Kayaku Kaishi, 9, 1452 (1984). Европейская патентная заявка № 108565, кл. МПК C07F 9/09, 9/58, А61К 31/685, A01N 57/10, опубл. 1984 (заявитель: Taked) 3 39163 где R5 обозначает линейный или разветвленный С10-С24-алкильный остаток, который может содержать также от одной до трех двойных и/или тройных связей; А обозначает простую связь или одну из групп фор мул II - VI где R5 обозначает линейный или разветвленный С10-C24-алкильный остаток, который может содержать также от одной до трех двойных и/или тройных связей; Х обозначает атом кислорода или серы; А обозначает простую связь или одну из групп фор мул II - VI (II) (II) (III) (III) (IV) (IV) (V) (V) (VI) (VI) причем R7 обозначает линейную С1-С 4-алкильную груп пу и группы II - VI ориентированы так, что атом кислорода связан с атомом фосфо ра соединения I; Х обозначает атом кислорода или серы; A1 обозначает линейный или разветвленный С2 - С10-алкильный остаток; R6 обозначает А1 обозначает линейный или разветвленный С 2 С10-алкильный оста ток; R6 обозначает Cогласно изобретению проводят взаимодействие соединения общей фор мулы VII R5 - X - А - Н, где R8, R9, R 10 - одинаковые или различные, обозначают независимо друг от др уга водород, линейный, разветвленный или циклически С 1-C6-алкильный остаток, или два остатка могут образовывать цикл, при этом Y обозначает Р, As, Sb или Bi, в качестве лекарственного средства. Кроме того, производные общей формулы I обладают противоопухолевой и/или противолейшманиозной активностью. Задачей изобретения является также разработка способа получения производных общей формулы I. Поставленная задача достигается тем, что способ получе ния получе ния производных общей формулы I (VII) где R5 обозначает линейный или разветвленный С10-C24 -алкильный оста ток, который может содержать также от одной до трех двойных и/или тройных связей; Х обозначает атом кислорода или серы; А обозначает простую связь или одну из групп фор мул II - VI (II) (III) (IV) |O| e (V) (I) 4 39163 Поставленная задача достигается тем, что Фармацевти ческая композиция, содержащая активное начало и добавки и обладающая противоопухолевым и/или противолейшманиозным действием, согласно изобретению, в качестве активного начала содержит по крайней мере одно производное формулы I (VI) с оксихлоридом фосфо ра в среде растворителя или в его отсутствии, получен ный продукт далее подвергают взаимодействию с соединением общей фор мулы VIII (I) 6 НО - А1 - R , где R5 обозначает линейный или разветвленный С10-C24-алкильный остаток, который может содержать также от одной до трех двойных и/или тройных связей; А обозначает простую связь или одну из групп фор мул II – VI где А1 обозначает линейный или разветвленный C2- С10-алкильный остаток; R5 обозначает линейный или разветвленный С10-С24-алкильный остаток, который может содержать также от одной до трех двойных и/или тройных связей; а затем осуществляют гидролиз. Кроме того, полученный продукт обрабатывают Н-ОН-ионообменником (совместного Н-ОНионирования) или одновременно или последовательно кислым и/или основным ионообменником. Предлагаемые согласно изобретению соединения можно применять в качестве лекарственного средства, в частности для терапии опухо лей и лечения кожных и аутоиммунных заболеваний. Для терапии заболеваний, вызванных простейшими, пригодны, например, соединения формулы I с Y в значении As и Sb. Сверх того, все соединения особенно пригодны в качестве средств против оп ухолевых заболеваний. Предлагаемые согласно изобретению соединения пригодны для терапии заболеваний крови, как, например, анемий, которые могут возникать в сочетании с опухо левыми заболеваниями. Далее предлагаемые согласно изобретению соединения можно применять для терапии заболеваний костной системы, например остеопороза. Далее соединения формулы I можно использовать для терапии вирусных заболеваний и бактериальных инфекций. Соединения отличаются низкой токсичностью. Так, соединения согласно примеру 3 при одноразовом введении перорально мыши имеет ЛД50 более чем 1470 мг/кг веса тела. Объектом изобретения также является фармацевтическая композиция, которая содержит соединение формулы I, и способ ее получе ния. Наиболее близкой по сущности и достигаемому результату к заявляемой композиции является фармацевтическая композиция, описанная в кн. Машковский М.Д. Лекарственные средства.- М.: Медицина, 1986, ч. II, с. 348. Известная композиция содержит динатриевую соль комплексного соединения пятивалентной сурьмы и глюконовой кислоты в качестве активного начала и добавки. Чаще все го препарат применяют в виде подкожных инъекций для лечения разных форм лейшманиоза. Недостатком известной композиции является относительно уз кая область ее применения. В основу настоящего изобретения поставлена задача - создать фармацевти ческую композицию более широкого спектра действия. (II) (III) (IV) (V) (VI) причем R7 обозначает линейную С 1-С4-алкильную груп пу и груп пы II - VI ориентированы так, что атом кислорода связан с атомом фосфо ра соединения I; Х обозначает атом кислорода или серы; А обозначает линейный или разветвленный С2-С10-алкильный остаток; R6 обозначает где R8, R9, R 10 - одинаковые или различные, обозначают независимо друг от др уга водород, линейный, разветвленный или циклически С 1-С6-алкильный остаток, или два остатка могут образовывать цикл, при этом Y обозначает Р, As, Sb или Bi в эффективном количестве. Наиболее близким по технической сущности и достигаемому результа ту способом получе ния 5 39163 фармацевтической композиции является способ, описанный в заявке ЕПВ № 0108565, кл. МПК C07F 9/09, 9/58, А61К 31/685, А 01 N 57/10, опубл. 1984. Известный способ включает смешивание фосфолипида с добавками и последующую переработку в обычные лекарственные формы. Недостатком известного способа является то, что он позволяет получить фармацевтическую композицию, которая обладает ограниченным действием, в частности противоопухолевым и противогрибковым. В основу настоящего изобретения поставлена задача разработки способа получения фармацевтической композиции более широкого действия. Поставленная задача достигается тем, что в способе получе ния фармацевтической композиции, обладающей противоопухо левым и/или противолейшманиозным действием, включающий смешивание фосфолипида и добавок, и последующую переработку получен ной смеси в обычные лекарственные формы согласно изобретению в качестве фосфо липида берут эффективное количество одного или более соединений общей формулы I R6 обозначает где R8, R9, R 10 - одинаковые или различные, обозначают независимо друг от др уга водород, линейный, разветвленный или циклически С 1-С6-алкильный остаток, или два остатка могут образовывать цикл, при этом Y обозначает Р, As, Sb или Bi. Соединения согласно изобретению получают по описанному ниже способу. Первая стадия способа состоит во взаимодействии оксихлорида фосфора со спиртом, тиоспиртом или амином в среде галогенированных углеводородов, насыщенных простых циклических эфиров, ациклических просты х эфиров, насыщенных углеводородов с 5-10 С-атомами, жидких ароматических углеводородов, которые также могут быть замещены галогенами (в особенности хло ром), или в смесях из вышеупомянуты х растворителей или без растворителей, в случае необходимости в присутствии обычного для этой цели основного вещества. В качестве галогенированных углеводородов принимают во внимание, например, углеводороды с 1-6 С-атомами, причем один или несколько или все атомы водорода могут быть заменены атомами хлора. Например, используют метиленхлорид, хло роформ, этилендихлорид, хлорбензол, дихлорбензол. В случае, если речь идет о замещенных га логенами ароматических углеводородах, то они предпочтительно замещены одним или двумя атомами галогенов. В качестве насыщенных циклических простых эфиров можно применять, например, простые эфиры с 5-6-членным кольцом, которые состоят из атомов углерода и одного или двух а томов кислорода. Примерами таких эфиров являются тетрагидрофуран и диоксан. Ациклические простые эфиры состоят из 2-8 С-атомов и являются жидкими. Например, принимают во внимание: диэтиловый эфир, диизобутиловый эфир, метилтретбутиловый эфир, диизопропиловый эфир. В качестве насыщенных углеводородов принимают во внимание неразветвленные и разветвленные углеводороды, которые состоят из 5-10 атомов углерода и являются жидкими. Например, принимают во внимание пентан, гексан, гептан, циклогексан. В качестве ароматических углеводородов принимают во внимание, например, бензол и алкилзамещенные бензолы, причем алкильные заместители состоят из 1-5 С-атомов. В качестве основных веществ, как для реакции оксихлорида фосфо ра со спиртом, тиоспиртом или амином, так и также для последующего взаимодействия с солью фосфо ния, стибония или висмутония, принимают во внимание амины, например, алифатические амины формулы NR6 R7 R8, причем R6, R7 и R8 являются одинаковыми или разными и обозначают во дород или С 1-С6-алкил, где R5 обозначает линейный или разветвленный С10-C24 -алкильный оста ток, который может содержать также от одной до трех двойных и/или тройных связей; А обозначает простую связь или одну из групп фор мул II – VI (II) (III) (IV) (V) (VI) причем R7 обозначает линейную С1-С4-алкильную группу и группы II-VI ориентированы так, что атом кислорода связан с атомом фосфо ра соединения I; Х обозначает атом кислорода или серы; А1 обозначает линейный или разветвленный С2 С10-алкильный остаток; 6 39163 или также ароматические амины, как пиридин или пиколин. Далее можно применять, например, хинолин, диизопропиламин, изохинолин, триэтиламин, основание Хюнига (Hunig, Kissel, Chem. Ber. 91 (380), 1958). При реакции взаимодействия с солью фосфо ния, стибония или висмутония необхо димые здесь основные вещества можно добавлять одновременно или также перед введением соли фосфония, стибония или висмутония. Для этой реакции в каждом случае необходим растворитель, т.е. в случае, если первую стадию реакции осуществляют без какого-либо растворителя, то теперь его нужно добавлять. Мо лярное соотношение оксихлорида фосфо ра к спирту, тиоспирту или амину составляет, например, 1,5:1 - 0,8:1. В случае, если реакцию оксихлорида фосфо ра со спиртом, соответственно, тиоспиртом или амином осуществляют в присутствии основного вещества, то количество основного вещества составляет, например, 1-3 моля, в расчете на 1 моль РОСІ3. Для последующего взаимодействия с солью фосфония, стибония или висмутония используемое количество основного ве щества составляет, например, 1 - 5 моль, в расчете на 1 моль спирта, тиоспирта или амина. Реакционная температура при взаимодействии оксихлорида фосфора со спиртом, тиоспиртом или амином составляет от -30 до +30°С, предпочтительно от -15 до 0°С, в особенности -10 - 0°С. Время этой реакции составляет, например, 0,5-5 часов, предпочти тельно 1-3 часа, в особенности 1,5-2 ча са. В случае, если реакцию проводят в присутствии основного вещества, то она протекает в общем быстро (примерно за 30 минут). Полученный продукт без вы деления и очистки в инертном растворителе вводят во взаимодействие с солью фосфо ния, стибония, арсония или висмутония формулы ОН - А1 - R6, Затем прикапывают основное вещество растворенным в одном из указанных растворителей или без растворителя. Предпочти тельно в качестве растворителей для основных ве ществ здесь применяют галогенированные углеводороды, насыщенные циклические простые эфиры, ациклические простые эфиры, насыщенные углеводороды с 5-10 Сатомами, жидкие ароматические углеводороды или смеси из выше упомянутых растворителей. Здесь речь идет о таких растворителях, которые можно применять для взаимодействия оксихлорида фосфо ра со спиртом, тиоспиртом или амином. Благодаря добавке основного вещества температура повышается. Необхо димо, чтобы температура поддерживалась в пределах 0-40°С, предпочтительно 10-30°С, в особенности 15-20°С. Реакционную смесь затем перемешивают еще при 5-30°С, предпочтительно при 15-25°С (например, в те чение 1-40 часов, предпочти тельно 3-15 часов). Гидролиз реакционной смеси осуществляют путем добавки воды, причем температуру нужно поддерживать при 10-30°С, предпочтительно 1530°С, в особенности 15-20°С. Вышеупомянутая реакционная смесь гидролиза может содержать основные вещества. В качестве таких основных веществ принимают во внимание карбонаты и гидрокарбонаты щелочных и ще лочноземельных металлов. Для полноты гидролиза затем перемешивают е ще 0,5-4 ча са, предпочти тельно 1-3 часа, в особенности 1,5-2,5 часа, при температуре 1030°С, предпочтительно 15-25°С, в особенности 1822°С. Реакционный раствор затем промывают смесью воды со спиртами (предпочтительно алифа тическими насыщенными спиртами с 1-4 С-атомами), которая может содержать еще основное вещество. Соотношение компонентов в смеси вода : спирт может составлять, например 5 - 0,5, предпочтительно 1-3 (по объему). В качестве основных веществ для промывной жидкости принимают во внимание, например, карбонаты и гидрокарбонаты щелочных и щелочноземельных металлов, а также аммиак (например, водный аммиак). Особенно предпочти тельно 3%-ный водный раствор карбоната натрия. В случае необхо димости затем можно осуществлять промывку, реакционного раствора с помощью кислого раствора. Кислую промывку предпочти тельно осуществляют для удаления непрореагировавших основных частей реакционного раствора, в особенности при применении метиленхлорида в качестве растворителя. Промывной раствор состоит из смеси воды со спирта ми. Предпочтительно принимают во внимание смеси из алифатических насыщенных спиртов с 1-4 С-атомами, причем в случае необходимости в них может присутствовать кислое вещество. Соотношение компонентов в смеси вода : спирт может составлять, например, 5 - 0,5, предпочти тельно 1-3 (по объему). В качестве кислого вещества для промывной жидкости принимают во внимание, например, соляную кислоту, серную кислоту, или винную кис (VIII) где А1 и R6 имеют вышеуказанные значения. Ар сенохолин и его соли можно получать, например, согласно данным К. Irgolic, Applied Organometallic Chemistry (1987), 1, с. 403-412, методикам. Сообразно с этим, соль фосфо ния, стибония или висмутония добавляют порциями или сразу полностью. В качестве кислот со ли фосфо ния, стибония или висмутония принимают во вни мание соли с неорга ническими кислотами (как, например, серная кислота, со ляная кисло та); да лее, соли с орга ническими кислотами как, например, ук сусная кислота , n-то луолсульфо кислота и подобные. Эту ста дию реакции осуществляют в инертном растворителе. В качестве растворителей здесь принимают во внимание такие же, которые применяют для взаимодействия оксихлорида фосфо ра со спиртом, тиоспиртом или амином, в случае, если это взаимодействие осуществляют в растворителе. 7 39163 лоту и ли монную кислоту. Особенно предпочтителен 10%-ный водный раствор соляной кислоты. Затем еще раз промывают смесью воды со спиртами. Предпочтительно принимают во внимание смеси из алифатических насыщенных спиртов с 1-4 С-атомами, причем в случае необходимости в них может еще присутствовать основное вещество. Соотношение компонентов в смеси вода:спирт может составлять, например, 5-0,5, предпочтительно 1-3. Промытые фазы затем объединяют и обычным образом сушат, и после этого растворитель (предпочтительно при пониженном давлении, например, 5-100 гПа), в случае необхо димости после добавки 150-1000 мл, предпочтительно 300-700 мл, в особенности 450-550 мл, алифатического спирта (в расчете на 1 моль сухо го продукта), удаляют. В качестве спиртов предпочти тельно используют насыщенные алифатические спирты с длиной цепи 1-5 С-атомов. Особенно предпочтительны в качестве спиртов при этом н-бутанол, изопропанол. Задачей этой спиртовой обработки является более полное удаление остаточной воды. Таким образом полученный продукт можно очищать обычным образом (например, путем хроматографии, перекристаллизации). Соединения согласно изобретению получают описанным ниже способом. Этот способ состоит во вве дении во взаимодействии циклического сложного три-эфира фосфорной кислоты с соединением формулы Х или XI. Циклический сложный эфир фосфорной кислоты получают согласно Европейскому патенту № 108565 путем взаимодействия циклического хло рангидрида сложного диэфира фосфорной кислоты со спиртом. Соединение формулы IX: тельно 1000-1750 гПа и в особенности 10001500 гПа. Продолжительность реакции составляет 0,54 часа; когда работают при повышенном давлении, например, при 1500 гПа и 85°С; то продолжительность реакции составляет 2 часа. Кроме того, соединения согласно изобретению можно получать также нижеописанным способом. Взаимодействие активированных производных сложных эфиров фосфор ной кислоты. Этот способ состоит во вве дении во взаимодействие гидрофосфа та с соединениями общей фор мулы XII: (XII) причем в фор муле XII R5, X, А, А, и R6 имеют вышеуказанные значения; Z обозначает груп пу согласно формуле X. "НО" в фор муле для гидрофосфа та может быть заменен галогенидом, тозилатом, мезилатом и трифлатом. В качестве водоотнимающих средств в реакции конденсации можно применять карбодиимиды как, например, дициклогексилкарбодиимид. В качестве растворителей для варианта способа принимают во внимание апротонные, полярные растворители как, например, ацетонитрил, диметилформамид, диметилацетамид, диметилсульфоксид, N-метилпирролидон, и хлорированные углеводороды. Температура составляет, например, 20-80°С, особенно предпочтительно 40-60°С. Продолжительность реакции составляет, например, 4 часа. Соединения по изобретению получают также тем, что соединение общей фор мулы XIII, которое представляет собой активированный на алифатическом остатке сложный эфир фосфорной кислоты (IX) причем m = 2 или 3, при повышенной температуре и в инертном растворителе вводят во взаимодействие с соединением формулы X 6 7 YR R R 8 , (XIII) где Z1 - хлор, бром, мезилат, тозилат, или йод (остальные символы имеют выше указанные значения), вводят во взаимодействие с соединением формулы (X). Эту реакцию осуществляют известным образом без растворителя или в инертном растворителе при температуре 50-150°С. В качестве растворителей принимают во внимание таковые, указанные в способе 2. Вслед за указанной выше реакцией осуществляют взаимодействие с кислотосвязующими, соответственно, галогенидсвязующими веществами как, например, Аg2СО3 , и с основаниями, например, с карбонатами щелочных и ще лочноземельных металлов и органическими аминами. В качестве растворителей используют алифатичес (X) [значения радикалов и индексов см. в формуле I]. В качестве инертных растворителей принимают во внимание алифатические нитрилы, например, как ацетонитрил, пропионитрил; далее, полярные растворители, как N-метилпирролидон, диметилформамид, диметилацетамид. Реакционная температура составляет 30140°С, предпочти тельно 50-120°С, особенно 70100°С. Можно работать как при атмосфер ном давлении, так и при повышенном давлении, причем давление составляет 1000-2000 гПа, предпочти 8 39163 кие спирты, например метанол, этанол и изопропанол. Можно работать при повышенной температуре. При выполнении всех реакций нужно соблюдать обычное в химии металлоорганических веществ исключение влаги и кислорода воздуха. Все четыре способа можно выполнять с проведением дополнительной стадии очистки. Очистку выше указанного соединения можно осуществлять тем, что остаток, который получают после выпаривания реакционной среды, в случае необхо димости при пониженном давлении, растворяют в органическом растворителе (предпочтительно, в низших спиртах с содержанием воды 0-4%, как, например, метанол, этанол, изопропанол, н-бутанол) и обрабатывают с помощью совместного НОН ионообменника или последовательно с помощью кислого и основного ионообменников. Получен ный фильтрат в та ком случае перемешивают с совместным Н-ОН-ионообменником, например, как Амберлит®МВ 3, например, в течение 1-5 часов, предпочтительно 2 часов, при температуре 10-50°С, предпочтительно 20°С. Вместо совместного Н-ОН ионообменника очистку можно осуществлять также последовательно с помощью кислого ионообменника и основного ионообменника. В качестве ионообменников можно применять все нерастворимые твердые вещества, которые содержат ионообменивающиеся группы. Кислыми ионообменниками являются такие, которые содержат, например, кислые группы, как сульфо кислотные группы, карбоксильные груп пы. Примерами являются ионообменники с сульфо кислотными группами на полистирольной матрице, как например, Amberlite®1R 120; Dowex®HCR: Duolite®C 20 или Lewatit®S 100. Слабокислыми ионообменниками являются, например, такие, которые на основе матрицы из полиакриловой кислоты как, например, Amberlite® IRC 76, Duolite®C 433 или Relite®CC, содержат группы карбоновой кислоты. В качестве основных ионообменников принимают во внимание, например, такие, которые на полимерной матрице (например, полистирольная матрица) несут первичные, вторичные, третичные или четвертичные аминогруп пы как, например, Duolite®A 101; Duolite®A 102; Duolite®A 348; Duotite ®A 365; Duolite®A 375; Amberlite®1 RA 67; Duolite®A 375; Amberlite®1 RA 458 и Duolite ®A 132. Совместными Н-ОН ионообменниками являются смеси из кислых и щелочных ионообменных смол, как например, Amberlite® МБ 1, Ambеrlite®MB 2, Amberlite ®MB 3 и Amberlite ® MB 6. Впрочем, нужно сослаться на Ullmann's Encyclopedia of Industrial Chemistry, 5-е издание (1989), т. А 14, с. 450, где описаны все имеющиеся в продаже ионообменники, которые можно использовать в способе очистки. После съема веществ с ионообменной смолы выпаривают при пониженном давлении (например) 20 торр - 200 торр при 40-70°С и после этого перекристаллизуют из га логенированных углеводородов, насыщенных алифатических кетонов, смесей спиртов с кетонами или из насыщенных или ароматических углеводородов. В качестве галогенированных углеводородов для перекристаллизации принимают во внимание, например, углеводороды с 1-6 С-атомами, причем один или несколько или все атомы водорода могут быть заменены на атомы хлора. Например, можно применять метиленхлорид, хлороформ, этиленхлорид, хлорбензол. В качестве спиртов принимают во внимание насыщенные алифатические спирты с 1-6 С-атомами и 1-3 гидроксильными группами. В качестве кетонов принимают во внимание насыщенные, алифатические кетоны с 3-6 С-атомами. Соотношение компонентов в смеси спирт:кетон составляет от 1:1 до 1:5 (по объему). Особенно предпочтительна смесь этанола с ацетоном в соотношении 1:1 (по объему). В качестве насыщенных или ароматических углеводородов принимают во внимание: высококипящий петролейный эфир, толуол, ксилол, этилбензол. Предлагаемые, согласно изобретению, соединения формулы (I) отличаются низкой токсичностью при хорошем противоопухолевом действии. Например, соединение согласно примеру 1 в опыте на L 1210-культуре клеток имеет ЭК90 = =2,9 мкг/мл. ЭК90 представляет собой эффективную концентрацию противоопухо леводействующего вещества, которая in vitro подавляет рост раковых клеток на 90% по сравнению с контрольным опытом без добавки противоопухо леводействующего вещества. Пример 1. Внутренняя соль 2-[/(октадецилокси)гидроксифосфе нил/окси]-As, As, As-триметиларсония: (название согласно номенклатуре ЮПАК) : 2,3 мл (25 ммоль) оксихлорида фосфора растворяют в 15 мл хло роформа и при 0-5°С по каплям смешивают с раствором 6,1 г (22,5 ммоль) октадеканола в 25 мл хло роформа, который содержит 8 мл пиридина. Продолжительность добавления составляет от 30 минут до 1 часа. Перемешивают еще 1 час при комнатной температуре и затем добавляют сра зу 7,4 г (30 ммоль) арсенохо линбромида. К этому раство ру по каплям добавляют 10 мл пиридина так, что бы температура не превыша ла 20-25°С. По окончании добавления дополнительно перемеши вают в течение 3 часов при комнатной температуре, после охлаждения до 5-10°С гидролизуют с помощью 4 мл воды и промывают с помощью 20 мл смеси во ды с метанолом (1:1), 20 мл 3%-но го карбоната натрия с метанолом (1:1), 20 мл 3%-ной лимонной кислоты с метанолом (1:1) и затем 20 мл смеси воды с метанолом (1:1). Ор ганическую фазу суша т над суль фа том магния, концентрируют и остаток обрабатывают 96%-ным этанолом. После отфильтровывания перемешивают с 30 г ионообменника Amberlite MB.3. 9 39163 Отсасывают через смесь кизельгура с активным углем, концентрируют в ва кууме и кристаллизуют из ацетона. Выход 2,54 г (23%). Элементный анализ приведен в табл. 1. Тонкослойная хроматограмма [хлороформ/метанол/ 1 М ацетат натрия в 25%-ном аммиаке - 70: 40:10]Rf = 0,53. Пример 2. Внутренняя соль 2-1 [ (гексадецилокси)гидроксифосфенил]окси]-А5, As, As-триметиларсония: (название согласно номенклатуре ЮП АК): получе на аналогично примеру 1: из 4,6 мл (50 ммоль) оксихлорида фосфора, 12,2 г (45 ммоль) октадеканола, 16+20 мл пиридина и 12,1 г (60 ммоль) фосфохолинбромида. Очистка путем обработки с помощью 50 г ионообменника Amberlite MB 3 в 96%-ном этаноле. Выход 2,1 г (10%). Элементный анализ приведен в табл. 3. Тонкослойная хроматограмма (хлороформ/метанол/1М ацетат натрия в 25%-ном аммиаке = 70:40:10):Rf=0,45. Пример 5. Внутренняя соль 2-[[(гексадецилокси)гидроксифосфе нил ]окси ]-Р, Р, Р-триметилфосфо ния: Получение аналогично примеру 1 из 2,3 мл (25 ммоль) оксихлорида фосфора, 5,5 г (22,5 ммоль) гексадеканола, 8-10 мл пиридина и 7,4 г (30 ммоль) арсенхо линбромида. Очистка путем обработки с помощью 23 г ионообменника Amberlite MB 3 в 96%-ном этаноле. Выход 1,4 г (13%). Элементный анализ приведен в табл. 2. Тонкослойная хроматограмма (хлороформ/метанол/1 М ацетат натрия в 25%-ном аммиаке = 70: 40:10): Rf = 0,48. Пример 3. Внутренняя соль 2-[[(цис-13-докозенилокси)гидроксифосфенил ]окси]-As, As, As триметиларсония (название согласно номенклатуре ЮПАК) Получение аналогично примеру 1 из 4,6 мл (50 ммоль) оксихлорида фосфо ра, 10,9 г (45 ммоль) гексадеканола, 16+20 мл пиридина и 12,1 г (60 ммоль) фосфохолинбромида. Очистка путем обработки с помощью ионообменника Amberlite MB 3 в 96%-ном этаноле. Выход 5,2 г (27%). Элементный анализ приведен в табл. 4. Тонкослойная хроматограмма [хлороформ/метанол/1М ацетат натрия в 25%-ном аммиаке = 70: 0: 0]:Rf=0,43. Пример 6. Внутренняя соль 2-[[(цис-13-докозенилокси)гидроксифосфенил ]окси ]-Р,Р, Р-триметилфосфо ния: Получение аналогично примеру 1 из 3,5 мл (38 ммоль) оксихлорида фосфо ра, 11,2 г (34 ммоль) эруцилового спирта, 12+15 мл пиридина и 9,2 г (46 ммоль) фосфо холинбромида. Очистка путем обработки с помощью 45 г ионообменника Amberlite MB 3 в 96%-ном этаноле. Выход 1,9 г (11%). Элементный анализ приведен в табл. 5. Тонкослойная хроматограмма (хлороформ/метанол/1 М ацетат натрия в 25%-ном аммиаке = 70:40:10):Rf=0,47. Пример 7. Внутренняя соль 2-[[ (октадецилокси)гидроксифосфе нил ]окси ] - As, As,As-триметилэтиларсония: Получение аналогично примеру 1 из 2,3 мл (25 моль) оксихлорида фосфора, 7,3 г (22,5 ммоль) эруцилового спирта, 8+10 мл пиридина и 7,4 (30 ммоль) арсенохолинбромида. Очистка путем обработки с помощью 23 г ионообменника Amberlite MB 3 в 95%-ном этаноле. Выход 1,1 г. Элементный анализ: Рассчитано %: С 55,28; Н 10,31; Найдено, %: С 54,98; Н 10,19 С 55,08; Н 10,30 Тонкослойная хроматограмма [хлороформ/метанол/1М ацетат натрия в 25%-ном аммиаке - 70:40:10]:Rf = 0,52. Внутренняя соль 2-[[(октадецилокси)гидроксифосфе нил]окси]-Р,Р,Р-триметилфосфония (название согласно номенклатуре ЮП АК): Получение аналогично примеру 1 из 3,5 мл (38 ммоль) оксихлорида фосфо ра, 9,33 г (35 10 39163 ммоль) октадеканола, 12+5 мл пиридина и 13,2 г (46 ммоль) триэтил-/2-гидроксиэтил/-арсонийбромида. Очистка путем обработки с помощью ионообменника Amberlite MB 3 в 96%-ном этаноле и последующей колоночной хроматографии на силикагеле с помощью смеси СН 2СІ2/СН3ОН/ 25%-ньій аммиак = 70:40:10. Выход 3,39 г (18%). Элементный анализ приведен в табл. 6. Тонкослойная хроматограмма (хлороформ/метанол/25%-ный аммиак = 80:25:5):Rf=0,60. Пример 8. Внутренняя соль 2- [[(гексадецилокси)гидроксифосфенил]окси]-As, As, As-триэтилэтиларсония: Получение аналогично примеру 1 из 4,0 мл (38 ммоль) оксихлорида фосфо ра, 10,8 г (35 ммоль) октадеканола, 14+17 мл пиридина и 13,2 г (53 ммоль) триметил-(2-гидроксиэтил)-арсонийбромида. Очистка путем обработки с помощью 30 г ионообменника Amberlite МВБ в 96% -ном этаноле и последующей колоночной хроматографии на силикагеле с помощью смеси СН 2СІ2/СН3ОН/ 25%ный аммиак = 70:40:10. Выход 1,97 г (10%). Элементный анализ приведен в табл. 9. Тонкослойная хроматограмма (хлороформ/метанол/25%-ный аммиак = 70:40:10):Rf= 0,47. Пример 11. Внутренняя соль 3-[[(гексадецилокси) гидроксифосфенил ]окси ]-As, As, As-триметилпропиларсония: Получение аналогично примеру 1 из 3,5 мл (38 ммоль) оксихлорида фосфо ра, 8,43 г (35 ммоль) гексадеканола, 12+15 мл пиридина и 13,2 г (46 ммоль) триметил-/2-гидроксиэтил/-арсонийбромида. Очистка путем обработки с помощью ионообменника Amberlite МВБ в 96%-ном этаноле и последующей колоночной хроматографии на силикагеле с помощью смеси СН 2СІ2/СН3ОН/25%ный аммиак = 70:40:10. Выход 2,26 г (13%). Элементный анализ приведен в табл. 7. Тонкослойная хроматограмма (хлороформ/метанол/25%-ный аммиак = 80:25:5):Rf=0,57. Пример 9. Внутренняя соль 2-[[(цис-13-докозенилокси)гидроксифосфенил ]окси ] - As, As, As-триэтилэтиларсония: Получение аналогично примеру 1 из 4,0 мл (43 ммоль) оксихлорида фосфора, 9,7 г (40 ммоль) гексадеканола, 14+17 мл пиридина и 13,6 г (53 ммоль) триметил-(3-гидроксиэтил)-арсонийбромида. Очистка путем обработки с помощью 30 г ионообменника Amberlite МВБ в 96%-ном этаноле и последующей колоночной хроматографии на силикагеле с помощью смеси СН 2СІ2/СН3ОН /25%ный аммиак = 70:40:10. Выход 2,0 г (10%). Элементный анализ приведен в табл. 10. Тонкослойная хроматограмма (хлороформ/метанол/25%-ный аммиак =70:40:10):Rf=0,47. Пример 12. Внутренняя соль 3[[(докозенилокси)гидроксифосфе нил]окси]-Аs, As, As-триметилпропиларсония: Получение аналогично примеру 1 из 3,5 мл (38 ммоль) оксихлорида фосфора, 11,4 г (35 ммоль) эруцилового спирта, 12 + 15 мл пиридина и 13,2 г (46 ммоль) триметил-/2-гидроксиэтил/-арсонийбромида. Очистка путем обработки с помощью 30 г ионообменника Amberlite МВБ в 96%-ном этаноле и последующей колоночной хроматографии из силикагеле с помощью смеси СН 2СІ2/СН3ОН/25%-ный аммиак=70:4:10. Выход 4,50 г (22%). Элементный анализ приведен в табл. 8. Тонкослойная хроматограмма (хлороформ/метанол/25%-ный аммиак = 80:25:5): Rf=0,57. Пример 10. Внутренняя соль 3-[[(окта децилокси) гидроксифосфе нил]окси]As, As, As-триметилпропиларсония: Получение аналогично примеру 1 из 4,0 мл (43 ммоль) оксихлорида фосфо ра, 13,0 г (40 ммоль) эруцилового спирта, 14+17 мл пиридина и 13,2 г (53 ммоль) триметил-(3-гидроксиэтил)-арсонийбромида. Очистка путем обработки с помощью ионообменника Amberlile МВБ в 96% -ном этаноле и последующей колоночной хроматографии на силикагеле с помощью смеси СН 2СІ2/СН3ОН /25%ный аммиак - 70:40:10. Выход 2,4 г (11%). Элементный анализ приведен в табл. 11. Тонкослойная хроматограмма (хлороформ/метанол/25-ный аммиак = 70:40:10):Rf=0,50. 11 39163 Пример 13. Внутренняя соль 3-[[(цис-13-докозенилокси)гидроксифосфенил ]окси ]-Р,Р,Р-триметилпропилфосфония: 55 г ионообменника Amberlite МВБ в 96%-ном этаноле и последующей колоночной хроматографии на силикагеле с помощью смеси СН 2СІ2/СН3ОН/ 25%-ный аммиак = 70:40:10. Выход: 1,86 г (10%). Элементный анализ приведен в табл. 14. Тонкослойная хроматограмма (хлороформ/метанол/1М ацетат натрия в 25%-ном аммиаке = 70:40:10):Rf=0,50. Пример 16. Внутренняя соль 3-[[(нонадецилокси)гидроксифосфе нил]окси]-Р,Р,Р-триметилэтилфосфо ния: Получение аналогично примеру 1 из 4,2 мл (45 ммоль) оксихлорида фосфо ра, 13,8 г (42 ммоль) эруцилового спирта; 14+18 мл пиридина и 12,0 г (56 ммоль) триметил-(3-гидроксипропил)-арсонийбромида. Очистка путем обработки с помощью 45 г ионообменника Amberlite МВБ в 96%-ном этаноле и последующей колоночной хроматографии на силикагеле с помощью смеси СН2СІ2/СН3ОН/25%-ный аммиак=70:40:10. Выход 2,93 г (13%). Элементный анализ приведен в табл. 12. Тонкослойная хроматограмма (хлороформ/метанол/1М ацетат натрия в 25%-ном аммиаке 70:40:10):Rf=0,25. Пример 14. Внутренняя соль 3-([(октадецилокси)гидроксифосфенил ]окси ]-Р,Р,Р-триметилпропилфосфо ния: Получение аналогично примеру 1 из 3,2 мл (35 ммоль) оксихлорида фосфо ра, 9,10 г (32 ммоль) монодеканола, 11 + 4 мл пиридина и 8,64 г (43 ммоль) фосфохолинбромида. Очистка путем обработки с помощью 23 г ионообменника Amberlite МВБ в 96%-ном этаноле и последующего кипячения 2 раза в ацетоне. Выход 1,85 г (12%). Элементный анализ приведен в табл. 15. Тонкослойная хроматограмма (хлороформ/метанол/ 1М ацетат натрия в 25%-ном аммиаке = 70:40:10:)Rf= 0,58. Пример 17. Внутренняя соль 2-[[(эйкозилокси-)-гидроксифосфе нил]окси]-Р,Р,Р-триметилэтилфосфо ния: Получение аналогично примеру 1 из 4,2 мл (45 ммоль) оксихлорида фосфо ра, 11,4 г (42 ммоль) октадеканола, 14+18 мл пиридина и 12,2 г (56 ммоль) триметил-(3-гидроксипропил)-фосфонийбромида. Очистка путем обработки с помощью 56 г ионообменника Amberlite МВБ в 96%-ном этаноле и последующей колоночной хроматографии на силикагеле с помощью смеси СН 2СІ2/СН3ОН/ /25%-ный аммиак = 70:40:10. Выход: 2,27 г /11%/. Элементный анализ приведен в табл. 13. Тонкослойная хроматограмма (хлороформ/метанол/1М ацетат натрия в 25%-ном аммиаке=70:40:10): Rf=0,50. Пример 15. Внутренняя соль 3- [ [(гексадецилок-си)гидроксифосфенил]окси]-Р,Р,Р-триметилпропилфосфо ния: Получение аналогично примеру 1 из 3,2 мл (35 ммоль) оксихлорида фосфо ра, 9,63 г (32 ммоль) эйкозанола, 11+14 мл пиридина и 8,64 (43 ммоль) фосфохолинбромида. Очистка путем обработки с помощью 25 г ионообменника Amberlite МВБ в 96%-ном этаноле и последующего кипячения 2 раза в ацетоне. Выход 0,02 г (7%). Элементный анализ приведен в табл. 16. Тонкослойная хроматограмма (хлороформ/метанол/1М ацетат натрия в 25%-ном аммиаке = 70:40:10):Rf=0,53. Пример 18. Внутренняя соль 2-[[(нонадецилокси)гидроксифосфе нил ]окси ]-As, As, As-триметилэтиларсония: Получение аналогично примеру 1 из 4,6 мл (50 ммоль) оксихлорида фосфо ра, 12,8 г (45 ммоль) нонадеканола, 16+20 мл пиридина и 14,7 г (60 ммоль) арсенохолинбромида. Очистка путем обработки с помощью 55 г ионообменника Amberlite МВБ в 96%-ном этаноле. Выход 4,05 г (18%). Элементный анализ приведен в табл. 17. Тонкос Получение аналогично примеру 1 из 4,2 мл (45 ммоль) оксихлорида фосфо ра, 10,2 г (42 ммоль) гексадеканола, 14+18 мл пиридина и 12,0 г (56 ммоль) триметил-(3-гидроксипропил)-фосфонийбромида. Очистка путем обработки с помощью 12 39163 лойная хроматограмма (хлороформ/метанол/25%ный аммиак = 80:25:5):Rf=0,45. Пример 19. Внутренняя соль 2-[[(эйкозилокси)гидроксифосфенил ]окси ]-As, As, As-триметилэтиларсония: Пример 22. Внутренняя соль 2-[[(цис-13-докозенилокси) гидроксифосфе нил ]окси ]-Р,Р-диэтил-Р-фе нилэтилфосфония: Получение аналогично примеру 1: из 4,6 мл (50 ммоль) оксихлорида фосфо ра, 13,4 г (45 ммоль) эйкозанола, 16+20 мл пиридина и 14,7 г (60 ммоль) арсенохолинбромида. Очистка путем обработки с помощью 50 г ионообменника Amberlite МВБ в 96%-ном этаноле. Выход 2,81 г (12%). Элементный анализ приведен в табл. 18. Тонкослойная хроматограмма (хлороформ/метанол /25% -ный аммиак = 80:25:5):Rf=0,45. Пример 20. Внутренняя соль 2- [[(гептадецилокси)гидроксифосфенил ]окси ]-As, As, As-триметилэтиларсония: Получение аналогично примеру 1 из 2,3 мл (25 ммоль) оксихлорида фосфора, 8,6 г (27 ммоль) эруцилового спирта, 8+10 мл пиридина и 7,28 г (27 ммоль) диэтил-(2-гидроксиэтил)-фе нилфосфонийбромида. Обрабатывают с помощью 30 г ионообменника Amberlita МВБ в 96%-ном этаноле и кристаллизуют из ацетона. Выход 2,53 г (17%). Элементный анализ приведен в табл. 21. Тонкослойная хроматограмма (хлороформ/метанол/25%-ный аммиак = 80:25:5):Rf=0,37. Пример 23. Внутренняя соль 2-[[[(4'-додецилциклогексил)метилокси] гидроксифосфе нил] окси ]-As, As, As-триметилэтиларсония: Получение аналогично примеру 1 из 4,6 мл (50 ммоль) оксихлорида фосфо ра, 11,5 г (45 ммоль) гепта деканола, 16+20 мл пиридина и 14,7 г (60 ммоль) арсенохолинбромида. Очистка путем обработки с помощью 35 г ионообменника Amberlite MBB в 96%-ном этаноле и последующего перемешива ния в ацетоне. Выход 1,20 г (6%). Элементный анализ приведен в табл. 19. Тонкослойная хроматограмма (хлороформ/метанол/1М ацетат натрия в 25%-ном аммиаке = 70:40:10): Rf=0,45. Пример 21. Внутренняя соль 2-[[(октадецилокси)гидроксифосфе нил]окси] - Р,Р-диэтил-Р-фе нилэтилфосфо ния: Получение аналогично примеру 1 из 2,4 мл (26 ммоль) оксихлорида фосфо ра) 6,50 г (23 ммоль) додецилциклогексилметанола, 9+12 мл пиридина и 7,59 г (31 ммоль) арсенохолинбромида. Очистка путем обработки с помощью 30 г ионообменника Amberlita МВБ в 96%-ном этаноле и путем перемешива ния в ацетоне. Выход 1,64 г (14%). Элементный анализ приведен в табл. 22. Тонкослойная хроматограмма (хлороформ/метанол/1М ацетат натрия в 25%-ном аммиаке = 70:40:10):Rf=0,37. Пример 24. 1-0-Октадецил-2-0-метил-рац-глицерофосфоарсенохолин: Получение аналогично примеру 1 из 2,3 мл (25 ммоль) оксихлорида фосфо ра, 7,17 г (26,5 ммоль) октадеканола, 8+10 мл пиридина и 7,28 г (26,5 ммоль) диэтил-(2-гидроксиэтил)-фе нил-фосфо нийбромида. Очистка путем обработки с помощью 21 г ионообменника Amberlita МВБ в 96%ном этаноле и двухкратной перекристаллизации из ацетона. Выход 1,76 г (13%). Элементный анализ приведен в табл. 20. Тонкослойная хроматограмма (хлороформ/ метанол/25%-ный аммиак = 80:25:5):Rf=0,37. Получение аналогично примеру 1 из 3,0 мл (33 ммоль) оксихлорида фосфо ра, 10,8 г (30 ммоль) 1-0-октадецил-2-0-метил-рац-глицерина, 11+13 мл пиридина и 9,8 г (40 ммоль) арсенохолинбромида. Очистка путем обработки с помощью 55 г ионообменника Amberlita МВБ в 96%-ном этаноле и путем перемешива ния с ацетоном. Выход 5,83 г (33%). 13 39163 Элементный анализ приведен в табл. 23. Тонкослойная хроматограмма (хлороформ/метанол/1 М ацетат натрия в 25%-ном аммиаке = 70:40:10):Rf=0,57. Пример 25. 1-0-Октадецил-2-0-метил-рац-глицерофосфо фосфо холин: фосфора, 0,87 г (3,50 ммоля) октадеканола, 11+14 мл пиридина и 1,22 г (4,28 ммоля) 1-метил-1-(2гидроксиэтил)арсенаниобромида. Очистку осуществляют путем обработки ионообменником Амберлит МБ 3, который берут в количестве 2,5 г в 96%ном этаноле. Затем осуществляют хро матографию на колонке, заполненной силикагелем с СН2СІ2/СН3ОН/ 25%-ный раствор аммиака (70:40: 10). Выход 160 мг (10%). Элементный анализ приведен в табл. 26. Температура плавления: 185°С Тонкослойная хроматограмма (СН2СІ2/СН3ОН/1М ацетат натрия в 25%-ном аммиаке 70:40:10): Rf=0,83. Согласно способу, описанному в примере 1, получе но соединение общей формулы I: Получение аналогично примеру 1 из 4,6 мл (50 ммоль) оксихлорида фосфо ра, 16,1 г (45 ммоль) 1-0-октадецил-2-0-метил-рац-глицерина, 16 + 20 мл пиридина и 12,1 г (60 ммоль) фосфохолинбромида. Очистка путем обработки с помощью 45 г ионообменника Amberlite МВБ в 96%-ном этаноле и путем перемешива ния с ацетоном. Выход: 6,25 г (26%). Элементный анализ приведен табл. 24. Тонкослойная хроматограмма (хлороформ/метанол/1М ацетат натрия в 25%-ном аммиаке 70:40:10):Rf=0,52. Пример 26. Внутренняя соль 2-[[(октадецилокси)гидроксифосфе нил ]окси ]-Sb, Sb, Sb-триметилэтилстибония: Наименование соединения (Д-51117): Внутренняя соль 2-[[(октадек-9-ин-1-илокси)гидроксифосфенил ]окси ]-Р,Р,Р-триметилэтилфосфо ния. Физико-химические данные этого соединения: Элементный анализ (Д-51117 × 1,5 Н2O) приведен в табл.27. Rf = 0,50 (SiO2, СН2СІ2/СН3ОН/1М NaOAc в 25% NH4OH 70:40:10). ЯМР (хи мическое смещение дельта в ppm) (500 МГц, СDСІ3), 0,85 (3Н, t, -СН3), 1,30 (18Н, m, -(СН2)n-), 1,45 (4Н, m, -CH2CC-CH2-), 1,57 (2Н, р, -СН2-), 2,12 (9Н, d, Р+(СН3)3), 2,75 (2Н, m, -СН2-Р+), 3,78 (2Н, q, СН2ОР(=0) (01-)-0-), 4,22 (2Н, m, -0-Р(=0)-0-СН2-С-Р+). Результа ты биологических испытаний представлены в табл. 28. Результа ты подавления лейшманиоза in vitro при употреблении ALPs представлены в табл. 29. Описание методики и результа ты испытаний на биологическую активность. Простые эфиры липидов являются важным классом мембранных липидов при лейшманиозах и используются для фиксации кодирующих гликолипидов (например, LPG, GJPLS и т.д.) и гли копротеинов (например, GP63) на промастиготной и амастиготной клеточной оболочкe (цитолемме). Поэтому изучали эффективность воздействия аналогов простых эфиров липидов, таких как Мултефосин (НЕ PC) на лейшманиозный метаболизм, т.к. предполагалось, что та кие синтетические аналоги являются новым классом противоопухо левых лекарственных средств и активируют метаболизм простых эфиров ли пидов и функции мембраны в раковых клетках. Противолейшманиозная in vitro активность ряда аналогов простых эфиров липидов сравнивали с активностью простых и сложных эфиров природного происхождения, а также с активностью уже известных лекарственных средств. Исследовали воздействие на заражение Leishmania mexicana и Leishmania donovani на стадии промастиготов на коже и внутренних органов. После 24 часов обработки Leishmania mexicana для различных лекарственных средств получи ли следующие значения ЛД50 (мкг/мл): Получение аналогично примеру 1 из 2,1 мл (23 ммоль) оксихлорида фосфо ра, 6,49 г (24,5 ммоль) октадеканола, 7 + 9 мл пиридина и 7,0 г (24 ммоль) стибонохолинбромида. Очистка путем обработки с помощью 15 г ионообменника Amberlite МВБ и последующей колоночной хроматографии на силикагеле с помощью смеси СН2Сl2/СН3ОН/25%-ный аммиак = 80:25:5. Содержащие продукты фракции обрабатывают диэтиловым эфиром и концентрируют. Выход 1,0 г (8%). Элементный анализ приведен в табл. 25. Тонкослойная хроматограмма (хлороформ/метанол/1М ацетат натрия в 25%-ном аммиаке = 70:40:10):Rf = 0,62. Пример 27. Октадецил-/2-(А-метиларсенанио)-этил/-фосфат Синтез соединения указанной выше формулы осуществляют аналогично описанному в примере 1. Берут 0,32 мл (3,50 ммоля) оксихлорида 14 39163 Пентостам >100; пентамидин 2,0; аминосидин 10,0; сложный эфир липида 2-LPC 45,0; простой эфир липида Lpaf 27,0; аналоги простого эфира липида: ЕТ 18 ОСН3 1,5; ЕТ PA >128; HE PC 2,0; соединения, согласно изобретению: по примеру 1 1,5 по примеру 4 0,7 по примеру 18 0,8 Активность против лейшманиоза всех, кроме одного, аналогов простых эфиров липидов оказалась значительно выше, чем у пентостама и аминосидина и почти одинакова активности пентамидина. Напротив, сложный и простой эфиры липидов природного происхождения 2 - LPC и L-Paf демонстрировали активность против лейшманиоза в 12 раз ниже, чем активность синтетических аналогов. К тому же аналог простого эфира липида ЕТ РА был в > 60 раз менее активным, чем его структур ные гомологи ЕТ 18 ОСН3 или НЕ PC, что позволяет предположить существование зависимости цитотоксичности от структуры в исследуе мом классе сложных и простыхэфиров липидов. Активность in vitro этого нового класса лекарственных средств против лейшманиоза в высокой степени сравнима и при поражении на коже, и при поражении внутренних ор ганов, причем как в случае внутриклеточного амастигота, так и в случае внеклеточного промастигота. Та ким образом, вполне можно считать подтвержденным предположение о механизме действия, а именно акти визации биосинтеза через простые эфиры липидов - и о механизме трансдукции сигнала - РКСторможение. Пример 28 (капсулы по 100 мг). Берут 1000 г одного из соединений согласно изобретению, а также 684 г моногидрата лактозы ДАВ 10, 345 г микрокристаллической целлюлозы ДАВ 10, 60 г талька, 15 г высокодисперсного силикагеля ДАВ 10 и 6 г стеарата магния, просеивают че рез сито с размером ячеек 0,8 мм и затем перемешивают в смесителе в те чение 45 минут. По 276 мг этой массы дозировали на капсулозаполняющей машине в капсулы из желатины размером 1. Каждая капсула содержит 100 мг соединения согласно изобретению. Пример 29 (таблетки по 60 мг). Берут 51,625 г соединения согласно изобретению а также 87,575 г моногидрата лакто зы ДАВ 10, 48,300 г микрокристаллической целлюлозы ДАВ 10, 2,800 г талька, 1,400 г высокодисперсного силикагеля ДАВ 10 и просеивают их че рез сито с размером ячеек 0,8 мм. Массу перемешивают в подходящем смесителе в течение 10 минут и затем добавляют 0,4 г стеарата магния, который также предварительно просеивают че рез сито с размером 0,8 мм. Смесь снова перемешивают в те чение 5 минут. Образовавшуюся таблеточную массу таблетируют на таблеточной машине в таблетки диаметром 8 мм и весом 180 мг. Таблица 1 Элементный анализ: Рассчитано,%: Найдено, %: C H 55,64 55,71 55,93 A 10,15 10,41 10,58 15,09 14,1 Таблица 2 Элементный анализ: Рассчитано,%: Найдено, %: C H 53,84 53,45 53,67 9,90 10,16 10,20 Таблица 3 Элементный анализ: Рассчитано,%: Найдено, %: C H 60,04 60,94 60,44 11,14 11,53 11,42 Таблица 4 Элементный анализ: Рассчитано.%: Найдено, %: C H 59,41 58,73 59,19 10,92 11,16 12,02 Таблица 5 Элементный анализ: Рассчитано,%: Найдено, %: C H 60,76 60,56 61,39 15 11,14 11,35 11,54 39163 Таблица 6 Элементный анализ: Рассчитано,%: Найдено, %: C H 54,35 54,65 54,41 10,52 11,58 11,78 Таблица 7 Элементный анализ: C Рассчитано,%: Найдено, %: H 51,05 50,22 50,81 10,35 11,37 11,77 Таблица 8 Элементный анализ: Рассчитано,%: Найдено, %: C H 51,05 50,22 50,81 10,35 11,37 11,77 Таблица 9 Элементный анализ: Рассчитано, %: Найдено, %: C H 52,74 52,22 52,19 10,33 10,38 10,37 Таблица 10 Элементный анализ: Рассчитано, %: Найдено, %: C H 51,86 51,55 51,74 10,09 10,05 10,17 Таблица 11 Элементный анализ: Рассчитано, %: Найдено, %: C H 54,36 54,45 54,86 10,43 10,34 10,51 Таблица 12 Элементный анализ: Рассчитано,%: Найдено, %: C H 59,44 59,28 59,57 11,22 10,92 11,54 Таблица 13 Элементный анализ: Рассчитано,%: Найдено, %: C H 58,39 59,08 58,63 11,23 11,42 11,39 Таблица 14 Элементный анализ: Рассчитано, %: Найдено, %: C H 57,87 57,30 57,02 11,04 11,20 11,29 16 39163 Таблица 15 Элементный анализ: Рассчитано,%: Найдено, %: C H 60,61 60,69 61,01 11,23 11,55 11,39 Таблица 16 Элементный анализ: Рассчитано,%: Найдено, %: C H 61,32 61,72 61,55 11,32 11,65 11,47 Таблица 17 Элементный анализ: Рассчитано,%: Найдено, %: C H 55,48 55,89 55,89 10,28 10,43 10,52 Таблица 18 Элементный анализ: Рассчитано,%: Найдено, %: C H 55,24 56,92 57,02 10,38 10,52 10,36 Таблица 19 Элементный анализ: Рассчитано,%: Найдено, %: C H 52,79 52,46 53,26 10,07 9,95 10,30 Таблица 20 Элементный анализ: Рассчитано, %: Найдено, %: C H 64,26 64,03 64.24 10,43 10,77 10,92 Таблица 21 Элементный анализ: Рассчитано, %: Найдено, %: C H 65,46 65,71 65,59 10,50 10,33 10,99 Таблица 22 Элементный анализ: Рассчитано, %: Найдено, %: C H 56,68 56,66 56,91 9,91 10,25 10,28 Таблица 23 Элементный анализ: Рассчитано, %: Найдено, %: C H 55,47 55,23 55,79 17 10,00 10,23 10,26 39163 Таблица 24 Элементный анализ: C H С 58,99 58,73 59,12 Рассчитано, %: Найдено, %: Н 10,82 11,19 11,05 Таблица 25 Элементный анализ: C 47,68 47,54 47,58 Рассчитано,%: Найдено, %: H 9,39 9,45 9,28 Таблица 26 Элементный анализ: С Н 57,24 57,26 Рассчитано,%: Найдено, %: 10,16 10,30 Таблица 27 теор. прак. прак. С 58.09% С 57,50% С 58,09% Н 10,39% Н 10,81% Н 10,75% Таблица 28 Результа ты биологических испытаний Соединение по примеру 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 ЕС90(мкг/мл) WHJ(%) ] WHJ (%) (КВ-кпетки in vitro) (KB in vitro) (ДМВА in vitro) 3,2 27 >10 3,1 >10 >10 3,0 >10 >10 5,8 >10 >10 >10 3,0 >10 2,6 3,0 3,0 нерастворим 3,2 3,1 3,1 >10 2,8 2,7 42,9(1х511 мг/кг) н.о. н.о. 111 (2х316 мг/кг) н.о. н.о. н.о. н.о. н.о. 104 (2х316 мг/кг) н.о. н.о. н.о. н.о. н.о. н.о. н.о. н.о. н.о. н.о. н.о. н.о. н.о. н.о. н.о. 112,8 (4х100 мг/кг) н.о. н.о. 108,7 (4х147 мг/кг) н.о. 43,9 (4х147 мг/кг) н.о. н.о. н.о. н.о. н.о. н.о. н.о. н.о. н.о. н.о. н.о. н.о. н.о. н.о. н.о. н.о. н.о. н.о. 73 (4х100 мг/кг) 3,0 н.о. н.о. 18 39163 Результа ты подавления лейшманиоза in vitro при употреблении AlPs Соединение по примеру IД50 (мкг/мл) Пентостам 1 24 4 25 1000,0 0,8 0,9 0,8 1,8 Таблица 29 Разброс мкмоли/л Примечания 0,1 0,2 1,6 1,5 1,8±0,22 3,3±0,37 Cтандарт С18, As As, ET С18,Р Р, ЕТ Примечание. Представленные в таблице данные являются средними из двух ве личин (± соответствующий разброс) Тираж 50 екз. Відкрите акціонерне товариство «Патент» Україна, 88000, м. Ужгород, вул. Гагаріна, 101 (03122) 3 – 72 – 89 (03122) 2 – 57 – 03 19
ДивитисяДодаткова інформація
Назва патенту англійськоюPhospholipid derivatives having antitumor and/or antiprotozoal activity, method for the preparation thereof, pharmaceutical composition based thereon and method for the preparation of pharmaceutical composition
Автори англійськоюNYOSNER Gerhard, STEKAR Yurii, Hilgard Peter, Kutscher Bernhard, ENGEL JUERGEN
Назва патенту російськоюПроизводные фосфолипидов, обладающие противоопухолевой и/или антипротозойной активностью, способ их получения, фармацевтическая композиция на их основе и способ получения фармацевтической композиции
Автори російськоюНЕСНЕР Герхард, СТЕКАР Юрий, Хильгард Петер, Кутшер Бернхард, Энгель Юрген
МПК / Мітки
МПК: A61P 19/10, A61K 31/665, A61P 31/04, C07F 9/09, A61P 31/12, A61P 35/00, A61P 7/02, C07F 9/94, A61P 37/00, A61K 31/67, A61P 43/00, A61K 38/00, A61P 3/00, A61P 33/02, C07F 9/655, C07F 9/90, A61K 31/675, C07F 9/10, A61K 31/66, C07F 9/6564, C07F 9/54, C07F 9/72, C07F 9/66
Мітки: мають, протипухлинну, антипротозойну, композиція, спосіб, фосфоліпідів, композиції, основі, фармацевтично, одержання, активність, похідні, фармацевтична
Код посилання
<a href="https://ua.patents.su/19-39163-pokhidni-fosfolipidiv-shho-mayut-protipukhlinnu-ta-abo-antiprotozojjnu-aktivnist-sposib-kh-oderzhannya-farmacevtichna-kompoziciya-na-kh-osnovi-ta-sposib-oderzhannya-farmacevtichno.html" target="_blank" rel="follow" title="База патентів України">Похідні фосфоліпідів, що мають протипухлинну та/або антипротозойну активність, спосіб їх одержання, фармацевтична композиція на їх основі та спосіб одержання фармацевтичної композиції</a>
Попередній патент: Тверда лікарська форма з регульованим вивільненням активного початку
Наступний патент: Елемент насадки
Випадковий патент: Спосіб моделювання розповсюдження заочеревинних рідинних утворень при гострому панкреатиті