Стабілізована фармацевтична композиція на основі рекомбінантного неглікозилованого інтерлейкіну il-2 людини у відновленому вигляді, спосіб її одержання і спосіб стабілізації даної фармацевтичної композиції
Текст
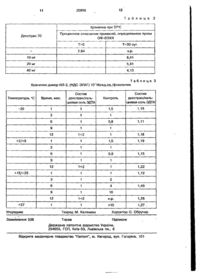
1. Стабилизированная фармацевтическая композиция на основе рекомбинатного негликозилированного интерлейкина IL-2 человека в восстановленном виде, содержащая лимонную кислоту и маннит, о т л и ч а ю щ а я с я тем, что она дополнительно содержит декстран со средней относительной молекулярной массой от 40000 до 110000 и кальциевую соль ЭДТА, при этом весовое соотношение IL-2 : декстран составляет 1;20~80. 2. Композиция ПО П.1, О Т Л И Ч а Ющ а я с я тем, что декстран имеет среднюю относительную молекулярную массу около 70000. 3. Композиция ПО П.2, о т л и ч а ю щ а я с я тем, что весовое соотношение IL-2 : декстран составляет 1:40. 4. Композиция ПО П.З, о т л и ч а ю щ а я с я тем, что весовое соотношение IL-2 : лимонная кислота : маннит : декстран : кальциевая соль ЭДТА составляет 1:10:5040:0,01. 5. Композиция по пп.1-4, о т л и ч а ю щ а я с я тем, что в ней содержится димер IL-2 а количестве не более 2%. 6. Способ получения стабилизированной фармацевтической композиции на основе рекомбииантного негликозилированного интерлейкина IL-2 человека в восстановленном виде, путем лиофилизации водного раствора, содержащего IL-2, лимонную кислоту и маннит, о т л и ч а ю щ и й с я тем, что перед лиофилизацией к водному раствору IL-2 и лимонной кислоты добавляют раствор, содержащий декстран, кальциевую соль ЭДТА и маннит, при этом весовое соотношение IL-2 : декстран составляет 1:2080. 7. Способ стабилизации фармацевтической композиции на основе рекомбинантного негликозилированного интерлейкина IL-2 человека в восстановленном виде, содержащей лимонную кислоту и маннит, о т л и ч а ю щ и й с я тем, что в фармацевтическую композицию добавляют декстран со средней относительной молекулярной массой от 40000 до 110000 и кальциевую соль ЭДТА, при этом весовое соотношение IL-2 : декстран составляет 1:20-80. Изобретение касается фармацевтической композиции на основе рекомбинантного, негликозилированного интерлейки на-2 (IL-2) человека, в восстановленном виде, имеющей улучшенную стойкость, особенно в лиофилизованном, готовом для С > ON 00 С» О 26898 использования в качестве лекарственного средства, виде. Натуральный IL-2 человека, являющийся лимфокином, способным стимулировать рост активированных Т-клеток, имеет 3 цистеина, локализованных в положениях 58, 105 и 125 последовательного ряда 133х белковых аминокислот. В натуральной молекуле цистеины 58 и 105 соединены дисульфидным мостиком, а цистеин 125 имеет свободную сульфгидрильную группу (Robb, R..J. и др. Ргос, Natl. Acad. Sci. США (1984) 81 6486-6490). Способы получения IL-2 человека, аллелей или производных, путем технологии рекомбинантной ДНК также описаны, например в европейском патенте № ЕР 091539. Получение натурального или рекомбинантного IL-2 особой чистоты, необходимой для его использования в качестве лекарства, обычно приводит к нестабильности его биологической активности, особенно при длительном хранении в жидком виде, в замороженном состоянии или в лиофилизованном виде. Известны и используются, стабилизирующие биологическую активность IL-2, вещества как, например, полиэтиленгликоль, восстанавливающие соединения, например, дитиотрейтол меркаптоэтанол или сывороточный альбумин. Так например, в заявке на Европейский патент № ЕР 0251001 описывается состав из натурального, чистого IL-2 со стабилизованной биологической активностью при длительном хранении в растворе в замороженном состоянии или в лиофилизованном виде добавлением альбумина или глобулина, при надобности, смешанных с другими агентами, такими как сахара-спирты моно- или полисахариды, такие как гидроксикрахмал или декстраны. Кроме того, новый рекомбинантный, негликозилированный IL-2 человека в восстановленном виде, проявляющий биологическую активность, по крайней мере, равную 0,5х107 Ед./мг и использующие его фармацевтические композиции, описываются (под обозначением r-hlL2) в заявке на патент [1]. Под восстановленной формой IL-2 понимают IL-2, у которого три цистеина в положениях 56, 105 и 125 содержат свободную сульфгидрильную группу, и проявляют биологическую активность, сравнимую с активностью соответствующего окисленного IL-2, содержащего дисульфидный мостик в положении 58-105. В Европейском патенте приводятся данные 5 10 15 20 25 30 35 40 45 50 55 по содержанию сульфгидрильных групп, определяемому спектрофотометрией с дитиопиридином, и по биологической активности, определяемой по разрастанию линии муриновых клеток CTLL-2. В патенте приводится пример вышеупомянутой лиофилизованной фармацевтической композиции на основе восстановленного r-hlL2, содержащей маннит и лимонную кислоту, пригодной, для инъекции, а также, например, жидкого препарата, особенно подходящего для непрерывного введения больному путем перфузии. Обычно длительное хранение фармацевтических композиций, содержащих чистый белок в качестве действующей основы и сохранение их активности - трудно совместимое требование. Такое хранение сопровождается деградацией, приводящей к утрате биологической активности протеина из-за ряда причин, например, физических изменений, таких, как образование димера или агломерата или, химических изменений, таких, как окисление или дезаминирование. Поэтому устойчивость композиции, содержащей терапевтический протеин, при хранении в течение относительно длительного периода, желательно в течение года и при надлежащей температуре, желательно близкой к +5°С - обычно необходимое условие. Достижение такой устойчивости требует добавления стабилизирующих агентов, тип которых зависит от используемого протеина. Требование улучшенной устойчивости фармацевтических композиций относится в том числе, и к вышеуказанному рекомбинантному восстановленному IL-2 и, особенно, к композициям на их основе в жидком или лиофилизованном виде, предназначающимся для применения больным. В противоположность известным композициям на основе или рекомбинантного IL-2, содержащего с положениях 56-105 дисульфидную связь и, обычно, обладающим недостаточной стабильностью биологической активности, жидкие или лиофилизованные композиции вышеуказанного восстановленного r-hlL2, которые описываются в заявке на европейский патент [1] обладают, при хранении, хорошей стабильностью такой активности, в том числе, в отсутствие альбумина. Однако образование димера, вышеупомянутого восстановленного r-hlL2, наблюдается путем натрийдисульфатного электрофореза на полиакриламидном геле (НДС-ЭПАГ), в том числе, при хранении лиофилизованных соединений при раз 26898 личных температурах, притом, без значительного проявления уменьшения биологической активности. С другой стороны, отсутствие альбумина в качестве стабилизирующего средства в композициях вышеупомянутого восстановленного r-h!L2 дает возможность проследить за их устойчивостью при помощи спектрофотометрического анализа, например, на длине 280 нм, после обрезаннофазной высокоэффективной жидкостной хроматографии (ОФ-ВЭЖХ), позволяющей выявить возможное образование примесей за счет IL-2, в зависимости от продолжительности хранения, не сопровождающееся однако уменьшением биологической активности. Несмотря на то, чго образование димера или примесей, обнаруженных путем ОФ-ВЭЖХ, в случае вышеупомянутого восстановленного r-hlL2, не сопровождается уменьшением биологической активности, которая наблюдается в пробирке, данные образования могут привести к нежелательному развитию антигенных реакций у больного при длительном применении данного средства. Задачей настоящего изобретения является создание новой стабилизированной композиции рекомбинантного негликозилированного IL-2 человека в восстановленном в виде, содержащая лимонную кислоту и маннит, характеризующаяся дополнительным содержанием декстрана и кальциевой соли ЭДТА и практически не содержащая димера JL-2 после длительного хранения, в лиофилиэованном виде, пригодном для применения в качестве лекарственного средства. Под практическим отсутствием димера понимают, что его содержание при хранении составляет значение, равное или меньше 2%. Неожиданным образом оказалось, что при хранении композиции на основе восстановленного r-h)L2 улучшение стабильности и отсутствие вышеупомянутого димера IL-2 достигается добавлением декстрана и однокальциевой динатриевой соли этилендиаминтетрауксусной кислоты (кальциевая соль ЭДТА) к раствору восстановленного r-hlL2, содержащему лимонную кислоту и маннит. Декстран ~ разветвленный полимер глюкозы, различные фракции которого определяют отдельные средние значения относительной молекулярной массы (отн.мол.м.) и в том числе используются в качестве заменителя кровяной плазмы в терапии человека. Кальциевая соль ЭДТА - хелатообразователь для фармацевтического применения. 5 10 15 20 25 30 35 40 45 50 55 Предметом настоящей заявки является, следовательно, фармацевтическая композиция рекомбинантного негликоаилированного IL-2 человека в восстановленном виде, содержащая лимонную кислоту и маннит и отличающаяся тем, что она содержит декстран и кальциевую соль ЭДТА. Рекомбинантный негликозилированный IL-2 человека в восстановленном виде согласно изобретению проявляет биологическую активность, равную как минимум 0,5хЮ7 ед./мг желательно, равнуюоколо 1x107 ед./мг в соответствии с вышеуказанным количественным анализом. Улучшение устойчивости фармацевтических композиций, состоящих из вышеопределенного восстановленного IL-2, лимонной кислоты и маннита, и добавленного Декстрана и кальциевой соли ЭДТА наблюдается у лиофилизованных композиций, длительно хранящихся при различных температурах. Улучшение устойчивости относится к физической устойчивости и химической стойкости восстановленного r-hll_2, которые можно проследить при помощи аналитических методов, например, путем НДС-ЭПАГ и ОФ-ВЭЖХ, соответственно, условия исполнения которых приводятся ниже. Согласно изобретению, фармацевтическая композиция на основе рекомбинантного негликозилированного IL-2 человека в восстановленном виде содержит лимонную кислоту и маннит и дополнительно содержит декстран со средней относительной молекулярной массой от 40000 до 110000 и кальциевую соль ЭДТА, при этом весовое соотношение IL-2: декстран составляет 1:20-80. Предпочтительно, декстран имеет среднюю относительную молекулярную массу, около 70000. Кроме того, весовое соотношение IL2 : декстран составляет 1:40. Предпочтительно, весовое соотношение IL-2 : лимонная кислота : маннит : декстран : кальциевая соль ЭДТА, приблизительно, равно 1:10:50:40:0,01. И кроме того, композиция может содержать димер IL-2, в количестве не более 2%. Предметом изобретения также является способ получения стабилизированной фармацевтической композиции на основе рекомбинантного негликозилированного IL2 человека в восстановленном виде, путем лиофилизации водного раствора, содержащего IL-2, лимонную кислоту и маннит, и дополнительно включающий стадию, которая предшествует лиофилизации, 7 26898 на которой к водному раствору IL-2 и лимонной кислоты добавляют раствор, содержащий декстран, со средней относительной молекулярной массой от 40000 до 110000 и кальциевую соль ЭДТА, при этом весовое соотношение IL-2 : декстран составляет 1:20-80, и далее, полученный таким образом раствор лиофилизуют. Ниже приводится пример получения. Кроме того, предметом настоящего изобретения является способ стабилизации фармацевтической композиции на основе рекомбинантного негликозилированного IL-2 человека в восстановленном виде, состоящий в введении в такую композицию декстрана со средней относительной молекулярной массой от 40000 до 110000 и кальциевой соли ЭДТА и при этом весовое соотношение IL-2 : декстран составляет 1:20-80. Следующие примеры иллюстрируют изобретение, не ограничивая, однако, его объема. П р и м е р 1. Фармацевтическая стабилизованная композиция восстановленного r-hlL2 для инъекций. К 1210 мл водного раствора, содержащего 2 мг/мл восстановленного r-h!L2 и 18,2 мг/мл лимонной кислоты, полученного как описывается, например, в заявке на европейский патент № Ер 0353150, добавляют 990 мл водного раствора, содержащего 88 г Декстран - 70, 0,022 г кальциевой соли ЭДТА и 110 г маннита. Полученный раствор фильтруют через пористую мембрану с диаметром пор 0,22 мкм. После распределения в стерильных условиях 1 мг, полученного, таким образом, гомогенного раствора во флакончики, с последующей лиофилизацией, флакончики-дозаторы закупоривают в азотной атмосфере, что дает возможность их хранения до использования, по крайней мере, год при температуре близкой к 4°С. Вышеуказанные лиофилизованные препараты имеют следующий состав, мг: Восстановлен. 1-2 Около 1 Лимонная к-та 10 Маннит 50 Декстран 70 40 Капьц. соль ЭДТА 0,01 Такие препараты пригодны, например, для инъекции больному, после разбавления содержимого впрыскиванием 1 мл стерильной дистиллированной воды, а также для непрерывной перфузии, например, после введения, полученного выше, раствора в перфузионный резервуар типа Виафлэкс {Viaflex) емкостью 500 мл 5% 5 10 15 20 25 30 35 8 ного глюкозного раствора для перфузии Травеноль (Travenol). П р и м е р 2. Стабилизация декстраном и кальциевой солью ЭДТА восстановленного r-hiL2. 1. Аналитические методы. а) Анализ путем ОФ-ВЭЖХ: Возможное образование примесей при хранении соединений восстановленного гhll_2, а также, дозировка восстановленного IL-2 выражаемая в мг протеина, определяются аналитической ОФ-ВЭЖХ на колонке С4 ВИДАК (0,46 х 25 см) 300 А, 5 мкм, пропускной способностью в 1 мл/ мин, линейным градиентом ацетонитрила, изменяющемся от 0 до 30% в течение 5 мин, затем, от 30% до 73% в течение 20 мин, содержащей 0,1% трифторуксусной кислоты путем спектрофотометрического анализа на длине 280 или 220 нм. б) НДС-ЭПАГ: Возможное образование димера IL-2 определяется путем электрофореза на 20%-ном акриламидном геле. Образец предварительно согревают при температуре 100°С в течение 2 мин в денатурирующем буферном растворе, содержащем 3% НДС и 5% меркаптоэтанола. Миграцию проводят в буферном растворе, содержащем 0,55% НДС, с последующим окрашиванием серебросодержащим красителем. Кажущаяся отн.мол.м. восстановленного r-hlL2 оказывается равной около 15,5 х х 104, а кажущаяся отн.мол.м. димера около 31 х 104. в) Биологическая активность: 40 Биологическую активность определяют путем измерения израстания поколений лейкозных клеток мышей рода СТ-2 путем колориметрического анализа при помощи тетразолия (Mossmann Т. и др., 45 J.Immunol, Meth (1983) 65 55-63). 2. Химическая стабилизация, восстановленного декстраном и кальциевой солью ЭДТА, r-hll_2. Химическая стабилизация r-h!L2 раз50 личными декстранами в смеси с кальциевой солью ЭДТА исследуется при температуре 37°С, позволяющей ускорить возможные химические изменения протеина и провести такое исследование в относи55 тельно краткие сроки. Исследование проводят с исходным раствором восстановленного r-hlL2, содержащего лимонную кислоту, к которой добавляют, в азотной атмосфере, раствор, содержащий кальциевую соль ЭДТА, 10 26898 маннит и один из подлежащих исследованию декстранов, соответственно. Полученный раствор лиофилизуют после распределения по 1 мл во флаконы-дозаторы, которые затем выдерживают различное время в течение месяца при 37°С. Контрольные флакончики, не содержащие ни декстрана, ни кальциевой соли ЭДТА, одновременно выдерживают при 37°С. Содержимое каждого флакончика извлекают 1 мл дистиллированной воды и анализируют путем ОФ-ВЭЖХ. Флакончики-дозаторы, испытанные на стабильность при 37°С, имели следующий состав, мг: Восстановлен. IL-2 0,55 Лимонная к-та 5 Маннит 50 Декстран 40 Кальц. соль ЭДТА 0,01 Были испытаны декстраны Т 40, Т 70 и Т 110, соответственно, выпускаемые в продажу фирмой Фармасия (франция). Были получены результаты, приведенные в табл.1. Для 40 мг дозы декстрана, т.е. при весовом отношении IL-2 : декстран, равном около 80, различные значения средней отн.мол м., изучаемых декстранов, имеют сходное значительное действие на химическую стойкость, восстановленного при 37°С r-hlt-2, в то время как в отсутствии декстрана и кальциевой соли ЭДТА, количество образующихся примесей делают невозможным расшифрование (н.р.) результатов ОФ-ВЭЖХ даже при 8-суточном периоде хранения. Влияние концентрации Декстрана 70 было проверено при 10 и 20 мг дозах, соответственно, относительно к 40 мг дозе, как указывалось выше. Были получены следующие результаты, приведенные в табл 2. Наблюдается заметное влияние Декстрана при самой небольшой дозе, соответстгсующей весовому отношению IL-2 : Декстран, равному около 1:20, на химическую стойкость восстановленного r-hlL2. 5 10 15 20 25 30 35 40 45 3. Физическая стабилизация, восстановленного декстраном и кальциевой солью ЭДТА, r-hlL2. Физическая стабилизация восстановленного декстраном смешанным с кальциевой солью ЭДТА, r-hlL2 изучалась при длительном хранении продолжительностью от одного месяца до одного года, при различных температурах: -20°С, +2/+8°С, при комнатной температуре (около 20пС, 5°С) и 37°С. Исследования проводились на описанной а примере 1 композиции. Контрольные флакончики без Декстрана и кальциевой солью ЭДТА одновременно помещают в одни и те же условия хранения. Содержимое каждого флакончика извлекают 1 мл денатурирующего, вышеупомянутого буферного раствора и анализируют путем НДС-ЭПАГ. Был определен процентный состав димера. Также определили биологическую активность во флакончиках, имеющих тот же состав Декстрана и кальциевой соли ЭДТА и хранящиеся в тех же условиях температуры. Были получены результаты, приведенные в табл.3. Характерен тот факт, что декстран/ кальциевая соль ЭДТА препятствует образованию димера при любых температурах исследования, в том числе, при комнатной температуре и при 37°С, при которых контрольный состав без декстрана и без кальциевой соли ЭДТА показывает значительное образование димера. Притом подтверждается тог факт, что физическая устойчивость, полученная при помощи декстран/кальциевая соль ЭДТА, позволяет также сохранить стабильной биологическую активность восстановленного IL-2 при любых температурах хранения. Достигаемая по способу изобретения стабильность обеспечивает длительное хранение препаратов восстановленного гhlL2, содержащего Декстран и кальциевую соль ЭДТА согласно требованиям его использования в качестве лекарственного средства. Т а б л и ц а 1 Хранение при 37°С Декстран Процентное отношение примесей, определенное путем ОФ-ВЭЖХ •т«о Т=8сут Т*15сут. Т=30 сут. _ 2,64 и.р. н.р. н.р. Декстран 40 3,17 3,65 4,35 5,13 Декстран 70 3,16 4,14 4,12 5,57 Декстран 110 2,98 3,54 ,., 3,51 4,35 , 12 26898 11 Т а б л и ц а 2 Хранение при 37°С Процентное отношение примесей, определенное путем ОФ-ВЭЖХ Декстран 70 Т-30сут. • Т=0 2,64 н.р. 10 мг 8,41 20 мг 5,81 40 мг 4,13 Таблица 3 Хранение димер ИЛ-2, (НДС-ЭПАГ) 10 Межд.ед./флакончик 7 Температура, °С Время, мес. Состав декстран/кальциевая соль ЭДТА Контроль Состав декстран/кальциевая соль ЭДТА -20 1 1 1,5 1,15 3 1 1 6 1 0,8 9 1 1 12 1+2 1 1,18 1,19 +2/+8 1,11 1 1,5 і 1 1 6 1 0,8 9 1 1 12 1+2 1 1,22 1 1 1 1,12 3 1 2 6 1 4 9 1 10 12 +37 I 3 +15/+25 1 1+2 н.р. 1,28 1 1 >10 1,27 . 1,13 1,49 Упорядник Техред М. Келемеш Коректор О. Обручар Замовлення 538 Тираж Підписне Державне патентне відомство України, 254655, ГСП, Киів-53, Львівська пл., 8 Відкрите акціонерне товариство "Патент", м. Ужгород, вул. Гагаріна, 101
ДивитисяДодаткова інформація
МПК / Мітки
МПК: A61K 38/02
Мітки: людини, даної, композиції, одержання, відновленому, спосіб, вигляді, стабілізації, основі, стабілізована, неглікозилованого, фармацевтично, рекомбінантного, композиція, фармацевтична, інтерлейкіну
Код посилання
<a href="https://ua.patents.su/6-26898-stabilizovana-farmacevtichna-kompoziciya-na-osnovi-rekombinantnogo-neglikozilovanogo-interlejjkinu-il-2-lyudini-u-vidnovlenomu-viglyadi-sposib-oderzhannya-i-sposib-stabilizaci-dano.html" target="_blank" rel="follow" title="База патентів України">Стабілізована фармацевтична композиція на основі рекомбінантного неглікозилованого інтерлейкіну il-2 людини у відновленому вигляді, спосіб її одержання і спосіб стабілізації даної фармацевтичної композиції</a>
Попередній патент: Спосіб проведення ендотермічних реакцій і пристрій для їх здійснення
Наступний патент: Гетероциклічні похідні заміщених 2-ациламіно-5-тіазолів, способи їх одержання, похідне заміщеного 2-амінотіазолу, похідне 2-аміно-4-фенілтіазолу
Випадковий патент: Спосіб очистки поверхні нанопорошків алмазу