Похідні циклічної амінокислоти, фармацевтична композиція та спосіб лікування
Номер патенту: 49011
Опубліковано: 16.09.2002
Автори: Брайанс Джастін С., Хартенштайн Йоханнес, Моррелл Ендрю І., Кнін Клер О., Реткліфф Джайлз С., Хоруелл Девід Крістофер
Формула / Реферат
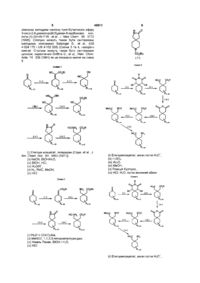
1. Похідні циклічної амінокислоти загальної формули (І)
, (I)
де
R1-R10 кожний незалежно вибраний з лінійного або розгалуженого алкілу з кількістю атомів вуглецю від 1 до 6, незаміщеного або заміщеного бензилу або фенілу, в яких замісники вибрані з галогену, алкілу, алкокси, гідрокси, карбокси, карбоалкокси, трифторметилу і нітро, і
будь-який R1-R10, якщо він не приймає значення, вказані вище, являє собою водень
та її фармацевтично прийнятні солі.
2. Похідні циклічної амінокислоти згідно з п. 1, в яких R1-R10 вибрані з метилу, етилу, пропілу, бутилу лінійного або розгалуженого.
3. Похідні циклічної амінокислоти згідно з п. 1, в яких R5 являє собою ізопропіл або трет-бутил.
4. Похідні циклічної амінокислоти згідно з п. 1, в яких R3 являє собою метил.
5. Похідні циклічної амінокислоти згідно з п. 1, в яких R1 являє собою метил або R5 являє собою метил.
6. Похідні циклічної амінокислоти згідно з п. 1, вибрані з
(1-амінометил-3-метилциклогексил)оцтової кислоти;
(1-амінометил-3-циклогексил)оцтової кислоти [IR-(1α,3β)];
(1-амінометил-4-трет-бутилциклогексил)оцтової кислоти;
цис (1-амінометил-4-метилциклогексил)оцтової кислоти;
(1-амінометил-3-метилциклогексил)оцтової кислоти [IS-(1α,3β)];
метилового ефіру (1-амінометил-3-метилциклогексил)оцтової кислоти моногідрохлориду;
[1-(ацетиламінометил)-3-метилциклогексил]оцтової кислоти;
[2-(1-амінометил-3-метилциклогексил)ацетиламіно]оцтової кислоти моногідрохлориду;
(±)-(1-амінометил-3,3-диметилциклогексил)оцтової кислоти;
(1-амінометил-3,3,5,5-тетраметилциклогексил)оцтової кислоти; і
(1-амінометил-4-метилциклогексил)оцтової кислоти.
7. Фармацевтична композиція, що містить терапевтично ефективну кількість сполуки згідно з п. 1 та фармацевтично прийнятний носій.
8. Спосіб лікування епілепсії, нападів непритомності, гіпокінезії, черепних захворювань, невродегенеративних або невропатологічних захворювань, депресії, неспокою, паніки або болю, який полягає в тому, що призначають терапевтично ефективну кількість сполуки згідно з п. 1 ссавцю, який потребує вказаного лікування.
Текст
1 ПОХІДНІ циклічної амінокислоти загальної формули (І) брані з (і-амшометил-З-метилциклогексил)оцтовоі кислоти, (і-амшометил-З-циклогексил)оцтовоі кислоти [IR 5 ПОХІДНІ ЦИКЛІЧНОЇ амінокислоти згідно з п 1, в яких Ri являє собою метил або Rs являє собою метил 6 ПОХІДНІ ЦИКЛІЧНОЇ амінокислоти згідно з п 1, ви NH (І) Де Ri-Rio кожний незалежно вибраний з ЛІНІЙНОГО або розгалуженого алкілу з КІЛЬКІСТЮ атомів вуглецю від 1 до 6, незаміщеного або заміщеного бензилу або фенілу, в яких замісники вибрані з галогену, алкілу, алкокси, гідрокси, карбокси, карбоалкокси, трифторметилу і нітро, і будь-який Ri-Rio, якщо він не приймає значення, вказані вище, являє собою водень та и фармацевтично прийнятні солі 2 ПОХІДНІ ЦИКЛІЧНОЇ амінокислоти згідно з п 1, в яких Ri-Rio вибрані з метилу, етилу, пропілу, бутилу ЛІНІЙНОГО або розгалуженого 3 ПОХІДНІ ЦИКЛІЧНОЇ амінокислоти згідно з п 1, в яких Rs являє собою ізопропіл або трет-бутил 4 ПОХІДНІ ЦИКЛІЧНОЇ амінокислоти згідно з п 1, в (1-амінометил-4-трет-бутилциклогексил)оцтовоі кислоти, цис (1-амшометил-4-метилциклогексил)оцтовоі кислоти, (і-амшометил-З-метилциклогексил)оцтовоі кислоти [IS-(1a,3[3)], метилового ефіру (1-амшометил-Зметилциклогексил)оцтовоі кислоти монопдрохлориду, [1-(ацетиламшометил)-3метилциклогексил]оцтовоі кислоти, [2-(1-амшометил-3метилциклогексил)ацетиламшо]оцтовоі кислоти монопдрохлориду, (±)-(1-амшометил-3,3-диметилциклогексил)оцтовоі кислоти, (1-амшометил-3,3,5,5тетраметилциклогексил)оцтовоі кислоти, і (1-амшометил-4-метилциклогексил)оцтовоі кислоти 7 Фармацевтична композиція, що містить терапевтично ефективну КІЛЬКІСТЬ сполуки згідно з п 1 та фармацевтично прийнятний носій 8 Спосіб лікування епілепсії, нападів непритомності, гіпокінезії, черепних захворювань, невродегенеративних або невропатологічних захворювань, депресії, неспокою, паніки або болю, який полягає в тому, що призначають терапевтично ефективну КІЛЬКІСТЬ сполуки згідно з п 1 ссавцю, який потребує вказаного лікування О о 49011 Сполуки формули H2N-CH,-j CH2-COOR, { 1 (CH2)n де Ri являє собою водень або нижчий алкільний радикал і п дорівнює 4,5 або 6 ВІДОМІ З патенту США № 4 024 175 та виділеного патенту США № 4 087 544 Властивостями цих сполук, які використовуються, є захисний ефект проти судом, що викликаються тюсемикарбазидом, захисна дія проти кардіазольних судом, церебральні захворювання, епілепсія, випадки непритомності, гіпокінезія, черепні травми, та покращення церебральних функцій Ці сполуки є корисними для геріатричних хворих Короткий зміст винаходу Нові заміщені ЦИКЛІЧНІ амінокислоти, їх ПОХІДНІ, та фармацевтичне прийнятні солі є корисними при численних розладах До таких розладів належать епілепсія, непритомність, гіпокінезія, черепні захворювання, невродегенеративні захворювання, депресії, неспокій, паніка, біль та невропатологічні захворювання Сполуки представлені формулою (І) та їх фармацевтичне прийняті солі або проліки, в яких Ri - R-іо кожний незалежно вибраний з ЛІНІЙНОГО або розгалуженого алкілу з КІЛЬКІСТЮ атомів вуглецю від 1 до 6, незаміщеного або заміщеного бензилу або фенілу, в яких замісники вибрані з галогену, алкокси, алкілу, гідрокси, карбокси, карбоалкокси, трифторметилу і нітро, і будь-який Ri - R-іо, якщо він не приймає значення, вказані вище, являє собою водень Особливо переважними сполуками згідно з винаходом є (1-амінометил-4-трет-бутил-циклогексил)оцтова кислота, (і-амшометил-З-метил-циклогексил)-оцтова кислота, (і-амшометил-З-метил-циклогексил)-оцтова кислота [І R-(1a,3p)], (і-амшометил-З-метил-циклогексил)-оцтова кислота [І S-(1a,3p)], цис (1-амшометил-4-метил-циклогексил)оцтова кислота, цис (1-амшометил-4-ізопропіл-циклогексил)оцтова кислота, (1 -амшометил-2-метил-циклогексил)-оцтова кислота, (±)-(1-амшометил-3,3-диметил-циклогексил)оцтова кислота, (1-амшометил-3,3,5,5-тетраметилциклогексил)-оцтова кислота, (1 -амшометил-4-метил-циклогексил)-оцтова кислота, метиловий ефір (1-амшометил-З-метилциклогексил)-оцтовоі кислоти монопдрохлорид, [1-(ацетиламшо-метил)-3-метил-циклогексил]оцтова кислота, і [2-(1-амшометил-3-метил-циклогексил)ацетиламшо]-оцтова кислота монопдрохлорид В заявці також описані нові проміжні сполуки, які використовуються для одержання кінцевих продуктів, а також нові способи одержання цих сполук Детальний опис винаходу Сполуки згідно з даним винаходом та їх фармацевтичне прийнятні солі визначаються формулою І Термін "алкіл" означає лінійну або розгалужену групу, що містить від 1 до 6 атомів вуглецю, яка включає, але не обмежується ними, метил, етил, пропіл, n-пропіл, ізопропіл, бутил, 2-бутил, третбутил, пентил, гексил та п-гексил Переважними групами є метил та трет-бутил Бензильна та фенільна групи можуть бути незаміщеними або заміщеними 1-3 замісниками, вибраними з галогену, алкілу, алкокси, гідрокси, карбокси, карбоалкокси, трифторметилу або нітро Галоген включає фтор, бром, хлор та йод Оскільки амінокислоти є амфотерними, фармакологічно сумісними солями у випадку, коли R є воднем, можуть бути солі з придатними неорганічними або органічними кислотами, наприклад, хлористоводневою, сірчаною, фосфорною, оцтовою, щавлевою, молочною, лимонною, яблучною, малеїновою, саліциловою, малоновою, янтарною та аскорбіновою Утворюються солі з лужними або лужноземельними металами, наприклад, натрієм, калієм, магнієм або кальцієм, починаючи з ВІДПОВІДНИХ гідроксидів або карбонатів Можуть також бути одержані солі з кватернізованими амонієвими іонами, наприклад, з іоном тетраметиламонію Карбоксильна група амінокислот може бути етерифікована відомими засобами Певні сполуки згідно з даним винаходом можуть існувати як в несольватованих формах, так і в сольватованих формах, у тому числі, у пдратованих формах Взагалі, сольватовані форми, у тому числі пдратовані, еквівалентні несольватованим формам і, мається на увазі, що вони описані в рамках даного винаходу Певні сполуки згідно з даним винаходом мають один або більше хіральних центрів, і кожний центр може існувати в R(D) або S(L) конфігураціях Даний винахід охоплює всі енантюмерні та епімерні форми, а також їх ВІДПОВІДНІ суміші Наприклад, сполука, описана в прикладі 1, являє собою суміш всіх чотирьох можливих стереоізомерів Сполука, описана в прикладі 6, являє собою один з ізомерів В цих сполуках, в яких конфігурація може бути визначена, конфігурація вуглецевих центрів циклогексанового кільця може бути R або S Сполуки згідно з винаходом можуть бути синтезовані, наприклад, з використанням загальної стратегії (Схема І, що наведена нижче), окресленої Gnffths G , et at, Helv Chirm Acta, 74 309 (1991) Альтернативно, вони можуть також бути одержані (Схема 2, наведена нижче) аналогічно до 49011 описаної методики синтезу трет-бутилового ефіру 3-оксо-2,8-діазаспіро[4,5]декан-8-карбоновоі кислоти (1) (Smith P W , et al, J Med Chem 38 3772 (1995) Сполуки можуть також бути синтезовані методами, описаними Satzmger G , et al, (US 4 024 175 і US 4 152 326) (Схема З та 4, наведені нижче) Сполуки можуть також бути синтезовані шляхом, окресленим Griffiths G , et а) , Hetv Chim Acta 74 309 (1991) як це показано нижче на схемі 5 Схема 1 NO. „CO.,Et Р) OEt O,Et МеО,С NCO МеО,С СО,Н HCI-NH, CO,H (VI) (і) Етилціа ноацетат, піперидин (Cope, et al , J Am Chem Soc 63 3452(1941)) (и) NaCN, EtOH/H2O, (їм) ЕЮН, HCI, (iv) H2O/H+, (v) H2, Rh/C, MeOH, (vi) HCI (і) Етилціаноацетат, аміак потім НзО , (м) H 2 SO 4 , (ні) Ас 2 О, (iv) MeOH, (v) Реакція Куртіуса , (vi) HCI, Н 2 О, потім аніонний обмін Схема 4 Схема 2 Ш0,С NCO МеО,С (і) Ph3P = СНСОзМе, (и) MeNO2, 1,1,3,3-тетраметилгуанідин, (їм) Нікель Ренея, ЕЮН / H2O, (iv) HCI (і) Етилціаноацетат, аміак потім НзО 49011 (м) H2SO4, (in) Ac2O, (iv) H2NOH, (v) PhSO2CI, (viJEtsN, MeOH, Схема 6 Н HCl-NH2 СЮ2 HCI-NH2 CO2Me (VII) H C I , H2O, п о т і м а н і о н н и й о б м і н Схема 5 і) (і)МеОН, НСІ Схема 7 НСІ-ПІН., СО2Н NH, CCLH МеСОН (і) МеСОСІ, NaOH, H2O Схема 8 (і) Етилціаноацетат, піперидин (Cope, et a) , J Am Chem Soc 63 3452(1941)) (n)NaCN, ЕЮН/Н2О, (in)BnOH, HCI, (iv)H2O/H+, (v)Hz, Rh/C, MeOH Прикладами проліків є HCINH, ССШе MeCOHN CO;Me н а т CONHCHXO^H HCI-NH; BnOCOKN СО г Н GONHCH,CO,Bn HCI-ЫН, CONHCH2CO2H liil Ці сполуки можуть бути синтезовані, наприклад, шляхом, описаним схемою 6 через схему 8, що подана нижче (і) BnOCOCI, Н2О, 1,4-дюксанб NaOH , (и) а) дициклогексилкарбодіїмід, пентафторфенол, етилацетат, б) гліцинбензиловий ефір, триетиламін, (III) Pd(OH)2/C, HCI, ЕЮН, Н2 Було проведено випробування зв'язування радюліганду з використанням [3Н]габапентину та а2р субодиниці, одержаної з мозкової тканини свині ("The Novel Anticonvutsant Drug, Gabapentm, Binds to the a2p Subunit og a Calcium Channel", Gee N , et at, J Biologicat Chemistry, in press) 49011 10 ТАБЛИЦЯ 1 Структура Сполука NH, ІС50 (мкм) СО 2 Н (1*амінометил-4-трет-бутилцикпогексил)оцтова кислота 200 \ \ NH2 CO2H (і-амінометил-З-метилциклогексил)оцтова кислота 0.13 a *н2 со 2 н (і-амінометил-З-метилцикпогексил)оцтова кислота [1R-(1ah 3(3)] (і-амінометил-З-метилциклогексил)оцтова кислота 11 S-( 1a, Зр)] 13 0 , NH. СО,Н 030 0 гАН , 2 СО 2 Н цис(1-амінометил-4-метилці4клогексил)оцтова кислота 10 ^н 2 со 2 н цис (1-амінометмл-4ізопропілциклогексил)оцтова кислота 10 49011 11 12 ТАБЛИЦЯ 1 (продовження) Сполука Структура NH 2 CO2H (1 -аміномети л-2-метил-цикпогексил)оцтова кислота 7 НО2С кислота НО2С {1 -амінометил-3,3,5,5-тетраметил циклогексил)оцтова кислота NH 2 HCI а ф-О-амінометил-З.З-диметилцишогексі^оцтова 1С 5 (МКМ) 0 NH2.HCI >а НО2С 0,5 10 NH2-HCI (1-амінометил-4-метилцикпогексил)оф'ова 0.33 кислота 9 Наведена вище таблиця 1 показує зв'язуючу лоту структурної формули СПОріДНеНІСТЬ СПОЛуК ЗГІДНО 3 ВИНаХОДОМ ДО (Х2Р субодиниці Габапентин (Neurontm(R|) в цих випробуваннях дає результат від 0 10 до 0 12|JM Очікується, що з цих причин сполуки згідно з даним винаходом повинні проявляти фармакологічні властивості, що порівнюються з габапентином Наприклад, як засіб при лікуванні судом, неспокою та болі Сполуки згідно з винаходом споріднені з Neurontm , комерційним лікарським препаратом, ефективним при лікування епілепсії Neurontm являє собою 1-(амшометил)-циклогексаноцтову кис Очікується, що сполуки згідно з винаходом також будуть корисними при лікуванні епілепсії Дивись дані ІС50 в вищенаведеній Табл 1 у порівнянні з Neurontm(R| Даний винахід також стосується терапевтичного застосування сполук миметичної дії як агентів для лікування невродегенеративних розладів 49011 13 Такими невродегенеративними розладами є, наприклад, хвороба Альцгеймера, хвороба Гунтшгтона, хвороба Паркінсона та амютрофний латеральний склероз Даний винахід також охоплює лікування невродегенеративних розладів, що викликаються гострими ушкодженнями мозку До таких відносяться, але не обмежуються ними удар, травма голови та асфіксія Удар розглядається як церебральне васкулярне захворювання, і також може бути віднесений до церебральних васкулярних (CVA) випадків і включає гострий тромбоемболічний удар Удар включає як фокальну так і глобальну ішемію Сюди також відносяться тимчасові церебральні ішемічні напади та ІНШІ церебральні васкулярні проблеми, пов'язані з церебральною ішемією Пацієнта піддають специфічній каротидній ендартеректомм або іншим цереброваскулярним або васкулярним хірургічним процедурам взагалі або діагностичним васкулярним процедурам, у тому числі церебральній ангіографії і таке інше До інших нещасних випадків відносяться травма голови, травма спинного мозку або ушкодження внаслідок загальної аноксії, гіпоксії, гіпоглікемії, гіпотензії, а також подібні ушкодження, що виникають в процесі емболії, пперфузм та гіпоксії Даний винахід повинен бути корисним деяких випадках, наприклад, хірургічного втручання, пов'язаного з використанням штучного кровообігу, у випадках внутрішньочерепного крововиливу, при перинатальній асфіксії, при зупинках серця, нападах епілепсії Звичайний лікар буде спроможнім визначити відповідну ситуацію, в якій суб'єкт є чутливим до удару або схильним до нього, а також зазнає удару при призначенні лікування методами згідно з даним винаходом Очікується, що сполуки згідно з даним винаходом будуть корисними при лікуванні депресії Депресія може бути результатом органічного захворювання, результатом стресу, пов'язаного з особистими втратами, або ідюпатичною в основі Існує сильна тенденція в спадковій прояві деяких форм депресії, що викликають механістичні причини для принаймні деяких форм депресії Діагностика депресії робиться спочатку КІЛЬКІСНОЮ ОЦІНКОЮ ЗМІН в настрою пацієнта Такі оцінки настрою робляться, як правило, лікарем або оцінюються невропсихологом з використанням діючої шкали оцінок, такої як Hamilton Depression Rating Scate або Brief Psychiatric Rating Scab Багаточисельні ІНШІ шкали розроблені для КІЛЬКІСНОГО визначення та вимірювання ступіню зміни настрою у пацієнта з депресією, такою як безсоння, труднощі в зосередженні, нестача енергії, відчуття непотрібності, а також почуття провини Стандарти для діагнозу депресії, а також психіатричних діагнозів зібрані в Діагностичному та статистичному посібнику по психічним захворюванням (четверте видання), який згадається як DSM-tV-R посібник, що опублікований Американською Асоціацією психіатрів, 1994 GABA є інгібітором нейротрансміттеру центральної нервової системи В рамках загального уявлення про інгібування здається схожим, що 14 GABA-міметики можуть зменшувати або інгібувати церебральні функції і можуть, таким чином, уповільнювати функцій та перешкоджати пригніченню настрою, що приводить до депресії Сполуки згідно з винаходом можуть викликати антиконвульсивний ефект шляхом збільшення нових створюваних GABA в синаптичних сполученнях Якщо габапентин дійсно збільшує рівень GABA або ефективність GABA в синаптичних сполученнях, то він може бути визначений як GABAміметик і може зменшувати або інгібувати церебральні функції і може, таким чином, уповільнювати функцій та перешкоджати пригніченню настрою, що приводить до депресії Той факт, що GABA агоніст або GABA-міметик можуть працювати саме в зворотньому напрямку шляхом перешкоджання пригніченню настрою і, таким чином, бути антидепресантом, є новою концепцією, ВІДМІННОЮ від поширеної раніше думки щодо активності GABA Очікується також, що сполуки згідно з винаходом будуть корисними при лікуванні неспокою та панічних станів, як це демонструється засобами стандартних фармакологічних процедур Матеріали і методи Каррагенін-індукована пперальгезія Пороги ноцицептивного тиску вимірювались в тестах по визначенню тиску в лапі щура з використанням анальгезиметру (Randat-Selhtto method Randat L О and SeHitto J J , A method for measurement of analgesic activity on mftamed tissue Arch, tnt Pharmacodyn 4 409-419 (1957)) Самців щурів лінії Sprague Dawley (70-90г) тренували на цьому апараті напередодні дня тестування Поступово прикладали тиск до задньої лапи кожного щура і визначали ноцицептивні пороги як тиск (г), що потрібний, щоб викликати відсмикування лапи Використовували максимальну вагу 250г, щоб попередити будь-яке ушкодження тканини лапи В день тестування було зроблено від двох до трьох вихідних вимірювань перед тим, як тварині призначали ІН'ЄКЦІЮ ЮОиі 2% каррагеншу в підощву правої задньої ноги Через 3 години після уведення каррагеншу знову визначали ноцицептивні пороги, щоб встановити, що у тварин проявляється пперальгезія Через 3,5 години після ін'єкції каррагеншу тваринам давали або габапентин (3-300мг), морфін (Змг/кг,) або салш і вивчали ноцицептивні пороги через 4, 4,5 та 5 годин після уведення каррагеншу Семікарбазид-шдуковані ТОНІЧНІ напади ТОНІЧНІ напади у мишей викликали призначенням підшкірного уведення семікарбізиду (750мг/кг) Реєстрували латентний період до тонічного випрямлення передньої лапи Те, що жодна з мишей не піддавалася конвульсіям протягом двох годин після прийому семікарбазиду, роглядалося як факт захисту з максимальним латентним періодом 120 хвилин Тварини Самців щурів лінії Hooded Lister (200-250r) одержували з tnterfauna (Huntingdon, UK) і самців мишей лінії ТО (20-25г) отримували від Bantm and Kmgman (Hull, UK) Обидва види гризунів розміщували групами по шість Десять Common Marmoset, вагою від 280 до 360г, що виведені в Медичній 49011 16 15 школі Манчестерського Університету (Manchester, ди Режим складався з чергування чотирьох 4UK) розміщували по парах Всіх тварин утримувахвилинних безкарних періодів змінного інтервалу в ли з 12-годинним циклом світло /темрява (світло межах ЗО секунд, сигналом яких було увімкнення вмикали о 7 00) та з забезпеченням їжі та води світла у камері, та трьох 3-хвилинних карних періодів при фіксованому співвідношенні 5 (шляхом Призначення ЛІКІВ удару, що супроводжував одержання їжі), сигнаЛІКИ призначали або внутрішньоочеревинно лом яких було вимкнення світла у камері Сила (IP) або підшкірне (SC) за 40 хвилин перед тестуудару регулювалася для кожного щура окремо для вання в об'ємі 1мл/кг для щурів та мавп і 10мл/кг одержання приблизно 80%-90% пригнічення реакдля мишей ції у порівнянні з безкарною реакцією Щури отриМишачий світлийл'емний бокс мували солоний наповнювач в дні тренувань Апарат являє собою бокс, що відкритий зверху, 45см довжиною, 27см шириною та 27см висоОчікується, що сполуки згідно з винаходом бутою, поділений на малі (2/5) та великі (3/5) площидуть також корисними при лікуванні болі та захвони перегородкою, що простинається на 20см вище рювань на фобію (Am J Pain Manag 5 7-9 стін (Costall В , et al , Exploration of mice in black (1995)) and white box validation as a model of anxiety Очікується також, що сполуки згідно з винахоPharmacol Boichem Behav , 32 777-785(1989)) дом будуть також корисними при лікуванні маніакальних симптомів, гострих або хронічних, поодиНа рівні підлоги в центрі перегородки існує ноких критичних або рецидивів Припускається отвір розміром 7,5x7 5см Малий ВІДДІЛОК пофартакож, що вони будуть корисними при лікуванні бований у чорний, а великий - у білий колір Білий і/або попередженні біполярних захворювань ВІДДІЛОК освітлюється 60-вт вольфрамовою лам(United States Patent Application Number 08/440 570 пою Лабораторія освітлюється червоним світлом filed May 15, 1995) Кожну мишу тестували, поміщаючи и в центр білої площі і дозволяючи їй вивчати нове середовище Сполуки згідно з винаходом можуть бути одепротягом 5 хвилин Час, проведений на освітленоржані та призначені в різних оральнихта парентему боці, вимірювали (Kilfoil Т , et al, Effects of anxральних дозованих формах Так, сполуки згідно з lohtic and anxiogemc drugs on exploratory activity in a винаходом можуть бути призначені у вигляді ІН'ЄКsimple model of anxiety in mice Neuropharmacol , 28 ЦІЙ, таких як внутрішньовенних, внутрішньом'язе901-905(1989)) вих, внутрішньошкірних, підшкірних, внутрішньодуоденальних або внутрішньоочеревинних Також Х-Лабіринт для щурів, що піднімається сполуки згідно з винаходом можуть бути признаСтандартний Х-лабіринт, що піднімається чені у вигляді інгаляцій, наприклад, штраназаль(Randley S L , el a) , Effects of alpha-adrenoceptor них Крім того, сполуки згідно з винаходом можуть agonists and antagonists in a maze-exploration бути призначені трансдермально Для фахівця в modet of 'fear'-motivated behavior Naunvnданій галузі очевидно, що вказані дозовані форми Schiedeberg's Arch Pharmacol, 327 1-5 (1984)), можуть містити в якості активного компоненту, як було автоматизовано, як описано раніше (Reid, et сполуку формули І так і відповідну фармацевтичне al , Automation of the rat elevated X-maze test of прийнятну сіль сполуки формули І anxiety Br J Pharmacol , 102 (Suppl) 304P(1991)) Тварин розміщували в центрі Х-лабіринту обличДля одержання фармацевтичних композицій із чям до вільних коридорів Для визначення анксюсполук згідно з винаходом фармацевтичне прийнлітичного ефекту входи та час, проведений в кінятними носіями можуть бути як тверді, так і рідкі цевих напівсекціях, вимірювався протягом 5речовини Тверді форми виготовлення включають хвилинного періоду теста (Costall, et al , Use of the порошки, пігулки, кульки, капсули, облатки, суппоelevated plus maze to assess anxiolytic potential in зиторм та дисперговані гранули Твердим носієм rat Br J Pharmacol , 96 (Suppl) 312p (1989)) може бути одна або більше субстанцій, які можуть також діяти як розріджувачі, ароматизатори, Тест загрози для людиноподібних мавп зв'язуючи агенти, консерванти, дезштегруючі агенЗагальна КІЛЬКІСТЬ ПОЗ тіла, що проявляють ти або як шкапсулюючий матеріал тварини по відношенню до джерела загрози (людина, що стоїть на відстані приблизно 0 5м від В порошках носій є тонкодисперсною твердою мавп'ячої клітки і пильно дивиться у очі мавпи), речовиною, яка знаходиться в суміші з тонкодисреєструвалась протягом 2-хвилинного періоду персним активним компонентом теста Зареєстрованими позами були прижмуреВ таблетках активний компонент змішується у ний погляд, пози хвоста, мічення запахом клітки / ВІДПОВІДНИХ пропорціях з носієм, що має необхідні насісту, пілоерекція, усамітнення, вигинання спизв'язуючи властивості, і пресується до бажаних ни Кожну тварину піддівали збудженню загрозою розмірів та форм ДВІЧІ протягом тесту - за день перед і після прийнПорошки та таблетки переважно містять від яття ЛІКІВ Різниця МІЖ двома вимірюваннями анап'яти або десяти до семидесяти ВІДСОТКІВ активнолізувалась з використанням єдиного методу аналіго компоненту Прийнятними носіями є карбонат зу змін згідно з Dunnett's t-test Всі прийоми ЛІКІВ магнію, стеарат магнію, тальк, цукор, лактоза, пекпроводились принаймні через 2 години після пертин, декстрин, крохмаль, желатин, трагакант мешого (контрольного) збудження загрозою Час потилцелюлоза, натрій-карбоксиметил целюлоза, переднього прийому для кожної сполуки становив низькоплавкі воски, масло какао і таке інше Під 40 хвилин терміном "приготування" розуміється одержання рецептури активної сполуки з шкапсулюючим маТест конфлікту для щурів терілом, таким як носій, що забезпечує одержання Щурів в дослідних камерах привчали натискукапсули, в якій активний компонент з або без швати на важіль для одержання харчової винагоро 49011 18 17 ших носив, оточений носієм, який, таким чином, 100мг/кг Дози, між тим, можуть змінюватись в запов'язаний з ним Аналогічно, це стосується облалежності від потреб та умов лікування, та сполуки, ток та пастилок Таблетки, порошки, капсули, яка застосовується Визначення належних доз у кульки, облатки та пастилки можуть бути викорисвиняткових випадках є компетенцією фахівця Затані як тверді дозовані форми, що придатні до галом, лікування починається з меньших доз, які є орального призначення меньшими ніж оптимальна доза сполуки Після чого доза поступово збільшується до досягнення Для одержання суппозиторієв низькоплавкий оптимального ефекту в конкретних обставинах воск, такий як суміш гліцеридів жирних кислот або Для зручності при бажанні сумарна добова доза масло какао, спочатку розплавляється і при переможе бути розподілена і призначена частинами мішуванні в ньому гомогенно диспергується активпротягом дня ний компонент Розплавлена гомогенна суміш потім виливається у ВІДПОВІДНОГО розміру форми, Наступні приклади ілюструють даний винахід, охолоджується і, таким чином, твердіє але вони не обмежують його об'єм РІДКІ рецептурні форми включають розчини, ПРИКЛАД 1 суспензії та емульсії, наприклад, водні або воднопропіленглікольні розчини Для парентерального уведення рідкі рецептури можуть бути одержані в розчині водного поліетиленгліколю Водні розчини, придатні для орального застосування, можуть бути одержані розчиненням активного компоненту у воді й, за бажанням, додаванням ВІДПОВІДНИХ барвників, ароматизаторів, стабілізаторів і загущуючих агентів Водні суспензії, придатні для орального викоCXEt ристання, можуть бути одержані диспергуванням тонко розподіленого у воді активного компоненту з в'язким матеріалом, таким як природні або синтетичні гуим, смоли, метилцелюлоза, натрійкарбоксиметилцелюлоза та ІНШІ добре ВІДОМІ су спендуючі агенти Сюди також відноситься виготовлення твердих форм, які призначені для перетворення безпосередньо перед використанням в рідку форму, придатну для орального застосування До таких рідких форм відносяться розчини, суспензії та емульсії Такі рецептури додатково до активного компоненту можуть містити барвники, ароматизатори, стабілізатори, буфери, штучні та природні підсолоджувачі, дисперсанти, загущувачі, агенти розчинення і таке інше Переважним є одержання фармацевтичних рецептур у одиничних дозованих формах Одержання таких форм передбачає одержання одиничних форм, що містять необхідну КІЛЬКІСТЬ активного компоненту Одинична доза може бути приготована упаковуванням, до таких упаковок, що містять дискретну КІЛЬКІСТЬ композиції, відносяться таблетки, капсули та порошки у пляшечках та ампулах Одиничні дозовані форми можуть бути також у вигляді капсул, таблеток, облаток або пастилок або їх певна КІЛЬКІСТЬ може бути спакована разом КІЛЬКІСТЬ активного компоненту в виготовленій одиничній дозі може змінюватись або регулюватись від 0,1мг до 1,0г в залежності від особливостей застосування та сили активного компоненту При медичному застосуванні ліки можуть призначатися тричі на день, наприклад в капсулах по 100 або ЗООмг Композиція може також, якщо це необхідно, містити ІНШІ сумісні терапевтичні агенти При терапевтичному застосуванні сполуки, що використовується в фармацевтичному методі згідно з даним винаходом, призначаються в початковій дозі від приблизно 0,01 мг до приблизно 100мг/кг за добу Переважний добовий інтервал складає від приблизно 0,01 мг до приблизно CO 2 HNH 7 HCl (i)EtO2CCH2CN, NH4Ac, AcOH, толуол, 120°С (и) a NaCN, ЕЮН (95%), H2O, 115°C, b HCI (g) (їм) ЕЮН, HCI (g), толуол (iv) HCI, H2O (v) H2, ЕЮН / NH3, нікель Ренеяб 30-50°С (vi) HCI, H2O, 140°C Загальні методи, що пояснюються синтезом транс- (Р)-З-етилгабапентину Стадія (і) Ціаноацетат Суміш 3-(Р)-метилциклогексанону (125 ммоль), етилціаноацетату (124ммоль), ацетату амонію (12,5ммоль) та льодяної оцтової кислоти (24ммоль) кип'ятили зі зворотнім холодильником з насадкою Діна Старка протягом 24 годин Суміш охолоджували і промивали водою Водний розчин екстрагували толуолом Толуольні екстракти об'єднували з вихідним органічним шаром, висушували над MgSO4, і розчинник випаровували Сире масло очищали дистиляцією Kugelrohr з одержанням масла Температура кипіння близько 150160°С Вихід 86% 1 Н NMR (CDCI3) 400 MHz 5 1 01-1 05 (ЗН, m), 1 17-1 32 (1Н, m), 1 35 (ЗН, t, J=7 Hz), 1 42-2 30 (6H, m), 2 98(1H, d, J=13Hz), 3 74(1H, d, J=13Hz), 4 27 (2H, q, J=7 Hz) MS (Cl) m/z 85, 91, 95, 135, 162, 178, 180, 200, 208 (100 % MH+), 209 IR (плівка) umax - cm 1 3437, 2956, 2930, 2870, 2223, 1729, 1603, 1448, 1367, 1347, 1313, 49011 20 19 1 1290,1262, 1246, 1218, 1101, 1084,1046, 1023, 974, Н NMR (CDCI3) 400 MHz 5 0 78-0 90 (1Н, m), 957, 914, 859, 822, 780 0 93 (ЗН, d, J=6 Hz), 0 91-1 00 (1H, m), 1 23-1 25 Мікроаналіз C12H17NO2 Обчислено С, 69 54, Н, 8 27, N, 6 76 Знайдено С, 69 44, Н, 8 22, N, 6 76 Стадія (м) Біснітрил До розчину NaCN (40ммоль) в бмл Н2О і 160мл етанолу (95%) додавали ціаноацетат (40ммоль) Після 22 годинного кип'ятіння зі зворотнім холодильником охолоджений розчин фільтрували, фільтрат підкислювали шляхом пропускання через нього газоподібного НСІ, і фільрували знову Розчинник видаляли, і сире масло очищали колонковою хроматографією з утворенням твердої кристалічної речовини світло-жовтого кольору Вихід 88% 1 Н NMR (CDCI3) 400 MHz 5 0 90 (1Н, m), 0 98 (ЗН, d, J=6 Hz), 111 (1H, t, J=12 Hz), 1 38 (1H, dt, J=4 9 Hz), 160-190 (4H, m), 2 07 (2H, m), 2 68 (2H, s) MS (Cl) m/z 91 (100%), 92, 108, 130, 136, 163, (50% MH+), 180 IR(CH2CI2)u 2956, 2932, 2862, 2234, 1714, 1457, 1447, 1427, 1386, 1358 Мікроаналіз C10H14N2 Обчислено С, 70 04, H, 8 70, N,17 27 Знайдено С, 74 05, Н, 8 71, N, 17 25 Стадія (їм)) Імідат До розчину бінітрілу (6 2ммоль) в ЗОмл етанолу (абсолютного) додавали ЗОмл сухого толуолу Розчин охолоджували льодом одночасно з насиченням газоподібними НСІ Потім отриманий розчин залишали стояти при кімнатній температурі протягом 24 годин Розчинник видаляли, твердий залишок розтирали з діетиловим ефіром, отримуючи осад, який висушували з одержанням кристалічної речовини білого кольору Вихід 50% Температура плавлення 118-120°С *Н NMR (DMSO) 400 MHz 5 0 8-0 89 (1Н, ш), 0 91 (ЗН, d, J=6 3 Hz), 1 06-1 12 (1Н, m), 1 24-1 35 (1Н, m), 1 37 (ЗН, t, J=7 Hz), 1 41-1 95 (6H, m), 3 02 (2H, s) 4 49 (2H, q, J=7 Hz) MS(CI) m/z 91, 133, 154, 164, 179, 181, (100%MH+-CN), 195(MH+), 209 IR (СН2С12)итах, cm 1 2957, 2938, 2858, 2233, 1651, 1573, 1446,1388, 1361,1137, 1103, 1022, 1005, 952, 933, 874, 834 Мікроаналіз Ci 2 H 2 oN 2 0 1 08 HCI Обчислено С, 58 19, H, 8 58, N, 11 31 Знайдено С, 58 25, Н, 8 59, N, 11 59 Стадія (iv) Ефір Імідат (1 Іммоль) розчиняли у охолодженій льодом воді (40мл) і доводили рН за допомогою 1N НСІ до величини 1 5 Розчин перемішували при кімнатній температурі на протязі 20 годин Додавали етилацетат (ЗОмл), промивали органічний шар водою, висушували і розчинник видаляли до одержання чистого масла Вихід 82% (1H, m), 1 29 (ЗН, t, J=7 2 Hz), 1 59-1 80 (4H, m), 2 05-2 08 (2H, Br t), 2 54 (2H, s), 4 20 (2H, q, J=7 2 Hz) MS (Cl) m/z 88, 95, 109, 122, 137, 160, 164, (100% MH+ - ЕЮН), 182, 183, 199, 210 (60%MH+), 230 IR (плівка) umax, cm 1 2930, 2870, 2235, 1737, 1458, 1414,1375, 1345,1264, 1196, 1171, 1096, 1041, 1026, 959,847 Мікроаналіз Ci2HigNO2 Обчислено С, 68 87, H, 9 15, N, 6 69 Знайдено С, 68 87, Н, 9 11, N, 6 90 Стадія (v) Лактам Ефір (8 Эммоль) розчиняли в ІЧНз / ЕЮН (7%, 40мл) разом з попередньо промитим нікелем Ренея (Н2О, після якої був ЕЮН) в 250мл колбі Парра Розчин гідрували при 30°С, тиску 46 psi протягом 24 годин Охолоджений розчин фільтрували через м'який шар целіту, промиваючи етилацетатом Потім видаляли з фільтрату розчинник, одержуючи тверду речовину білого кольору Вихід 30% Температура плавлення 92-98°С 1 Н NMR (DMSO) 400 MHz 5 0 75-0 82 (1Н, ш), 0 84 (ЗН, d, J=6 4 Hz), 0 88-0 94 (1Н, m), 1 14-1 19 (1H,m), 120-150 (2H,m), 150-163 (4H,m), 191 (2H,s), 3 03(2H,s), 7 42(1H-s), MS (Cl) m/z 166, 167, 168, (100% MH+), 182, 196 IR (плівка)иНах, c m 1 3260, 2907, 1695, 1652, 1446, 1318, 1255, 1210, 1068 Мікроаналіз C10H17NO 1 08 HCI Обчислено С, 71 81, H, 10 25, N, 8 37 Знайдено С, 71 80, Н, 10 29, N, 8 31 Стадія (vi) З-Метилгабапентин Лактам (2 17ммоль) розчиняли 2 розчині 10М НСІ (5мл) і води (5мл), суміш кип'ятили зі зворотнім холодильником приблизно при 140°С на протязі 5 годин Охолоджений розчин розбавляли Юмл Н2О і Юмл DCM і водний шар в подальшому промивали 2x15мл DCM Водний шар потім піддавали висушуванню з утворенням твердої речовини білого кольору Вихід 76% Температура плавлення 148-150°С [a]D= -2 5 (Т - 20°С, с=1, МеОН) Один ізомер (RR) 1 Н NMR (СОСІз) 400 MHz 5 0 6-0 79 (1Н, ш), 082 (ЗН, d, J=6 Hz), 087-090 (1Н, m), 1121 20(1 Н, dt, J=4 5, 13 3 Hz), 1 34-1 50(3H, m), 1 601 63(3H, m), 2 30 (2H,s), 3 01 (2H, s), 7 93(3H, Brs) MS (Cl) m/z 95, 109, 121,151, 167, 168, (100% MH + -H 2 O), 186 (MH+) IR (MeOH) umax, c m 1 2924, 2353,1708, 1599, 1523, 1454, 1216 Мікроаналіз Ci 0 Hi 9 NO 2 1 1 HCI Обчислено С, 53 29, H, 8 99, N, 6 21 Знайдено С, 53 23, Н, 8 99, N, 6 45 21 49011 ПРИКЛАД 2 О). •О,В 22 1 IR (Плівка)и т ах cm 2939, 2865, 2255, 2237, 1750, 1720, 1450, 1425, 1387, 1356, 1337, 1316, 1269, 1160, 1097, 992, 929, 879 Мікроаналіз C i 0 H i 4 N 2 0 1H 2 O, Вираховано С, 73,49, H, 8 69, N, 16 86 Знайдено С, 73 24, Н, 8 73, N, 17 08 Стадія (їм) Імідат Бінітрил (7 Зммоль) піддавали реакції згідно з загальним методом стадії (їм) з утворенням білої твердої речовини Вихід 70% Температура плавлення 107-114°С 1 Н NMR (DMSO) 400 MHz 5 1 00-1 06 (ЗН, 2xt, J=6 4 Hz), 1 10-1 38 (2Н, m), 1 38 (ЗН, t, J=6 8 Hz), 1 40-2 10 (7H, m), 2 86, 2 92, 3 10, 3 28 (2H, 4xd, J = 1 4 J = 6 , 1 8 M % CO,HNK,HCI M H S + I R 1 6 5 6 , 4 4 , 1 4 8 , 1 4 H z , В І Д П О В І Д Н О ) , 4 4 8 ( 2 H , q , H z ) m / z ( C l ) ) , 2 ( C H 1 5 1 2 7 8 7 , 9 5 , 1 5 4 , 1 6 3 , 1 8 1 2 , 1 9 5 , 0 9 ( 1 0 0 0 C I 5 , 2 ) u 1 m 4 a x 4 c 6 , 1 m 1 2 9 3 8 , 3 8 9 , 1 2 8 6 4 , 3 6 7 , 2 6 6 4 , 1 1 3 9 , 2 2 3 5 , 1 1 0 0 , 1 0 0 7 , 9 4 8 , 8 8 1 , 8 3 7 , 8 0 9 (і) EtO 2 CCH 2 CN, NH 4 Ac, AcOH, толуол, 120°С, (м) a NaCN, ЕЮН (95%), Н 2 О, 115°С, b HCI (г), (їм) ЕЮН, НСІ (г), толуол, (iv) НСІ, Н 2 О, (v) Hz, ЕЮН / NH 3 , нікель Ренея, 30-50°С, (vi) НСІ, Н 2 О, 140°С Ц и с / т р а н с (RSJ-2-метил габапентин Стадія (і) Ціаноацетат (±)-2-Метилциклогексанон (80ммоль), етилціаноацетат (80ммоль), ацетат амонію (8ммоль) та льодяна оцтова кислота (Ібммоль) взаємодіяли згідно з загальним методом стадії (і) з утворенням чистого масла Вихід 76% Температура кипіння близько 120-14СГС, 3 мбар 1 Н NMR (CDCI 3 ) 400 MHz 5 1 23 (ЗН, dd, J=7, 10 Hz), 1 35 (ЗН, t, J=7Hz), 1 55-1 82 (5H,m), 1 932 05(1H,m), 2 17 (1H, dt,J=5, 14Hz), 2 47 (1 H.dt,J=5, 9Hz), 2 92-2 97 (1H, Br d, J=15 Hz), 3 30-3 35 (1H, m), 3 81-3 86 (1H, B r d , J=15 Hz), 4 06-4 14 (1H, m), 4 23-4 ЗО (ЗН, dg, J=1, 6 Hz) MS (Cl) m/z 9 1 , 105, 120, 162, 180, 184, 189, 208 (MH + ) 216, 133,134, 1\242, 2 6 1 , 262 (100%), 263 IR (Плівка) umax cm 1 3438, 2978, 2938, 2864, 2223, 1732, 1596, 1463, 1447, 1391, 1368, 1334, 1311, 1289, 1247, 1224, 1164, 1144, 1103, 1077, 1058, 1032, 993, 982, 957 907, 892, 858,781 Мікроаналіз Ci 2 Hi7NO 2 , Вираховано С, 69 54, H, 8 27, N, 6 76 Знайдено С, 69 26, Н, 8 26, N, 6 66 Стадія (и) Біснітрил Ціаноацетат (37 ммоль) і NaCN (37ммоль) взаємодіяли згідно з загальним методом стадії (м) Сирий твердий продукт очищали колонковою хроматографією (3 16 гептан етилацетат) з утворенням чистого масла Вихід 76% 1 Н NMR (CDCI 3 ) 400 MHz 5 1 06 (ЗН, d, J=6 8 Hz), 1 11 (ЗН, d, J=6 8 Hz), 1 20-2 20 (18H, m), 2 77 (2H, dd, J=16 8 Hz), 2 63 (2H, dd, J=16 8 Hz) MS (Cl) m/z 9 1 , 95,108, 109, 136,163 (100 % MH + ) Мікроаналіз C i 2 H 2 0 N 2 O 1 06HCI, Вираховано С, 58 37, H, 8 60, N, 1 1 3 4 Знайдено С, 58 15, Н, 8 63, N, 11 60 Стадія (iv) Ефір Імідат (4 1 ммоль) піддавали реакції згідно з загальним методом стадії (iv) з утворенням чистого масла Вихід 82% 1 Н NMR (CDCI 3 ) 400MHz 5 1 03 , 1 09 (ЗН, 2xd, J=7 Hz), 1 27-1 ЗО (ЗН, m), 1 32-2 00 (8Н, m), 2 102 20 (1Н, m), 2 44, 2 82 (ЗН, 2xd, J=14 8 Hz), 2 54 (1H, m), 4 16-4 22 (2H, m) MS (Cl) m/z 88, 95, 109, 122, 164, 182, 210 (MH + 100%) IR (Плівка) umax cm 1 2936, 2864, 2234, 1737, 1449, 1418, 1385, 1372, 1345, 1270, 1225, 1186, 1128, 1098,1029, 1001, 932, 883, 864, 808, 732 Мікроаналіз Ci 2 HigNO 2 , Вираховано С, 68 67, H, 9 15, N, 6 69 Знайдено С, 68 84, Н, 9 13, N, 6 75 Стадія (v) Лактам Ефір (8 4ммоль) піддавали реакції згідно з загальним методом стадії (v) протягом 24 годин при 10°С, 50 psi Сире масло очищали колонковою хроматографією (етилацетат), з утворенням твердого продукту білого кольору Вихід 34 % Температура плавлення 85-90°С ^Н NMR (CDCI 3 ) 400MHz 5 0 88-0 91 (ЗН, dd, J=4, 6 8Hz), 1 41-1 78 (9H, m), 2 00-2 30 (2H, m), 3 06-3 23 (2H, m), 7 27(1 Н, Brs) MS (Cl) m/z 8 1 , 95, 108,137,166,167,168 (100% MH + ), 169,182, 196 IR (CH 2 CI 2 ) umax c m 1 3210, 2920, 2846, 1690, 1491, 1446, 1379, 1298, 1242, 1070 Мікроаналіз C10H17NO, Вираховано С, 71 8 1 , Н, 10 24, N, 8 37 Знайдено С, 71 83, Н, 10 19, N, 8 27 Стадія (vi) 2-Метил габапентин Лактам (2,5ммоль) піддавали реакції згідно з загальним методом стадії (vi) з утворенням білої твердої речовини Вихід 42% Температура плавлення 108-110°С [a] D =0(T=20 5°С, С = 1 , МеОН) Два діастереоізомери 3 1 1 Н NMR (DMSO + D 2 O) 400 MHz 5 0 79, 0 85 (ЗН, 2xd, J=6 8Hz), 1 21-1 65 (9Н, m), 2 22, 2 43(1 Н, 49011 24 23 2xd, J=15Hz), 2 46,2 49 (1H, 2xd, J=15Hz), 2 83-2 92 очищали колонковою хроматографією (3 1, гептан утилацетат) з утворенням чистого масла Вихід (1H, 2xd, J=13 6Hz), 3 05, 3 15 (1H, 2xd, J=13 6Hz) 66% MS (Cl) m/z 95, 109, 137, 166, 168 (100% лак1 там), 169 (MH+ - HgO), 186 (MH+), 196 Н NMR (CDCI 3 ) 400MHz 5 0 95 (ЗН, d, J=5 6 1 Hz), 1 30-1 40 (ЗН, m), 1 50 (2H, m), 1 73-1 92 (2H, IR (MeOH) umax c m 3384, 2931, 2861, 1703, m), 2 10 (2H, d, J=12 4Hz), 2 68 (2H, s) 1608, 1506, 1456, 1406, 1232, 1206,1068, 999 Мікроаналіз CioHi 9 N0 2 1 3 HCI, MS (Cl) m/z 95, 136,163 (100% MH + ), 164,182 Вираховано С, 51 64, H, 8 79, N, 6 02 IR (Плівка) umax cm 1 3628, 3288, 2932, 2859, Знайдено С, 51 66, Н, 8 91, N, 616 2252, 2238, 1779, 1748, 1721, 1626, 1455, 1423 ПРИКЛАД 3 ; о л NH, н а (і) EtO 2 CCH 2 CN, NH 4 Ac, AcOH, толуол, 120°С, (м) a NaCN, ЕЮН (95%), Н 2 О, 115°С, b HCI (г), (їм) ЕЮН, НСІ (г), толуол, (iv) HCI, Н 2 О, (v) Н 2 , ЕЮН / NH 3 , нікель Ренея, 30-50°С, (vi) HCI, Н 2 О, 140°С Стадія (і) Ціаноацетат 4-Метилциклогексанон (125ммоль), етилціаноацетат (124ммоль), ацетат амонію (12 4ммоль) та льодяна оцтова (24 4ммоль) піддавали реакції згідно з загальним методом стадії (і) на протязі 8 годин з утворенням чистого масла Вихід 82 % Температура кипіння близько 160-190°С, 4 мбар 1 Н NMR (CDCI 3 ) 400 MHz 5 0 95 (ЗН, d, J=6 8 Hz), 1 20-1 31 (2H, m), 1 35 (ЗН, t, J=7 2 Hz), 1 801 90 (1H, m), 1 90-2 10 (2H, m), 2 15 (1H, dt, J=4 8, 13 6 Hz), 2 34 (1H, dt, J=4 8, 13 6 Hz), 3 02 (1H, dd, J=2 4, 14 Hz), 3 84(11-1, dd, J=2 4, 14Hz), 4 27(2H, q, J=7 2 Hz) MS (Cl) m/z 114, 134, 151,162,179,180, 207, 2 0 8 ( 1 0 0 % MH + ), 209, 236 IR (Плівка) umax cm1 2927, 2225,1728,1601,1456, 1367,1288,1242, 1192,1095,1028, 959, 857, 779 Мікроаналіз Сі 2 Ні7І\ІО 2 , Вираховано С, 69 54, Н, 8 27, N, 6 76 Знайдено С, 69 39, Н, 8 27, N, 6 77 Стадія (и) Бінітрил Ціаноацетат (ЗОммоль) та NaCN (ЗОммоль) піддавали реакції згідно з загальним методом стадії (м) з утворенням неочищеного масла Масло 1381, 1371, 1332, 1287, 1263, 1194, 1170, 1143, 1109, 1004, 953,893, 852 Мікроаналіз C i 0 H i 4 N 2 0 6 H 2 O, Вираховано С, 72 74, H, 8 74, N, 16 97 Знайдено С, 72 98, Н, 8 6 1 , N, 16 65 Стадія (їм) )мідат Бінітрил (12 4ммоль) піддавали реакції згідно з загальним методом стадії (і) з утворенням білої твердої речовини з незначними домішками Ніякого очищення не проводилось, і речовину використовували в наступній стадії Стадія (iv) Ефір імідат (4 7ммоль) піддавали реакції згідно з загальним методом стадії (iv) з утворенням низькоплавкої твердої речовини Вихід 75% з розрахунку на бінітрил 1 Н NMR (CDCI 3 ) 400 MHz 5 0 92-1 01 (ЗН, m), 1 27-1 31 (ЗН, m), 1 37 (5Н, m), 1 70-1 73 (2Н, m), 2 10-2 13 (2Н, m), 2 54 (2Н, s), 4 21 (2Н, q, J=7 2Hz) MS (Cl) m/z 95, 112, 122, 164, 182 (100% M H + C 2 H 5 ), 210 (MH + ) IR (CH 2 CI 2 ) umax cm 1 2926, 2856, 2235, 2238, 1735, 1733, 1452, 1373, 1345, 1253, 1191,1033,953 Мікроаналіз C i 2 H i 9 N 2 O 2 0 12 H 2 O, Вираховано С, 68 16, H, 9 17, N, 6 62 Знайдено С, 6 8 1 4 , H, 8 9 1 , N, 6 77 Стадія (v) Лактам Ефір (2 Эммоль) піддавали реакції згідно з загальним методом стадії (v) з утворенням твердої волокноподібної речовини білого кольору Вихід 95% Температура плавлення 150-152°С 1 Н NMR (DMSO) 400MHz 5 0 85 (ЗН, d, J=6Hz), 0 93-1 06 (2Н, m), 1 27-1 ЗО (ЗН, m), 1 51 (2Н, d, J=116Hz), 1 6 2 (2Н, d, J=132Hz), 192(21-1, s), 3 02(2H,s), 7 43(1 H, Brs) MS (CL) m/z 8 1 , 95, 110, 166, 167, 168, (100% MH + ), 169, 182, 196 IR (CH 2 CI 2 ) Umax c m 1 3189, 3093, 2945, 2921, 2864, 1679,1486, 1447,1417,1260 Мікроаналіз C10H17NO 0 15 H 2 O, Вираховано С, 70 67, H, 10 17, N, 8 24 Знайдено С, 70 69, Н, 10 05, N, 7 87 Стадія (vi) 4-Метил габапентин Лактам (2 5ммоль) піддавали реакції згідно з загальним методом стадії (vi) з утворенням гігроскопічної твердої речовини Вихід 92% Температура плавлення 146-151 °С [a] D = 0 (Т=21°С, С = 1 , МеОН) Один діастереомер (цис) 1N NMR (DMSO) 400 MHz 5 0 88 (ЗН, d, J=6Hz), 1 02-1 12 (2Н, m), 1 25-1 32 (ЗН, m), 1431 47 (2Н, m), 2 33 (2H,s), 2 99(2Н, s), 8 03(ЗН, Brs), 12 33(11-1, Brs) MS (Cl) m/z 8 1 , 95, 109, 166,167,168 (100% MH + - H 2 O), 169, 182, 186 (MH + ), 196 49011 26 25 IR (MeOH) umax cm 1 3393, 2925, 2862, 1714 Н NMR (CDCI ) 400 MHz 5 0 91(6Hd,J=6 8 Hz), 1 00-1 20 (1H, m), 1 3-1 6 (5H, m), 1 85 (2H, d, 1613, 1514, 1451, 1387, 1251, 1232, 1192, 1151. J=12 8 Hz), 2 14 (2H, d, J=12 Hz),, 2 70 (2H, m) 1119,864 1 3 Мікроаналіз C10H19NO21HCI 1H 2 O, Вираховано С, 50 04, H, 9 26, N, 5 84 Знайдено С, 50 04, Н, 9 18, N, 5 82 ПРИКЛАД 4 (i) EtO 2 CCH 2 CN, NH 4 Ac, AcOH, толуол, 120°С, (и) a NaCN, EtOH(95%), H 2 O, 115°C, b HCI (r), (їм) ЕЮН, HCI (г), толуол, (iv) HCI, H 2 O, (v) H 2 , EtOH/NH 3 , нікель Ренея 30-50°С, (vi) HCI, H 2 O, 140°C Цис 4-ізопропіл габапентин Стадія (і) Ціаноацетат 4-ізопропіл-циклогексанон (57ммоль), етилацетат (57ммоль), ацетат амонію (58ммоль) та льодяну оцтову кислоту (11 Зммоль) піддавали реакції згідно з загальним методом стадії (і) Дистиляцією Kugetrohr отримували чисте масло Вихід 83% Температура кипіння близько 170-19°С, 4 мбар 1 Н NMR (CDCI 3 ) 400 MHz 5 0 89 (6Н, d, J=6 8Hz), 1 20-1 33 (2Н, m), 1 35(ЗН, t, J=7 2 Hz), 1 37-1 50 (2H, m), 2 00-2 11 (3H, m), 2 30 (1H, dt, J=5, 14 Hz), 3 10 (1H, m), 3 92 (1H, m),4 27(2H, q, J=7 2Hz) MS (Cl) m/z 163, 179, 190, 207, 208, 235, 236 (100% MH + ), 237, 264 iR (Плівка) umax cm 1 2959, 2871, 2225, 1730, 1603, 1448, 1387, 1368, 1291, 1264, 1239, 1214, 1190, 1140, 1101, 1029, 918, 852, 777 Мікроаналіз Ci4H 2 iNO 2 , Вираховано С, 71 46, H, 8 99, N, 5 95 Знайдено С, 71 28, Н, 8 95, N, 5 90 Стадія (и) Бінітрил Ціаноацетат (37ммоль) та NaCN (37ммоль) піддавали реакції згідно з загальним методом стадії (м) з утворенням твердої речовини жовтого кольору Вихід 100% Температура плавлення 7981 °С MS (Cl) m/z 95, 121, 148, 164,191 (100% MH + ), 192, 209, 210, 219, 231 IR (CH 2 CI 2 ) umax c m 1 2961, 2933, 2868, 2250, 2237, 1468, 1451, 1388, 1370, 1344, 1318, 1266,1238, 1216, 1146, 1093, 1065, 1035, 998, 968, 934, 909, 738 Мікроаналіз Ci 2 HisN 2 , Вираховано С, 75 74, H, 9 53, N, 14 72 Знайдено С, 75 45, Н, 9 5 1 , N, 14 64 Стадія (їм) Імідат Бінітрил (12 Зммоль) піддавали реакції згідно з загальним методом стадії (їм) з утворенням білої твердої речовини з незначними домішками Ніякого очищення не проводилось, і речовину використовували в наступній стадії Стадія (iv) Ефір Імідат (4 4ммоль) піддавали реакції згідно з загальним методом стадії (iv) з утворенням низькоплавкої твердої речовини Вихід 76% з розрахунку на бінітрил 1 Н NMR (CDCI 3 ) 400 MHz 5 0 89 (6H,d,J=6 8 Hz), 0 91-1 04 (1H, m), 1 29 (3H, t, J=7 Hz), 1 331 51 (5H, m), 1 74-1 78 (2H, m), 2 14-217 (2H, m), 2 54(2H,s), 4 17-4 22 (2H, q, J=7 Hz) MS (Cl) m/z 88,123, 150, 192 (MH + - ЕЮН), 210 (MH + - CO), 238 (100% MH + ) IR (Плівка) иНах cm 1 2955, 2927, 2863, 2235, 1733, 1450, 1369, 1244, 1187,1033, 933 Мікроаналіз C i 4 H 9 N O 2 0 12 H 2 O, Вираховано С, 70 2 1 , H, 9 78, N, 5 85 Знайдено С, 70 18, Н, 9 82, N, 6 03 Стадія (v) Лактам Ефір (2 Эммоль) гідрували згідно з загальним методом стадії (v) при 50°С, 50 psi, з утворенням неочищеної твердої речовини Тверду речовину очищали колонковою хроматографією з утворенням твердої речовини білого кольору Вихід 38% Температура плавлення 130-134°С 1 Н NMR (CDCI 3 ) 400 MHz 5 0 85-0 90 (6Н, dd, J=0 8, 6 8 Hz), 1 00-1 05 (3H, m), 1 34-1 45 (3H, m), 1 63-1 65 (2H, m), 1 73-1 81 (2H, m), 2 13 (2H, d, J=0 8 H z ) , 3 1 9 ( 2 H , s), 5 91 (1H, Brs) MS (Cl) m/z 95,152, 194, 195, 196 (100% MH + ), 197, 210, 224 IR (CH 2 CI 2 ) Umax c m 1 3210, 3094, 2931, 2857, 1699, 1493, 1449, 1382, 1322, 1301, 1265, 919, 788 Мікроаналіз Ci 2 H 2 iNO, Вираховано С, 73 80, H, 10 84, N, 7 77 Знайдено С, 73 83, Н, 10 90, N,7 11 Стадія (vi) 4-Ізопропіл габапентин Лактам (Іммоль) піддавали реакції згідно з загальним методом стадії (vi) з утворенням порошку білого кольору Вихід 60% Температура плавлення 167-170°С [a] D = 0 Л~=20°С, С = 1 , МеОН) Один діастереомер (цис) 1 Н NMR (DMSO) 400 MHz 5 0 84 (6Н, d, J=6 8Hz), 0 90-1 00 (1Н, m), 1 00-1 56 (2Н, m), 1 231 30 (2Н, m), 1 38-1 48(3H,m), 1 66-1 70 (2H, m), 2 32 (2H, s), 2 97 (2H, s), 8 00 (3H, Brs), 12 00 (1H, Brs) MS (Cl) m/z 190, 196 (100% лактам Н + ), 214 49011 28 27 (MH+) 0 032моль) в толуолі (25мл) додавали етилціаноацетат (3 37мл, 0 032моль, 1екв), ацетат амонію IR (MeOH) umax cm 1 3557, 3144, 3027, 2949, (0 24г, 0 ООЗмоль, 0 1екв) та оцтову кислоту 2865, 2354, 1712, 1591, 1507, 1455, 1468, 1409, (0 Збмл, 0 ООбмоль, 0 2 екв ) Розчин жовтого ко1322, 1286, 1246, 1199, 1077, 852 Мікроаналіз C12H23NO21 1 2 H C I , Вираховано С, 56 7 1 , Н, 9 57, N, 5 51 Знайдено С, 56 77, Н, 9 56, N, 5 51 ПРИКЛАД 5 СОМ льору нагрівали зі зворотнім холодильником до кипіння і кип'ятили з насадкою Діна-Старка до тих пір, поки в насадці більше не конденсувалося води Після охолодження новий розчин оранжевого кольору промивали водою (3x2 5мл) і органічний шар висушували (MgSO4) Після фільтрації та видалення у вакуумі розчинника утворювався сирий продукт у вигляді рідини насиченого оранжевого кольору Очищення, проведене дистиляцією Kugetrohr, приводило до утворення суміші цис- та транс- продуктів у вигляді рідини блідо-жовтого кольору, температура кипіння 160-170°С, 4 мбар (5 83г, 83%) 1 CCLH NH, HCI (і) Cul, MeLi, NH 4 CI, NH 3 (92%), (it) NCCH 2 CO 2 Et, NH4OAC, AcOH, толуол (83%), (їм) NaCN, ЕЮН, H 2 O (57%), (iv) НО, ЕЮН, толуол (93%), (v) H 2 , нікель Ренея, ЕЮН, NH 3 (84%), (vi) HCIt, H 2 O (64%) Стадія (і) 3,3-Диметилциклогексанон Синтезовано за методом, описаним в Pelletier S W and Mody N V J Org Chem , 41 1069 (1969) Розчин диметилкупрату ЛІТІЮ готували додаванням метиллітію (1 4 М в ефірі, 77 25мл, 2 45моль) до йодиду МІДІ (І) ( 8 8 Г, 0 046моль) в атмосфері аргону Розчин охолоджували до 0°С і по краплинам при перемішуванні додавали 3метилциклогексен-1-он (5мл, 0 044моль), в результаті чого утворювався осад насиченого жовтого кольору Суспензію перемішували при кімнатній температурі протягом 1 години перед тим, як вилити й в розчин водного аміаку (ЮОмл) та ацетату амонію (близько 5г) Шари розділяли і водний шар промивали діетиловим ефіром (Зх50мл) Об'єднані органічні фази промивали насиченим соляним розчином (ЗхЮОмл), висушували (MgSO4) і розчинник видаляли під вакуумом, отримуючи рідину темножовтого кольору 1 Н NMR (CDCI 3 ) 400 MHz 0 98 (6Н, s, 2xMe), 1 59 (2Н, т ) , 1 88 (2Н, т ) , 2 14 (2Н, т ) , 2 26 (2Н, IR (Плівка) и т ах cm 1 2956, 1711 (С = О), 1457, 1368, 1292, 1226, 1076 Стадія (м) Ціаноацетат До розчину 3,3-диметилциклогексанону (4г, Н NMR (CDCI 3 ) 400 MHz 0 96 (6Н, s, 2xMe), 0 99 (6Н, s, 2хМе), 1 34(6Н, ш, 2хМе ефіру), 1 49 (4Н, щ), 1 75 (2Н, квінтет, J=6 4), 1 82 (2Н, квінтет, J=6 4), 2 46 (2Н, s), 2 60 (2Н, t, J=6 4), 2 80 (2Н, s), 2 93 (2Н, t, J=6 4), 4 27 (4Н, m, 2xCH 2 ефір) MS (СІ) z/e 222 (М + = 1, 100%), 221 (5), 206 (4), 194(6), 176(5) IR (Плівка) Umax cm 1 2958, 2870, 2224 (CN), 1731 (С = О), 1606 (С = С), 1277, 1223 Мікроаналіз C13H19C2N , Вираховано С, 70 56, Н, 8 65, N, 6 32 Знайдено С, 70 35, Н, 8 79, N, 6 25 Стадія (їм) Біснітрил До розчину ненасиченого ціаноефіру (1 26г, 0 ООбмоль) в етанолі (ЮОмл) і воді (4мл) додавали ціанід натрію (0 28г, 0 ООбмоль, 1екв) Розчин жовтуватого кольору нагрівали зі зворотнім холодильником протягом 8 годин і потім піддавали охолодженню, протягом якого утворювався осад білуватого кольору Суспензію фільтрували під вакуумом і фільтрат підкислювали за допомогою газоподібного НСІ до досягнення рН приблизно 2 Потім суміш вдруге фільтрували і розчинник видаляли під вакуумом, одержуючи сирий продукт у вигляді твердої речовини блідо-зеленого кольору Проводили флеш-колонкову хроматографію, і після абсорбцій сирого продукту на кремнії проводили елюювання розчином 0-50% ЕЮАс в гептані з утворенням бінітрилу у вигляді безбарвної твердої речовини (0 57г, 57%) 1 Н NMR (CDCI 3 ) 400MHz 0 99 (ЗН, s, Me), 1 13 (1Н, td, J=13 2, 4 2 Hz), 1 21 (3H,s, Me), 1 32 (2H, m), 1 54 (1H, m), 1 82 (3H, m), 2 15 (1H, m), 2 65 (2H, s, CH 2 CN) 13 C NMR (CDCI3) 400 MHz 19 6 1 , 25 17, 30 79, 3 1 1 8 , 33 77, 34 79, 35 37, 37 92, 46 26, 115 06, 122 19 MS (Cl) z/e 177 (M + + 1, 100%), 161 (10), 150 (20), 136(5), 120(4), 109(5) IR (Плівка) Umax cm-1 2988, 2937, 2869, 2237 (2xCN), 1749, 1456, 1423, 1369, 1202, 1180, 1031,972 Мікроаналіз СцНібГ\І2 Вираховано С, 74 96, Н, 9 15, N, 15 89 Знайдено С, 75 08, Н, 9 32, N, 15 80 Стадія (iv) Ціаноефір Бінітрил (0 50г, 2 84ммоль розчиняли в абсолютному етанолі (20мл) при кімнатній температурі і потім охолоджували до 0°С Толуол (20мл) дода 29 ЗО 49011 вали до розчину і потім реакційну суміш підкисляли шляхом пропускання через неї газоподібного НСІ з невеликою швидкістю приблизно протягом 45 хвилин Колбу потім закривали і залишали при кімнатній температурі на 24 години Жовтий розчин розподіляли між етилацетатом і водою, і шари розділяли Водний шар ектрагували етилацетатом (ЗхЗОмл) і об'єднані органічні шари промивали водним насиченим розчином гідрокарбонату натрію (Зх50мл), висолювали (Зх50мл), висушували (MgSO4) і розчинник видаляли при зменшеному тиску з утворенням рідини блідо-жовтого кольору (0 59г, 93%) 1 Н NMR (CDCI3) 400 NMHz 0 94 (ЗН, s, Me), 1 16(31-1, m), 1 21 (ЗН, s, Me), 1 29(3H, t, J=7 2, CH2CH3), 150 (1H, m), 165(11-1, dt, J=14 4, 7 6), 1 84 (1H, gt, J=13 3, 3 2), 1 96 (1H dt, J=13 7, 2 2), 2 16 (1H,m), 2 48(1 H, d, J=15 6, C-2H), 2 54(1 H, d, J=156, C-2H), 4 20 (2H, q, J=7 2, CH2CH3) 13 C NMR (CDCI3) 400 MHz 14 21, 19 65, 25 42, 3103, 34 04, 34 14, 36 08, 38 44, 46 14, 46 80, 61 20, 123 67, 169 00 MS (Cl) z/e 224 (M+ + 1, 100%), 196 (12), 178 (35), 136(13), 109(12) IR (Плівка) umax cm 1 2998, 2937, 2889, 2234 (CN), 1738 (C = O), 1457, 1372, 1217, 1181, 1154,1026 і потім поділяли між водою і дихлорметаном, утворені шари відокремлювали один від одного Водний шар промивали дихлорметаном (Зх20мл) і воду/НСІ видаляли роторним випарюванням з утворенням сирого продукту у вигляді твердої речовини майже білого кольору Розтирання цієї твердої речовини з етилацетатом та фільтрування утвореного продукту дає 3, 3-диметилгабапентину пдрохлоридну сіль у вигляді безбарвної твердої речовини (140г, 42%, 64% від вихідного матеріаЛ У) . 1 Н NMR (DMSO) 400 MHz 0 90 (ЗН, s, Me), 0 92 (ЗН, s, Me), 1-15-1 49 (8Н, m), 2 45 (2Н, s, СНзСОзН), 2 90 (2Н, brq, J=13 5, CH2NH3), 7 96 (ЗН, brs, NH3), 12 36(11-1 brs, ОН) IR (Плівка) umax cm i 2930, 1728 (с = О), 1272, 1123 Мікроаналіз C11H22NO2CI, Вираховано С, 56 04, Н, 9 41, N, 5 94, Знайдено С, 55 79, Н, 9 61, N, 6 23 ПРИКЛАД Є Мікроаналіз C13H21NO2, Вираховано С, 69 92, H, 9 48, N, 6 27, Знайдено С, 69 63, Н, 9 45, N, 6 15 Стадія (v) Лактам Ціаноефір (0 5г, 2 23ммоль) гідрували в етальному розчині аміаку (600мл) в присутності нікелю Ренея як каталізатора (приблизно 0 25г) при 50°С і 50 psi протягом 48 годин Каталізатор відокремлювали шляхом фільтрації через целіт, а розчинник видаляли в вакуумі, в результаті чого отримували тверду кристалічну речовину зеленуватого кольру Проводили флеш-колонкову хроматографію з елююванням розчином етилацетату (від 0% до 100% в гептані, в результаті отримували чистий лактам у вигляді твердої безбарвної речовини (340мг, 84%) 1 Н NMR (CDCI3) 400 MHz 0 89 (ЗН, s, Me), 0 92 (ЗН, s, Me), 1 25 (2H, m), 1 36 (2H, m), 1 51 (ЗН, m), 1 68 (1H, s), 2 18 (1H, d, J=16 4, CH2NH), 2 24 (1H, d, J=16 4, CH2NH), 3 15 (2H, s, CH2CO) 13 CNMR(CDOI3) 400 MHz 19 16, 29 88, 30 36, 3128, 36 57, 39 05, 39 61,44 58, 49 54, 54 79, 177 72 MS (Cl) z/e 182 (M+ + 1,100%), 181 (15), 180 (5), 166(3) IR (Плівка) umax cm 1 3203, 3100 (NH), 2914, 2860, 1698 (C = O), 1486, 1374, 1317, 1289, 1257, 1076 Мікроаналіз СцН-ідІМО, Вираховано С, 72 88, Н, 10 56, N, 7 73, Знайдено С, 72 38, Н, 10 47, N, 7 56 Стадія (vi) 3,3-Диметилгабапентину пдрохлорид Лактам (0 Зг, 1 ббммоль) розчиняли в суміші НСІ (концентрована, 5мл) і води (5мл) і отриманий безбарвний розчин нагрівали зі зворотнім холодильником протягом 20 годин Розчин охолоджували N H , HCI (і) EtO2CCH2CN, MeOH, NH3 (67%), (м) H2SO4, 180°С(79%), (їм) Ас20, 120°С(82%), (iv) MeOH, NaOMe (83%), (v) N3P(0)(OPh)2, Et3N, MeCN, 60°C потім кип'ятіння з НСІ, потім кристалізація (13%) Стадії (і) та (it) (Р)-З-Метилциклогексанон (10 92мл, 89 2ммоль) розчиняли в метанолі (25мл) з етилціаноацетатом (18 96мл, 178ммоль) і охолоджували до 0°С Пропускали газоподібний аміак через розчин протягом 25 хвилин, після чого розчин закривали і залишали стояти при -20°С Після 66 годин до суміші додавали діетиловий ефір (100мл) і утворену тверду речовину білого кольру відфільтровували, промивали діетиловим ефіром (2х50мл) і висушували з одержанням 15 71г (67%) твердої білої речовини Без подальшого очищення зразок цієї твердої речовини (4 0г, 15 3ммоль) розчиняли у концентрованій H2SO4 (40мл) з м'яким нагріванням і залишали стояти на ніч Потім обережно додавали воду (40мл) і отриману СІМІШ нагрівали до 170°С Через 5 годин вся тверда речовина розчинялась Суміш охолоджували до кімнатної температури, розводили водою (200мл) і екстрагували діетиловим ефіром (Зх150мл) Ефірні екстракти об'єднували, висушували над сульфатом магнію і розчинник відганяли у вакуумі Маслоподібний залишок розтирали з гептаном з утворенням осаду, який відфільтровували і висушували, одержуючи 2 57г 31 49011 (79%) твердої речовини тм'яно-жовтого кольору 1 Н NMR (CDCI 3 ) 400 MHz 5 0 85-0 94 (2Н, m), 0 87 (ЗН, d, J=6Hz), 1 15(1 Н, m), 1 39-1 61 (ЗН, m), 1 71 (1Н, brd, J=12 8 Hz), 1 87 (2H, m), 2 48 (2H, ABq, J=4 Hz), 2 67 (2H, s) MS (ES) z/e 214 ([M], 13%), 213 (100%) IR (тонка плівка) u ma x c m 1 1204, 1290, 1413, 1458, 1702, 2924 Мікроаналіз CnHisO4 Вираховано С, 61 66, H, 8 47, Знайдено С, 61 67, Н, 8 51 Стадія (їм) Ангідрид Дикислоту (2 5г, 11 68ммоль) нагрівали до кипіння в оцтовому ангідриді (ЗОмл) Після 3 годин розчинник видаляли під вакуумом Залишок розчиняли в дихлорметані (50мл) і промивали насиченим водним розчином бікарбонату натрію, висушували (MgSO4) і розчинник видаляли в вакуумі з одержанням 1 83г (82%) масла коричневого кольору 1 Н NMR (CDCI 3 ) 400 MHz 50 84, 0 89 (ЗН, d, J=6Hz), 0 98 (1Н, m), 1 38-1 60 (4Н, m), 1 64-1 80 (2Н, m), 2 53 (2Н, s), 2 74 (2Н, s) MS (APCI+) z/e 197 ([MH], 100%), 126(32%) IR (тонка плівка) u m a x с м 1 947,1073,1181, 1761, 1810, 2925 Мікроаналіз СцНібОз Вираховано С, 67 32 , Н, 8 22, Знайдено С, 66 98, Н, 8 07 Стадія (iv) Напівефір, цисл'ранс суміш Ангідрид (1 865г, 9 5ммоль) розчиняли в сухому метанолі (Юмл) з метоксидом натрію (0 5 М в МеОН, 20мл, Юммоль) і перемішували при кімнатній температурі Після 3 годин розчинник видаляли під вакуумом і залишок розподіляли між етилацетатом (150мл) та 1N НСІ (50мл) Органічну фазу відокремлювали, а водну фазу повторно екстрагували етилацетатом (2х100мл) Органічні екстракти об'єднували, висушували (MgSO4) і розчинник видаляли під вакуумом з утворенням 1 8г (83%) масла блідно-коричневогоо кольору, яке являло собою суміш 1 1 цис- та транс- ізомерів 1 Н NMR (CDCI 3 ) 400 MHz 5 0 85-0 93 (2Н, m), 0 86 (ЗН, d, J=6Hz), 1 17 (1Н, m),1 39- 1 62(ЗН, m), 1 64-1 80 (ЗН, m) 2 48 (2Н, m), 2 64-2 65(2Н, 2xs один від іншого ізомеру) MS(ES+)z/e 227([M-H] + , 100%) IR (тонка плівка) u m a x c m 1 1163, 1194, 1440, 1705, 1738, 2926,3200 Мікроаналіз С12Н20О4 Вираховано С, 63 13 , Н, 8 83, Знайдено С, 63 29, Н, 8 83 Стадія (v) (1-Амшометил-З-метилциклогексил)оцтова кислота [(1s-(1a, Зр)] Суміш ізомерів напівефіру (515мг, 2 26ммоль) розчиняли в ацетоні (бмл) і охолоджували до 10°С Додавали триетиламш (377мл, 2 7ммоль), після чого додавали хлорформіат (259мл, 2 7ммоль) Суміш перемішували при -10°С протягом 40 хвилин, після чого додавали розчин азиду натрію (220мг, 3 ЗЭммоль) у воді )1мл) і суміш нагрівали до 0°С Через 40 хвилин суміш виливали в холодну льодяну воду (20мл) і екстрагували охолодженим до температури льоду толуолом (Зх20мл) Толуольні екстракти об'єднували і висушували над сульфатом магнію при 0°С Потім то 32 луольний розчин по краплям додавали в колбу, яку попередньо нагрівали до 180°С в масляній бані при 180°С Розчинник видаляли перегонкою Після закінчення процесу суміш перемішували при 180°С протягом 20 хвилин, до того часу, поки видалиться увесь розчинник Потім додавали діоксан (5мл) та концентровану НСІ (5мл) і суміш кип'ятили протягом 3 годин Потім суміш знову охолоджували до кімнатної температури, розводили водою (ЗОмл) і промивали дихлорметаном (2х30мл) Водну фазу збирали і видаляли розчинник під вакуумом з утворенням смоли коричневого кольору, яку розтирали з етилацетатом, одержуючи тверду речовину тьмяно-жовтого кольору Цю речовину перекристалізовували з суміші метанолу, етилацетату та гептану, одержуючи 35мг (7%) твердої речовини білого кольру 1 Н NMR (DMSO) 400 MHz 5 0 70-0 88 (2Н, т ) , 0 83 (ЗН, d, J=6Hz), 1 06-1 17(1Н, т ) , 1 36-1 69 (6Н, т ) , 2 44 (2Н, s), 2 84 (2Н, s), 7 92(4Н, brs) MS (ES+) z/e 186 ([МН-НСІ1, 100%) IR (Тонка плівка) и т а х cm 1211, 1408, 1709, 2925, 3200 Мікроаналіз Ci 0 H 2 oN0 2 CI 0 25 Н 2 О, Вираховано С, 53 09, Н, 9 13, N, 6 19, СІ, 15 67 Знайдено С, 53 24, Н, 9 26, N, 6 23, СІ, 15 43 ПРИКЛАД 7 СО,Н цис/транс цис/транс (і) EtO 2 CCH 2 CN, MeOH, NH 3 , (м) H 2 SO 4 , 180°C, (їм) Ас 2 О, 120°С, (iv) MeOH, NaOMe, (v) EtOCOCI, Net3, потім ІЧаІЧз, потім нагрівання, потім кип'ятіння З НСІ Цис^ранс 3,5-диметилгабапентин Стадії (і) та (м) Дикислота Цис-3,5-диметилциклогексанон (11 24г, 89 2ммоль) розчиняли у метанолі (25мл) та етилціаноацетаті (18 96мл, 178 2ммоль) і охолоджували до 0°С Потім пропускали через розчин газоподібний аміак протягом ЗО хвилин Після чого розчин перемішували при -20°С Через 66 годин відфільтровували тверду речовину, промивали її ефіром і висушували з одержанням 18 46г (75%) твердої речовини білого кольору Без подальшого очищення частину одержаної твердої речовини (6 0г, 21 7ммоль) розчиняли в концентрованій сірчаній кислоті (40мл) з нагріванням і залишали стояти на ніч Потім обережно додавали воду (40мл) і одержаний розчин нагрівали 33 49011 до 180°С Через 5 годин суміш охолоджували до кімнатної температури, розводили водою (200мл) і екстрагували діетиловим ефіром (Зх150мл) Органічні екстракти об'єднували, промивали соляним розчином, висушували (MgSO4) і розчинник відганяли у вакуумі Залишок розтирали з гептаном з одержанням твердої речовини, яку перекристалізовували із суміші дихлорметан/гептан з одержанням 3 1 2 2 г (63%) твердої речовини тмьяножовтого кольору 1 Н NMR (CDCI 3 ) 400 MHz 5 0 49 (1Н, m), 0 80 (2Н, m), 0 87 (6Н, d, J=6Hz), 1 55-1 76 (3H, m), 1 85(2H, br, d, J=13 2Hz), 2 50 (2H, s), 2 67 (2H, s) MS (ES) z/e 228 ([M]+, 14%), 227 ([M-H] + , 100%) IR (тонка плівка) u ma x c m 1 893, 1147, 1208, 1312, 1337, 1407, 1450, 1699, 2846, 2914, 2947, 3100 Мікроаналіз С12Н20О4 Вираховано С, 63 13, H, 8 83, Знайдено С, 63 22, Н, 8 95 Стадія (їм) Ангідрид Дикислоту (3 0г, 13 16ммоль) розчиняли в оцтовому ангідриді (40мл) і нагрівали до кипіння Після 3 годин кип'ятіння, суміш охолоджували до кімнатної температури і розчинник видаляли під вакуумом Залишок розчиняли в дихлорметані (150мл) і промивали один раз насиченим водним розчином бікарбонату натрію Органічну фазу відокремлювали, висушували (MgSO4) і розчинник відганяли під вакуумом, одержуючи 2 60г (94%) масла коричневого кольору, яке тверділо при стоянні 1 Н NMR (CDCI 3 ) 400 MHz 5 0 53 (1Н, m), 0 8 1 0 96 (2Н, m і 6Н, d, J=6Hz), 1 43-1 71 (4Н, m), 1 76 (1Н, m), 2 5 4 ( 2 Н , s), 2 73 (2Н, s) MS(APCI+)z/e 211 ([МН]+, 100%) IR (Тонка плівка) u ma x c m 1 950, 1073, 1183, 1459, 1756, 1767, 1812, 2910, 2952 Мікроаналіз С12Н18О3, Вираховано С, 68 55, Н, 8 75 Знайдено С, 68 32, Н, 8 75 Стадія (iv) Ц и с ^ р а н с напівефір Розчиняли ангідрид (2 556г, 12 17ммоль) в сухому метанолі (15мл), перемішували у вакуумі і залишок розподіляли між I N HCI (150мл) і етилацетатом (150мл) Органічну фазу відокремлювали, промивали соляним розчином, висушували (MgSO4) і розчинник видаляли у вакуумі з одержанням жовтого масла Масло очищали флешхроматографією (кремній, етилацетат гептан, 1 1) з одержанням 2 68г (91%) безбарвного масла 1 Н NMR (CDCI 3 ) 400 MHz 5 0 47 (2Н, m), 0 82 (4Н, m), 0 87 (12Н, d, J=6Hz), 1 57-1 80 (10Н, m), 2 46 (2Н, s, ізомер А), 2 48 (2Н, s, ізомер В), 2 63 (2Н, s, ізомер В), 2 64 (2Н, s, ізомер А), 3 67 (6Н, s) M S ( E S ) z / e 241 ([М-Н] + , 100%) IR (тонка плівка) и н а х c m 1 1163, 1197, 1437, 1459, 1706, 1736, 2913, 2951, 3100 Мікроаналіз С13Н22О4 Вираховано С, 64 44, Н, 9 15, Знайдено С, 6 4 1 7 , Н, 9 17 Стадія (v) Цисл'ранс-3,5-диметилгабапентин Суміш цис^ранс напівефірів (1 09г, 4 5ммоль) розчиняли в ацетоні (15мл) і охолоджували до 10°С Потім додавали триетиламш (попередньо 34 висушений над літій-алюміній гідридом) (660мл, 4 74ммоль), після чого додавали етилхлорформіат (453мл, 4 764ммоль) Після витримки протягом 40 хвилин при -10°С додавали розчин азиду натрію (337мг, 5 19ммоль) у воді (2 5мл) і суміш нагрівали до 0°С Через 40 хвилин суміш виливали у холодну льодяну воду (ЗОмл) і екстрагували холодним толуолом (Зх20мл) Органічні екстракти об'єднували, сушили (MgSO4) і залишали при 0°С Потім толуольний розчин по краплям додавали у колбу, встановлену для дистиляції у масляну баню при 180°С Розчинник видалявся дистиляцією в процесі додавання Після завершення процесу суміш перемішували при 180°С протягом 1 години, після чого через неї обережно пропускали азот для видалення залишків розчиннику Потім обережно додавали соляну кислоту (75% від об'єму, 20мл) і одержаний розчин кип'ятили протягом 3 годин Суміш охолоджували до кімнатної температури і залишали при кімнатній температурі на ніч Потім суміш розводили водою (20мл) і екстрагували дихлорметаном (2x15мл) Водну фазу збирали і розчинник видаляли у вакуумі Залишок розтирали з етилацетатом з одержанням 255мг (24%) твердої речовини білого кольору 1Н NMR (d 6 DMSO) 400 MHz 5 0 46 (2Н, m), 0 76-0 90 (16Н, m), 1 50-1 70 (10Н, m),, 2 ЗО (2Н, s, ізомер А), 2 44 (2Н, s, ізомер В), 2 84 (2Н, s, ізомер В), 3 00 (2Н, s, ізомер А), 7 91 (6Н, brs), 12 4 0 ( 2 H , brs) MS (ES+1 z/e 200 ([MH-HCI] + , 100%) IR (тонка плівка) u m a x c m 1 1201, 1458, 1715, 2949, 3200 Мікроаналіз C11H22NO2CI Вираховано С, 56 04, Н, 9 4 1 , N, 5 94 Знайдено С, 55 75, Н, 9 46, N, 5 87 ПРИКЛАД а НОХ NJ-LHC! тла/трат цис/транс (і) EtO 2 CCH 2 CN, MeOH, NH 3 , (м) H2SO4, 180°С, (їм) Ас 2 О, 120°С, (iv) MeOH, NaOMe, (v) EtOCOCi, Net3, потім ІЧаІЧз, потім нагрівання, потім кип'ятіння З НСІ Цис^ранс 4-метилгабапентин Стадія (і) І (ІІ) Дикислота 4-Метилциклогексанон (5мл, 40 74ммоль) розчиняли у метанолі (15мл) з етилціаноацетатом (8 67мл, 81 48ммоль) і охолоджували до 0°С Пропускали через розчин на протязі 25 хвилин газопо 35 49011 дібний аміак, після чого розчин закривали і витримували при -20°С Через 20 годин додавали до СІМІШІ діетиловий ефір (ЮОмл) і утворену тверду речовину білого кольору відфільтровували, промивали діетиловим ефіром (2х50мл), і висушували з одержанням 7 51г (70%) твердої речовини білого кольору Без подальшого очищення зразок цієї твердої речовини (4 0г, 15 3ммоль) розчиняли в концентрованій H2SO4 (40мл) при м'якому нагріванні і залишали стояти на ніч Потім обережно додавали воду (40) мл) і одержану суміш нагрівали до 170°С Через 3 години вся тверда речовина розчинювалась Суміш охолоджували до кімнатної температури, розводили водою (150мл) і екстрагували діетиловим ефіром (3x1 ООмл) Ефірні ектракти об'єднували, висушували над сульфатом магнію і розчинник видаляли у вакуумі Маслоподібний залишок розтирали з гептаном, одержуючи осад, який відфільтровували і висушували, отримуючи 2 Зг (73%) твердої речовини тмьяно-жовтого кольору 1 Н NMR (d 6 DMSO) 400MHz 5 0 87 (ЗН, d, J=6 Hz), 1 1 (2H, m), 1 27 (3H,m), 1 44 (2H, m), 1 70 (2H, brd, J=13 Hz), 2 34 (2H, s), 2 45 (2H,s) MS (ES) z/e 214 ([M] + , 13%), 213 ([M-H] + , 10%) IR (тонка плівка) u m a x c m 1 917, 1183, 1215, 1289, 1349, 1399, 1455, 1704, 2858, 2925, 3100 Мікроаналіз СЦН^СЧ Вираховано С, 61 66, Н, 8 47 Знайдено С, 61 54, Н, 8 47 Стадія (їм) Ангідрид Дикислоту (2 30г, 10 75ммоль) кип'ятили зі зворотнім холодильником в оцтовому ангідриді (ЗОмл) Через 3 5 години розчинник видаляли у вакуумі Залишок розчиняли в дихлорметані (50мл) і промивали насиченим водним розчином бікарбонату натрію, після чого висушували (МдІЗСч) і розчинник видаляли у вакуумі, одержуючи 2 07г (98%) масла коричневого кольору, яке тверділо при стоянні 1 Н NMR (CDCI 3 ) 400 MHz 5 0 93 (ЗН, d, J=6Hz),1 07 (2Н, m), 1 37 (ЗН, m), 1 49-1 71 (4Н, m), 2 56 (2Н, s), 2 72 (2Н, s) MS (АРС) +) z/e 197 ([MH] + , 100%) IR (тонка плівка) u ma x c m 1 953, 1064, 1183, 1241, 1455, 1761, 1810, 2924 Мікроаналіз C11H16N3 Вираховано С, 67 32 , Н, 8 22 Знайдено С, 67 4 1 , Н, 8 29 Стадія (iv) Ц и с ^ р а н с напівефір Ангідрид (2 06г, 10 5ммоль) розчиняли у сухому метанолі (40мл) і перемішували з метоксидом натрію (624мг, 11 55ммоль) Через 4 години розчинник відганяли у вакуумі і залишок розподіляли між 1N НСІ (150мл) і дихлорметаном (150мл) Органічну фазу відокремлювали, промивали соляним 36 розчином, сушили (МдЭСч) і розчинник видаляли у вакуумі з одержанням масла жовтого кольору Продукт очищали флеш-хроматографією (диоксид кремнію, етилацетат гептан, 1 1), одержуючи 1 98г (83%) безбарвного масла 1 Н NMR (CDCI 3 ) 400 MHz 5 0 83-0 92 (2Н, m), 0 91 (6Н, d, J=6Hz), 1 14(4Н, m), 1 21-1 42(4Н, m), 1 54(4Н, m), 1 77(4Н, m), 2 49 (2Н, s, ізомер А), 2 50 (2H,s, ізомер В), 2 62 (2Н, s, ізомер В), 2 64(2H,s, ізомер А), 3 66 (3H,s, ізомер А), 3 67(3H,s, ізомер В) MS (ES) z/e 227 ([М-Н]+, 100 %) IR (тонка плівка) u ma x c m 1 1162, 1193, 1434, 1699, 1731, 2922,32100 Мікроаналіз С12Н20О4 Вираховано С, 63 13, Н, 8 83, Знайдено С, 6 3 1 2 , Н, 8 71 Стадія (v) Ц и с ^ р а н с 4-метилгабапентин Суміш цис^гранс напівефірів (1 90г, 8 Зммоль) розчиняли в ацетоні (20мл) і охолоджували до 10°С Потім додавали триетиламш (попередньо висушений над літій-алюміній гідридом) (1 21 мл, 8 7ммоль), після чого додавали етилхлорформіат (832мкп, 8 7ммоль) Через 50 хвилин витримки при -10°С додавали розчин азиду натрію (630мг, 9 69ммоль) у воді (5мл) і суміш нагрівали до 0°С Через 40 хвилин суміш виливали в холодну льодяну воду (50мл) і екстрагували холодним толуолом (Зх50мл) Органічні екстракти об'єднували, сушили (MgSO4) і залишали при 0°С Потім толуольний розчин по краплям додавали у колбу, встановлену для дистиляції у масляну баню при 180 °С Розчинник видалявся дистиляцією в процесі додавання Після завершення процесу суміш перемішували при 180°С протягом 1 години, після чого через неї обережно пропускали азот для видалення залишків розчиннику Потім обережно додавали соляну кислоту (75% від об'єму, 20мл) і одержаний розчин кип'ятили протягом 3 годин Суміш охолоджували до кімнатної температури і залишали при кімнатній температурі на ніч Потім суміш розводили водою (ЗОмл) і екстрагували дихлорметаном (ЗхЗОмл) Водну фазу збирали і розчинник видаляли у вакуумі Залишок розтирали з етилацетатом з одержанням 590мг (32%) твердої речовини білого кольору 1 Н NMR (d 6 DMSO) 400 MHz 5 0 87 (6Н, d, J=6Hz), 1 07 (4Н, m), 1 19-1 40 (6Н, m), 1 41-1 58 (6Н, m), 1 61 (2Н, m), 2 32 (2Н, s, ізомер А), 2 44 (2Н, s, ізомер В), 2 85 (2Н, s, ізомер В), 2 99 (2Н, s, ізомер А), 7 96 (6Н, brs), 12 36 (2Н, brs) MS (ES+) z/e 186 ([МН-НСІ] + , 100%) IR (тонка плівка) u m a x c m 1 1195, 1404, 1457, 1506, 1607, 1712,2924,3200 Мікроаналіз C10H20NO2CI Вираховано С, 54 17, Н, 9 09, N, 6 32 Знайдено С, 5 4 1 3 , Н, 9 18, N, 6 45 37 49011 ДП «Український інститут промислової власності» (Укрпатент) вул Сім'ї Хохлових, 15, м Київ, 04119, Україна ( 0 4 4 ) 4 5 6 - 2 0 - 90 ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)216-32-71 38
ДивитисяДодаткова інформація
Назва патенту англійськоюDerivatives of cyclic amino acid, pharmaceutical composition and method of treatment
Назва патенту російськоюПроизводные циклической аминокислоты, фармацевтическая композиция и способ лечения
МПК / Мітки
МПК: A61P 25/22, A61P 25/16, A61P 25/18, A61P 25/08, A61K 31/195, A61K 31/00, C07C 229/28, A61P 25/24, A61P 25/12, C07C 233/47, A61P 25/14, A61P 25/28
Мітки: спосіб, циклічної, похідні, лікування, композиція, амінокислоти, фармацевтична
Код посилання
<a href="https://ua.patents.su/19-49011-pokhidni-ciklichno-aminokisloti-farmacevtichna-kompoziciya-ta-sposib-likuvannya.html" target="_blank" rel="follow" title="База патентів України">Похідні циклічної амінокислоти, фармацевтична композиція та спосіб лікування</a>
Попередній патент: Тримач для перенесення предметів (варіанти)
Наступний патент: Спосіб розкрою одягу та пристрій для зняття мірок
Випадковий патент: Спосіб наповнення пневматичних шин нетрадиційним наповнювачем