Клітинний гомогенат зі стовбурових клітин, отриманих із зростаючих рогів оленя, спосіб його одержання та його використання
Формула / Реферат
1. Клітинний гомогенат, вироблений за допомогою деструкції клітин, що належать лінії стовбурової клітини МІС-1, отриманої зі зростаючих рогів оленя (Cervidae), задепонованої у DSMZ під номером доступу DSM ACC2854.
2. Гомогенат відповідно до пункту 1 формули винаходу, який характеризується тим, що деструкція клітин виконана з використанням ультразвуку.
3. Гомогенат відповідно до пунктів 2 або 3 формули винаходу, який характеризується тим, що одна одиниця гомогенату включає екстракт з 1 мільйону клітин.
4. Спосіб одержання біологічно активного клітинного гомогенату, який характеризується тим, що підтримують клітинну культуру, клітини відділяють від середовища та потім піддають деструкції ультразвуком, де клітини, що використовуються, є клітинами лінії стовбурової клітини МІС-1, отриманої зі зростаючих рогів оленя (Cervidae), задепонованої у DSMZ під номером доступу DSM ACC2854.
5. Спосіб відповідно до пункту 4 формули винаходу, який характеризується тим, що культура є культурою на твердому середовищі або є суспензійною культурою.
6. Спосіб відповідно до пункту 4 або 5 формули винаходу, який характеризується тим, що вироблений титр гомогенату, який включає екстракт, отриманий з 1 мільйона клітин в одній одиниці.
7. Фармацевтична композиція або косметична композиція, що включає активний інгредієнт та фармацевтично допустимий носій, яка характеризується тим, що активний інгредієнт є гомогенатом, виробленим із клітин, що належать лінії стовбурової клітини МІС-1, отриманої зі зростаючих рогів оленя (Cervidae), задепонованої у DSMZ під номером доступу DSM ACC2854.
8. Композиція відповідно до пункту 7 формули винаходу, яка характеризується тим, що одна одиниця гомогенату включає екстракт з 1 мільйона клітин.
9. Композиція відповідно до пункту 7 або 8 формули винаходу, яка характеризується тим, що вона розроблена для локального або інтрадермального застосування.
10. Застосування гомогенату, виробленого із клітин, що належать лінії стовбурової клітини МІС-1, отриманої зі зростаючих рогів оленя (Cervidae), задепонованої у DSMZ під номером доступу DSM ACC2854, у виробництві препарату для медичного та/або косметичного лікування шкіри.
11. Застосування відповідно до пункту 10 формули винаходу, яке характеризується тим, що препарат розроблений для локального або інтрадермального застосування.
12. Застосування гомогенату, виробленого із клітин, що належать лінії стовбурової клітини МІС-1, отриманої зі зростаючих рогів оленя (Cervidae), задепонованої у DSMZ під номером доступу DSM ACC2854, у виробництві препарату для регенерації тканини, відібраної з числа нервової, епітеліальної та м'язової тканини.
13. Застосування відповідно до пункту 12 формули винаходу, яке характеризується тим, що препарат використовується у формі очних крапель, мазі, препарату, що вводиться, або препарату для насичення спонгостану.
14. Застосування відповідно до пункту 13 формули винаходу, яке характеризується тим, що композиція очних крапель включає в 1 мл гомогенат у розрахунку 10 Од/мл 50 мг або 10 Од/мл 25 мг, а також допоміжні речовини.
15. Застосування відповідно до пункту 14 формули винаходу, яке характеризується тим, що допоміжні речовини відібрані із групи, що включає полівініловий спирт, двонатрієвий гідрогенфосфат, натрієвий гідрогенфосфат, хлорид натрію, хлорид бензалконію та воду.
16. Застосування відповідно до пункту 12 або 13 формули винаходу, яке характеризується тим, що очна мазь включає гомогенат у розрахунку 10 Од/мл 50 мг, препарат, що вводиться, включає гомогенат у розрахунку 10 Од/мл 100 мг, та препарат для насичення спонгостану включає гомогенат у розрахунку 10 Од/мл 100 мг.
Текст
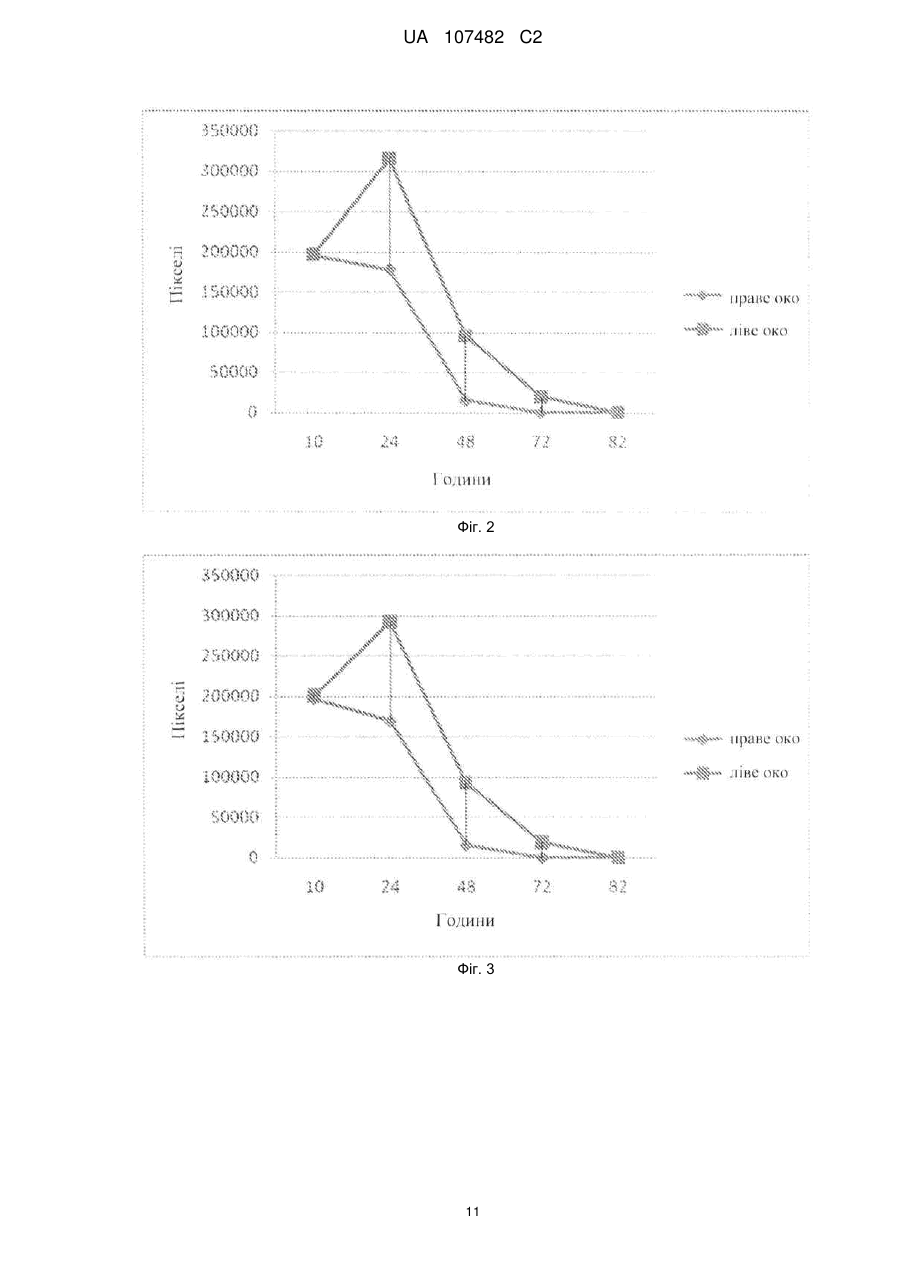
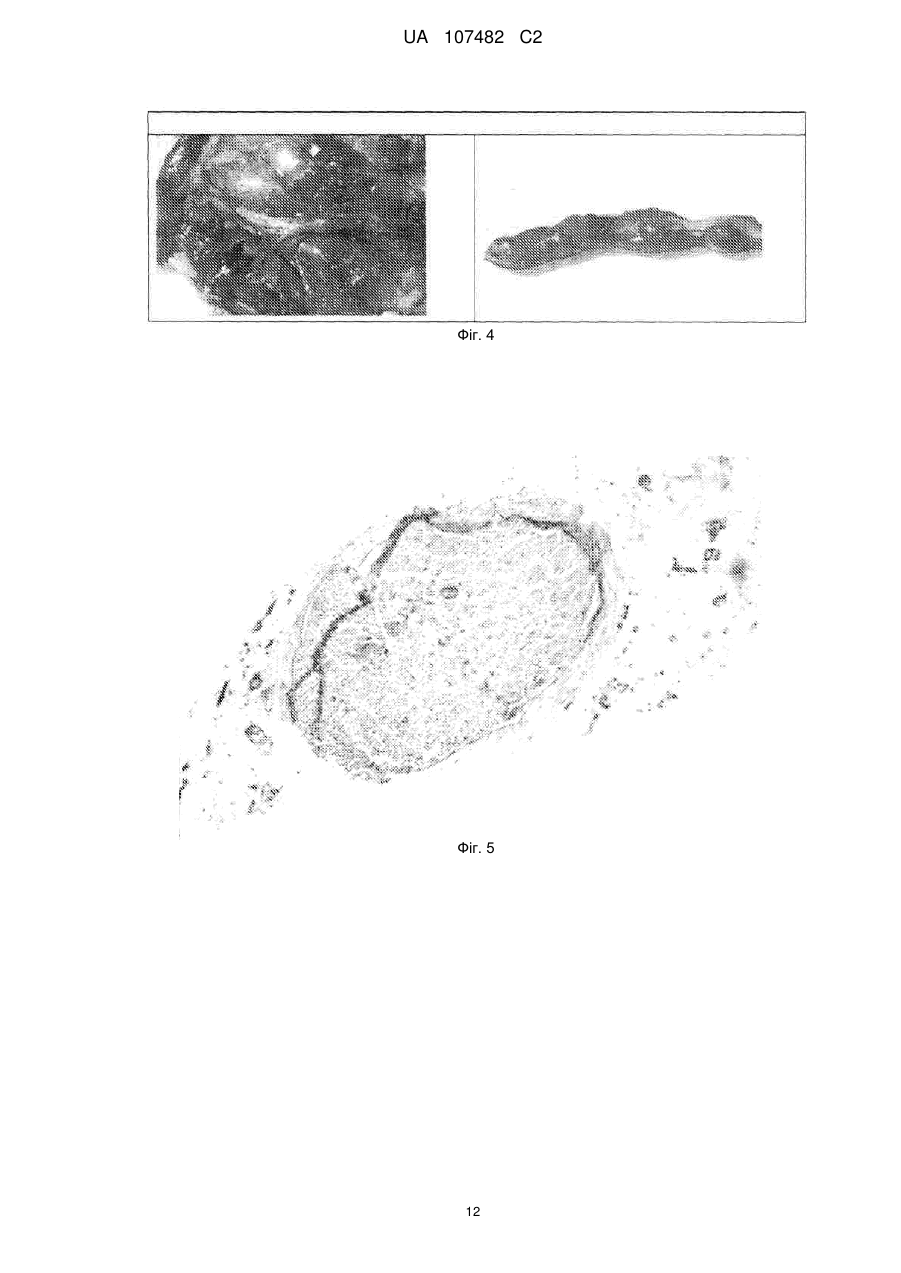
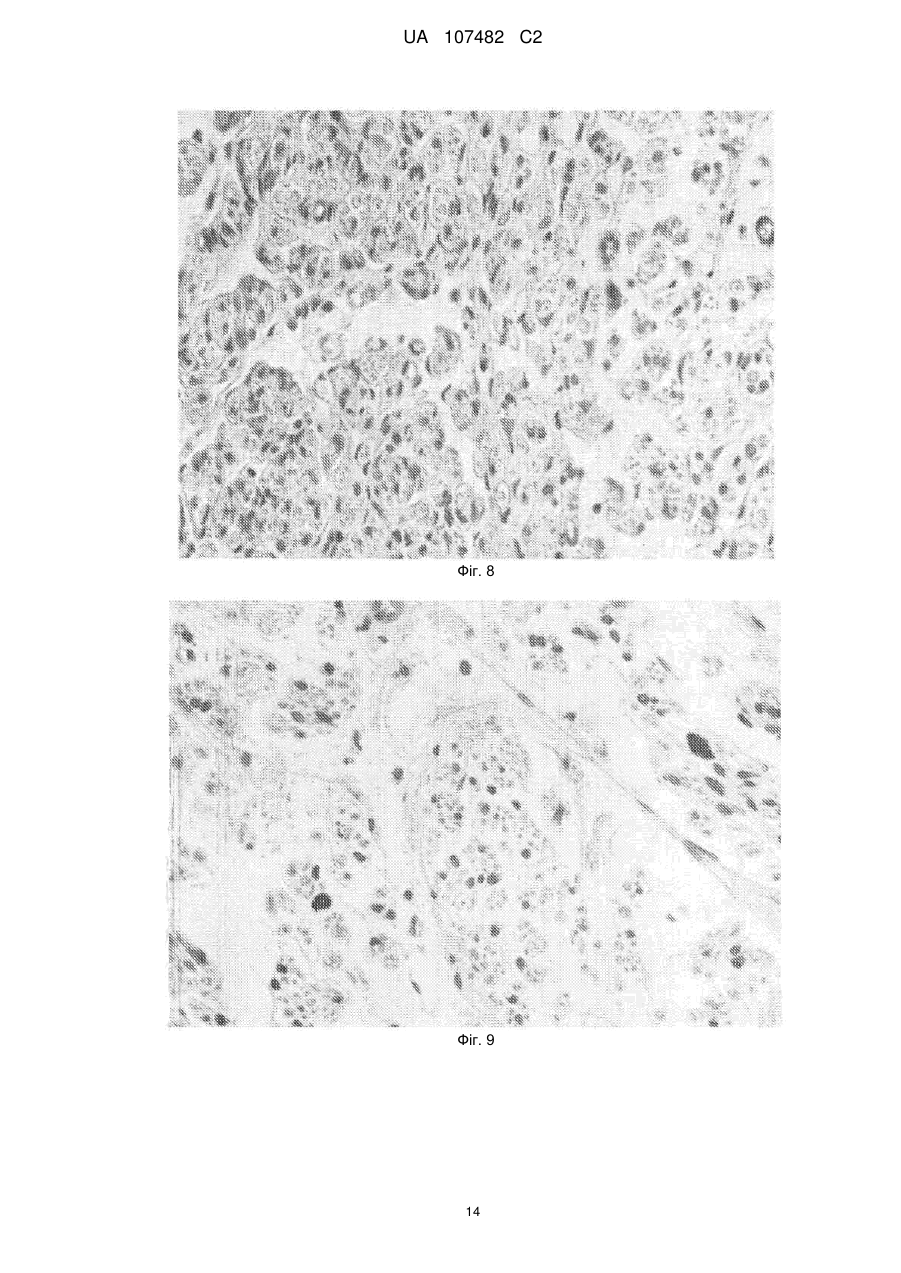
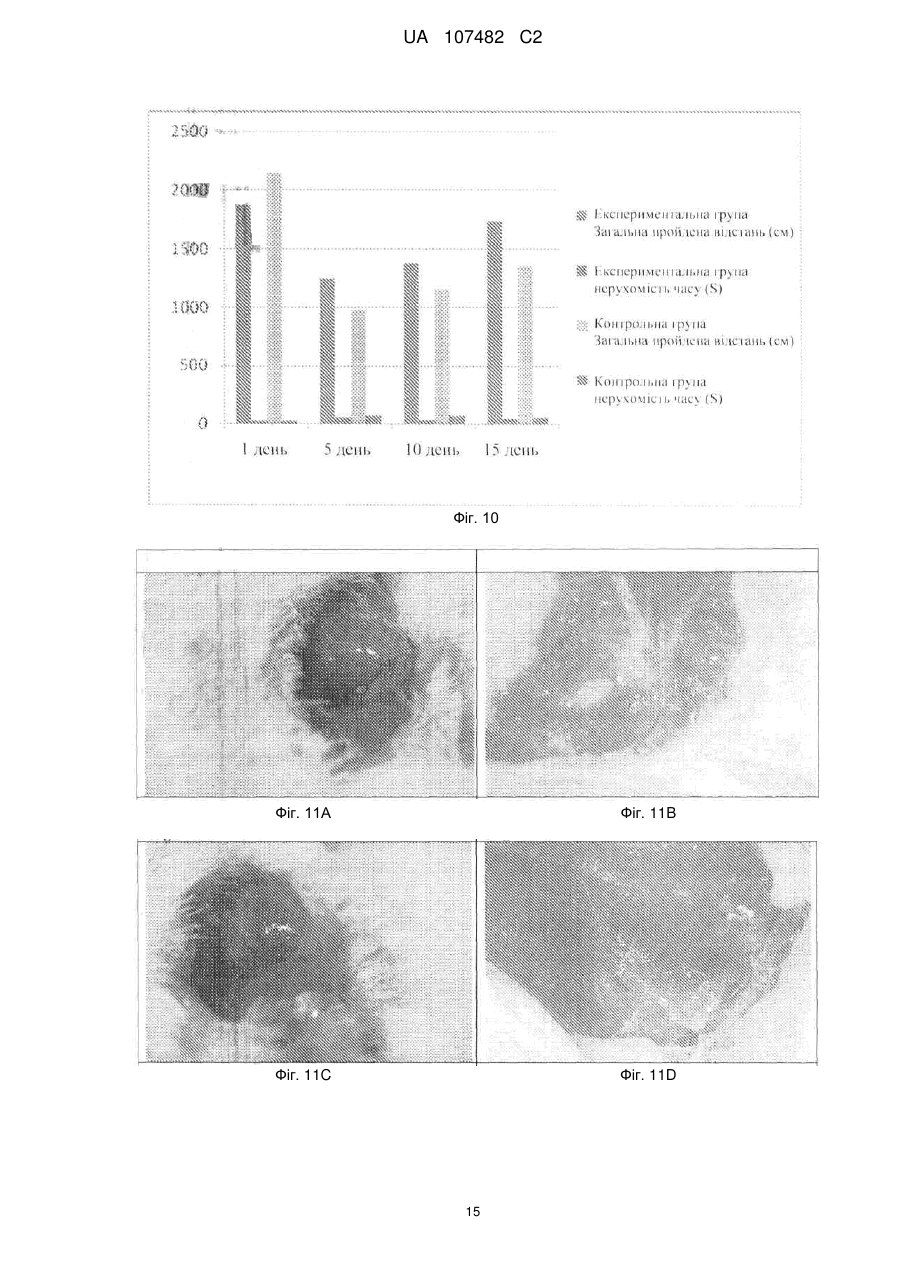
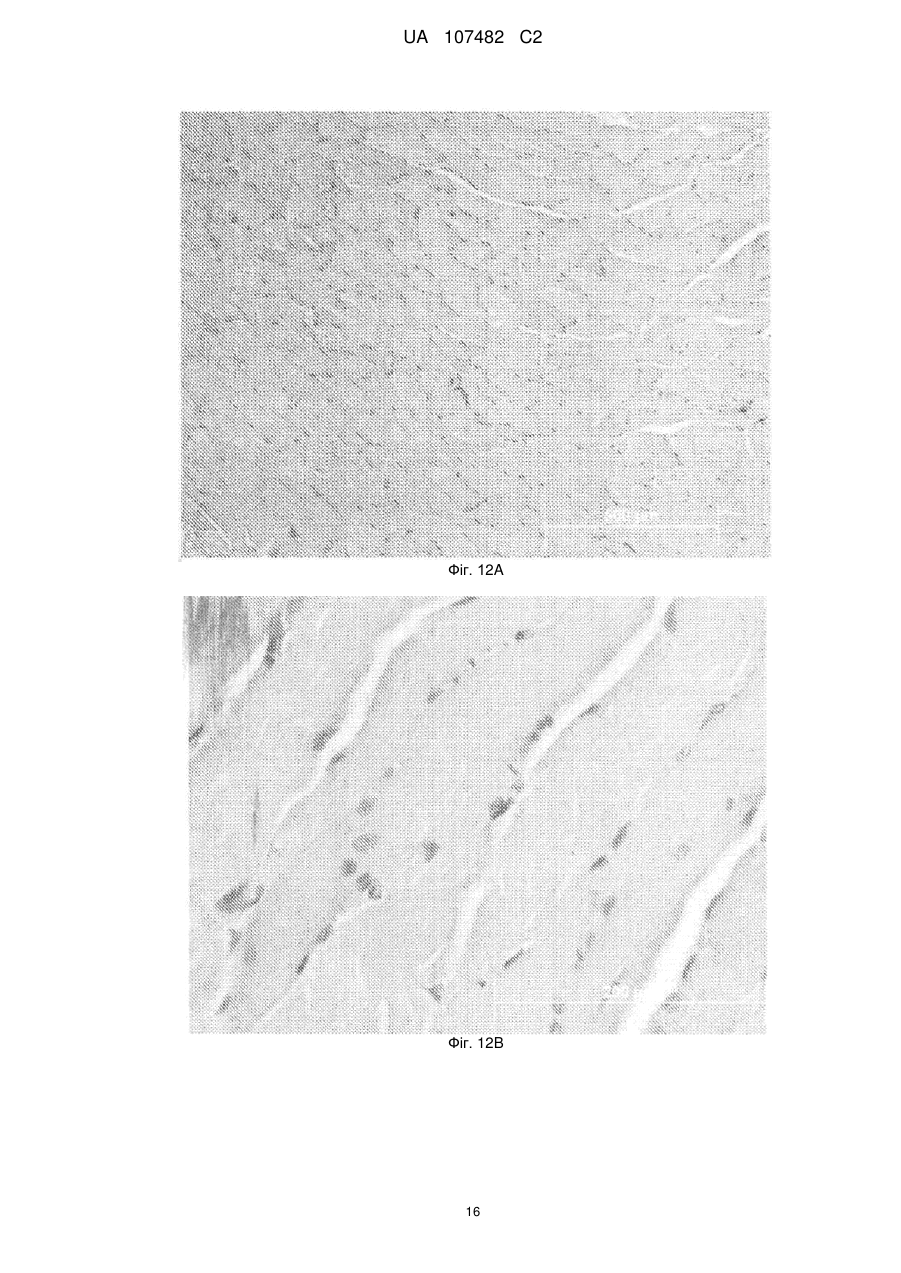
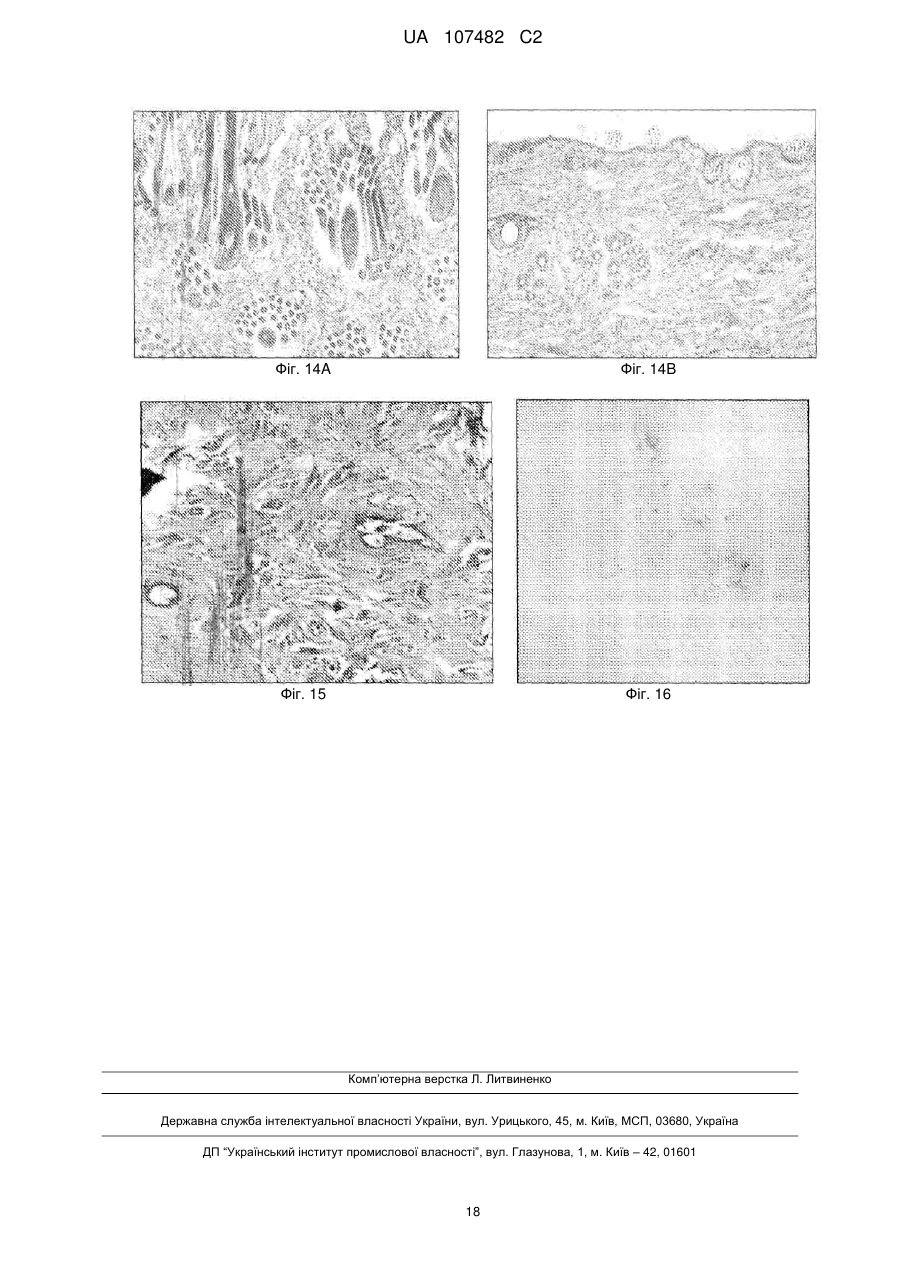
Реферат: Предметом даного винаходу є біологічно активний клітинний гомогенат, вироблений із клітин, що належать лінії стовбурової клітини МІС-1, отриманої зі зростаючих рогів оленя (Cervidae), задепонованої у PSMZ під номером доступу DSM ACC2854, спосіб його виробництва та застосування. Даний винахід також охоплює фармацевтичну та косметичну композицію, що містить вищезгаданий гомогенат. UA 107482 C2 (12) UA 107482 C2 UA 107482 C2 5 10 15 20 25 30 35 40 45 50 55 60 Предметом даного винаходу є клітинний гомогенат, отриманий зі стовбурових клітин зростаючих рогів оленя, спосіб його одержання та використання. Предметом даного винаходу є також фармацевтична або косметична композиція, що містить вищезгаданий клітинний гомогенат. В сучасному рівні техніки було багато відомих спроб, щоб виокремити та виробити стійкі лінії стовбурової клітини, з яких було б можливо зробити стабільні препарати для різного використання. Розкриті рішення, що стосуються одержання стовбурових клітин, які диференціюються в остеобласт, отримані винятково з різних типів людської тканини. Заявки WO 2005/085422 та US 2005/0048644 розкривають стовбурові клітини, виокремлені з жирової тканини, що використовуються у лікуванні хвороб м'язів та скелету. Заявка W0 2005/038012 розкриває спосіб одержання стовбурових клітин, здатних до диференціації в остеобласт або хондробласт, з людської постнатальної тканини. Заявка US 2007/0122902 розкриває спосіб виокремлення та культивування мультипотентних стовбурових клітин, отриманих з пуповинної крові. Були також спроби генетично змінити клітини, здатні до регенерації хряща та кісткової тканини, які були розкриті в описі патенту US6398816. Найбільш етичне протиріччя стосується застосувань, що стосуються стовбурових клітин, отриманих з ембріональної тканини (W0003068937, WO02064755, WO000385831). Використання людських стовбурових клітин, широко описане у відомому рівні техніки, спричиняє багато проблем, які є доказом нагальної необхідності провести подальші дослідження в цій сфері. Деякі з головних перешкод, викликаних використанням ембріональних клітин, є етичні питання, небезпека проявлення генетичних дефектів так само як ризик передачі вірусних та онкогенних хвороб. Таким чином, є нагальна необхідність у лініях стовбурової клітини, використання яких виключало б ризик вищезгаданих перешкод. Відомий рівень техніки розкриває властивості тканини рога оленя, яка визнана найшвидше зростаючою формою кості серед тканин ссавців. Були спроби використовувати проліферативні властивості цієї тканини, особливо через виокремлення факторів росту. Заявка W093/19085 розкриває спосіб виокремлення фактору росту, що є практично здатним при регенерації ушкодженої кісткової тканини. Розкритий спосіб одержання екстракту, виокремленного з рогів японського оленя (Cervus nippon), який стимулює проліферацію кровотворних стовбурових клітин та мегакаріоцитів. Заявка WO 2004/112806 розкриває композицію для лікування нейронних порушень, зроблену з маркерів гормону росту, отриманих з рогів оленя. В 2005 році автори даного винаходу почали досліджувати процес росту рогів шляхетного оленя (Cervus elaphus). У цих експериментах зі зростаючих рогів оленя була отримана лінія стовбурової клітини MIC-1. Стійка клітинна лінія була задепонована у DSMZ під номером доступу DSM ACC2854. В 2006 році була зроблена заявка на патент P. 378963, предмети якого включали нову лінію стовбурової клітини MIC-1 із зростаючих рогів оленя, використання граничних бічних фрагментів зростаючих рогів оленя у виробництві стійкої лінії стовбурової клітини так само як використання цих клітин у реконструкції кістки та ушкоджень хряща у людей та тварин. У цей час, одним з головних напрямків дослідження є пошук джерел препарату для стимулювання регенеративних процесів у складних органах, таких як шкіра. Дослідження в області фізіології процесів старіння та регенерації в тканинах призвело до відкриття ролі стовбурових клітин у цих процесах. Мета даного винаходу полягає в тому, щоб забезпечити препарат та вироби, засновані на стовбурових клітинах, які мають сприятливий вплив на регенерацію шкіри та реконструкцію її елементів. Неочікувано, виявилося, що цей клітинний гомогенат з клітин лінії стовбурової клітини MIC-1 демонструє особливо вигідну активність у стимулюванні росту та регенерації хворих або ушкоджених елементів шкіри. Предметом даного винаходу є клітинний гомогенат, отриманий деструкцією клітин з лінії стовбурової клітини MIC-1, отриманої зі зростаючих рогів оленя (Cervidae), задепонований у DSMZ під номером доступу DSM ACC2854. Краще, якщо деструкція клітин та гомогенати виконані із використанням ультразвуку. Деструкція антлерогенних стовбурових клітин вивільняє активні речовини, що там утримувалися, які активізують регенеративні процеси. У кращому втіленні даного винаходу одна одиниця гомогенату включає екстракт із 1 мільйона клітин. Наступним предметом даного винаходу є спосіб одержання біологічно активного клітинного гомогенату, який характеризується тим, що клітини є культивовані та згодом відділені від середовища, деструктуровані із використанням ультразвуку, де клітини, що були використані, є 1 UA 107482 C2 5 10 15 20 25 30 35 40 45 50 55 60 клітинами лінії стовбурової клітини MIC-1, отриманої зі зростаючих рогів оленя (Cervidae), задепоновані у DSMZ під номером доступу DSM ACC2854. Краще, якщо у способі відповідно до даного винаходу клітини культивовані на твердому середовищі або в суспензії. Краще, якщо у способі відповідно до даного винаходу, вироблений стандартизований гомогенат, який включає екстракт, отриманий з 1 мільйона клітин в одній одиниці. Наступним предметом даного винаходу є фармацевтична або косметична композиція, яка включає активний інгредієнт та фармацевтично допустимий носій, що характеризується тим, що активною речовиною є гомогенат клітин з лінії стовбурової клітини MIC-1, отриманої зі зростаючих рогів оленя (Cervidae), за депонованих у DSMZ під номером доступу DSM ACC2854. Краще, якщо композиція призначена для інтрадермального або локального застосування. Перевагами даного винаходу є, насамперед, умови культивування еталонної клітини та клітини з високим потенціалом проліферації, так само як відсутність етичних міркувань, які звичайно піднімаються проти дослідження в області людських ембріональних клітин. Інший предмет даного винаходу - використання гомогенату, отриманого із клітин з лінії стовбурової клітини MIC-1, отриманої зі зростаючих рогів оленя (Cervidae), задепонованих у DSMZ під номером доступу DSM ACC2854, у виробництві препарату для медичного та косметичного лікування шкіри. Краще, якщо препарат розроблений для локального або інтрадермального застосування. Шкіра, як бар'єрний орган, є особливо схильною до хвороб та травм через її захисну функцію. Процеси відновлення відбуваються в ній протягом життя. Завдяки біостимулюючим властивостям, екстракт корисний у широко визначеній регенеративній медицині та косметології. Клітинний гомогенат з клітин з лінії стовбурової клітини MIC-1 має сприятливий вплив на формування епітелію, стимулює зцілення ран та ушкоджень шкіри, активізує волосяні фолікули, стимулює виробництво волокон колагену, збільшує проліферацію фібробластів та активізує васкуляризацію тканини. Гомогенат лінії стовбурової клітини MIC-1 проявляє властивості, які впливають на регенерацію шкіри та її біооновлення, яке дозволяє відновити погіршення стану, пов'язане з віком. Клітинний гомогенат та препарати, зроблені на його основі, широко застосовуються як засоби проти зморшок, засоби ліфтингу та антивікові засоби, які відновлюють шкіру, ушкоджену сонячним випромінюванням, відновлюють шкіру, збільшуючи її ніжність та еластичність, так само як косметичні препарати для використання на слизових оболонках. Крім того, клітинний гомогенат та препарати, зроблені на його основі, широко корисні як засоби для лікування важких для лікування ран, що виникають, наприклад, у результаті діабету, виразки гомілки, що випливають із судинного захворювання, такого як поверхневі пошкодження, хвороба Рено, так само як засоби для ослаблення радіаційної шкоди та ушкодження шкіри після хіміотерапії. Клітинний гомогенат, що становить предмет даного винаходу, та препарат, вироблений на його основі, є крім того корисні в естетичній медицині, дерматології та у спортивній медицині, особливо як засоби для стимулюючої регенерації після прищів, для лікування опіків та для лікування судинних розладів після травми. Предмет даного винаходу є корисним як біостимулюючий препарат для слизових оболонок, особливо при пародонтозі, виразці слизової оболонки, наприклад, у ротовій порожнині, носі та піхві. Клітинний гомогенат, що є предметом даного винаходу, так само як препарати, зроблені з нього, також корисні у ветеринарії при прискоренні зцілення та відрощуванні волосся. Наступним предметом даного винаходу є нове використання клітинного гомогенату, зробленого із використанням деструкції клітин з лінії стовбурової клітини MIC-1, отриманих зі зростаючих рогів оленя (Cervidae), задепонованих у DSMZ під номером доступу DSM ACC2854, у виробництві препаратів для регенерації тканини, відібраної із числа м'язової, нервової та епітеліальної тканини. Краще, якщо препарат використовується у формі крапель для очей, мазі для очей та препарату для ін'єкцій, або препарату для насичення спонгостану. Краще, якщо композиція очних крапель містить у собі, на мілілітр, гомогенат у розрахунку 10 Од/мл (U/ml), 50 мг або 10 U/ml 25 мг, а також допоміжні речовини. Краще, якщо допоміжні речовини відібрані з групи, що включає полівініловий спирт, двонатрієвий гідроген фосфат, натрієвий гідроген фосфат, хлорид натрію, хлорид бензалконію та воду. Краще, якщо очна мазь містить модуль у розрахунку 10 U/ml 50 мг, препарат для ін'єкцій включає гомогенат у розрахунку 10 U/ml 100 мг, та препарат для насичення спонгостану включає гомогенат у розрахунку 10 U/ml 100 мг. Предмет даного винаходу показаний в ілюстраціях, де 2 UA 107482 C2 5 10 15 20 25 30 35 40 45 50 55 60 Фіг. 1 показує ефект клітинного гомогенату MIC-1 на проліферацію: фібробластів (F), міоцитів (M), хрондроцитів (CH) та гепатоцитів (H). Гомогенат фібробласти-MIC-1 (F+HMIC-1), гомогенат міоцити-MIC-1 (M+HMIC-1), гомогенат хрондроцити-MIC-1 (CH+HMIC-1), гомогенат гепатоцити-MIC-1 (H+HMIC 1), Фіг. 2 представляє поверхню ушкодження в пікселях після використання краплі з концентрацією 0,5 мільйонів клітин /мл препарату, Фіг. 3 представляє поверхню ушкодження в пікселях після застосування краплі з концентрацією 0,5 мільйонів клітин /мл препарату. Фіг. 4A представляє відкритий нерв після 12 тижнів спостереження, Фіг. 4B показує виокремлений нейрон, видимі шви, що з'єднують імплантати із залишками, Фіг. 5 представляє контрольну групу 12 тижнів, впровадження сідничного нерва в пацюка, Фіг. 6 представляє контрольну групу після 12 тижнів, впровадження сідничного нерву в пацюка, Фіг. 7 представляє експериментальну групу після 12 тижнів, периферійної регенерації імплантату, Фіг. 8 представляє експериментальну групу 12 тижнів після операції, периферійної регенерації впровадження, Фіг. 9 показує експериментальні групи після 12 тижнів, нервові волокна у центрі імплантату, Фіг. 10 показує довжину шляху в сантиметрах та час відпочинку в секундах миші після 180 с відеозапису, Фіг. 11А показує зображення м'язу негайно після ушкодження, Фіг. 11B представляє зображення м'язу після 14 днів після використання гомогенізованих, Фіг. 11C показує зображення м'язу негайно після ушкодження, Фіг. 11D показує зображення м'язу після 14 днів використання середовища, Фіг. 12А показує тварину з експериментальної групи: зображення майже незмінного кісткового м'язу – заключні етапи лікування, Фіг. 12B показує експериментальну групу, повністю відновлений кістковий м'яз, повздовжній переріз. Ушкодження, якому піддалися, підтверджене окремими ядрами, розташованими в центральній частині волокон м'язу, Фіг. 13A представляє контрольну групу, де м'язові трубочки та шрам, що формується, видимі після того, як тканина була подрібнена, Фіг. 13B представляє тварину з контрольної групи, що відновлює ушкоджений м'яз, у центрі є видимий шрам з поглинанням тканини та гігантських клітин, Фіг. 14A представляє тангенціальний розріз шкіри після 21-денного застосування дермального гомогенату, видимим є збільшена кількість вторинного волосся у волосяних фолікулах так само як численні існуючі зв'язки колагенових волокон, Фіг. 14B представляє контрольний тангенціальний розріз шкіри після 21-денного застосування фізіологічного розчину (контроль), Фіг. 15 представляє паралельний розріз шкіри після 21-денного застосування інтрадермальної гомології. Окраска Ван Гісона показує нещодавно сформовані колагенові волокна, Фіг. 16 показує рану, що вилікувана у п'ятий 24-годинний період після виокремлення секції тканини, яка охопила всі шари шкіри. Предмет даного винаходу також показаний на прикладах втілення, які не обмежують обсяг його охорони. Приклад 1. Виробництво гомогенату, що містить мезенхімну стовбурову клітину MIC-1 з рогів оленя Культура утримується в термостаті при нормальних умовах, при температурі +37 °C та атмосфері, що містить 5 % CО2. Антлерогенні клітини є адгезивними, та ростуть у колбах на 175 мл (колба клітинної культури BD Falcon) у мінімальному підтримуючому середовищі від Cambrex, яке містить 10 % ембріональну бичачу сироватку, 100 U/ml пеніциліну та 0,1 мг/мл стрептоміцину. Ефективність від однієї пляшки – приблизно 30 мільйонів клітин за 14-денний цикл культури. Після того, як отриманий повний моношар, клітини від'єднанні від дна колби, використовуючи 0,05 % трипсин з 0,02 % етилендіамінотетраоцтовою кислотою (EDTA) та передані до центрифужних пробірок. Трипсин у центрифужних пробірках інактивований шляхом додавання10 мл надосадової рідини. Потім клітини двічі промиті в PBS та центрифуговані. Центрифугування виконане в центрифузі Heraeus протягом 10 хвилин приблизно при 1000 обертах за хвилину. У результаті надосадова рідина декантирована у клітинний осадок. Це осаджується у 0,9 % хлористому натрію у розрахунку 1 мільярд клітин на 50 мл рідини. Гомогенна суспензія охолоджена у гомогенизаційній камері, що охолоджується водою, до 3 UA 107482 C2 5 10 15 20 25 30 35 40 45 50 55 температури приблизно 4 °C. Для деструктування клітин у сталевій камері, з безперервним охолодженням, 30 секунд використовуються ультразвуки з частотою 20 кГц (надзвуковий дезінтегратор UD-20, Techpan). Розчин масштабований в одиницях біологічної активності, одна одиниця представляє екстракт, отриманий з 1 мільйона клітин. Гомогенат зберігається заморожений при -80 °C. Приклад 2. Виробництво форми клітинного гомогенату, що містить мезенхімні стовбурові клітини MIC-1 з рогів оленя Препарат, заснований на клітинному гомогенаті, може зустрічатися у формі мазі, крему, тонізуючого засобу або будь-якої іншої форми, що підходить для місцевого застосування. Препарат може також мати нашкірне використання. Приклад основи мазі – Hascobase або будьяка інша відома та звичайно використовувана основа мазі, що використовується фахівцями, така як Lekobaza, безводний еуцерин, холестеринова мазь або вазелін (Farmacja stosowana. red. Stanislaw Janicki i Adolf Flebig, PZWL Warszawa 1996). 10 г суспензії, що містить 50 одиниць гомогенату, були додані до 40 г середовища. Суміш була гомогенізована, використовуючи напівавтоматичну суміш, PA 200 Alpine a (Польща). Гомогенізація була виконана більш, ніж п'ять хвилин у спеціалізованому контейнері, об'ємом 50 мл, на автоматичних параметрах настроювання. Був виготовлений тонізуючий засіб, де 50 мл 96 % етилового спирту були додані до 50 мл суспензії, що містить 100 одиниць біологічної активності гомогенату. Препарати, отримані у результаті, зберігались в холодних умовах. Приклад 3. Експертиза ефекту клітинного гомогенату на шкіру після одиничної локальної або інтрадермальної дози Оцінка ефекту клітинного гомогенату на шкіру після одиничного локального або інтрадермального застосування проводилася на 2 з 4 груп, що містили 6 осіб, кожна відібрана із групи з 24 білих новозеландських кроликів. 2 Під час локального застосування, 6 см позбавленої волосся неушкодженої шкіри на одній стороні кролика (в області грудної клітини) обробили 0,5 мл препарату. Ту ж саму поверхню з іншої сторони (контрольну) обробили відповідним середовищем. Місце застосування було досліджено більш, ніж 96 годин. 2 Під час інтрадермального застосування, на 6 см поголеної неушкодженої шкіри на одній стороні кролика (в області грудної клітини) були введені на визначеному місці інтрадермальним способом 0,5 мл препарату. На визначене місце з іншої сторони кролика було введено 0,5 мл фізіологічного розчину, та стан шкіри був оцінений після 96 годин. Після одиничної дози ми спостерігали невелике почервоніння шкіри, що почалося на другий день спостереження, яке закінчилося після 10 днів. Обидві форми добре перенеслись. Приклад 4. Оцінка ефекту клітинного гомогенату на шкіру після багаторазового локального та інтрадермального застосування Оцінка ефекту гомогенату клітини на шкіру після багаторазового локального або інтрадермального застосування проводилася на 2 з 4 груп, що містять 6 осіб, кожна відібрана із групи з 24 білих новозеландських кроликів. 2 Під час локального застосування, 6 см позбавленої волосся неушкодженої шкіри на одній стороні кролика (в області грудної клітини) обробляли 0,5 мл препарату один раз щодня більш, ніж 28 днів поспіль. Ідентична поверхня з іншої сторони контрольно була оброблена відповідним середовищем у такий же спосіб як препарат, що досліджувався. Місце застосування контролювали багаторазово у перші 8 годин лікування та потім щодня протягом наступних 21 дня. 2 Під час інтрадермального застосування, 6 см позбавленої волосся неушкодженої шкіри на одній стороні кролика (в області грудної клітини) обробляли 0,5 мл препарату один раз щодня більш, ніж 14 днів поспіль. Ту ж саму поверхню з іншого боку контрольно обробили відповідним середовищем ідентичним способом як препаратом, що досліджувався. Місце застосування контролювали багаторазово у перші 8 годин лікування та потім щодня більш, ніж наступних 21 дня. На 14-й день спостереження у 6 тварин з групи багаторазового застосування ми зібрали зрізи шкіри для гістологічної оцінки з місць із інтенсивним волосяним ростом. У 3 тварин з контрольної групи зрізи тканини з місць, де застосовували фізіологічний розчин, були зібрані для гістологічної оцінки. Застосування гомогенату інтрадермальним способом не наносило жодної шкоди шкірі та добре переносилось. У препаратах ми спостерігали збільшену кількість волосся у фазі росту в порівнянні з контрольною групою, так само як потовщення волосся навколо волосяної цибулини. У шкірі ми спостерігали збільшену кількість волокон колагену. Ці 4 UA 107482 C2 5 10 15 20 25 30 35 40 45 50 55 60 процеси спостерігалися найбільш чітко в групі, що одержувала клітинний гомогенат MIC-1 інтрадермально. Ділянки шкіри, які обробили клітинами, показали більш швидке відростання волосся, ніж області, що оброблялися фізіологічним розчином. Видимі відмінності спостерігалися на 6-й день спостереження. Повне відростання волосся до його належної довжини для даної особини, маючи на увазі від 35 до 42 мм, відбулося приблизно після 10-14 тижнів. Волосяний ріст протягом 2-3 тижнів був прискорений та становив приблизно 4 мм на тиждень. Ніякого значного росту не спостерігалося в контрольній групі. Згодом, ріст становив 2-3 мм на тиждень. Застосування гомогенату інтрадермально не нанесло жодної шкоди шкірі та добре переносилось. Гістологічні препарати після застосування гомогенату, у порівнянні з контрольною групою, призвели до значного росту вторинного волосся та збільшення кількості нещодавно синтезованих волокон колагену. Приклад 5. Оцінка ефекту мазі, заснованої на гомогенаті стовбурової клітини MIC-1 Оцінка була виконана на 9 кроликах, розбитих на 3 групи з 3 тварин кожна, використовуючи 3 типи мазі різних концентрацій: 1 Од/л (U/l) г Hascobase, 0.5 U/l г Hascobase так само як 0.1 U/l г Hascobase. Групу 1 кроликів обробили маззю 1 U/l г, групу 2 обробили маззю 0,5 U/l г, та групу 3 2 обробили 0,1 U/l г. Усі групи обробили відповідно до наступної процедури: 6 см позбавленої волосся неушкодженої шкіри на одній стороні кролика (в області грудної клітини) обробляли 0,5 мл препарату один раз щодня більш, ніж 28 днів поспіль. Ту ж саму поверхню на протилежній стороні (контрольну) обробляли відповідним середовищем (Hascobase) у такий же спосіб як препаратом, що досліджувався. Місце застосування контролювали багаторазово протягом перших 8 годин після застосування та потім щодня у наступні 28 днів. В групі, що одержувала мазь 0,1 U/l г жодного посилення росту волосся не спостерігалося. Група, що оброблялась маззю 0,5 U/l г. спостерігався прискорений волосяний ріст приблизно на 26-й день після застосування. Найбільша концентрація була активною приблизно на 21-й день після застосування. Ми виміряли кровотік в шкірі кроликів групи 1, як на обробленій, так і на контрольній сторонах. Вимірювання було зроблене з використанням лазерного вимірювача потоку Доплера, та MBF3D (Moor Instruments Ltd) та зонду P4s, 0.46 мм у діаметрі. Обладнання випромінює монохроматичне світло в довжині хвилі 780-820 нм, що виробляється напівпровідниковим лазером, 1,5 мВт потужністю. Метод лазера Доплера заснований на емісії монохроматичного оптичного випромінювання в тканині та виявлення розсіяного світла, яке повертається до поверхні тканини. Під час розсіювання світла на еритроцитах, які переміщаються, частота хвилі змінюється залежно від швидкості еритроцитів та куту, зробленого еритроцитами та фотоном (явище Доплера). Відповідне обладнання виявлення з перетворювачем сигналу та аналізатором дозволяє зібрати інформацію щодо насиченості крові даної тканини, визначеної як виріб місцевої швидкості крові та концентрації еритроцитів, усереднених на об'єм тканини, куди проникає світло. Виміри кровотоку в одній області шкіри тривали хвилину. Аналіз був виконаний на самому повільному 20-секундному інтервалі потоку. Міра течії крові, перфузія, була виражена як результат концентрації еритроцитів та їх швидкості, використовуючи відносну одиницю (одиниця перфузії). 47 % збільшення перфузії крові в шкірі спостерігалося в порівнянні з контрольною шкірою. Використання мазі на шкірі добре переносилося. Ми спостерігали незначну гіперперфузію в області застосування, та більш швидке відростання волосся на стороні, де тонізуючий засіб використовувався. Рани на місцях, де зразки тканини були зібрані для гістології, виліковувались набагато швидше, ніж на контрольній стороні. Гістологічний аналіз продемонстрував подібні зміни як у групі, що одержує гомогенат як ін'єкцію. Приклад 6. Оцінка in vitro (у лабораторних умовах) Дослідження in vitro (у лабораторних умовах) показали, що речовини, що містяться у оксамиті (м'яка шкіра, що покриває зачатки рогів в період росту) та у екстракті оленячих рогів, стимулюють проліферацію фібробластів, спленоцитів та кровотворних стовбурових клітин. Беручи до уваги присутність кровоносних судин м'язів у рогах, ми також оцінили ефект гомогенату антлерогенних клітин на фібробластах (сполучна та епітеліальна тканина), гладких м'язових клітинах (м'язова тканина), хондробластах (сполучна тканина), гепатоцитах (епітеліальна тканина) та нейронах (тканина нервової системи). Для цього дослідження ми використовували наступні зразкові клітинні лінії: мишині ембріональні фібробласти (3T3 Balb/c) та людські міоцити від ембріональної аорти (UASMC). Основна хондробластна культура була отримана з механічно деструктурованих фрагментів хряща вуха кролика (білий каліфорнійський кролик, жіноча особина, приблизно 4-кілограмової 5 UA 107482 C2 5 10 15 20 25 30 35 40 45 50 55 60 ваги). Щоб забезпечити основну гепатоцитну культуру та культуру нейрона, ми використовували фрагменти органу, зібрані від неонатального пацюка (Wistar), які були механічно деструктуровані та культивовані в середовище гладкого м'язу для вирощування (Cambrex Bio Science, Walkersville Maryland USA). Міоцити були культивовані в середовищі гладкого м'язу для вирощування, тоді як клітинні лінії, що залишились, в DMEM (Bio Whittaker, Lonza, Verviers, Belgium) у межах додавання 10 % ембріональної бичачої сироватки та 1 % розчину, що містить L-глютамін, пеніцилін та стрептоміцин (Sigma-Aldrich, Chemie, Steinheim, Germany). Культури утримувались при 37 °C у вологій атмосфері, що містить 5 % CО2. Час, що був потрібен для досягнення 70 % злиття у колбах з культурою (75 мл) був: 5 днів для міоцитів та нейронів, 10 днів для фібробластів та хондробластів, та 21 день для гепатоцитів. Оцінені клітини були вилучені з колб з культурою, використовуючи розчин 0,25 % тріпсин-EDTA (Sigma-Aldrich) та повторно інокульовані 100 000 клітин на лунку на 12 лункових тарілок. Після 24 годин середовище було змінено та гомогенізована суспензія клітин MIC-1 була додана в дозі 0,2 одиниць (1 одиниця біологічної активності дорівнює гомогенату, отриманому з 1 000 000 клітин MIC-1). Чашки були культивовані протягом 120 годин, після цього часу клітини були сфотографовані та підраховані із використанням колориметричного тесту SRB (де тест SRB визначає число живих клітин, які зв'язують фарбник, sulphorhodamine B). Клітини були закріплені 50 % трихлороцтовою кислотою та потім пофарбовані з 0,4 % SRB у 1 % оцтовій кислоті протягом 30 хвилин. Незв'язаний фарбник був вилучений промиванням у 1 % оцтовій кислоті та пофарбована зона до білків клітин була екстрагована з 10 mM небуферизованим Трісом. Тоді оптична щільність була зчитана на пристрої для зчитування чашок Elx-800 (Bio-Tek instruments, USA) при довжині хвилі 562 нм. Зразковий контроль складався з того ж самого середовища, що використовувалось у способі. Усі реактиви для тестів були куплені від Sigma. Щоб оцінити значення відмінностей між окремими групами результатів, ми використовували t-тест Стьюдента та як статистично значимий, ми прийняли p
ДивитисяДодаткова інформація
Назва патенту англійськоюCell homogenate from stem cells derived from growing deer antlers, a method of obtaining it and its use
Автори англійськоюDziewiszek, Wojciech, Cegielski, Marek, Bochnia, Marek
Автори російськоюДзэвишек Войцех, Цэгелски Марэк, Бохня Марэк
МПК / Мітки
МПК: A61K 35/32
Мітки: одержання, використання, клітин, клітинний, оленя, зростаючих, стовбурових, гомогенат, спосіб, отриманих, рогів
Код посилання
<a href="https://ua.patents.su/20-107482-klitinnijj-gomogenat-zi-stovburovikh-klitin-otrimanikh-iz-zrostayuchikh-rogiv-olenya-sposib-jjogo-oderzhannya-ta-jjogo-vikoristannya.html" target="_blank" rel="follow" title="База патентів України">Клітинний гомогенат зі стовбурових клітин, отриманих із зростаючих рогів оленя, спосіб його одержання та його використання</a>
Попередній патент: Реактор швидкого піролізу
Наступний патент: Опалубка для колон
Випадковий патент: Спосіб відбору паратерфенілу для пластмасових сцинтиляторів