Рідкі катіоніти
Номер патенту: 112980
Опубліковано: 25.11.2016
Автори: Пфеффер Ян Крістоф, Хаас Томас, Такке Томас, Ерхардт Франк, Пшибильські-Фройнд Марі-Домінік, Пфенніг Андреас, Роос Мартін, Деміколі Даніель, Хегер Харальд, Шуберт Аня, Пьоттер Маркус
Формула / Реферат
1. Спосіб видалення органічної сполуки з водного розчину, який включає стадії
a) одержання органічної сполуки, що містить водний розчин, і гідрофобного органічного розчину, що містить рідкий катіоніт,
причому рідкий катіоніт є гідрофобним,
b) контактування водного розчину і органічного розчину, і
c) відокремлення органічного розчину від водного розчину, причому органічною сполукою є сполука формули (І)
NH3+-A-COO- або NH3+-A-COOR1 (I),
причому R1 означає водень, метил, етил, а А означає незаміщену, нерозгалужену алкіленову групу, що містить принаймні три, переважно принаймні вісім, атомів вуглецю, і причому рідким катіонітом є жирна кислота.
2. Спосіб за п. 1, причому температура на стадії b) становить від 28 до 70, переважно від 30 до 37 °C.
3. Спосіб за п. 1 або п. 2, причому значення рН на стадії b) становить від 6 до 8, переважно від 6,2 до 7,2.
4. Спосіб за будь-яким із пп. 1-3, причому кількісне співвідношення між рідким катіонітом і органічною сполукою становить принаймні 1.
5. Спосіб за будь-яким із пп. 1-4, причому об'ємне співвідношення між органічним і водним розчинами становить від 1:10 до 10:1.
6. Спосіб за будь-яким із пп. 1-5, причому як рідкий катіоніт беруть жирну кислоту, що містить понад 12 атомів вуглецю.
7. Спосіб за пунктом 6, причому як рідкий катіоніт беруть жирну кислоту, що містить від 14 до 22, зокрема від 16 до 18 атомів вуглецю.
8. Спосіб за будь-яким із пп. 1-5, причому як рідкий катіоніт беруть ненасичену жирну кислоту.
9. Спосіб за п. 8, причому як рідкий катіоніт беруть олеїнову або ерукову кислоту.
10. Спосіб за будь-яким із пп. 1-9, причому водний розчин додатково містить каталітично активний біологічний агент, який є клітиною.
11. Спосіб за п. 10, причому як біологічний агент беруть бактеріальну клітину.
12. Спосіб за п. 10, причому як клітину застосовують рекомбінантну алканмонооксигеназу або рекомбінантну трансаміназу.
13. Спосіб за п. 10, причому клітина містить принаймні один фермент, вибраний із групи, що включає алкогольдегідрогеназу, аланіндегідрогеназу і генний продукт AlkL або його варіанти.
14. Спосіб за п. 10, причому присутність органічної сполуки формули (І) негативно впливає на каталітичну активність, переважно внаслідок того, що як органічну сполуку формули (І) застосовують токсичну для клітини сполуку.
15. Спосіб за будь-яким із пп. 1-14, причому органічний розчин містить додатково принаймні один органічний розчинник.
16. Спосіб за п. 15, причому як органічний розчинник беруть жирну кислоту та/або естер жирної кислоти.
17. Спосіб за п. 15, причому органічний розчин містить як рідкий катіоніт від 20 до 80 об. % олеїнової кислоти, а як розчинник - метиловий естер лауринової кислоти, і як органічну сполуку беруть метиловий естер 12-амінолауринової кислоти.
18. Спосіб за п. 17, причому водний розчин містить бактеріальну клітину, вміщуючу рекомбінантну алканмонооксигеназу або рекомбінантну трансаміназу.
19. Спосіб за п. 17, причому водний розчин містить бактеріальну клітину, що містить принаймні один фермент, вибраний із групи, що включає алкогольдегідрогеназу, аланіндегідрогеназу і генний продукт AlkL або його варіанти.
20. Реакційна суміш, що містить водний розчин і гідрофобний органічний розчин, причому гідрофобний органічний розчин містить жирну кислоту як рідкий катіоніт, і причому водний розчин є сполукою формули (І)
NH3+-A-COO- або NH3+-A-COOR1 (I),
причому R1 означає водень, метил, етил, а А означає незаміщену, нерозгалужену алкіленову групу, що містить принаймні три атоми вуглецю.
21. Реакційна суміш за п. 20, причому А означає незаміщену, нерозгалужену алкіленову групу, що містить принаймні вісім атомів вуглецю.
22. Реакційна суміш за п. 20 або п. 21, причому жирна кислота містить понад 12 атомів вуглецю.
23. Реакційна суміш за п. 20 або 21, причому жирна кислота є ненасиченою жирною кислотою.
24. Реакційна суміш за будь-яким із пп. 20-23, причому водний розчин додатково містить клітину, що містить рекомбінантну алканмонооксигеназу або рекомбінантну трансаміназу.
25. Реакційна суміш за будь-яким із пп. 20-23, причому водний розчин додатково містить клітину, що містить принаймні один фермент, який є вибраний із групи, що включає алкогольдегідрогеназу, аланіндегідрогеназу і генний продукт AlkL або його варіанти.
Текст
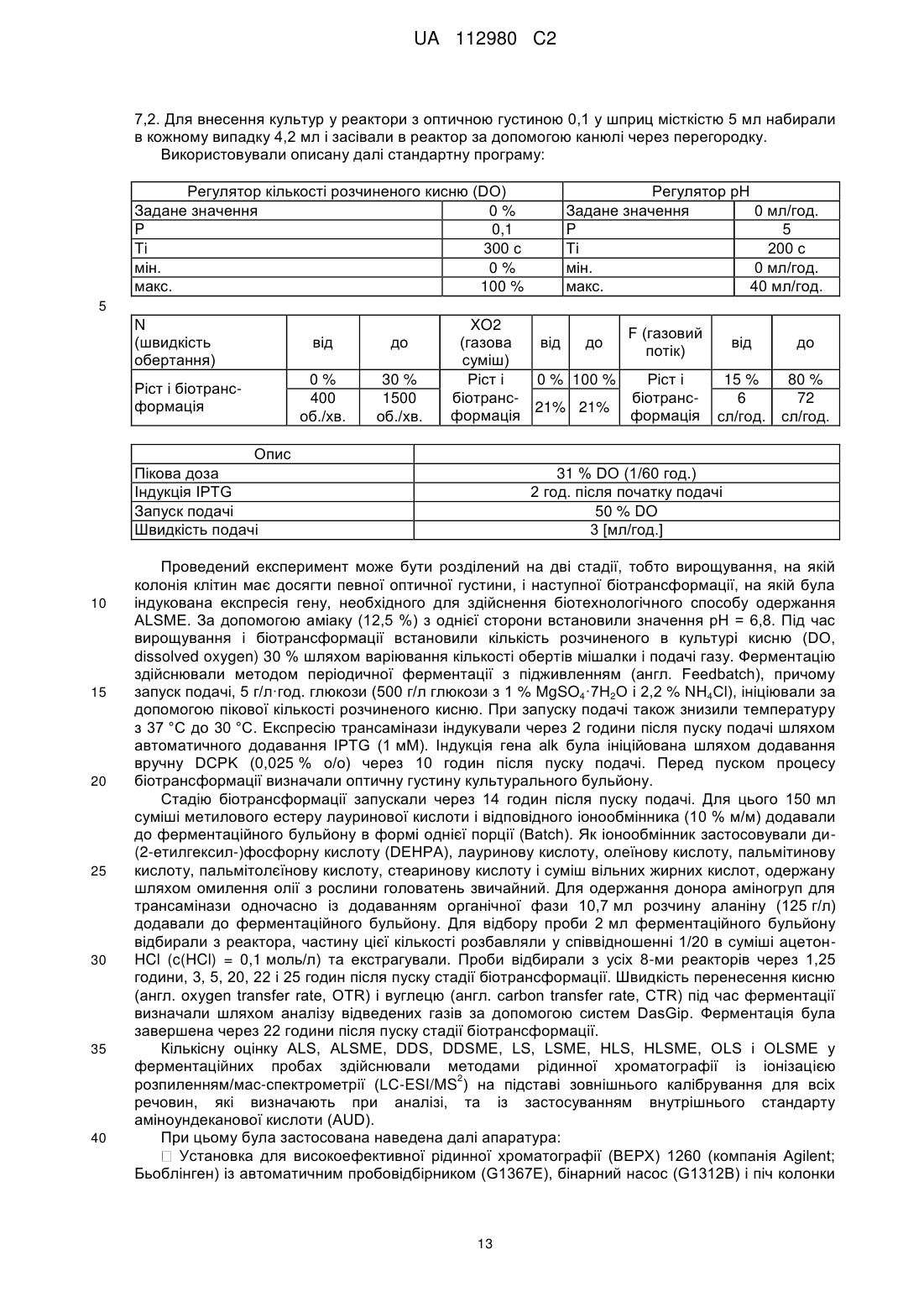
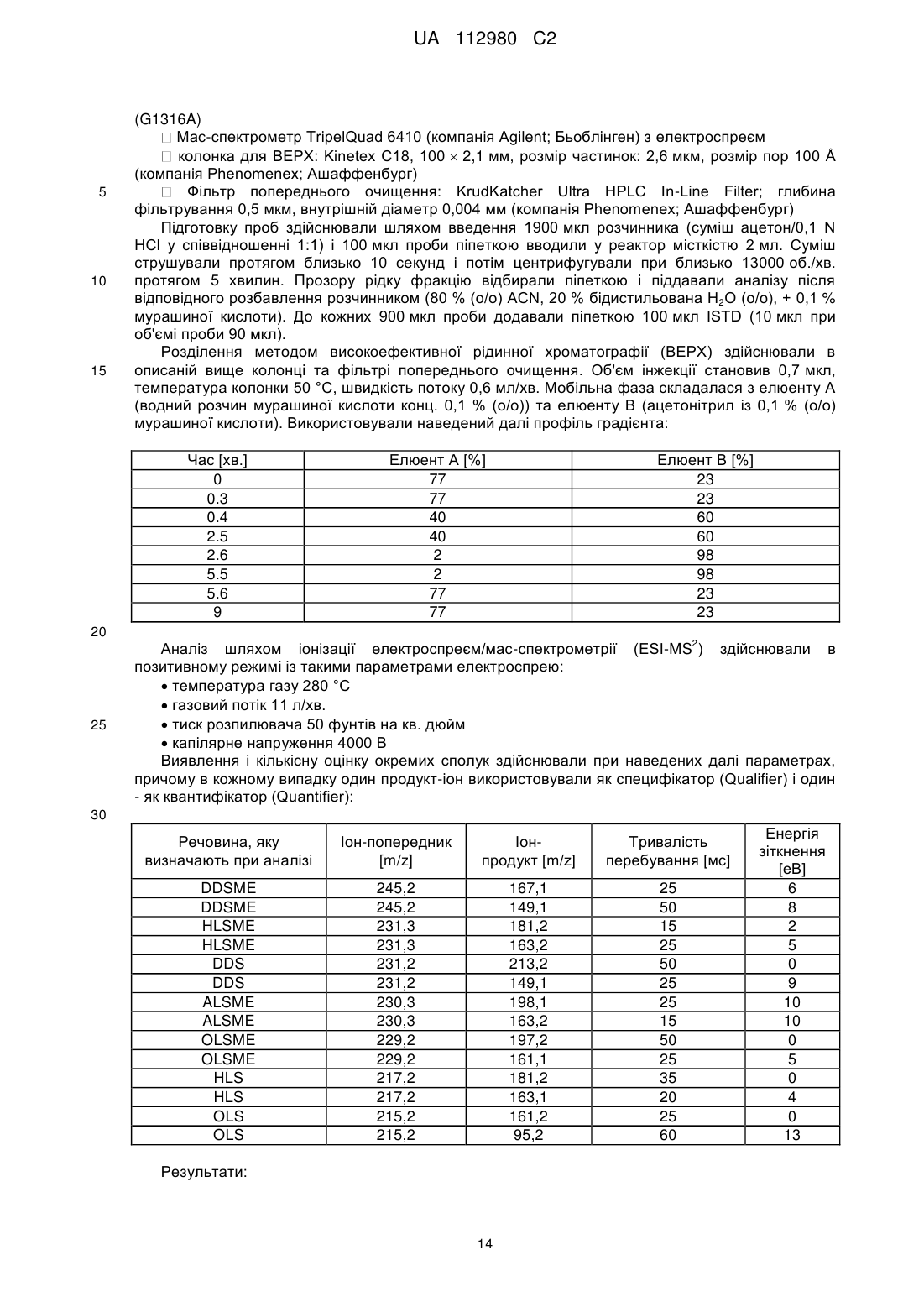
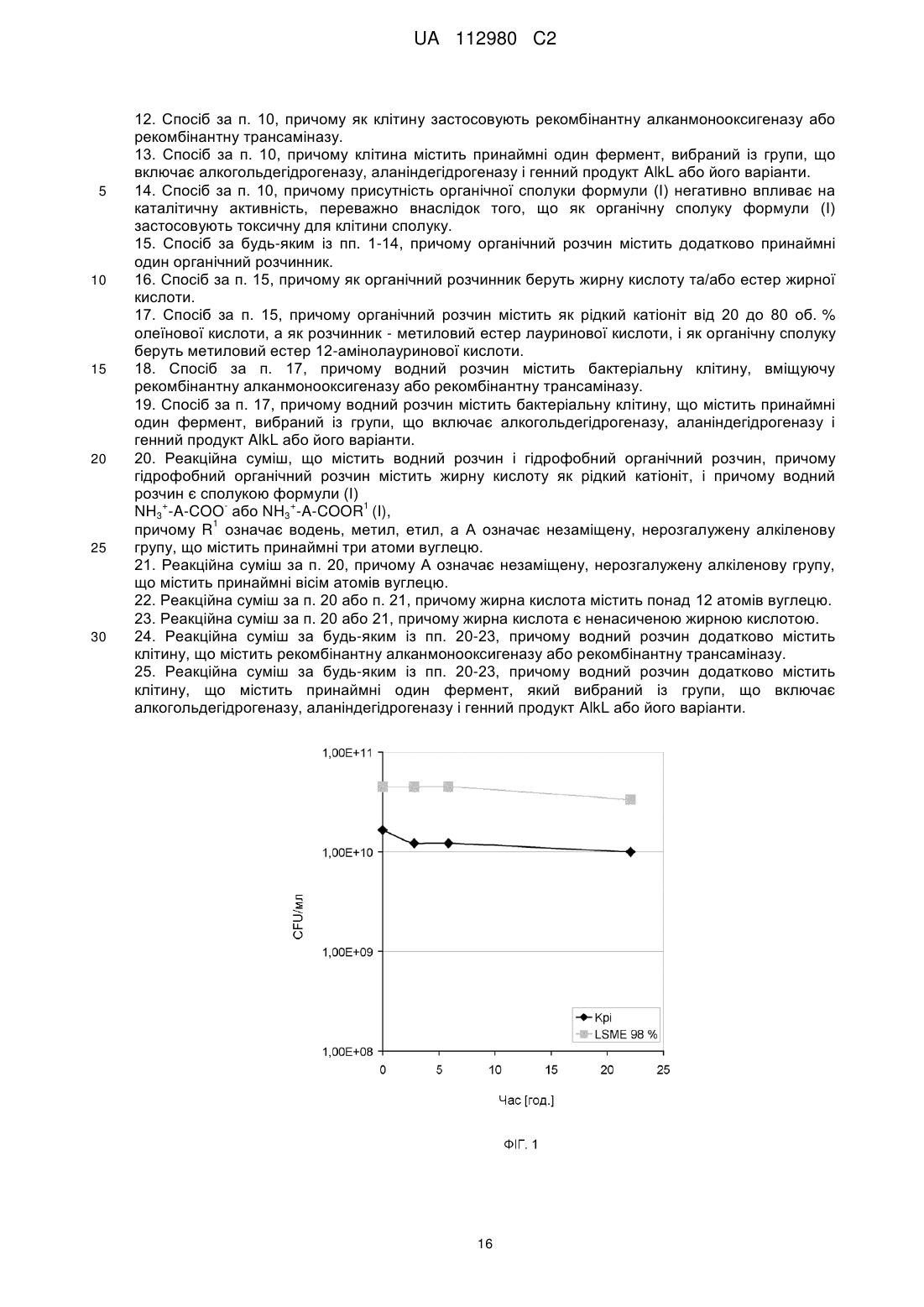
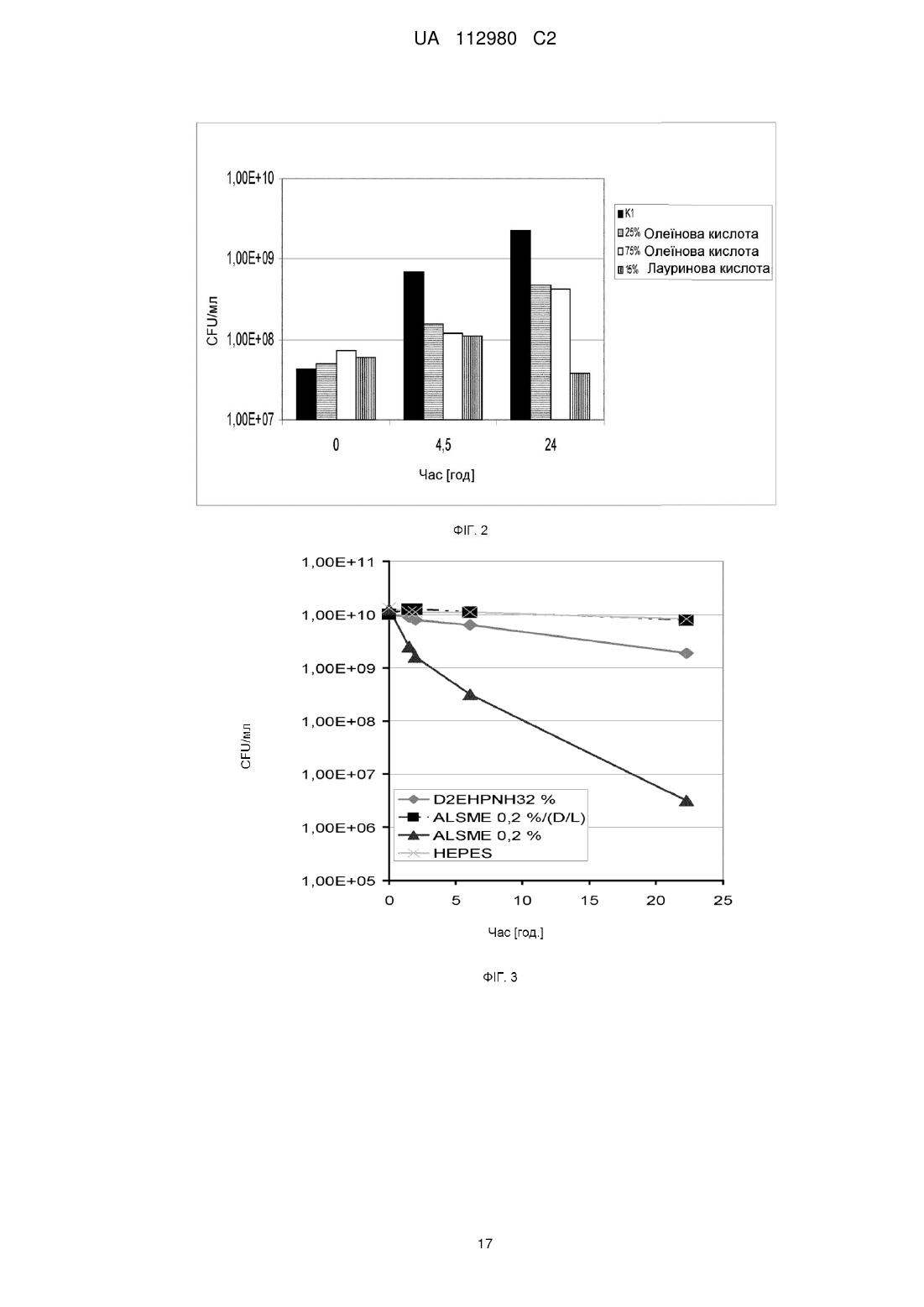
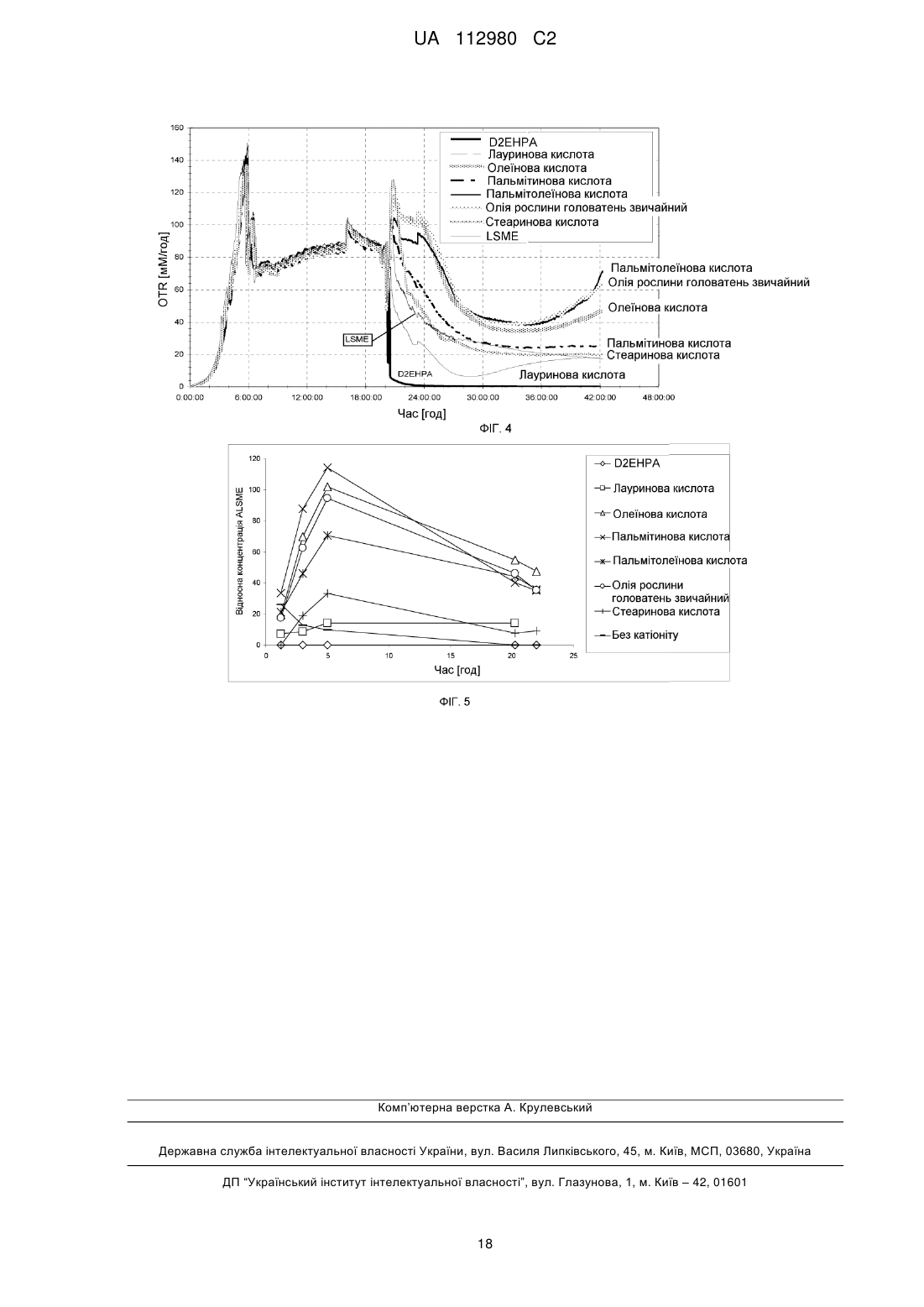
Реферат: Винахід стосується способу видалення органічної сполуки, що містить один або кілька позитивних зарядів, із водного розчину, який включає стадії а) одержання водного розчину, що містить органічну сполуку, і гідрофобного органічного розчину, що містить рідкий катіоніт, причому рідкий катіоніт є жирною кислотою, b) введення в контакт водного розчину і органічного розчину і с) відокремлення органічного розчину від водного розчину. UA 112980 C2 (12) UA 112980 C2 UA 112980 C2 5 10 15 20 25 30 35 40 45 50 55 60 Заявка стосується способу видалення органічної сполуки, що має один або кілька позитивних зарядів, із водного розчину, який включає стадії a) одержання водного розчину, що містить органічну сполуку, і гідрофобного органічного розчину, що містить рідкий катіоніт, причому рідкий катіоніт є гідрофобним, b) контактування водного розчину і органічного розчину і c) відокремлення органічного розчину від водного розчину, причому органічною сполукою є + 1 сполука формули NH3 -A-COOR , а також взаємопов'язані реакційні суміші. Основна проблема біотехнологічних способів одержання чистих хімікатів із використанням відновлюваної сировини, які зазвичай синтезують, виходячи з викопних видів палива, полягає в перенесенні одержаного продукту, який в типовому випадку перебуває у великооб'ємній водній фазі, в органічну фазу. Це перенесення здійснюють, з однієї сторони, для концентрації готового проміжного або кінцевого продукту і в разі необхідності забезпечення можливості синтетичної обробки на наступних стадіях реакції в органічному розчині; з іншої сторони - для поліпшення виходу реакції у водній фазі шляхом видалення бажаного продукту або взагалі можливості здійснення реакції в технічно раціональних рамках. Безпосереднє термічне згущування продукту, концентрація якого часто буває низькою, із великооб'ємного водного розчину, як правило, є недоцільним. Розподіл сполуки в двофазовій системі, що містить незмішувані між собою водну, гідрофільну фазу та органічну, гідрофобну фазу, значною мірою залежить від фізико-хімічних параметрів відповідної сполуки. В той час як сполуки, що містять велику частку або виключно незаміщені вуглеводні, перебувають переважно в гідрофобній фазі, сполуки з великим вмістом полярних груп, таких як вміщуючі гетероатоми функціональні групи, і цілком особливо сполуки, що несуть заряди, переважно або практично виключно перебувають у водній фазі, що ускладнює перенесення в органічну фазу. Розподіл сполуки у вказаній двофазовій системі після встановлення рівноваги часто описують за допомогою коефіцієнтів розподілу, наприклад згідно з рівнянням Нернста (Nernst) = cфаза 1 / cфаза 2. KОВ є спеціальним коефіцієнтом розподілу, який називають також параметром Р, що характеризує рівновагу розподілу сполуки між октаноловою і водною фазою: KОВ = P = cоктанол / Cвода. Прикладом позитивно зарядженої органічної сполуки, що користується великим попитом у промисловості, є 12-амінолауринова кислота (ALS) та її похідні, зокрема метиловий естер 12амінолауринової кислоти (ALSME). ALS є важливим вихідним продуктом для одержання полімерів, наприклад для виготовлення провідних систем і нейлону. Традиційно ALS одержують із викопної сировини у процесі з низьким виходом через лауринлактам, який синтезують шляхом тримеризації бутадієну, наступного гідрування з утворенням циклододекану, потім окиснення з одержанням циклододеканону, перетворення із застосуванням гідроксилаурину і наступного перегрупування Бекмана (Beckmann). Багатообіцяючий шлях біотехнологічного одержання ALS чи ALSME описаний в публікації DE10200710060705. Із рівня техніки відоме одержання позитивно заряджених органічних сполук шляхом контактування водної реакційної суміші, що містить біологічний агент, із органічною фазою, що містить органічний розчинник. Наприклад, у публікації DE10200710060705 описане одержання продукту ALSME шляхом екстрагування струшуванням із застосуванням етилового естеру оцтової кислоти із водної реакційної суміші. В публікації Asano et al. (2008) описане екстрагування ALS із застосуванням толуолу із водної реакційної суміші, що містить фермент, синтезуючий ALS. Тому в основу винаходу було покладено задачу розроблення способу видалення позитивно заряджених органічних сполук, зокрема -амінокарбонових кислот, що мають принаймні один позитивний заряд, із водної реакційної суміші, причому бажаним є якомога більш переважне положення рівноваги розподілу між реакційною сумішшю та застосовуваною як екстрагент гідрофобною органічною фазою, тобто рівновага розподілу має бути якнайдалі зміщена в сторону гідрофобної органічної фази. Іншою покладеною в основу винаходу задачею було розроблення способу видалення органічних сполук із принаймні одним позитивним зарядом, особливо -амінокарбонових кислот, із водного розчину, що містить біологічний агент, із застосуванням гідрофобної органічної фази як екстрагенту, в якому рівновага розподілу зміщена якомога далі в сторону гідрофобної органічної фази. Іншою покладеною в основу винаходу задачею було розроблення способу видалення органічних сполук із принаймні одним позитивним зарядом, особливо -амінокарбонових кислот, із водного розчину, який містить біологічний агент, із застосуванням гідрофобної органічної фази як екстрагенту, який якнайменше погіршує чи уповільнює ріст застосовуваних у 1 UA 112980 C2 5 10 15 20 25 30 35 40 45 50 55 60 біотехнологічних методах мікроорганізмів, зокрема Escherichia coli, та/або при цьому якомога менше зменшує кількість здатних до ділення та/або життєздатних, та/або респіраторно активних, та/або метаболічно активних і здатних до синтезу активних клітин. Іншою покладеною в основу винаходу задачею було розроблення способу видалення органічних сполук із принаймні одним позитивним зарядом, особливо -амінокарбонових кислот, із водного розчину, який містить біологічний агент, із застосуванням гідрофобної органічної фази як екстрагенту, в якому сукупність параметрів, які є вирішальними для виходу, сукупного обороту і швидкості здійснення покладеного в основу біотехнологічного способу, зокрема токсичність органічної фази порівняно з біологічним агентом і поглинання сполуки органічним екстрагентом, оптимізована стосовно загального виходу або прискорення здійснення процесу, або, в разі здійснення безперервного процесу, якнайтривалішої здатності біологічного агента до застосування, особливо в тому випадку, якщо органічна сполука з принаймні одним позитивним зарядом є продуктом або проміжним продуктом методу синтезу, одержаним із використанням каталітичної активності біологічного агента. Ці та інші задачі вирішені у предметі даної заявки і зокрема також у предметі додаткових незалежних пунктів формули винаходу, причому форми виконання є предметом залежних пунктів формули винаходу. Задачу, покладену в основу винаходу, в першому аспекті вирішено в способі видалення із водного розчину органічної сполуки, що містить один або кілька позитивних зарядів, який включає описані далі стадії: a) одержання водного розчину, що містить органічну сполуку, та гідрофобного органічного розчину, що містить рідкий катіоніт, причому рідкий катіоніт є гідрофобним, b) контактування водного і органічного розчинів, та c) відокремлення органічного розчину від водного розчину, причому органічна сполука є сполукою формули (I) + 1 NH3 -A-COOR (I), 1 причому R означає водень, метил, етил або негативний заряд, а A означає незаміщену, нерозгалужену алкіленову групу, що містить принаймні три, переважно принаймні вісім атомів вуглецю, і причому рідким катіонітом є жирна кислота. У першій формі виконання першого аспекту винаходу задачу вирішено в способі за пунктом 1, причому температура на стадії b) становить від 28 до 70, переважно від 30 до 37 °C. У другій формі виконання винаходу, яка також є формою виконання першої форми виконання першого аспекту, задачу вирішено в способі за будь-яким із пунктів 1-2, причому значення pH на стадії b) становить від 6 до 8, переважно від 6,2 до 7,2. У третій формі виконання винаходу, яка також є формою виконання 1-2 форм виконання першого аспекту, задачу вирішено в способі, причому кількісне співвідношення між рідким катіонітом і органічною сполукою становить принаймні 1. У третій формі виконання винаходу, яка також є формою виконання 1-3 форм виконання першого аспекту, задачу вирішено в способі, причому об'ємне співвідношення між органічним розчином і водним розчинами становить від 1:10 до 10:1. У четвертій формі виконання винаходу, яка також є формою виконання 1-3 форм виконання першого аспекту, задачу вирішено в способі, причому рідким катіонітом є жирна кислота, що містить понад 12, переважно від 14 до 22, ще переважніше від 16 до 18 атомів вуглецю. У п'ятій формі виконання винаходу, яка також є формою виконання 1-4 форм виконання першого аспекту, задачу вирішено в способі, причому рідким катіонітом є жирна кислота, переважно олеїнова або ерукова кислота. У шостій формі виконання винаходу, яка також є формою виконання 1-5 форм виконання першого аспекту, задачу вирішено в способі, причому водний розчин містить також біологічний агент, який має каталітичну активність. У сьомій формі виконання винаходу, яка також є формою виконання 1-6 форм виконання першого аспекту, задачу вирішено в способі, причому біологічним агентом є клітина, переважно біологічна клітина, і клітина ще переважніше містить рекомбінантну алканмонооксигеназу, рекомбінантну трансаміназу, а також переважно, крім цього, принаймні один фермент, вибраний із групи, що включає алкогольдегідрогеназу, аланін-дегідрогеназу і генний продукт AlkL або його варіанти. У восьмій формі виконання винаходу, яка також є формою виконання 1-7 форм виконання першого аспекту, задачу вирішено в способі, причому присутність органічної сполуки негативно впливає на каталітичну активність, переважно внаслідок того, що органічною сполукою є 2 UA 112980 C2 5 10 15 20 25 30 35 40 45 50 55 60 токсична для клітини сполука. У дев'ятій формі виконання винаходу, яка також є формою виконання 1-8 форм виконання першого аспекту, задачу вирішено в способі, причому органічний розчин містить крім цього принаймні один органічний розчинник, переважно жирну кислоту та/або естер жирної кислоти. У десятій формі виконання винаходу, яка також є формою виконання 1-9 форм виконання першого аспекту, задачу вирішено в способі за пунктом 12, причому органічний розчин як рідкий катіоніт містить від 20 до 80 об. %, переважно від 25 до 75 об. % олеїнової кислоти, а як розчинник - метиловий естер лауринової кислоти, і органічною сполукою є метиловий естер 12амінолауринової кислоти, а водний розчин містить бактеріальну клітину, що містить рекомбінантну алканмонооксигеназу, рекомбінантну трансаміназу, а також переважно, крім цього, принаймні один фермент, вибраний із групи, що включає алкогольдегідрогеназу, аланіндегідрогеназу і генний продукт AlkL або його варіанти. У другому аспекті задачу, покладену в основу винаходу, вирішено в реакційній суміші, яка містить водний розчин і гідрофобний органічний розчин, причому гідрофобний органічний розчин містить жирну кислоту, переважно жирну кислоту, що містить понад 12 атомів вуглецю, ще переважніше ненасичену жирну кислоту як рідкий катіоніт, і причому водним розчином є сполука формули (I) + 1 NH3 -A-COOR (I), 1 причому R означає водень, метил, етил або негативний заряд, а A означає незаміщену, нерозгалужену алкіленову групу, що містить принаймні три, переважно принаймні вісім атомів вуглецю. У формі виконання другого аспекту задачу, покладену в основу винаходу, вирішено в реакційній суміші згідно з першим аспектом, причому водний розчин містить також клітину, що вміщує рекомбінантну алканмонооксигеназу, рекомбінантну трансаміназу, а також переважно, крім цього, принаймні один фермент, вибраний із групи, що включає алкогольдегідрогеназу, аланін-дегідрогеназу і генний продукт AlkL або його варіанти. Інші форми виконання другого аспекту охоплюють усі форми виконання першого аспекту. Задачу, покладену в основу винаходу, в четвертому аспекті вирішено в способі видалення з водного розчину органічної сполуки, що містить один або кілька позитивних зарядів, який включає описані далі стадії: a) одержання водного розчину, що містить органічну сполуку, і гідрофобного органічного розчину, що містить рідкий катіоніт, причому рідкий катіоніт є гідрофобним, і причому рідкий катіоніт містить один або кілька негативних зарядів і має негативний загальний заряд, b) контактування водного розчину з органічним розчином, і c) відокремлення органічного розчину від водного розчину. У другій формі виконання четвертого аспекту даного винаходу, яка є також формою виконання першої форми виконання даного винаходу, спосіб містить стадію: d) обробка органічного розчину, переважно шляхом реекстрагування органічної сполуки в інший водний розчин. У третій формі виконання четвертого аспекту даного винаходу, яка також є формою виконання 1-2 форм виконання даного винаходу, температура на стадії b) відповідного винаходові способу становить від 28 до 70°C, переважно від 30 до 37°C. У четвертій формі виконання четвертого аспекту даного винаходу, яка також є формою виконання 1-3 форм виконання даного винаходу, значення pH на стадії b) відповідного винаходові способу становить 3 до 8, переважно від 6 до 8, особливо переважно від 6,2 до 7,2. У п'ятій формі виконання четвертого аспекту даного винаходу, яка також є формою виконання 1-4 форм виконання даного винаходу, кількісне співвідношення між рідким катіонітом і органічною сполукою при здійсненні способу становить принаймні 1. У шостій формі виконання четвертого аспекту даного винаходу, яка також є формою виконання 1-5 форм виконання даного винаходу, об'ємне співвідношення між органічним і водним розчинами становить від 1:10 до 10:1. У сьомій формі виконання четвертого аспекту даного винаходу, яка також є формою виконання 1-6 форм виконання даного винаходу, органічна сполука містить принаймні один позитивно заряджений замісник формули (I) + 2 3 4 -N R R R (I), 2 3 4 або, якщо принаймні один замісник із групи, що включає R , R і R є воднем, його непротоновану форму, 3 UA 112980 C2 2 5 10 15 20 25 30 35 40 45 50 55 60 3 4 причому R , R і R незалежно один від одного вибрані з групи, що включає водень, метил, етил, пропіл, 2-пропіл, бутил, трет-бутил, пентил, гексил, бензил, гідроксил, заміщений або незаміщений та/або нерозгалужений або розгалужений або циклічний алкіл або алкеніл. У восьмій формі виконання четвертого аспекту даного винаходу, яка також є формою виконання 1-7 форм виконання даного винаходу, органічна сполука має формулу (II) + 2 3 4 Z-A-N R R R (II), 2 3 4 або, якщо принаймні один замісник із групи, що включає R , R і R , є воднем, є його непротонованою формою, 2 3 4 причому R , R і R незалежно один від одного вибрані з групи, що включає водень, метил, етил, пропіл, 2-пропіл, бутил, трет-бутил, пентил, гексил, бензил, гідроксил, заміщений або незаміщений та/або нерозгалужений або розгалужений або циклічний алкіл або алкеніл, причому A є вуглеводневим ланцюгом, що містить принаймні три атоми вуглецю, переважно незаміщену алкенільну групу, 5 і причому Z вибраний із групи, що включає -COOH, -COOR , -COH, -CH2OH і їх непротоновані форми, 5 причому R вибраний із групи, що включає водень, метил, етил, пропіл, 2-пропіл, бутил, трет-бутил, пентил, гексил, бензил, гідроксил, заміщений або незаміщений та/або нерозгалужений або розгалужений, або циклічний алкіл або алкеніл. У дев'ятій формі виконання четвертого аспекту даного винаходу, яка також є формою виконання 1-8 форм виконання даного винаходу, органічна сполука має формулу (III) + 1 NH3 -A-COOR (III), 1 або її непротоновану форму, причому R водень, метил або етил, а A означає незаміщену, нерозгалужену алкілeнову групу, що містить принаймні три атоми вуглецю. У десятій формі виконання четвертого аспекту даного винаходу, яка також є формою виконання 1-9 форм виконання даного винаходу, рідкий катіоніт містить принаймні одну алкільну або алкенільну групу, що містить принаймні шість атомів вуглецю, а також кінцевий замісник, вибраний із групи, що включає -COOH, -OSO2H, -OPO(OH)2- і -OPO(OH)O- та їх непротоновані форми. В одинадцятій формі виконання четвертого аспекту даного винаходу, яка також є формою виконання 1-10 форм виконання даного винаходу, рідким катіонітом є ненасичена жирна кислота, переважно олеїнова кислота. У дванадцятій формі виконання четвертого аспекту даного винаходу, яка також є формою виконання 1-11 форм виконання даного винаходу, водний розчин містить також біологічний агент, що має каталітичну активність. У тринадцятій формі виконання четвертого аспекту даного винаходу, яка також є формою виконання 1-12 форм виконання даного винаходу, біологічний агент є клітиною, переважно бактеріальною клітиною. У чотирнадцятій формі виконання четвертого аспекту даного винаходу, яка також є формою виконання 1-13 форм виконання даного винаходу, присутність органічної сполуки негативно впливає на каталітичну активність. У п'ятнадцятій формі виконання четвертого аспекту даного винаходу, яка також є формою виконання 1-14 форм виконання даного винаходу, органічний розчин містить крім цього принаймні один органічний розчинник, переважно жирну кислоту та/або естер жирної кислоти. У шістнадцятій формі виконання четвертого аспекту даного винаходу, яка також є формою виконання 1-15 форм виконання даного винаходу, органічний розчин містить як рідкий катіоніт від 20 до 80 об. %, переважно від 25 до 75 об. % олеїнової кислоти, а як розчинник - метиловий естер лауринової кислоти, і органічною сполукою є метиловий естер 12-амінолауринової кислоти, а водний розчин містить бактеріальну клітину, що має каталітичну активність, яку використовують у синтезі метилового естеру 12-амінолауринової кислоти. У п'ятому аспекті задачу, покладену в основу винаходу, вирішено у біореакторі, що містить водний розчин, вміщуючий біологічний агент, і гідрофобний органічний розчин, вміщуючий рідкий катіоніт. У переважній формі виконання даного винаходу поняття "біореактор", застосовуване в даному випадку, означає будь-який резервуар, в якому придатні до використання у біотехнологічних методах мікроорганізми культивують у контрольованих умовах та/або можуть бути використані для здійснення біотехнологічного способу, переважно синтезу органічної сполуки. У другій формі виконання п'ятого аспекту, яка також є формою виконання першої форми виконання третього аспекту даного винаходу, рідким катіонітом є жирна кислота, переважно олеїнова кислота. У третій формі виконання п'ятого аспекту, яка також є формою виконання 1-2 форм 4 UA 112980 C2 5 10 15 20 25 30 35 40 45 50 55 60 виконання третього аспекту даного винаходу, гідрофобний органічний розчин містить також естер жирної кислоти, переважно метиловий естер лауринової кислоти. У четвертій формі виконання п'ятого аспекту, яка також є формою виконання 1-3 форм виконання другого аспекту даного винаходу, гідрофобний органічний розчин містить як катіоніт олеїнову кислоту, а як розчинник - від 25 до 75 об. % метилового естеру лауринової кислоти. У п'ятій формі виконання, яка також є формою виконання 1-4 форм виконання п'ятого аспекту даного винаходу, органічною сполукою є сполука згідно з однією з форм виконання першого аспекту винаходу. У шостому аспекті задачу, покладену в основу даного винаходу, вирішено в способі одержання органічної сполуки, що має один або кілька позитивних зарядів, причому органічна сполука є токсичною для клітин, який включає культивування у водному розчині клітин, використовуваних у синтезі органічної сполуки, переважно клітин, які каталізують принаймні одну стадію синтезу, в присутності гідрофобного органічного розчину, що містить рідкий катіоніт і необов'язково органічний розчинник. У другій формі виконання шостого аспекту даного винаходу органічною сполукою є 12амінолауринова кислота або метиловий естер 12-амінолауринової кислоти, а органічним розчинником є метиловий естер лауринової кислоти. Інші форми виконання четвертого, п'ятого і шостого аспектів охоплюють усі форми виконання першого і другого аспектів даного винаходу. Авторами даного винаходу було винайдено, що ефективність видалення із водного розчину органічної сполуки, що має один або кілька позитивних зарядів, у гідрофобний органічний розчин може бути неочікувано збільшена, якщо цей органічний розчин містить рідкий катіоніт. Не бажаючи бути обмеженими будь-якою теорією, автори даного винаходу припускали, що між негативним зарядом чи негативними зарядами рідкого катіоніту та позитивним зарядом чи позитивними зарядами органічної сполуки відбувається іонна взаємодія, і що ця взаємодія веде до маскування принаймні одного позитивного заряду, що підвищує розчинність в органічній фазі. У переважній формі виконання поняття "рідкий катіоніт", який застосовують у цьому описі, означає розчинну в гідрофобному органічному розчиннику сполуку, яка внаслідок одного або кількох негативних постійних зарядів є здатною до іонної взаємодії принаймні з одним катіоном. У типовому випадку рідкий катіоніт містить принаймні один насичений або ненасичений вуглеводневий ланцюг, який може бути нерозгалуженим або розгалуженим, а також негативно заряджену групу, наприклад карбоксильну групу. У переважній формі виконання рідким іонообмінником є жирна кислота, у ще переважнішій формі виконання - ненасичена жирна кислота, наприклад олеїнова кислота. У переважній формі виконання рідким іонообмінником є ди(2-етилгексил)фосфорна кислота (називана також DEHPA або D2EHPA). У переважній формі виконання рідкий іонообмінник має не лише негативний сукупний заряд, а взагалі не має позитивного заряду. У переважній формі виконання поняття "загальний заряд" іонообмінника або іншої молекули, яке використовують в цьому описі, означає суму зарядів усіх ковалентно сполучених із молекулою функціональних груп. Наприклад, лауринова кислота при pH = 7 має негативний загальний заряд, незалежно від присутності інших молекул або протиіонів, таких як іони калію, які присутні у водному розчині. У переважній формі виконання даного винаходу поняття "контактування", яке застосоване в цьому описі, означає, що дві фази безпосередньо і зокрема без проміжного включення фізичного бар'єру, такого як мембрана, вводять у контакт між собою. Контактування в найпростішому випадку здійснюють шляхом закладання обох фаз в один резервуар і змішування їх між собою відповідним чином, наприклад шляхом перемішування за допомогою мішалки. У переважній формі виконання винаходу органічна сполука має позитивний загальний заряд. В іншій переважній формі виконання органічна сполука не має негативних зарядів. У переважній формі виконання органічною сполукою є -амінокарбонова кислота. У переважній формі виконання винаходу поняття "має заряд", застосовуване в даному описі, означає, що конкретна сполука має відповідний заряд у водному розчині при pH від 0 до 14, переважно від 2 до 12, від 2 до 6, від 8 до 12, від 3 до 10, від 6 до 8, найбільш переважно при pH = 7. У переважній формі виконання винаходу йдеться про сталий заряд. В іншій переважній формі виконання винаходу поняття "має заряд" застосовуване в даному описі, означає, що відповідна функціональна група або сполука при pH = 7 має відповідний заряд переважно, тобто принаймні на 50, переважно на 90, ще переважніше на 99 %. У переважній формі виконання винаходу поняття "містить" слід розуміти як "охоплює", тобто "містить не виключно". Суміш, що містить A, в цьому смислі може, крім A, містити інші 5 UA 112980 C2 5 10 15 20 25 30 35 40 45 50 55 60 компоненти. Формулювання "один або кілька зарядів" означає принаймні один заряд відповідної природи. У переважній формі виконання винаходу поняття "гідрофобний", застосовуване в даному описі, означає властивість рідини в присутності водної фази утворювати власну, чітко відокремлену від водної фази рідку фазу. Остання може бути однорідною рідкою фазою або емульсією. В іншій переважній формі виконання винаходу поняття "гідрофобний", застосовуване в даному описі, слід розуміти як властивість сполуки в основному не розчинятися у воді. Насамкінець, це поняття в іншій переважній формі виконання винаходу, застосовуване в даному описі, слід розуміти так, що охарактеризована таким чином сполука має такий параметр Р (J. Sangster, Octanol-Water Partition Coefficients: Fundamentals and Physical Chemistry, Wiley Series in Solution Chemistry, том 2, John Wiley & Sons, Чичестер, 1997 р.), десятковий логарифм якого перевищує 0, переважно перевищує 0,5, ще переважніше перевищує 1 і особливо переважно перевищує 2. В іншій формі виконання даного винаходу рідкий іонообмінник не справляє або справляє лише помірну токсичну дію на застосовувані в біотехнологічних методах мікроорганізми. Поняття "токсична дія", застосовуване в даному описі, у переважній формі виконання винаходу означає властивість сполуки при контакті з відповідними мікроорганізмами зменшувати швидкість їх росту та метаболічну активність, підвищувати їх енергоспоживання, знижувати оптичну щільність або кількість здатних до росту клітин та/або безпосередньо призводити до їх відмиранню та лізису. У переважній формі виконання винаходу принаймні один із цих ефектів досягається вже при невеликій концентрації токсичної сполуки, переважно при концентрації 1000, переважніше 100, ще переважніше 50 або 25, особливо переважно 5 мг/л. Фахівцям відомі численні традиційно застосовувані методи дослідження токсичності. До них належать, наприклад, вимірювання дихання відповідних мікроорганізмів за допомогою кисневих електродів або порівняльне висівання мікроорганізмів на пластини з живильним матеріалом і наступний підрахунок колонієутворюючих одиниць (CFU). У переважній формі виконання винаходу "помірна токсична дія" означає, що мікроорганізми, що перебувають на стадії росту, в присутності сполуки продовжують рости та/або зберігають метаболічну активність проте в меншому обсязі, ніж контрольна група, яку інкубували в таких самих умовах без застосування відповідної сполуки, та/або відрізняються подовженою лаг-фазою. Контактування водного і органічного розчинів здійснюють у відповідних умовах і зокрема протягом часу, який є достатнім для переходу органічної сполуки з водної фази в органічну фазу, в ідеальному випадку навіть для встановлення відповідної рівноваги. Тривалість і умови можуть бути визначені фахівцями за результатами звичайних дослідів. В особливо переважній формі виконання винаходу органічною сполукою, що має один або кілька позитивних зарядів, є амінована по кінцевій групі жирна кислота, особливо переважно 12амінолауринова кислота, або її естер, або суміш обох сполук. Фахівцям відомо, що естер жирної кислоти в присутності біологічної системи, яка містить активні естерази, частково може перебувати в формі відповідної кислоти, і обидві сполуки в цьому зв'язку слід розглядати як еквівалентні. Відповідно до цього поняття "жирні кислоти" або "похідні жирних кислот" в особливо переважній формі виконання винаходу, застосовуване в даному описі, охоплює також відповідні естери, переважно метиловий естер, і навпаки. В особливо переважній формі виконання винаходу поняття "алкілeнова група", застосовуване в даному описі, означає групу формули -(CH2)n-, тобто алкан, що містить два незайняті, переважно кінцевих замісники. Якщо кількість замісників дорівнює двом, один із них може бути аміногрупою, а інший - карбоксильною групою. У переважній формі виконання винаходу n становить принаймні 3, більш переважно принаймні 6, ще переважніше 11. У "заміщеному алкілeновому ланцюгу" принаймні атом водню заміщений іншим замісником, який не є атомом водню або алкільним залишком, переважно інший атом, який не є атомом водню. На відміну від цього, в особливій формі виконання винаходу поняття "незаміщена алкілeнова група", застосовуване в даному описі, означає вуглеводневий ланцюг формули -(CH2)n- без подібних замісників. Температура на стадії b) залежить не лише від властивостей рідкого катіоніту, а, зокрема в тому випадку, якщо контактування водного і органічного розчинів в процесі реакції відбувається у водній фазі, також від температур, необхідних для здійснення реакцій, що відбуваються у водній фазі. Зокрема в тому випадку, якщо біологічний агент, такий як жива клітина, є активним у водній фазі, температура має бути відповідною для підтримання цієї активності. У переважній формі виконання винаходу температура на стадії b) становить від 0 до 100 °C, переважніше від 20 до 80 °C, від 28 до 70 °C, від 30 до 37 °C, від 35 до 40 °C. Значення pH на стадії b) також має відповідати вимогам відповідних одночасно 6 UA 112980 C2 5 10 15 20 25 30 35 40 45 50 55 60 здійснюваних реакцій, стабільності реагентів, продуктів, проміжних кінцевих продуктів або агентів. У переважній формі виконання винаходу значення pH становить від 3 до 8, переважніше від 6 до 8, ще переважніше від 6,2 до 7,2. Для переведення якнайбільшої кількості органічної сполуки з водної фази в органічну необхідно застосовувати достатню кількість рідкого катіоніту. В переважній формі виконання даного винаходу сумарне кількісне співвідношення між рідким катіонітом і органічною сполукою принаймні на одній стадії в безперервному процесі протягом всього часу здійснення реакції становить принаймні 1, тобто на одну молекулу органічної сполуки застосовують принаймні одну молекулу рідкого катіоніту. В ще більш переважній формі виконання винаходу співвідношення перевищує 2, 3, 5, 10, 15, або 20, переважно становить від 1,5 до 3. Об'ємне співвідношення між органічним і водним розчином, разом із кількісним співвідношенням катіоніт/органічна сполука, є вирішальним для ефективного здійснення способу. В особливій формі виконання винаходу воно становить від 100:1 до 1:100, переважніше від 20:1 до 1:20, ще переважніше від 10:1 до 1:10, від 4:1 до 1:4, від 3:1 до 1:3 або особливо переважно від 1:2 до 2:1. У переважній формі виконання даного винаходу жирну кислоту застосовують як рідкий катіоніт. У переважній формі виконання даного винаходу поняття "жирна кислота", застосовуване в даному описі, означає карбонову кислоту, переважно алканову кислоту, що містить принаймні 6, переважно 8, ще переважніше 10, цілком переважно 12 атомів вуглецю. У переважній формі виконання винаходу йдеться про жирні кислоти з нерозгалуженим ланцюгом, в іншій формі виконання винаходу - із розгалуженим. У переважній формі виконання винаходу йдеться про насичені жирні кислоти. В особливо переважній формі виконання винаходу йдеться про ненасичені жирні кислоти. У іншій переважній формі виконання винаходу йдеться про жирну кислоту з нерозгалуженим ланцюгом, що містить принаймні 12 атомів вуглецю і подвійний зв'язок, переважно у 9-му положенні. В іншій переважній формі виконання винаходу йдеться про мононенасичену жирну кислоту, в якій подвійний зв'язок перебуває в 9-му та/або 11-му положенні. В іншій переважній формі виконання винаходу рідким катіонітом є ненасичена жирна кислота, вибрана із групи, що включає олеїнову, пальмітолеїнову і гадолеїнову кислоти та ейкозенову кислоту. У цілком переважній формі виконання винаходу йдеться про олеїнову кислоту. В особливо переважній формі виконання винаходу йдеться про жирну кислоту, що містить 6, 7, 8 9, 10,11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 атомів вуглецю, переважно понад 12, переважніше понад 14 атомів вуглецю, ще переважніше від 14 до 28, від 14 до 22, цілком переважно від 16 до 18 атомів вуглецю. В іншій переважній формі виконання винаходу як рідкий іонообмінник застосовують суміш різних жирних кислот, яка перебуває, наприклад, у формі соєвої олії або олії з рослини головатень звичайний. В разі потреби здійснюють попередній гідроліз, якщо жирні кислоти перебувають у формі естерів. В особливо переважній формі виконання даного винаходу застосовують комбінацію двох рідких катіонітів, переважно принаймні одним із яких є жирна кислота. Особливою перевагою даного винаходу є сумісність відповідного винаходові способу з біотехнологічними методами і використовуваними в них біологічними агентами. В особливій формі виконання даного винаходу поняття "біологічний агент, що має каталітичну активність", застосовуване в даному описі, слід розуміти як синтезований клітиною біокаталізатор на всіх стадіях очищення, від усієї клітини до ізольованої молекули. У переважній формі виконання винаходу йдеться про клітину, що продукує ферменти, які мають каталітичну активність. Клітиною може бути прокаріот, включаючи археї (Аrchaea), або евкаріоти, переважно із групи, що включає Pseudomonas, Corynebacterium і E. coli. У більш переважній формі виконання винаходу агентом є бактеріальна клітина, ще переважніше - грам-негативна бактеріальна клітина, цілком переважно E. coli. В іншій переважній формі виконання винаходу йдеться про клітину-евкаріот, переважніше про клітину гриба, ще переважніше про дріжджову клітину, цілком переважно про Saccharomyces або Candida, Pichia, зокрема Candida tropicalis. Поняття "клітина" та "мікроорганізм" в особливій формі виконання, в цій заявці застосовують як рівнозначні та взаємозамінні. Крім цього, як клітина може бути застосована ізольована клітина або суміш культур. Застосовувана як біологічний агент клітина може бути життєздатною або препарованою, наприклад це може бути мембранна або цитозольна фракції, або неочищений екстракт клітини. Якщо біологічним агентом є ізольована молекула на різних стадіях очищення, це може бути вся каталітично активна, продукована клітиною молекула. В особливо переважній формі виконання йдеться про молекулу з групи, що включає пептиди, поліпептиди, вуглеводи, нуклеїнові кислоти або їх змішані форми. У ще переважнішій формі виконання винаходу 7 UA 112980 C2 5 10 15 20 25 30 35 40 45 50 55 60 йдеться про каталітично активний поліпептид. В іншій переважній формі виконання винаходу йдеться про іммобілізовану молекулу. Необхідні для синтетичного біотехнологічного способу каталітичні функції є різноманітними. У переважній формі виконання поняття "каталітична активність", застосовуване в даному описі, означає синтетичну активність, тобто каталіз хімічних реакцій, що включає утворення принаймні одного нового ковалентного зв'язку. В іншій переважній формі виконання винаходу йдеться про транспортувальну активність, тобто здатність молекули забезпечувати перенесення іншої молекули із одного компартменту в інший, наприклад вбирання речовини з водного середовища через клітинну мембрану всередину клітини. В особливо переважній формі виконання винаходу біологічним агентом є жива клітина, яку в присутності рідкого катіоніту застосовують для каталізу, переважно для синтезу органічної сполуки з одним або кількома позитивними зарядами, яку потім або одночасно за допомогою рідкого катіоніту видаляють із гідрофобної органічної фази. В особливо переважній формі виконання присутність органічної сполуки негативно впливає на каталітичну активність. В одній з форм виконання винаходу внаслідок цього може зменшуватися наявна активність, яка може бути виражена нижчим значенням k cat ферменту. В іншій формі виконання винаходу спорідненість агента, що проявляє каталітичну активність, може проявлятися в смислі збільшення KM ферменту. В іншій формі виконання винаходу може бути змінена специфічність каталітичної активності, наприклад таким чином, що він перетворює або переважно перетворює іншу, відмінну від бажаної молекулу-основу. В іншій формі виконання винаходу органічна сполука справляє токсичну дію на клітину як біологічний агент. В іншій формі виконання органічною сполукою є органічна сполука, яка зменшує доступність незамінного косубстрату або коферменту. Це може мати місце, наприклад, у тому випадку, якщо органічна сполука інгібує відповідну реакцію регенерації. Окрім рідкого катіоніту, гідрофобна органічна фаза може містити також гідрофобний розчинник. Це може сприяти збільшенню поглинальної здатності рідкого катіоніту в гідрофобній фазі і запобіганню небажаним ефектам, наприклад коагуляції. У переважній формі виконання винаходу розчинником є реагент, що використовують у реакції, яку здійснюють у водному розчині, найбільше переважно субстрат каталізованої ферментом реакції, яку здійснюють у водному розчині. В переважній формі виконання винаходу йдеться про естер жирної кислоти. В особливо переважній формі виконання винаходу розчинником є естер жирної кислоти, переважно - метиловий естер жирної кислоти, що діє як рідкий катіоніт. Вміст розчинника, якщо його застосовують, у гідрофобній органічній фазі в переважній формі виконання становить від 1до 99 об. %. У переважній формі виконання вміст розчинника становить від 10 до 90, переважніше від 20 до 80, особливо переважно від 25 до 75 об. %. У цілком переважній формі виконання способу органічною сполукою є 12-амінолауринова кислота та/або метиловий естер 12-амінолауринової кислоти, яку чи який одержують у водній фазі рекомбінантного штама E. coli шляхом покрокового окиснення кінцевого атому вуглецю метилового естеру лауринової кислоти, як описано в публікації DE10200710060705, а гідрофобна фаза містить від 25 до 75 % олеїнової кислоти як рідкий катіоніт, розчиненої в метиловому естері лауринової кислоти як субстраті реакції. Ідея даного винаходу може бути пояснена не лише із застосуванням точної послідовності аміно- або нуклеїнових кислот вказаних у цьому описі біологічних макромолекул, але також із застосуванням варіантів подібних макромолекул, які можуть бути одержані шляхом делеції, приєднання або заміщення однієї чи кількох амінокислот або нуклеїнових кислот. У переважній формі виконання винаходу поняття "варіант" означає послідовність нуклеїнових або амінокислот, далі застосовуване як рівнозначне і замінне з поняттям "гомолог", застосовуване в даному описі, інша послідовність нуклеїнових або амінокислот, яка з урахуванням відповідної первинної послідовності нуклеїнових або амінокислот дикого типу має гомологію, в даному випадку застосовувану як поняття, рівнозначне ідентичності, що становить 70, 75, 80, 85, 90, 92, 94, 96, 98, 99 % або більше відсотків, причому переважно інші на відміну від утворюючих каталітично активний центр амінокислот або структуру, або складчасту структуру незамінні амінокислоти видалені або заміщені, або останні лише консервативно заміщені, наприклад глутамат замість аспартату або лейцин замість валіну. У рівні техніки описані алгоритми, які можуть бути застосовані для розрахунку міри гомології двох послідовностей, наприклад у публікації Arthur Lesk (2008), Introduction to bioinformatics, 3-я редакція. В іншій переважній формі виконання даного винаходу один варіант послідовності аміно- або нуклеїнових кислот, переважно додатково до вказаної вище гомології послідовностей, в основному проявляє таку саму ферментативну активність, як молекула дикого типу чи первинна молекула. Наприклад, варіант ферментативно активного як протеаза поліпептиду має таку саму або в основному таку 8 UA 112980 C2 5 10 15 20 25 30 35 40 45 50 55 60 саму протеолітичну активність, що й поліпептидний фермент, тобто здатність каталізувати гідроліз пептидного зв'язку. В особливій формі виконання поняття "в основному таку саму ферментативну активність" означає активність відносно субстрату поліпептиду дикого типу, яка є значно вищою, ніж фонова активність та/або менше ніж на три, переважно на два, ще переважніше на один порядок відрізняється від значень KM- та/або kcat-, які має поліпептид дикого типу відносно однакових субстратів. В іншій переважній формі виконання винаходу поняття "варіант" послідовності нуклеїнових або амінокислот охоплює принаймні одну активну частину/або фрагмент послідовності нуклеїнових або амінокислот. В іншій переважній формі виконання винаходу поняття "активна частина", застосовуване в даному описі, означає послідовність аміно- або нуклеїнових кислот, що має меншу ніж повна довжину послідовності амінокислот чи кодує меншу ніж повна довжину послідовності амінокислот, причому послідовність амінокислот або кодована послідовність амінокислот із меншою довжиною, ніж послідовність амінокислот дикого типу, в основному проявляє таку саму ферментативну активність, що й поліпептид дикого типу або його варіант, наприклад як алкогольдегідрогеназа, монооксигеназа або трансаміназа. В особливій формі виконання винаходу поняття "варіант" нуклеїнової кислоти охоплює нуклеїнову кислоту, комплементарний ланцюг якої, переважно в обов'язкових умовах, прив'язаний до нуклеїнової кислоти дикого типу. Обов`язковість умов реакції гібридизації може бути легко визначена фахівцями і залежить в загальному випадку від довжини зонда, температури при промиванні та концентрації солі. В загальному випадку довші зонди потребують вищої температури для гібридизації, на відміну від чого для коротших проб достатніми є нижчі температури. Чи відбувається гібридизація, залежить в основному від здатності денатурованої ДНК до анелювання до комплементарних ланцюгів, наявних в їх оточенні, а саме нижче температури розплавлення. Обов'язковість реакції гібридизації і відповідні умови докладно описані в публікації Ausubel et al. 1995. У переважній формі виконання поняття "варіант" нуклеїнової кислоти, застосовуване в даному описі, охоплює будьяку послідовність нуклеїнових кислот, яка кодує таку саму послідовність амінокислот, що й вихідна нуклеїнова кислота або варіант цієї послідовності амінокислот в рамках здатності генетичного коду до дегенерації. Придатні до застосування поліпептиди, які можуть бути використані для одержання органічних сполук формули (I), зокрема алканмонооксигеназ, AlkL, трансаміназ, альдегіддегідрогеназ і аланіндегідрогеназ, описані в рівні техніки, наприклад у публікаціях DE10200710060705, EP11004029 або PCT/EP2011/053834. У цілком переважній формі виконання винаходу алканмонооксигеназою є алканмонооксигеназа AlkB-типу. AlkB є оксидоредуктазою з системи AlkBGT із Pseudomonas putida, яка відома своєю гідроксилaзною активністю. Вона залежить від двох інших поліпептидів, AlkG і AlkT. AlkT характеризують як FAD-залежну редуктазу рубредоксин, яка передає електрони із NADH до AlkG. AlkG є рубредоксином, залізовмісним редокс-білком, який функціонує як прямий донор електронів для AlkB. У переважній формі виконання винаходу поняття "алканмонооксигеназа AlkB-типу", застосовуване в даному описі, слід розуміти як мембранну алканмонооксидазу. В іншій переважній формі виконання винаходу те саме поняття " алканмонооксигеназа AlkB-типу" означає поліпептид із гомологією послідовностей у порядку зростання від переважно принаймні 75, 80, 85, 90, 92, 94, 96, 98 або 99 % до послідовності AlkB Pseudomonas putida Gpo1 (код банку даних: CAB54050.1). В іншій переважній формі виконання винаходу це поняття означає цитохром-незалежну монооксигеназу. В іншій переважній формі виконання винаходу поняття "алканмонооксигеназа AlkB-типу" означає цитохромнезалежну монооксигеназу, яка використовує принаймні рубредоксин або його гомолог як донор електронів. В особливо переважній формі виконання винаходу поняття слід розуміти як мембранну, цитохром-незалежну алканмонооксигеназу у порядку зростання від переважно принаймні 60, 70, 80, 80, 85, 90, 92, 94, 96, 98 або 99 % до послідовності AlkB Pseudomonas putida Gpo1, яка потребує як донор електронів принаймні AlkG (CAB54052.1), проте переважно комбінацію AlkG з редуктазою AlkT (CAB54063.1), причому alkG та/або alkT також можуть бути гомологами відповідного поліпептиду. Поняття "послідовність", застосовуване в даному описі, може стосуватися послідовності амінокислот поліпептиду та/або кодуючої послідовності нуклеїнових кислот. В іншій переважній формі виконання поняття "алканмонооксигеназа AlkBтипу", застосовуване в даному описі, означає цитохром-незалежну оксиредуктазу, тобто оксиредуктазу, що не містить цитохром як кофактор. Далі винахід пояснюється докладніше за допомогою креслень і необмежуючих прикладів, у яких описані інші ознаки яких, форми виконання, аспекти і переваги даного винаходу. Фіг. 1 Контрольний експеримент для підтвердження, що LSME не спричиняє токсичної дії, із застосуванням штаму E. coli W3110 порівняно з буферним розчином фосфату калію (Kpi) як 9 UA 112980 C2 5 10 15 20 25 30 35 40 45 50 55 60 негативного контролю. Фіг. 2 Життєздатність штаму E. coli W3110 в формі кількості cfu, які можуть бути утворені штамом за відсутності рідкого катіоніту і в присутності різних рідких катіонітів через 0 год., 4 год. і 24 год. Фіг. 3 Вплив застосовуваного рідкого катіоніту на токсичність, визначений на підставі зміни кількості живих клітин штаму E. coli W3110 в присутності ALSME 0,2 %, із встановленим за допомогою аміаку DEHPA ("D2EHPNH3 2%") чи суміші DEHPA/LSME (2 %/98 %) ("D/L") у присутності ALSME 0,2 %. Фіг. 4 Вплив різних рідких катіонітів на OTR продукуючого метиловий естер амінолауринової кислоти штаму E. coli. Методика здійснення експерименту відповідає описаній у Прикладі 4. Фіг. 5 Вплив різних рідких катіонітів на вихід метилового естеру амінолауринової кислоти, який продукує штам E. coli відповідної генетичної модифікації. Методика здійснення експерименту відповідає описаній у Прикладі 4. Приклад 1: Дослідження токсичності розчинника LSME, застосовуваного в композиціях із рідкими катіонітами У цьому досліді було встановлено відносно малу токсичність LSME стосовно застосовуваних у біотехнологічних методах мікроорганізмів, які перетворюють LSME на органічний розчинник, який є придатним для використання у відповідному винаходові способі. Перед визначенням CFU пластину LB (10 г/л пептону з казеїну, 5 г/л екстракту дріжджів, 10 г/л NaCl) змащували E. coli BW3110 та інкубували протягом 24 годин. Увечері наступної доби вихідну культуру засівали матеріалом з цієї попередньо змащеної пластини. Ця вихідна культура мала об'єм 50 мл середовища LB і була піддана інкубуванню протягом ночі близько 16 годин. Наступної доби вихідну культуру із OD600 = 0,2 пересівали в 200 мл середовища M9 (Na2HPO4 6,79 г/л; KH2PO4 3,0 г/л; NaCl 0,5 г/л; NH4Cl 1g/L; 1 мл/л розчину мікроелементів, pH 7,4. Розчин мікроелементів: HCl 37 % (= 455,8 г/л) 36,50 г/л; MnCl2·7H2O 1,91 г/л; ZnSO4·7H2O 1,87 г/л; Na-EDTA·2H2O (Titriplex III) 0,84 г/л; H3BO3 0,30 г/л; Na2MoO4·2H2O 0,25 г/л; CaCl2·2H2O 4,70 г/л; FeSO4·7H2O 17,80 г/л; CuCl2·2H2O 0,15 г/л) із 3 % глюкози (м/о) та інкубували протягом близько 20 год. Після інкубування головної культури збирали клітини, центрифугували при 5258 g і 4 °C протягом 10 хвилин, після чого ресуспендували при OD600 = 30 в 10 мл 50 мМ буферного розчину Kpi із pH = 7,4 (або 25 мМ буферного розчину HEPES із pH = 7,4, якщо для визначення CFU застосовували ALSME). Обидва застосовуваних буферних розчини містили 5 % глюкози (м/о). Потім суспензію бактерій перекладали в струшувану колбу і змішували з розчинами відповідних речовин. Після перемішування шляхом струшування колби відбирали піпеткою 100 мкл суспензії і виливали в 900 мкл стерильного сольового розчину. Це відповідало відбору проби в момент t 0. Потім інкубували вихідні розчини при 250 об/хв. і 30 °C. CFU визначали протягом періоду 22 години. Проби відбирали спочатку в моменти часу t0, t3, t6 і t22. Для деяких вихідних розчинів додавали ще один момент відбору проби t1,5 та, крім цього, наносили на пластини додатковий ряд розбавлених розчинів для мінімізації відхилень. OD600 дорівнювало 60. Клітини ресуспендували в 10 мл буферного розчину Kpi, після чого змішували в колбі з 5 мл LSME 98 % (м/м). Одну ступінь розбавлення кожного вихідного розчину наносили на пластини. Кількість CFU/мл протягом 6 годин залишалася незмінною. Через 22 години можна було спостерігати зменшення кількості живих клітин у відсотках, яке становило лише 30,3 %. Приклад 2: Порівняльні досліди для визначення токсичності різних рідких катіонітів порівняно із мікроорганізмами, застосовуваними в біотехнологічних методах Цей приклад підтверджує низьку токсичність нерозгалужених жирних кислот порівняно з іншими рідкими катіонітами, такими як DEHPA, а також розгалуженими і нерозгалуженими насиченими жирними кислотами. Спочатку попередню культуру, що містила 20 мл середовища LB в колбі з дефлектором місткістю 100 мл, засівали кріокультурою відповідного штаму. Культуру культивували протягом ночі при 37 °C зі струшуванням при 200 об./хв. і застосовували наступної доби для засівання головної культури до OD = 0,2. Потім продовжували інкубування головних культур (30 мл середовища LB кожна) в таких самих умовах. При OD від 0,4 до 0,5 головну культуру в кожному випадку покривали рівним об'ємом (30 мл) розчинника, після чого продовжували інкубування. Для визначення кількості cfu (колонієутворюючих одиниць, англ. colony-forming units) в описаних далі дослідах відбирали проби 0,1 мл і розбавляли стерильним розчином NaCl 0,9 %. Відповідні ступені розбавлення наносили на агарові пластини LB. Після інкубування при температурі 34 °C протягом ночі підраховували утворені колонії і визначали cfu. Дослід 1: Порівняння токсичності DE2HPA і насиченої жирної кислоти як рідкого катіоніту 10 UA 112980 C2 5 DEHPA (50 %) та лауринову кислоту (15 %) в кожному випадку розчиняли в LSME і вводили еквімолярно або 25 мол. % ALSME, як рідкий катіоніт вводити в контакт зі штамом E. coli BL21 (DE3) і досліджували вплив цих обох сполук на здатність штаму до утворення колоній, виражену в cfu. У попередніх дослідах було доведено, що метиловий естер лауринової кислоти - який внаслідок відсутності заряду не може діяти як рідкий катіоніт - добре переноситься застосовуваними штамами. Таблиця 1 Дослід Застосований Застосований Кількість cfu через 22 та 24 год. відносно t = 0 год. № штам E. coli рідкий катіоніт 1a E. coli BL21(DE3) 244 % 1b E. coli BL21(DE3) DEHPA 0% 1c E. coli BL21(DE3) лауринова кислота 1,2 % 10 15 Було виявлено, що обидва рідких катіоніти помітно зменшують кількість cfu, але при застосуванні лауринової кислоти на відміну від DEHPA ще залишаються деякі живі клітини, тому насиченій жирній кислоті слід надавати перевагу як рідкому катіоніту. Дослід 2: Порівняння токсичності розгалужених насичених жирних кислот і різних кількостей олеїнової кислоти як рідкого катіоніту При цьому застосовували дві різних концентрації олеїнової кислоти і узгоджували об'єм шляхом додавання відповідної кількості LSME (метилового естеру лауринової кислоти). Таблиця 2 Дослід № Застосований штам E. coli 2a 2b 2c E. coli W3110 2h 35 E. coli W3110 E. coli W3110 2g 30 E. coli BL21(DE3) 2e 2f 25 E. coli BL21(DE3) 2d 20 E. coli BL21(DE3) E. coli BL21(DE3) E. coli W3110 Застосований рідкий катіоніт Ізононанова кислота 2-етилгексанова кислота LSME/25% олеїнова кислота LSME/75% олеїнова кислота Ізононанова кислота 2-етилгексанова кислота LSME/25% олеїнова кислота LSME/75% олеїнова кислота Кількість cfu через 22 та 24 год. відносно t = 0 год. 0 0 11 % 18 % 0 0 29 % 17 % Буловиявлено, що кількість життєздатних клітин при застосуванні ненасиченої жирної кислоти - олеїнової кислоти - разом із LSME відповідно є помітно вищою, ніж при застосуванні розгалужених насичених жирних кислот. Дослід 3: Порівняння токсичності нерозгалужених насичених жирних кислот і ненасичених жирних кислот як рідких катіонітів При цьому порівнювали токсичність різних кількостей ненасиченої жирної кислоти із токсичністю ненасиченої жирної кислоти при їх застосуванні як рідких катіонітів. Внаслідок низької розчинності ненасиченої жирної кислоти - лауринової кислоти - її застосовували в меншій кількості. Об'єми різних катіонітів порівнювали з LSME. Кількість cfu визначали на початку, через 4,5 та 24 години. Як зображено на фіг. 2, додавання насиченої жирної кислоти як рідкого катіоніту навіть у меншій концентрації, ніж концентрація ненасиченої жирної кислоти спричиняє зменшення кількості cfu, на відміну від чого у разі застосування ненасиченої жирної кислоти спостерігають збільшення кількості cfu. В цілому було виявлено зменшення токсичності різних досліджуваних рідких катіонітів у такій послідовності: DEHPA > насичені жирні кислоти > ненасичені жирні кислоти. Приклад 3: Зменшення токсичності органічної сполуки із позитивним зарядом шляхом контактування з рідким катіонітом 11 UA 112980 C2 5 10 15 20 25 30 35 40 45 50 55 60 Результати цього досліду свідчать, що завдяки присутності рідкого катіоніту токсична дія позитивно зарядженої органічної сполуки у водній фазі, яка є ферментаційним бульйоном, може бути зменшена шляхом екстрагування цієї сполуки в органічну фазу. Принципова методика досліду відповідала описаній у Прикладі 1. Оскільки ALSME 0,2 % (м/о), розчинений у водних системах, проявляє бактерицидну дію, цей дослід в комбінації з D2EHPNH3/LSME 2/98 % (м/м) повторно проводили в струшуваній колбі, причому D2EHPNH3 означає насичений амонієм D2EHPA. Застосування рідкого іонообмінника сприяє переходу ALSME в органічну фазу, завдяки чому його концентрація у водній фазі, в якій перебувають також і клітини, зменшується. Для зменшення токсичної дії, зумовленої D2EHPA, застосовують нижчі концентрації 2 % (м/м) D2EHPNH3. Бактерії ресуспендували спочатку в 5 мл (що відповідає половині об'єму буферного розчину). Наступні 5 мл буферного розчину в разі потреби змішували з 0,4 % (м/о) ALSME і потім у разі потреби струшували з 5 мл D2EHPNH3/LSME 2/98 % (м/м) протягом 1 хв. при 3000 об./хв. Цей розчин додавали до поміщеної в струшувану колбу суспензії бактерій і перемішували. Після цього відбирали першу пробу. Розчин мав пінисту консистенцію на початку дослідів, яка, проте, зникла при відборі 2-ї проби в обох дослідах. Скорочення "D/L" застосовували для D2EHPNH3 (насиченого аміаком D2EHPA)/LSME 2/98 % (м/м). Між відбором проб t0 і t1,5 кількість CFU/мл зросла на 34,3 %. За час від відбору проби (t1,5) до відбору останньої проби (t22) кількість CFU/мл зменшилася на 54,9 %. Порівняно з вихідним розчином із D2EHPNH3/LSME 2/98 % (м/м) без додавання ALSME 0,2 % (м/о), кількість здатних до розмноження клітин через 22 години була в 4,5 раза більше і становила 3,4 %, що було не значно нижче, ніж середнє значення для контрольних проб у буферному розчині HEPES (див. фіг. 4). Порівняно із вихідним розчином, який містив ALSME 0,2 % (м/о) в струшуваній колбі, без додавання органічної фази, кількість CFU/мл була у 2800 разів вищою. Було виявлено, що присутність рідкого катіоніту зменшує токсичність позитивно зарядженої сполуки, в даному випадку встановлену на підставі кількості живих cfu. Приклад 4: Порівняльні досліди для визначення токсичності різних рідких катіонітів порівняно з мікроорганізмом, що продукує -амінолауринову кислоту (ALS) і метиловий естер амінолауринової кислоти (ALSME) Біотрансформацію метилового естеру лауринової кислоти на метиловий естер амінолауринової кислоти досліджували у 8-компонентній паралельній системі ферментерів DasGip із різними іонообмінниками. Для ферментації застосовували реактори місткістю 1 літр. Зонди для визначення pH калібрували двоточковим методом із застосуванням титрованих розчинів із pH = 4,0 і pH = 7,0. Реактори заповнювали 300 мл води і протягом 20 хвилин витримували в автоклаві при 121 °C для забезпечення стерильності. Потім зонди pO2 поляризували протягом ночі (принаймні протягом 6 годин). Наступного ранку відбирали воду в асептичних умовах (Clean Bench) і заміняли її середовищем для вирощування культур із високою густиною клітин, яка містила 50 мг/л канаміцину (Kanamycin) і 34 мг/л хлорамфеніколу (Сhloramphenicol). Потім одноточковим методом калібрували зонди для вимірювання pO2 (мішалка: 600 об./хв./подача газу: 10 сл/год. повітря) і очищували лінії подачі розчинів, коригуючих та індукційних засобів за допомогою системи "очищення на місці" (англ. Clean-in-Place). Для цього шланги промивали етанолом концентрацією 70 %, потім 1 M NaOH, після чого стерильною повністю знесоленою водою і насамкінець заповнювали відповідними речовинами. Продукуючий ALS і ALSME штам E. coli BL21 (DE3) T1r pBT10 pACYC:Duet[TAcv] спочатку вирощували з кріокультури в середовищі LB (25 мл в колбі з дефлектором місткістю 100 мл), що містило 50 мл/л канаміцину і 34 мг/л хлорамфеніколу протягом ночі при 37 °C і 200 об./хв. протягом близько 18 год. Потім по 2 мл культури в кожному випадку пересівали у середовище для вирощування культур із високою густиною клітин (глюкоза 15 г/л (30 мл/л окремо витриманого в автоклаві 500 г/л вихідного розчину з 1 % MgSO4·7H2O і 2,2 % NH4Cl), (NH4)2SO4 1,76 г/л, K2HPO4 19,08 г/л, KH2PO4 12,5 г/л, екстракт дріжджів 6,66 г/л, тринатрію цитрат дигідрат 11,2 г, розчин цитрату амонію-заліза 17 мл/л окремо автоклавованого вихідного розчину концентрацією 1 %, розчин мікроелементів 5 мл/л окремо автоклавованого вихідного розчину (HCl (37 %) 36,50 г/л, MnCl2·4H2O 1,91 г/л, ZnSO4·7H2O 1,87 г/л, дигідрат етилeндіамінтетраоцтової кислоти 0,84 г/л, H3BO3 0,30 г/л, Na2MoO4·2H2O 0,25 г/л, CaCl2·2H2O 4,70 г/л, FeSO4·7H2O 17,80 г/л, CuCl2·2H2O 0,15 г/л)) (тричі по 25 мл у колбі з дефлектором місткістю 100 мл) із 50 мг/л канаміцину і 34 мг/л хлорамфеніколу і при температурі 37 °C/200 об./хв. продовжували інкубувати протягом наступних 6 годин. Три культури об'єднували в струшуваній колбі і визначали оптичну густину, що становила 12 UA 112980 C2 7,2. Для внесення культур у реактори з оптичною густиною 0,1 у шприц місткістю 5 мл набирали в кожному випадку 4,2 мл і засівали в реактор за допомогою канюлі через перегородку. Використовували описану далі стандартну програму: Регулятор кількості розчиненого кисню (DO) Задане значення 0% P 0,1 Ti 300 с мін. 0% макс. 100 % Регулятор pH Задане значення 0 мл/год. P 5 Ti 200 с мін. 0 мл/год. макс. 40 мл/год. 5 N (швидкість обертання) Ріст і біотрансформація від до 0% 400 об./хв. 30 % 1500 об./хв. XO2 F (газовий (газова від до від потік) суміш) 0 % 100 % 15 % Ріст і Ріст і біотрансбіотранс6 21% 21% формація формація сл/год. Опис Пікова доза Індукція IPTG Запуск подачі Швидкість подачі 10 15 20 25 30 35 40 до 80 % 72 сл/год. 31 % DO (1/60 год.) 2 год. після початку подачі 50 % DO 3 [мл/год.] Проведений експеримент може бути розділений на дві стадії, тобто вирощування, на якій колонія клітин має досягти певної оптичної густини, і наступної біотрансформації, на якій була індукована експресія гену, необхідного для здійснення біотехнологічного способу одержання ALSME. За допомогою аміаку (12,5 %) з однієї сторони встановили значення pH = 6,8. Під час вирощування і біотрансформації встановили кількість розчиненого в культурі кисню (DO, dissolved oxygen) 30 % шляхом варіювання кількості обертів мішалки і подачі газу. Ферментацію здійснювали методом періодичної ферментації з підживленням (англ. Feedbatch), причому запуск подачі, 5 г/л·год. глюкози (500 г/л глюкози з 1 % MgSO4·7H2O і 2,2 % NH4Cl), ініціювали за допомогою пікової кількості розчиненого кисню. При запуску подачі також знизили температуру з 37 °C до 30 °C. Експресію трансамінази індукували через 2 години після пуску подачі шляхом автоматичного додавання IPTG (1 мM). Індукція гена alk була ініційована шляхом додавання вручну DCPK (0,025 % о/о) через 10 годин після пуску подачі. Перед пуском процесу біотрансформації визначали оптичну густину культурального бульйону. Стадію біотрансформації запускали через 14 годин після пуску подачі. Для цього 150 мл суміші метилового естеру лауринової кислоти і відповідного іонообмінника (10 % м/м) додавали до ферментаційного бульйону в формі однієї порції (Batch). Як іонообмінник застосовували ди(2-етилгексил-)фосфорну кислоту (DEHPA), лауринову кислоту, олеїнову кислоту, пальмітинову кислоту, пальмітолєїнову кислоту, стеаринову кислоту і суміш вільних жирних кислот, одержану шляхом омилення олії з рослини головатень звичайний. Для одержання донора аміногруп для трансамінази одночасно із додаванням органічної фази 10,7 мл розчину аланіну (125 г/л) додавали до ферментаційного бульйону. Для відбору проби 2 мл ферментаційного бульйону відбирали з реактора, частину цієї кількості розбавляли у співвідношенні 1/20 в суміші ацетонHCl (c(HCl) = 0,1 моль/л) та екстрагували. Проби відбирали з усіх 8-ми реакторів через 1,25 години, 3, 5, 20, 22 і 25 годин після пуску стадії біотрансформації. Швидкість перенесення кисню (англ. oxygen transfer rate, OTR) і вуглецю (англ. carbon transfer rate, CTR) під час ферментації визначали шляхом аналізу відведених газів за допомогою систем DasGip. Ферментація була завершена через 22 години після пуску стадії біотрансформації. Кількісну оцінку ALS, ALSME, DDS, DDSME, LS, LSME, HLS, HLSME, OLS і OLSME у ферментаційних пробах здійснювали методами рідинної хроматографії із іонізацією 2 розпиленням/мас-спектрометрії (LC-ESI/MS ) на підставі зовнішнього калібрування для всіх речовин, які визначають при аналізі, та із застосуванням внутрішнього стандарту аміноундеканової кислоти (AUD). При цьому була застосована наведена далі апаратура: Установка для високоефективної рідинної хроматографії (ВЕРХ) 1260 (компанія Agilent; Бьоблінген) із автоматичним пробовідбірником (G1367E), бінарний насос (G1312B) і піч колонки 13 UA 112980 C2 5 10 15 (G1316A) Мас-спектрометр TripelQuad 6410 (компанія Agilent; Бьоблінген) з електроспреєм колонка для ВЕРХ: Kinetex C18, 100 2,1 мм, розмір частинок: 2,6 мкм, розмір пор 100 Å (компанія Phenomenex; Ашаффенбург) Фільтр попереднього очищення: KrudKatcher Ultra HPLC In-Line Filter; глибина фільтрування 0,5 мкм, внутрішній діаметр 0,004 мм (компанія Phenomenex; Ашаффенбург) Підготовку проб здійснювали шляхом введення 1900 мкл розчинника (суміш ацетон/0,1 N HCl у співвідношенні 1:1) і 100 мкл проби піпеткою вводили у реактор місткістю 2 мл. Суміш струшували протягом близько 10 секунд і потім центрифугували при близько 13000 об./хв. протягом 5 хвилин. Прозору рідку фракцію відбирали піпеткою і піддавали аналізу після відповідного розбавлення розчинником (80 % (о/о) ACN, 20 % бідистильована H2O (о/о), + 0,1 % мурашиної кислоти). До кожних 900 мкл проби додавали піпеткою 100 мкл ISTD (10 мкл при об'ємі проби 90 мкл). Розділення методом високоефективної рідинної хроматографії (ВЕРХ) здійснювали в описаній вище колонці та фільтрі попереднього очищення. Об'єм інжекції становив 0,7 мкл, температура колонки 50 °C, швидкість потоку 0,6 мл/хв. Мобільна фаза складалася з елюенту A (водний розчин мурашиної кислоти конц. 0,1 % (о/о)) та елюенту B (ацетонітрил із 0,1 % (о/о) мурашиної кислоти). Використовували наведений далі профіль градієнта: Час [хв.] 0 0.3 0.4 2.5 2.6 5.5 5.6 9 Елюент A [%] 77 77 40 40 2 2 77 77 Елюент B [%] 23 23 60 60 98 98 23 23 20 25 2 Аналіз шляхом іонізації електроспреєм/мас-спектрометрії (ESI-MS ) здійснювали в позитивному режимі із такими параметрами електроспрею: температура газу 280 °C газовий потік 11 л/хв. тиск розпилювача 50 фунтів на кв. дюйм капілярне напруження 4000 В Виявлення і кількісну оцінку окремих сполук здійснювали при наведених далі параметрах, причому в кожному випадку один продукт-іон використовували як специфікатор (Qualifier) і один - як квантифікатор (Quantifier): 30 Речовина, яку визначають при аналізі Іон-попередник [m/z] Іонпродукт [m/z] Тривалість перебування [мс] DDSME DDSME HLSME HLSME DDS DDS ALSME ALSME OLSME OLSME HLS HLS OLS OLS 245,2 245,2 231,3 231,3 231,2 231,2 230,3 230,3 229,2 229,2 217,2 217,2 215,2 215,2 167,1 149,1 181,2 163,2 213,2 149,1 198,1 163,2 197,2 161,1 181,2 163,1 161,2 95,2 25 50 15 25 50 25 25 15 50 25 35 20 25 60 Результати: 14 Енергія зіткнення [eВ] 6 8 2 5 0 9 10 10 0 5 0 4 0 13 UA 112980 C2 5 10 15 20 25 30 35 40 45 50 55 Якщо як катіоніт застосовують DEHPA згідно з рівнем техніки, безпосередньо після додавання сполуки до культури відбувається різке зменшення швидкості перенесення кисню (OTR). Крива швидко спадає до нуля, тобто культура вже не містить метаболічно активних клітин. Отже, DEHPA справляє на клітини високотоксичну дію. Якщо замість DEHPA як рідкий катіоніт застосовують лауринову кислоту, в цьому випадку, хоча і відбувається також зменшення швидкості перенесення кисню (OTR), проте, воно не є настільки значним, і протягом наступних 22 годин клітини відновлюються і проявляють зростаючу метаболічну активність. Таким чином, лауринова кислота є помітно менш токсичною, ніж DEHPA. Ще кращі результати можна спостерігати при застосуванні насичених жирних кислот, які містять довші вуглецеві ланцюги. Якщо застосовують пальмітинову і стеаринову кислоти, падіння кривої OTR є помітно менш крутим, ніж у разі застосуванні лауринової кислоти або навіть DEHPA. Крім цього, можна зробити висновок, що ці жирні кислоти справляють явно менш токсичну дію. Застосування ненасичених жирних кислот, таких як пальмітолеїнова кислота, омилена олія з рослини головатень звичайний (що містить переважно лінолеву кислоту) і олеїнової кислоти неочікувано дозволяє одержати ще помітно кращі результати. Ці жирні кислоти неочікувано проявляють ще меншу токсичність, аніж насичені жирні кислоти. Цитована література: 1. J. Sangster, Octanol-Water Partition Coefficients: Fundamentals and Physical Chemistry, Wiley Series in Solution Chemistry, том 2, John Wiley & Sons, Чичестер, 1997 р. 2. Asano, Y., Fukuta, y., Yoshida, Y., and Komeda, H. (2008): The Screening, Characterisation, and Use of w-Laurolactam Hydrolase: A New Enzymatic Synthesis of 12-Aminolauric Acid, Biosc. Biotechn. Biochem., 72 (8), стор. 2141-2150. 3. DE10200710060705 (2007): Рекомбінантні клітини, що продукують -амінокислоти або їх лактами (-Aminocarbonsäuren або ihre Lactame, herstellende, rekombinante Zellen). 3. F. M. Ausubel (1995), Current Protocols in Molecular Biology. John Wiley & Sons, Inc. 4. M. Lesk (2008), Introduction to Bioinformatics, 3-е видання. ФОРМУЛА ВИНАХОДУ 1. Спосіб видалення органічної сполуки з водного розчину, який включає стадії a) одержання органічної сполуки, що містить водний розчин, і гідрофобного органічного розчину, що містить рідкий катіоніт, причому рідкий катіоніт є гідрофобним, b) контактування водного розчину і органічного розчину, і c) відокремлення органічного розчину від водного розчину, причому органічною сполукою є сполука формули (І) + + 1 NH3 -A-COO або NH3 -A-COOR (I), 1 причому R означає водень, метил, етил, а А означає незаміщену, нерозгалужену алкіленову групу, що містить принаймні три, переважно принаймні вісім, атомів вуглецю, і причому рідким катіонітом є жирна кислота. 2. Спосіб за п. 1, причому температура на стадії b) становить від 28 до 70, переважно від 30 до 37 °C. 3. Спосіб за п. 1 або п. 2, причому значення рН на стадії b) становить від 6 до 8, переважно від 6,2 до 7,2. 4. Спосіб за будь-яким із пп. 1-3, причому кількісне співвідношення між рідким катіонітом і органічною сполукою становить принаймні 1. 5. Спосіб за будь-яким із пп. 1-4, причому об'ємне співвідношення між органічним і водним розчинами становить від 1:10 до 10:1. 6. Спосіб за будь-яким із пп. 1-5, причому як рідкий катіоніт беруть жирну кислоту, що містить понад 12 атомів вуглецю. 7. Спосіб за пунктом 6, причому як рідкий катіоніт беруть жирну кислоту, що містить від 14 до 22, зокрема від 16 до 18 атомів вуглецю. 8. Спосіб за будь-яким із пп. 1-5, причому як рідкий катіоніт беруть ненасичену жирну кислоту. 9. Спосіб за п. 8, причому як рідкий катіоніт беруть олеїнову або ерукову кислоту. 10. Спосіб за будь-яким із пп. 1-9, причому водний розчин додатково містить каталітично активний біологічний агент, який є клітиною. 11. Спосіб за п. 10, причому як біологічний агент беруть бактеріальну клітину. 15 UA 112980 C2 5 10 15 20 25 30 12. Спосіб за п. 10, причому як клітину застосовують рекомбінантну алканмонооксигеназу або рекомбінантну трансаміназу. 13. Спосіб за п. 10, причому клітина містить принаймні один фермент, вибраний із групи, що включає алкогольдегідрогеназу, аланіндегідрогеназу і генний продукт AlkL або його варіанти. 14. Спосіб за п. 10, причому присутність органічної сполуки формули (І) негативно впливає на каталітичну активність, переважно внаслідок того, що як органічну сполуку формули (І) застосовують токсичну для клітини сполуку. 15. Спосіб за будь-яким із пп. 1-14, причому органічний розчин містить додатково принаймні один органічний розчинник. 16. Спосіб за п. 15, причому як органічний розчинник беруть жирну кислоту та/або естер жирної кислоти. 17. Спосіб за п. 15, причому органічний розчин містить як рідкий катіоніт від 20 до 80 об. % олеїнової кислоти, а як розчинник - метиловий естер лауринової кислоти, і як органічну сполуку беруть метиловий естер 12-амінолауринової кислоти. 18. Спосіб за п. 17, причому водний розчин містить бактеріальну клітину, вміщуючу рекомбінантну алканмонооксигеназу або рекомбінантну трансаміназу. 19. Спосіб за п. 17, причому водний розчин містить бактеріальну клітину, що містить принаймні один фермент, вибраний із групи, що включає алкогольдегідрогеназу, аланіндегідрогеназу і генний продукт AlkL або його варіанти. 20. Реакційна суміш, що містить водний розчин і гідрофобний органічний розчин, причому гідрофобний органічний розчин містить жирну кислоту як рідкий катіоніт, і причому водний розчин є сполукою формули (І) + + 1 NH3 -A-COO або NH3 -A-COOR (I), 1 причому R означає водень, метил, етил, а А означає незаміщену, нерозгалужену алкіленову групу, що містить принаймні три атоми вуглецю. 21. Реакційна суміш за п. 20, причому А означає незаміщену, нерозгалужену алкіленову групу, що містить принаймні вісім атомів вуглецю. 22. Реакційна суміш за п. 20 або п. 21, причому жирна кислота містить понад 12 атомів вуглецю. 23. Реакційна суміш за п. 20 або 21, причому жирна кислота є ненасиченою жирною кислотою. 24. Реакційна суміш за будь-яким із пп. 20-23, причому водний розчин додатково містить клітину, що містить рекомбінантну алканмонооксигеназу або рекомбінантну трансаміназу. 25. Реакційна суміш за будь-яким із пп. 20-23, причому водний розчин додатково містить клітину, що містить принаймні один фермент, який вибраний із групи, що включає алкогольдегідрогеназу, аланіндегідрогеназу і генний продукт AlkL або його варіанти. 16 UA 112980 C2 17 UA 112980 C2 Комп’ютерна верстка А. Крулевський Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 18
ДивитисяДодаткова інформація
Назва патенту англійськоюLiquid cation exchanger
Автори англійськоюErhardt, Frank, Haas, Thomas, Roos, Martin, Devicoli, Daniel, Potter, Markus, Schubert, Anja, Pfeffer, Jan Christoph, Tacke, Thomas, Hager, Harald, Pfennig, Andreas, Przybylski-Freund, Marie-Dominique
Автори російськоюЭрхардт Франк, Хаас Томас, Роос Мартин, Демиколи Даниель, Пёттер Маркус, Шуберт Аня, Пфеффер Ян Кристоф, Такке Томас, Хегер Харальд, Пфенниг Андреас, Пшибильськи-Фройнд Мари-Доминик
МПК / Мітки
МПК: C07C 227/40, B01J 39/16, C13B 20/14, C02F 1/42, B01D 11/04
Код посилання
<a href="https://ua.patents.su/20-112980-ridki-kationiti.html" target="_blank" rel="follow" title="База патентів України">Рідкі катіоніти</a>