Застосування бензоконденсованих гетероциклічних сульфамідних похідних як нейропротективних агентів
Формула / Реферат
1. Спосіб нейропротекції, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки формули (І):
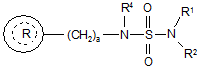 , (I)
, (I)
де
кожний R1 і R2, незалежно, вибраний з групи, що включає водень і нижчий алкіл;
R4 вибраний з групи, що включає водень і нижчий алкіл;
а означає ціле число від 1 до 2;
![]() являє собою
являє собою
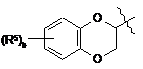 ,
,
де b є цілим числом від 0 до 4;
кожний R5 незалежно вибраний з групи, що включає галоген і нижчий алкіл;
або її фармацевтично прийнятної солі.
2. Спосіб за п. 1, де у сполуці формули І
кожний R1 і R2, незалежно, вибраний з групи, що включає водень і нижчий алкіл;
R4 вибраний з групи, що включає водень і нижчий алкіл;
а означає ціле число від 1 до 2;
![]() являє собою
являє собою
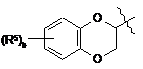 ,
,
де b є цілим числом від 0 до 2;
кожний R5 незалежно вибраний з групи, що включає галоген і нижчий алкіл;
або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі.
3. Спосіб за п. 1, де у сполуці формули І
кожний R1 і R2, незалежно, вибраний з групи, що включає водень і нижчий алкіл;
R4 вибраний з групи, що включає водень і метил;
а означає ціле число від 1 до 2;
![]() вибраний з групи, що включає
вибраний з групи, що включає
2-(2,3-дигідробензо[1,4]діоксиніл),
2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(6-фтор-2,3-дигідробензо[1,4]діоксиніл),
2-(5-фтор-2,3-дигідробензо[1,4] діоксиніл),
2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(7-метил-2,3-дигідробензо[1,4]діоксиніл),
2-(5-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(6-бром-2,3-дигідробензо[1,4]діоксиніл),
2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл) і
2-(8-хлор-2,3-дигідробензо[1,4]діоксиніл),
або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі.
4. Спосіб за п. 3, де у сполуці формули І
кожний R1 і R2, незалежно, вибраний з групи, що включає водень і метил;
R4 вибраний з групи, що включає водень і метил;
а означає ціле число від 1 до 2;
![]() вибраний з групи, що включає
вибраний з групи, що включає
2-(2,3-дигідробензо[1,4]діоксиніл),
2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(7-метил-2,3-дигідробензо[1,4]діоксиніл),
2-(6-бром-2,3-дигідробензо[1,4]діоксиніл) і
2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл),
або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі.
5. Спосіб за п. 1, де сполука формули (І) вибрана з групи, що включає (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфамід або його фармацевтично прийнятні солі.
6. Спосіб нейропротекції, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки, вибраної з групи, що включає (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфамід;
або її фармацевтично прийнятної солі.
7. Спосіб лікування гострого нейродегенеративного захворювання, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки формули (І):
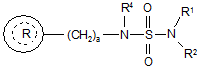 , (I)
, (I)
де
кожний R1 і R2, незалежно, вибраний з групи, що включає водень і нижчий алкіл;
R4 вибраний з групи, що включає водень і нижчий алкіл;
а означає ціле число від 1 до 2;
![]() являє собою
являє собою
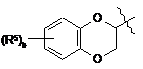 ,
,
де b є цілим числом від 0 до 4;
кожний R5, незалежно, вибраний з групи, що включає галоген і нижчий алкіл;
або її фармацевтично прийнятної солі.
8. Спосіб за п. 7, де у сполуці формули І
кожний R1 і R2, незалежно, вибраний з групи, що включає водень і нижчий алкіл;
R4 вибраний з групи, що включає водень і нижчий алкіл;
а означає ціле число від 1 до 2;
![]() являє собою
являє собою
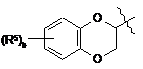 ,
,
де b є цілим числом від 0 до 4;
кожний R5, незалежно, вибраний з групи, що включає галоген і нижчий алкіл;
або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі.
9. Спосіб за п. 8, де у сполуці формули І
кожний R1 і R2, незалежно, вибраний з групи, що включає водень і нижчий алкіл;
R4 вибраний з групи, що включає водень і метил;
а означає ціле число від 1 до 2;
![]() вибраний з групи, що включає
вибраний з групи, що включає
2-(2,3-дигідробензо[1,4]діоксиніл),
2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(6-фтор-2,3-дигідробензо[1,4]діоксиніл),
2-(5-фтор-2,3-дигідробензо[1,4]діоксиніл),
2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(7-метил-2,3-дигідробензо[1,4]діоксиніл),
2-(5-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(6-бром-2,3-дигідробензо[1,4]діоксиніл),
2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл) і
2-(8-хлор-2,3-дигідробензо[1,4]діоксиніл),
або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі.
10. Спосіб за п. 9, де у сполуці формули І
кожний R1 і R2, незалежно, вибраний з групи, що включає водень і метил;
R4 вибраний з групи, що включає водень і метил;
а означає ціле число від 1 до 2;
![]() вибраний з групи, що включає
вибраний з групи, що включає
2-(2,3-дигідробензо[1,4]діоксиніл),
2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(7-метил-2,3-дигідробензо[1,4]діоксиніл),
2-(6-бром-2,3-дигідробензо[1,4]діоксиніл) і
2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл),
або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі.
11. Спосіб за п. 7, де сполука формули (І) вибрана з групи, що включає (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфамід або його фармацевтично прийнятні солі.
12. Спосіб лікування гострого нейродегенеративного захворювання, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки, вибраної з групи, що включає (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфамід;
або її фармацевтично прийнятної солі.
13. Спосіб лікування хронічного нейродегенеративного захворювання, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки формули (І):
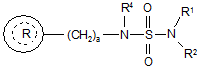 , (I)
, (I)
де
кожний R1 і R2, незалежно, вибраний з групи, що включає водень і нижчий алкіл;
R4 вибраний з групи, що включає водень і нижчий алкіл;
а означає ціле число від 1 до 2;
![]() являє собою
являє собою
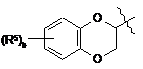 ,
,
де b є цілим числом від 0 до 4;
кожний R5, незалежно, вибраний з групи, що включає галоген і нижчий алкіл;
або її фармацевтично прийнятної солі.
14. Спосіб за п. 13, де у сполуці формули І
кожний R1 і R2, незалежно, вибраний з групи, що включає водень і нижчий алкіл;
R4 вибраний з групи, що включає водень і нижчий алкіл;
а означає ціле число від 1 до 2;
![]() являє собою
являє собою
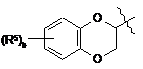 ,
,
де b є цілим числом від 0 до 2;
кожний R5, незалежно, вибраний з групи, що включає галоген і нижчий алкіл;
або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі.
15. Спосіб за п. 13, де у сполуці формули І
кожний R1 і R2, незалежно, вибраний з групи, що включає водень і нижчий алкіл;
R4 вибраний з групи, що включає водень і метил;
а означає ціле число від 1 до 2;
![]() вибраний з групи, що включає
вибраний з групи, що включає
2-(2,3-дигідробензо[1,4]діоксиніл),
2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(6-фтор-2,3-дигідробензо[1,4]діоксиніл),
2-(5-фтор-2,3-дигідробензо[1,4]діоксиніл),
2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(7-метил-2,3-дигідробензо[1,4]діоксиніл),
2-(5-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(6-бром-2,3-дигідробензо[1,4]діоксиніл),
2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл) і
2-(8-хлор-2,3-дигідробензо[1,4]діоксиніл),
або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі.
16. Спосіб за п. 15, де у сполуці формули І
кожний R1 і R2, незалежно, вибраний з групи, що включає водень і метил;
R4 вибраний з групи, що включає водень і метил;
а означає ціле число від 1 до 2;
![]() вибраний з групи, що включає
вибраний з групи, що включає
2-(2,3-дигідробензо[1,4]діоксиніл),
2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(7-метил-2,3-дигідробензо[1,4]діоксиніл),
2-(6-бром-2,3-дигідробензо[1,4]діоксиніл) і
2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл),
або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі.
17. Спосіб за п. 13, де сполука формули (І) вибрана з групи, що включає (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфамід або його фармацевтично прийнятні солі.
18. Спосіб лікування хронічного нейродегенеративного захворювання, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки, вибраної з групи, що включає (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфамід;
або її фармацевтично прийнятної солі.
19. Спосіб запобігання загибелі або пошкодженню нейрона в результаті травми або пошкодження мозку, голови або спинного мозку, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки формули (І):
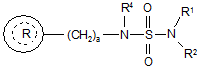 , (I)
, (I)
де
кожний R1 і R2, незалежно, вибраний з групи, що включає водень і нижчий алкіл;
R4 вибраний з групи, що включає водень і нижчий алкіл;
а означає ціле число від 1 до 2;
![]() являє собою
являє собою
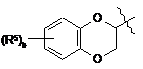 ,
,
де b є цілим числом від 0 до 4;
кожний R5, незалежно, вибраний з групи, що включає галоген і нижчий алкіл;
або її фармацевтично прийнятної солі.
20. Спосіб за п. 19, де у сполуці формули І
кожний R1 і R2, незалежно, вибраний з групи, що включає водень і нижчий алкіл;
R4 вибраний з групи, що включає водень і нижчий алкіл;
а означає ціле число від 1 до 2;
![]() являє собою
являє собою
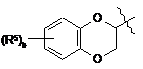 ,
,
де b є цілим числом від 0 до 2;
кожний R5, незалежно, вибраний з групи, що включає галоген і нижчий алкіл;
або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі.
21. Спосіб за п. 20, де у сполуці формули І
кожний R1 і R2, незалежно, вибраний з групи, що включає водень і нижчий алкіл;
R4 вибраний з групи, що включає водень і метил;
а означає ціле число від 1 до 2;
![]() вибраний з групи, що включає
вибраний з групи, що включає
2-(2,3-дигідробензо[1,4]діоксиніл),
2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(6-фтор-2,3-дигідробензо[1,4]діоксиніл),
2-(5-фтор-2,3-дигідробензо[1,4]діоксиніл),
2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(7-метил-2,3-дигідробензо[1,4]діоксиніл),
2-(5-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(6-бром-2,3-дигідробензо[1,4]діоксиніл),
2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл) і
2-(8-хлор-2,3-дигідробензо[1,4]діоксиніл),
або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі.
22. Спосіб за п. 19, де у сполуці формули І
кожний R1 і R2, незалежно, вибраний з групи, що включає водень і метил;
R4 вибраний з групи, що включає водень і метил;
а означає ціле число від 1 до 2;
![]() вибраний з групи, що включає
вибраний з групи, що включає
2-(2,3-дигідробензо[1,4]діоксиніл),
2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл),
2-(7-метил-2,3-дигідробензо[1,4]діоксиніл),
2-(6-бром-2,3-дигідробензо[1,4]діоксиніл) і
2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл),
або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі.
23. Спосіб за п. 22, де сполука формули (І) вибрана з групи, що включає (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфамід або його фармацевтично прийнятні солі.
24. Спосіб запобігання загибелі або пошкодженню нейрона в результаті травми або пошкодження мозку, голови або спинного мозку, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки, вибраної з групи, що включає (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфамід;
або її фармацевтично прийнятної солі.
25. Спосіб запобігання загибелі або пошкодженню нейрона в результаті окислювального стресу, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки формули:
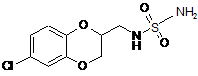
або її фармацевтично прийнятної солі.
26. Спосіб лікування гострого нейродегенеративного захворювання, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки формули:
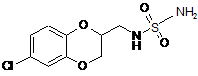
або її фармацевтично прийнятної солі.
27. Спосіб лікування хронічного нейродегенеративного захворювання, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки формули:
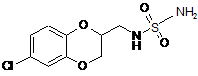
або її фармацевтично прийнятної солі.
28. Спосіб запобігання загибелі або пошкодженню нейрона в результаті травми або пошкодження мозку, голови або спинного мозку, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки формули:
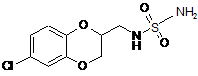
або її фармацевтично прийнятної солі.
Текст
1. Спосіб нейропротекції, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки формули (І): 2 3 96747 3. Спосіб за п. 1, де у сполуці формули І 1 2 кожний R і R , незалежно, вибраний з групи, що включає водень і нижчий алкіл; 4 R вибраний з групи, що включає водень і метил; а означає ціле число від 1 до 2; R вибраний з групи, що включає 2-(2,3-дигідробензо[1,4]діоксиніл), 2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(6-фтор-2,3-дигідробензо[1,4]діоксиніл), 2-(5-фтор-2,3-дигідробензо[1,4] діоксиніл), 2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3-дигідробензо[1,4]діоксиніл), 2-(5-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(6-бром-2,3-дигідробензо[1,4]діоксиніл), 2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл) і 2-(8-хлор-2,3-дигідробензо[1,4]діоксиніл), або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі. 4. Спосіб за п. 3, де у сполуці формули І 1 2 кожний R і R , незалежно, вибраний з групи, що включає водень і метил; 4 R вибраний з групи, що включає водень і метил; а означає ціле число від 1 до 2; R вибраний з групи, що включає 2-(2,3-дигідробензо[1,4]діоксиніл), 2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3-дигідробензо[1,4]діоксиніл), 2-(6-бром-2,3-дигідробензо[1,4]діоксиніл) і 2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл), або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі. 5. Спосіб за п. 1, де сполука формули (І) вибрана з групи, що включає (2S)-(-)-N-(6-хлор-2,3дигідробензо[1,4]діоксин-2-ілметил)сульфамід або його фармацевтично прийнятні солі. 6. Спосіб нейропротекції, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки, вибраної з групи, що включає (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2ілметил)сульфамід; або її фармацевтично прийнятної солі. 7. Спосіб лікування гострого нейродегенеративного захворювання, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки формули (І): R4 O R (CH2)a N S O R1 N R2 , (I) де 1 2 кожний R і R , незалежно, вибраний з групи, що включає водень і нижчий алкіл; 4 R вибраний з групи, що включає водень і нижчий алкіл; а означає ціле число від 1 до 2; R являє собою 4 O (R5) b O , де b є цілим числом від 0 до 4; 5 кожний R , незалежно, вибраний з групи, що включає галоген і нижчий алкіл; або її фармацевтично прийнятної солі. 8. Спосіб за п. 7, де у сполуці формули І 1 2 кожний R і R , незалежно, вибраний з групи, що включає водень і нижчий алкіл; 4 R вибраний з групи, що включає водень і нижчий алкіл; а означає ціле число від 1 до 2; R являє собою O (R5) b O , де b є цілим числом від 0 до 4; 5 кожний R , незалежно, вибраний з групи, що включає галоген і нижчий алкіл; або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі. 9. Спосіб за п. 8, де у сполуці формули І 1 2 кожний R і R , незалежно, вибраний з групи, що включає водень і нижчий алкіл; 4 R вибраний з групи, що включає водень і метил; а означає ціле число від 1 до 2; R вибраний з групи, що включає 2-(2,3-дигідробензо[1,4]діоксиніл), 2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(6-фтор-2,3-дигідробензо[1,4]діоксиніл), 2-(5-фтор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3-дигідробензо[1,4]діоксиніл), 2-(5-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(6-бром-2,3-дигідробензо[1,4]діоксиніл), 2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл) і 2-(8-хлор-2,3-дигідробензо[1,4]діоксиніл), або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі. 10. Спосіб за п. 9, де у сполуці формули І 1 2 кожний R і R , незалежно, вибраний з групи, що включає водень і метил; 4 R вибраний з групи, що включає водень і метил; а означає ціле число від 1 до 2; R вибраний з групи, що включає 2-(2,3-дигідробензо[1,4]діоксиніл), 2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3-дигідробензо[1,4]діоксиніл), 2-(6-бром-2,3-дигідробензо[1,4]діоксиніл) і 2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл), або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі. 11. Спосіб за п. 7, де сполука формули (І) вибрана з групи, що включає (2S)-(-)-N-(6-хлор-2,3 5 96747 дигідробензо[1,4]діоксин-2-ілметил)сульфамід або його фармацевтично прийнятні солі. 12. Спосіб лікування гострого нейродегенеративного захворювання, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки, вибраної з групи, що включає (2S)-()-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2ілметил)сульфамід; або її фармацевтично прийнятної солі. 13. Спосіб лікування хронічного нейродегенеративного захворювання, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки формули (І): R4 O R (CH2)a N S R1 N R2 O , (I) де 1 2 кожний R і R , незалежно, вибраний з групи, що включає водень і нижчий алкіл; 4 R вибраний з групи, що включає водень і нижчий алкіл; а означає ціле число від 1 до 2; R являє собою O (R5) b O , де b є цілим числом від 0 до 4; 5 кожний R , незалежно, вибраний з групи, що включає галоген і нижчий алкіл; або її фармацевтично прийнятної солі. 14. Спосіб за п. 13, де у сполуці формули І 1 2 кожний R і R , незалежно, вибраний з групи, що включає водень і нижчий алкіл; 4 R вибраний з групи, що включає водень і нижчий алкіл; а означає ціле число від 1 до 2; 6 2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3-дигідробензо[1,4]діоксиніл), 2-(5-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(6-бром-2,3-дигідробензо[1,4]діоксиніл), 2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл) і 2-(8-хлор-2,3-дигідробензо[1,4]діоксиніл), або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі. 16. Спосіб за п. 15, де у сполуці формули І 1 2 кожний R і R , незалежно, вибраний з групи, що включає водень і метил; 4 R вибраний з групи, що включає водень і метил; а означає ціле число від 1 до 2; R вибраний з групи, що включає 2-(2,3-дигідробензо[1,4]діоксиніл), 2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3-дигідробензо[1,4]діоксиніл), 2-(6-бром-2,3-дигідробензо[1,4]діоксиніл) і 2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл), або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі. 17. Спосіб за п. 13, де сполука формули (І) вибрана з групи, що включає (2S)-(-)-N-(6-хлор-2,3дигідробензо[1,4]діоксин-2-ілметил)сульфамід або його фармацевтично прийнятні солі. 18. Спосіб лікування хронічного нейродегенеративного захворювання, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки, вибраної з групи, що включає (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2ілметил)сульфамід; або її фармацевтично прийнятної солі. 19. Спосіб запобігання загибелі або пошкодженню нейрона в результаті травми або пошкодження мозку, голови або спинного мозку, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки формули (І): R4 O R R являє собою O (R5)b O , де b є цілим числом від 0 до 2; 5 кожний R , незалежно, вибраний з групи, що включає галоген і нижчий алкіл; або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі. 15. Спосіб за п. 13, де у сполуці формули І 1 2 кожний R і R , незалежно, вибраний з групи, що включає водень і нижчий алкіл; 4 R вибраний з групи, що включає водень і метил; а означає ціле число від 1 до 2; R вибраний з групи, що включає 2-(2,3-дигідробензо[1,4]діоксиніл), 2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(6-фтор-2,3-дигідробензо[1,4]діоксиніл), 2-(5-фтор-2,3-дигідробензо[1,4]діоксиніл), (CH2)a N S O R1 N R2 , (I) де 1 2 кожний R і R , незалежно, вибраний з групи, що включає водень і нижчий алкіл; 4 R вибраний з групи, що включає водень і нижчий алкіл; а означає ціле число від 1 до 2; R являє собою O (R5)b O , де b є цілим числом від 0 до 4; 5 кожний R , незалежно, вибраний з групи, що включає галоген і нижчий алкіл; або її фармацевтично прийнятної солі. 20. Спосіб за п. 19, де у сполуці формули І 1 2 кожний R і R , незалежно, вибраний з групи, що включає водень і нижчий алкіл; 7 4 R вибраний з групи, що включає водень і нижчий алкіл; а означає ціле число від 1 до 2; R являє собою O (R5)b O , де b є цілим числом від 0 до 2; 5 кожний R , незалежно, вибраний з групи, що включає галоген і нижчий алкіл; або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі. 21. Спосіб за п. 20, де у сполуці формули І 1 2 кожний R і R , незалежно, вибраний з групи, що включає водень і нижчий алкіл; 4 R вибраний з групи, що включає водень і метил; а означає ціле число від 1 до 2; R вибраний з групи, що включає 2-(2,3-дигідробензо[1,4]діоксиніл), 2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(6-фтор-2,3-дигідробензо[1,4]діоксиніл), 2-(5-фтор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3-дигідробензо[1,4]діоксиніл), 2-(5-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(6-бром-2,3-дигідробензо[1,4]діоксиніл), 2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл) і 2-(8-хлор-2,3-дигідробензо[1,4]діоксиніл), або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі. 22. Спосіб за п. 19, де у сполуці формули І 1 2 кожний R і R , незалежно, вибраний з групи, що включає водень і метил; 4 R вибраний з групи, що включає водень і метил; а означає ціле число від 1 до 2; R вибраний з групи, що включає 2-(2,3-дигідробензо[1,4]діоксиніл), 2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3-дигідробензо[1,4]діоксиніл), 2-(6-бром-2,3-дигідробензо[1,4]діоксиніл) і 2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл), або цю сполуку формули І вводять у вигляді фармацевтично прийнятної солі. 96747 8 23. Спосіб за п. 22, де сполука формули (І) вибрана з групи, що включає (2S)-(-)-N-(6-хлор-2,3дигідробензо[1,4]діоксин-2-ілметил)сульфамід або його фармацевтично прийнятні солі. 24. Спосіб запобігання загибелі або пошкодженню нейрона в результаті травми або пошкодження мозку, голови або спинного мозку, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки, вибраної з групи, що включає (2S)-(-)-N-(6-хлор-2,3дигідробензо[1,4]діоксин-2-ілметил)сульфамід; або її фармацевтично прийнятної солі. 25. Спосіб запобігання загибелі або пошкодженню нейрона в результаті окислювального стресу, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки формули: O O Cl NH2 S N H O O або її фармацевтично прийнятної солі. 26. Спосіб лікування гострого нейродегенеративного захворювання, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки формули: O O Cl NH2 S N H O O або її фармацевтично прийнятної солі. 27. Спосіб лікування хронічного нейродегенеративного захворювання, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки формули: O O Cl N H NH2 S O O або її фармацевтично прийнятної солі. 28. Спосіб запобігання загибелі або пошкодженню нейрона в результаті травми або пошкодження мозку, голови або спинного мозку, при якому вводять потребуючому цього суб'єкту терапевтично ефективну кількість сполуки формули: O O Cl N H NH2 S O O або її фармацевтично прийнятної солі. Дана заявка заявляє про пріоритет Попередньої Заявки США 60/751494, поданої 19 грудня 2005 року, яка включена у даний опис за допомогою посилання у повному об'ємі. Даний винахід направлений на застосування бензоконденсованих гетероциклічних сульфамідних похідних як нейропротективних агентів. Даний винахід також направлений на застосування бен зоконденсованих гетероциклічних сульфамідних похідних у терапії гострих і/або хронічних нейродегенеративних захворювань, більш конкретно у терапії гострих або хронічних нейродегенеративних захворювань, що характеризуються пошкодженням або загибеллю нейрона. Нейродегенеративні захворювання уражують множину людей, як у США, так і за їх межами. На 9 приклад, багато людей страждає від нейродегенеративних захворювань. Вказані захворювання включають ряд тяжких ослаблюючих захворювань, таких як хвороба Паркінсона, бічний аміотрофічний склероз (БАС, "хвороба Лу Геріга"), розсіяний склероз, хвороба Хантінгтона, хвороба Альцгеймера, діабетична ретинопатія, мультиінфарктна деменція, дегенерація жовтої плями і т.п. Збільшення тривалості життя людей привело до збільшення частоти випадків нейродегенеративних захворювань. Відносно висока частота виникнення вказаних захворювань (у межах 2-15% населення старше 70 років) викликає істотні медичні, соціальні і фінансові ускладнення у пацієнтів, осіб, які доглядають їх, і також у суспільства загалом. Після виникнення, вказані захворювання можуть привести дуже швидко до смерті, або вони можуть повільно прогресувати протягом багатьох років, часто приводячи до потреби пацієнта у спеціалізованому догляді в умовах стаціонару. У міру старіння населення частота, з якою у пацієнтів діагностують нейродегенеративні захворювання, особливо такі, які зачіпають розумові здібності, такі як хвороба Альцгеймера, швидко зростає. Число людей з хворобою Альцгеймера росте по експоненті, і як оцінюють, сьогодні у всьому світі число хворих даним захворюванням може складати не менше 24 мільйонів людей. Хвороба Альцгеймера (ХА) викликана дегенеративним процесом, який характеризується прогресуючою втратою клітин базальних відділів переднього мозку, кори головного мозку та інших областей мозку. Особливо зачіпаються нейрони, що передають ацетилхолін, і їх цільові нерви. Присутні старечі бляшки і нейрофібрилярні клубки. Хвороба Піка має клінічну картину, подібну до хвороби Альцгеймера, але трохи більш повільний перебіг і обмежену атрофію, головним чином зачіпаючи лобові і скроневі частки. Одна з тваринних моделей хвороби Альцгеймера та інших деменцій показує спадкову тенденцію до формування вказаних бляшок. Вважають, що якщо препарат викликає ефект у моделі, то він також може застосовуватися щонайменше при деяких формах хвороб Альцгеймера і Піка. У наш час існують паліативні терапії, які тимчасово полегшують прояв захворювання, але при цьому немає яких-небудь засобів відновлення функцій пацієнтів з хворобою Альцгеймера. Хвороба Паркінсона (ХП) є захворюванням середнього або літнього віку, з дуже повільним розвитком і тривалим проходженням. HARRISON'S PRINCIPLES OF INTERNAL MEDICINE, Vol. 2, 23d ed., Ed by Isselbacher, Braunwald, Wilson, Martin, Fauci and Kasper, McGraw-Hill Inc., New York City, 1994, стор. 2275. Зміни, що найбільш регулярно спостерігаються у пацієнтів з хворобою Паркінсона, були присутніми в агрегатах меланінвмісних нервових клітин у стовбурі мозку (чорна речовина, блакитна пляма), де у різній мірі спостерігається втрата нервових клітин з подальшим гліозом (найбільш явним у чорній речовині) нарівні з характерними еозинофільними інтрацитоплазматичними включеннями. У своїй повністю розвиненій формі ХП легко виявляється у пацієнтів, при цьому осно 96747 10 вними симптомами є нахилена поза, малорухомість і повільність руху, нерухомість міміки обличчя, ритмічне тремтіння кінцівок, яке слабшає при активному довільному русі або повному розслабленні. У більшості випадків, інші ознаки повністю розвиненого захворювання супроводжує дрібочуча хода, при якій пацієнт рухається або йде швидкими кроками з темпом, що прискорюється, неначе намагається наздогнати центр ваги тіла. Лікування хвороби Паркінсона із застосуванням таких фармакологічних засобів, як леводопа, у комбінації зі стереотактичною хірургією, у найкращому випадку дає лише частковий ефект. Основна причина складності лікування пов'язана з тим, що жоден з вказаних терапевтичних заходів не забезпечує вплив на причину захворювання, яка полягає у нейронній дегенерації. Зрештою, очевидно, досягнута точка, коли фармакологія більше не може компенсувати втрату допаміну базальних гангліїв. Інші нейродегенеративні захворювання, що уражують людей, виникають у результаті або викликані іншим чином, щонайменше частково, інсультом або іншою травмою або ушкодженням. Відповідно до одного джерела, щорічно відбувається не менше 700000 нових випадків інсульту. У США інсульт відбувається кожну хвилину. Більшість постраждалих від інсульту відчувають постійну непрацездатність, при цьому інсульт є основною причиною неврологічної непрацездатності у дорослих осіб, зачіпаючи 3-4 мільйони громадян США. Таким чином, зберігається потреба в ефективному лікуванні гострих і хронічних нейродегенеративних захворювань. Крім того, зберігається потреба в агентах, які є нейропротективними і, таким чином, можуть застосовуватися з метою запобігання загибелі і/або пошкодженню нейрона. Даний винахід направлений на спосіб нейропротекції, що включає введення потребуючому цього суб'єкту терапевтично ефективної дози сполуки формули (І): в якій 1 2 кожний R і R незалежно вибраний з групи, що включає водень і нижчий алкіл; 4 R вибраний з групи, що включає водень і нижчий алкіл; а є цілим числом від 1 до 2; вибраний з групи, що включає: 11 96747 де b є цілим числом від 0 до 4; і де с є цілим числом від 0 до 2; 5 кожний R незалежно вибраний з групи, що включає галоген, нижчий алкіл і нітро; за умови, що коли являє собою або , тоді а дорівнює 1; або її фармацевтично прийнятної солі. Даний винахід також направлений на спосіб нейропротекції, що включає введення потребуючому цього суб'єкту терапевтично ефективної дози сполуки формули (II): або її фармацевтично прийнятної солі. Прикладом винаходу є спосіб нейропротекції, що включає введення потребуючому цього суб'єкту терапевтично ефективної дози будь-якої зі сполук, описаних вище. В одному з прикладів винахід направлений на спосіб лікування гострих нейродегенеративних захворювань, що включає введення потребуючому цього суб'єкту терапевтично ефективної дози будь-якої зі сполук, описаних вище. В іншому прикладі винахід направлений на спосіб лікування хронічних нейродегенеративних захворювань. Також прикладом винаходу є спосіб запобігання загибелі або пошкодженню нейронів після інсульту або пошкодження мозку, центральної нервової системи або периферичної нервової системи. Даний винахід направлений на спосіб нейропротекції, що включає введення потребуючому цього суб'єкту терапевтично ефективної дози сполуки формули (І): або її фармацевтично прийнятної солі, де 1 2 4 , a, R , R і R визначені вище. Даний винахід також направлений на спосіб лікування гострих або хронічних нейродегенеративних захворювань. Даний винахід також направлений на спосіб запо 12 бігання загибелі або пошкодженню нейронів після пошкодження. Використовуване у даному описі поняття "нейропротекція" повинно означати захист нейронів у мозку, центральній нервовій системі або периферичній нервовій системі (переважно у мозку або спинному мозку) від загибелі і/або пошкодження. Переважно нейрони захищені від загибелі або пошкодження, викликаного окиснювальним стресом, наприклад, кисневими радикалами. Поняття "гострі нейродегенеративні захворювання", включене у способи даного винаходу, включає, крім іншого, різні типи гострих нейродегенеративних захворювань, пов'язаних з загибеллю або пошкодженням нейронів, включаючи недостатність мозкового кровообігу, локальну травму мозку, велику травму мозку, і також пошкодження спинного мозку, тобто мозкову ішемію або інфаркт, включаючи емболічне і тромбозне закупорення, реперфузію після гострої ішемії, перинатальне гіпоксійно-ішемічне пошкодження, зупинку серця, і також внутрішньочерепний крововилив будь-якого типу (включаючи, крім іншого, епідуральний, субдуральний, субарахноїдальний і внутрішньоцеребральний), і внутрішньочерепні і внутрішньохребетні пошкодження (включаючи, крім іншого, удар, відкрите поранення, зміщення, здавлювання і розрив), і також епісиндром у дітей. Переважно гостре нейродегенеративне захворювання є наслідком інсульту, гострої ішемії, травми голови або пошкоджень хребта. Поняття "хронічні нейродегенеративні захворювання", включене у способи даного винаходу, включає, крім іншого, хворобу Альцгеймера, хворобу Піка, хворобу дифузних тілець Леві, прогресуючий супрануклеарний параліч (синдром СтілаРічардсона-Ольшевського), мультисистемну дегенерацію (синдром Ши-Дрегера), хронічні епілептичні захворювання, пов'язані з нейродегенерацією, захворювання моторного нейрона, включаючи бічний аміотрофічний склероз, дегенеративну атаксію, кортико-базальну дегенерацію, гуамський комплекс БАС і деменції при паркінсонізмі, підгострий склерозуючий лейкоенцефаліт, хворобу Хантінгтона, хворобу Паркінсона, синуклеїнопатії (включаючи мультисистемну атрофію), первинну прогресуючу афазію, стріатонігральну дегенерацію, хворобу Мачадо-Джозефа/спінальноцеребелярну атаксію 3 типу і оливопонтоцеребелярні дегенерації, хворобу Жиля Де Ла Туретта, бульбарний і псевдобульбарний параліч, спінальну і спінально-бульбарну м'язову атрофію (хвороба Кеннеді), розсіяний склероз, первинний бічний склероз, спадкову спастичну параплегію, хворобу Вердніга-Хофмана, хворобу КугельбергаВеландер, хворобу Тея-Сакса, хворобу Сандхофа, спадкову спастичну хворобу, хворобу ВольфартаКугельберга-Веландера, спастичний парапарез, прогресуючу багатоосередкову лейкоенцефалопатію, спадкову вегетативну дистонію (синдром Райлі-Дея), і також захворювання, викликані пріонами (включаючи, крім іншого, хворобу КрейцфельдтаЯкоба, хворобу Герстмана-Страуслера-Шейнкера, Куру і смертельне спадкове безсоння). Переважно хронічне нейродегенеративне захворювання виб 13 ране з хвороби Альцгеймера, хвороби Паркінсона, розсіяного склерозу або церебрального паралічу. Як передбачається, інші захворювання, при яких відбувається загибель або пошкодження нейронів, також повинні бути включені у способи даного винаходу, і включають деменції, незалежно від основної етіології, включаючи старечу деменцію та інші деменції і захворювання з втратою пам'яті, включаючи деменцію, пов'язану з хворобою Альцгеймера, судинну деменцію, субкортикальну артеріосклеротичну енцефалопатію (хвороба Бінсвангера), деменцію ендокринного або метаболічного походження, деменцію при травмі голови і великому пошкодженні головного мозку, деменцію боксерів і лобову деменцію. Також у даний винахід включені способи нейропротекції (тобто способи запобігання загибелі і/або пошкодженню нейронів) після пошкодження мозку, центральної нервової системи або периферичної нервової системи, де пошкодження відбувається внаслідок хімічного, токсичного, інфекційного, радіаційного і/або травматичного пошкодження. Переважно способи даного винаходу спрямовані на запобігання загибелі або пошкодженню нейронів після травми або пошкодження мозку, голови і/або спинного мозку, незалежно від причини. Використовуване у даному описі поняття "суб'єкт" стосується тварини, переважно ссавця, найбільш переважно людини, яка була об'єктом лікування, спостереження або експерименту. Використовуване у даному описі поняття "терапевтично ефективна доза" означає ту кількість активної речовини або фармацевтичного агента, що проявляє біологічну або лікувальну відповідь у системі тканин, тварині або людині, яка підбирається дослідником, ветеринаром, лікарем або іншим клініцистом і включає полегшення симптомів захворювання або порушення, підданих терапії. 1 У варіанті здійснення даного винаходу R вибраний з групи, що включає водень і метил. В ін2 шому варіанті здійснення даного винаходу R вибраний з групи, що включає водень і метил. У ще одному варіанті здійснення даного винаходу кож1 2 1 2 ний R і R являє собою водень або кожний R і R являє собою метил. У варіанті здійснення даного винаходу -(СН2)авибраний з групи, що включає -СН2- і -СН2-СН2-. В іншому варіанті здійснення даного винаходу (СН2)а- являє собою -СН2-. 4 У варіанті здійснення даного винаходу R вибраний з групи, що включає водень і метил, пере4 важно R являє собою водень. У варіанті здійснення даного винаходу а дорівнює 1. У варіанті здійснення даного винаходу b є цілим числом від 0 до 2. В іншому варіанті здійснення даного винаходу с є цілим числом від 0 до 2. В іншому варіанті здійснення даного винаходу b є цілим числом від 0 до 1. В іншому варіанті здійснення даного винаходу с є цілим числом від 0 до 1. У ще одному варіанті здійснення даного винаходу сума b і с дорівнює цілому числу від 0 до 2, переважно цілому числу від 0 до 1. У ще одному 96747 14 варіанті здійснення даного винаходу b є цілим числом від 0 до 2, і с дорівнює 0. У варіанті здійснення даного винаходу вибраний з групи, що включає В іншому варіанті здійсненняданого винаходу вибраний з групи, що включає В одному з варіантів здійснення даного винаходу вибраний з групи, що включає 2-(2,3дигідробензо[1,4]діоксиніл), 2-(бензо[1,3]діоксоліл), 3-(3,4-дигідробензо[1,4]діоксепініл), 2-(6-хлор-2,3дигідробензо[1,4]діоксиніл), 2-(6-фтор-2,3дигідробензо[1,4]діоксиніл), 2-(хроманіл), 2-(5фтор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-хлор2,3-дигідробензо[1,4]діоксиніл), 2-(6-хлорбензо[1,3]діоксоліл), 2-(7-нітро-2,3Дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3дигідробензо[1,4]діоксиніл), 2-(5-хлор-2,3Дигідробензо[1,4]діоксиніл), 2-(6-бром-2,3дигідробензо[1,4]діоксиніл), 2-(6,7-дихлор-2,3Дигідробензо[1,4]діоксиніл), 2-(8-хлор-2,3дигідробензо[1,4]діоксиніл), 2-(2,3дигідронафто[2,3-b][1,4]діоксиніл) і 2-(4дигідронафто [1,3]діоксоліл). В іншому варіанті здійснення даного винаходу вибраний з групи, що включає 2(бензо[1,3]діоксоліл), 2-(2,3дигідробензо[1,4]діоксиніл), 2-(6-хлор-2,3дигідробензо[1,4]діоксиніл), 2-(7-хлор-2,3дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3дигідробензо[1,4]діоксиніл), 2-(6-бром-2,3дигідробензо[1,4]діоксиніл) і 2-(6,7-дихлор-2,3дигідробензо[1,4]діоксиніл). В іншому варіанті здійснення даного винаходу вибраний з групи, що включає 2-(2,3дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3дигідробензо[1,4]діоксиніл) і 2-(6-бром-2,3дигідробензо[1,4]діоксиніл). 5 У варіанті здійснення даного винаходу R вибраний з групи, що включає галоген і нижчий алкіл. 5 В іншому варіанті здійснення даного винаходу R вибраний з хлору, фтору, брому і метилу. 15 У варіанті здійснення даного винаходу стереоцентр сполуки формули (І) знаходиться в Sконфігурації. В іншому варіанті здійснення даного винаходу стереоцентр сполуки формули (І) знаходиться в R-конфігурації. У варіанті здійснення даного винаходу сполука формули (І) присутня у вигляді енантіомерно збагаченої суміші, де % енантіомерного збагачення (% ее) вище приблизно 75%, переважно вище приблизно 90%, більш переважно вище приблизно 95%, найбільш переважно вище приблизно 98%. Додаткові варіанти здійснення даного винаходу включають варіанти здійснення, в яких замісники, вибрані для однієї або більше змінних, визна1 2 3 4 чених у даному описі (тобто R , R , R , R , X-Y і А), незалежно вибрані, щоб бути будь-яким індивідуальним замісником або будь-якою підгрупою замісників, вибраних з повного списку, визначеного у даному описі. Типові сполуки даного винаходу наведені у таблиці 1 нижче. Додаткові сполуки даного винаходу наведені у таблиці 3. У таблицях 1 і 2 нижче колонка, озаглавлена "стерео", визначає стереоконфігурацію атома вуглецю у гетероциклі, приєднаного до зв'язку, поміченого зірочкою. Коли якенебудь позначення не наведене, сполуку одержували у вигляді суміші стереоконфігурацій. Коли наведене позначення "R" або "S", стереоконфігурація базувалася на енанті ом ерно збагаченому стартовому матеріалі. 96747 16 Використовуваний у даному описі "галоген", якщо не вказано інше, повинен означати хлор, бром, фтор і йод. Використовуване у даному описі позначення "алкіл", якщо не вказано інше, що використовується або окремо, або як частина замінної групи, включає лінійні і розгалужені ланцюги. Наприклад, алкільні радикали включають метил, етил, пропіл, ізопропіл, бутил, ізобутил, втор-бутил, трет-бутил, пентил і т.п. Якщо не вказано інше, позначення "нижчий" при використанні з алкілом означає вуглецевий ланцюг з 1-4 атомами вуглецю. Використовуваний у даному описі "алкокси", якщо не вказано інше, повинен означати кисневмісний ефірний радикал з описаних вище алкільних груп з лінійними або розгалуженими ланцюгами. Наприклад, метокси, етокси, н-пропокси, вторбутокси, трет-бутокси, н-гексилокси і т.п. Використовуваний у даному описі символ "*" повинен означати присутність стереогенного центру. Коли конкретна група є "заміщеною" (наприклад, алкілом, арилом і т.д.), то дана група може мати один або декілька замісників, переважно від одного до п'яти замісників, більш переважно від одного до трьох замісників, найбільш переважно від одного до двох замісників, незалежно вибраних зі списку замісників. Відносно замісників поняття "незалежно" означає, що коли може бути присутньо більше одного з вказаних замісників, такі замісники можуть бути однаковими або різними. Відповідно до стандартної номенклатури, що використовується у всьому описі даного винаходу, спочатку описується термінальна частина ланцюга, що визначається, і потім суміжні функціональні групи у напрямі до точки приєднання. Таким чином, наприклад, "феніл-алкіл-аміно-карбонілалкільний" замісник відповідає групі формули: Скорочення, що використовуються в описі, особливо у схемах і прикладах, наведені нижче: 17 ДЦК (DCC) ДХЕ (DCE) ДХМ (DCM) ДІПЕА (DIPEA) або ДІЕА (DIEA) ДМФА ДМСО ЕДК (EDC) Et3N або TEA (TEA) Et2O EA (EA) або EtOAc EtOH ІПС (IPA) Гепт ГБТ (HOBT) ВЕРХ ЛАГ (LAH) Μ або МеОН ЯМР Pd-C ОФ-ВЕРХ КТ або кт TEA (TEA) ТФА (TFA) ТГФ ТШХ Дициклогексилкарбодіімід Дихлоретан Дихлорметан Діізопропілетиламін Ν,Ν-диметилформамід Диметилсульфоксид Етилкарбодіімід Триетиламін Діетиловий ефір Етилацетат Етанол 2-пропанол Гептан 1-гідроксибензотриазол Високоефективна рідинна хроматографія Алюмогідрид літію Метанол Ядерний магнітний резонанс Паладієвий каталізатор на вугіллі Обернено-фазова високоефективна рідинна хроматографія Кімнатна температура Триетиламін Трифтороцтова кислота Тетрагідрофуран Тонкошарова хроматографія Коли сполуки відповідно до даного винаходу мають щонайменше один хіральний центр, вони відповідно можуть існувати у вигляді енантіомерів. Коли сполуки мають два або більше хіральних центрів, вони додатково можуть існувати у вигляді діастереомерів. Потрібно розуміти, що всі вказані ізомери і їх суміші включені в об'єм даного винаходу. Крім того, деякі з кристалічних форм сполук можуть існувати у вигляді поліморфних модифікацій, і, як передбачається, повинні бути включені у даний винахід. Крім того, деякі зі сполук можуть утворювати сольвати з водою (тобто гідрати) або зі звичайними органічними розчинниками, при цьому вказані сольвати, як передбачається, також повинні бути включені в об'єм даного винаходу. З метою застосування у медицині солі сполук даного винаходу належать до нетоксичних "фармацевтично прийнятних солей". Однак інші солі можуть використовуватися при одержанні сполук відповідно до даного винаходу або їх фармацевтично прийнятних солей. Придатні фармацевтично прийнятні солі сполук включають кислотноадитивні солі, які можуть бути одержані, наприклад, при змішуванні розчину сполуки з розчином фармацевтично прийнятної кислоти, такої як соляна кислота, сірчана кислота, фумарова кислота, малеїнова кислота, бурштинова кислота, оцтова кислота, бензойна кислота, лимонна кислота, винна кислота, вугільна кислота або фосфорна кислота. Крім того, коли сполуки винаходу несуть кислотну групу, їх придатні фармацевтично прийнятні солі можуть включати солі лужних металів, напри 96747 18 клад, солі натрію або калію; солі лужноземельних металів, наприклад, солі кальцію або магнію; а також солі, утворені з придатними органічними лігандами, наприклад, солі четвертинного амонію. Таким чином, приклади фармацевтично прийнятних солей включають наведені нижче: ацетат, бензолсульфонат, бензоат, бікарбонат, бісульфат, бітартрат, борат, бромід, едетат кальцію, камсилат, карбонат, хлорид, клавуланат, цитрат, дигідрохлорид, едетат, едисилат, естолат, езилат, фумарат, глюцептат, глюконат, глутамат, гліколіларсанілат, гексилрезорцинат, гідрабамін, гідробромід, гідрохлорид, гідроксинафтоат, йодид, ізотіонат, лактат, лактобіонат, лаурат, малат, малеат, манделат, мезилат, метилбромід, метилнітрат, метилсульфат, мукат, напсилат, нітрат, амонієва сіль N-метилглюкаміну, олеат, памоат (ембонат), пальмітат, пантотенат, фосфат/дифосфат, полігалактуронат, саліцилат, стеарат, сульфат, основний ацетат, сукцинат, танат, тартрат, теоклат, тозилат, триетйодид і валерат. Приклади кислот і основ, які можуть використовуватися в одержанні фармацевтично прийнятних солей, включають наведені нижче: кислоти, включаючи оцтову кислоту, 2,2дихлороцтову кислоту, ацетиловані амінокислоти, адипінову кислоту, альгінову кислоту, аскорбінову кислоту, L-аспарагінову кислоту, бензолсульфонову кислоту, бензойну кислоту, 4ацетамідобензойну кислоту, (+)-камфорну кислоту, камфорсульфонову кислоту, (+)-(1S)-камфор-10сульфонову кислоту, капринову кислоту, капронову кислоту, каприлову кислоту, коричну кислоту, лимонну кислоту, цикламову кислоту, додецилсірчану кислоту, етан-1,2-дисульфонову кислоту, етансульфонову кислоту, 2гідроксіетансульфонову кислоту, мурашину кислоту, фумарову кислоту, галактарову кислоту, гентизинову кислоту, глюкогептонову кислоту, Dглюконову кислоту, D-глюкуронову кислоту, Lглутамінову кислоту, α-оксоглутарову кислоту, гліколеву кислоту, гіпурову кислоту, бромоводневу кислоту, хлороводневу кислоту, (+)-L-молочну кислоту, (±)-DL-молочну кислоту, лактобіонову кислоту, малеїнову кислоту, (-)-L-яблучну кислоту, малонову кислоту, (±)-DL-мигдалеву кислоту, метансульфонову кислоту, нафталін-2сульфонову кислоту, нафталін-1,5-дисульфонову кислоту, 1-гідрокси-2-нафтенову кислоту, нікотинову кислоту, азотну кислоту, олеїнову кислоту, оротову кислоту, щавлеву кислоту, пальмітинову кислоту, памову кислоту, фосфорну кислоту, Lпіроглутамінову кислоту, саліцилову кислоту, 4аміносаліцилову кислоту, себацинову кислоту, стеаринову кислоту, бурштинову кислоту, сірчану кислоту, дубильну кислоту, (+)-L-винну кислоту, тіоціанову кислоту, п-толуолсульфонову кислоту і ундециленову кислоту; і основи, включаючи аміак, L-аргінін, бенетамін, бензатин, гідроксид кальцію, холін, деанол, діетаноламін, діетиламін, 2-(діетиламіно)етанол, етаноламін, етилендіамін, N-метилглюкамін, гідрабамін, 1H-імідазол, L-лізин, гідроксид магнію, 4-(2гідроксіетил)морфолін, піперазин, гідроксид калію, 1-(2-гідроксіетил)піролідин, вторинний амін, гідрок 19 96747 сид натрію, триетаноламін, трометамін і гідроксид цинку. Сполуки формули (І) можуть бути одержані відповідно до способу, наведеного на схемі 1. 20 Сполуки формули (X), де вибраний з , можуть бути одержані відповідно до способу, представленого на схемі 3. Таким чином, відповідним способом заміщена сполука формули (X), відома сполука або сполука, одержана відомими способами, взаємодіє з сульфамідом, відомою сполукою, де сульфамід переважно присутній у кількості у діапазоні від приблизно 2 до приблизно 5 еквівалентів в органічному розчиннику, такому як ТГФ, діоксан і т.п., переважно при підвищеній температурі у діапазоні від приблизно 50°С до приблизно 100°С, більш переважно приблизно при температурі дефлегмації, що приводить до відповідної сполуки формули (Іа). Як альтернатива заміщена відповідним чином сполука формули (X), відома сполука або сполука, одержана відомими способами, взаємодіє із заміщеною сполукою формули (XI), відомою сполукою або сполукою, одержаною відомими способами, у присутності основи, такої як TEA, ДІПЕА, піридин і т.п., в органічному розчиннику, такому як ДМФА, ДМСО і т.п., що приводить до відповідної сполуки формули (І). Сполуки формули (X), де являє собою Таким чином, придатним способом заміщена сполука формули (XIV), відома сполука або сполука, одержана відомими способами, взаємодіє з NH4OH, у присутності зшивального агента, такого як ДЦК і т.п., необов'язково в органічному розчиннику, такому як ацетонітрил і т.п., що приводить до відповідної сполуки формули (XV). Сполука формули (XV) взаємодіє з правильно підібраним відновлювальним агентом, таким як ЛАГ і т.п., в органічному розчиннику, такому як ТГФ, діетиловий ефір і т.п., що приводить до відповідної сполуки формули (Хb). Сполуки формули (X), де вибраний з і де а дорівнює 2, можуть бути одержані відповідно до способу, представленого на схемі 4. , можуть бути одержані відповідно до способу, представленого на схемі 2. Таким чином, придатним способом заміщена сполука формули (XII), відома сполука або сполука, одержана відомими способами (наприклад, як описано у схемі 3 вище), взаємодіє з NH4OH, відомою сполукою, необов'язково в органічному розчиннику, такому як ацетонітрил і т.п., що приводить до відповідної сполуки формули (XIII). Сполука формули (XIII) взаємодіє з правильно підібраним відновлювальним агентом, таким як ЛАГ і т.п., в органічному розчиннику, такому як ТГФ, діетиловий ефір і т.п., що приводить до відповідної сполуки формули (Ха). Таким чином, придатним способом заміщена 1 сполука формули (XVI), де J є придатною відхідною групою, такою як Вr, СІ, І, тозил, мезил, трифліл і т.п., відома сполука або сполука, одержана відомими способами (наприклад, активацією від1 повідної сполуки, де J являє собою ОН), взаємодіє з ціанідом, таким як ціанід калію, ціанід натрію і т.п., в органічному розчиннику, такому як ДМСО, ДМФА, ТГФ і т.п., що приводить до відповідної сполуки формули (XVII). Сполуку формули (XVII) відновлюють відповідно до відомих способів, наприклад, взаємодією з придатним відновлювальним агентом, таким як ЛАГ, боран і т.п., що приводить до відповідної сполуки формули (Хс). 21 96747 Сполуки формули (X), де вибраний з і де а дорівнює 1, можуть бути одержані відповідно до способу, представленого на схемі 5. Таким чином, придатним способом заміщену сполуку формули (XVIII), відому сполуку або сполуку, одержану відомими способами, активують відповідно до відомого способу, що приводить до 2 відповідної сполуки формули (XIX), де J являє собою придатну відхідну групу, таку як тозилат, СІ, Вr, І, мезилат, трифлат і т.п. Сполука формули (XIX) взаємодіє з фталімідною сіллю, такою як фталімід калію, фталімід натрію і т.п., в органічному розчиннику, такому як ДМФА, ДМСО, ацетонітрил і т.п., переважно при підвищеній температурі у діапазоні від 50°С до приблизно 200°С, більш переважно приблизно при температурі дефлегмації, що приводить до відповідної сполуки формули (XX). Сполука формули (XX) взаємодіє з N2H4, відомою сполукою, в органічному розчиннику, такому як етанол, метанол і т.п., переважно при підвищеній температурі у діапазоні від приблизно 50°С до приблизно 100°С, більш переважно приблизно при температурі дефлегмації і т.п., що приводить до відповідної сполуки формули (Xd). Фахівець, кваліфікований у даній галузі техніки, буде розуміти, що сполуки формули (X), де вибраний , з 22 можуть бути одержані відомими способами або, наприклад, відповідно до способів, представлених на схемах 2-5 вище, вибираючи і заміщаючи відповідні нафтилконденсовані сполуки для бензоконденсованих вихідних матеріалів. Фахівець, кваліфікований у даній галузі техніки, також буде розуміти, що коли необхідний єдиний енантіомер сполуки формули (X) (або суміш енантіомерів, де один енантіомер є збагаченим), зазначені вище способи, описані у схемах 1-5, можуть бути застосовані за допомогою заміщення відповідного єдиного енантіомеру (або суміші енантіомерів, де один енантіомер є збагаченим) для відповідного вихідного матеріалу. Фахівець, кваліфікований у даній галузі техніки, буде розуміти, що стадія реакції даного винаходу може бути проведена у різних розчинниках або системах розчинників, вказана стадія реакції може також бути проведена у суміші придатних розчинників або систем розчинників. Коли способи одержання сполук відповідно до винаходу дають суміші стереоізомерів, то вказані ізомери можуть бути розділені звичайними способами, такими як препаративна хроматографія. Сполуки можуть бути одержані у рацемічній формі, або окремі енантіомери можуть бути одержані енантіоселективним синтезом або за допомогою виділення. Сполуки можуть, наприклад, бути розділені на енантіомери, що складають їх, стандартними способами, такими як утворення діастереомерних пар шляхом утворення солі з оптично активною кислотою, такою як (-)-ди-п-толуоїл-Dвинна кислота і/або (+)-ди-п-толуоїл-L-винна кислота, з подальшою фракційною кристалізацією і регенерацією вільної основи. Сполуки можуть також бути розділені за допомогою утворення діастереомерних складних ефірів або амідів, з подальшим хроматографічним розділенням і видаленням хіральної допоміжної сполуки. Як альтернатива, сполуки можуть бути розділені з використанням хіральної ВЕРХ-колонки. При здійсненні будь-якого зі способів одержання сполук даного винаходу може бути необхідним і/або бажаним захистити чутливі або реакційноздатні групи на будь-якій з відповідних молекул. Це може бути досягнуто за допомогою звичайних захисних груп, таких як описані у Protective Groups in Organic Chemistry, ed. J.F.W. McOmie, Plenum Press, 1973; і T.W. Greene & P.G.M. Wuts, Protective Groups in Organic Synthesis, John Wiley & Sons, 1991. Захисні групи можуть бути видалені на одній зі зручних подальших стадій, використовуючи способи, відомі з рівня техніки. Даний винахід додатково включає фармацевтичні композиції, що містять одну або більше сполук формули (І) з фармацевтично прийнятним носієм. Фармацевтичні композиції, що містять як активний компонент одну або більше сполук винаходу, описані у даному описі, можуть бути одержані ретельним змішуванням сполуки або сполук з фармацевтичним носієм відповідно до стандартних методик складання фармацевтичних композицій. Носій може мати великий діапазон форм в залежності від бажаного шляху введення (наприклад, орального, парентерального). Таким чином, 23 у випадку рідких препаратів для перорального застосування, таких як суспензії, еліксири і розчини, придатні носії і домішки включають воду, гліколі, масла, спирти, ароматизатори, консерванти, стабілізатори, барвники і т.п.; у випадку твердих препаратів для перорального застосування, таких як порошки, капсули і таблетки, придатні носії і домішки включають крохмалі, цукри, розріджувачі, гранулюючі агенти, ковзні речовини, зв'язувальні речовини, дезінтегруючі домішки і т.п. Тверді препарати для перорального застосування можуть бути також покриті такими речовинами, як цукри, або покриті ентеросолюбільним покриттям, щоб змінити основну ділянку абсорбції. У випадку парентерального введення носій звичайно буде складатися зі стерильної води, при цьому з метою підвищення розчинності або для консервації можуть бути додані інші компоненти. Суспензії або розчини для ін'єкцій можуть бути також приготовані з використанням водних носіїв нарівні з відповідними домішками. Для приготування фармацевтичних композицій даного винаходу одну або більше сполук даного винаходу як активний компонент ретельно перемішують з фармацевтичним носієм відповідно до звичайних методик складання фармацевтичних композицій, де вказаний носій може мати великий діапазон форм в залежності від форми препарату, необхідної для введення, наприклад, оральної або парентеральної, такої як внутрішньом'язова. У ході приготування композицій у лікарській формі для перорального застосування може використовуватися будь-який зі стандартних фармацевтичних носіїв. Таким чином, у випадку рідких препаратів для перорального застосування, таких як, наприклад, суспензії, еліксири і розчини, придатні носії і домішки включають воду, гліколі, масла, спирти, ароматизатори, консерванти, барвники і т.п.; у випадку твердих препаратів для перорального застосування, таких як, наприклад, порошки, капсули, каплети, желатинові капсули і таблетки, придатні носії і домішки включають крохмалі, цукри, розріджувачі, гранулюючі агенти, ковзні речовини, зв'язувальні речовини, дезінтегруючі домішки і т.п. Завдяки легкості введення таблетки і капсули являють собою найбільш вигідну лікарську форму для перорального застосування, і у цьому випадку, очевидно, застосовуються тверді фармацевтичні носії. Якщо необхідно, таблетки можуть бути покриті цукром або ентеросолюбільним покриттям за допомогою стандартних методик. У випадку препаратів для парентерального застосування носій звичайно буде включати стерильну воду, хоча можуть бути включені інші компоненти, призначені, наприклад, для підвищення розчинності або консервації. Також можуть бути приготовані суспензії для ін'єкцій, при цьому можуть використовуватися відповідні рідкі носії, суспендуючі домішки і т.п. Фармацевтичні композиції у даному описі будуть містити таку кількість активного компонента, з розрахунку на лікарську форму, наприклад, таблетку, капсулу, порошок, ін'єкцію, чайну ложку і т.п., яка необхідна для доставки ефективної дози, як описано вище. Фармацевтичні композиції у даному описі будуть містити, з розрахунку на лікарську 96747 24 форму, наприклад, таблетку, капсулу, порошок, ін'єкцію, свічку, чайну ложку і т.п., приблизно 0,11000 мг і зможуть прийматися у дозуванні приблизно 0,01-200,0 мг/кг/день, переважно приблизно 0,1-100 мг/кг/день, більш переважно приблизно 0,5-50 мг/кг/день, більш переважно приблизно 1,025,0 мг/кг/день або у будь-якому вказаному діапазоні. Дозування, однак, можуть бути різні в залежності від потреби пацієнтів, тяжкості захворювання, яке лікують, і застосовуваної сполуки. Може використовуватися або щоденне введення, або постперіодичне дозування. Переважно вказані композиції знаходяться у стандартних лікарських формах, таких як таблетки, пілюлі, капсули, порошки, гранули, стерильні розчини для парентерального введення або суспензії, дозовані аерозолі або рідкі спреї, краплі, ампули, автоінжекторні пристрої або свічки; для орального, парентерального, інтраназального, сублінгвального або ректального введення, або для введення за допомогою інгаляції або вдування. Як альтернатива, композиція може бути присутньою у формі, придатній для щотижневого або щомісячного введення; наприклад, нерозчинна сіль активної сполуки, така як деканоат, може бути придатною для забезпечення препарату пролонгованої дії для внутрішньом'язової ін'єкції. Для приготування твердих композицій, таких як таблетки, основний активний компонент змішують з фармацевтичним носієм, наприклад, зі звичайними компонентами таблетування, такими як кукурудзяний крохмаль, лактоза, сахароза, сорбіт, тальк, стеаринова кислота, стеарат магнію, фосфат дикальцію або камеді, і також з іншими фармацевтичними розріджувачами, наприклад, водою, що дозволяє одержати тверду попередню композицію, яка містить гомогенну суміш сполуки даного винаходу або її фармацевтично прийнятної солі. Коли вказані попередні композиції згадуються як гомогенні, це означає, що активний компонент рівномірно диспергований по всьому об'єму композиції, і таким чином композиція може бути легко розділена на рівноефективні лікарські форми, такі як таблетки, пілюлі і капсули. Потім вказану тверду попередню композицію розділяють на стандартні лікарські форми описаного вище типу, що містять від 0,1 до приблизно 1000 мг активного компоненту даного винаходу. Таблетки або пілюлі нової композиції можуть бути покриті або складені іншим способом, що забезпечує лікарську форму, яка володіє перевагою пролонгованої дії. Наприклад, таблетка або пілюля може включати внутрішній і зовнішній компоненти дозування, причому останній присутній у формі оболонки поверх основи. Вказані два компоненти можуть бути розділені ентеросолюбільним шаром, який служить для запобігання розпаду у шлунку і дозволяє внутрішньому компоненту проходити у вихідному вигляді у дванадцятипалу кишку або забезпечує затримку вивільнення. Для вказаних ентеросолюбільних шарів або покриттів можуть використовуватися різні матеріали, які включають ряд полімерних кислот і такі матеріали, як шелак, цетиловий спирт і ацетат целюлози. 25 Рідкі форми для перорального введення або ін'єкцій, в які можуть бути включені нові сполуки даного винаходу, включають водні розчини, ароматизовані сиропи, водні або масляні суспензії і ароматизовані емульсії з харчовими оліями, такими як бавовняна олія, кунжутна олія, кокосова олія або арахісова олія, і також еліксири і подібні фармацевтичні носії. Придатні диспергуючі або суспендуючі домішки для водних суспензій включають синтетичні і натуральні камеді, такі як трагакантова камедь, гуміарабік, альгінат, декстран, натрієва сіль карбоксиметилцелюлози, метилцелюлоза, полівінілпіролідон або желатин. Спосіб лікування депресії, описаний у даному винаході, може також здійснюватися з використанням фармацевтичної композиції, що включає будьяку зі сполук, визначених у даному описі, і фармацевтично прийнятний носій. Фармацевтична композиція може містити від приблизно 0,1 до 1000 мг, переважно від приблизно 50 до 500 мг сполуки, і може бути складена у будь-якій формі, придатній для вибраного способу введення. Носії включають необхідні та інертні фармацевтичні наповнювачі, включаючи, крім інших, зв'язувальні речовини, суспендуючі домішки, ковзні речовини, ароматизатори, підсолоджувачі, консерванти, барвники і покриття. Композиції, придатні для орального введення, включають тверді форми, такі як пілюлі, таблетки, каплети, капсули (кожна форма включає композиції негайного вивільнення, з регульованим часом вивільнення і уповільненим вивільненням), гранули і порошки, і також рідкі форми, такі як розчини, сиропи, еліксири, емульсії та суспензії. Форми, що застосовуються для парентерального введення, включають стерильні розчини, емульсії та суспензії. Переважно, сполуки даного винаходу можна вводити в єдиній щоденній дозі, або повна щоденна доза може бути введена у роздільних дозах, два, три або чотири рази на день. Крім того, сполуки даного винаходу можна вводити в інтраназальній формі за допомогою місцевого застосування придатних інтраназальних носіїв, або за допомогою трансдермальних пластирів, відомих середнім фахівцям у даній галузі техніки. При введенні у формі трансдермальної системи доставки, введення дози, безумовно, буде здійснюватися безперервно, і не періодично, протягом всього режиму дозування. Наприклад, для орального введення у формі таблетки або капсули, активний компонент лікарського засобу може бути об'єднаний з нетоксичним фармацевтично прийнятним інертним носієм для орального застосування, таким як етанол, гліцерин, вода і т.п. Крім того, коли бажано або необхідно, у суміш можуть бути також включені придатні зв'язувальні речовини, ковзні речовини, дезінтегруючі домішки і барвники. Придатні зв'язувальні речовини включають, крім інших, крохмаль, желатин, натуральний цукор, такий як глюкоза або бета-лактоза, цукристі речовини кукурудзи, натуральні і синтетичні камеді, такі як гуміарабік, трагакант або олеат натрію, стеарат натрію, стеарат магнію, бензоат натрію, ацетат натрію, хлорид натрію і т.п. Дезінтегратори включають, крім інших, 96747 26 крохмаль, метилцелюлозу, агар, бентоніт, ксантанову камедь і т.п. У рідкі форми звичайно додають суспендуючі або диспергуючі домішки, такі як синтетичні і натуральні камеді, наприклад, трагакант, гуміарабік, метилцелюлозу і т.п. Для парентерального введення переважними є стерильні суспензії і розчини. Ізотонічні препарати, які звичайно містять придатні консерванти, застосовуються у випадках, коли переважне внутрішньовенне введення. Сполуки даного винаходу можна вводити у складі будь-якої з попередніх композицій і відповідно до режимів дозування, встановлених у рівні техніки, у всіх випадках, коли потрібне лікування депресії. Щоденна доза продуктів може варіювати у широкому діапазоні від 0,01 до 200 мг/кг для дорослої людини на день. У випадку перорального введення сполуки переважно забезпечуються у формі таблеток, що містять 0,01, 0,05, 0,1, 0,5, 1,0, 2,5, 5,0, 10,0, 15,0, 25,0, 50,0, 100, 150, 200, 250, 500 і 1000 міліграмів активного компонента для симптоматичного регулювання дозування підданого лікуванню пацієнта. Ефективна доза препарату звичайно знаходиться на рівні дозування від приблизно 0,01 мг/кг до приблизно 200 мг/кг маси тіла на день. Переважно діапазон дозування складає від приблизно 0,1 до приблизно 100,0 мг/кг маси тіла на день, більш переважно від приблизно 0,5 мг/кг до приблизно 50 мг/кг, більш переважно від приблизно 1,0 до приблизно 25,0 мг/кг маси тіла на день. Сполуки можна вводити у режимі 1-4 рази на день. Оптимальні дози, що вводяться, можуть бути легко визначені фахівцями, кваліфікованими у даній галузі техніки, і варіюють в залежності від конкретної використовуваної сполуки, способу введення, концентрації препарату і поліпшення протягом захворювання. Крім того, фактори, пов'язані з конкретним пацієнтом, підданим лікуванню, що включають вік пацієнта, вагу, режим харчування і час введення, приводять до необхідності корекції дозувань. Фахівець, кваліфікований у даній галузі техніки, буде розуміти, що випробування і in vivo, і in vitro з використанням придатних, відомих і загальноприйнятих клітинних і/або тваринних моделей дозволяють прогнозувати здатність випробовуваної сполуки при лікуванні або профілактиці даного порушення. Фахівець, кваліфікований у даній галузі техніки, також буде розуміти, що клінічні випробування на людях, включаючи первинні випробування на людині, випробування з підбору дози і випробування на ефективність, у здорових пацієнтів і/або страждаючих від даного порушення, можуть бути проведені відповідно до способів, відомих у клінічній і медичній галузях. Наведені нижче приклади викладені з метою допомоги при розумінні винаходу, і не призначені і не повинні розглядатися, як такі, що обмежують яким-небудь чином винахід, викладений у формулі, яка представлена далі. Приклад 1 27 96747 28 ((3,4-дигідро-2Н-бензо[b][1,4]діоксепін-3іл)метил)сульфамід (сполука № 3) Катехін (5,09 г, 46,2 ммоль) і карбонат калію змішували в ацетонітрилі і нагрівали до кипіння зі зворотним холодильником протягом однієї години. Потім додавали 2-хлорметил-3-хлор-1-пропен (5,78 г, 46,2 ммоль), і взаємодію продовжували при кип'ятінні зі зворотним холодильником протягом 24 годин. Розчин охолоджували до кімнатної температури і відфільтровували. Фільтрат випарювали, і залишок розчиняли у воді і екстрагували діетиловим ефіром (3 рази). Об'єднаний органічний розчин сушили над MgSO4 і концентрували. Очищали за допомогою хроматографії (2% діетилового ефіру і гексані), внаслідок чого одержували 3метилен-3,4-дигідро-2Н-бензо[b][1,4]діоксепін у вигляді безбарвного масла. + MC (ESI): 163,2 (М+Н ) 1 H-ЯМР (300 МГц, CDCI3) δ: 6,94 (м, 4Н), 5,07 (с, 2Н), 4,76 (с, 4Н). 3-метилен-3,4-дигідро-2Нбензо[b][1,4]діоксепін (5,00 г, 30,8 ммоль) розчиняли у сухому ТГФ (100 мл). Боран-ТГФ (1,0 Μ у ТГФ, 10,3 мл) додавали при 0°С. Реакційну суміш перемішували при кімнатній температурі протягом 5 годин. Додавали аміносульфонову кислоту (6,97 г, 61,6 ммоль). Реакційну суміш нагрівали до кипіння зі зворотним холодильником протягом ночі. Реакційну суміш охолоджували до кімнатної температури і додавали водний розчин гідроксиду натрію (3,0 М, 100 мл). Розчин екстрагували етилацетатом (3×100 мл). Об'єднаний органічний розчин сушили над MgSO4. Розчин концентрували у вакуумі і очищали хроматографією (2-8% метанолу у дихлорметані), внаслідок чого ((3,4-дигідро-2Нбензо[b][1,4]діоксепін-3-іл)метил)амін одержували у вигляді безбарвного масла. + MC (ESI): 180,1 (М+Н ) 1 Н-ЯМР (300 МГц, ДМСО) δ: 6,92 (м, 4Н), 4,21 (м, 2Н), 4,07 (м, 2Н), 3,33 (широкий, 2Н), 3,16 (д, J=4 Гц, 1Н), 2,72 (д, J=4 Гц, 1Н), 2,30 (м, 1Н). ((3,4-дигідро-2Н-бензо[b][1,4]діоксепін-3іл)метил)амін (2,90 г, 16,2 ммоль) і сульфамід (3,11 г, 32,4 ммоль) змішували у сухому діоксані (60 мл) і нагрівали до кипіння зі зворотним холодильником протягом ночі. Додавали хлороформ, і осад видаляли за допомогою фільтрації. Фільтрат концентрували у вакуумі і очищали за допомогою хроматографії (2-8% ацетону у дихлорметані), внаслідок чого одержували вказану у заголовку сполуку у вигляді не зовсім білої твердої речовини. + 258,8 (М+Н ) 1 H-ЯМP (300 МГц, ДМСО) δ: 6,92 (м, 4Н), 6,71 (широкий, 1Н), 6,59 (широкий, 2Н), 4,19 (м, 2Н), 4,04 (м, 2Н), 3,00 (м, 2Н), 2,39 (м, 1Н). Приклад 2 N-(2,3-дигідробензо[1,4]діоксин-2ілметил)сульфамід (сполука № 1) Рацемічний 2,3-дигідро-1,4-бензодіоксин-2ілметиламін (4,4 г, 26 ммоль) і сульфамід (5,1 г, 53 ммоль) змішували в 1,4-діоксані (100 мл) і кип'ятили зі зворотним холодильником протягом 2 годин. Реакційну суміш охолоджували до кімнатної температури, після чого невелику кількість твердої речовини відфільтровували і видаляли. Фільтрат випарювали у вакуумі, і залишок очищали за допомогою колонкової флеш-хроматографії (ДХМ:метанол - 10:1), одержуючи білу тверду речовину. Тверду речовину перекристалізовували від ДХМ, внаслідок чого одержували вказану у заголовку сполуку у вигляді білої твердої речовини. Т.пл.: 97,5-98,5°С Елементний аналіз: Розрахунковий склад: С, 44,25; Н, 4,95; Ν, 11,47; S, 13,13 Одержаний склад: С, 44,28; Н, 4,66; Ν, 11,21; S, 13,15 1 Н-ЯМР (ДМСО-d6) δ: 6,85 (м, 4Н), 6,68 (шир.с, 3Н, ΝΗ), 4,28 (м, 2Н), 3,97 (дд, J=6,9, 11,4 Гц, 1Н), 3,20 (м, 1Н), 3,10 (м, 1Н). Приклад 3 (Бензо[1,3]діоксол-2-ілметил)сульфамід (сполука № 2) Катехін (10,26 г, 93,2 ммоль), метоксид натрію (25% за масою у метанолі, 40,3 г, 186 ммоль) і метил дихлорацетат (13,3 г, 93,2 ммоль) змішували у сухому метанолі (100 мл). Розчин нагрівали до кипіння зі зворотним холодильником протягом ночі. Реакційну суміш охолоджували до кімнатної температури, підкислювали шляхом додавання концентрованої хлороводневої кислоти, і потім концентрували у вакуумі до об'єму приблизно 50 мл. Додавали воду, і суміш екстрагували діетиловим ефіром (3×100 мл). Об'єднаний органічний розчин сушили над MgSO4, концентрували до одержання коричневого твердого залишку, і очищали за допомогою хроматографії (2% етилацетату у гексані), внаслідок чого одержували метиловий ефір бензо[1,3]діоксол-2-карбонової кислоти у вигляді безбарвного масла. + MC (ESI): 195,10 (М+Н ). 1 Н-ЯМР (300 МГц, CDCI3) δ: 6,89 (широкий, 4Н), 6,29 (с, 1Н), 4,34 (кв., J=7 Гц, 2Н), 1,33 (т, J=7 Гц, 3Н). До метилового ефіру бензо[1,3]діоксол-2карбонової кислоти (7,21 г, 40,0 ммоль) додавали гідроксид амонію (29% у воді, 10 мл) і достатню кількість ацетонітрилу для одержання гомогенної суміші (приблизно 5 мл). Розчин перемішували протягом двох годин при кімнатній температурі, і потім додавали дистильовану воду. Амід бензо[1,3]діоксол-2-карбонової кислоти, що випав у вигляді білого осаду, збирали за допомогою філь 29 трації і використовували без подальшого очищення. + MC (ESI): 160,00 (М+H ) 1 H-ЯМР (300 МГц, ДМСО) δ: 7,99 (с, широкий, 1Н), 7,72 (с, широкий, 1Н), 6,94 (м, 2Н) 6,86 (м, 2Н), 6,30 (с, 1Н). Амід бензо[1,3]діоксол-2-карбонової кислоти (5,44 г, 32,9 ммоль) розчиняли у тетрагідрофурані (ТГФ, 100 мл). До розчину при кімнатній температурі повільно додавали алюмогідрид літію (ЛАГ, 1 Μ у ТГФ, 39,5 мл, 39,5 ммоль). Реакційну суміш перемішували при кімнатній температурі протягом 24 годин. Потім з метою гідролізу надлишку ЛАГ додавали дистильовану воду. Додавали водний розчин гідроксиду натрію (3,0 М, 100 мл), після чого розчин екстрагували етилацетатом (3×100 мл). Об'єднаний органічний розчин промивали водою і сушили над MgSO4. Розчинник випарювали, внаслідок чого одержували Сбензо[1,3]діоксол-2-ілметиламін у вигляді безбарвного масла. + MC (ESI): 152,1 (М+Н ) 1 Н-ЯМР (300 МГц, CDCI3) δ: 6,87 (м, 4Н), 6,09 (т, J=4 Гц, 1Н), 3,13 (д, J=4 Гц, 2Н). С-бензо[1,3]діоксол-2-ілметиламін (2,94 г, 19,4 ммоль) і сульфамід (3,74 г, 38,9 ммоль) змішували у сухому діоксані (50 мл), і одержаний розчин нагрівали до кипіння зі зворотним холодильником протягом ночі. Реакційну суміш концентрували, і залишок очищали за допомогою хроматографії (210% ацетону у дихлорметані), внаслідок чого одержували вказану у заголовку сполуку у вигляді білої твердої речовини. + MC (ESI): 230,0 (М+Н ) 1 Н-ЯМР (300 МГц, CDCI3) δ: 6,87 (м, 4Н), 6,25 (т, J=4 Гц, 1Н), 4,79 (широкий, 1Н), 4,62 (широкий, 1Н), 3,64 (д, J=4 Гц, 2Н). Приклад 4 (2S)-(-)-N-(2,3-дигідробензо[1,4]діоксин-2ілметил)сульфамід (сполука № 4) Катехін (13,2 г, 0,12 моль) і карбонат калію (16,6 г, 0,12 моль) змішували у ДМФА (250 мл), додавали (2R)-гліцидилтозилат (22,8 г, 0,10 моль) і реакційну суміш перемішували при 60°С протягом 24 годин. Реакційну суміш охолоджували до кімнатної температури, розбавляли льодяною водою (1 л) і екстрагували діетиловим ефіром (4 рази). Об'єднаний органічний розчин промивали 3 рази 10%-им розчином карбонату калію, однократно водою, однократно насиченим розчином солі і випарювали у вакуумі, внаслідок чого одержували білу тверду речовину, яку очищали за допомогою колонкової флеш-хроматографії (ДХМ:метанол 50:1), одержуючи ((2S)-2,3дигідробензо[1,4]діоксин-2-іл)метанол у вигляді твердої речовини. Одержану тверду речовину (13,3 г, 68 ммоль) розчиняли у піридині (85 мл), охолодженому до 0°С, додавали п-толуолсульфонілхлорид (13,0 г, 68 ммоль), після чого реакційну суміш перемішували при кімнатній температурі протягом 20 годин. 96747 30 Реакційну суміш розбавляли діетиловим ефіром (1 л) і 1 н. НСI (1,2 л). Органічний шар виділяли і промивали 2 рази 1 н. НСI (500 мл), 4 рази водою (150 мл), однократно насиченим розчином солі, сушили (MgSO4) і випарювали у вакуумі, внаслідок чого одержували білу тверду речовину, яку очищали за допомогою колонкової флешхроматографії (гептан:ЕА - 2:1), одержуючи (2S)2,3-дигідробензо[1,4]діоксин-2-ілметиловий ефір толуол-4-сульфонової кислоти у вигляді білої твердої речовини. Білу тверду речовину змішували з фталімідом калію (14,4 г, 78 ммоль) у ДМФА (250 мл) і нагрівали до кипіння зі зворотним холодильником протягом 1 години, охолоджували до кімнатної температури і одержану суміш вливали у воду, що енергійно перемішується (1,5 л), після чого перемішували 30 хвилин. Білий осад відфільтровували і одержану тверду речовину промивали декілька разів водою, 2%-им розчином NaOH, і потім знову водою, і потім сушили на повітрі, одержуючи (2S)2-(2,3-дигідробензо[1,4]діоксин-2-ілметил)ізоіндол1,3-діон у вигляді білої порошкоподібної речовини. Одержану білу порошкоподібну речовину змішували з гідразином (2,75 г, 86 ммоль) в ЕtOН (225 мл), після чого нагрівали при кип'ятінні зі зворотним холодильником протягом 2 годин, і потім охолоджували до кімнатної температури, додавали 1 н. НСI до рН 1,0 і перемішували протягом 15 хвилин. Одержану білу тверду речовину відфільтровували і промивали свіжим ЕtOН (осад видаляли), після чого фільтрат випарювали у вакуумі до одержання твердої речовини, яку розділяли між діетиловим ефіром і водним розчином NaOH. Розчин діетилового ефіру сушили (Na2SO4) і випарювали у вакуумі, одержуючи світло-жовте масло. Одержане масло очищали за допомогою колонкової флеш-хроматографії (ДХМ:МеОН - 10:1), одержуючи масло. Частину одержаного масла (4,82 г, 29 ммоль) у 2-пропанолі (250 мл) обробляли 1 н. НСI (30 мл) і нагрівали на паровій бані до одержання гомогенного розчину, і потім охолоджували до кімнатної температури. Через 3 години суміш охолоджували на льоді протягом 2 годин. Білу пластівчасту речовину (відповідна сіль НСI (2S)-С(2,3-дигідробензо[1,4]діоксин-2-іл)метиламіну) відфільтровували, і потім знову перекристалізовували з 2-пропанолу, одержуючи білу тверду речовину. [α]D=-69,6(c=1,06,EtOH). Одержану білу тверду речовину розділяли між ДХМ і розбавленим розчином NaOH, після чого ДХМ сушили (Na2SO4) і випарювали у вакуумі, одержуючи (2S)-С-(2,3-дигідробензо[1,4]діоксин-2іл)метиламін у вигляді масла. [α]D=-57,8 (c=1,40, СНСI3). Одержане масло (2,1 г, 12,7 ммоль) і сульфамід (2,44 г, 25,4 ммоль) кип'ятили зі зворотним холодильником у діоксані (75 мл) протягом 2 годин, сирий продукт очищали за допомогою колонкової флеш-хроматографії (ДХМ:МеОН - 10:1), внаслідок чого одержували білу тверду речовину, яку перекристалізовували з ДХМ, одержуючи вказану у заголовку сполуку у вигляді білої кристалічної речовини. 31 Т.пл. 102-103 °С [α]D=-45,1°(c=1,05,M); 1 Н-ЯМР (ДМСО-d6) δ: 6,86 (м, 4Н), 6,81 (шир.с, 3Н, ΝΗ), 4,3 (м, 2Н), 3,97 (дд, J=6,9, 11,4 Гц, 1Н), 3,20 (дд, J=5,5, 13,7 Гц, 1Н), 3,10 (дд, J=6,9, 13,7 Гц, 1Н). Елементний аналіз: Розрахунковий склад: С, 44,25; Н, 4,95; N, 11,47; S, 13,13 Одержаний склад: С, 44,20; Н, 4,69; N, 11,40; S, 13,22. Приклад 5 N-(2,3-дигідробензо[1,4]діоксин-2-ілметил)N',N'-диметилсульфамід (сполука № 6) Рацемічний 2,3-дигідро-1,4-бенздіоксин-2ілметиламін (8,25 г, 5,0 ммоль) і триетиламін (1,52 г, 15 ммоль) змішували у ДМФА (10 мл) і після додання диметилсульфамоїлхлориду (1,44 г, 10 ммоль) охолоджували на льодяній бані. Потім реакційну суміш перемішували протягом 3 годин з постійним охолоджуванням. Реакційну суміш розділяли між етилацетатом і водою, після чого етилацетатний розчин промивали насиченим розчином солі, сушили (MgSO4) і випарювали у вакуумі, одержуючи масло. Одержане масло очищали за допомогою колонкової флеш-хроматографії (етилацетат:гептан - 1:1), одержуючи білу тверду речовину, яку перекристалізовували (етилацетат/гексан), внаслідок чого одержували вказану у заголовку сполуку у вигляді білої пластівчастої речовини. Т.пл. 76-78°С + МС 273 (МН ) Елементний аналіз: Розрахунковий склад: С, 48,52; Н, 5,92; N, 10,29; S, 11,78 Одержаний склад: С, 48,63; Н, 5,62; N, 10,20; S, 11,90 1 Н-ЯМР (CDCI3) δ: 6,87 (м, 4Н), 4,59 (шир.м, 1Н, ΝΗ), 4,35 (м, 1Н), 4,27 (дд, J=2,3, 11,4 Гц, 1Н), 4,04 (дд, J=7,0, 11,4, 1Н), 3,36 (м, 2Н), 2,82 (с, 6Н). Приклад 6 N-(2,3-дигідробензо[1,4]діоксин-2-ілметил)-Nметилсульфамід (сполука № 7) Рацемічний 2,3-дигідро-1,4-бенздіоксин-2ілметиламін (825 мг, 5 ммоль) розчиняли в етил форміаті (15 мл), кип'ятили зі зворотним холодильником протягом 30 хвилин, після чого випарювали у вакуумі, одержуючи N-(2,3дигідробензо[1,4]діоксин-2-ілметил)формамід у вигляді масла. Одержане масло у діетиловому ефірі (25 мл) обробляли 1 Μ ЛАГ у ТГФ (9,0 мл, 9,0 ммоль) при 0°С і перемішували протягом 5 годин при кімнатній температурі. Реакційну суміш охолоджували на льодяній бані і розбавляли водою (0,50 мл), після 96747 32 чого додавали 3 н. NaOH (0,50 мл) і воду (0,50 мл). Потім суміш перемішували при кімнатній температурі протягом 1 години. Осад відфільтровували, і фільтрат випарювали у вакуумі, одержуючи залишок, який був розділений між 1 н. НСI і діетиловим ефіром. Водну фазу нейтралізували 1 н. NaOH і екстрагували діетиловим ефіром. Органічну фазу сушили (MgSO4) і випарювали у вакуумі, одержуючи (2,3-дигідробензо[1,4]діоксин-2ілметил)метиламін у вигляді масла. + МС 180 (МН ) 1 Н-ЯМР (CDCI3) δ: 6,85 (м, 4Н), 4,30 (м, 2Н), 4,02 (дд, J=7,9, 11,6 Гц, 1Н), 2,85 (м, 2Η), 2,50 (с, 3Н). Одержане масло (380 мг, 2,1 ммоль) і сульфамід (820 мг, 8,5 ммоль) змішували у діоксані (15 мл), кип'ятили зі зворотним холодильником протягом 1,5 год. і випарювали у вакуумі, одержуючи неочищений залишок. Залишок очищали за допомогою колонкової хроматографії (етилацетат/гептан - 1:1), після чого одержану тверду речовину перекристалізовували з етилацетату/гексану, одержуючи вказану у заголовку сполуку у вигляді білої твердої речовини. Т.пл. 97-98°С 1 МС 257 (М- ) Елементний аналіз: Розрахунковий склад: С, 46,50; Н, 5,46; N, 10,85; S, 12,41 Одержаний склад: С, 46,48; Н, 5,65; N, 10,90; S, 12,07 1 H-ЯМР (CDCI3) δ: 6,86 (м, 4Н), 4,52 (шир.с, 2Н), 4,46 (м, 1Н), 4,29 (дд, J-2,3, 11,5 Гц, 1Н), 4,05 (дд, J=6,5, 11,5 Гц, 1Н), 3,51 (дд, J=6,7, 14,9 Гц, 1Н), 3,40 (дд, J=5,9, 14,9 Гц, 1Н), 2,99 (с, 3Н). Приклад 7 (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин2-ілметил)сульфамід (сполука № 8) Відповідно до методики, представленої у прикладі 4 вище, у реакції брав участь 4-хлоркатехін, внаслідок чого була одержана суміш (2S)-С-(7хлор-2,3-дигідробензо[1,4]діоксин-2-іл)метиламіну і (2S)-C-(6-хлор-2,3-дигідробензо[1,4]діоксин-2іл)метиламіну (приблизно зі співвідношенням 3:1 6-хлор-:7-хлорізомерів, за даними ОФ-ВЕРХ). Одержану суміш розчиняли у 2-пропанолі (100 мл) і додавали 1 н. НСI у діетиловому ефірі до одержання рН 1,0. Гідрохлорид, що випав в осад, відфільтровували (2,65 г) і перекристалізовували з метанолу/ІПС, одержуючи білі кристали. Одержані білі кристали розділяли між ДХМ і розбавленим розчином NaOH. ДХМ сушили і випарювали у вакуумі, одержуючи очищений (2S)-C-(6-хлор-2,3дигідробензо[1,4]діоксин-2-іл)метиламін у вигляді масла. [α]D=-67,8(c=1,51, CHCl3). Одержане масло (7,75 ммоль) і сульфамід (1,50 г, 15,5 ммоль) змішували у діоксані (50 мл) і кип'ятили зі зворотним холодильником протягом 2,0 год., після чого суміш охолоджували до кімнатної температури і випарювали у вакуумі, одержую 33 чи тверду речовину. Продукт очищали на флешколонці, використовуючи ДХМ/метанол 20:1, одержуючи вказану у заголовку сполуку у вигляді білої твердої речовини. 1 МС 277 (М- ) [α]D=-59,9°(c=1,11, M) 1 H-ЯМР (CDCI3) δ: 6,90 (д, J=2,2 Гц, 1Н), 6,81 (м, 2Н), 4,76 (м, 1Н), 4,55 (с, 2Н), 4,40 (м, 1Н), 4,29 (дд, J=2,4, 11,5 Гц, 1Н), 4,05 (дд, J=7,1, 11,5 Гц, 1Н), 3,45 (м, 2Н). Елементний аналіз: Розрахунковий склад: С, 38,78; Η, 3,98; Ν, 10,05 Одержаний склад: С, 38,80; Η, 3,67; Ν, 9,99. Фільтрати кристалізованого гідрохлориду (2S)С-(6-хлор-2,3-дигідробензо[1,4]діоксин-2іл)метиламіну, одержаного раніше, виділяли (співвідношення 6-хлор-:7-хлорізомерів приблизно 1:1) і випарювали у вакуумі, внаслідок чого одержували тверду речовину, яку розділяли між ДХМ (200 мл) і розбавленим розчином NaOH (0,5 Μ, 50 мл). Розчин ДХМ промивали один раз насиченим розчином солі, сушили (Na2SO4) і випарювали у вакуумі, внаслідок чого одержували масло, яке очищали за допомогою обернено-фазової ВЕРХ (10-50% ацетонітрилу з 0,16% ТФА у воді і 0,20% ТФА), одержуючи (2S)-С-(7-хлор-2,3дигідробензо[1,4]діоксин-2-іл)метиламін у вигляді залишку. Одержаний залишок змішували з сульфамідом (0,90 г, 9,4 ммоль) у діоксані (25 мл) і кип'ятили зі зворотним холодильником протягом 2,5 год., після чого охолоджували до кімнатної температури і випарювали у вакуумі, одержуючи масло. Масло очищали за допомогою колонкової флешхроматографії з використанням ДХМ/метанол 10:1, одержуючи (2S)-(-)-N-(7-xлop-2,3дигідробензо[1,4]діоксин-2-ілметил)сульфамід у вигляді білої твердої речовини. 1 МС 277 (М- ) 1 H-ЯМР (CDCI3/CD3OD) δ: 6,88 (д, J=0,7 Гц, 1Н), 6,81 (м, 2Н), 4,37 (м, 1Н), 4,30 (дд, J=2,3, 11,6 Гц, 1Н), 4,04 (дд, J=7,0, 11,6 Гц, 1Н), 3,38 (м, 2Н). Приклад 8 Хроман-2-ілметилсульфамід (сполука № 10) Хроман-2-карбонову кислоту (4,5 г, 25 ммоль) і ГБТ (3,86 г, 25 ммоль) змішували у ДХМ (40 мл) і ДМФА (10 мл). Диметиламінопропілетилкарбодіімід (ЕДК, 4,84 г, 25 ммоль) додавали при кімнатній температурі, після чого реакційну суміш перемішували протягом 30 хвилин. Додавали гідроксид амонію (2,26 мл, 33,4 ммоль) і реакційну суміш перемішували протягом 16 годин. Реакційну суміш розбавляли ДХМ (50 мл) і водою (50 мл), після чого рН суміші доводили 1 н. НСI до приблизно рН 3,0. ДХМ відділяли, після чого водну фазу двічі екстрагували ДХМ. Об'єднану ДХМ фазу сушили (Na2SO4) і випарювали у вакуумі, внаслідок чого одержували масло, яке очищали за допомогою колонкової флеш-хроматографії (етилацетат), одержуючи масло. 96747 34 Одержане масло (5,35 г, 30 ммоль) у ТГФ (90 мл) перемішували з 1 Μ ЛАГ у ТГФ (36 мл, 36 ммоль), після чого реакційну суміш перемішували при кімнатній температурі протягом 20 годин. Потім реакційну суміш розбавляли водою, перемішували протягом 2 годин, одержаний розчин проціджували, сушили (Na2SO4) і випарювали у вакуумі, одержуючи С-хроман-2-ілметиламін у вигляді маслоподібного аміну. Маслоподібний амін (1,63 г, 10 ммоль) і сульфамід (1,92 г, 20 ммоль) змішували у діоксані (50 мл) і нагрівали до кипіння зі зворотним холодильником протягом 2 годин. Потім розчин охолоджували і випарювали у вакуумі, одержуючи масло, яке очищали за допомогою колонкової хроматографії (ДХМ:метанол - 10:1), внаслідок чого одержували білу тверду речовину. Одержану тверду речовину перекристалізовували з етилацетату/гексану, одержуючи хроман-2ілметилсульфамід у вигляді білої твердої речовини. Т.пл. 100-101°С 1 МС 241 (М- ) Елементний аналіз: Розрахунковий склад: С, 49,57; Н, 5,82; N, 11,56; S, 13,23 Одержаний склад: С, 49,57; Η, 5,80; Ν, 11,75; S, 13,33. Приклад 9 2-(2,3-дигідробензо [1,4]діоксин-2іл)етилсульфамід (сполука № 16) Ціанід калію (2,05 г, 31,5 ммоль) додавали до 2-бромметил-(2,3-дигідробензо[1,4]діоксину) (6,87 г, 30 ммоль) у ДМСО (90 мл) і перемішували при температурі навколишнього середовища протягом 20 годин. Потім реакційну суміш розбавляли водою (250 мл) і двічі екстрагували діетиловим ефіром. Діетиловий ефір промивали водою, потім двічі промивали насиченим розчином солі, сушили (Na2SO4) і випарювали у вакуумі, одержуючи 2ціанометил-(2,3-дигідробензо[1,4]діоксин) у вигляді білої твердої речовини. 1 Н-ЯМР (CDCI3) δ: 6,89 (м, 4Н), 4,50 (м, 1Н), 4,31 (дд, J=2,3, 11,5 Гц, 1Н), 4,08 (дд, J=6,2, 11,6 Гц, 1Н), 2,78 (д, J=6,1, Гц, 2Н). 2-ціанометил-(2,3-дигідробензо[1,4]діоксин) розчиняли у ТГФ (50 мл), після чого додавали 1 Μ ВН3 у ТГФ (80 мл, 80 ммоль) і реакційну суміш кип'ятили зі зворотним холодильником протягом 5 годин, потім перемішували при температурі навколишнього середовища протягом 16 годин. При охолоджуванні на льодяній бані, рН доводили до 1,0 за допомогою 2 н. НСI. Потім реакційну суміш перемішували протягом 1 години при кімнатній температурі, після чого випарювали у вакуумі, одержуючи масло. Масло розділяли між 3 н. NaOH і діетиловим ефіром, розчин діетилового ефіру промивали насиченим розчином солі, сушили (Na2SO4) і випарювали у вакуумі, одержуючи неочищений 2-(2,3-дигідробензо[1,4]діоксин-2іл)етиламін. 35 + МС (М+Н) 180. Неочищений 2-(2,3-дигідробензо[1,4]діоксин-2іл)етиламін у діоксані (100 мл) змішували з сульфамідом (3,0 г, 31 ммоль) і нагрівали до кипіння зі зворотним холодильником протягом 2 годин. Потім розчин охолоджували і випарювали у вакуумі, одержуючи помаранчевий залишок, який очищали за допомогою колонкової хроматографії (ДХМ:МеОН - 10:1), одержуючи білу тверду речовину. Тверду речовину перекристалізовували з ДХМ, одержуючи вказану у заголовку сполуку у вигляді твердої речовини. 1 МС (М- ) 257 Т.пл. 101-103°С (розкл.) 1 Н-ЯМР (CDCI3) δ: 6,86 (м, 4Н), 4,70 (м, 1Н), 4,52 (с, 2Н), 4,30 (м, 2Н), 3,94 (дд, J=7,4, 11,3 Гц, 1Н), 3,43 (дд, J=6,4, 12,9 Гц, 2Н), 1,94 (дд, J=6,5, 12,9, 2Н). Елементний аналіз: Одержаний склад: С, 46,48; Н, 5,60; N, 10,81; S, 12,41 Розрахунковий склад: С, 46,50; Н, 5,46; N, 10,85; S, 12,41. Приклад 10 (2S)-(-)-N-(6,7-дихлор-2,3дигідробензо[1,4]діоксин-2-ілметил)сульфамід (сполука № 29) 4,5-дихлоркатехін (8,6 г, 48 ммоль) і карбонат калію (6,64 г, 48 ммоль) перемішували у ДМФА (200 мл). Потім додавали (2R)-гліцидилтозилат (9,12 г, 40 ммоль), після чого реакційну суміш перемішували при 60°С протягом 24 годин. Реакційну суміш охолоджували до кімнатної температури, і потім розбавляли льодяною водою (600 мл) і екстрагували діетиловим ефіром (4 рази). Об'єднаний органічний розчин промивали 3 рази 10%-им розчином карбонату калію, двічі насиченим розчином солі, сушили (MgSO4) і випарювали у вакуумі, одержуючи в'язке масло, що являє собою (2S)-2-(6,7дихлор-2,3-дигідробензо[1,4]діоксин)метанол. Маслоподібний (2S)-2-(6,7-дихлор-2,3дигідробензо[1,4]діоксин)метанол (6,4 г, 27 ммоль) розчиняли у піридині (50 мл), охолодженому до 0°С. Потім додавали п-толуолсульфонілхлорид (5,2 г, 27 ммоль), після чого реакційну суміш перемішували при кімнатній температурі протягом 20 годин. Реакційну суміш розбавляли діетиловим ефіром і 1 н. НСI (750 мл), після чого органічний шар відділяли і промивали 2 рази 1 н. НСI (250 мл), один раз водою (150 мл), двічі насиченим розчином солі, сушили (MgSO4) і випарювали у вакуумі, внаслідок чого одержували (2S)-6,7-дихлор2,3-дигідробензо[1,4]діоксин-2-ілметиловий ефір толуол-4-сульфонової кислоти у вигляді світложовтої твердої речовини. 1 H-ЯМР (CDCI3) δ: 7,79 (д, J=8,3 Гц, 2Н), 7,36 (д, J=8,0 Гц, 2Н), 6,94 (с, 1Н), 6,83 (с, 1Н), 4,37 (м, 1Н), 4,2 (м, 3Н), 4,03 (дд, J=6,3, 11,7 Гц, 1Н), 2,47 (с, 3Н). (2S)-6,7-дихлор-2,3-дигідробензо[1,4]діоксин-2ілметиловий ефір толуол-4-сульфонової кислоти 96747 36 (8,0 г, 20,5 ммоль) змішували з фталімідом калію (6,1 г, 33 ммоль) у ДМФА (75 мл) і нагрівали до кипіння зі зворотним холодильником протягом 1 години, охолоджували до кімнатної температури і вливали у воду, що енергійно перемішується (0,5 л), і потім перемішували 30 хв. Білу тверду речовину відфільтровували і промивали декілька разів водою, 2%-им розчином NaOH, і знову водою, і потім сушили на повітрі, одержуючи (2S)-2-(6,7дихлор-2,3-дигідробензо[1,4]діоксин-2ілметил)ізоіндол-1,3-діон (6,0 г, 80%) у вигляді білої порошкоподібної речовини. Білу порошкоподібну речовину змішували з гідразином (1,06 г, 33 ммоль) в ЕtOН (80 мл) і нагрівали при кип'ятінні зі зворотним холодильником протягом 2 годин, і потім охолоджували до кімнатної температури. Потім додавали 1 н. НСI, доводячи рН реакційної суміші до 1,0, після чого реакційну суміш перемішували протягом 15 хвилин. Білу тверду речовину відфільтровували і промивали свіжим ЕtOН (осад видаляли), після чого фільтрат випарювали у вакуумі, одержуючи тверду речовину, яку потім розділяли між діетиловим ефіром і водним розчином NaOH. Розчин діетилового ефіру сушили (Na2SO4) і випарювали у вакуумі, одержуючи в'язке масло, що являє собою (2S)-2амінометил-(6,7-дихлор-2,3дигідробензо[1,4]діоксин). 1 Н-ЯМР (CDCI3) δ: 6,98 (с, 1Н), 6,96 (с, 1Н), 4,25 (дд, J=2,0, 11,2 Гц, 1Н), 4,15 (м, 1Н), 4,0 (м, 1Н), 2,97 (д, J=5,5 Гц, 2Н). Частину одержаного масла (3,8 г, 16 ммоль) і сульфамід (3,1 г, 32,4 ммоль) кип'ятили зі зворотним холодильником у діоксані (100 мл) протягом 2 годин, і одержаний у результаті неочищений продукт очищали за допомогою колонкової флешхроматографії (ДХМ:МеОН - 20:1), одержуючи вказану у заголовку сполуку у вигляді білої твердої речовини, яку потім перекристалізовували з етилацетату/гексану, внаслідок чого вказану у заголовку сполуку одержували у вигляді білої кристалічної речовини. МС [М-Н] 311,0 Т.пл. 119-121°С [α]D=-53,4° (c=1,17, M) 1 Н-ЯМР (ДМСO-d6) δ: 7,22 (с, 1Н), 7,20 (с, 1Н), 6,91 (шир.с, 1Н), 6,68 (шир.с, 2Н), 4,35 (м, 2Н), 4,05 (дд, J=6,5, 11,5 Гц, 1Н), 3,15 (м, 2Н). Елементний аналіз: Одержаний склад: С, 34,52; Η, 3,22; Ν, 8,95; СІ, 22,64; S, 10,24 Розрахунковий склад: С, 34,64; Η, 2,68; Ν, 8,87; СІ, 22,94; S, 10,35. Приклад 11 (25)-(-)-N-(7-аміно-2,3дигідробензо[1,4]діоксин-2-ілметил)сульфамід (сполука № 36) (2S)-(-)-N-(2,3-дигідро-7-нітробензо[1,4]діоксин2-ілметил)сульфамід (1,2 г, 4,15 ммоль) одержували з 4-нітрокатехіну відповідно до методики, представленої у прикладі 4. Потім (2S)-(-)-N-(2,3 37 96747 дигідро-7-нітробензо[1,4]діоксин-2ілметил)сульфамід змішували з 10%-им розчином Pd/C у метанолі (120 мл) і струшували в атмосфері водню (268,9 кПа) при кімнатній температурі протягом 3 годин. Тверді частинки відфільтровували і промивали 10%-им Μ у ДХМ, після чого фільтрат випарювали у вакуумі, одержуючи неочищений продукт. Неочищений продукт розчиняли в 0,2 н. НСI (25 мл), заморожували і ліофілізували, одержуючи вказану у заголовку сполуку, у вигляді білої пластівчастої речовини, у формі відповідного гідрохлориду. + МС (М+Н) 260 1 Н-ЯМР (ДМСО-d6) δ: 10,2 (шир.с, 3Н), 6,86 (м, 1Н), 6,85 (с, 1Н), 6,74 (дд, J=2,5, 8,4 Гц, 1Н), 4,22 (м, 2Н), 3,88 (дд, J=6,7, 11,4 Гц, 1Н), 3,04 (м, 2Н). Приклад 12 (2S)-(-)-N-(7-метил-2,3дигідробензо[1,4]діоксин-2-ілметил)сульфамід (сполука № 19) Вказану у заголовку сполуку одержували відповідно до методики, описаної у прикладі 4 вище, з використанням як вихідної сполуки 4метилкатехіну, внаслідок чого одержували білу тверду речовину, яку перекристалізовували з етилацетату/гексану, одержуючи вказану у заголовку сполуку у вигляді білої твердої речовини. МС [М-Н] 257 1 Н-ЯМР (CDCI3) δ: 6,76 (м, 1Н), 6,66 (м, 2Н), 4,80 (м, 1Н), 4,57 (шир.с, 1Н), 4,40 (м, 1Н), 4,28 (м, 1Н), 4,03 (дд, J=6,9, 11,4 Гц, 1Н), 3,45 (м, 2Н), 2,25 (с, 3Н). Елементний аналіз: Розрахунковий склад: С, 46,50; Н, 5,46; N, 10,85; S, 12,41 Одержаний склад: С, 46,65; Н, 5,60; N, 10,84; S, 12,61. Приклад 13 Набір CellTiter-Glow®/життєздатність клітин у тесті in vitro Тест проводили відповідно до методики, прикладеної до набору, одержаного від Promega (дивіться додаток у кінці заявки). Культури клітин готували наступним чином. Культури дисоційованих гіпокампальних і коркових клітин культури одержували від ембріонів щурів 38 18-денного розвитку. Ембріони видаляли за допомогою кесаревого розтину у вагітних самок (Харлан Спраг-Доулі), анестезованих галотаном відповідно до правил умертвіння AVMA. Після обезголовлювання у щурят видаляли мозки, які потім вміщували у буферний сольовий розчин Хенка (1xHBSS; Gibco, Rockville, MD). Гіпокампи і кору вирізали і об'єднували у пул відповідно до типу тканини. Тканину обробляли трипсином протягом 15 хв. (1 мг/мл трипсин-HBSS; Worthington, Lakewood, NJ), відмивали свіжим HBSS, витримували в інгібіторі трипсину (1 мг/мл; Sigma, St.Louis, МО) протягом 5 хвилин, знову відмивали свіжим HBSS, і потім суспендували в 1 мл чистого HBSS оплавленою скляною піпеткою. Дисоційовані клітини висівали у кількості 10000 клітин на ямку у 96ямковий планшет, покритий полі-D-лізином, (BD BioScience, Bedford, MA), що містить по 100 мкл на ямку мінімального середовища Ігла (MEM; Gibco) з додаванням 26 мМ NaHCO3 (Sigma), 40 мМ глюкози (Sigma), 20 мМ KСl (Sigma), 1 мМ пірувату натрію (Sigma), 10% (об./об.) термоінактивованої ембріональної бичачої сироватки (Hyclone, Logan, UT), і також 0,001% гентаміцину сульфату (Sigma) (pH 7,4). Безсироваткові культури висівали і вирощували у середовищі Neurobasal плюс домішка В27 (Gibco). Перед дослідною обробкою клітини інкубували протягом 24 годин у вологому інкубаторі при 37°С в атмосфері з 5% СО2. Сполуки, що тестуються, готували наступним чином: 10 мМ стокового розчину кожної сполуки у ДМСО розбавляли 1:50 у DPBS, одержуючи стоковий розчин з кінцевою концентрацією 200 мкМ. Потім стоковий розчин знову розбавляли у DPBS, одержуючи кінцеву концентрацію сполуки 0,1, 1 і 120 мкМ у кожній 100-мкл ямці. У кожну культуральну ямку додавали рівні кількості носія або розбавленої сполуки. Розчин концентрованого 30%-ого перекису водню (Н2О2; Sigma) розбавляли DPBS 1:100, одержуючи 3 мМ стоковий розчин. П'ять мікролітрів носія або стокового розчину Н2О2 додавали у кожну 100-мкл ямку, одержуючи кінцеву концентрацію 150 мкМ. Сполуку № 8 тестували відповідно до методики, описаної у даному описі, одержані результати наведені у таблицях 4 і 5 нижче. Потрібно зазначити, що при одержанні наведених нижче даних, тест з кожним планшетом повторювали три рази (загалом n=9). Таблиця 4 Культури клітин гіпокампу щура, інсульт викликаний 150 мкМ Н 2О2 Носій Планшет 1 Планшет 2 Планшет 3 Середнє Стандартне відхилення 0,5 0,6 0,5 0,5 0,1 Сполука № 8 0,1 мкМ 24 26 24 25** 1 Сполука № 8 1 мкМ 16 17 17 17 0,6 Сполука № 8 10 мкМ 10 14 15 13 3 39 96747 40 Таблиця 5 Культури клітин кори мозку щура, інсульт викликаний 150 мкМ Н 2О2 Носій Планшет 1 Планшет 2 Планшет 3 Середнє Стандартне відхилення 1,2 1 0,8 1 0,2 Сполука № 8 0,1 мкМ 28 64 97 63* 35 Сполука № 8 1 мкМ 19 51 38 36 16 Сполука № 8 10 мкМ 10 18 51 26 22 Критерій множинного порівняння Крускал-Валліса з подальшим тестом Данна: *р
ДивитисяДодаткова інформація
Назва патенту англійськоюUse of benzo-fused heterocycle sulfamide derivatives as neuroprotective agents
Автори англійськоюSmith-Swintosky, Virginia L., Reitz, Allen B.
Назва патенту російськоюПрименение бензоконденсированных гетероциклических сульфамидных производных как нейропротективных агентов
Автори російськоюСмит-Свинтоски Вирджиния Л., Рейтц Аллен Б.
МПК / Мітки
МПК: A61P 25/14, A61P 25/02, A61P 25/08, A61K 31/353, A61P 25/16, A61K 31/357
Мітки: похідних, застосування, нейропротективних, агентів, бензоконденсованих, гетероциклічних, сульфамідних
Код посилання
<a href="https://ua.patents.su/20-96747-zastosuvannya-benzokondensovanikh-geterociklichnikh-sulfamidnikh-pokhidnikh-yak-nejjroprotektivnikh-agentiv.html" target="_blank" rel="follow" title="База патентів України">Застосування бензоконденсованих гетероциклічних сульфамідних похідних як нейропротективних агентів</a>
Попередній патент: Спосіб і пристрій для різання пластичного матеріалу
Наступний патент: Застосування похідних бензоконденсованого гетероциклічного сульфаміду для лікування ожиріння
Випадковий патент: 2-(флуорениліден-9'-гідразоно)-5-(3"-метоксі-4"-оксібензиліден)-тіазолідон-4, що виявляє антивірусну та фунгіцидну дію












