Застосування бензоконденсованих гетероциклічних сульфамідних похідних для зниження рівнів ліпідів і глюкози у крові
Формула / Реферат
1. Спосіб лікування пов'язаного з глюкозою розладу, що включає введення потребуючому цього суб'єкту терапевтично ефективної кількості сполуки формули (I)
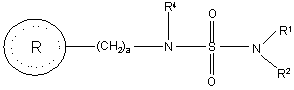 , (I)
, (I)
де
R1 і R2 кожний незалежно вибраний з групи, що складається з атома водню і нижчого алкілу;
R4 вибраний з групи, що складається з атома водню і нижчого алкілу;
а дорівнює цілому числу від 1 до 2;
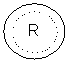 вибраний з групи, що складається з
вибраний з групи, що складається з
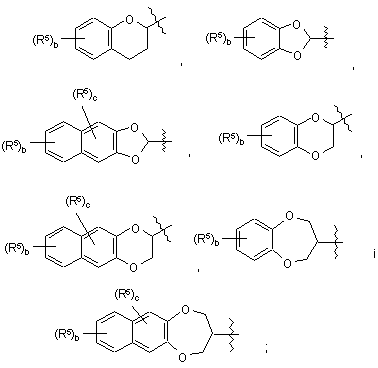
де b дорівнює цілому числу від 0 до 4; і де с дорівнює цілому числу від 0 до 2;
кожний R5 незалежно вибраний з групи, що складається з галогену, нижчого алкілу і нітро;
за умови, що, якщо 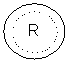 являє собою
являє собою
 або
або 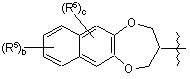 ,
,
то а дорівнює 1;
або її фармацевтично прийнятної солі.
2. Спосіб за п. 1, де
R1 і R2 кожний незалежно вибраний з групи, що складається з атома водню і нижчого алкілу;
R4 вибраний з групи, що складається з атома водню і нижчого алкілу;
а дорівнює цілому числу від 1 до 2;
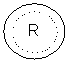 вибраний з групи, що включає
вибраний з групи, що включає

де b дорівнює цілому числу від 0 до 2; і де
с дорівнює цілому числу від 0 до 1;
кожний R5 незалежно вибраний з групи, що складається з галогену, нижчого алкілу і нітро;
за умови, що, якщо 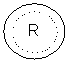 являє собою
являє собою
 або
або  ,
,
то а дорівнює 1;
або їх фармацевтично прийнятної солі.
3. Спосіб за п. 2, де
R1 і R2 кожний незалежно вибраний з групи, що складається з атома водню і нижчого алкілу;
R4 вибраний з групи, що включає атом водню і нижчий алкіл;
а дорівнює цілому числу від 1 до 2;
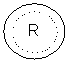 вибраний з групи, що включає
вибраний з групи, що включає
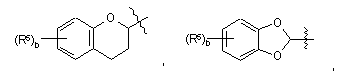
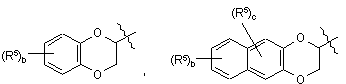 ,
,
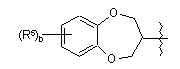 ;
;
де b дорівнює цілому числу від 0 до 2; і де
с дорівнює 0;
кожний R5 незалежно вибраний з групи, що складається з галогену, нижчого алкілу і нітро;
за умови, що, якщо 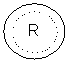 являє собою
являє собою  , то а дорівнює 1;
, то а дорівнює 1;
або їх фармацевтично прийнятної солі.
4. Спосіб за п. 3, де
R1 і R2 кожний незалежно вибраний з групи, що складається з атома водню і нижчого алкілу;
R4 вибраний з групи, що складається з атома водню і метилу;
а дорівнює цілому числу від 1 до 2;
 вибраний з групи, що складається з:
вибраний з групи, що складається з:
2-(2,3-дигідробензо[1,4]діоксинілу), 2-(бензо[1,3]діоксолілу), 2-(3,4-дигідро-2Н-бензо[1,4]діоксепінілу), 2-(2,3-дигідробензо[1,4]діоксинілу), 2-(6-хлор-2,3-дигідробензо[1,4]діоксинілу), 2-(6-фтор-2,3-дигідробензо[1,4]діоксинілу), 2-(хроманілу), 2-(5-фтор-2,3-дигідробензо[1,4]діоксинілу), 2-(7-хлор-2,3-дигідробензо[1,4]діоксинілу), 2-(6-хлорбензо[1,3]діоксолілу), 2-(7-нітро-2,3-дигідробензо[1,4]діоксинілу), 2-(7-метил-2,3-дигідробензо[1,4]діоксинілу), 2-(5-хлор-2,3-дигідробензо[1,4]діоксинілу), 2-(6-бром-2,3-дигідробензо[1,4]діоксинілу), 2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксинілу), 2-(8-хлор-2,3-дигідробензо[1,4]діоксинілу), 2-(2,3-дигідронафто[2,3-b][1,4]діоксинілу) і 2-(4-метилбензо[1,3]діоксолілу);
за умови, що, якщо  являє собою 2-(3,4-дигідро-2Н-бензо[1,4]діоксепініл), то а дорівнює 1;
являє собою 2-(3,4-дигідро-2Н-бензо[1,4]діоксепініл), то а дорівнює 1;
або їх фармацевтично прийнятної солі.
5. Спосіб за п. 4, де
R1 і R2 кожний незалежно вибраний з групи, що складається з атома водню і метилу;
R4 вибраний з групи, що складається з атома водню і метилу;
а дорівнює цілому числу від 1 до 2;
 вибраний з групи, що складається з:
вибраний з групи, що складається з:
2-(бензо[1,3]діоксолілу), 2-(2,3-дигідробензо[1,4]діоксинілу), 2-(2,3-дигідробензо[1,4]діоксинілу), 2-(6-хлор-2,3-дигідробензо[1,4]діоксинілу), 2-(7-хлор-2,3-дигідробензо[1,4]діоксинілу), 2-(7-метил-2,3-дигідробензо[1,4]діоксинілу), 2-(6-бром-2,3-дигідробензо[1,4]діоксинілу) і 2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксинілу);
або їх фармацевтично прийнятної солі.
6. Спосіб за п. 1, де сполука формули (І) вибрана з групи, що складається з (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфаміду і його фармацевтично прийнятної солі.
7. Спосіб лікування пов'язаного з глюкозою розладу, що включає введення потребуючому цього суб'єкту терапевтично ефективної кількості сполуки, вибраної з групи, що складається з (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфаміду і його фармацевтично прийнятної солі.
8. Спосіб за п. 1, де пов'язаний з глюкозою розлад вибраний з групи, що включає підвищені рівні глюкози і цукровий діабет типу II.
9. Спосіб за п. 7, де пов'язаний з глюкозою розлад вибраний з групи, що включає підвищені рівні глюкози і цукровий діабет типу II.
10. Спосіб лікування пов'язаного з глюкозою розладу, що включає введення потребуючому цього суб'єкту терапевтично ефективної кількості сполуки формули (II)
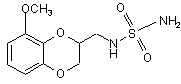 (II)
(II)
або її фармацевтично прийнятної солі.
11. Спосіб лікування пов'язаного з ліпідами розладу, що включає введення потребуючому цього суб'єкту терапевтично ефективної кількості сполуки формули (I)
 , (I)
, (I)
де
R1 і R2 кожний незалежно вибраний з групи, що складається з атома водню і нижчого алкілу;
R4 вибраний з групи, що включає атом водню і нижчий алкіл;
а дорівнює цілому числу від 1 до 2;
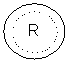 вибраний з групи, що складається з:
вибраний з групи, що складається з:

де b дорівнює цілому числу від 0 до 4; і де
с дорівнює цілому числу від 0 до 2;
кожний R5 незалежно вибраний з групи, що складається з галогену, нижчого алкілу і нітро;
за умови, що, якщо 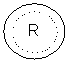 являє собою
являє собою
 або
або  ,
,
то а дорівнює 1;
або її фармацевтично прийнятної солі.
12. Спосіб за п. 11, де
R1 і R2 кожний незалежно вибраний з групи, що складається з атома водню і нижчого алкілу;
R4 вибраний з групи, що складається з атома водню і нижчого алкілу;
а дорівнює цілому числу від 1 до 2;
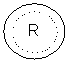 вибраний з групи, що складається з
вибраний з групи, що складається з

де b дорівнює цілому числу від 0 до 2; і де
с дорівнює цілому числу від 0 до 1;
кожний R5 незалежно вибраний з групи, що складається з галогену, нижчого алкілу і нітро;
за умови, що, якщо 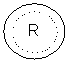 являє собою
являє собою
 або
або  ,
,
то а дорівнює 1;
або їх фармацевтично прийнятної солі.
13. Спосіб за п. 12, де
R1 і R2 кожний незалежно вибраний з групи, що складається з атома водню і нижчого алкілу;
R4 вибраний з групи, що складається з атома водню і нижчого алкілу;
а дорівнює цілому числу від 1 до 2;
 вибраний з групи, що складається з
вибраний з групи, що складається з
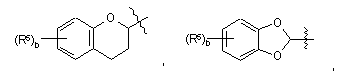
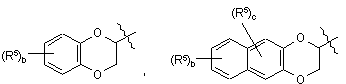 ,
,
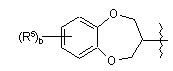 ;
;
де b дорівнює цілому числу від 0 до 2; і де
с дорівнює 0;
кожний R5 незалежно вибраний з групи, що складається з галогену, нижчого алкілу і нітро;
за умови, що, якщо 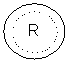 являє собою
являє собою  ,
,
то а дорівнює 1;
або їх фармацевтично прийнятної солі.
14. Спосіб за п. 13, де
R1 і R2 кожний незалежно вибраний з групи, що складається з атома водню і нижчого алкілу;
R4 вибраний з групи, що складається з атома водню і метилу;
а дорівнює цілому числу від 1 до 2;
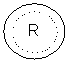 вибраний з групи, що складається з
вибраний з групи, що складається з
2-(2,3-дигідробензо[1,4]діоксинілу), 2-(бензо[1,3]діоксолілу), 2-(3,4-дигідро-2Н-бензо[1,4]діоксепінілу), 2-(2,3-дигідробензо[1,4]діоксинілу), 2-(6-хлор-2,3-дигідробензо[1,4]діоксинілу), 2-(6-фтор-2,3-дигідробензо[1,4]діоксинілу), 2-(хроманілу), 2-(5-фтор-2,3-дигідробензо[1,4]діоксинілу), 2-(7-хлор-2,3-дигідробензо[1,4]діоксинілу), 2-(6-хлорбензо[1,3]діоксолілу), 2-(7-нітро-2,3-дигідробензо[1,4]діоксинілу), 2-(7-метил-2,3-дигідробензо[1,4]діоксинілу), 2-(5-хлор-2,3-дигідробензо[1,4]діоксинілу), 2-(6-бром-2,3-дигідробензо[1,4]діоксинілу), 2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксинілу), 2-(8-хлор-2,3-дигідробензо[1,4]діоксинілу), 2-(2,3-дигідронафто[2,3-b][1,4]діоксинілу) і 2-(4-метилбензо[1,3]діоксолілу);
за умови, що, якщо 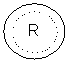 являє собою 2-(3,4-дигідро-2Н-бензо[1,4]діоксепініл), то а дорівнює 1;
являє собою 2-(3,4-дигідро-2Н-бензо[1,4]діоксепініл), то а дорівнює 1;
або їх фармацевтично прийнятної солі.
15. Спосіб за п. 14, де
R1 і R2 кожний незалежно вибраний з групи, що складається з атома водню і метилу;
R4 вибраний з групи, що складається з атома водню і метилу;
а дорівнює цілому числу від 1 до 2;
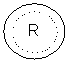 вибраний з групи, що складається з
вибраний з групи, що складається з
2-(бензо[1,3]діоксолілу), 2-(2,3-дигідробензо[1,4]діоксинілу), 2-(2,3-дигідробензо[1,4]діоксинілу), 2-(6-хлор-2,3-дигідробензо[1,4]діоксинілу), 2-(7-хлор-2,3-дигідробензо[1,4]діоксинілу), 2-(7-метил-2,3-дигідробензо[1,4]діоксинілу), 2-(6-бром-2,3-дигідробензо[1,4]діоксинілу) і 2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксинілу);
або їх фармацевтично прийнятної солі.
16. Спосіб за п. 11, де сполука формули (І) вибрана з групи, що складається з (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфаміду і його фармацевтично прийнятних солей.
17. Спосіб лікування пов'язаного з ліпідами розладу, що включає введення потребуючому цього суб'єкту терапевтично ефективної кількості сполуки, вибраної з групи, що складається з (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфаміду і його фармацевтично прийнятних солей.
18. Спосіб за п. 11, де пов'язаний з ліпідами розлад вибраний з групи, що включає підвищені рівні тригліцеридів і низькі рівні HLD-холестерину.
19. Спосіб за п. 17, де пов'язаний з ліпідами розлад вибраний з групи, що включає підвищені рівні тригліцеридів і низькі рівні HLD-холестерину.
20. Спосіб лікування пов'язаного з ліпідами розладу, що включає введення потребуючому цього суб'єкту терапевтично ефективної кількості сполуки формули (II)
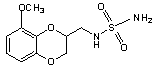 (II)
(II)
або її фармацевтично прийнятної солі.
Текст
1. Спосіб лікування пов'язаного з глюкозою розладу, що включає введення потребуючому цього суб'єкту терапевтично ефективної кількості сполуки формули (I) 3 94077 4 а дорівнює цілому числу від 1 до 2; R за вибраний з групи, що включає умови, R що, якщо являє собою O O O (R5)b (R5)b O O , або їх фармацевтично прийнятної солі. 4. Спосіб за п. 3, де R1 і R2 кожний незалежно вибраний з групи, що складається з атома водню і нижчого алкілу; R4 вибраний з групи, що складається з атома водню і метилу; а дорівнює цілому числу від 1 до 2; , (R5)c O O (R5)b (R5)b , O , O (R5)c R O O (R5)b (R5)b i O , O (R5)c O (R5)b ; O де b дорівнює цілому числу від 0 до 2; і де с дорівнює цілому числу від 0 до 1; кожний R5 незалежно вибраний з групи, що складається з галогену, нижчого алкілу і нітро; R за умови, що, якщо являє собою (R5)c O O (R5)b 2-(2,3-дигідробензо[1,4]діоксинілу), 2(бензо[1,3]діоксолілу), 2-(3,4-дигідро-2Нбензо[1,4]діоксепінілу), 2-(2,3дигідробензо[1,4]діоксинілу), 2-(6-хлор-2,3дигідробензо[1,4]діоксинілу), 2-(6-фтор-2,3дигідробензо[1,4]діоксинілу), 2-(хроманілу), 2-(5фтор-2,3-дигідробензо[1,4]діоксинілу), 2-(7-хлор2,3-дигідробензо[1,4]діоксинілу), 2-(6хлорбензо[1,3]діоксолілу), 2-(7-нітро-2,3дигідробензо[1,4]діоксинілу), 2-(7-метил-2,3дигідробензо[1,4]діоксинілу), 2-(5-хлор-2,3дигідробензо[1,4]діоксинілу), 2-(6-бром-2,3дигідробензо[1,4]діоксинілу), 2-(6,7-дихлор-2,3дигідробензо[1,4]діоксинілу), 2-(8-хлор-2,3дигідробензо[1,4]діоксинілу), 2-(2,3дигідронафто[2,3-b][1,4]діоксинілу) і 2-(4метилбензо[1,3]діоксолілу); за умови, що, якщо O OO O , O O (R5)b 5 (R5(R )b )b O O (R5) O , O O , , b O , , c (R5)(R5)c O c OO (R5)b , O , O O , (R5)b 5) (R O b O O , O (R5)b (R5)b O O O ; де b дорівнює цілому числу від 0 до 2; і де O с дорівнює 0; O кожний R5 незалежно вибраний з групи, що складається з галогену, нижчого алкілу і нітро; (R5)b являє собою 2-(3,4 вибраний з групи, що включає (R5)b (R5 (R5))b b (R5)b (R5) R дигідро-2Н-бензо[1,4]діоксепініл), то а дорівнює 1; або їх фармацевтично прийнятної солі. 5. Спосіб за п. 4, де R1 і R2 кожний незалежно вибраний з групи, що складається з атома водню і метилу; R4 вибраний з групи, що складається з атома водню і метилу; а дорівнює цілому числу від 1 до 2; R (R5)b вибраний з групи, що складається з: (R5)b O O або , то а дорівнює 1; або їх фармацевтично прийнятної солі. 3. Спосіб за п. 2, де R1 і R2 кожний незалежно вибраний з групи, що складається з атома водню і нижчого алкілу; R4 вибраний з групи, що включає атом водню і нижчий алкіл; а дорівнює цілому числу від 1 до 2; R , то а дорівнює 1; (R5)b вибраний з групи, що складається з: 2-(бензо[1,3]діоксолілу), 2-(2,3дигідробензо[1,4]діоксинілу), 2-(2,3дигідробензо[1,4]діоксинілу), 2-(6-хлор-2,3дигідробензо[1,4]діоксинілу), 2-(7-хлор-2,3дигідробензо[1,4]діоксинілу), 2-(7-метил-2,3дигідробензо[1,4]діоксинілу), 2-(6-бром-2,3дигідробензо[1,4]діоксинілу) і 2-(6,7-дихлор-2,3дигідробензо[1,4]діоксинілу); або їх фармацевтично прийнятної солі. 6. Спосіб за п. 1, де сполука формули (І) вибрана з групи, що складається з (2S)-(-)-N-(6-хлор-2,3дигідробензо[1,4]діоксин-2-ілметил)сульфаміду і його фармацевтично прийнятної солі. 7. Спосіб лікування пов'язаного з глюкозою розладу, що включає введення потребуючому цього суб'єкту терапевтично ефективної кількості сполу 5 94077 ки, вибраної з групи, що складається з (2S)-(-)-N(6-хлор-2,3-дигідробензо[1,4]діоксин-2ілметил)сульфаміду і його фармацевтично прийнятної солі. 8. Спосіб за п. 1, де пов'язаний з глюкозою розлад вибраний з групи, що включає підвищені рівні глюкози і цукровий діабет типу II. 9. Спосіб за п. 7, де пов'язаний з глюкозою розлад вибраний з групи, що включає підвищені рівні глюкози і цукровий діабет типу II. 10. Спосіб лікування пов'язаного з глюкозою розладу, що включає введення потребуючому цього суб'єкту терапевтично ефективної кількості сполуки формули (II) O OCH3 O NH2 S N H 6 за умови, що, якщо R являє собою (R5)c O O (R5)b (R5)b O O або , то а дорівнює 1; або її фармацевтично прийнятної солі. 12. Спосіб за п. 11, де R1 і R2 кожний незалежно вибраний з групи, що складається з атома водню і нижчого алкілу; R4 вибраний з групи, що складається з атома водню і нижчого алкілу; а дорівнює цілому числу від 1 до 2; R O вибраний з групи, що складається з O (II) або її фармацевтично прийнятної солі. 11. Спосіб лікування пов'язаного з ліпідами розладу, що включає введення потребуючому цього суб'єкту терапевтично ефективної кількості сполуки формули (I) R4 O (CH2)a O , O N S O O N (R5)b (R5)b , O R2 O , (I) де R1 і R2 кожний незалежно вибраний з групи, що складається з атома водню і нижчого алкілу; R4 вибраний з групи, що включає атом водню і нижчий алкіл; а дорівнює цілому числу від 1 до 2; , (R5)c R1 R O (R5)b (R5)b O , (R5)c O O (R5)b (R5)b i O , O (R5)c O R вибраний з групи, що складається з: (R5)b ; O O де b дорівнює цілому числу від 0 до 2; і де с дорівнює цілому числу від 0 до 1; кожний R5незалежно вибраний з групи, що складається з галогену, нижчого алкілу і нітро; O (R5)b (R5)b O , , (R5)c за умови, що, якщо O O (R5)b , O O , (R5)c (R5)b O , O i (R5)c O (R5)b O (R5)c O (R5)b O O (R5)b являє собою O (R5)b O R (R5)b ; де b дорівнює цілому числу від 0 до 4; і де с дорівнює цілому числу від 0 до 2; кожний R5 незалежно вибраний з групи, що складається з галогену, нижчого алкілу і нітро; O або , то а дорівнює 1; або їх фармацевтично прийнятної солі. 13. Спосіб за п. 12, де R1 і R2 кожний незалежно вибраний з групи, що складається з атома водню і нижчого алкілу; R4 вибраний з групи, що складається з атома водню і нижчого алкілу; а дорівнює цілому числу від 1 до 2; R вибраний з групи, що складається з 7 94077 OO O O , , дигідронафто[2,3-b][1,4]діоксинілу) метилбензо[1,3]діоксолілу); O O (R5(R5)b )b (R )b (R55)b , , (R5)(R5)c c OO (R5))b (R5 b O , , O O (R5(R5) )b O O b O , O (R5)b (R5) O b O ; O де b дорівнює цілому числу від 0 до 2; і де с дорівнює 0; кожний R5 незалежно вибраний з групи, що складається з галогену, нижчого алкілу і нітро; за умови, що, якщо R являє собою O (R5)b O , то а дорівнює 1; або їх фармацевтично прийнятної солі. 14. Спосіб за п. 13, де R1 і R2 кожний незалежно вибраний з групи, що складається з атома водню і нижчого алкілу; R4 вибраний з групи, що складається з атома водню і метилу; а дорівнює цілому числу від 1 до 2; R 8 вибраний з групи, що складається з 2-(2,3-дигідробензо[1,4]діоксинілу), 2(бензо[1,3]діоксолілу), 2-(3,4-дигідро-2Нбензо[1,4]діоксепінілу), 2-(2,3дигідробензо[1,4]діоксинілу), 2-(6-хлор-2,3дигідробензо[1,4]діоксинілу), 2-(6-фтор-2,3дигідробензо[1,4]діоксинілу), 2-(хроманілу), 2-(5фтор-2,3-дигідробензо[1,4]діоксинілу), 2-(7-хлор2,3-дигідробензо[1,4]діоксинілу), 2-(6хлорбензо[1,3]діоксолілу), 2-(7-нітро-2,3дигідробензо[1,4]діоксинілу), 2-(7-метил-2,3дигідробензо[1,4]діоксинілу), 2-(5-хлор-2,3дигідробензо[1,4]діоксинілу), 2-(6-бром-2,3дигідробензо[1,4]діоксинілу), 2-(6,7-дихлор-2,3дигідробензо[1,4]діоксинілу), 2-(8-хлор-2,3дигідробензо[1,4]діоксинілу), 2-(2,3 Дана заявка заявляє про пріоритет попередньої заявки США 60/751677 від 19 грудня 2005, включеної у повному об'ємі у даний опис як посилання. Даний винахід стосується використання бензоконденсованих гетероциклічних сульфамідних похідних з метою зниження рівнів ліпідів, зниження за умови, що, якщо R і 2-(4 являє собою 2-(3,4 дигідро-2Н-бензо[1,4]діоксепініл), то а дорівнює 1; або їх фармацевтично прийнятної солі. 15. Спосіб за п. 14, де R1 і R2 кожний незалежно вибраний з групи, що складається з атома водню і метилу; R4 вибраний з групи, що складається з атома водню і метилу; а дорівнює цілому числу від 1 до 2; R вибраний з групи, що складається з 2-(бензо[1,3]діоксолілу), 2-(2,3дигідробензо[1,4]діоксинілу), 2-(2,3дигідробензо[1,4]діоксинілу), 2-(6-хлор-2,3дигідробензо[1,4]діоксинілу), 2-(7-хлор-2,3дигідробензо[1,4]діоксинілу), 2-(7-метил-2,3дигідробензо[1,4]діоксинілу), 2-(6-бром-2,3дигідробензо[1,4]діоксинілу) і 2-(6,7-дихлор-2,3дигідробензо[1,4]діоксинілу); або їх фармацевтично прийнятної солі. 16. Спосіб за п. 11, де сполука формули (І) вибрана з групи, що складається з (2S)-(-)-N-(6-хлор-2,3дигідробензо[1,4]діоксин-2-ілметил)сульфаміду і його фармацевтично прийнятних солей. 17. Спосіб лікування пов'язаного з ліпідами розладу, що включає введення потребуючому цього суб'єкту терапевтично ефективної кількості сполуки, вибраної з групи, що складається з (2S)-(-)-N(6-хлор-2,3-дигідробензо[1,4]діоксин-2ілметил)сульфаміду і його фармацевтично прийнятних солей. 18. Спосіб за п. 11, де пов'язаний з ліпідами розлад вибраний з групи, що включає підвищені рівні тригліцеридів і низькі рівні HLD-холестерину. 19. Спосіб за п. 17, де пов'язаний з ліпідами розлад вибраний з групи, що включає підвищені рівні тригліцеридів і низькі рівні HLD-холестерину. 20. Спосіб лікування пов'язаного з ліпідами розладу, що включає введення потребуючому цього суб'єкту терапевтично ефективної кількості сполуки формули (II) O OCH3 O N H NH2 S O O (II) або її фармацевтично прийнятної солі. рівнів глюкози у крові, поліпшення глікемічного контролю, лікування цукрового діабету типу II, метаболічного синдрому, гіперглікемії і споріднених розладів. Цукровий діабет - це медичне позначення наявності підвищеного рівня глюкози у крові. У людей з діабетом або не продукується інсулін, або 9 продукується дуже мало інсуліну, або вони не реагують на інсулін, що веде до збільшення кількості глюкози у крові. Найбільш загальною формою діабету є діабет типу II, позначений як діабет дорослих або інсуліннезалежний діабет (NIDDM), який може пояснювати >90% випадків діабету у дорослих. Однак, оскільки все більше і більше молодих людей мають надлишки ваги або ожиріння, діабет типу II стає більш поширеним серед підлітків і дітей. Діабет можна також визначити як гестаційний діабет, діабет типу 1 або аутоімунний діабет, одного разу позначений як ювенільний діабет і діабет типу 1½ , що також називають латентним аутоімунним діабетом дорослих або LADA. Діабет може виникати внаслідок шкідливих традицій харчування або нестачі фізичної активності (наприклад, сидячого способу життя), генетичних мутацій, ураження підшлункової залози, під впливом ліків (наприклад, СНІД-терапії) або хімічних препаратів (наприклад, стероїдів) або захворювання (наприклад, кістозного фіброзу), синдрому Дауна, синдрому Кушинга. Два рідких типи генетичних дефектів, що ведуть до діабету, називають діабет молодих, що з'являється у період статевого дозрівання (MODY) і атипічний цукровий діабет (ADM). Цукровий діабет типу II (інсуліннезалежний цукровий діабет або NIDDM) являє собою метаболічний розлад, що включає порушення регуляції метаболізму глюкози і резистентність до інсуліну, і довгострокові ускладнення, що зачіпають очі, нирки, нерви і кровоносні судини. Цукровий діабет типу II звичайно розвивається у людей у дорослому віці (у середині життя або пізніше) і описаний як нездатність організму виробляти досить інсуліну (аномальна секреція інсуліну) або нездатність організму ефективно використовувати інсулін (резистентність до дії інсуліну в уражених органах і тканинах). Частіше пацієнти, які страждають від цукрового діабету типу II, мають відносний дефіцит інсуліну. Тобто, у цих пацієнтів рівні інсуліну у плазмі відповідають значенням від нормальних до високих в абсолютних значеннях, хоча вони нижчі, ніж прогнозовані для рівня глюкози, яка присутня у плазмі. Цукровий діабет типу II характеризується наступними клінічними ознаками або симптомами: стійко підвищена концентрація глюкози у плазмі або гіперглікемія; поліурія; полідипсія і/або поліфагія; хронічні мікросудинні ускладнення, такі як ретинопатія, нефропатія і нейропатія; і макросудинні ускладнення, такі як гіперліпідемія і гіпертензія, яка може вести до сліпоти, ниркового захворювання на останній стадії, ампутації кінцівок та інфаркту міокарда. Синдром X, який також називають синдромом резистентності до інсуліну (IRS), метаболічним синдромом або метаболічним синдромом X, є розладом, який представляє фактори ризику для розвитку цукрового діабету типу II і серцевосудинного захворювання, включаючи непереносимість глюкози, гіперінсулінемію і резистентність до інсуліну, гіпертригліцеридемію, гіпертензію і ожиріння. Діагностування цукрового діабету типу II включає оцінку симптомів і визначення глюкози у сечі і 94077 10 крові. Визначення рівня глюкози у крові є необхідним для точного діагнозу. Більш конкретно, стандартним використовуваним підходом є визначення рівня глюкози у крові на голодний шлунок. Однак вважається, що пероральний тест толерантності до глюкози (OGTT) є більш чутливим, ніж рівень глюкози у крові на голодний шлунок. Цукровий діабет типу II пов'язаний з погіршеною пероральною толерантністю до глюкози (OGT). Таким чином, OGTT може надати допомогу при діагностуванні цукрового діабету типу II, хоча звичайно не є необхідним для діагнозу діабету (Emancipator K, Am J Clin Pathol 1999 Nov; 112(5):665-74; Type 2 Diabetes Mellitus, Decision Resources Inc., March 2000). OGTT дозволяє оцінити секреторну функцію бета-клітин підшлункової залози і чутливість до інсуліну, що допомагає при діагностуванні цукрового діабету типу II і для оцінки тяжкості або прогресування захворювання (наприклад, Caumo A, Bergman RN, Cobelli С,. J Clin Endocrinol Metab 2000, 85(11):4396-402). Частіше OGTT є надзвичайно корисним для визначення ступеню гіперглікемії у пацієнтів з множинними випадками граничних рівнів глюкози у крові на голодний шлунок, які не мають діагнозу як діабетики. Крім того, OGTT придатний при тестуванні пацієнтів з симптомами цукрового діабету типу II, коли можливий діагноз аномального метаболізму вуглеводів чітко встановлений або спростований. Таким чином, діагностують знижену переносимість глюкози у індивідуумів, які мають рівні глюкози у крові на голодний шлунок нижчі рівнів, необхідних для діагнозу цукрового діабету типу II, але мають реакцію глюкози у плазмі при проведенні OGTT, проміжну між нормальною і характерною для діабетиків. Знижена переносимість глюкози вважається переддіабетичним станом, і знижена переносимість глюкози (як визначають за допомогою OGTT) є строгим прогнозом розвитку цукрового діабету типу II (Haffner SM, Diabet Med 1997 Aug; 14 Suppl 3:S12-8). Цукровий діабет типу II являє собою прогресуюче захворювання, пов'язане зі зниженням функції підшлункової залози і/або іншими процесами, що стосуються інсуліну, посиленими підвищеними рівнями глюкози у плазмі. Таким чином, цукровий діабет типу II звичайно має тривалу переддіабетичну фазу, і різні патофізіологічні механізми можуть вести до патологічної гіперглікемії і зниженої переносимости глюкози, наприклад, аномалій утилізації і ефективності глюкози, дії інсуліну і/або виробництва інсуліну при переддіабетичному стані (Goldberg RB, Med Clin North Am 1998 Jul; 82(4):805-21). Переддіабетичний стан, пов'язаний з непереносимістю глюкози, може також бути пов'язаний зі схильністю до абдомінального ожиріння, резистентності до інсуліну, гіперліпідемії і високого кров'яного тиску, тобто, синдрому X (Groop 1, Forsblom С, Lehtovirta M, Am J Hypertens 1997 Sep; 10(9 Pt 2): 172S-180S; Haffner SM, J Diabetes Complications 1997 Mar-Apr; 11(2):69-76; Beck-Nielsen H, Henriksen JE, Alford F, Hother-Nielson O, Diabet Med 1996 Sep; 13(9 Suppl 6):S78-84). 11 Таким чином, дефектний метаболізм вуглеводів є основним для патогенезу цукрового діабету типу II і зниженої переносимості глюкози (Dinneen SF, Diabet Med 1997 Aug; 14 Suppl 3: S19-24). Дійсно, існує безперервна низка станів від зниженої переносимості глюкози і погіршених показників глюкозрі на голодний шлунок до остаточного цукрового діабету типу II (Ramlo-Halsted ΒΑ, Edelman SV, Prim Care 1999 Dec; 26(4):771-89). Раннє втручання у індивідуумів з ризиком розвитку цукрового діабету типу II, що направляється на зниження патологічної гіперглікемії або погіршеної переносимості глюкози, може попереджати або уповільнювати прогресування до цукрового діабету типу II і пов'язаних ускладнень і/або синдрому X. Отже, шляхом ефективного лікування погіршеної пероральної толерантності до глюкози і/або підвищених рівнів глюкози у крові можна попереджати або інгібувати прогресування розладу до цукрового діабету типу II або синдрому X. Дисліпідемія являє собою групу захворювань, що характеризуються аномальними змінами або рівнями концентрацій ліпопротеїнів і зв'язаних ліпідів, таких як тригліцериди і холестерин, у крові. Ліпіди переносяться з течією крові у формах ліпопротеїнів, що включають, по суті ядро з неполярних молекул, таких як наприклад, тригліцериди і холестериновий складний ефір, оточене оболонкою з амфіпатичних ліпідів, головним чином, фосфоліпідів. Набута гіперліпідемія/гіперліпопротеїнемія розвивається як наслідок дисбалансу харчування, дії лікарських засобів або сполук або захворювання, такого як недостатність щитовидної залози або діабет. Сімейна гіперліпідемія/гіперліпопротеїнемія характеризується аутосомним успадкуванням і пов'язана з підвищенням вмісту ліпопротеїнів і ліпідів у крові. Сімейна гіперліпідемія/гіперліпопротеїнемія поділяється на п'ять категорій (типи I-V) в залежності від складу і типу частинок ліпопротеїну у крові. Наприклад, при гіперліпопротеїнемії типу І і типу IV рівень тригліцеридів підвищений переважно у хіломікронах і VLDL-частинках, відповідно. Взагалі, існує обернена залежність між рівнями HDL-холестерину і тригліцеридів, які здійснюють внесок у дисліпідемію. Якщо залишити дисліпідемію (наприклад, низький рівень HDL-холестерину і високі рівні тригліцеридів або LDL-холестерину) нелікованою, то можна загострити інші стани, такі як панкреатит, аномальна переносимість глюкози, діабет, хвороба коронарної артерії, ішемічні хвороби серця, атеросклероз, гепатоспленомегалія і хвороба ожиріння печінки. Залишається потреба забезпечення ефективного лікування пов'язаних з глюкозою розладів, таких як підвищені рівні глюкози, цукровий діабет типу II, синдром X і подібні. Залишається також потреба забезпечення ефективного лікування пов'язаних з ліпідами розладів, таких як підвищені рівні глюкози, дисліпідемія і подібні. Даний винахід стосується способу лікування пов'язаних з глюкозою розладів і/або пов'язаних з ліпідами розладів, що включає введення потребуючому цього суб'єкту терапевтично ефективної кількості сполуки формули (І) 94077 12 де R1 і R2 кожний незалежно вибраний з групи, що складається з атома водню і нижчого алкілу; R4 вибраний з групи, що складається з атома водню і нижчого алкілу; а дорівнює цілому числу від 1 до 2; вибраний з групи, що складається з де b дорівнює цілому числу від 0 до 4; і де с дорівнює цілому числу від 0 до 2; кожний R5 незалежно вибраний з групи, що складається з галогену, нижчого алкілу і нітро; за умови, коли являє собою тоді а дорівнює 1; або її фармацевтично прийнятної солі. Даний винахід також стосується способу лікування пов'язаних з глюкозою розладів і/або пов'язаних з ліпідами розладів, що включають введення потребуючому цього суб'єкту терапевтично ефективної кількості сполуки формули (II) або її фармацевтично прийнятної солі. Винахід ілюструє спосіб лікування пов'язаних з глюкозою розладів, що включають введення потребуючому цього суб'єкту терапевтично ефективної кількості будь-якої з описаних вище сполук. В іншому прикладі винахід стосується способу лікування пов'язаних з ліпідами розладів, що включає введення потребуючому цього суб'єкту терапевтично ефективної кількості будь-якої з описаних вище сполук. Даний винахід також стосується способу лікування пов'язаного з глюкозою розладу, що включає спільну терапію з використанням, щонайменше, одного антидіабетичного агента і сполуки формули (І) або формули (II), які описані у даному описі. Даний винахід також стосується способу 13 лікування пов'язаного з ліпідами розладу, що включає спільну терапію з використанням, щонайменше, одного антиліпідного агента і сполуки формули (І) або формули (II), які описані у даному описі. Даний винахід також стосується способу лікування пов'язаного з глюкозою розладу або пов'язаного з ліпідами розладу, що включає спільну терапію з використанням, щонайменше, одного антидіабетичного агента, і/або, щонайменше, одного антиліпідного агента, і сполуки формули (І) або формули (II), які описані у даному описі. Даний винахід також стосується способу лікування пов'язаного з глюкозою розладу, що включає спільну терапію з використанням агента проти ожиріння і сполуки формули (І) або формули (II), які описані у даному описі. Даний винахід стосується способу лікування пов'язаних з глюкозою розладів і/або пов'язаних з ліпідами розладів, що включає введення потребуючому цього суб'єкту терапевтично ефективної кількості сполуки формули (І). або її фармацевтично прийнятної солі, де, a, R1, R2 і R4 такі, як визначено у даному описі. Даний винахід також стосується способів лікування пов'язаних з глюкозою розладів і пов'язаних з ліпідами розладів, що включають спільну терапію з використанням, щонайменше, одного антидіабетичного і/або, щонайменше, одного антиліпідного агента і сполуки формули (І) або формули (II), які описані у даному описі. Фахівець у даній галузі усвідомлює, що лікування пов'язаних з глюкозою розладів і/або пов'язаних з ліпідами розладів може також здобувати користь з лікування супровідних хворобливих станів надмірної ваги і ожиріння. Таким чином, в одному варіанті способи за даним винаходом включають спільну терапію з використанням агента проти ожиріння і сполуки формули (І) або формули (II), які описані у даному описі. Використовуваний у даному описі термін «пов'язаний з глюкозою розлад» визначають як будьякий розлад, який характеризується підвищеними рівнями глюкози. Пов'язані з глюкозою розлади включають підвищені рівні глюкози, потенційний діабет, погіршену пероральну толерантність до глюкози, слабкий глікемічний контроль, цукровий діабет типу II, синдром X (також відомий як метаболічний синдром), гестаційний діабет, резистентність до інсуліну, гіперглікемію і втрату м'язової маси у результаті гіперглікемії (виснаження). Лікування пов'язаних з глюкозою розладів може включати зниження рівнів глюкози, поліпшення глікемічного контролю, зниження резистентності до інсуліну і/або профілактику розвитку пов'язаного з глюкозою розладу (наприклад, профілактику розвитку цукрового діабету типу II у пацієнта, який страждає від погіршеної пероральної толерантності до глюкози або підвищених рівнів глюкози). Використовуваний у даному описі термін «пов'язаний з ліпідами розлад» визначають як будьякий розлад, який характеризується аномальними 94077 14 рівнями ліпідів. Пов'язані з ліпідами розлади включають підвищені рівні тригліцеридів, низькі рівні HDL-холестерину і дисліпідемію, переважно підвищені рівні тригліцеридів або низькі рівні HDLхолестерину. Лікування пов'язаного з ліпідами розладу може включати зниження рівня тригліцеридів, підвищення HDL-холестерину і/або поліпшення співвідношення тригліцерид/HDL. Використовуваний у даному описі термін «антидіабетичний агент» означає будь-який фармацевтичний агент, який знижує рівні глюкози у крові, поліпшує глікемічний контроль і/або поліпшує чутливість до інсуліну. Антидіабетичні агенти, придатні для лікування цукрового діабету типу II і синдрому X, включають, але не обмежені цим, сульфонілсечовини, меглітиніди, агенти, які модифікують секрецію інсуліну, бігуаніди, тіазолідиндіони, PPAR-гамма агоністи, модулятори ретиноїдних-Х рецепторів (RXR), інсулін-сенсибілізуючі агенти, інгібітори альфа-глюкозидази, інсуліни, малі молекули-імітатори інсуліну, інгібітори котранспортерів Na-глюкози, агоністи аміліну, антагоністи глюкагону, GLP-1 і GLP-1 аналоги, інгібітори DPPIV і подібні. Придатні приклади антидіабетичних агентів включають, ексенатид, хлорпропамід, толазамід, толбутамід, глібурид, гліпізид, глімепірид, репаглінід, метформін, розиглітазон, піоглітазон, троглітазон, ізаглітазон (відомий як МСС-555), 2-[2-[(2R)-4гексил-3,4-дигідро-3-оксо-2Н-1,4-бензоксазин-2іл]етокси]бензолоцтову кислоту, GW2570, таргретин, 9-цис-ретиноєву кислоту, аскарбозу, міглітол, L-783281, ТЕ-17411, Т-1095, BAY-279955, флоризен, прамлінтид, інсулін звичайної дії, інсулін короткострокової дії, інсулін проміжної дії, інсулін тривалої дії, інсулін, що вводиться шляхом інгаляції, аналоги інсуліну, ацетоксамід, буформін, глібомурид, глігексамід, глімідин, ліноглірид, пальмоксират, зополрестат; етоформін, глікалзид, гліпінамід і подібні. Більш конкретно, антидіабетичні агенти включають, але не обмежені цим: (a) сульфонілсечовини, що підвищують виробництво інсуліну за допомогою стимуляції бетаклітин підшлункової залози, і, отже, діють як стимулятори секреції інсуліну. Основним механізмом дії сульфонілсечовин є закриття АТФ-чутливих калієвих каналів у плазматичній мембрані бетаклітин, що ініціює ланцюг подій, внаслідок яких вивільняється інсулін. Придатні приклади сульфонілсечовин включають, але не обмежені цим, хлорпропамід, толазамід, толбутамід, глібурид, гліпізид, глімепірид і подібні; (b) меглітиніди, інший клас стимуляторів секреції інсуліну, які мають механізм дії, відмінний від механізму дії сульфонілсечовин. Придатні приклади меглітинідів включають, але не обмежені цим, репаглінід; (c) агенти, що модифікують секрецію інсуліну, такі як глюкагоноподібний пептид 1 (GLP-1) і його міметики, глюкоза-інсулінотропний пептид (GIP) і його міметики, ексендин і його міметики та інгібітори дипептидилпротеази (DPPIV); (d) бігуаніди, що знижують виробництво глюкози печінкою і підвищують поглинання глюкози. 15 Придатні приклади включають, але не обмежені цим, метформін; (e) тіазолідиндіони, інсулін-сенсибілізуючі ліки, що знижують периферичну резистентність до інсуліну, посилюючи ефекти інсуліну на уражені органи і тканини. Ці ліки зв'язують і активують ядерний рецептор, рецептор, активований проліфератором пероксисом-гамма (PPAR-гамма), який підвищує транскрипцію специфічних інсулін-залежних генів. Придатними прикладами агоністів PPAR-гамма є тіазолідиндіони, які включають, але не обмежені цим, розиглітазон, піоглітазон, троглітазон, ізаглітазон (відомий як МСС-555), 2-[2-[(2R)-4-гексил3,4-дигідро-3-оксо-2Н-1,4-бензоксазин-2іл]етокси]бензолоцтову кислоту і подібні. Також нетіазолідиндіони діють як інсулін-сенсибілізуючі ліки і включають, але не обмежені цим, GW2570 і подібні; (f) модулятори ретиноїдних-Х рецепторів (RXR), також інсулін-сенсибілізуючі ліки, які включають, але не обмежені цим, таргретин, 9-цисретиноєву кислоту і подібні; (g) інші інсулін-сенсибілізуючі агенти включають, але не обмежені цим, INS-1, інгібітори РТР1В, інгібітори GSK3, інгібітори глікогенфосфорилази, інгібітори фруктоза-1,6-біфосфатази і подібні; (h) інгібітори альфа-глюкозидази, які діють, інгібуючи альфа-глюкозидазу. Альфа-глюкозидаза перетворює фруктозу у глюкозу, таким чином, ці інгібітори уповільнюють перетравлювання вуглеводів. Неперетравлені вуглеводи згодом руйнуються у кишечнику, знижуючи тим самим післяобідній пік глюкози. Придатні приклади включають, але не обмежені цим, акарбозу і міглітол; (і) інсуліни, включаючи інсуліни звичайної або короткострокової дії, проміжної і тривалої дії, інсулін, що вводиться шляхом інгаляції, і аналоги інсуліну, такі як молекули інсуліну з незначними відмінностями у послідовності природних амінокислот. Ці модифіковані інсуліни можуть мати більш швидкий початок дії і/або меншу тривалість дії; (j) малі молекули-імітатори інсуліну, включаючи, але не обмежуючись цим, L-783281, ТЕ-17411 і подібні; (k) інгібітори котранспортерів Na-глюкози, які інгібують ниркову реабсорбцію глюкози, такі як Т1095, Т-1095А, флоризен і подібні; (l) агоністи аміліну, які включають, але не обмежені цим прамлінтид і подібні; і (m) антагоністи глюкагону, такі як AY-279955 і подібні. Використовуваний у даному описі термін (доки не вказано інакше) «антиліпідний агент» означає будь-який фармацевтичний агент, здатний знижувати рівні тригліцеридів, знижувати рівні ліпідів, підвищувати HDL-рівні або поліпшувати співвідношення тригліцерид/HDL-холестерин. Придатні приклади включають, але не обмежені цим, антиліпемічні агенти, жовчнокислотні смоли, інгібітори абсорбції холестерину, похідні фібринової кислоти, інгібітори HMG-CoA редуктази (тобто статини). Переважним антиліпідним агентом є статин, вибраний з групи, що включає аторвастатин (Lipitor), церивастатин (Ваусоl), флувастатин (Lescol), ло 94077 16 вастатин, (Mevacor), правастатин (Pravachol), розувастатин (Crestor), симвастатин (Zocor). Використовуваний у даному описі термін (доки не вказано інакше) «агент проти ожиріння» означає будь-який фармацевтичний агент, який лікує ожиріння, сприяє втраті ваги і/або придушує апетит. Придатні приклади промоторів втрати ваги включають, але не обмежені цим, римонабант, орлістат, сибутрамін, мазіндол, бензфетамін, фенметразин, фентермін, діетилпропіон, мазіндол, фенілпропаноламін, ефедрин, квіпазин, флуоксетин, сертралін, фенфлурамін, дексфенфлурамін, апоморфін, екзендин, дегідроепіандростерон, етіозоландіон, тестостерон, оксандролон, топірамат і подібні. Переважним агентом, що промотує втрату ваги, є римонабант, топірамат, орлістат або сибутрамін. Використовуваний у даному описі термін «суб'єкт», стосується тварини, переважно ссавця, найбільш переважно людини, яка є об'єктом лікування, спостереження або експерименту. Використовуваний у даному описі термін «терапевтично ефективна кількість» означає, що кількість активної сполуки або фармацевтичного агента викликає біологічну або медичну відповідь у системі тканин, у тварини або людини, яка піддається втручанню дослідника, ветеринара, лікаря або іншого клініциста, що включає полегшення симптомів захворювання або розладу, що підлягає лікуванню. Коли даний винахід стосується спільної терапії або комбінаційної терапії, що включає введення однієї або більше сполук формули (І) або формули (II) і одного або більше антидіабетичних і/або антиліпідних агентів, то «терапевтично ефективна кількість» означає таку кількість комбінації агентів, взятих разом, що об'єднаний ефект викликає необхідну біологічну або медичну відповідь. Наприклад, терапевтично ефективна кількість при спільній терапії, що включає введення сполуки формули (І) або формули (II) і антидіабетичного і/або антиліпідного агента, дорівнює такій кількості сполуки формули (І) або формули (II) і кількості придатного фармацевтичного агента, які, за умови, що їх приймають разом або послідовно, мають об'єднаний ефект, який є терапевтично ефективним. Крім того, фахівці у даній галузі визнають, що у випадку спільної терапії з використанням терапевтично ефективної кількості, як у прикладі вище, кількість сполуки формули (І) або формули (II) і/або кількість антидіабетичного і/або антиліпідного агента індивідуально може бути або не бути терапевтично ефективною. Використовувані у даному описі терміни «спільна терапія» і «комбінаційна терапія» означають лікування потребуючого цього суб'єкта за допомогою введення однієї або більше сполук формули (І) або формули (II) у комбінації з одним або декількома антидіабетичними і/або антиліпідними агентами, де сполуку(сполуки) формули (І) або формули (II) і антидіабетичний і/або антиліпідний агент(и) вводять будь-якими придатними способами: одночасно, послідовно, окремо або у вигляді єдиного фармацевтичного препарату. Якщо сполуку(сполуки) формули (І) або формули (II) і анти 17 94077 діабетичний і/або антиліпідний агент(и) вводять у вигляді окремих дозованих форм, кількість доз, що вводяться за день для кожної сполуки може бути однаковою або різною. Сполуку(сполуки) формули (І) або формули (II) і антидіабетичний і/або антиліпідний агент(и) можна вводити однаковими або різними способами введення. Приклади придатних способів введення включають, але не обмежені цим, пероральний, внутрішньовенний (iv), внутрішньом'язовий (іm), підшкірний (sc), трансдермальний і ректальний. Сполуки також можна вводити безпосередньо у нервову систему, включаючи, але не обмежуючись цим, інтрацеребральний, інтравентрикулярний, інтрацеребровентрикулярний, інтратекальний, інтрацистернальний, інтраспінальний і/або периспінальний способи введення, здійснюючи доставку за допомогою внутрішньочерепних або внутрішньохребетних голок і/або катетерів, з або без застосування компресійних пристроїв. Сполуку(сполуки) формули (І) або формули (II) і антидіабетичний і/або антиліпідний агент(и) можна вводити за схемами з одночасним прийомом або прийомом, що чергується, в один і той же або різний час протягом курсу терапії, спільно, поділивши на частини або у вигляді єдиних форм. У варіанті даного винаходу R1 вибраний з групи, що складається з атома водню і метилу. В іншому варіанті даного винаходу R2 вибраний з групи, що складається з атома водню і метилу. Ще в одному варіанті даного винаходу кожний R1 і R2 означає атом водню, або кожний R1 і R2 означає метил. У варіанті даного винаходу -(СН2)а- вибраний з групи, що складається з -СН2- і -СН2СН2-. В іншому варіанті даного винаходу -(СН2)а- являє собою СН2-. У варіанті даного винаходу R4 вибраний з групи, що складається з атома водню і метилу, переважно R4 означає атом водню. У варіанті даного винаходу а дорівнює 1. У варіанті даного винаходу b дорівнює цілому числу від 0 до 2. В іншому варіанті даного винаходу с дорівнює цілому числу від 0 до 2. В іншому варіанті даного винаходу b дорівнює цілому числу від 0 до 1. В іншому варіанті даного винаходу с дорівнює цілому числу від 0 до 1. Ще в одному варіанті даного винаходу сума b і с дорівнює цілому числу від 0 до 2, переважно цілому числу від 0 до 1. Ще в одному варіанті даного винаходу b дорівнює цілому числу від 0 до 2 і с дорівнює 0. У варіанті даного винаходу групи, що складається з вибраний з 18 В іншому варіанті даного винаходу ви браний з групи, що складається з У варіанті даного винаходу вибраний з групи, що складається з 2-(2,3дигідробензо[1,4]діоксинілу), 2(бензо[1,3]діоксолілу), 3-(3,4дигідробензо[1,4]діоксепінілу), 2-(6-хлор-2,3дигідробензо[1,4]діоксинілу), 2-(6-фтор-2,3дигідробензо[1,4]діоксинілу), 2-(хроманілу), 2-(5фтор-2,3-дигідробензо[1,4]діоксинілу), 2-(7-хлор2,3-дигідробензо[1,4]діоксинілу), 2-(6хлорбензо[1,3]діоксолілу), 2-(7-нітро-2,3дигідробензо[1,4]діоксинілу), 2-(7-метил-2,3дигідробензо[1,4]діоксинілу), 2-(5-хлор-2,3дигідробензо[1,4]діоксинілу), 2-(6-бром-2,3дигідробензо[1,4]діоксинілу), 2-(6,7-дихлор-2,3дигідробензо[1,4]діоксинілу), 2-(8-хлор-2,3дигідробензо[1,4]діоксинілу), 2-(2,3дигідронафто[2,3-b][1,4]діоксинілу) і 2-(4метилбензо[1,3]діоксолілу). В іншому варіанті даного винаходу ви браний з групи, що складається з 2(бензо[1,3]дioксолілу), 2-(2,3дигідробензо[1,4]діоксинілу), 2-(6-хлор-2,3дигідробензо[1,4]діоксинілу), 2-(7-хлор-2,3дигідробензо[1,4]діоксинілу), 2-(7-метил-2,3дигідробензо[1,4]діоксинілу), 2-(6-бром-2,3дигідробензо[1,4]діоксинілу) і 2-(6,7-дихлор-2,3дигідробензо[1,4]діоксинілу). В іншому варіанті даного винаходу вибраний з групи, що складається з 2-(2,3-дигідробензо[1,4]діоксинілу), 2-(7-метил-2,3-дигідробензо[1,4]діоксинілу) і 2-(6бром-2,3-дигідробензо[1,4]діоксинілу). У варіанті даного винаходу R5 вибраний з групи, що складається з галогену і нижчого алкілу. В іншому варіанті даного винаходу R5 вибраний з хлору, фтору, брому і метилу. У варіанті даного винаходу стереоцентр на сполуці формули (І) знаходиться в S-конфігурації. В іншому варіанті даного винаходу стереоцентр на сполуці формули (І) знаходиться в R-конфігурації. У варіанті даного винаходу сполука формули (І) присутня у вигляді енантіомерно збагаченої суміші, де % енантіомерного збагачення (% ее) складає величину більше приблизно 75%, переважно, більше приблизно 90%, більш переважно, більше приблизно 95%, найбільш переважно, більше приблизно 98%. Додаткові варіанти даного винаходу включають такі варіанти, де замісники, вибрані для однієї або декількох змінних, визначених у даному описі (тобто R1, R2, R5, R4, X-Y і А), вибрані незалежно, являючи собою будь-які індивідуальні замісники або будь-яку підмножину замісників, вибраних з повного переліку, який визначений у даному описі. 19 Типові сполуки за даним винаходом, перераховані нижче у таблиці 1. Додаткові сполуки за даним винаходом перераховані у таблиці 3. У наведених нижче таблицях 1 і 2 стовпчик, озаглавлений «стерео», визначає стереоконфігурацію на атомі вуглецю гетероциклу, приєднаному по відмі 94077 20 ченому зірочкою зв'язку. Якщо позначення відсутнє, це означає, що сполуку одержують у вигляді суміші стереоконфігурацій. Де наведене позначення «R» або «S», там стереоконфігурація вказана на основі енантіомерно збагаченого вихідного матеріалу. 21 Використовуваний у даному описі, доки не вказано інакше, термін «галоген» означає хлор, бром, фтор і йод. Використовуваний у даному описі, доки не вказано інакше, термін «алкіл», сам по собі або як частина групи замісника, включає лінійні і розгалужені ланцюги. Наприклад, алкільні радикали включають метил, етил, пропіл, ізопропіл, бутил, ізобутил, втор-бутил, трет-бутил, пентил і подібні. Доки не вказано інакше, використовуване з алкілом визначення «нижчий» означає вуглецевий ланцюг, що складається з 1-4 атомів вуглецю. Використовуваний у даному описі, доки не вказано інакше, термін «алкокси» означає радикал простого кисневого ефіру з описаними вище лінійними або розгалуженими алкільними групами, наприклад, метокси, етокси, н-пропокси, вторбутокси, трет-бутокси, н-гексилокси і подібними. Використовувана у даному описі мітка «*» означає наявність стереогенного центру. Якщо конкретна група є «заміщеною» (наприклад, алкільною, арильною та ін.), то ця група може мати один або більше замісників, переважно від одного до п'яти замісників, більш переважно від одного до трьох замісників, найбільш переважно від одного до двох замісників, незалежно вибраних з переліку замісників. З посиланням на замісники термін «незалежно» означає, що, якщо можлива присутність більше одного замісника, то такі замісники можуть бути однаковими або різними. За стандартною номенклатурою, що використовується протягом всієї цієї заявки, спочатку опи 94077 22 сується кінцева частина позначеного бічного ланцюга, потім сусідня фукціональність у напрямі до точки приєднання. Таким чином, наприклад, замісник «феніл-алкіл-аміно-карбоніл-алкіл» стосується групи формули Далі наведені скорочення, що використовуються в описі, зокрема, на схемах і у прикладах. ДЦК = дициклогексилкарбодіімід ДХЕ = дихлоретан ДХМ = дихлорметан ДІПЕА або = діізопропілетиламін ІЕА ДМФА = Ν,Ν-диметилформамід ДМСО = диметилсульфоксид EDC = етилкарбодіімід Et3N або = триетиламін TEA Et2O = діетиловий ефір ЕА або = етилацетат EtOAc EtOH = етанол ІРА = 2-пропанол Hept = гептан ГОБТ = 1-гідроксибензотриазол ВЕРХ = рідинна хроматографія при високому тиску ЛАГ = літійалюмінійгідрид 23 Μ або МеОН ЯМР Pd-C ОФ ВЕРХ = метанол = ядерний магнітний резонанс = каталізатор: паладій на вугіллі = рідинна хроматографія при високому тиску з оберненою фазою ΚТ або к.т. = кімнатна температура TEA = триетиламін ТΦΟ = трифтороцтова кислота ТГΦ = тетрагідрофуран ТШХ = тонкошарова хроматографія Коли сполуки за даним винаходом мають, щонайменше, один хіральний центр, то, відповідно, вони можуть існувати у вигляді енантіомерів. Коли сполуки мають два або більше хіральних центрів, вони можуть додатково існувати у вигляді діастереомерів. Потрібно розуміти, що всі такі ізомери і їх суміші включені в об'єм даного винаходу. Крім того, деякі з кристалічних форм сполук можуть існувати у вигляді поліморфів і, передбачається, що як такі вони включені у даний винахід. Крім того, деякі сполуки можуть утворювати сольвати з водою (тобто, гідрати) або звичайними органічними розчинниками, і, передбачається також, що такі сольвати включені в об'єм даного винаходу. У зв'язку з тим, що солі сполук за даним винаходом використовуються у медицині, вони належать до нетоксичних «фармацевтично прийнятних солей». Однак інші солі можуть бути придатні при одержанні сполук за даним винаходом або їх фармацевтично прийнятних солей. Придатні фармацевтично прийнятні солі сполук включають адитивні солі кислот, які можуть утворюватися, наприклад, при змішуванні розчину сполуки з розчином фармацевтично прийнятної кислоти, такої як соляна кислота, сірчана кислота, фумарова кислота, малеїнова кислота, бурштинова кислота, оцтова кислота, бензойна кислота, лимонна кислота, винна кислота, вугільна кислота або фосфорна кислота. Крім того, якщо сполуки за винаходом несуть кислотний фрагмент, то їх придатні фармацевтично прийнятні солі можуть включати солі лужних металів, наприклад, солі натрію або калію; солі лужноземельних металів, наприклад, солі кальцію або магнію; і солі, утворені з придатними органічними лігандами, наприклад, четвертинні амонійні солі. Таким чином, типові фармацевтично прийнятні солі включають наступні: ацетат, бензолсульфонат, бензоат, бікарбонат, бісульфат, бітартрат, борат, бромід, едетат кальцію, камзилат, карбонат, хлорид, клавуланат, цитрат, дигідрохлорид, едетат, едизилат, естолат, езилат, фумарат, глюцептат, глюконат, глутамат, гліколіларсанілат, гексилрезорцинат, гідрабамін, гідробромід, гідрохлорид, гідроксинафтоат, йодид, ізотіонат, лактат, лактобіонат, лаурат, малат, малеат, мандеат, мезилат, метилбромід, метилнітрат, метилсульфат, мукат, напзилат, нітрат, сіль N-метилглюкамінамонію, олеат, памоат (ембонат), пальмітат, пантотенат, фосфат/дифосфат, полігалактуронат, саліцилат, стеарат, сульфат, субацетат, сукцинат, танат, тартрат, теоклат, тозилат, триетіодид і валерат. 94077 24 Типові кислоти і основи, які можна використовувати при одержанні фармацевтично прийнятних солей, включають наступні сполуки: Кислоти включають оцтову кислоту, 2,2дихлороцтову кислоту, ациловані амінокислоти, адипінову кислоту, альгінову кислоту, аскорбінову кислоту, L-аспарагінову кислоту, бензолсульфонову кислоту, бензойну кислоту, 4ацетамідобензойну кислоту, (+)-камфорну кислоту, камфорсульфонову кислоту, (+)-(1S)-камфор-10сульфонову кислоту, капринову кислоту, капронову кислоту, каприлову кислоту, коричну кислоту, лимонну кислоту, цикламову кислоту, додецилсірчану кислоту, етан-1,2-дисульфонову кислоту, етансульфонову кислоту, 2гідроксіетансульфонову кислоту, мурашину кислоту, фумарову кислоту, галактарову кислоту, гентизинову кислоту, глюкогептонічну кислоту, Dглюконову кислоту, D-глюкоронову кислоту, Lглутамінову кислоту, а-оксо-глутарову кислоту, гліколеву кислоту, гіпурову кислоту, бромистоводневу кислоту, соляну кислоту, (+)-L-молочну кислоту, (±)-DL-молочну кислоту, лактобіонову кислоту, малеїнову кислоту, (-)-L-яблучну кислоту, малонову кислоту, (±)-DL-манделову кислоту, метансульфонову кислоту, нафталін-2-сульфонову кислоту, нафталін-1,5-дисульфонову кислоту, 1гідрокси-2-нафтойну кислоту, нікотинову кислоту, азотну кислоту, олеїнову кислоту, оротову кислоту, щавлеву кислоту, пальмітинову кислоту, памоєву кислоту, фосфорну кислоту, L-піроглутамінову кислоту, саліцилову кислоту, 4-аміносаліцилову кислоту, себацинову кислоту, стеаринову кислоту, бурштинову кислоту, сірчану кислоту, дубильну кислоту, (+)-L-винну кислоту, тіоціанову кислоту, пара-толуолсульфонову кислоту і ундециленову кислоту; і основи включають: аміак, L-аргінін, бенетамін, бензатин, гідроксид кальцію, холін, деанол, діетаноламін, діетиламін, 2-(діетиламіно)етанол, етаноламін, етилендіамін, N-метилглюкамін, гідрабамін, 1Н-імідазол, L-лізин, гідроксид магнію, 4-(2гідроксієтил)морфолін, піперазин, гідроксид калію, 1-(2-гідроксіетил)піролідин, вторинний амін, гідроксид натрію, триетаноламін, трометамін і гідроксид цинку. Сполуки формули (І) можна одержати відповідно до способу, зображеного на схемі 1. Схема 1 Таким чином, проводять взаємодію заміщеної придатним чином сполуки формули (X), відомої сполуки або сполуки, одержаної відомими способами, з сульфамідом, відомою сполукою, де сульфамід переважно присутній у кількості приблизно від 2 до 5 еквівалентів, в органічному розчиннику, такому як ТГФ, діоксан і подібні, переважно при 25 94077 підвищеній температурі приблизно від 50°С до 100°С, більш переважно приблизно при температурі кипіння зі зворотним холодильником, одержуючи відповідну сполуку формули (Іа). Альтернативно, проводять взаємодію заміщеної придатним чином сполуки формули (X), відомої сполуки або сполуки, одержаної відомими способами, із заміщеною придатним чином сполукою формули (XI), відомою сполукою або сполукою, одержаною відомими способами, у присутності основи, такої як TEA, ДІПЕА, піридин і подібні, в органічному розчиннику, такому як ДМФА, ДМСО і подібному, одержуючи відповідну сполуку формули (І). Сполуки формули (X) де являє собою 26 му розчиннику, наприклад, ацетонітрилі і подібному, одержуючи відповідну сполуку формули (XV). Проводять взаємодію сполуки формули (XV) з вибраним придатним чином відновником, таким як ЛАГ і подібні, в органічному розчиннику, наприклад, ТГФ, діетиловому ефірі і подібному, одержуючи відповідну сполуку формули (Хb). Сполуки формули (X), де вибраний з і де а дорівнює 2, можна одержати відповідно до способу, зображеного на схемі 4. можна одержати відповідно до способу, зображеного на схемі 2. Схема 2 Таким чином, проводять взаємодію заміщеної придатним чином сполуки формули (XII), відомої сполуки або сполуки, одержаної відомим способом (наприклад, як описано на схемі 3 вище), з NH4OH, відомою сполукою, необов'язково в органічному розчиннику, такому як ацетонітрил і подібні, одержуючи відповідну сполуку формули (XIII). Проводять взаємодію сполуки формули (XIII) з вибраним придатним чином відновником, таким як ЛАГ і подібні, в органічному розчиннику, наприклад, ТГФ, діетиловому ефірі і подібному, одержуючи відповідну сполуку формули (Ха). Сполуки формули (X), де вибраний з Схема 4 Таким чином, проводять взаємодію заміщеної придатним чином сполуки формули (XVI), де J1 являє собою придатну відхідну групу, таку як Вr, СІ, І, тозил, мезил, трифліл і подібні, відомої сполуки або сполуки, одержаної відомими способами (наприклад, активацією відповідної сполуки, де J1 являє собою ОН), з ціанідом, наприклад, ціанідом калію, ціанідом натрію і подібним в органічному розчиннику, такому як ДМСО, ДМФА, ТГФ і подібні, одержуючи відповідну сполуку формули (XVII). Сполуку формули (XVII) відновлюють відповідно до відомих способів, наприклад, за допомогою взаємодії з придатним відновником, таким як ЛАГ, боран і подібні, одержуючи відповідну сполуку формули (Хс). Сполуки формули (X), де вибраний з і де а дорівнює 1, можна одержати відповідно до способу, зображеного на схемі 5. можна одержати відповідно до способу, зображеного на схемі 3. Схема 3 Таким чином, проводять взаємодію заміщеної придатним чином сполуки формули (XIV), відомої сполуки або сполуки, одержаної відомими способами, з NH4OH у присутності агента поєднання, такого як ДЦК і подібні, необов'язково в органічно Схема 5 Таким чином, заміщену придатним чином сполуку формули (XVIII), відому сполуку або сполуку, одержану відомими способами, активують, відповідно до відомого способу, одержуючи відповідну 27 94077 сполуку формули (XIX), де J2 являє собою придатну відхідну групу, наприклад, тозилат, СІ, Вr, І, мезилат, трифлат і подібні. Проводять взаємодію сполуки формули (XIX) з фталімідною сіллю, такою як фталімід калію, фталімід натрію і подібні, в органічному розчиннику, наприклад, ДМФА, ДМСО, ацетонітрилі і подібному, переважно при підвищеній температурі у діапазоні від 50°С приблизно до 200°С, більш переважно, близько температури кипіння зі зворотним холодильником, одержуючи відповідну сполуку формули (XX). Проводять взаємодію сполуки формули (XX) з N2H4, відомою сполукою, в органічному розчиннику, такому як етанол, метанол і подібні, переважно, при підвищеній температурі у діапазоні приблизно від 50°С до 100°С, більш переважно, близько температури кипіння зі зворотним холодильником, одержуючи відповідну сполуку формули (Xd). Фахівець у даній галузі усвідомлює, що сполуки формули (X), де вибраний з можна аналогічно одержати відповідно до відомих способів або, наприклад, відповідно до способів, зображених вище на схемах 2-5, вибираючи і здійснюючи відповідну заміну бензоконденсованих вихідних матеріалів нафтил-конденсованими сполуками. Крім того, фахівець у даній галузі розуміє, що, якщо потрібен окремий енантіомер (або суміш енантіомерів, збагачена одним енантіомером) сполуки формули (X), можна застосовувати способи, описані вище на схемах 1-5, замінюючи придатний вихідний матеріал відповідним окремим енантіомером (або сумішшю енантіомерів, збагаченою одним енантіомером). Фахівець у даній галузі розуміє, що, якщо реакційну стадію за даним винаходом можна проводити у різних розчинниках або системах розчинників, то вказану реакційну стадію також можна проводити у суміші придатних розчинників або систем розчинників. Коли способи одержання сполук за винаходом дають суміш стереоізомерів, ці ізомери можна розділити, використовуючи звичайні методики, наприклад, препаративну хроматографію. Сполуки 28 можна одержати у рацемічному вигляді або у вигляді індивідуальних енантіомерів за допомогою енантіоспецифічного синтезу або розділення. Наприклад, можна, розділити сполуки на складові енантіомери стандартними методиками, такими як утворення діастереомерних пар при утворенні солі з оптично активною кислотою, такою як (-)-дипара-толуоїл-D-винна кислота і/або (+)-ди-паратолуоїл-L-винна кислота, з подальшою фракціонованою кристалізацією і регенерацією вільної основи. Сполуки також можна розділити за допомогою утворення діастереомерних складних ефірів або амідів з подальшим хроматографічним розділенням і видаленням хірального допоміжного агента. Інакше сполуки можна розділити використовуючи хіральну ВЕРХ-колонку. Протягом якого-небудь з процесів одержання сполук за даним винаходом може бути необхідно і/або бажано захистити чутливі або реакційноздатні групи на яких-небудь з молекул, що розглядаються. Цього можна досягти за допомогою звичайних захисних груп, таких як групи, описані у роботах Protective Groups 1N Organic Chemistry, ed. J.F.W. McOmie, Plenum Press, 1973; і T.W. Greene & P.G.M. Wuts, Protective Groups 1N Organic Synthesis, John Wiley & Sons, 1991. Захисні групи можна видалити на наступній звичайній стадії, використовуючи способи, відомі у даній галузі. Крім того, даний винахід включає фармацевтичні композиції, що містять одну або більше сполук формули (І) з фармацевтично прийнятним носієм. Фармацевтичні композиції, що містять як активний інгредієнт одну або більше з описаних у даному описі сполук за винаходом, можна одержати шляхом ретельного перемішування сполуки або сполук з фармацевтичним носієм відповідно до звичайних методик одержання фармацевтичних препаратів. Носій може мати різноманітні форми в залежності від необхідного способу введення (наприклад, перорального, парентерального). Таким чином, для рідких пероральних препаратів, таких як суспензії, еліксири і розчини, придатні носії і домішки включають воду, гліколі, масла, спирти, смакові агенти, консерванти, стабілізатори, барвники і подібне; для твердих препаратів для перорального прийому, таких як порошки, капсули і таблетки, придатні носії і домішки включають крохмалі, цукри, розріджувачі, гранулюючі агенти, лубриканти, зв'язуючі, розпушувачі і подібне. Поверх твердих препаратів для перорального прийому можна також нанести такі речовини як цукри або ентеросолюбільне покриття з метою регулювання основного місця абсорбції. Носії для препаратів парентерального введення звичайно містять стерильну воду, і можна додавати інші інгредієнти для підвищення розчинності або консервації. Суспензії або розчини, що вводяться шляхом ін'єкції, можна також приготувати, використовуючи водні носії разом з придатними домішками. Для одержання фармацевтичних композиції за даним винаходом одну або більше сполук за даним винаходом як активний інгредієнт ретельно змішують з фармацевтичним носієм відповідно до звичайних методик одержання фармацевтичних препаратів, вказаний носій може мати різноманітні 29 форми в залежності від форми необхідного для введення препарату, наприклад, перорального або парентерального, такого як внутрішньом'язове. При одержанні композицій у вигляді дозованої форми для перорального прийому можна використовувати будь-яке зі звичайних фармацевтичних середовищ. Таким чином, для рідких пероральних препаратів, таких як суспензії, еліксири і розчини, придатні носії і домішки включають воду, гліколі, масла, спирти, смакові агенти, консерванти, стабілізатори, барвники і подібні; для твердих пероральних препаратів, таких як, наприклад, порошки, капсули, таблетки у вигляді капсул, желатинові капсули і таблетки, придатні носії і домішки включають крохмалі, цукри, розріджувачі, гранулюючі агенти, лубриканти, зв'язуючі, розпушувачі і подібні. Через простоту введення таблетки і капсули представляють найбільш корисні дозовані форми для перорального прийому, зрозуміло, що у цьому випадку застосовують тверді фармацевтичні носії. Якщо потрібно, на таблетки можна нанести покриття з цукру або ентеросолюбільне покриття за стандартними методиками. Носій для парентеральних препаратів звичайно містить стерильну воду, хоча можна включати інші інгредієнти, наприклад, для підвищення розчинності або консервації. Можна також приготувати суспензії для ін'єкцій, у цьому випадку можна використовувати придатні рідкі носії, суспендуючі агенти і подібне. Фармацевтичні композиції, що згадуються у даному описі, містять деяку кількість активного інгредієнта, необхідну для доставки ефективної дози, яка описана вище, на стандартну дозу, наприклад, таблетку, капсулу, порошок, ін'єкцію, чайну ложку і подібне. Фармацевтичні композиції, що згадуються у даному описі, містять приблизно від 0,1 до 1000мг на стандартну дозу, наприклад, таблетку, капсулу, порошок, ін'єкцію, супозиторій, чайну ложку і подібне, і можуть застосовуватися при дозі приблизно від 0,01 до 200,0мг/кг/день, переважно приблизно від 0,01 до 100мг/кг/день, більш переважно приблизно від 0,5 до 50мг/кг/день, більш переважно приблизно від 1,0 до 25,0мг/кг/день, більш переважно приблизно від 0,5 до 10,0мг/кг/день, найбільш переважно приблизно від 1,0 до 5,0мг/кг/день або у будь-якому діапазоні всередині вказаних. Однак дозування можна варіювати в залежності від потреб пацієнтів, тяжкості підлягаючого лікуванню стану і використовуваної сполуки. Можна застосовувати щоденне введення або постперіодичне дозування. Перевалено, якщо ці композиції знаходяться у вигляді одиничної дозованої форми, вибраної з таких форм як таблетки, пілюлі, капсули, порошки, гранули, стерильні розчини або суспензії для парентерального введення, дозований аерозоль або рідкі спреї, краплі, ампули, автоінжекторні пристрої або супозиторії для перорального, парентерального, внутрішньоносового, під'язикового або ректального введення або для введення за допомогою інгаляції або інсуфляції. Інакше, композицію можна представити у вигляді, придатному для введення один раз на тиждень або один раз на місяць; наприклад, нерозчинну сіль активної сполуки, таку як сіль деканоат, можна адаптувати для забезпечен 94077 30 ня запасу препарату для внутрішньом'язової ін'єкції. Для приготування твердих композицій, таких як таблетки, основний активний інгредієнт змішують з фармацевтичним носієм, наприклад, звичайними інгредієнтами таблетування, такими як кукурудзяний крохмаль, лактоза, сахароза, сорбіт, тальк, стеаринова кислота, стеарат магнію, дикальційфосфат або смоли, та іншими фармацевтичними розріджувачами, наприклад, водою, з утворенням твердої попередньої композиції, що містить гомогенну суміш сполуки за даним винаходом або її фармацевтично прийнятної солі. Називаючи ці попередні композиції гомогенними, вважають, що активний інгредієнт рівномірно диспергований по всій композиції, таким чином, що композицію можна легко поділити на рівно ефективні дозовані форми, такі як таблетки, пілюлі і капсули. Ці тверді попередні композиції потім ділять на одиничні дозовані форми описаних вище типів, що містять від 0,01 приблизно до 1000мг активного інгредієнта за даним винаходом. На таблетки або пілюлі з нової композиції можна нанести покриття або, поіншому, скомбінувати їх для одержання дозованої форми, що забезпечує перевагу тривалої дії. Наприклад, таблетка або пілюля може містити внутрішній і зовнішній дозовані компоненти, причому останній знаходиться у вигляді оболонки поверх першого. Два компоненти можуть бути розділені ентеросолюбільним шаром, який служить для протидії руйнуванню у шлунку і дозволяє внутрішньому компоненту проходити незачепленим у дванадцятипалу кишку або для затримки вивільнення. Для таких ентеросолюбільних шарів або покриттів можна використовувати різноманітні матеріали: матеріали, що включають ряд полімерних кислот, з такими матеріалами як шелак, цетиловий спирт і ацетат целюлози. Рідкі форми, в які можна включати нові композиції за даним винаходом для перорального введення або введення за допомогою ін'єкції, включають водні розчини з придатними смаковими агентами, водні або масляні суспензії і емульсії, що містять смакові агенти, з придатними до їжі оліями, такими як бавовняна олія, кунжутна олія, кокосова олія або арахісова олія, а також еліксири і подібні фармацевтичні носії. Придатні диспергуючі або суспендуючі агенти для водних суспензій включають синтетичні і природні смоли, такі як трагакант, гуміарабік, альгінат, декстран, натрійкарбоксиметилцелюлоза, метилцелюлоза, полівінілпіролідон або желатин. Спосіб лікування депресії, описаний у даному винаході, також можна здійснити, використовуючи фармацевтичну композицію, що включає будь-яку з визначених у даному описі сполук і фармацевтично прийнятний носій. Фармацевтична композиція може містити приблизно від 0,1мг до 1000мг, переважно від 50мг до 500мг сполуки і може знаходитися у будь-якій з форм, придатних для вибраного способу введення. Носії включають необхідні та інертні фармацевтичні наповнювачі, включаючи, але не обмежуючись цим, зв'язуючі, суспендуючі агенти, лубриканти, смакові агенти, підсолоджувачі, консерванти, барвники і покриття. Композиції, придатні для перорального введення, 31 включають тверді форми, такі як пілюлі, таблетки, таблетки у вигляді капсул, капсули (кожний вид включає препарати безпосереднього вивільнення, синхронного вивільнення і тривалого вивільнення), гранули і порошки, і рідкі форми, такі як розчини, сиропи, еліксири, емульсії і суспензії. Форми, придатні для парентерального введення, включають стерильні розчини, емульсії і суспензії. Сполуки за даним винаходом переважно можна вводити у вигляді окремих денних доз, або можна вводити загальну денну дозу, поділивши її на дві, три або чотири дози на день. Крім того, сполуки за даним винаходом можна використовувати як форму для внутрішньоносового введення за допомогою придатних внутрішньоносових носіїв місцевого застосування або як трансдермальні шкірні пластири, добре відомі фахівцеві у даній галузі. Звичайно, при трансдермальній системі доставки введення дози буде скоріше безперервним, ніж періодичним, протягом всієї схеми прийому. Наприклад, для перорального прийому у вигляді таблетки або капсули активний лікарський компонент можна об'єднати з нетоксичним фармацевтично прийнятним інертним носієм для перорального прийому, таким як етанол, гліцерин, вода і подібні. Більш того, якщо бажано або необхідно, можна також включити у суміш придатні зв'язуючі, лубриканти, розпушувачі і барвники. Придатні зв'язуючі включають (без обмеження) крохмаль, желатин, природні цукри, такі як глюкоза або бета-лактоза, кукурудзяні підсолоджувачі, природні і синтетичні смоли, такі як гуміарабік, трагакант або олеат натрію, стеарат натрію, стеарат магнію, бензоат натрію, ацетат натрію, хлорид натрію і подібні. Розпушувачі включають (без обмеження) крохмаль, метилцелюлозу, агар, бентоніт, ксантанову смолу і подібні. Рідкі форми у суспендуючих або диспергуючих агентах з придатними смаковими агентами, таких як синтетичні і природні смоли, наприклад, трагакант, гуміарабік, метилцелюлоза і подібні. Для парентерального введення потрібні стерильні суспензії і розчини. Коли потрібне внутрішньовенне введення, застосовують ізотонічні препарати, які звичайно містять придатні консерванти. Сполуки за даним винаходом можна вводити у вигляді будь-якої з описаних вище композицій і відповідно до схем прийому доз, встановлених у даній галузі, коли б не було потрібне лікування депресії. Денне дозування продуктів можна варіювати у широкому діапазоні від 0,01 до 200мг/кг для дорослої людини на день або у будь-якому вказаному діапазоні. Для перорального прийому переважно одержують композиції у вигляді таблеток, що містять 0,01, 0,05, 0,1, 0,5, 1,0, 2,5, 5,0, 10,0, 15,0, 25,0, 50,0, 100, 150, 200, 250, 500 і 1000мг активного інгредієнта для симптоматичного регулювання введення дози пацієнту, який приймає лікування. Ефективна кількість ліків звичайно доставляється при рівні доз приблизно від 0,01мг/кг до 200мг/кг маси тіла на день. Переважний діапазон складає приблизно від 0,1 до 100,0мг/кг маси тіла на день, більш переважно, приблизно від 0,5мг/кг до 50мг/кг, більш переважно, приблизно від 1,0 до 94077 32 25,0мг/кг маси тіла на день. Сполуки можна вводити за схемою від 1 до 4 разів на день. Фахівець у даній галузі може легко визначити оптимальні дози, що підлягають введенню, і варіювати їх в залежності від конкретної використовуваної сполуки, способу введення, сили препарату і прогресування хворобливого стану. Крім того, необхідність регулювання дозування обумовлюють фактори, що стосуються підлягаючого лікуванню конкретного пацієнта, включаючи вік, масу, харчування пацієнта і час введення. Фахівцеві у даній галузі зрозуміло, що і 1N vivo, і 1N vitro випробування, що використовують придатні відомі і загальноприйняті клітинні і/або тваринні моделі, передбачають здатність досліджуваної сполуки лікувати або попереджати даний розлад. Крім того, фахівцеві у даній галузі зрозуміло, що клінічні випробування на людях, які включають перші дослідження на людях діапазону доз і ефективності, можна виконати на здорових пацієнтах і/або пацієнтах, які страждають від даного розладу, відповідно до способів, добре відомих у клінічній і медичній практиці. Подані нижче приклади наведені для допомоги у розумінні винаходу і жодним чином не призначені і не повинні тлумачитися як обмеження винаходу, викладеного у формулі винаходу, яка наведена далі. Приклад 1 ((3,4-Дигідро-2Н-бензо[b][1,4]діоксепін-3іл)метил)сульфамід (сполука №3) Катехол (5,09г, 46,2ммоль) і карбонат калію об'єднували в ацетонітрилі і нагрівали при кип'ятінні зі зворотним холодильником протягом однієї години. Додавали 2-хлорметил-3-хлор-1-пропен (5,78г, 46,2ммоль) і продовжували взаємодію при кип'ятінні зі зворотним холодильником протягом 24 годин. Розчин охолоджували до кімнатної температури і фільтрували. Фільтрат випарювали і залишок розбавляли водою і екстрагували діетиловим ефіром (3×). Об'єднаний органічний розчин сушили над MgSO4 і концентрували. Хроматографія (2% етиловий ефір у гексані) давала 3метилен-3,4-дигідро-2Н-бензо[b][1,4]діоксепін у вигляді безбарвного масла. MC (ESI): 163,2 (М+Н+). 1 H ЯМР (300МГц, CDCI3) δ: 6,94 (м, 4Н), 5,07 (с, 2Н), 4,76 (с, 4Н). 3-Метилен-3,4-дигідро-2Нбензо[b][1,4]діоксепін (5,00г, 30,8ммоль) розчиняли у сухому ТГФ (100мл). Додавали при 0°С боранТГФ (1,0Μ у ТГФ, 10,3мл). Реакційну суміш перемішували при к.т. протягом 5 годин. Додавали аміносульфонову кислоту (6,97г, 61,6ммоль). Реакційну суміш нагрівали при кип'ятінні зі зворотним холодильником протягом ночі. Охолоджували реакційну суміш до кімнатної температури і додавали водний гідроксид натрію (3,0М, 100мл). Розчин екстрагували етилацетатом (3×100мл). Об'єднаний органічний розчин сушили над MgSO4. Розчин 33 концентрували у вакуумі і очищали методом хроматографії (від 2% до 8% метанолу у дихлорметані), з одержанням ((3,4-дигідро-2Нбензо[b][1,4]діоксепін-3-іл)метил)аміну у вигляді безбарвного масла. MC (ESI): 180,1 (М+Н+) 1 H ЯМР (300МГц, CDCI3) δ: 6,92 (м, 4Н), 4,21 (м, 2Н), 4,07 (м, 2Н), 3,33 (широкий, 2Н), 3,16 (д, J=4Гц, 1Н), 2,72 (д, J=4Гц, 1Н), 2,30 (м, 1Н). ((3,4-Дигідро-2Н-бензо[b][1,4]діоксепін-3іл)метил)амін (2,90г, 16,2ммоль) і сульфамід (3,11г, 32,4ммоль) об'єднували у сухому діоксані (60мл) і нагрівали при кип'ятінні зі зворотним холодильником протягом ночі. Додавали хлороформ і осад видаляли фільтруванням. Фільтрат концентрували у вакуумі і очищали методом хроматографії (від 2% до 8% ацетону у дихлорметані), з одержанням вказаної у заголовку сполуки у вигляді не зовсім білої твердої речовини. МС 258,8 (М+Н+) 1 H ЯМР (300МГц, ДМСО) δ: 6,92 (м, 4Н), 6,71 (широкий, 1Н), 6,59 (широкий, 2Н), 4,19 (м, 2Н), 4,04 (м, 2Н), 3,00 (м, 2Н), 2,39 (м, 1Н). Приклад 2 N-(2,3-Дигідробензо[1,4]діоксин-2ілметил)сульфамід (сполука №1) Рацемічний 2,3-дигідро-1,4-бенздіоксин-2ілметиламін (4,4г, 26ммоль) і сульфамід (5,1г, 53ммоль) об'єднували в 1,4-діоксані (100мл) і кип'ятили зі зворотним холодильником протягом 2 годин. Реакційну суміш охолоджували до кімнатної температури і невелику кількість твердої речовини відфільтровували і відкидали. Фільтрат випарювали у вакуумі і залишок очищали, використовуючи колонку для флеш-хроматографії (ДХМ:метанол=10:1) з одержанням білої твердої речовини. Тверду речовину перекристалізовували з ДХМ, з одержанням вказаної у заголовку сполуки у вигляді білої твердої речовини. Т. пл.: 97,5-98,5°С. Елементний аналіз: Розрахунок: С, 44,25; Н, 4,95; N, 11,47; S, 13,13; Знайдено: С, 44,28; Н, 4,66; N, 11,21; S, 13,15. 1 H ЯМР (ДМСО-d6) δ: 6,85 (м, 4Н), 6,68 (широкий с, 3Н, ΝΗ), 4,28 (м, 2Н), 3,97(дд, J=6,9, 11,4Гц, 1Н), 3,20 (м, 1Н),3,10 (м, 1Н). Приклад 3 (Бензо[1,3]дiоксол-2-ілметил)сульфамід (сполука №2) Катехол (10,26г, 93,2ммоль), метилат натрію (25% мас. у метанолі, 40,3г, 186ммоль) і метилдихлорацетат (13,3г, 93,2ммоль) об'єднували у сухому метанолі (100мл). Розчин нагрівали при кип'ятінні зі зворотним холодильником протягом ночі. Реакційну суміш охолоджували до кімнатної тем 94077 34 ператури, підкислювали, додаючи концентровану соляну кислоту, і потім зменшували об'єм приблизно до 50мл у вакуумі. Додавали воду і суміш екстрагували діетиловим ефіром (3×100мл). Об'єднаний органічний розчин сушили MgSO4, концентрували до коричневої твердої речовини і хроматографували (2% етилацетат у гексані) з одержанням метилового ефіру бензо[1,3]діоксол2-карбонової кислоти у вигляді безбарвного масла. MC (ESI): 195,10 (М+H+). 1 H ЯМР (300МГц, CDCI3) δ: 6,89 (широкий, 4Н), 6,29 (с, 1Н), 4,34 (кв, J=7Гц, 2Н), 1,33 (т, J=7Гц, 3Н). До метилового ефіру бензо[1,3]діоксол-2карбонової кислоти (7,21г, 40,0ммоль) додавали гідроксид амонію (29% у воді, 10мл) і досить ацетонітрилу, щоб суміш була гомогенною (~5мл). Розчин перемішували протягом години при кімнатній температурі і потім додавали дистильовану воду. Амід бензо[1,3]діоксол-2-карбонової кислоти, що випав в осад у вигляді білої твердої речовини, збирали фільтруванням і використовували без додаткового очищення. MC (ESI): 160,00 (М+Н+). 1 H ЯМР (300МГц, ДМСО) δ: 7,99 (с, широкий, 1Н), 7,72 (с, широкий, 1Н), 6,94 (м, 2Н) 6,86 (м, 2Н), 6,30 (с, 1Н). Амід бензо[1,3]діоксол-2-карбонової кислоти (5,44г, 32,9ммоль) розчиняли у тетрагідрофурані (ТГФ, 100мл). Повільно додавали до розчину при кімнатній температурі літійалюмінійгідрид (ЛАГ, 1М у ТГФ, 39,5мл, 39,5ммоль). Реакційну суміш перемішували при кімнатній температурі протягом 24 годин. Додавали дистильовану воду для розкладання надлишку ЛАГ. Додавали водний гідроксид натрію (3,0М, 100мл) і розчин екстрагували етилацетатом (3×100мл). Об'єднаний органічний розчин промивали водою і сушили над MgSO4. Розчинник випарювали з одержанням С-бензо[1,3]діоксол-2ілметиламіну у вигляді безбарвного масла. MC (ESI): 152,1 (M+H+). 1 H ЯМР (300МГц, CDCI3) δ: 6,87 (м, 4Н), 6,09 (т, J=4Гц, 1Н), 3,13 (д, J=4H), 2Н). С-Бензо[1,3]діоксол-2-ілметиламін (2,94г, 19,4ммоль) і сульфамід (3,74г, 38,9ммоль) об'єднували у сухому діоксані (50мл) і розчин нагрівали при кип'ятінні зі зворотним холодильником протягом ночі. Реакційну суміш концентрували і залишок хроматографували (від 2% до 10% ацетону у дихлорметані) з одержанням вказаної у заголовку сполуки у вигляді білої твердої речовини. МС (ESI): 230,0 (М+Н+). 1 H ЯМР (300МГц, CDCI3) δ: 6,87 (м, 4Н), 6,25 (т, J=4Гц, 1Н), 4,79 5 (широкий, 1Н), 4,62 (широкий, 1Н), 3,64 (д, J=4Гц, 2Н). Приклад 4 (2S)-(-)-N-(2,3-Дигідробензо[1,4]діоксин-2ілметил)сульфамід (сполука №4) 35 Катехол (13,2г, 0,12моль) і карбонат калію (16,6г, 0,12моль) перемішували у ДМФА (250мл), додавали (2R)-гліцидилтозилат (22,8г, 0,10моль) і реакційну суміш перемішували при 60°С протягом 24 годин. Охолоджували реакційну суміш до кімнатної температури, розбавляли льодяною водою (1л) і екстрагували діетиловим ефіром (4 рази). Об'єднаний органічний розчин промивали 3 рази 10% карбонатом калію, один раз водою, один раз насиченим розчином солі і випарювали у вакуумі, з одержанням білої твердої речовини, яку очищали методом колонкової флеш-хроматографії (ДХМ:метанол=50:1), з одержанням ((2S)-2,3дигідробензо[1,4]діоксин-2-іл)метанолу у вигляді твердої речовини. Тверду речовину (13,3г, 68ммоль) розчиняли у піридині (85мл), охолодженому до 0°С, додавали пара-толуолсульфонілхлорид (13,0г, 68ммоль) і реакційну суміш перемішували при кімнатній температурі протягом 20 годин. Реакційну суміш розбавляли діетиловим ефіром (1л) і 1N HCІ (1,2л). Органічний шар відділяли і промивали 2 рази 1N HCІ (500мл), 4 рази водою (150мл), один раз насиченим розчином солі, сушили (MgSO4) і випарювали у вакуумі, з одержанням білої твердої речовини, яку очищали методом колонкової флешхроматографії (Hept:EA=2:1), з одержанням (2S)2,3-дигідробензо[1,4]діоксин-2-ілметилового ефіру толуол-4-сульфонової кислоти у вигляді білої твердої речовини. Білу тверду речовину об'єднували з фталімідом калію (14,4г, 78ммоль) у ДМФА (250мл) і нагрівали при кип'ятінні зі зворотним холодильником протягом 1 години, охолоджували до кімнатної температури, виливали у воду, що енергійно перемішується (1,5л), і перемішували 30хв. Білу тверду речовину відфільтровували і тверду речовину промивали декілька разів водою, 2% NaOH і знову водою, і сушили на повітрі, з одержанням (2S)-2(2,3-дигідробензо[1,4]діоксин-2-ілметил)ізоіндол1,3-діону у вигляді білої порошкової твердої речовини. Порошкоподібну білу тверду речовину об'єднували з гідразином (2,75г, 86ммоль) в ЕtOН (225мл) і нагрівали при кип'ятінні зі зворотним холодильником протягом 2 годин, охолоджували до кімнатної температури, додавали 1N HCІ до рН1,0 і перемішували протягом 15хв. Білу тверду речовину відфільтровували і промивали свіжим ЕtOН (тверду речовину відкидають), фільтрат випарювали у вакуумі до твердої речовини, яку розподіляли між діетиловим ефіром і розбавленим водним NaOH. Розчин у діетиловому ефірі сушили (Na2SO4) і випарювали у вакуумі з одержанням світло-жовтого масла. Масло очищали методом колонкової флеш-хроматографії (ДХМ:МеОН=10:1) з одержанням масла. Частину масла (4,82г, 29ммоль) в 2-пропанолі (250мл) обробляли 1N HCІ (30мл) і нагрівали на паровій бані до гомогенності і потім давали охолонути до кімнатної температури. Через 3 години суміш охолоджували на льоді протягом 2 годин. Білу пластівчасту тверду речовину (відповідну НСІ-сіль (2S)-C-(2,3дигідробензо[1,4]діоксин-2-іл)метиламіну) відфіль 94077 36 тровували і потім знову перекристалізовували з 2пропанолу з одержанням білої твердої речовини. [α]D=-69,6 (c=1,06, EtOH). Білу тверду речовину розподіляли між ДХМ і розбавленим NaOH, ДХМ-фракцію сушили (Na2SO4) і випарювали у вакуумі з одержанням (2S)-C-(2,3-дигідробензо[1,4]діоксин-2іл)метиламіну у вигляді масла. [α]D=-57,8 (c=1,40, СНСІ3). Масло (2,1г, 12,7ммоль) і сульфамід (2,44г, 25,4ммоль) кип'ятили зі зворотним холодильником у діоксані (75мл) протягом 2 годин і неочищений продукт очищали методом колонкової флешхроматографії (ДХМ:МеОН=10:1) з одержанням білої твердої речовини, яку перекристалізовували з ДХМ з одержанням вказаної у заголовку сполуки у вигляді білої кристалічної твердої речовини. Т.пл. 102-103°С; [α]D=-45,1° (c=1,05, M); 1 H ЯМР (ДМСО-d6) δ: 6,86 (м, 4Н), 6,81 (широкий с, 3Н, ΝΗ), 4,3 (м, 2Н), 3,97 (дд, J=6,9, 11,4Гц, 1Н), 3,20 (дд, J=5,5, 13,7Гц, 1Н), 3,10 (дд, J=6,9, 13,7Гц, 1Н). Елементний аналіз: Розрахунок: С, 44,25; Н, 4,95; N, 11,47; S, 13,13; Знайдено: С, 44,20; Н, 4,69; N, 11,40; S, 13,22. Приклад 5 N-(2,3-Дигідробензо[1,4]діоксин-2-ілметил)N',N'-диметилсульфамід (сполука №6) Рацемічний 2,3-Дигідро-1,4-бенздіоксин-2ілметиламін (8,25г, 5,0ммоль) і триетиламін (1,52г, 15ммоль) об'єднували у ДМФА (10мл) і охолоджували на бані з льодом, додавали диметилсульфамоїлхлорид (1,44г, 10ммоль). Потім реакційну суміш перемішували протягом 3 годин при безперервному охолоджуванні. Реакційну суміш розподіляли між етилацетатом і водою і етилацетатний розчин промивали насиченим розчином солі, сушили (MgSO4) і випарювали у вакуумі з одержанням масла. Масло очищали, використовуючи колонку для флеш-хроматографії (етилацетат:гептан=1:1) і одержуючи білу тверду речовину, яку перекристалізовували (етилацетат/гексан), з одержанням вказаної у заголовку сполуки у вигляді білої пластівчастої твердої речовини. Т.пл. 76-78°С; МС 273 (МН+). Елементний аналіз: Розрахунок: С, 48,52; Н, 5,92; N, 10,29; S, 11,78; Знайдено: С, 48,63; Н, 5,62; N, 10,20; S, 11,90. 1 Н ЯМР (CDCI3) δ: 6,87 (м, 4Н), 4,59 (широкий м, 1H, ΝΗ), 4,35 (м, 1Н), 4,27 (дд, J=2,3, 11,4Гц, 1Н), 4,04 (дд, J=7,0, 11,4, 1Н), 3,36 (м, 2Н), 2,82 (с, 6Н). Приклад 6 N-(2,3-Дигідробеизо[1,4]діоксин-2-ілметил)-Nметилсульфамід (сполука №7) 37 Рацемічний 2,3-дигідро-1,4-бенздіоксин-2ілметиламін (825мг, 5ммоль) розчиняли в етил форміаті (15мл), кип'ятили зі зворотним холодильником протягом 30 хвилин і випарювали у вакуумі з одержанням N-(2,3-дигідробензо[1,4]діоксин-2ілметил)формаміду у вигляді масла. Масло у діетиловому ефірі (25мл) обробляли 1М ЛАГ у ТГФ (9,0мл, 9,0ммоль) при 0°С і перемішували протягом 5 годин при кімнатній температурі. Реакційну суміш охолоджували на бані з льодом і гасили водою (0,50мл) з подальшим доданням 3N NaOH (0,50мл) і води (0,50мл). Потім суміш перемішували при кімнатній температурі протягом 1 години. Тверду речовину відфільтровували і випарювали фільтрат у вакуумі, одержуючи залишок, який розподіляли між 1N HCІ і діетиловим ефіром. Водну фазу підлуговували 1N NaOH і екстрагували діетиловим ефіром. Органічну фазу сушили (MgSO4) і випарювали у вакуумі з одержанням (2,3-дигідробензо[1,4]діоксин-2ілметил)метиламіну у вигляді масла. МС 180 (МН+); 1 Н ЯМР (CDCI3) δ: 6,85 (м, 4Н), 4,30 (м, 2Н), 4,02 (дд, J=7,9, 11,6Гц, 1Н), 2,85 (м, 2Н), 2,50 (с, 3Н). Масло (380мг, 2,1ммоль) і сульфамід (820мг, 8,5ммоль) об'єднували у діоксані (15мл), кип'ятили зі зворотним холодильником протягом 1,5 години і випарювали у вакуумі, одержуючи сирий залишок. Залишок очищали методом колонкової хроматографії (етилацетат/гептан=1:1) і одержану тверду речовину перекристалізовували з суміші етилацетат/гексан з одержанням вказаної у заголовку сполуки у вигляді білої твердої речовини. Т.пл. 97-98°С; МС 257 (М-1). Елементний аналіз: Розрахунок: С, 46,50; Н, 5,46; N, 10,85; S, 12,41; Знайдено: С, 46,48; Н, 5,65; N, 10,90; S, 12,07. 1 Н ЯМР (CDCI3) δ: 6,86 (м, 4Н), 4,52 (ш.с, 2Н), 4,46 (м, 1Н), 4,29 (дд, J=2,3, 11,5Гц, 1Н), 4,05 (дд, J=6,5, 11,5Гц, 1Н), 3,51 (дд, J=6,7, 14,9Гц, 1Н), 3,40 (дд, J=5,9, 14,9Гц, 1Н), 2,99 (с, 3Н). Приклад 7 (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин2-ілметил)сульфамід (сполука №8) Дотримуючись методики, описаної вище у прикладі 4, проводили взаємодію 4-хлоркатехолу, одержуючи суміш (2S)-С-(7-хлор-2,3дигідробензо[1,4]діоксин-2-іл)метиламіну і (2S)-С(6-хлор-2,3-дигідробензо[1,4]діоксин-2іл)метиламіну (співвідношення ізомерів 6-хлор:7хлор становило приблизно 3:1 за даними ОФ ВЕРХ). 94077 38 Суміш розчиняли у 2-пропанолі (100мл) і додавали 1N HCІ у діетиловому ефірі до досягнення рН1,0. Сіль гідрохлориду, яка випадала в осад, відфільтровували (2,65г) і перекристалізовували з суміші метанол/ІРА з одержанням білих кристалів. Білі кристали розподіляли між ДХМ і розбавленим NaOH. ДХМ-фазу сушили і випарювали у вакуумі з одержанням очищеного (2S)-С-(6-хлор-2,3дигідробензо[1,4]діоксин-2-іл)метиламіну у вигляді масла. [α]D=-67,8 (c=1,51, CHCl3). Масло (7,75ммоль) і сульфамід (1,50г, 15,5ммоль) об'єднували у діоксані (50мл) і кип'ятили зі зворотним холодильником протягом 2,0 годин, охолоджували до кімнатної температури і випарювали у вакуумі з одержанням твердої речовини. Продукт очищали методом колонкової флеш-хроматографії, використовуючи суміш ДХМ/метанол=20:1 і одержуючи вказану у заголовку сполуку у вигляді білої твердої речовини. МС 277 (М-1); [α]D=-59,9° (с=1,11 М); 1 H ЯМР (CDCI3) δ: 6,90 (д, J=2,2Гц, 1Н), 6,81 (м, 2H), 4,76 (м, 1Н), 4,55 (с, 2Н), 4,40 (м, 1Н), 4,29 (дд, J=2,4, 11,5Гц, 1Н), 4,05 (дд, J=7,1, 11,5Гц, 1Н), 3,45 (м, 2Н). Елементний аналіз: Розрахунок: С, 38,78; Η, 3,98; Ν, 10,05; Знайдено: С, 38,80; Η, 3,67; Ν, 9,99. Фільтрати утвореної внаслідок кристалізації одержаної вище солі гідрохлориду (2S)-С-(6-хлор2,3-дигідробензо[1,4]діоксин-2-іл)метиламіну відділяли (співвідношення ізомерів 6-хлор:7-хлор становило приблизно 1:1) і випарювали у вакуумі з одержанням твердої речовини, яку розподіляли між ДХМ (200мл) і розбавленим NaOH (0,5Μ, 50мл). ДХМ-розчин промивали один раз насиченим розчином солі, сушили (Na2SO4) і випарювали у вакуумі з одержанням масла, яке очищали методом ВЕРХ з оберненою фазою (10-50% ACN з 0,16% ТФО у воді з 0,20% ТФО) з одержанням у залишку (2S)-С-(7-хлор-2,3дигідробензо[1,4]діоксин-2-іл)метиламіну. Залишок об'єднували з сульфамідом (0,90г, 9,4ммоль) у діоксані (25мл) і кип'ятили зі зворотним холодильником протягом 2,5 годин, охолоджували до кімнатної температури і випарювали у вакуумі з одержанням масла. Масло очищали методом колонкової флеш-хроматографії, використовуючи суміш ДХМ/метанол=10:1 і одержуючи (2S)-(-)-N-(7-хлор-2,3-дигідробензо[1,4]діоксин-2ілметил)сульфамід у вигляді білої твердої речовини. МС 277 (М-1); 1 Н ЯМР (CDCI3/CD3OD) δ: 6,88 (д, J=0,7Гц, 1Н), 6,81 (м, 2Н), 4,37 (м, 1Н), 4,30 (дд, J=2,3, 11,6Гц, 1Н), 4,04 (дд, J=7,0, 11,6Гц, 1Н), 3,38 (м, 2Н). Приклад 8 Хроман-2-ілметилсульфамід (сполука №10) 39 Хроман-2-карбонову кислоту (4,5г, 25ммоль) і ГОБТ (3,86г, ммоль) об'єднували у ДХМ (40мл) і ДМФА (10мл). Додавали диметиламінопропілетилкарбодіімід (EDC, 4,84г, 25ммоль) при кімнатній температурі і реакційну суміш перемішували протягом 30 хвилин. Додавали гідроксид амонію (2,26мл, 33,4ммоль) і перемішували реакційну суміш протягом 16 годин. Реакційну суміш розбавляли ДХМ (50мл) і водою (50мл) і доводили рН суміші приблизно до рН3,0 за допомогою 1N HCІ. ДХМ-фазу відділяли і водну фазу двічі екстрагували ДХМ. Об'єднану ДХМ-фазу сушили (Na2SO4) і випарювали у вакуумі, одержуючи масло, яке очищали методом колонкової флешхроматографії (етилацетат) з одержанням масла. Масло (5,35г, 30ммоль) у ТГФ (90мл) перемішували, додавали у цей час 1М ЛАГ у ТГФ (36мл, 36ммоль) і потім реакційну суміш перемішували при кімнатній температурі протягом 20 годин. Реакційну суміш гасили водою, перемішували протягом 2 годин, розчин декантували, сушили (Na2SO4) і випарювали у вакуумі з одержанням С-хроман-2ілметиламіну у вигляді маслянистого аміну. Маслянистий амін (1,63г, 10ммоль) і сульфамід (1,92г, 20ммоль) об'єднували у діоксані (50мл) і доводили до кипіння зі зворотним холодильником протягом 2 годин. Розчин охолоджували і випарювали у вакуумі, одержуючи масло, яке очищали методом колонкової хроматографії (ДХМ:метанол 10:1) з одержанням білої твердої речовини. Тверду речовину перекристалізовували з суміші етилацетат/гексан з одержанням хроман-2ілметилсульфаміду у вигляді білої твердої речовини. Т.пл. 100-101°С; МС 241 (М-1). Елементний аналіз: Розрахунок: С, 49,57; Н, 5,82; N, 11,56; S, 13,23; Знайдено: С, 49,57; Н, 5,80; N, 11,75; S, 13,33. Приклад 9 2-(2,3-Дигідробензо[1,4]діоксин-2іл)етилсульфамід (сполука №16) Додавали ціанід калію (2,05г, 31,5ммоль) до 2бромметил-(2,3-дигідробензо[1,4]діоксину) (6,87г, 30ммоль) у ДМСО (90мл) і перемішували при температурі навколишнього середовища протягом 20 годин. Потім реакційну суміш розбавляли водою (250мл) і двічі екстрагували діетиловим ефіром. Розчин у діетиловому ефірі промивали водою, потім двічі промивали насиченим розчином солі, сушили (Na2SO4) і випарювали у вакуумі з одержанням 2-ціанометил-(2,3дигідробензо[1,4]діоксину) у вигляді білої твердої речовини. 1 Н ЯМР (CDCI3) δ: 6,89 (м, 4Н), 4,50 (м, 1Н), 4,31 (дд, J=2,3, 11,5Гц, 1Н), 4,08 (дд, J=6,2, 11,6Гц, 1Н), 2,78 (д, J=6,1,Гц, 2Н). 2-Ціанометил-(2,3-дигідробензо[1,4]діоксин) розчиняли у ТГФ (50мл), додавали 1М ВН3 у ТГФ (80мл, 80ммоль) і реакційну суміш кип'ятили зі 94077 40 зворотним холодильником протягом 5 годин, потім перемішували при температурі навколишнього середовища протягом 16 годин. При охолоджуванні на бані з льодом додавали 2N НСI до досягнення рН1,0. Потім реакційну суміш перемішували протягом 1 години при кімнатній температурі і випарювали у вакуумі з одержанням масла. Масло розподіляли між 3N NaOH і діетиловим ефіром і розчин у діетиловому ефірі промивали насиченим розчином солі, сушили (Na2SO4) і випарювали у вакуумі з одержанням неочищеного 2-(2,3дигідробензо[1,4]діоксин-2-іл)етиламіну. MS (M+H)+180. Неочищений 2-(2,3-дигідробензо[1,4]діоксин-2іл)етиламін у діоксані (100мл) об'єднували з сульфамідом (3,0г, 31ммоль) і нагрівали при кип'ятінні зі зворотним холодильником протягом 2 годин. Розчин охолоджували і випарювали у вакуумі, одержуючи помаранчеву тверду речовину, яку очищали методом колонкової хроматографії (ДХМ:МеОН=10:1) з одержанням білої твердої речовини. Тверду речовину перекристалізовували з ДХМ з одержанням вказаної у заголовку сполуки у вигляді твердої речовини. МС (М-1) 257; Т.пл. 101-103°С (уточнена); 1 Н ЯМР (CDCI3) δ: 6,86 (м, 4Н), 4,70 (м, 1Н), 4,52 (с, 2Н), 4,30 (м, 2Н), 3,94 (дд, J=7,4, 11,3Гц, 1Н), 3,43 (дд, J=6,4, 12,9Гц, 2Н), 1,94 (дд, J=6,5, 12,9Гц, 2Н). Елементний аналіз: Знайдено: С, 46,48; Н, 5,60; N, 10,81; S, 12,41; Розрахунок: С, 46,50; Н, 5,46; N, 10,85; S, 12,41. Приклад 10 (2S)-(-)-N-(6,7-дихлор-2,3дигідробензо[1,4]діоксин-2-ілметил)сульфамід (сполука №29) 4,5-Дихлоратехол (8,6г, 48ммоль) і карбонат калію (6,64г, 48ммоль) перемішували у ДМФА (200мл). Додавали (2R)-гліцидилтозилат (9,12г, 40ммоль) і реакційну суміш перемішували при 60°С протягом 24 годин. Реакційну суміш охолоджували до кімнатної температури і потім розбавляли льодяною водою (600мл) і екстрагували діетиловим ефіром (4 рази). Об'єднаний органічний розчин промивали 3 рази 10% карбонатом калію, двічі насиченим розчином солі, сушили (MgSO4) і випарювали у вакуумі з одержанням в'язкого масла (2S)-2-(6,7-дихлор-2,3дигідробензо[1,4]діоксин)метанолу. Масло (2S)-2-(6,7-дихлор-2,3дигідробензо[1,4]діоксин)метанол (6,4г, 27ммоль) розчиняли у піридині (50мл) і охолоджували до 0°С. Потім додавали пара-толуолсульфонілхлорид (5,2г, 27ммоль) і реакційну суміш перемішували при кімнатній температурі протягом 20 годин. Реакційну суміш розбавляли діетиловим ефіром і 1N HCІ (750мл) і органічний шар відділяли і промивали 2 рази 1N HCІ (250мл), один раз водою (150мл), 41 двічі насиченим розчином солі, сушили (MgSO4) і випарювали у вакуумі з одержанням світло-жовтої твердої речовини (2S)-6,7-дихлор-2,3дигідробензо[1,4]діоксин-2-ілметилового ефіру толуол-4-сульфонової кислоти. 1 H ЯМР (CDCI3) δ: 7,79 (д, J=8,3Гц, 2Н), 7,36 (д, J=8,0Гц, 2Н), 6,94 (с, 1Н), 6,83 (с, 1Н), 4,37 (м, 1Η), 4,2 (м, 3Н), 4,03 (дд, J=6,3, 11,7Гц, 1Н), 2,47 (с, 3Н). (2S)-6,7-дихлор-2,3-дигідробензо[1,4]діоксин-2ілметиловий ефір толуол-4-сульфонової кислоти (8,0г, 20,5ммоль) об'єднували з фталімідом калію (6,1г, 33ммоль) у ДМФА (75мл) і нагрівали при кип'ятінні зі зворотним холодильником протягом 1 години, охолоджували до кімнатної температури, виливали у воду, що енергійно перемішується (0,5л), і потім перемішували 30хв. Білу тверду речовину відфільтровували і промивали декілька разів водою, 2% NaOH і знову водою і потім сушили на повітрі з одержанням (2S)-2-(6,7-дихлор-2,3дигідробензо[1,4]дioксин-2-ілметил)ізоіндол-1,3діону (6,0г, 80%) у вигляді білої порошкоподібної твердої речовини. Білу порошкоподібну тверду речовину об'єднували з гідразином (1,06г, 33ммоль) в ЕtOН (80мл) і нагрівали при кип'ятінні зі зворотним холодильником протягом 2 годин, потім охолоджували до кімнатної температури. Додавали 1N НСI, доводячи рН реакційної суміші до рН1,0 і потім реакційну суміш перемішували протягом 15 хвилин. Білу тверду речовину відфільтровували і промивали свіжим ЕtOН (тверду речовину відкидали), фільтрат випарювали у вакуумі, одержуючи тверду речовину, яку розподіляли між діетиловим ефіром і розбавленим водним NaOH. Розчин у діетиловому ефірі сушили (Na2SO4) і випарювали у вакуумі з одержанням в'язкого масла (2S)-2амінометил-(6,7-дихлор-2,3дигідробензо[1,4]діоксину). 1 Н ЯМР (CDCI3) δ: 6,98 (с, 1Н), 6,96 (с, 1Н), 4,25 (дд, J=2,0, 11,2Гц, 1Н), 4,15 (м, 1H), 4,0 (м, 1Н), 2,97 (д, J=5,5Гц, 2Н). Частину масла (3,8г, 16ммоль) і сульфамід (3,1г, 32,4ммоль) кип'ятили зі зворотним холодильником у діоксані (100мл) протягом 2 годин і неочищений продукт очищали методом колонкової флеш-хроматографії (ДХМ:МеОН=20:1), з одержанням вказаної у заголовку сполуки у вигляді білої твердої речовини, яку перекристалізовували з суміші етилацетат/гексан з одержанням вказаної у заголовку сполуки у вигляді білої кристалічної твердої речовини. МС [М-Н]- 311,0; Т.пл. 119-121°С; [α]D=-53,4°(c=1,17, M). 1 H ЯМР (ДМСО-d6) δ: 7,22 (с, 1Н), 7,20 (с, 1Н), 6,91 (широкий с, 1Н), 6,68 (широкий с, 2Н), 4,35 (м, 2Н), 4,05 (дд, J=6,5, 11,5Гц, 1Н), 3,15 (м, 2Н). Елементний аналіз: Знайдено: С, 34,52; Η, 3,22; Ν, 8,95; СІ, 22,64.; S, 10,24; Розрахунок: С, 34,64; Η, 2,68; Ν, 8,87; СІ, 22,94; S, 10,35. Приклад 11 94077 42 (2S)-(-)-N-(7-аміно-2,3дигідробензо[1,4]діоксин-2-ілметил)сульфамід (сполука №36) (2S)-(-)-N-(2,3-дигідро-7-нітробензо[1,4]діоксин2-ілметил)сульфамід (1,2г, 4,15ммоль) одержували з 4-нітрокатехолу відповідно до способу, описаного у прикладі 4. Потім (2S)-(-)-N-(2,3-дигідро-7нітробензо[1,4]діоксин-2-ілметил)сульфамід об'єднували з 10% Pd/C у метанолі (120мл) і струшували в атмосфері водню (2,7кг/см2=39фунт/дюйм2) при кімнатній температурі протягом 3 годин. Тверді речовини відфільтровували і промивали 10%Μ у ДХМ і фільтрат випарювали у вакуумі, одержуючи неочищений продукт. Неочищений продукт розчиняли в 0,2N НСI (25мл), заморожували і ліофілізували з одержанням вказаної у заголовку сполуки у. вигляді білої пластівчастої твердої речовини, відповідної солі гідрохлориду. МС (М+Н)+ 260; 1 Н ЯМР (ДМСО-d6) δ: 10,2 (широкий с, 3Н), 6,86 (м, 1Н), 6,85 (с, 1Н), 6,74 (дд, J=2,5, 8,4Гц, 1Н), 4,22 (м, 2Н), 3,88 (дд, J=6,7, 11,4Гц, 1Н), 3,04 (м, 2Н). Приклад 12 (2S)-(-)-N-(7-метил-2,3дигідробензо[1,4]діоксин-2-ілметил)сульфамід (сполука №19) Вказану у заголовку сполуку одержували відповідно до методики, описаної вище у прикладі 4, виходячи з 4-метилкатехолу і одержуючи білу тверду речовину, яку перекристалізовували з суміші етилацетат/гексан з одержанням вказаної у заголовку сполуки у вигляді білої твердої речовини. MS [М-Н]- 257; 1 Н ЯМР (CDCI3) δ: 6,76 (м, 1Н), 6,66 (м, 2Н), 4,80 (м, 1Н), 4,57 (широкий с, 1Н), 4,40 (м, 1Н), 4,28 (м, 1Н), 4,03 (дд, J=6,9, 11,4Гц, 1Н), 3,45 (м, 2Н), 2,25 (с, 3Н). Елементний аналіз: Розрахунок: С, 46,50; Н, 5,46; N, 10,85; S, 12,41; Знайдено: С, 46,65; Н, 5,60; N, 10,84; S, 12,61. Приклад 13 In vivo дослідження на діабетичних мишах db/db Миші db/db, як відомо у даній галузі, сприйнятливі до діабету типу II (Sharma K, McCue P, Dunn SR. Am J Physiol Renal Physiol. 2003 Jun; 284(6):F1138-44). Як відомо у даній галузі, миші db/db також є придатною моделлю для дисліпідемії. Одержували 8-тижневих самок мишей db/db (C57BL/6J=repdb/db, Jackson Laboratories, Bar Harbor, ME, USA), розміщували по одній і годували у звичайному режимі. Відбір крові проводили, роб 43 94077 лячи прокол в області хвоста, і контролюючи глюкозу за допомогою глюкометра (OneTouch Basic, Lifescan, Newtown, PA). Мишей у віці 10 тижнів ділили випадковим чином на піддослідні групи на основі рівнів глюкози (перший критерій, середнє значення 250мг/дл) і маси тіла (другий критерій, середнє значення 37г). Мишам вводили перорально через зонд один раз на день (0,2мл у 1500-1700год.) контрольний носій (0,5% метилцелюлозу, рН 7,4) і носій, що містить досліджувану сполуку (А 300мг/кг). На 11 день миші голодували протягом 4 годин під час світлового циклу (їжу прибирали о 06.00-10.00 годині), і за допомогою глюкометра у них вимірювали рівні глюкози у крові, роблячи прокол в області хвоста о 10.00 годині. Потім мишей анестезували пентабарбіталом натрію (1мл/кг, внутрішньочеревинно, Sleepaway, Fort Dodge, Iowa), і відбирали кров за допомогою пункції серця і збирали у гепаринізовані пробірки. Вирізали і зважували білий жир (WAT) (ретроперитонеальний жир) і скелетні м'язи (литковий і камбалоподібний м'язи). Зразки плазми одержували центрифугуванням при 2000g і 4°С протягом 15хв. і проводили визначення інсуліну, HDLхолестерину і тригліцеридів. Наведені нижче дані представлені у вигляді середнього значення зі стандартною помилкою, розрахованого при використанні 9-10 мишей на піддослідну групу. Для статистичного аналізу використовували двосторонні t-тести Стьюдента. У всіх дослідженнях на тваринах дотримувалися 44 вказівок Institutional Animal Care and Use Committee. Сполуку №8 оцінювали відповідно до описаної вище методики. Рівні глюкози у крові самок мишей db/db становили 255±15мг/дл за 5 днів до експериментів. У кінці експерименту рівні глюкози у крові контрольних мишей, оброблених носієм, були підвищеними - 166% (420±22мг/дл). Рівні глюкози у крові мишей db/db значно нижчі при обробці сполукою №8 у порівнянні з мишами, обробленими носієм. Рівні інсуліну у тварин, оброблених сполукою №8, не відрізнялися статистично при порівнянні з тваринами, обробленими носієм. Миші, оброблені сполукою №8, демонстрували більшу масу скелетного м'яза у порівнянні з тваринами, обробленими носієм. Крім того, було відсутнє істотне зниження маси жиру у тварин, оброблених сполукою №8. Миші, оброблені сполукою №8, також демонстрували значне зниження співвідношення маси жир:м'ясо (носій: 27,9±1,4 відносно сполуки №8: 23,4±0,9, р
ДивитисяДодаткова інформація
Назва патенту англійськоюUse of benzo-fused heterocycle sulfamide derivatives for lowering lipids and lowering blood glucose levels
Автори англійськоюSmith-Swintosky, Virginia L., Reitz, Allen B.
Назва патенту російськоюПрименение бензоконденсированных гетероциклических сульфамидных производных для снижения уровней липидов и глюкозы в крови
Автори російськоюСмит-Свинтоски Вирджиния Л., Рейтц Аллен Б.
МПК / Мітки
МПК: A61P 3/06, A61K 31/357, A61K 31/535, A61P 3/10, A61K 31/352
Мітки: сульфамідних, застосування, похідних, зниження, глюкози, гетероциклічних, бензоконденсованих, ліпідів, рівнів, крові
Код посилання
<a href="https://ua.patents.su/27-94077-zastosuvannya-benzokondensovanikh-geterociklichnikh-sulfamidnikh-pokhidnikh-dlya-znizhennya-rivniv-lipidiv-i-glyukozi-u-krovi.html" target="_blank" rel="follow" title="База патентів України">Застосування бензоконденсованих гетероциклічних сульфамідних похідних для зниження рівнів ліпідів і глюкози у крові</a>
Наступний патент: Застосування похідних сульфаміду, які включають гетероцикл, конденсований з бензольним кільцем, для лікування депресії
Випадковий патент: Шина












