Безперевний процес перетворення вуглеводневої сировини на один або більше вищих вуглеводнів (варіанти)
Номер патенту: 95276
Опубліковано: 25.07.2011
Автори: Уірста Майкл Д., Гроссо Філіп, Комон Закарі Дж. А., Макфарленд Ерік, Жанг Айхуа, Шерман Джеффрі Х., Гадівар Сагар Б.
Формула / Реферат
1. Безперервний процес перетворення вуглеводневої сировини на один або більше вищих вуглеводнів, який включає:
(a) утворення алкілгалогенідів шляхом реакції молекулярного галогену з вуглеводневою сировиною, яка містить метан, в умовах процесу, достатніх для утворення алкілгалогенідів та гідрогалогеніду, причому практично весь молекулярний галоген витрачають;
(b) утворення перепропорціонованих алкілгалогенідів шляхом реакції деяких або всіх алкілгалогенідів з алканом, який подають, завдяки чому збільшують частку присутніх моногалогенованих вуглеводнів;
(c) контактування перепропорціонованих алкілгалогенідів з першим каталізатором в умовах процесу, достатніх для утворення вищих вуглеводнів та додаткового гідрогалогеніду;
(d) відокремлення вищих вуглеводнів від гідрогалогеніду;
(e) регенерацію молекулярного галогену шляхом контактування гідрогалогеніду з другим каталізатором у присутності джерела кисню в умовах процесу, достатніх для утворення молекулярного галогену та води;
(f) відокремлення молекулярного галогену від води для забезпечення можливості повторного використання галогену; та
(g) повторення етапів з (а) по (f) потрібну кількість разів.
2. Безперервний процес за п. 1, який відрізняється тим, що включає відокремлення моногалогенованих алкілгалогенідів від полігалогенованих алкілгалогенідів після етапів (а) та/або (b).
3. Безперервний процес за п. 1, який відрізняється тим, що вуглеводнева сировина включає один або більше С1-С4 вуглеводнів.
4. Безперервний процес за п. 1, який відрізняється тим, що вуглеводнева сировина включає природний газ.
5. Безперервний процес за п. 1, який відрізняється тим, що галоген означає бром.
6. Безперервний процес за п. 1, який відрізняється тим, що галоген означає хлор.
7. Безперервний процес за п. 1, який відрізняється тим, що завантажуваний алкан містить принаймні 1 % за об'ємом одного або кількох С2-С5 вуглеводнів.
8. Безперервний процес за п. 1, який відрізняється тим, що кількість присутнього(іх) моногалогенованого(их) алкілгалогеніду(ів) збільшують у присутності каталізатора перепропорціонування.
9. Безперервний процес за п. 8, який відрізняється тим, що каталізатор перепропорціонування включає метал, метало-кисневий матеріал або металгалогенід.
10. Безперервний процес за п. 1, який відрізняється тим, що перший каталізатор включає цеоліт.
11. Безперервний процес за п. 10, який відрізняється тим, що цеоліт включає легований металом або іонообмінний цеоліт.
12. Безперервний процес за п. 10, який відрізняється тим, що цеоліт є легований марганцем.
13. Безперервний процес за п. 1, який відрізняється тим, що другий каталізатор включає принаймні один матеріал, вибраний з групи, яка складається з СаО, СеО2, СО3О4, CuO, NiO, MgO, карбідів, нітридів, вугілля та глин.
14. Безперервний процес за п. 1, який відрізняється тим, що другий каталізатор включає CuO або СеO2.
15. Безперервний процес за п. 1, який відрізняється тим, що другий каталізатор включає принаймні один матеріал, вибраний з групи, яка складається з галогенідів, оксидів та оксигалогенідів Ag, Аu, Ва, Са, Се, Co, Cr, Cu, Fe, Mg, Mn, Mo, Nb, Ni, Pb, Pd, Pt, Sr, Та, V, W або Zn.
16. Безперервний процес за п. 1, який відрізняється тим, що гідрогалогенід відокремлюють від вищих вуглеводнів, які містять HBr та водну бромистоводневу кислоту, та HBr відокремлюють від водної бромистоводневої кислоти із застосуванням дистиляції з коливанням тиску або екстрактивної дистиляції.
17. Безперервний процес за п. 16, який відрізняється тим, що відокремлення HBr від водної бромистоводневої кислоти включає застосування екстрактивної дистиляції з водним розчином СаВr2, MgBr2, KBr, NaBr, LiBr або їх сумішей, які застосовують як екстрагуючий агент.
18. Безперервний процес за п. 16, який відрізняється тим, що відокремлення HBr від водної бромистоводневої кислоти включає застосування екстрактивної дистиляції, з сірчаною кислотою, яку застосовують як екстрагуючий агент.
19. Безперервний процес за п. 1, який відрізняється тим, що завантажуваний алкан, який застосовують для перепропорціонування, включає газоподібний вуглеводень, який містить значну кількість С2-С5 вуглеводнів.
20. Безперервний процес за п. 1, який відрізняється тим, що утворення алкілгалогенідів та утворення перепропорціонованих алкілгалогенідів здійснюють в окремих реакторах.
21. Безперервний процес перетворення вуглеводневої сировини на один або більше вищих вуглеводнів, який включає:
(a) утворення алкілгалогенідів шляхом реакції молекулярного галогену з вуглеводневою сировиною, яка містить метан, в реакторі для галогенування, в умовах процесу, достатніх для утворення алкілгалогенідів та гідрогалогеніду, причому практично весь молекулярний галоген витрачають;
(b) відокремлення непрореагованого метану від алкілгалогенідів і спрямування його назад у реактор для галогенування;
(c) утворення перепропорціонованих алкілгалогенідів шляхом реакції деяких або всіх алкілгалогенідів з алканом, який подають, і який містить принаймні 1 % за об'ємом С2-С5 вуглеводнів, завдяки чому збільшують частку присутніх моногалогенованих вуглеводнів;
(d) контактування перепропорціонованих алкілгалогенідів з першим каталізатором в умовах процесу, достатніх для утворення вищих вуглеводнів та додаткового гідрогалогеніду;
(e) відокремлення вищих вуглеводнів від гідрогалогеніду;
(f) регенерацію молекулярного галогену шляхом контактування гідрогалогеніду з другим каталізатором у присутності джерела кисню в умовах процесу, достатніх для утворення молекулярного галогену та води;
(g) відокремлення молекулярного галогену від води для забезпечення можливості повторного використання галогену; та
(h) повторення етапів з (а) по (g) потрібну кількість разів.
22. Безперервний процес за п. 21, який відрізняється тим, що утворення алкілгалогенідів та утворення перепропорціонованих алкілгалогенідів здійснюють в окремих реакторах.
Текст
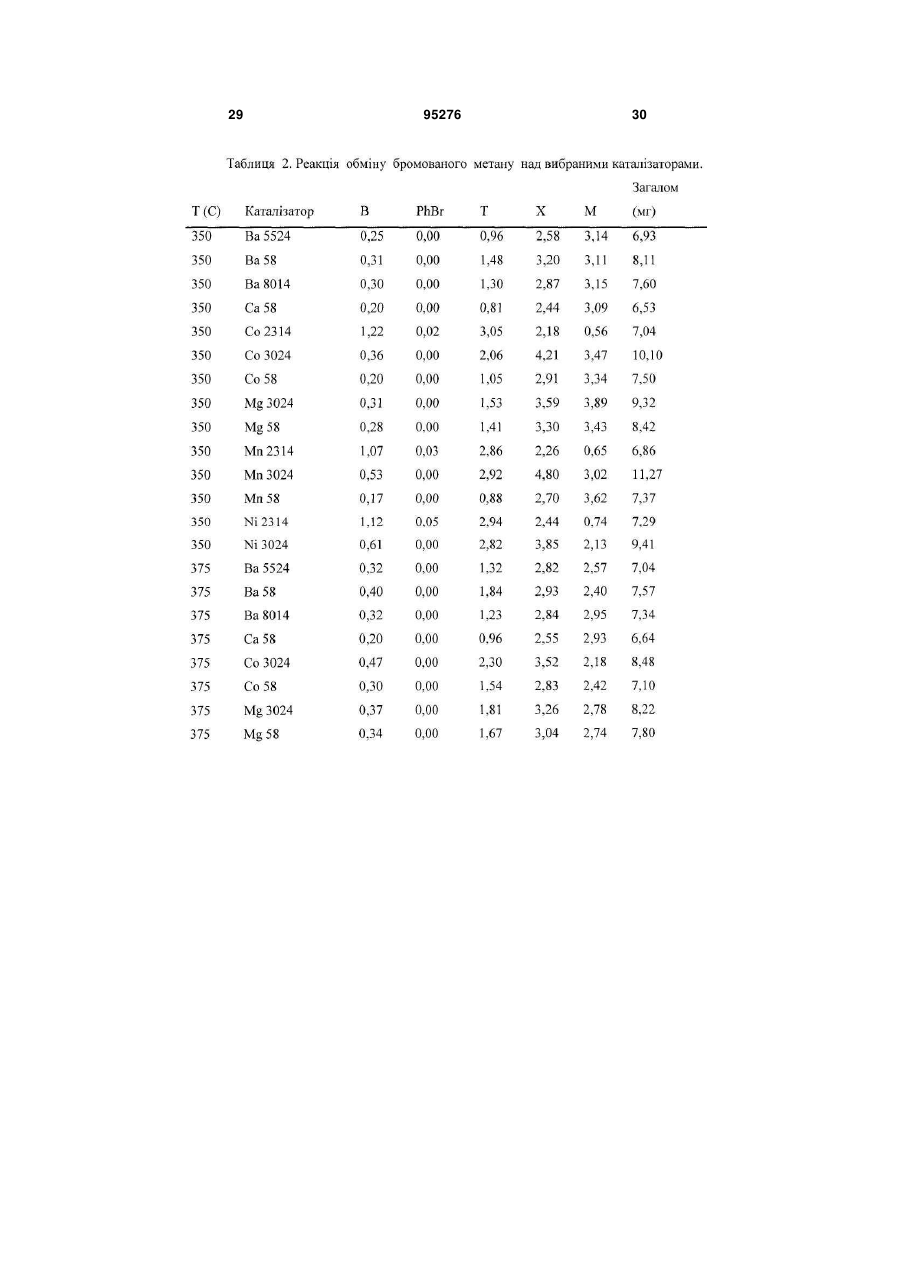
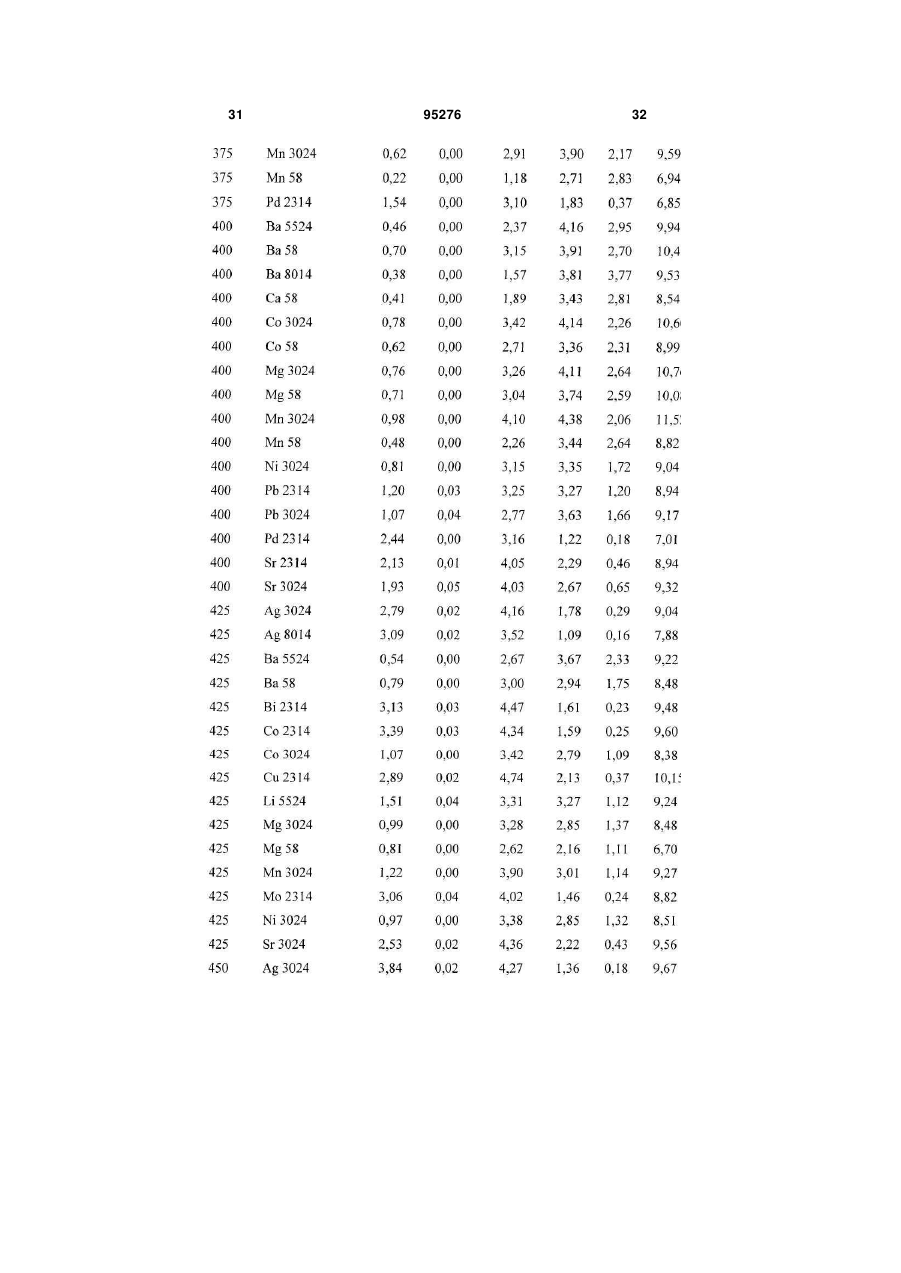
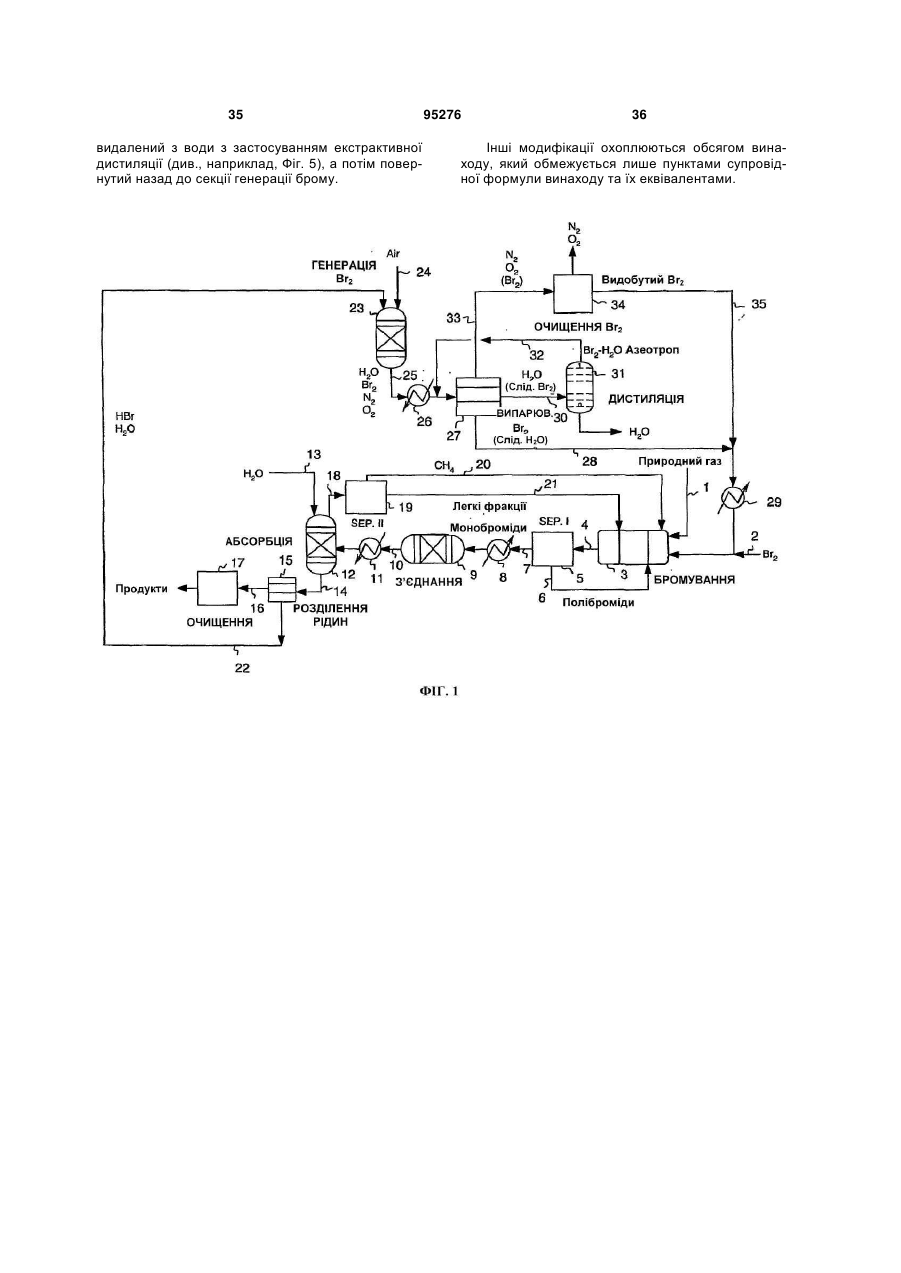
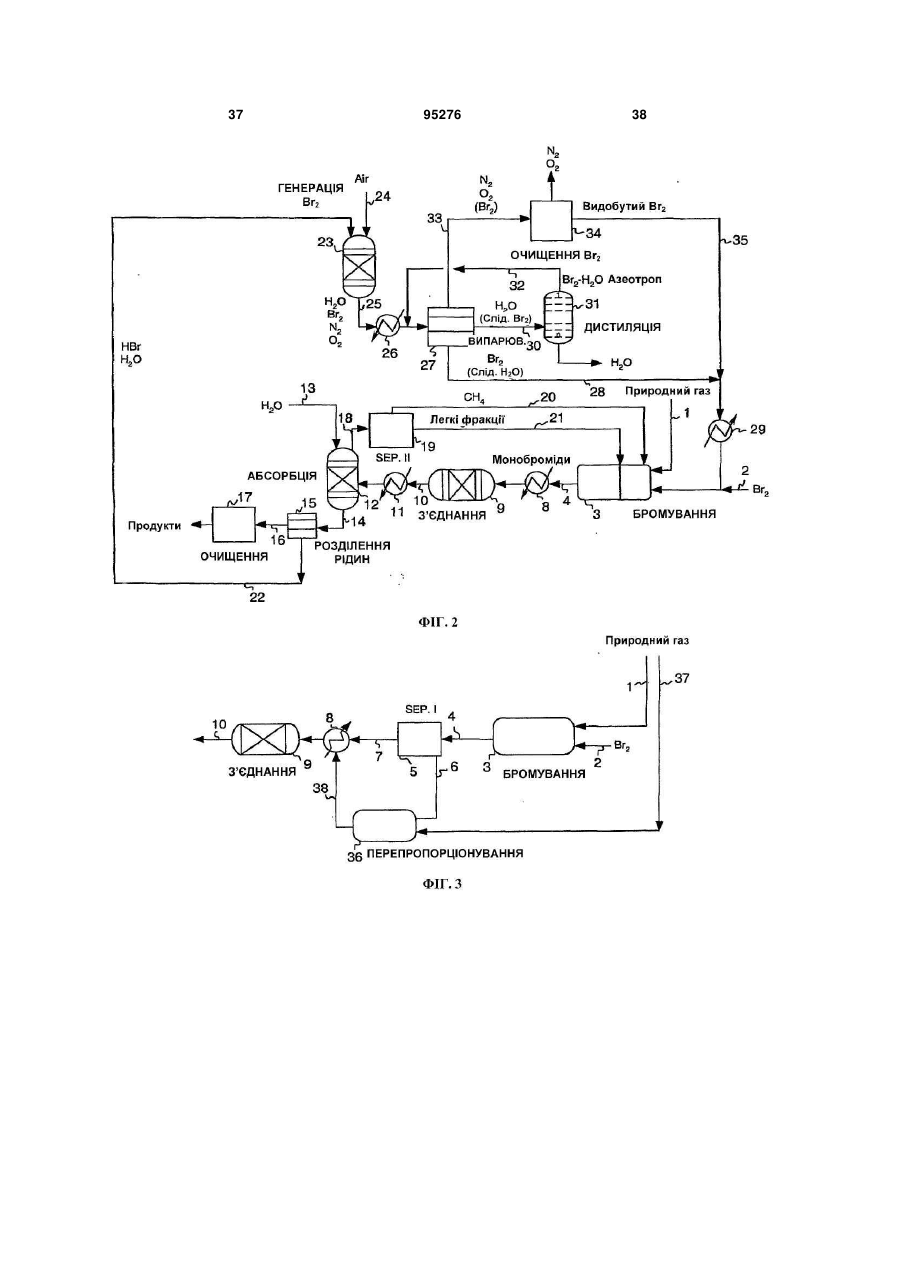
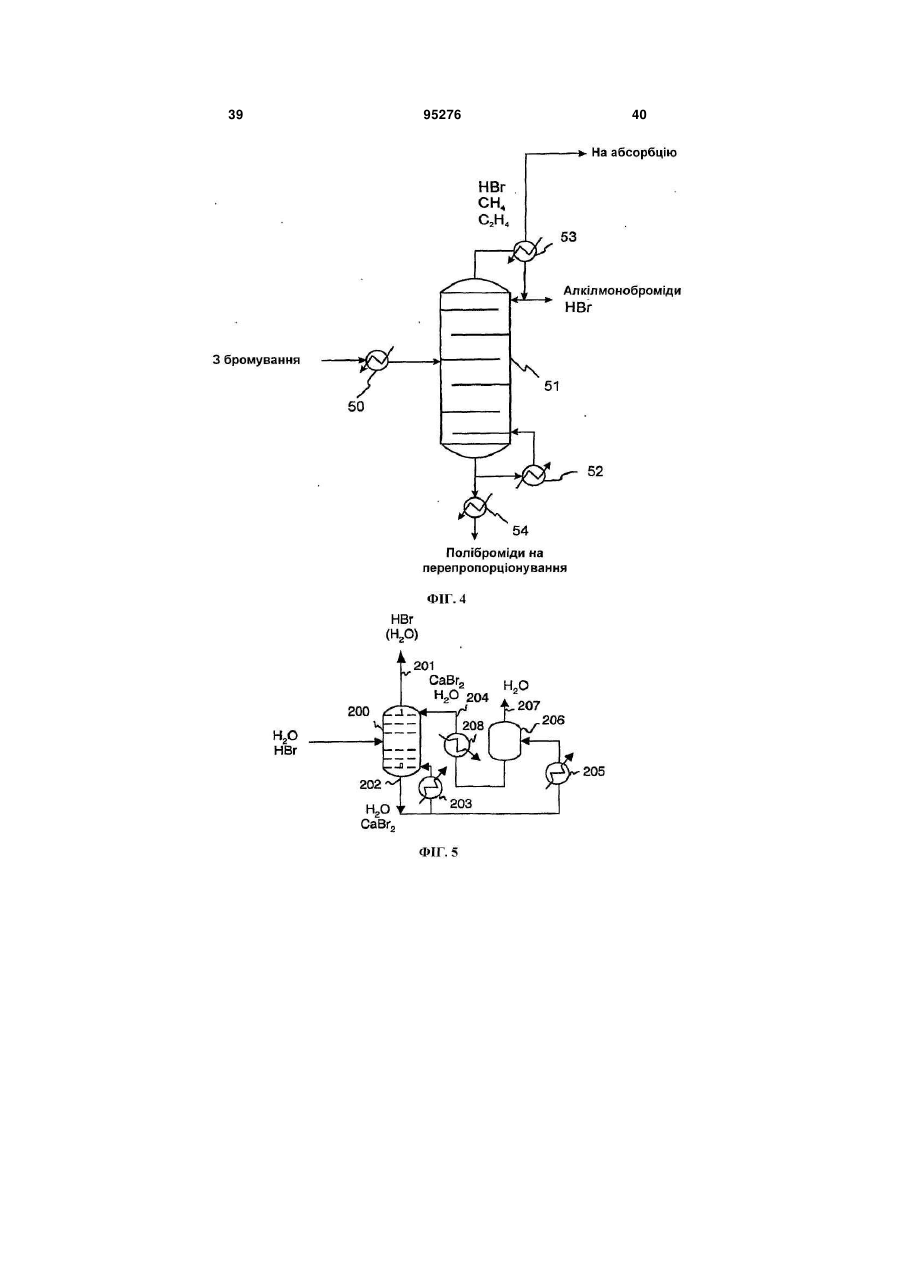
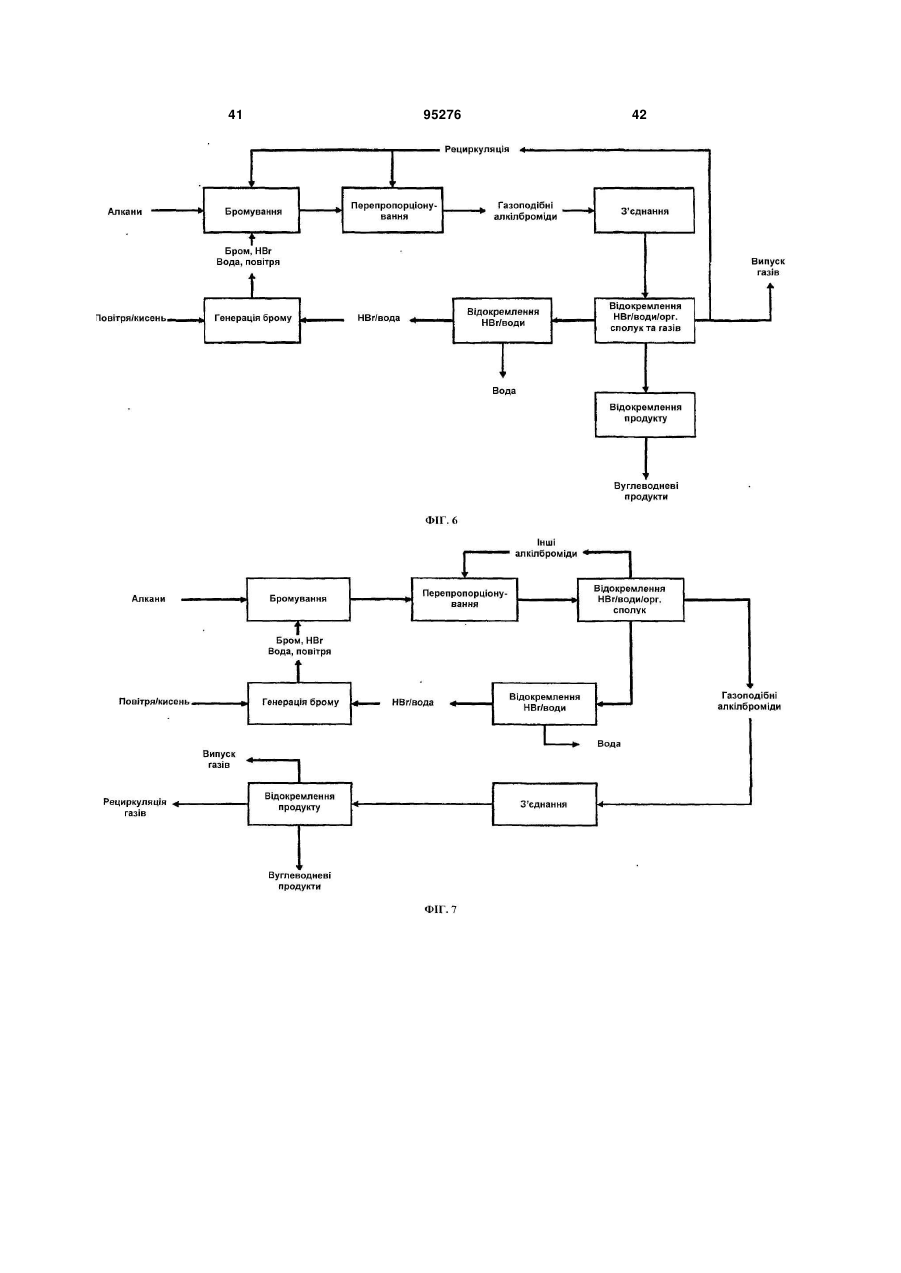
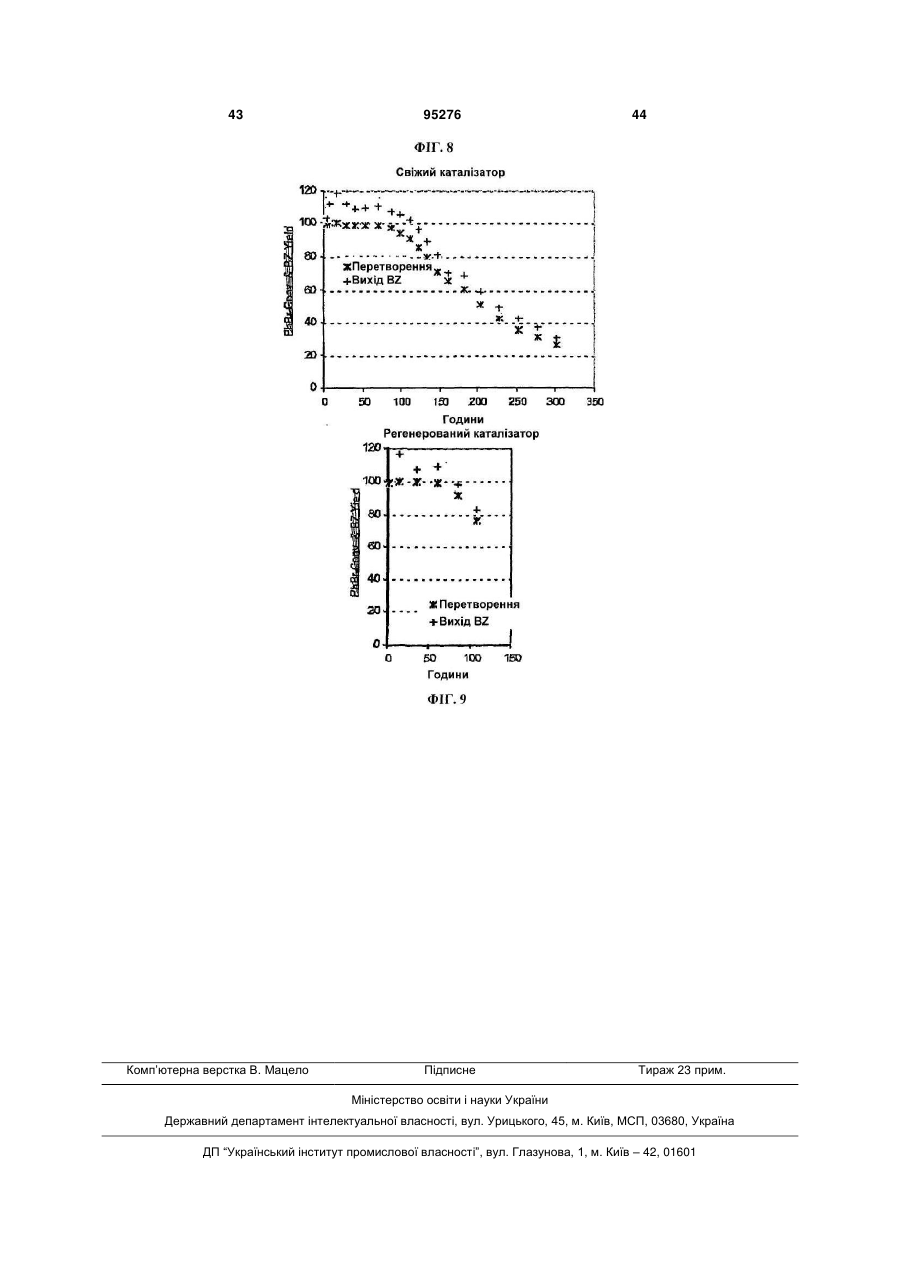
1. Безперервний процес перетворення вуглеводневої сировини на один або більше вищих вуглеводнів, який включає: (a) утворення алкілгалогенідів шляхом реакції молекулярного галогену з вуглеводневою сировиною, яка містить метан, в умовах процесу, достатніх для утворення алкілгалогенідів та гідрогалогеніду, причому практично весь молекулярний галоген витрачають; (b) утворення перепропорціонованих алкілгалогенідів шляхом реакції деяких або всіх алкілгалогенідів з алканом, який подають, завдяки чому збільшують частку присутніх моногалогенованих вуглеводнів; (c) контактування перепропорціонованих алкілгалогенідів з першим каталізатором в умовах процесу, достатніх для утворення вищих вуглеводнів та додаткового гідрогалогеніду; (d) відокремлення вищих вуглеводнів від гідрогалогеніду; (e) регенерацію молекулярного галогену шляхом контактування гідрогалогеніду з другим каталізатором у присутності джерела кисню в умовах процесу, достатніх для утворення молекулярного галогену та води; (f) відокремлення молекулярного галогену від води для забезпечення можливості повторного використання галогену; та (g) повторення етапів з (а) по (f) потрібну кількість разів. 2 (19) 1 3 95276 4 Ag, Аu, Ва, Са, Се, Co, Cr, Cu, Fe, Mg, Mn, Mo, Nb, Ni, Pb, Pd, Pt, Sr, Та, V, W або Zn. 16. Безперервний процес за п. 1, який відрізняється тим, що гідрогалогенід відокремлюють від вищих вуглеводнів, які містять HBr та водну бромистоводневу кислоту, та HBr відокремлюють від водної бромистоводневої кислоти із застосуванням дистиляції з коливанням тиску або екстрактивної дистиляції. 17. Безперервний процес за п. 16, який відрізняється тим, що відокремлення HBr від водної бромистоводневої кислоти включає застосування екстрактивної дистиляції з водним розчином СаВr2, MgBr2, KBr, NaBr, LiBr або їх сумішей, які застосовують як екстрагуючий агент. 18. Безперервний процес за п. 16, який відрізняється тим, що відокремлення HBr від водної бромистоводневої кислоти включає застосування екстрактивної дистиляції, з сірчаною кислотою, яку застосовують як екстрагуючий агент. 19. Безперервний процес за п. 1, який відрізняється тим, що завантажуваний алкан, який застосовують для перепропорціонування, включає газоподібний вуглеводень, який містить значну кількість С2-С5 вуглеводнів. 20. Безперервний процес за п. 1, який відрізняється тим, що утворення алкілгалогенідів та утворення перепропорціонованих алкілгалогенідів здійснюють в окремих реакторах. 21. Безперервний процес перетворення вуглеводневої сировини на один або більше вищих вуглеводнів, який включає: (a) утворення алкілгалогенідів шляхом реакції молекулярного галогену з вуглеводневою сирови ною, яка містить метан, в реакторі для галогенування, в умовах процесу, достатніх для утворення алкілгалогенідів та гідрогалогеніду, причому практично весь молекулярний галоген витрачають; (b) відокремлення непрореагованого метану від алкілгалогенідів і спрямування його назад у реактор для галогенування; (c) утворення перепропорціонованих алкілгалогенідів шляхом реакції деяких або всіх алкілгалогенідів з алканом, який подають, і який містить принаймні 1 % за об'ємом С2-С5 вуглеводнів, завдяки чому збільшують частку присутніх моногалогенованих вуглеводнів; (d) контактування перепропорціонованих алкілгалогенідів з першим каталізатором в умовах процесу, достатніх для утворення вищих вуглеводнів та додаткового гідрогалогеніду; (e) відокремлення вищих вуглеводнів від гідрогалогеніду; (f) регенерацію молекулярного галогену шляхом контактування гідрогалогеніду з другим каталізатором у присутності джерела кисню в умовах процесу, достатніх для утворення молекулярного галогену та води; (g) відокремлення молекулярного галогену від води для забезпечення можливості повторного використання галогену; та (h) повторення етапів з (а) по (g) потрібну кількість разів. 22. Безперервний процес за п. 21, який відрізняється тим, що утворення алкілгалогенідів та утворення перепропорціонованих алкілгалогенідів здійснюють в окремих реакторах. Цей винахід в цілому стосується вуглецьвуглецевого зв'язку, зокрема, способів перетворення вуглеводневої сировини на корисні продукти. Рівень техніки Науковці тривалий час намагаються знайти ефективні шляхи перетворення метану та інших вуглеводнів на вуглеводні з довшими ланцюгами, олефіни, ароматичні вуглеводні та інші продукти. На активації СН-зв'язку протягом десятиліть було зосереджено інтенсивні дослідження, з різними результатами. Більш ефективні процеси можуть бути корисними з багатьох точок зору, включаючи сприяння використанню розташованої на відстані вуглеводневої сировини (такої, як важкодоступний природний газ) шляхом перетворення на види палива та сировини, які частіше використовуються й легше піддаються транспортуванню, та можливість застосування дешевих видів сировини (наприклад, метану та інших легких вуглеводнів) для кінцевих продуктів, які часто виготовляються з вищих вуглеводнів. У патенті U.S. 6,525,230 описуються способи перетворення алканів на інші сполуки з застосуванням "зонного реактора", який складається з порожньої, нерозділеної внутрішньої частини, яка обмежує першу, другу та третю зони. Кисень реагує з бромідом металу у першій зоні для забезпе чення брому; бром реагує з алканом у другій зоні для утворення алкілброміду та бромистого водню; і алкілбромід реагує з оксидом металу у третій зоні для утворення відповідного продукту. В одному варіанті втілення потік газів через реактор повертається у зворотному напрямку для перетворення оксиду металу знову на бромід металу і для перетворення броміду металу знову на оксид металу. Реактор по суті функціонує у циклічному режимі. У патенті U.S. 6,452,058 описується процес окиснювального галогенування для одержання алкілгалідів з алкану, гідрогалогеніду та, в оптимальному варіанті, кисню, з застосуванням галід рідкісноземельного металу або оксигалогеніду як каталізатора. Згадується також альтернатива застосуванню молекулярного галогену. В інших патентах, таких, як U.S. 3,172,915, 3,657,367, 4,769,504 та 4,795,843, описується застосування галідів металів як каталізаторів для окиснювального галогенування алканів. Однак окиснювальне галогенування, має кілька недоліків, включаючи утворення пергалогенованих продуктів та неприйнятної кількості продуктів глибокого окиснення (CO та СО2). У трьох опублікованих патентних заявках США, №№ 2005/0234276, 2005/0234277 та 2006/0100469 (кожна на ім'я Waycuilis), описуються процеси на основі брому для перетворення газо 5 подібних алканів на рідкі вуглеводні. Описано кілька основних етапів, включаючи (1) реакцію брому з алканами для утворення алкілбромідів та бромистоводневої кислоти (бромування), (2) реакцію утворених алкілброміду та бромистоводневої кислоти з кристалічним алюмосилікатним каталізатором для утворення високомолекулярних вуглеводнів та бромистоводневої кислоти (з'єднання), (3) нейтралізацію бромистоводневої кислоти шляхом реакції з водним розчином частково окиснених бромідів металів (як оксидів / оксибромідів / бромідів металів) для утворення броміду металу та води у водному розчині, або шляхом реакції бромистоводневої кислоти з повітрям над каталізатором бромідом металу і (4) регенерацію брому шляхом реакції броміду металу з киснем для одержання брому та окисненої солі. До можливих недоліків процесів належать низьке перетворення метану; короткий просторовий час та менше, ніж 100% перетворення брому в результаті; неекономічне надмірне бромування етану, пропану та вищих алканів, що в результаті призводить до утворення дибромометану та інших полібромованих алканів, які можуть утворювати нагар за описаних умов реакції; порівняно низьке перетворення алкілброміду; потреба у відокремленні потоку вуглеводневого продукту від потоку водної галогеноводневої кислоти; та недостатнє захоплення галогену під час регенерації каталізатора для видалення галоген-вмісного нагару. Крім того, запропоноване відведення цього бром-вмісного потоку як з економічної, так і з екологічної точки зору є неприйнятним. Вищезгаданий процес (Waycuilis) також явно передбачає здійснення при відносно низьких температурах для запобігання значній селективності до метану. Так само результатом може бути неповне перетворення алкілбромідів та, оскільки в основі описаного процесу лежить розділення потоків для видобування продуктів, значна кількість неперетворених алкілбромідів може залишитись у продуктах. Це означає неприйнятну втрату брому (у формі неперетвореного метилброміду) та знижену ефективність вуглецю. Нейтралізація бромистоводневої кислоти шляхом реакції з водним розчином частково окиснених бромідів металів та наступна реакція утворених бромідів металів з киснем для утворення брому та окисненої солі, як описано у патенті Waycuilis, також має багато недоліків. По-перше будь-який присутній вуглекислий газ утворює карбонати у гідросуміші, яка не піддається регенерації. По-друге, максимальна температура обмежується через збільшення тиску, які не витримуються при температурі понад приблизно 200 °С, таким чином, перешкоджаючи повному видобуванню галогену. По-третє, хоча застосування окисновідновно-активних оксидів металів (наприклад, оксидів V, Cr, Mn, Fe, Co, Се та Сu) сприяє утворенню молекулярного брому під час нейтралізації бромистоводневої кислоти, неповне перетворення НВr через застосування твердої бромідної солі, у свою чергу, призводить до суттєвої втрати брому з системи (у водній фазі). Якщо враховувати застосування надлишкового повітря, бромідна сіль зрештою може бути перетворена на оксидну форму, 95276 6 що припиняє будь-яку подальшу втрату НВr з відпрацьованою водою. Для відокремлення води від брому у патенті Waycuilis пропонується застосування конденсації та розділення фаз з метою утворення напівсухого рідкого брому та суміші води/брому. Іншими авторами пропонувались інші способи відокремлення води від брому, такі, як застосування інертного газу для відокремлення брому від водної фази або застосування способів на основі адсорбції; однак такі способи мають мінімальну ефективність і в результаті призводять до значної загальної втрати галогену. Процес оксихлорування існуючого рівня техніки спочатку видаляє воду з НСl (етап, який вимагає великих витрат) з наступною реакцією НСl безпосередньо з киснем та вуглеводнем. В основі процесів оксихлорування лежить відокремлення НСl від непрореагованих алканів та вищих вуглеводневих продуктів через застосування водопоглинання і наступне видобування безводного НСl від водної хлористоводневої кислоти. У Патенті США № 2,220,570 описується процес та пристрій для абсорбції НСl у воді, при якому теплота абсорбції розсіюється через контактування газу НСl з навколишнім повітрям, а також через випарювання води. Спосіб одержання водної хлористоводневої кислоти з концентрацією принаймні 35,5 мас. % шляхом абсорбування газоподібного НСl у воду описується у Патенті США № 4,488,884. У Патенті США № 3,779,870 описується спосіб видобування безводного газу НСl шляхом екстрактивної дистиляції з застосуванням хлоридної солі. У Патенті США № 4,259,309 описується спосіб одержання газоподібного НСl з розведеної водної НСl з застосуванням аміну разом з інертним незмішуваним з водою розчинником. Хоча дослідниками був досягнутий певний прогрес у пошуку більш ефективних шляхів активації СН-зв'язку для перетворення природного газу та іншої вуглеводневої сировини на паливо та інші продукти, все ж зберігається велика потреба у безперервному, економічно стимулюючого і більш ефективного процесу. Короткий опис винаходу В одному аспекті винаходу пропонується безперервний процес перетворення метану, природного газу та інших видів вуглеводневої сировини на один або кілька вищих вуглеводнів або олефінів. В одному варіанті втілення винаходу процес включає етапи галогенування алкану, "перепропорціонування" полігалогенованих сполук для збільшення кількості утворених моногалідів, олігомеризації (С-С-зв'язування) алкілгалідів (та, необов'язково, олефінів) для утворення продуктів з вищим вуглецевим числом, відокремлення продуктів від гідрогалогеніду, безперервної регенерації галогену і відокремлення та видобування молекулярного галогену з води. Винахід ґрунтується на виявленні того факту, що після витрати практично всього молекулярного галогену у реакторі для галогенування алкану утворені полігалогеновані вуглеводні для збільшення загального виходу моногалідів можуть реагувати з негалогенованими алканами, які ефектив 7 ніше реагують на подальших етапах процесу і утворюють більше потрібних продуктів, ніж полігалогеновані різновиди. Після реакції початкового галогенування алкану, в якій витрачається практично весь молекулярний галоген, додаткове галогенування здійснюють шляхом перенесення галогену з полігалогенованих алканів до негалогенованих алканів, таким чином, знижуючи недопал палива та утворення нагару. Наприклад, може бути змінене співвідношення дибромометану з метаном для утворення метилброміду і співвідношення дибромометану з етаном або пропаном для утворення етилброміду та етилену і/або пропілброміду та пропілену. Без прив'язування до теорії, вважається, що у деяких варіантах втілення збагачення моногаліду також відбувається через утворення олефіну з наступною реакцією з полігалогенованими алканами. У деяких варіантах втілення перепропорціонування стимулюють каталізатором. Винахід передбачає багато унікальних підпроцесів, удосконалень та переваг, включаючи перепропорціонування полігалідів; видобування галогену, який вивільнюється під час необхідного спалювання нагару; безперервну регенерацію молекулярного галогену шляхом реакції гідрогалогеніду та кисню над каталізатором (що дозволяє здійснювати загальний процес безперервно); та застосування ретельно вибраних антикорозійних матеріалів для подолання природного корозійного характеру процесу на основі галогену (що дозволяє здійснювати процес у промислових масштабах); та застосування придатних, надійних каталізаторів для довготривалого видобутку галогену. Реактор для бромування може функціонувати адіабатично і в широкому діапазоні температур. Вуглекислий газ та вода легко переносяться, так само, як незначні домішки вуглеводню. Недопал палива через утворення нагару мінімізується завдяки передбаченій вибірковій реакції моногалідів над каталізатором з'єднання, таким, як цеоліт або інший реакційноздатний метало-кисневий матеріал. Повне відновлення галогену для повторного використання також є важливою перевагою цього винаходу. Ці виявлені факти, об'єднані у загальному процесі, складають основу винаходу і забезпечують дійсну перевагу у таких випадках застосування, як перетворення природного газу на рідке паливо (включаючи бензин та присадки до бензину) та хімікати (включаючи ароматичні вуглеводні, такі, як бензол, ксилол та толуол, та легкі олефіни, такі, як етилен та пропілен). Короткий опис фігур Фіг. 1 є схематичним зображенням одного варіанта втілення безперервного процесу перетворення метану або природного газу на вуглеводневі хімікати згідно з винаходом; Фіг. 2 є схематичним зображенням одного варіанта втілення безперервного процесу перетворення метану або природного газу на вуглеводневе паливо згідно з винаходом; Фіг. 3 є схематичним зображенням підпроцесу перепропорціонування полігалідів згідно з альтернативним варіантом втілення винаходу; 95276 8 Фіг. 4 є схематичним зображенням одного варіанта втілення колони для відокремлення моноброміду для застосування у практичному втіленні винаходу; Фіг. 5 є схематичним зображенням одного варіанта втілення системи екстрактивної дистиляції для застосування у практичному втіленні винаходу; Фіг. 6 є спрощеною блок-схемою одного варіанта втілення безперервного процесу перетворення алканів на вуглеводневі продукти згідно з винаходом, у якому вода відокремлюється від вуглеводневих продуктів; Фіг. 7 є спрощеною блок-схемою одного варіанта втілення безперервного процесу перетворення алканів на вуглеводневі продукти згідно з винаходом, у якому вода відокремлюється після етапу бромування алкану; Фіг. 8 є графіком перетворення бромобензолу та виходу бензолу залежно від часу для експерименту, який здійснюється згідно з одним варіантом втілення винаходу; і Фіг. 9 є графіком ефективності каталізатора залежно від часу для експерименту, який здійснюється згідно з одним варіантом втілення винаходу. Детальний опис винаходу Даний винахід забезпечує хімічний процес, який дозволяє перетворювати природний газ та інші види вуглеводневої сировини на високомолекулярні вуглеводневі продукти, з застосуванням молекулярного галогену для активації С-Н-зв'язків у сировині. Згідно з одним аспектом винаходу, безперервний процес перетворення вуглеводневої сировини на один або кілька вищих вуглеводнів включає етапи (а) утворення алкілгалідів шляхом реакції молекулярного галогену з вуглеводневою сировиною (в оптимальному варіанті - сировиною, яка містить метан) в умовах процесу, достатніх для утворення алкілгалідів та гідрогалогеніду, причому практично весь молекулярний галоген витрачається; (b) утворення перепропорціонованих алкілгалідів шляхом реакції деяких або всіх алкілгалідів з алканом, який подається, завдяки чому збільшується частка присутніх моногалогенованих вуглеводнів; (с) контактування перепропорціонованих алкілгалідів з першим каталізатором в умовах процесу, достатніх для утворення вищих вуглеводнів та додаткового гідрогалогеніду; (d) відокремлення вищих вуглеводнів від гідрогалогеніду; (е) регенерації молекулярного галогену шляхом контактування гідрогалогеніду з другим каталізатором у присутності джерела кисню в умовах процесу, достатніх для утворення молекулярного галогену та води; (f) відокремлення молекулярного галогену від води для забезпечення можливості повторного використання галогену; та (g) повторення етапів з (а) по (f) потрібну кількість разів. Ці етапи можуть здійснюватися у представленому порядку або, в альтернативному варіанті, в іншому порядку. Згідно з другим аспектом винаходу, безперервний процес перетворення вуглеводневої сировини на один або кілька вищі вуглеводні включає етапи (а) утворення алкілгалідів шляхом реакції молекулярного галогену з вуглеводневою сирови 9 ною, яка містить метан, у реакторі для галогенування в умовах процесу, достатніх для утворення алкілгалідів та гідрогалогеніду, причому практично весь молекулярний галоген витрачається; (b) відокремлення непрореагованого метану від алкілгалідів і спрямування його назад у реактор для галогенування; (с) утворення перепропорціонованих алкілгалідів шляхом реакції деяких або всіх алкілгалідів з алканом, який подається, і який містить принаймні 1% за об'ємом одного або кількох С2С5 вуглеводнів, завдяки чому збільшується частка присутніх моногалогенованих вуглеводнів; (d) контактування перепропорціонованих алкілгалідів з першим каталізатором в умовах процесу, достатніх для утворення вищих вуглеводнів та додаткового гідрогалогеніду; (e) відокремлення вищих вуглеводнів від гідрогалогеніду; (f) регенерації молекулярного галогену шляхом контактування гідрогалогеніду з другим каталізатором у присутності джерела кисню в умовах процесу, достатніх для утворення молекулярного галогену та води; (g) відокремлення молекулярного галогену від води для забезпечення можливості повторного використання галогену; та (h) повторення етапів з (а) по (g) потрібну кількість разів. У кожному з аспектів та варіантів втілення винаходу передбачається, що алкілгаліди, утворені на етапі (а), можуть бути однаковими (наприклад, 100% бромометан) або, як правило, різними (наприклад, суміші бромометану, дибромометану, дибромоетану і т. ін.). Подібним чином передбачається, що "вищі вуглеводні", утворені на етапі (с), можуть бути однаковими (наприклад, 100% ізооктан) або, як правило, різними (наприклад, суміші аліфатичних та/або ароматичних сполук). Вжитий авторами термін "вищі вуглеводні" стосується вуглеводнів, які мають більшу кількість атомів вуглецю, ніж один або кілька компонентів вуглеводневої сировини, а також олефінових вуглеводнів, які мають таку саму або більшу кількість атомів вуглецю як один або кілька компонентів вуглеводневої сировини. Наприклад, якщо сировиною є природний газ - як правило, суміш легких вуглеводнів, переважно метану, з меншою кількістю етану, пропану та бутану, і ще меншою кількістю вуглеводнів з довшими ланцюгами, таких, як пентан, гексан і т. ін., до "вищих вуглеводнів", утворених згідно з винаходом, можуть належать С2 або ще вищий вуглеводень, такий, як етан, пропан, бутан, С5+ вуглеводні, ароматичні вуглеводні і т. ін. та, необов'язково етилен, пропілен та/або довші олефіни. Термін "легкі вуглеводні" (іноді вживається абревіатура "LHC") стосується С1-С4 вуглеводнів, наприклад, метану, етану, пропану, етилену, пропілену, бутанів та бутенів, усі з яких зазвичай є газами при кімнатній температурі та атмосферному тиску. Необмежувальними прикладами вуглеводневої сировини, придатної для застосування згідно з даним винаходом, є алкани, наприклад, метан, етан, пропан і навіть більші алкани; олефіни; природний газ та інші суміші вуглеводнів. У більшості випадків сировина у природі є первісно аліфатичною. Деякі нафтоочисні процеси на виході дають потоки легких вуглеводнів (так звані "легкі продук 95276 10 ти", зазвичай суміш С1 –С3 вуглеводнів), які в одному варіанті втілення винаходу можуть застосовуватися з додаванням або без додавання метану як вуглеводневої сировини. До типових галогенів належать бром (Вr2) та хлор (Сl2). Також передбачається, що можуть використовуватися фтор та йод, хоча й не обов'язково з рівноцінними результатами. Деякі з проблем, пов'язаних з фтором, так само можуть бути розв'язані через застосування потоків розведеного фтору (наприклад, газоподібного фтору, який переноситься гелієм, азотом або іншим розріджувачем). Щоправда, очікується, що для з'єднання алкілфторидів та утворення вищих вуглеводнів вимагатимуться жорсткіші умови реакції через силу фторовуглецевого зв'язку. Подібним чином проблеми, пов'язані з йодом (наприклад, ендотермічний характер деяких реакцій йоду) можуть розв'язуватися через здійснення реакцій галогенування та/або з'єднання при високих температурах та/або тиску. Перевагу віддають застосуванню брому або хлору, причому найбільшу перевагу віддають бромові. Фігури 1 та 2 схематично пояснюють два необмежувальні варіанти втілення процесу згідно з винаходом, причому Фіг. 1 показує процес одержання вуглеводневих хімікатів (наприклад, бензолу, толуолу, ксилолів, інших ароматичних сполук і т. ін.), а Фіг. 2 показує процес одержання паливних вуглеводнів, наприклад, вуглеводнів, які включають переважну кількість C5 та вищих аліфатичних вуглеводнів і (необов'язково) ароматичних вуглеводнів. Основна різниця у двох варіантах втілення полягає в тому, що процес, показаний на Фіг. 2, не передбачає першого відокремлювального вузла (SEP І) і не повертає полібромовані сполуки до реактора для бромування для "перепропорціонування". У схемі, показаній на Фіг. 2, кількість утворених полібромідів суттєво зменшується через введення легких газів у реактор для бромування. Поліброміди (від бромування метану) реагують з легкими газами для утворення монобромоалканів. Для зручності на фігурах показано процес на основі брому. Однак в альтернативних варіантах втілення винаходу застосовують хлор або інші галогени. Як показано на Фіг. 1, природний газ (або іншу вуглеводневу сировину) та молекулярний бром подають по окремих лініях 1, 2 у нагрітий реактор для бромування 3 і піддають реакції. Продукти (НВr, алкілброміди, необов'язково олефіни) та, можливо, непрореаговані вуглеводні виходять з реактора і переносяться по лінії 4 у перший відокремлювальний вузол 5 (SEP І), де монобромовані вуглеводні та НВr відокремлюють від полібромованих вуглеводнів. Поліброміди переносяться по лінії 6 назад до реактора для бромування, де вони піддаються "перепропорціонуванню" з метаном та/або іншими легкими вуглеводнями, які є присутніми у природному газі і/або вводяться у реактор для бромування, як описано нижче. Перепропорціонування утворених полібромідів під час реакції бромування збагачує вихідний потік монобромідами та олефіновими сполуками і зменшує кількість полібромованих вуглеводнів, які надходять у реактор для з'єднання. Це, у свою 11 чергу, зменшує кількість нагару, який утворюється під час реакцій вуглець-вуглецевого зв'язування. Для великомасштабного виробництва ароматичних вуглеводнів можуть застосовуватися додаткові відокремлювальні вузли, які можуть додатково очищати потік, який подається у реактор для з'єднання, шляхом відокремлення та рециркуляції полібромідів, таким чином, зменшуючи кількість нагару та загальну потребу у бромі. Непрореагована вуглеводнева сировина, НВr, моноброміди та (необов'язково) олефіни, утворені в реакторі для бромування, переносяться по лінії 7, через теплообмінник 8, і надходять у нагрітий реактор для з'єднання 9, де моноброміди (та, необов'язково, будь-які присутні олефіни) реагують у присутності каталізатора з'єднання для утворення вищих вуглеводнів. НВr, вищі вуглеводні та (можливо) непрореаговані вуглеводні та алкілброміди виходять з реактора для з'єднання і переносяться по лінії 10, через інший теплообмінник 11, і надходять до вузла абсорбції НВr 12. Воду вводять у цей вузол через окрему лінію 13. НВr абсорбується в цьому вузлі, який може бути насадною колоною або іншим пристроєм для контакту газурідини. Вихідний потік, який містить рідкі вуглеводні та водний НВr, переноситься по лінії 14 до колони для розділення рідин 15, яка здійснює фазове відокремлення рідких вуглеводнів від потоку водного НВr. Рідкі вуглеводневі продукти потім переносяться по лінії 16 до установки для очищення продукту 17 для одержання на виході кінцевих вуглеводневих продуктів. Після відокремлення НВr від вуглеводневих продуктів та непрореагованого метану (та будьяких інших легких вуглеводнів, які можуть бути присутніми) у вузлі абсорбції НВr, метан (та інші легкі вуглеводні, за їх наявності) переносяться по лінії 18 у другий відокремлювальний вузол 19 (SEP II), у якому застосовується адсорбція зі змінним тиском або температурою, мембранне відокремлення, кріогенна дистиляція (якій віддають перевагу для великомасштабного виробництва) або інший прийнятний спосіб відокремлення. Метан та, можливо, інші легкі вуглеводні, повертаються до реактора для бромування через одну або кілька ліній 20, 21. У показаному варіанті втілення метан спрямовується до попередньої ділянки або "зони" реактора для бромування, а інші легкі вуглеводні спрямовуються до середньої або нижньої зони реактора (останню передбачено для сприяння перепропорціонуванню полібромідів). Потік водного НВr, який виходить з колони для розділення рідин, переноситься по лінії 22 до вузла генерації брому 23. Кисень, повітря або збагачений киснем газ також подається у вузол через окрему лінію 24. Бром регенерується шляхом реакції НВr з киснем у присутності придатного каталізатора. Утворений в результаті потік містить воду, молекулярний бром, кисень, азот (якщо повітря застосовували як джерело кисню) та, можливо, інші гази. Цей потік продукту переноситься по лінії 25 через теплообмінник 26 у вузол миттєвого випарювання 27, який відокремлює більшу частину молекулярного брому від присутніх води, кисню, азоту та інших газів (за наявності). Молекулярний 95276 12 бром, рідкий або пароподібний (який містить не більше, ніж слідову кількість Н2О) переноситься по лінії 28 до теплообмінника 29, а потім повертається до реактора для бромування. Вода з вузла миттєвого випарювання (яка містить до 3 мас. % молекулярного брому) надходить по лінії 30 до дистиляційного вузла 31, який випускає воду як нижній погон та бром або азеотропну суміш брому-води як дистилят. Дистилят повертається через лінію 32 назад до вузла миттєвого випарювання. Газоподібні продукти з вузла миттєвого випарювання (наприклад, кисень, азот, необов'язково інші гази та не більше, ніж несуттєва або незначна кількість брому) переносяться по лінії 33 до бромоочисного вузла 34, який відокремлює молекулярний бром від інших газів. Видобутий бром потім переноситься по лінії 35 через теплообмінник 29 і повторно вводиться у реактор для бромування. Кількість брому, який надходить у газоочищувач, може бути додатково знижена через збільшення кількості брому, видобутого на етапі миттєвого випарювання, через застосування сольових розчинів та прямого контактного охолодження для забезпечення можливості застосування температур, нижчих за 0°С. Інші гази (наприклад, азот, кисень) можуть відводитися в атмосферу. Різні варіанти втілення та особливості окремих підпроцесів та інші вдосконалення втілення винаходу нижче описуються більш детально. Бромування Бромування вуглеводневої сировини здійснюють у нерухомому шарі, псевдорозрідженому шарі або іншому придатному реакторі при температурі та тиску, при яких продукти бромування та реагенти є газоподібними, наприклад, 1-50 атм., 150600°С, ще краще - 400-600 °С, ще краще - 450515°С, з часом утримання 1-60 секунд, ще краще 1-15 секунд. Вищі температури сприяють утворенню нагару, а нижчі температури вимагають більших реакторів. Застосування псевдорозрідженого шару забезпечує перевагу поліпшеної теплопередачі. Бромування алкану започатковують через застосування теплоти або світла, причому перевагу віддають тепловим засобам. В одному варіанті втілення реактор також містить каталізатор галогенування, такий, як цеоліт, аморфний алюмосилікат, кислотний діоксид цирконію, вольфрамати, тверді фосфорні кислоти, оксиди металів, змішані оксиди металів, галіди металів, змішані галіди металів (металами у таких випадках є, наприклад, нікель, мідь, церій, кобальт і т. ін.), та/або інші каталізатори, як описано, наприклад, у U.S. 3,935,289 та 4,971,664. В альтернативному варіанті втілення реактор містить пористий або непористий інертний матеріал, який забезпечує достатню площу поверхні для утримання утвореного нагару в реакторі та запобігання його виходові. Інертний матеріал також може сприяти утворенню полігалогенованих вуглеводнів, таких, як трибромопропан. У ще одному варіанті втілення у реакторі передбачаються як каталізатор, так і інертний матеріал. Необов'язково реактор містить інші ділянки або зони, що дозволяє здійснювати в одній або кількох 13 зонах повне перетворення молекулярного брому для вироблення алкілбромідів та бромистого водню. Реакція бромування також може здійснюватися у присутності каталізатора ізомеризації, такого, як бромід металу (наприклад, NaBr, KBr, CuBr, NiBr2, MgBr2, СаВr2), оксид металу (наприклад, SiO2, ZrO2, AI2O3,) або метал (Pt, Pd, Ru, Ir, Rh) для сприяння утворенню потрібного(их) бромованого(их) ізомеру(ів). Оскільки умови ізомеризації та бромування є подібними, бромування та ізомеризацію здійснюють в одному резервуарі реактора. В альтернативному варіанті може застосовуватись окремий реактор для ізомеризації, розташований за реактором для бромування і перед реактором для з'єднання. Перепропорціонування У деяких варіантах втілення основною особливістю винаходу є "перепропорціонування" полігалогенованих вуглеводнів (полігалідів), тобто, галогенованих вуглеводнів, які містять два або більше атомів галогену на молекулу. Моногалогеновані алкани (моногаліди), створені під час реакції галогенування, є бажаними як переважні реагенти для наступних реакцій з'єднання та утворення високомолекулярних вуглеводнів. Для деяких вибраних продуктів можуть бути бажаними полігалогеновані алкани. Перепропорціонування дозволяє досягати потрібного збагачення моногалідів шляхом реакції полігалогенованих алкілгалідів з негалогенованими алканами, як правило, практично за відсутності молекулярних галогенів, для контролювання співвідношення моно- та полігалогенованих сполук. Наприклад, дибромометан піддають реакції з метаном для утворення метилброміду; дибромометан піддають реакції з пропаном для утворення метилброміду та пропілброміду та/або пропілену; і т. д. Реакційне перепропорціонування здійснюють, дозволяючи вуглеводневій сировині та/або рециркульованим алканам прореагувати з полігалогенованими сполуками з реактора для галогенування, в оптимальному варіанті - практично за відсутності молекулярного галогену. На практиці майже весь молекулярний галоген, який надходить до реактора для галогенування, швидко витрачається, утворюючи моно- та полігаліди; таким чином, перепропорціонування вищих бромідів може здійснюватися просто шляхом введення полібромідів у середню або нижню ділянку або "зону" реактора для галогенування, необов'язково нагріту до температури, яка відрізняється від температури решти реактора. В альтернативному варіанті перепропорціонування здійснюють в окремому "реакторі для перепропорціонування", в якому полігалідам та негалогенованим алканам дають прореагувати, в оптимальному варіанті - практично за відсутності молекулярного галогену. На Фіг. 3 показано один такий варіант втілення, в якому для зрозумілості показуються лише суттєві елементи системи. Як і на Фіг. 1, природний газ або іншу вуглеводневу сировину та молекулярний бром подають по окремих лініях 1, 2 до нагрітого реактора для бромування 3 і піддають реакції. Продукти (НВr, алкілб 95276 14 роміди) та, можливо, непрореаговані вуглеводні, виходять з реактора і переносяться по лінії 4 у перший відокремлювальний вузол 5 (SEP І), де монобромовані вуглеводні та НВr відокремлюють від полібромованих вуглеводнів. Моноброміди, НВr та, можливо, непрореаговані вуглеводні переносяться по лінії 7 через теплообмінник 8 до реактора для з'єднання 9 і піддаються реакції, як показано на Фіг. 1. Поліброміди переносяться по лінії 6 до реактора для перепропорціонування 36. Додатковий природний газ або іншу алканову сировину також вводять у реактор для перепропорціонування через лінію 37. Поліброміди реагують з небромованими алканами у реакторі для перепропорціонування для утворення монобромідів, які переносяться по лінії 38 у реактор для з'єднання 9 після попереднього пропущення через теплообмінник. В іншому варіанті втілення винаходу (не показано), в якому вуглеводнева сировина включає природний газ, який містить значну кількість С2 та вищі вуглеводні, "свіжий" природний газ подається безпосередньо у реактор для перепропорціонування. і рециркульований метан (який проходить через реактор для перепропорціонування неперетвореним), повертається назад у реактор для галогенування. Перепропорціонування запускається термічно і/або стимулюється через застосування каталізатора. Необмежувальними прикладами прийнятних каталізаторів є оксиди металів, галіди металів та цеоліти. У патенті США 4,654,449 описується перепропорціонування полігалогенованих алканів з алканами з застосуванням кислотного цеолітного каталізатора. У патентах США 2,979,541 та 3,026,361 описується застосування тетрахлориду вуглецю як хлоруючого агента для метану, етану, пропану та їх хлорованих аналогів. Усі три патенти включаються авторами шляхом посилання в їх повному обсязі. Застосування перепропорціонування у контексті безперервного процесу збагачення реакційноздатної сировини для одержання вищих вуглеводнів, наскільки відомо авторам, раніше не описувалося. Перепропорціонування С1-С5 алканів з дибромометаном та/або іншими полібромідами відбувається при температурах від 350 до 550°С, з оптимальною температурою, яка залежить від присутнього(іх) поліброміду(ів) та алкану(ів), які піддаються бромуванню. Крім того, перепропорціонування відбувається швидше при підвищеному тиску (наприклад, 2-30 бар). Через досягнення високого первісного перетворення метану в реакторі для галогенування створюється значна кількість ди-та трибромометану; ці сполуки потім можуть застосовуватись як реагенти для бромування на етапі перепропорціонування. Застосування дита трибромометану дозволяє здійснювати контрольоване бромування С1-С5 алканів до монобромованих С1-С5 бромоалканів та С2-С5 олефінів. Перепропорціонування ди- та трибромометану сприяє високому первісному перетворенню метану під час бромування, що має знижувати швидкість потоку рециркуляції метану і збагачувати потік газу-реагента С2-С5 монобромоалканами та оле 15 фінами, які з'єднуються з рідкими продуктами над різними каталізаторами, включаючи цеоліти. В цьому полягає головне вдосконалення нового процесу. В іншому варіанті втілення винаходу перепропорціонування здійснюють без попереднього відокремлення полігалідів у відокремлювальному вузлі. Цьому сприяє наповнення "зони перепропорціонування" каталізатором, таким, як цеоліт, який дозволяє відбуватися реакції при зниженій температурі. Наприклад, хоча пропан реагує з дибромометаном для утворення бромометану та бромопропану (приклад "перепропорціонування"), реакція не досягає прийнятного ступеня при температурах, нижчих за приблизно 500 °С. Застосування цеоліту забезпечує можливість перепропорціонування при зниженій температурі, що дозволяє здійснювати бромування таких сполук, як метан та етан, в одній зоні реактора та перепропорціонування ди-, три-та інших полібромідів в іншій зоні реактора. Видобування брому під час видалення нагару У процесах галогенування та перепропорціонування неодмінно відбувається утворення нагару. Якщо застосовують каталізатори у реакторі(ах) або зоні(ах) реактора, ці каталізатори можуть бути дезактивовані через нагар; таким чином, вимагається періодичне видалення вуглецевмісних відкладів. Крім того, авторами було виявлено, що в утвореному нагарі також може міститися бром, і дуже бажаним є видобування цього брому з метою мінімізації втрати брому в загальному процесі, що є важливим як з економічної, так і з екологічної точки зору. Існує кілька форм бромідів: НВr, органічні броміди, такі, як метилбромід та дибромометан і молекулярний бром. Винахід забезпечує засоби видобування цього брому з процесу видалення нагару. В оптимальному варіанті втілення даний реактор вимикають і вводять повітря або кисень для спалювання відкладів вуглецю та утворення НВr із залишків брому. Вихідний потік газу додають до потоку повітря (або кисню), який подається до реактора для генерації брому, таким чином, забезпечуючи повне видобування брому. Цей процес повторюють періодично. Хоча даний реактор є відімкнутим, загальний процес, незважаючи на це, може відбуватися безперервно завдяки застосуванню резервного реактора, розташованого паралельно аналогічному реакторові. Наприклад, можуть застосовуватися спарені реактори для бромування та спарені реактори для з'єднання, з відведенням технологічних газів від одного, але не від іншого з реакторів для бромування (або реакторів для з'єднання), якщо вимагається операція з видалення нагару. Застосування псевдорозрідженого шару може зменшувати утворення нагару і сприяти видаленню теплоти та регенерації каталізатора. Інший варіант втілення процесу видалення нагару включає неокиснювальне видалення нагару з застосуванням алкану або суміші алканів, яке може знижувати як втрату адсорбованих продуктів, так і потребу в кисні для процесу. В іншому варіанті втілення процесу видалення нагару, окисник, 95276 16 такий, як кисень, повітря або збагачене повітря спільно подаються у секцію для бромування для перетворення нагару на вуглекислий газ та/або оксид вуглецю під час реакції бромування, таким чином, усуваючи або знижуючи потребу у видаленні нагару у неробочому стані. Відокремлення алкілгалідів Наявність високої концентрації полігалогенованих сполук у матеріалі, який завантажується у реактор для з'єднання, в результаті може призводити до збільшення утворення нагару. У багатьох випадках, наприклад, при виробленні ароматичних вуглеводнів та легких олефінів, бажаною є подача лише моногалідів до реактора для з'єднання з метою поліпшення перетворення продуктів. В одному варіанті втілення винаходу додають спеціальний етап відокремлення між реактором(ами) для галогенування / перепропорціонування та реактором для з'єднання. Наприклад, дистиляційну колону та відповідні теплообмінники ("SEP І" на Фігурах 1 та 2) застосовують для відокремлення монобромідів від полібромованих сполук через використання великої різниці у точках кипіння сполук. Полібромовані сполуки, видобуті як нижній погон, можуть бути перепропорціоновані з алканами для утворення монобромідних сполук та олефінів, або у реакторі для бромування, або в окремому реакторі для перепропорціонування. Дистиляційна колона може працювати при будь-якому тиску від 1 до 50 бар. Вищий тиск допускає застосування вищих температур конденсатора, таким чином, знижуючи потребу в заморожуванні. На Фіг. 4 показано один варіант втілення відокремлювального вузла для відокремлення монобромідів від полібромованих сполук. Алкілброміди з реактора для бромування охолоджують шляхом пропущення через теплообмінник 50, апотім подають до дистиляційної колони 51, оснащеної двома теплообмінниками 52 та 53. У нижній частині колони теплообмінник 52 діє як ребойлер, а у верхній частині колони теплообмінник 53 діє як парціальний конденсатор. Ця конфігурація дозволяє виводити з дистиляційної колони рідкі "низи", які є збагаченими на поліброміди (і містять не більше, ніж незначну кількість монобромідів). Поліброміди пропускають через інший теплообмінник 54 для їх перетворення знову на газ перед їх поверненням до реактора для бромування (або надходження до окремого реактора для перепропорціонування) для перепропорціонування з небромованими алканами. У верхній частині колони частковому поверненню рідини з приймача зрошувальної фракції сприяє теплообмінник 53, що забезпечує на виході пару, збагачену легкими компонентами, включаючи метан та НВr, і потік рідини, яка складається з монобромідів та НВr (і містить не більше, ніж незначну кількість полібромідів). Альтернативні варіанти конфігурації дистиляції включають колону бокової фракції з ректифікатором або відпарювачем бокового потоку або без нього. Якщо матеріал, який подається з реактора для бромування, містить воду, нижній погон з дистиляційної колони також міститиме воду, і рідинно 17 рідинне розщеплення фаз у нижньому погоні застосовують для відокремлення води від полібромованих сполук. Через присутність НВr у потоці води він може або надсилатися до абсорбційної колони для НВr, або до реактора для генерації брому. Каталітичне з'єднання алкілгалідів з високомолекулярними продуктами Алкілгаліди, утворені на етапі галогенування / перепропорціонування, реагують над каталізатором для утворення вищих вуглеводнів та гідрогалогеніду. Завантажений реагент також може містити гідрогалогенід та негалогеновані алкани з реактора для бромування. Згідно з винаходом, застосовують будь-який з багатьох каталізаторів для сприяння утворенню вищих вуглеводневих продуктів з галогенованих вуглеводнів. Необмежувальними прикладами є некристалічні алюмосилікати (аморфні тверді кислоти), суперкислоти вольфраму / діоксиду цирконію, сульфатований діоксид цирконію, алюмофосфати, такі, як SAPO34 та його заміщені у каркасі аналоги (заміщені, наприклад, Ni або Мn), цеоліти, такі, як ZSM-5 та його іонообмінні аналоги, та заміщений у каркасі ZSM-5 (заміщений Ті, Fe, Ті + Fe, В або Ga). Оптимальними каталізаторами для одержання рідких при кімнатній температурі вуглеводнів є іонообмінний ZSM-5, який має співвідношення SiO2/Al2O3, нижче за 300, в оптимальному варіанті - нижче за 100, у найкращому варіанті - 30 або нижче. Необмежувальними прикладами оптимального іонного обміну є іони Ag, Ba, Bi, Ca, Fe, Li, Mg, Sr, K, Na, Rb, Mn, Co, Ni, Cu, Ru, Pb, Pd, Pt та Се. Ці іони можуть обмінюватися як чисті солі або як суміші солей. Приготування легованих цеолітів та їх застосування як каталізаторів вуглець-вуглецевого зв'язування описується у патентній публікації США 2005/0171393 А1 та сторінках 4-5, яка включається авторами шляхом посилання у повному обсязі. В одному варіанті втілення винаходу Mnобмінений цеоліт ZSM-5, який має співвідношення SіО2/Аl2О3 30, застосовують як каталізатор з'єднання. За певних умов процесу він може забезпечувати задану селективність рідких вуглеводневих продуктів. З'єднання галоалканів в оптимальному варіанті здійснюють у нерухомому шарі, псевдорозрідженому шарі або в іншому придатному реакторі при відповідній температурі (наприклад, 150-600 °С, в оптимальному варіанті - 275-425 °С) та тиску (наприклад, від 0,1 до 35 атм.) та часі утримання () 1-45 секунд. Як правило, відносно довгий час утримання сприяє перетворенню реагентів на продукти, а також селективності продуктів, тоді, як короткий час утримання означає вищу продуктивність та (можливо) більшу економію. Існує можливість регулювання селективності продукту шляхом зміни каталізатора, зміни температури реакції та/або зміни часу утримання в реакторі. Наприклад, при помірному часі утримання у 10 секунд та помірній температурі 350 °С ксилол та мезитилени є домінуючими компонентами ароматичної фракції (бензол + толуол + ксилоли + мезитилени; "ВТХМ"), одержаної при подачі продукту реакції бромування метану в реактор для з'єднання, на 95276 18 повнений імпрегнованим іонами металів каталізатором ZSM-5, у якому імпрегнуючим металом є Ag, Ba, Bi, Ca, Co, Cu, Fe, La, Li, Mg, Mn, Ni, Pb, Pd або Sr, і каталізатором ZSM-5 є Zeolyst CBV 58, 2314, 3024, 5524 або 8014, (від Zeolyst International (Valley Forge, PA)). При температурі реакції 425 °С та часі утримання 40 секунд толуол та бензол є домінуючими продуктами фракції ВТХМ. Селективність продукту також можна варіювати шляхом контролюванняконцентрації дибромометану, який утворюється або подається в реактор для з'єднання. У деяких установках передбачається відведення теплоти реакції та безперервне видалення нагару і регенерація каталізатора з застосуванням конфігурації реактора для з'єднання з псевдорозрідженим шаром. В одному варіанті втілення реакцію з'єднання здійснюють у парі паралельно розташованих реакторів для з'єднання. Це забезпечує безперервне здійснення загального процесу без зупинок, навіть якщо один з реакторів для з'єднання відключають для видалення нагару або з якихось інших причин. Подібні резервні засоби можуть застосовуватися в установках для бромування, відокремлення продукту, генерації галогену та інших вузлах, які застосовують у загальному процесі. Відокремлення вуглеводневого продукту та видобування галогену До продуктів з'єднання належать вищі вуглеводні та НВr. У варіантах втілення, показаних на Фігурах 1 та 2, продукти, які виходять з реактора для з'єднання, спочатку охолоджуються у теплообміннику, а потім надходять до абсорбційної колони. НВr абсорбують у воді, застосовуючи насадну колону або інший контактний пристрій. Вхідна вода та потік продукту можуть контактувати у паралельному або зустрічному потоці, причому для більшої ефективності перевагу віддають зустрічному потокові. Абсорбція НВr може відбуватись або по суті адіабатично, або по суті ізотермічно. В одному варіанті втілення концентрація бромистоводневої кислоти після абсорбції становить від 5 до 70 мас. %, в оптимальному варіанті - від 20 до 50 мас. %. Робочий тиск становить від 1 до 50 бар, ще краще - від 1 до 30 бар. У лабораторії застосовують скляну колонку або колонку зі скляним покриттям з керамічним або скляним наповненням. В експериментальній або промисловій установці застосовують один або кілька довговічних, резистентних до корозії матеріалів (як описано нижче). В одному варіанті втілення винаходу вуглеводневі продукти видобувають як рідину з абсорбційної колони для НВr. Цей рідкий вуглеводневий потік піддають розділенню фаз з відокремленням від потоку водного НВr з застосуванням колони для розділення рідин і надсилають до вузла для очищення продукту. В іншому варіанті втілення вуглеводневі продукти видобувають з колони НВr як потік газу, разом з неперетвореним метаном та інші легкі гази. Продукти після цього відокремлюють і видобувають з метану та легких газів з застосуванням будь-якого з багатьох способів. Необмежувальними прикладами є дистиляція, абсорбція з коливанням тиску та мембранне відокремлення. 19 У деяких варіантах втілення установка для очищення продукту включає або містить реактор для перетворення галогенованих вуглеводнів, присутніх у потоці продукту, на негалогеновані вуглеводні. Наприклад, за певних умов мала кількість С1-С4 бромоалканів, бромобензолу та/або інших бромованих сполук утворюється й проходить від реактора для з'єднання до колони для розділення рідин 16, а потім до установки для очищення продукту 17. Ці бромовані сполуки можуть бути "гідродегалогеновані" у відповідному реакторі. В одному варіанті втілення такий реактор включає безперервний нерухомий шар, каталітичний конвертер, наповнений каталізатором з металу або оксиду металу на основі. Необмежувальними прикладами активного компонента є мідь, оксид міді, паладій та платина, причому оптимальним є паладій. Необмежувальними прикладами матеріалів для основи є активоване вугілля, глинозем, кремнезем та цеоліти, причому оптимальним є глинозем. Реактор функціонує при тиску 0150 psi, в оптимальному варіанті - 0-5 psi, та температурі 250-400 °С, в оптимальному варіанті -1 300-350 °С, з GHSV 1200-60 год , в оптимальному -1 варіанті 240 год . Коли бромобензол (наприклад) проходить через такий реактор, він легко перетворюється на бензол та НВr, з утворенням деяких легких вуглеводнів (наприклад, С3-С7) як побічних продуктів. Хоча відкладення вуглецю (утворення нагару) може дезактивувати каталізатор, каталізатор може бути відновлений через дію кисню та водню, наприклад, при 500 °С та 400 °С, відповідно. Після відокремлення НВr від вуглеводневих продуктів неперетворений метан виходить з легкими газами через випуск для пари вузла абсорбції НВr. В одному варіанті втілення винаходу неперетворений метан відокремлюється від легких газів у відокремлювальному вузлі ("SEP II" на Фігурах), в якому здійснюється адсорбція з застосуванням коливання тиску або температури, мембранне відокремлення, кріогенна дистиляція (в оптимальному варіанті - для великомасштабного виробництва) або якийсь інший прийнятний процес відокремлення. Низьке перетворення метану в реакторі для бромування в результаті може призводити до перенесення продуктів з'єднання легкими газами, що, у свою чергу, викликає необхідність у видобуванні цих сполук з легких газів. До способів відокремлення, які можуть застосовуватися з цією метою, крім інших, належать дистиляція, адсорбція з коливанням тиску або температури та мембранні технології. В іншому аспекті винаходу пропонується спосіб відокремлення безводного НВr від водного розчину НВr. НВr утворює висококиплячу азеотропну суміш з водою; таким чином, відокремлення НВr від водного розчину вимагає або руйнування азеотропної суміші з застосуванням екстрагуючого агента, або обхідного спрямування азеотропної суміші з застосуванням дистиляції з коливанням тиску. Фіг. 5 пояснює один варіант втілення вузла екстрактивної дистиляції для відокремлення НВr від води. Воду видаляють у дистиляційній колоні 200, і НВr одержують як потік дистиляту 201. Потік 95276 20 дистиляту також може містити невелику кількість води. В одному варіанті втілення дистиляційна колона 200 є тарілчастою колоною або насадною колоною. Традиційному керамічному наповненню віддають перевагу перед структурованим наповненням. Водний розчин броміду, такого, як СаВr2, додають у верхню частину дистиляційної колони, в результаті чого видаляється вода з водного розчину НВr. Колона може не потребувати конденсатора. Ребойлер 203 застосовують для підтримання потоку пари у дистиляційній колоні. Розріджений потік водного СаВr2 202 надсилається до секції випарювання 206, яка необов'язково має тарілчасту секцію або секцію з насадкою. Нижній погон з колони нагрівається перед надходженням до секції випарювання. Потік 207, який складається здебільшого з води (і містить не більше, ніж слідову кількість НВr), виходить із секції випарювання. В одному варіанті втілення НВr витісняється як газ з його водного розчину у присутності електро+ літу, який має спільний іон (Вr або Н ) або іон (на2+ 2приклад, Са або SO4 ), який має вищу енергію гідратації, ніж у НВr. Присутність електроліту зміщує рівновагу HBraq HBrgas у напрямку газовиділення, якому додатково сприяє нагрівання розчину. Водні розчини бромідів металів, таких, як CaBr2, MgBr2, а також KBr, NaBr, LiBr, RbBr, CsBr, SrBr2, BaBr2, MnBr2, FeBr2, FeBr3, CoBr2, NiBr2, CuBr2, ZnBr2, CdBr2, AlBr3, LаВr3, YBr3 та BiBr3, застосовують як екстрагуючі агенти, причому перевагу віддають водним розчинам CaBr2, MgBr2, KBr, NaBr, LiBr або їх сумішам. Нижній погон дистиляційної колони містить розріджений розчин екстрагуючого агента. Цей потік надсилається до іншої дистиляційної колони або випарника, в якому воду випарюють і екстрагуючий агент концентрують перед поверненням до екстракційної дистиляційної колони. Як екстрагуючий агент застосовують сірчану кислоту, якщо його реакція з НВr для утворення брому та діоксиду сірки може бути зменшена до мінімуму. Експерименти, які здійснювалися для демонстрації відокремлення безводного НВr від водного розчину НВr, описуються у Прикладі 1 та 2. В іншому аспекті винаходу пропонуються нові підходи до очищення продукту (відокремлення та/або очищення в інший спосіб). У потоці неочищеного продукту можуть бути присутніми багато бромідних сполук: НВr, органічні броміди, такі, як метилбромід та дибромометан, а також бромоароматичні сполуки. В одному варіанті втілення винаходу вуглеводневі продукти відокремлюють від бромованих сполук шляхом пропущення потоку продукту над металевою міддю, NiO, CaO, ZnO, MgO, BaO або їх комбінаціями. В оптимальному варіанті продукти пропускають над одним або кількома з вищеперелічених матеріалів при температурі 25-600 °С, ще краще - 400-500 °С. Цьому процесові не зашкоджує СО2, який може бути присутній. В іншому варіанті втілення, зокрема, для великомасштабного виробництва вуглеводнів, неперетворений метан відокремлюють від інших легких вуглеводнів, а також більш важких продуктів (на 21 приклад, бензолу, толуолу і т. ін.) з застосуванням дистиляції. Наприклад, на Фігурах 1 та 2 показано, що метан та інші легкі вуглеводні виходять з абсорбційної колони через випуск для газу і спрямовуються у відокремлювальний вузол (SEP. II). Будьякий неперетворений метилбромід видаляється з легкими газами і може бути повернутий до реактора для бромування / перепропорціонування. Більш важкі вуглеводні видаляються як рідкий дистилят. Генерація молекулярного галогену В одному варіанті втілення винаходу каталітичну генерацію галогену здійснюють шляхом реакції галогеноводневої кислоти та молекулярного кисню над відповідним каталізатором. Загальна реакція може бути представлена рівнянням (1): каталізатор (1) 2HX+1/2O2 Tx2 + H2O Процес відбувається у діапазоні температур та молярних співвідношень галогеноводневої кислоти (НХ) та молекулярного кисню (О2), тобто, від 4:1 до 0,001:1 НХ/О2, в оптимальному варіанті -4:1 (для відповідності стехіометрії реакції), ще краще 3,5:1 (для уникнення можливого прориву НВr). Галоген генерують, застосовуючи чистий кисень, повітря або збагачений киснем газ, і реакція може відбуватися з різними інертними нереагуючими газами, такими, як азот, вуглекислий газ, аргон, гелій, та присутнім потоком води. Будь-яка пропорція цих газів може комбінуватися у формі чистих газів або їх вибраних сумішей для пристосування до вимог процесу. Багато матеріалів визначаються як каталізатори генерації галогенів. Існує можливість застосування одного типу каталізатора або комбінації будь-якої кількості, конфігурації або пропорцій каталізаторів. Прикладами можуть бути оксиди, галіди та/або оксигаліди одного або кількох металів, таких, як Cu, Ag, Au, Fe, Co, Ni, Mn, Ce, V, Nb, Mo, Pd, Та або W, ще краще - Mg, Са, Sr, Ва, V, Cr, Mn, Fe, Co, Ni, Cu, Zn або Се. Найкращими каталізаторами є оксиди, галіди та/або оксигаліди Cu. Без прив'язування до теорії, представлені нижче рівняння вважаються такими, що представляють хімічні реакції, які відбуваються при застосуванні таких матеріалів для каталізу утворення галогенів: СаО + 2НВr СаВr2 + Н2О (2) СаВr2 + ½ О2 СаО + Вr2 (3) для оксидів металів, у яких метал не змінює стан окиснення, і Со3O4 + 8НВr 3СоВr2 + 4Н2О + Вr2 (4) 3CoBr2 + 2О2 Со3О4 + 3Вr2 (5) для оксидів металів, у яких метал змінює стан окиснення. Результуючою реакцією для (2) + (3) та (4) + (5) є (7): каталізатор 2НВr + 1/2О2 Н2О + Вr2 (7) яка є рівноцінною (1). В одному варіанті втілення винаходу хлор застосовують як агент галогенування, і оксид церію (СеО2) застосовують для каталізу генерації хлору з хлористоводневої кислоти. Типовими вважають такі рівняння: СеО2 + 4НСl СеСl2 + 2Н2О + Сl2 (8) 95276 22 СеСl2 + О2 СеО2 + Сl2 (9) Для загальної реакції: 2НСl + ½ О2 Н2О + Сl2 (10) яка також є рівноцінною (1). Застосування оксиду церію є досить новим, і воно забезпечує практично повну витрату НСl. Натомість попередні реакції оксидів металів, НСl та кисню зазвичай забезпечували на виході суміші НСl/Сl2. Таким чином, застосуванню оксиду церію віддають перевагу як каталізаторові регенерації каталізатора, зокрема, у випадках, коли хлор застосовують для галогенування алкану, з характерною для хлору низькою вартістю та звичністю застосування у галузі. В одному варіанті втілення винаходу каталізатор(и) генерації галогену тримаються на пористому або непористому глиноземі, кремнеземі, діоксиді цирконію, діоксиді титану або їх сумішах, або іншій придатній основі. Діапазон температур, який може застосовуватися для досягнення максимальної ефективності процесу, становить, наприклад, 200-600 °С, ще краще - 350-450 °С. Видобування та рециркуляція молекулярного галогену Генерація галогену утворює воду та молекулярний галоген. Воду відокремлюють від галогену і видаляють перед реакцією галогену з вуглеводневою сировиною. Якщо галогеном є бром, бромоводне, рідинно-рідинне розщеплення фаз досягається при конденсації суміші цих сполук. Наприклад, в одному варіанті втілення винаходу застосовують рідинно-рідинний випарний вузол для відокремлення більшості брому від води у простий і недорогий спосіб. Фазам брому зазвичай містить дуже малу кількість води і може надсилатися безпосередньо на реактор для бромування. Однак водна фаза містить 1-3 мас. % брому. Щоправда, якщо на етапі генерації брому застосовують повітря, азот та неперетворений кисень є присутніми у потоці брому та води, який надходить до випарника. Газ, який виходить з випарного вузла, здебільшого складається з азоту та неперетвореного кисню, але захоплює з собою певну кількість брому та води. Кількість брому, який виходить з паровою фазою залежить від температури та тиску випарника. Випарник може функціонувати при температурах від 0 до 50 °С; однак для зменшення кількості брому, який виходить у потоці пари, перевагу віддають нижчій температурі (приблизно від 2 до 10 °С). Потік пари надсилається до секції видобування брому для видобування брому. В одному варіанті втілення робочий тиск становить від 1 до 50 бар, ще краще - від 1 до 30 бар. Оскільки вода замерзає при 0 °С, це не дозволяє суттєво знизити температуру випарника 19. Однак потік пари з випарника може бути приведений у контакт з охолодженим сольовим розчином при температурах від -30 °С до 10 °С. Температура охолодженого сольового розчину, нижча за температуру випарника, може суттєво знизити потребу у видобуванні брому в очисному вузлі. У цьому разі може відбуватися випарювання брому шляхом нагрівання сольового розчину, з подальшим нагрі 23 ванням, яке застосовують для сприяння концентруванню сольового розчину для повторного застосування. Цей підхід до видобування брому може здійснюватися безперервно або у порційному режимі. Бром, який міститься у багатій на воду фазі, яка виходить з рідинно-рідинного випарника, може бути ефективно видобута шляхом дистиляції. Інші засоби, такі, як застосування інертного газу для відокремлення брому від водної фази (описано у патенті Waycuilis) та адсорбційні способи, є не дуже ефективними і в результаті можуть призводити до суттєвої втрати брому. Описаний авторами підпроцес дистиляції утворює бром або азеотропну суміш брому-води як дистилят, який повертається назад до випарного вузла. Вода міститься у нижньому погоні. Бром може оборотно реагувати з водою для утворення малої кількості НВr та НОВr. Таким чином, у схемі дистиляції НВr (та/або НОВr) може бути присутнім у нижньому погоні на рівні мільйонних часток. Ректифікатор або відпарювач бокового потоку може застосовуватися для зниження вмісту брому в нижньому погоні для створення потоку чистої води. До інших альтернативних варіантів, які дозволяють знижувати вміст брому у воді до рівня, нижчого за 10 ррт, крім інших, належать додавання кислот, таких, як сірчана кислота, хлористоводнева кислота та фосфорна кислота, у дуже малій кількості для зниження рівня рН водного потоку. Зниження рівня рН повертає потік НВr та НОВr до брому та води, таким чином, суттєво знижуючи втрату брому у водному потоці. НВr, присутній у водному потоці, також може бути видобутий з застосуванням іонообмінних смол або електрохімічних засобів. Повне відновлення галогену для повторного застосування. Як з економічної, так і з екологічної точки зору, бажаними є мінімізація або навіть повне усунення втрат галогену, який використовується у загальному процесі. Молекулярний бром може виходити з відведеними азотом та неперетвореним киснем, якщо він не захоплюється після генерації Вr2. Видобування брому може відбуватись у шарі, який містить твердий CuBr або МnВr2, який наносять на основу або застосовують у формі порошку, для уловлення Вr2 з потоку газу, який також може містити Н2О, CO2, О2, метан та/або N2. В одному варіанті втілення винаходу, видобування брому здійснюють у діапазоні температур, тобто, від -10 ° до 200 °С. Коли видобування брому завершується, молекулярний бром може вивільнюватися з шару через підвищення температури шару до 220 °С або вище, в оптимальному варіанті - вище за 275 °С. Важливим є максимальне зменшення, якщо не відсутність О2 у шарі під час вивільнення брому, оскільки О2 окиснює метал і з часом знижує бромоочищувальну здатність шару. Конструкція ключових елементів процесу з унікальних стійких до корозії матеріалів Корозія, викликана галоген-вмісним процесом, у конденсованій фазі або паровій фазі, являє значну проблему при виборі довговічних матеріалів для побудови реакторів, трубопроводів та допоміжного обладнання. Керамічні матеріали, такі, як 95276 24 глинозем, діоксид цирконію та карбіди кремнію, забезпечують виключну стійкість до корозії для більшості умов, які трапляються в описаному авторами процесі. Однак кераміка має багато недоліків, включаючи відсутність конструкційної міцності в умовах деформації розтягнення, труднощі з повним утриманням реакцій газової фази (через дифузію або масопередачу уздовж стикових поверхонь) та можливі небажані характеристики теплопередачі, властиві для більшості керамічних матеріалів. Побудова довговічного, газонепроникного і стійкого до корозії обладнання для контролювання процесу (тобто, теплообмінників оболонкового та трубчастого типу, клапанів, насосів і т. ін.) для функціонування при підвищених температурах та тиску і протягом тривалого періоду часу, очевидно, вимагає застосування металів, які піддаються формуванню, таких, як Au, Co, Cr, Fe, Nb, Ni, Pt, Та, Ті та/або Zr, або сплавів цих основних металів, які містять такі елементи, як Аl, В, С, Co, Cr, Cu, Fe, H, Ha, La, Mn, Mo, N, Nb, Ni, О, Р, Pd, S, Si, Sn, Та, Ті, V, W, Y та/або Zr. Згідно з одним варіантом втілення винаходу, описані авторами процес та підпроцеси здійснюють у реакторах, трубопроводах та допоміжному обладнанні, які є достатньо міцними і достатньо стійкими до корозії для забезпечення довготривалого безперервного функціонування. Вибір прийнятних матеріалів для конструкції значною мірою залежить від температури та середовища впливу для кожного з компонентів контролю над процесом. Прийнятні матеріали для компонентів, які зазнають впливу циклічних умов (наприклад, окиснення та відновлення), порівняно з односпрямованими умовами (окиснення або відновлення), можуть бути різними. Необмежувальними прикладами матеріалів, визначених як прийнятні для циклічних умов при експлуатації в діапазоні температур 150-550 °С, є Аu і сплави Ті та Ni, причому найбільш придатними є Al/V у сплаві з Ті (зокрема, Ті Grd-5) та сплави Ni-Cr-Mo з високим вмістом Сr, низьким вмістом Fe та низьким вмістом С (зокрема, ALLCORR®, Alloy 59, С-22, 625 та НХ). Необмежувальними прикладами матеріалів, визначених як прийнятні для впливу повітря на галогенангідрид або циклічних умов впливу повітря на молекулярний галоген у діапазоні температур 150-550 °С, для впливу повітря на галогенангідрид або молекулярний галоген, є сплави Fe та Ni, причому найбільш придатними є сплави груп NiCr-Mo та Ni-Mo. Необмежувальними прикладами матеріалів, визначених як прийнятні для односпрямованих умов середовища, у діапазоні температур 100°С-550°С, є Та, Аu і сплави Fe, Co та Ni. Для більш низькотемпературних умов (
ДивитисяДодаткова інформація
Назва патенту англійськоюContinuous process for converting hydrocarbon feedstock into one or more higher hydrocarbons
Автори англійськоюGadewar Sagar B., Wyrsta, Michael, D., Grosso Philip, Zhang, Aihua, Mcfarland Eric, Komon, Zachary, J.A., Sherman Jeffrey H.
Назва патенту російськоюНепрерывный процесс преобразования углеводного сырья в один или более высших углеводородов (варианты)
Автори російськоюГадивар Сагар Б., Уирста Макл Д., Гроссо Филип, Жанг Айхуа, Макфарленд Эрик, Комон Закари Дж. А., Шерман Джеффри Х.
МПК / Мітки
Мітки: процес, безперевний, вуглеводневої, перетворення, більше, сировини, вищих, вуглеводнів, варіанти
Код посилання
<a href="https://ua.patents.su/22-95276-bezperevnijj-proces-peretvorennya-vuglevodnevo-sirovini-na-odin-abo-bilshe-vishhikh-vuglevodniv-varianti.html" target="_blank" rel="follow" title="База патентів України">Безперевний процес перетворення вуглеводневої сировини на один або більше вищих вуглеводнів (варіанти)</a>
Попередній патент: Плавлений литий тугоплавкий продукт з високим вмістом цирконію, спосіб його одержання, склоплавильна піч та електролізна камера, що його містять
Наступний патент: Рідка гербіцидна композиція
Випадковий патент: Мотор-колесо вовка