Аналоги 20(s)-камптотецину, спосіб їх одержання, фармацевтична композиція та спосіб лікування раку, лейкозу або станів пов’язаних з віл
Номер патенту: 51666
Опубліковано: 16.12.2002
Автори: Дуввурі Субрахманян, Тхунгатхуртхі Састрі В.Р.С, Ведула Шарма Манохара, Акелла Венкатесварлу, Чінтакунта Вамсі Крішна, Мадабхуші Шобха
Формула / Реферат
1. Аналоги 20(S)-камптотецину формули 1:
,
1
де R1, R2, R3, і R4 незалежно означають водень або вибрані з групи, яка складається з гідрокси, нижчого алкокси, нижчого алканоїлу, нітро, ціано, галогену, карбокси, карбонілокси, аміно, заміщеного аміно, де аміногрупа є моно або дизаміщеною, в якій замісники вибрані з алкілу, галогеналкілу, бензилу. бензоїлу, карбоксилу, амідо або алкіламіно; нижчого алкілу або заміщеного нижчого алкілу, в якому замісники вибрані з гідроксилу, галогеналкілу, бензилу, алкокси, бензилокси, ціано, нітро, аміно або алкіламіно; кожен із R1, R2, R3 і R4 є різними, за винятком, коли кожен із R1, R2, R3 і R4 є воднем, або R2 і R3 разом означають -О-(СН2)n-O-, де n=1 або 2;
R5 означає водень, нижчий алкіл, заміщений нижчий алкіл, де замісник вибраний з гідроксилу, галогену, бензилокси, карбоксилу, амідо або аміно, де аміногрупа є моно або дизаміщеною, в якій замісники вибрані з алкілу, галогеналкілу, бензилу, бензоїлу, коли аміногрупа є дизаміщеною, замісники є незалежними або об'єднаними разом з утворенням циклічного кільця, яке має 5 або 6 кільцевих атомів, і кільцевими атомами є атоми вуглецю, атом азоту і один або два гетероатоми, вибрані з азоту, кисню або сірки; або нижчий аралкіл, де арильною групою є феніл, біфеніл або нафтил; і
R6 означає водень; феніл або бензил, де фенільна група може бути незаміщеною або заміщеною одним, двома, трьома замісниками, вибраними з галогену, нижчого алкокси, ціано, нітро, нижчого алкілу, аміно, заміщеного аміно, де аміногрупа є моно або дизаміщеною, в якій замісниками є нижчі алкільні групи; циклоалкіл або циклоалкіл нижчого алкілу, де циклічне ядро містить від 3 до 7 атомів кільця, всі з яких є атомами вуглецю; нижчі алкільні групи, заміщені гетероциклічними ядрами, які містять від 3 до 7 атомів кільця, які є атомами вуглецю і одним або двома гетероатомами, вибраними з кисню, азоту і сірки; нижчий алканоїл; бензоїл, в якому фенільна група може бути незаміщеною або заміщеною, коли фенільна група заміщена, замісник вибраний з нижчого алкілу, галогеналкілу, галогену, нижчого алкокси, тіоалкокси, ціано, нітро, амідо, аміно або алкіламіно; нижчий алкеніл, нижчий алкіл, заміщений нижчий алкіл, заміщений нижчий алкеніл, заміщений нижчий алканоїл, в яких замісники вибрані з галогену, гідрокси, алкокси, арилокси, тіо, тіоалкілу, тіоарилу, арилу, де арильна група вибрана з фенілу, біфенілу або нафтилу; гетероарилу, де гетероарил вибраний з піридилу, хіноліну, ізохіноліну, індолу, піролу, фурану, бензофурану, тіофену, піримідину, тіазолу і імідазолу; карбокси, ціано, нітро, амідо або аміно, в якому аміногрупа може бути незаміщеною або моно або дизаміщеною, в якій замісники вибрані з гідроксилу, алкілу, галогеналкілу, бензилу, бензоїлу, алкокси, карбоксилу, амідо, аміно або алкіламіно, коли аміногрупа є дизаміщеною, замісники є незалежними або об'єднані з утворенням циклічного кільця, яке містить 5 або 6 кільцевих атомів, кільцевими атомами є атоми вуглецю, атом азоту і один або два гетероатоми, вибрані з азоту, кисню або сірки;
за умови, що (І) коли R1 є метокси, R6 не є воднем або нижчою алкільною групою; (II) коли R2 є гідрокси, нижчий алкокси, нітро, аміно, алкіламіно, ациламіно або галоген, R6 не є воднем, нижчою алкільною групою або алканоїлом; (III) коли R5 є нижчий алкіл, нижчий аралкіл, де арильна група представляє феніл, біфеніл або нафтил, СН2ОН, СООН, СООМе або CH2OR", де R" представляє нижчу алкільну або ацильну групу, R6 не є воднем, нижчою алкільною групою або алканоїлом; (IV) коли R1 представляє метоксигрупу, R2 представляє гідрокси, нижчий алкокси, нітро, аміно, алкіламіно, ациламіно або галоген, R5 представляє нижчий алкіл, нижчий аралкіл. CH2OH, СООН, СООМе, CH2R", де R" представляє нижчу алкільну або ацильну групу, R6 не є воднем або нижчою алкільною групою; або (V) коли R1 - R5 представляють водень, R6 не є воднем, нижчою алкільною групою, алканоїлом або бензилом.
2. Сполука згідно з п. 1, де нижчим алкілом є (С1-С8) алкіл, нижчим алкенілом є (С2-С8) алкеніл, і нижчим алкокси є (С1-С8) алкокси.
3. Сполука згідно з п. 1, вибрана із:
5-трифторетокси-СРТ;
9-нітро-10-гідрокси-5-(2'-метоксіетокси)-СРТ;
9-нітро-5-(2'-метоксіетокси)-СРТ;
9-гідроксі-5-етокси-СРТ;
9-нітро-5-етокси-СРТ;
9-нітро-5-гідрокси-СРТ;
7-етил-5-хлоретокси-СРТ;
5-(2'-гідроксіетокси)-CPT;
10-гідрокси-5-(2'-гідроксіетокси)-СРТ;
7-етил-10-гідрокси-5-(2'-гідроксіетокси)-СРТ;
9-нітро-5-фторетокси-СРТ;
10-гідрокси-5-трифторетокси-СРТ;
7-етил-10-гідрокси-5-трифторетокси-СРТ;
7-етил-5-піролідиноетокси-СРТ;
7-етил-5-диметиламінопропокси-СРТ;
7-етил-10-гідрокси-5-фторетокси-СРТ;
5-(2'-riдpoкcіeтoкcи)-7-eтил-CPT;
5-(2'-метоксіетокси)-СРТ;
де СРТ означає 20(S)-камптотецин.
4. Сполука формули 1 згідно з будь-яким із пп. 1-3, де R1-R6 мають значення, вказані в будь-якому з пп. 1-3, у вигляді суміші двох діастереомерів, де вказані діастереомери мають конфігурації 20 (S), 5 (R ) і 20 (S), 5 (S).
5. Сполуки формули 1 згідно з будь-яким із пп. 1-3, в яких кожен із діастереомерів, що має конфігурації 20 (S), 5 (R ) і 20 (S), 5 (S) у вигляді окремого ізомера, по суті вільні від другого ізомера, де R1-R6 мають значення, вказані в пп. 1-3.
6. Фармацевтична композиція, що містить ефективну кількість сполуки формули 1, вказану в будь-якому з пп. 1-5, або її похідної і фармацевтично прийнятний нетоксичний ексципієнт, розріджувач або розчинник.
7. Сполука згідно з будь-яким з пп. 1-5, яка використовується при одержанні лікарського засобу для лікування раку, лейкозу або станів, пов'язаних з ВІЛ.
8. Спосіб одержання сполук формули 1, що включає стадії:
(І) взаємодії сполук формули 2:
,
2
де R1 – R5 мають значення, вказані в п. 1, в присутності кислоти, вибраної із неорганічної кислоти або кислот Льюіса, і солі заліза (ІІІ), із сполукою, що має формулу: R6-OH, де R6 означає нижчий алкіл, нижчий алкеніл, (С3-С7)-циклоалкіл, галогеналкіл або гідроксиалкіл, з одержанням сполук формули 12 і сполук формули 13:
12
,
13
де R1, R2, R3, R4, R5 мають значення, вказані в п. 1, необов'язково;
(II) розділення сполук формул 12 і 13, отриманих на стадії (І), необов'язково;
(III) гідроліз сполук формули 12 з одержанням додаткової кількості сполук формули 13 і, необов'язково;
(IV) взаємодії сполуки формули 13 в присутності кислоти, вибраної з неорганічної кислоти, кислот Льюіса або органічних кислот, зі сполукою, що має формулу: R6-ОН, з одержанням сполук формули 1:
,
де R1, R2, R3, R4 і R5 мають значення, вказані в п. 1, і R6 означає водень, феніл або бензил, де фенільна група може бути незаміщеною або заміщеною одним, двома або трьома замісниками, вибраними з галогену, нижчого алкокси, ціано, нітро, нижчого алкілу, аміно або заміщеного аміно, де аміногрупа є моно або дизаміщеною, в якій замісниками є нижчі алкільні групи; циклоалкіл або циклоалкіл нижчий алкіл, де циклічне кільце містить від 3 до 7 атомів кільця, всі з яких є атомами вуглецю; нижчі алкільні групи, заміщені гетероциклічними кільцями, що містять від 5 до 7 атомів кільця, які є атомами вуглецю і одним або двома гетероатомами, вибраними з кисню, азоту і сірки; нижчий алканоїл; бензоїл, в якому фенільна група може бути незаміщеною або заміщеною, коли фенільна група заміщена, замісник вибраний з нижчого алкілу, галогеналкілу, галогену, нижчого алкокси, тіоалкокси, ціано, нітро, амідо, аміно або алкіламіно; нижчий алкеніл, нижчий алкіл, заміщений нижчий алкіл, заміщений нижчий алкеніл, заміщений нижчий алканоїл, в яких замісники вибрані із галогену, гідрокси, алкокси, арилокси, тіо, тіоалкілу, тіоарилу, арилу, де арильна група вибрана з фенілу, біфенілу або нафтилу; гетероарилу, де гетероарил вибраний з піридилу, хіноліну, ізохіноліну, індолу, піролу, фурану. бензофурану, тіофену, піримідину, тіазолу та імідазолу; карбокси, ціано, нітро, амідо або аміно, в якому аміногрупа може бути незаміщеною або моно або дизаміщеною, в якій замісники вибрані з гідроксилу, алкілу, галогеналкілу, бензилу, бензоїлу, алкокси, карбоксилу, амідо, аміно або алкіламіно, коли аміногрупа є дизаміщеною, замісники є незалежними або об'єднані з утворенням циклічного кільця, що містить 5 або 6 кільцевих атомів, кільцевими атомами є атоми вуглецю, атом азоту і один або два гетероатоми, вибрані з азоту, кисню або сірки;
за умови, що (І) коли R1 є метокси, R6 не є воднем або нижчою алкільною групою; (II) коли R2 є гідрокси, нижчий алкокси, нітро, аміно, алкіламіно, ациламіно або галоген, R6 не є воднем, нижчою алкільною групою або алканоїлом; (ІІІ) коли R5 означає нижчий алкіл, нижчий аралкіл, де арильна група представляє феніл, біфеніл або нафтил, CH2OH, СООН, COOMe, CH2OR", де R" означає нижчу алкільну або ацильну групу, R6 не є воднем, нижчою алкільною групою або алканоїлом; (IV) коли R1 означає метоксигрупу, R2 означає гідрокси, нижчий алкокси, нітро, аміно, алкіламіно, ациламіно або галоген, R5 означає нижчий алкіл, нижчий аралкіл, СН2ОН, СООН, COOMe, CH2OR", де R" означає нижчу алкільну або ацильну групу, R6 не є воднем або нижчою алкільною групою; або (V) коли R1-R5 означає водень, R6 не є воднем, нижчою алкільною групою, алканоїлом або бензилом.
9. Спосіб згідно з п. 8 одержання сполуки формули 1, де R1, R3, R4 і R5 означає атоми водню, R2 означає гідроксильну групу, і R6 означає трифторетильну групу, що включає стадії:
(І) взаємодії сполуки формули 2:
,
де R1, R3, R4 і R5 означають водень, R2 означає гідроксильну групу, в присутності концентрованої сірчаної кислоти і тригідрату хлорида заліза (ІІІ), з етанолом, і нагрівання суміші в умовах кип'ятіння зі зворотним холодильником з одержанням сполуки формули 12 і сполуки формули 13:
12
,
13
де R1, R3, R4 і R5 означають водень, R2 означає гідроксильну групу, і R6 означає етильну групу,
(II) розділення сполук формул 12 і 13, одержаних на стадії (І),
(III) гідролізу сполук формули 12 шляхом розчинення у водному етанолі і кип'ятіння зі зворотним холодильником з хлороводневою кислотою з одержанням додаткової кількості сполуки формули 13,
(IV) взаємодії сполуки формули 13 в пристуності концентрованої сірчаної кислоти з трифторетанолом, розчиненим у розчиннику дихлоретані, з одержанням сполуки формули 1:
,
де R1, R3, R4, і R5 означають водень, R2 означає гідроксильну групу, і R6 означає трифторетильну групу.
10. Спосіб одержання згідно з п. 8 сполук формули 1
,
де R6 означає водень або нижчий алкіл, R1 означає водень або метокси, R2 означає водень, гідрокси, нижчий алкокси, ацилокси, SH, тіоалкіл, тіоацил, нітро, аміно, алкіламіно, ациламіно або галоген; R3 і R4 означають водень, і R5 означає водень, нижчий алкіл, нижчий аралкіл, CH2OH, СООН, СООМе або CH2OR', де R' означає нижчу алкільну або ацильну групу, що включає стадії:
(І) взаємодії сполук формули 2:
,
де R1 - R5 мають вказані вище значення, в присутності кислоти, вибраної з неорганічних кислот або кислот Льюіса, і солей заліза (ІІІ) із сполукою формули: R6-OH, де R6 означає нижчі алкільні групи, для одержання сполук формули 12 і сполук формули 13;
12
,
13
де R1, R2, R3, R4, і R5 мають вказані вище значення,
(II) розділення сполук формул 12 і 13, одержаних на стадії (І),
(IIІ) гідролізу сполук формули 12 з одержанням додаткової кількості сполук формули 13, і, необов'язково,
(IV) взаємодії сполуки формули 13 в присутності кислоти, вибраної з органічної кислоти, неорганічних кислот або кислот Льюіса, зі сполукою, що має формулу: R6-OH, з одержанням сполук формули 1:
,
де R1 , R2 , R3 , R4 , і R5 мають вказані вище значення і R6 означає нижчу алкільну групу.
11. Спосіб згідно з пп. 8 або 10, де сіллю заліза (ІІІ) є хлорид заліза (3).
12. Спосіб лікування раку, лейкозу або станів, пов'язаних з ВІЛ, який передбачає введення сполуки згідно з будь-яким із пп. 1-5.
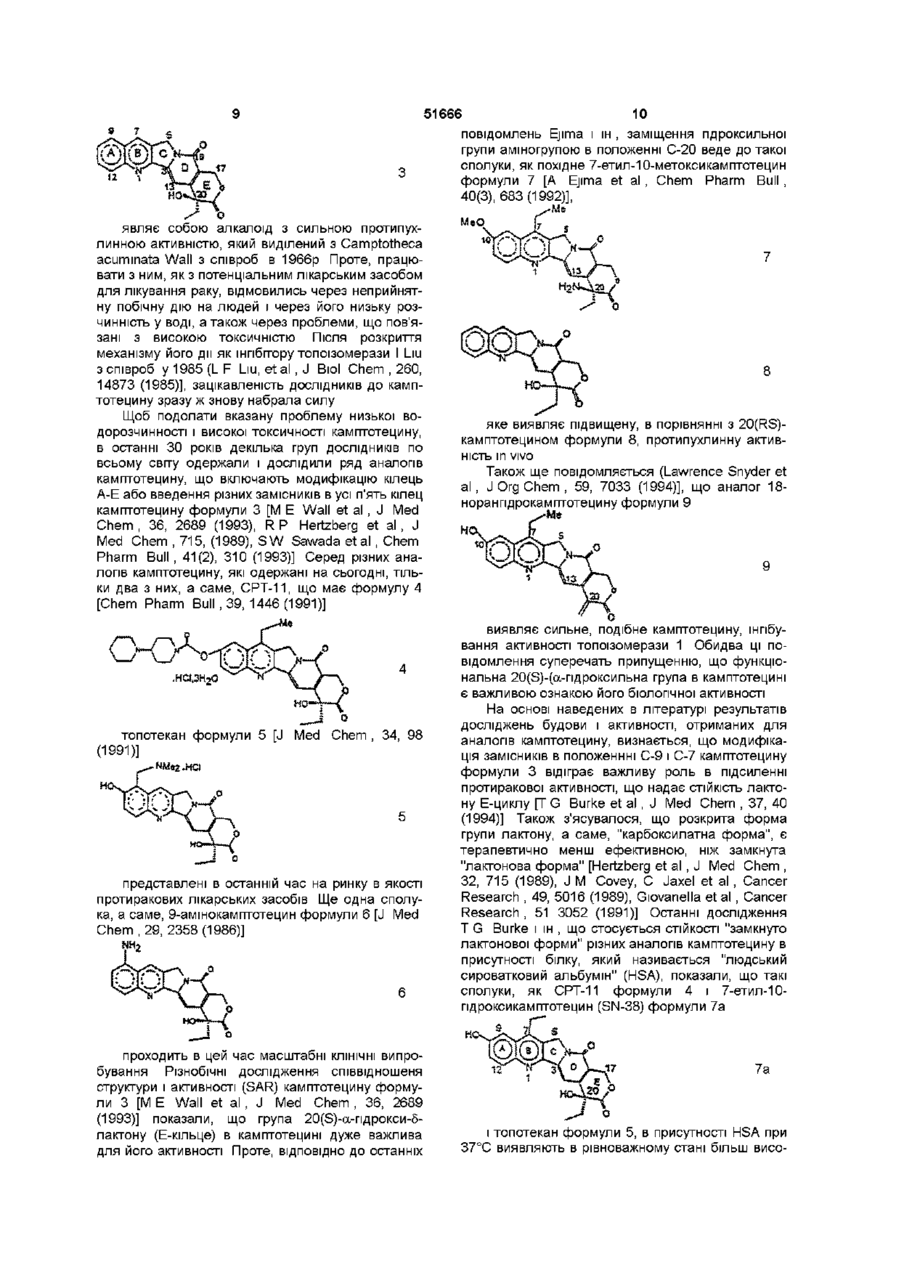
Текст
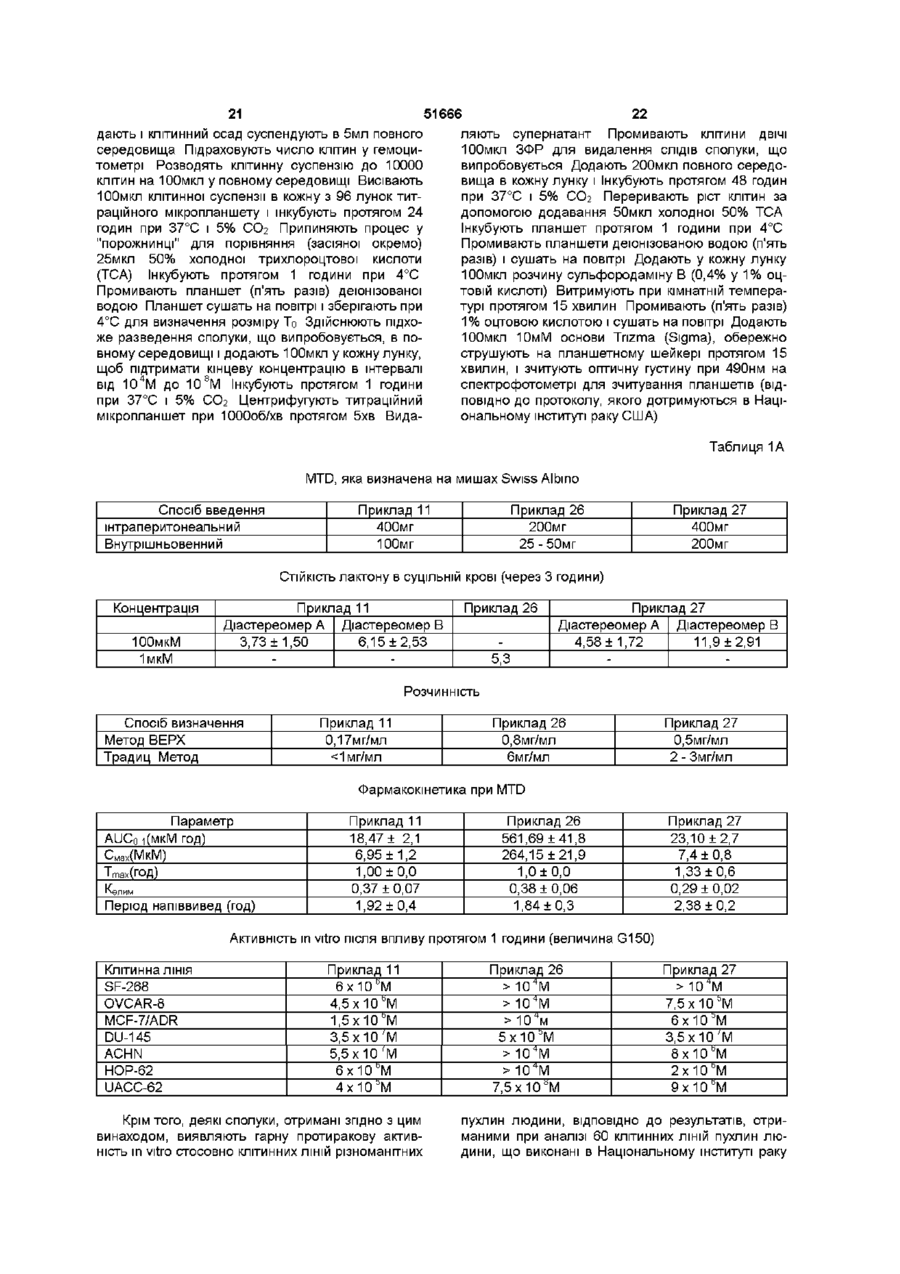
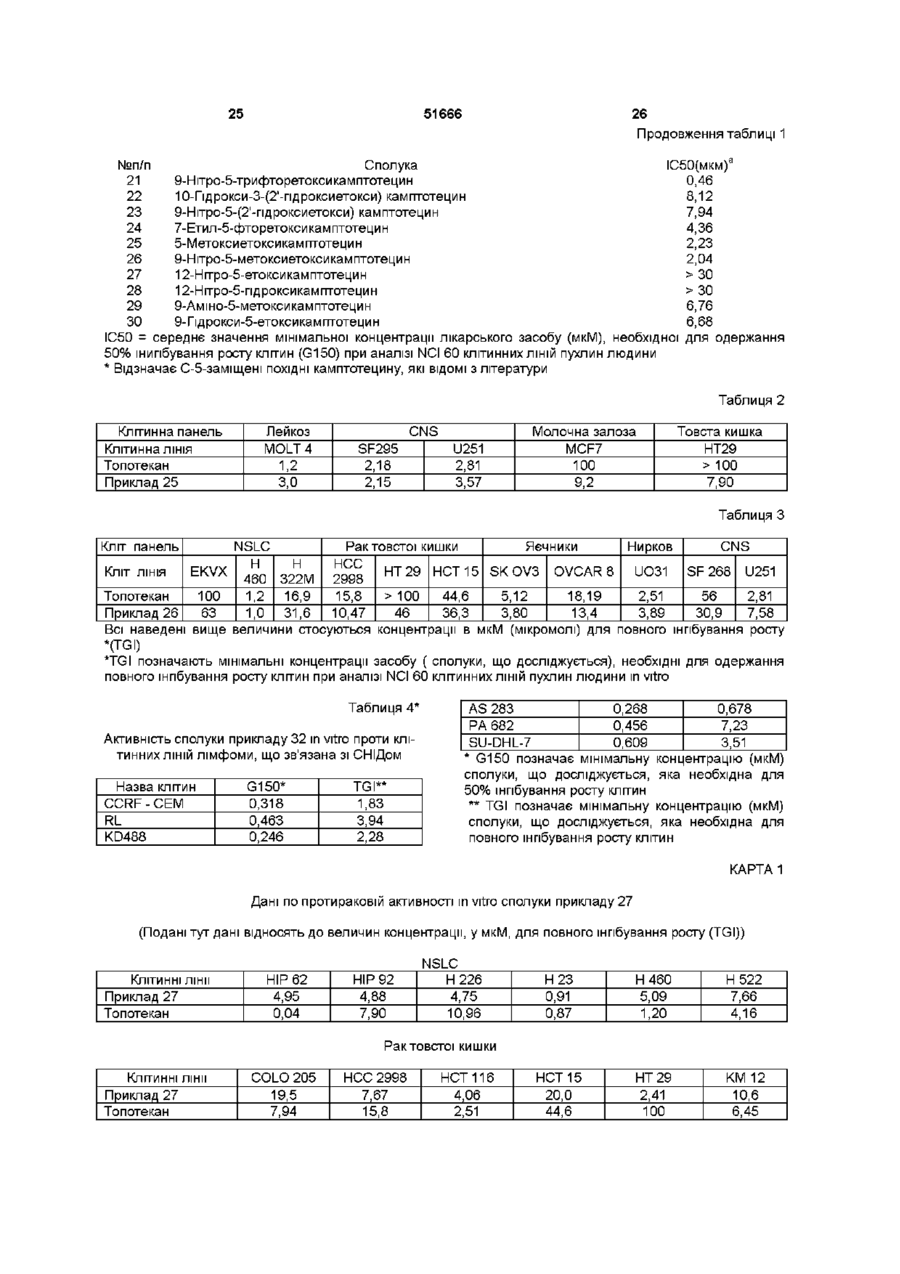
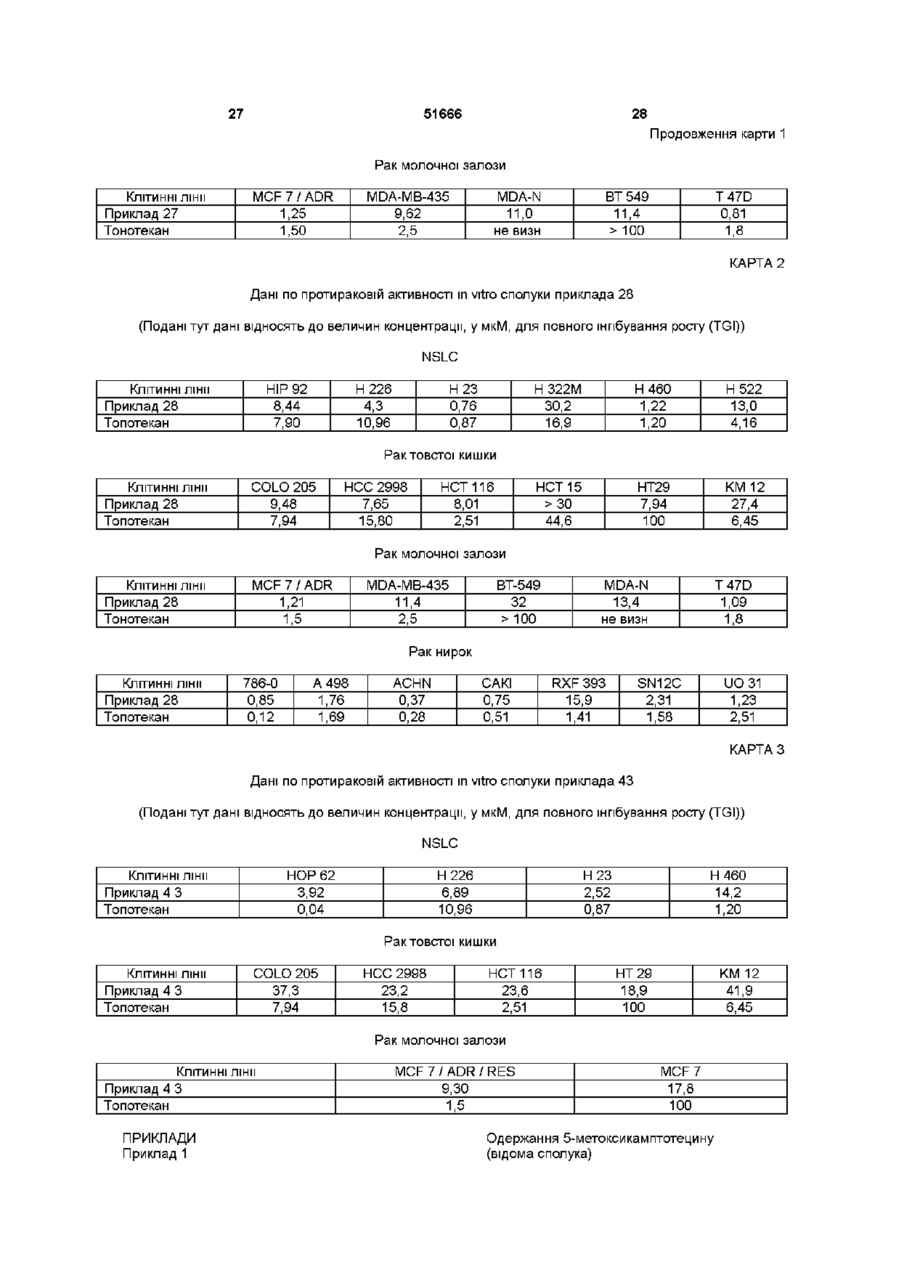
1 Аналоги 20(Э)-камптотецину формули 1 де R1, R2, R3, і R4 незалежно означають водень або вибрані з групи, яка складається з гідрокси, нижчого алкокси, нижчого алканоілу, нітро, ціано, галогену, карбокси, карбонілокси, аміно, заміщеного аміно, де аміногрупа є моно або дизаміщеною, в якій замісники вибрані з алкілу, галогеналкілу, бензилу бензоілу, карбоксилу, амідо або алкіламіно, нижчого алкілу або заміщеного нижчого алкілу, в якому замісники вибрані з гідроксилу, галогеналкілу, бензилу, алкокси, бензилокси, ціано, нітро, аміно або алкіламіно, кожен із R1, R2, R3 і R4 є різними, за винятком коли кожен із R1, R2, R3 і R4 є воднем, або R2 і R разом означають -O-fCbhJn-O-, де п=1 або 2, R5 означає водень, нижчий алкіл, заміщений нижчий алкіл, де замісник вибраний з гідроксилу, галогену, бензилокси, карбоксилу, амідо або аміно, де аміногрупа є моно або дизаміщеною, в якій заміс ТА ники вибрані з алкілу, галогеналкілу, бензилу, бензоїлу, коли аміногрупа є дизаміщеною, замісники є незалежними або об'єднаними разом з утворенням циклічного кільця, яке має 5 або 6 кільцевих атомів, і кільцевими атомами є атоми вуглецю, атом азоту і один або два гетероатоми, вибрані з азоту, кисню або сірки, або нижчий аралкіл, де арильною групою є феніл, біфеніл або нафтил, і R6 означає водень, феніл або бензил, де фенільна група може бути незаміщеною або заміщеною одним, двома, трьома замісниками, вибраними з галогену, нижчого алкокси, ціано, нітро, нижчого алкілу, аміно, заміщеного аміно, де аміногрупа є моно або дизаміщеною, в якій замісниками є нижчі алкільні групи, циклоалкіл або циклоалкіл нижчого алкілу, де циклічне ядро містить від 3 до 7 атомів кільця, всі з яких є атомами вуглецю, нижчі алкільні групи, заміщені гетероциклічними ядрами, які містять від 3 до 7 атомів кільця, які є атомами вуглецю і одним або двома гетероатомами, вибраними з кисню, азоту і сірки, нижчий алканоїл, бензоіл, в якому фенільна група може бути незаміщеною або заміщеною, коли фенільна група заміщена, замісник вибраний з нижчого алкілу, галогеналкілу, галогену, нижчого алкокси, тюалкокси, ціано, нітро, амідо, аміно або алкіламіно, нижчий алкеніл, нижчий алкіл, заміщений нижчий алкіл, заміщений нижчий алкеніл, заміщений нижчий алканоїл, в яких замісники вибрані з галогену, гідрокси, алкокси, арилокси, тю, тюалкілу, тюарилу, арилу, де арильна група вибрана з фенілу, біфенілу або нафтилу, гетероарилу, де гетероарил вибраний з піридилу, хіноліну, ізохшоліну, індолу, піролу, фурану, бензофурану, тюфену, піримідину, тіазолу і імідазолу, карбокси, ціано, нітро, амідо або аміно, в якому аміногрупа може бути незаміщеною або моно або дизаміщеною, в якій замісники вибрані з гідроксилу, алкілу, галогеналкілу, бензилу, бензоілу, алкокси, карбоксилу, амідо, аміно або алкіламіно, коли аміногрупа є дизаміщеною, замісники є незалежними або об'єднані з утворенням циклічного кільця, яке містить 5 або 6 кільцевих атомів, кільцевими атомами є атоми вуглецю, атом азоту і один або два гетероатоми, вибрані з азоту, кисню або сірки, за умови, що (І) коли R1 є метокси, R6 не є воднем або нижчою алкільною групою, (II) коли R2 є гідро О (О (О (О ю 51666 кси, нижчий алкокси, нітро, аміно, алкіламшо, аци6 ламіно або галоген, R не є воднем, нижчою алкі5 льною групою або алканоілом, (III) коли R є нижчий алкіл, нижчий аралкіл, де арильна група представляє феніл, біфеніл або нафтил, СЬЬОН, СООН, СООМе або CH2OR", де R" представляє 6 нижчу алкільну або ацильну групу, R не є воднем, нижчою алкільною групою або алканоілом, (IV) 1 2 коли R представляє метоксигрупу, R представляє гідрокси, нижчий алкокси, нітро, аміно, алкіла5 мшо, ациламшо або галоген, R представляє нижчий алкіл, нижчий аралкіл СЬЬОН, СООН, СООМе, CH2R", де R" представляє нижчу алкільну 6 або ацильну групу, R не є воднем або нижчою 1 5 алкільною групою, або (V) коли R - R представ6 ляють водень, R не є воднем, нижчою алкільною групою, алканоілом або бензилом 2 Сполука згідно з п 1, де нижчим алкілом є ( d Cs) алкіл, нижчим алкенілом є (Сг-Сз) алкеніл, і нижчим алкокси є (С-і-Сз) алкокси 3 Сполука згідно з п 1, вибрана із 5-трифторетокси-СРТ, 9-нітро-10-пдрокси-5-(2'-метоксіетокси)-СРТ, 9-нітро-5-(2'-метоксіетокси)-СРТ, 9-пдроксі-5-етокси-СРТ, 9-нітро-5-етокси-СРТ, 9-нітро-5-пдрокси-СРТ, 7-етил-5-хлоретокси-СРТ, 5-(2'-пдроксіетокси)-СРТ, 10-пдрокси-5-(2'-пдроксіетокси)-СРТ, 7-етил-10-пдрокси-5-(2'-пдроксіетокси)-СРТ, 9-нітро-5-фторетокси-СРТ, 10-пдрокси-5-трифторетокси-СРТ, 7-етил-10-пдрокси-5-трифторетокси-СРТ, 7-етил-5-піролідиноетокси-СРТ, 7-етил-5-диметиламшопропокси-СРТ, 7-етил-10-пдрокси-5-фторетокси-СРТ, 5-(2'-пдроксіетокси)-7-етил-СРТ, 5-(2'-метоксіетокси)-СРТ, де СРТ означає 20(3)-камптотецин 4 Сполука формули 1 згідно з будь-яким із пп 1 З, де R1-R6 мають значення, вказані в будь-якому з пп 1-3, у вигляді суміші двох діастереомерів, де вказані діастереомери мають конфігурації 20 (S), 5 (R) і 20 (S), 5(S) 5 Сполуки формули 1 згідно з будь-яким із пп 1 З, в яких кожен із діастереомерів, що має конфігурації 20 (S), 5 (R ) і 20 (S), 5 (S) у вигляді окремого ізомера, по суті ВІЛЬНІ ВІД другого ізомера, де R1-R6 мають значення, вказані в пп 1-3 6 Фармацевтична композиція, що містить ефективну КІЛЬКІСТЬ сполуки формули 1, вказану в будьякому з пп 1 - 5, або її похідної і фармацевтично прийнятний нетоксичний ексципієнт, розріджувач або розчинник 7 Сполука згідно з будь-яким з пп 1 - 5, яка використовується при одержанні лікарського засобу для лікування раку, лейкозу або станів, пов'язаних з ВІЛ 8 Спосіб одержання сполук формули 1, що включає стадії (І) взаємодії сполук формули 2 1 5 де R - R мають значення, вказані в п 1, в присутності кислоти, вибраної із неорганічної кислоти або кислот Льюіса, і солі заліза (III), із сполукою, що 6 6 має формулу R -OH, де R означає нижчий алкіл, нижчий алкеніл, (Сз-С7)-циклоалкіл, галогеналкіл або пдроксиалкіл, з одержанням сполук формули 12 і сполук формули 13 .R OS 12 13 R* де R1, R2, R3, R4, R5 мають значення, вказані в п 1, необов'язково, (II) розділення сполук формул 12 і 13, отриманих на стадії (І), необов'язково, (III) гідроліз сполук формули 12 з одержанням додаткової КІЛЬКОСТІ сполук формули 13 і, необов'язково, (IV) взаємодії сполуки формули 13 в присутності кислоти, вибраної з неорганічної кислоти, кислот Льюіса або органічних кислот, зі сполукою, що має формулу R6-OH, з одержанням сполук формули 1 11 й5 *• де R1, R2, R3, R4 і R5 мають значення, вказані в п 1, і R6 означає водень, феніл або бензил, де фенільна група може бути незаміщеною або заміщеною одним, двома або трьома замісниками, вибраними з галогену, нижчого алкокси, ціано, нітро, нижчого алкілу, аміно або заміщеного аміно, де аміногрупа є моно або дизаміщеною, в якій замісниками є нижчі алкільні групи, циклоалкіл або циклоалкіл нижчий алкіл, де циклічне кільце містить від 3 до 7 атомів кільця, всі з яких є атомами вуглецю, нижчі алкільні групи, заміщені гетероциклічними кільцями, що містять від 5 до 7 атомів кільця, які є атомами вуглецю і одним або двома гетероатомами, вибраними з кисню, азоту і сірки, нижчий алканоїл, бензоїл, в якому фенільна група може бути незаміщеною або заміщеною, коли фенільна група заміщена, замісник вибраний з нижчого алкілу, галогеналкіл у, галогену, нижчого алкокси, тюалко 51666 кси, ціано, нітро, амідо, аміно або алкіламіно, нижчий алкеніл, нижчий алкіл, заміщений нижчий алкіл, заміщений нижчий алкеніл, заміщений нижчий алканоїл, в яких замісники вибрані із галогену, гідрокси, алкокси, арилокси, тю, тюалкілу, тюарилу, арилу, де арильна група вибрана з фенілу, біфенілу або нафтилу, гетероарилу, де гетероарил вибраний з піридилу, хіноліну, ізохшоліну, індолу, піролу, фурану бензофурану, тюфену, піримідину, тіазолу та імідазолу, карбокси, ціано, нітро, амідо або аміно, в якому аміногрупа може бути незаміщеною або моно або дизаміщеною, в якій замісники вибрані з гідроксилу, алкілу, галогеналкілу, бензилу, бензоілу, алкокси, карбоксилу, амідо, аміно або алкіламіно, коли аміногрупа є дизаміщеною, замісники є незалежними або об'єднані з утворенням циклічного кільця, що містить 5 або 6 кільцевих атомів, кільцевими атомами є атоми вуглецю, атом азоту і один або два гетероатоми, вибрані з азоту, кисню або сірки, за умови, що (І) коли R1 є метокси, R6 не є воднем або нижчою алкільною групою, (II) коли R2 є гідрокси, нижчий алкокси, нітро, аміно, алкіламіно, ациламіно або галоген, R6 не є воднем, нижчою алкільною групою або алканоілом, (III) коли R5 означає нижчий алкіл, нижчий аралкіл, де арильна група представляє феніл, біфеніл або нафтил, СН2ОН, СООН, COOMe, CH2OR", де R" означає нижчу алкільну або ацильну групу, R6 не є воднем, нижчою алкільною групою або алканоілом, (IV) коли R1 означає метоксигрупу, R2 означає гідрокси, нижчий алкокси, нітро, аміно, алкіламіно, ациламшо або галоген, R5 означає нижчий алкіл, нижчий аралкіл, СН2ОН, СООН, COOMe, CH2OR", де R" означає нижчу алкільну або ацильну групу, R6 не є воднем або нижчою алкільною групою, або (V) коли R1-R5 означає водень, R6 не є воднем, нижчою алкільною групою, алканоілом або бензилом 9 Спосіб згідно з п 8 одержання сполуки формули 1, де R1, R3, R4 і R5 означає атоми водню, R означає гідроксильну групу, і R6 означає трифторетильну групу, що включає стадії (І) взаємодії сполуки формули 2 де R1, R3, R4 і R5 означають водень, R2 означає гідроксильну групу, в присутності концентрованої сірчаної кислотиі трипдрату хлорида заліза (III), з етанолом, і нагрівання суміші в умовах кип'ятіння зі зворотним холодильником з одержанням сполуки формули 12 і сполуки формули 13 .OR6 12 13 1 3 4 5 2 де R , R , R і R означають водень, R означає 6 гідроксильну групу, і R означає етильну групу, (II) розділення сполук формул 12 і 13, одержаних на стадії (І), (III) гідролізу сполук формули 12 шляхом розчинення у водному етанолі і кип'ятіння зі зворотним холодильником з хлороводневою кислотою з одержанням додаткової КІЛЬКОСТІ сполуки формули 13, (IV) взаємодії сполуки формули 13 в пристуності концентрованої сірчаної кислоти з трифторетанолом, розчиненим у розчиннику дихлоретані, з одержанням сполуки формули 1 де R1, R3, R4, і R5 означають водень, R2 означає гідроксильну групу, і R6 означає трифторетильну групу 10 Спосіб одержання згідно з п 8 сполук формули 1 де R6 означає водень або нижчий алкіл, R1 означає водень або метокси, R2 означає водень, гідрокси, нижчий алкокси, ацилокси, SH, тюалкіл, тюацил, нітро, аміно, алкіламіно, ациламіно або галоген, R3 і R4 означають водень, і R5 означає водень, нижчий алкіл, нижчий аралкіл, СН2ОН, СООН, СООМе або CH2OR', де R' означає нижчу алкільну або ацильну групу, що включає стадії (І) взаємодії сполук формули 2 a S 1 ^ де R - R мають вказані вище значення, в присутності кислоти, вибраної з неорганічних кислот або кислот Льюіса, і солей заліза (III) із сполукою формули R6-OH, де R6 означає нижчі алкільні групи, для одержання сполук формули 12 і сполук формули 13, OS R 12 51666 8 них кислот або кислот Льюіса, зі сполукою, що має формулу R6-OH, з одержанням сполук формули 1 он 17 13 де R1, R2, R3, R4, і R5 мають вказані вище значення, (II) розділення сполук формул 12 і 13, одержаних на стадії (І), (III) гідролізу сполук формули 12 з одержанням додаткової КІЛЬКОСТІ сполук формули 13, і, необов'язково, (IV) взаємодії сполуки формули 13 в присутності кислоти, вибраної з органічної кислоти, неорганіч Цей винахід стосується нових водорозчинних (С-циклічних) аналогів 20(3)-камптотецину, що містять циклічну систему з атомів вуглецю, які мають загальну формулу 1 В наведеній вище формулі 1 R1, R2, R3, і R4 є, незалежно, однаковими або різними й представляють водень, гідрокси, арилокси, нижчий алкокси, нижчий алканоїл, нітро, ціано, галоген, карбокси, карбонілокси, аміно, заміщений аміно нижчий алкіл, заміщений нижчий алкіл, або R і R3 разом представляють -О-(СН2)п-О-, де п = 1 або 2, R5 представляє водень, нижчий алкіл, заміщений нижчий алкіл, нижчий аралкіл, пдроксиметил, карбоксиметил, амінометил, заміщений амінометил, де аміногрупа може бути моно- або дизаміщеною, і в якій обидва замісники є незалежними або об'єднані з утворенням циклічної ядерної системи в цілому з 5-6 атомів, що містить атоми вуглецю і, необов'язково, один або два гетероатоми, обраних з кисню, азоту або сірки, і R6 представляє водень, феніл або бензил, де фенільна група може бути незаміщеною або з моно-, ди- або тризамісниками, які можуть бути обрані з галогену, гідрокси, нижчого алкокси, ціано, карбоксилу, нітро, аміно або заміщеного аміно, нижчого алкілу, заміщеного нижчого алкілу, циклоалкіл або циклоалкіл нижчого алкілу, де циклічне кільце представляє 3-7-членну кільцеву систему, що містить тільки атоми вуглецю, нижчі алкільні групи, які заміщені гетероциклічними ядрами, де гетероциклічна ядерна система містить, в цілому, 3-7 атомів, причому гетероциклічні ядра містять атоми вуглецю і, принаймні, один гетероатом, такий як атом кисню, азоту або сірки, нижчий алканоїл, бензоїл, де фенільна група може бути незаміщеною або заміщеною, нижчий алкеніл, нижчий алкіл, заміщений нижчий алкіл, заміщений нижчий алкеніл або заміщений нижчий ал де R1 , R2 , R3 , R4 , і R" мають вказані вище значення і R6 означає нижчу алкільну групу 11 Спосіб згідно з пп 8 або 10, де сіллю заліза (III) є хлорид заліза (3) 12 Спосіб лікування раку, лейкозу або станів, пов'язаних з ВІЛ, який передбачає введення сполуки згідно з будь-яким із пп 1 - 5 каноїл, де замісники можуть представляти собою галоген, гідрокси, нижчий алкокси, арилокси, тю, тюалкіл, тюарил, арил, гетероарил, карбокси, ціано нітро, амідо або аміно, при цьому аміногрупа може бути незаміщеною або моно- або дизамещеною, де обидва замісника є незалежними або об'єднаними з утворенням 5- або 6-членноі циклічної кільцевої системи, що містить атоми вуглецю, і, необов'язково, один або два гетероатоми, обраних з кисню, азоту або сірки, а загальна КІЛЬКІСТЬ атомів в ЦИКЛІЧНІЙ ядерній системі дорівнює 5 або 6, при умові, що (І) коли R1 представляє метоксигрупу R6 не є воднем або нижчою алкільною групою, (II) коли R2 являє собою гідрокси, нижчий алкокси, тюалкіл, нітро, аміно, алкіламшо, ациламшо або галоген, R6 не є воднем або нижчою алкільною групою, (III) коли R представляє нижчий алкіл, нижчий аралкіл, СН2ОН, СООН, СООМе або CH2OR", де R" представляє нижчу алкільну або ацильну групу, R6 не є воднем або нижчою алкільною групою, (IV) коли R1 являє собою метоксигрупу, R представляє гідрокси, нижчий алкокси, тюалкіл, нітро, аміно, алкіламшо, ациламшо або галоген, R5 представляє нижчий алкіл, нижчий аралкіл, СН2ОН, СООН, СООМе або CH2OR", де R" представляє нижчу алкільну або ацильну группу, R6 не є воднем або нижчою алкільно групою, (V) коли R1-R5 представляють собою атоми водню, R не є воднем або нижчою алкільною групою Всі вказані сполуки формули 1 одержують із сполук загальної формули 2 з хіральним центром 20(S) де замісники R -R мають значення, вказані вище Камптотецин, що має формулу З 51666 10 повідомлень Ejima і ш , заміщення гідроксильної групи аміногрупою в положенні С-20 веде до такої сполуки, як похідне 7-етил-10-метоксикамптотецин формули 7 [A Ejima et al , Chem Pharm Bull , 40(3), 683(1992)], являє собою алкалоїд з сильною протипухлинною активністю, який виділений з Camptotheca acummata Wall з співроб в 1966р Проте, працювати з ним, як з потенціальним лікарським засобом для лікування раку, відмовились через неприйнятну побічну дію на людей і через його низьку розчинність у воді, а також через проблеми, що пов'язані з високою токсичністю Після розкриття механізму його дії як інгібітору топоізомерази І Liu з співроб у 1985 (L F Liu, et al , J Biol Chem , 260, 14873 (1985)], зацікавленість ДОСЛІДНИКІВ ДО камптотецину зразу ж знову набрала силу Щоб подолати вказану проблему низької водорозчинності і високої токсичності камптотецину, в останні ЗО років декілька груп ДОСЛІДНИКІВ ПО всьому світу одержали і дослідили ряд аналогів камптотецину, що включають модифікацію кілець А-Е або введення різних замісників в усі п'ять кілец камптотецину формули З [М Е Wall et al , J Med C h e m , 36, 2689 (1993), R P Hertzberg et al , J Med Chem , 715, (1989), S W Sawada et al , Chem Pharm Bull , 41(2), 310 (1993)] Серед різних аналогів камптотецину, які одержані на сьогодні, тільки два з них, а саме, СРТ-11, що має формулу 4 [Chem Pharm Bull , 39, 1446 (1991)] яке виявляє підвищену, в порівнянні з 20(RS)камптотецином формули 8, протипухлинну активність in vivo Також ще повідомляється (Lawrence Snyder et al , J Org Chem , 59, 7033 (1994)], що аналог 18норанпдрокамптотецину формули 9 виявляє сильне, подібне камптотецину, інгібування активності топоізомерази 1 Обидва ці повідомлення суперечать припущенню, що функціональна 20(3)-(а-пдроксильна група в камптотецині є важливою ознакою його біологічної активності топотекан формули 5 [J Med (1991)] -NM82.HC! Chem , 34, 98 представлені в останній час на ринку в якості протиракових лікарських засобів Ще одна сполука, а саме, 9-амшокамптотецин формули 6 [J Med Chem , 2 9 , 2358(1986)] проходить в цей час масштабні КЛІНІЧНІ випробування Різнобічні дослідження співвідношеня структури і активності (SAR) камптотецину формули З [М Е Wall et al , J Med Chem , 36, 2689 (1993)] показали, що група 20(3)-а-пдрокси-5лактону (Е-кільце) в камптотецині дуже важлива для його активності Проте, ВІДПОВІДНО ДО останніх На основі наведених в літературі результатів досліджень будови і активності, отриманих для аналогів камптотецину, визнається, що модифікація замісників в положеннні С-9 і С-7 камптотецину формули 3 відіграє важливу роль в підсиленні протиракової активності, що надає СТІЙКІСТЬ лактону Е-циклу [Г G Burke et al , J Med Chem , 37, 40 (1994)] Також з'ясувалося, що розкрита форма групи лактону, а саме, "карбоксплатна форма", є терапевтично менш ефективною, ніж замкнута "лактонова форма" [Hertzberg et al , J Med Chem , 32, 715 (1989), J M Covey, С Jaxel et al , Cancer Research , 49, 5016 (1989), Giovanella et al , Cancer Research , 51 3052 (1991)] Останні дослідження T G Burke і IH , що стосується СТІЙКОСТІ "замкнуто лактонової форми" різних аналогів камптотецину в присутності білку, який називається "людський сироватковий альбумін" (HSA), показали, що такі сполуки, як СРТ-11 формули 4 і 7-етил-10пдроксикамптотецин (SN-38) формули 7а 7а і топотекан формули 5, в присутності HSA при 37°С виявляють в рівноважному стані більш висо 12 11 51666 кий процентний вміст (%) лактонової форми, ніж Автори ідентифікували реакцію окислення в спиртових розчинниках для цієї мети Одержані в ре20(Э)-камптотецин формули 3 і 9зультаті дані завершилися відкриттям нової синтеамінокамптотецин формули 6 [ТО Burke and тичної зміни, яку можна здійснити в різних Zihou Mi, J Med Chem, 37, 40 (1994), те ж алкоксильних групах в С-5-положенні 20(S)Biochemistry, 33, 12540 (1994)] На основі цих докамптотецинів Зміна функціональної групи таких сліджень з'ясувалося, що уявлення про фактори, 5-алкоксикамптотецинів дає широкий ряд нових які впливають на рівновагу лактон-карбоксилат, аналогів С-5-заміщених 20(S) камптотецинів форстає важливим вирішальним моментом при ствомули 14 ренні нових і терапевтично ефективних передбачуваних лікарських засобів групи камптотецину Хоча для швидкості одержання нових аналогів СРТ здійснувалась модифікація кілець А і В камптотецину, одержання аналогів камптотецину з модифікацією кільця "С" обмежувалося, можливо, через дослідження, що виконані Sawada і ш , які заявили, що введення замісників в положення С-5 камптотецину приводить, в результаті, до зниження протипухлинної активності камптотецинів і до утворення неактивних аналогів [Sawada S et aL, Chem Pharm Bull , 39(10), 2574 (1991)] Заявлені Sawada і ін С-5-заміщені камптотецини (патент Японії 58154584, патенти США 4513138, 4473692, 4545880, 433_9282) мають структурну формулу 10 R 10 де R представляє гідроксильну, нижчу алкільну, нижчу алкоксильну, ацилоксильну групи, R1 представляє водень, метокси в положенні 9, водень, гідрокси, нижчий алкокси, ацилокси, SH, тюалкіл, тюацил, нітрогрупу, аміногрупу, алкіламшогрупу, ациламшогрупу і галоген в положенні 10, і R2 представляє водень, нижчий алкіл, нижчий аралкіл, СН2ОН, СООН, COOMe, CH2OR', де R1 представляє нижчу алкільну або ацильну групу Недавні дослідження К Н Lee і ш [Bio Org Med Chem Lett, 5(1), 77 (1995)], що включають одержання 5-пдроксиметилкамптотецину за допомогою взаємодії формальдегіду в N,Nдиметилформаміді і 4-піперидинопіперидині з 20(Э)-камптотецином, показали знижену протипухлинну активність цих сполук Також, Damshefsky і ш одержали деякі С-5-заміщені ПОХІДНІ 20(RS)камптотецину при повністю синтетичному ПІДХОДІ [патенти США 5391745 и 5446047] Проте, заявлено [Terasawa et al , Heterocycles 38, 81 (1994)], що одержане синтетичним шляхом 5-заміщене похідне камптотецину формули 11 має протипухлинну активність, що може бути порівняна з активністю 20(3)-камптотецину э т .0 12 11 Маючи на увазі всі ці фактори, автори зосередили свої дослідження на 20(3)-камптотецині з метою створення нових аналогів камптотецину, які можуть виявляти підвищену розчинність у воді і підвищену СТІЙКІСТЬ лактонової форми в розчині 14 в якій X представляє NH або NR і СН2 або CHR, a R6 має значення, вказані вище Таким чином, вказане відкриття привело до легкої і універсальної напівсинтетичної методологи, за допомогою якої фактично кожне похідне камптотецину, відоме з літератури, можна перетворити в різні 5-заміщені аналоги камптотецину Отже, даний винахід стосується нового способу одержання різних С-5-заміщених похідних 20(S)камптотецину, в формулі яких R6 має вказані вище значення Крім того, згідно з цим винаходом, в камптотецин загальної формули 2 вводиться другий хіральний центр в положенні С-5, без порушення існуючої 20-пдроксильноі групи - хірального центру C-20(S) Крім того, широке різноманіття замісників OR6 при С-5-вуглеці 20(S)камптотецинів формули 1 приводить до сполук з поліпшеною розчинністю в воді в інтервалі від 1мг до Юмг на мл Всі сполуки, які одержані згідно з цим винаходом, проявляють істотну протипухлинну активність in vitro проти широкого ряду клітинних ЛІНІЙ пухлин людини Докладний опис винаходу Цей винахід стосується, особливо, водорозчинних С-5-О-замдщених аналогів 20(S)камптотецину, що мають формулу 1 де R1, R2, R3, R4, R5 і R6 мають вказані раніше значення В цьому винаході терміни, що представляють замісники R1-R6, мають такі визначення Термін "нижчий алкіл" позначає одновалентний, розгалуджений або ЛІНІЙНИЙ, вуглеводневий ланцюг, що містить 1-8 атомів вуглецю Представниками таких алкільних груп є метил, етил, пропіл, ізопропіл, бутил, втор-бутил, трет-бутил, пентил, ізопентил, трет-пентил, гексил, ізогексил і октил Термін "нижчий алкеніл" позначає розгалужений або ЛІНІЙНИЙ вуглеводневий ланцюг з sp або sp2 вуглецевими центрами, що містить 1-8 атомів вуглецю Представниками таких алкенільних групп є ВІНІЛ, пропеніл, бутеніл, пентеніл, ізопропеніл ізобутеніл, пропарпніл, гексеніл і октеніл Термін "галоген" або "гало" представляє хлор, бром або фтор Термін "галогеналкіл" позначає алкільні групи, що заміщені гелогенами, переваж 14 13 51666 но, фтором, бромом або хлором Представниками но, піперазино, морфоліно, імідазоліно або тіазогалогеналкільних груп є хлоретил, бромпропіл, лідино фторетил, трифторетил, трихлоретил і трифторУ ВІДПОВІДНОСТІ до цього винаходу пропонуєтьбутил ся спосіб одержання сполук загальної формули 1 Термін "нижчий алкокси" позначає нижчі алкільні групи, визначення яких дано вище, які приєднані до решти молекули через кисневий зв'язок Представниками таких груп є метокси, етокси, ізопропокси, трет-бутокси, гексокси, гептокси і октокси Термін "нижчий алканоїл" позначає нижчі алкі1 z 3 де R , R , R , FT, незалежно, є однаковими або льні або алкенільні групи, визначення яких дано різними і представляють водень, гідрокси, арилоквище, які приєднані до решти молекули через карси, нижчий алкокси, нижчий алканоїл, нітро, ціано, бонільну групу Представниками цих груп є ацегалоген, карбокси, карбонілокси, аміно, заміщений тил, пропюніл, пропеноїл, кротаноїл, бутаноїл, аміно нижчий алкіл, заміщений нижчий алкіл, або пентаноїл і ізопентаноїл 2 R 1 R разом представляють -О-(СЬІ2)п-О-, де п = 1 Термін "аміноалкіл" представляє нижчі алкільабо 2, R5 представляє водень, нижчий алкіл, заміні групи, визначення яких дано вище, що заміщені щений нижчий алкіл, нижчий аралкіл, пдроксимеаміногрупами Представниками таких аміноалкільтил, карбоксиметил, амшометил, заміщений амініх груп є 2-амшопропіл, 4-амінобутил, 5нометил, де аміногрупа може бути моно- або амінопентил Аміногрупи також можуть бути монодизаміщеною, при цьому обидва замісники є незаабо дизаміщеними, і представниками таких замілежними або об'єднаними з утворенням циклічної щених аміногруп є диметиламшо, диетиламіно, системи в цілому з 5-6 атомів, яка містить атоми дибензиламшо, етилізопропіламшо, пірол ідино, вуглецю і, необов'язково, один або два гетероатопіперидино, морфоліно або піперазіно ми, що обрані з кисню, азоту або сірки, і R6 предТермін "гетероатом" відноситься до атому киставляє водень, феніл або бензил, де фенільна сню, азоту або сірки Термін "арил або гетероарил" група може бути незаміщеною або заміщеною мопредставляє групи ароматичного характеру з 5но-, ди- або три-замісниками, які можуть бути обабо 6-членними кільцями, які можна обирати серані з галогену, гідрокси, нижчого алкокси, ціано, ред фенілу, біфенілу, нафтилу, піридилу, хіноліну, карбоксилу, нітро, аміно або заміщеного аміно, ізохшоліну, індолу, піролу, фурану, бензофурану, нижчого алкілу, заміщеного нижчого алкілу, циклотюфену, піримідину, піперазину, тіазолідину або алкіл або циклоалкіл нижчого алкілу, де циклічне імідазолу кільце є 3-7-членною кільцевою системою, що місТермін "заміщена фенільна" група, який викотить тільки атоми вуглецю, нижчі алкільні групи, ристовується в цьому винаході, відноситься до заміщені гетероциклічними ядрами, в яких гетерогрупи з замісниками, які можуть бути обрані з таких циклічна система має, в цілому, 3-7 атомів, циклічзамісників, як гідроксил, нижчий алкіл, галогенална система містить атоми вуглецю і, принаймні, кіл, феніл, бензил, галоген, нижчий алкокси, тюалодин гетероатом, такий як атом кисню, азоту або кокси, бензилокси, карбоксил, ціано, нітро, амідо, сірки, нижчий алканоїл, бензоїл, в якому фенільна аміно і алкіламшо Прикладами таких груп є 4група може бути незаміщеною або заміщеною, пдроксифеніл, 3-метоксифеніл, 4-фторфеніл, 4нижчий алкеніл, нижчий алкіл, заміщений нижчий трифторметилфеніл, N.N-диметиламінофеніл і 4алкіл, заміщений нижчий алкеніл або заміщений карбометоксифеніл нижчий алканоїл, де замісниками можуть бути галоген, гідрокси, нижчий алкокси, арілокси, тю, тюТермін "заміщена алкільна" група, який викоалкіл, тюарил, арил або гетероарил, карбокси, ристовується в цьому винаході, відноситься до ціано, нітро, амідо або аміно, при цьому аміногругрупи з замісниками, які можуть бути обрані з таких па може бути незаміщеною або моно- або дизамізамісників, як гідроксил, алкіл, галогеналкіл, феніл, щеною, і обидва замісники є незалежними або бензил, галоген, алкокси, тюалкокси, бензилокси, об'єднані з утворенням 5- або 6-членноі циклічної карбоксил, карбонілокси, ціано, нітро, амідо, аміно кільцевої системи, що містить атоми вуглецю, і і алкіламшо Прикладами таких груп є фторетил, містить, необов'язково, один або два гетероатоми, хлорпропіл, пдроксиетил, метоксипропіл, N, Nякі обрані з кисню, азоту або сірки, причому загадиетиламшоетил, N-бензоіламінопропіл, трифтольна КІЛЬКІСТЬ атомів в ЦИКЛІЧНІЙ системі складає 5 ретоксиетил, феноксиетил, карбометоксиетил, (пабо 6, при умові, що (І) коли R1 представляє метофторбензоілокси) етил, амінопропіл і 2-тюетил ксигрупу, R6 не є воднем або нижчою алкільною Термін "заміщена аміногрупа", який викорисгрупою, (II) коли R2 являє собою гідрокси, нижчий товується в цьому винаході, відноситься до груп з алкокси, тюалкіл нітро, аміно, алкіламшо, ацилазамісниками, які можуть бути обрані з таких замісмшо і галоген, R не є воднем або нижчою алкільників, як гідроксил, алкіл, галогеналкіл, бензил, ною групою, (III) коли R5 представляє нижчий албензоїл, алкокси, карбоксил, амідо, аміно і алкілакіл, нижчий аралкіл, СН2ОН, СООН, СООМе або мшо Прикладами таких груп є г\І,г\І-діетиламшо-, CH2OR", де R" представляє нижчу алкільну або N-бензоіламшо-, N-метоксиамшо-, Nацильну групу, R6 не є воднем або нижчою алкількарбоетоксиамшо- і N-хлоретиламшогрупи Крім ною групою, (IV) коли R1 являє собою метоксигрутого, обидва замісники в аміногрупі можуть об'єдпу, R представляє гідрокси, нижчий алкокси, тюнуватися з утворенням 5- або 6-членноі циклічної алкіл, нітро, аміно, алкіламшо, ациламшо або системи, яку представляють піролідино, піпериди 16 15 51666 5 галоген, R представляє нижчий алкіл, нижчий де R представляє водень або нижчий алкіл, 1 2 аралкіл, СН2ОН, СООН, СООМе або CH2OR", де R представляє водень або метокси, R представR" представляє нижчу алкільну або ацильну групу, ляє водень, гідрокси, нижчий алкокси, ацилокси, 6 R не є воднем або нижчою алкільною групою, (V) тюалкіл, SH, тюацил, нітро аміно, алкіламіно, 1 6 3 коли R -R представляють атом водню, R не є ациламшо і галоген, R і R представляють во5 воднем або нижчою алкільною групою, який вклюдень, і R представляє водень, нижчий алкіл, нижчає (І) взаємодію сполук формули 2 чий аралкіл, СН2ОН, СООН, СООМе або CH2OR', де R, представляє нижчу алкільную або ацильну зі й5 групу, що включає (І) взаємодію сполук формули 2 1 5 де замісники R -R мають вказані вище значення, в присутності кислоти і окислювача, який являє собою сіль заліза (3), з сполукою, що має формулу R6-OH, де R6 представляє нижчий алкіл, нижчий алкеніл, (Сз-С7)-циклоалкіл, галогеналкіл або пдроксиалкіл, з одержанням сполук формули 12 і сполук формули 13 12 де замісники R1-R5 мають вказані вище значення, в присутності кислоти і окислювача, такого як сіль заліза (3), із сполукою, що має формулу R6-OH, де R6 представляє нижчі алкільні групи, з одержанням сполук формули 12 і сполук формули 13 QR6 12 13 13 де R1, R2, R3, R4, R5 мають вказані вище значення, (II) поділ сполук формул 12 і 13, отриманих на стадії (І), звичайними способами (III) гідроліз сполук формули 12 звичайними способами з одержанням додаткової КІЛЬКОСТІ сполук формули 13, (IV) взаємодія сполуки формули 13 в присутності кислоти із сполукою, що має формулу R6ОН, з одержанням сполук формули 1 де R1, R2, R3, R4 і R5 мають вказані вище значення, і R6 має вказані вище значення ВІДПОВІДНО ДО ІНШОЇ своєї особливості, цей ви нахід стосується альтернативного способу одержання відомих С-5-заміщених сполук формули 1 де R1, R2, R3, R4 і R5 мають вказані вище значення, (II) поділ сполук формул 12 і 13, отриманих на стадії (І), звичайними способами, (III) гідроліз сполук формули 12 звичайними способами з одержанням додаткової КІЛЬКОСТІ сполук формули 13, (IV) взаємодія сполуки формули 13 в присутності кислоти зі сполукою, що має формулу R6ОН, з одержанням сполук формули 1, де R представляє нижчі алкільні групи, R1 представляє водень або метокси, R2 представляє водень або гідрокси, нижчий алкокси, ацилокси, SH, тюалкіл, тюацил, нітро аміно, алкіламіно, ациламшо і галоген, R3 і R представляють водень, і R5 представляє водень, нижчий алкіл, нижчий аралкіл, СН2ОН, СООН, СООМе або CH2OR', де R' представляє нижчу алкільную або ацильну групу Методологія, розроблена і описана в цьому винаході, створює новий хіральний центр біля позиції С-5 у сполуках формули 2 без порушення ЦІЛІСНОСТІ лактонової групи 20(3)-а-пдрокси Екільця Розроблений спосіб становить легкий і універсальний напівсинтетичний спосіб одержання С5-заміщених, відомих і нових, похідних камптоте 18 17 51666 цину формули 1, виходячи зі сполук формули 2 лу суміші сполук формул 12 і 13, що одержана на Сполуки формули 1, отримані згідно із способом стадії (І), суміш піддають, переважно, або кристацього винаходу, представляють, таким чином, діалізації, або колонковій хроматографії з викорисстереомери, що містять знову утворений хіральтанням силікагелю Суміші розчинників, що застоний центр С-5 Справді, сполуки загальної формусовуються при вищезгаданих методах, можуть ли 1 виділяються у виді суміші 20(S), 5(R) і 20(S), містити сполучення органічних розчинників, таких 5(3)-діастереомерів Проте, завдяки застосуванню як хлороформ, етилацетат, метанол, етанол, диезвичайних аналітичних методів, два показаних тиловый ефір, ацетон і гексан діастереомери розділяють на їх окремі оптично Сполуки формули 13 також можна одержати чисті даності на стадії (III) способу цього винаходу за допомо1 2 3 гою обробки сполук формули 12 кислотами в споВзагалі, всі сполуки формули 1, де R , R , R , 4 5 лученні з водою при температурі в інтервалі 40 R і R мають вказані вище значення, можна син120°С Кислоти, що використані для цієї мети, мотезувати, виходячи зі сполук формули 2, згідно з жуть бути обрані з хлористоводневої кислоти, описаним вище способом, і можна проілюструвати бромистоводневої кислоти, сірчаної кислоти, пприкладами, що, описані в розділі "Приклади" 1 2 3 4 толуолсульфонової кислоти, оцтової кислоти і пеОдержання сполук формули 12, де R , R , R , R 6 рхлорної кислоти Розчинниками, що використоR і R мають вказані вище значення, із сполук вуються при цій реакції, можуть бути метанол, формули 2, як згадується на стадії (І), є новим пеетанол, бутанол, ізопропанол або 1,4-дюксан ретворенням, при якому досягається безпосереднє введення різних алкоксизамісників в положення На стадії (IV) способу цього винаходу сполуки С-5 формули 13 вводять у взаємодію зі сполуками формули R6-OH, де R6 має вказані вище значенЗаміщені в КІЛЬЦІ А або КІЛЬЦІ А/В ПОХІДНІ 20(S)2 3 ня, при наявності кислого середовища при темпекамптотецину загальної формули 2, де R , R , R , ратурі в інтервалі від 20 до 140°С, що дає сполуки R4 і R5 мають вказані вище значення, які викорисформули 1 Кислоти, що використовуються при товуються в якості вихідних речовин в цьому винавказаній реакції, можуть бути обрані з сірчаної ході, є широко відомими, і їх одержують ВІДПОВІДНО кислоти, хлористоводневої кислоти, оцтової кисдо відомого рівня техніки, що відображений в літелоти, п-толуолсульфонової кислоти, піридиній-пратурі Наприклад, 7-етилкамптотецин, 10-пдротолуол-сульфонової кислоти, камфорсульфонової ксикаптотецин, 9-нітрокамптотецин, 12-нітрокампкислоти, метансульфонової кислоти, перхлорної тотецин, 10-пдрокси-7-етилкаптотецин (SN-38), 9кислоти або кислот Л'юіса, таких як тетрахлорид амінокамптотецин, 9-метоксикаптотецин, 9-пдротитану, ефірат BF3 і хлорид цинку Розчинники, що ксикамптотецин, 9-метокси-7-етилкамптотецин, 9використовані при вказаній реакції, можуть бути пдрокси-7-етилкамптотецин, 10,11-метилендюксиобрані з гексану, бензолу, толуолу, ксилолу, хлокамптотецин, 10,11-етилендюксикамптотецин, 10роформу, тетрахлориду вуглецю, дихлоретану, пдрокси-9-(г\І,г\І-диметиламінометил)камптотецин дихлорметану і 1,4-дюксану одержують згідно із способами, що ВІДОМІ З літератури [Т R Govindachan et al , Ind J Chem , 10(B), Таким чином, цей винахід має особливе зна453 (1972), S Sawada et al , Chem Pharm Bull , чення для розробки С-5-заміщених похідних 20(S)39(10), 2574 (1991), там же, 39(12), 3183 (1991), камптотецину як нового класу С-циклічних модифіпатент США №4604463 і патент США №4545880, кованих аналогів каптотецину, що корисні в якості Jaffery L Wood et al , J Org Chem , 60, 5739 протипухлинних і/або противірусних засобів Цей (1995)], і використовують у якості вихідних речовин винахід також має особливе значення, тому що для одержання нових С-циклічних заміщених анарозроблений і описаний тут спосіб є універсальлогів 20(3)-камптотецину загальної формули 1, що ним і прийнятним для одержання в значному масописані в цьому винаході штабі такий похідних каптотецину загальної фор Наприклад, сполуки формули 12, де R1, R2, R3, R4, R5 і R6, незалежно, є однаковими або різними і мають вказані вище значення, можна одержати так, як описано на стадії (І), за допомогою взаємодії сполук формули 2 із сполуками, що мають формулу R6-OH, де R6 представляє водень, нижчий алкіл, нижчий алкеніл, галогеналкіл, пдроксиалкіл, (Сз-С7)-циклоалкіл, в присутності сильної кислоти і солі заліза (3) Кислоти, що використовують при цій взаємодії, можуть бути обрані з перхлорної кислоти, хлористоводневої кислоти, азотної кислоти, сірчаної кислоти або кислот Л'юіса, таких як трифторид бору, хлорид цинку, хлорид олову, тетрахлорид титану Сіль заліза (3), що використовується у вказаній вище реакції, може бути обрана з нітрату заліза (3), подвійної солі сульфату заліза (3) і сульфату амонію, хлориду заліза (3) Як правило, згадану вище взаємодію здійснюють при температурі в інтервалі 40 - 150°С, краще - 60 120°С На стадії (II) способу цього винаходу для поді мули 1 Методологія, розроблена й описана в цьому винаході, дозволить ПІДІЙТИ ДО різноманітних С-5заміщених С-циклічних аналогів з різними замісниками на кільцях А і В 20(3)-камптотецину Окремими кращими сполуками є сполуки, в яких R1 представляє нітро, аміно, аміноалкіл, гідрокси, метокси, R2 подано гідрокси, карбонілокси, галоген, R2 і R3, з'єднані разом, представляють метилендюкси або етилендюкси, R4 представляє водень або нітро, R5 подано етил, амінометил або заміщений амінометил, R6 представляє 2'-пдроксиетил, алкоксиетил, хлоретил, фторетил, трифторетил або аміноетил або амінопропіл, в яких аміногрупа може бути диметиламшо, диетиламіно, пірол ід ино, піперидино, морфоліно, піперазино, імідазоліно Характерними представниками сполук формули 1 є 1) 5-метокси-СРТ*, 2) 5-етокси-СРТ*, 3) 5-бутокси-СРТ*, 20 51666 випадку концентрації сполуки ЮОмкМ і флуоресценція у випадку концентрації сполуки 1мкМ) Розведений зразок (200мкл) вводять в колонку для ВЕРХ, попередньо врівноважену рухливою фазою Вимірюють площу під піком, що відповідає певним 8) 7-ЄТИЛ-5-ЄТОКСИ-СРТ*, формам лактону Площу піка в нульовий момент 9) 7-ЄТИЛ-5-ПДРОКСИ-СРТ*, часу приймають за 100% і обчисляють частку 10) 9-нітро-5-етокси-СРТ, площі піка лактону в різні моменти часу, щоб ви11) 9-нітро-5-пдрокси-СРТ, значити рівноважну СТІЙКІСТЬ лактону як придбану 12) 7-етил-5-хлоретокси-СРТ, при сталій частці лактону в два послідовних моме13)10-пдрокси-7-етил-5-етокси-СРТ*, нти часу (Biochemistry, 1994, 33 10325-10336, і J 14) 5-(2'-пдроксиетокси)-СРТ, Pharm Sci , 1995,84 518-519) 15) 7-етил-9-пдрокси-5-етокси-СРТ, 16) 10-пдрокси-5-(2'-пдроксиетокси)-СРТ, 3 Фармакокінетика при MTD 17) 7-етил-10-пдрокси-5-(2'-пдроксиетокси)Всі дослідження здійснюють на мишах Swiss СРТ, albino з масою в інтервалі 35 - 40г Тварин не годують протягом ночі перед введенням дози лікар18) 9-нітро-5-фторетокси-СРТ, ського засобу і дають корм через 3 години після 19) 9-нітро-5-трифторетокси-СРТ, введення дози Тваринам вводять дозу штрапери20) Ю-пдрокси-5-трифторетокси-СРТ, тонеально у вигляді розчину в суміші ДМСО-вода 21) 7-етил-10-пдрокси-5-трифторетокси-СРТ, (50 50 о/о) Зразки крові відбирають у пробірки з 22) 7-етил-5-піролілиноетокси-СРТ, гепарином з очної западини через 1, 2, 4, 6 і 8 го23) 7-етил-5-диметиламшопропокси-СРТ, дин після введення дози і центрифугують при 24) 7-етил-10-пдрокси-5-фторетокси-СРТ, 13000об/хв протягом Юхв Відокремлюють зразки 25) 5-(2'-пдроксиетокси)-7-етил-СРТ, плазми і аналізують за допомогою ВЕРХ До 50мкл 26) 5-(2'-метоксиетокси)-СРТ, зразку додають 10Омкл охолодженого підкисленоде СРТ позначає 20(3)-камптотецин, а * відміго метанолу і перемішують для осадження білків чає сполуки, ВІДОМІ з літератури Зразок центрифугують при 13000об/хв протягом БІЛЬШІСТЬ сполук, отриманих згідно з цим виЮхв Доводять 10Омкл супернатанту до об'єму находом, мають розчинність у воді в інтервалі від 200мкл сумішшю метанол - вода (50 50, о/о) і 1мг до Юмг на 1мл при 37°С В таблиці 1А наво10Омкл вводять в пристрій ВЕРХ Для кількісної дяться дані по максимально переносимій дозі оцінки використовують площу піка лікарського за(MTD), що визначалася на мишах Swiss Albino, собу Зразки для калібрування, контролю і витягу СТІЙКОСТІ лактону в суцільній крові (через 3 години), готують за допомогою внесення 50мкл контрольної розчинності, фармакокінетиці MTD і активності m плазми з відомою КІЛЬКІСТЮ лікарського засобу і vitro після впливу протягом 1 години для сполук обробляють їх так само, як зразки (J Natl Cancer прикладів 11, 26 і 27 Inst, 1996, 88 817-824) Експерименти здійснюють ВІДПОВІДНО до приведених нижче протоколів 4 Розчинність ЗГІДНО З методом ВЕРХ Надлишок сполуки замочують у 0,5мл 0,1 М 1 Визначення MTD на мишах Swiss Albino Кожній МИШІ SWISS Albino ІН'ЄКЦІЮЮТЬ одноранатрій-ацетатного буферу при рН 5,0 протягом 24 зову дозу сполуки, що випробовується, в день, що годин при кімнатній температурі Розчин фільтрупозначається як день 1 Дози, що випробовують, ють через насадку для шприца з 0,45-мк ПОЛІВИНІстановлять 400, 200, 100, 50, 25, 12,5, 8,3, 6,25 і ліденфторидним (PVDF) фільтром (Gelman 3,13мг/кг маси тіла За тваринами спостерігають Sciences) Фільтрат вводять в пристрої для ВЕРХ в щодня на предмет смертності і захворюваності і різних об'ємах (10 і 20мкл) Реєструють хроматогреєструють масу тіла тварин, які виживають, в 1, рами Зареєстровані відгуки екстраполюють від 5, 10 і 14 день Максимальну переносиму дозу викалібровочної кривої і обчисляють розчинність значають як дозу, при якій сполука, що досліджусполуки (J Med Chem , 1995, 38 400) ється, не викликає будь-якої хворобливості і зни5 Розчинність згідно з традиційним методом ження маси тіла більш ніж на 30% в порівнянні з Сполуку суспендують в 5мл деіонізованої води днем 1 (ВІДПОВІДНО ДО протоколу, якого дотримуі гріють при 27°С протягом Юхв Потім розчин фіються в Національному інституті раку США ) льтрують і фільтрат упарюють до сухого стану з використанням метанолу, і зважують твердий за2 СТІЙКІСТЬ лактону в суцільній крові лишок У здорового добровольця беруть 2мл крові в пробірку, що містить 40мкл гепарину (572МЕ) для 6 Активність in vitro після впливу протягом 1 запобігання коагуляції, готують 4мМ і 40мкМ робогодини чі розчини лікарського засобу в ДМСО і додають Вирощують клітини в 15мл повного середовидо аліквот суцільної крові для одержання кінцевої ща (RPMI-1640 з 10% фетальної коров'ячої сироконцентрації ЮОмкМ і 1мкМ, ВІДПОВІДНО Лікарсьватки і 0,2% ІЧаНСОз) протягом 3 - 5 діб і одержукий засіб шкубують в суцільній крові при 37°С і ють клітини в КІЛЬКОСТІ 106клітин/матрац Середовідбирають 20-мкл зразки в 180мкл охолодженого вище видаляють, а зв'язані клітини промивають метанолу (-30°С) через різні проміжки часу (0, 1, 2 і забуференим фосфатом фізіологічним розчином З години) Струшують і перемішують, а потім (ЗФР) Додають 1мл 0,1% трипсин-ЕДТК і шкубуцентрифугують при 11000об/хв протягом 3 хвилин ють протягом 5 хвилин при 37°С Обережно витяна мікроцентрифузі при кімнатній температурі гають матраци і додають 5мл повного середовиРозводять 10Омкл супернатанту водою до 300 ща Витягають клітинну суспензію і центрифугують 500мкл, в залежності від сигнального відгуку (УФ у при 2000об/хв протягом 5хв Супернатант відки19 4) 5-хлоретокси-СРТ*, 5) Э-метокси-б-етокси-СРТ*, 6) 9-пдрокси-5-етокси-СРТ, 7) Ю-пдрокси-б-етокси-СРТ*, 22 21 51666 дають і клітинний осад суспендують в 5мл повного ляють супернатант Промивають клітини ДВІЧІ середовища Підраховують число клітин у гемоциЮОмкл ЗФР для видалення СЛІДІВ сполуки, що тометрі Розводять клітинну суспензію до 10000 випробовується Додають 200мкл повного середоклітин на 10Омкл у повному середовищі Висівають вища в кожну лунку і Інкубують протягом 48 годин ЮОмкл клітинної суспензії в кожну з 96 лунок титпри 37°С і 5% СОг Переривають ріст клітин за раційного мікропланшету і шкубують протягом 24 допомогою додавання 50мкл холодної 50% ТСА годин при 37°С і 5% СОг Припиняють процес у Інкубують планшет протягом 1 години при 4°С "порожнинці" для порівняння (засіяної окремо) Промивають планшети деіонізованою водою (п'ять 25мкл 50% холодної трихлороцтової кислоти разів) і сушать на повітрі Додають у кожну лунку (ТСА) Інкубують протягом 1 години при 4°С ЮОмкл розчину сульфородаміну В (0,4% у 1% оцПромивають планшет (п'ять разів) деюнізованої товій кислоті) Витримують при кімнатній темпераводою Планшет сушать на повітрі і зберігають при турі протягом 15 хвилин Промивають (п'ять разів) 4°С для визначення розміру То Здійснюють підхо1% оцтовою кислотою і сушать на повітрі Додають же разведення сполуки, що випробовується, в поЮОмкл ЮмМ основи Tnzma (Sigma), обережно вному середовищі і додають 10Омкл у кожну лунку, струшують на планшетному шейкері протягом 15 щоб підтримати кінцеву концентрацію в інтервалі хвилин, і зчитують оптичну густину при 490нм на 4 8 від 10 М до 10 М Інкубують протягом 1 години спектрофотометрі для зчитування планшетів (ВІДпри 37°С і 5% СОг Центрифугують титраційний ПОВІДНО до протоколу, якого дотримуються в Націмікропланшет при 1000об/хв протягом 5хв Видаональному інституті раку США) Таблиця 1А MTD, яка визначена на мишах Swiss Albino Спосіб введення штраперитонеальний Внутрішньовенний Приклад 11 400мг ЮОмг Приклад 26 200мг 25 -50мг Приклад 27 400мг 200мг СТІЙКІСТЬ лактону в суцільній крові (через 3 години) Концентрація ЮОмкМ 1мкМ Приклад 11 Діастереомер А Діастереомер В 3,73 ±1,50 6,15 ±2,53 Приклад 26 5,3 Приклад 27 Діастереомер А Діастереомер В 4,58 ±1,72 11,9 ±2,91 Розчинність Спосіб визначення Метод ВЕРХ Традиц Метод Приклад 11 0,17мг/мл Ю4М > Ю4М > 10 4 м 5x10DM > Ю4М > Ю4М 7,5х10°М Приклад 27 > Ю4М 7,5x10 D M 6x10DM 3,5хЮ'М 8x10DM 2x10DM 9x10DM пухлин людини, ВІДПОВІДНО до результатів, отриманими при аналізі 60 клітинних ЛІНІЙ пухлин людини, що виконані в Національному інституті раку 24 23 51666 (NCI), Bethesda, Мэриленд, США сліджують, оцінюють при п'яти - 10-кратному разведенні Найвища концентрація в ямці, що викориВ табл 1 наводиться активність стосовно клі4 стана при дослідах, становить 10 М Потім клітини тинних ЛІНІЙ in vitro, яка виражена у величинах інкубують в присутності лікарського засобу (сполуІС50, для різних С-циклічних аналогів 20(S)ка, яка досліджується) ще протягом 48 годин в камптотецину, що одержані згідно з цим винахоатмосфері з 5% СОг і 100% вологості По закіндом В картах 1 - 3 наводяться дані, які одержані ченні цього періоду клітини, що прилипли, фіксуна основі усереднених графіків NCI для повного ють на планшеті за допомогою трихлороцтової інгібування росту (TGI) різних типів людських ракислоти, і після декількох промивань клітинний кових клітинних ЛІНІЙ для сполук, що отримані у прошарок обробляють барвником для білків сульприкладах 27, 28 і 43 3 метою порівняння, вклюфородаміном В Потім, за допомогою автоматиччені також подібні дані для топотекану, які отриманого спектрофотометру для читання планшетів, ні на основі усередненого графіку NCI Дані, подані при довжині хвилі 515нм, зчитують оптичну густив таблицях 2 і 3, показують, що С-циклічні аналоги ну, що пропорційна масі білка Дані вносять у мік20(3)-камптотецину, які одержані згідно з цим вирокомпьютер і з використанням спеціально розронаходом, виявляють протипухлинну активність, бленої програми одержують остаточні результати рівну або переважаючу активність топотекану у відношенні деяких клітинних ЛІНІЙ різних панелей Сполуки формули 1 цього винаходу і їх фарракових клітин В табл 4 наводяться дані, що одемацевтично прийнятні солі, що описані вище, і ржані для сполуки, яка отримана в прикладі 32, композиції, що їх містять, є корисними як протирастосовно клітинних ЛІНІЙ лімфоми, яка зв'язана зі кові і противірусні засоби Введення нових активСНІДом (ARL) Всі сполуки, які використані в проних сполук формули 1, у чистій формі або у формі грамі протиракового скринінгу in vitro NCI, є суміпідхожої фармацевтичної композиції, можна здійсшами, що містять як діастереомери з 20(S), 5(S), нити за допомогою будь-якого способу введення, так і конфігурації 20(S), 5(R) у різних співвідноприйнятого для доставки подібних засобів Так, шеннях наприклад, активні засоби можна вводити перораРезультати, подані в картах 1 - 3 і таблицях 1 4, одержують при проведенні експериментів ВІДПОВІДНО до протоколів Національного інституту раку (NCI), що наведені нижче Кожна випробовувана сполука скринінгує по відношенню до групи з 60 людських клітинних ЛІНІЙ, що отримані з восьми органів При типовій процедурі, КЛІТИННІ суспензії, що розводять ВІДПОВІДНО до конкретного типу клітин і очікуваної густини клітин-мішеней (5000 - 40000 клітин на ямку, базуючись на особливостях клітинного росту), вносять у 96-ямкові титраційні мікропланшети Інокуляти лишають перед інкубацією на 24 годин при 37°С для стабілізації У ямки титраційного мікропланшету в момент часу "нуль" додають ЮОмкл аліквоти розведених в два рази призначених для ДОСЛІДІВ концентрацій Звичайно сполуки, що до льно, назально, парентерально або місцево, у твердій, напівтвердій, формі люфілізованого порошку або рідкій лікарській формі, наприклад, у формі таблеток, супозиториїв, пілюль, капсул, порошків, розчинів, суспензій, емульсій, кремів, лосьйонів, аерозолів, мазів, ІН'ЄКЦІЙ або подібній формі, переважно - у виді підхожих стандартних лікарських форм, для спрощення введення точних доз Композиції будуть включати звичайний фармацевтичний носій, розріджувач або ексципієнт і активну нову сполуку формули 1, і, крім того, можуть включати будь-які лікарські засоби, фармацевтичні засоби, носи, ад'юванти і т п Цей винахід описується докладно за допомогою конкретних прикладів, наведених нижче, які наводяться тільки для ілюстрації і не повинні розглядатися як такі, що обмежують об'єм винаходу Таблиця 1 №п/п 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 Сполука 5-Метоксикамптотецин* 5-Етоксикамптотецин* 5-н-Бутоксикамптотецин* 5-(2'-Гідроксиетокси) камптотецин 5-(2'-Хлоретокси) камптотецин 7-Етил-5-етоксикамптотецин* 9-Метокси-7-етил-5-етоксикамптотецин 7-етил-5-хлоретоксикамптотецин 7-Етил-5-амшоетоксикамптотецин 7-Етил-5-піролідиноетоксикамптотецин 7-Етил-5-піперидиноетоксикамптотецин 7-Етил-5-^^диметиламшоетоксикамптотецин 7-Етил-5-^^диметиламшопропоксикамптотецин 9-Метокси-5-етоксикамптотецин 5-Трифторетоксикамптотецин 5-Амшоетоксикамптотецин 7-Етил-5-трифторетоксикамптотецин 7-Етіл-5-(2'-пдроксиетокси) камптотецин 5-Фторетоксикамптотецин 10-Гідрокси-З-Трифторетоксикамптотецин ІС50(мкм)с 8,5 9,54 6,16 1,51 4,57 1/41 2/13 2,75 18,6 18,6 >30 13,8 >30 2,45 1,82 30,0 7,41 4,78 1,58 0,38 25 26 51666 Продовження таблиці 1 №п/п Сполука ІС50(мкм) а 21 9-Нітро-5-трифторетоксикамптотецин 0,46 8,12 22 10-Гідрокси-3-(2'-пдроксиетокси) камптотецин 7,94 23 9-Нітро-5-(2'-пдроксиетокси) камптотецин 4,36 24 7-Етил-5-фторетоксикамптотецин 2,23 25 5-Метоксиетоксикамптотецин 2,04 26 9-Нітро-5-метоксиетоксикамптотецин >30 27 12-Нітро-5-етоксикамптотецин >30 28 12-Нітро-5-пдроксикамптотецин 6,76 29 9-Амшо-5-метоксикамптотецин 30 9-Гідрокси-5-етоксикамптотецин 6,68 ІС50 = середнє значення мінімальної концентрації лікарського засобу (мкМ), необхідної для одержання 50% шипбування росту клітин (G150) при аналізі NCI 60 клітинних ЛІНІЙ пухлин людини * Відзначає С-5-заміщені ПОХІДНІ камптотецину, які ВІДОМІ З літератури Таблиця 2 Клітинна панель Клітинна ЛІНІЯ Топотекан Приклад 25 Лейкоз MOLT 4 1,2 3,0 CNS SF295 2,18 2,15 U251 2,81 3,57 Молочна залоза MCF7 100 9,2 Товста кишка НТ29 > 100 7,90 Таблиця З Кпіт панель NSLC Рак товстої кишки Яєчники Нирков CNS Н Н НСС Кпіт ЛІНІЯ EKVX Н Т 2 9 НСТ 15 S K O V 3 OVCAR 8 UO31 S F 2 6 8 U251 460 322М 2998 Топотекан 100 1,2 16,9 15,8 > 100 44,6 5,12 18,19 2,51 56 2,81 Приклад 26 63 1,0 31,6 10,47 46 36,3 3,80 13,4 3,89 30,9 7,58 Всі наведені вище величини стосуються концентрації в мкМ (мікромолі) для повного інгібування росту •ста О *TGI позначають мінімальні концентрації засобу ( сполуки, що досліджується), необхідні для одержання повного інгібування росту клітин при аналізі NCI 60 клітинних ЛІНІЙ пухлин людини in vitro Таблиця 4* Активність сполуки прикладу 32 in vitro проти клітинних ЛІНІЙ лімфоми, що зв'язана зі СНІДом Назва клітин C C R F - СЕМ RL KD488 G150* 0,318 0,463 0,246 TGI** 1,83 3,94 2,28 AS 283 0,268 0,678 PA 682 0,456 7,23 SU-DHL-7 0,609 3,51 * G 1 5 r j позначає мінімальну концентрацію (мкМ) сполуки, що досліджується, яка необхідна для 50% інгібування росту клітин ** TGI позначає мінімальну концентрацію (мкМ) сполуки, що досліджується, яка необхідна для повного інгібування росту клітин КАРТА 1 Дані по протираковій активності in vitro сполуки прикладу 27 (Подані тут дані відносять до величин концентрації, у мкМ, для повного інгібування росту (TGI)) КЛІТИННІ ЛІНІЇ Приклад 27 Топотекан НІР 62 4,95 0,04 НІР 92 4,88 7,90 NSLC Н226 4,75 10,96 Н23 0,91 0,87 Н460 5,09 1,20 Н522 7,66 4,16 НСТ 15 20,0 44,6 НТ29 2,41 100 KM 12 10,6 6,45 Рак товстої кишки КЛІТИННІ ЛІНІЇ Приклад 27 Топотекан COLO 205 19,5 7,94 НСС 2998 7,67 15,8 НСТ 116 4,06 2,51 27 28 51666 Продовження карти 1 Рак молочної залози КЛІТИННІ ЛІНІЇ Приклад 27 Тонотекан MCF7/ADR 1,25 1,50 MDA-MB-435 9,62 2,5 MDA-N 11,0 не визн ВТ 549 11,4 > 100 T47D 0,81 1,8 КАРТА 2 Дані по протираковій активності in vitro сполуки приклада 28 (Подані тут дані відносять до величин концентрації, у мкМ, для повного інгібування росту (TGI)) NSLC НІР 92 8,44 7,90 КЛІТИННІ ЛІНІЇ Приклад 28 Топотекан Н226 4,3 10,96 Н23 0,76 0,87 Н322М 30,2 16,9 Н460 1,22 1,20 Н522 13,0 4,16 НСТ 15 >30 44,6 НТ29 7,94 100 KM 12 27,4 6,45 Рак товстої кишки КЛІТИННІ ЛІНІЇ Приклад 28 Топотекан COLO 205 9,48 7,94 НСС 2998 7,65 15,80 НСТ 116 8,01 2,51 Рак молочної залози КЛІТИННІ ЛІНІЇ Приклад 28 Тонотекан MCF7/ADR 1,21 1,5 MDA-MB-435 11,4 2,5 ВТ-549 32 > 100 MDA-N 13,4 не визн T47D 1,09 1,8 Рак нирок КЛІТИННІ ЛІНІЇ Приклад 28 Топотекан 786-0 0,85 0,12 А 498 1,76 1,69 ACHN 0,37 0,28 САКІ 0,75 0,51 RXF 393 15,9 1,41 SN12C 2,31 1,58 UO31 1,23 2,51 КАРТА З Дані по протираковій активності in vitro сполуки приклада 43 (Подані тут дані відносять до величин концентрації, у мкМ, для повного інгібування росту (TGI)) NSLC HOP 62 3,92 0,04 КЛІТИННІ ЛІНІЇ Приклад 4 3 Топотекан Н226 6,89 10,96 Н23 2,52 0,87 Н460 14,2 1,20 Рак товстої кишки КЛІТИННІ ЛІНІЇ Приклад 4 3 Топотекан COLO 205 37,3 7,94 НСС 2998 23,2 15,8 НСТ 116 23,6 2,51 НТ29 18,9 100 KM 12 41,9 6,45 Рак молочної залози ПРИКЛАДИ Приклад 1 MCF7/ADR/RES 9,30 "ел КЛІТИННІ ЛІНІЇ Приклад 4 3 Топотекан MCF7 17,8 100 Одержання 5-метоксикамптотецину (відома сполука) 30 29 51666 Стадія 1 До суміші 20(3)-камптотецину форти і етанолу видаляють у вакуумі, а залишок екстмули 3 (2г) і хлориду заліза (3) (2г), що розчинена рагують етилацетатом Органічний прошарок проу 80мл метанолу, додають по краплях Юмл сірчамивають водою, ропою і сушать над безв ної кислоти і нагрівають при 70°С протягом 24год сульфатом натрію Випарювання розчинника дає Надлишок кислоти і метанолу видаляють у вакуу1,6г коричнюватого порошку, що містить 5-етоксимі, а залишок екстрагують етилацетатом Органіч7-етилкамптотецин і 5-пдрокси-7-етилкамптотецин ний прошарок промивають водою, ропою і сушать у співвідношенні 10 1 над безв сульфатом натрію Випарювання розСтадія 2 Поділ суміші за допомогою колонкочинника дає 1,8г жовтуватого порошку, що містить вої хроматографії дає 1г 5-етокси-75-метоксикамптотецин і 5-пдроксикамптотецин у етилкамптотецину і ЮОмг 5-пдрокси-7співвідношенні 5 1 етилкамптотецину, т пл 150°С, [а]о при 27°С = + 10,526 (с 0,085, СНСІз), ІК 3419, 1751, 1662, 1613, Стадія 2 Поділ суміші за допомогою колонко1 1 1157, 1075, 1050, 764см , Н ЯМР (CDCI3, вої хроматографії на силікагелі з використанням у 200МГц) 5 8,20(д, J = 8Гц, 1Н) , 8,15 (д, J = 8Гц, якості елюенту суміші розчинників метанол - хло1Н), 7,81 (т, J = 6,8Гц, 1Н), 7,66 (т, 7,3Гц, 1Н), 7,54 роформ, дає 1,5г 5-метоксикамптотецину і ЗООмг (с, 0,5Н), 7,51 (с, 0,5Н), 7,01 (с, 0,5Н), 6,89 (с, 5-пдроксикамптотецину Результати аналізу 50,5Н), 5,72 (д, J = 16,5Гц, 0,5Н), 5,71 (д, J = 16,5Гц, метоксикамптотецину т пл 156°С, [а]о при 28°С = 0,5Н), 5,28 (д, J = 16,5Гц, 0,5Н), 5,26 (д, J = 16,5Гц, + 41,74 (с 0,103, СНСІз), ІК 3426, 1747, 1664, 1616, 0,5Н), 4,3 - 3,6 (м, ЗН), 3,5 - 3,1 (м, 2Н), 2,05 - 1,71 1228, 1155, 1046, 762 см \ 1Н ЯМР (CDCI3, (м, 2Н), 1,45 (т, J = 7,5Гц, ЗН), 1,06 (т, J = 7Гц, ЗН) 200МГц) 5 8,42 (с, 1Н), 8,26 (д, J = 8Гц, 1Н), 7,96 (д, J = 8Гц, 1Н), 7,88 (т, J = 6,8Гц, 1Н), 7,68 (т, J = Приклад 4 6,8Гц, 1Н), 7,58 (с, 0,5Н), 7,54 (с, 0,5Н), 6,95(с, Одержання 5-пдрокси-7-етилкамптотецину 0,5Н), 6,80 (с, 0,5Н), 5,74 (д, J = 16,5Гц, 0,5Н), (відома сполука) 5,72(д, J = 16,5Гц, 0,5Н), 5,25 (д, J = 16,5Гц, 1Н), Стадія 1 Одержання 5-етокси-7-етилкамптоте3,75 (с, 1Н), 3,70 (с, 1,5Н), 3,50 (с, 1,5Н), 2,01 - 1,82 цину (м, 2Н), 1,06 (т, J = 7Гц, ЗН), М -с (m/z) 379 5-Етокси-7-етилкамптотецин формули 1, де R1 (М+Н), 348, 319 2 = R = R3 = R4 = Н, і R5 = R6 = Et, одержують із 20(3)-камптотецину формули 2 так, як описано в Приклад 2 прикладі З Одержання 5-пдроксикамптотецину (відома сполука) Стадія 2 Додають 50мл 25% H2SO4 до 1,0г 5Стадія 1 Одержання 5-метоксикамптотецину етокси-7-етилкамптотецину формули 1, де R1 = R2 = R3 = R4 = Н, і R5 = R - Et, розчиненого в ЗОмл 5-Метоксикамптотецин формули 1, де R = R2 етанолі, і кип'ятять з оберненим холодильником = R3 = R4 = R5 = Н, R6 = Me, одержують із 20(S)протягом ЗОгод По закінченні нагрівання надликамптотецину формули 3 так, як описано в пришок води і етанолу видаляють у виді азеотропної кладі 1 суміші, а залишок екстрагують етилацетатом ОрСтадія 2 Розчиняють 1,5г 5-метоксикамптотеганічний прошарок промивають ропою і сушать цину формули 1, де R1 = R2 = R3 = R4 = R5 = Н, і R6 над безв сульфатом натрію Після випарювання = Me, у 50мл метанолу і обробляють 50мл 50% розчинника і очищення за допомогою колонкової НСІ Розчин кип'ятять з оберненим холодильником хроматографії на силікагелі одержують 700мг 5протягом ЗОгод По закінченні нагрівання надлипдрокси-7-етилкамптотецину, т пл 252°С, ІК шок води і метанолу видаляють у виді азеотропної 3349, 1752, 1656 1605, 1159, 1054, 766см 1 , частсуміші, а залишок екстрагують етилацетатом Оркові результати Н ЯМР (CDCI3 + АМСО - d6) 5 ганічний прошарок промивають ропою і сушать 7,19(ушир з, 1Н, D2O обмінюваний), 7,15 (с, 0,5Н), над безв сульфатом натрію Після випарювання 7,05 (с, 0,5Н), 5,75 (ушир, с, 1Н, D2O обмінюваний), розчинника і очищення за допомогою колонкової 5,65 (д, J = 16,5Гц, 1Н), 5,25 (д, J = 16,6Гц, 1Н), хроматографії на силікагелі з використанням су3,52 - 3,19 (м, 2Н), 1,45 (т, J = 7,5ш, ЗН), 1,02 (м, міші розчинників етилацетат - хлороформ одерЗН) жують 1,2г 5-пдроксикамптотецину, т пл 220°С, [
ДивитисяДодаткова інформація
Назва патенту англійськоюAnalogues of 20(s)-camptothecin, method of their preparation, pharmaceutical composition and method to treat cancer, leikocythemia or hiv related conditions
Назва патенту російськоюАналоги 20(s)-камптотецина, способ их получения, фармацевтическая композиция и способ лечения рака, лейкоза или состояний связанных с вич
МПК / Мітки
МПК: A61K 31/4745, C07D 491/22, A61K 31/47, C07D 209/56, C07D 221/18, C07D 215/00
Мітки: лейкозу, одержання, лікування, 20(s)-камптотецину, фармацевтична, раку, композиція, станів, віл, спосіб, пов'язаних, аналоги
Код посилання
<a href="https://ua.patents.su/24-51666-analogi-20s-kamptotecinu-sposib-kh-oderzhannya-farmacevtichna-kompoziciya-ta-sposib-likuvannya-raku-lejjkozu-abo-staniv-povyazanikh-z-vil.html" target="_blank" rel="follow" title="База патентів України">Аналоги 20(s)-камптотецину, спосіб їх одержання, фармацевтична композиція та спосіб лікування раку, лейкозу або станів пов’язаних з віл</a>
Попередній патент: Композиція для покриттів
Наступний патент: Рейкова шахтна транспортна система вижленкова
Випадковий патент: Спосіб приготування будівельної суміші