N-(гетероцикліл)бензол- або -піридинсульфонаміди як антитромботичні та антикоагуляційні засоби
Номер патенту: 71667
Опубліковано: 15.12.2004
Автори: Лассаль Жільбер, Альтанбюргер Жан-Мішель, Кремер Жерар, Матругі Мостафа
Формула / Реферат
1. Сполуки формули (І):
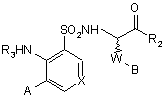 (І)
(І)
в яких:
Χ являє собою групу =CR4 або атом нітрогену,
W являє собою групи -(СН2)2-, -(СН2)3-, -СН2-СºС- (потрійний зв'язок) або -СН2-СН=СН- (подвійний зв'язок у цис- або транс-конфігурації),
R2 являє собою:
піперидил, який, як варіант, заміщений:
одною або двома групами, вибраними з гідроксилу, (С1-С4)алкілу, гідроксі(С1-С4)алкілу, (С1-С4)-алкоксі(С1-С4)алкілу, (С1-С4)алкоксилу, (С1-С4)алкілтіогрупи, монофлуорметилу, дифлуорметилу, трифлуорметилу та (С3-С6)циклоалкілу,
групою =CYZ [Y та Ζ вибрані, незалежно один від одного, з атомів гідрогену, атомів галогену та
(С1-С4)алкілів (як варіант заміщених 1-3 атомами галогену)],
групою:
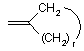
(r=1-3) або
спіро[(С3-С6)циклоалкановою] групою,
або 1,2,3,6-тетрагідропіридил, як варіант, заміщений (С1-С4)алкілом (цей (С1-С4)алкіл, як варіант, заміщений 1-3 атомами галогену) або (С3-С6)циклоалкілом,
або гексагідро-1Н-азепініл, як варіант, заміщений у позиції 4 трифлуорметилом або дифлуорметиленовою групою,
або гептагідроазоцин-1-іл,
або октагідро-1Н-азонін-1-іл,
або групу
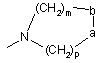
(а-b являє собою групу -CONR'-, m=1-2, p=1-2, a R' - атом гідрогену або (С1-С4)алкіл),
або групу
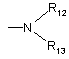 ,
,
в якій R12 являє собою (С1-С4)алкіл, карбоксі(С1-С4)алкіл або (С1-С4)алкоксикарбоніл(С1-С4)-алкіл, а R13 - (С1-С4)алкоксил або (С1-С4)алкіл, або R12 являє собою (С1-С4)алкіл або групу
-СН2СF3, а R13 являє собою групу
![]()
(Q - атом карбону або атом нітрогену, а r=1-3),
або піперазиніл, як варіант, заміщений (С1-С4)алкілом або (С1-С4)-алкілсульфонілом,
або морфолініл,
R4 являє собою
атом галогену
або атом гідрогену,
R3 являє собою
(С1-С5)алкіл
або групу -COR1, де R1 - атом гідрогену або (С1-С4)алкіл, -(СН2)nОСН3, -СН2O(С2Н4O)nСН3, -(СН2)nСF3 або -(СН2)nОН (n=1-4),
або групу -SO2R5,
або групу -CONHR5,
або групу -SO2N(R5)2, в якій R5 - (С1-С4)алкіл,
А являє собою
феніл, як варіант, заміщений 1-3 замісниками, вибраними з
атома галогену та
груп: (С1-С4)алкіл, (С1-С4)алкоксил, трифлуорметил, трифлуорметоксил, -CH2OR10, -CH2OCOR10, -CH2OCONR10R11, -COOR10, -CONR10R11, нітрогрупа, -NR10R11, -NHCOR10 та -NH(CH2)qOR10, де R10 та R11 являють собою, незалежно один від одного, атом гідрогену або (С1-С4)алкіл, а q=0-6,
або гетероцикліл, вибраний з піридилу, тієнілу, фурилу, піримідинілу та тіазолілу, де вказані групи можливо є заміщеними аналогічно вищезазначеному фенілу,
або (С5-С8)циклоалкіл,
а В являє собою
піридил, як варіант, заміщений 1 або 2 замісниками, вибраними з (С1-С4)алкілу, гідроксилу або
(С1-С4)алкоксилу,
або амінопіразиніл,
або амінопіридазиніл,
або піримідиніл, як варіант, заміщений аміногрупою,
або піперидил,
або амінопіридил, як варіант, заміщений на піридині (С1-С4)алкілом або (С1-С4)алкоксилом або атомом галогену, аміногрупа може також бути заміщеною (С1-С4)алкілом,
або амінофеніл, де аміногрупа може бути заміщеною (С1-С4)алкілом, а феніл може бути заміщеним (С1-С4)алкілом або атомом галогену,
у формі рацематів чи чистих енантіомерів або суміші енантіомерів, чи альтернативно у формі кислот або вільних основ чи адитивних солей фармацевтично прийнятних кислот.
2. Сполуки за п. 1, які відрізняються тим, що:
X, W, R4, А та В визначено за п. 1,
R2 являє собою
піперидил, який, як варіант, заміщений:
одною або двома групами, вибраними з гідроксилу, (С1-С4)алкілу, гідроксі(С1-С4)алкілу, (С1-С4)-алкоксі(С1-С4)алкілу, (С1-С4)алкоксилу, (С1-С4)алкілтіогрупи, монофлуорметилу, дифлуорметилу, трифлуорметилу та (С3-С6)циклоалкілу,
групою =CYZ [Y та Ζ вибрані, незалежно один від одного, з атомів гідрогену, атомів галогену та (С1-С4)алкілів (як варіант заміщених 1-3 атомами галогену)],
або 1,2,3,6-тетрагідропіридил, як варіант, заміщений (С1-С4)алкілом (цей (С1-С4)алкіл, як варіант, заміщений 1-3 атомами галогену), або (С3-С6)циклоалкіл,
або гексагідро-1H-азепініл, як варіант, заміщений у позиції 4 трифлуорметилом або дифлуорметиленовою групою,
або групу 
в якій
R12 - (С1-С4)алкіл, карбоксі(С1-С4)алкіл або (С1-С4)алкоксикарбоніл(С1-С4)алкіл, а R13 - (С1-С4)алкоксил або (С1-С4)алкіл,
або піперазиніл, як варіант, заміщений (С1-С4)алкілом або (С1-С4)алкілсульфоніл,
або морфолініл,
R3 являє собою
(С1-С5)алкіл,
або групу -COR1, в якій R1 - атом гідрогену або групи (С1-С4)алкіл, -(СН2)nОСН3,
-СН2O(С2Н4O)nСН3, -(СН2)nСF3 або -(СН2)nОН (n=1-4),
у формі рацематів чи чистих енантіомерів або суміші енантіомерів, чи альтернативно у формі кислот або вільних основ чи адитивних солей фармацевтично прийнятних кислот.
3. Сполуки за будь-яким з пп. 1 та 2, які відрізняються тим, що:
X, R4 та В визначено за п. 1,
W являє собою групи -(СН2)3- або -СH2-СН=СН- (подвійний зв'язок у цис- або транс-конфігурації),
R2 являє собою
піперидил, який, як варіант, заміщений:
одною або двома групами, вибраними з гідроксилу, (С1-С4)алкілу, гідроксі(С1-С4)-алкілу, (С1-С4)-алкоксі(С1-С4)алкілу, (С1-С4)алкоксилу, (С1-С4)алкілтіогрупи, монофлуорметилу, дифлуорметилу та трифлуорметилу,
групою =CYZ [Y та Ζ вибрані, незалежно один від одного, з атомів гідрогену, атомів галогену та (С1-С4)алкілів (як варіант заміщених 1-3 атомами галогену)],
або 1,2,3,6-тетрагідропіридил, як варіант, заміщений (С1-С4)алкілом (цей (С1-С4)алкіл, як варіант, заміщений 1-3 атомами галогену),
або гексагідро-1Н-азепініл,
або піперазиніл, як варіант, заміщений (С1-С4)алкілсульфонілом,
або морфолініл,
R3 являє собою групу -COR1, в якій R1 - групи (С1-С4)алкіл, -(СН2)nОСН3 або -(CH2)nCF3 (n=1-4), А являє собою
феніл, як варіант, заміщений 1-3 замісниками, вибраними з
атома галогену та
(С1-С4)алкілу та (С1-С4)алкоксилу,
або гетероцикліл, вибраний з піридилу та тієнілу,
або (С5-С8)циклоалкіл,
у формі рацематів чи чистих енантіомерів або суміші енантіомерів, чи альтернативно у формі кислот або вільних основ, чи адитивних солей фармацевтичнo прийнятних кислот.
4. Сполуки згідно за будь-яким з пп. 1-3, які відрізняються тим, що вибрані з групи, до складу якої входять:
N-[2-[[[(1S)-4-(5-аміно-3-метилпірид-2-ил)-1-[[4-(дифлуорметилен)піперид-1-ил]карбоніл]бутил]аміно]сульфоніл]-6-тієн-2-ілфеніл]пропанамід,
N-[2-[[[(1S)-4-(6-аміно-4-етилпірид-3-ил)-1-[[4-(дифлуорметилен)піперид-1-ил]карбоніл]бутил]аміно]сульфоніл]-6-циклопентилфеніл]ацетамід,
N-[3-[[[(1S)-4-(5-амінопірид-2-ил)-1-[[4-(дифлуорметилен)піперид-1-ил]карбоніл]бутил]аміно]сульфоніл]-3'-флуор[1,1'-дифеніл]-2-іл]пропанамід,
N-[3-[[[(1S)-4-(5-амінопіридин-2-ил)-1-[[4-(дифлуорметилен)піперид-1-ил]карбоніл]бутил] аміно]сульфоніл]-3'-флуор[1,1'-дифеніл]-2-іл]ацетамід,
N-[2-[[[(1S)-4-(5-амінопірид-2-ил)-1-[(4-етилпіперид-1-ил)карбоніл]бутил]аміно]сульфоніл]-6-тієн-2-ілфеніл]пропанамід,
N-[2-[[[(1S)-4-(6-амінопірид-3-ил)-1-піперид-1-ил-карбоніл)бутил]аміно]сульфоніл]-6-циклопентилфеніл]пропанамід,
Ν-[2-[[[(1S)-4-(5-амінопірид-2-ил)-1-[[4-(дифлуорметилен)піперид-1-ил]карбоніл]бутил]аміно]сульфоніл]-6-циклопентилфеніл]пропанамід,
N-[3-[[[(1S)-4-(5-aмiнoпipид-2-ил)-1-[[4-(дифлyopмeтилeн)пiпepид-1-ил]]карбоніл]бутил]аміно]сульфоніл][1,1'-дифеніл]-2-іл]ацетамід,
N-[2-[[[(1S)-4-(6-амінопірид-3-ил)-1-[[4-(дифлуорметилен)піперид-1-ил]карбоніл]бутил]аміно]сульфоніл]-6-тієн-2-ілфеніл]ацетамід,
Ν-[2-[[[(1S)-4-(6-аміно-4-метилпірид-3-ил)-1-[[4-(дифлуорметилен)піперид-1-ил]карбоніл]бутил]аміно]сульфоніл]-6-тієн-2-ілфеніл]пропанамід,
N-[2-[[[(1S)-4-(6-амінопірид-3-ил)-1-[[4-(дифлуорметилен)піперид-1-ил]карбоніл]бутил]-аміно]сульфоніл]-6-циклопентилфеніл]ацетамід,
N-[2-[[[(1S)-4-(амінопірид-3-ил)-1-[[4-(трифлуорметил)-1,2,3,6-тетрагідропірид-1-ил]карбоніл]бутил]аміно]сульфоніл]-6-тієн-2-ілфеніл]пропанамід,
N-[2-[[[(1S)-4-(6-амінопірид-3-ил)-1-[[4-(дифлуорметилен)піперид-1-ил]карбоніл]бутил]аміно]сульфоніл]-6-циклопентилфеніл]пропанамід,
N-[3-[[[(1S)-4-(5-aмiнoпipид-2-ил)-1-[[4-(дифлyopмeтилeн)пiпepид-1-ил]карбоніл]бутил]аміно]сульфоніл][1,1'-дифеніл]-2-іл]пропанамід,
Ν-[2-[[[(1S)-4-(6-аміно-4-метилпірид-3-ил)-1-[[4-дифлуорметилен)піперид-1-ил]карбоніл]бутил]аміно]сульфоніл]-6-циклопентилфеніл]пропанамід,
N-[3-[[[(1S)-4-(6-амінопірид-3-ил)-1-[[4-(дифлуорметилен)піперид-1-ил]карбоніл]бутил]аміно]сульфоніл]-3'-флуор[1,1'-дифеніл]-2-іл]пропанамід,
Ν-[2-[[[(1S)-4-(5-амінопірид-2-ил)-1-[(4-метилпіперид-1-ил)карбоніл]бутил]аміно]сульфоніл]-6-тієн-2-ілфеніл]ацетамід,
N-[2-[[[(1S)-4-(6-амінопірид-3-ил)-1-[(4-етилпіперид-1-ил)карбоніл]бутил]аміно]сульфоніл]-6-тієн-2-ілфеніл]пропанамід,
N-[2-[[[(1S)-4-(6-амінопірид-3-ил)-1-[(4-метилпіперид-1-ил)карбоніл]бутил]аміно]сульфоніл]-6-циклопентилфеніл]ацетамід,
N-[3-[[[(1S)-4-(5-амінопірид-2-ил)-1-[(4-метилпіперид-1-ил)карбоніл]бутил]аміно]сульфоніл]-3'-метил[1,1'-дифеніл]-2-іл]ацетамід,
Ν-[3-[[[(1S)-4-(6-аміно-4-метоксипірид-3-ил-1-[[4-(дифлуорметилен)піперид-1-ил]карбоніл]бутил]аміно]сульфоніл][1,1'-дифеніл]-2-іл]пропанамід,
N-[3-[[[(1S)-4-(5-амінопірид-2-ил)-1-[(4-метилпіперид-1-ил)карбоніл]бутил]аміно]сульфоніл]-3'-метил[1,1'-дифеніл]-2-іл]пропанамід,
N-[3-[[[(1S)-4-(5-амінопірид-2-ил)-1-[(4-метилпіперид-1-ил)карбоніл]бутил]аміно]сульфоніл]-3'-флуор[1,1'-дифеніл]-2-іл]ацетамід,
N-[3-[[[(1S)-4-(5-амінопірид-2-ил)-1-[(4-метилпіперид-1-ил)карбоніл]бутил]аміно]сульфоніл]-3'-метокси[1,1'-дифеніл]-2-іл]пропанамід,
N-[(1S)-4-(5-аміно-2-піридил)-1-[[4-(дифлуорметилен)-1-піперидил]карбоніл]бутил]-2-(форміламіно)-3'-метил[1,1'-дифеніл]-3-сульфонамід,
N-[3-[[[(1S,3Z)-4-(5-аміно-2-піридил)-1-[[4-(дифлуорметилен)-1-піперидил]карбоніл]-3-бутеніл]аміно]сульфоніл][1,1'-дифеніл]-2-іл]ацетамід,
-N-[3-[[[(1S,3Z)-4-(5-аміно-2-піридил)-1-[(4-метил-1-піперидил)карбоніл]-3-бутеніл]аміно]сульфоніл]-[1,1'-дифеніл]-2-іл]ацетамід,
у формі рацематів чи чистих енантіомерів або суміші енантіомерів, чи альтернативно у формі кислот або вільних основ чи адитивних солей фармацевтичнo прийнятних кислот.
5. Сполуки за будь-яким з пп. 1-4, які відрізняються тим, що кращою конфігурацією центральної амінокислотної частини
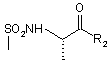
є (S).
6. Спосіб отримання сполук формули (І) за п. 1, в яких Χ являє собою групу =CR4, в якій R4 визначено за п. 1, який відрізняється тим, що сполуку формули (V)
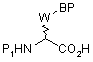 (V),
(V),
в якій Р1 - захисна група для аміно-функціональної групи, В та W визначено за п. 1, а Ρ - захисна група або атом гідрогену, піддають реакції, на етапі (і), зі сполукою формули (VI)
R2H (VI),
в якій R2 визначено за п. 1, з отриманням сполуки формули (IV)
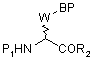 (IV),
(IV),
яку далі обробляють гідрогенхлоридом на етапі (іі), з отриманням сполуки формули (III)
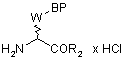 (III),
(III),
яку на етапі (ііі) конденсують зі сполукою формули (II)
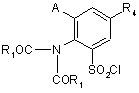 (II),
(II),
в якій R1, R4 та А визначено за п. 1, а потім, на етапі (iv), піддають гідрогенолізу, коли це потрібно, з отриманням сполуки формули (І), в якій R4 - атом гідрогену.
7. Спосіб отримання сполук формули (І) за п. 1, в яких Χ являє собою групу =CR4, в якій R4 визначено за п. 1, який відрізняється тим, що сполуку формули (III), яку отримано на етапі (іі) способу за п. 6 та, в якій Ρ являє собою атом гідрогену
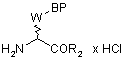 (III)
(III)
піддають реакції, на етапі (і), зі сполукою формули (ІІа)
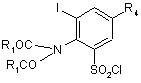 (ІІа),
(ІІа),
в якій R4 та R1 визначено за п. 1, з отриманням сполуки формули (Іа)
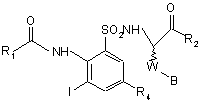 (Іа),
(Іа),
яку сполучають зі сполукою формули (VII)
A-Sn(R5)3 (VII),
в якій А визначено за п. 1, a R5 - (С1-С4)алкіл, а потім, на етапі (ііі), піддають гідрогенолізу, коли це потрібно, з отриманням сполуки формули (І), в якій R4 - атом гідрогену.
8. Спосіб отримання сполук формули (І) за п. 1, в яких Χ являє собою атом нітрогену, який відрізняється тим, що сполуку формули (III) піддають сполученню, як визначено за п. 6 або за п. 7, зі сполукою формули (XV)
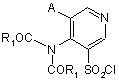 (XV).
(XV).
9. Сполуки формули (III)
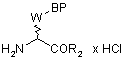 (III),
(III),
в яких В та R2 визначено за п. 1, а Р - захисна група для аміно-функціональної групи або атом гідрогену, які є корисними як інтермедіати у синтезі сполук формули (І) за п. 1.
10. Сполуки формули (ХV)
 (ХV),
(ХV),
в яких А та R1 визначено за п. 1, які є корисними як інтермедіати у синтезі сполук формули (І) за п. 1.
11. Медичний продукт, який відрізняється тим, що містить щонайменше одну сполуку за будь-яким з пп. 1-5.
12. Фармацевтична композиція, яка відрізняється тим, що містить щонайменше одну сполуку за будь-яким з пп. 1-5, а також щонайменше один фармацевтичнo прийнятний ексципієнт.
Текст
1. Сполуки формули (І): O 2 3 71667 4 атома галогену та або групу -COR1 , в якій R1 - атом гідрогену або груп: (С1-С4)алкіл, (С1-С4)алкоксил, трифлуормегрупи (С1-С4)алкіл, -(СН2)nОСН3, тил, трифлуорметоксил, -CH2OR10, -CH2OCOR10, -СН2O(С2Н4O)nСН3, -(СН2)nСF 3 або -(СН2)nОН (n=1CH2OCONR10R11, -COOR 10, -CONR10R 11, нітрогру4), па, -NR10R11, -NHCOR10 та -NH(CH2)q OR10, де R10 у формі рацематів чи чистих енантіомерів або сута R11 являють собою, незалежно один від одного, міші енантіомерів, чи альтернативно у формі кисатом гідрогену або (С1-С4)алкіл, а q=0-6, лот або вільних основ чи адитивних солей фармаабо гетероцикліл, вибраний з піридилу, тієнілу, цевтично прийнятних кислот. фурилу, піримідинілу та тіазолілу, де вказані групи 3. Сполуки за будь-яким з пп. 1 та 2, які відрізняможливо є заміщеними аналогічно вищезазначеються тим, що: ному фенілу, X, R4 та В визначено за п. 1, або (С5-С8)циклоалкіл, W являє собою групи -(СН2)3- або -СH2-СН= СНа В являє собою (подвійний зв'язок у цис- або транс-конфігурації), піридил, як варіант, заміщений 1 або 2 замісникаR2 являє собою ми, вибраними з (С1-С4)алкілу, гідроксилу або піперидил, який, як варіант, заміщений: (С1-С4)алкоксилу, одною або двома групами, вибраними з гідроксиабо амінопіразиніл, лу, (С1-С4)алкілу, гідроксі(С 1-С4)-алкілу, (С1-С4)або амінопіридазиніл, алкоксі(С 1-С4)алкілу, (С1-С4)алкоксилу, (С1або піримідиніл, як варіант, заміщений аміногруС4)алкілтіогрупи, монофлуорметилу, дифлуормепою, тилу та трифлуорметилу, або піперидил, групою =CYZ [Y та Ζ вибрані, незалежно один від або амінопіридил, як варіант, заміщений на піриодного, з атомів гідрогену, атомів галогену та (С1дині (С1-С4)алкілом або (С1-С4)алкоксилом або С4)алкілів (як варіант заміщених 1-3 атомами галоатомом галогену, аміногрупа може також бути загену)], міщеною (С1-С4)алкілом, або 1,2,3,6-тетрагідропіридил, як варіант, заміщеабо амінофеніл, де аміногрупа може бути заміщений (С1-С4)алкілом (цей (С1-С4)алкіл, як варіант, ною (С1-С4)алкілом, а феніл може бути заміщеним заміщений 1-3 атомами галогену), (С1-С4)алкілом або атомом галогену, або гексагідро-1Н-азепініл, у формі рацематів чи чистих енантіомерів або суабо піперазиніл, як варіант, заміщений (С1міші енантіомерів, чи альтернативно у формі кисС4)алкілсульфонілом, лот або вільних основ чи адитивних солей фармаабо морфолініл, цевтично прийнятних кислот. R3 являє собою групу -COR 1, в якій R1 - групи (С12. Сполуки за п. 1, які відрізняються тим, що: С4)алкіл, -(СН2)nОСН3 або -(CH2)nCF3 (n=1-4), А X, W, R 4, А та В визначено за п. 1, являє собою R2 являє собою феніл, як варіант, заміщений 1-3 замісниками, випіперидил, який, як варіант, заміщений: браними з одною або двома групами, вибраними з гідроксиатома галогену та лу, (С1-С4)алкілу, гідроксі(С 1-С4)алкілу, (С1-С4)(С1-С4)алкілу та (С1-С4)алкоксилу, алкоксі(С 1-С4)алкілу, (С1-С4)алкоксилу, (С1або гетероцикліл, вибраний з піридилу та тієнілу, С4)алкілтіогрупи, монофлуорметилу, дифлуормеабо (С5-С8)циклоалкіл, тилу, три флуорметилу та (С3-С6)циклоалкілу, у формі рацематів чи чистих енантіомерів або сугрупою =CYZ [Y та Ζ вибрані, незалежно один від міші енантіомерів, чи альтернативно у формі кисодного, з атомів гідрогену, атомів галогену та (С1лот або вільних основ, чи адитивних солей фарС4)алкілів (як варіант заміщених 1-3 атомами галомацевтичнo прийнятних кислот. гену)], 4. Сполуки згідно за будь-яким з пп. 1-3, які відріабо 1,2,3,6-тетрагідропіридил, як варіант, заміщезняються тим, що вибрані з групи, до складу якої ний (С1-С4)алкілом (цей (С1-С4)алкіл, як варіант, входять: заміщений 1-3 атомами галогену), або (С3N-[2-[[[(1S)-4-(5-аміно-3-метилпірид-2-ил)-1-[[4С6)циклоалкіл, (дифлуорметилен)піперид-1або гексагідро-1H-азепініл, як варіант, заміщений у ил]карбоніл]бутил]аміно]сульфоніл]-6-тієн-2позиції 4 трифлуорметилом або дифлуорметилеілфеніл]пропанамід, новою групою, N-[2-[[[(1S)-4-(6-аміно-4-етилпірид-3-ил)-1-[[4(дифлуорметилен)піперид-1R12 ил]карбоніл]бутил]аміно]сульфоніл]-6N циклопентилфеніл]ацетамід, R13 N-[3-[[[(1S)-4-(5-амінопірид-2-ил)-1-[[4або групу (дифлуорметилен)піперид-1в якій ил]карбоніл]бутил]аміно]сульфоніл]-3'-флуор[1,1'R12 - (С1-С4)алкіл, карбоксі(С 1-С4)алкіл або (С1дифеніл]-2-іл]пропанамід, С4)алкоксикарбоніл(С 1-С4)алкіл, а R13 - (С1N-[3-[[[(1S)-4-(5-амінопіридин-2-ил)-1-[[4С4)алкоксил або (С1-С4)алкіл, (дифлуорметилен)піперид-1-ил]карбоніл]бутил] або піперазиніл, як варіант, заміщений (С1аміно]сульфоніл]-3'-флуор[1,1'-дифеніл]-2С4)алкілом або (С1-С4)алкілсульфоніл, іл]ацетамід, або морфолініл, N-[2-[[[(1S)-4-(5-амінопірид-2-ил)-1-[(4-етилпіперидR3 являє собою 1-ил)карбоніл]бутил]аміно]сульфоніл]-6-тієн-2(С1-С5)алкіл, ілфеніл]пропанамід, 5 71667 6 N-[2-[[[(1S)-4-(6-амінопірид-3-ил)-1-піперид-1-илN-[3-[[[(1S)-4-(5-амінопірид-2-ил)-1-[(4карбоніл)бутил]аміно]сульфоніл]-6метилпіперид-1циклопентилфеніл]пропанамід, ил)карбоніл]бутил]аміно]сульфоніл]-3'-флуор[1,1'Ν-[2-[[[(1S)-4-(5-амінопірид-2-ил)-1-[[4дифеніл]-2-іл]ацетамід, (дифлуорметилен)піперид-1N-[3-[[[(1S)-4-(5-амінопірид-2-ил)-1-[(4ил]карбоніл]бутил]аміно]сульфоніл]-6метилпіперид-1циклопентилфеніл]пропанамід, ил)карбоніл]бутил]аміно]сульфоніл]-3'N-[3-[[[(1S)-4-(5-aмiнoпipид-2-ил)-1-[[4метокси[1,1'-дифеніл]-2-іл]пропанамід, (дифлyopмeтилeн)пiпepид-1N-[(1S)-4-(5-аміно-2-піридил)-1-[[4ил]]карбоніл]бутил]аміно]сульфоніл][1,1'-дифеніл](дифлуорметилен)-1-піперидил]карбоніл]бутил]-22-іл]ацетамід, (форміламіно)-3'-метил[1,1'-дифеніл]-3N-[2-[[[(1S)-4-(6-амінопірид-3-ил)-1-[[4сульфонамід, (дифлуорметилен)піперид-1N-[3-[[[(1S,3Z)-4-(5-аміно-2-піридил)-1-[[4ил]карбоніл]бутил]аміно]сульфоніл]-6-тієн-2(дифлуорметилен)-1-піперидил]карбоніл]-3ілфеніл]ацетамід, бутеніл]аміно]сульфоніл][1,1'-дифеніл]-2Ν-[2-[[[(1S)-4-(6-аміно-4-метилпірид-3-ил)-1-[[4іл]ацетамід, (дифлуорметилен)піперид-1-N-[3-[[[(1S,3Z)-4-(5-аміно-2-піридил)-1-[(4-метил-1ил]карбоніл]бутил]аміно]сульфоніл]-6-тієн-2піперидил)карбоніл]-3-бутеніл]аміно]сульфоніл]ілфеніл]пропанамід, [1,1'-дифеніл]-2-іл]ацетамід, N-[2-[[[(1S)-4-(6-амінопірид-3-ил)-1-[[4у формі рацематів чи чистих енантіомерів або су(дифлуорметилен)піперид-1-ил]карбоніл]бутил]міші енантіомерів, чи альтернативно у формі кисаміно]сульфоніл]-6-циклопентилфеніл]ацетамід, лот або вільних основ чи адитивних солей фармаN-[2-[[[(1S)-4-(амінопірид-3-ил)-1-[[4цевтичнo прийнятних кислот. (трифлуорметил)-1,2,3,6-тетрагідропірид-15. Сполуки за будь-яким з пп. 1-4, які відрізняил]карбоніл]бутил]аміно]сульфоніл]-6-тієн-2ються тим, що кращою конфігурацією центральної ілфеніл]пропанамід, амінокислотної частини N-[2-[[[(1S)-4-(6-амінопірид-3-ил)-1-[[4O (дифлуорметилен)піперид-1SO 2NH ил]карбоніл]бутил]аміно]сульфоніл]-6R2 циклопентилфеніл]пропанамід, N-[3-[[[(1S)-4-(5-aмiнoпipид-2-ил)-1-[[4є (S). (дифлyopмeтилeн)пiпepид-16. Спосіб отримання сполук формули (І) за п. 1, в ил]карбоніл]бутил]аміно]сульфоніл][1,1'-дифеніл]яких Χ являє собою груп у =CR4, в якій R4 визначе2-іл]пропанамід, но за п. 1, який відрізняється тим, що сполуку Ν-[2-[[[(1S)-4-(6-аміно-4-метилпірид-3-ил)-1-[[4формули (V) дифлуорметилен)піперид-1ил]карбоніл]бутил]аміно]сульфоніл]-6BP W циклопентилфеніл]пропанамід, N-[3-[[[(1S)-4-(6-амінопірид-3-ил)-1-[[4(дифлуорметилен)піперид-1P1HN CO 2H (V), ил]карбоніл]бутил]аміно]сульфоніл]-3'-флуор[1,1'в якій Р1 - захисна група для аміно-функціональної дифеніл]-2-іл]пропанамід, групи, В та W визначено за п. 1, а Ρ - захисна груΝ-[2-[[[(1S)-4-(5-амінопірид-2-ил)-1-[(4па або атом гідрогену, піддають реакції, на етапі метилпіперид-1(і), зі сполукою формули (VI) ил)карбоніл]бутил]аміно]сульфоніл]-6-тієн-2R2H (VI), ілфеніл]ацетамід, в якій R2 визначено за п. 1, з отриманням сполуки N-[2-[[[(1S)-4-(6-амінопірид-3-ил)-1-[(4-етилпіперидформули (IV) 1-ил)карбоніл]бутил]аміно]сульфоніл]-6-тієн-2BP ілфеніл]пропанамід, W N-[2-[[[(1S)-4-(6-амінопірид-3-ил)-1-[(4метилпіперид-1P1HN COR 2 ил)карбоніл]бутил]аміно]сульфоніл]-6(IV), циклопентилфеніл]ацетамід, яку далі обробляють гідрогенхлоридом на етапі (іі), N-[3-[[[(1S)-4-(5-амінопірид-2-ил)-1-[(4з отриманням сполуки формули (III) метилпіперид-1BP ил)карбоніл]бутил]аміно]сульфоніл]-3'-метил[1,1'W дифеніл]-2-іл]ацетамід, Ν-[3-[[[(1S)-4-(6-аміно-4-метоксипірид-3-ил-1-[[4H 2N COR 2 x HCl (дифлуорметилен)піперид-1(III), ил]карбоніл]бутил]аміно]сульфоніл][1,1'-дифеніл]яку на етапі (ііі) конденсують зі сполукою формули (II) 2-іл]пропанамід, N-[3-[[[(1S)-4-(5-амінопірид-2-ил)-1-[(4метилпіперид-1ил)карбоніл]бутил]аміно]сульфоніл]-3'-метил[1,1'дифеніл]-2-іл]пропанамід, 71667 8 потрібно, з отриманням сполуки формули (І), в якій R4 - атом гідрогену. 8. Спосіб отримання сполук формули (І) за п. 1, в яких Χ являє собою атом нітрогену, який відрізняR 1OC N ється тим, що сполуку формули (III) піддають споSO 2Cl лученню, як визначено за п. 6 або за п. 7, зі сполуCOR 1 (II), кою формули (XV) в якій R1, R4 та А визначено за п. 1, а потім, на A N етапі (iv), піддають гідрогенолізу, коли це потрібно, з отриманням сполуки формули (І), в якій R4 - атом R 1OC гідрогену. N 7. Спосіб отримання сполук формули (І) за п. 1, в COR 1 SO 2Cl яких Χ являє собою груп у =CR4, в якій R4 визначе(XV). но за п. 1, який відрізняється тим, що сполуку 9. Сполуки формули (III) формули (III), яку отримано на етапі (іі) способу за BP п. 6 та, в якій Ρ являє собою атом гідрогену W BP W H 2N COR 2 x HCl (III), в яких В та R2 визначено за п. 1, а Р - захисна груH 2N COR 2 x HCl (III) па для аміно-функціональної групи або атом гідропіддають реакції, на етапі (і), зі сполукою формули гену, які є корисними як інтермедіати у синтезі (ІІа) сполук формули (І) за п. 1. I R4 10. Сполуки формули (ХV) A N R 1OC N R 1OC R 1CO N SO2Cl (ІІа), COR 1 SO 2Cl в якій R4 та R1 визначено за п. 1, з отриманням (ХV), сполуки формули (Іа) в яких А та R1 визначено за п. 1, які є корисними як O інтермедіати у синтезі сполук формули (І) за п. 1. O 11. Медичний продукт, який відрізняється тим, SO 2NH що містить щонайменше одну сполуку забудьR2 R1 NH яким з пп. 1-5. 12. Фармацевтична композиція, яка відрізняється W тим, що містить щонайменше одну сполуку за B I R4 будь-яким з пп. 1-5, а також щонайменше один (Іа), фармацевтичнo прийнятний ексципієнт. яку сполучають зі сполукою формули (VII) A-Sn(R5)3 (VII), в якій А визначено за п. 1, a R5 - (С1-С4)алкіл, а потім, на етапі (ііі), піддають гідрогенолізу, коли це A 7 R4 Представлений винахід стосується похідних N(гетероцикпт)бензол- або -піридинсульфонамідів, їх отримання та їх терапевтичного застосування. Сполуки представленого винаходу відповідають формулі [1]: в якій: X представляє гр упу=CR4 - або атом нітрогену, W представляє групи -(СН2)2-, -(СН2)3-, -СН2СºС- (потрійний зв'язок) або -СН2-СН=СН - (подвійний зв'язок у цис- або транс-конфігурацїі), R2 представляє: піперидил, який, як варіант, заміщений: одною або двома групами, вибраними з гідроксилу, (С1-С4)алкілу, гирокси(С 1-С4)алкілу, (С1-С4)алкокси(С 1-С4)алкілу, .(С1-С4)алкоксилу, .(С1С4)алкілтіогрупи, монофлуорметилу, дифлуорметилу, три флуорметилу та (С3-С6)циклоалкілу, групою=CYZ [Y та Ζ вибрані, незалежно один від одного, з атомів гідрогену, атомів галогену та (С1-С4)алкілів (як варіант заміщених 1-3 атомами галогену)], групою: (r=1-3) або спіро [(С3-С6)циклоалкановою] групою, або 1,2,3,6-тетрагідропіридил, як варіант, за 9 71667 10 міщений (С1-С4)алкілом (цей (С1-С4)алкіл, як варі(С1-С4)алкоксилу, ант, заміщений 1-3 атомами галогену) або (С3або амінопіразиніл, С6)циклоалкілом, або амінопіридазиніл, або гексагідро-1Н-азепініл, як варіант, заміщеабо піримідиніл, як варіант, заміщений аміноний у позиції 4 трифлуорметилом або дифпуормегрупою, тиленовою групою, або піперидил або гептагідроазоцин-1-іл, або амінопіридил, як варіант, заміщений на піабо октагідро-1Н-азонін-1-іл, ридині (С1-С4)алкілом або (С1-С4)алкоксилом або або група атомом галогену, аміногрупа може також бути заміщеною (С1-С4)алкілом, або амінофеніл, де аміногрупа може бути заміщеною (С1-С4)алкілом 1 а феніл може бути заміщеним (С1-С4)апкілом або атомом галогену. У контексті винаходу, терміни нижнє мають наступні значення: (a-b представляє групу –CONR’-, m=1-2, p=1-2, (С1-С4)алкіл - лінійний чи розгалужений, насиа R’ – атом гідрогену або (С1-С4)алкіл), чений вуглеводневий ланцюг, що містить 1-4 атоабо група ми карбону, (Сx-Сy)циклоалкіл - циклічний вуглеводневий ланцюг, що містить від х до y а томів карбону, (С1-С4)алкоксил - оксигеновий радикал, замінений визначеним вище (С1-С4)алкілом, в якій R12 представляє (С1-С4)алкіл, карбокатом галогену - атом хлор у, брому, йоду або си(С1-С4)алкіл або (С1-С4)алксикарбоніл(С 1-С4)флуору. алкіл, a R13 представляє (С1-С4)алкоксил або (С1У контексті винаходу атомами галогену є пеС4)алкіл, або R12 представляє (С1-С4) алкіл або реважно хлор, флуор та бром. груп у -CH2CF3, a R 13 представляє груп у Залежно від природи групи W сполуки формули (І) згідно з винаходом можуть бути представленими нижченаведеними формулами (І1), (І2), (І3) та(І4): (q представляє атом карбону або атом нітрогену, а r=1-3), або піперазиніл, як варіант, заміщений С1С4)алкілом або (С1-С4)-алкілсульфонілом, або морфолініл, R4 представляє атом галогену, або атом гідрогену, R3 представляє (С1-С5)алкіл, або групу –COR1 де R1 представляє атом гідрогену або (С1-С4)алкіл, -(СН2)n-ОСН3, СН2O(С2H4O)nCH3, -(СН2)nСF 3 або -(СН2)nОН (n=14), або групу -SO2R5 , або групу -CONHR5, або групу -SO2N(R5) 2, в якій R5 - (С1-С4)алкіл, А представляє феніл, як варіант, заміщений 1-3 замісниками, вибраними з атому галогену та груп (С1-С4)алкіл, (С1-С4)алкоксил, трифлуорметил, трифлуорметоксил, -CH2OR10, CH2OCOR10, CH2OCONR10R11, -COOR 10 , CONR10R11, нiтрогрупа, -NR10R11, -NHCOR10 та – NH(CH2)q OR10, де R10 та R11 представляють, незалежно один вiд одного, атом гідрогену або (С1-С4) алкіл, a q=0-6, або гетероцикліл, вибраний з піридилу, тієнілу, фурилу, піримідинілу та тіазолілу, де вказані групи можливо заміщені аналогічно вище зазначеному фенілу, або (С5-С8)циклоалкіл, а В представляє піридил, як варіант, заміщений 1 або 2 замісниками, вибраними з (С1-С4)алкілу, гідроксилу та Сполуками, що є кращими згідно з винаходом, є сполуки формули [І], в яких: 11 71667 12 X, W, R 4, Ата В визначено вище, вибраними з атому галогену та (С1-С4)алкілу та R2 представляє (С1-С4)алкоксилу, піперидил, який, як варіант, заміщений: або гетероцикліл, вибраний з піридилу та тієодною або двома групами, вибраними з гідронілу, ксилу, (С1-С4)алкілу, гідрокси(С 1-С4)алкілу, (С1-С4)або (С5-С8)циклоалкіл. алкокси(С 1-С4)алкілу, (С1-С4)алкоксилу, (С1Кращою конфігурацією центральної амінокисС4)алкілтіогрупи, монофлуорметилу, дифлуормелотної частини сполук згідно з представленим витилу, три флуорметилу та (С3-С6)циклоалкілу, находом: групою =CYZ [Y та Ζ вибрані, незалежно один від одного, з атомів гідрогену, атомів галогену та (С1-С4)алкілів (як варіант заміщених 1-3 атомами галогену)], або 1,2,3,6-тетрагідропіридил, як варіант, заміщений (С1-С4)алкілом (цей (С1-С4)алкіл, як варіє [S]. ант, заміщений 1-3 атомами галогену),або(С3Сполуки формули [І] згідно з винаходом моС6)циклоалкіл, жуть існувати у формі рацематів або чистих енанабо гексагідро-1Н-азепініл, як варіант, заміщетіомерів або суміші енантіомерів. Вони можуть ний у позиції 4 трифлуорметилом або дифлуорметакож існувати у формі вільних кислот або основ, тиленовою групою, або адитивних солей з фармацевтично прийнятабо група ними кислотами, наприклад, у формі гідрохлориду або метансульфонату. Можна згадати зокрема наступні сполуки, у формі рацематів або чистих енантіомерів або суміші енантіомерів, або альтернативно у формі вільних кислот або основ, гідрохлориду або будьв якій якої іншої фармацевтично прийнятної солі, які R12 - (С1-С4)алкіл, карбокси(С 1-С4)алкіл або представляють частину винаходу: (С1-С4)алкоксикарбоніл(С 1-С4)алкіл, a R13 - (С1Ν-[2-[[[(1S)-4-(5-аміно-3-метилпірид-2-ил)-1-[[4С4)алкоксил або (С1-С4)алкіл, (дифлуорметилен)піперид-1або піперазиніл, як варіант, заміщений (С1ил]карбоніл]бутил]аміно]сульфоніл]-6-тієн-2С4)алкілом або (С1-С4)алкілсульфоніл, ілфеніл]пропанамід, або морфолініл, Ν-[2-[[[(1S)-4-(6-аміно-4-етилпірид-3-ил)-1-[[4R3 представляє (дифлуорметилен)піперид-1(С1-С5)алкіл, ил]карбоніл]бутил]аміно]сульфоніл]-6або група –COR1 в якій R1 - атом гідрогену або циклопентилфеніл]ацетамід, групи (С1-С4)алкіл, -(СН2)nОСН3, Ν-[3-[[[(1S)-4-(5-амінопірид-2-ил)-1-[[4СH2O(С2H4О)nОСНз, -(CH2)nCF 3 або -(СН2)nОН (дифлуорметилен)піперид-1(n=1-4). ил]карбоніл]бутил]аміно]сульфоніл]-3’-флуор[1,1'Серед кращих визначених вище сполук, сподифеніл]-2-іл]-пропанамід, луками, що є особливо кращими, є сполуки форΝ-[3-[[[(1S)-4-(5-амінопірид-2-ил)-1-[[4мули [І], в яких: (дифлуорметилен)піперид-1X, R4 та В визначено вище, ил]карбоніл]бутил]аміно]сульфоніл]-3’-флуор[1,1'W представляє групи -(СН2)3- або -СН2дифеніл]-2-іл]-ацетамід, СН=СН - (подвійний зв'язок у цис- або трансΝ-[2-[[[(1S)-4-(5-амінопірид-2-ил)-1-[(4конфігурації), етилпіперид-1-ил]карбоніл]бутил]аміно]сульфоніл]R2 представляє 6-тієн-2-ілфеніл]пропанамід, піперидил, який, як варіант, заміщений: Ν-[2-[[[(1S)-4-(6-амінопірид-3-ил)-1-піперид-1одною або двома групами, вибраними з гідроил-карбоніл)бутил]аміно]сульфоніл]-6ксилу, (С1-С4)алкілу, гідрокси(С 1-С4)-алкілу, (С1циклопентилфеніл]пропанамід, С4)-алкокси(С 1-С4)алкілу, (С1-С4)алкоксилу, (С1Ν-[2-[[[(1S)-4-(5-амінопірид-2-ил)-1-[[4С4)алкілтіогрупи, монофлуорметилу, дифлуорме(дифлуорметилен)піперид-1тилу та трифлуорметилу, ил]карбоніл]бутил]аміно]сульфоніл]-6групою=CYZ [Y та Ζ вибрані, незалежно один циклопентилфеніл]пропанамід, від одного, з атомів гідрогену, атомів галогену та Ν-[3-[[[(1S)-4-(5-амінопірид-2-ил)-1-[[4(С1-С4)алкілів (як варіант заміщених 1-3 атомами (дифлуорметилен)піперид-1галогену)], ил]карбоніл]бутил]аміно]сульфоніл][1,1'-дифеніл]або 1,2,3,6-тетрагідропіридил, як варіант, за2-іл]-ацетамід, міщений (С1-С4)алкілом (цей (С1-С4)алкіл, як варіΝ-[2-[[[(1S)-4-(6-амінопірид-3-ил)-1-[[4ант, заміщений 1-3 атомами галогену), (дифлуорметилен)піперид-1або гексагідро-1Н-азепініл, ил]карбоніл]бутил]аміно]сульфоніл]-6-тієн-2-ілабо піперазиніл, як варіант, заміщений (С1феніл]ацетамід, С4)алкілсульфонілом, Ν-[2-[[[(1S)-4-(6-аміно-4-метилпірид-3-ил)-1-[[4або морфолініл, (дифлуорметилен)піперид-1-ил]карбоніл]бутил]R3 представляє групу –COR1, в якій R1 - групи аміно]сульфоніл]-6-тієн-2-ілфеніл]пропанамід, (С1-С4)алкіл, -(СН2)nОСН3 або -(СН2)nСF3 (n=1-4), Ν-[2-[[[(1S)-4-(6-амінопірид-3-ил)-1-[[4А представляє (дифлуорметилен)піперид-1феніл, як варіант, заміщений 1-3 замісниками, 13 71667 14 ил]карбоніл]бутил]аміно]сульфоніл]-6найменше одну сполуку формули (І), яку визначециклопентилфеніл]ацетамід, но вище, а також щонайменше один фармацевтиΝ-[2-[[[(1S)-4-(амінопірид-3-ил)-1-[[4чно прийнятний ексципієнт. (трифлуорметилен)-1,2,3,6-тетрагідропірид-1З огляду на схему 1 для отримання сполуки ил]карбоніл]бутил]аміно]сульфоніл]-6-тієн-2-ілформули [І] згідно з представленим винаходом, в феніл]пропанамід, якій X представляє гр упу=CR4-, сполука формули Ν-[2-[[[(1S)-4-(6-амінопірид-3-ил)-1-[[4[V], в якій Р1 - захисна група для аміно(дифлуорметилен)піперид-1функціональної групи, зокрема третил]карбоніл]бутил]аміно]сульфоніл]-6бутоксикарбоніл (Вос), В та W визначено вище, а циклопентилфеніл]пропанамід, Ρ - захисна група, як-то фенілметоксикарбоніл, Ν-[3-[[[(1S)-4-(5-амінопірид-2-ил)-1-[[4або атом гідрогену, реагує на етапі (і), зі сполукою (дифлуорметилен)піперид-1формули [VI], в якій R2 визначено вище. Сполуку ил]карбоніл]бутил]аміно]сульфоніл][1,1'-дифеніл]формули [IV], що так отримують, обробляють гід2-іл]пропанамід, рогенхлоридом на етапі (іі) для отримання сполуки Ν-[2-[[[(1S)-4-(6-аміно-4-метилпірид-3-ил)-1-[[4формули [III]. (дифлуорметилен)піперид-1-ил]карбоніл]бутил]аміно]сульфоніл]-6-циклопентилфеніл]пропанамід, Ν-[3-[[[(1S)-4-(6-амінопірид-3-ил)-1-[[4(дифлуорметилен)піперид-1ил]карбоніл]бутил]аміно]сульфоніл]-3’-флуор[1,1'дифеніл]-2-іл]-пропанамід, Ν-[2-[[[(1S)-4-(5-амінопірид-2-ил)-1[(4метилпіперид-1ил]карбоніл]бутил]аміно]сульфоніл]-6-тієн-2ілфеніл]ацетамід, Ν-[2-[[[(1S)-4-(6-амінопірид-3-ил)-1-[(4етилпіперид-1-ил]карбоніл]бутил]аміно]сульфоніл]-6-тієн-2-ілфеніл]пропанамід Ν-[2-[[[(1S)-4-(6-амінопірид-3-ил)-1-[(4метилпіперид-1-ил]карбоніл]бутил]аміно]сульфоніл]-6-циклопентилфеніл]ацетамід, Ν-[3-[[[(1S)-4-(5-амінопірид-2-ил)-1-[(4метилпіперид-1-ил]карбоніл]бутил]аміно]сульфоніл]-3’-метил[1,1'-дифеніл]-2-іл]-ацетамід, Ν-[3-[[[(1S)-4-(6-аміно-4-метоксипірид-3-ил-1[[4-(дифлуорметилен)піперид-1-ил]карбоніл]бутил]аміно]сульфоніл][1,1'-дифеніл]-2-іл]пропанамід, Ν-[3-[[[(1S)-4-(5-амінопірид-2-ил)-1-[(4метилпіперид-1-ил]карбоніл]бутил]аміно]сульфоніл]-3’-метил[1,1'-дифеніл]-2-іл]пропанамід, Ν-[3-[[[(1S)-4-(5-амінопірид-2-ил)-1-[(4На етапі (ііі), сполуку формули [III] сполучають, метилпіперид-1-ил]карбоніл]бутил]аміно]у присутк хлі триетиламіну зі сполукою формули сульфоніл]-3’-флуор[1,1'-дифеніл]-2-іл]-ацетамід, [II], в якій R1, R4 та А визначено вище, для отриΝ-[3-[[[(1S)-4-(5-амінопірид-2-ил)-1-[[4мання, після обробки аміаком, сполуки формули метилпіперид-1-ил]карбоніл]бутил]аміно][І]. Моди фікацію групи -NHCOR 1 у груп у –NHR3 яку сульфоніл]-3’-метокси[1,1'-дифеніл]-2-іл]визначено вище стосовно формули [І], проводять пропанамід, згідно зі способами органічної хімії, що відомі фаΝ-[(1S)-4-(5-аміно-2-піридил)-1-[[4хівцям. (дифлуорметилен)-1-піперидил]карбоніл]бутил]-2Коли це потрібно для отримання сполуки фоформіламіно)-3’-метил[1,1'-дифеніл]-3рмули [І], в якій R4 - атом пдрогену, на етапі (іν) сульфонамід, далі проводять гідрогеноліз сполуки [І] для отриΝ-[3-[[[(1S,3Z)-4-(5-аміно-2-піридил)-1-[[4мання сполуки формули [Іb]. (дифлуорметилен)-1-піперидил]карбоніл]-3Згідно з одним кращим втіленням процесу бутеніл]аміно]сульфоніл][1,1'-дифеніл]-2-іл]отримання сполуки формули (І) представленого ацетамід, винаходу, Ν-[3-[[[(1S,3Z)-4-(5-аміно-2-піридил)-1-[(4етап (і), згаданий вище, можна проводити у метил-1-піперидил]карбоніл]-3присутності Ν,Ν-діізопропілетиламіну (DIEA) у дибутеніл]аміно]сульфоніл][1,1'-дифеніл]-2-іл]хлорметані або у диметилформаміді додаванням, ацетамід, під азотом, гексафлуорфосфату О-(1Об'єктом винаходу є також медичний продукт, бензотриазоліл)-Ν,Ν,Ν',N'-тетраметилуронію який відрізняється тим, що містить щонайменше (HBTU), одну сполуку формули (І), яку визначено вище. етап (іі) можна проводити у дихлорметані у Об'єктом винаходу є також фармацевтична присутності газуватого гідрогенхлориду, композиція, яка відрізняється тим, що містить щоетап (ііі) можна проводити спершу у дихлорме 15 71667 16 тані та триетиламіні (TEA), а далі переносом медіат при отриманні сполуки формули (І), в якій отриманого продукту у тетрагідрофуран (ТГФ) та W=СН2-СН = СН -(подвійний зв'язок у цисдалі пропусканням а струменя аміаку, з наступною конфігурації), обробкою 0,1Н гідрогенхлоридом у ізопропанолі, сполуки формули [Vg], яка корисна як інтерабо гідрогенбромідом у оцтовій кислоті, медіат при отриманні сполуки формули (І), в якій етап (іν) можна проводити переносом сполуки W=-СН2-СНСН -( подвійний зв'язок у транс= формули [І] у 0,1Η розчин гідрогенхлориду та в конфігурації), ізопропанолі. сполуки формули [Vh], яка корисна як інтерЗгідно з одним варіантом процесу згідно з медіат при отриманні сполуки формули (І), вякій представленим винаходом, сполуки формули [І], в W=-(CH2)3-, яких X представляє гр упу =CR4-, також отримують сполуки формули [Vc], яка корисна як інтермезгідно зі схемою 2. З огляду на схему 2, ці сполуки діат при отриманні сполуки формули (І), в якій можна отримати реакцією, на етапі (і), сполуки W=СН2-С= С-, формули [ІІІ], яку отримано на етапі (іі) описаного сполуки формули [Vi], яка корисна як інтермевище процесу винаходу (Схема 1) [де Ρ=атом гід діат при отриманні сполуки формули (І), вякій W=рогену] зі сполукою формули [ІІа], в якій R4 - атом (CH2)2-. галогену, a R1 визначено вище. Сполуку формули [Іа], що так отримують, сполучають зі сполукою формули [VIІ], в якій А визначено вище, a R5 -(С1С4)алкіл, для отримання сполуки формули [І]. Коли це потрібно для отримання сполуки формули [І], в якій R4 - атом гідрогену, далі на етапі (ііі) проводять гідрогеноліз сполуки [І] для отримання сполуки формули [Іb]. Згідно з одним кращим втіленням цього варіанту процесу для отримання сполуки формули [І] представленого винаходу, в якій X представляє груп у =CR4-, етап (і), згаданий вище, можна проводити спершу у дихлорметан, у присутності три-етиламіну, а далі наступним піддаванням отриманого продукту струменю аміаку. чи [І], де CR4-=-H етап (іі) можна проводити у суміш йодиду купруму та трифеніларсину (Рh3Аs) у безводному диметилформаміді (ДМФ) з додаванням бісдибензиліденацетонпаладію(0) [Pd(dba)2], етап (ііі) можна проводити у присутності активного паладію на вугіллі (Pd-C) та форміату амонію у метанолі, етап (іν) можна проводити переносом сполуки формули [І] у а 0,1Η розчин гідрогенхлориду та в ізопропанолі. Сполуки формули [V] представленого винаходу, які представлено у схемі 1, отримують згідно зі схемами 3 та 4. Схеми 3 та 4 ілюструють отримання різних типів сполук формули [V], а саме: сполуки формули [Ve], яка корисна як інтер Для отримання сполуки формули [Vc], проводять наступні етапи, наприклад, (Схема 3): на етапі (і) та аналогічно синтезу, розкритому у патентній заявці WO97/40052, сполук формули 17 71667 18 [Va], в якій Р1 визначено вище, реагує зі сполукою залізом у суміші етанол/оцтова кислота, формули [Vb], в якій В1 - ароматична основа, що етап (іν), що дає сполуку [Ve], можна проводинесе захищену або незахищену первинну або втоти з гідроксидом літію у суміші метанол/вода, ринну аміно-функціональну групу, або попередник етап (ν) можна проводити зі сполукою [Va], що аміно-функціональної групи, як-то нітрогрупа, а X має на собі захисну гр уп у Р 1, як-то тритил, для представляє атом галогену, для отримання сполук поліпшення регіоселективності реакції гідростаніформули [Vc]. лування. Це проводять гідридом трибутилстануму Для перетворення сполуки формули [Vc] у у тетрагідрофурані у присутності тетрасполуку формули [V], яке можна використовувати кіс(трифенілфосфін)паладію(0). Сполучення з безпосередньо у представленому у процесі на електрофільним реагентом [Vb] проводять у безсхемі 1, проводять омилення есте-рної групи, а водному діоксані у присутності тетраколи В1 має на собі попередник амінокіс(трифенілфосфін)-паладію(0), функціональної групи, цей попередник перетвоколи група Р1 сполуки формули [Vf] -тритил, рюють на аміногрупу, як варіант, захищену гр упою етап (vi) складається з перетворення групи Р1 типу Р, способами органічної хімії, що відомі фахівцям. тритилу у трет-бутилоксикарбоніл у присутності Для отримання сполуки формули [Vh] прововодного розчину гідроксиду натрію, використовуюдять наступні етапи, наприклад, (Схема 3): чи біс(ди-трет-бутил)карбонат. У цій операції, мена етапі (іі) сполуку формули [Vc] піддають затиловий естер гідролізують до карбонової кислоти, гальному гідрогенуванню як потрійного зв'язку, так отже, одержавши сполук формули [Vg]. і нітрогенового гетероциклу, як варіант, а потім З огляду на схему 4, можна отримати інтермезвичайному ортогональному захисту неароматичдіат сполуки формули [Vi], отже це робить можлиного вторинного аміну, який може бути створювавим отримання сполуки формули [І], в якій W - груним групою Р, як-то фенілметоксикарбонілом, або па (СН2)2-, таким чином: селективному гідрогенуванню потрійного зв'язку, а на етапі (і), похідну від глутамової кислоти потім омиленню, для отримання сполуки формули сполуку формули [VII], в якій Р1 визначено вище, a [Vh]. Ph представляє феніл, піддають реакції ХансдейДля отримання сполуки формули [Ve], провокера для отримання сполуки формули [VIII], дять наступні етапи, наприклад, (Схема 3): на етапі (іі), сполуку формули [VIII] перетвона етапі (ііі), сполуку [Vc] прдають дії контрорюють у відповідне цинкорганічне похідне, як спольованого гідрогенування потрійного зв'язку, як лучають in situ, шляхом каталізу паладієм, у споваріант, а потім звичайному ортогональному захилуку формули [Vb], в якій В1 визначено вище, а X сту вторинного аміну на групі В групою Р, як-то представляє атом галогену, для отримання сполутрет-бутоксикарбоніл (Вос). На етапі (іν) проводять ки формули [ІХ], омилення естерної групи сполуки [Vd] для отрина етапі (ііі), сполук формули [IX] гідрогенують мання сполуки [Ve]. на паладієвому каталізаіторі для отримання споДля отримання сполуки формули [Vg], проволуки формули [VI], що має на собі вільну карбокдять наступні етапи, наприклад, (Схема 3): сильну функціональну гр упу. на етапі (ν) сполуку [Va] піддають спершу гідЗгідно з одним кращим втіленням цього проростанілуванню потрійного зв'язку, з наступним цесу отримання сполуки формули [VI] представкаталізованим сполученням за допомогою комплеленого винаходу, ксу паладію зі сполукою [Vb], в якій В1 - ароматичетап (і), згаданий вище, можна проводити у на основа, що має на собі захищену або незахитетрахлориді карбону в атмосфері аргону, у прищену первинну або вторинну аміно-функціональну сутності ді(ацетилокси)йодбензолу та молекуляргруп у, або попередник аміно-функціональної груного йоду. Цей етап тому проводять за допомогою пи, як-то нітро-група, а X представляє атом галоУФ-опромінювання, гену, для отримання сполуки формули [Vf], етап (іі), згаданий вище, можна проводити у на етапі (νі), естерну групу сполуки [Vf] гідролідиметилформаміді в атмосфері аргону у присутзують для отримання сполуки формули [Vg]. ності порошку цинку, активованого додаванням Згідно з одним кращим втіленням процесу для триметилсилілхлориду та 1,2-диброметану. Цинотримання сполуки формули [V] представленого корганічне похідне, так отримане, далі обробляють винаходу, який ілюстровано у схемі 3: електрофілом В1Х, наприклад, у присутності етап (і), згаданий вище, можна проводити у трис(дибензиліденацетон)-дипаладію та три-ортодиметилформаміді, у присутності каталізатору на толілфосфін у при кімнатній температурі, основі паладію, як-то комплекс дихлорбісетап (ііі), згаданий вище, можна проводити у (трифенілфосфін)паладій/йодид купруму, у основсуміші метанол/вода у присутності активного катаному середовищі, наприклад, з гідрокарбонатом лізатору з 10% паладієм на вугіллі та при тиску калію та у безводному диметилформаміді, водню 50фунт/кв.дюйм. етап (іі), згаданий вище, можна проводити з З огляду на схему 5, для отримання сполук воднем або форміатом амонію, у метанолі, у приформули [XV], які корисні як інтермедіати для сутності каталізатору на основі паладію, як-то акотримання сполук формули [І] згідно з винаходом, тивного паладію на вугіллі, та омиленням гідров яких X=N, проводять наступні етапи; ксидом літію у суміші метанол/вода, на етапі (і), 4-амінопіридинову сполуку формуетап (ііі), згаданий вище, можна проводити у ли [X], в якій аміно-функціональну групу захи щаприсутності паладію на сульфаті барію у етилацеють захисною групою Р1, яку визначено вище, петаті. Коли Ві має на собі нітро-функціональну груретворюють у похідне формули [XI], що має на пу, її бажано попередньо відновити, переважно собі два атоми брому, розташовані попередньо 19 71667 20 для уведення потрібних груп, мули [І] згідно з винаходом, в яких Χ=Ν, за наступна етапі (іі), сполуку формули [XI] сполучають ним протоколом, описаним наетапі (ііі) схеми 1, з похідним боронової кислоти формули АВ(ОН)2, в тобто сполученням сполуки формули [ХV], зі споякому А - фенільне ядро або гетероцикл, який, як лукою формули [ІІІ], яку визначено вище. варіант, заміщений, у присутності паладієвого каВихідні сполуки, як-то сполука формули [Vb] є талізатору, для отримання сполуки формули [XII], комерційно доступними або описані у літературі, або альтернативно їх можна отримати способами, які описані там, або, які відомі фахівцям. Приклади, які наведено нижче, ілюструють отримання деяких сполук згідно з винаходом. Мікро-аналізи та спектри ІЧ та ЯМР підтверджують структур у отриманих сполук. Номери ілюстрованих сполук стосуються номерів у наведених нижче таблицях, які ілюструють хімічні структури та фізичні властивості ряду сполук згідно з винаходом. Співвідношення (x:y) представляє співвідношення кислота: основа. Прикладі (сполука 3): Ν-[2-[[[(1S)-4-(5-аміно-3-метилпірид-2-ил)-1-[[4(дифлуорметилен)піперид-1ил]карбоніл]бутил]аміно]сульфоніл]-6-тієн-2-ілфеніл]пропанамід, 1.1. Ν-(5-бромпірид-2-ил)-2,2,2-трифлуорацетамід, 68,0мл (0,477моль) розчину трифлуороцтового ангідриду у 250мл дихлорметану додають при 0°С, під азотом, до розчину 75,0г (0,433моль) 5-бром-2піридинаміну та 41,25мл (0,519моль) піридину у 250мл дихлорметану. С уміші дають помірно нагріна етапі (ііі), атом сульфур у. який є поперетися до кімнатної температури та перемішування дником сульфонілхлоридної групи, уводять шляпродовжують протягом 18 годин. Реакційну суміш хом каталізованої паладієм реакції сполучення розбавляють 300мл дихлорметану та далі промисполуки формули [XIІ] та стануморганічного похідвають водою (2х400мл), а далі насиченим розчиного, отриманого попередньо з бензолметантіолу, ном хлориду натрію (2х200мл), після чого її сушать на етапі (iv), захисну груп у Р1 видаляють обсульфатом натрію та концентрують під зниженим робкою кислотою у звичайних умовах для отритиском. Отриманий залишок очищають хроматогмання сполуки формули [XIV], рафією на гель-колонці, елюючи під тиском суміна етапі (ν), сполуку формули [XIV] перетвошшю дихлорметан/гентан (1:1). 100г N-(5рюють у змішаний імід обробкою ангідридом та бромпірид-2-ил)-2,2,2-трифлуорацетаміду отрибензилтіолову гр упу далі безпосередньо окиснюмують у формі білого твердого продукту. Вихід (%) ють до хлорсульфонільного похідного формули =86; темп. п.л. (°С)=73. [XV] суль фурилхлоридом у присутності оцтової 1.2. Ме тилу (S)-.2-[[(1,1-диметилетокси)кислоти та води. карбоніл]аміно]-5-[6-[(трифлуорацетил)Згідно з одним кращим втіленням цього проаміно]пірид-3-ил]пент-4-иноат цесу отримання сполуки формули [XV]: 1,7г (2,4ммоль) дихлорбіс(трифенілетап (і), згаданий вище, можна проводити в фосфін)паладію додають при кімнатній темпераацетонітрилі з Ν-бромсукцинімідом, турі, в а тмосфері аргону, до суміші 13,0г етап (іі), згаданий вище, можна проводити у (48,3ммоль) N-(5-бром-2-піридил)-2,2,2суміші діоксан/вода у присутності карбонату натрифлуорацетаміду, 16,0г (70,5ммоль) метилу (S)трію та тетракіс(трифенілфосфін)паладію(0), 2-[[(1,1-диметилетокси)-карбоніл]аміно]пент-4етап (ііі), згаданий вище, можна проводити у иноату, 0,46г (2,4ммоль) йодиду купруму та 13,35г безводному діоксані у присутності тетра(96,6ммоль) карбонату калію у 25мл безводного кіс(трифенілфосфін)паладію(0) з трибудиметилформаміду (ДМФ). Суміш гріють протягом тил[(фенілметил)тіо]стананом, отриманим попе5 годин при 65°С. Суміш переносять у ефір редньо, (800мл) та далі промивають водою (2х600мл), а етап (іν), згаданий вище, можна проводити потім насиченим розчином хлориду натрію (300мл) звичайно у метанолі з пропусканням у суміш струта сушать суль фатом натрію. Отриманий продукт меня гідрогенхлориду, фільтрують та далі концентрують під зниженим етап (ν), згаданий вище, можна проводити натиском. Отриманий залишок очищають хроматоггріванням у чистому ангідриді, як-то пропіоновий рафією на колонці з силікагелем, елюючи під тисангідрид. Після випарювання надлишку реагенту, ком сумішшю етилацетат/циклогексан з градієнтом обробка сумішшю оцтової кислоти та води з сульвід 0 до 20% етилацетату. 10г метилу (S)-2-[[(1,1фурилхлоридом дає очікувану хпорсульфонільну диметилетокси)-карбоніл]аміно-5-[6сполуку формули [XV] безпосередньо. (трифлуорацетил)аміно]пірид-3-ил]пент-4-иноату Сполуку формули [XV], отриману так, можна отримують так у формі масла. Вихід (%)=52 далі використовувати для отримання сполук фор1.3. (S)-6-аміно-a-[[1,1-(диметилетокси) 21 71667 22 карбоніл]піридин-3-пентанова кислота (1:2) отримують у формі білого твердого продукту, Суміш 8,04г метилу (S)-2[[1,1-(диметилетокси)який використовують без подальшої очистки на карбоніл]аміно]-5-[6-(трифлуорацетил)аміно]піриднаступному етапі. 3-ил]пент-4-иноат (20ммоль) та активного 10% Вихід (%)=100; темп. п.л. (°С)=65. паладію на вугіллі (0,8г) у метанолі (80мл) та оц1.6. Гідрохлорид (S)-Ν-[[[4-(6-амінопірид-3-ил)тову кислоту (1,32мл; 22ммоль) перемішують про1-(4етилпіперид-3тягом 7 годин під тиском водню 50фунт/кв.дюйм ил)карбоніл]бутил]аміно]сульфоніл]-6-тієн-2при кімнатній температурі. Суміш - фільтрують та ілфеніл]- пропанаміду, далі концентрують під зниженим тиском. Отрима1,84мл (13,2ммоль) триєтиламіну (ТЕА) доданий залишок переносять у етилацетат (400мл) та ють, при 0°С, до розчину 1,5г гідрохлориду далі промивають насиченим розчином гідрокарбо(4ммоль) (S)-1-[2-аміно-5-(6-амінопірид-3-ил)-1нату натрію, (200мл) та насиченим розчин хлориду оксопентил]-4-етилпіперидин (1:2) у 20мл дихлорнатрію (200мл), фільтрують та сушать сульфатом метану, а потім порціями додають 1,54г (4ммоль) натрію і далі концентрують під зниженим тиском. 2-[біс(1оксопропіл)аміно]-3-тієн-2Моногідрат гідроксиду літію(1,1г, 26ммоль) додаілбензосульфонілхлоріду. Через 4 години при 0°С ють при 0°С до розчину отриманого так залишку у додають 200мл етилацетату та суміш далі промиметанолі (50мл) та воді (15мл). Суміші дають навають 100мл насиченого розчину гідрокарбонату грітися до кімнатної температури та перемішуваннатрію та 100мл насиченого розчину хлориду наня продовжують протягом 18 годин. Реакційну сутрію. Отриманий продукт сушать сульфатом наміш охолоджують до 0°С, нейтралізують 1Η трію та концентрують під зниженим тиском. Отрирозчином гідрохлоридної кислоти та далі концентманий так залишок переносять у 100мл тетрагідрофурану (ТГФ) та далі охолоджують до рують під зниженим тиском. 7г (S)-6-аміно-a-[[1,1(диметилетокси)-карбоніл]піридин-3-пентанової 0°С і обробляють протягом 5 хвилин стр уменем аміаку. Реакційній суміші дають нагрітися до кімкислоти (літію хлорид) отримують у формі густого натної температури та, через 4 години, далі конмасла, яку використовують без подальшої очистки центрують під зниженим тиском. Отриманий зана наступному етапі. лишок переносять у 50мл 0,1Η розчину Вихід (%) =88 1.4. 1,1-диметилетилу (S)-[4-(6-амінопірид-3гідрогенхлориду у ізопропанолі (5ммоль) та далі концентрують під зниженим тиском та очищають ил)-1-([4-етилпіперид-3-ил)карбоніл]бутил]хроматографією на колонці RP18, елюючи сумішкарбамат шю ацетонітрил/вода з градієнтом від 5/95 до 2,1г (5,5ммоль) гексафлуорфосфа ту О30/70. Отримують 2г гідрохлориду (S)-N-[2-[[[4-(6(бензотриазол-1-іл)-N,Ν,Ν',Ν'-тетраметилуронію (HBTU) додають порціями з перемішуванням, при амінопірид-3-ил)]-1-(4-етилпіперид-3-ил)карбоніл]бутиламіно]сульфоніл]-6-тієн-20°С під азотом, до суміші 2,0г (S)-6-аміно-a-[[1,1ілфеніл]пропанаміду. (диметилетокси)-карбоніл]аміно]піридин-3Вихід (%) =79; темп.пл. (°С)=144-148; пентанова кислоти (5,5ммоль), 1,14г (7,5ммоль) [a]20D(°)=+120 (c=0,2; метанол) гідрохлориду 4-етилпіперидину, Ν,ΝПриклад 2 (сполука 5): діізопропілетиламін (DIEA) (25мл; 14ммоль) у дихГідрохлорид (S)-N-[2-[[[4-(6-амінопірид-3-ил)-1лорметані (30мл) та 3мл безводного диметилфор[(4-етилпіперид-3маміду (ДМФ). С уміші дають нагрітися до кімнатної ил)карбоніл]бутил]аміно]сульфоніл]-4-пірид-2-илтемператури та перемішування продовжують профеніл]пропанаміду (1:2). тягом 18 годин. Реакційну суміш переносять у 2.1. (S)-N-[2-[|[4-(6-амінопірид-3-ил)-1-[(4250мл етилацетату та промивають 50мл 0,1N розетилпіперид-3чину гідрохлоридної кислоти та 50мл насиченого ил)карбоніл]бутил]аміно]сульфоніл]-4-бром-6розчину гідрокарбонату натрію і 50мл насиченого йодфеніл]-пропанамід розчину хлориду натрію. Отриманий продукт далі Використовують той же спосіб, що у прикладі сушать сульфа том натрію та фільтрують і концен1,6, окрім обробки 0,1Η розчином гідрогенхлориду трують під зниженим тиском. Отриманий залишок у ізопропанолі та очистки хроматографією на коочищають хроматографією на колонці з силікагелонці RP 18. Отже, починаючи з 1,4г (3, 6ммоль) лем, елюючи під тиском етилацетатом. 1,48г 1,1гідрохлориду (S)-1-[2-аміно-5-(6-аміно-пірид-3-ил)диметилетил(S)-[4-(6-амінопірид-3-ил)-1-([41-оксопентил]-4-етилпіперидину (1:2) та 1,88г етилпіперид-3-ил)карбоніл]бутил]карбамату отри(3,6ммоль) 2-[біс(1-оксопропіл)аміно]-5-бром-3мують у формі густого масла. йодобензосульфонілхлориду, 1,9г (S)-Ν-[2-[[[4-(6Вихід (%) =74 амінопірид-3-ил)-1-([4-етилпіперид-31.5. Гідрохлорид (S)-1-[2-аміно-5-(6ил]карбоніл]бутил]аміно]сульфоніл]-4-бром-6амінопірид-3-ил)-1-оксопентил]-4-етилпіперидин йодфеніл]пропанаміду отримують у формі білого (1:2) порошку. Ви хід (%)=81; темп. п.л. (°С)=193. Розчин 1,48г (3,6ммоль) 1,1-диметилетил(S-[42.2. (S)-N-[2-[[[4-(6-амінопірид-3-ил)-1-[(4(6-амінопірид-3-іл)-1-[(4-етилпіперид-3етилпіперид-3-ил)карбоніл]бутил]ил)карбоніл]бутил]карбамату у 40мл дихлорметааміно]сульфоніл]-4-бром-6-пірид-2-илфеніл]ну обробляють протягом 1 хвилини при 0°С струпропанамід менем гідрогенхлориду. Через одну годину при 0,08г (0,14ммоль) біс(дибензиліден0°С реакційній суміші дають нагрітися до кімнатної ацетон)паладію(0) додають, при кімнатній темпетемператури та далі концентрують під зниженим ратурі, до суміші 1,8г (2,76ммоль) (S)-N-[2-[[[4-(6тиском. 1,4г гідрохлориду (S)-1-[2-аміно-5-(6амінопірид-3-ил)]-1-[(4-етилпіперид-3-ил)карбоніл]амінопірид-3-ил)-1-оксопентил]-4-етилпіперидин 23 71667 24 бутил]аміно]сульфоніл]-4-бром-6-йодфеніл]ний залишок переносять у 10мл тетрагідрофурану пропанамід, 1,22г
ДивитисяДодаткова інформація
Назва патенту англійськоюN-(heterocyclyl)benzol- or pyridinesulfonamides as antithrombotic and anticoagulation agents
Назва патенту російськоюN-(гетероциклил)бензол- або -пиридинсульфонамиды как антитромботические и антикоагуляцийные средства
МПК / Мітки
МПК: A61K 31/444, A61P 7/02, C07D 401/06, A61K 31/4545, C07D 401/12, C07D 409/12, A61P 43/00, A61K 31/506, A61K 31/497, C07D 211/70, A61K 31/44, C07D 409/14, C07D 401/14, A61K 31/55, A61K 31/4436, A61K 31/496, A61K 31/445, C07D 213/73, A61K 31/5377
Мітки: антитромботичні, піридинсульфонаміди, засоби, n-(гетероцикліл)бензол, антикоагуляційні
Код посилання
<a href="https://ua.patents.su/24-71667-n-geterociklilbenzol-abo-piridinsulfonamidi-yak-antitrombotichni-ta-antikoagulyacijjni-zasobi.html" target="_blank" rel="follow" title="База патентів України">N-(гетероцикліл)бензол- або -піридинсульфонаміди як антитромботичні та антикоагуляційні засоби</a>
Попередній патент: Комплекс для збереження радіоактивних відходів
Наступний патент: Спосіб утилізації відхідних агломераційних газів
Випадковий патент: Всесезонний внутрішньостільниковий ізолятор бджоломатки












