Шестичленні ароматичні сполуки, їх одержання та застосування (варіанти)
Номер патенту: 100862
Опубліковано: 11.02.2013
Автори: Штоллер Андре Деніс, Цамбах Вернер, Майєнфіш Петер, Юнг П'єр Жозеф Марсель, Годфрі Крістофер Річард Айлес
Формула / Реферат
1. Застосування сполуки формули (І)
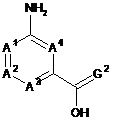 , (I)
, (I)
у якій А1, А2, А3, А4 і G2 є такими, як визначено нижче для сполуки формули (IV), або її N-оксиду або солі як проміжного продукту для одержання сполуки формули (IV)
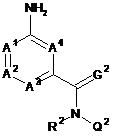 , (IV)
, (IV)
у якій
А1, А2, А3 і А4 незалежно один від одного означають C-R3 або азот, за умови, що не більше двох з А1, А2, А3 і А4 означають азот;
R2 означає водень, С1-С4-алкіл або С1-С4-алкілкарбоніл;
G2 означає кисень або сірку:
кожний R3 незалежно означає водень, галоген, ціаногрупу, нітрогрупу, С1-С4-алкіл, С1-С4-галогеналкіл, гідроксигрупу, С1-С4-алкоксигрупу, С1-С4-галогеналкоксигрупу, тіогрупу, С1-С4-алкілтіогрупу, С1-С4-галогеналкілтіогрупу, С1-С4-алкілсульфініл, С1-С4-галогеналкілсульфініл, С1-С4-алкілсульфоніл, С1-С4-галогеналкілсульфоніл, аміногрупу, N-С1-С4-алкіламіногрупу або N-ді-(С1-С4-алкіл)аміногрупу; і
Q2 означає фрагмент формули (А) або (В)
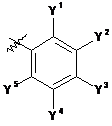 , (A)
, (A) 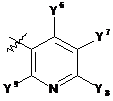 , (B)
, (B)
у якій
Y1 і Y5 незалежно один від одного означають галоген, ціаногрупу, тіоціанатну групу, С1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкоксі-С1-С4-алкіл, ціано-С1-С4-алкіл, С1-С3-алкілтіогрупу, С1-С3-галогеналкілтіогрупу, С1-С3-алкілсульфініл, С1-С3-галогеналкілсульфініл, С1-С3-алкілсульфоніл або С1-С3-галогеналкілсульфоніл;
Y3 означає С2-С6-перфторалкіл, С1-С6-перфторалкілтіогрупу, С1-С6-перфторалкілсульфініл або С1-С6-перфторалкілсульфоніл;
Y2 і Y4 незалежно один від одного означають водень, галоген або С1-С4-алкіл;
Y6 і Y9 незалежно один від одного означають галоген, ціаногрупу, тіоціанатну групу, С1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкоксі-С1-С4-алкіл, ціано-С1-С4-алкіл, С1-С3-алкілтіогрупу, С1-С3-галогеналкілтіогрупу, С1-С3-алкілсульфініл, С1-С3-галогеналкілсульфініл, С1-С3-алкілсульфоніл або С1-С3-галогеналкілсульфоніл;
Y8 означає С1-С4-галогеналкоксигрупу, С2-С6-перфторалкіл, С1-С6-перфторалкілтіогрупу, С1-С6-перфторалкілсульфініл або С1-С6-перфторалкілсульфоніл;
Y7 означає водень, галоген або С1-С4-алкіл;
або її N-оксиду або солі.
2. Застосування сполуки формули (ІІ)
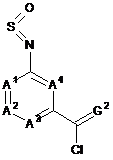 , (II)
, (II)
у якій А1, А2, А3, А4 і G2 є такими, як визначено нижче для сполуки формули (IV);
або її N-оксиду або солі як проміжного продукту для одержання сполуки формули (IV)
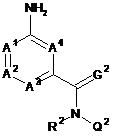 , (IV)
, (IV)
у якій
А1, А2, А3 і А4 незалежно один від одного означають C-R3 або азот, за умови, що не більше двох з А1, А2, А3 і А4 означають азот;
R2 означає водень, С1-С4-алкіл або С1-С4-алкілкарбоніл;
G2 означає кисень або сірку:
кожний R3 незалежно означає водень, галоген, ціаногрупу, нітрогрупу, С1-С4-алкіл, С1-С4-галогеналкіл, гідроксигрупу, С1-С4-алкоксигрупу, С1-С4-галогеналкоксигрупу, тіогрупу, С1-С4-алкілтіогрупу, С1-С4-галогеналкілтіогрупу, С1-С4-алкілсульфініл, С1-С4-галогеналкілсульфініл, С1-С4-алкілсульфоніл, С1-С4-галогеналкілсульфоніл, аміногрупу, N-С1-С4-алкіламіногрупу або N-ді-(С1-С4-алкіл)аміногрупу; і
Q2 означає фрагмент формули (А) або (В)
 , (A)
, (A) 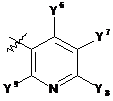 , (B)
, (B)
у якій
Y1 і Y5 незалежно один від одного означають галоген, ціаногрупу, тіоціанатну групу, С1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкоксі-С1-С4-алкіл, ціано-С1-С4-алкіл, С1-С3-алкілтіогрупу, С1-С3-галогеналкілтіогрупу, С1-С3-алкілсульфініл, С1-С3-галогеналкілсульфініл, С1-С3-алкілсульфоніл або С1-С3-галогеналкілсульфоніл;
Y3 означає С2-С6-перфторалкіл, С1-С6-перфторалкілтіогрупу, С1-С6-перфторалкілсульфініл або С1-С6-перфторалкілсульфоніл;
Y2 і Y4 незалежно один від одного означають водень, галоген або С1-С4-алкіл;
Y6 і Y9 незалежно один від одного означають галоген, ціаногрупу, тіоціанатну групу, С1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкоксі-С1-С4-алкіл, ціано-С1-С4-алкіл, С1-С3-алкілтіогрупу, С1-С3-галогеналкілтіогрупу, С1-С3-алкілсульфініл, С1-С3-галогеналкілсульфініл, С1-С3-алкілсульфоніл або С1-С3-галогеналкілсульфоніл;
Y8 означає С1-С4-галогеналкоксигрупу, С2-С6-перфторалкіл, С1-С6-перфторалкілтіогрупу, С1-С6-перфторалкілсульфініл або С1-С6-перфторалкілсульфоніл;
Y7 означає водень, галоген або С1-С4-алкіл;
або її N-оксиду або солі.
3. Застосування сполуки формули (ІІІ)
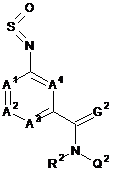 , (III)
, (III)
у якій А1, А2, А3, А4, G2 і Q2 є такими, як визначено нижче для сполуки формули (IV); або її N-оксиду або солі як проміжного продукту для одержання сполуки формули (IV)
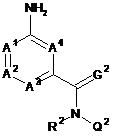 , (IV)
, (IV)
у якій
А1, А2, А3 і А4 незалежно один від одного означають C-R3 або азот, за умови, що не більше двох з А1, А2, А3 і А4 означають азот;
R2 означає водень, С1-С4-алкіл або С1-С4-алкілкарбоніл;
G2 означає кисень або сірку;
кожний R3 незалежно означає водень, галоген, ціаногрупу, нітрогрупу, С1-С4-алкіл, С1-С4-галогеналкіл, гідроксигрупу, С1-С4-алкоксигрупу, С1-С4-галогеналкоксигрупу, тіогрупу, С1-С4-алкілтіогрупу, С1-С4-галогеналкілтіогрупу, С1-С4-алкілсульфініл, С1-С4-галогеналкілсульфініл, С1-С4-алкілсульфоніл, С1-С4-галогеналкілсульфоніл, аміногрупу, N-С1-С4-алкіламіногрупу або N-ді-(С1-С4-алкіл)аміногрупу; і
Q2 означає фрагмент формули (А) або (В)
 , (A)
, (A) 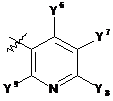 , (B)
, (B)
у якій
Y1 і Y5 незалежно один від одного означають галоген, ціаногрупу, тіоціанатну групу, С1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкоксі-С1-С4-алкіл, ціано-С1-С4-алкіл, С1-С3-алкілтіогрупу, С1-С3-галогеналкілтіогрупу, С1-С3-алкілсульфініл, С1-С3-галогеналкілсульфініл, С1-С3-алкілсульфоніл або С1-С3-галогеналкілсульфоніл;
Y3 означає С2-С6-перфторалкіл, С1-С6-перфторалкілтіогрупу, С1-С6-перфторалкілсульфініл або С1-С6-перфторалкілсульфоніл;
Y2 і Y4 незалежно один від одного означають водень, галоген або С1-С4-алкіл;
Y6 і Y9 незалежно один від одного означають галоген, ціаногрупу, тіоціанатну групу, С1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкоксі-С1-С4-алкіл, ціано-С1-С4-алкіл, С1-С3-алкілтіогрупу, С1-С3-галогеналкілтіогрупу, С1-С3-алкілсульфініл, С1-С3-галогеналкілсульфініл, С1-С3-алкілсульфоніл або С1-С3-галогеналкілсульфоніл;
Y8 означає С1-С4-галогеналкоксигрупу, С2-С6-перфторалкіл, С1-С6-перфторалкілтіогрупу, С1-С6-перфторалкілсульфініл або С1-С6-перфторалкілсульфоніл;
Y7 означає водень, галоген або С1-С4-алкіл;
або її N-оксиду або солі.
4. Спосіб одержання сполуки формули (III)
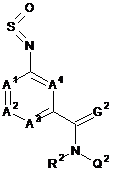 , (III)
, (III)
у якій А1, А2, А3, А4, G2 і Q2 є такими, як визначено у п. 1,
шляхом обробки сполуки формули (II)
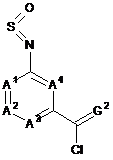 , (II)
, (II)
у якій А1, А2, А3, А4 і G2 є такими, як визначено у п. 1,
аміном формули HNR2Q2, у якій R2 і Q2 є такими, як визначено у п. 1, у лужному середовищі.
5. Спосіб одержання сполуки формули (IV)
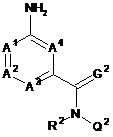 , (IV)
, (IV)
у якій А1, А2, А3, А4, R2, G2 і Q2 є такими, як визначено у п. 1,
шляхом обробки сполуки формули (III)
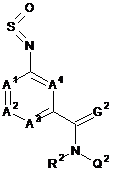 , (III)
, (III)
у якій А1, А2, А3, А4, G2 і Q2 є такими, як визначено у п. 1,
водою.
6. Спосіб одержання сполуки формули (IV)
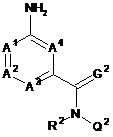 , (IV)
, (IV)
у якій А1, А2, А3, А4, R2, G2 і Q2 є такими, як визначено у п. 1,
шляхом обробки сполуки формули (II)
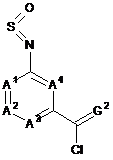 , (II)
, (II)
у якій А1, А2, А3, А4 і G2 є такими, як визначено у п. 1,
аміном формули HNR2Q2, у якій R2 і Q2 є такими, як визначено у п. 1, у лужному середовищі, з наступною обробкою проміжного продукту водою.
7. Сполука формули (ІI)
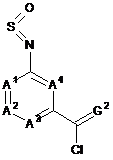 , (ІI)
, (ІI)
у якій А1, А2, А3, А4 і G2 є такими, як визначено у п. 1; або її N-оксид або сіль, за умови, що сполука формули (ІI) не являє собою 2-хлор-5-сульфініламінобензоїлхлорид, 4-метокси-3-сульфініламінобензоїлхлорид, 4-метил-3-сульфініламінобензоїлхлорид, 3-сульфініламінобензоїлхлорид, 2,3,4,6-тетрайод-5-сульфініламінобензоїлхлорид або 2,4,6-трийод-3-сульфініламінобензоїлхлорид.
8. Сполука формули (ІIІ)
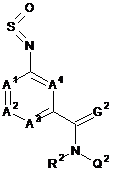 , (ІIІ)
, (ІIІ)
у якій А1, А2, А3, А4, G2 і Q2 є такими, як визначено у п. 1;
або її N-оксид або сіль.
Текст
Реферат: У заявці описані способи застосування деяких сполук формули (І), (II) і (III) для синтезу проміжного продукту формули (IV), призначеного для синтезу інсектицидів, UA 100862 C2 (12) UA 100862 C2 O NH2 S N A 1 A 2 A A 4 3 A 2 OH 1 A G 2 A A 4 G 3 , (I) 2 Cl , (II) O NH2 S N A A 1 A A 2 A A G 3 R (III) 1 2 4 2 2 A A G 3 R N Q 2 4 2 N 2 2 Q , , (IV) у якій замісники є такими, як визначено у пункті 1 формули винаходу, способи одержання цих сполук, способи, у яких ці сполуки застосовуються для одержання проміжних продуктів, призначених для синтезу інсектицидів, і деякі нові сполуки формули (ІI) і (III). UA 100862 C2 5 10 15 20 25 30 35 40 Даний винахід відноситься до способів застосування деяких сполук формули (I), (II) і (III) як проміжні продукти, до способів одержання цих сполук, до способів, у яких ці сполуки застосовуються для одержання проміжних продуктів формули (IV) для синтезу інсектицидів, і до деяких нових сполук формули (II') і (III'). Сполуки, запропоновані у даному винаході, є проміжними продуктами, які застосовуються для синтезу карбаматних інсектицидів, як це розкрито, наприклад, в EP 1661886 і JP 2006225340, і для синтезу бісамідних інсектицидів, як це розкрито, наприклад, в EP 1714958, JP 2006/306771, EP 1911751, EP 1916236 і WO 07/017075. Способи одержання карбаматних інсектицидів і бісамідних інсектицидів і деяких придатних проміжних продуктів, таких як 3-аміно-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1трифторметилетил)-феніл]-бензамід і інші 3-амінобензаміди, розкриті в EP 1661886, JP 2006225340, EP 1714958, JP 2006/306771, EP 1911751, EP 1916236 і WO 07/017075. У цих публікаціях 3-аміно-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилетил)-феніл]-бензамід одержували в такий спосіб: a) 3-нітробензойну кислоту перетворювали у 3-нітробензоїлхлорид, b) 3-нітробензоїлхлорид уводили в реакцію з аніліном, тобто з 2,6-диметил-4-(1,2,2,2тетрафтор-1-трифторметилетил)-феніламіном, і одержували 3-нітро-бензамід, тобто 3-нітро-N[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилетил)-феніл]-бензамід, і c) 3-нітро-бензамід, тобто 3-нітро-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1трифторметилетил)-феніл]-бензамід, відновлювали й одержували шуканий 3-амінобензамід, тобто 3-аміно-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилетил)-феніл]-бензамід. Одержували інші 3-амінобензаміди, наприклад, шляхом використання заміщеної 3нітробензойної кислоти, такої як 2-фтор-3-нітробензойна кислота, на стадії a) і/або іншого аніліну, такого як 2-етил-6-метил-4-(1,2,2,2-тетрафтор-1-трифторметилетил)-феніламін, на стадії b). Хоча цей трьохстадійний синтез приводить до задовільних результатів у лабораторії, для виробництва карбаматних інсектицидів або бісамідних інсектицидів у промисловому масштабі необхідний більше короткий шлях одержання 3-амінобензамідів. Необхідні нові й кращі способи одержання бісамідних інсектицидів і проміжних продуктів і для цього у даному винаході запропоновані проміжні продукти й відповідні реакції. Даний винахід відноситься до альтернативного трьохстадійного синтезу й до більше короткого двохстадійного синтезу, які краще підходять для одержання карбаматних інсектицидів або бісамідних інсектицидів у промисловому масштабі. У цих синтезах не використовуються реакції, що мають несприятливі характеристики (наприклад, дорогі реагенти несприятливі внаслідок високої вартості, реакції, для проведення яких необхідний газ, такий як водень, несприятливі з погляду безпеки, реакції, для проведення яких необхідний важкий метал, такий як хлорид олова(II), несприятливі з погляду (еко)токсичності). Замість цього у даному винаході для синтезу проміжних продуктів запропоновані шляхи з використанням реакцій, що мають сприятливі характеристики (наприклад, сульфонілхлорид є недорогим реагентом і не потрібний ні газ, ні важкий метал). Тому даний винахід відноситься до способу застосування як проміжний продукт для одержання сполуки формули (IV) NH2 1 4 A A 2 A 45 50 3 A G 2 (IV) 2 N 2 R Q у якій 1 2 3 4 3 A , A , A і A незалежно один від одного означають C-R або азот, за умови, що не більше 1 2 3 4 двох з A , A , A і A означають азот; 2 R означає водень, C1-C4-алкіл або C1-C4-алкілкарбоніл; 2 G означає кисень або сірку; 3 кожний R незалежно означає водень, галоген, ціаногрупу, нітрогрупу, C1-C4-алкіл, C1-C4галогеналкіл, гідроксигрупу, C1-C4-алкоксигрупу, C1-C4-галогеналкоксигрупу, тіогрупу, C1-C4 алкілтіогрупу, C1-C4-галогеналкілтіогрупу, C1-C4-алкілсульфініл, C1-C4-галогеналкілсульфініл, C1C4-алкілсульфоніл, C1-C4-галогеналкілсульфоніл, аміногрупу, N-C1-C4-алкіламіногрупу або N, Nді-(C1-C4-алкіл)-аміногрупу; і 2 Q означає фрагмент формули (A) або (B) 1 UA 100862 C2 1 Y 6 Y 2 Y 7 Y (A) 5 (B) 3 Y Y 9 8 Y N Y Y у якій 1 5 Y і Y незалежно один від одного означають галоген, ціаногрупу, тіоціанатну групу, C1-C4алкіл, C1-C4-галогеналкіл, C1-C4-алкоксі-C1-C4-алкіл, ціано-C1-C4-алкіл, C1-C3-алкілтіогрупу, C1C3-галогеналкілтіогрупу, C1-C3-алкілсульфініл, C1-C3-галогеналкілсульфініл, C1-C3алкілсульфоніл або C1-C3-галогеналкілсульфоніл; 3 Y означає C2-C6-перфторалкіл, C1-C6-перфторалкілтіогрупу, C1-C6-перфторалкілсульфініл або C1-C6-перфторалкілсульфоніл; 2 4 Y і Y незалежно один від одного означають водень, галоген або C1-C4-алкіл; 6 9 Y і Y незалежно один від одного означають галоген, ціаногрупу, тіоціанатну групу, C1-C4алкіл, C1-C4-галогеналкіл, C1-C4-алкоксі-C1-C4-алкіл, ціано-C1-C4-алкіл, C1-C3-алкілтіогрупу, C1C3-галогеналкілтіогрупу, C1-C3-алкілсульфініл, C1-C3-галогеналкілсульфініл, C1-C3алкілсульфоніл або C1-C3-галогеналкілсульфоніл; 8 Y означає C1-C4-галогеналкоксигрупу, C2-C6-перфторалкіл, C1-C6-перфторалкілтіогрупу, C1C6-перфторалкілсульфініл або C1-C6-перфторалкілсульфоніл; 7 Y означає водень, галоген або C1-C4-алкіл; або його N-оксиду або солі; a) сполуки формули (I) NH2 4 5 10 15 1 A 4 2 A 20 A 2 A G 3 OH 1 2 3 4 2 у якій A , A , A , A і G є такими, як визначено для сполуки формули (IV); або його N-оксиду або солі; або b) сполуки формули (II) O S N 1 4 A G 3 A 2 Cl 1 2 3 4 2 у якій A , A , A , A і G є такими, як визначено для сполуки формули (IV); або його N-оксиду або солі; або c) сполуки формули (III) O S N 1 4 A A 2 A 30 (II) A 2 A 25 (I) 3 A (III) G 2 2 N 2 R Q 1 2 3 4 2 2 2 у якій A , A , A , A , R , G і Q є такими, як визначено для сполуки формули (IV); або його Nоксиду або солі. Сполуки формули (I), (II), (III) і (IV) можуть існувати у вигляді різних геометричних або оптичних ізомерів або у різних таутомерних формах. В обсяг даного винаходу входять всі такі 2 UA 100862 C2 5 10 15 20 25 30 35 40 45 50 55 60 ізомери й таутомери і їх суміші у всіх співвідношеннях, а також ізотопозаміщенні форми, такі як дейтеровані сполуки. Кожний алкільний фрагмент, окремо або у вигляді частини більшої групи (такої як алкоксигрупа, алкоксикарбоніл, алкілкарбоніл або алкілен), має лінійний або розгалужений ланцюг і означає, наприклад, метил, етил, н-пропіл, проп-2-іл, н-бутил, бут-2-ил, 2-метилпроп-1іл або 2-метилпроп-2-іл. Алкільні групи переважно являють собою C1-C6-алкільні групи, більш переважно - C1-C4- і найбільше переважно - C1-C3-алкільні групи. Галоген означає фтор, хлор, бром або йод. Галогеналкільні групи (окремо або у вигляді частини більшої групи, такої як галогеналкоксигрупа або галогеналкілтіогрупа) являють собою алкільні групи, які заміщені одним або більшою кількістю однакових або різних атомів галогенів і являють собою, наприклад, трифторметил, хлордифторметил, 2,2,2-трифторетил або 2,2-дифторетил. Перфторалкільні групи (окремо або у вигляді частини більшої групи, такої як перфторалкілтіогрупа) являють собою особливий тип галогеналкільної групи; вони являють собою алкільні групи, які повністю заміщені атомами фтору, і являють собою, наприклад, трифторметил, пентафторетил, гептафторпроп-2-іл або нонафторбут-2-ил. Ціаноалкільні групи являють собою алкільні групи, які заміщені одним або більшою кількістю ціаногруп, наприклад, ціанометил або 1,3-диціанопропіл. 1 2 3 4 2 2 3 2 Кращі групи для A , A , A , A , R , G , R і Q у будь-якій їхній комбінації наведені нижче. Переваги відносяться до сполук формули (I), (II), (III) і (IV) відповідно. 1 3 Переважно, якщо A означає C-R . 2 3 Переважно, якщо A означає C-R . 3 3 Переважно, якщо A означає C-R . 4 3 Переважно, якщо A означає C-R . 2 Переважно, якщо R означає водень, метил, етил або ацетил, більш переважно - водень, метил або етил, ще більш переважно - водень або етил, найбільше переважно - водень. 2 Переважно, якщо G означає кисень. 3 Переважно, якщо кожний R незалежно означають водень, галоген, ціаногрупу, нітрогрупу, C1-C4-алкіл, C1-C4-галогеналкіл або C1-C4-алкоксигрупу, більш переважно - водень, галоген, ціаногрупу, нітрогрупу, метил, трифторметил або метоксигрупу, ще більш переважно - водень, фтор, ціаногрупу, нітрогрупу, трифторметил або метоксигрупу, ще більш переважно - водень, фтор або ціаногрупу, найбільше переважно - водень. 2 Переважно, якщо Q означає фрагмент формули (A). 1 Переважно, якщо Y означає галоген, ціаногрупу, метил, етил, трифторметил або метоксиметил, більш переважно - бром, хлор, метил, етил або метоксиметил, ще більш переважно - бром, метил або етил, найбільше переважно - метил. 2 Переважно, якщо Y означає водень, хлор, фтор або метил, найбільше переважно - водень. 3 Переважно, якщо Y означає гептафторпропіл, гептафторпроп-2-іл, гептафторпропілтіогрупу, гептафторпропілсульфініл, гептафторпропілсульфоніл, гептафторпроп-2-ілтіогрупу, гептафторпроп-2-ілсульфініл, гептафторпроп-2-ілсульфоніл або нонафторбут-2-ил, більш переважно - гептафторпроп-2-іл або нонафторбут-2-ил, найбільше переважно - гептафторпроп-2-іл. 4 Переважно, якщо Y означає водень, хлор, фтор або метил, найбільше переважно - водень. 5 Переважно, якщо Y означає галоген, ціаногрупу, метил, етил або трифторметил, більш переважно - бром, хлор, метил або етил, ще більш переважно - бром, метил або етил, найбільше переважно - метил. 6 Переважно, якщо Y означає галоген, ціаногрупу, метил, етил, трифторметил або метоксиметил, більш переважно - бром, хлор, метил, етил або метоксиметил, ще більш переважно - бром, метил або етил, найбільше переважно - метил. 7 Переважно, якщо Y означає водень, хлор, фтор або метил, найбільше переважно - водень. 8 Переважно, якщо Y означає гептафторпропіл, гептафторпроп-2-іл, гептафторпропілтіогрупу, гептафторпропілсульфініл, гептафторпропілсульфоніл, гептафторпроп-2-ілтіогрупу, гептафторпроп-2-ілсульфініл, гептафторпроп-2-ілсульфоніл або нонафторбут-2-ил, більш переважно - гептафторпроп-2-іл або нонафторбут-2-ил, найбільше переважно - гептафторпроп-2-іл. 9 Переважно, якщо Y означає галоген, ціаногрупу, метил, етил, трифторметил або метоксиметил, більш переважно - бром, хлор, метил, етил або метоксиметил, ще більш переважно - бром, метил або етил, найбільше переважно - метил. 1 2 3 4 У кращому варіанті здійснення A , A , A , A означають CH. 1 2 3 4 У кращому варіанті здійснення A означає C-F і A , A і A означають CH. 3 UA 100862 C2 2 5 10 15 20 25 30 1 3 4 У кращому варіанті здійснення A означає C-F і A , A і A означають CH. 3 1 2 4 У кращому варіанті здійснення A означає C-F і A , A і A означають CH. 4 1 2 3 У кращому варіанті здійснення A означає C-F і A , A і A означають CH. 1 2 3 4 У кращому варіанті здійснення A означає C-CN і A , A і A означають CH. 2 1 3 4 У кращому варіанті здійснення A означає C-CN і A , A і A означають CH. 3 1 2 4 У кращому варіанті здійснення A означає C-CN і A , A і A означають CH. 4 1 2 3 У кращому варіанті здійснення A означає C-CN і A , A і A означають CH. 1 2 3 4 У кращому варіанті здійснення A означає C-NO2 і A , A і A означають CH. 2 1 3 4 У кращому варіанті здійснення A означає C-NO2 і A , A і A означають CH. 3 1 2 4 У кращому варіанті здійснення A означає C-NO2 і A , A і A означають CH. 4 1 2 3 У кращому варіанті здійснення A означає C-NO2 і A , A і A означають CH. 2 У кращому варіанті здійснення Q означає 2,6-диметил-4-(гептафторпроп-2-іл)-феніл. 2 У кращому варіанті здійснення Q означає 2-етил-6-метил-4-(гептафторпроп-2-іл)-феніл. 2 У кращому варіанті здійснення Q означає 2,6-діетил-4-(гептафторпроп-2-іл)-феніл. 2 У кращому варіанті здійснення Q означає 2-метоксиметил-6-метил-4-(гептафторпроп-2-іл)феніл. 2 У кращому варіанті здійснення Q означає 2-бром-6-метил-4-(гептафторпроп-2-іл)-феніл. 2 У кращому варіанті здійснення Q означає 2-бром-6-етил-4-(гептафторпроп-2-іл)-феніл. 2 У кращому варіанті здійснення Q означає 2,6-дихлор-4-(гептафторпроп-2-іл)-феніл. 2 У кращому варіанті здійснення Q означає 2,6-дибром-4-(гептафторпроп-2-іл)-феніл. 2 У кращому варіанті здійснення Q означає 2,6-диметил-4-(нонафторбут-2-ил)-феніл. 2 У кращому варіанті здійснення Q означає 2-етил-6-метил-4-(нонафторбут-2-ил)-феніл. 2 У кращому варіанті здійснення Q означає 2,6-діетил-4-(нонафторбут-2-ил)-феніл. 2 У кращому варіанті здійснення Q означає 2-метоксиметил-6-метил-4-(нонафторбут-2-ил)феніл. 2 У кращому варіанті здійснення Q означає 2-бром-6-метил-4-(нонафторбут-2-ил)-феніл. 2 У кращому варіанті здійснення Q означає 2-бром-6-етил-4-(нонафторбут-2-ил)-феніл. 2 У кращому варіанті здійснення Q означає 2,6-дихлор-4-(нонафторбут-2-ил)-феніл. 2 У кращому варіанті здійснення Q означає 2,6-дибром-4-(нонафторбут-2-ил)-феніл. Приклади сполук формули (I), які ілюструють даний винахід, наведені в таблиці 1. Таблиця 1: 2 1 2 3 4 У таблиці 1 наведені 13 сполук формули (I), у якій G означає кисень і значення X , X , X і X є такими, як визначено в таблиці 1. NH2 4 1 X X (I) G 2 X 3 X 35 Сполука № 1.01 1.02 1.03 1.04 1.05 1.06 1.07 1.08 1.09 1.10 1.11 1.12 1.13 40 2 OH 1 X H -F H H H -CN H H H -NO2 H H H 2 3 X H H -F H H H -CN H H H -NO2 H H X H H H -F H H H -CN H H H -NO2 H 4 X H H H H -F H H H -CN H H H -NO2 Приклади сполук формули (II), які ілюструють даний винахід, наведені в таблиці 2. Таблиця 2: 2 1 2 3 У таблиці 2 наведені 13 сполук формули (II), у якій G означає кисень і значення X , X , X і 4 X є такими, як визначено в таблиці 2. 4 UA 100862 C2 O S N A A 1 A 4 (II) 2 A G 3 2 Cl 1 Сполука № 2.01 2.02 2.03 2.04 2.05 2.06 2.07 2.08 2.09 2.10 2.11 2.12 2.13 5 X H -F H H H -CN H H H -NO2 H H H 2 X H H -F H H H -CN H H H -NO2 H H 3 X H H H -F H H H -CN H H H -NO2 H 4 X H H H H -F H H H -CN H H H -NO2 Приклади сполук формули (III), які ілюструють даний винахід, наведені в таблицях 3-18. Таблиця 3: 2 2 У таблиці 3 наведені 13 сполук формули (III), у якій G означає кисень, R означає водень, 2 1 2 3 4 Q означає 2,6-диметил-4-(гептафторпроп-2-іл)-феніл і значення X , X , X і X є такими, як визначено в таблиці 3. O S N 1 4 A A 2 A G 3 A R 2 N 10 Сполука № 3.01 3.02 3.03 3.04 3.05 3.06 3.07 3.08 3.09 3.10 3.11 3.12 3.13 Q 2 (III) 2 1 X H -F H H H -CN H H H -NO2 H H H 2 X H H -F H H H -CN H H H -NO2 H H 3 X H H H -F H H H -CN H H H -NO2 H 4 X H H H H -F H H H -CN H H H -NO2 Таблиця 4: 2 2 У таблиці 4 наведені 13 сполук формули (III), у якій G означає кисень, R означає водень, 2 1 2 3 4 Q означає 2-етил-6-метил-4-(гептафторпроп-2-іл)-феніл і значення X , X , X і X є такими, як 5 UA 100862 C2 5 10 15 20 25 30 35 40 45 50 55 визначено в таблиці 3. Таблиця 5: 2 2 У таблиці 5 наведені 13 сполук формули (III), у якій G означає кисень, R означає водень, 2 1 2 3 4 Q означає 2,6-діетил-4-(гептафторпроп-2-іл)-феніл і значення X , X , X і X є такими, як визначено в таблиці 3. Таблиця 6: 2 2 У таблиці 6 наведені 13 сполук формули (III), у якій G означає кисень, R означає водень, 2 1 2 3 4 Q означає 2-метоксиметил-6-метил-4-(гептафторпроп-2-іл)-феніл і значення X , X , X і X є такими, як визначено в таблиці 3. Таблиця 7: 2 2 У таблиці 7 наведені 13 сполук формули (III), у якій G означає кисень, R означає водень, 2 1 2 3 4 Q означає 2-бром-6-метил-4-(гептафторпроп-2-іл)-феніл і значення X , X , X і X є такими, як визначено в таблиці 3. Таблиця 8: 2 2 У таблиці 8 наведені 13 сполук формули (III), у якій G означає кисень, R означає водень, 2 1 2 3 4 Q означає 2-бром-6-етил-4-(гептафторпроп-2-іл)-феніл і значення X , X , X і X є такими, як визначено в таблиці 3. Таблиця 9: 2 2 У таблиці 9 наведені 13 сполук формули (III), у якій G означає кисень, R означає водень, 2 1 2 3 4 Q означає 2,6-дихлор-4-(гептафторпроп-2-іл)-феніл і значення X , X , X і X є такими, як визначено в таблиці 3. Таблиця 10: 2 2 У таблиці 10 наведені 13 сполук формули (III), у якій G означає кисень, R означає водень, 2 1 2 3 4 Q означає 2,6-дибром-4-(гептафторпроп-2-іл)-феніл і значення X , X , X і X є такими, як визначено в таблиці 3. Таблиця 11: 2 2 У таблиці 11 наведені 13 сполук формули (III), у якій G означає кисень, R означає водень, 2 1 2 3 4 Q означає 2,6-диметил-4-(нонафторбут-2-ил)-феніл і значення X , X , X і X є такими, як визначено в таблиці 3. Таблиця 12: 2 2 У таблиці 12 наведені 13 сполук формули (III), у якій G означає кисень, R означає водень, 2 1 2 3 4 Q означає 2-етил-6-метил-4-(нонафторбут-2-ил)-феніл і значення X , X , X і X є такими, як визначено в таблиці 3. Таблиця 13: 2 2 У таблиці 13 наведені 13 сполук формули (III), у якій G означає кисень, R означає водень, 2 1 2 3 4 Q означає 2,6-діетил-4-(нонафторбут-2-ил)-феніл і значення X , X , X і X є такими, як визначено в таблиці 3. Таблиця 14: 2 2 У таблиці 14 наведені 13 сполук формули (III), у якій G означає кисень, R означає водень, 2 1 2 3 4 Q означає 2-метоксиметил-6-метил-4-(нонафторбут-2-ил)-феніл і значення X , X , X і X є такими, як визначено в таблиці 3. Таблиця 15: 2 2 У таблиці 15 наведені 13 сполук формули (III), у якій G означає кисень, R означає водень, 2 1 2 3 4 Q означає 2-бром-6-метил-4-(нонафторбут-2-ил)-феніл і значення X , X , X і X є такими, як визначено в таблиці 3. Таблиця 16: 2 2 У таблиці 16 наведені 13 сполук формули (III), у якій G означає кисень, R означає водень, 2 1 2 3 4 Q означає 2-бром-6-етил-4-(нонафторбут-2-ил)-феніл і значення X , X , X і X є такими, як визначено в таблиці 3. Таблиця 17: 2 2 У таблиці 17 наведені 13 сполук формули (III), у якій G означає кисень, R означає водень, 2 1 2 3 4 Q означає 2,6-дихлор-4-(нонафторбут-2-ил)-феніл і значення X , X , X і X є такими, як визначено в таблиці 3. Таблиця 18: 2 2 У таблиці 18 наведені 13 сполук формули (III), у якій G означає кисень, R означає водень, 2 1 2 3 4 Q означає 2,6-дибром-4-(нонафторбут-2-ил)-феніл і значення X , X , X і X є такими, як визначено в таблиці 3. Схема A 6 UA 100862 C2 O O NH2 1 S N N 4 A A 2 A S G 3 A 2 (1) 1 (2) A 2 A OH 1 4 A G 3 A 4 A A 2 A 2 Cl (I) G 3 A R N 2 Q 2 2 (II) (III) (5) (3) NH2 (4) A A 1 4 A 2 G 3 A R 2 N Q 2 2 (IV) 5 10 15 На схемі A наведені реакції (1), (2), (3), (4) і (5), у яких проміжний продукт формули (II) для синтезу інсектициду одержують зі сполуки формули (I), проміжний продукт формули (III) для синтезу інсектициду одержують зі сполуки формули (II), проміжний продукт формули (IV) для синтезу інсектициду одержують зі сполуки формули (III), проміжний продукт формули (IV) для синтезу інсектициду одержують зі сполуки формули (II) і проміжний продукт формули (III) для синтезу інсектициду одержують зі сполуки формули (IV) відповідно. Реакції типу (1) O NH2 S N SOCl2 1 4 A A 1 4 2 2 A A A G 3 2 2 A A G 3 A OH Cl (I) (II) 1) Хлорангідриди кислот формули (II) можна одержати з амінокарбонової кислоти формули (I) за методиками, відомими фахівцеві у даній області техніки, такими як обробка тіонілхлоридом. Така реакція описана, наприклад, у публікації Journal fuer Praktische Chemie (Leipzig) (1937), 148, 161-169. Реакцію переважно можна проводити у придатному розчиннику, переважно - в апротонному розчиннику, наприклад, простому ефірі (такому як тетрагідрофуран або діетиловий ефір), галогенованному вуглеводні (такому як дихлорметан, хлороформ, тетрахлорид вуглецю або 1,1,1-трихлоретан), галогенованній або не галогенованній ароматичній сполуці (такій як толуол або хлорбензол) або в їхній суміші. Реакції типу (2) 7 UA 100862 C2 5 10 15 20 2) Сполуки формули (III) можна одержати шляхом обробки сполуки формули (II) аміном 2 2 формули HNR Q з утворенням амідного зв'язку у лужному середовищі (наприклад, у присутності органічної основи, такої як піридин, триетиламін, 4-(диметиламіно)-піридин, 2 2 діізопропілетиламін, або надлишку аміну HNR Q , або в присутності поглинача кислоти, такого як карбонат натрію, гідрокарбонат натрію, карбонат калію або гідрокарбонат калію). Реакцію переважно можна проводити у придатному розчиннику, переважно - в апротонному розчиннику, наприклад, простому ефірі (такому як тетрагідрофуран або діетиловий ефір), галогенованному вуглеводні (такому як дихлорметан, хлороформ, тетрахлорид вуглецю або 1,1,1-трихлоретан), галогенованній або не галогенованній ароматичній сполуці (такій як толуол або хлорбензол) або в їхній суміші. Реакції типу (3) O NH2 S N 1 4 A A H2O 1 4 2 2 A A A G 3 2 2 A A G 3 A 2 N 2 R Q 2 N 2 R Q (IV) (III) 3) Сполуки формули (IV) можна одержати шляхом обробки сполуки формули (III) водою у нейтральному, кислому або лужному середовищі (переважно - у кислому середовищі, наприклад, у присутності розведеного водяного розчину хлористоводневої кислоти). Реакцію переважно можна проводити у придатному розчиннику, переважно - в апротонному розчиннику, наприклад, простому ефірі (такому як тетрагідрофуран або діетиловий ефір), галогенованному вуглеводні (такому як дихлорметан, хлороформ, тетрахлорид вуглецю або 1,1,1-трихлоретан), галогенованній або не галогенованній ароматичній сполуці (такій як толуол або хлорбензол) або в їхній суміші (такій як суміш дихлорметану й тетрагідрофурану). Реакції типу (4) 8 UA 100862 C2 5 10 15 20 25 4) Реакції типу (4) являють собою комбінацію реакції типу (2) і реакції типу (3). Оскільки сполуки формули (III) можуть легко піддаватися гідролізу, їх зручно не виділяти, а безпосередньо перетворювати у сполуки формули (IV), які звичайно зручніше використовувати. Крім того, при цьому кількість стадій реакції зменшується на одну, оскільки останнє перетворення можна легко провести під час обробки водою реакційної суміші, що містять сполуки формули (III). Реакція 3-сульфініламінобензоїлхлориду з первинним аміном описана, наприклад, в EP 54,839. Реакції 3-сульфініламінобензоїлхлориду з аніліном, 2-метиланіліном і 2-метоксіаніліном описані, наприклад, у публікаціях Deposited Doc. (1975), (VINITI 2561-2575), (CAN 87:134385), Реакція 2-сульфініламінобензоїлхлориду з аніліном описана, наприклад, у публікації Journal of Organic Chemistry (2001), 66(8), 2784-2788. Однак у жодній із цих публікацій не розкритий проміжний продукт формули (III). Відповідно до винаходу було показано, що сполука формули (III) являє собою прямий продукт реакції типу (2) і що сполука формули (III) потім гідролізується, наприклад, під час обробки водою. Реакцію переважно можна проводити у придатному розчиннику, переважно - в апротонному розчиннику, наприклад, простому ефірі (такому як тетрагідрофуран або діетиловий ефір), галогенованному вуглеводні (такому як дихлорметан, хлороформ, тетрахлорид вуглецю або 1,1,1-трихлоретан), галогенованній або не галогенованній ароматичній сполуці (такій як толуол або хлорбензол) або в їхній суміші. Реакції типу (5) O NH2 S N 1 4 SO2Cl A A 1 4 2 2 A A A G 3 2 2 A A G 3 A 2 N 2 R Q 2 N 2 R Q (IV) (III) 5) Сполуки формули (III) можна одержати шляхом обробки похідного амінокарбонової кислоти формули (IV) за методиками, відомими фахівцеві у даній області техніки, такими як обробка тіонілхлоридом. Реакцію переважно можна проводити у придатному розчиннику, переважно - в апротонному розчиннику, наприклад, простому ефірі (такому як тетрагідрофуран або діетиловий ефір), галогенованному вуглеводні (такому як дихлорметан, хлороформ, тетрахлорид вуглецю або 1,1,1-трихлоретан), галогенованній або не галогенованній ароматичній сполуці (такій як толуол або хлорбензол) або в їхній суміші. Деякі сполуки формули (II) і (III) є новими і як такі утворюють ще один об'єкт даного винаходу. Тому даний винахід відноситься до сполуки формули (II') 9 UA 100862 C2 O S N A A 1 A 4 (II') 2 A G 3 2 Cl 5 , у якій 1 2 3 4 2 A , A , A , A і G є такими, як визначено для сполуки формули (I); або його N-оксиду або солі, за умови, що (II') не являє собою 2-хлор-5-сульфініламінобензоїлхлорид, 4-метокси-3сульфініламінобензоїлхлорид, 4-метил-3-сульфініламінобензоїлхлорид, 3сульфініламінобензоїлхлорид, 2,3,4,6-тетрайодо-5-сульфініламінобензоїлхлорид або 2,4,61 2 3 4 2 трийодо-3-сульфініламінобензоїлхлорид. Кращими значеннями для A , A , A , A і G є ті ж кращі значення, які зазначені для відповідних замісників сполуки формули (I). Крім того даний винахід відноситься до сполуки формули (III') O S N A A 10 15 20 1 A 4 (III') 2 A G 3 R 2 N Q 2 2 , у якій 1 2 3 4 2 2 2 A , A , A , A і G є такими, як це визначено для сполуки формули (I); R і Q є такими, як 1 визначено для сполуки формули (III); або його N-оксиду або солі. Кращими значеннями для A , 2 3 4 2 A , A , A і G є ті ж кращі значення, які зазначені для відповідних замісників сполуки формули 2 2 (I). Кращими значеннями для R і Q є ті ж кращі значення, які зазначені для відповідних замісників сполуки формули (III). Наведені нижче приклади ілюструють, але не обмежують даний винахід. Приклади одержання сполук: 1. Реакції типу (1) Приклад 1.1: Одержання 3-сульфініламінобензоїлхлорид O S NH2 N SOCl2 O O OH 25 Cl Тіонілхлорид (95,17 г, 0,8 моля) додавали до розчину 3-амінобензойної кислоти (27,43 г, 0,2 моля) у толуолі (250 мл). Реакційну суміш кип'ятили зі зворотним холодильником протягом 2 год. Надлишок тіонілхлориду й толуолу відганяли при зниженому тиску. Очищення залишку проводили за допомогою перегонки з колби в колбу при 167 °C у вакуумі (0,40 мбар) і одержували 3-сульфініламінобензоїлхлорид (29,6 г, вихід 73,4 %). Приклад 1.2: Одержання 3-сульфініламіно-4-бромбензоїлхлориду 10 UA 100862 C2 O NH2 S SOCl2 Br N Br O O OH 5 10 15 20 25 Cl Тіонілхлорид (4,4 г, 37 ммолей) додавали до розчину 3-аміно-4-бромбензойної кислоти (2 г, 9,25 ммоля) у толуолі (12 мл). Реакційну суміш кип'ятили зі зворотним холодильником протягом 2 год. Надлишок тіонілхлориду й толуолу відганяли при зниженому тиску. Очищення залишку проводили за допомогою перегонки з колби в колбу при 130 °C у вакуумі (0,40 мбар) і одержували 3-сульфініламіно-4-бромбензоїлхлорид (0,978 г, вихід 48,9 %). Приклад 1.3: Одержання 3-сульфініламіно-4-ціанобензоїлхлориду O S NH2 SOCl2 N NC NC O O OH Cl Тіонілхлорид (4,4 г, 37 ммолей) додавали до розчину 3-аміно-4-ціанобензойної кислоти (2,0 г, 9,25 ммоля) (приклад 6.1) у толуолі (12 мл). Реакційну суміш кип'ятили зі зворотним холодильником протягом 2 год. Надлишок тіонілхлориду й толуолу відганяли при зниженому тиску. Продукт використовували без додаткового очищення. 2. Реакції типу (2) Приклад 2.1: Одержання 3-сульфініламіно-N-[2-етил-6-метил-4-(1,2,2,2-тетрафтор-1трифторметилетил)-феніл]-бензаміду До розчину 3-сульфініламінобензоїлхлориду (0,033 г, 0,165 ммоля) (приклад 1.1) у сухому дейтерохлороформі (0,5 мл) при 25 °C при перемішуванні додавали розчин 2-етил-6-метил-4(1,2,2,2-тетрафтор-1-трифторметилетил)-феніламіну (0,050 г, 0,165 ммоля) (одержували відповідно до методики, описаної в EP 1,006,102) у дейтерохлороформі (0,5 мл). Після перемішування при 40 °C протягом 14 год. до реакційної суміші додавали піридин (0,013 г, 0,16 ммоля), потім суміш перемішували при 25 °C протягом 60 год. Аліквоту реакційної суміші розбавляли сухим ацетонітрилом і вводили у мас-спектрометр шляхом прямого упорскування (умови див. нижче). Розрахована точна маса: 468; [M-H] знайдена: 467,01. Мас-спектрометричний (МС) аналіз: пряме упорскування з використанням ацетонітрилу як розчинник. Швидкість потоку, що вводиться, становила 5 мкл/хв. Мас-спектрометричне детектування проводили на мас-спектрометрі Quattro Micro із трьома квадрупольними лінзами (Waters). 11 UA 100862 C2 Режим сканування: Методика МС: Режим іонізації: Напруга на капілярі: Напруга на конусі: Температура десольватації: Температура блоку джерела: Швидкість газу при десольватації: Швидкість газу на конусі: Діапазон сканування: Час сканування: Квадрупольне сканування Іонізація електророзпиленням (ІЕР) Позитивні іони Негативні іони 3,2 кВ 3,2 кВ 20 В 30 В 350 °C 350 °C 120 °C 120 °C 500 л/год. 500 л/год. 50 л/год. Не використовується від 100 до 1000 Да від 100 до 1000 Да 0,5 с 0,5 с Приклад 2.2: Альтернативна методика одержання 3-сульфініламіно-N-[2-етил-6-метил-4(1,2,2,2-тетрафтор-1-трифторметилетил)-феніл]-бензаміду O S CH 3 N H 2N O S CF3 N CH 3 O F CF3 CH3 HN O CF3 Cl 5 10 15 20 CH3 F CF3 До розчину 3-сульфініламінобензоїлхлориду (0,033 г, 0,165 ммоля) (приклад 1.1) у сухому дейтерохлороформі (0,5 мл) при 25 °C при перемішуванні додавали розчин 2-етил-6-метил-4(1,2,2,2-тетрафтор-1-трифторметилетил)-феніламіну (0,050 г, 0,165 ммоля) (одержували відповідно до методики, описаної в EP 1,006,102) у дейтерохлороформі (0,5 мл). Після перемішування при 25 °C протягом 60 год. зразок реакційної суміші аналізували за допомогою 1 спектроскопії H-ЯМР. У реакційній суміші виявляли шукану сполуку й не прореагувавші вихідні 1 речовини. Інтегрування сигналів показувало, що перетворення пройшло на 40 %. H-ЯМР (CDCl3, 400 МГц): 8,35 (s, 1H), 8,07 (d, 1H), 7,95 (d, 1H) 7,58 (t, 1H), 7,49 (s, 1H), 7,37 (s, 2H), 2,70 (q, 2H), 2,31 (s, 3H), 1,22 (t, 3H) част./млн. Приклад 2.3: Альтернативна методика одержання 3-сульфініламіно-N-[2-етил-6-метил-4(1,2,2,2-тетрафтор-1-трифторметилетил)-феніл]-бензаміду До розчину 2-етил-6-метил-4-(1,2,2,2-тетрафтор-1-трифторметилетил)-феніламіну (0,100 г, 0,33 ммоля) (одержували відповідно до методики, описаної в EP 1,006,102) у дейтерохлороформі (1,0 мл) при 25 °C при перемішуванні додавали розчин 3сульфініламінобензоїлхлориду (0,033 г, 0,165 ммоля) (приклад 1.1) у сухому дейтерохлороформі (1,0 мл). Після перемішування при 40 °C протягом 8 год. зразок реакційної 1 суміші аналізували за допомогою спектроскопії H-ЯМР. У реакційній суміші виявляли шукану 1 сполуку на підставі його характеристичних сигналів (див. дані спектрів H-ЯМР, наведені у 12 UA 100862 C2 5 прикладі 2.2) і не прореагувавші вихідні речовини. Інтегрування сигналів показувало, що перетворення пройшло на 85 %. Аліквоту реакційної суміші розбавляли сухим ацетонітрилом і вводили у мас-спектрометр шляхом прямого упорскування (при умовах, аналогічних описаним у прикладі 2.1). Розрахована точна маса: 468; [M-H] знайдена: 467,06. Приклад 2.4: Альтернативна методика одержання 3-сульфініламіно-N-[2-етил-6-метил-4(1,2,2,2-тетрафтор-1-трифторметилетил)-феніл]-бензаміду O S CH3 N H2N O CF3 S N CH3 O F CF3 CH3 HN O K2CO3 CF3 Cl 10 15 20 25 30 CH3 F CF3 До суспензії 2-етил-6-метил-4-(1,2,2,2-тетрафтор-1-трифторметилетил)-феніламіну (0,082 г, 0,27 ммоля) (одержували відповідно до методики, описаної в EP 1,006,102) і тонкоподрібненого карбонату калію (0,112 г, 0,81 ммоля) у дейтерохлороформі (1,0 мл) при 25 °C при перемішуванні додавали 3-сульфініламінобензоїлхлорид (0,055 г, 0,27 ммоля) (приклад 1.1), розчинений у сухому дейтерохлороформі (1,0 мл). Реакційну суміш перемішували при 40 °C 1 протягом 16 год. Зразок надосадової рідини аналізували за допомогою спектроскопії H-ЯМР. У реакційній суміші виявляли шукану сполуку на підставі його характеристичних сигналів (див. 1 дані спектрів H-ЯМР, наведені у прикладі 2.2) і не прореагувавші вихідні речовини. Аліквоту реакційної суміші розбавляли сухим ацетонітрилом і вводили у мас-спектрометр шляхом прямого упорскування (при умовах, аналогічних описаним у прикладі 2.1). Розрахована точна маса: 468; [M-H] знайдена: 467,00. 3. Реакції типу (3) Приклад 3.1: Одержання 3-аміно-N-[2-етил-6-метил-4-(1,2,2,2-тетрафтор-1трифторметилетил)-феніл]-бензаміду Розчин 3-сульфініламіно-N-[2-етил-6-метил-4-(1,2,2,2-тетрафтор-1-трифторметилетил)феніл]-бензаміду (0,111 г, 0,237 ммоля) (наприклад, приклад 2.1) у дихлорметані (2 мл) і тетрагідрофурані (2 мл) обробляли 2 н. водяним розчином хлористоводневої кислоти (1 мл) і перемішували при 25 °C протягом 30 хв. Органічні розчинники видаляли з реакційної суміші при зниженому тиску. Залишок нейтралізували насиченим водяним розчином гідрокарбонату натрію й екстрагували дихлорметаном. Органічну фазу сушили над сульфатом натрію й випарювали й 1 одержували шукану сполуку. H-ЯМР (CDCl3, 400 МГц): 7,44 (s, 1H), 7,38 (s, 2H), 7,30-7,20 (m, 3H), 6,89 (d, 1H), 3,85 (bs, 2H), 2,69 (q, 2H), 2,32 (s, 3H), 1,22 (t, 3H) част./млн. 4. Реакції типу (4) Приклад 4.1: Альтернативна методика одержання 3-аміно-N-[2-етил-6-метил-4-(1,2,2,2тетрафтор-1-трифторметилетил)-феніл]-бензаміду 13 UA 100862 C2 5 10 15 20 25 30 До розчину 2-етил-6-метил-4-(1,2,2,2-тетрафтор-1-трифторметилетил)-феніламіну (2,09 г, 6,9 ммоля) (одержували відповідно до методики, описаної в EP 1,006,102) у дихлорметані (30 мл) при 25 °C при перемішуванні послідовно додавали піридин (0,8 мол, 9,9 ммоля) і розчин 3сульфініламінобензоїлхлориду (1,39 г, 6,9 ммоля) (приклад 1.1) у дихлорметані (7 мл). Реакційну суміш перемішували при температурі навколишнього середовища протягом 6 год. Реакцію зупиняли шляхом додавання 2 н. водяного розчину хлористоводневої кислоти (4 мл) і суміш енергійно перемішували протягом 20 хв. Суміш розбавляли водою (20 мл) і фази розділяли. Водну фазу двічі екстрагували етилацетатом. Об'єднані органічні фази послідовно промивали насиченим водяним розчином гідрокарбонату натрію й розсолом, сушили над сульфатом натрію й концентрували. Залишок очищали за допомогою колоночної хроматографії на силікагелі (елюент: етилацетат/циклогексан від 1:4 до 3:2). Після випарювання розчинників жовте масло розтирали з гексаном і при цьому воно кристалізувалося. Шукану сполуку виділяли 1 у вигляді білих кристалів. Т. пл. (температура плавлення): 143-145 °C. Дані H-ЯМР збігаються з наведеними у прикладі 3.1. Приклад 4.2: Одержання 3-аміно-N-[2-метил-4-(1,2,2,2-тетрафтор-1-трифторметилетил)-6тіоціанатофеніл]-бензаміду До розчину 2-метил-4-(1,2,2,2-тетрафтор-1-трифторметилетил)-6-тіоціанатофеніламіну (3,00 г, 9,05 ммоля) (приклад 6.2) у безводному дихлорметані (80 мл) при 20 °C послідовно додавали розчин 3-сульфініламінобензоїлхлориду (2,74 г, 13,58 ммоля) (приклад 1.1) у безводному дихлорметані (10 мл) і розчин піридину (2,15 г, 27,15 ммоля) у безводному дихлорметані (10 мл). Реакційну суміш перемішували при температурі навколишнього середовища протягом 1 год. Реакцію зупиняли шляхом додавання води (50 мл). Після поділу фаз водний шар екстрагували дихлорметаном. Об'єднані органічні фази сушили над сульфатом натрію й концентрували. Залишок очищали за допомогою колоночної хроматографії на силікагелі (елюент: етилацетат/циклогексан 2:3) і одержували 3-аміно-N-[2-метил-4-(1,2,2,2-тетрафтор-11 трифторметилетил)-6-тіоціанатофеніл]-бензамід (2,3 г, вихід 56,3 %). H-ЯМР (CDCl3, 400 МГц): 7,95 (s, 1H), 7,45 (s, 1H), 7,29-7,28 (m, 3H), 6,92 (m, 1H), 5,73 (s, 2H), 2,59 (s, 6H) част./млн. Приклад 4.3: Одержання 3-аміно-4-бром-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1трифторметилетил)-феніл]-бензаміду 14 UA 100862 C2 5 10 15 20 25 30 До розчину 2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилетил)-феніламіну (0,31 г, 1,1 ммоля) (одержували відповідно до методики, описаної в EP 1,006,102) у безводному тетрагідрофурані (2 мл) при 20 °C послідовно додавали піридин (0,174 г, 2,2 ммоля) і розчин 3сульфініламінобензоїлхлориду (0,25 г, 0,86 ммоля) (приклад 1.2) у безводному тетрагідрофурані (2 мл). Реакційну суміш перемішували при температурі навколишнього середовища протягом 3 год. Реакцію зупиняли шляхом додавання води (5 мл). Після поділу фаз водний шар екстрагували етилацетатом. Об'єднані органічні фази сушили над сульфатом натрію й концентрували. Залишок очищали за допомогою колоночної хроматографії на силікагелі (елюент: етилацетат/циклогексан 1:3) і одержували 3-аміно-4-бром-N-[2,6-диметил-41 (1,2,2,2-тетрафтор-1-трифторметилетил)-феніл]-бензамід (0,235 г, вихід 78 %). H-ЯМР (ДМСОd6 (диметилсульфоксид), 400 МГц): 7,53 (d, 1H), 7,44 (s, 2H), 7,38 (d, 1H), 7,10 (q, 1H), 5,6 (s, 2H), 2,24 (s, 6H) част./млн. Приклад 4.4: Одержання 3-аміно-4-бром-N-[2,6-дихлор-4-(1,2,2,2-тетрафтор-1трифторметилетил)-феніл]-бензаміду До розчину 2,6-дихлор-4-(1,2,2,2-тетрафтор-1-трифторметилетил)-феніламіну (1,02 г, 3,1 ммоля) (приклад 6.3) у безводному дихлорметані (25 мл) при 20 °C послідовно додавали піридин (0,74 г, 2,0 ммоля) і 3-сульфініламінобензоїлхлорид (0,94 г, 9,30 ммоля) (приклад 1.2). Реакційну суміш перемішували при температурі навколишнього середовища протягом 1 год. Потім реакційну суміш нагрівали при 50 °C протягом 16 год. Реакційній суміші давали остудитися до температури навколишнього середовища й потім додавали диметилформамід (50 мл). Дихлорметан відганяли й реакційну суміш нагрівали при 130 °C протягом 16 год. Реакцію зупиняли шляхом додавання насиченого водяного розчину гідрокарбонату натрію (10 мл). Після поділу фаз водний шар екстрагували етилацетатом. Об'єднані органічні фази сушили над сульфатом натрію й концентрували. Залишок очищали за допомогою колоночної хроматографії на силікагелі (елюент: етилацетат/циклогексан від 1:5 до 1:0) і одержували 3аміно-4-бром-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилетил)-феніл]-бензамід 1 (кількісний вихід, 100 %). H-ЯМР (CDCl3, 400 МГц): 7,73 (m, 3H), 7,27 (m, 3H), 6,91 (m, 1H), 3,9 (s, 2H) част./млн. Приклад 4.5: Одержання 3-аміно-4-ціано-N-[2,6-диметил-4-(1,2,2,2-тетрафтор-1трифторметилетил)-феніл]-бензаміду 15 UA 100862 C2 5 10 До розчину 2,6-диметил-4-(1,2,2,2-тетрафтор-1-трифторметилетил)-феніламіну (0,19 г, 0,69 ммоля) (одержували відповідно до методики, описаної в EP 1,006,102) у тетрагідрофурані (3 мл) при 20 °C послідовно додавали піридин (0,145 г, 1,84 ммоля) і розчин 3-сульфініламіно-4ціанобензоїлхлориду (0,150 г, 0,92 ммоля) (приклад 1.3). Через 2 год. реакцію зупиняли шляхом додавання суміші насиченого водяного розчину гідрокарбонату калію й води (1:1, 10 мл). Після поділу фаз водний шар екстрагували етилацетатом. Органічні фази сушили над сульфатом натрію й концентрували. Залишок очищали за допомогою колоночної хроматографії на силікагелі (елюент: етилацетат/циклогексан від 1:1 до 1:0) і одержували 3-аміно-4-ціано-N-[2,61 диметил-4-(1,2,2,2-тетрафтор-1-трифторметилетил)-феніл]-бензамід (0,049 г, вихід 16,4 %). HЯМР (CDCl3, 400 МГц): 7,54 (s, 1H), 7,49 (d, 2H), 7,36 (m, 3H), 7,15 (q, 1H), 2,3 (s, 6H) част./млн. 5. Реакції типу (5) Приклад 5.1: Альтернативна методика одержання 3-сульфініламіно-N-[2-етил-6-метил-4(1,2,2,2-тетрафтор-1-трифторметилетил)-феніл]-бензаміду O S NH2 N O SOCl2 CH3 O HN HN CF3 15 20 25 CF3 F CH3 CF3 CH3 F CF3 Суспензію 3-аміно-N-[2-етил-6-метил-4-(1,2,2,2-тетрафтор-1-трифторметилетил)-феніл]бензаміду (0,100 г, 0,237 ммоля) (приклад 4.1) у тетрахлориді вуглецю (1 мл) нагрівали при 50 °C до одержання прозорого розчину. Додавали розчин тіонілхлориду у тетрахлориді вуглецю (1,68 M) (0,725 мл, 1,218 ммоля) і суміш нагрівали при 80 °C протягом 1 год. Реакційну суміш випарювали при зниженому тиску й залишок розтирали із циклогексаном. Суспензію фільтрували й тверду речовину сушили у високому вакуумі. Шукану сполуку одержували у 1 вигляді білих кристалів. Т. пл.: 100-108 °C. Дані H-ЯМР збігаються з наведеними у прикладі 2.2. Мас-спектрометричний аналіз: умови, аналогічні описаним у прикладі 2.1. Розрахована точна маса: 468; [M-H] знайдена: 467,06. 6. Синтез проміжних продуктів Приклад 6.1: Одержання 3-аміно-4-ціанобензойної кислоти NH2 NH2 Br ZnCN NC Pd(PPh3)4 O O OH 30 CH3 OH До розчину 3-аміно-4-бромбензойної кислоти (6,0 г, 276 ммолей) у диметилформаміді (30 мл) при температурі навколишнього середовища послідовно додавали ціанід цинку (11,66 г, 99,4 ммоля) і тетракіс(трифенілфосфін)паладій (9,57 г, 8,28 ммоля). Суміш нагрівали при 100 °C 16 UA 100862 C2 5 10 протягом 14 год. Реакційній суміші давали остудитися до температури навколишнього середовища, потім при температурі навколишнього середовища послідовно додавали додаткову кількість ціаніду цинку (0,65 г, 5,54 ммоля) і тетракіс(трифенілфосфін)паладію (1,9 г, 1,64 ммоля). Суміш нагрівали при 100 °C протягом ще 1 год. Реакційній суміші давали остудитися до температури навколишнього середовища й реакцію зупиняли шляхом додавання суміші толуолу й водяного розчину аміаку (1M). Фази розділяли й водний шар екстрагували толуолом. Об'єднані органічні фази сушили над сульфатом натрію й концентрували. Залишок очищали за допомогою колоночної хроматографії на силікагелі (елюент: етилацетат/циклогексан від 1:2 до 1:0) і одержували 3-аміно-4-ціанобензойну кислоту (2,94 г, вихід 67 %). Приклад 6.2: Одержання 2-метил-4-(1,2,2,2-тетрафтор-1-трифторметилетил)-6тіоціанатофеніламіну CH3 CH3 H2N Br2, KSCN HN 2 CF3 S F CF3 15 20 25 N Cl F CF3 35 F CF3 До розчину 2-метил-4-(1,2,2,2-тетрафтор-1-трифторметилетил)-феніламіну (5,0 г, 18,20 ммоля) (одержували відповідно до методики, описаної в EP 1,006,102) в оцтовій кислоті (30 мл) додавали розчин тіоціанату калію (7,25 г, 74,62 ммоля) в оцтовій кислоті (20 мл). Розчин охолоджували до 5 °C, потім додавали бром (3,2 г, 1,03 мол) в оцтовій кислоті (10 мл). Реакційній суміші давали нагрітися до температури навколишнього середовища й перемішували при температурі навколишнього середовища протягом 3 год. Реакцію зупиняли, виливаючи суміш у воду. Суміш екстрагували етилацетатом (3100 мл). Об'єднані органічні екстракти послідовно промивали водяним розчином гідроксиду натрію (10 г/л, 100 мл), водою (100 мл) і розсолом (100 мл), сушили над сульфатом натрію й концентрували. Залишок очищали за допомогою колоночної хроматографії на силікагелі (елюент: етилацетат/циклогексан 1:3) і одержували 2-метил-4-(1,2,2,2-тетрафтор-1-трифторметилетил)1 6-тіоціанатофеніламін (3,7 г, вихід 61,2 %). H-ЯМР (CDCl3, 400 МГц): 7,68 (s, 1H), 7,33 (s, 1H), 5,73 (s, 2H), 2,59 (s, 6H) част./млн. Приклад 6.3: Одержання 2,6-дихлор-4-(1,2,2,2-тетрафтор-1-трифторметилетил)-феніламіну Cl H2N H2N NCS CF3 30 CF3 CF3 F CF3 До розчину 4-(1,2,2,2-тетрафтор-1-трифторметилетил)-феніламіну (10 г, 38,30 ммоля) (одержували відповідно до методики, описаної в EP 1,006,102) у дихлорметані (150 мл) при 20 °C додавали N-хлорсукцинімід ("NCS") (21,48 г, 160,8 ммоля). Реакційну суміш перемішували при температурі навколишнього середовища протягом ночі. Реакцію зупиняли шляхом додавання 2 н. водяного розчину гідроксиду натрію й фази розділяли. Водний шар екстрагували дихлорметаном. Об'єднані органічні фази сушили над сульфатом натрію й концентрували. Залишок очищали за допомогою колоночної хроматографії на силікагелі (елюент: етилацетат/циклогексан 1:4) і одержували 2,6-дихлор-4-(1,2,2,2-тетрафтор-11 трифторметилетил)-феніламін (7,6 г, вихід 60,1 %). H-ЯМР (CDCl3, 400 МГц): 7,41 (s, 2H), 4,77 (s, 2H) част./млн. 17 UA 100862 C2 ФОРМУЛА ВИНАХОДУ 1. Застосування сполуки формули (І) NH2 A A 5 1 2 A A 4 G 3 2 OH , (I) 3 4 2 у якій А , А , А , А і G є такими, як визначено нижче для сполуки формули (IV), або її N-оксиду або солі як проміжного продукту для одержання сполуки формули (IV) 1 2 NH2 A 1 A 2 A A G 3 R 10 15 4 2 N 2 2 Q , (IV) у якій 1 2 3 4 3 А , А , А і А незалежно один від одного означають C-R або азот, за умови, що не більше двох 1 2 3 4 з А , А , А і А означають азот; 2 R означає водень, С1-С4-алкіл або С1-С4-алкілкарбоніл; 2 G означає кисень або сірку: 3 кожний R незалежно означає водень, галоген, ціаногрупу, нітрогрупу, С 1-С4-алкіл, С1-С4галогеналкіл, гідроксигрупу, С1-С4-алкоксигрупу, С1-С4-галогеналкоксигрупу, тіогрупу, С1-С4алкілтіогрупу, С1-С4-галогеналкілтіогрупу, С1-С4-алкілсульфініл, С1-С4-галогеналкілсульфініл, С1С4-алкілсульфоніл, С1-С4-галогеналкілсульфоніл, аміногрупу, N-С1-С4-алкіламіногрупу або N-ді(С1-С4-алкіл)аміногрупу; і 2 Q означає фрагмент формули (А) або (В) Y 1 Y 2 Y 6 Y Y 20 25 30 35 5 Y Y 7 3 4 , (A) Y 9 N Y8 , (B) у якій 1 5 Y і Y незалежно один від одного означають галоген, ціаногрупу, тіоціанатну групу, С 1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкоксі-С1-С4-алкіл, ціано-С1-С4-алкіл, С1-С3-алкілтіогрупу, С1-С3галогеналкілтіогрупу, С1-С3-алкілсульфініл, С1-С3-галогеналкілсульфініл, С1-С3-алкілсульфоніл або С1-С3-галогеналкілсульфоніл; 3 Y означає С2-С6-перфторалкіл, С1-С6-перфторалкілтіогрупу, С1-С6-перфторалкілсульфініл або С1-С6-перфторалкілсульфоніл; 2 4 Y і Y незалежно один від одного означають водень, галоген або С1-С4-алкіл; 6 9 Y і Y незалежно один від одного означають галоген, ціаногрупу, тіоціанатну групу, С 1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкоксі-С1-С4-алкіл, ціано-С1-С4-алкіл, С1-С3-алкілтіогрупу, С1-С3галогеналкілтіогрупу, С1-С3-алкілсульфініл, С1-С3-галогеналкілсульфініл, С1-С3-алкілсульфоніл або С1-С3-галогеналкілсульфоніл; 8 Y означає С1-С4-галогеналкоксигрупу, С2-С6-перфторалкіл, С1-С6-перфторалкілтіогрупу, С1-С6перфторалкілсульфініл або С1-С6-перфторалкілсульфоніл; 7 Y означає водень, галоген або С1-С4-алкіл; або її N-оксиду або солі. 2. Застосування сполуки формули (ІІ) 18 UA 100862 C2 O S N A 1 A 2 A A 4 G 3 2 Cl , (II) 3 4 2 у якій А , А , А , А і G є такими, як визначено нижче для сполуки формули (IV); або її N-оксиду або солі як проміжного продукту для одержання сполуки формули (IV) 1 2 NH2 A 1 A 2 A A G 3 R 5 10 15 4 2 N 2 2 Q , (IV) у якій 1 2 3 4 3 А , А , А і А незалежно один від одного означають C-R або азот, за умови, що не більше двох 1 2 3 4 з А , А , А і А означають азот; 2 R означає водень, С1-С4-алкіл або С1-С4-алкілкарбоніл; 2 G означає кисень або сірку: 3 кожний R незалежно означає водень, галоген, ціаногрупу, нітрогрупу, С 1-С4-алкіл, С1-С4галогеналкіл, гідроксигрупу, С1-С4-алкоксигрупу, С1-С4-галогеналкоксигрупу, тіогрупу, С1-С4алкілтіогрупу, С1-С4-галогеналкілтіогрупу, С1-С4-алкілсульфініл, С1-С4-галогеналкілсульфініл, С1С4-алкілсульфоніл, С1-С4-галогеналкілсульфоніл, аміногрупу, N-С1-С4-алкіламіногрупу або N-ді(С1-С4-алкіл)аміногрупу; і 2 Q означає фрагмент формули (А) або (В) Y 1 Y 2 Y 6 Y Y 5 Y Y 20 25 30 7 3 4 , (A) Y 9 N Y8 , (B) у якій 1 5 Y і Y незалежно один від одного означають галоген, ціаногрупу, тіоціанатну групу, С 1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкоксі-С1-С4-алкіл, ціано-С1-С4-алкіл, С1-С3-алкілтіогрупу, С1-С3галогеналкілтіогрупу, С1-С3-алкілсульфініл, С1-С3-галогеналкілсульфініл, С1-С3-алкілсульфоніл або С1-С3-галогеналкілсульфоніл; 3 Y означає С2-С6-перфторалкіл, С1-С6-перфторалкілтіогрупу, С1-С6перфторалкілсульфініл або С1-С6-перфторалкілсульфоніл; 2 4 Y і Y незалежно один від одного означають водень, галоген або С1-С4-алкіл; 6 9 Y і Y незалежно один від одного означають галоген, ціаногрупу, тіоціанатну групу, С 1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкоксі-С1-С4-алкіл, ціано-С1-С4-алкіл, С1-С3-алкілтіогрупу, С1-С3галогеналкілтіогрупу, С1-С3-алкілсульфініл, С1-С3-галогеналкілсульфініл, С1-С3-алкілсульфоніл або С1-С3-галогеналкілсульфоніл; 8 Y означає С1-С4-галогеналкоксигрупу, С2-С6-перфторалкіл, С1-С6-перфторалкілтіогрупу, С1-С6перфторалкілсульфініл або С1-С6-перфторалкілсульфоніл; 7 Y означає водень, галоген або С1-С4-алкіл; або її N-оксиду або солі. 3. Застосування сполуки формули (ІІІ) 19 UA 100862 C2 O S N A 1 A 2 A A 4 G R 2 2 Q 3 2 N , (III) 4 2 2 у якій А , А , А , А , G і Q є такими, як визначено нижче для сполуки формули (IV); або її Nоксиду або солі як проміжного продукту для одержання сполуки формули (IV) 1 2 3 NH2 A 1 A 2 A A G 3 R 5 10 15 4 2 N 2 2 Q , (IV) у якій 1 2 3 4 3 А , А , А і А незалежно один від одного означають C-R або азот, за умови, що не більше двох 1 2 3 4 з А , А , А і А означають азот; 2 R означає водень, С1-С4-алкіл або С1-С4-алкілкарбоніл; 2 G означає кисень або сірку; 3 кожний R незалежно означає водень, галоген, ціаногрупу, нітрогрупу, С 1-С4-алкіл, С1-С4галогеналкіл, гідроксигрупу, С1-С4-алкоксигрупу, С1-С4-галогеналкоксигрупу, тіогрупу, С1-С4алкілтіогрупу, С1-С4-галогеналкілтіогрупу, С1-С4-алкілсульфініл, С1-С4-галогеналкілсульфініл, С1С4-алкілсульфоніл, С1-С4-галогеналкілсульфоніл, аміногрупу, N-С1-С4-алкіламіногрупу або N-ді(С1-С4-алкіл)аміногрупу; і 2 Q означає фрагмент формули (А) або (В) Y 1 Y 2 Y 6 Y Y 5 Y Y 20 25 30 7 3 4 , (A) Y 9 N Y8 , (B) у якій 1 5 Y і Y незалежно один від одного означають галоген, ціаногрупу, тіоціанатну групу, С 1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкоксі-С1-С4-алкіл, ціано-С1-С4-алкіл, С1-С3-алкілтіогрупу, С1-С3галогеналкілтіогрупу, С1-С3-алкілсульфініл, С1-С3-галогеналкілсульфініл, С1-С3-алкілсульфоніл або С1-С3-галогеналкілсульфоніл; 3 Y означає С2-С6-перфторалкіл, С1-С6-перфторалкілтіогрупу, С1-С6-перфторалкілсульфініл або С1-С6-перфторалкілсульфоніл; 2 4 Y і Y незалежно один від одного означають водень, галоген або С1-С4-алкіл; 6 9 Y і Y незалежно один від одного означають галоген, ціаногрупу, тіоціанатну групу, С 1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкоксі-С1-С4-алкіл, ціано-С1-С4-алкіл, С1-С3-алкілтіогрупу, С1-С3галогеналкілтіогрупу, С1-С3-алкілсульфініл, С1-С3-галогеналкілсульфініл, С1-С3-алкілсульфоніл або С1-С3-галогеналкілсульфоніл; 8 Y означає С1-С4-галогеналкоксигрупу, С2-С6-перфторалкіл, С1-С6-перфторалкілтіогрупу, С1-С6перфторалкілсульфініл або С1-С6-перфторалкілсульфоніл; 7 Y означає водень, галоген або С1-С4-алкіл; або її N-оксиду або солі. 4. Спосіб одержання сполуки формули (III) 20 UA 100862 C2 O S N A 1 A 2 A A 4 G 2 Q 2 3 R 2 N , (III) 4 2 2 у якій А , А , А , А , G і Q є такими, як визначено у п. 1, шляхом обробки сполуки формули (II) 1 2 3 O S N A 1 A 2 A A 4 G 3 2 Cl 5 , (II) 3 4 2 у якій А , А , А , А і G є такими, як визначено у п. 1, 2 2 2 2 аміном формули HNR Q , у якій R і Q є такими, як визначено у п. 1, у лужному середовищі. 5. Спосіб одержання сполуки формули (IV) 1 2 NH2 A 1 A 2 A A 4 G 3 R 2 1 10 N 2 2 2 3 Q , (IV) 4 2 2 2 у якій А , А , А , А , R , G і Q є такими, як визначено у п. 1, шляхом обробки сполуки формули (III) O S N A 1 A 2 A A 4 G 2 Q 2 3 R 2 N , (III) 4 2 2 у якій А , А , А , А , G і Q є такими, як визначено у п. 1, водою. 6. Спосіб одержання сполуки формули (IV) 1 2 3 21 UA 100862 C2 NH2 A 1 A 2 A A 4 G 3 R 2 1 N 2 2 2 3 Q , (IV) 4 2 2 2 у якій А , А , А , А , R , G і Q є такими, як визначено у п. 1, шляхом обробки сполуки формули (II) O S N A 1 A 2 A A 4 G 3 2 Cl 5 , (II) 3 4 2 у якій А , А , А , А і G є такими, як визначено у п. 1, 2 2 2 2 аміном формули HNR Q , у якій R і Q є такими, як визначено у п. 1, у лужному середовищі, з наступною обробкою проміжного продукту водою. 7. Сполука формули (ІI) 1 2 O S N A 1 A 2 A A 4 G 3 2 Cl 10 15 , (ІI) 2 3 4 2 у якій А , А , А , А і G є такими, як визначено у п. 1; або її N-оксид або сіль, за умови, що сполука формули (ІI) не являє собою 2-хлор-5-сульфініламінобензоїлхлорид, 4-метокси-3сульфініламінобензоїлхлорид, 4-метил-3-сульфініламінобензоїлхлорид, 3сульфініламінобензоїлхлорид, 2,3,4,6-тетрайод-5-сульфініламінобензоїлхлорид або 2,4,6трийод-3-сульфініламінобензоїлхлорид. 8. Сполука формули (ІIІ) 1 O S N A 1 A 2 A A 4 G 3 R 2 2 Q 2 N , (ІIІ) 1 2 3 4 2 2 у якій А , А , А , А , G і Q є такими, як визначено у п. 1; або її N-оксид або сіль. 22 UA 100862 C2 Комп’ютерна верстка М. Мацело Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 23
ДивитисяДодаткова інформація
Назва патенту англійськоюHexatomic aromatic compounds, preparation and use thereof
Автори англійськоюStoller, Andre, Denis, Jung, Pierre, Joseph, Marcel, Godfrey, Christopher, Richard, Ayles, Maienfisch, Peter, Zambach, Werner
Назва патенту російськоюШестичленные ароматические соединения, их получение и применение (варианты)
Автори російськоюШтоллер Андре Денис, Юнг Пьер Жозеф Марсель, Годфри Кристофер Ричард Айлес, Майэнфиш Петер, Цамбах Вернер
МПК / Мітки
МПК: C07C 253/30, C07C 255/58, C07C 231/02, C07C 331/00, C07C 381/00, C07C 237/40
Мітки: шестичленні, одержання, варіанти, застосування, ароматичні, сполуки
Код посилання
<a href="https://ua.patents.su/25-100862-shestichlenni-aromatichni-spoluki-kh-oderzhannya-ta-zastosuvannya-varianti.html" target="_blank" rel="follow" title="База патентів України">Шестичленні ароматичні сполуки, їх одержання та застосування (варіанти)</a>
Попередній патент: Транспортний засіб для внесення лужних речовин у водойми
Наступний патент: Протиударна вставка для прийняття і розподілення потоку розплавленого металу та розливний пристрій
Випадковий патент: Заміщені анілінові піперидини як селективні антагоністи mch












