Сперміцидна та/або протигрибкова композиція та способи її застосування
Номер патенту: 82864
Опубліковано: 26.05.2008
Автори: Наварро Гернан А., Томас Брайєн Фрезіер, Кук Кларенс Едгар, Слоун Керол Делта
Формула / Реферат
1.Спосіб знищення рухливих сперматозоїдів, у якому:
суміш, що містить сперматозоїди, приводять у взаємодію зі сперміцидною композицією, що містить сполуку формули І(а):
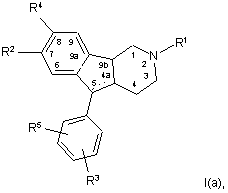
у якій
R1 являє собою атом водню, лінійний або розгалужений С1-6 алкіл або С3-C8 циклоалкіл;
R2 являє собою атом водню, лінійний або розгалужений С1-6 алкіл;
R3 та R5 кожний незалежно являє собою атом водню, SO3H, лінійний або розгалужений С1-6 алкіл, СН2ОН, СН2ОМе, лінійну або розгалужену C1-6 алкоксигрупу, карбоксил (СООН), не складноефірну групу, яка може бути перетворена у фізіологічних умовах ссавця в карбоксильну групу, складноефірну карбоксильну групу (COOR, де R являє собою С1-10 алкіл, C6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну групу (CH2OC(O)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 і галоген; та
R4 являє собою атом водню, галоген, R3Si або COR.
2. Спосіб за пунктом 1, який відрізняється тим, що сполука являє собою сполуку формули І(b):
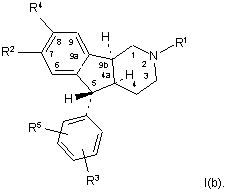
3. Спосіб за пунктом 1, який відрізняється тим, що R1 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, н-пентил, ізопентил, н-гексил, ізогексил, циклопропіл, циклопентан та циклогексил;
R2 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, н-пентил, ізопентил, н-гексил та ізогексил;
R3 знаходиться у 4 положенні і вибраний з групи, яка включає водень, SO3H, лінійний або розгалужений С1-6 алкіл, СН2ОН, СН2ОМе, лінійну або розгалужену С1-6 алкоксигрупу, карбоксил (СООН), не складноефірну групу, яка може бути перетворена у фізіологічних умовах ссавця в карбоксильну групу, гідроксиметильну групу (СН2ОН), формільну груп (СНО), карбоксил (СООН), складноефірну карбоксильну групу (COOR, де R являє собою С1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну групу (СН2OC(O)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 та галоген;
R5 являє собою водень; та
R4 вибраний з групи, яка включає водень і галоген.
4. Спосіб за пунктом 3, який відрізняється тим, що R1 являє собою метил, етил, н-пропіл або ізопропіл;
R2 являє собою метил, етил, н-пропіл або ізопропіл;
R3 являє собою 4-СООН або 4-COOR, де R приймає значення, вказані вище;
R5 являє собою водень; та
R4 являє собою галоген.
5. Сперміцидна композиція, що містить ефективну сперміцидну дозу сполуки формули І(а):

у якій
R1 являє собою атом водню, лінійний або розгалужений C1-6 алкіл або С3-C8 циклоалкіл;
R2 являє собою атом водню, лінійний або розгалужений С1-6 алкіл;
R3 та R5 кожний незалежно являє собою атом водню, SO3H, лінійний або розгалужений С1-6 алкіл, СН2ОН, СН2ОМе, лінійну або розгалужену С1-6 алкоксигрупу, карбоксил (СООН), не складноефірну групу, яка може бути перетворена у фізіологічних умовах ссавця в карбоксильну групу, складноефірну карбоксильну групу (COOR, де R являє собою С1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну групу (CH2OC(O)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 і галоген; та
R4 являє собою атом водню, галоген, R3Si або COR,
та прийнятний носій.
6. Сперміцидна композиція за пунктом 5, яка відрізняється тим, що композиція представлена у формі, вибраній з групи, яка включає гелі, желе, креми, піни, мазі та бальзами.
7. Сперміцидна композиція за пунктом 5, яка відрізняється тим, що сполука являє собою сполуку формули І(b):

8. Сперміцидна композиція за пунктом 5, яка відрізняється тим, що
R1 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, н-пентил, ізопентил, н-гексил, ізогексил, циклопропіл, циклопентил та циклогексил;
R2 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, н-пентил, ізопентил, н-гексил та ізогексил;
R3 знаходиться у 4 положенні і вибраний з групи, яка включає водень, SO3H, лінійний або розгалужений С1-6 алкіл, СН2ОН, СН2ОМе, лінійну або розгалужену С1-6 алкоксигрупу, карбоксил (СООН), не складноефірну групу, яка може бути перетворена у фізіологічних умовах ссавця в карбоксильну групу, гідроксиметильну групу (СН2ОН), формільну групу (СНО), карбоксил (СООН), складноефірну карбоксильну групу (COOR, де R являє собою С1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну групу (CH2OC(O)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 та галоген;
R5 являє собою водень; та
R4 вибраний з групи, яка включає водень і галоген.
9. Сперміцидна композиція за пунктом 8, яка відрізняється тим, що
R1 являє собою метил, етил, н-пропіл або ізопропіл;
R2 являє собою метил, етил, н-пропіл або ізопропіл;
R3 являє собою 4-СООН або 4-COOR, де R приймає значення, вказані вище;
R5 являє собою водень; та
R4 являє собою галоген.
10. Сперміцидно оброблений пристрій для контрацепції, що включає: ефективну сперміцидну дозу сполуки формули І(а):

у якій
R1 являє собою атом водню, лінійний або розгалужений C1-6 алкіл або С3-С8 циклоалкіл;
R2 являє собою атом водню, лінійний або розгалужений С1-6 алкіл;
R3 та R5 кожний незалежно являє собою атом водню, SO3H, лінійний або розгалужений С1-6 алкіл, СН2ОН, СН2ОМе, лінійну або розгалужену С1-6 алкоксигрупу, карбоксил (СООН), не складноефірну групу, яка може бути перетворена у фізіологічних умовах ссавця в карбоксильну групу, складноефірну карбоксильну групу (COOR, де R являє собою С1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну групу (CH2OC(O)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 і галоген; та
R4 являє собою атом водню, галоген, R3Si або COR,
та прийнятний носій; і
бар'єрний пристрій для контрацепції.
11. Сперміцидно оброблений пристрій для контрацепції за пунктом 10, який відрізняється тим, що сполука являє собою сполуку формули І(b):

12. Сперміцидно оброблений пристрій для контрацепції за пунктом 10, який відрізняється тим, що
R1 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, н-пентил, ізопентил, н-гексил, ізогексил, циклопропіл, циклопентил та циклогексан;
R2 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, н-пентил, ізопентил, н-гексил та ізогексил;
R3 знаходиться у 4 положенні і вибраний з групи, яка включає водень, гідроксиметильну групу (СН2ОН), формільну групу (СНО), карбоксил (СООН), складноефірну карбоксильну групу (COOR, де R являє собою С1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну групу (СН2ОС(О)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 та галоген;
R5 являє собою водень; та
R4 вибраний з групи, яка включає водень і галоген.
13. Сперміцидно оброблений пристрій для контрацепції за пунктом 12, який відрізняється тим, що
R1 являє собою метил, етил, н-пропіл або ізопропіл;
R2 являє собою метил, етил, н-пропіл або ізопропіл;
R3 являє собою 4-СООН або 4-COOR, де R приймає значення, вказані вище;
R5 являє собою водень; та
R4 являє собою галоген.
14. Сперміцидно оброблений пристрій для контрацепції за пунктом 10, який відрізняється тим, що бар'єрний пристрій для контрацепції вибраний з групи, яка включає діафрагми, контрацептивні губки і презервативи.
15. Спосіб знищення грибів, у якому:
вводять пацієнту, який потребує такої протигрибкової обробки, композицію, що містить протигрибково ефективну кількість сполуки формули І(а):

у якій
R1 являє собою атом водню або лінійний або розгалужений С1-6 алкіл або С3-С8 циклоалкіл;
R2 являє собою атом водню, лінійний або розгалужений С1-6 алкіл;
R3 та R5 кожний незалежно являє собою атом водню, SO3H, лінійний або розгалужений С1-6 алкіл, СН2ОН, СН2ОМе, лінійну або розгалужену С1-6 алкоксигрупу, карбоксил (СООН), не складноефірну групу, яка може бути перетворена у фізіологічних умовах ссавця в карбоксильну групу, складноефірну карбоксильну групу (COOR, де R являє собою С1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну групу (СН2OC(O)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 і галоген; та
R4 являє собою атом водню, галоген, R3Si або COR,
та прийнятний носій.
16. Спосіб за пунктом 15, який відрізняється тим, що сполука являє собою сполуку формули І(b):

17. Спосіб за пунктом 15, який відрізняється тим, що R1 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, н-пентил, ізопентил, н-гексил, ізогексил, циклопропіл, циклопентил та циклогексил;
R2 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, н-пентил, ізопентил, н-гексил та ізогексил;
R3 знаходиться у 4 положенні і вибраний з групи, яка включає водень, гідроксиметильну групу (СН2ОН), формільну групу (СНО), карбоксил (СООН), складноефірну карбоксильну групу (COOR, де R являє собою С1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну групу (СН2OC(O)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 та галоген;
R5 являє собою водень; та
R4 вибраний з групи, яка включає водень і галоген.
18. Спосіб за пунктом 17, який відрізняється тим, що R1 являє собою метил, етил, н-пропіл або ізопропіл;
R2 являє собою метил, етил, н-пропіл або ізопропіл;
R3 являє собою 4-СООН або 4-COOR, де R приймає значення, вказані вище;
R5 являє собою водень; та
R4 являє собою галоген.
19. Спосіб за пунктом 15, який відрізняється тим, що застосування є місцевим застосуванням.
20. Спосіб за пунктом 15, який відрізняється тим, що застосування є внутрішнім застосуванням.
21. Спосіб контрацепції, що включає:
пероральне введення пацієнту композиції, що містить ефективну сперміцидну кількість першої сполуки формули І(а):

у якій
R1 являє собою атом водню, лінійний або розгалужений С1-6 алкіл або С3-C8 циклоалкіл;
R2 являє собою атом водню, лінійний або розгалужений С1-6 алкіл;
R3 та R5 кожний незалежно являє собою атом водню, SO3H, лінійний або розгалужений С1-6 алкіл, СН2ОН, СН2ОМе, лінійну або розгалужену С1-6 алкоксигрупу, карбоксил (СООН), не складноефірну групу, яка може бути перетворена у фізіологічних умовах ссавця в карбоксильну групу, складноефірну карбоксильну групу (COOR, де R являє собою С1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну групу (СН2OC(O)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 і галоген; та
R4 являє собою атом водню, галоген, R3Si або COR,
у фармакологічно прийнятному носії; та
паралельне застосування зазначеним пацієнтом сперміцидно обробленого пристрою для контрацепції, що включає:
ефективну сперміцидну кількість другої сполуки формули І(а):

у якій
R1 являє собою атом водню, лінійний або розгалужений С1-6 алкіл або С3-С8 циклоалкіл;
R2 являє собою атом водню, лінійний або розгалужений С1-6 алкіл;
R3 та R5 кожний незалежно являє собою атом водню, SO3H, лінійний або розгалужений С1-6 алкіл, СН2ОН, СН2ОМе, лінійну або розгалужену С1-6 алкоксигрупу, карбоксил (СООН), не складноефірну групу, яка може бути перетворена у фізіологічних умовах ссавця в карбоксильну групу, складноефірну карбоксильну групу (COOR, де R являє собою С1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну групу (СН2OC(O)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 і галоген; та
R4 являє собою атом водню, галоген, R3Si або COR,
та носій; і
бар'єрний пристрій для контрацепції;
причому зазначена перша сполука формули І(а) і зазначена друга сполука формули І(а) можуть бути однаковими або різними.
22. Спосіб за пунктом 21, який відрізняється тим, що перша сполука являє собою сполуку формули І(b):

23. Спосіб за пунктом 21, який відрізняється тим, що перша сполука являє собою сполуку формули І(а), у якій
R1 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, н-пентил, ізопентил, н-гексил, ізогексил, циклопропіл, циклопентил та циклогексил;
R2 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, н-пентил, ізопентил, н-гексил та ізогексил;
R3 знаходиться у 4 положенні і вибраний з групи, яка включає водень, гідроксиметильну групу (СН2ОН), формільну групу (СНО), карбоксил (СООН), складноефірну карбоксильну групу (COOR, де R являє собою С1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну групу (СН2ОС(О)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 та галоген;
R5 являє собою водень; та
R4 вибраний з групи, яка включає водень і галоген.
24. Спосіб за пунктом 23, який відрізняється тим, що перша сполука являє собою сполуку формули І(а), у якій
R1 являє собою метил, етил, н-пропіл або ізопропіл;
R2 являє собою метил, етил, н-пропіл або ізопропіл;
R3 являє собою 4-СООН або 4-COOR, де R приймає значення, вказані вище;
R5 являє собою водень; та
R4 являє собою галоген.
25. Спосіб за пунктом 21, який відрізняється тим, що бар'єрний пристрій для контрацепції вибраний з групи, яка включає діафрагми, контрацептивні губки і презервативи.
26. Спосіб за пунктом 21, який відрізняється тим, що друга сполука являє собою сполуку формули І(b):

27. Спосіб за пунктом 21, який відрізняється тим, що друга сполука являє собою сполуку формули І(а), у якій
R1 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, н-пентил, ізопентил, н-гексил, ізогексил, циклопропіл, циклопентил та циклогексил;
R2 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, н-пентил, ізопентил, н-гексил та ізогексил;
R3 знаходиться у 4 положенні і вибраний з групи, яка включає водень, гідроксиметильну групу (СН2ОН), формільну групу (СНО), карбоксил (СООН), складноефірну карбоксильну групу (COOR, де R являє собою С1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну групу (СН2OC(O)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 та галоген;
R5 являє собою водень; та
R4 вибраний з групи, яка включає водень і галоген.
28. Спосіб за пунктом 27, який відрізняється тим, що у вказаній другій сполуці формули І(а)
R1 являє собою метил, етил, н-пропіл або ізопропіл;
R2 являє собою метил, етил, н-пропіл або ізопропіл;
R3 являє собою 4-СООН або 4-COOR, де R приймає значення, вказані вище;
R5 являє собою водень; та
R4 являє собою галоген.
29. Спосіб за пунктом 21, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою однакові сполуки.
30. Спосіб за пунктом 21, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою різні сполуки.
31. Спосіб за пунктом 22, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою однакові сполуки.
32. Спосіб за пунктом 22, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою різні сполуки.
33. Спосіб за пунктом 23, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою однакові сполуки.
34. Спосіб за пунктом 23, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою різні сполуки.
35. Спосіб за пунктом 24, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою однакові сполуки.
36. Спосіб за пунктом 24, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою різні сполуки.
37. Спосіб за пунктом 25, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою однакові сполуки.
38. Спосіб за пунктом 25, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою різні сполуки.
39. Спосіб за пунктом 26, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою однакові сполуки.
40. Спосіб за пунктом 26, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою різні сполуки.
41. Спосіб за пунктом 27, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою однакові сполуки.
42. Спосіб за пунктом 27, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою різні сполуки.
43. Спосіб за пунктом 28, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою однакові сполуки.
44. Спосіб за пунктом 28, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою різні сполуки.
Текст
1.Спосіб знищення рухли вих сперматозоїдів, у якому: суміш, що містить сперматозоїди, приводять у взаємодію зі сперміцидною композицією, що містить сполуку формули І(а): 3 82864 4. Спосіб за пунктом 3, який відрізняється тим, що R1 являє собою метил, етил, н-пропіл або ізопропіл; R2 являє собою метил, етил, н-пропіл або ізопропіл; R3 являє собою 4-СООН або 4-COOR, де R приймає значення, вказані вище; R5 являє собою водень; та R4 являє собою галоген. 5. Сперміцидна композиція, що містить ефективну сперміцидну дозу сполуки формули І(а): R4 R1 8 9 R2 7 6 1 9a 5 9b 4a 4 2 N 3 R5 R3 I(a), у якій R1 являє собою атом водню, лінійний або розгалужений C1-6 алкіл або С 3-C8 циклоалкіл; R2 являє собою атом водню, лінійний або розгалужений С1-6 алкіл; R3 та R5 кожний незалежно являє собою атом водню, SO3H, лінійний або розгалужений С 1-6 алкіл, СН2ОН, СН2ОМе, лінійну або розгалужену С 1-6 алкоксигрупу, карбоксил (СООН), не складноефірну груп у, яка може бути перетворена у фізіологічних умовах ссавця в карбоксильну груп у, складноефірну карбоксильну групу (COOR, де R являє собою С 1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну груп у (CH2OC(O)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 і галоген; та R4 являє собою атом водню, галоген, R3Si або COR, та прийнятний носій. 6. Сперміцидна композиція за пунктом 5, яка відрізняється тим, що композиція представлена у формі, вибраній з групи, яка включає гелі, желе, креми, піни, мазі та бальзами. 7. Сперміцидна композиція за пунктом 5, яка відрізняється тим, що сполука являє собою сполуку формули І(b): R4 H 8 9 R2 7 6 R1 1 9a 5 9b 4a H 4 2 N 3 H R5 R3 I(b). 8. Сперміцидна композиція за пунктом 5, яка відрізняється тим, що R1 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, н 4 пентил, ізопентил, н-гексил, ізогексил, циклопропіл, циклопентил та циклогексил; R2 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, нпентил, ізопентил, н-гексил та ізогексил; R3 знаходиться у 4 положенні і вибраний з групи, яка включає водень, SO3H, лінійний або розгалужений С1-6 алкіл, СН2ОН, СН2ОМе, лінійну або розгалужену С 1-6 алкоксигрупу, карбоксил (СООН), не складноефірну групу, яка може бути перетворена у фізіологічних умовах ссавця в карбоксильну групу, гідроксиметильну груп у (СН2ОН), формільну груп у (СНО), карбоксил (СООН), складноефірну карбоксильну груп у (COOR, де R являє собою С 1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну груп у (CH2OC(O)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 та галоген; R5 являє собою водень; та R4 вибраний з групи, яка включає водень і галоген. 9. Сперміцидна композиція за пунктом 8, яка відрізняється тим, що R1 являє собою метил, етил, н-пропіл або ізопропіл; R2 являє собою метил, етил, н-пропіл або ізопропіл; R3 являє собою 4-СООН або 4-COOR, де R приймає значення, вказані вище; R5 являє собою водень; та R4 являє собою галоген. 10. Сперміцидно оброблений пристрій для контрацепції, що включає: ефективну сперміцидну дозу сполуки формули І(а): R4 R1 8 9 R2 7 6 1 9a 5 9b 4a 4 2 N 3 R5 R3 I(a), у якій R1 являє собою атом водню, лінійний або розгалужений C1-6 алкіл або С 3-С8 циклоалкіл; R2 являє собою атом водню, лінійний або розгалужений С1-6 алкіл; R3 та R5 кожний незалежно являє собою атом водню, SO3H, лінійний або розгалужений С 1-6 алкіл, СН2ОН, СН2ОМе, лінійну або розгалужену С 1-6 алкоксигрупу, карбоксил (СООН), не складноефірну груп у, яка може бути перетворена у фізіологічних умовах ссавця в карбоксильну груп у, складноефірну карбоксильну групу (COOR, де R являє собою С 1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну груп у (CH2OC(O)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 і галоген; та R4 являє собою атом водню, галоген, R3Si або COR, та прийнятний носій; і бар'єрний пристрій для контрацепції. 5 82864 11. Сперміцидно оброблений пристрій для контрацепції за пунктом 10, який відрізняється тим, що сполука являє собою сполуку формули І(b): R4 H 8 9 R2 7 6 R1 1 9a 5 9b 4a H 4 2 N 3 H R5 R3 I(b). 12. Сперміцидно оброблений пристрій для контрацепції за пунктом 10, який відрізняється тим, що R1 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, нпентил, ізопентил, н-гексил, ізогексил, циклопропіл, циклопентил та циклогексан; R2 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, нпентил, ізопентил, н-гексил та ізогексил; R3 знаходиться у 4 положенні і вибраний з групи, яка включає водень, гідроксиметильну групу (СН2ОН), формільну груп у (СНО), карбоксил (СООН), складноефірну карбоксильну груп у (COOR, де R являє собою С1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну гр упу (СН2ОС(О)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 та галоген; R5 являє собою водень; та R4 вибраний з групи, яка включає водень і галоген. 13. Сперміцидно оброблений пристрій для контрацепції за пунктом 12, який відрізняється тим, що R1 являє собою метил, етил, н-пропіл або ізопропіл; R2 являє собою метил, етил, н-пропіл або ізопропіл; R3 являє собою 4-СООН або 4-COOR, де R приймає значення, вказані вище; R5 являє собою водень; та R4 являє собою галоген. 14. Сперміцидно оброблений пристрій для контрацепції за пунктом 10, який відрізняється тим, що бар'єрний пристрій для контрацепції вибраний з групи, яка включає діафрагми, контрацептивні губки і презервативи. 15. Спосіб знищення грибів, у якому: вводять пацієнту, який потребує такої протигрибкової обробки, композицію, що містить протигрибково ефективну кількість сполуки формули І(а): R4 R1 8 9 R2 7 6 1 9a 5 9b 4a 4 2 N 3 R5 R3 у якій I(a), 6 R1 являє собою атом водню або лінійний або розгалужений С1-6 алкіл або С 3-С8 циклоалкіл; R2 являє собою атом водню, лінійний або розгалужений С1-6 алкіл; R3 та R5 кожний незалежно являє собою атом водню, SO3H, лінійний або розгалужений С 1-6 алкіл, СН2ОН, СН2ОМе, лінійну або розгалужену С 1-6 алкоксигрупу, карбоксил (СООН), не складноефірну груп у, яка може бути перетворена у фізіологічних умовах ссавця в карбоксильну груп у, складноефірну карбоксильну групу (COOR, де R являє собою С 1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну груп у (СН2OC(O)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 і галоген; та R4 являє собою атом водню, галоген, R3Si або COR, та прийнятний носій. 16. Спосіб за пунктом 15, який відрізняється тим, що сполука являє собою сполуку формули І(b): R4 H 8 9 7 9a 6 R2 1 5 9b 4a H 4 N R1 2 3 H R5 R3 I(b). 17. Спосіб за пунктом 15, який відрізняється тим, що R1 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, нпентил, ізопентил, н-гексил, ізогексил, циклопропіл, циклопентил та циклогексил; R2 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, нпентил, ізопентил, н-гексил та ізогексил; R3 знаходиться у 4 положенні і вибраний з групи, яка включає водень, гідроксиметильну групу (СН2ОН), формільну груп у (СНО), карбоксил (СООН), складноефірну карбоксильну груп у (COOR, де R являє собою С1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну гр упу (СН2OC(O)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 та галоген; R5 являє собою водень; та R4 вибраний з групи, яка включає водень і галоген. 18. Спосіб за пунктом 17, який відрізняється тим, що R1 являє собою метил, етил, н-пропіл або ізопропіл; R2 являє собою метил, етил, н-пропіл або ізопропіл; R3 являє собою 4-СООН або 4-COOR, де R приймає значення, вказані вище; R5 являє собою водень; та R4 являє собою галоген. 19. Спосіб за пунктом 15, який відрізняється тим, що застосування є місцевим застосуванням. 20. Спосіб за пунктом 15, який відрізняється тим, що застосування є внутрішнім застосуванням. 21. Спосіб контрацепції, що включає: 7 82864 пероральне введення пацієнту композиції, що містить ефективну сперміцидну кількість першої сполуки формули І(а): R4 8 9 R2 7 1 9a 6 5 9b 4a 4 2 3 N R1 R5 R3 R4 8 9 7 1 9a 6 5 9b 4a 4 2 3 N R1 R5 R3 де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 і галоген; та R4 являє собою атом водню, галоген, R3Si або COR, та носій; і бар'єрний пристрій для контрацепції; причому зазначена перша сполука формули І(а) і зазначена друга сполука формули І(а) можуть бути однаковими або різними. 22. Спосіб за пунктом 21, який відрізняється тим, що перша сполука являє собою сполуку формули І(b): R4 I(a), у якій R1 являє собою атом водню, лінійний або розгалужений С1-6 алкіл або С 3-C8 циклоалкіл; R2 являє собою атом водню, лінійний або розгалужений С1-6 алкіл; R3 та R5 кожний незалежно являє собою атом водню, SO3H, лінійний або розгалужений С 1-6 алкіл, СН2ОН, СН2ОМе, лінійну або розгалужену С 1-6 алкоксигрупу, карбоксил (СООН), не складноефірну груп у, яка може бути перетворена у фізіологічних умовах ссавця в карбоксильну груп у, складноефірну карбоксильну групу (COOR, де R являє собою С 1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну груп у (СН2OC(O)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 і галоген; та R4 являє собою атом водню, галоген, R3Si або COR, у фармакологічно прийнятному носії; та паралельне застосування зазначеним пацієнтом сперміцидно обробленого пристрою для контрацепції, що включає: ефективну сперміцидну кількість другої сполуки формули І(а): R2 8 I(a), у якійR1 являє собою атом водню, лінійний або розгалужений С1-6 алкіл або С 3-С8 циклоалкіл; R2 являє собою атом водню, лінійний або розгалужений С1-6 алкіл; R3 та R5 кожний незалежно являє собою атом водню, SO3H, лінійний або розгалужений С 1-6 алкіл, СН2ОН, СН2ОМе, лінійну або розгалужену С 1-6 алкоксигрупу, карбоксил (СООН), не складноефірну груп у, яка може бути перетворена у фізіологічних умовах ссавця в карбоксильну груп у, складноефірну карбоксильну групу (COOR, де R являє собою С 1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну груп у (СН2OC(O)-R, H 8 9 R2 7 6 R1 1 9a 5 9b 4a H 4 2 N 3 H R5 R3 I(b). 23. Спосіб за пунктом 21, який відрізняється тим, що перша сполука являє собою сполуку формули І(а), у якій R1 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, нпентил, ізопентил, н-гексил, ізогексил, циклопропіл, циклопентил та циклогексил; R2 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, нпентил, ізопентил, н-гексил та ізогексил; R3 знаходиться у 4 положенні і вибраний з групи, яка включає водень, гідроксиметильну групу (СН2ОН), формільну груп у (СНО), карбоксил (СООН), складноефірну карбоксильну груп у (COOR, де R являє собою С1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну гр упу (СН2ОС(О)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 та галоген; R5 являє собою водень; та R4 вибраний з групи, яка включає водень і галоген. 24. Спосіб за пунктом 23, який відрізняється тим, що перша сполука являє собою сполуку формули І(а), у якій R1 являє собою метил, етил, н-пропіл або ізопропіл; R2 являє собою метил, етил, н-пропіл або ізопропіл; R3 являє собою 4-СООН або 4-COOR, де R приймає значення, вказані вище; R5 являє собою водень; та R4 являє собою галоген. 25. Спосіб за пунктом 21, який відрізняється тим, що бар'єрний пристрій для контрацепції вибраний з групи, яка включає діафрагми, контрацептивні губки і презервативи. 26. Спосіб за пунктом 21, який відрізняється тим, що друга сполука являє собою сполуку формули І(b): 9 82864 R4 H 8 9 R2 7 1 9a 6 5 9b 4a H 4 2 3 N R1 H R5 R3 I(b). 27. Спосіб за пунктом 21, який відрізняється тим, що друга сполука являє собою сполуку формули І(а), у якій R1 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, нпентил, ізопентил, н-гексил, ізогексил, циклопропіл, циклопентил та циклогексил; R2 вибраний з групи, яка включає водень, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, нпентил, ізопентил, н-гексил та ізогексил; R3 знаходиться у 4 положенні і вибраний з групи, яка включає водень, гідроксиметильну групу (СН2ОН), формільну груп у (СНО), карбоксил (СООН), складноефірну карбоксильну груп у (COOR, де R являє собою С1-10 алкіл, С6-10 арил, С7-10 аралкіл), гідроксиметильну складноефірну гр упу (СН2OC(O)-R, де R приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 та галоген; R5 являє собою водень; та R4 вибраний з групи, яка включає водень і галоген. 28. Спосіб за пунктом 27, який відрізняється тим, що у вказаній другій сполуці формули І(а) R1 являє собою метил, етил, н-пропіл або ізопропіл; R2 являє собою метил, етил, н-пропіл або ізопропіл; R3 являє собою 4-СООН або 4-COOR, де R приймає значення, вказані вище; R5 являє собою водень; та R4 являє собою галоген. 29. Спосіб за пунктом 21, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою однакові сполуки. 30. Спосіб за пунктом 21, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою різні сполуки. 31. Спосіб за пунктом 22, який відрізняється тим, що вказана перша сполука формули І(а) і вказана Даний винахід стосується гексагідроінденопіридинових сполук, які мають активність як сперміцидні та/або протигрибкові засоби, сперміцидних та протигрибкових композицій, що їх містять, та способів знищення рухливих сперматозоїдів або грибів із застосуванням сполук і композицій. У США і великій частині Західного світу високий та зростаючий попит на протизаплідні засоби 10 друга сполука формули І(а) являють собою однакові сполуки. 32. Спосіб за пунктом 22, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою різні сполуки. 33. Спосіб за пунктом 23, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою однакові сполуки. 34. Спосіб за пунктом 23, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою різні сполуки. 35. Спосіб за пунктом 24, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою однакові сполуки. 36. Спосіб за пунктом 24, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою різні сполуки. 37. Спосіб за пунктом 25, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою однакові сполуки. 38. Спосіб за пунктом 25, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою різні сполуки. 39. Спосіб за пунктом 26, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою однакові сполуки. 40. Спосіб за пунктом 26, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою різні сполуки. 41. Спосіб за пунктом 27, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою однакові сполуки. 42. Спосіб за пунктом 27, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою різні сполуки. 43. Спосіб за пунктом 28, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою однакові сполуки. 44. Спосіб за пунктом 28, який відрізняється тим, що вказана перша сполука формули І(а) і вказана друга сполука формули І(а) являють собою різні сполуки. результат вибору способу життя, у той час як у багатьох країнах, що розвиваються, контроль за народжуваністю являє собою значне занепокоєння служби охорони здоров'я. Приймаючи до уваги, що контрацепція є глобальною потребою з погляду здоров'я, з різних причин у різних частинах світу, загальний ринок чоловічих протизаплідних засобів міг би бути набагато більшим, ніж він становить у 11 82864 тільки США. У Західному світі за останні 50 років ринок протизаплідних засобів змінився відносно несильно, з "пігулкою (протизаплідним засобом)", яка була розроблена в 1951 і до сих пір не має собі рівних як популярний вибір для контрацепції. Новітні розробки в дослідженні контрацепції запропонували додатково лише декілька засобів, всі для жінок, які історично несли головний тягар відповідальності, витрат, і ризику для здоров'я (зокрема ризиків серцево-судинної хвороби і певних типів раку, пов'язаних з тривалим використанням гормональних протизаплідних засобів) від контрацепції. Презерватив, винайдений в 16-му сторіччі, є єдиною переважною формою контрацепції, доступною для чоловіків (окрім "вилучення (зупинки статевого акту)" і вазектомії). Єдине реально новаторське вдосконалення, що стосувалося презервативів, прийшло з вулканізацією каучуку в 19-му сторіччі [3 New Scientist, 20 April 1994, Vol 142 No 1923.]. Оскільки фармацевтичні компанії розробляють засоби для лікування статевих порушень (наприклад, Viagra для еректильної дисфункції), попит на протизаплідні засоби, як очікують, буде зростати. Протягом 1999 року продажі презервативів в США зросли на 5,8%, привівши до доходів в 260 мільйонів доларів США, що деяких виданнях назвали новою Американською сексуальною революцією [Drag Store News, Nov 29,1999 v21 119 p29.]. Хоча більшість жінок дітородного віку вже практикують контрацепцію (58 % всіх одружених жінок у світі репродуктивного віку використовують певного виду протизаплідні методи [The Population Division of the United Nations Department of Economic and Social Affairs 2000)], усе ще половина всіх вагітностей є випадковою [NICHD, Contraception and Reproductive Health Branch: Report to the NACHHD Council September 1999.]. Існує постійне звернення від служби здоров'я та груп споживачів у щодо збільшення кількості альтернатив, особливо альтернатив, які дозволяли б чоловікам нести більшу частину протизаплідної відповідальності. Загальні занепокоєння привели організації, такі як World Health Organization та Family Health International до запровадження ініціатив, спрямованих на розвиток чоловічих протизаплідних засобів. Протягом цього десятиліття принаймні дві компанії, Schering і Organon, інвестують великі капітали з метою забезпечення гормональної чоловічої контрацепції на ринку. Безпечні і ефективні перорально активні чоловічі протизаплідні препарати розробляються вже багато років. Однак, розробка лікарського засобу, який би міг безпечно перервати сперматогенез, не впливаючи на лібідо, і у такий спосіб функціонувати як чоловічий протизаплідний засіб, виявилося дуже складним завданням. Ідеальним протизаплідним засобом для чоловіка був би такий засіб, який би ефективно зупиняв продукування сперматозоїдів, блокував їх здатність до запліднення, не впливаючи на лібідо або допоміжні статеві органи та їх функції, та/або знищував р ухливі сперматозоїди. Крім того, він повинен мати широкий інтервал між ефективною і токсичною дозами, та цей спосіб повинен бути 12 оборотним. Такий ідеальний чоловічий протизаплідний засіб на сьогоднішній день недоступний. Деякі загальні клітинні токсичні речовини, такі як протипухлинні засоби та алкілюючі агенти впливають на сперматогенез, але очевидно є не прийнятними як протизаплідні засоби. Сполуки, які заважають енергетичним процесами у клітині, такі як тіосахари також заважають сперматогенезу, але є не достатньо селективними. Андрогени, такі як тестостерон та його аналоги, коли їх застосовують у досить великих дозах, заважають сперматогенезу, імовірно через механізм, що включає гіпоталамо-гіпофізарну вісь. Ці стероїдні сполуки успішно використовувались в клінічних дослідженнях. Однак, анаболічні властивості цих стероїдів можуть призвести до небажаних побічних ефектів. Аналоги гормону вивільнення гонадотропіну (GNRH) були активно досліджені як сполуки, які ефективно блокують сперматогенез. Однак, аналоги GNRH заважають ендогенному продукуванню тестостерону та у такий спосіб зменшують лібідо, якщо не застосовуються додаткові андрогени. Один з підходів до чоловічих протизаплідних засобів оснований на ідентифікації та використанні біохімії репродуктивного процесу чоловіка. Чоловіча статева залоза (яєчко) складається із трьох функціональних частин. Перша частина, відповідальна за продукування сперми, складається із сім'яних канальців, які містять зародкові клітки, що розвиваються. Друга частина являє собою клітину Сертолі, також розташовану у сім'яному канальці, що робить внесок в організаційну й функціональну координацію сперматогенного процесу та ймовірно відіграє паракринну та а утокринну ролі. Через складний організаційний взаємозв'язок між клітиною Сертолі та зародковими клітинами, що розвиваються, та наявність непроникних перегородок між сусідніми клітинами Сертолі, утворюється кров'яний яєчковий бар'єр, що розділяє сім'яний канадець на області, які ізольовані від прямого доступу хімічних речовин або живильних речовин, що переносяться з кров'ю. Оточення канальців, у інтерстиціальній тканині, являє собою клітини Лейдига, які мають декілька ендокринних і паракринних функцій, серед яких найкраще описане продукування тестостерону. Зародкові клітини діляться та диференціюються прогресивно, рухаючись, після того, як вони дозрівають, від базальної мембрани до порожнини канальця. Сперматогонії знаходяться в основній частині, та селективно дозріла сперматогонія ділиться мейотично, щоб стати або клітинами, які зберігаються як сперматогонія, або диференціюються в первинні сперматоцити. Первинні сперматоцити мігрують через перегородки між клітинами Сертолі та діляться мейотично з утворенням вторинних сперматоцитів. Вторинні сперматоцити діляться з утворенням сперматидів. Далі сперматиди диференціюються в зрілу сперму. Ди ференціонування сперматидів часто називають сперматогенезом. Однак, з метою цього застосування, "сперматогенез", як визначено, охоплює весь процес формування і дозрівання (диференціонування) сперми, причому "протисперматогенна сполука" це 13 82864 така сполука та, що порушує будь-яку частину цього процесу. Сумарно функціями клітин Сертолі є наступні: (а) підтримання та живлення епітелію сім'яного канальця, (b) вивільнення сперматидів, що дозрівають, у порожнину канальця, (с) формування морфологічного та фізіологічного кров'яного яєчкового бар'єру, (d) фагоцитоз зародкових клітин, що вироджуються, та (e) регулювання циклу епітелію сім'яного канальцю. Клітина Лейдига також підтримує сперматогенез. Лютеїнізуючий гормон (LH) з гіпофізу стимулює продукування тестостерону клітиною Лейдига. Тестостерон та його метаболіт, дигідротестостерон, є необхідними для підтримання нормального сперматогенезу. Рецептори тестостерону присутні на різних типах зародкових клітин. Тестостерон доставляється через кров'яний яєчковий бар'єр, імовірно через транспортування у клітину Сертолі, де він метаболізується у естрадіол, дигідротестостерон, або залишається незмінним. Деякі, якщо не всі типи зародкових клітин, взаємодіють із клітиною Лейдига та/або клітиною Сертолі. Ці взаємодії відбуваються у формі хімічних месенджерів, які продукуються клітиною(ами) Сертолі, Лейдига, та зародковою клітиною(ами). Наприклад, пахітеновий сперматоцит модулює секрецію білкового фактору клітин Сертолі, що у свою чергу стимулює стероїдогенез клітиною Лейдига. Прикріплення сперматидів відбувається тільки до клітин Сертолі, які стають прийнятними або функціональними при взаємодії з FSH (фолікулостимулюючий гормон). Клітина Сертолі пацюків секретує кілька білків циклічним способом, з максимальним продукуванням, що має місце на певній стадії епітелію сім'я ного канальцю; тобто, коли вона знаходиться у зв'язку з певною групою зародкових клітин. Кластерін виробляється максимально клітинами Сертолі, коли епітелій сім'яного канальцю перебуває у Стадії VII або VIII конфігурації, яка не залежить від FSH стимуляції, пропонуючи місцеве регулювання секреторної функції Сертолі зародковими клітками. Було показано, що гексагідроінденопіридинова сполука №20-438, розроблена Sandoz, Ltd. (сполука 1 на Фіг.1), забезпечує оборотне інгібування сперматогенезу при пероральному застосуванні до тварин. [Дивись Arch. Toxicol. Suppl., 1984, 7: 171-173; Arch. To xicol. Suppl, 1978, 1: 323-326; та Mutation Research, 1979, 66: 113-127]. Синтез цілого ряду інденопіридинових сполук у вигляді рацемічних сумішей відомий та описаний, [наприклад, у Патентах США №№ 2 470 108; 2 470 109; 2 546 652; 3 627 773; З 678 057; 3 462 443; 3 408 353; 3 497 517; 3 574 686; 3 678 058 та 3 991 066]. Ці інденопіридинові сполуки мають широкий спектр застосувань, включаючи застосування як антагоністів серотоніну, з протизапальними та болезаспокійливими властивостями, інгібіторів агрегації тромбоцитів, седативних засобів, та нейролептичних сполук, так само як і захищаючих від виразки, гіпотензивних та анорексигенних сполук. [Патенти США №№ 5 319 084 та 5 952 336] розкривають гексагідроінденопіридинові сполуки, що мають протисперматогенну активність, у яких 5 14 положення заміщене фенільним кільцем, яке має замісник у пара-положенні. Незважаючи на значні дослідження в цій галузі, продовжує існувати потреба у активних оборотних чоловічих протизаплідних препаратах, які мають обмежені побічні ефекти. Довготривалою проблемою є потреба в застосуванні відомих сполук при рівнях доз, які можуть викликати побічні ефекти. Додатковою проблемою в цій галузі є недостатня кількість прийнятних радіофармацевтичних засобів, що мають специфічні зв'язуючі сайти на або в яєчках. Продовжує існувати потреба у сполуках, які можуть використовуватися як радіофармацевтичні засоби у дослідженні тестикулярної функції та у діагностиці тестикулярної дисфункції. Додатково до чоловічих пероральних протизаплідних засобів існує потреба і в більш ефективних сперміцидних композиціях для застосування в традиційній місцевій/зовнішній контрацепції. Відповідно, одна ціль даного винаходу полягає в забезпеченні перорально активного чоловічого протизаплідного лікарського засобу, що не впливає на лібідо, має високу ефективність та активність, і має мінімальні побічні ефекти або токсичність. Додаткова ціль даного винаходу полягає в забезпеченні перорально активного чоловічого протизаплідного лікарського засобу, що пригнічує сперматогенез, та способу пригнічення сперматогенезу, з застосуванням цього лікарського засобу. Додаткова ціль даного винаходу полягає в забезпеченні композиції, яка діє як сперміцид, знищуючи р ухливу сперму, і, таким чином, є ефективною як протизаплідний засіб для зовнішнього застосування. Ще одна додаткова ціль даного винаходу полягає в забезпеченні композиції, яка діє як протигрибкова композиція. Ці та інші цілі даного винаходу були досягнуті з винайденням гексагідроінденопіридинових сполук даного винаходу та з встановленням, що ці сполуки є дуже ефективними, переривають сперматогенез і діють на рухливу сперму як сперміцидний засіб, та показують ефективні протигрибкові властивості. Сполуки даного винаходу вирішують проблеми, описані вище. Сполуки винаходу показують високу ефективність при більш низьких відносних дозах, ніж відома сполука 1, та знижують можливість виникнення побічних ефектів, таких як седативні ефекти, що спостерігаються при застосуванні цієї сполуки. Крім того, сполуки винаходу взаємодіють із макромолекулярним сайтом у яєчках. Сполуки винаходу, які містять мітку, таку як радіоактивна мітка, вирішують проблему радіофармацевтичних засобів, що не відповідають вимогам, забезпечуючи радіофармацевтичний засіб, який є корисним у дослідженні тестикулярної функції та для діагностики тестикулярної дисфункції. Також було встановлено, що сполуки даного винаходу діють як сперміцидний засіб, знищуючи рухливу сперму дуже ефективним та дієвим способом, передбачаючи їх застосування в цілому ряді сперміцидних композицій. Також знайдено, що сполуки даного мають протигрибкову активність. 15 82864 На ФІГ.1 показано структур у трьох гексагідроінденопіридинових сполук та зображено систему нумерації цих сполук. На ФІГ.2 показано спосіб одержання проміжних сполук даного винаходу. На ФІГ.3 показано енантіоселективний синтез проміжних сполук для сполук даного винаходу. На ФІГ.4 показано схему синтезу для йодування проміжних сполук, одержаних як показано на ФІГ.2 та ФІГ.3, та перетворення цих йодних сполук на додаткові сполуки, що входять в область винаходу. Було знайдено, що гексагідроінденопіридинові сполуки, що мають структуру І(а), представлену нижче, переважно відповідають структурі, показаній у І(Ь) нижче: де атоми водню у положеннях 4а, 5 та 9b мають показану відносну стереохімію (атоми водню у положеннях 4а та 5 знаходяться у транс положенні, атоми водню у положеннях 4а та 9b знаходяться у цис положенні один до другого; Формула І(b)); або відносна стереохімія у положенні 9Ь може бути обернена таким чином, що атоми водню у положеннях 4а та 5 знаходяться у транс положенні, атоми водню у положеннях 4а та 9b знаходяться у транс положенні один до другого; або всі три атоми водню можуть знаходитися у цис положенні один до другого; або де пунктирна лінія між 4а та 5 показує, що сполука також може бути 4а,5-дегідро сполукою, таким чином, маючи подвійний зв'язок між атомами вуглецю 4а та 5 та де R1 являє собою атом водню або лінійний або розгалужений C1-6алкіл, переважно С1-3алкіл, або С3-С8 циклоалкіл; R2 являє собою атом водню, лінійний або розгалужений C13 5 6алкіл, переважно С 1-3 алкіл; R та R являють собою незалежно атом водню, галоген, SO3H, лінійний або розгалужений C1-6алкіл, СН2ОН, СН2ОМе, 16 лінійний або розгалужений C1-6алкокси, карбоксил (СООН) або групу, яка може бути перетворена у фізіологічних умовах ссавця в карбоксильну гр упу, складноефірну карбоксильну гр упу (COOR, де R являє собою C1-6алкіл, С6-10арил, С7-10аралкіл), гідроксиметильну складноефірну груп у (СН2OC(O)R, де R приймає значення, указані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHC0NH2 та галоген; і R4 являє собою атом водню, галоген, R3Si або COR є не тільки протисперматогенними та мають активності приблизно в 40 разів більші, ніж пероральна протисперматогенна активність найбільш відомих сполук, які описано у [попередньому Патенті США 5 319 084], але також діють як сперміциди для того, щоб знищити рухливу сперму, та також діють як протигрибковий засіб. У контексті даного винаходу, термін "протисперматогенний" відноситься до здатності порушувати продукування сперми у яєчках, у той час як термін "сперміцид" або "сперміцидний" відноситься до здатності знищувати рухли ву сперму після її продукування та, більш переважно, після еякуляції. Сполуки даного винаходу мають відносну стереохімію, показану у стр уктурі (І). Цей винахід включає як окремі енантіомерні форми (головним чином оптично чисті), також як і будь-які суміші цих форм, наприклад, рацемічну суміш. Фармацевтично прийнятні солі сполук, що мають структуру (І), представлену ви ще, також включені в область даного винаходу. Фармацевтично прийнятні солі включають, але не обмежуються ними, солі основної функціональної групи (такої як, але не обмежуючись нею, аміно група) з неорганічними кислотами, такі як гідрохлорид, гідройодид, сульфат, фосфат, дифосфат, гідробромід та нітрат або солі основної функціональної групи з органічними кислотами, такі як ацетат, малат, малеат, фумарат, тартрат, сукцинат, цитрат, лактат, метансульфонат, п-толуолсульфонат, пальміат, саліцилат та стеарат; або солі кислотної функціональної групи з іонами металів, такими як (але не обмежуючись ними) Na, K, Са або солі кислотної функціональної групи з іоном амонію, або солі кислотної функціональної групи з органічними іонами, такими як (але не обмежуючись ними) аміни та тетразаміщені іони амонію. Замісник R1 являє собою переважно лінійну алкільну (н-алкільну), ізо-алкільну або циклоалкільну груп у, таку як метил, етил, н-пропіл, ізопропіл, н-бутил, ізо-бутил, н-пентил, ізо-пентил, нгексил, ізо-гексил, циклопропіл, циклопентил, циклогексил. Найбільш переважно, R1 являє собою етил. Замісник R2 також являє собою переважно лінійну або ізо-алкільну груп у, як описано для замісника R1, представленого вище. Замісник R3 знаходиться переважно у пара або 4 положенні кільця та являє собою переважно груп у, вибрану з гр уп: гідроксиметил (СН2ОН), форміл (СНО), карбоксил (СООН), складноефірна карбоксильна група (COOR, де R являє собою С110 алкіл, С 6-10арил, С 7-10аралкіл), та гідроксиметильну складноефірну групу (СН2 ОС(О)-R, де R 17 82864 приймає значення, вказані вище), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2, та галоген. Замісник R4 являє собою переважно галоген, включаючи І, Br, Cl та F. Сильна активність цих сполук є неочікуваною. Галоген може являти собою радіоактивний ізотоп, наприклад, 123І, 125 І, або 131 І. Звичайні (нерадіоактивні) ізотопи у описаних вище сполуках можуть бути заміщені на інші радіоактивні ізотопи, такі як, наприклад, 11С, трітій (3Н) або 18F, або радіоактивні ізотопи брому та хлору. Сполука 1 являє собою рацемічну суміш. Структура сполуки 1 показана на ФІГ.1, сполука 1. Гексагідроінденопіридини мають три асиметричні центри, які можуть бути визначені, використовуючи відому номенклатуру. Альтернативно, відносна стереохімія може бути визначена цис-транс відношеннями атомів водню, прикріплених до вуглецевох системи у положеннях 4а, 5 та 9b трициклічної кільцевої системи, що веде до стереохімічного розподілення. Відповідно до номенклатури Кана-Інгольда-Прелога, стереохімія та назва сполуки 1 є наступною (4aRS,5SR,9bRS)-2eTM-2,3,4,4a,5,9b-reкcaгідро-7-метил-5-(4метилфеніл)-1Н-індено[1,2-с]піридин. Сполука 1 має гідрофобний метильний замісник на 5-фенільній групі, що відповідає заміснику R3 у стр уктурі (І), представленій вище. Протисперматогенна активність сполуки 1 притаманна головним чином виключно (+) ізомеру (оптичне обертання є право обертаючим при вимірюванні в умовах, описаних у Cook та інших, 1995), який є ефективним протисперматогенним лікарським засобом для мишей. Протисперматогенна активність інших сполук цього ряду також притаманна головним чином виключно одному оптичному ізомеру. Виміряне оптичне обертання цих сполук, однак, може бути (+) або (-), в залежності від системи замісників та умов вимірювання, які відомі спеціалісту, кваліфіцированому у стереохімії. З іншого боку, протигрибкові властивості сполук даного винаходу є не стереоспецифічними, з активними як (+) так і (-) ізомерами, хоча їх відносні активності можуть відрізнятися. Сперміцидна дія сполук даного винаходу знайдена у протисперматогенних ізомерів та, як очікується, є також і у інших ізомерів. Дуже полярна карбоксильна група або групи, які можуть бути метаболізовані у фізіологічних умовах ссавця до карбоксильної групи можуть знаходитися у будь-якому положенні, переважно пара-положенні, 5-фенільного кільця сполук винаходу із збереженням сперміцидної та/або протигрибкової активності. Наприклад, сполуки, у яких пара-положення заміщене гідроксиметильною (СН2ОН), формільною (СНО), карбоксильною (СООН) та метоксикарбонільною (С(О)ОСН3) групами, зберігають сильну активність. Ці сполуки показують активність незважаючи на присутність полярного замісника у пара-положенні 5фенільного кільця. Під "метаболізована у фізіологічних умовах ссавця" розуміють функціональну групу R3 , яка перетворюється на карбоксильну групу, коли спо 18 луку, що має структур у (І), застосовують до живого ссавця, якому необхідна протисперматогенна обробка. Застосування може бути здійснене будьяким зручним способом або шляхом, включаючи, але не обмежуючись ними, пероральний, внутрішньочеревинний, внутрішньовенний, підшкірний, внутрішньом'язовий шлях застосування, інгаляції, буккальний шлях застосування та проникнення через шкіру. Такі ж самі шляхи застосування підходять сперміцидного та/або протигрибкового лікувань, поряд з місцевим застосуванням. Перетворення групи R3 в карбоксильну груп у легко визначається шляхом контролювання метаболітів сполуки, що має стр уктур у (І), у крові або у сечі. Метаболіти можна контролювати, використовуючи звичайні методи аналізу, такі як мас-спектрометрія (MS), газова хроматографія (GC), то що. Переважно, принаймні, 50%, краще, принаймні, 80% та навіть ще краще 90%, 95% або 100% функціональних груп R3 метаболізуються до карбоксильної групи при застосуванні до ссавця, хоча це не є необхідним для того, щоб одержати сперміцидні та/або фунгіцидні властивості. Відсоток перетворення може бути визначений кількісно, аналізуючи зразок крові або сечі для того, щоб визначити відносні кількості неперетворених сполук, що містять функціональну групу R3, по відношенню до сполук, у яких R3 перетворилася на карбоксильну гр упу, використовуючи один з прийнятних методів аналізу, зазначених ви ще. Протисперматогенна активність сполуки 1 спостерігається після застосування одноразової пероральної дози в 30мг/кг до пацюків, що після цього значно втрачають вагу яєчок протягом 24 годин. Спостерігаються дегенеративні зміни у сім'яних канальцях. Сперматиди стають пікнотичними, періодично утворюючи багатоядерні утворення. Виявилося, що клітини Сертолі є цитологічно нормальними. Що вказує на те, що сполука 1 вражає сперматиди або клітину Сертолі, зв'язану з цими сперматидами, так як насамперед у цих сперматидах спостерігаються гістологічні зміни. Сполука 1 спричиняє деяку загальмованість та заспокоєння у мишей при пероральному застосуванні дози в 30мг/кг та надзвичайну загальмованість при тій же дозі, введеній підшкірно. Загальмованість та заспокоєння є очевидно небажаними побічними ефектами у контрацептивних засобів. На відміну від загальмованості та заспокоєння, що спостерігаються при застосуванні сполуки 1, сполуки даного винаходу призводять до мінімальної загальмованості. Сполуки даного винаходу дозволяють розділити протизаплідну активність від заспокійливої активності, що спостерігається при застосуванні сполуки 1. Тому, сполуки винаходу є е фективними протизаплідними лікарськими засобами, у яких небажані побічні ефекти заспокоєння та загальмованості є помітно зменшеними. Сполуки винаходу випробовували на мишах за їх впливом на сперматогенез через три дні після одиничної пероральної дози з допомогою процедури, описаної у Cook та інші (1995), представленої нижче. Показано, що сполуки, активні у цьому 19 82864 випробуванні, також є протизаплідними сполуками. Сполуки піддали випробуванням на протисперматогенну активність шляхом введення через зонд дози мишам чоловічої статі у день 1 з дозою: контрольного наповнювача, позитивного контролю (сполука 1) або сполуки винаходу. Через 72 годин після введення дози, тварин умертвили та яєчки вирізали, очистили від жиру та зважили. Одне яєчко перевіряли гістологічно та оцілювали на сперматогенний потенціал, використовуючи Сперматогенний Показник [(Spermatogenic Index) (J. M. Whitsett, P. F. Noden, J. Cherry та A. D. Lawton, J. Reprod. Fertil., 72, 277 (1984)], який являє собою напівкількісну оцінку здатності яєчок продукувати сперму. Цей показник оснований на гістологічному прояві сперматогенних клітин у сім'яних канальцях. Використовують шкалу від 1 до 6, із значенням 5-6, що позначує нормальний статус. Друга оцінка основана на масі яєчок. В Таблиці 1 та 2 показано відповідні біологічні результати, виходячи зі зміни у масі яєчок (TW) та сперматогенного показника (SI) по відношенню до контролю, що містить тільки застосовуваний наповнювач, а не інденопіридин. У Таблиці 1 та 2, R3 та R4 відно 20 сяться до структур Іb, де R знаходиться у пара положенні; R являє собою етил; R являє собою метил; та R5 являє собою атом водню. З 8-йод-7-метил-4'-карбокси або 4'карбометокси структурою замісників, пероральна доза 2mмоль/кг (1мг/кг) рацемата привела до 5767% зниження сперматогенного показнику та була, принаймні, такою ж ефективною, як і 79mмоль/кг (30мг/кг) доза відповідного аналогу без 8-йод замісника. У випадку 8-бром або 8-хлор аналогів, найнижча доза, яку тестували, (6 або 2mмоль/кг; 3 або 1мг/кг) також була, принаймні, такою ж ефективною, як і 79mмоль/кг (30мг/кг) доза негалогенованого аналогу (дивись Таблицю 1). Порівняння активного (лівообертаючого) енантіомеру 8-йод-7метил-4'-карбометокси аналогу з активним енантіомером 8-Н-7-метил-4'-карбометокси аналогу (Таблиця 2) показало, що перша сполука має той самий або більший ефект при 0,6 та 2mмоль/кг (0,3 та 1мг/кг), що і друга сполука при 25 та 75mмоль/кг (10 та 30мг/кг). Таким чином, приблизно 40-разове збільшення у молярній ефективності досягнуто шляхом галогенування 8-положення. Таблиця 1 Протисперматогенний ефект рацемічних інденопіридинових сполук на дорослих swiss мишах чоловічої статіа Сполука 1 2 2 18 18 18 17 17 17 19 19 19 20 20 20 а R3 Me СО2Н СО2Н СО2Ме СО2Ме СО2Ме СО2Н СО2Н СО2Н СО2Н со2н со2н СО2Н СО2Н СО2Н R4 н н н І І І І І І Вг Вг Вг СІ СІ СІ Доза (мг/кг) 30 10 30 1 3 10 1 3 10 3 10 зо 1 3 10 TWb Зміна (%) 19%* 2% -7% -16% -27%* -36%* -18% -9% -32%* -8% -28%* -39%* -16% -23% -22% SIC Зміна (%) -55%* -24%* -52%* -57%* -69%* -74%* -67%* -66%* -76%* -69%* -71%* -72%* -55%* -66%* -72%* Значення розраховують з середнього (n=5) як [100(тестконтроль)/контроль]. Для сполук, які були неактивні, показана тілька найбільша доза. Одноразова доза інденопіридину або наповнювача була введена мишам через зонд при 10мл/кг. Наповнювач складався з 90% води, 7% Tween20, та 3% етанолу. Аутопсію проводили на день 3, починаючи приблизно через 72 годин після введення дози. b Маса яєчок [% зміни від контрольного наповнювача 217,8±46,0 (S.E.) мг] с Сперматогенний Показник [% зміни від контрольного наповнювача 5,8±0,2 (S.E.)] *3начно відрізняється від контрольного наповнювача; односторонній Т критерій Данетта (Dunnett's onetailed T test), p190°С. (розклад). 1Н ЯМР (250МГц, CDCl3, у вигляді вільної основи); d 1,15 (3Н, t, J=7,2Гц), 1,65 (1Н, bd), 1,8-2,1 (3Н, m), 2,32 (3Н, s), 2,48 (3Н, q, J=7,2Гц, +m), 2,80 (1Н, bd), 2,97 (1H, dd, J=11,8, 5,8Гц), 3,41 (1H, m), 3,91 (3Н, s), 4,19 (1Н, d, J=9,8Гц), 6,78 (1H, s), 7,22 (2Н, d, J=8,3Гц), 7,73 (1Н, s), 8,00 (2Н, d, J=8,3Гц). HRMS: Розраховано для C23H26NO2I (що відповідає вільній основі): m/z 475,1008. Знайдено: m/z 475,1004. Аналіз: розраховано для C23H27CIINO 2 1/2Н2О: С, 53,04; Н, 5,42; N, 2,69. Знайдено: С, 52,70; Н, 5,60; N, 2,57. Активний енантіомер, (1)-18, синтезували подібним способом, починаючи з (1)-3. [a]D =-5,6 (с=1,18, СНСl3). Приклад 4 Синтез (4аRS,5SR,9bRS)-2-етил-2,3,4,4а,5,9bгексагідро-8-йод-7-метил-5-(4-карбокси-феніл)-1Ніндено[1,2-с]піридину гідрохлориду (17) До (4аRS,5SR,9bRS)-2-етил-2,3,4,4а,5,9bгексагідро-7-метил-5-(4-карбоксифеніл)-1Ніндено[1,2-с]піридину гідрохлориду (250мг, 0,673ммоль) у 2мл оцтової кислоти додали 6мл 1:1 суміші оцтової кислоти та перхлорної кислоти. HgO (1,35ммоль) додали та реакційну суміш перемішували при кімнатній температурі до розчинення HgO. Розчин І2 (427мг, 1,68ммоль) у 4мл оцтової кислоти та 6 л СН2СІ2 додали по краплях до реакційної суміші з допомогою додавальної лійки. Реа 44 кційну суміш перемішували протягом ночі при кімнатній температурі та потім відфільтрували через Celite. Червону тверду речовину промили водою та СН2СІ2. Обєднаний двофазний фільтрат розділили з допомогою ділильної лійки. Органічну фазу промили насиченим розчином бісульфату натрію, висушили над суль фатом натрію (безводний), відфільтрували та сконцентрували з одержанням 234мг жовто-коричневої твердої речовини, перетворили у гідрохлорид звичайним способом. 1Н ЯМР (250МГц, CDCI3/CD3OH) d 1,28 (3Н, t, J=7,2Гц), 2,0-2,1 (1H, m), 2,3 (3Н, s), 2,56 (2Н, т), 3,04 (ЗН, т), 3,24 (1Н, m), 3,46 (2Н, m), 4,18 (1H, d, J=11Гц), 6,73 (1H, s), 7,13 (2Н, d, J=8,2Гц), 7,71 (1H, s), 7,89 (2Н, d, J=8,2Гц). HRMS Розраховано для C22H24NO2I (що відповідає вільній основі): m/z 461,0852. Знайдено: m/z 461,0857. Приклад 5 Синтез (4аRS,5SR,9bRS)-2-етил-8-бром-7метил-2,3,4,4а,5,9b-гексагідро-5-(4-карбоксилфеніл)-1Н-індено[1,2-с]піридину гідрохлориду (19) (4аRS,5SR,9bRS)-2-Етил-8-йод-7-метил2,3,4,4а,5,9b-гексагідро-5-(4-карбоксилфеніл)-1Hіндено[1,2-с]піридину гідрохлорид (200мг, 0,402ммоль) розчинили у 20мл THF та 0,4мл гексаметилфосфораміду. До цього розчину додали 50мг гідриду натрію (60% у мінеральному маслі). Суміш нагрівали зі зворотним холодильником протягом 1 години та потім охолодили до -78°С. Повільно додали розчин трет-бутиллітію (0,73мл, 1,1М у пентані, 0,804ммоль). Після додавання суміш перемішували при -78°С протягом 20 хвилин. Додали 1,2-диброметилен (1мл). Суміш перемішували при -78°С впродовж ще 30 хвилин та потім нагріли до кімнатної температури. 5% соляну кислоту додавали до розчину, поки розчин не стане кислим. Суміш екстрагували метиленхлоридом. Метиленхлоридний розчин промили сольовим розчином та висушили над MgSO4. Сирий продукт очистили з допомогою флеш колоночної хроматографії (силікагель; метиленхлорид та метанол, 10:1) з одержанням заглавної сполуки: 30мг, 17% вихід, температура плавлення: 169,6-170,3°С. 1Н ЯМР (250МГц, D2O-CDCl3), d 1,25 (3Н, t, J=7,0Гц), 1,72 (1Н, d, J=15Гц), 1,90-2,15 (1Н, m), 2,19 (3Н, s), 2,36 (1Н, t, J=12,5Гц), 2,5-2,65 (1H, m), 2,7-3,0 (3Н, m), 3,2-3,4 (4Н, m), 3,4-3,6 (1Н, m), 4,13 (1Н, d, J=10,5Гц), 6,71 (1Н, s), 7,11 (2Н, d, J=8,0Гц), 7,43 (1H, s), 7,89 (2Н, d, J=8,0Гц). MS: 413 (М). Анал. (C22H25O 2BrClN 1,8Н2О): Розраховано С 54,68, Н 5,22, N 2,90; Знайдено С 54,77, Н 5,52, N 2,57. HRMS Розраховано для C22H24NO2Br (що відповідає вільній основі): m/z 413,0990. Знайдено: m/z 413,0994. Приклад 6 Синтез (4аRS,5SR,9bRS)-2-етил-8-хлор-7метил-2,3,4,4а,5,9b-гексагідро-5-(4-карбоксилфеніл)-1Н-індено[1,2-с]піридину гідрохлориду (20) (4аRS,5SR,9bRS)-2-Етил-8-йод-7-метил2,3,4,4а,5,9b-гексагідро-5-(4-карбоксилфеніл)-1Ніндено[1,2-с]піридину гідрохлорид (250мг, 0,5ммоль) розчинили у 25мл THF та 0.5мл НМРА. До цього розчину додали 60мг гідриду натрію (60% у мінеральному маслі). Суміш нагрівали зі зворотним холодильником протягом 1 години та потім 45 82864 охолодили до -78°С. Повільно додали розчин третбутиллітію (0,91мл, 1,1М у пентані, 1,04ммоль). Після додавання суміш перемішували при -78°С протягом 20 хвилин. Додали розчин гексахлоретану (2,46г, 10,4ммоль) у 2мл THF. Суміш перемішували при -78°С протягом ще 30 хвилин та потім нагріли до кімнатної температури. 5% соляну кислоту додавали до розчин поки розчин не став кислим. Суміш екстрагували метиленхлоридом. Розчин метиленхлориду промили сольовим розчином та висушили над MgSO4. Сирий продукт очистили з допомогою флеш колоночної хроматографії (метиленхлорид та метанол, 10:1) з одержанням заглавної сполуки, 60мг, 30% вихід. 1Н ЯМР (250МГц, D2O-CDCl3) d 1,35 (3Н, t, J=7,25Гц), 1,751,95 (1Н, m), 2,30 (3Н, s), 2,45-2,75 (2Н, m), 2,803,15 (2Н, m), 3,20-3,50 (4Н, m), 3,50-3,70 (1Н, m), 4,25 (1H, d, J=10Гц), 6,80 (1Н, s), 7,25 (2Н, d, J=7,5Гц), 7,32 (1Н, s), 8,0 (2H, d, J=7,5Гц). MS: 370 (M). Анал. (C22H25O 2Cl2N): Розраховано C 65,50, H 6,20, N 3,45; Знайдено C 65,65, H 6,73, N 3,59. HRMS Розраховано C22H24NO2Cl (що відповідає вільній основі): m/z 369,1495. Знайдено: m/z 369,1494. Приклад 7 Синтез (4аRS,9bRS)-2-етил-1,2,3,4,4а,9bгексагідро-1Н-індено[1,2-с]піридин-5-ону (7) Сирий метил 1-етил-3-(4-метилфеніл)-4піридинкарбоксилат [одержаний як описано у Патенті США № 5,319,084 для аналогічного етилового складного ефіру] з 165г метил 1-етил-1,2,5,6тетрагідропіридинкарбоксилату розчинили у 1л водної 18% НСl та екстрагували ефіром (300мл) для видалення бітолілу, що залишився як побічний продукт з його синтезу. Потім водний розчин нагрівали зі зворотним холодильником протягом 48 годин та далі сконцентрували при зниженому тиску з доданим ацетонітрилом (азеотроп) з одержанням сирого гідрохлориду 1-етил-1,2,5,6тетрагідропіридинкарбонової кислоти (283г), який повністю висушили при 100°С у високому вакуумі. Так як цей матеріал є дуже гігроскопічним, його зберігали у атмосфері азоту. Тіонілхлорид (150мл) обережно додали до нерозбавленої сполуки 7 (45г, 159ммоль) при 5°С. Після додавання, льодяну баню видалили; та одержаний гомогенний розчин перемішували при кімнатній температурі впродовж 4 годин. Надлишок SOCl2 видалили у вакуумі з одержанням темної, густої, пастоподібної маси. До цього матеріалу додали 1,2-дихлоретан (250мл) та 30мл розчиннику видалили у вакуумі для того, щоб усун ути будь-який залишковий SOCl2. До мутної суміші додавали АІСІ3 (53г, 397ммоль) частинами впродовж 45 хвилин. Температуру контролювали з допомогою водяної бані при приблизно 25°С. Після додавання, темний, червоно-коричневий розчин перемішували при 3540°С протягом години та потім вилили у хімічну склянку, що містить приблизно 400г подрібненого льоду та 50мл концентрованої НСl. Водний шар підлужили до рН приблизно 12 з допомогою 30% NaOH (приблизно 350мл) з охолодженням у водно-льодяній бані. Отриману суміш екстрагували з охолодженням у водно-льодяній бані. Отриману суміш екстрагували е фіром (3´400мл), та об'єдна 46 ні ефірні шари промили послідовно водою та сольовим розчином, висушили (MgSO 4), відфільтрували, та сконцентрували при зниженому тиску з одержанням помаранчево-червоного масла. Це масло відігнали, використовуючи апарат Кугельрора (Kugelrohr apparatus) (125-135°С при 0,5мм Hg) з одержанням 21,6г (59%) кетону 7 у вигляді світло-жовтої твердої речовини, з ЯМР властивостями, ідентичними до справжнього матеріалу. Приклад 8 Синтез енантіомерів (4aRS,5SR,9bRS)-2-етил7-метил-5-(4-карбометоксифеніл)-2,3,4,4а,5,9bгексагідроіндено[1,2-с]піридину та (4aRS,5SR,9bRS)-2-етил-7-метил-5-(4карбоксифеніл)-2,3,4,4а,5,9b-гексагідроіндено[1,2с]піридину Енантіомери описані як (d) або (1), виходячи з оптичного обертання при D лінії натрію у даному розчиннику. Сполуки, що мають те ж саме позначення обертання, необов'язково мають таку ж абсолютну конфігурацію. 1-Етил-4-карбокси-1,2,5,6-тетрагідропіридину гідрохлорид. Метил 1-етил-1,2,5,6тетрагідропіридинкарбоксилат (11) нагрівали зі зворотним холодильником у 250мл 1,5М НСl впродовж 4 годин. Суміш сконцентрували досуха, використовуючи тепло та струмінь азоту з одержанням високо-кристалічної твердої речовини. Тверду речовину перекристалізували з МеОН та одержали 19,6г HCl солі сполуки 12; температура плавлення = 265°С (розклад). Аналіз: розраховано для C8H14CINO2: C, 50,14; Н, 7,36; N, 7,31. Знайдено: С, 50,23; Н, 7,36; N, 7,28. (I)-Еноїл-султам ((1)-13), одержаний з IS(-)(2,10)камфорсултаму. До гідрохлориду сполуки 12 (1,3г, 6,79ммоль) додали тіонілхлорид (15мл), та отриману суміш нагрівали до зрошення впродовж 2 годин. Надлишок SOCl2 видалили у вакуумі, та осад розтерли з 10мл сухого толуолу та сконцентрували у вакуумі. Процес розтирання повторили ще два рази з одержанням жовтої порошкоподібної твердої речовини. У окремій посудині, нбутиллітій (15ммоль, 6,0мл 2,5М розчин у гексані) додали по краплях до розчину lS-(-)-2,10камфорсултаму (3,16г, 14,7ммоль) у THF (30мл) при 5°С. Після додавання, прозорий, безбарвний розчин довели до кімнатної температури та перемішували протягом ще 45 хвилин. Розчин аніону султаму потім перенесли з допомогою трубочки у колбу, що містить хлорангідриду амінокислоти гідрохлорид при 5°С. Після додавання, помаранчеву суміш залишили для досягнення кімнатної температури та перемішували протягом 18 годин. Реакцію зупинили додаванням насиченого NH4CI (приблизно 1мл) та сконцентрували у вакуумі до коричневого смолистого осаду. Цей осад розподілили між ефіром та водою, та ефірний шар промили ще раз водою. Ефірний шар потім промили розбавленою водною НСl (приблизно 5%) та відділили. Вільний султам (ефірний шар) одержали (1,2г) при перекристалізації з абсолютного ЕtOН. Продукт [(1)-13] одержали шляхом підлуження кислого водного шару з допомогою конц. NH4OH до рН 12, екстрагування ефіром та перекристалізації з н-гексану осаду з Випарювання ефірного 47 82864 шару. Це привело до одержання 1,9г сполуки (1)13 у вигляді білих, товсти х голочок; температура плавлення = 120°С, [a]D21 = -74,8° (с=1,0, СНСІ3), 1 Н ЯМР ідентичний з його антиподом (дивись нижче). Аналіз: розраховано для C8H28N2O3S: C, 61,33; Н, 8,01; N, 7,95. Знайдено: С, 61,35; Н, 8,06; N, 7,89. (d)-Еноїлсултамовий енантіомер сполуки 13 одержаний з 1R(+)-(2,10)-камфорсултаму. Його отримали з гідрохлориду амінокислоти 12 (6,5г, 34,1ммоль) та lR-(+)-2,10-камфорсултаму (15,4г, 71,4ммоль) за процедурою, подібною до описаної для антиподу (дивись вище) з 86% виходом. Температура плавлення = 118,5°С-119,6°С. (перекристалізований з гексану у вигляді товстих, блідожовтих пластинок); [a]D21 = +74,1° (с=1,0, СНСІ3); 1 Н ЯМР (250МГц, CDC13): d 1,00 (3Н, s), 1,12 (3Н, t, J=7,1Гц), 1,22 (3Н, s), 1,3-1,5 (2Н, m), 1,8-2,1 (5Н, m), 2,2-2,4 (1H, m), 2,55 (2Н, q, J=7,1Гц), 2,6-2,7 (3Н, m), 3,1-3,3 (2Н, m), 3,38 (1Н, d, J=13,6Гц), 3,50 (1Н, d, J=13,6Гц), 4,0-4,1 (1 h, m), 6,5-6,6 (1Н, m); Аналіз: розраховано для C18H28N2O3S: C, 61,33; Н, 8,01; N, 7,95. Знайдено: С, 61,48; Н, 8,02; N, 7,98. Кристалічна форма цього матеріалу змінювалася в залежності від того, як швидко він випадає в осад з гексану та концентрації протягом стадії очищення. 1,4-Аддукт (1)-14 одержаний з (1)-13. До розчину еноїлсултаму (1)-13 (5,6г, 16,0ммоль) у толуолі (200мл) при -78°С додавали птолілмагнійбромід (33,6ммоль, 33,6мл 1.0М розчину у е фірі) впродовж 10 хвилин. Після перемішування додаткових 30 хвилин при -78°С, реакційну суміш помістили у холодильник (-10°С) на ніч та потім нагрівали до +5°С впродовж ще двох годин. Реакцію у суміші зупинили додаванням його до насиченого NH4CI (200мл). Після екстракції водного шару ефіром (400мл), шар ефіру екстрагували з допомогою 3% НСl (3´200мл). Кислі шари об'єднали, зробили лужними з допомогою концентрованої NH4OH (рН=12), екстрагували ефіром (3´200мл), та ефірні шари промили сольовим розчином, висушили (MgSO 4), відфільтрували, та сконцентрували при зниженому тиску з одержанням помаранчевої твердої речовини (7,12г). Цю тверду сполуку перекристалізували з суміші ефір-гексан (приблизно 40мл приблизно 1:2 суміші, відповідно). Вихід = 3,64г. Др угий збір привів до одержання ще 1,24г. Загальний вихід = 4,68г (66%). Температура плавлення = 150,5-151,7°С. (ефір-гексан; щільні, товсті, блідо-жовті призми); [a]D21 = 26,2° (с=1,14, СНСl3); 1Н ЯМР (500МГц, CDCl3); d 0,44 (3Н, s), 0,82 (3Н, s), 1,13 (3Н, t, J=7,16Гц), 1,20-1,30 (2Н, m), 1,40-1,55 (1Н, m), 1,62-1,65 (1Н, m), 1,701,85 (3Н, m), 1,95-2,05 (1H, m), 2,05-2,10 (1H, m), 2,27 (3Н, s), 2,55 (2Н, q, J=7,16Гц), 2,55-2,62 (1H, m), 2,68-2,72 (1H, m), 2,82 (1H, dd, J=10,64, 3,47Гц), 3,12 (1H, t, J=10,8Гц), 3,24-3,28 (1H, m), 3,30 (1Н, d, J=14,0Гц), 3,32 (1H, d, J=14,0Гц), 3,553,60 (1H, m), 3,67-3,71 (1H, m), 7,02 (2Н, d, J=7,96Гц), 7,15 (2Н, d, J=7,96Гц); Аналіз: розраховано для C25H36N2O3S: C, 67,53; Н, 8,16; N, 6,30. Знайдено: С, 67,58; Н, 8,15; N,6,30. Енантіомерно чистий кетон (d)-7 одержаний з (1)-14. До розчину 1,4-аддукту (1)-14 (6,86г, 48 15,45ммоль) у THF (40мл) додали свіжо приготовлений розчин LiOH.multidot.H2O (6,43г, 153ммоль) у воді (40мл). Одержану гетерогенну суміш енергійно перемішували при обережному нагріванні зі зворотним холодильником впродовж 26 годин. Суміш охолодили до приблизно +5°С, підкислили до рН=0 концентрованою HCl, та більшу частину летких компонентів видалили направленням помірно сильного струменю газу азоту над поверхнею суміші, в той час як суміш занурили у теплу водяну баню (температура = 50°С). Тверду речовину, що залишилася, повність висушили у високому вакуумі. Одержаний сирий матеріал циклізували до кетону (d)-7 за способом, подібним до рацемічного матеріалу (дивись вище), використовуючи тіонілхлорид та потім АІСІ3 у 1,2-ди хлоретані. Це привело до одержання 1,12 г вільного основного кетону (d)-7 у вигляді масла, яке затверділо при стоянні впродовж ночі. Частину цього матеріалу очистили після виділення з наступної стадії для того, щоб одержати фізичні дані. [a]D20 = +95.9° (вільна основа, с=1,2, СНСІ3); [a]D20 = +71,9° (НСl сіль, с=1,1, СНСl3). Енантіомерно чистий олефін(d)-15 одержаний з кетону (d)-7. Цей матеріал одержали з кетону (d)7 (1,12г, 4,89ммоль) за способом, подібним до рацемічної процедури [дивись Патент США №5,319,084]. Вихід склав 850мг (47%). [a]D19 = +21,2° (с=1,24, СНСl3). Синтез (1)-2-етил-7-метил2,3,4,4а,5,9b-гексагідро-5-(4-бромфеніл)-5гідрокси-1Н-індено[1,2-е]піридин. До енергійно перемішуваного розчину 4-бромйодбензолу (13,8г, 48,9ммоль) у 160мл THF при -78°С дуже повільно додали розчин н-бутиллітію (19,6мл, 2,5М у пентані, 49ммоль). Після додавання, розчин перемішували при -78°С протягом 10 хвилин. Розчин став жовтим та мутним. Додали розчин (d)-2-етил-7метил-1,2,3,4,4а,5,9b-гексагідроіндено[1,2с]піридин-5-ону (8г, 34,9мМ) у 40мл THF. Суміш далі перемішували при -78°С впродовж 2 годин. Охолоджуючу баню забрали та реакцію у суміші зупинили водою. Органічну фазу відділили та водну фазу екстрагували метиленхлоридом. Органічні фази об'єднали, промили сольовим розчином та висушили над MgSO4. Випарювання розчиннику привело до отримання сирого продукту, який перекристалізували з метиленхлориду для одержання заглавної сполуки (10,8г, 80%). температура плавлення: 169,6-170,3°С. 1Н ЯМR (250МГц, CDCl3), d 1,00 (3Н, t, J=7,3Гц), 1,70-2,00 (2Н, m), 2,15-2,30 (1Н, m), 2,29 (3Н, s), 2,38 (2Н, q, J=7,3Гц), 2,5-2,7 (2Н, m), 2,70-2,85 (1H, m), 2,85-3,00 (1H, m), 3,30 - 3,50 (1Н, m), 6,84 (1H, s), 7,17 (2Н, q, J=7,5Гц), 7,31 (2Н, d, J=11Гц), 7,43 (2Н, d, J=11Гц). MS: 386 (М), 230 (100%). [a]D = -11,5° (с=1,03, СНСІ3). Аналіз (C22H24OBrN): Розраховано С, 65,28, Н 6,26, N 3,62; Знайдено С 65,11, Н 6,21, N 3,64. Синтез (і)-енантіомеру (4aSR,5RS,9bSR)-2eтил-7-метил-2,3,4,4a,5,9b-гексагідро-5-(4бромфеніл)-1Н-індено[1,2-с]піридину (1). Розчин (1)-10-2-етил-7-метил-2,3,4,4а,5,9b-гексагідро-5-(4бромфеніл)-5-гідрокси-1Н-індено[1,2-с]піридину (4,5г, 13ммоль) та 100мл триетилсилану у 300мл безводного метиленхлориду охолодили до -78°С. 49 82864 Газ трифторборану барботували у розчин протягом 10 хвилин. Безбарвний розчин перетворився у помаранчевий. Суміш нагріли до кімнатної температури та додали 10 г карбонату калію, а потім воду. Органічну фазу відділили та водну фазу екстрагували метиленхлоридом. Органічні фази об'єднали, промили сольовим розчином та висушили над MgSO4. Розчинник випарили з одержанням сирого продукту. Сирий продукт розчинили у 40мл н-бутанолу. Додали гідроксид калію (9г). Суміш нагріли до зрошення при перемішуванні. Після нагрівання зі зворотним холодильником протягом 20 годин, суміш охолодили до кімнатної температури та вилили у лід. Суміш екстрагували метиленхлоридом. Розчин метиленхлориду промили сольовим розчином та висушили над MgSO4. Розчинник випарили та сирий продукт розподілили між диетиловим ефіром та 18% розчином соляної кислоти. Шари розділили та водний розчин промили ще один раз диетиловим ефіром. Водний розчин охолодили до 0°С та підлужили з допомогою 50 % розчину гідроксиду натрію до рН>14. Суміш екстрагували метиленхлоридом три рази. Органічний розчин промили сольовим розчином та висушили над MgSO4. Випарювання розчиннику привело до одержання сирого продукту, який очистили з допомогою флеш колоночної хроматографії (силікагель, СН2СІ2 та МеОН , 100:3) з отриманням заглавної сполуки (1)-10, 3,2г, 67% вихід (за дві стадії). Гідрохлоридну сіль одержали звичайним способом, температура плавлення 240°С (розклад). 1Н ЯМР (250МГц, CDCl3), d 1,12 (3Н, t, J=7,25), 1,6-1,8 (1H, m), 1,80-2,05 (2Н, m), 2,15-2,40 (2Н, m), 2,26 (3Н, s), 2,70-2,85 (1H, m), 2,90-3,10 (1Н, m), 3,303,45(1Н, m), 4,12 (1Н, d, J=10,25Гц), 6,72 (1H, s), 7,00-7,30 (4Н, m), 7,44 (2Н, d, J=9,0Гц). MS: 370 (М). [a]D - -7,8° (с=0,83, МеОН). Аналіз (C21H24BrNHCl): Розраховано С 62,00, Н 6,19, N 3,44; Знайдено С 61,96, Н 6,23, N 3,35. Синтез (І)-енантіомеру (4aRS,5SR,9bRS)-2eraii-2,3,4,4a,5,9b-гексагідро)-7-метил-5-(4карбоксифеніл)-1Н-індено[1,2-с]піридину гідрохлориду [(1)-2]. Розчин 100мг (0,27ммоль) (1)-10 сполуки у 5мл THF охолодили до -78°С. До цього розчину додали 0,54 мл розчину н-бутиллітію (2,5 М у пентані, 1,35ммоль). Розчин перемішували при 78°С протягом 30 хвилин. Газ диоксиду вуглецю 50 барботували у розчин впродовж 10 хвилин через голку. Суміш перемішували при -78°С впродовж ще 10 хвилин та нагріли до кімнатної температури. THF випарили та осад підкислили з допомогою 18% розчину соляної кислоти. Суміш екстрагували метиленхлоридом. Метиленхлоридний розчин промили сольовим розчином та висушили над MgSO4 . Осушуючий реагент відфільтрували та розчин сконцентрували з одержанням сирого продукту. Колоночна хроматографія (силікагель, СН2Сl2 та МеОН, 10:1 до 1:1) сирого продукту привела до одержання 72мг (71% вихід) (-)-2. [a]D = 15,5° (с=1,24, МеОН). Синтез (сі)-енантіомеру (4aRS,5SR,9bRS)-2emn-2,3,4,4a,5,9b-гексагідро-7-метил-5-(4карбометоксифеніл)-1Н-індено[1,2-с]піридину гідрохлориду [(d)-3]. Розчин (1)-2 (20мг) у 1мл метанолу охолодили до -10°С (льодяний ацетон). Додали надлишок тіонілхлориду. Після додавання, суміш нагріли до кімнатної температури та перемішували протягом ночі. Надлишок тіонілхлориду та розчинник видули струменем азоту та осад висушили у вакуумі. Сирий продукт проаналізували з допомогою HPLC (Sumichiral, QA-4900, 4мм´25см; Розчинники: 53,8% 1,2-дихлоретану, 44% гексану, 2,2% етанолу, та 0,1% TFA; Швидкість потоку: 0,8мл/хвилину; X=254нм), яка показала >97% ее (d)-3. Синтез (d)-енантіомеру(4aRS,5SR,9bRS)-2eтил-2,3,4,4a,5,9b-гексагідро-7-метил-5-(4карбоксифеніл)-1H-індено[1,2-с]піридину гідрохлориду [(d)-2] та (і)-енантіомеру (4аRS,5SR,9bRS)-2етил-2,3,4,4а,5,9b-гексагідро-7-метил-5-(4карбометоксифеніл)-1H-індено[1,2-с]піридину гідрохлориду [(1)-3]. Ці дві сполуки можуть бути синтезовані починаючи з еноїлсултаму (d)-13, описаного вище, та виконуючи послідовні стадії, використані вище для синтезу їх енантіомерів. їх властивості описані вище. [Дивись Cook та інші, J. Med. Chem., 38: 753763 (1995)]. Очевидно, численні модифікації та варіації даного винаходу є можливими у світлі описаних вище ідей. Тому, слід розуміти, що в області доданої формули винаходу, винахід може бути застосований іншим способом, ніж це конкретно описано у описі. 51 Комп’ютерна в ерстка Н. Лисенко 82864 Підписне 52 Тираж 26 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюSpermicidal and/or antifungal composition and methods of using the same
Автори англійськоюCook Clarence Edgar, Sloan Carol Delta, Thomas Brian Frazier, Navarro Hernan A.
Назва патенту російськоюСпермицидная и/или противогрибковая композиция и способы ее применение
Автори російськоюКук Кларенс Эдгар, Слоун Керол Делта, Томас Брайен Фрезиер, Наварро Гернан А.
МПК / Мітки
МПК: A61K 31/473
Мітки: способи, сперміцидна, протигрибкова, композиція, застосування
Код посилання
<a href="https://ua.patents.su/26-82864-spermicidna-ta-abo-protigribkova-kompoziciya-ta-sposobi-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Сперміцидна та/або протигрибкова композиція та способи її застосування</a>
Попередній патент: Пристрій для розкриття і закриття посівної борозни та сільськогосподарська машина, що містить такий пристрій
Наступний патент: Пристрій для поліпшення сумішоутворення в карбюраторному двигуні внутрішнього згоряння
Випадковий патент: Зубчаста передача












