Імплантований пристрій для введення рисперидону та спосіб його використання
Формула / Реферат
1. Спосіб доставки суб'єктові рецептури, що містить ефективну кількість рисперидону, який включає введення суб'єктові імплантованого пристрою, що містить:
а) полімер на основі поліуретану, якому надається така форма, щоб обмежувати незаповнений простір; і
b) тверду рецептуру лікарського препарату, що містить рисперидон, і, за потреби, один або декілька фармацевтично прийнятних носіїв, при цьому зазначена тверда форма рисперидону міститься у вказаному незаповненому просторі.
2. Спосіб за п. 1, який відрізняється тим, що полімер на основі поліуретану утворений одним або декількома багатоатомними спиртами, при цьому загальна структура багатоатомного спирту вибирається з групи, що складається з:
-[О-(СН2)n]х-О-;
О-(СН2-СН2-СН2-СН2)х-О-; і
О-[(СН2)6-СО3]n-(СН2)-О-.
3. Спосіб за п. 2, який відрізняється тим, що багатоатомний спирт містить -[O-(СН2)n]x-O- і в якому полімер на основі поліуретану має рівноважний вологовміст між близько 5 % - 200 %.
4. Спосіб за п. 3, який відрізняється тим, що полімер на основі поліуретану має рівноважний вологовміст принаймні близько 15 %.
5. Спосіб за п. 2, який відрізняється тим, що рисперидон вивільняється із швидкістю нульового порядку близько 149 мкг/добу на квадратний сантиметр площі поверхні імплантованого пристрою.
6. Спосіб за п. 2, який відрізняється тим, що багатоатомний спирт містить -[O-(СН2)n]x-O- і в якому полімер на основі поліуретану має модуль пружності на вигин між близько 689,5-63430 ньютон на квадратний сантиметр.
7. Спосіб за п. 6, який відрізняється тим, що полімер на основі поліуретану має модуль пружності на вигин близько 1568 ньютон на квадратний сантиметр.
8. Спосіб за п. 6, який відрізняється тим, що рисперидон вивільняється із швидкістю нульового порядку близько 146 мкг/добу на квадратний сантиметр площі поверхні імплантованого пристрою.
9. Спосіб за п. 2, який відрізняється тим, що багатоатомний спирт містить O-[(СН2)6-СО3]n-(СН2) -O- і при якому полімер на основі поліуретану має модуль пружності на вигин між біля 427,5-63430 ньютон на квадратний сантиметр.
10. Спосіб за п. 9, який відрізняється тим, що полімер на основі поліуретану має модуль пружності на вигин близько 427,5 ньютон на квадратний сантиметр.
11. Спосіб за п. 9, який відрізняється тим, що рисперидон вивільняється із швидкістю нульового порядку близько 40 мкг/добу на квадратний сантиметр площі поверхні імплантованого пристрою.
12. Пристрій доставки лікарських засобів призначений для контрольованого вивільнення рисперидону протягом тривалого періоду часу з тим, щоб забезпечити досягнення місцевої або системної фармакологічної дії, що містить:
a) полімер на основі поліуретану, якому надається така форма, щоб обмежувати незаповнений простір; і
b) тверду рецептуру лікарського препарату, що містить рисперидон, і, за потреби, один або декілька фармацевтично прийнятних носіїв, при цьому тверда рецептура лікарського препарату міститься в зазначеному незаповненому просторі і при цьому пристрій забезпечує бажану швидкість вивільнення рисперидону з пристрою після імплантації.
13. Пристрій за п. 12, який відрізняється тим, що йогокондиціонують і активують в умовах, вибраних так, щоб бути сумісними з показниками розчинності у воді принаймні одного активного компоненту.
14. Пристрій за п. 13, який відрізняється тим, що фармацевтично прийнятний носій є стеариновою кислотою.
15. Пристрій за п. 12, який відрізняється тим, що полімер на основі поліуретану утворений одним або декількома багатоатомними спиртами, при цьому загальна структура багатоатомного спирту вибирається з групи, що складається з:
-[О-(СН2)n]х-О-;
O-(СН2-СН2-СН2-СН2)х-О-; і
О-[(СН2)6-СО3]n-(СН2)-О-.
16. Пристрій за п. 15, який відрізняється тим, що багатоатомний спирт містить -[O-(СН2)n] х-O- та при якому полімер на основі поліуретану має рівноважний вологовміст між близько 5 % - 200 %.
17. Пристрій за п. 16, який відрізняється тим, що полімер на основі поліуретану має рівноважний вологовміст принаймні близько 15 %.
18. Пристрій за п. 15, який відрізняється тим, що рисперидон вивільняється із швидкістю нульового порядку близько 149 мкг/добу на квадратний сантиметр площі поверхні імплантованого пристрою.
19. Пристрій за п. 15, який відрізняється тим, що багатоатомний спирт містить -[O-(СН2)n]х-O- і при якому полімер на основі поліуретану має модуль пружності на вигин між близько 689,5-63430 ньютон на квадратний сантиметр.
20. Пристрій за п. 19, який відрізняється тим, що полімер на основі поліуретану має модуль пружності на вигин близько 1586 ньютон на квадратний сантиметр.
21. Пристрій за п. 19, який відрізняється тим, що рисперидон вивільняється із швидкістю нульового порядку близько 146 мкг/добу на квадратний сантиметр площі поверхні імплантованого пристрою.
22. Пристрій за п. 15, який відрізняється тим, що багатоатомний спирт містить O-[(СН2)6-СО3]n(СН2)-O- і в якому полімер на основі поліуретану має модуль пружності на вигин між близько 427,5-63430 ньютон на квадратний сантиметр.
23. Пристрій за п. 22, який відрізняється тим, що полімер на основі поліуретану має модуль пружності на вигин близько 427,5 ньютон на квадратний сантиметр.
24. Пристрій за п. 22, який відрізняється тим, що рисперидон вивільняється із швидкістю нульового порядку близько 40 мкг/добу на квадратний сантиметр площі поверхні імплантованого пристрою.
25. Пристрій за п. 12, який відрізняється тим, що в цілях встановлення бажаних швидкостей доставки принаймні одного активного компоненту можуть бути вибрані відповідні параметри кондиціонування і активації, при цьому параметрами активації є час, температура, кондиціонуюче середовище та активуюче середовище.
Текст
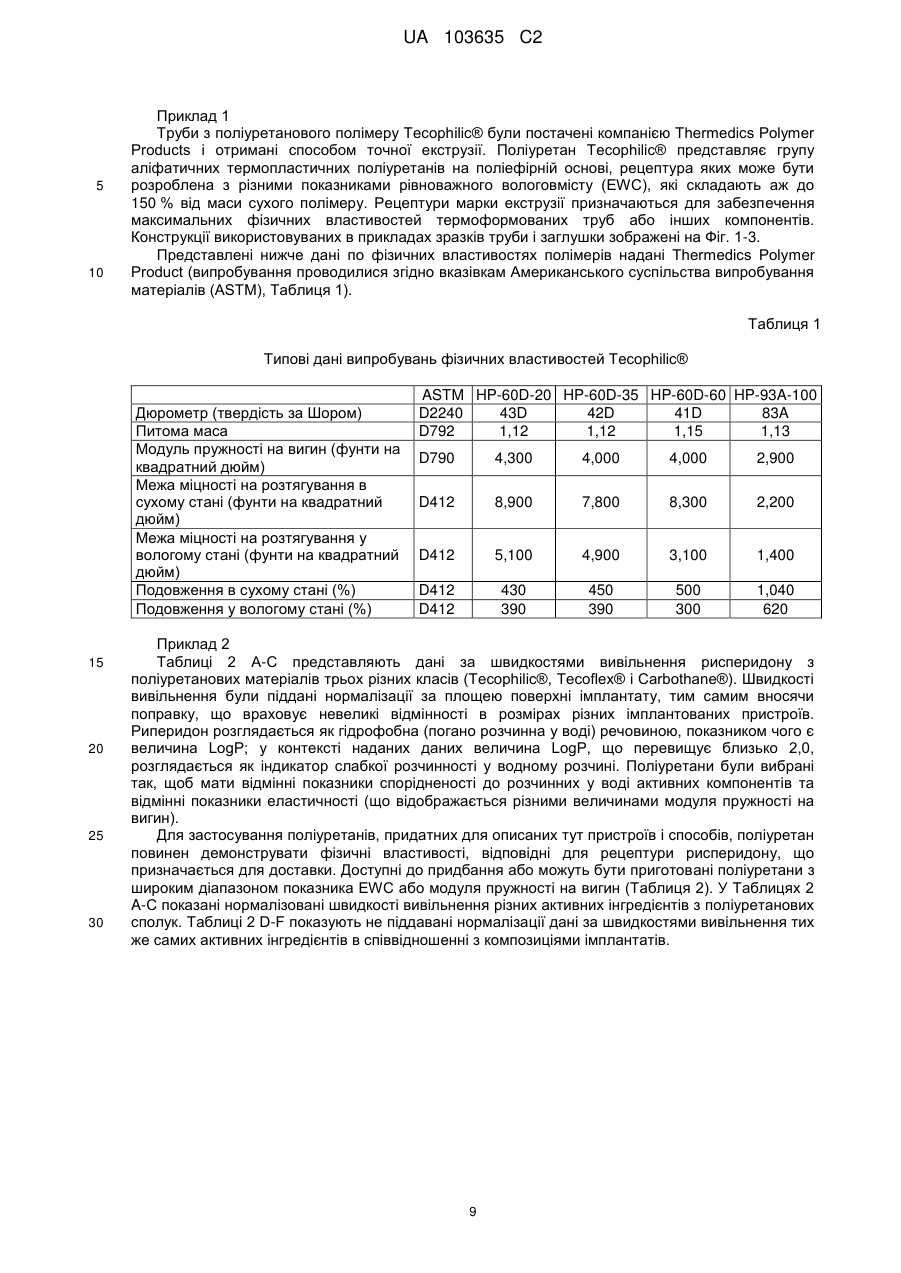
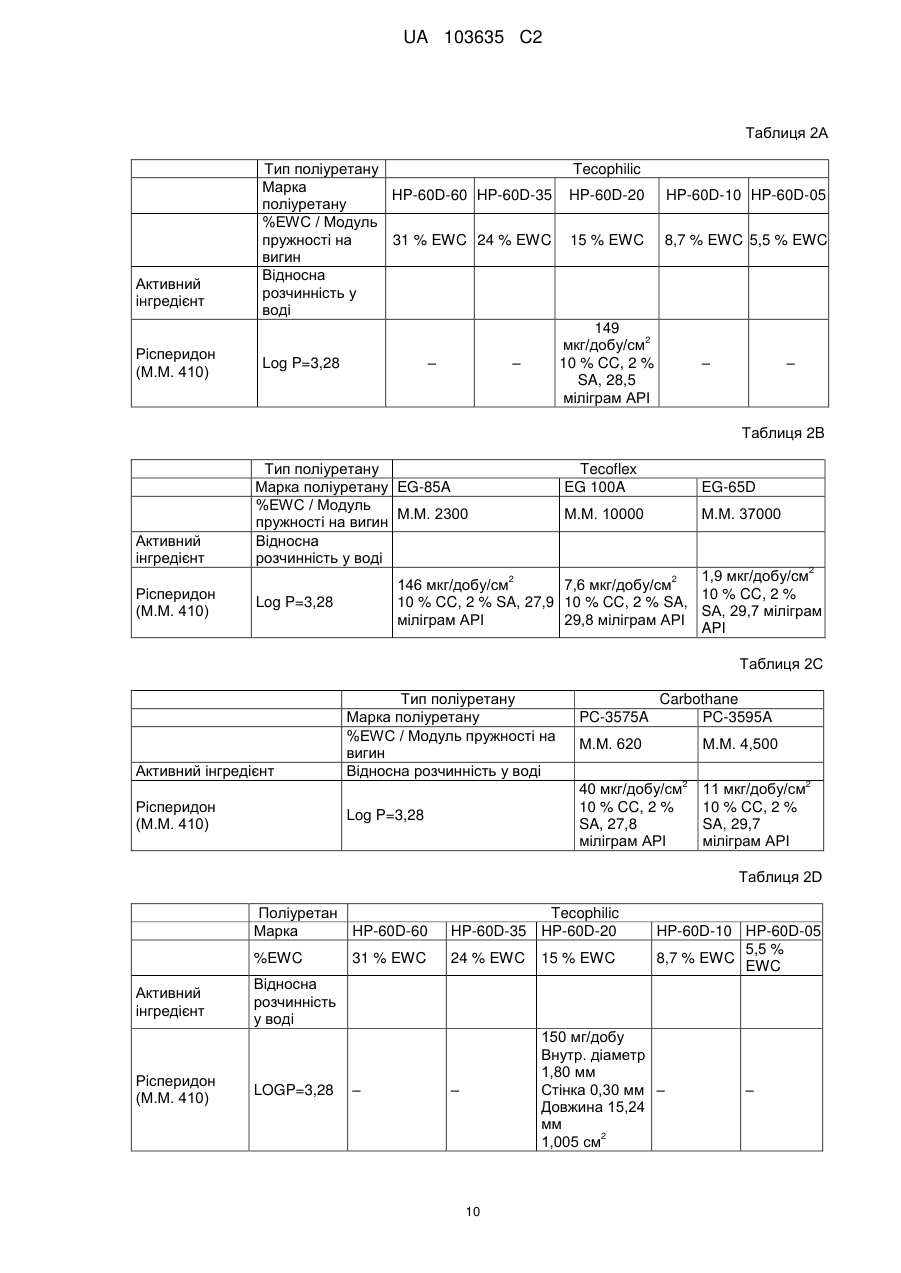
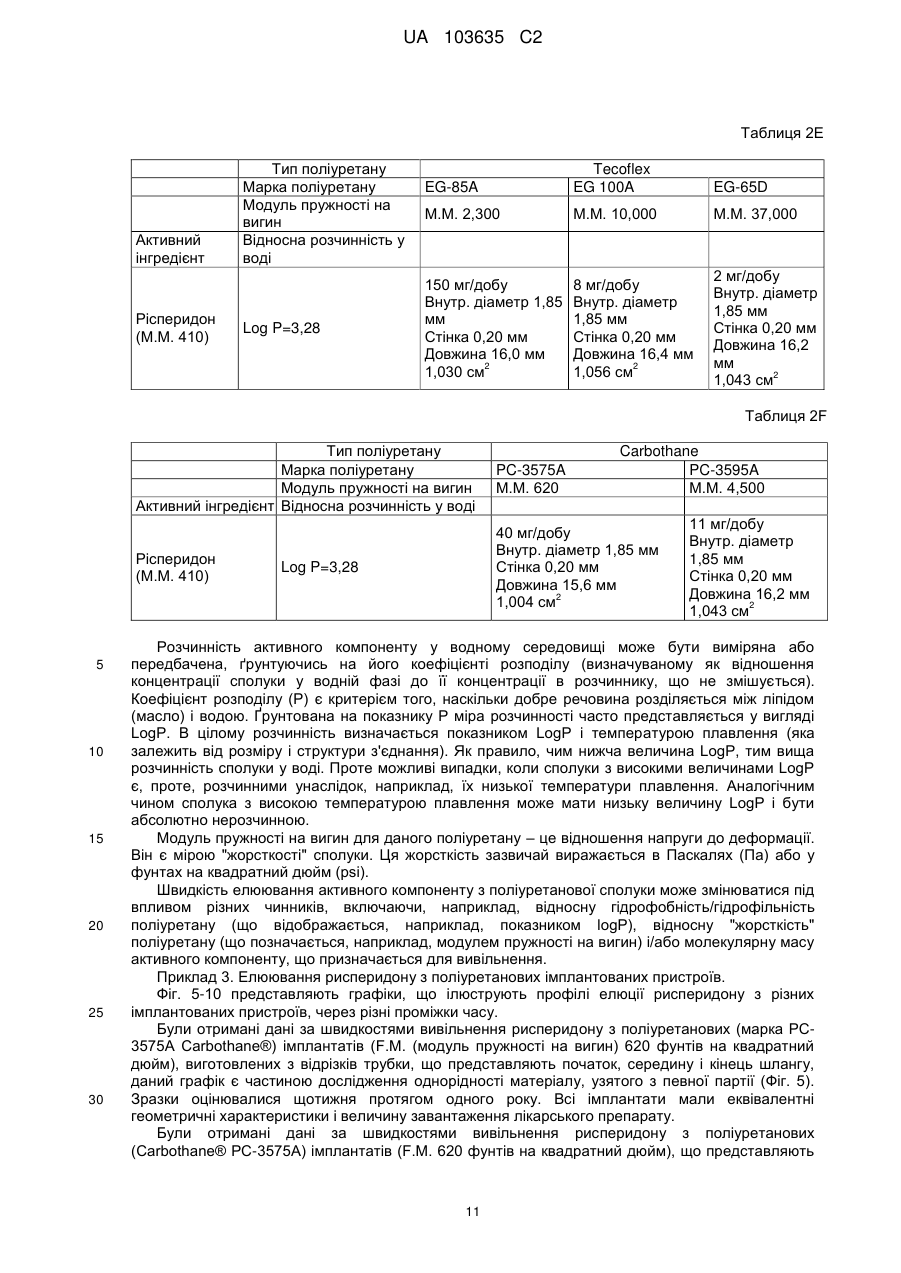
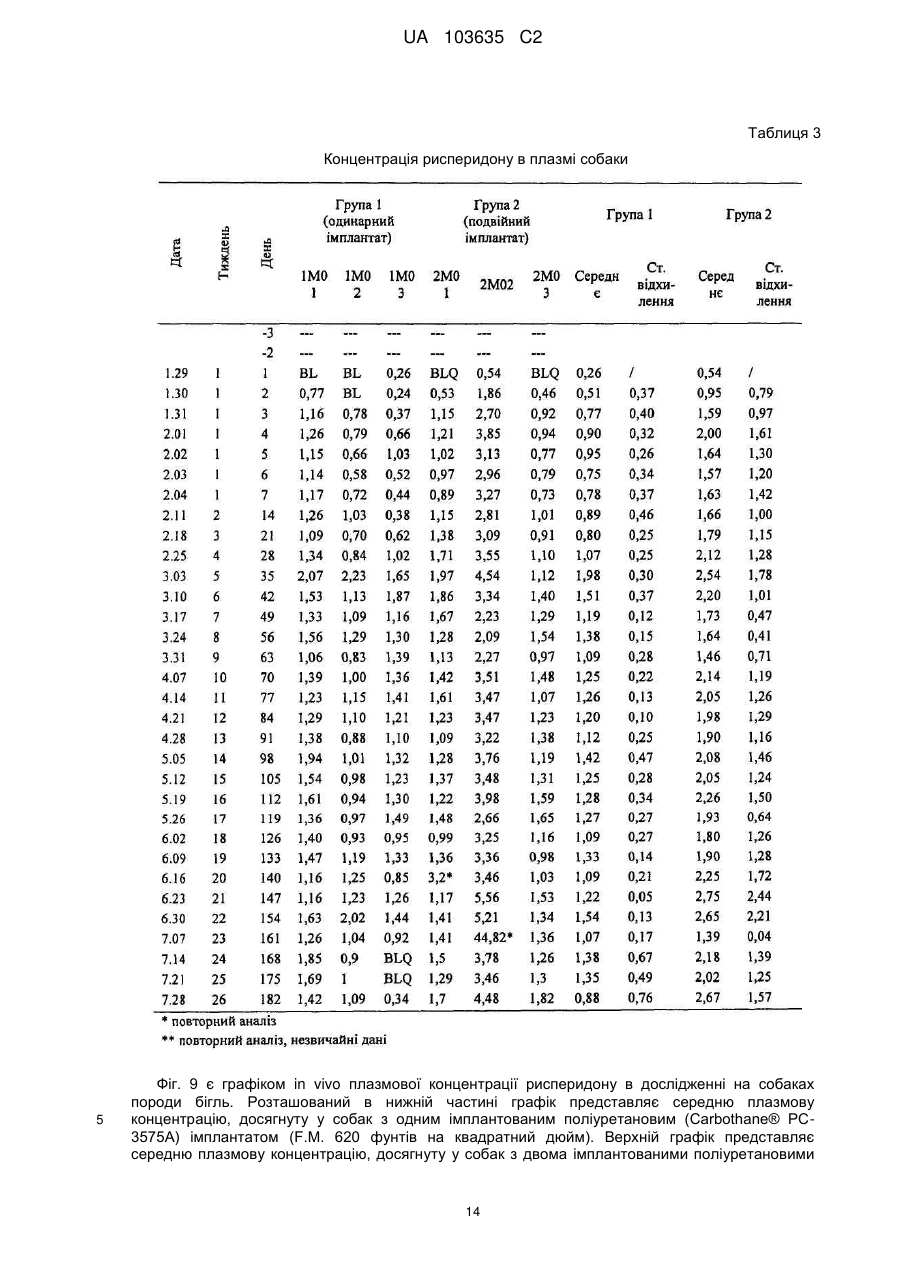
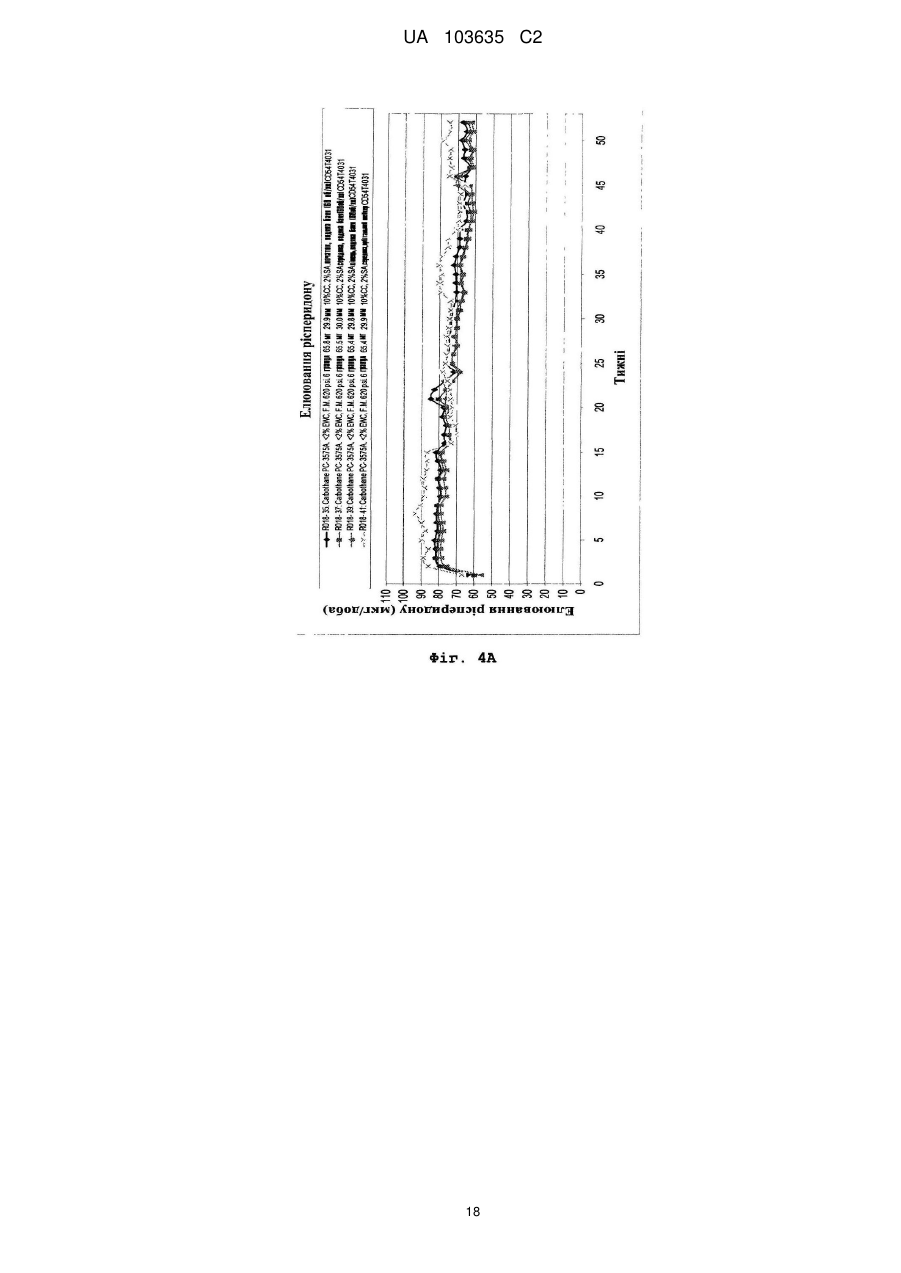
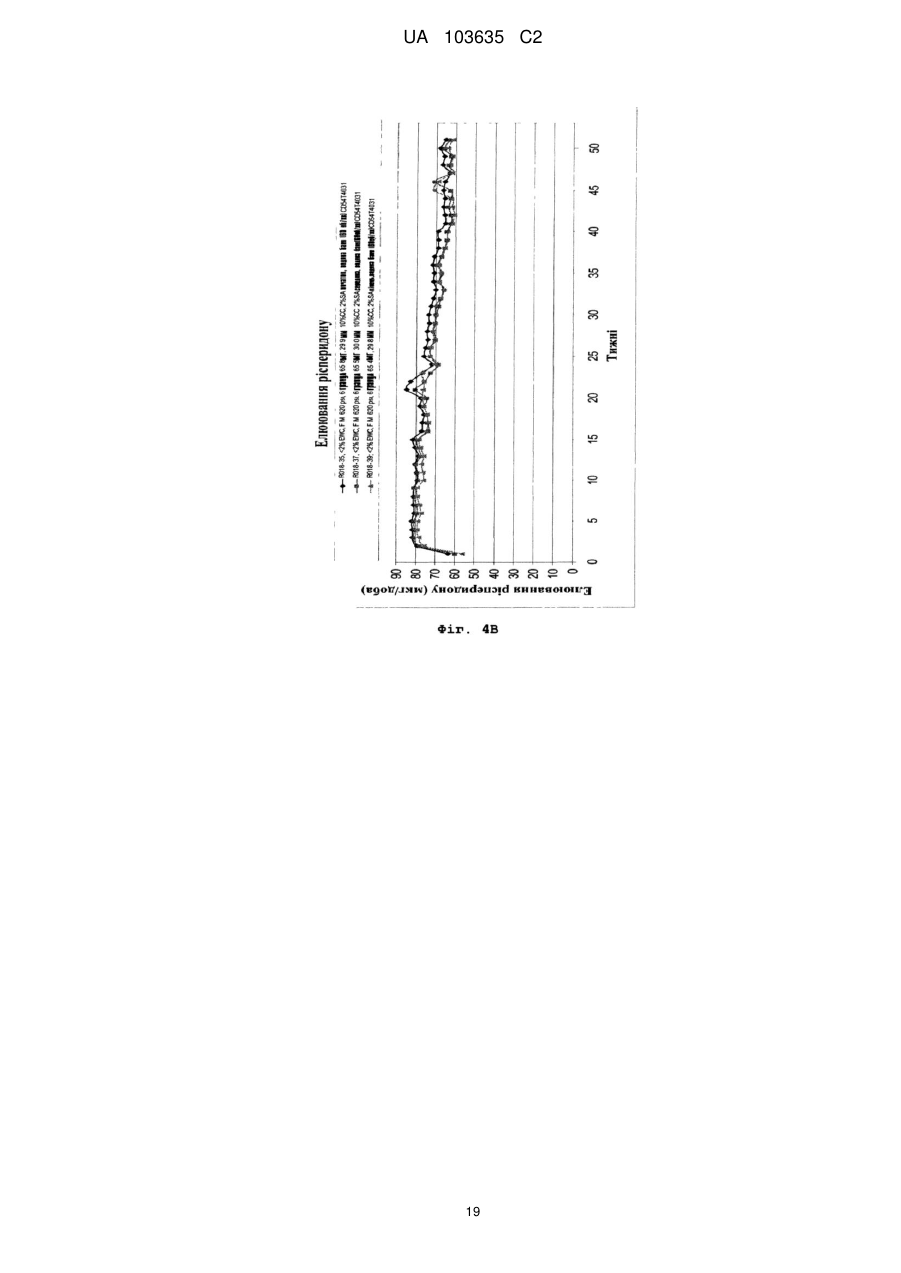
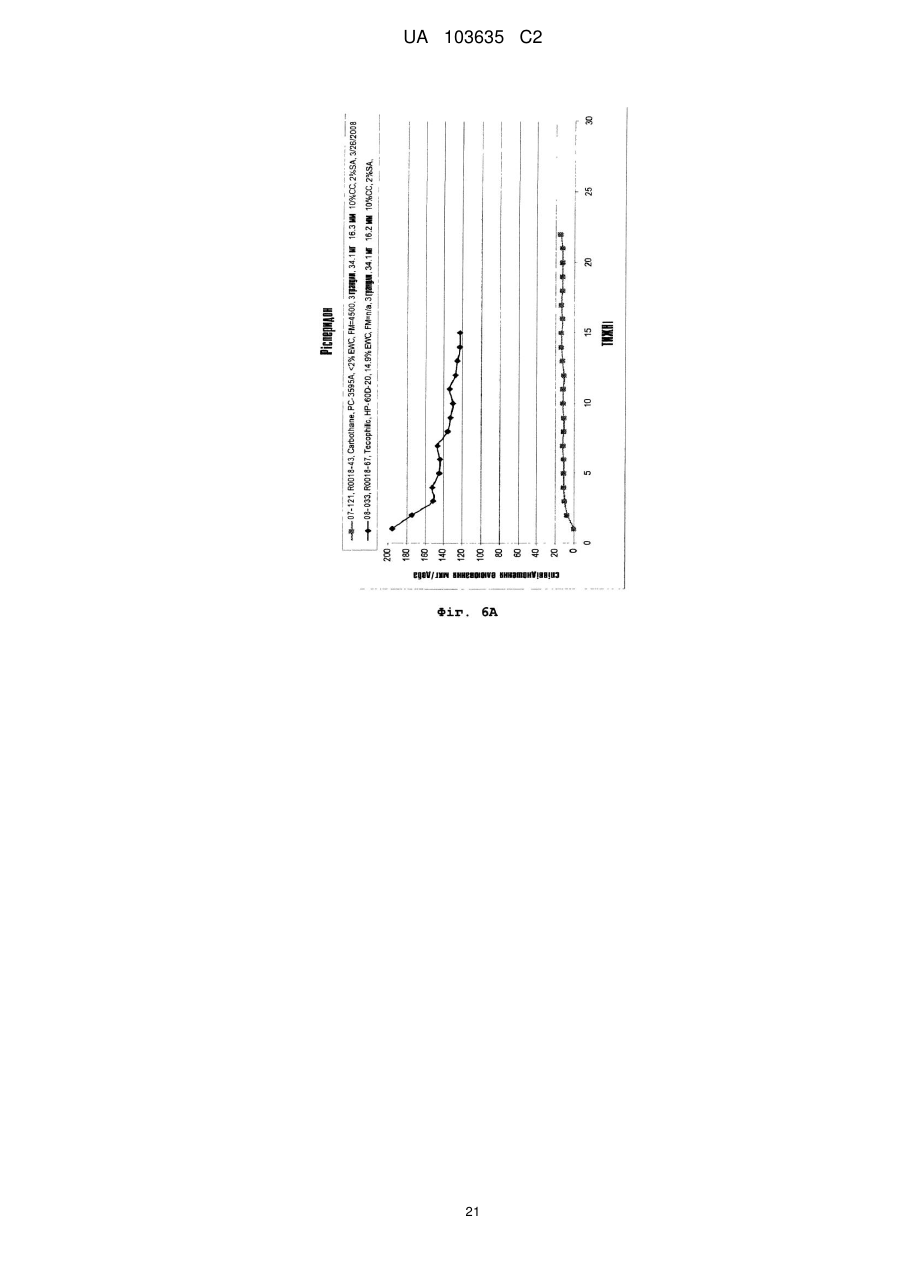
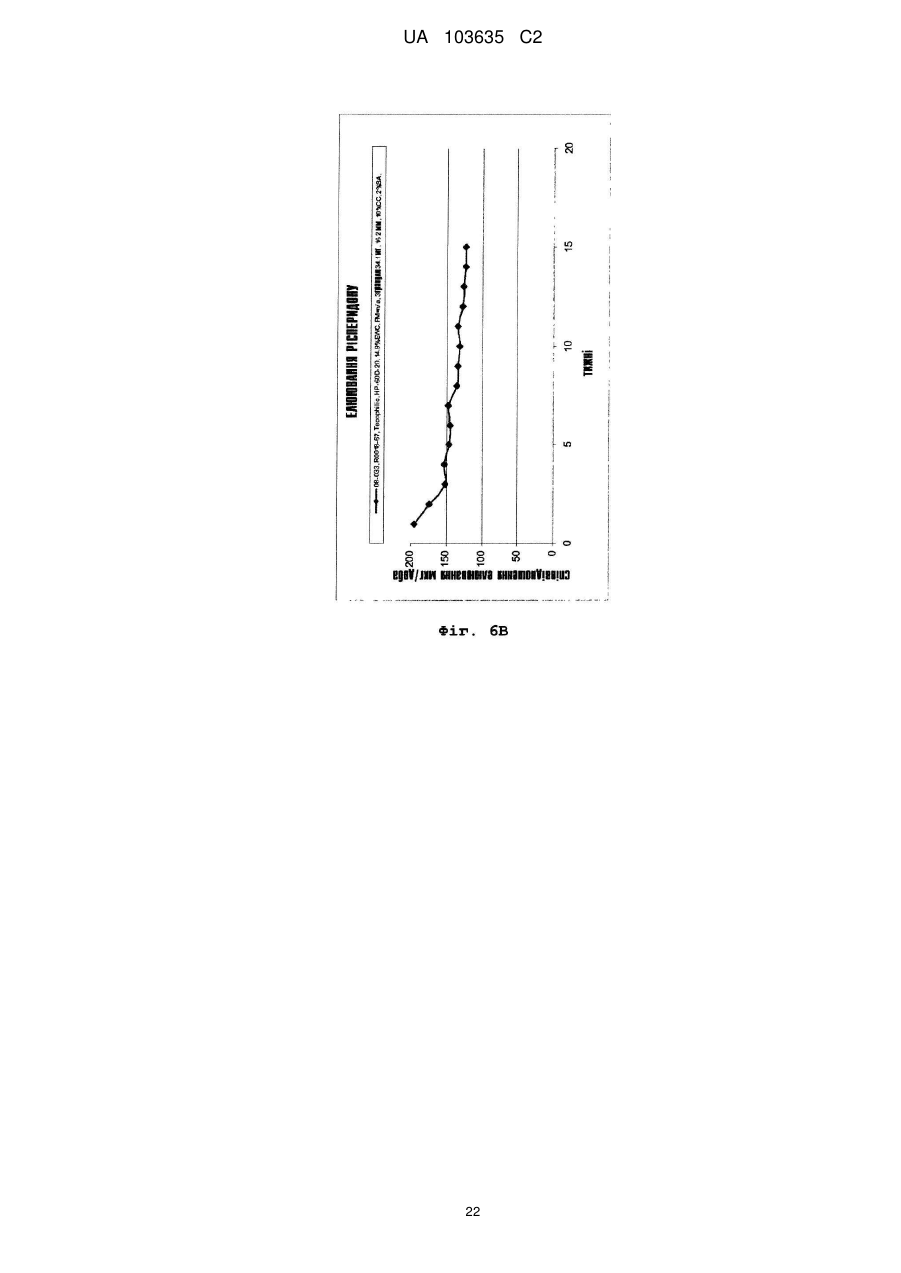
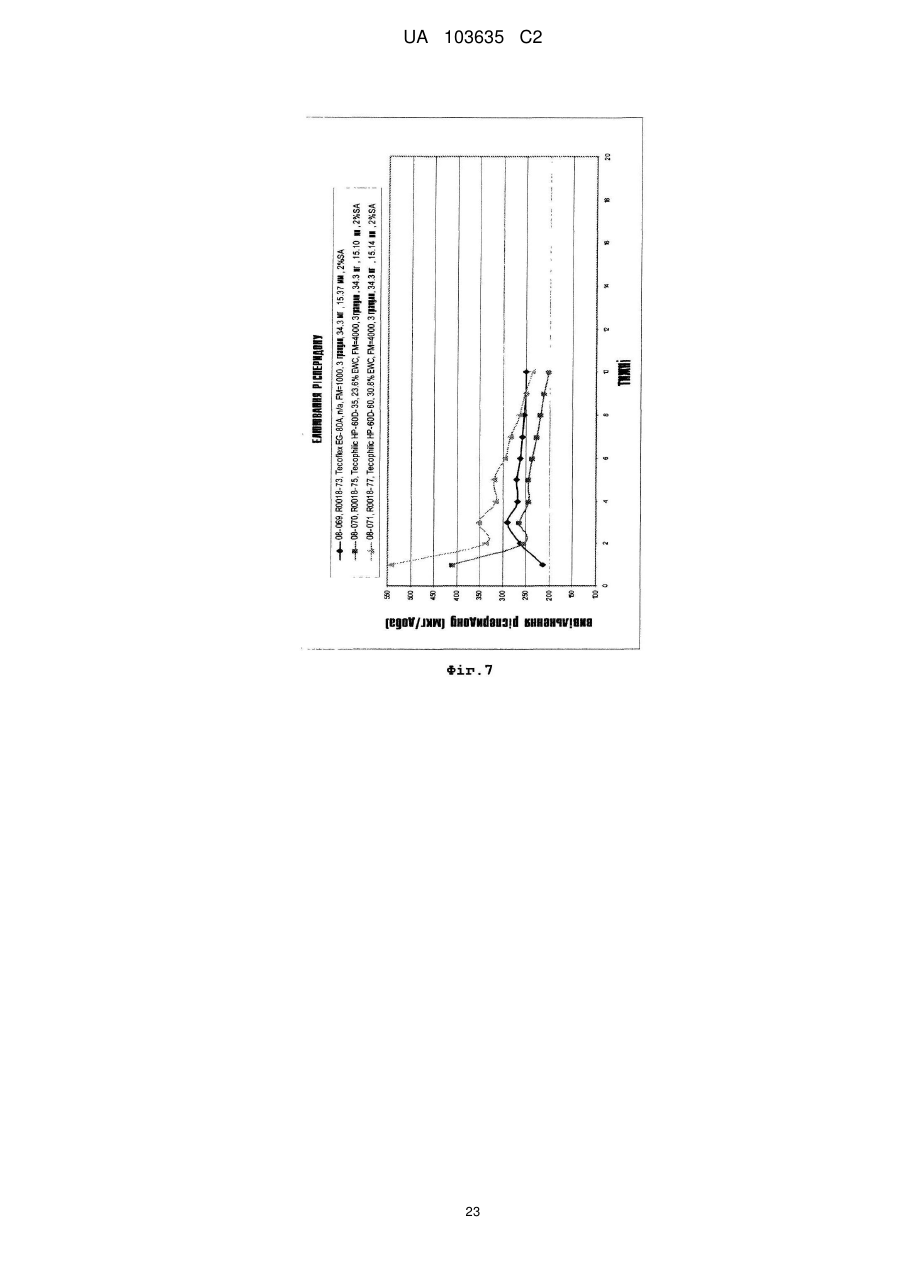
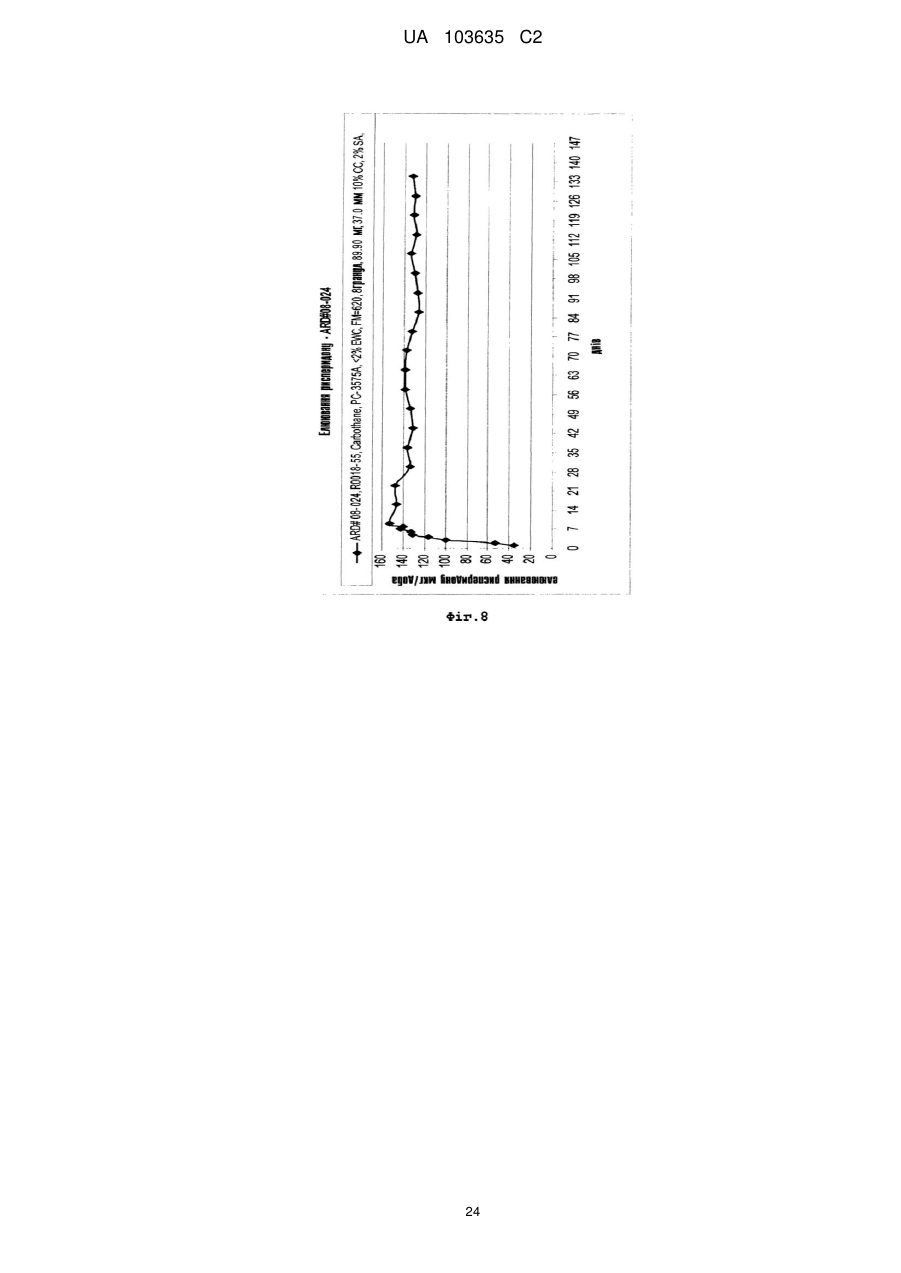
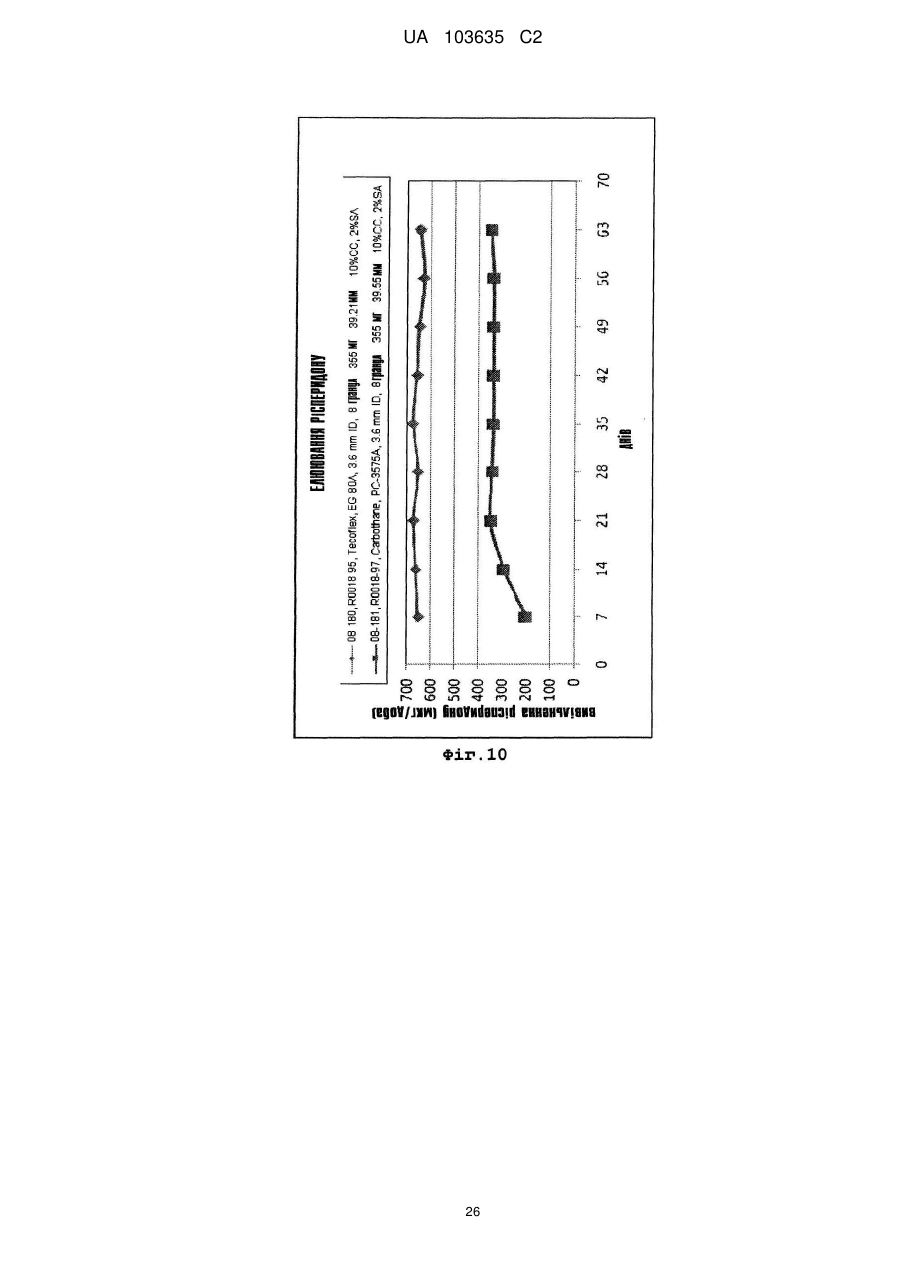
Реферат: Винахід належить до застосування полімеру на основі поліуретану як пристрою введення лікарських засобів для забезпечення доставки рисперидону з постійною швидкістю протягом тривалого періоду часу, а також до способів його виготовлення, де рисперидон міститься у незаповненому просторі, утвореному вказаним полімером. UA 103635 C2 (12) UA 103635 C2 UA 103635 C2 5 10 15 20 25 30 35 40 45 50 55 60 Рівень техніки Завдяки чудовій біосумісності, біостабільності та фізичним властивостям, поліуретан або полімери, що містять поліуретан, застосовуються для виготовлення великого числа імплантованих пристроїв, включаючи електроди кардіо-стимуляторів, штучні серця, клапани серця, покриття для стентів, штучні сухожилля, артерії та вени. Проте рецептури для доставки активних компонентів за допомогою поліуретанових імплантованих пристроїв, для дифузії лікарського препарату із швидкістю нульового порядку вимагають застосування рідкого середовища або носія. Розкриття винаходу Описані тут способи і композиції ґрунтуються на несподіваному відкритті того, що в серцевині (ядрі) поліуретанового імплантованого пристрою, можуть застосовуватися тверді рецептури, які містять один або декілька активних компонентів, так, щоб активний компонент вивільнявся з імплантованого пристрою, шляхом контрольованого вивільнення з кінетикою нульового порядку. Виходячи з різних фізичних параметрів, можуть бути вибрані активні компоненти і поліуретанове покриття, а потім, ґрунтуючись на клінічних і/або випробуваннях in vitro, може бути оптимізована швидкість вивільнення активного компоненту з імплантованого пристрою, до клінічно значущого показника швидкості вивільнення. Одне втілення винаходу направлене на спосіб доставки суб'єктові рецептури, що містить ефективну кількість рисперидону, який включає імплантацію суб'єктові пристрою, який містить рисперидон або його рецептуру, суттєво оточену полімером на основі поліуретану. У одному переважному втіленні полімер на основі поліуретану утворений одним або декількома багатоатомними спиртами, при цьому загальна структура багатоатомного спирту вибирається з групи, що складається з -[O-(CH2)n]x-O-; O-(CH2-CH2-CH2-CH2)x-O-; і O-[(CH2)6-CO3]n-(CH2)-O-. Для описаних тут композицій і способів величини n та x є цілими числами між близько 11'000'000; між близько 2-500'000; між близько 5-250'000; та між близько 10 і – 100'000. У одному переважному втіленні багатоатомний спирт містить -[O-(CH2)n]x-O-, при цьому полімер на основі поліуретану має рівноважний вологовміст між близько 5 % - 200 %, наприклад, принаймні близько 15 %. У одному переважному втіленні рисперидон вивільняється із швидкістю нульового порядку близько 149 мкг/добу на квадратний сантиметр площі поверхні імплантованого пристрою. У одному переважному втіленні багатоатомний спирт містить O-(CH2CH2-CH2-CH2)x-O-, при цьому полімер на основі поліуретану має величину модуля пружності на вигин між близько 1000 і близько 92000 фунтів на квадратний дюйм, наприклад, близько 2300 фунтів на квадратний дюйм. У одному переважному втіленні рисперидон вивільняється із швидкістю нульового порядку близько 146 мкг/добу на квадратний сантиметр площі поверхні імплантованого пристрою. У одному переважному втіленні багатоатомний спирт містить O[(CH2)6-CO3]n-(CH2)-O-, при цьому полімер на основі поліуретану має величину модуля пружності на вигин між близько 620 і близько 92000 фунтів на квадратний дюйм, наприклад, близько 620 фунтів на квадратний дюйм. У одному переважному втіленні рисперидон вивільняється із швидкістю нульового порядку близько 40 мкг/добу на квадратний сантиметр площі поверхні імплантованого пристрою. Одне втілення направлене на пристрій введення (доставки) лікарських засобів для контрольованого вивільнення рисперидону протягом тривалого періоду часу з тим, щоб забезпечити досягнення місцевої або системної фармакологічної дії, і при цьому містить: а) полімер на основі поліуретану, якому надається така форма, щоб обмежувати незаповнений простір; і b) тверду рецептуру лікарського препарату, що містить рисперидон, і можливо один або декілька фармацевтично прийнятних носіїв, при цьому тверда рецептура лікарського препарату міститься в незаповненому просторі і при цьому даний пристрій забезпечує бажану швидкість вивільнення рисперидону з пристрою після імплантації. У одному переважному втіленні пристрій доставки лікарських засобів кондиціонують і активують відповідно до умов, вибраних так, щоб бути сумісним з показниками розчинності у воді принаймні одного активного компоненту. У одному переважному втіленні фармацевтично прийнятний носій є стеариновою кислотою. У одному переважному втіленні полімер на основі поліуретану утворений одним або декількома багатоатомними спиртами, при цьому загальна структура багатоатомного спирту вибирається з групи, що складається з -[O-(CH2)n]x-O-; O-(CH2-CH2-CH2-CH2)x-O-; і O-[(CH2)6-CO3]n-(CH2)-O 1 UA 103635 C2 5 10 15 20 25 30 35 40 45 50 55 60 У одному переважному втіленні багатоатомний спирт містить -[O-(CH2)n]x-O-, при цьому полімер на основі поліуретану має рівноважний вологовміст між близько 5 % - 43 %, наприклад, принаймні близько 15 %. У одному переважному втіленні рисперидон вивільняється із швидкістю нульового порядку близько 149 мкг/добу на квадратний сантиметр площі поверхні імплантованого пристрою. У одному переважному втіленні багатоатомний спирт містить O-(CH2CH2-CH2-CH2)x-O-, при цьому полімер на основі поліуретану має величину модуля пружності на вигин між близько 1 000 і близько 92 000 фунтів на квадратний дюйм, наприклад, близько 2 300 фунтів на квадратний дюйм. У одному переважному втіленні рисперидон вивільняється із швидкістю нульового порядку близько 146 мкг/добу на квадратний сантиметр площі поверхні імплантованого пристрою. У одному переважному втіленні багатоатомний спирт містить O[(CH2)6-CO3]n-(CH2)-O-, при цьому полімер на основі поліуретану має величину модуля пружності на вигин між близько 620 і близько 92 000 фунтів на квадратний дюйм, наприклад, близько 620 фунтів на квадратний дюйм. У одному переважному втіленні рисперидон вивільняється із швидкістю нульового порядку близько 40 мкг/добу на квадратний сантиметр площі поверхні імплантованого пристрою. У одному переважному втіленні в цілях встановлення бажаних швидкостей доставки, принаймні, одного активного компоненту можуть бути вибрані відповідні параметри кондиціонування і активації, при цьому параметрами активації є час, температура, кондиціонуюче середовище і активуюче середовище. Короткий опис креслень Фіг. 1 є видом збоку імплантату з двома відкритими кінцями. Фіг. 2 є видом збоку готових торцевих заглушок, використовуваних для закупорювання імплантатів. Фіг. 3 є видом збоку імплантату з одним відкритим кінцем. Фіг. 4 є графіком швидкості вивільнення рисперидону з поліуретанових (марка PC-3575A Carbothane®) імплантатів (модуль пружності на вигин 620 фунтів на квадратний дюйм), виготовлених з відрізків трубки, що представляють початок, середину і кінець шланга, даний графік є частиною дослідження однорідності матеріалу, узятого з певної партії. Зразки оцінювалися щотижня протягом одного року. Всі імплантати мали еквівалентні геометричні характеристики і величину завантаження лікарського препарату. Фіг. 5 є графіком швидкості вивільнення рисперидону з поліуретанових (Carbothane® PC3575A) імплантатів (модуль пружності на вигин 620 фунтів на квадратний дюйм), що представляє частину дослідження ефекту застосування в якості елююючого середовища фізіологічного розчину порівняно з водним розчином оксипропіл-бета-целюлози (15 % у фізіологічному розчині з фосфатним буфером). Зразки оцінювалися щотижня протягом 11 тижнів. Всі імплантати мали еквівалентні геометричні характеристики і величину завантаження лікарського препарату. Фіг. 6A і 6B є графіками, що порівнюють швидкості вивільнення рисперидону з імплантатів, виготовлених з поліуретану Carbothane® PC-3595A (модуль пружності на вигин 4 500 фунтів на квадратний дюйм), та імплантатів, виготовлених з поліуретану Tecophilic® HP-60D-20 (EWC (рівноважний вологовміст) 14,9 %), що є частиною оцінки вивільнення активного компоненту з будь-яких гідрофільних і гідрофобних поліуретанових матеріалів. Для імплантату Carbothane® зразки оцінювалися щотижня протягом 22 тижнів. У разі імплантату Tecophilic® зразки оцінювалися щотижня протягом 15 тижнів. Всі імплантати мали еквівалентні геометричні характеристики і величину завантаження лікарського препарату. Фіг. 11B є графіком швидкості вивільнення рисперидону тільки з поліуретанових (Tecophilic® HP-60D-20) імплантатів (EWC 14,9 %), виміри по яких проводилися щотижня протягом 15 тижнів. Фіг. 7 є графіком, що порівнює швидкості вивільнення рисперидону з імплантатів, виготовлених з поліуретану Tecoflex® EG-80A (модуль пружності на вигин 1 000 фунтів на квадратний дюйм), і двох марок поліуретану Tecophilic®, HP-60D-35 і HP-60D-60 (EWC 23,6 % і 30,8 %, відповідно). Вимірювання проводилися щотижня протягом 10 тижнів. Всі імплантати мали еквівалентні геометричні характеристики і величину завантаження лікарського препарату. Фіг. 8 є графіком швидкості вивільнення рисперидону з поліуретанових (Carbothane® PC3575A) імплантатів (модуль пружності на вигин 620 фунтів на квадратний дюйм), які служили in vitro як контрольні для імплантатів, що застосовувалися в описаному в прикладі 8 дослідженні на собаках породи бігль. Дослідження in vitro елюції з цих імплантатів було почате в день імплантації імплантатів, що є об'єктом винаходу, як частина вивчення in vivo-in vitro кореляції. Фіг. 9 є графіком in vivo плазмової концентрації рисперидону в описаному в прикладі 8 дослідженні на собаках породи бігль. Розташований в нижній частині графік представляє середню плазмову концентрацію, досягнуту у собак з одним імплантованим поліуретановим 2 UA 103635 C2 5 10 15 20 25 30 (Carbothane® PC-3575A) імплантатом (модуль пружності на вигин 620 фунтів на квадратний дюйм). Верхній графік представляє середню плазмову концентрацію, досягнуту у собак з двома імплантованими поліуретановими (Carbothane® PC-3575A) імплантатами (модуль пружності на вигин 620 фунтів на квадратний дюйм). Фіг. 10 є графіком, що демонструє in vitro вивільнення рисперидону з імплантатів Tecoflex® і Carbothane®. Гранули, що містять рецептуру рисперидону, мали діаметр 3,5 мм, довжина близько 4,5 мм і маса 5,4 міліграм. Імплантат мав довжину резервуару близько 39-40 мм, товщину стінки 0,2 мм і внутрішній діаметр 3,6 мм при загальній довжині близько 45 мм. Фіг. 11 є графіком, що демонструє in vitro вивільнення рисперидону з імплантатів Tecoflex® і Carbothane® порівняно з контролем. Гранули, що містять рецептуру рисперидону, мали діаметр 3,5 мм, довжину близько 4,5 мм і масу 5,4 міліграм. Імплантат мав довжину резервуару близько 39-40 мм, товщину стінки 0,2 мм і внутрішній діаметр 3,6 мм при загальній довжині близько 45 мм. Здійснення винаходу Для того, щоб скористатися перевагами, що надаються чудовими властивостями полімерів на основі поліуретану, цей винахід звертається до застосування полімерів на основі поліуретану у вигляді пристрою для доставки лікарських засобів за допомогою вивільнення лікарських засобів з контрольованою швидкістю протягом тривалого періоду часу в цілях забезпечення місцевого або системного фармакологічного ефекту. Пристрій доставки лікарських засобів може містити резервуар циліндрової форми, оточений полімером на основі поліуретану, який контролює швидкість доставки лікарського препарату в резервуарі. Резервуар містить рецептуру, наприклад, тверду рецептуру, що включає один або декілька активних інгредієнтів і, можливо, фармацевтично прийнятних носіїв. Рецептури носіїв розроблені так, щоб сприяти дифузії активних інгредієнтів через полімер і забезпечувати рівноважний вміст лікарських препаратів в резервуарі. Поліуретан є будь-яким полімером, що складається з ланцюжка органічних ланок, сполучених уретановими зв'язками. Поліуретанові полімери утворюються в результаті реакції, що протікає у присутності каталізатора, мономера, який містить, принаймні, дві ізоціанатні функціональні групи, з іншим мономером, що містить, принаймні, дві спиртові групи. Рецептури поліуретанів охоплюють широкі діапазони показників жорсткості, твердості та щільності. узагальнена реакція утворення поліуретану 35 40 45 50 55 Поліуретани відносяться до класу сполук, званих "реактивними полімерами", які включають епоксидні сполуки, ненасичені поліефіри та фенольні сполуки. Уретановий зв'язок утворюється при взаємодії ізоціанатної групи –N=C=O з гідроксилом (спиртова) група – OH. Поліуретани отримують реакцією адитивної полімеризації поліізоціанату з поліолом (багатоатомний спирт) у присутності каталізатора та інших добавок. В цьому випадку поліізоціанат є молекулою з двома або більш ізоціанатними функціональними групами R-(N=C=O)n≥2, а багатоатомний спирт є молекулою з двома або більш гідроксильними функціональними групами R'-(OH)n≥2. Продуктом реакції є полімер, що містить уретановий зв'язок -RNHCOOR'-. Ізоціанати вступають в реакції з будь-якими молекулами, що містять активний водень. Важливо, що ізоціанати вступають у взаємодію з водою з утворенням угрупування сечовини і газоподібного діоксиду вуглецю; вони також вступають в реакцію з поліефірамінами з утворенням полісечовини. У промисловості поліуретани отримують реакцією рідкого ізоціанату з рідкою сумішшю багатоатомних спиртів, каталізатора та інших добавок. Ці два компоненти згадуються як поліуретанова система або просто система. Ізоціанат зазвичай згадується в Північній Америці як "компонент А" ("A-side") або просто "ізо" ("iso") і представляє жорсткий основний ланцюг (або "жорсткий сегмент") системи. Суміш багатоатомних спиртів і інших добавок зазвичай згадується як "компонент B" ("B-side") або як "полі" ("poly") і представляє функціональну ділянку (або "м'який сегмент") системи. Ця суміш може також називатися "смолою" або "смоляною сумішшю". Добавки в смоляну суміш можуть включати подовжувачі ланцюга, перехреснозшиваючі агенти, сурфактанти, вогнезахисні засоби, пороутворювачі, барвники і наповнювачі. У застосуваннях, пов'язаних з доставкою лікарських засобів, "м'які сегменти" представляють ділянки полімеру, які додають йому якості, що визначають здібність активного фармацевтичного інгредієнта (API) до дифузії через такий полімер. Пружні властивості цих матеріалів досягаються завдяки розділенню фаз твердих і м'яких співполімерних сегментів полімеру таким чином, що домени жорстких уретанових сегментів 3 UA 103635 C2 5 10 15 виконують функцію поперечного скріплення між неврегульованими доменами м'яких поліефірних сегментів. Це розділення фаз відбувається тому, що головним чином неполярні, легкоплавкі м'які сегменти несумісні з полярними, твердими сегментами з високою температурою плавлення. М'які сегменти, які утворюються високомолекулярними багатоатомними спиртами, є рухомими і зазвичай присутні в згорнутому вигляді, тоді як жорсткі сегменти, утворені ізоціанатом і подовжувачами ланцюга, є жорсткими і нерухомими. Оскільки тверді сегменти ковалентним чином пов'язані з м'якими сегментами, вони перешкоджають пластичній деформації полімерних ланцюжків, тим самим, забезпечуючи прояви високоеластичної пружності. При механічній деформації ділянка м'яких сегментів піддається розмотуючому зусиллю, а жорсткі сегменти вирівнюються відповідно до напряму навантаження. Ця переорієнтація жорстких сегментів і подальше утворення міцних водневих зв'язків сприяє досягненню високих величин міцності на розтягування, подовження та опору розриву. Реакція полімеризації каталізується третинними амінами, такими як, наприклад, диметилциклогексиламін, і металоорганічними сполуками, такими як, наприклад, дибутилдилаурат олова або октаноат вісмуту. Крім того, вибір каталізаторів може бути зроблений на основі того, чи сприяють вони утворенню при реакції уретанового гелю, як, наприклад, 1,4-диазабицикло[2.2.2]октан (також званий DABCO або TEDA), або реакції, що протікає з піноутворенням, з сечовиною, як біс(2-диметиламіноетил) ефір, або вибірково направляють реакцію тримеризації ізоціанату, як октоат калію. 20 Поліуретановий полімер, утворений взаємодією диізоціанату з багатоатомним спиртом 25 30 35 40 45 50 Для отримання поліуретанових полімерів необхідні ізоціанати з двома або більш функціональними групами. За об'ємом ароматичні ізоціанати представляють переважну більшість загального виробництва диізоціанатів. Аліфатичні і циклоаліфатичні ізоціанати також є важливими складовими поліуретанових матеріалів, але в набагато менших об'ємах. Для цього є безліч причин. По-перше, ізоціанатна група, що знаходиться в з'єднанні з ароматичною, є набагато більш реакційноздатною, ніж пов'язана з аліфатичною групою. По-друге, використання ароматичних ізоціанатів виявляється економічно вигіднішим. Аліфатичні ізоціанати застосовуються тільки у випадках, коли потрібне надання кінцевому продукту будь-яких особливих властивостей. Наприклад, тільки за допомогою аліфатичних ізоціанатів можуть бути отримані світлостійкі покриття та еластомери. Аліфатичні ізоціанати також переважні при виробництві поліуретанових біоматеріалів, унаслідок властивих їм стабільності і пружних властивостей. Приклади аліфатичних і циклоаліфатичних ізоціанатів включають, наприклад, 1,6гексаметилендиізоціанат (HDI), 1-ізоціанато-3-ізоціанатометил-3,5,5-триметилциклогексан (диізоціанат ізофорону, IPDI) і 4,4'-диізоціанатодициклогексилметан (H12MDI). Вони застосуються для отримання світлостійких, не схильних до пожовтіння поліуретанових покриттів і еластомерів. Форполімери H12MDI застосовуються для отримання високоякісних покриттів і еластомерів, що володіють оптичною прозорістю і гідролітичною стійкістю. Все поліуретани Tecoflex®, Tecophilic® і Carbothane® проводяться з форполімерів H12MDI. Багатоатомні спирти є речовинами з вищою молекулярною масою, що отримуються з ініціатора і мономірних елементарних ланок, які при вбудовуванні в поліуретанові системи представляють "м'які сегменти" полімеру. Найпростіше їх класифікувати як поліефірполіоли, отримані реакцією епоксидів (оксиранів) з ініціюючими сполуками, що містять активний водень, або поліефірполіоли, отримані поліконденсацією поліфункціональних карбонових кислот і гідроксильних з'єднань. Поліуретани Tecoflex®, поліуретани Tecogel® і поліуретани Tecophilic® є циклоаліфатичними полімерами і відносяться до типу отримуваних з багатоатомних спиртів на поліефірній основі. Для поліуретанів Tecoflex® загальна структура сегменту багатоатомного спирту представляється як O–(CH2–CH2–CH2–CH2)x–O– при цьому збільшення "x" представляє збільшення еластичності (зниження модуля пружності на вигин "FM"), призводячи до отримання показника FM в межах від близько 1 000 до 92 000 фунтів на квадратний дюйм. З погляду вивільнення з цих матеріалів лікарського 4 UA 103635 C2 5 10 15 20 25 30 35 40 45 50 55 препарату, із збільшенням показника FM вивільнення відносно гідрофобного API зменшується. Для описаних тут композицій і способів величини x є цілими числами між близько 1-1000000; між близько 2 - 500000; між близько 5-250000; і між біля 10-100000. Проте в інших втіленнях x може знаходитися в діапазоні від близько 2 до 500, від близько 2 до 100, від близько 5 до 50 і від 10 до 30. Для поліуретанів Tecophilic® (гідрофільні) або поліуретанів Tecogel® загальна структура сегменту багатоатомного спирту представляється як [O–(CH2)n]x–O– при цьому збільшення показників "n" і "x" представляє зміни в гідрофільності і призводять до величини рівноважного вологовмісту (%EWC) в межах від близько 5 % до 200 %. Для описаних тут композицій і способів величини n і x є цілими числами між близько 1-1000000; між близько 2500000; між біля 5-250000; і між близько 10-100000. Проте, в інших втіленнях показники n і x можуть мати однакові або такі, що розрізняються, величини, із значеннями в межах від близько 2 до 500, від близько 2 до 100, від близько 5 до 50 і від 10 до 30. З погляду вивільнення з цих матеріалів лікарського препарату, із збільшенням показника %EWC вивільнення відносно гідрофільного API зростає. Вибір багатоатомних спиртів включає, наприклад, полікарбонатні багатоатомні спирти, полікапролактонові багатоатомні спирти, полібутадієнові багатоатомні спирти та полісульфідні багатоатомні спирти. Поліуретани Carbothane® є циклоаліфатичними полімерами і відносяться до типу отримуваних з багатоатомних спиртів на полікарбонатній основі. Загальна структура сегменту такого багатоатомного спирту представляється як O–[(CH2)6–CO3]n–(CH2)–O– при цьому збільшення "n" представляє збільшення еластичності (зниження показника FM), призводячи до отримання показника FM в межах від близько 620 до 92 000 фунтів на квадратний дюйм. Для описаних тут композицій і способів величини n є цілими числами між біля 1-1000000; між близько 2-500000; між близько 5-250000; і між близько 10-100000. Проте в інших втіленнях n може знаходитися в діапазоні від близько 2 до 500, від близько 2 до 100, від близько 5 до 50 і від 10 до 30. З погляду вивільнення з цих матеріалів лікарського препарату, із збільшенням показника FM вивільнення відносно гідрофобного API зменшується. Подовжувачі ланцюга і перехреснозшиваючі агенти є низькомолекулярними сполуками з гідроксильними та амінними кінцевими групами, які відіграють важливу роль в морфології полімерів поліуретанових волокон, еластомерів, клейких матеріалів і деяких спінених дрібнопористих або таких, що мають монолітну поверхню, матеріалів. Приклади подовжувачів ланцюга включають, наприклад, етилгліколь, бутан-1,4-діол (1,4-BDO або BDO), гексан-1,6-діол, циклогександиметанол і гідрохінон-біс(2-гідроксиетил) ефір (HQEE). Всі ці гліколі утворюють поліуретани з фазами, що добре розділяються, створюючими чітко певні домени жорстких сегментів і що переробляються в розплаві. Всі вони є відповідними для термопластичних поліуретанів, за винятком етилгліколю, оскільки виходячий з нього біс-фенілуретан при високих рівнях вмісту жорстких сегментів схильний до несприятливої деградації. Всі поліуретани Tecophilic®, Tecoflex® і Carbothane® включають застосування як подовжувач ланцюга 1,4бутандіолу. Цей винахід надає пристрій доставки лікарських засобів, яке може забезпечити досягнення наступних цілей: контрольована швидкість вивільнення (наприклад, швидкість вивільнення нульового порядку) для максимізації терапевтичних ефектів і мінімізації небажаних побічних дій, легкий спосіб витягання пристрою у випадках, якщо необхідно завершити терапію, збільшення біологічної доступності із зменшенням відхилень у величині показника поглинання та відсутність пресистемного метаболізму. Швидкість вивільнення лікарського препарату підкоряється закону дифузії Фіка в додатку до пристрою у формі циліндрового резервуару (патрон). Залежність між різними параметрами описується наступним рівнянням де: dM/dt :швидкість вивільнення лікарського препарату; h: довжина заповненої ділянки пристрою; ∆C: градієнт концентрації упоперек стінки резервуару; ro/ri : відношення величини зовнішнього радіусу пристрою до величини його внутрішнього радіусу; і 5 UA 103635 C2 5 10 15 20 25 30 35 40 45 50 55 60 p: коефіцієнт проникності вживаного полімеру. Коефіцієнт проникності визначається перш за все гідрофільністю або гідрофобністю полімеру, структурою полімеру і взаємодією між лікарським препаратом і полімером. Для даних вибраних полімеру і активного інгредієнта p є константою, h, r o і ri фіксуються і зберігаються постійними після виготовлення пристрою, що має циліндрову форму. ∆C підтримується постійним. Для витримки геометрії пристрою настільки точною, наскільки це можливо, пристрій, наприклад, пристрій з циліндровою формою може бути отриманий за допомогою способів точного екструдування або точного литва – у разі термопластичних поліуретанових полімерів та способів реакційного литва під тиском або відцентрового литва – у разі термотужавіючих поліуретанових полімерів. Патрон може бути виготовлений або з одним закритим кінцем або з обома відкритими кінцями. Відкритий кінець може закупорюватися, наприклад, заздалегідь виготовленою торцевою заглушкою(-ми) для того, щоб забезпечити гладкість кінця і щільність закупорки, або, у разі термопластичних поліуретанів, за допомогою технологій запечатування термозварюванням, відомих фахівцям в даній області. Тверді активні інгредієнти і носії можуть пресуватися у формі гранул для забезпечення максимального завантаження активних інгредієнтів. Для забезпечення можливості ідентифікації місця локалізації імплантату в пристрій доставки може бути включений рентгеноконтрастний матеріал за допомогою внесення його до резервуару або виготовлення з нього торцевої заглушки, використовуваної для закупорки патрона. Після закупорювання з обох кінців патронів із заповненим резервуаром вони можливо піддаються кондиціонуванню і активації протягом відповідного періоду часу для того, щоб забезпечити постійну швидкість доставки. Кондиціонування пристроїв доставки лікарських засобів включає завантаження активних інгредієнтів (лікарський препарат) в полімер на основі поліуретану, який оточує резервуар. Активація виконується для того, щоб зупинити завантаження лікарського препарату в полімер на основі поліуретану і тим самим попередити втрати активного інгредієнта перед практичним застосуванням імплантату. Умови, використовувані на етапах кондиціонування і активації, залежать від активного інгредієнта, температури і середовища, в якому вони здійснюються. Умови для виконання кондиціонування і активації в деяких випадках можуть бути однаковими. Етап кондиціонування і активації в ході приготування пристроїв для доставки лікарських засобів виконується для того, щоб досягти певної швидкості вивільнення конкретного лікарського препарату. Етап кондиціонування і активації імплантату, що містить гідрофільний лікарський препарат, може виконуватися у водному середовищі, наприклад, у фізіологічному розчині. Етап кондиціонування і активації пристрою для доставки лікарських засобів, що містить гідрофобний лікарський препарат, зазвичай проводять в гідрофобному середовищі, такому як, наприклад, середовище на масляній основі. Етапи кондиціонування і активації можуть виконуватися за допомогою керування трьома певними чинниками, а саме, температурою, середовищем і періодом часу. Фахівцеві в даній області ясно, що етапи кондиціонування і активації пристрою доставки лікарських засобів піддаються дії середовища, в яке поміщається даний пристрій. Гідрофільний лікарський препарат може бути підданий кондиціонуванню і активації, наприклад, у водному розчині, наприклад, у фізіологічному розчині. Температура, вживана для кондиціонування і активації пристрою доставки лікарських засобів, може змінюватися в широкому діапазоні температур, складаючи, наприклад, біля 37ºC. Інтервал часу, використовуваний для кондиціонування і активації пристрою для доставки лікарських засобів, може варіювати від біля одного дня до декількох тижнів залежно від швидкості вивільнення, бажаної для конкретного імплантату або лікарського препарату. Бажана швидкість вивільнення визначається фахівцем в даній області відповідно до конкретного активного компоненту, використовуваного в даній рецептурі гранули. Фахівцеві в даній області очевидно, що етапи кондиціонування і активації імплантатів мають на меті оптимізацію швидкості вивільнення лікарського препарату, імплантату, що міститься усередині. Як такий, коротший час кондиціонування і активації пристрою доставки лікарських засобів призводить до нижчої швидкості вивільнення лікарського препарату в порівнянні з аналогічним пристроєм доставки лікарських засобів, що піддався тривалішій обробці на етапі кондиціонування і активації. Температура на етапі кондиціонування і активації також впливає на швидкість вивільнення таким чином, що нижча температура призводить до нижчої швидкості вивільнення лікарського 6 UA 103635 C2 5 10 15 20 25 30 35 40 45 50 55 60 препарату, що міститься в пристрої для доставки лікарських засобів, порівняно з аналогічним пристроєм доставки лікарських засобів, який піддався обробці при вищій температурі. Аналогічним чином у разі водних розчинів, наприклад, фізіологічних розчинів вміст в розчині хлориду натрію визначає, яка швидкість вивільнення буде досягнута для даного пристрою доставки лікарських засобів. Конкретніше, нижчий вміст хлориду натрію призводить до вищої швидкості вивільнення лікарського препарату в порівнянні з пристроєм доставки лікарських засобів, етап кондиціонування і активації якого здійснювався з вищим вмістом хлориду натрію. Аналогічні умови застосовуються для гідрофобних лікарських препаратів, для яких основна відмінність при здійсненні етапу кондиціонування і активації полягає в тому, що середовище для кондиціонування і активації є гідрофобним середовищем, конкретніше, середовищем на масляній основі. Доставка рисперидону може бути корисна, наприклад, при терапії шизофренії, маніакальних станів, біполярних розладів, дратівливості, аутизму, обсесивно-компульсивного розладу, важкої, такої, що не піддається лікуванню, депресії з або без психотичних проявів, синдрому Туретта, розладів соціальної поведінки у дітей і розладів харчової поведінки. Рісперидон належить до класу нейролептичних лікарських препаратів, відомих як "атипові нейролептичні засоби". Він є вираженим антагоністом дофаміну. Він володіє високою спорідненістю до дофамінергічних D2рецепторів. Він володіє дією на рецептори декількох 5-HT (серотонін) підтипів. Це 5-HT2C, що пов'язується із збільшенням маси тіла, 5-HT2A з його нейролептичною дією і ослабленням деяких з екстрапірамідних побічних ефектів, що виявляються з "типовими нейролептичними засобами" завдяки дії на 5-HT1A. Остання дія призводить до збільшення виділення дофаміну з мезокортикальних нейронів в мозку. Відомі і встановлені ефективні рівні вмісту рисперидону в крові, які можуть знаходитися в діапазоні, наприклад, від близько 0,1 до близько 10 нг/мл, від близько 0,5 до близько 8 нг/мл або від близько 1,0 до близько 5 нг/мл. Фахівець в даній області здатний регулювати вивільнення рисперидону за допомогою варіювання різних параметрів імплантату. Наприклад, як показано в прикладах, застосування поліуретанів різних сортів веде до різних швидкостей вивільнення рисперидону. Окрім цього, в межах одного сорту поліуретану різні швидкості вивільнення рисперидону можуть забезпечуватися варіюванням величин EWC і/або модуля пружності на вигин поліуретану. Більш того, фахівець в даній області може змінювати розмір імплантату так, щоб збільшувати або зменшувати площу поверхні імплантату і тим самим змінювати швидкість вивільнення рисперидону з імплантату. Таке варіювання умов призводить до швидкостей вивільнення у фізіологічно-значущому діапазоні, наприклад, від близько 0,001 до близько 15 мг/добу, від близько 0,1 до близько 15 мг/добу, від близько 1 до близько 12,5 мг/добу, від близько 7,5 до близько 12,5 мг/добу або близько 12,5 мг/добу. Швидкість вивільнення з імплантатів може також змінюватися за допомогою, наприклад, регулювання кількості і природи інертних наповнювачів, що містяться в рецептурі рисперидону. Імплантати, що забезпечують досягнення фізіологічно значущих швидкостей вивільнення рисперидону, можуть варіювати в розмірах залежно від, наприклад, природи вживаного поліуретану. Діапазон величини внутрішнього діаметру імплантату циліндрової форми може складати, наприклад, від близько 1 мм до близько 10 мм, від близько 1,5 мм до близько 5 мм, від близько 1,8 мм до близько 3,6 мм, близько 3,6 мм або близько 1,8 мм. Довжина імплантату може знаходитися в діапазоні від біля, наприклад, 5 мм до близько 100 мм, від близько 7,5 мм до близько 50 мм, від близько 10 мм до близько 40 мм, від близько 15 мм до близько 30 мм, близько 37 мм, близько 40 мм або близько 15,24 мм. Цей винахід зосереджений на застосуванні полімерів на основі поліуретану, термопластів або термореактивних матеріалів, на створенні імплантованих пристроїв, призначених для доставки біологічно активних з'єднань з регульованими швидкостями протягом тривалих проміжків часу. Поліуретанові полімери можуть виготовлятися у вигляді, наприклад, циліндрових порожнистих труб з одним або двома відкритими кінцями за допомогою екструзії, (реакційного) литва під тиском, пресування у формі або відцентрового литва (див. наприклад, патенти США №№ 5 266 325 та 5 292 515), залежно від типу використовуваного поліуретану. Термопластичний поліуретан може оброблятися за допомогою екструзії, литва під тиском або пресування у формі. Термореактивний поліуретан може оброблятися за допомогою реакційного литва під тиском, пресування у формі або відцентрового литва. Величини вимірів порожнистої циліндрової труби повинні витримуватися настільки точними, наскільки це можливо. Полімери на основі поліуретану синтезуються з поліфункціональних багатоатомних спиртів, ізоціанатів і подовжувачів ланцюга. Характеристики кожного поліуретану можуть визначатися його структурою. 7 UA 103635 C2 5 10 15 20 25 30 35 40 45 50 55 60 Термопластичні поліуретани виготовляються з макродіолів, диізоціанатів та біфункціональних подовжувачів ланцюга (наприклад, патенти США №№ 4 523 005 і 5 254 662). Макродіоли складають м'які домени. Діізоціанати і подовжувачі ланцюга складають жорсткі домени. Жорсткі домени служать в полімерах як ділянки, що фізично здійснюють поперечне скріплення. Варіювання співвідношення вмісту цих двох видів доменів може змінювати фізичні властивості поліуретанів, наприклад, модуль пружності на вигин. Термореактивні поліуретани можуть виготовлятися з поліфункціональних (більш ніж біфункціональних) багатоатомних спиртів і/або ізоціанатів і/або подовжувачів ланцюга (наприклад, патенти США №№ 4 386 039 і 4 131 604). Термореактивні поліуретани можуть також готуватися за допомогою введення в полімерні ланцюжки ненасичених зв'язків і відповідних зшиваючих агентів і/або ініціаторів, щоб забезпечити хімічне поперечне скріплення (наприклад, патент США № 4 751 133). Керуючи кількістю ділянок поперечного скріплення та їх розподілом, можна регулювати швидкість вивільнення активного компоненту. Залежно від бажаних властивостей, за допомогою модифікування головних ланцюгів багатоатомних спиртів в полімерні ланцюги поліуретану можуть вводитися різні функціональні групи. У випадках, коли пристрій застосовується для доставки лікарських препаратів, розчинних у воді, в багатоатомні спирти для збільшення гідрофільності полімеру вводяться гідрофільні бічні групи, такі як іонні, карбоксильні, ефірні і гідроксильні групи (наприклад, патенти США №№ 4 743 673 і 5 354 835). Коли ж пристрій використовується для доставки гідрофобних лікарських препаратів, для збільшення гідрофобності полімеру в багатоатомні спирти включаються гідрофобні бічні групи, такі як алкільна, силоксанова групи (наприклад, патент США № 6 313 254). Швидкостями вивільнення активних компонентів можна також керувати за допомогою регулювання гідрофільності/гідрофобності поліуретанових полімерів. Для термопластичних поліуретанів переважним вибором при отриманні порожнистих труб (Фіг. 1) з двома відкритими кінцями та постійними фізичними розмірами є точне екструдування або литво під тиском. Резервуар може вільно заповнюватися відповідними рецептурами, що містять активні компоненти і носії, або ж заповнюватися готовими гранулами з тим, щоб забезпечити максимальне завантаження активних інгредієнтів. Спочатку, перед завантаженням рецептури в порожнисту трубу, один її відкритий кінець повинен бути закупорений. Для закупорювання обох відкритих кінців можуть використовуватися дві готові торцеві заглушки (Фіг. 2). Етап закупорювання може виконуватися за допомогою застосування теплової обробки або розчинника, або ж будь-якого іншого засобу для закупорювання кінців, що переважно забезпечує постійне закупорювання. У разі термореактивних поліуретанів залежно від механізму затвердіння переважним вибором є точне реактивне литво під тиском або відцентрове литво. Реактивне литво під тиском застосовується, якщо механізм затвердіння реалізується за допомогою додавання тепла, а відцентрове литво використовується, якщо механізм затвердіння реалізується за допомогою світла і/або тепла. Наприклад, порожнисті труби з одним відкритим кінцем (Фіг. 3) можуть виготовлятися відцентровим литвом. Порожнисті труби з двома відкритими кінцями можуть бути виготовлені за допомогою, наприклад, реактивного литва під тиском. Резервуар може заповнюватися таким же чином, як і у разі термопластичних поліуретанів. Для закупорювання відкритого кінця може використовуватися відповідна ініційована світлом і/або теплом рецептура термореактивного поліуретану, якою заповнюється відкритий кінець і яка потім отверджується під дією світла і/або тепла. Для закупорювання відкритого кінця може також використовуватися, наприклад, готова торцева заглушка за допомогою нанесення на поверхню між готовою торцевою заглушкою і відкритим кінцем відповідної ініційованої світлом і/або теплом рецептури термореактивного поліуретану та затвердіння її під дією світла і/або тепла, або ж може застосовуватися будь-який інший спосіб закупорювання кінців, що переважно забезпечує постійне закупорювання. Завершальний процес включає кондиціонування і активацію імплантатів для досягнення швидкостей доставки, потрібних для даних активних компонентів. Відповідні для виконання кондиціонування і активації середовища вибираються залежно від типу активного інгредієнта – гідрофільного або гідрофобного. Для гідрофільних активних інгредієнтів переважними є водні середовища, а для гідрофобних активних інгредієнтів переважні середовища на масляній основі. Як абсолютно зрозуміло фахівцеві в даній області, в переважні втілення винаходу, не відступаючи від його об'єму домагань, може бути внесене безліч змін. Це означає, що весь матеріал, що міститься тут, слід розглядати по відношенню до даного винаходу як ілюстративний і такий, що не обмежує його. Приклади пояснень 8 UA 103635 C2 5 10 Приклад 1 Труби з поліуретанового полімеру Tecophilic® були постачені компанією Thermedics Polymer Products і отримані способом точної екструзії. Поліуретан Tecophilic® представляє групу аліфатичних термопластичних поліуретанів на поліефірній основі, рецептура яких може бути розроблена з різними показниками рівноважного вологовмісту (EWC), які складають аж до 150 % від маси сухого полімеру. Рецептури марки екструзії призначаються для забезпечення максимальних фізичних властивостей термоформованих труб або інших компонентів. Конструкції використовуваних в прикладах зразків труби і заглушки зображені на Фіг. 1-3. Представлені нижче дані по фізичних властивостях полімерів надані Thermedics Polymer Product (випробування проводилися згідно вказівкам Американського суспільства випробування матеріалів (ASTM), Таблиця 1). Таблиця 1 Типові дані випробувань фізичних властивостей Tecophilic® Дюрометр (твердість за Шором) Питома маса Модуль пружності на вигин (фунти на квадратний дюйм) Межа міцності на розтягування в сухому стані (фунти на квадратний дюйм) Межа міцності на розтягування у вологому стані (фунти на квадратний дюйм) Подовження в сухому стані (%) Подовження у вологому стані (%) 15 20 25 30 ASTM HP-60D-20 HP-60D-35 HP-60D-60 HP-93A-100 D2240 43D 42D 41D 83A D792 1,12 1,12 1,15 1,13 D790 4,300 4,000 4,000 2,900 D412 8,900 7,800 8,300 2,200 D412 5,100 4,900 3,100 1,400 D412 D412 430 390 450 390 500 300 1,040 620 Приклад 2 Таблиці 2 A-C представляють дані за швидкостями вивільнення рисперидону з поліуретанових матеріалів трьох різних класів (Tecophilic®, Tecoflex® і Carbothane®). Швидкості вивільнення були піддані нормалізації за площею поверхні імплантату, тим самим вносячи поправку, що враховує невеликі відмінності в розмірах різних імплантованих пристроїв. Риперидон розглядається як гідрофобна (погано розчинна у воді) речовиною, показником чого є величина LogP; у контексті наданих даних величина LogP, що перевищує близько 2,0, розглядається як індикатор слабкої розчинності у водному розчині. Поліуретани були вибрані так, щоб мати відмінні показники спорідненості до розчинних у воді активних компонентів та відмінні показники еластичності (що відображається різними величинами модуля пружності на вигин). Для застосування поліуретанів, придатних для описаних тут пристроїв і способів, поліуретан повинен демонструвати фізичні властивості, відповідні для рецептури рисперидону, що призначається для доставки. Доступні до придбання або можуть бути приготовані поліуретани з широким діапазоном показника EWC або модуля пружності на вигин (Таблиця 2). У Таблицях 2 A-C показані нормалізовані швидкості вивільнення різних активних інгредієнтів з поліуретанових сполук. Таблиці 2 D-F показують не піддавані нормалізації дані за швидкостями вивільнення тих же самих активних інгредієнтів в співвідношенні з композиціями імплантатів. 9 UA 103635 C2 Таблиця 2А Активний інгредієнт Рісперидон (М.М. 410) Тип поліуретану Марка HP-60D-60 HP-60D-35 поліуретану %EWC / Модуль пружності на 31 % EWC 24 % EWC вигин Відносна розчинність у воді – Log P=3,28 Tecophilic HP-60D-20 HP-60D-10 HP-60D-05 15 % EWC 8,7 % EWC 5,5 % EWC 149 2 мкг/добу/см 10 % CC, 2 % SA, 28,5 міліграм API – – – Таблиця 2B Активний інгредієнт Тип поліуретану Марка поліуретану EG-85A %EWC / Модуль М.М. 2300 пружності на вигин Відносна розчинність у воді Tecoflex EG 100A EG-65D М.М. 10000 М.М. 37000 2 Рісперидон (М.М. 410) 1,9 мкг/добу/см 2 2 146 мкг/добу/см 7,6 мкг/добу/см 10 % CC, 2 % 10 % CC, 2 % SA, 27,9 10 % CC, 2 % SA, SA, 29,7 міліграм міліграм API 29,8 міліграм API API Log P=3,28 Таблиця 2C Активний інгредієнт Рісперидон (М.М. 410) Тип поліуретану Марка поліуретану %EWC / Модуль пружності на вигин Відносна розчинність у воді PC-3575A Carbothane PC-3595A М.М. 620 М.М. 4,500 40 мкг/добу/см 10 % CC, 2 % SA, 27,8 міліграм API Log P=3,28 2 11 мкг/добу/см 10 % CC, 2 % SA, 29,7 міліграм API 2 Таблиця 2D Поліуретан Марка HP-60D-60 %EWC Активний інгредієнт Рісперидон (М.М. 410) Tecophilic HP-60D-35 HP-60D-20 24 % EWC 15 % EWC – 150 мг/добу Внутр. діаметр 1,80 мм Стінка 0,30 мм – Довжина 15,24 мм 2 1,005 см 31 % EWC HP-60D-10 HP-60D-05 5,5 % 8,7 % EWC EWC Відносна розчинність у воді LOGP=3,28 – 10 – UA 103635 C2 Таблиця 2E Активний інгредієнт Рісперидон (М.М. 410) Тип поліуретану Марка поліуретану Модуль пружності на вигин Відносна розчинність у воді Log P=3,28 EG-85A Tecoflex EG 100A EG-65D М.М. 2,300 М.М. 10,000 М.М. 37,000 150 мг/добу Внутр. діаметр 1,85 мм Стінка 0,20 мм Довжина 16,0 мм 2 1,030 см 8 мг/добу Внутр. діаметр 1,85 мм Стінка 0,20 мм Довжина 16,4 мм 2 1,056 см 2 мг/добу Внутр. діаметр 1,85 мм Стінка 0,20 мм Довжина 16,2 мм 2 1,043 см Таблиця 2F Тип поліуретану Марка поліуретану Модуль пружності на вигин Активний інгредієнт Відносна розчинність у воді Рісперидон (М.М. 410) 5 10 15 20 25 30 PC-3575A М.М. 620 40 мг/добу Внутр. діаметр 1,85 мм Стінка 0,20 мм Довжина 15,6 мм 2 1,004 см Log P=3,28 Carbothane PC-3595A М.М. 4,500 11 мг/добу Внутр. діаметр 1,85 мм Стінка 0,20 мм Довжина 16,2 мм 2 1,043 см Розчинність активного компоненту у водному середовищі може бути виміряна або передбачена, ґрунтуючись на його коефіцієнті розподілу (визначуваному як відношення концентрації сполуки у водній фазі до її концентрації в розчиннику, що не змішується). Коефіцієнт розподілу (P) є критерієм того, наскільки добре речовина розділяється між ліпідом (масло) і водою. Ґрунтована на показнику P міра розчинності часто представляється у вигляді LogP. В цілому розчинність визначається показником LogP і температурою плавлення (яка залежить від розміру і структури з'єднання). Як правило, чим нижча величина LogP, тим вища розчинність сполуки у воді. Проте можливі випадки, коли сполуки з високими величинами LogP є, проте, розчинними унаслідок, наприклад, їх низької температури плавлення. Аналогічним чином сполука з високою температурою плавлення може мати низьку величину LogP і бути абсолютно нерозчинною. Модуль пружності на вигин для даного поліуретану – це відношення напруги до деформації. Він є мірою "жорсткості" сполуки. Ця жорсткість зазвичай виражається в Паскалях (Па) або у фунтах на квадратний дюйм (psi). Швидкість елюювання активного компоненту з поліуретанової сполуки може змінюватися під впливом різних чинників, включаючи, наприклад, відносну гідрофобність/гідрофільність поліуретану (що відображається, наприклад, показником logP), відносну "жорсткість" поліуретану (що позначається, наприклад, модулем пружності на вигин) і/або молекулярну масу активного компоненту, що призначається для вивільнення. Приклад 3. Елюювання рисперидону з поліуретанових імплантованих пристроїв. Фіг. 5-10 представляють графіки, що ілюструють профілі елюції рисперидону з різних імплантованих пристроїв, через різні проміжки часу. Були отримані дані за швидкостями вивільнення рисперидону з поліуретанових (марка PC3575A Carbothane®) імплантатів (F.M. (модуль пружності на вигин) 620 фунтів на квадратний дюйм), виготовлених з відрізків трубки, що представляють початок, середину і кінець шлангу, даний графік є частиною дослідження однорідності матеріалу, узятого з певної партії (Фіг. 5). Зразки оцінювалися щотижня протягом одного року. Всі імплантати мали еквівалентні геометричні характеристики і величину завантаження лікарського препарату. Були отримані дані за швидкостями вивільнення рисперидону з поліуретанових (Carbothane® PC-3575A) імплантатів (F.M. 620 фунтів на квадратний дюйм), що представляють 11 UA 103635 C2 5 10 15 20 25 30 35 40 45 50 частину дослідження ефекту застосування як елюююче середовище фізіологічного розчину порівняно з водним розчином оксипропіл-бета-целюлози (15 % у фізіологічному розчині з фосфатним буфером) (Фіг. 6). Зразки оцінювалися щотижня протягом 11 тижнів. Всі імплантати мали еквівалентні геометричні характеристики і величину завантаження лікарського препарату. Було виконано порівняння швидкостей вивільнення рисперидону з імплантатів, виготовлених з поліуретану Carbothane® PC-3595A (F.M. 4500 фунтів на квадратний дюйм), і імплантатів, виготовлених з поліуретану Tecophilic® HP-60D-20 (EWC (рівноважний вологовміст) 14,9 %), що є частиною оцінки вивільнення активного інгредієнта з будь-яких гідрофільних і гідрофобних поліуретанових матеріалів (Фіг. 7A і 7B). У разі імплантату Carbothane® зразки оцінювалися щотижня протягом 22 тижнів. У разі імплантату Tecophilic® зразки оцінювалися щотижня протягом 15 тижнів. Всі імплантати мали еквівалентні геометричні характеристики і величину завантаження лікарського препарату. Було виконано порівняння швидкостей вивільнення рисперидону з імплантатів, виготовлених з поліуретану Tecoflex® EG-80A (F.M. 1000 фунтів на квадратний дюйм) і двох марок поліуретану Tecophilic®, HP-60D-35 і HP-60D-60 (EWC 23,6 % і 30,8 %, відповідно) (Фіг. 8). Вимірювання проводилися щотижня протягом 10 тижнів. Всі імплантати мали еквівалентні геометричні характеристики і величину завантаження лікарського препарату. Були отримані величини швидкостей вивільнення рисперидону з поліуретанових (Carbothane® PC-3575A) імплантатів (F.M. 620 фунтів на квадратний дюйм), які служили in vitro як контрольні для імплантатів, що застосовувалися в описаному в прикладі 8 дослідженні на собаках породи бігль. Дослідження in vitro елюції з цих імплантатів було почате в день імплантації імплантатів, що є об'єктом винаходу, як частина вивчення in vivo-in vitro кореляція. Приклад 4. Оцінка поліуретанових імплантованих підшкірно пристроїв, що містять рісперидон, на собаках породи бігль. Це дослідження визначає рівні рисперидону в крові, що досягаються за допомогою одного або двох імплантатів, та тривалість часу вивільнення з імплантатів лікарського препарату. Імплантовані пристрої на основі поліуретану, що містять гранули з риперидоном, були імплантовані собакам породи бігль з метою визначення швидкостей вивільнення рисперидону in vivo. Результати аналізу проб підсумовані в таблиці 3 і на Фіг. 10. Риперидон все ще був присутній у високих рівнях вмісту в плазмі собаки в кінці третього місяця. Вивчення проводилося відповідно до встановлених WCFP стандартних робочих процедур (SOP), протоколу і будь-яких поправок до протоколу. Всі процедури виконувалися відповідно до Порадника з догляду та використання лабораторних тварин (National Research Center, National Academy Press, округ Колумбію, 1996) і схвалені Інституційним комітетом з догляду за тваринами та їх використанню в WCFP. Початково імплантати містили близько 80 міліграма рисперидону і призначалися для забезпечення доставки приблизно по 130 мкг/добу протягом 3 місяців. Випробовувані зразки перед застосуванням зберігалися при температурі між 2 і 8 °C. Тварини були наступними: Вид: собака Порода: бігль Джерело: Pharm. Industrial Research Institute, Гуанчжоу Свідоцтво № SCXK(YUE) 2003 Ѓ|0007 Вік на момент початку обробки: 6~9 місяців Маса: 8~10 кг Кількість і стать: 6 самців. Перед початком досліджень тваринам були привласнені ідентифікаційні номери попередньої обробки. Перед введенням всі тварини щотижня зважувалися і протягом періоду акліматизації піддавалися в місцях догляду щоденному огляду кваліфікованим ветеринаром. Перед відбором для досліджень всі тварини пройшли клінічне обстеження. Тварини з якиминебудь ознаками захворювань або фізичних відхилень для досліджень не відбиралися. У 3-й і 2й день до імплантації імплантату був виконаний відбір зразків крові, результати дослідження яких розглядалися як початкові. Потім тварини були рандомізовані по 2 групам з наступними режимами дозування: 55 12 UA 103635 C2 5 10 15 20 25 30 Кожна тварина для імплантації пристрою була анестезована загальною анестезією фенобарбіталом натрію в дозуванні 30 міліграм/кг. Лікарський препарат вивільнявся з рівномірною швидкістю протягом декількох місяців. Половині тварин був імплантований один імплантат (група 1), а інші отримали два імплантату (група 2). На плечі виголювалася ділянка 2 площею 5 см і для забезпечення втрати чутливості даної ділянки підшкірно вводилося 2 мл маркаїну. На плечі робився невеликий надріз і пристрій всовувався під шкіру. Невеликий надріз зашивався, тварині давали можливість відновитися і повертали в його загорожу. Протягом наступних п'яти - семи днів місце імплантації імплантату спостерігалося з метою виявлення симптомів інфекції або будь-яких реакцій. Дужки, що стягують шкіру, видалялися, коли шкіра достатньо гоїлася. В кінці періоду в три місяці пристрої вилучалися, так само, як це повинно робитися в клінічних умовах. Перед відбором зразків крові тварини не отримували їжу протягом принаймні чотирьох годин. Оскільки відбір крові виконувався вранці, корм не видавався протягом ночі. Проби крові відбиралися за допомогою голки 20G і збиралися безпосередньо в 5 мл пробірки з гепариннатрієм і до центрифугування зберігалися в охолодженому вигляді. Потім зразки центрифугували протягом 5 хвилин при температурі 4 °C і швидкості 5000 об/хв. Відокремлена плазма потім переносилася в дві 3 мл кріопробірки. Зразки маркірувалися по фактичній даті відбору зразка, відповідному дню дослідження, ідентифікатору собаки і покажчику дубліката проби (або A або B). До готовності до проведення аналізів зразки зберігалися при -20 °C. Початкові проби крові відбиралися в два послідовні дні до імплантації пристрою доставки. Окрім цього, зразки крові відбиралися щодня протягом першого тижня і щотижня проби крові відбиралися впродовж трьох місяців після імплантації. Кожного разу від кожного собаки отримували по 2 зразки крові об'ємом по 5 мл. Проби крові відбиралися перш за все з головної вени, як резервні використовувалися підшкірна вена ноги або яремна вена. Для обох груп, як з одинарними, так і з подвійними імплантатами, проби крові відбиралися у відповідні моменти часу, позначені нижче в Таблиці 3. Для аналізу було потрібно принаймні 2 мл плазми, для якої необхідне було отримання у разі кожного зразка не менше 10 мл крові. Аналіз показників плазмової концентрації рисперидону виконувався за допомогою методу LC/MS (рідинна хроматографія / мас-спектрометрія), розширеного для цієї сполуки. Для кожного зразка було проведено по одному випробуванню. Зразки відбиралися, витримувалися за відповідних умов і аналізувалися партіями. 13 UA 103635 C2 Таблиця 3 Концентрація рисперидону в плазмі собаки 5 Фіг. 9 є графіком in vivo плазмової концентрації рисперидону в дослідженні на собаках породи бігль. Розташований в нижній частині графік представляє середню плазмову концентрацію, досягнуту у собак з одним імплантованим поліуретановим (Carbothane® PC3575A) імплантатом (F.M. 620 фунтів на квадратний дюйм). Верхній графік представляє середню плазмову концентрацію, досягнуту у собак з двома імплантованими поліуретановими 14 UA 103635 C2 5 10 15 20 25 30 (Carbothane® PC-3575A) імплантатами (F.M. 620 фунтів на квадратний дюйм). Приклад 5. Оцінка поліуретанових імплантованих підшкірно пристроїв, що містять риперидон, на собаках породи бігль. При розширенні на дані, представлені в прикладі 4, це дослідження визначає рівні рисперидону в крові, що досягаються за допомогою одного або двох крупніших імплантатів, а також тривалість часу вивільнення з імплантатів лікарського препарату. Імплантовані пристрої на основі поліуретану, що містять гранули з риперидоном, були імплантовані собакам породи бігль з метою визначення швидкостей вивільнення рисперидону in vivo. Результати по крупніших імплантатам в звідному вигляді представлені на Фіг. 10 (in vitro профіль елюції) і Фіг. 11 (елюція у собак породи бігль). Гранули, що застосовувалися в даному дослідженні, містять рецептуру рисперидону, та мали діаметр 3,5 мм, довжину близько 4,5 мм і масу 5,4 міліграм. Імплантат мав довжину резервуару близько 39-40 мм, товщину стінки 0,2 мм і внутрішній діаметр 3,6 мм при загальній довжині близько 45 мм, спочатку містив близько 80 міліграма рисперидону і призначався для доставки приблизно по 130 мкг/добу протягом 3 місяців. Еквіваленти Справжнє розкриття не слід розглядати як обмежуване описаними в цій заявці переважними втіленнями, призначеними для ілюстрації різних об'єктів винаходу. Фахівцям в даній області очевидно, що без відступу від суті і об'єму домагань справжнього розкриття в даний винахід може бути внесене множину модифікацій та змін. Окрім перерахованих тут, з вищевикладених описів фахівцям в даній області очевидні й інші функціонально еквівалентні способи, системи і пристрої, що знаходяться в рамках даного розкриття. Такі модифікації і зміни вважаються підпадаючими під об'єм, що охоплюється формулою винаходу, яка додається. Справжнє розкриття слід розглядати як обмежуване тільки доданою формулою винаходу, охоплює весь об'єм еквівалентів, на які дана формула винаходу поширює свої права. Слід розуміти, що це розкриття не обмежується конкретними способами, реактивами, композиціями сполук або біологічними системами, які можуть, зрозуміло, змінюватися. Слід також розуміти, що використовувана тут термінологія застосовується лише для цілей опису конкретних втілень і не призначається для обмежувальних цілей. Фахівцям в даній області ясно, що в будь-яких випадках, наприклад, для цілей надання письмового опису, всі розкривані тут діапазони також охоплюють і всі їх можливі піддіапазони та комбінації піддіапазонів. При тому, що тут розкриваються різні об'єкти і втілення, фахівцям в даній області очевидні й інші об'єкти і втілення. Всі використані при експертизі заявки матеріали є такими, що включаються тут у всій своїй повноті за допомогою посилання. 35 ФОРМУЛА ВИНАХОДУ 40 45 50 55 60 1. Спосіб доставки суб'єктові рецептури, що містить ефективну кількість рисперидону, який включає введення суб'єктові імплантованого пристрою, що містить: а) полімер на основі поліуретану, якому надається така форма, щоб обмежувати незаповнений простір; і b) тверду рецептуру лікарського препарату, що містить рисперидон, і, за потреби, один або декілька фармацевтично прийнятних носіїв, при цьому зазначена тверда форма рисперидону міститься у вказаному незаповненому просторі. 2. Спосіб за п. 1, який відрізняється тим, що полімер на основі поліуретану утворений одним або декількома багатоатомними спиртами, при цьому загальна структура багатоатомного спирту вибирається з групи, що складається з: -[О-(СН2)n]х-О-; О-(СН2-СН2-СН2-СН2)х-О-; і О-[(СН2)6-СО3]n-(СН2)-О-. 3. Спосіб за п. 2, який відрізняється тим, що багатоатомний спирт містить -[O-(СН2)n]x-O- і в якому полімер на основі поліуретану має рівноважний вологовміст між близько 5 % - 200 %. 4. Спосіб за п. 3, який відрізняється тим, що полімер на основі поліуретану має рівноважний вологовміст принаймні близько 15 %. 5. Спосіб за п. 2, який відрізняється тим, що рисперидон вивільняється із швидкістю нульового порядку близько 149 мкг/добу на квадратний сантиметр площі поверхні імплантованого пристрою. 6. Спосіб за п. 2, який відрізняється тим, що багатоатомний спирт містить -[O-(СН2)n]x-O- і в якому полімер на основі поліуретану має модуль пружності на вигин між близько 689,5-63430 ньютон на квадратний сантиметр. 15 UA 103635 C2 5 10 15 20 25 30 35 40 45 50 55 7. Спосіб за п. 6, який відрізняється тим, що полімер на основі поліуретану має модуль пружності на вигин близько 1568 ньютон на квадратний сантиметр. 8. Спосіб за п. 6, який відрізняється тим, що рисперидон вивільняється із швидкістю нульового порядку близько 146 мкг/добу на квадратний сантиметр площі поверхні імплантованого пристрою. 9. Спосіб за п. 2, який відрізняється тим, що багатоатомний спирт містить O-[(СН2)6-СО3]n(СН2)-O- і при якому полімер на основі поліуретану має модуль пружності на вигин між близько 427,5-63430 ньютон на квадратний сантиметр. 10. Спосіб за п. 9, який відрізняється тим, що полімер на основі поліуретану має модуль пружності на вигин близько 427,5 ньютон на квадратний сантиметр. 11. Спосіб за п. 9, який відрізняється тим, що рисперидон вивільняється із швидкістю нульового порядку близько 40 мкг/добу на квадратний сантиметр площі поверхні імплантованого пристрою. 12. Пристрій доставки лікарських засобів призначений для контрольованого вивільнення рисперидону протягом тривалого періоду часу з тим, щоб забезпечити досягнення місцевої або системної фармакологічної дії, що містить: a) полімер на основі поліуретану, якому надається така форма, щоб обмежувати незаповнений простір; і b) тверду рецептуру лікарського препарату, що містить рисперидон, і, за потреби, один або декілька фармацевтично прийнятних носіїв, при цьому тверда рецептура лікарського препарату міститься в зазначеному незаповненому просторі і при цьому пристрій забезпечує бажану швидкість вивільнення рисперидону з пристрою після імплантації. 13. Пристрій за п. 12, який відрізняється тим, що його кондиціонують і активують в умовах, вибраних так, щоб бути сумісними з показниками розчинності у воді принаймні одного активного компонента. 14. Пристрій за п. 13, який відрізняється тим, що фармацевтично прийнятний носій є стеариновою кислотою. 15. Пристрій за п. 12, який відрізняється тим, що полімер на основі поліуретану утворений одним або декількома багатоатомними спиртами, при цьому загальна структура багатоатомного спирту вибирається з групи, що складається з: -[О-(СН2)n]х-О-; O-(СН2-СН2-СН2-СН2)х-О-; і О-[(СН2)6-СО3]n-(СН2)-О-. 16. Пристрій за п. 15, який відрізняється тим, що багатоатомний спирт містить -[O-(СН2)n]х-Oта при якому полімер на основі поліуретану має рівноважний вологовміст між близько 5 % - 200 %. 17. Пристрій за п. 16, який відрізняється тим, що полімер на основі поліуретану має рівноважний вологовміст принаймні близько 15 %. 18. Пристрій за п. 15, який відрізняється тим, що рисперидон вивільняється із швидкістю нульового порядку близько 149 мкг/добу на квадратний сантиметр площі поверхні імплантованого пристрою. 19. Пристрій за п. 15, який відрізняється тим, що багатоатомний спирт містить -[O-(СН2)n]х-O- і при якому полімер на основі поліуретану має модуль пружності на вигин між близько 689,563430 ньютон на квадратний сантиметр. 20. Пристрій за п. 19, який відрізняється тим, що полімер на основі поліуретану має модуль пружності на вигин близько 1586 ньютон на квадратний сантиметр. 21. Пристрій за п. 19, який відрізняється тим, що рисперидон вивільняється із швидкістю нульового порядку близько 146 мкг/добу на квадратний сантиметр площі поверхні імплантованого пристрою. 22. Пристрій за п. 15, який відрізняється тим, що багатоатомний спирт містить O-[(СН2)6СО3]n(СН2)-O- і в якому полімер на основі поліуретану має модуль пружності на вигин між близько 427,5-63430 ньютон на квадратний сантиметр. 23. Пристрій за п. 22, який відрізняється тим, що полімер на основі поліуретану має модуль пружності на вигин близько 427,5 ньютон на квадратний сантиметр. 24. Пристрій за п. 22, який відрізняється тим, що рисперидон вивільняється із швидкістю нульового порядку близько 40 мкг/добу на квадратний сантиметр площі поверхні імплантованого пристрою. 25. Пристрій за п. 12, який відрізняється тим, що в цілях встановлення бажаних швидкостей доставки принаймні одного активного компонента можуть бути вибрані відповідні параметри 16 UA 103635 C2 кондиціонування і активації, при цьому параметрами кондиціонуюче середовище та активуюче середовище. 17 активації є час, температура, UA 103635 C2 18 UA 103635 C2 19 UA 103635 C2 20 UA 103635 C2 21 UA 103635 C2 22 UA 103635 C2 23 UA 103635 C2 24 UA 103635 C2 25 UA 103635 C2 26 UA 103635 C2 Комп’ютерна верстка С. Чулій Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 27
ДивитисяДодаткова інформація
Назва патенту англійськоюImplantable device for the delivery of risperidone and methods of use thereof
Автори англійськоюKuzma, Petr, Quandt, Harry
Автори російськоюКузма Петр
МПК / Мітки
МПК: A61K 47/34, A61K 31/519, A61K 9/54
Мітки: рисперидону, пристрій, спосіб, введення, використання, імплантований
Код посилання
<a href="https://ua.patents.su/29-103635-implantovanijj-pristrijj-dlya-vvedennya-risperidonu-ta-sposib-jjogo-vikoristannya.html" target="_blank" rel="follow" title="База патентів України">Імплантований пристрій для введення рисперидону та спосіб його використання</a>
Попередній патент: Азаіндазоли як антагоністи рецептора ccr1
Наступний патент: Шліфувальний верстат
Випадковий патент: Комплексний тренажер екіпажу бойової машини піхоти бмп-2