Спосіб одержання пропінілового естеру (r)(+)-2-[4-(5-хлор-3-фторпіридин-2-ілокси)фенокси]пропіонової кислоти
Номер патенту: 64718
Опубліковано: 15.03.2004
Автори: Зайферт Готфрід, Стінг Андреа Рольф, Урвілер Бернхард
Формула / Реферат
1. Спосіб одержання пропінілового естеру (R)(+)-2-[4-(5-хлор-3-фторпіридин-2-ілокси)фенокси]пропіонової кислоти формули (І)
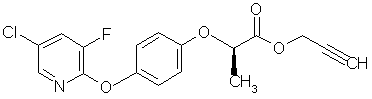 , (I)
, (I)
який відрізняється тим, що сполуку формули (II) перетворюють
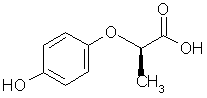 , (II)
, (II)
в інертному органічному розчиннику разом з М2СО3, де М являє собою натрій чи калій, і без відокремлення проміжних продуктів, в сполуку формули (III)
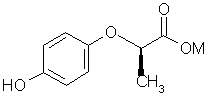 , (III)
, (III)
де М являє собою натрій чи калій, цю сполуку вводять в реакцію зі сполукою формули (IV)
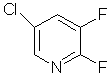 , (IV)
, (IV)
з утворенням сполуки формули (V)
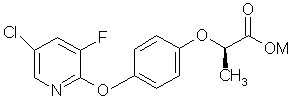 , (V)
, (V)
де М являє собою натрій чи калій, цю сполуку перетворюють шляхом проведення реакції зі сполукою формули (VI)
![]() , (VI)
, (VI)
де Z являє собою фенілсульфоніл, толілсульфоніл, метилсульфоніл, нонілсульфоніл, бромфеніл, Сl-, Вr- або СlСО-, в сполуку формули (I).
Текст
Даний винахід стосується способу одержання пропінілового естеру (R)(+)-2-[4-(5-хлор-3-фторпіридин2-ілокси)-фенокси]-пропіонової кислоти. Пропініловий естер (R)(+)-2-[4-(5-хлор-3-фторпіридин-2-ілокси)-фенокси]-пропіонової кислоти має гербіцидну активність і його описано, наприклад, в Європейському патенті №А-0248968. Похідні 4-(5-хлор3-фторпіридин-2-ілокси)-фенокси]- пропіонової кислоти можуть бути одержані, наприклад, згідно з Європейським патентом №А 0439857 в результаті реакції 5-хлор-2,3-дифторпіридину з відповідними естерами 4-гідроксипропіонової кислоти в присутності основи, що не містить води, та за відсутності розчинника. Однак цей спосіб непридатний для одержання пропінілового естеру (R)(+)-2-[4-(5-хлор-3фторпіридин-2-ілокси)-фенокси]-пропіонової кислоти, бо потрійний зв'язок естеру гідроксипропіонової кислоти має тенденцію до утворення полімерів в умовах, в яких проводять процес, та в основних умовах. Крім того, відомий процес є особливо проблематичним, що стосується безпеки, бо реакційну суміш можна нагрівати лише без розчинників, а це є почасти ризикованою операцією внаслідок високого термічного потенціалу цього потрійного зв'язку. Згідно з Європейським патентом №А 0248968, сторінки 12 - 14 пропініловий естер (R)(+)-2-[4-(5-хлор-3фторпіридин-2-ілокси)-фенокси]-пропіонової кислоти одержують шляхом процесу, в якому: а) на першій стадії сполуку формули А в диметилсульфоксиді вводять в реакцію з сумішшю диметилсульфоксиді для одержання сполуки формули В гідрохінону та гідроксиду калію в цю сполуку б) на наступній стадії вводять в реакцію в диметилсульфоксиді в присутності карбонату калію з тозілатом метилового естеру S(-) молочної кислоти з утворенням сполуки формули С цю сполуку в) на третій стадії вводять в реакцію в діоксані в присутності розчину гідроксиду натрію з утворенням сполуки формули D цю сполуку г) на четвертій стадії вводять в реакцію в толуолі з хлоридом тіонілу з утворенням сполуки формули Е сполуки, яку нарешті без подальшого відокремлення д) вводять в реакцію з сумішшю триетиламіну та пропінолу в толуолі з утворенням пропінілового естеру (R)(+)-2-[4-(5-хлор-3-фторпіридин-2-ілокси)-фенокси]-пропіонової кислоти. Головними недоліками цього процесу є необхідність залучення стадій відокремлення та очищення, бо реакція проходить в чотири етапи. Це зменшує вихід продукту. Крім того, при проведенні процесу двічі виникає потреба в заміні розчинника. Це потребує додаткового часу та залучення стадії дистиляції, що призводить до додаткових витрат. Таким чином, відомий спосіб не є оптимальним, особливо при його промисловому використанні. Задачею даного винаходу є розробка способу, який би дозволяв одержувати пропініловий естер (R)(+) 2-[4-(5-хлор-3-фторпіридин-2-ілокси)-фенокси]-пропіонової кислоти за допомогою спрощеного процесу з одержанням продукту вищого рівня чистоти при більшому виході кінцевого продукту. Було виявлено, що пропініловий естер (R)(+)-2-[4-(5-хлор-3-фторпіридин-2-ілокси)-фенокси]пропіонової кислоти формули І можна одержати за допомогою кращого способу шляхом перетворення сполуки формули II в інертному органічному розчиннику разом з М2СО3, де М являє собою натрій чи калій, і без відокремлення проміжних продуктів у сполуку формули III де М являє собою натрій чи калій, введення цієї сполуки в реакцію зі сполукою формули IV з утворенням сполуки формули V де М являє собою натрій чи калій, і перетворення цієї сполуки шляхом проведення реакції зі сполукою формули VI де Z позначає групу, що відокремлюється, таку як фенілсульфоніл, тозіл, метилсульфоніл, нозіл, бромфеніл, СІ-, Вг- або СІСО-, в сполуку формули І. Вихідні сполуки можна брати в стехіометричних кількостях. Сполуку формули IV краще брати в надлишку від 0,05 до 0,3 еквіваленту, ще краще 0,1 еквіваленту відносно сполуки формули III. Сполуку формули VI краще брати в надлишку від 0,05 до 0,15 еквіваленту. Згідно з даним винаходом краще, коли М в сполуці М2СО3 являє собою калій. Інертними органічними розчинниками, які можна використати згідно з даним винаходом, є, наприклад, кетони, естери і прості ефіри. Як розчинники краще використовувати диметилформамід, диметилсульфоксид, N-метилпіролідон або ацетонітріл. Краще брати диметилформамід або ацетонітріл, а найкраще - диметилформамід. В переважному варіанті реалізації способу згідно з винаходом Z в формулі VI являє собою хлор. Спосіб згідно з винаходом можна проводити при підвищених температурах, особливо при 40 - 120°С Кращим є температурний діапазон від 60 до 90°С, а найкращим - від 70 до 75° С Реакцію сполуки формули III зі сполукою формули IV для прискорення реакції можна проводити в присутності каталізатора фазового переносу. Придатними каталізаторами фазового переносу є четвертинні амонієві солі, четвертинні фосфонієві солі або краун-ефіри. Вихідні сполуки формул II, IV та VI відомі, або їх можна одержати за допомогою відомих методів. Сполука формули IV описана, наприклад, в Європейському патенті №А 0248968, а сполука формули II - в Європейському патенті №А 0083556. Сполуки формули VI, де Z являє собою хлор, можна одержати, наприклад, згідно з прикладом, описаним в [J. Am. Chem. Soc. 77, 1831 (1955)], причому придатними сполуками для цієї реакції є піридин, краще 5-етил-2-метилпіридин. Процес згідно з винаходом відрізняється від відомих процесів тим, що його можна проводити в одній посудині без заміни розчинника. Таким чином, знижуються не тільки витрати на обладнання, а також відпадає потреба в стадіях відокремлення та дистиляції, що призводить до значної економії в часі. Крім того, значне зниження кількості залишків розчинників, що досягається завдяки процесу згідно з винаходом, є особливо вигідним з екологічної точки зору. Завантаження продукту при нижчій температурі знижує утворення побічних продуктів, а селективний хід реакції дозволяє досягти більш точного дозування реагентів, що в кінцевому результаті призводить до більшого виходу продукту зі значно вищим рівнем чистоти. Приклади по приготуванню Приклад П1: Приготування пропінілового естеру (R)(+)-2-[4-(5-хлор-3-фторпіридин-2-ілокси)-фенокси]пропіонової кислоти 182г 100%-ної (R)-2-(n-гідроксифенокси)-пропіонової кислоти(1моль) в 600г диметилформаміду(ДМФ) перетворювали у відповідну калієву сіль додаванням при 70°С 69г порошку карбонату калію(0,5моль) при розщепленні СО2. До цього розчину додавали 193г порошку карбонату калію(1,4моль), а потім при температурі 70 - 75°С додавали 165г 5-хлор-2,3-дифторпіридину(1,1моль) протягом 30хвилин. Через 4 години, одержана, таким чином, сполука формули V, повністю прореагувала шляхом дозування в 86г хлориду пропаргілу(1,15моль) як 60 - 70%-ного розчину толуолу протягом 2 годин напряму, без відокремлення при температурі 70 - 75°С з утворенням пропінілового естеру(R)(+)-2-[4-(5хлор-3-фторпіридин-2-ілокси)-фенокси]-пропіонової кислоти. Солі відфільтровували, промивали в 300г ДМФ по частинах, а фільтрат концентрували до розплаву на випарнику, що обертається, у вакуумі при температурі 120°С. Сирий розплав пропінілового естеру (R)(+)-2-[4-(5-хлор-3-фторпіридин-2-ілокси)фенокси]-пропіонової кислоти змішували при температурі 50°С з 300г етанолу/води в пропорції 9 : 1, затравлювали при температурі 30 - 35°С і охолоджували до температури 0 - 5°С Кристалічну пульпу вводили у вакуум-фільтр, промивали в 70г етанолу/води в пропорції 9 : 1 та висушували у вакуумі при температурі 30°С Одержали 307г активної сполуки з вмістом 97%(газова хроматографія), що відповідає теоретичному виходу 85%, якщо рахувати по (R)-2-(n-гідроксифенокси)-пропіоновій кислоті. Приклад П2: Приготування пропінілового естеру (R)(+)-2-[4-(5-)хлop-3-фторпіридин-2-ілокси)-фенокси]пропіонової кислоти 182г 100%-ної (R)-2-(n-гідроксифенокси)-пропіонової кислоти(1моль) в 1500г ацетонітрілу перетворювали у відповідну калієву сіль додаванням при 70°С 69г порошку карбонату калію(0,5моль) при розщепленні СО2. Потім до реакційної суміші додавали 193г порошку карбонату калію(1,4моль) і 2г броміду тетрабутиламонію як каталізатора фазового переносу, і при температурі 70 75°С додавали 165г 5-хлор-2,3-дифторпіридину(1,1моль) протягом 30хвилин. Через 8 годин одержана таким чином сполука формули V повністю прореагувала шляхом дозування в 154г метилсульфонату пропаргілу(1,15моль) у формі 60 - 70%-го розчину в толуолі протягом 2 годин напряму без відокремлення при температурі 70 - 75°С з утворенням пропінілового естеру (R)(+)-2-[4-(5-хлор-3-фторпіридин-2-ілокси)фенокси]-пропіонової кислоти. Доведення до кондиції проводили згідно з методикою прикладу П1. Одержали 304г пропінілового естеру (R)(+)-2-[4-(5-хлор-3-фторпіридин-2-ілокси)-фенокси]-пропіонової кислоти з вмістом 98%(газова хроматографія), що відповідає теоретичному виходу 85%, якщо рахувати по (R)-2-(n-гідроксифенокси)-пропіоновій кислоті. Приклад П3: Приготування пропінілового естеру (R)(+)-2-[4-(5-хлор-3-фторпіридин-2-ілоксі)-фенокси]пропіонової кислоти. Хлорид пропаргілу в прикладі П1 замінили на 226г(1,15моль) пропаргілового естеру бензосульфокислоти і одержали 305г пропінілового естеру (R)(+)-2-[4-(5-хлор-3-фторпіридин-2-ілокси)фенокси]-пропіонової кислоти з вмістом 96%(газова хроматографія), що відповідає теоретичному виходу 84%, якщо рахувати по (R)-2-(n-гідроксифенокси)-пропіоновій кислоті. Приклад П4: Приготування пропінілового естеру (R)(+)-2-[4-(5-хлор-3-фторпіридин-2-ілокси)-фенокси]пропіонової кислоти 182г 100%-ної (R)-2-(n-гідроксифенокси)-пропіонової кислоти(1моль) в 1500г ацетонітрілу перетворювали у відповідну калієву сіль додаванням при 70°С 69г порошку карбонату калію(0,5моль) при розщепленні СО2. Потім до реакційної суміші додавали 193г порошку карбонату калію(1,4моль) і 2г броміду тетрабутиламонію як каталізатора фазового переносу, і при температурі 70 75°С додавали 165г 5-хлор-2,3-дифторпіридину(1,1моль) протягом 30хвилин. Через 8 годин, одержана, таким чином сполука формули V, повністю прореагувала повністю з утворенням пропінілового естеру (R)(+)-2-[4-(5-хлор-3-фторпіридин-2-ілокси)-фенокси]-пропіонової кислоти напряму без відокремлення при температурі 70 - 75°С шляхом дозування в пропаргіловому естері хлормурашиної кислоти, в результаті чого відбулось виділення СО2. Доведення до кондиції проводили згідно з методикою прикладу П1. Одержали пропініловий естер (R)(+)-2-[4-(5-хлор-3-фторпіридин-2-ілокси)-фенокси]-пропіонової кислоти з вмістом 97%(газова хроматографія), що відповідає теоретичному виходу 80%, якщо рахувати по (R)-2-(nгідроксифенокси)-пропіоновій кислоті.
ДивитисяДодаткова інформація
Назва патенту англійськоюA method for preparing propionic acid derivatives
Назва патенту російськоюСпособ получения производных пропионовой кислоты
МПК / Мітки
МПК: C07D 213/61, C07D 213/643, A01P 13/00
Мітки: одержання, пропінілового, естеру, кислоти, спосіб, r)(+)-2-[4-(5-хлор-3-фторпіридин-2-ілокси)фенокси]пропіонової
Код посилання
<a href="https://ua.patents.su/3-64718-sposib-oderzhannya-propinilovogo-esteru-r-2-4-5-khlor-3-ftorpiridin-2-iloksifenoksipropionovo-kisloti.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання пропінілового естеру (r)(+)-2-[4-(5-хлор-3-фторпіридин-2-ілокси)фенокси]пропіонової кислоти</a>
Попередній патент: Похідні гідроксиламіну як лікарський засіб для лікування або профілактики захворювань, спричинених пошкодженням васкулярних ендотеліальних клітин та спосіб лікування
Наступний патент: Розкладна коробка для сигарет
Випадковий патент: Спосіб підготовки вологих залізовмісних шламів металургійного виробництва до окускування







