Спосіб одержання 6-аміно-3,5-диціано-4-циклоалкілспіро-1,2,3,4-тетрагідропірид-2-онів
Формула / Реферат
Спосіб одержання 6-аміно-3,5-диціано-4-циклоалкілспіро-1,2,3,4-тетрагідропірид-2-онів загальної формули (І)
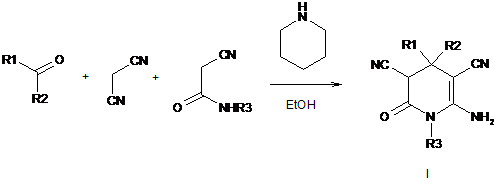 ,
,
де R1 - R2 = (CH2)4, (CH2)5, CH(Alk)(CH2)4, (CH2)2CH(Alk)(CH2)2, R3 = H, NH2,
який відрізняється тим, що конденсують рівномолярні кількості циклічних кетонів, малононітрилу, ціаноацетамідів у середовищі етанолу в присутності каталізатора - піперидину при короткостроковому нагріванні протягом 5-10 хв.
Текст
Спосіб одержання 6-аміно-3,5-диціано-4циклоалкілспіро-1,2,3,4-тетрагідропірид-2-онів загальної формули (І) 2 3 66108 16, p. 3767-3770; K. Motokura, N. Fujita, K. Mori, T. Mizugaki, K. Ebitani, K. Kaneda. Journal of the American Chemical Society, 2005, vol. 127, # 27, p. 96749675; Cairns et al. Journal of the American Chemical Society, 1958, vol. 80, p. 2775-2777; І. A. El-Sakka, S. M. El-Kousy. Journal fuer Praktische Chemie (Leipzig), 1991, vol. 333, # 2, p. 345-350; A. Corma, M. Renz. Collection of Czechoslovak Chemical Communications, 2005, vol. 70, # 10, p. 1727-1736; T. Hayamizu, H. Maeda, K. Mizuno. Journal of Organic Chemistry, 2004, vol. 69, # 15, p. 4997-5004; M. M. Heravi, M. Tajbakhsh, B. Mohajerani, M. Ghassemzadeh. Zeitschrift fuer Naturforschung, В.: Chemical Sciences, 1999, vol. 54, # 4, p. 541-543; M. Gora, B. Kozik, K. Jamrozy, M. K. Luczynski, P. Brzuzan, M. Wozny, Green Chemistry, 2009, vol. 11, # 6, p. 863867; F. Geneste, N. Racelma, A. Moradpour. Synthetic Communications, 1997, vol. 27, # 6, p. 957-960; T. G. Rymareva, B. A. Khaskin, V. B. Sandakov, V. K. Promonenkov. J. Gen. Chem. (USSR), 1981, vol. 51, # 11, p. 2633-2634], по-друге, дозволяє уникнути багатостадійних методів синтезу сполук (І), зменшити їх собівартість та екологічні наслідки реалізації. Виходячи із зазначеного, в основу корисної моделі поставлено задачу створення нового доступного способу одержання 6-аміно-3,5-диціано-4циклоалкілспіро-1,2,3,4-тетрагідропірид-2-онів. Рішення поставленої задачі забезпечується тим, що у способі одержання сполук загальної формули (І), згідно корисної моделі, конденсують рівномолярні кількості циклічних кетонів, малононітрилу, ціаноацетамідів у середовищі етанолу в присутності каталізатора - піперидину, при короткостроковому нагріванні протягом 5-10 хв. за схемою: H N O R1 + R2 R1 CN CN R2 CN NC + CN O NHR3 EtOH O N NH2 R3 I , де R1-R2 = (CH2)4, (CH2)5, CH(Alk)(CH2)4, (CH2)2CH(Alk)(CH2)2, R3=H, NH2. Можливість модифікації хімічної структури циклічних кетонів та ціаноацетамідів шляхом варіювання їх замісників дозволяє одержувати широкий набір сполук (І), у тому числі й невідомих раніше. Експериментальним шляхом було підібрано співвідношення: "прийнятне сполучення вихідних реагентів - час реакції - вихід кінцевого продукту". Так, було помічено, що використання ціаноацетаміду в кількості значно більшій, ніж рівномолярна, хоча і сприяє підвищенню швидкості реакції і утворенню сполук (І), тим не менше цей надлишок заважає виділенню кінцевого продукту, забруднюючи його. У цьому випадку необхідне очищення речовин шляхом додаткових перекристалізацій. Оптимальним виявилось використання циклічного кетону в кількості 1,1 ммоль на 1 ммоль малононітрилу та 1 ммоль відповідного ціаноацетаміду. 4 Легкість протікання реакції і ступінь перетворення вихідних сполук у кінцеві визначається часом здійснення процесу. При одержанні сполук формули (І), для повного розчинення вихідних сполук було потрібне нетривале кип'ятіння реакційної маси - 5-10 хв., потім реакція проходить протягом 3-12 годин при кімнатній температурі в залежності від замісників у циклічних кетонах та ціаноацетамідах. Вихід сполук (І), отриманих згідно корисної моделі, що заявляється, складає 6188 %. Вибір компонентів реагуючої суміші, їх мольні співвідношення, середовище для проведення реакції, час проходження процесу утворення цільових продуктів - все це відбивається на чистоті кінцевих продуктів - після виділення із реакційної маси і промивки етанолом сполуки формули (І) мають достатню чистоту для подальшого використання, 1 їх будова доведена за допомогою ІЧ- і ЯМР Нспектроскопії. Корисна модель підтверджується наступними прикладами, які ілюструють, але не обмежують її об'єм. Приклад 1. 6-Аміно-3,5-диціано-4-циклогексанспіро1,2,3,4-тетрагідропірид-2-он (R1-R2 = (СН2)5, R3 = Н). Суміш, що складається із 1,1 ммоль циклогексанону, 1 ммоль малононітрилу, 1 ммоль ціаноацетаміду (R3 = Н), 1 ммоль піперидину в 10 мл етанолу, кип'ятять 3 хв. і залишають при кімнатній температурі на 12 годин, розбавляють 10 %-ною соляною кислотою до рН = 5. Осад, що утворився, через 3 години відфільтровують, промивають етанолом. Вихід 71 %, т. пл. 212-214 °C (літ. 210 °C (із бензолу)). Приклад 2. 6-Аміно-3,5-диціано-4-циклопентанспіро1,2,3,4-тетрагідропірид-2-он (R1-R2 = (СН2)4, R3 = Н). Суміш, що складається із 1,1 ммоль циклопентанону, 1 ммоль малононітрилу, 1 ммоль цианоацетаміду (R3 = Н), 1 ммоль піперидину в 10 мл етанолу, кип'ятять 8 хв. і залишають при кімнатній температурі на 12 годин, розбавляють 10 %-ною соляною кислотою до рН = 5. Осад, що утворився, через 3 години відфільтровують, промивають етанолом. Вихід 62 %, т. пл. 169-172 °C (літ. 165 °C (із бензолу)). 1 ІЧ- та ЯМР Н-спектри наведених прикладів відповідають даним роботи [А. К. El-Shafei, A. A. Sultan, A. M. Soliman, E. A. Ahmed. Synthetic Communications, 1995, vol. і 25, #20, p, 3211-3218] в межах похибки використаних приборів. Таким чином, корисна модель, що пропонується, має наступні переваги у порівнянні з аналогами: - базується на простих та доступних реагентах промислового виробництва (циклічних кетонах, малононітрилі, ціаноацетамідах,піперидині, етанолі); - можливість модифікації хімічної структури циклічних кетонів та ціаноацетамідів шляхом варіювання їх замісників дозволяє одержувати широкий набір 6-аміно-3,5-диціано-4-циклоалкілспіро1,2,3,4-тетрагідропірид-2-онів, у тому числі й невідомих раніше; 5 - дозволяє уникнути багатостадійних методів синтезу згаданих кінцевих сполук, зменшити їх собівартість та екологічні наслідки реалізації; - отримані продукти реакції не потребують подальшого очищення; Комп’ютерна верстка Г. Паяльніков 66108 6 - може бути відтворена в умовах лабораторії та хімічних підприємств з використанням стандартного обладнання. Підписне Тираж 23 прим. Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of 6-amino-3,5-dicyano-4-cycloalkylspiro-1,2,3,4-tetrahydropyrid-2-ones
Автори англійськоюKryvokolysko Serhii Hennadiiovych
Назва патенту російськоюСпособ получения 6-амино-3,5-дициано-4-циклоалкилспиро-1,2,3,4-тетрагидропирид-2-онов
Автори російськоюКривоколиско Сергей Геннадиевич
МПК / Мітки
МПК: C07D 221/20
Мітки: одержання, 6-аміно-3,5-диціано-4-циклоалкілспіро-1,2,3,4-тетрагідропірид-2-онів, спосіб
Код посилання
<a href="https://ua.patents.su/3-66108-sposib-oderzhannya-6-amino-35-diciano-4-cikloalkilspiro-1234-tetragidropirid-2-oniv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 6-аміно-3,5-диціано-4-циклоалкілспіро-1,2,3,4-тетрагідропірид-2-онів</a>
Попередній патент: Спосіб діагностики деталей двигуна внутрішнього згорання
Наступний патент: Система автономного водяного опалення багатоповерхового будинку
Випадковий патент: Спосіб виробництва дієтичної добавки "нутріо-гем" з крові великої рогатої худоби







