2-галогено-6-дифторометоксипохідні нітробензолу, аніліну та n-фенілтіосечовини
Номер патенту: 69144
Опубліковано: 16.08.2004
Автори: Фіалков Юрій Аркадійович, Ягупольський Лев Мусійович
Формула / Реферат
2-Галогено-6-дифторометоксипохідні нітробензолу, аніліну та N-фенілтіосечовини загальної формули (І)
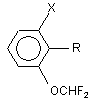 ,
,
І
де Х=Сl, R=NO2 (Іа); Х=Br, R=NO2 (Iб); Х=Сl, R=NH2 (Iв);
Х=Br, R=NH2 (Iг); Х=Сl, ![]() (Ід); Х=Br ,
(Ід); Х=Br ,![]() (Іе).
(Іе).
Текст
Винахід належить до органічної хімії, конкретно до нових фторовмісних похідних бензолу з азотовмісними замісниками загальної формули (І) Сполуки, що заявляються, є новими і в літературі не описані. Цінність речовин подібного типу - 2,6дизамісних азотовмісних похідних бензолу полягає в тому, що вони можуть бути використані, як синтони для одержання важливих біологічно активних сполук типу антигіпертензивного засобу "Клофелін" (II) ("Клонідін") [1, 2]. Відомо, що введення атомів фтору в молекули потенційних біологічно активніх сполук сприяє проявленню фармакологічної дії, підвищує стійкість з'єднань, знижує токсичність [3]. Виходячи з цього положення, випливає задача винаходу - створення нових синтонів - фторовмісних реакційноздатних вихідних речовин, які можуть бути використані для синтезу різноманітних біологічно активніх сполук з покращеними властивостями. Так, наприклад, на основі 2-хлоро(бромо)-6-дифторометоксифенілтіосечовин (I), був здійснений синтез нових сполук - фторовмісних аналогів препарату "Клофелін" (II), які в експерименті виявили виразну антигіпертензивну активність, перевищуючи його по ряду показників [4]. Задача вирішується шляхом синтезу нових хімічних з'єднань - азотовмісних 2-галогено-6дифторометоксипохідних нітробензолу, аніліну, та N-фенілтіосечовини загальної формули (І) Синтез вказаної серії нових сполук, що заявляються, здійснюється за схемою: Основні вихідні речовини в синтезі нових сполук, що заявляються, -2-нітро-3-хлор(бром)феноли одержувались нітруванням відповідно м-хлор- та м-бромфенолів концентрованою азотною кислотою в присутності олеуму [5, 6]. Отримані галогенонітрофеноли перетворювались у відповідні нові дифторометоксигалогенонітропохідні [(І), Х=Сl, Br; R=NO2)] шляхом дифторометилювання дією хладону-22 (дифторохлорометану) в присутності надлишку гідроксиду натрію у водно-ізопропанольному середовищі. Відновлення цих отриманих нітропохідних та одержання 2-хлоро(бромо)-6-дифторометоксианілінів [(І), Х=С l, Br; R=NH2)] здійснювалось за допомогою залізного порошку у воді з додаванням хлориду амонію як електроліту. Взаємодією цих похідних аніліну з бензоїлізотіоціанатом були отримані бензоїльні похідні тіосечовин, гідроліз яких гідроксидом натрію у воді приводить до відповідних фторовмісних N-арилтіосечовин [(І), Х=С l, Br; R=NHC(S)-NH2)]. Склад та будова усіх нових сполук, що заявляються, підтверджені даними елементного аналізу та спектрами ЯМР 1H. Далі наведені конкретні приклади одержання сполук, що заявляються. Приклади 1. 2-Хлоро-6-дифторометоксинітробензол. [(Іа), Х=Сl, R=NO2)]. У тригорлу колбу місткістю 500см3, що має ефективну механічну мішалку, зворотний холодильник з гідрозатвором, термометр та барботер для подачі хладону-22 (дифторохлорометану), завантажують 34,7г (0,2моль) 2-нітро-3-хлорофенолу [5], 100см3 ізопропилового спирту і розмішують до повного розчинення нітрохлорофенолу (при необхідності підігрівають реакційну суміш до 35-40°С). Починають подавати через барботер хладон-22 та поступово додають розчин 50г (1,2моль) гідроокису натрію у 60см3 води. Реакційна суміш перетворюється у червоно-чорну суспензію кристалів нітрохлорофеноляту натрію. Температуру підвищують до 65-70°С і при ефективному розмішуванні подають ток хладону-22 протягом 3 год. Перевіряють лужність реакційної суміші та при необхідності додають 5-10см3 50% розчину гідроокису натрію і продовжують пропускати хладон-22 ще 30-40хв. Закінчення процесу дифторометилювання фіксують по поступовому переходу червоно-чорного кольору реакційної суміші до жовтого та проскоку хладону через гідрозатвор. Суміш охолоджують до 20-25°С, відфільтровують осад солей, який на фільтрі промивають 2 рази по 50см3 ефіру. Фільтрат розбавляють 500см3 води та екстрагують продукт реакції 4 рази по 150-170см3 ефіру. З'єднані ефірні промивки та екстракти промивають водою до нейтральної реакції і сушать сульфатом магнію. Ефір відганяють, залишок переганяють у вакуумі, збираючи фракцію, яка кипить в інтервалі 127-130°С при 1мм.рт.ст. Вихід 2-хлоро-6-дифторометоксинітробензолу 39г (87%). Знайдено, %: Сl 16.08, 16.15; N 6.01, 6.12. С7Н4СlF2NО3. Вираховано, %: Сl 15.88; N 6.26. Спектр ЯМР 1Н ( d , м.ч.) в СDСl3: група сигналів у діапазоні 7.2-7.4 - протони бензольного кільця; триплет з центром 6.5 - дифторометильна група. 2. 2-Бромо-6-дифторометоксинітробензол [(Iб), Х=Br, R=NО2)]. Одержаний за аналогічним способом, виходячи з 2-нітро-3-бромофенолу [6]. Вихід 2-бромо-6-дифторометоксинітробензолу 57%, т.кип. 91-93°С (0.1мм.рт.ст.). Знайдено, %: Br 29.58, 29.65; N 4.98, 5.10. С7Н4ВrF2NО3. Вираховано, %: Br 29.85; N 5.22. Спектр ЯМР1H ( d , м.ч.) в СDСl3: група сигналів у діапазоні 7.36-7.68 - протони бензольного кільця; триплет з центром 6.89 - дифторометильна група. 3. 2-Хлоро-6-дифторометоксианілін [(Iв), X=Сl, R=NH2 )]. У довгогорлу колбу для відгонки з паром місткістю 500см3, обладнану ефективною механічною мішалкою, завантажують 18г (0.32моль) залізного порошку марки ПЖР 3.200.28 або 3.200.30, 3г хлориду амонію та 70см3 води. При інтенсивному розмішуванні підігривають суспензію залізного порошку на киплячій водяній бані та за 30хв додають 18г (0.08моль) 2-хлоро-б-дифторометоксинітробензолу. Дають витримку на киплячій бані впродовж 2.5 год, а потім ще кип’ятять реакційну суміш при розмішуванні 30хв. Додають 10г гідроокису натрію та 5см3 води, приєднують до колби пристрій для відгонки з паром та холодильник-конденсатор і, не перериваючи кипіння суміші, ведуть відгонку продукту відновлення з паром у охолоджувану приймальну колбу. Туди вміщують 100г хлориду натрію, який допомагає виділенню аміну. Після закінчення відгонки аміну останній екстрагують з дистиляту ефіром або бензолом (3 рази по 100см3). З'єднані екстракти промивають водою до нейтральної реакції, сушать сульфатом магнію, розчинник відганяють, а залишок перегоняють у вакуумі. Одержують 13.1г (84%) 2-хлоро-6-дифторометоксианіліну з т.кип. 84-86°С (0.8мм.рт.ст.). Знайдено, %: С 43.48, 43.50; Н 2.97, 3.00; N 7.04, 7.19. C7H6ClF2NO. Вираховано, %: С 43.41; Н 3.10; N 7.23. Спектр ЯМР 1Н ( d , м.ч.) в CDCl3: два дублети в діапазоні 6.9-7.1 - нерівноцінні орто-протони атома хлору та дифторометоксигрупи; триплет з центром 6.6 - пара-протон аміногрупи; уширений синглет з центром 4.2 протони аміногрупи; триплет з центром 6.4 - дифторометильна група. 4. 2-Бромо-6-дифторометоксианілін [(Іг), Х=Br, R=NH2]. Одержаний за аналогічним способом з відповідного нітропохідного. Вихід 72%, т.кип. 93-95°С (0.8мм.рт.ст.). Знайдено, %: Br 33.29, 33.40; N 4.01; 4.12. С7Н6ВrF2NО. Вираховано, %: Br 33.61; N 4.20. Спектр ЯМР 1Н ( d , м.ч.) в CDCl3: група сигналів у діапазоні 6.7-7.5 - протони бензольного кільця; уширений синглет з центром 4.4 - протони аміногрупи; триплет з центром 6.7 - дифторометильна група. 5. 2-Хлоро-6-дифторометоксифенілтіосечовина. [(Ід), Х=С l, R=NH-C(S)-NH2 )]. Розчиняють 2.51г (0.033моль) сухого тіоціанату амонію в 20см3 сухого ацетону та при ефективному розмішуванні додають по краплям 4.22г (0.03моль) бензоїлхлориду. Після додавання хлороангідриду розмішують 5хв, потім киплятять 7-8хв. Охолоджують суміш та додають одразу 5.81г (0.03моль) 2-хлоро-6-дифторометоксианіліну. Суміш киплятять 1012хв та після охолодження виливають на 200см3 льодяної води. Розмішують доти, доки випавша в'язка маса не розсипається у порошок, який відфільтровують та промивають холодною водою. Одержаний осад суспендують у розчині 4.4г (0.11моль) гідроокису натрію у 40см3 води та кип'ятять при розмішуванні 10хв. Після охолодження розчин відфільтровують від мулу та на холоду підкисляють концентрованою соляною кислотою, а потім поступово додають 10% розчин аміаку до появлення лужної реакції. Реакційну суміш на 1 добу залишають у холодильнику, потім продукт екстрагують сумішшю ефір-бензол (1:1) три рази по 70-80см3. Об'єднані екстракти промивають водою та сушать сульфатом магнію. З розчину спочатку відганяють ефір, а потім частину бензолу так, щоб зосталося 40-50см3 об'єму та залишають на ніч у холодильнику. Кристали, що випали, відфільтровують та промивають холодним бензолом. Одержують 4.6г (61%) 2-хлоро-6-дифторометокси-фенілтіосечовини з т. пл. 149,5-150,5°С. Знайдено, %: С 37.92, 38.12; Н 3.00, 3.21; N 11.16, 11.21. C8H7ClF2N2OS. Вираховано, %: С 38.02; Н 2.77; N 11.09. 6. 2-Бромо-6-дифторометоксифенілтіосечовина [(Ie), X=Br, R=NH-C(S)-NH2)] одержана за аналогічним способом, виходячи з 2-бромо-6-дифторометоксианіліну з виходом 53%, т. пл. 144-146°С. Знайдено, %: С 32.60, 32.64; Н 2.37, 2.49; N 9.44, 9.52. C8H7BrF2N2OS. Вираховано, %: С 32.32; Н 2.36; N 9.43. Спектр ЯМР 1H ( d , м.ч.) в CDCl3: уширений синглет з центром 6.8 - протони аміногрупи; триплет з центром 6.96 - дифторометильна група; два дублети з центрами 7.36-7.72 - орто-протони атома брому та дифторометоксигрупи у бензольному кільці; триплет з центром 7.48 - пара-протон аміногрупи бензольного кільця; уширений синглет з центром 7.76 -протон групи NH. Спектри ЯМР 1H записані на спектрометрі Bruker WR-200. Джерел інформації: 1. Машковский М.Д. Лекарственные средства: В 2-х т.- М.: Новая волна, 2000.-T.1.-539 с. 2. Brit. Pat. 1034938 MKI 3 С07D49/34. 2-Phenylamino-1,3-diazacydopent-2-enes /Boehringer Engelheim G. m.b.H.Заявка №39420/64; Заявл. 28.09.1964; Опубл. 06.07.1966. 3. Organofluorine compounds in medicinal chemistry and biomedical applications /Eds. R. Filler, Y.Kobayashi, L.Yagupolskii.- Amsterdam, London, New York, Tokyo: Elsevier, 1993.- 386 P. 4. 2-(2-Галогено-6-дифторометоксифеніламіно)імідазоліни та гідрохлориди 2-(2-галогено-6дифторометоксифеніламіно) імідазолінів. Заявка ІОХ НАН України. 5. Hodson H., Moore F. The nitration of m-chlorophenol //J. Chem. Soc.- 1925.-Vol. 117. - P.1599-1604. 6. Hodson H., Moore F. The nitration of m-bromophenol //J. Chem. Soc.- 1926.-Vol.ll8. - P.155-161.
ДивитисяДодаткова інформація
Назва патенту англійською2-halogeno-6-difluoromethoxy derivatives of nitrobenzol, aniline, and n-phenylthiourea
Автори англійськоюYahupolskyi Lev Musiiovych, Fialkov Yurii Arkadiovych
Автори російськоюЯгупольский Лев Мусийович, Фиалков Юрий Аркадиевич
МПК / Мітки
МПК: C07B 41/00, C07B 35/00, C07C 22/00, C07C 335/00, C07B 43/00
Мітки: 2-галогено-6-дифторометоксипохідні, аніліну, n-фенілтіосечовини, нітробензолу
Код посилання
<a href="https://ua.patents.su/3-69144-2-galogeno-6-diftorometoksipokhidni-nitrobenzolu-anilinu-ta-n-feniltiosechovini.html" target="_blank" rel="follow" title="База патентів України">2-галогено-6-дифторометоксипохідні нітробензолу, аніліну та n-фенілтіосечовини</a>
Попередній патент: 2-(2-галогено-6-дифторометоксифеніламіно)імідазоліни та гідрохлориди 2-(2-галогено-6-дифторометоксифеніламіно)імідазолінів
Наступний патент: Спосіб лікування переломів довгих кісток
Випадковий патент: Пристрій для різання канатів







