Спосіб одержання 2,5-діарилоксазолів
Номер патенту: 86166
Опубліковано: 25.03.2009
Автори: Шершуков Віктор Михайлович, Пшеничников Станіслав Володимирович, Гриньов Борис Вікторович, Єлісєєв Дмитро Анатолійович
Формула / Реферат
1. Спосіб одержання 2,5-діарилоксазолів формули І
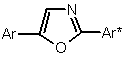 , I
, I
де Аr, Аr* - незаміщений або алкілзаміщений фенільний радикал або багатоядерний ароматичний радикал, який відрізняється тим, що включає взаємодію похідних гіпурової кислоти з п'ятихлористим фосфором, взаємодію утворених хлорангідридів з відповідним ароматичним вуглеводнем з одержанням амідів, циклодегідратацію останніх сірчаною кислотою і наступне очищення одержаних технічних продуктів до ступеня сцинтиляційної чистоти, причому на стадії утворення хлорангідридів додатково використовують каталізатор - триетиламін у кількості 1,5-5 % мас. відносно маси зазначеної кислоти.
2. Спосіб за п. 1, який відрізняється тим, що очищення одержаних технічних 2,5-діарилоксазолів формули І до ступеня сцинтиляційної чистоти здійснюють шляхом елюювання їхніх розчинів в петролейному ефірі на оксиді алюмінію.
Текст
УКРАЇНА (19) UA (11) 86166 (13) C2 (51) МПК (2009) C07D 263/00 МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ ДЕРЖАВНИЙ ДЕПАРТАМЕНТ ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ ОПИС ДО ПАТЕНТУ НА ВИНАХІД (54) СПОСІБ ОДЕРЖАННЯ 2,5-ДІАРИЛОКСАЗОЛІВ 1 2 де Аr, Аr* - незаміщений або алкілзаміщений фенільний радикал або багатоядерний ароматичний радикал, який відрізняється тим, що включає взаємодію похідних гіпурової кислоти з п'ятихлористим фосфором, взаємодію утворених хлорангідридів з відповідним ароматичним вуглеводнем з одержанням амідів, циклодегідратацію останніх сірчаною кислотою і наступне очищення одержаних технічних продуктів до ступеня сцинтиляційної чистоти, причому на стадії утворення хлорангідридів додатково використовують каталізатор - триетиламін у кількості 1,5-5% мас. відносно маси зазначеної кислоти. 2. Спосіб за п. 1, який відрізняється тим, що очищення одержаних технічних 2,5-діарилоксазолів формули І до ступеня сцинтиляційної чистоти здійснюють шляхом елюювання їхніх розчинів в петролейному ефірі на оксиді алюмінію. Винахід відноситься до області хімії, а саме до технології одержання заміщених 2,5діарилоксазолів (РРО) формули І: активаторами в яких служать РРО. Тому пошук раціональних методів синтезу цих сполук, що забезпечують технологічність хімічного процесу, скорочення сировинних, енергетичних і трудових ресурсів, а також підвищення якості готового продукту є на сьогоднішній день досить актуальною задачею. Відомий спосіб одержання заміщених 2,5діарилоксазолів [патент України №19866, С07С205/45, 207/02, C07D263/32], що полягає у взаємодії ω-амінометиларилкетона з хлорангідридами ароматичних кислот з наступною циклодегідратацією амідів, що утворюються, у сірчаній кислоті. Спосіб одержання РРО здійснюють за схемою: Згідно відомого способу необхідний для синтезу заміщених 2,5-діарилоксазолів ω (11) UA (19) де Аr, Аr* - незаміщений або алкілзаміщений фенільний радикал або багатоядерний ароматичний радикал. Сполуки формули І являють собою ефективні органічні люмінофори синьо-фіолетового світіння і широко використовуються в сцинтиляційній техніці як активатори рідких і пластмасових сцинтиляторів, як активні середовища лазерів з частотою випромінювання, що перебудовується, а також у якості оптичних відбілювачів для текстильної і паперової промисловості. В останні роки вчені все більше уваги приділяють дослідженням в області ядерної фізики по глибоководному детектуванню нейтрино. У цих експериментах, як правило, застосовуються величезні обсяги (~20т і більше) рідких сцинтиляторів, 86166 (13) C2 (21) a200713885 (22) 11.12.2007 (24) 25.03.2009 (46) 25.03.2009, Бюл.№ 6, 2009 р. (72) ГРИНЬОВ БОРИС ВІКТОРОВИЧ, UA, ШЕРШУКОВ ВІКТОР МИХАЙЛОВИЧ, UA, ЄЛІСЄЄВ ДМИТРО АНАТОЛІЙОВИЧ, UA, ПШЕНИЧНИКОВ СТАНІСЛАВ ВОЛОДИМИРОВИЧ, UA (73) ІНСТИТУТ СЦИНТИЛЯЦІЙНИХ МАТЕРІАЛІВ НАЦІОНАЛЬНОЇ АКАДЕМІЇ НАУК УКРАЇНИ, UA (56) UA 19866 C2, 25.12.1997 SU 1051083 A, 30.10.1983 US 4874876 A, 17.10.1989 (57) 1. Спосіб одержання 2,5-діарилоксазолів формули І N Ar* Ar O ,I 3 амінометиларилкетон одержують за наступною схемою: Істотними недоліками зазначеного способу є багатостадійність (5 технологічних стадій), тривалість хімічного процесу, а також застосування сильнотоксичних речовин і речовин, які легко розкладаються - хлорангідридів ароматичних кислот і особливо ω-бромацетофенонів, що є аналогами бойових отруйних речовин сльозоточивої дії "черемшина". Крім того, вихід готового продукту за відомим способом не перевищує 50%. В основу винаходу поставлена задача розробки простого способу одержання заміщених 2,5діарилоксазолів (РРО) з високими сцинтиляційними характеристиками, що забезпечує високий вихід готового продукту, зниження його собівартості за рахунок скорочення тривалості технологічного процесу і заощадження енергетичних і трудових витрат. Рішення поставленої задачі забезпечується тим, що в способі одержання заміщених 2,5діарилоксазолів формули І, де Аr, Аr* - незаміщений або алкілзаміщений фенільний радикал, або багатоядерний ароматичний радикал, відповідно до винаходу, проводять взаємодію похідних гіпурової кислоти з п'ятихлористим фосфором, взаємодію хлорангідридів, що утворилися, з відповідним ароматичним вуглеводнем з одержанням амідів, циклодегідратацію останніх сірчаною кислотою і наступне очищення отриманих технічних продуктів до ступеня сцинтиляційної чистоти, причому на стадії утворення хлорангідридів додатково використовують каталізатор - триетиламін у кількості 1,5-5% ваг. відносно ваги зазначеної кислоти. Очищення отриманих технічних заміщених 2,5діарилоксазолів формули І до ступеня сцинтиляційної чистоти здійснюють шляхом елюювання їхніх розчинів у петролейному ефірі, на оксиді алюмінію. Використання триетиламіну як каталізатора у кількості 1,5-5% ваг. відносно ваги кислоти приводить, як показали експерименти, до різкого підвищення швидкості реакції (2 години). Крім того, використання каталізатору забезпечує вибірковість реакції одержання хлорангідридів без протікання побічних реакцій і, відповідно, утворення побічних продуктів, завдяки чому досягається висока чистота заміщених бензоїламіноацетофенона, які утворюються. 86166 4 Отриманий у такий спосіб бензоїламіноацетофенон за температурою плавлення згідно з літературними даними відповідає кваліфікації "чистий" (Тпл.=132°С) і, таким чином, виключається необхідність його очищення. Введення на стадії утворення хлорангідридів триетиламіну як каталізатора у кількості 1,5-5% ваг. відносно ваги кислоти позитивно позначається і на якості кінцевих продуктів (РРО), отриманих після циклодегідратації заміщених бензоїламіноацетофенона в сірчаній кислоті, тому що застосування каталізатора забезпечує проходження реакції тільки в напрямку утворення хлорангідрида гіпурової кислоти, виключаючи побічні реакції, а також неповне перетворення кислоти у хлорангідрид. Таким чином, за своїми основними експлуатаційними характеристиками (температура плавлення, максимум люмінесценції, світловий вихід) отримані технічні продукти РРО відповідають вимогам Технічних умов ТУ 6-09-3952-79 "2,5дифенілоксазол сцинтиляційний хімічно чистий" (див. таблицю), що виключає необхідність їхнього ретельного очищення. Для досягнення більш високих показників сцинтиляційної чистоти і прозорості отриманих за способом, що заявляється, заміщених 2,5діарилоксазолів здійснюють очищення останніх шляхом елюювання їхніх розчинів у петролейному ефірі на оксиді алюмінію. Тривалість такого очищення складає не більш 2-3 годин. Вихід готових продуктів складає 75-80% для РРО. Зменшення або збільшення концентрації каталізатора, що вводиться на стадії утворення хлорангідридів, недоцільне через те, що приводить до значного зниження виходу готового продукту. У таблиці приведені порівняльні дані технологічних і основних фізико-хімічних характеристик РРО, отриманих за пропонованим способом і способом - аналогом (дані приведені з розрахунку на 1кг готового продукту). Спосіб одержання заміщених 2,5діарилоксазолів формули І здійснюють на наступних прикладах. Приклад 1 Одержання 2,5-дифенілоксазола У трьохгорлу круглодонну колбу місткістю 1л, постачену мішалкою, зворотним холодильником і термометром, завантажують 300мл бензолу, 90г (0,5моль) тонкоздрібненої гипурової кислоти і 1,8г (2% ваг. відносно ваги кислоти) каталізатора - триетиламіна. При інтенсивному перемішуванні в реакційну масу невеликими порціями обережно завантажують 114г (0,55моль) п'ятихлористого фосфору РСІ5 з такою швидкістю, щоб температура реакційної маси не перевищувала 30°С (тривалість завантаження складає приблизно 1,5 години), колбу при цьому охолоджують на водяній лазні холодною водою. Потім реакційну масу при інтенсивному перемішуванні витримують протягом 2-х годин при температурі 35°С, після чого охолоджують до 20°С і невеликими порціями присипають до неї 200г (1,5моль) АІСl3 безводного з такою швид 5 86166 кістю, щоб температура маси не перевищувала 30°С (приблизно 1 година). Під час додавання АІСl3 відбувається розігрів реакційної маси, можливе її вспінення внаслідок активного виділення НСl, тому колбу також охолоджують на водяній лазні. Після закінчення додавання усього АІСl3 реакційну масу витримують при температурі 30°С протягом 1 години. Потім її повільно нагрівають на водяній лазні, за 2 години доводять температуру до 65°С і при цій температурі перемішують масу ще 2 години, після чого дають їй трохи охолонути і при температурі 50°С виливають на 1кг подрібненого льоду для нейтралізації надлишку АlСl3. Потім з реакційної маси з водяною парою відганяють бензол, осад, що залишився, фільтрують і промивають на фільтрі спочатку 5% розчином NH3, потім водою, після чого осад добре віджимають і сушать при 70°С. Висушений до постійної ваги осад невеликими порціями при перемішуванні додають у 250мл концентрованої сірчаної кислоти з такою швидкістю, щоб температура реакційної суміші не перевищувала 40°С. Після додатку всієї кількості продукту суміш при перемішуванні і температурі 35°С витримують протягом 3-х годин, після чого виливають на 1кг льоду. Осад утвореного продукту, що випав, фільтрують, промивають водою до нейтральної реакції промивних вод на лакмус і сушать. Висушений продукт очищують шляхом елюювання його розчину в петролейному ефірі через колонку з Аl2О3. Вихід 2,5-дифенілоксазола - 88г (80%), Tпл. 73°С. Приклад 2 Одержання 2-(4-бифенілил)-5-фенілоксазола Одержання 2-(4-бифенілил)-5-фенілоксазола здійснюють аналогічно прикладу 1, але замість бензолу в реакційну масу завантажують 77г (0,5моль) дифенілу, розчиненого в 250мл чотирихлористого вуглецю. Вихід продукту - 126,2г (86%); Тпл. - 121°С. 6 Приклад 3 Одержання 2(4-метилфеніл)-5-фенілоксазола Одержання 2(4-метилфеніл)-5-фенілоксазола здійснюють аналогічно прикладу 1, але замість бензолу в реакційну масу завантажують 300мл толуолу. Вихід продукту - 96г (88%); Тпл. - 95°С. Приклад 4 Одержання 2(4-третбутилфеніл)-5фенілоксазола Одержання 2(4-третбутилфеніл)-5фенілоксазола здійснюють аналогічно прикладу 1, але замість бензолу в реакційну масу завантажують 300мл 4-третбутилбензола. Вихід продукту - 116,0г (89%); Тпл. - 105°С. Приклад 5 Одержання 2-( 2,5-диметилфеніл)-5фенілоксазола. Одержання 2-(2,5-диметилфеніл)-5фенілоксазола здійснюють аналогічно прикладу 1, але замість бензолу в реакційну масу завантажують 300мл п-ксилола. Вихід продукту - 113,3г (93%); Тпл. - 92°С. Як видно з даних таблиці, продукти, отримані способом, що заявляється, за своїми показниками значно перевищують продукти, отримані за способом-аналогом. Промислове впровадження способу, що заявляється, дозволить більш ніж у два рази скоротити тривалість технологічного процесу одержання заміщених 2,5-діарилоксазолів, практично в 10 разів скоротити витрати електроенергії, майже в 1,5 рази знизити витрати на сировину й одночасно підвищити вихід готового продукту в порівнянні з діючими на сьогоднішній день технологіями. Крім того, важливою перевагою способу, що заявляється, є той факт, що одержувані готові продукти за своїми основними характеристиками світловому виходу і прозорості - значно перевершують сполуки, одержані за способом-аналогом, і можуть успішно конкурувати на зовнішньому ринку як по якості, так і по вартості. Таблиця Найменування показника Тривалість технічного процесу, год Енергетичні витрати, кВт/година Сировинні витрати, дол США Вихід продукту Температура плавління, °С Максимум люмінесценції в толуолі, нм Сцинтиляційний вихід, % Прозорість, м Комп’ютерна верстка О. Рябко Одержання РРО за способом, що заявляється за способом по пат №19866 15 58 10 120 38,0 69,0 80% (з розрахунку на вихід- Не більше за 50% (з розрахунку ний продукт - гіпурову кисло- на вихідний продукт - ацетофету) нон) 73,5 73,0 365 365 99 80 25,0 8,0 Підписне Тираж 28 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of the 2,5-diaryloxazoles
Автори англійськоюHryniov Borys Viktorovych, Shershukov Viktor Mykhailovych, Eliseev Dmytro Anatoliiovych, Pshenychnykov Stanislav Volodymyrovych
Назва патенту російськоюСпособ получения 2,5-диарилоксазолов
Автори російськоюГринев Борис Викторович, Шершуков Виктор Михайлович, Елисеев Дмитрий Анатольевич, Пшеничников Станислав Владимирович
МПК / Мітки
МПК: C07D 263/00
Мітки: спосіб, 2,5-діарилоксазолів, одержання
Код посилання
<a href="https://ua.patents.su/3-86166-sposib-oderzhannya-25-diariloksazoliv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 2,5-діарилоксазолів</a>
Попередній патент: Спосіб відбору корів у донори ембріонів для трансплантації
Наступний патент: Пристрій для контролю параметрів фотоелектричних перетворювачів
Випадковий патент: Фільтрувальна тканина







