Спосіб одержання 5-(трифлуорометил)піролідин-2-ону та його оптичних ізомерів
Номер патенту: 94532
Опубліковано: 10.05.2011
Автори: Бездудний Андрій Васильович, Алєксєєнко Анатолій Миколайович, Пустовіт Юрій Митрофанович
Формула / Реферат
Спосіб одержання 5-(трифлуорометил)піролідин-2-ону та його оптичних ізомерів формули (1):
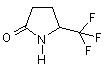 , 1
, 1
який відрізняється тим, що рацемічну 2-піролідон-5-карбонову кислоту або її оптичні ізомери піддають взаємодії з тетрафторидом сірки у присутності безводного фториду водню при температурі 20-25 °С протягом 16-20 годин з наступним виділенням цільових продуктів звичайними методами.
Текст
Спосіб одержання 5(трифлуорометил)піролідин-2-ону та його оптичних ізомерів формули (1): Винахід відноситься до органічної хімії, а саме до нового способу одержання 5(трифлуорометил)піролідин-2-ону та його оптичних ізомерів формули (1): присутності каталізатора (паладій на вугіллі) з утворенням проміжного метилового естеру 4аміно-5,5,5-трифлуоропентанової кислоти. Останній без виділення гетероциклізується у рацемічний 5-(трифлуорометил)піролідин-2-он з загальним виходом 74,5% на двох останніх стадіях [1]. Незважаючи на те, що вказаний метод є єдиним, він має ряд суттєвих недоліків, які обмежують його синтетичну значимість. По-перше, спосіб вимагає використання дорогих 1,1,1 -трифлуоро-2нітроетану та паладію. По-друге, низький загальний вихід рацемічного 5(трифлуорометил)піролідин-2-ону у 13% обмежує його використання у препаративному органічному синтезі. По-третє, цей спосіб не надає можливості синтезувати більш важливі у біологічному плані оптичні ізомери 5-(трифлуорометил)піролідин-2ону. Задачею винаходу є пошук нового зручного та ефективного способу одержання 5(трифлуорометил)піролідин-2-ону і невідомих раніше його оптичних ізомерів. Задача досягається фторуванням тетрафторидом сірки комерційно доступних та дешевих рацемату 2-піролідон-5-карбонової кислоти або її оптичних ізомерів. Спосіб отримання, який заявляється, полягає в тому, що комерційно доступні піроглутамову кис O N H F F UA (11) 94532 (13) C2 ,1 який відрізняється тим, що рацемічну 2піролідон-5-карбонову кислоту або її оптичні ізомери піддають взаємодії з тетрафторидом сірки у присутності безводного фториду водню при температурі 20-25 °С протягом 16-20 годин з наступним виділенням цільових продуктів звичайними методами. (19) Сполука даного типу знаходить застосування як вихідна для отримання речовин з гербіцидними властивостями [1] та фармакологічно важливих похідних з ноотропною активністю [2]. Спосіб одержання 5(трифлуорометил)піролідин-2-ону та його оптичних ізомерів, який заявляється, в науковій літературі та патентних виданнях не описаний. З патентної літератури відомий [1, 3] єдиний тристадійний двореакторний спосіб одержання рацемічного 5-(трифлуорометил)піролідин-2-ону з загальним виходом у 12,7%. Цей метод базується на реакції 1,1,1-трифлуоро-2-нітроетану з метиловим естером акрилової кислоти з утворенням метилового естеру 5,5,5-трифлуоро-4нітропентанової кислоти з виходом у 17% [3]. На другій стадії його нітрогрупу відновлюють воднем у F 3 лоту або її оптичні ізомери піддають обробці тетрафторидом сірки у присутності фториду водню при температурі 20-25°С на протязі 16-20 годин. Виходи цільових 5-(трифлуорометил)піролідин-2ону та його оптичних ізомерів становлять 88-92%. В умовах реакції рацемізація не спостерігається. Оптична чистота (S) та (R) енантіомерів 5(трифлуорометил)піролідин-2-ону перевищує 97% Одержаний результат не є заздалегідь передбачуваним, оскільки з літератури відомо [4], що фторування тетрафторидом сірки 3-(2,5диоксоімідазолідин-4-іл)пропанової кислоти, фрагменти молекули якої подібні до 2-піролідон-5карбонової кислоти, проходить зі значною рацемізацією. Склад та будова отриманих речовин підтверджені даними елементного аналізу та спектрами ядерного магнітного резонансу. Оптична чистота енантіомерів встановлювалась за допомогою хроматографічного аналізу на колонках з оптично активною фазою. Винахід ілюструється прикладами одержання цільових сполук рацемічного 5(трифлуорометил)піролідин-2-ону, (5S)- та (5R)-5(трифлуоро-метил)-піролідин-2-онів загальної формули (1) (див. Приклади 1, 2, 3). Приклад 1 Рацемічний 5-(трифлуорометил)піролідин-2он. 6,47 г (0,05 моль) Рацемічної 2-піролідон-53 карбонової кислоти, 5 см безводного фториду водню та 11,9 г (0,11 моль) тетрафториду сірки витримують у неіржавстальному автоклаві при температурі 25°С на протязі 16 годин. Газоподібні продукти реакції випускають з охолодженого автоклава, а залишок виливають на 50 г криги. Реакційну суміш нейтралізують 10% водним розчином аміаку, концентрують до третини вихідного об'єму на роторному випарювачі і залишають на ніч при температурі 5°С. Кристалічний осад відфільтровують. Вихід 6,74 г (88%). При необхідності продукт перекристалізовують з бензолу. Т.топл. 102103°С. Знайдено, %: F 37,09, N 9,18. C5H6F3NO. Вирахувано, %: F 37,23, N 9,15. 1 Спектр ЯМР Н (CDCІ3, ТМС): 2,2-2,28 м. (1Н), 2,30-2,41 м. (2Н), 2,46-2,60 м. (1Н), 4,09 уш.с. (1Н, NCHCF3), 7,54 уш.с. (1Н, NH). 19 Спектр ЯМР F (CDCІ3, FCCI3): -79,24 д. 3 ( JFН=7,0 Гц, 3F, CF3). 13 3 Спектр ЯМР С (CDCІ3, ТМС): 20,58 д. ( JCF=2 2 Гц, С4), 28,53 с. (С3), 55,15 кв. ( JCF=32 Гц, С5), 1 125,23 кв. ( JCF=280 Гц, CF3), 178.88 с. (С2). Приклад 2 (5S)-(-)-5-(Трифлуорометил)піролідин-2-он. 96,84 г (0,75 моль) (S)-(-)-2-Піролідон-5карбонової кислоти, 50 см безводного фториду водню та 178 г (1,65 моль) тетрафториду сірки витримують у неіржавстальному автоклаві при температурі 20°С на протязі 20 годин. Газоподібні продукти реакції випускають з охолодженого автоклава, а залишок виливають на 500 г криги. Реакційну суміш нейтралізують 10% водним розчином аміаку, кристалічний осад відфільтровують, фільт 94532 4 рат концентрують до третини вихідного об'єму на роторному випарювачі і залишають на ніч при температурі 5°С. Кристалічний осад відфільтровують 3 . Об'єднані осади перекристалізовують з 300 см води, сушать на повітрі. Вихід 106 г (92,3%). При необхідності продукт перекристалізовують з бензолу. Т.топл. 107-108°С. Оптична чистота одержаного (5S)-5-(трифлуорометил)піролідин-2-ону становить не менше ніж 98%, а питома оптична 20 активність складає [α] D= -5,5° (С=20, МеОН). Знайдено, %: F 37,19, N 9,03. C5H6F3NO. Вирахувано, %: F 37,23, N 9,15. 1 Спектр ЯМP H (CDCІ3, ТМС): 2,2-2,28 м. (1Н), 2,30-2,41 м. (2Н), 2,46-2,60 м. (1Н), 4,09 уш.с. (1Н, NCHCF3), 7,54 уш.с. (1Н, NH). 19 Спектр ЯМР F (CDCІ3, FCCI3): -79,24 д. 3 ( JFH=7,0 Гц, 3F, CF3). 13 3 Спектр ЯМР С (CDCІ3, ТМС): 20,58 д. ( JCF=2 2 Гц, С4), 28,53 с. (С3), 55,15 кв. ( JCF=32 Гц, С5), 1 125,23 кв. ( JCF=280 Гц, CF3), 178,88 с. (С2). Приклад 3 (5R)-(+)-5-(Трифлуорометил)піролідин-2-он. 6,47 г (0,05 моль) (R)-(+)-2-Піролідон-53 карбонової кислоти, 5 см безводного фториду водню та 11,9 г (0,11 моль) тетрафториду сірки витримують у неіржавстальному автоклаві при температурі 20°С на протязі 18 годин. Газоподібні продукти реакції випускають з охолодженого автоклава, а залишок виливають на 50 г криги. Реакційну суміш нейтралізують 10% водним розчином аміаку, концентрують до третини вихідного об'єму на роторному випарювані і залишають на ніч при температурі 5°С. Кристалічний осад відфільтровують. Вихід 6,81 г (89%). При необхідності продукт перекристалізовують з бензолу. Т.топл. 106107°С. Оптична чистота одержаного (5S)-5(трифлуорометил)піролідин-2-ону становить не менше ніж 97%, а питома оптична активність 20 складає [a] D= +5,4° (С=20, МеОН). Знайдено, %: F 37,21, N 9,21. C5H6F3NO. Вирахувано, %: F 37,23, N 9,15. 1 Спектр ЯМР Н (CDCІ3, ТМС): 2,2-2,28 м. (1Н), 2,30-2,41 м. (2Н), 2,46-2,60 м. (1Н), 4.09 уш.с. (1Н, NCHCF3), 7,54 уш.с. (1Н, NH). 19 Спектр ЯМР F (CDCІ3, FCCI3): -79.24 д. 3 ( JFH=7,0 Гц, 3F, CF3). 13 3 Спектр ЯМР С (CDCІ3, ТМС): 20,58 д. ( JCF=2 2 Гц, С4), 28,53 с. (С3), 55,15 кв. ( JCF=32 Гц, С5), 1 125,23 кв. ( JCF=280 Гц, CF3), 178,88 с. (С2). Література: 1. Μ. Negele, В. Baasner, H.-J. Bertram, J. Hartwig N-Acylpyrrolidine derivatives Pat. USA 5171355, Publ. 15.12.1992. 2. N. Lui, M. Negele, B. Baasner, M. Jonge, T. Schuurman Verwendung von N-substituierten αfluoralkyl-lactamen Pat. DE 4433266, Publ. 19.09.1994. 3. M. Negele, B. Baasner, A. Marhold Neue fluorierte nitroalkylverbindungen und ein verfahren zur herstellung von neuen und bekannten fluorierten nitroalkylverbindungen Pat. DE 3739784, Publ. 24.11.1987. 4. R.M. Babb, F.W. Bollinger Ω,Ω,ΩTrifluoroamino Acids J.Org.Chem. 1970, 35, 1438. 5 Комп’ютерна верстка А. Рябко 94532 6 Підписне Тираж 24 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of 5-(trifluoromethyl)pyrrolidine-2-one and optical isomers thereof
Автори англійськоюPustovit Yurii Mytrofanovych, Alieksieenko Anatolii Mykolaiovych, Bezdudnyi Andrii Vasyliovych
Назва патенту російськоюСпособ получения 5-(трифлуорометил)пирролидин-2-она и его оптических изомеров
Автори російськоюПустовит Юрий Митрофанович, Алексеенко Анатолий Николаевич, Бездудный Андрей Васильевич
МПК / Мітки
МПК: C07D 207/26
Мітки: одержання, спосіб, ізомерів, 5-(трифлуорометил)піролідин-2-ону, оптичних
Код посилання
<a href="https://ua.patents.su/3-94532-sposib-oderzhannya-5-trifluorometilpirolidin-2-onu-ta-jjogo-optichnikh-izomeriv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 5-(трифлуорометил)піролідин-2-ону та його оптичних ізомерів</a>
Попередній патент: Шприц для екстемпорального виготовлення ін’єкційного розчину
Наступний патент: Спосіб функціонування радіомаяка і пошукового обладнання при пошуку постраждалих під завалами
Випадковий патент: Судноплавний тунель для зимової навігації у арктиці







