Спосіб синтезу (7-метокси-1-нафтил)ацетонітрилу і застосування у синтезі агомелатину
Формула / Реферат
1. Спосіб промислового синтезу сполуки формули (І)
 , (I)
, (I)
який відрізняється тим, що використовують 7-метокси-1-нафтойну кислоту формули (III):
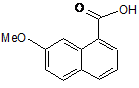 , (III)
, (III)
яку піддають дії відновного агента для одержання сполуки формули (IV):
 , (IV)
, (IV)
ОН групу сполуки формули (IV) перетворюють у відхідну групу і піддають реакції з реагентом ціанування для одержання сполуки формули (І), яку виділяють у формі твердої речовини.
2. Спосіб синтезу сполуки формули (І) за п. 1, який відрізняється тим, що відновлення кислоти формули (III) проводять, використовуючи ВН3-ТГФ.
3. Спосіб синтезу сполуки формули (І) за п. 1, який відрізняється тим, що групу ОН сполуки формули (IV) перетворюють у хлор шляхом впливу тіонілхлориду.
4. Спосіб синтезу сполуки формули (І) за п. 1, який відрізняється тим, що реагент ціанування, який використовують, являє собою ціанід калію.
5. Спосіб синтезу агомелатину, починаючи зі сполуки формули (І), який відрізняється тим, що сполуку формули (І) одержують відповідно до способу синтезу за будь-яким з пп. 1-4 і піддають відновленню, а потім реакції зв'язування з оцтовим ангідридом.
Текст
1. Спосіб промислового синтезу сполуки формули (І) CN 2 3 94837 (I). Сполука формули (І), одержана відповідно до способу за даним винаходом, є корисною у синтезі агомелатину, або N-[2-(7-метокси-1нафтил)етил]ацетаміду, формули (II): (II). Агомелатин, або N-[2-(7-метокси-1нафтил)етил]ацетамід, має цінні фармакологічні властивості. Дійсно, він має подвійні характеристики, являючись, з одного боку, агоністом рецепторів мелатонінергічної системи та, з іншого боку, антагоністом рецептора 5-НТ2С. Ці властивості забезпечують його активний вплив на центральну нервову систему та, зокрема, під час лікування глибокої депресії, сезонного афективного розладу, порушень сну, серцево-судинної патології, патології травної системи, безсоння та втоми внаслідок порушення добового ритму організму, порушень апетиту та ожиріння. Агомелатин, його одержання та застосування у терапевтиці були описані у Європейському патенті ЕР 0 447 285, а також у заявці на Європейський патент 1 564 202. Зважаючи на фармацевтичну цінність цієї сполуки, виключно важливим завданням було її одержання, використовуючи ефективний спосіб промислового синтезу, що може бути легко відтворений у промисловому масштабі і забезпечує агомелатин у хорошому виході і з високим ступенем чистоти, починаючи з економних та легкоодержуваних вихідних матеріалів. Опис патенту ЕР 0 447 285 розкриває одержання агомелатину у вісім етапів, починаючи з 7метокси-1-тетралону, із середнім виходом менше ніж 30%. Зокрема, одержання (7-метокси-1нафтил)ацетонітрилу залучає шість реакційних етапів, і ускладнення при здійсненні даного способу проявляють себе одразу при відтворенні у промисловому масштабі. В літературі розкрите одержання (7-метокси-1нафтил)ацетонітрилу у 3 етапи, починаючи з 7метокси-1-тетралону, шляхом впливу LiCH2CN з наступною гідрогенізацією з DDQ (2,3-дихлор-5,6диціано-1,4-бензохінон) і нарешті дегідруванням у кислотному середовищі (Synthetic Communication, 2001, 31(4), 621-629). Однак, загальний вихід є дуже посереднім (76%) і, зокрема, DDQ, використаний у реакції дегідрогенізації, а також нагрівання зі зворотним холодильником з бензолом, необхідне на третьому етапі, не задовольняє промисло 4 вим вимогам щодо вартості і впливу на навколишнє середовище. Опис патенту ЕР 1 564 202 розкриває значно більш ефективний і втілюваний у промисловому масштабі спосіб всього у чотири етапи, починаючи з 7-метокси-1-тетралону, включаючи два етапи на одержання (7-метокси-1-нафтил)ацетонітрилу, що дає можливість одержати середній вихід у більше ніж 60%. Хоча різні методики синтезу, розкриті у попередньому рівні техніки, описують одержання (7метокси-1-нафтил)ацетонітрилу, більшість з них застосовують 7-метокси-1-тетралон як вихідний матеріал, який являє собою сполуку, що дорого коштує і синтез якої є проблематичним. Відповідно, розробка нових шляхів синтезу, які є простими і відтворюваними і які залучають інші вихідні матеріали, залишається досі актуальною. Заявник розробив новий спосіб промислового синтезу, який відтворюваним чином і без залучення трудомісткого очищення, дає можливість одержати агомелатин такої чистоти, яка є сумісною з його застосуванням як фармацевтично активного інгредієнта, починаючи з вихідного матеріалу, який менше коштує і є легко одержуваним. Зокрема, Заявник розробив новий спосіб промислового синтезу, який дає можливість одержати (7-метокси-1-нафтил)ацетонітрил відтворюваним чином і без залучення трудомісткого очищення, використовуючи 7-метокси-1-нафтойну кислоту як вихідний матеріал. Одержання 7-метокси-1нафтойної кислоти розкрите у попередньому рівні техніки D. Becker et al., починаючи з анізолу, з відмінним виходом: Tetrahedron Letters, 27 (32), 37753776, 1986. Більш конкретно даний винахід стосується способу промислового синтезу сполуки формули (І): (I), який відрізняється тим, що 7-метокси-1нафтойну кислоту формули (III) використовують для реакції: (III), яку піддають дії відновного агента для одержання сполуки формули (IV): 5 94837 (IV), ОН функцію сполуки формули (IV) перетворюють у відхідну групу і піддають реакції з реагентом ціанування для одержання сполуки формули (І), яку виділяють у формі твердої речовини. Серед відновних агентів, які можуть використовувати для відновлення кислоти формули (III) у способі за даним винаходом, можуть бути згадані, без будь-якого обмеження, ВН3, NaBH4/AlCl3, 9борабіцикло[3.3.1]нонан, LiAlH4, AlH3, діізобутилалюміній гідрид (DIBAL-H) і, більш конкретно, ВН3ТГФ. Відновлення кислоти формули (III) у способі за даним винаходом можуть також проводити, переважно, після перетворення кислоти формули (III) у кислотне похідне і, більш конкретно, в ефір, з наступним відновленням цього кислотного похідного у спирт формули (IV), використовуючи відновні агенти LiAlH4, NaBH4, пов'язаний або не пов'язаний з МеОН, LiBH4, DIBAL-H або біс(2метоксіетокси)-алюміній натрій гідрид (Red-Al). Переважно, групу ОН сполуки формули (IV) способу за даним винаходом перетворюють в галоген і, більш конкретно, бром або хлор, або в тозилатну, мезилатну, нозилатну або трифлатну групу. Більш переважно, перетворення у відхідну групу проводять, використовуючи трибромід бору, тіоніл хлорид, мезил хлорид, тозил хлорид, трифторметансульфоніл хлорид або нозил хлорид. Переважно, ОН групу сполуки формули (IV) перетворюють в хлор шляхом дії тіоніл хлориду. Серед реагентів ціанування, які можуть бути використані у способі за даним винаходом, можуть бути згадані, без будь-якого обмеження, триметилсиліл ціанід, ціанід літію, ціанід натрію, ціанід калію і тетрабутиламоній ціанід. Переважний реагент ціанування являє собою ціанід калію. Сполуку формули (І), одержану таким чином, коли потрібно, піддають відновленню, а потім реа Комп’ютерна верстка Л. Литвиненко 6 кції зв'язування з оцтовим ангідридом для одержання агомелатину. Приклад: (7-Метокси-1-нафтил)ацетонітрил Стадія А: (7-Метокси-1-нафтил)метанол До 1 еквіваленту 7-метокси-1-нафтойної кислоти (100 г) в ТГФ (3,8 мл/г) повільно додають 2,5 еквіваленти 1М ВН3-ТГФ (1,235 літри). Під час додавання температуру реакційної суміші підтримують при 5°С (+/- 2°С) і потім суміш залишають при температурі навколишнього середовища на 3 години. Після випаровування під зниженим тиском залишок вміщують в дихлорметан і промивають водою. Органічну фазу висушують над MgSO4 і потім розчинники випаровують під зниженим тиском для одержання вказаної у заголовку сполуки у формі світло-коричневої твердої речовини з виходом 91%. Точка плавлення: 72-74°С. Стадія В: 1-(Хлорметил)-7-метоксинафтален До розчину сполуки, одержаної на Стадії А, (100 г) в дихлорметані (5 мл/г) додають 2 еквіваленти тіоніл хлориду (126,35 г). Суміш нагрівають зі зворотним холодильником і підтримують при нагріванні зі зворотним холодильником протягом 2 годин. Після повернення до температури навколишнього середовища розчинник випаровують під зниженим тиском. Одержану олію вміщують в етилацетат і промивають водою і потім насиченим розчином NaCl. Розчинник випаровують під зниженим тиском і сирий продукт очищують шляхом пропускання через подушку силікагелю (елюент: гептан). Вказану у заголовку сполуку одержують у формі твердої речовини жовтого кольору з виходом 84%. Стадія С: (7-Метокси-1-нафтил)ацетонітрил До розчину сполуки, одержаної на Стадії В, (100 г) у 30 мл/г ДМСО і 5 мл/г води додають 1,2 еквіваленти ціаніду калію (37,8 г). Реакційну суміш нагрівають до 65°С і підтримують при 65°С протягом 3 годин. Після повернення до температури навколишнього середовища, до суміші додають подвійну систему МТВЕ/вода (1/1). Водну фазу видаляють. Органічну фазу промивають декілька разів водою і потім насиченим розчином NaCl. Розчинники дистилюють і вказану у заголовку сполуку одержують у кількісному виході. Точка плавлення: 83°С. Підписне Тираж 24 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the synthesis of (methoxy-1-naphthyl) acetonitrile and use in the synthesis of agomelatine
Автори англійськоюDubuffet Thierry, Lecouve, Jean-Pierre, Hermet, Jean-Paul
Назва патенту російськоюСпособ синтеза (7-метокси-1-нафтил)ацетонитрила и применение в синтезе агомелатина
Автори російськоюДюбюффе Тьерри, Лекув Жан-Пьер, Эрме Жан-Поль
МПК / Мітки
МПК: C07C 255/37, C07C 231/02, C07C 233/18, C07C 253/14
Мітки: застосування, 7-метокси-1-нафтил)ацетонітрилу, синтезу, агомелатину, синтезі, спосіб
Код посилання
<a href="https://ua.patents.su/3-94837-sposib-sintezu-7-metoksi-1-naftilacetonitrilu-i-zastosuvannya-u-sintezi-agomelatinu.html" target="_blank" rel="follow" title="База патентів України">Спосіб синтезу (7-метокси-1-нафтил)ацетонітрилу і застосування у синтезі агомелатину</a>







