Спосіб синтезу (7-метокси-1-нафтил)ацетонітрилу і його застосування у синтезі агомелатину
Формула / Реферат
1. Спосіб промислового синтезу сполуки формули (І)
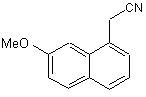 (I),
(I),
який відрізняється тим, що 7-метокси-1-тетралон формули (IV):
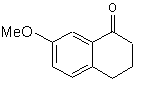 (IV)
(IV)
піддають реакції з ціанооцтовою кислотою формули (V):
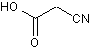 (V)
(V)
в умовах, коли воду, що утворилась, видаляють, у присутності каталітичної кількості сполуки формули (VI):
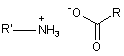 (VI),
(VI),
де R і R', які можуть бути однаковими або відрізнятися, кожний являє собою лінійну або розгалужену (С3-С10)алкільну групу, незаміщену або заміщену арильну групу, або незаміщену або заміщену лінійну або розгалужену арил(С1-С6)алкільну групу,
з одержанням, після фільтрування і промивання основним розчином, (7-метокси-3,4-дигідро-1-нафталеніл)ацетонітрилу формули (VII):
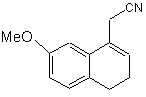 (VII),
(VII),
сполуку формули (VII) піддають реакції з каталізатором гідрогенізації у присутності сполуки алілу,
з одержанням сполуки формули (І) після фільтрування і видалення розчинника за допомогою випаровування, сполуку формули (І) виділяють у формі твердої речовини після перекристалізації,
де:
- арил, як повинно розумітися, означає фенільну, нафтильну або біфенільну групу,
- термін "заміщений", що визначає терміни "арил" і "арилалкіл", означає, що ароматична частина цих груп може бути заміщена від 1 до 3 однаковими або різними групами, вибираними з лінійного або розгалуженого (С1-С6)алкілу, гідрокси і лінійного або розгалуженого (С1-С6)алкокси,
- "сполука алілу", як повинно розумітися, являє собою будь-яку молекулу, яка містить від 3 до 10 атомів вуглецю, що можуть містити в доповнення від 1 до 5 атомів кисню, і містить щонайменше одну -СН2-СН=СН2 групу.
2. Спосіб синтезу сполуки формули (І) за п. 1, який відрізняється тим, що перетворення сполуки формули (IV) у сполуку формули (VII) проводять при нагріванні зі зворотним холодильником з толуолом.
3. Спосіб синтезу сполуки формули (І) за п. 1, який відрізняється тим, що каталізатор, залучений для перетворення сполуки формули (IV) у сполуку формули (VII), являє собою каталізатор формули (VIa):
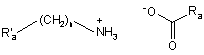 , (VIa)
, (VIa)
де R'a являє собою фенільну групу, незаміщену або заміщену однією або більше лінійною або розгалуженою (С1-С6)алкільними групами, n являє собою 0 або 1, і Ra являє собою лінійну (С3-С10)алкільну групу.
4. Спосіб синтезу сполуки формули (І) за п. 1, який відрізняється тим, що R являє собою гексильну групу.
5. Спосіб синтезу сполуки формули (І) за п. 1, який відрізняється тим, що R' являє собою бензильну групу.
6. Спосіб синтезу сполуки формули (І) за п. 1, який відрізняється тим, що каталізатор, використаний для перетворення сполуки формули (IV) у сполуку формули (VII), являє собою гептаноат бензиламонію формули (VIII):
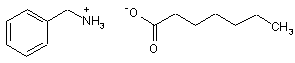 (VIII).
(VIII).
7. Сполука формули (VII), яка являє собою (7-метокси-3,4-дигідро-1-нафталеніл)ацетонітрил для застосування як проміжної сполуки у синтезі агомелатину.
8. Спосіб синтезу сполуки формули (І) за п. 1, який відрізняється тим, що перетворення сполуки формули (VII) у сполуку формули (І) проводять при нагріванні зі зворотним холодильником толуолу.
9. Спосіб синтезу сполуки формули (І) за п. 1, який відрізняється тим, що каталізатор гідрогенізації, використаний у перетворенні сполуки формули (VII) у сполуку формули (І), являє собою паладій.
10. Спосіб синтезу сполуки формули (І) за п. 1, який відрізняється тим, що каталізатор гідрогенізації, використаний у перетворенні сполуки формули (VII) у сполуку формули (І), являє собою 5% паладій-на-вугіллі.
11. Спосіб синтезу сполуки формули (І) за п. 1, який відрізняється тим, що кількість каталізатора гідрогенізації, використаного у перетворенні сполуки формули (VII) у сполуку формули (І), складає 5% за вагою каталізатора відносно ваги субстрату.
12. Спосіб синтезу агомелатину, починаючи зі сполуки формули (VII), який відрізняється тим, що сполуку формули (VII) одержують способом синтезу за будь-яким з пп. 1-6 і піддають ароматизації з наступним відновленням і потім піддають сполученню з оцтовим ангідридом.
13. Спосіб синтезу агомелатину, починаючи зі сполуки формули (І), який відрізняється тим, що сполуку формули (І) одержують способом синтезу за будь-яким з пп. 1-6 і 8-11 і піддають відновленню і потім сполученню з оцтовим ангідридом.
Текст
1. Спосіб промислового синтезу сполуки формули (І) 2 3 79479 4 де R'a являє собою фенільну груп у, незаміщену нагріванні зі зворотним холодильником толуолу. або заміщену однією або більше лінійною або роз9. Спосіб синтезу сполуки формули (І) за п.1, який галуженою (С1-С6)алкільними групами, n являє відрізняє ться тим, що каталізатор гідрогенізації, собою 0 або 1, і Ra являє собою лінійну (С3використаний у перетворенні сполуки формули С10)алкільну груп у. (VII) у сполуку формули (І), являє собою паладій. 4. Спосіб синтезу сполуки формули (І) за п.1, який 10. Спосіб синтезу сполуки формули (І) за п.1, відрізняє ться тим, що R являє собою гексильну який відрізняється тим, що каталізатор гідрогенігруп у. зації, використаний у перетворенні сполуки фор5. Спосіб синтезу сполуки формули (І) за п.1, який мули (VII) у сполуку формули (І), являє собою 5% відрізняє ться тим, що R' являє собою бензильну паладій-на-вугіллі. груп у. 11. Спосіб синтезу сполуки формули (І) за п.1, 6. Спосіб синтезу сполуки формули (І) за п.1, який який відрізняється тим, що кількість каталізатора відрізняє ться тим, що каталізатор, використаний гідрогенізації, використаного у перетворенні сподля перетворення сполуки формули (IV) у сполуку луки формули (VII) у сполук у формули (І), складає формули (VII), являє собою гептаноат бензиламо5% за вагою каталізатора відносно ваги субстрату. нію формули (VIII): 12. Спосіб синтезу агомелатину, починаючи зі -O + сполуки формули (VII), який відрізняється тим, NH 3 CH 3 що сполуку формули (VII) одержують способом синтезу за будь-яким з пп.1-6 і піддають ароматиO (VIII). зації з наступним відновленням і потім піддають 7. Сполука формули (VII), яка являє собою (7сполученню з оцтовим ангідридом. метокси-3,4-дигідро-1-нафталеніл)ацетонітрил для 13. Спосіб синтезу агомелатину, починаючи зі застосування як проміжної сполуки у синтезі агосполуки формули (І), який відрізняється тим, що мелатину. сполуку формули (І) одержують способом синтезу 8. Спосіб синтезу сполуки формули (І) за п.1, який за будь-яким з пп.1-6 і 8-11 і піддають відновленню відрізняє ться тим, що перетворення сполуки фоі потім сполученню з оцтовим ангідридом. рмули (VII) у сполуку формули (І) проводять при Даний винахід відноситься до способу промислового синтезу (7-метокси-1нафтил)ацетонітрилу і його застосування у промисловому виробництві агомелатину, або N-[2-(7метокси-1-нафтил)етил]ацетаміду. Більш конкретно, даний винахід відноситься до способу промислового синтезу сполуки формули (І): (I) Сполука формули (І), одержана відповідно до способу даного винаходу, є корисною в синтезі агомелатину, або N-[2-(7-метокси-1нафтил)етил]ацетаміду, формули (II): (II) Агомелатин, або N-[2-(7-метокси-1нафтил)етил]ацетамід, володіє цінними фармакологічними властивостями. Дійсно, він має подвійну особливість існування, з одного боку, він є агоністом рецепторів мелатонінергічної системи і, з іншого боку, антагоністом 5-НТ2C рецептора. Такі властивості надають активність в центральній нервовій системі і, більш конкретно, у лікуванні суворої депресії, сезонних емоційних розладів, розладів сну, серцево-судинних патологій, патологій травного тракту, безсоння і втоми, яка виникає через порушення добового ритму організму, розладів апетиту і ожиріння. Агомелатин, його одержання і терапевтичне застосування були розкриті в [описі патентної заявки ЕР 0 447 285]. Беручи до уваги фармацевтичне значення цієї сполуки, важливим було спромогтись одержати її ефективним промисловим способом синтезу, який є легко транспонованим на промислові ваги і дає агомелатин з хорошим виходом і відмінною чистотою. [Опис патентної заявки ЕР 0 447 285] розкриває одержання агомелатину за вісім стадій, починаючи з 7-метокси-1-тетралону, даючи середній вихід менше ніж 30%. Цей спосіб включає дію етил бромацетату, з наступними ароматизацією і омиленням, для одержання відповідної кислоти, яку потім перетворюють в ацетамід і згодом дегідрують для одержання (7-метокси-1-нафтил)ацетонітрилу, з наступним відновленням, а потім конденсацією ацетил хлориду. Зокрема, одержання (7-метокси-1нафтил)ацетонітрилу включає шість стадій реакції і, транспонований на промислові ваги, швидко демонстрував труднощі здійснення способу, що викликаються, головним чином, проблемами відтворюваності першої стадії, що складає дію етил бромацетату на 7-метокси-1-тетралон відповідно до реакції Реформатскі, даючи етил (7-метокси3,4-дигідро-1(2Н)нафталеніліден)етаноат. Крім того, наступна стадія ароматизації етил (7-метокси-3,4-дигідро-1(2Н)нафталеніліден)етаноату часто була незавершеною і в результаті давала, після омилення, суміші продуктів, які важко очищува ти. 5 79479 6 Література описує одержання (7-метокси-1мішки, формули (III): нафтил)ацетонітрилу в трьох стадіях, починаючи з 7-метокси-1-тетрагону, дією LiCH2CN, з наступною (III) дегідрогенізацією з DDQ (2,3-дихлор-5,6-диціано1,4-бензохінон) і нарешті дегідруванням в кислотному середовищі (Synthetic Communication, 2001, домішка якого не може бути піддана наступній 31(4), 621-629). Повний вихід є середнім (76%), ароматизації в робочих умовах, які сумісні з прооднак, і зокрема DDQ, використаний в реакції дегімисловими вимогами з метою проведення синтезу дрогенізації і нагріванні бензолу зі зворотним хоагомелатину. лодильником, необхідним на третій стадії, не відБільш конкретно, даний винахід відноситься повідають промисловим вимогам стосовно до способу промислового синтезу сполуки формувартості і навколишнього середовища. ли (І): Заявник в даний момент розробив новий спосіб промислового синтезу, який в результаті дає, відтворюваним чином і без необхідності важкого (I) очищення, агомелатин чистоти, сумісної з його використанням як фармацевтично активного інгякий відрізняється тим, що 7-метокси-1редієнта. тетралон формули (IV): Альтернатива до складностей, які зустрічаються у способі, розкритому в [описі патентної заявки ЕР 0 447 285], була одержана безпосеред(IV) нім конденсуванням ціано сполуки з 7-метокси-1тетралоном. Крім того необхідним було, щоб одепіддають реакції з ціанооцтовою кислотою форжана конденсована сполука могла бути легко рмули (V): піддана ароматизації для одержання (7-метокси-1нафтил)ацетонітрилу без необхідності в сильноді(V) ючих умовах, і щоб могли бути використаними реактиви, сумісні з промисловими вимогами щодо в умовах, коли воду, що утворилась, видалявартості і навколишнього середовища. ють, у присутності каталітичної кількості сполуки Очевидно, що (7-метокси-3,4-дигідро-1формули (VI): нафталеніл)ацетонітрил буде являти собою ідеальну проміжну сполуку синтезу, що відповідає ви(VI) могам для прямого синтезу з 7-метокси-1тетралону, і буде відмінним субстратом для стадії де R і R', які можуть бути однаковими або відароматизації. різнятись, кожний являє собою лінійну або розгаРеакції для прямої конденсації тетралонів з лужену (С3-С10)алкільну групу, незаміщену або ацетонітрилу або сполук ацетонітрилу описані в заміщену арильну групу, або незаміщену або залітературі. Зокрема, [опис патентної заявки US 3 міщену лінійну або розгалужену арил (С1992 403] розкриває конденсацію ціанометил фосС6)алкільну груп у, фонату з 6-фтор-1-тетралоном, і [опис патентної для одержання, після фільтрування і промизаявки US 3 931 188] розкриває конденсацію ацевання основним розчином, (7-метокси-3,4-дигідротонітрилу з тетралоном, який веде до проміжної 1-нафталеніл)ацетонітрилу формули (VII): ціано сполуки, яка безпосередньо залучена у наступній реакції. Застосована до 7-метокси-1-тетралону, кон(VII) денсація ацетонітрилу дає суміш ізомерів, в яких "екзо" складає більшу частину і "ендо" - незначну частину, відповідно до Фігури 1: сполуку формули (VII) якої піддають реакції з каталізатором гідрогенізації у присутності сполуки алілу, для одержання сполуки формули (І) після фільтрування і видалення розчинника за допомогою випаровування, сполуку формули (І) якої виділяють у формі твердої речовини після перекристалізації, таку суміш, що потребує наступних сильнодіюде: чих умов ароматизації, які не сумісні з промисло- арил, як повинно розумітись, означає фенівими вимогами з метою проведення синтезу агольну, нафтильну або біфенільну груп у, мелатину. - термін "заміщений", що визначає терміни Заявник в даний момент розробив новий спо"арил" і "арилалкіл", означає, що ароматична чассіб промислового синтезу, який дозволяє одержатина цих груп може бути заміщена від 1 до 3 однати (7-метокси-1-нафтил)ацетонітрил з 7-метоксиковими або різними групами, вибираними з лінійтетралону, з можливістю відтворення і без необного або розгалуженого (С1-С6)алкілу, гідрокси і хідності у важкому очищенні, тільки за дві стадії за лінійного або розгалуженого (С1-С6)алкокси, допомогою використання як проміжної сполуки - "сполука алілу", як повинно розумітись, являє синтезу (7-метокси-3,4-дигідро-1собою будь-яку молекулу, яка містить від 3 до 10 нафталеніл)ацетонітрилу, вільного від "екзо" до 7 79479 8 атомів вуглецю, що можуть містити в доповнення більш конкретно 5%. від 1 до 5 атомів кисню, і містить щонайменше Водневий акцептор, переважно використаний одну -СН2-СН=СН2 групу. в реакції перетворення сполуки формули (VII) у Більш конкретно, в реакції перетворення спосполуку формули (І), являє собою сполуку алілу і, луки формули (IV) в сполук у формули (VII), воду, більш конкретно, аліл акрилат або ефір аліл гліцияка утворюється, видаляють дистиляцією. Передилу. Переважний аліл акрилат способу відповідважно використовують реакційний розчинник, що но до даного винаходу являє собою аліл метакримає температуру кипіння вище або яка дорівнює лат. температурі кипіння води, і навіть більш переважЦей спосіб представляє конкретний інтерес з но той, що утворює азеотроп з водою, такий як, наступних причин: наприклад, ксилол, толуол, анізол, етилбензол, - він дозволяє одержати "ендо" сполуку фортетрахлоретилен, циклогексен або мезитилен. мули (VII), виключно, на промислових вагах. Цей Переважно, перетворення сполуки формули результат зовсім дивує, зважаючи на літературу, (IV) у спонуку формули (VII) проводять при нагріяка має відношення до такого тину реакції, яка ванні зі зворотним холодильником толуолу або найбільш часто повідомляє про одержання "екксилолу і, більш конкретно, при нагріванні зі зворозо"/"ендо" суміші (Tetrahedron, 1966, 22, 3021тним холодильником толуолу. 3026). Результат є таким завдяки використанню У реакції перетворення сполуки формули (IV) сполуки, формули (VI) як каталізатора реакції зау сполуку формули (VII), переважно одна з груп R мість амоній ацетатів, які в даний момент викорисабо R' залученого каталізатора являє собою лінійтовуються в таких реакціях (Bull. Soc. Chim. Fr, ну або розгалужену (С3-С10)алкільну групу, а інша 1949, 884-890), являє собою арильну або арилалкільну гр упу. - ступінь перетворення сполуки формули (IV) у Більш конкретно, переважним каталізатором є сполуку формули (VII) є дуже високою, перевищукаталізатор формули (VIa): ючи 97%, на відміну від того, що могло б спостерігатись при використанні оцтової кислоти, для якої ступінь не перевищує 75%, (VI a) - використання каталізатора гідрогенізації у присутності сполуки алілу для перетворення споде R'a являє собою фенільну груп у, незаміщелуки формули (VII) у сполуку формули (І) є цілком ну або заміщену однією або більше лінійною або сумісним з промисловими вимогами щодо вартості розгалуженою (С1-С6)алкільними групами, η являє і навколишнього середовища, на відміну від хінособою 0 або 1, і Ra являє собою лінійну (С3нів, які в даний момент використовуються, С10)алкільну груп у. - до того ж, він дозволяє сполуку формули (І), Переважно, R'a являє собою незаміщену або виключно, зокрема вільну від відповідного продукзаміщену фенільну групу, більш конкретно незату відновлення формули (IX): міщену фенільну гр упу. Переважна група Ra являє собою гексильну груп у. Переважним значенням n є 1. Переважним каталізатором, який використовується у перетворенні сполуки формули (IV) у сполуку формули (VII) відповідно до способу даного винаходу, є бензиламоній гептаноат формули (VIII): (VIII) Переважно, сполуку формули (VII) одержують після фільтрування і промивання мінеральним або органічним основним розчином, таким як NaOH, KОН, Са(ОН)2, Sr(OH)2 або NH4OH, і більш конкретно розчином гідроксиду натрію. Переважно, перетворення сполуки формули (VII) у сполук у формули (І) проводять при нагріванні зі зворотним холодильником толуолу або ксилолу, більш переважно при нагріванні зі зворотним холодильником толуолу. Каталізатор, який переважно використовують у перетворенні сполуки формули (VII) у сполуку формули (І), являє собою каталізатор або у формі оксиду або підтримуваний як, наприклад, паладій, платина, нікель, Аl2О3 і, більш конкретно, паладій. Переважно, буде використано від 1 до 20% паладію-на-вуглеці, і більш конкретно від 5% або 10% паладію-на-вуглеці. Переважно, паладій-навуглеці буде використаний у кількості від 1 до 10% за вагою каталізатора відносно ваги субстрату, і (IX) одержати на промислових вага х, - нарешті, ступені перетворення сполуки формули (VII) у сполук у формули (І), що спостерігаються, є високими, перевищуючи 90%. Сполука формули (VII), одержана відповідно до способу даного винаходу, є новою і корисною як проміжна сполука в синтезі агомелатину, в якому її піддають ароматизації, з наступним відновленням і потім піддають зв'язуванню з оцтовим ангідридом. Сполуку формули (І), одержану таким чином, якщо необхідно, піддають відновленню і потім зв'язуванню з оцтовим ангідритом для одержання агомелатину. Приклади, вказані нижче, ілюструють винахід, але не обмежують його жодним чином. Приклад 1: (7-Метокси-1-нафтил)ацетамід Стадія А: (7-Ме токси-3,4-дигідро-1нафталеніл)ацетонітрил В 670-літровий реактор вміщують 85,0кг 7метокси-1-тетралону, 60,3кг ціанооцтової кислоти і 15,6кг гептанової кислоти в толуолі у присутності 12,7кг бензиламіну. Суміш нагрівають зі зворотним холодильником. Коли весь вихідний субстрат зникає, розчин охолоджують і фільтрують. Одержаний осад промивають толуолом і потім одержаний фільтрат промивають 2Ν розчином гідроксиду натрію 9 79479 10 і потім водою до нейтрального стану. Після видаревищує 99%. лення розчинника випаровуванням, одержану твеТочка плавлення: 83°С. рду речовину перекристалізовують з суміші етаПриклад 2: (7-Метокси-1-нафтил)ацетонітрил нол/вода (80/20), для одержання вказаного у Стадія А: (7-Ме токси-3,4-дигідро-1заголовку продукту з виходом 90% і хімічною чиснафталеніл)ацетонітрил тотою, яка перевищує 99%. В 670-літровий реактор вміщують 85,0кг 7Точка плавлення: 48-50°С. метокси-1-тетралону, 60,3кг ціанооцтової кислоти і Стадія В: (7-Метокси-1-нафтил)ацетонітрил 15,6кг гепатнової кислоти в толуолі у присутності В 670-літровий реактор вміщують 12,6кг 5% 11,0кг аніліну. Суміш нагрівають зі зворотним хопаладію-на-вуглеці в толуолі, який нагрівають зі лодильником. Коли весь початковий субстрат знизворотним холодильником; потім 96,1кг (7кає, розчин охолоджують і фільтрують. Одержаний метокси-3,4-дигідро-1-нафталеніл)ацетонітрилу, осад промивають толуолом і потім одержаний фіякий розчиняють в толуолі, додають також як і льтрат промивають 2N розчином гідроксиду натрію 63,7кг аліл метакрилату. Реакцію продовжують при і потім водою до нейтрального стану. Після виданагріванні зі зворотним холодильником з наступлення розчинника випаровуванням, одержану твеною парофазною хроматографією. Коли весь порду речовину перекристалізовують з суміші етачатковий субстрат зникає, реакційну суміш охолонол/вода (80/20), для одержання вказаного у джують до температури навколишнього заголовку продукту з виходом 87% і хімічною чиссередовища і потім фільтрують. Після видалення тотою, яка перевищує 99%. толуолу випаровуванням, одержаний твердий заТочка плавлення: 48-50°С. лишок перекристалізовують з суміші етанол/вода Стадія В: (7-Метокси-1-нафтил)ацетонітрил (80/20), для одержання вказаного у заголовку проМетодика є такою ж, як і на Стадії В Прикдукту з виходом 91% і хімічною чистотою, яка пеладу 1. Комп’ютерна в ерстка Т. Чепелев а Підписне Тираж 26 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for (7-methoxy-1-naphtyl) ethane nitrile synthesis and its use in agomelatin synthesis
Автори англійськоюSouvie Jean-Claude, Isaac GONZALES BLANKO
Назва патенту російськоюСпособ синтеза (7-метокси-1-нафтил) ацетонитрила и его применения в синтезе агомелатина
Автори російськоюСувье Жан-Клод
МПК / Мітки
МПК: C07C 253/30, C07C 233/18, C07C 231/00, C07C 255/37, C07B 61/00
Мітки: синтезі, 7-метокси-1-нафтил)ацетонітрилу, синтезу, агомелатину, спосіб, застосування
Код посилання
<a href="https://ua.patents.su/5-79479-sposib-sintezu-7-metoksi-1-naftilacetonitrilu-i-jjogo-zastosuvannya-u-sintezi-agomelatinu.html" target="_blank" rel="follow" title="База патентів України">Спосіб синтезу (7-метокси-1-нафтил)ацетонітрилу і його застосування у синтезі агомелатину</a>
Попередній патент: Ранозагоювальний препарат та спосіб його одержання
Наступний патент: Лікарський засіб, що містить дизоразоли та їх похідні, для лікування доброякісних та злоякісних пухлинних захворювань
Випадковий патент: Спосіб культивування шкіри людини









