Ефіри циклогексеноноксимів та гербіцидний засіб
Номер патенту: 34414
Опубліковано: 15.03.2001
Автори: Вестфален Карль-Отто, Гербер Маттіас, Каст Юрген, Мейер Норберт, Вюрцер Бруно, Міссліц Ульф, Харреус Альбрехт, Гетц Норберт, Вальтер Хельмут
Текст
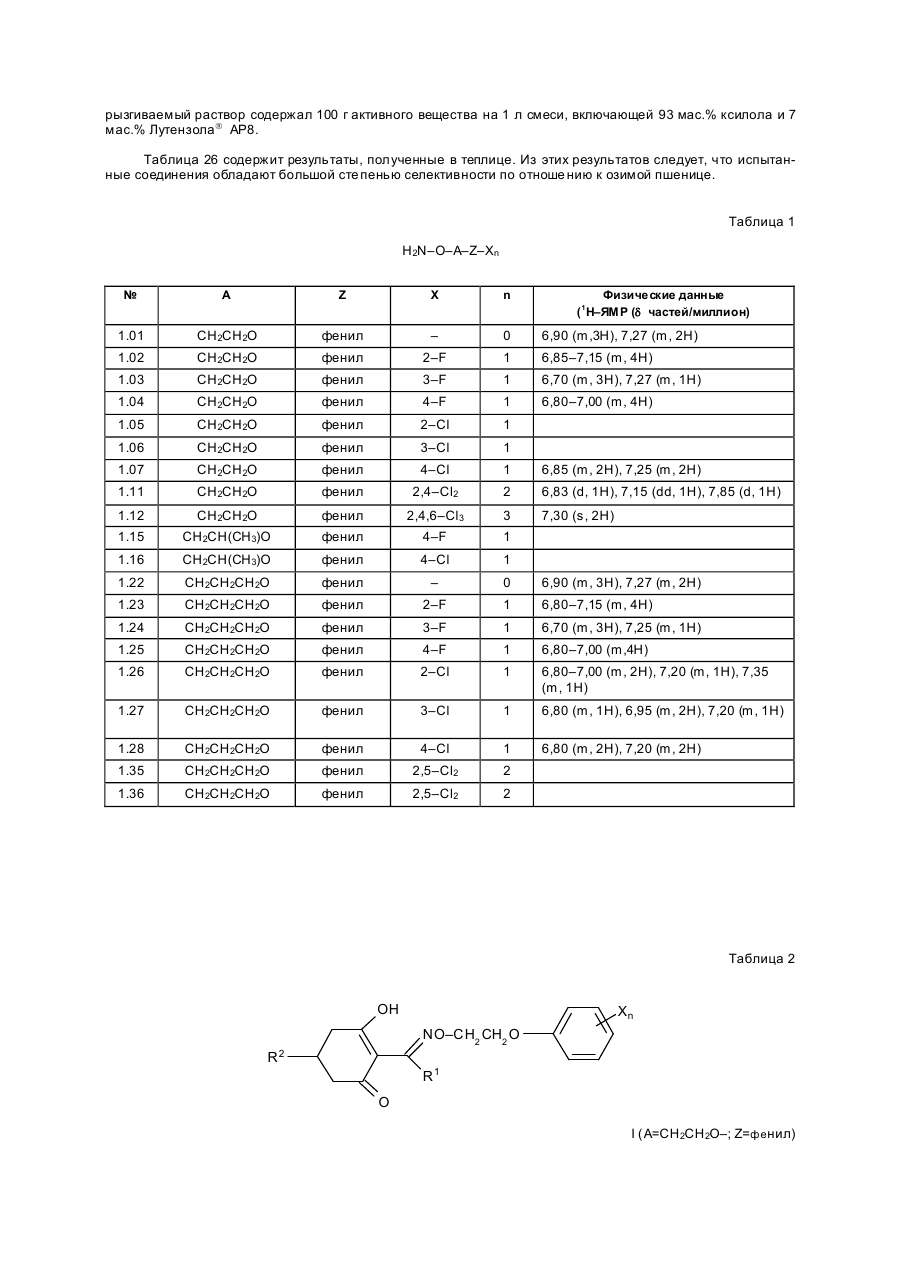
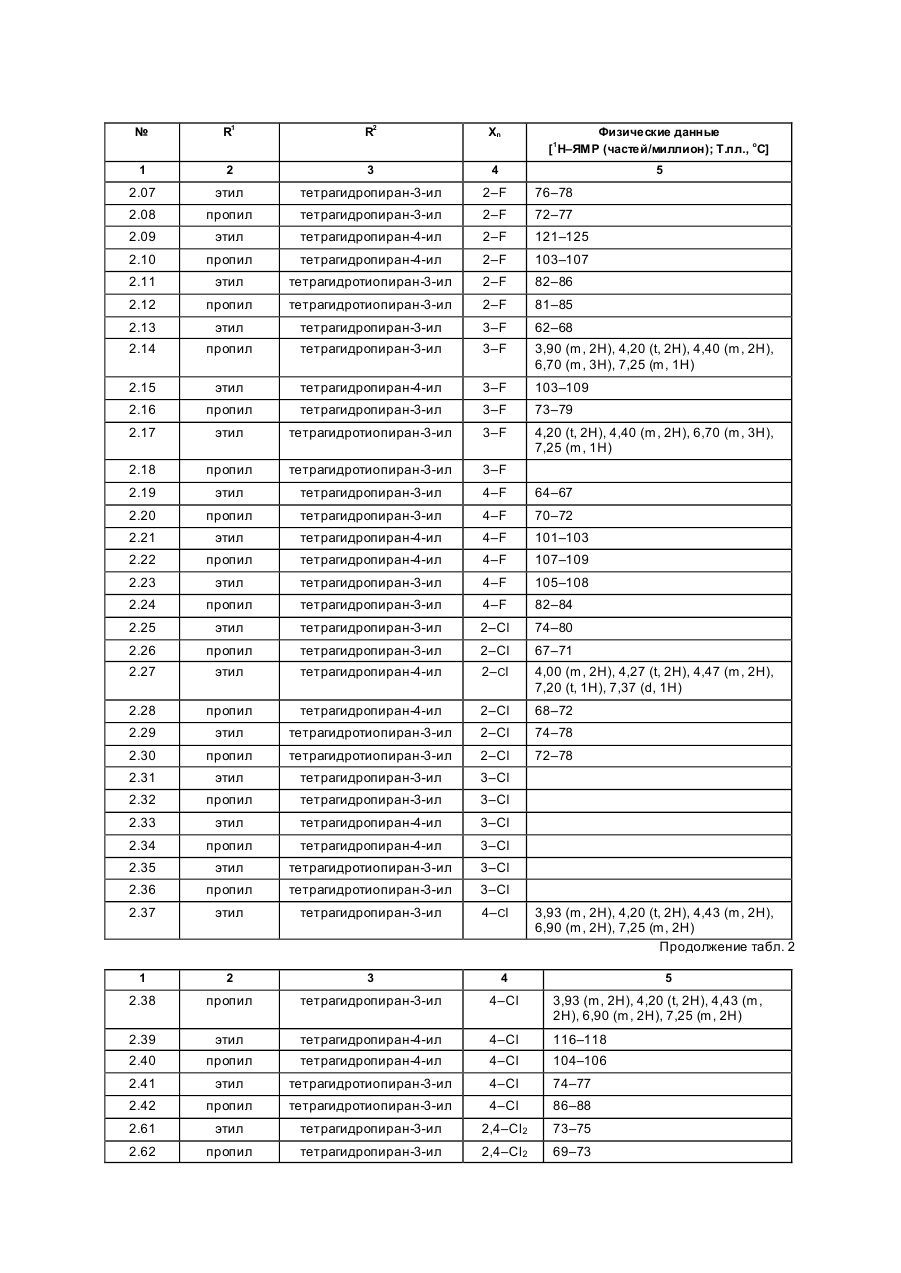
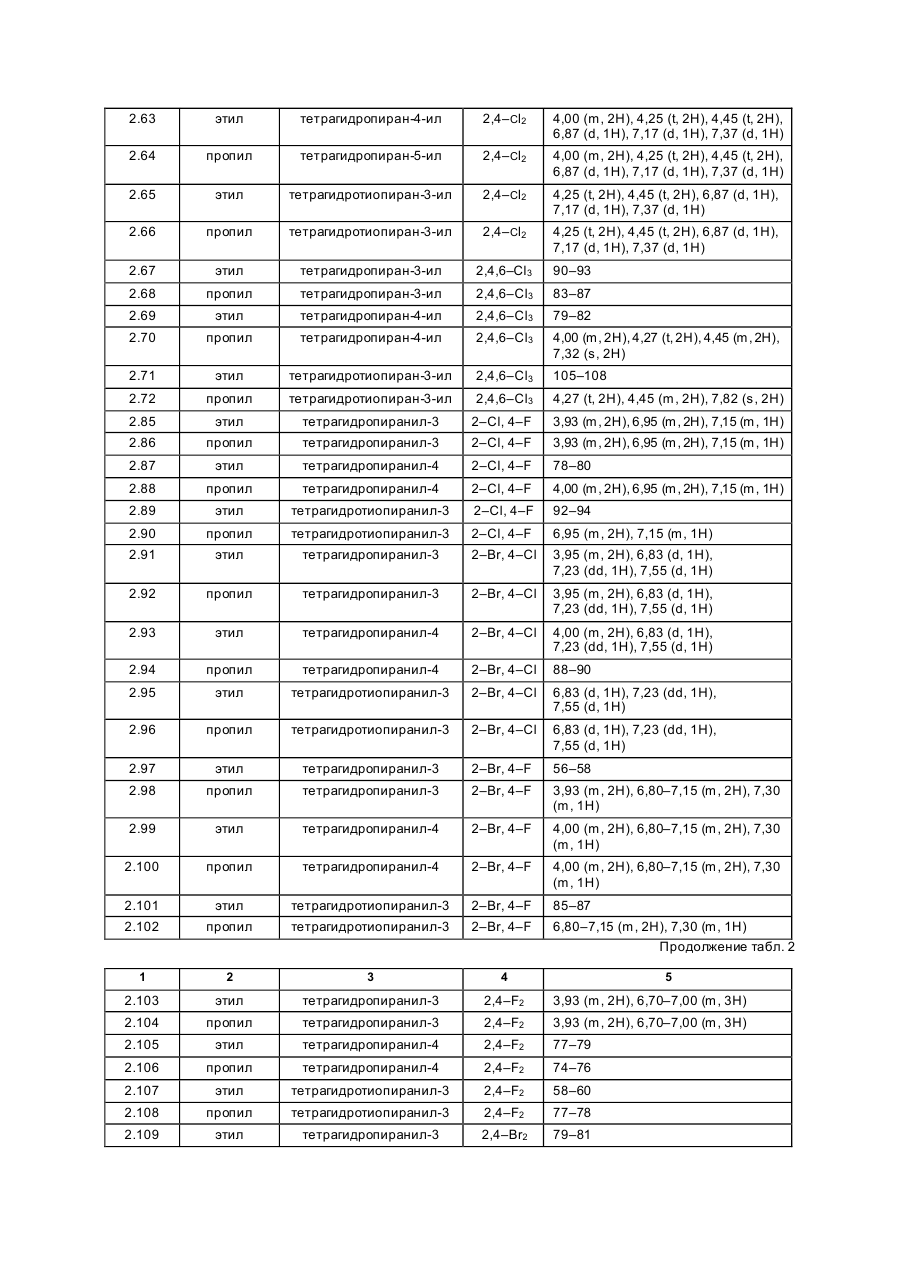
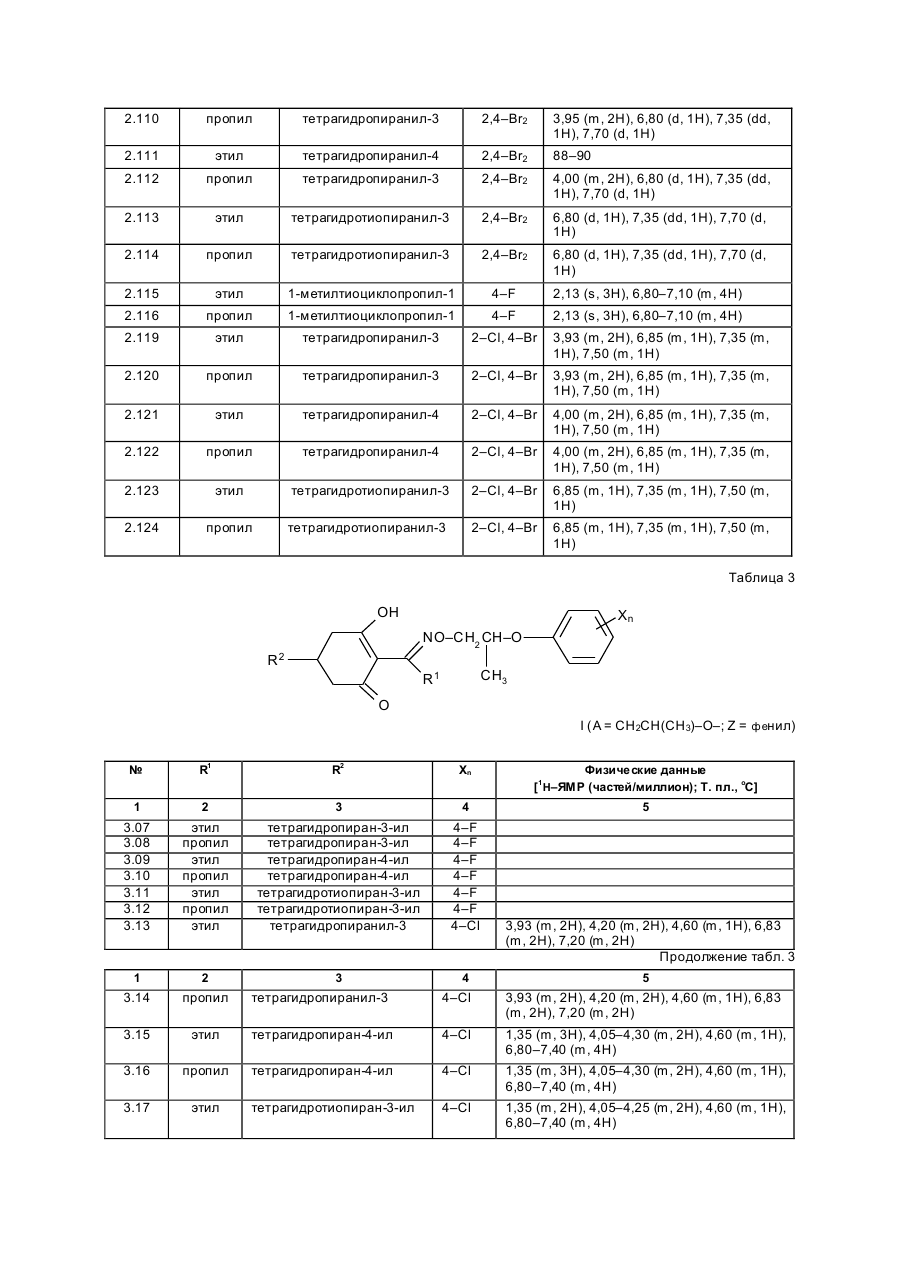
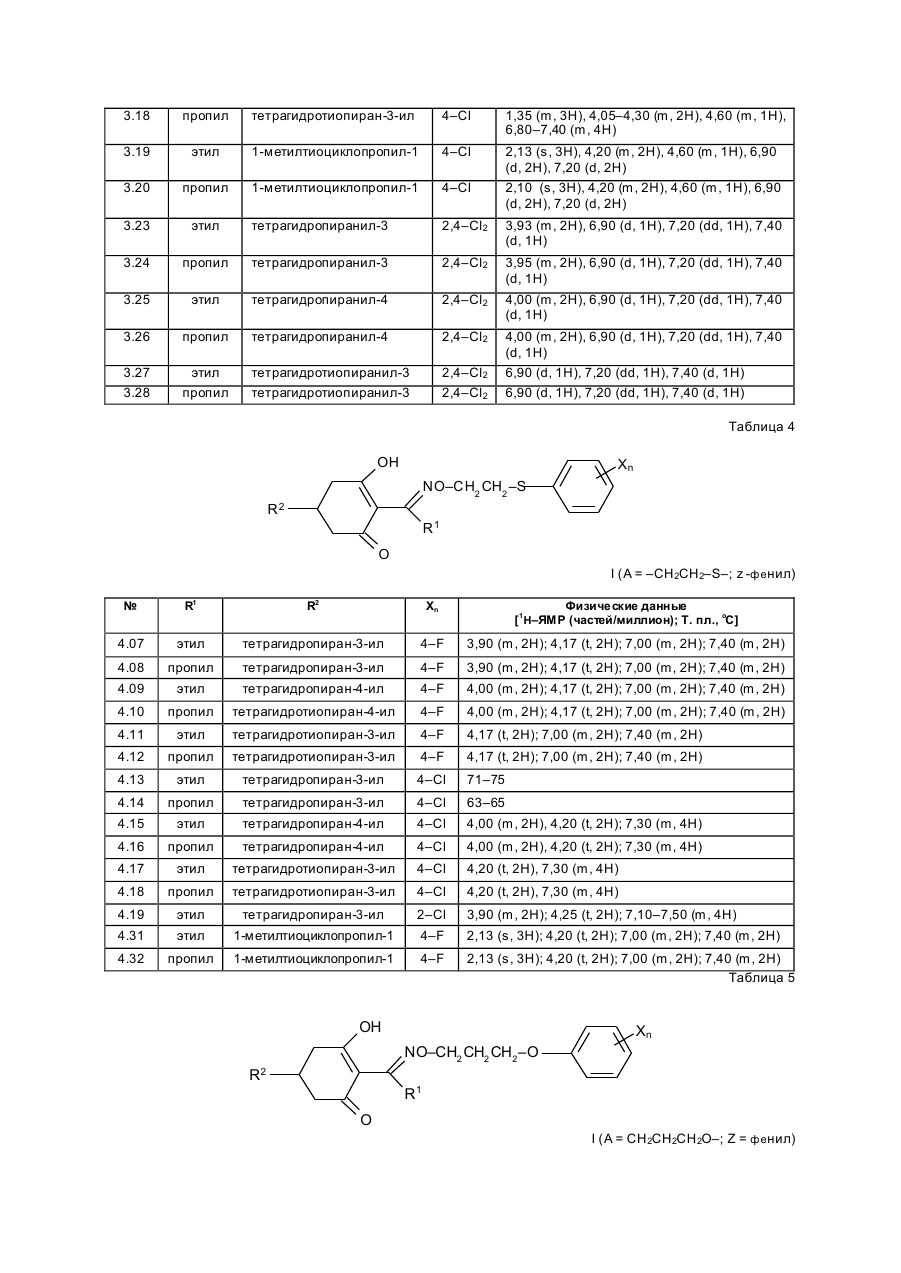
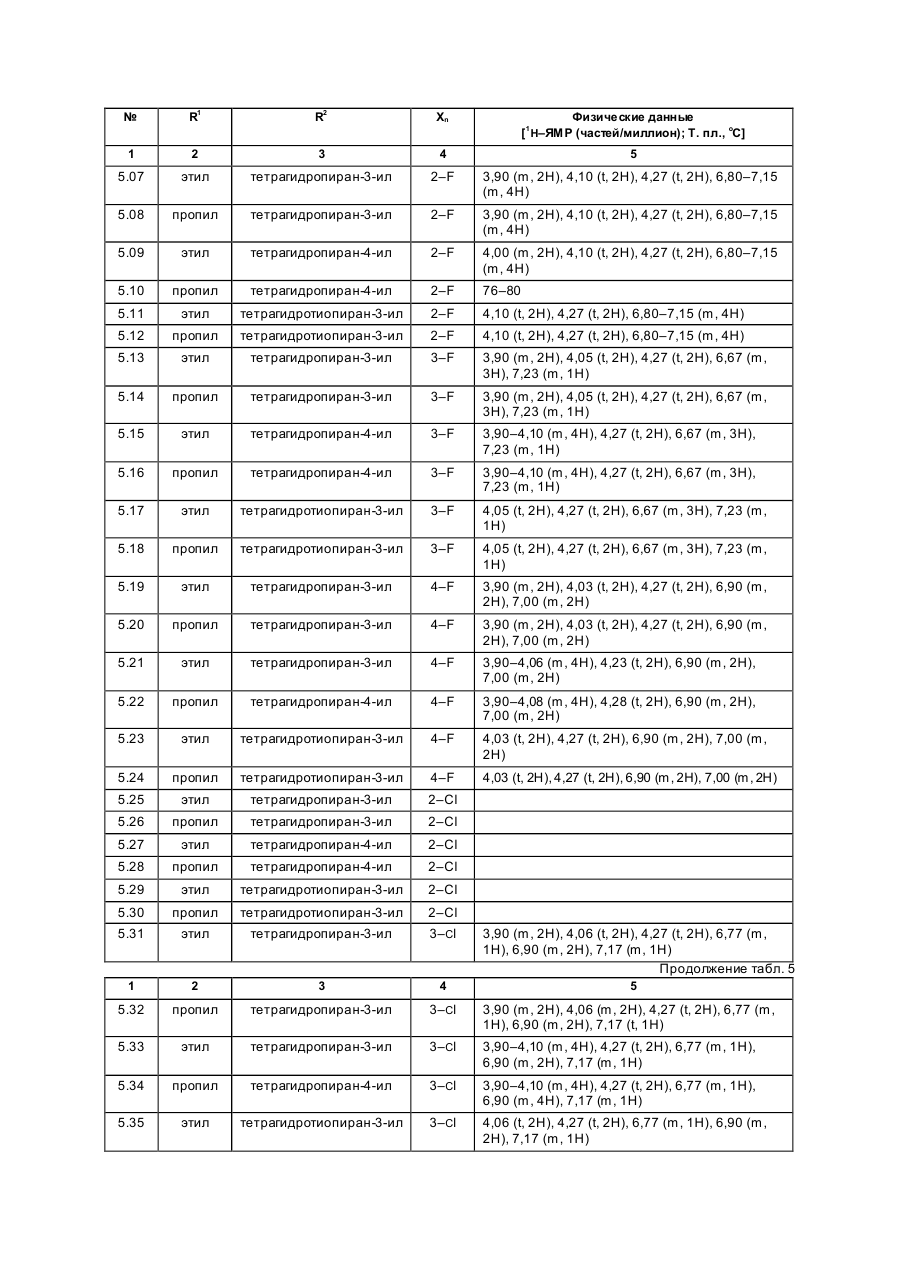
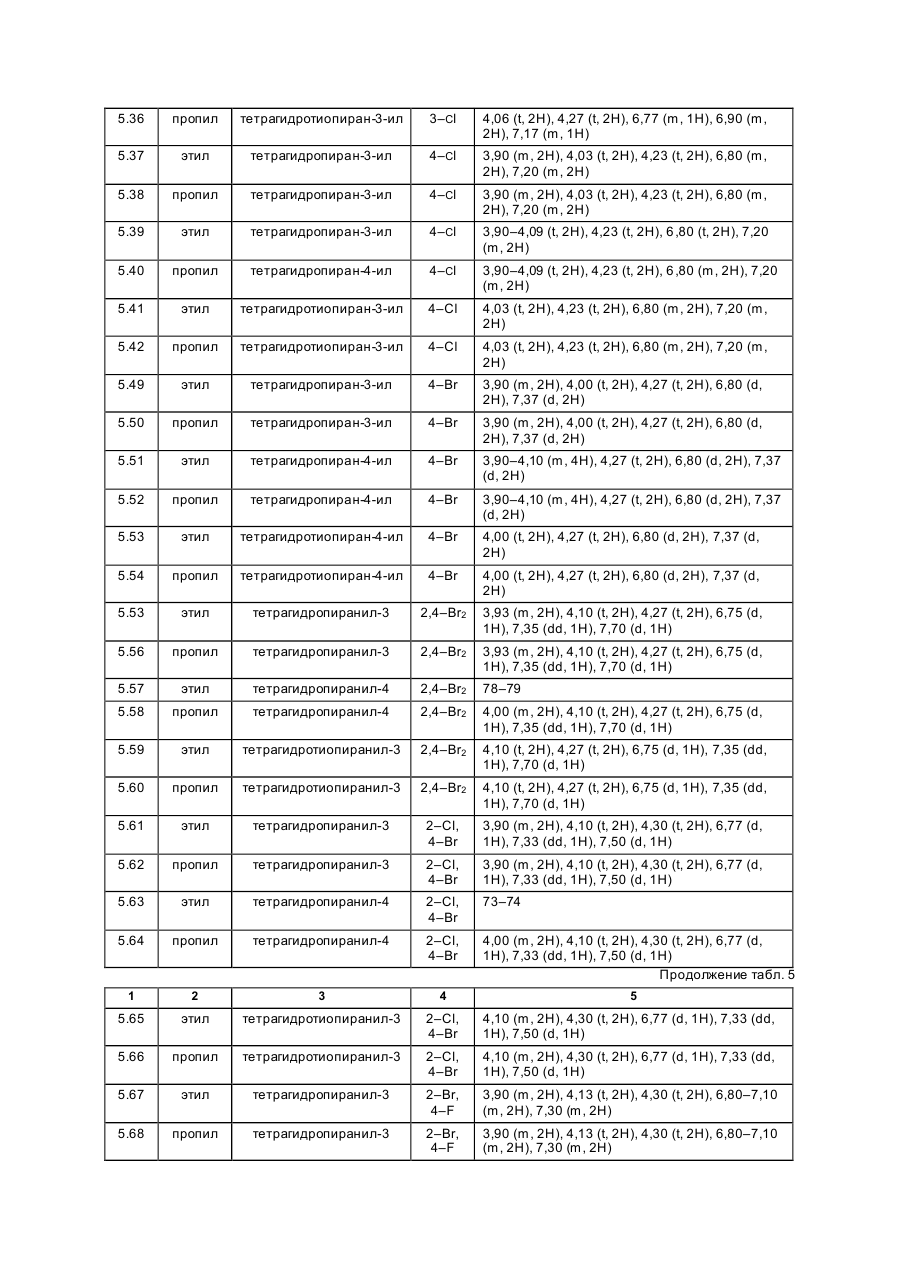
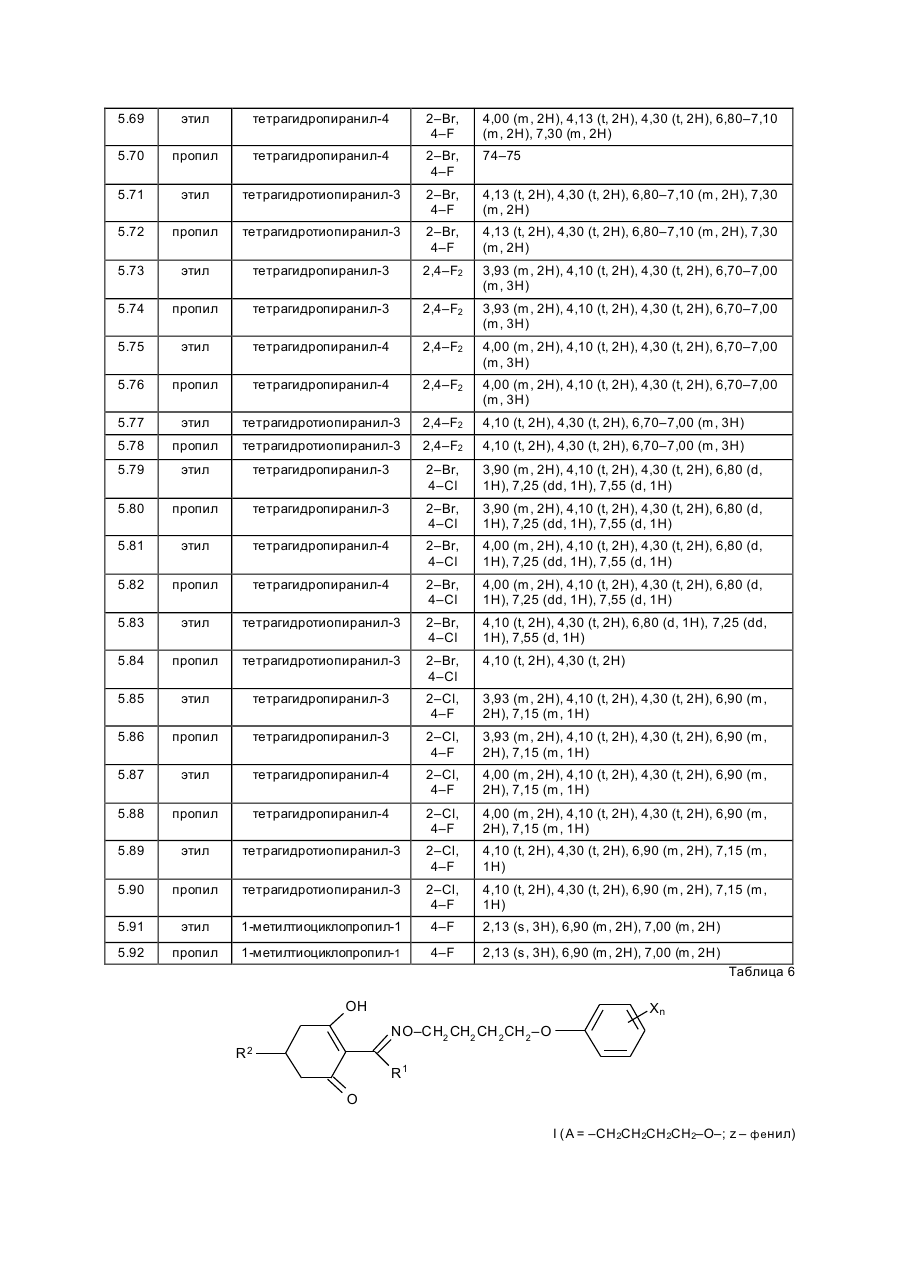
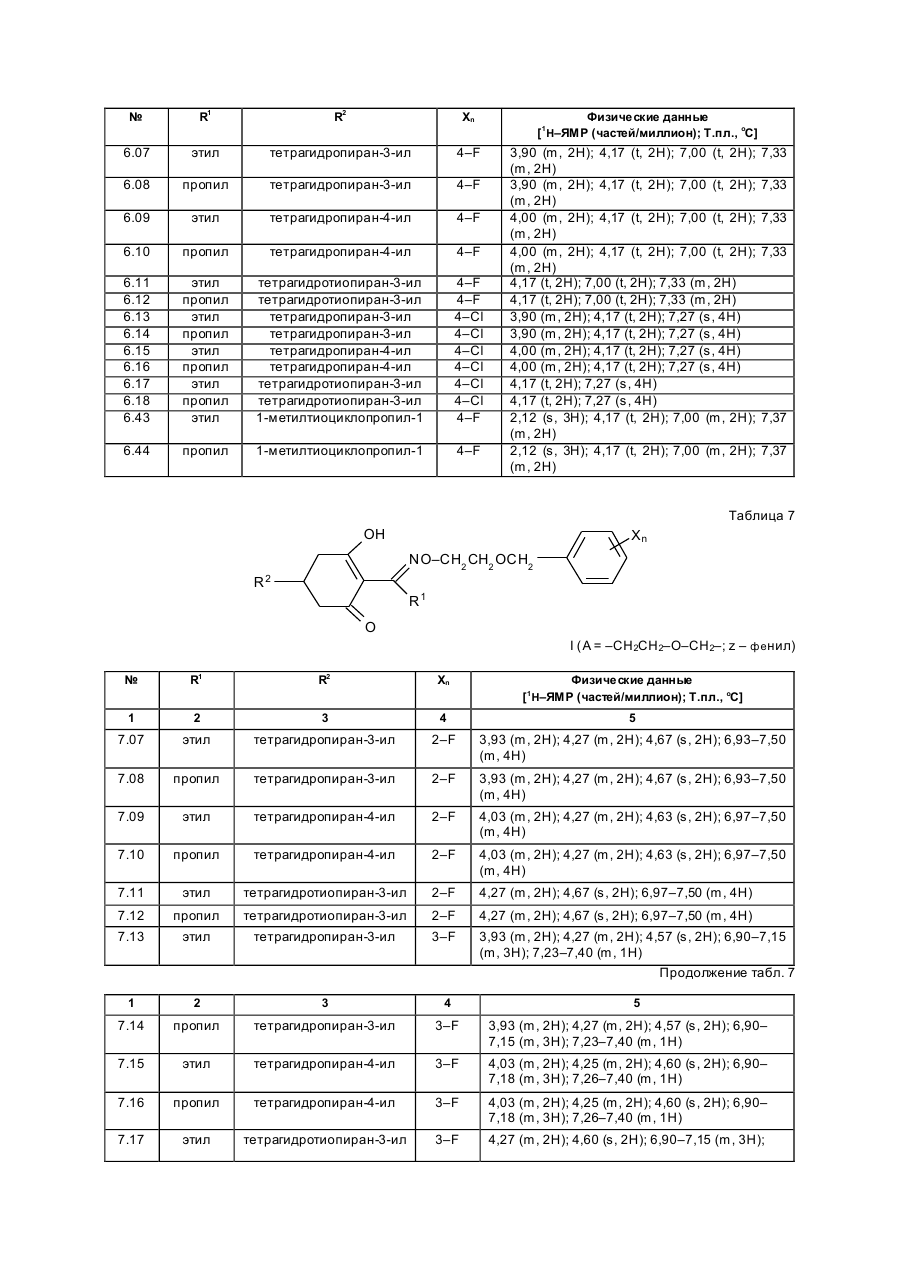
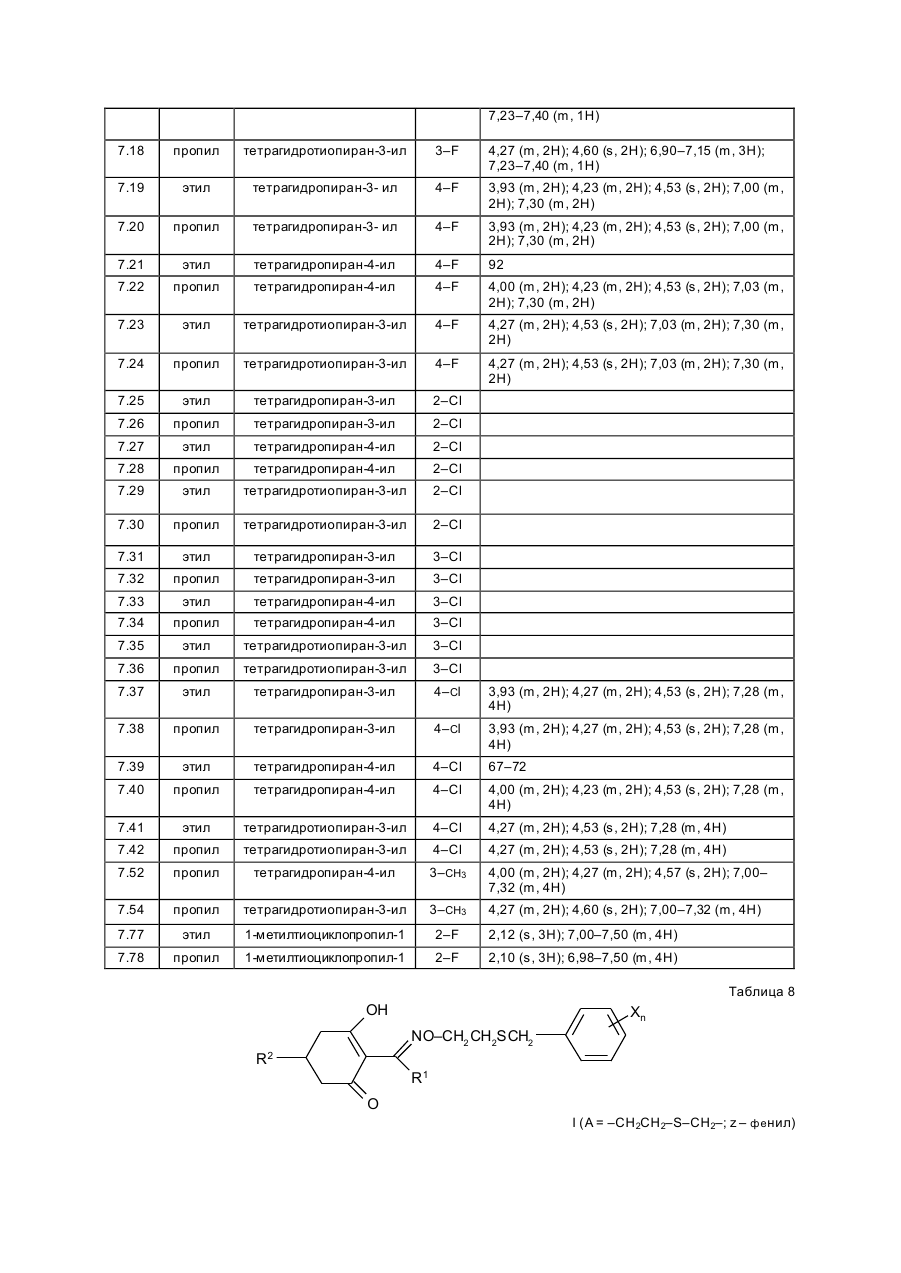
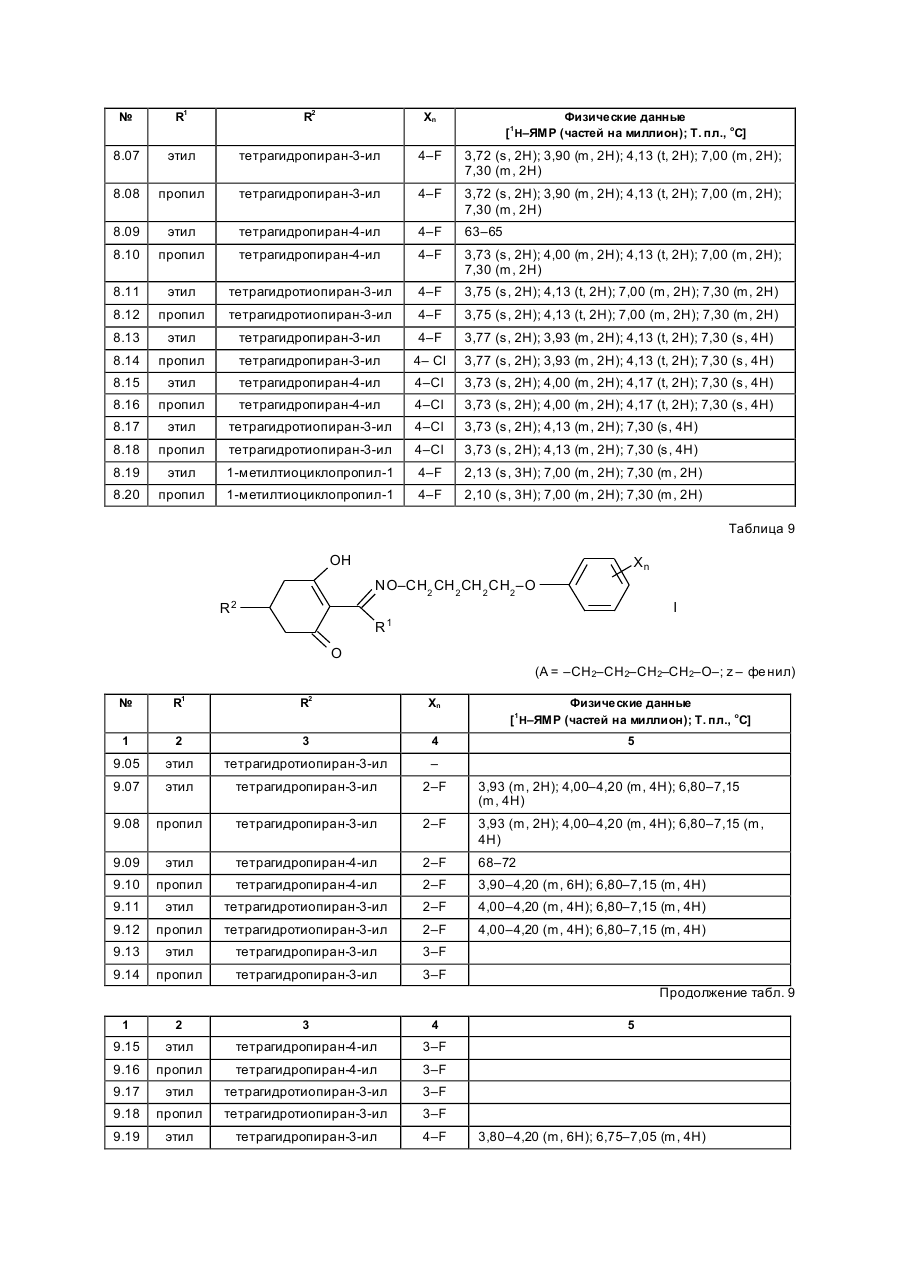
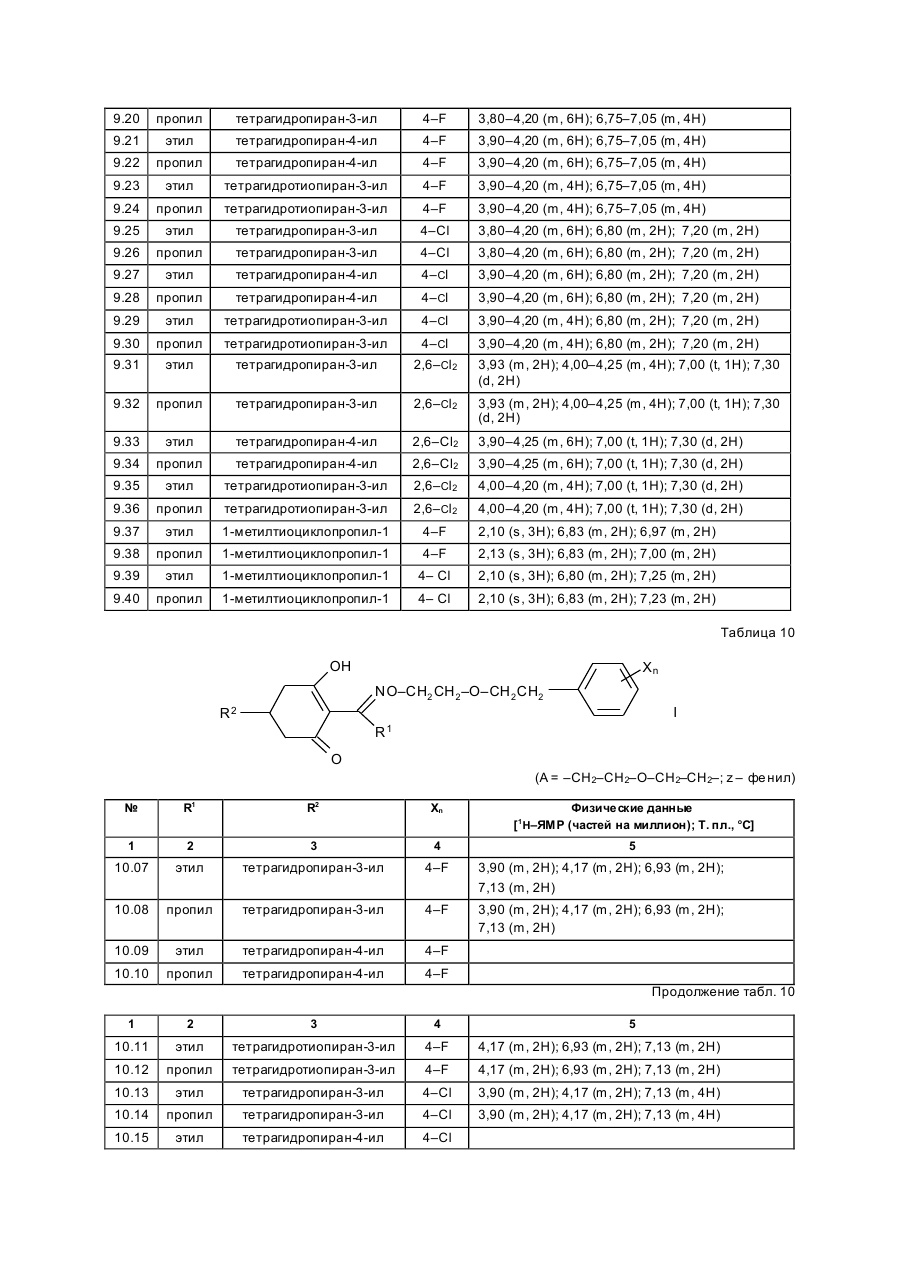
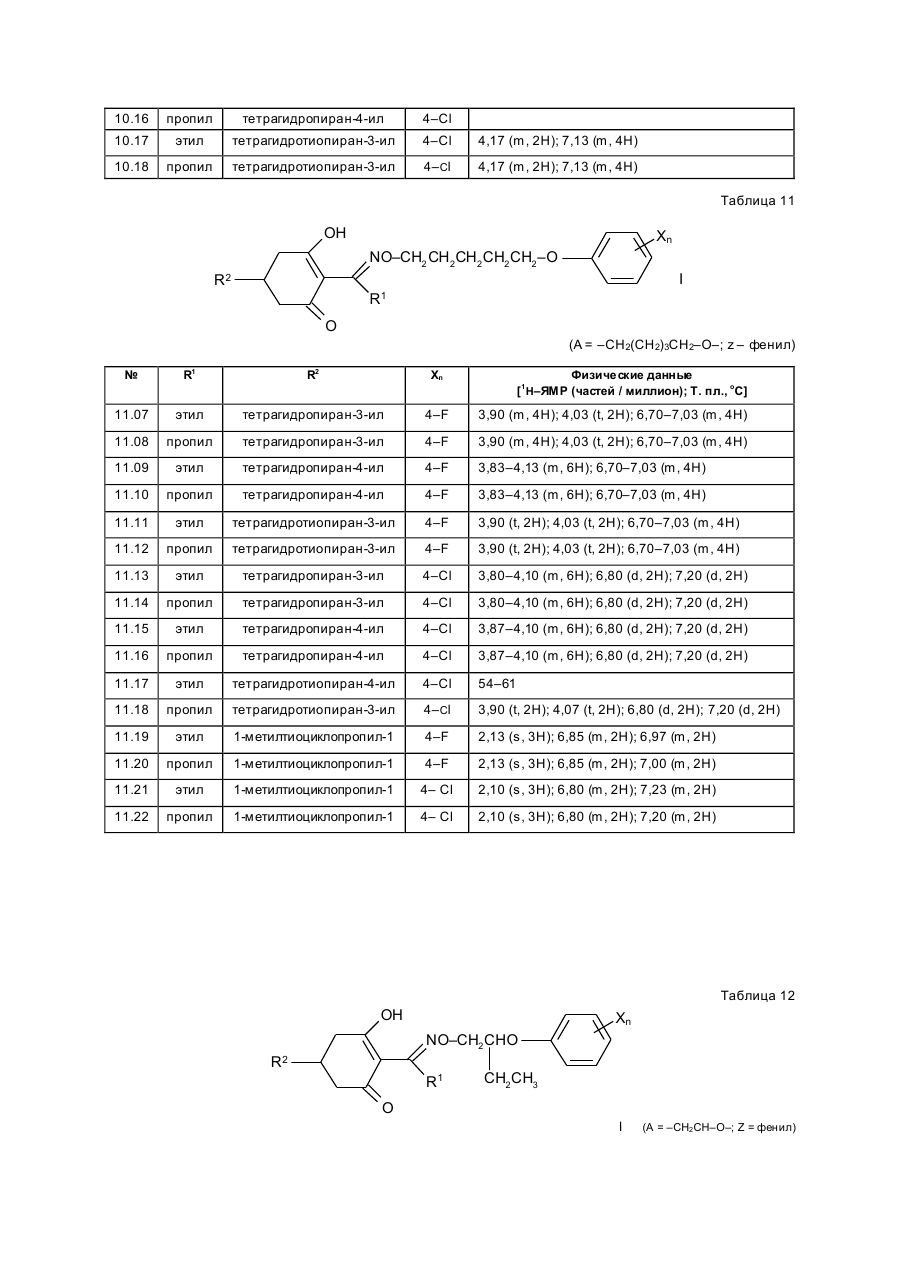
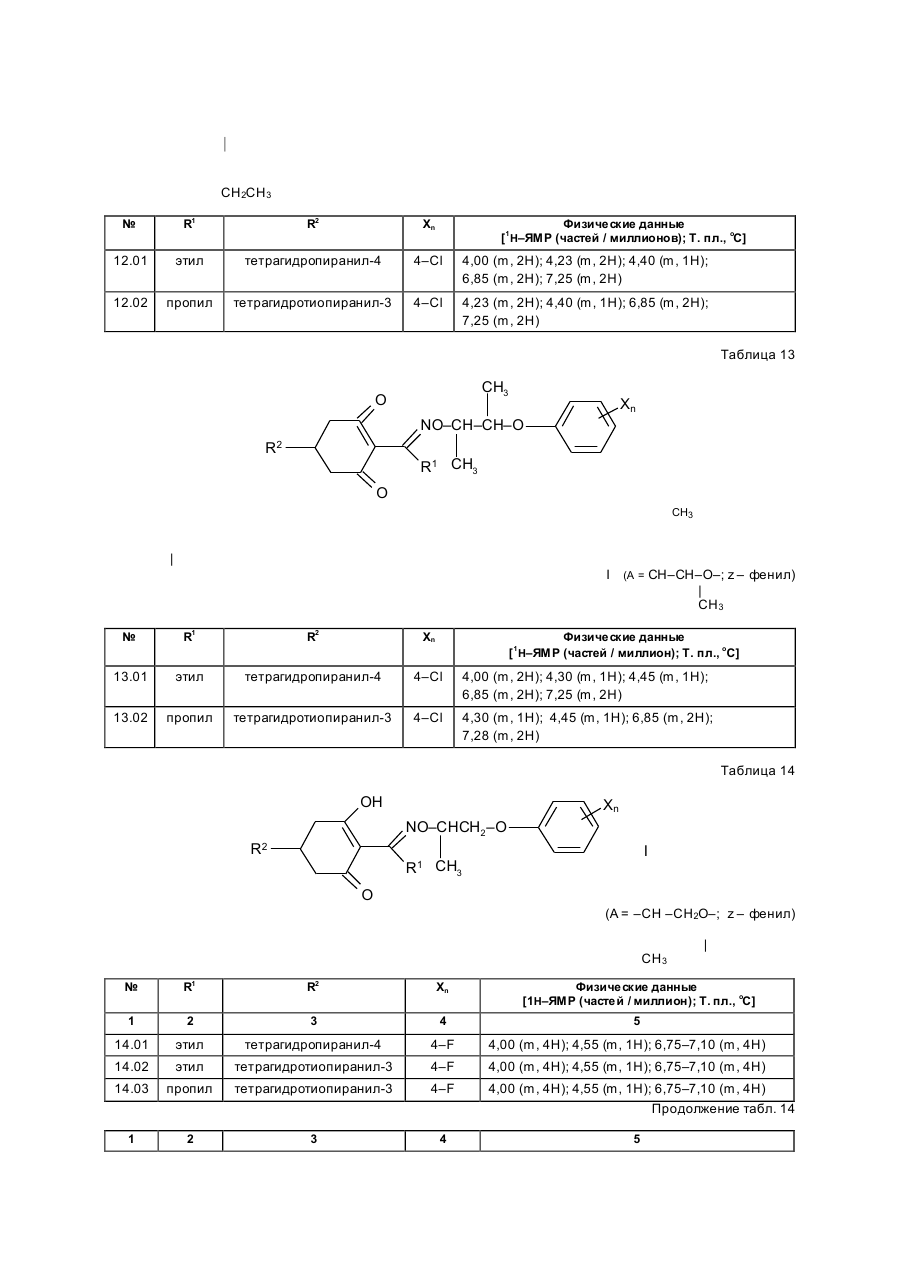
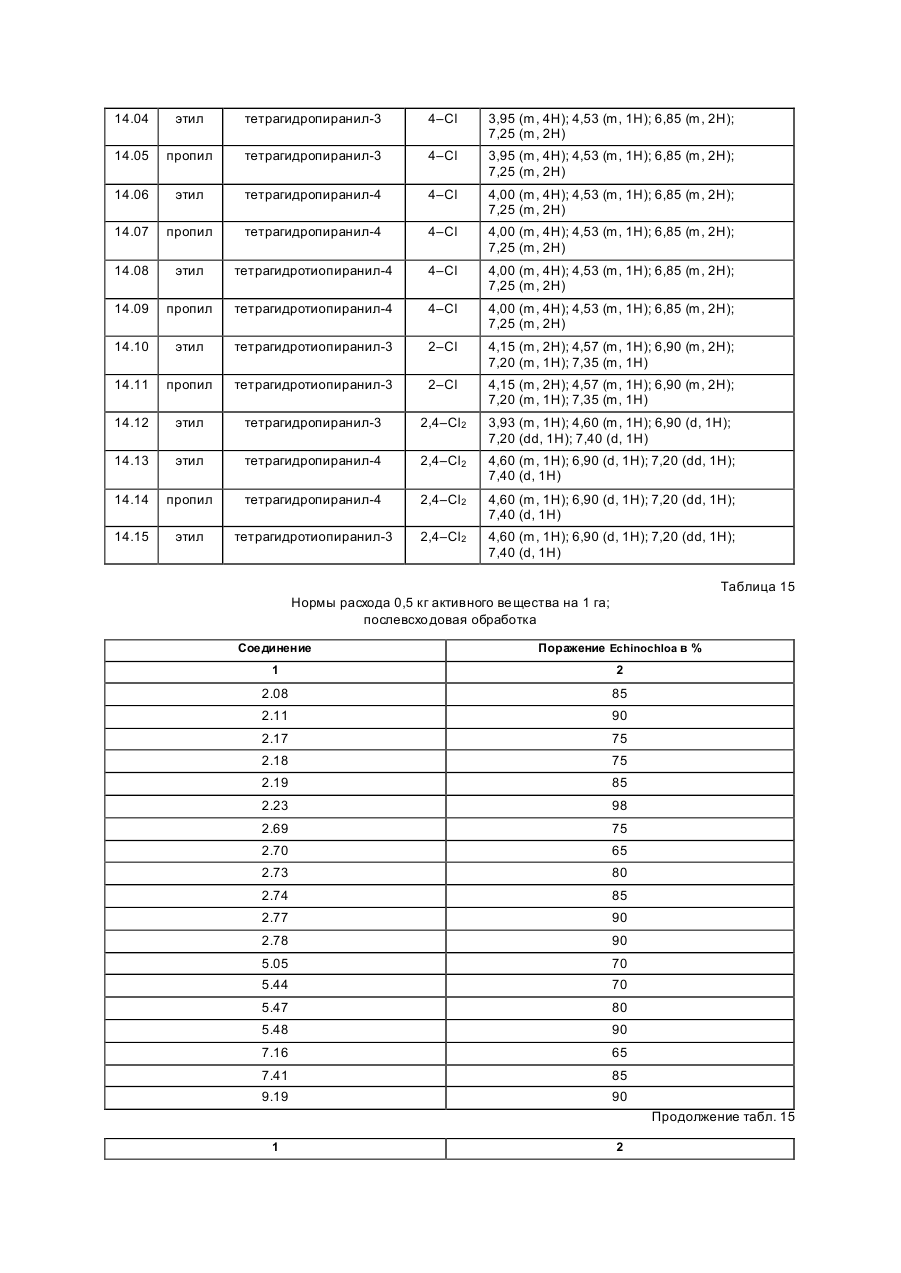
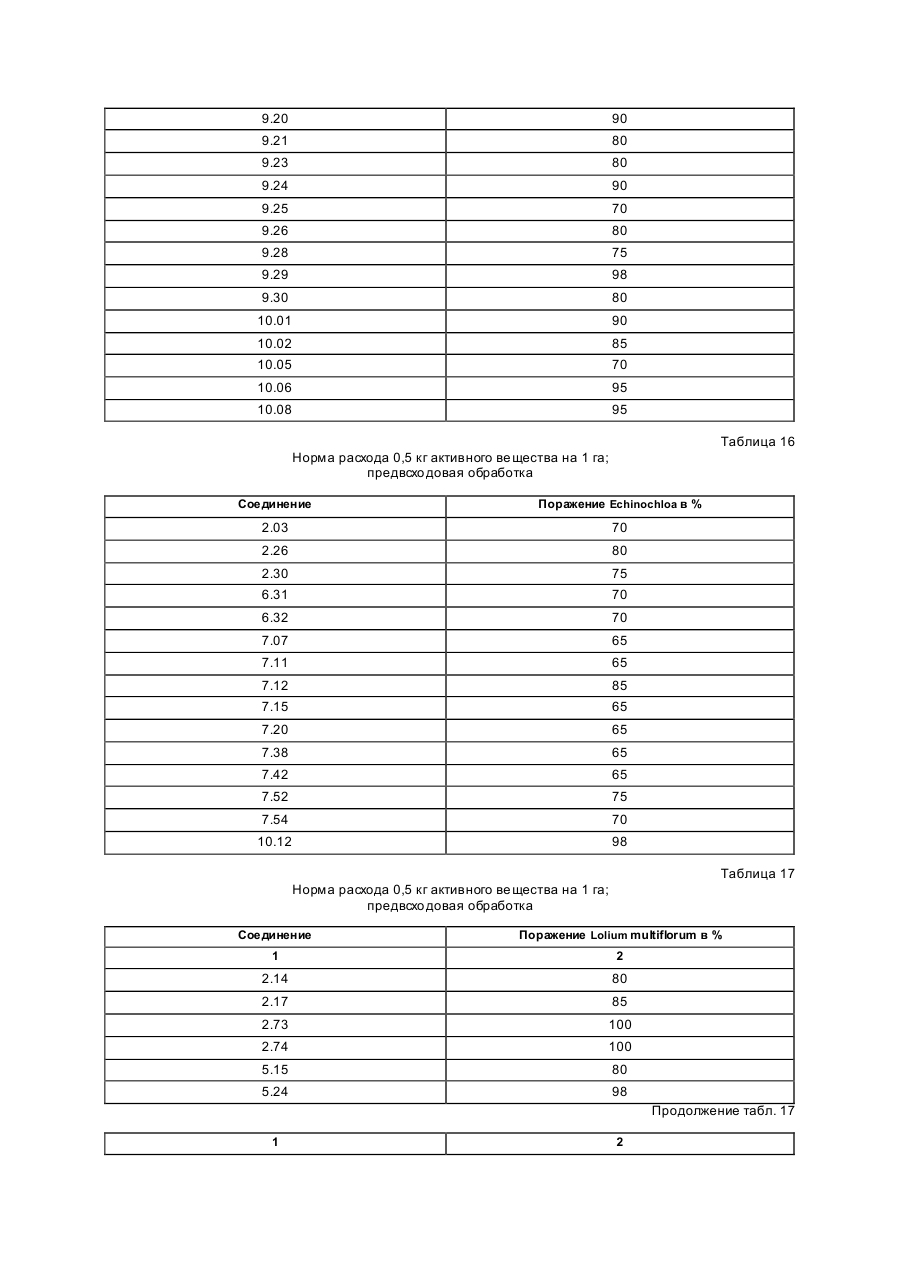
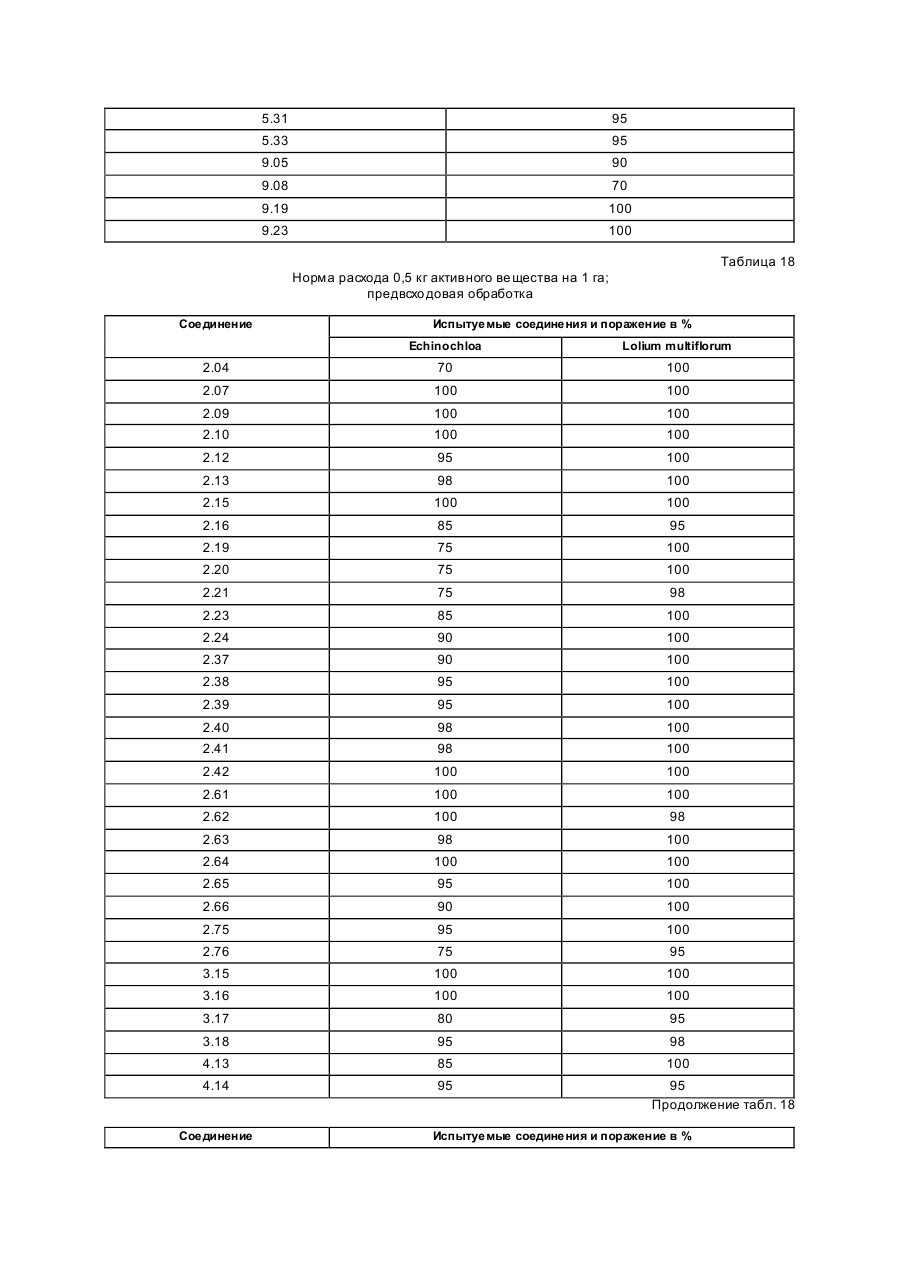
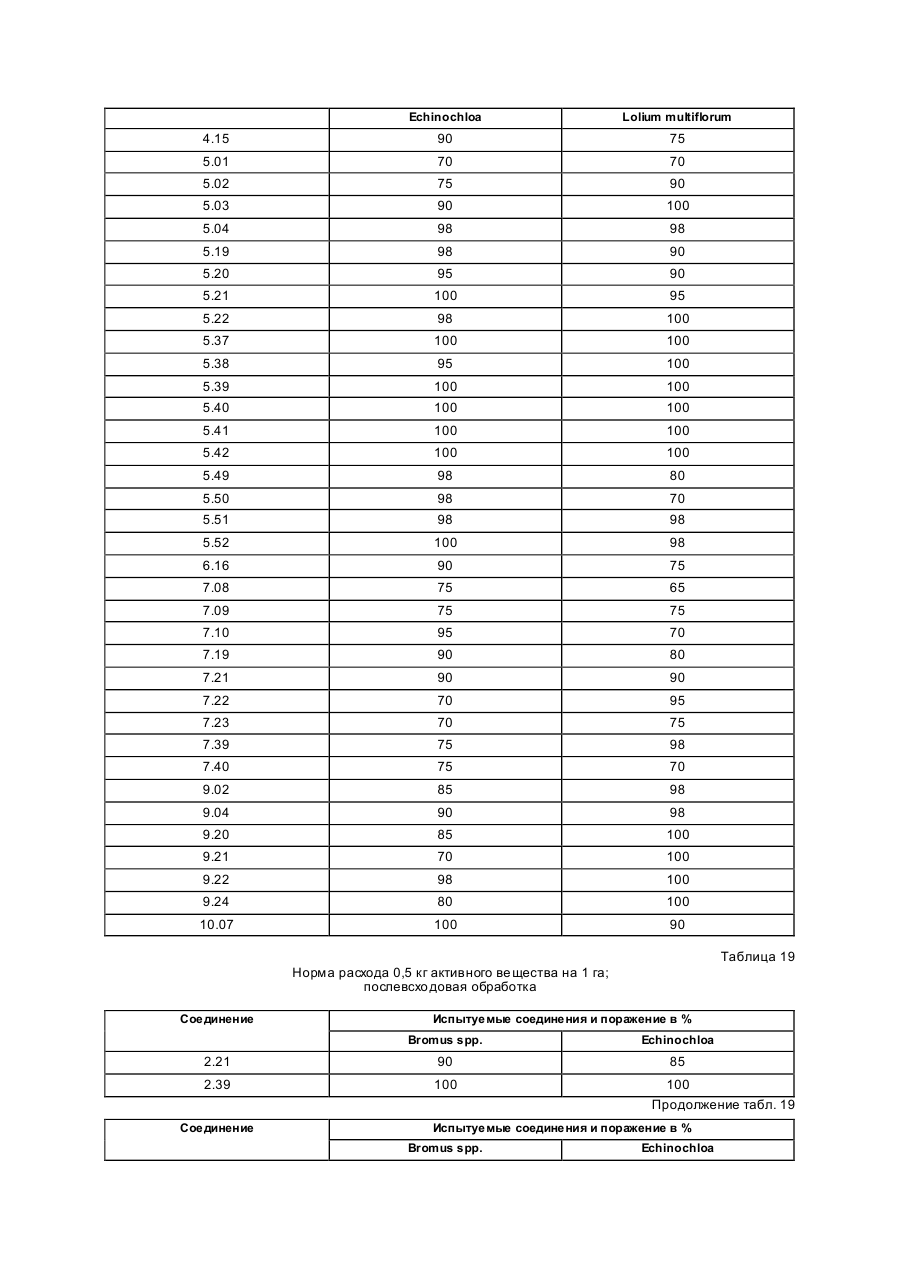
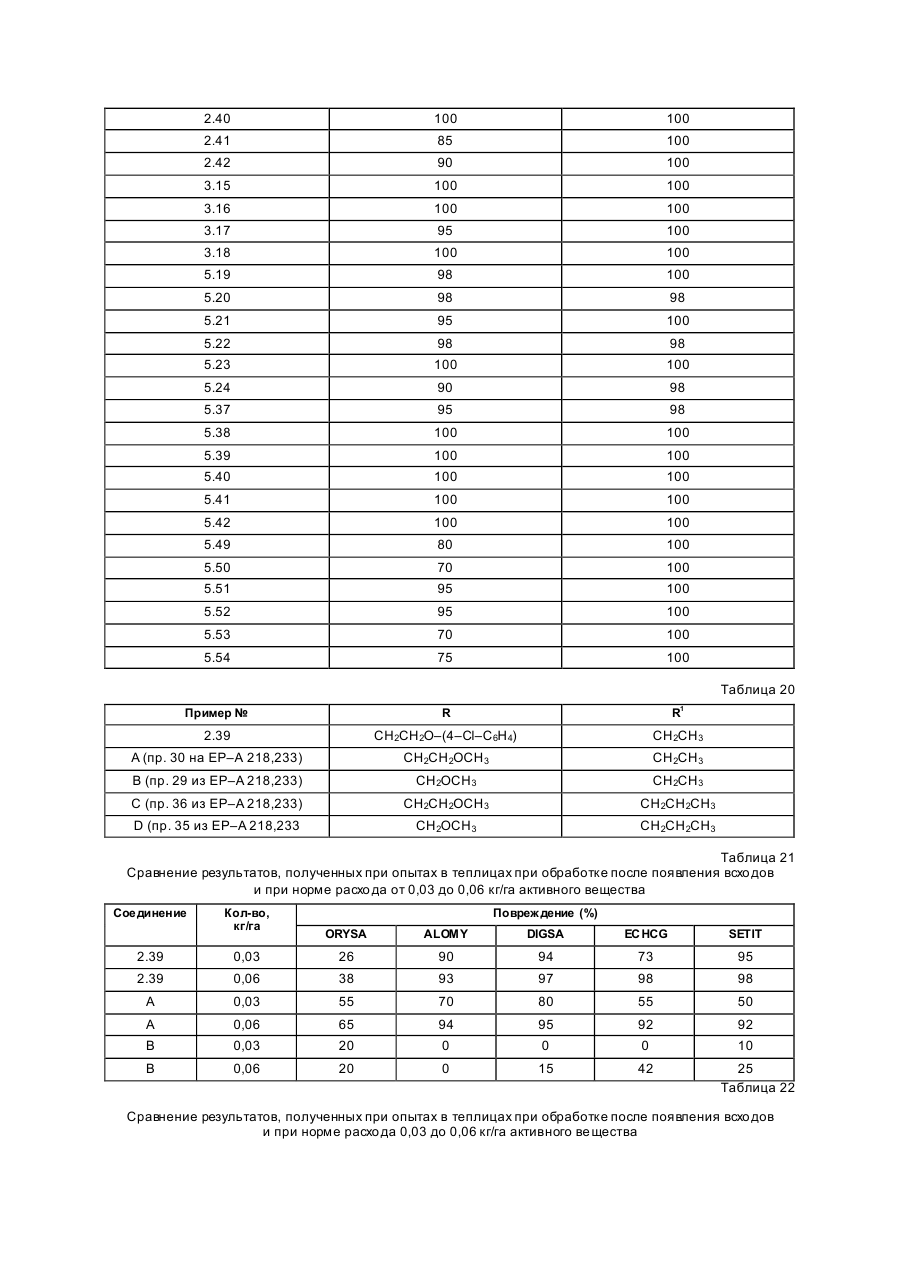
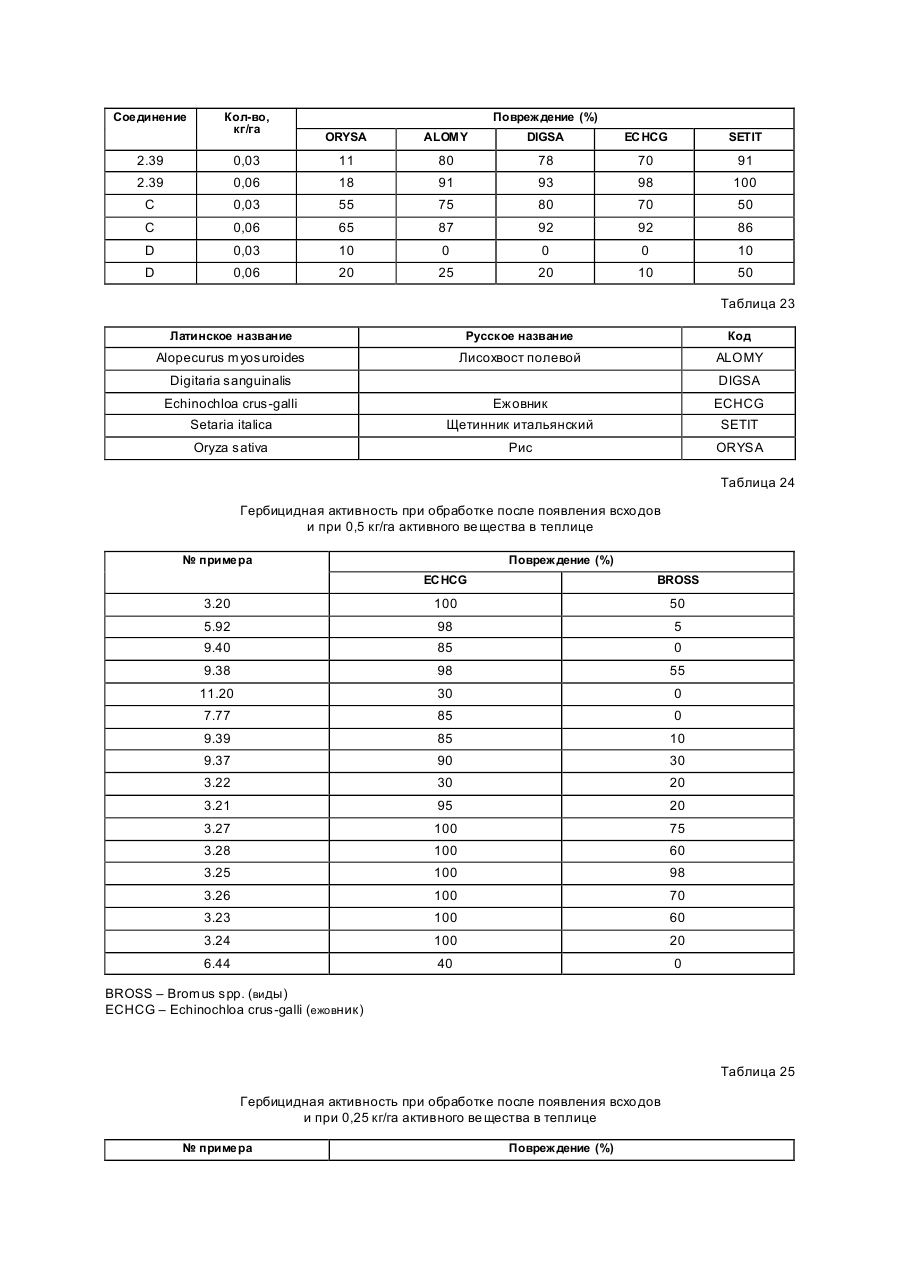
Изобретение касается новых гербицидно-активных эфиров циклогексеноноксимов формулы (I) OH N O A Z Xn 2 R R1 , (I) O в которой R – низшая алкильная группа, А – -СН2СН2-О-, -СН2СН2СН2-О-, -СН(СН 3)- -СН2-О- или -СН2СН (СН3)-О-; Z – фенил; Х – галоген; n=1, 2, 3; R2 – 2-этилтиопропил, 1-метилтиоциклопропил, тетрагидропиран-3-ил, тетрагидропиран-4-ил, тетрагидротиопиран-3-ил, и гербицидной композиции на их основе. Циклогексеноноксимовые эфиры в соответствии с изобрете нием общей фор мулы (I) имеют явно выраженный кислый характер, то есть они очень просто могут образовывать продук ты взаимодействия, такие как соли ще лочных или ще лочно-земельных соединений или эфиры енолов. Соединения формулы (I) могут нахо диться в нескольких та утомерных фор мах, каждая из кото рых вхо дит в объем притязаний данного изобретения. В литературе описаны в качестве гербицидов эфиры циклогексеноноксимов общей формулы (I) OH NO—D 1 E C R , O в которой D означает бензил и Е -2-этилтиопропил (американский патент 4,440,566), D – бензил, и буте нил-2 и Е-замещенный пятичленный гетероарильный оста ток (европейские заявки 238.021, 125,094), D – бензил, бутенил-2- и Е-замещенный фенил (европейская заявка 80,301), D – бутенил-2- и Е-5-7-членное гетероциклическое кольцо, содержащее до двух О-, S-ато мов и до двух двойных свя зей (ЕР-А 218, 233). Однако были сделаны попытки найти соединения, которые обладают высокой селективностью при малых расходных нормах, то есть поражающие вредные растения, не нанося вреда при этом культурным расте ниям. В соответствии с этой задачей были обнаружены новые эфи ры циклогексеноноксимов формулы (I), которые отличаются хорошей гербицидной активностью по отноше нию к нежелательным травам. Соединения совмести мы с широколистными культур ными растениями, а также с некоторыми граминиевыми культурами, как рис. Циклогексеноноксимовые эфиры формулы (I) могут быть получены известными методами из уже известных производных фор мулы (II) (акцептованная европейская заявка 80, 301, 125, 094, 142, 741, американская акцептованная заявка 4, 249, 397, европейская акцептованная заявка 137, 174 и 177, 913) и соответствующи х гидроксиламинов формулы (III) Губен-Вейль, 10/1, стр. 1181 ff) (европейская акцептованная заявка 169, 521) по схеме: OH O R2 + H2 N–O–A–Z–Xn R 1 O (II) (III) OH N –O–A–Z–Xn R2 R1 (I) O Целесообразно проводить взаимодействие в гете рогенной фазе в растворителе, с температурой кипения ниже 80оС, в присутствии основания и применять гидроксиламин III в ви де его аммониевой соли. Подхо дящи ми основаниями являются, например, карбонаты, бикарбонаты, ацета ты, алкоголяты или оксиды щелочных или щелочно-земельных металлов, в частности гидроксиды натрия, калия, магния, кальция. Кроме того, могут найти применение органические основа ния, как пиридин или третичные амины. Ос нования добавляют, например, в количестве от 0,5 до 2 моль-эквивалентов, считая на аммониевое соединение. В качестве растворителя пригодны, например, диметилсульфоксид, спирты, как мета нол, этанол и изопропанол; ароматические углеводороды, как бензол и толуол; хло рированные углеводороды, как хлороформ и дихлорэтан; алифати ческие углеводороды, как гексан и циклогексан; сложные эфиры, как этилацетат; и простые эфи ры, как диэтиловый эфир, диоксан и тетрагидрофуран. Предпочтительно проводить взаимодействие в метаноле с бикарбонатом натрия в качестве основания. Реакция заканчивается через несколько часов. Целевое соединение можно выделить, например, испарением смеси, растворением остатка в смеси метиленхлорида с водой и отгонкой растворителя при пониженном давлении. Но можно также для этого взаимодействия применять непосредственно свободное основа ние гидроксиламина, например, в виде водного раствора; в зависимости от применяемого растворителя для соединения (II) получают одно- или двухфазную реакционную систему. Подхо дящи ми раство рите лями в случае этого варианта способа являются, например, спирты, как мета нол, этанол, изопропанол и циклогексанол; алифа тические и аромати ческие, в соответствующем случае хло рированные, углеводороды, как гексан, циклогексан, метиленхлорид, толуол и дихлорэтан; сложные эфи ры, как этилацетат; нитрилы, как ацето нитрил; и циклические эфи ры, как диоксан и тетрагидрофуран. Соли ще лочных металлов соединений формулы (I) могут быть получены обработкой 3-гидроксисоединений гидроксидом натрия или калия или алкоголятами натрия или калия в водном растворе или в органическом растворителе, как метанол, эта нол, ацетон или толуол. Др угие со ли металлов, как со ли марганца, ме ди, цин ка, железа, кальция, магния и ба рия, могут быть получены из натриевы х со лей известными мето дами, также как и соли аммония и фосфо ния с помощью аммиака, гидроксидов фо сфо ния, суль фо ния или сульфок сония. Соединения типа (II) могут быть получены, например, из соответствующи х циклогексан-1,3-дионов формулы (IV), в которой Y означает водород или метоксикарбонил, известными мето дами [Tetrahedron Lettr., 2491 (1975)]. OH R2 Y (IV) O Возможно также соединения формулы (II) получать по схе ме через промежуточную ста дию енольных эфи ров, которые в свою очередь получаются при взаимодействии соединений формулы (IV) с хло рангидридами кислот в присутствии оснований и непосредственно после этого осаждаются определенными производственными имидазола или пиридина (выложенная заявка на японский патент 79/063, 052). Схема: O O OH R1 OH O O + R2 R2 R1 Y O R2 R1 Cl Y O O (II) (IV) Соединения формулы (IV) можно получить через ряд известных стадий способа, исхо дя из известных исходных продук тов. Синтез гидроксиламинов формулы (III) осуществляют в соответствии с нижеприведенной схемой реакции: VII–III, где Y – удаляемая группа, например, галоген, как хлор, бром, йод или СН 3SO2OXn–Z– A– Y (VII) O O N — OH VII + D D O (V) N —O—A—Z—Xn O (VI) OH III N Необхо димые для синтеза новых гидроксиламинов формулы (III) алкилирующие средства могут быть получены известными в литературе мето дами [см. акцепто ванная заявка ФРГ 3, 437, 919, Tetrahedron Lettr., 28, 2639 (1970), Org. Synth. Coll., том 1, 436 (1944); акционерная заявка на патент ФРГ 2,654, 646, 2,714,561, J. Org. Chem. 52, 3587 (1987); выложенные заявки на патент ФРГ 948,871, 948,872, J. Med. Chem. 26, 1570 (1983); Synthesis 675 (1983) и J.Org. Chem. 48, 4970 (1983). Соединение VII обрабатывают циклическим гидроксиимидом V и полученное защи щенное производное гидроксиламина VI расщепляют до сво бодного гидроксиламина III с по мощью, например, 2-аминоэтанола. В циклических гидроксимидах V D означает, например, С2–С3-алкилен, С2–С3-алкилен, С2-алкенилен или 5- или 6-членное кольцо, содержащее до трех двой ных связей и в соответствующем случае 1 атом азота, например фенилен, пиридинилен, циклопентилен, циклогексилен или циклогексенилен. В качестве примеров могут быть приведены следующие соединения VI + H O O NOH O N–OH N–OH N O O O O O NOH O O N–OH N–OH O O O N–OH O Взаимодействие соединений формулы (VII) с гидроксимидами формулы (V) целесообразно проводить в присутствии основания. Пригодными являются в принципе все основания, кото рые могут депротонировать гидроксимиды V без воздействия на имидную систему. Они, в частности, являются так называемыми ненуклеофильными основаниями. В качестве примеров следует назвать, например, минеральные основания, как карбонаты ще лочных или щелочно-земельных металлов, бикарбонаты щелочных или щелочно-земельных например, минеральные основания, как карбонаты щелочных или ще лочно-земельных металлов, бикарбонаты ще лочных или щелочно-земельных металлов, бикарбонаты ще лочных или щелочно-земельных металлов, органические основания, как алифа тические, циклоалифати ческие и ароматические третичные амины. Можно применять также смесь этих оснований. В качестве отдельных соединений следует привести следующие основания: карбонат натрия, карбонат калия, карбонат магния, карбонат кальция, карбонат бария, бикарбонаты эти х металлов, триметиламин, триэтиламин, трибутиламин, этилдиизопропиламин, N,N-диметиланилин, 4-N,N-диметиламинопиридин, диазабициклооктан, диазабициклоундекан, N-метилпиперидин, 1,4-диметилпиперазин, пиридин, хи нолин, бипиридин, фенантронил. Предпочтительными являются дешевые основания – карбонаты натрия и калия. Основания добавляют, как правило, в эквивалентных количествах и до избытка 5 эквивалентов, считая на гидроксимид. Возможны и большие избытки, но это излишне. Применение малых количеств основания также возможно. Однако, предпочти тельны количества основа ний от 1 до 3, в частности от 1 до 2 эквивалентов, счи тая на гидроксимид формулы (V). Можно применять также нуклеофильные основания, например, гидроксиды щелочных и щелочноземельных металлов, и особенно гидроксид натрия и калия. В этом случае выгодно добавлять основание в эквива лентных количествах по отношению к гидроксимиду V, что бы предотвратить нуклеофильную ата ку карбоксильными ионами карбонильной функции имидной группировки. Целесообразно проводить взаимодействие исходных соединений формулы (VII) с гидроксимидами V в растворите ле, инертном по отношению к компонентам реакции в реакционных условиях. Предпочтительными растворителями являются, например, полярные апротонные растворители, как диметилфор мамид, N-метилпирролидон, диметилсульфоксид, сульфо лан и циклические мочеви ны. Количества растворителя, как правило, не являются критическими. Взаимодействие исходных соединений VII с гидроксимидами V можно проводить также при применении ката лиза в условиях фа зового переноса. В этом случае используют растворитель, образующий с водой две фазы, предпочтительно хлоруглево дороды. В качестве катализаторов фазового переноса пригодны применяемые обычно для таких целей четвертичные соли аммония и Weinheim, 1980. Катализаторы переноса целесообразно использовать в количествах от 1 до 10 об.%, предпочтительно в количестве от 3 до 5 об.%, считая на объем реакционной смеси. Взаимодействие исходных продук тов VII с гидроксимидами V, как правило, осуществляют в температурном интерва ле от 0 до 140оС, особенно желательно от 20 до 100оС, и, в частности, от 40 до 80оС. Целесообразно при этом поступать таким образом, чтобы гидроксимид V вместе с основанием нахо дился в растворителе и исходное соединение формулы (VII) до бавляли в этот раствор. При этом оказалось удачным добавление гидроксимида при более низкой температуре, например, при 0–50оС, и только после этого нагревать реакционную смесь до нужной температуры реакции. По окончании реакции охлажденную реакционную смесь целесообразно разбавлять водой, при этом образовавшиеся производные гидроксиламина VI осаждаются в виде кристаллического твер дого продук та или в виде масла. Полученные таким образом производные гидроксиламина можно при желании очистить или кристаллизацией, или экстракцией. Производные гидроксиламина VI могут быть подвергнуты сразу же превраще нию в производные гидроксиламина III со свободной аминогруппой. Это превраще ние можно проводить известными способами, которые описаны, например, в акцептованной заявке ФРГ 36, 15, 973 и в цитированных в ней публикациях. Предпочти тельно осуществлять способ в соотноше нии с акцептованной заявкой ФРГ 36, 15, 973, по которому производные гидроксиламина III вы деляют с помощью этаноламина. Выделение производных гидроксиламинов III возможно также с помощью других оснований, как водные минеральные основания, аминами, гидразинами, гидроксиламинами или с помощью водных кислот. Из реакционных смесей, полученных этим способом, можно выделить производные гидроксиламинов III с помощью обычных способов выделения, например, путем экстракции или кристаллизации. Для повышения тенденции к кристаллизации этих производных гидроксиламинов часто необхо димо перевести их в соли с минеральными или органическими кислотами. Для этой цели, как правило, разбавленные раство ры этих кислот подвергают взаимодействию с и х в со ли с минеральными или органическими кислотами. Для этой цели, как правило, разбавленные растворы этих кислот подвергают взаимодействию с производными гидроксиламинов, целесообразно в эквивалентных количества х. Полученные соли гидроксиламмония можно перерабатывать далее как производные гидроксиламина со свободными аминогруппами непосредственно до гербицидов формулы (I) или в случае необхо димости хранить их в та ком виде. С точки зрения биологической активности циклогексеноноксимовые эфи ры формулы (I) предпочтительны со следующим значением замести телей; R1-алкил, как метил, этил, пропил, 1-метилэтил, бутил, 1-метилпропил, 2-метилпропил, 1,1диметилэтил, пентил, 1-метилбутил, 2-метилбутил, 3-метилбутил, 1,1-диметилпропил, 1,2-диметилпропил, 2,2-диметилпропил, 1-этилпропил, гексил, 1-метилпропил, 2-метилпентил, 2-метилпентил, 4-метилпентил 1,1-диметилбутил, 1,2-ди метилбутил, 1,3-диметилбутил, 2,2-диметилбутил, 2,3-диметилбутил, 3,2-диметилбутил, 1-этилбутил, 2-этилбутил, 1,1,2-три метилпропил, 1,2,2-триметилпропил, 1-этил-1-метилпропил и 1-этил-2-метилпропил, в частности этил и пропил. А–С3-алкилен, в котором метиленовая группа заменена атомом кислорода, как например, 3-оксапропилен. Наиболее предпочтителен 2-оксапропилен. Эфиры циклогексеноноксимов формулы (I) пригодны в качестве гербицидов, в частности для борьбы с растениями из семейства трав. Предметом изобретения является также гербицидное средство, включающее активный ингредиент – эфи ры циклогексеноноксимов формулы (I), в эффективном количестве и целевые добавки. Эфиры циклогексеноноксимов формулы (I) или содержащие эти ве щества гербицидные средства можно применять, например, в виде непосредственно разбрызгиваемых растворов, порошков, суспензий, а также высококонцентрированных, водных, масляных или иных суспензий или дисперсий, эмульсий, масляных суспензий, паст, порошков для распыления, препаратов для внесения в почву в ви де гранул, или гранулятов, путем разбрызгивания, тонкого распыления, внесения в почву гра нулятов или полива. Форма применения выбирается в зави симости от цели применения, каждый метод должен гарантировать наиболее тонкое распределение эффективных ве ществ в соответствии с изобретением. Соединения формулы (I) пригодны, как правило, для приготовления непосредственно разбрызгиваемых растворов, эмульсий, паст или масляных суспензий. В качестве инертных добавок следует иметь в виду фракции минеральных масел со средними и высокими температурами кипения, как керосин или дизельные масла, кроме того, масла природного происхождения, как расти тельные или животные масла, алифатические, циклические и ароматические углеводороды, как, например, толуол, ксилол, парафи ны, тетрагидронафталин, алкилированные нафталины или их производные, метанол, этанол, пропанол, бутанол, циклогексанон, циклогексанол, хлорбензол, изофорон или сильно полярные растворители, как N,N-диметилформамид, диметилсульфоксид, N-метилпирролидон или вода. Применяемые водные формы могут быть приготовлены из эмульсионных концентратов, дисперсий, паст, смачивающи хся порошков или диспергирующи хся в воде гранулятов п утем добавления воды. Для получения эмульсий, паст или масляных дисперсий можно субстраты, как таковые или растворенные в масле или растворителе, гомогенизировать в воде с помощью смачивающи х, диспергирующих, эмульги рующи х средств или аппретуру. Но можно также получать из концентратов, состоящих из биологи чески активного вещества, смачивающе го, схватывающего, диспергирующего или эмульгирующего вещества, а также растворите ля или масла, кото рые пригодны для разбавления водой. В качестве поверхностно-активных веществ сле дует иметь в виду со ли щелочных, щелочно-земельных металлов, аммония, ароматических сульфокислот, например, лигнин-, фенол-, нафта лин- и дибутилнафталинсульфо кислоты, а также жирные кислоты, алкил- или алкарилсульфо наты, алкиловые или лауриловые эфи ры сульфатов спиртов жирного ряда, а также соли суль фати рованных гекса-, гепта- и оксадодеканолов, а также гликолевые эфи ры спиртов жирного ряда, продукты конденсации сульфонированного нафталина и его производных, полученных с фор мальдегидом, продук ты конденсации нафта лина или нафталинсульфокислоты с фе нолом и формальдегидом, полиоксиэтиленокситиофе ноловые эфиры, этоксилированный изооктил-, октил- или нонилфенолы, полигликолевый эфир алкилфенола, три бутилфенилполигликолевой эфир, спирты алкиларилполиэфиров, изотридециловый спирт, конденсаты эти леноксида и спиртов жирного ряда, этоксилированное касторовое масло, полиоксиэтиленалкиловые эфи ры или полиоксипропилены, ацетат полигликолевого эфи ра лаурилового спирта, сорбитовый эфир, суль фатный щелок лигнина или метилцеллюлоза. Средства в ви де гранул, по рошков для внесения в почву и по рошков для распыления можно приготовить путем смеши вания или тонкого измельчения биологически активных ве ществ с твердыми носителями. Грануляты, например, с оболочкой, пропитанные и гомогенные, могут быть приготовлены путем связывания биологи чески активного вещества с твердым носителем. Твердыми носите лями являются минералы, как кремниевая кислота, силикагель, силикаты, тальк, каолин, известь негаше ная, мел, болюс, гли на, доломит, диато митовая земля, сульфа т кальция и магния, оксид магния, измельченные полимерные вещества, удобрения, как сульфа т аммония, фосфа т аммония, нитрат аммония, мочеви на и растительные продукты, как мука злаковы х растений, мука из древесной щепы, скорлупы орехо в, порошкообразная целлюлоза или другие твер дые носители. Готовые препараты содержат, как правило, от 0,02 до 95 вес. %, предпочти тельно от 0,5 до 90 вес. % биологически активного вещества. Активное вещество при этом испльзуют с чистотой от 90 до 100%, предпочти тельно 95–100% (данные ГХ/ЖХВД или ЯМР-спектров). Гербицидные средства в соответствии с изобретением могут быть приготовлены, например, следующим образом: 1. Смешивают 90 вес.ч. сое динения №7.21 и 20 вес.ч. N-метил-a-пирролидона и получают раствор, который пригоден для нанесения его в виде мельчайших капель. 2. 20 вес.ч. соединения № 7.23 растворяют в смеси, содержащей 80 вес.ч. ксилола, 10 вес.ч. продукта конденсации 8–10 моль этиленоксида с 1 моль N-моноэтаноламида масляной кислоты, 5 вес.ч. кальциевой соли додецилбензосульфо кислоты и 5 вес.ч. продук та конденсации 40 моль этиленоксида с 1 моль касторово го масла. В результате сливания и тонкого смешивания раствора с 100000 вес.ч. воды получают водную дисперсию, которая содержит 0,02 вес.% биологически активногове щества. 3. 10 вес.ч. соединения № 7.21 растворяют в смеси, состоящей из 40 вес.ч. циклогексанона, 30 вес.ч. изобутанола, 20 вес.ч. продукта конденсации, 7 мол. этиленоксида и 1 моль изооктилфенола и 10 вес.ч. продукта конденсации 40 моль этиленоксида и 1 моль касторово го масла. Путем приливания и тонкого перемеши вания раствора в 100000 вес.ч. воды получают водный раствор (дисперсию), которая содержит 0,02 вес.% биологически активного ве щества. 4. 20 вес.ч. активного вещества № 7.23 растворяют в смеси, состоящей из 25 вес.ч. циклогексанона, 65 вес.ч. фракций минеральных масел с температурой кипения от 210 до 280оС и 10 вес.ч. продук та конденсации 40 моль этиленоксида и 1 моль касторового масла. Путем вливания и тонкого размешивания получают раствор в 100000 вес.ч. воды, представляющий собой водную дисперсию, которая содержит 0,02 вес.% активного ве щества. 5. 20 вес.ч. активного ве щества № 7.23 хорошо перемешивают с 3 вес.ч. натриевой соли диизобутилнафталин-a-сульфокислоты, 17 вес.ч. натриевой соли лигнинсульфо кислоты, полученной из сульфитной ще лочи, и 60 вес.ч. порошкообразного геля кремневой кислоты, и измельчают в ударной мельнице. В результате тонкого измельчения этой смеси в 20000 вес.ч. воды получают раствор для разбрызгивания, который содержит 0,1 вес.% биологически активного ве щества. 6. 3 вес. ч. активного вещества № 7.15 перемешивают с 97 вес. ч. тонкоизмельченного каолина и таким образом получают порошок для распыления, который содержит 3 вес. % активного вещества. 7. 30 вес.ч. активного вещества № 7.21 тонко смеши вают со смесью, состоящей из 92 вес.ч. порошкообразного геля кремниевой кислоты и 8 вес.ч. па рафи нового масла, которую разбрызгивают на поверх ность этого геля кремневой кислоты. Та ким образом получают готовый препарат биологически активного вещества с хо рошей схватываемостью. 8. 2 вес. ч. активного вещества № 7.23 тонко смеши вают с 2 вес.ч. кальциевой соли додецилбензолсульфо кислоты, 8 вес.ч. полигликолевого эфи ра жирного спирта, 2 вес.ч. натриевой соли конденсата фенола-мочевины-формальдегида и 68 вес.ч. парафинового минерального масла. Получают стабильную дисперсию. Наносить средство можно до и после прорастания всходов. Если активные вещества не очень совместимы с некоторыми культур ными растениями, то применяют такие методы нанесения, при которых гербицидные средства наносятся на растения специальными устройствами для нанесения, чтобы листья защи щаемых растений по возможности меньше затрагивать, в то время как активное вещество должно попадать на листья и окружающую землю нежелательных растений. Расходные нормы активного вещества составляют в зависимости от вре мени года, зеленых растений и стадии роста, от 0,001 до 3 кг/га, предпочтительно 0,01–2,0 кг/га. Охваты ваемый спектр действия для борьбы с сорняками, совместимость с культурными растениями или желаемое влияние на рост этих расте ний, а также многообразие методов нанесения – все это дают соединения в соответствии с изобретением с большим количеством культур ных растений, приведенных в конце описания. Для расширения спектра действия и для достижения синергизма производные циклогексенонов формулы (I) можно смешивать как друг с другом, так и с представите лями других гербицидных или регулирующи х рост растений групп биологически активных веществ и наносить самостоятельно. Примерами компонентов возможных смесей являются диазины, 4Н-3,1-бензоксазиновые производные, бензотиадиазиноны, 2,6-динитроанилины, N-фенилкарбаматы, тиокарбаматы, га логенкарбоновые кислоты, триазины, амиды, мочевины, дифе ниловые эфиры, триазиноны, урацилы, производные бензофурана, хинолинкарбоновые кислоты, производные сульфонилмочевин, циклогексанон, гетеро-арилоксипропионовые кислоты, их со ли, эфи ры, амиды и прочее. Кроме того, полезно использовать производные циклогексеноксимовых эфи ров формулы (I) или гербицидные средства, содержащие их, самостоятельно или в комбинации с другими гербицидами или также с другими средствами защиты растений и наносить, например, со средствами для борьбы с вредителями или фитопато генными грибами или бактериями. Представляют интерес, кроме того, смеси с раство рами минеральных солей, которые используют для увеличения содержания питательных веществ и микроэлементов. Можно добавлять также нефи тотоксичные масла и масляные концентраты. В нижеприведенных примерах синтеза использовали соответствующие исходные соединения для получения других гидроксиламинов фор мулы (III) и циклогексеноксимовых эфиров фор мулы (I); полученные соединения приведены в нижеприведенной таблице с фи зико-химическими данными. Приме ры получения гидроксиламинов III. N-[2-(2-фторбензилокси)этокси]фта лимид. К смеси, состоящей из 165 г (0,71 моль) 1-бром-2-(2-фторбензилокси)этана, 116 г (0,7 моль) N-гидроксифталамида и 710 мл N-метилпирролидона. Через 5 ч при 60оС холодную реакционную смесь выливают в 2000 мл ледяной воды, отсасывают осадок, промывают водой и изопропанолом и высушенным в вакууме над пентаоксидом фосфора 185 г (82%) фталимидного эфи ра. Т.пл. 62–64оС; Спектр ЯМР–1Н (250 МГц, d6-D MSO): d 3,85 (m, 2H); 4,35 (m, 2H) + 7,10 – 7,40 (m, 4H); 7,88 (s, 4H). O–[2-(2-фторбензилокси)этил]гидроксиламин. 184 г (0,58 моль, полученного, как описано выше) эфира фта лимида порциями вносят в 270 мл этаноламина. Через 3 ч при 60оС холодную реакционную смесь выливают в 1000 мл воды со льдом. Гидролизат трижды экстрагируют дихлорметаном порциями по 800 мл. Соединенные органические фазы промывают 200 мл насыщенного раствора поваренной соли, высушивают над сульфатом магния и выпаривают в вакууме. Получают 98 г (91%) гидроксиламина. 1 Н–ЯМР-спектр (250 МГц, CDCl3): d 3,70 (dd, 2H); 3,85 (dd, 2H); 4,54 (s, 2H); 5,50 (br.s., 2H); 7.00 – 7,50 (m. 4H). Пример получения эфира циклогексеноноксима I. 2-[1-[[2-(2-фторбензилокси)этокси]имино]бутил]-3-гидрокси-5-(2Н-тетрагидропиран-4-ил)-2-циклогексен-1-он. Смесь из 4,0 г (10 ммол) 2-бутирил-3-гидрокси-5-(2Н-тетрагидропиран-4-ил)-2-циклогексен-1-она и 2,6 г (14 ммол) О-[2-(2-фторбензилокси)этил]-гидроксиламина в 100 мл метанола перемеши вают 24 ч. Реакционную смесь испаряют в ва кууме и сырой продукт хроматографи руют че рез 100 г силикагеля в колонке 30 ·4 см (элюирующую жидкость:эфир). Получают 3,5 г (54%) эфи ра циклогексеноноксима. 1 Н–ЯМР (300 МГц, CDCl3): d 0,93 (t, 3H); 1,20 – 1,77 (m, 7H); 1,90 (m, 1H); 2,23 (m, 4H); 2,58 (m, 2H); 2,92 (m, 2H); 3,38 (t, 2H); 3,80 (m, 2H); 4,03 (m, 2H); 4,25 (m, 2H); 4,68 (s, 2H); 6,93–7,50 (m, 4H); 14,30 (s, 1H). Результа ты испытаний представлены в табл. 1–14. Приме ры на применение. Гербицидное действие эфи ров циклогексеноноксимов формулы (I) продемонстрировано опыта ми, приведенными в теплице. В качестве сосудов для культур служили пласти ковые цветочные горшки с глинистым песком приблизительно с 3% навоза в качестве субстрата. Се мена испытываемых расте ний раздельно по видам. При обработке перед прораста нием диспергированное или суспендированное в воде биологически активное вещество наносили непосредственно после высевания с помощью тонко разбрызгивающе го соп ла. Сосуды были слегка увлажнены, чтобы обеспечить прорастание и рост, и непосредственно после этого были накрыты проницаемыми пластиковыми цилиндрами до прорастания растений. Эти покрытия способствовали равномерному прорастанию испытуе мых растений, так как им не был причинен ущерб со стороны биологически активного вещества. С целью обработки после прорастания всхо дов испыты ваемые растения в зависимости от форм роста обрабатывали при их вы соте от 3 до 15 см суспендированными или диспергированными в во де биологически активными веществами. Расходные нормы для способа обработки после прорастания всхо дов составляли 0,25 кг/га. Растения выдерживали в зависимости от их типа при 10–25оС или 20–35оС. Опыт продолжали от 2 до 4 недель. В это вре мя за растениями уха живали и оценивали их реакцию на отдельные обработки. Оценку проводили по шкале от 0 до 100. При этом 100 означает отсутствие всхо жести растений или полное разрушение, по крайней мере, части, находящейся над землей, и 0 – это отсутствие повреждения или нормальный процесс роста. Для испытания в опытах бы ли взяты сле дующие типы тепличных растений: щетинник итальянский, 3; зеленый щетинник. В опыте при обработке после прорастания всходов использовали 0,25 кг/га активного ве щества – соединения из примера 7.21 и 7.23, при этом было достигнуто очень хорошее поражение нежелательных травянистых растений при одновременной совместимости с культурой риса. Все соединения формулы (I) проявляют аналогичную активность в отношении риса. Для подтверждения гербицидного действия заявленных эфи ров циклогексеноноксимов формулы (I) были осуществлены испытания на поражение сорняков указанными гербицидно-активными соединениями. Для испытаний каждый раз брали средства, представляющие собой жидкий состав. Состав содержал 100 г активного действующего начала в 1 л смеси из 93 вес.% ксилола и 7 вес.% лутензолаR AP8 (смачиватель с эмульгирующим и диспергирующим действием на основе восьмикратного этоксилированного нонилфе нола). Результа ты испытаний представлены в табл. 15–19. Полифункциональное соединение № 3.29 формулы CH3 OH N–O–CH 2–CH–O Cl C2H5–S–HC–H2C C3H7 CH3 O (3.29) является высокоактивным веществом. Так, при количестве расхо да этого соединения 0,05 кг/га (при обработке после появлениявсходов) достигается 100%-ное действие против нежелательных растений Echinochloa cruss galli (ежовник) Lolium-multiflorum. Следующие опыты бы ли произве дены в соответствии со с. 65 описания. При этом соединение № 2.39 подвергли сравнению с известными из ЕР–А 218.333 сравнитель ными продук тами A–D , фор мулы которых из ложены в табл. 20 : OH N–O–R O C R1 O Из данных нижеследующи х таблиц 21 и 22 ясно следует, что соединения согласно изобретению проявляют лучшее действие. Кроме хорошего гербицидного действия сравнение с примерами А и С показывает очень хорошую се лективность в культуре риса. Повреждение в размере 55 и 65% соответственно, которое видно при использовании А и С соответственно, не допусти мое при употреблении в этой культуре. По сравнению с соединениями В и D соединение согласно изобретению проявляет более высокую гербицидную активность. Указанные в табл. 23 коды растений имеют следующие значения. Гербицидная активность соединения согласно изобретению подтверждается примерами, указанными в табл. 24 и 25. Препарат получен как концентрат эмульсии в смеси из 7% Luthensol AP8 (алкилфенолэтоксилат) и 93% ксилола, причем содержание активного вещества составляет 100 г/л. Ниже приводится дополнительное доказательство положительного эффекта для соединений № 12.01, 12.02, 13.01 и 13.02. Опыты были прове дены методами, описанными на с.65, причем активные вещества были применены после появления всхо дов (норма расхо да 0,25 кг/га) активного вещества). Разб рызгиваемый раствор содержал 100 г активного вещества на 1 л смеси, включающей 93 мас.% ксилола и 7 мас.% ЛутензолаÒ AP8. Таблица 26 содержит результаты, полученные в теплице. Из этих результатов следует, что испытанные соединения обладают большой сте пенью селективности по отноше нию к озимой пшенице. Таблица 1 Н2N–O–A–Z–Xn № А Z X n Физические данные ( 1Н–ЯМР (d частей/миллион) 1.01 СН2СН2О фенил – 0 6,90 (m,3Н), 7,27 (m, 2H) 1.02 СН2СН2О фенил 2–F 1 6,85–7,15 (m, 4H) 1.03 СН2СН2О фенил 3–F 1 6,70 (m, 3H), 7,27 (m, 1H) 1.04 СН2СН2О фенил 4–F 1 6,80–7,00 (m, 4H) 1.05 СН2СН2О фенил 2–Cl 1 1.06 СН2СН2О фенил 3–Cl 1 1.07 СН2СН2О фенил 4–Cl 1 6,85 (m, 2H), 7,25 (m, 2H) 1.11 СН2СН2О фенил 2,4–Cl2 2 6,83 (d, 1H), 7,15 (dd, 1H), 7,85 (d, 1H) 1.12 СН2СН2О фенил 2,4,6–Cl3 3 7,30 (s, 2H) 1.15 СН2CH(СН3)О фенил 4–F 1 1.16 CH2CH(CH3)O фенил 4–Cl 1 1.22 СН2СН2CH2О фенил – 0 6,90 (m, 3H), 7,27 (m, 2H) 1.23 СН2СН2CH2О фенил 2–F 1 6,80–7,15 (m, 4H) 1.24 СН2СН2CH2О фенил 3–F 1 6,70 (m, 3H), 7,25 (m, 1H) 1.25 СН2СН2CH2О фенил 4–F 1 6,80–7,00 (m,4H) 1.26 СН2СН2CH2О фенил 2–Cl 1 6,80–7,00 (m, 2H), 7,20 (m, 1H), 7,35 (m, 1H) 1.27 СН2СН2CH2О фенил 3–Cl 1 6,80 (m, 1H), 6,95 (m, 2H), 7,20 (m, 1H) 1.28 СН2СН2CH2О фенил 4–Cl 1 6,80 (m, 2H), 7,20 (m, 2H) 1.35 СН2СН2CH2О фенил 2,5–Cl2 2 1.36 СН2СН2CH2О фенил 2,5–Cl2 2 Таблица 2 OH Xn NO–CH2 CH2 O R2 R1 O I (A=CH 2CH2O–; Z=фе нил) № R1 R2 Xn Физические данные [ 1Н–ЯМР (частей/миллион); Т.пл., оС] 1 2 3 4 5 2.07 этил тетрагидропиран-3-ил 2–F 76–78 2.08 пропил тетрагидропиран-3-ил 2–F 72–77 2.09 этил тетрагидропиран-4-ил 2–F 121–125 2.10 пропил тетрагидропиран-4-ил 2–F 103–107 2.11 этил тетрагидротиопиран-3-ил 2–F 82–86 2.12 пропил тетрагидротиопиран-3-ил 2–F 81–85 2.13 этил тетрагидропиран-3-ил 3–F 62–68 2.14 пропил тетрагидропиран-3-ил 3–F 3,90 (m, 2H), 4,20 (t, 2H), 4,40 (m, 2H), 6,70 (m, 3H), 7,25 (m, 1H) 2.15 этил тетрагидропиран-4-ил 3–F 103–109 2.16 пропил тетрагидропиран-3-ил 3–F 73–79 2.17 этил тетрагидротиопиран-3-ил 3–F 4,20 (t, 2H), 4,40 (m, 2H), 6,70 (m, 3H), 7,25 (m, 1H) 2.18 пропил тетрагидротиопиран-3-ил 3–F 2.19 этил тетрагидропиран-3-ил 4–F 64–67 2.20 пропил тетрагидропиран-3-ил 4–F 70–72 2.21 этил тетрагидропиран-4-ил 4–F 101–103 2.22 пропил тетрагидропиран-4-ил 4–F 107–109 2.23 этил тетрагидропиран-3-ил 4–F 105–108 2.24 пропил тетрагидропиран-3-ил 4–F 82–84 2.25 этил тетрагидропиран-3-ил 2–Cl 74–80 2.26 пропил тетрагидропиран-3-ил 2–Сl 67–71 2.27 этил тетрагидропиран-4-ил 2–Сl 4,00 (m, 2H), 4,27 (t, 2H), 4,47 (m, 2H), 7,20 (t, 1H), 7,37 (d, 1H) 2.28 пропил тетрагидропиран-4-ил 2–Сl 68–72 2.29 этил тетрагидротиопиран-3-ил 2–Сl 74–78 2.30 пропил тетрагидротиопиран-3-ил 2–Сl 72–78 2.31 этил тетрагидропиран-3-ил 3–Сl 2.32 пропил тетрагидропиран-3-ил 3–Сl 2.33 этил тетрагидропиран-4-ил 3–Сl 2.34 пропил тетрагидропиран-4-ил 3–Сl 2.35 этил тетрагидротиопиран-3-ил 3–Сl 2.36 пропил тетрагидротиопиран-3-ил 3–Сl 2.37 этил тетрагидропиран-3-ил 4–Сl 1 2 3 4 2.38 пропил тетрагидропиран-3-ил 4–Сl 3,93 (m, 2H), 4,20 (t, 2H), 4,43 (m, 2H), 6,90 (m, 2H), 7,25 (m, 2H) 2.39 этил тетрагидропиран-4-ил 4–Сl 116–118 2.40 пропил тетрагидропиран-4-ил 4–Сl 104–106 2.41 этил тетрагидротиопиран-3-ил 4–Сl 74–77 2.42 пропил тетрагидротиопиран-3-ил 4–Сl 86–88 2.61 этил тетрагидропиран-3-ил 2,4–Сl2 73–75 2.62 пропил тетрагидропиран-3-ил 2,4–Сl2 69–73 3,93 (m, 2H), 4,20 (t, 2H), 4,43 (m, 2H), 6,90 (m, 2H), 7,25 (m, 2H) Продолжение табл. 2 5 2.63 этил тетрагидропиран-4-ил 2,4–Сl2 4,00 (m, 2H), 4,25 (t, 2H), 4,45 (t, 2H), 6,87 (d, 1H), 7,17 (d, 1H), 7,37 (d, 1H) 2.64 пропил тетрагидропиран-5-ил 2,4–Сl2 4,00 (m, 2H), 4,25 (t, 2H), 4,45 (t, 2H), 6,87 (d, 1H), 7,17 (d, 1H), 7,37 (d, 1H) 2.65 этил тетрагидротиопиран-3-ил 2,4–Сl2 4,25 (t, 2H), 4,45 (t, 2H), 6,87 (d, 1H), 7,17 (d, 1H), 7,37 (d, 1H) 2.66 пропил тетрагидротиопиран-3-ил 2,4–Сl2 4,25 (t, 2H), 4,45 (t, 2H), 6,87 (d, 1H), 7,17 (d, 1H), 7,37 (d, 1H) 2.67 этил тетрагидропиран-3-ил 2,4,6–Cl3 90–93 2.68 пропил тетрагидропиран-3-ил 2,4,6–Cl3 83–87 2.69 этил тетрагидропиран-4-ил 2,4,6–Cl3 79–82 2.70 пропил тетрагидропиран-4-ил 2,4,6–Cl3 4,00 (m, 2H), 4,27 (t, 2H), 4,45 (m, 2H), 7,32 (s, 2H) 2.71 этил тетрагидротиопиран-3-ил 2,4,6–Cl 3 105–108 2.72 пропил тетрагидротиопиран-3-ил 2,4,6–Cl 3 4,27 (t, 2H), 4,45 (m, 2H), 7,82 (s, 2H) 2.85 этил тетрагидропиранил-3 2–Cl, 4–F 3,93 (m, 2H), 6,95 (m, 2H), 7,15 (m, 1H) 2.86 пропил тетрагидропиранил-3 2–Cl, 4–F 3,93 (m, 2H), 6,95 (m, 2H), 7,15 (m, 1H) 2.87 этил тетрагидропиранил-4 2–Cl, 4–F 78–80 2.88 пропил тетрагидропиранил-4 2–Cl, 4–F 4,00 (m, 2H), 6,95 (m, 2H), 7,15 (m, 1H) 2.89 этил тетрагидротиопиранил-3 2–Cl, 4–F 92–94 2.90 пропил тетрагидротиопиранил-3 2–Cl, 4–F 6,95 (m, 2H), 7,15 (m, 1H) 2.91 этил тетрагидропиранил-3 2–Br, 4–Cl 3,95 (m, 2H), 6,83 (d, 1H), 7,23 (dd, 1H), 7,55 (d, 1H) 2.92 пропил тетрагидропиранил-3 2–Br, 4–Cl 3,95 (m, 2H), 6,83 (d, 1H), 7,23 (dd, 1H), 7,55 (d, 1H) 2.93 этил тетрагидропиранил-4 2–Br, 4–Cl 4,00 (m, 2H), 6,83 (d, 1H), 7,23 (dd, 1H), 7,55 (d, 1H) 2.94 пропил тетрагидропиранил-4 2–Br, 4–Cl 88–90 2.95 этил тетрагидротиопиранил-3 2–Br, 4–Cl 6,83 (d, 1H), 7,23 (dd, 1H), 7,55 (d, 1H) 2.96 пропил тетрагидротиопиранил-3 2–Br, 4–Cl 6,83 (d, 1H), 7,23 (dd, 1H), 7,55 (d, 1H) 2.97 этил тетрагидропиранил-3 2–Br, 4–F 56–58 2.98 пропил тетрагидропиранил-3 2–Br, 4–F 3,93 (m, 2H), 6,80–7,15 (m, 2H), 7,30 (m, 1H) 2.99 этил тетрагидропиранил-4 2–Br, 4–F 4,00 (m, 2H), 6,80–7,15 (m, 2H), 7,30 (m, 1H) 2.100 пропил тетрагидропиранил-4 2–Br, 4–F 4,00 (m, 2H), 6,80–7,15 (m, 2H), 7,30 (m, 1H) 2.101 этил тетрагидротиопиранил-3 2–Br, 4–F 85–87 2.102 пропил тетрагидротиопиранил-3 2–Br, 4–F 6,80–7,15 (m, 2H), 7,30 (m, 1H) Продолжение табл. 2 1 2 3 4 2.103 этил тетрагидропиранил-3 2,4–F2 3,93 (m, 2H), 6,70–7,00 (m, 3H) 2.104 пропил тетрагидропиранил-3 2,4–F2 3,93 (m, 2H), 6,70–7,00 (m, 3H) 2.105 этил тетрагидропиранил-4 2,4–F2 77–79 2.106 пропил тетрагидропиранил-4 2,4–F2 74–76 2.107 этил тетрагидротиопиранил-3 2,4–F2 58–60 2.108 пропил тетрагидротиопиранил-3 2,4–F2 77–78 2.109 этил тетрагидропиранил-3 2,4–Br2 79–81 5 2.110 пропил тетрагидропиранил-3 2,4–Br2 3,95 (m, 2H), 6,80 (d, 1H), 7,35 (dd, 1H), 7,70 (d, 1H) 2.111 этил тетрагидропиранил-4 2,4–Br2 88–90 2.112 пропил тетрагидропиранил-3 2,4–Br2 4,00 (m, 2H), 6,80 (d, 1H), 7,35 (dd, 1H), 7,70 (d, 1H) 2.113 этил тетрагидротиопиранил-3 2,4–Br2 6,80 (d, 1H), 7,35 (dd, 1H), 7,70 (d, 1H) 2.114 пропил тетрагидротиопиранил-3 2,4–Br2 6,80 (d, 1H), 7,35 (dd, 1H), 7,70 (d, 1H) 2.115 этил 1-метилтиоциклопропил-1 4–F 2,13 (s, 3H), 6,80–7,10 (m, 4H) 2.116 пропил 1-метилтиоциклопропил-1 4–F 2,13 (s, 3H), 6,80–7,10 (m, 4H) 2.119 этил тетрагидропиранил-3 2–Cl, 4–Br 3,93 (m, 2H), 6,85 (m, 1H), 7,35 (m, 1H), 7,50 (m, 1H) 2.120 пропил тетрагидропиранил-3 2–Cl, 4–Br 3,93 (m, 2H), 6,85 (m, 1H), 7,35 (m, 1H), 7,50 (m, 1H) 2.121 этил тетрагидропиранил-4 2–Cl, 4–Br 4,00 (m, 2H), 6,85 (m, 1H), 7,35 (m, 1H), 7,50 (m, 1H) 2.122 пропил тетрагидропиранил-4 2–Cl, 4–Br 4,00 (m, 2H), 6,85 (m, 1H), 7,35 (m, 1H), 7,50 (m, 1H) 2.123 этил тетрагидротиопиранил-3 2–Сl, 4–Br 6,85 (m, 1H), 7,35 (m, 1H), 7,50 (m, 1H) 2.124 пропил тетрагидротиопиранил-3 2–Сl, 4–Br 6,85 (m, 1H), 7,35 (m, 1H), 7,50 (m, 1H) Таблица 3 OH Xn NO–CH2 CH–O R2 CH3 R1 O I (A = CH 2CH(CH3)–O–; Z = фенил) № R1 R2 Xn Физические данные [ 1H–ЯМР (частей/миллион); Т. пл., оС] 5 1 2 3 4 3.07 3.08 3.09 3.10 3.11 3.12 3.13 этил пропил этил пропил этил пропил этил тетрагидропиран-3-ил тетрагидропиран-3-ил тетрагидропиран-4-ил тетрагидропиран-4-ил тетрагидротиопиран-3-ил тетрагидротиопиран-3-ил тетрагидропиранил-3 4–F 4–F 4–F 4–F 4–F 4–F 4–Cl 3 4 3,93 (m, 2H), 4,20 (m, 2H), 4,60 (m, 1H), 6,83 (m, 2H), 7,20 (m, 2H) Продолжение табл. 3 1 2 3.14 пропил тетрагидропиранил-3 4–Cl 3,93 (m, 2H), 4,20 (m, 2H), 4,60 (m, 1H), 6,83 (m, 2H), 7,20 (m, 2H) 5 3.15 этил тетрагидропиран-4-ил 4–Cl 1,35 (m, 3H), 4,05–4,30 (m, 2H), 4,60 (m, 1H), 6,80–7,40 (m, 4H) 3.16 пропил тетрагидропиран-4-ил 4–Cl 3.17 этил тетрагидротиопиран-3-ил 4–Cl 1,35 (m, 3H), 4,05–4,30 (m, 2H), 4,60 (m, 1H), 6,80–7,40 (m, 4H) 1,35 (m, 2H), 4,05–4,25 (m, 2H), 4,60 (m, 1H), 6,80–7,40 (m, 4H) 3.18 пропил тетрагидротиопиран-3-ил 4–Cl 1,35 (m, 3H), 4,05–4,30 (m, 2H), 4,60 (m, 1H), 6,80–7,40 (m, 4H) 3.19 этил 1-метилтиоциклопропил-1 4–Cl 3.20 пропил 1-метилтиоциклопропил-1 4–Cl 2,13 (s, 3H), 4,20 (m, 2H), 4,60 (m, 1H), 6,90 (d, 2H), 7,20 (d, 2H) 2,10 (s, 3H), 4,20 (m, 2H), 4,60 (m, 1H), 6,90 (d, 2H), 7,20 (d, 2H) 3.23 этил тетрагидропиранил-3 2,4–Cl2 3,93 (m, 2H), 6,90 (d, 1H), 7,20 (dd, 1H), 7,40 (d, 1H) 3.24 пропил тетрагидропиранил-3 2,4–Cl2 3,95 (m, 2H), 6,90 (d, 1H), 7,20 (dd, 1H), 7,40 (d, 1H) 3.25 этил тетрагидропиранил-4 2,4–Cl2 4,00 (m, 2H), 6,90 (d, 1H), 7,20 (dd, 1H), 7,40 (d, 1H) 3.26 пропил тетрагидропиранил-4 2,4–Cl2 3.27 3.28 этил пропил тетрагидротиопиранил-3 тетрагидротиопиранил-3 2,4–Cl2 2,4–Cl2 4,00 (m, 2H), 6,90 (d, 1H), 7,20 (dd, 1H), 7,40 (d, 1H) 6,90 (d, 1H), 7,20 (dd, 1H), 7,40 (d, 1H) 6,90 (d, 1H), 7,20 (dd, 1H), 7,40 (d, 1H) Таблица 4 OH Xn NO–CH2 CH2 –S R2 R1 O I (A = –CH 2CH2–S–; z -фе нил) № R1 R2 Xn Физические данные [ 1H–ЯМР (частей/миллион); Т. пл., оC] 4.07 этил тетрагидропиран-3-ил 4–F 3,90 (m, 2H); 4,17 (t, 2H); 7,00 (m, 2H); 7,40 (m, 2H) 4.08 пропил тетрагидропиран-3-ил 4–F 3,90 (m, 2H); 4,17 (t, 2H); 7,00 (m, 2H); 7,40 (m, 2H) 4.09 этил тетрагидропиран-4-ил 4–F 4,00 (m, 2H); 4,17 (t, 2H); 7,00 (m, 2H); 7,40 (m, 2H) 4.10 пропил тетрагидротиопиран-4-ил 4–F 4,00 (m, 2H); 4,17 (t, 2H); 7,00 (m, 2H); 7,40 (m, 2H) 4.11 этил тетрагидротиопиран-3-ил 4–F 4,17 (t, 2H); 7,00 (m, 2H); 7,40 (m, 2H) 4.12 пропил тетрагидротиопиран-3-ил 4–F 4,17 (t, 2H); 7,00 (m, 2H); 7,40 (m, 2H) 4.13 этил тетрагидропиран-3-ил 4–Cl 71–75 4.14 пропил тетрагидропиран-3-ил 4–Cl 63–65 4.15 этил тетрагидропиран-4-ил 4–Cl 4,00 (m, 2H), 4,20 (t, 2H); 7,30 (m, 4H) 4.16 пропил тетрагидропиран-4-ил 4–Cl 4,00 (m, 2H), 4,20 (t, 2H); 7,30 (m, 4H) 4.17 этил тетрагидротиопиран-3-ил 4–Cl 4,20 (t, 2H), 7,30 (m, 4H) 4.18 пропил тетрагидротиопиран-3-ил 4–Cl 4,20 (t, 2H), 7,30 (m, 4H) 4.19 этил тетрагидропиран-3-ил 2–Cl 3,90 (m, 2H); 4,25 (t, 2H); 7,10–7,50 (m, 4H) 4.31 этил 1-метилтиоциклопропил-1 4–F 2,13 (s, 3H); 4,20 (t, 2H); 7,00 (m, 2H); 7,40 (m, 2H) 4.32 пропил 1-метилтиоциклопропил-1 4–F 2,13 (s, 3H); 4,20 (t, 2H); 7,00 (m, 2H); 7,40 (m, 2H) Таблица 5 OH Xn NO–CH2 CH2 CH 2–O R2 R1 O I (A = CH 2CH2CH2O–; Z = фе нил) № R1 R2 Xn Физические данные [ 1H–ЯМР (частей/миллион); Т. пл., оC] 1 2 3 4 5 5.07 этил тетрагидропиран-3-ил 2–F 3,90 (m, 2H), 4,10 (t, 2H), 4,27 (t, 2H), 6,80–7,15 (m, 4H) 5.08 пропил тетрагидропиран-3-ил 2–F 3,90 (m, 2H), 4,10 (t, 2H), 4,27 (t, 2H), 6,80–7,15 (m, 4H) 5.09 этил тетрагидропиран-4-ил 2–F 4,00 (m, 2H), 4,10 (t, 2H), 4,27 (t, 2H), 6,80–7,15 (m, 4H) 5.10 пропил тетрагидропиран-4-ил 2–F 76–80 5.11 этил тетрагидротиопиран-3-ил 2–F 4,10 (t, 2H), 4,27 (t, 2H), 6,80–7,15 (m, 4H) 5.12 пропил тетрагидротиопиран-3-ил 2–F 4,10 (t, 2H), 4,27 (t, 2H), 6,80–7,15 (m, 4H) 5.13 этил тетрагидропиран-3-ил 3–F 3,90 (m, 2H), 4,05 (t, 2H), 4,27 (t, 2H), 6,67 (m, 3H), 7,23 (m, 1H) 5.14 пропил тетрагидропиран-3-ил 3–F 3,90 (m, 2H), 4,05 (t, 2H), 4,27 (t, 2H), 6,67 (m, 3H), 7,23 (m, 1H) 5.15 этил тетрагидропиран-4-ил 3–F 3,90–4,10 (m, 4H), 4,27 (t, 2H), 6,67 (m, 3H), 7,23 (m, 1H) 5.16 пропил тетрагидропиран-4-ил 3–F 3,90–4,10 (m, 4H), 4,27 (t, 2H), 6,67 (m, 3H), 7,23 (m, 1H) 5.17 этил тетрагидротиопиран-3-ил 3–F 4,05 (t, 2H), 4,27 (t, 2H), 6,67 (m, 3H), 7,23 (m, 1H) 5.18 пропил тетрагидротиопиран-3-ил 3–F 4,05 (t, 2H), 4,27 (t, 2H), 6,67 (m, 3H), 7,23 (m, 1H) 5.19 этил тетрагидропиран-3-ил 4–F 3,90 (m, 2H), 4,03 (t, 2H), 4,27 (t, 2H), 6,90 (m, 2H), 7,00 (m, 2H) 5.20 пропил тетрагидропиран-3-ил 4–F 3,90 (m, 2H), 4,03 (t, 2H), 4,27 (t, 2H), 6,90 (m, 2H), 7,00 (m, 2H) 5.21 этил тетрагидропиран-3-ил 4–F 3,90–4,06 (m, 4H), 4,23 (t, 2H), 6,90 (m, 2H), 7,00 (m, 2H) 5.22 пропил тетрагидропиран-4-ил 4–F 3,90–4,08 (m, 4H), 4,28 (t, 2H), 6,90 (m, 2H), 7,00 (m, 2H) 5.23 этил тетрагидротиопиран-3-ил 4–F 4,03 (t, 2H), 4,27 (t, 2H), 6,90 (m, 2H), 7,00 (m, 2H) 5.24 пропил тетрагидротиопиран-3-ил 4–F 4,03 (t, 2H), 4,27 (t, 2H), 6,90 (m, 2H), 7,00 (m, 2H) 5.25 этил тетрагидропиран-3-ил 2–Сl 5.26 пропил тетрагидропиран-3-ил 2–Сl 5.27 этил тетрагидропиран-4-ил 2–Сl 5.28 пропил тетрагидропиран-4-ил 2–Сl 5.29 этил тетрагидротиопиран-3-ил 2–Сl 5.30 пропил тетрагидротиопиран-3-ил 2–Сl 5.31 этил тетрагидропиран-3-ил 3–Сl 1 2 3 4 5.32 пропил тетрагидропиран-3-ил 3–Сl 3,90 (m, 2H), 4,06 (m, 2H), 4,27 (t, 2H), 6,77 (m, 1H), 6,90 (m, 2H), 7,17 (t, 1H) 5.33 этил тетрагидропиран-3-ил 3–Сl 3,90–4,10 (m, 4H), 4,27 (t, 2H), 6,77 (m, 1H), 6,90 (m, 2H), 7,17 (m, 1H) 5.34 пропил тетрагидропиран-4-ил 3–Сl 3,90–4,10 (m, 4H), 4,27 (t, 2H), 6,77 (m, 1H), 6,90 (m, 4H), 7,17 (m, 1H) 5.35 этил тетрагидротиопиран-3-ил 3–Сl 4,06 (t, 2H), 4,27 (t, 2H), 6,77 (m, 1H), 6,90 (m, 2H), 7,17 (m, 1H) 3,90 (m, 2H), 4,06 (t, 2H), 4,27 (t, 2H), 6,77 (m, 1H), 6,90 (m, 2H), 7,17 (m, 1H) Продолжение табл. 5 5 5.36 пропил тетрагидротиопиран-3-ил 3–Сl 4,06 (t, 2H), 4,27 (t, 2H), 6,77 (m, 1H), 6,90 (m, 2H), 7,17 (m, 1H) 5.37 этил тетрагидропиран-3-ил 4–Сl 3,90 (m, 2H), 4,03 (t, 2H), 4,23 (t, 2H), 6,80 (m, 2H), 7,20 (m, 2H) 5.38 пропил тетрагидропиран-3-ил 4–Сl 3,90 (m, 2H), 4,03 (t, 2H), 4,23 (t, 2H), 6,80 (m, 2H), 7,20 (m, 2H) 5.39 этил тетрагидропиран-3-ил 4–Сl 3,90–4,09 (t, 2H), 4,23 (t, 2H), 6 ,80 (t, 2H), 7,20 (m, 2H) 5.40 пропил тетрагидропиран-4-ил 4–Сl 3,90–4,09 (t, 2H), 4,23 (t, 2H), 6 ,80 (m, 2H), 7,20 (m, 2H) 5.41 этил тетрагидротиопиран-3-ил 4–Cl 4,03 (t, 2H), 4,23 (t, 2H), 6,80 (m, 2H), 7,20 (m, 2H) 5.42 пропил тетрагидротиопиран-3-ил 4–Cl 4,03 (t, 2H), 4,23 (t, 2H), 6,80 (m, 2H), 7,20 (m, 2H) 5.49 этил тетрагидропиран-3-ил 4–Br 3,90 (m, 2H), 4,00 (t, 2H), 4,27 (t, 2H), 6,80 (d, 2H), 7,37 (d, 2H) 5.50 пропил тетрагидропиран-3-ил 4–Br 3,90 (m, 2H), 4,00 (t, 2H), 4,27 (t, 2H), 6,80 (d, 2H), 7,37 (d, 2H) 5.51 этил тетрагидропиран-4-ил 4–Br 3,90–4,10 (m, 4H), 4,27 (t, 2H), 6,80 (d, 2H), 7,37 (d, 2H) 5.52 пропил тетрагидропиран-4-ил 4–Br 3,90–4,10 (m, 4H), 4,27 (t, 2H), 6,80 (d, 2H), 7,37 (d, 2H) 5.53 этил тетрагидротиопиран-4-ил 4–Br 4,00 (t, 2H), 4,27 (t, 2H), 6,80 (d, 2H), 7,37 (d, 2H) 5.54 пропил тетрагидротиопиран-4-ил 4–Br 4,00 (t, 2H), 4,27 (t, 2H), 6,80 (d, 2H), 7,37 (d, 2H) 5.53 этил тетрагидропиранил-3 2,4–Br2 3,93 (m, 2H), 4,10 (t, 2H), 4,27 (t, 2H), 6,75 (d, 1H), 7,35 (dd, 1H), 7,70 (d, 1H) 5.56 пропил тетрагидропиранил-3 2,4–Br2 3,93 (m, 2H), 4,10 (t, 2H), 4,27 (t, 2H), 6,75 (d, 1H), 7,35 (dd, 1H), 7,70 (d, 1H) 5.57 этил тетрагидропиранил-4 2,4–Br2 78–79 5.58 пропил тетрагидропиранил-4 2,4–Br2 4,00 (m, 2H), 4,10 (t, 2H), 4,27 (t, 2H), 6,75 (d, 1H), 7,35 (dd, 1H), 7,70 (d, 1H) 5.59 этил тетрагидротиопиранил-3 2,4–Br2 4,10 (t, 2H), 4,27 (t, 2H), 6,75 (d, 1H), 7,35 (dd, 1H), 7,70 (d, 1H) 5.60 пропил тетрагидротиопиранил-3 2,4–Br2 4,10 (t, 2H), 4,27 (t, 2H), 6,75 (d, 1H), 7,35 (dd, 1H), 7,70 (d, 1H) 5.61 этил тетрагидропиранил-3 2–Cl, 4–Br 3,90 (m, 2H), 4,10 (t, 2H), 4,30 (t, 2H), 6,77 (d, 1H), 7,33 (dd, 1H), 7,50 (d, 1H) 5.62 пропил тетрагидропиранил-3 2–Cl, 4–Br 3,90 (m, 2H), 4,10 (t, 2H), 4,30 (t, 2H), 6,77 (d, 1H), 7,33 (dd, 1H), 7,50 (d, 1H) 5.63 этил тетрагидропиранил-4 2–Cl, 4–Br 73–74 5.64 пропил тетрагидропиранил-4 2–Сl, 4–Br 4,00 (m, 2H), 4,10 (t, 2H), 4,30 (t, 2H), 6,77 (d, 1H), 7,33 (dd, 1H), 7,50 (d, 1H) Продолжение табл. 5 1 2 3 4 5.65 этил тетрагидротиопиранил-3 2–Сl, 4–Br 4,10 (m, 2H), 4,30 (t, 2H), 6,77 (d, 1H), 7,33 (dd, 1H), 7,50 (d, 1H) 5.66 пропил тетрагидротиопиранил-3 2–Сl, 4–Br 4,10 (m, 2H), 4,30 (t, 2H), 6,77 (d, 1H), 7,33 (dd, 1H), 7,50 (d, 1H) 5.67 этил тетрагидропиранил-3 2–Br, 4–F 3,90 (m, 2H), 4,13 (t, 2H), 4,30 (t, 2H), 6,80–7,10 (m, 2H), 7,30 (m, 2H) 5.68 пропил тетрагидропиранил-3 2–Br, 4–F 3,90 (m, 2H), 4,13 (t, 2H), 4,30 (t, 2H), 6,80–7,10 (m, 2H), 7,30 (m, 2H) 5 5.69 этил тетрагидропиранил-4 2–Br, 4–F 4,00 (m, 2H), 4,13 (t, 2H), 4,30 (t, 2H), 6,80–7,10 (m, 2H), 7,30 (m, 2H) 5.70 пропил тетрагидропиранил-4 2–Br, 4–F 74–75 5.71 этил тетрагидротиопиранил-3 2–Br, 4–F 4,13 (t, 2H), 4,30 (t, 2H), 6,80–7,10 (m, 2H), 7,30 (m, 2H) 5.72 пропил тетрагидротиопиранил-3 2–Br, 4–F 4,13 (t, 2H), 4,30 (t, 2H), 6,80–7,10 (m, 2H), 7,30 (m, 2H) 5.73 этил тетрагидропиранил-3 2,4–F2 3,93 (m, 2H), 4,10 (t, 2H), 4,30 (t, 2H), 6,70–7,00 (m, 3H) 5.74 пропил тетрагидропиранил-3 2,4–F2 3,93 (m, 2H), 4,10 (t, 2H), 4,30 (t, 2H), 6,70–7,00 (m, 3H) 5.75 этил тетрагидропиранил-4 2,4–F2 4,00 (m, 2H), 4,10 (t, 2H), 4,30 (t, 2H), 6,70–7,00 (m, 3H) 5.76 пропил тетрагидропиранил-4 2,4–F2 4,00 (m, 2H), 4,10 (t, 2H), 4,30 (t, 2H), 6,70–7,00 (m, 3H) 5.77 этил тетрагидротиопиранил-3 2,4–F2 4,10 (t, 2H), 4,30 (t, 2H), 6,70–7,00 (m, 3H) 5.78 пропил тетрагидротиопиранил-3 2,4–F2 4,10 (t, 2H), 4,30 (t, 2H), 6,70–7,00 (m, 3H) 5.79 этил тетрагидропиранил-3 2–Br, 4–Cl 3,90 (m, 2H), 4,10 (t, 2H), 4,30 (t, 2H), 6,80 (d, 1H), 7,25 (dd, 1H), 7,55 (d, 1H) 5.80 пропил тетрагидропиранил-3 2–Br, 4–Cl 3,90 (m, 2H), 4,10 (t, 2H), 4,30 (t, 2H), 6,80 (d, 1H), 7,25 (dd, 1H), 7,55 (d, 1H) 5.81 этил тетрагидропиранил-4 2–Br, 4–Cl 4,00 (m, 2H), 4,10 (t, 2H), 4,30 (t, 2H), 6,80 (d, 1H), 7,25 (dd, 1H), 7,55 (d, 1H) 5.82 пропил тетрагидропиранил-4 2–Br, 4–Cl 4,00 (m, 2H), 4,10 (t, 2H), 4,30 (t, 2H), 6,80 (d, 1H), 7,25 (dd, 1H), 7,55 (d, 1H) 5.83 этил тетрагидротиопиранил-3 2–Br, 4–Cl 4,10 (t, 2H), 4,30 (t, 2H), 6,80 (d, 1H), 7,25 (dd, 1H), 7,55 (d, 1H) 5.84 пропил тетрагидротиопиранил-3 2–Br, 4–Cl 4,10 (t, 2H), 4,30 (t, 2H) 5.85 этил тетрагидропиранил-3 2–Cl, 4–F 3,93 (m, 2H), 4,10 (t, 2H), 4,30 (t, 2H), 6,90 (m, 2H), 7,15 (m, 1H) 5.86 пропил тетрагидропиранил-3 2–Cl, 4–F 3,93 (m, 2H), 4,10 (t, 2H), 4,30 (t, 2H), 6,90 (m, 2H), 7,15 (m, 1H) 5.87 этил тетрагидропиранил-4 2–Сl, 4–F 4,00 (m, 2H), 4,10 (t, 2H), 4,30 (t, 2H), 6,90 (m, 2H), 7,15 (m, 1H) 5.88 пропил тетрагидропиранил-4 2–Сl, 4–F 4,00 (m, 2H), 4,10 (t, 2H), 4,30 (t, 2H), 6,90 (m, 2H), 7,15 (m, 1H) 5.89 этил тетрагидротиопиранил-3 2–Cl, 4–F 4,10 (t, 2H), 4,30 (t, 2H), 6,90 (m, 2H), 7,15 (m, 1H) 5.90 пропил тетрагидротиопиранил-3 2–Cl, 4–F 4,10 (t, 2H), 4,30 (t, 2H), 6,90 (m, 2H), 7,15 (m, 1H) 5.91 этил 1-метилтиоциклопропил-1 4–F 2,13 (s, 3H), 6,90 (m, 2H), 7,00 (m, 2H) 5.92 пропил 1-метилтиоциклопропил-1 4–F 2,13 (s, 3H), 6,90 (m, 2H), 7,00 (m, 2H) Таблица 6 OH Xn NO–CH2 CH2 CH 2CH 2–O R2 R1 O I (A = –CH 2CH2CH2CH2–O–; z – фе нил) № R1 R2 Xn 6.07 этил тетрагидропиран-3-ил 4–F 6.08 пропил тетрагидропиран-3-ил 4–F 6.09 этил тетрагидропиран-4-ил 4–F 6.10 пропил тетрагидропиран-4-ил 4–F 6.11 6.12 6.13 6.14 6.15 6.16 6.17 6.18 6.43 этил пропил этил пропил этил пропил этил пропил этил тетрагидротиопиран-3-ил тетрагидротиопиран-3-ил тетрагидропиран-3-ил тетрагидропиран-3-ил тетрагидропиран-4-ил тетрагидропиран-4-ил тетрагидротиопиран-3-ил тетрагидротиопиран-3-ил 1-метилтиоциклопропил-1 4–F 4–F 4–Cl 4–Cl 4–Cl 4–Cl 4–Cl 4–Cl 4–F 6.44 пропил 1-метилтиоциклопропил-1 4–F Физические данные [ 1H–ЯМР (частей/миллион); Т.пл., оС] 3,90 (m, 2H); 4,17 (t, 2H); 7,00 (t, 2H); (m, 2H) 3,90 (m, 2H); 4,17 (t, 2H); 7,00 (t, 2H); (m, 2H) 4,00 (m, 2H); 4,17 (t, 2H); 7,00 (t, 2H); (m, 2H) 4,00 (m, 2H); 4,17 (t, 2H); 7,00 (t, 2H); (m, 2H) 4,17 (t, 2H); 7,00 (t, 2H); 7,33 (m, 2H) 4,17 (t, 2H); 7,00 (t, 2H); 7,33 (m, 2H) 3,90 (m, 2H); 4,17 (t, 2H); 7,27 (s, 4H) 3,90 (m, 2H); 4,17 (t, 2H); 7,27 (s, 4H) 4,00 (m, 2H); 4,17 (t, 2H); 7,27 (s, 4H) 4,00 (m, 2H); 4,17 (t, 2H); 7,27 (s, 4H) 4,17 (t, 2H); 7,27 (s, 4H) 4,17 (t, 2H); 7,27 (s, 4H) 2,12 (s, 3H); 4,17 (t, 2H); 7,00 (m, 2H); (m, 2H) 2,12 (s, 3H); 4,17 (t, 2H); 7,00 (m, 2H); (m, 2H) 7,33 7,33 7,33 7,33 7,37 7,37 Таблица 7 OH Xn NO–CH2 CH2 OCH2 R2 R1 O I (A = –CH 2CH2–O–CH2–; z – фе нил) № R1 R2 Xn Физические данные [ 1H–ЯМР (частей/миллион); Т.пл., оС] 1 2 3 4 5 7.07 этил тетрагидропиран-3-ил 2–F 3,93 (m, 2H); 4,27 (m, 2H); 4,67 (s, 2H); 6,93–7,50 (m, 4H) 7.08 пропил тетрагидропиран-3-ил 2–F 3,93 (m, 2H); 4,27 (m, 2H); 4,67 (s, 2H); 6,93–7,50 (m, 4H) 7.09 этил тетрагидропиран-4-ил 2–F 4,03 (m, 2H); 4,27 (m, 2H); 4,63 (s, 2H); 6,97–7,50 (m, 4H) 7.10 пропил тетрагидропиран-4-ил 2–F 4,03 (m, 2H); 4,27 (m, 2H); 4,63 (s, 2H); 6,97–7,50 (m, 4H) 7.11 этил тетрагидротиопиран-3-ил 2–F 4,27 (m, 2H); 4,67 (s, 2H); 6,97–7,50 (m, 4H) 7.12 пропил тетрагидротиопиран-3-ил 2–F 4,27 (m, 2H); 4,67 (s, 2H); 6,97–7,50 (m, 4H) 7.13 этил тетрагидропиран-3-ил 3–F 3,93 (m, 2H); 4,27 (m, 2H); 4,57 (s, 2H); 6,90–7,15 (m, 3H); 7,23–7,40 (m, 1H) Продолжение табл. 7 1 2 3 4 7.14 пропил тетрагидропиран-3-ил 3–F 3,93 (m, 2H); 4,27 (m, 2H); 4,57 (s, 2H); 6,90– 7,15 (m, 3H); 7,23–7,40 (m, 1H) 7.15 этил тетрагидропиран-4-ил 3–F 4,03 (m, 2H); 4,25 (m, 2H); 4,60 (s, 2H); 6,90– 7,18 (m, 3H); 7,26–7,40 (m, 1H) 7.16 пропил тетрагидропиран-4-ил 3–F 4,03 (m, 2H); 4,25 (m, 2H); 4,60 (s, 2H); 6,90– 7,18 (m, 3H); 7,26–7,40 (m, 1H) 7.17 этил тетрагидротиопиран-3-ил 3–F 4,27 (m, 2H); 4,60 (s, 2H); 6,90–7,15 (m, 3H); 5 7,23–7,40 (m, 1H) 7.18 пропил тетрагидротиопиран-3-ил 3–F 4,27 (m, 2H); 4,60 (s, 2H); 6,90–7,15 (m, 3H); 7,23–7,40 (m, 1H) 7.19 этил тетрагидропиран-3- ил 4–F 3,93 (m, 2H); 4,23 (m, 2H); 4,53 (s, 2H); 7,00 (m, 2H); 7,30 (m, 2H) 7.20 пропил тетрагидропиран-3- ил 4–F 3,93 (m, 2H); 4,23 (m, 2H); 4,53 (s, 2H); 7,00 (m, 2H); 7,30 (m, 2H) 7.21 этил тетрагидропиран-4-ил 4–F 92 7.22 пропил тетрагидропиран-4-ил 4–F 4,00 (m, 2H); 4,23 (m, 2H); 4,53 (s, 2H); 7,03 (m, 2H); 7,30 (m, 2H) 7.23 этил тетрагидротиопиран-3-ил 4–F 4,27 (m, 2H); 4,53 (s, 2H); 7,03 (m, 2H); 7,30 (m, 2H) 7.24 пропил тетрагидротиопиран-3-ил 4–F 4,27 (m, 2H); 4,53 (s, 2H); 7,03 (m, 2H); 7,30 (m, 2H) 7.25 этил тетрагидропиран-3-ил 2–Cl 7.26 пропил тетрагидропиран-3-ил 2–Cl 7.27 этил тетрагидропиран-4-ил 2–Cl 7.28 пропил тетрагидропиран-4-ил 2–Cl 7.29 этил тетрагидротиопиран-3-ил 2–Cl 7.30 пропил тетрагидротиопиран-3-ил 2–Cl 7.31 этил тетрагидропиран-3-ил 3–Cl 7.32 пропил тетрагидропиран-3-ил 3–Cl 7.33 этил тетрагидропиран-4-ил 3–Cl 7.34 пропил тетрагидропиран-4-ил 3–Cl 7.35 этил тетрагидротиопиран-3-ил 3–Cl 7.36 пропил тетрагидротиопиран-3-ил 3–Cl 7.37 этил тетрагидропиран-3-ил 4–Сl 3,93 (m, 2H); 4,27 (m, 2H); 4,53 (s, 2H); 7,28 (m, 4H) 7.38 пропил тетрагидропиран-3-ил 4–Сl 3,93 (m, 2H); 4,27 (m, 2H); 4,53 (s, 2H); 7,28 (m, 4H) 7.39 этил тетрагидропиран-4-ил 4–Сl 67–72 7.40 пропил тетрагидропиран-4-ил 4–Cl 4,00 (m, 2H); 4,23 (m, 2H); 4,53 (s, 2H); 7,28 (m, 4H) 7.41 этил тетрагидротиопиран-3-ил 4–Cl 4,27 (m, 2H); 4,53 (s, 2H); 7,28 (m, 4H) 7.42 пропил тетрагидротиопиран-3-ил 4–Cl 4,27 (m, 2H); 4,53 (s, 2H); 7,28 (m, 4H) 7.52 пропил тетрагидропиран-4-ил 3–СН3 4,00 (m, 2H); 4,27 (m, 2H); 4,57 (s, 2H); 7,00– 7,32 (m, 4H) 7.54 пропил тетрагидротиопиран-3-ил 3–СН3 4,27 (m, 2H); 4,60 (s, 2H); 7,00–7,32 (m, 4H) 7.77 этил 1-метилтиоциклопропил-1 2–F 2,12 (s, 3H); 7,00–7,50 (m, 4H) 7.78 пропил 1-метилтиоциклопропил-1 2–F 2,10 (s, 3H); 6,98–7,50 (m, 4H) Таблица 8 OH Xn NO–CH2 CH2SCH2 R2 R1 O I (A = –CH 2CH2–S–CH2–; z – фе нил) № R1 R2 Xn Физические данные [ 1H–ЯМР (частей на миллион); Т. пл., оС] 8.07 этил тетрагидропиран-3-ил 4–F 3,72 (s, 2H); 3,90 (m, 2H); 4,13 (t, 2H); 7,00 (m, 2H); 7,30 (m, 2H) 8.08 пропил тетрагидропиран-3-ил 4–F 3,72 (s, 2H); 3,90 (m, 2H); 4,13 (t, 2H); 7,00 (m, 2H); 7,30 (m, 2H) 8.09 этил тетрагидропиран-4-ил 4–F 63–65 8.10 пропил тетрагидропиран-4-ил 4–F 3,73 (s, 2H); 4,00 (m, 2H); 4,13 (t, 2H); 7,00 (m, 2H); 7,30 (m, 2H) 8.11 этил тетрагидротиопиран-3-ил 4–F 3,75 (s, 2H); 4,13 (t, 2H); 7,00 (m, 2H); 7,30 (m, 2H) 8.12 пропил тетрагидротиопиран-3-ил 4–F 3,75 (s, 2H); 4,13 (t, 2H); 7,00 (m, 2H); 7,30 (m, 2H) 8.13 этил тетрагидропиран-3-ил 4–F 3,77 (s, 2H); 3,93 (m, 2H); 4,13 (t, 2H); 7,30 (s, 4H) 8.14 пропил тетрагидропиран-3-ил 4– Cl 3,77 (s, 2H); 3,93 (m, 2H); 4,13 (t, 2H); 7,30 (s, 4H) 8.15 этил тетрагидропиран-4-ил 4–Cl 3,73 (s, 2H); 4,00 (m, 2H); 4,17 (t, 2H); 7,30 (s, 4H) 8.16 пропил тетрагидропиран-4-ил 4–Cl 3,73 (s, 2H); 4,00 (m, 2H); 4,17 (t, 2H); 7,30 (s, 4H) 8.17 этил тетрагидротиопиран-3-ил 4–Cl 3,73 (s, 2H); 4,13 (m, 2H); 7,30 (s, 4H) 8.18 пропил тетрагидротиопиран-3-ил 4–Cl 3,73 (s, 2H); 4,13 (m, 2H); 7,30 (s, 4H) 8.19 этил 1-метилтиоциклопропил-1 4–F 2,13 (s, 3H); 7,00 (m, 2H); 7,30 (m, 2H) 8.20 пропил 1-метилтиоциклопропил-1 4–F 2,10 (s, 3H); 7,00 (m, 2H); 7,30 (m, 2H) Таблица 9 OH Xn NO–CH2 CH 2CH 2CH2–O I R2 R1 O (А = –CH 2–CH2–CH2–CH2–O–; z – фе нил) № R1 R2 Xn Физические данные [ 1H–ЯМР (частей на миллион); Т. пл., оС] 1 2 3 4 5 9.05 этил тетрагидротиопиран-3-ил – 9.07 этил тетрагидропиран-3-ил 2–F 3,93 (m, 2H); 4,00–4,20 (m, 4H); 6,80–7,15 (m, 4H) 9.08 пропил тетрагидропиран-3-ил 2–F 3,93 (m, 2H); 4,00–4,20 (m, 4H); 6,80–7,15 (m, 4H) 9.09 этил тетрагидропиран-4-ил 2–F 68–72 9.10 пропил тетрагидропиран-4-ил 2–F 3,90–4,20 (m, 6H); 6,80–7,15 (m, 4H) 9.11 этил тетрагидротиопиран-3-ил 2–F 4,00–4,20 (m, 4H); 6,80–7,15 (m, 4H) 9.12 пропил тетрагидротиопиран-3-ил 2–F 4,00–4,20 (m, 4H); 6,80–7,15 (m, 4H) 9.13 этил тетрагидропиран-3-ил 3–F 9.14 пропил тетрагидропиран-3-ил 3–F Продолжение табл. 9 1 2 3 4 9.15 этил тетрагидропиран-4-ил 3–F 9.16 пропил тетрагидропиран-4-ил 3–F 9.17 этил тетрагидротиопиран-3-ил 3–F 9.18 пропил тетрагидротиопиран-3-ил 3–F 9.19 этил тетрагидропиран-3-ил 4–F 5 3,80–4,20 (m, 6H); 6,75–7,05 (m, 4H) 9.20 пропил тетрагидропиран-3-ил 4–F 3,80–4,20 (m, 6H); 6,75–7,05 (m, 4H) 9.21 этил тетрагидропиран-4-ил 4–F 3,90–4,20 (m, 6H); 6,75–7,05 (m, 4H) 9.22 пропил тетрагидропиран-4-ил 4–F 3,90–4,20 (m, 6H); 6,75–7,05 (m, 4H) 9.23 этил тетрагидротиопиран-3-ил 4–F 3,90–4,20 (m, 4H); 6,75–7,05 (m, 4H) 9.24 пропил тетрагидротиопиран-3-ил 4–F 3,90–4,20 (m, 4H); 6,75–7,05 (m, 4H) 9.25 этил тетрагидропиран-3-ил 4–Cl 3,80–4,20 (m, 6H); 6,80 (m, 2H); 7,20 (m, 2H) 9.26 пропил тетрагидропиран-3-ил 4–Cl 3,80–4,20 (m, 6H); 6,80 (m, 2H); 7,20 (m, 2H) 9.27 этил тетрагидропиран-4-ил 4–Сl 3,90–4,20 (m, 6H); 6,80 (m, 2H); 7,20 (m, 2H) 9.28 пропил тетрагидропиран-4-ил 4–Сl 3,90–4,20 (m, 6H); 6,80 (m, 2H); 7,20 (m, 2H) 9.29 этил тетрагидротиопиран-3-ил 4–Сl 3,90–4,20 (m, 4H); 6,80 (m, 2H); 7,20 (m, 2H) 9.30 пропил тетрагидротиопиран-3-ил 4–Сl 3,90–4,20 (m, 4H); 6,80 (m, 2H); 7,20 (m, 2H) 9.31 этил тетрагидропиран-3-ил 2,6–Сl2 3,93 (m, 2H); 4,00–4,25 (m, 4H); 7,00 (t, 1H); 7,30 (d, 2H) 9.32 пропил тетрагидропиран-3-ил 2,6–Сl2 3,93 (m, 2H); 4,00–4,25 (m, 4H); 7,00 (t, 1H); 7,30 (d, 2H) 9.33 этил тетрагидропиран-4-ил 2,6–Cl2 3,90–4,25 (m, 6H); 7,00 (t, 1H); 7,30 (d, 2H) 9.34 пропил тетрагидропиран-4-ил 2,6–Cl2 3,90–4,25 (m, 6H); 7,00 (t, 1H); 7,30 (d, 2H) 9.35 этил тетрагидротиопиран-3-ил 2,6–Сl2 4,00–4,20 (m, 4H); 7,00 (t, 1H); 7,30 (d, 2H) 9.36 пропил тетрагидротиопиран-3-ил 2,6– Сl2 4,00–4,20 (m, 4H); 7,00 (t, 1H); 7,30 (d, 2H) 9.37 этил 1-метилтиоциклопропил-1 4–F 2,10 (s, 3H); 6,83 (m, 2H); 6,97 (m, 2H) 9.38 пропил 1-метилтиоциклопропил-1 4–F 2,13 (s, 3H); 6,83 (m, 2H); 7,00 (m, 2H) 9.39 этил 1-метилтиоциклопропил-1 4– Cl 2,10 (s, 3H); 6,80 (m, 2H); 7,25 (m, 2H) 9.40 пропил 1-метилтиоциклопропил-1 4– Cl 2,10 (s, 3H); 6,83 (m, 2H); 7,23 (m, 2H) Таблица 10 OH Xn NO–CH2 CH 2–O–CH 2CH2 I R2 R 1 O (А = –CH 2–CH2–O–CH2–CH2–; z – фе нил) № R1 R2 Xn Физические данные [ 1H–ЯМР (частей на миллион); Т. пл., оС] 1 2 3 4 5 10.07 этил тетрагидропиран-3-ил 4–F 3,90 (m, 2H); 4,17 (m, 2H); 6,93 (m, 2H); 7,13 (m, 2H) 10.08 пропил тетрагидропиран-3-ил 4–F 3,90 (m, 2H); 4,17 (m, 2H); 6,93 (m, 2H); 7,13 (m, 2H) 10.09 этил тетрагидропиран-4-ил 4–F 10.10 пропил тетрагидропиран-4-ил 4–F Продолжение табл. 10 1 2 3 4 5 10.11 этил тетрагидротиопиран-3-ил 4–F 4,17 (m, 2H); 6,93 (m, 2H); 7,13 (m, 2H) 10.12 пропил тетрагидротиопиран-3-ил 4–F 4,17 (m, 2H); 6,93 (m, 2H); 7,13 (m, 2H) 10.13 этил тетрагидропиран-3-ил 4–Cl 3,90 (m, 2H); 4,17 (m, 2H); 7,13 (m, 4H) 10.14 пропил тетрагидропиран-3-ил 4–Cl 3,90 (m, 2H); 4,17 (m, 2H); 7,13 (m, 4H) 10.15 этил тетрагидропиран-4-ил 4–Cl 10.16 пропил тетрагидропиран-4-ил 4–Cl 10.17 этил тетрагидротиопиран-3-ил 4–Cl 4,17 (m, 2H); 7,13 (m, 4H) 10.18 пропил тетрагидротиопиран-3-ил 4–Сl 4,17 (m, 2H); 7,13 (m, 4H) Таблица 11 OH Xn NO–CH2 CH 2CH 2CH2CH2–O I R2 R1 O (А = –CH 2(CH2)3CH2–О–; z – фенил) № R1 R2 Xn 11.07 этил тетрагидропиран-3-ил 4–F 3,90 (m, 4H); 4,03 (t, 2H); 6,70–7,03 (m, 4H) 11.08 пропил тетрагидропиран-3-ил 4–F 3,90 (m, 4H); 4,03 (t, 2H); 6,70–7,03 (m, 4H) 11.09 этил тетрагидропиран-4-ил 4–F 3,83–4,13 (m, 6H); 6,70–7,03 (m, 4H) 11.10 пропил тетрагидропиран-4-ил 4–F 3,83–4,13 (m, 6H); 6,70–7,03 (m, 4H) 11.11 этил тетрагидротиопиран-3-ил 4–F 3,90 (t, 2H); 4,03 (t, 2H); 6,70–7,03 (m, 4H) 11.12 пропил тетрагидротиопиран-3-ил 4–F 3,90 (t, 2H); 4,03 (t, 2H); 6,70–7,03 (m, 4H) 11.13 этил тетрагидропиран-3-ил 4–Cl 3,80–4,10 (m, 6H); 6,80 (d, 2H); 7,20 (d, 2H) 11.14 пропил тетрагидропиран-3-ил 4–Cl 3,80–4,10 (m, 6H); 6,80 (d, 2H); 7,20 (d, 2H) 11.15 этил тетрагидропиран-4-ил 4–Cl 3,87–4,10 (m, 6H); 6,80 (d, 2H); 7,20 (d, 2H) 11.16 пропил тетрагидропиран-4-ил 4–Cl 3,87–4,10 (m, 6H); 6,80 (d, 2H); 7,20 (d, 2H) 11.17 этил тетрагидротиопиран-4-ил 4–Сl 54–61 11.18 пропил тетрагидротиопиран-3-ил 4–Сl 3,90 (t, 2H); 4,07 (t, 2H); 6,80 (d, 2H); 7,20 (d, 2H) 11.19 этил 1-метилтиоциклопропил-1 4–F 2,13 (s, 3H); 6,85 (m, 2H); 6,97 (m, 2H) 11.20 пропил 1-метилтиоциклопропил-1 4–F 2,13 (s, 3H); 6,85 (m, 2H); 7,00 (m, 2H) 11.21 этил 1-метилтиоциклопропил-1 4– Cl 2,10 (s, 3H); 6,80 (m, 2H); 7,23 (m, 2H) 11.22 пропил 1-метилтиоциклопропил-1 4– Cl 2,10 (s, 3H); 6,80 (m, 2H); 7,20 (m, 2H) Физические данные [ 1H–ЯМР (частей / миллион); Т. пл., оС] Таблица 12 OH Xn NO–CH2CHO R2 R1 CH2CH3 O I (А = –CH2CH–О–; Z = фенил) ½ СН2СН3 № R1 R2 Xn 12.01 этил тетрагидропирaнил-4 4–Сl 4,00 (m, 2H); 4,23 (m, 2H); 4,40 (m, 1H); 6,85 (m, 2H); 7,25 (m, 2H) 12.02 пропил тетрагидротиопирaнил-3 4–Сl 4,23 (m, 2H); 4,40 (m, 1H); 6,85 (m, 2H); 7,25 (m, 2H) Физические данные [ 1H–ЯМР (частей / миллионов); Т. пл., оС] Таблица 13 CH3 O Xn NO–CH–CH–O R2 R 1 CH3 O CH3 | I (А = CH–СН–О–; z – фенил) | СН3 № R1 R2 Xn 13.01 этил тетрагидропиранил-4 4–Сl 4,00 (m, 2H); 4,30 (m, 1H); 4,45 (m, 1H); 6,85 (m, 2H); 7,25 (m, 2H) 13.02 пропил тетрагидротиопиранил-3 4–Сl 4,30 (m, 1H); 4,45 (m, 1H); 6,85 (m, 2H); 7,28 (m, 2H) Физические данные [ 1H–ЯМР (частей / миллион); Т. пл., оС] Таблица 14 OH Xn NO–CHCH 2–O R2 I R 1 CH3 O (А = –СН –СН2О–; z – фенил) СН3 | № R1 R2 Xn Физические данные [1H–ЯМР (частей / миллион); Т. пл., оС] 1 2 3 4 5 14.01 этил тетрагидропиранил-4 4–F 4,00 (m, 4H); 4,55 (m, 1H); 6,75–7,10 (m, 4H) 14.02 этил тетрагидротиопиранил-3 4–F 4,00 (m, 4H); 4,55 (m, 1H); 6,75–7,10 (m, 4H) 14.03 пропил тетрагидротиопиранил-3 4–F 4,00 (m, 4H); 4,55 (m, 1H); 6,75–7,10 (m, 4H) Продолжение табл. 14 1 2 3 4 5 14.04 этил тетрагидропиранил-3 4–Cl 3,95 (m, 4H); 4,53 (m, 1H); 6,85 (m, 2H); 7,25 (m, 2H) 14.05 пропил тетрагидропиранил-3 4–Cl 3,95 (m, 4H); 4,53 (m, 1H); 6,85 (m, 2H); 7,25 (m, 2H) 14.06 этил тетрагидропиранил-4 4–Cl 4,00 (m, 4H); 4,53 (m, 1H); 6,85 (m, 2H); 7,25 (m, 2H) 14.07 пропил тетрагидропиранил-4 4–Cl 4,00 (m, 4H); 4,53 (m, 1H); 6,85 (m, 2H); 7,25 (m, 2H) 14.08 этил тетрагидротиопиранил-4 4–Cl 4,00 (m, 4H); 4,53 (m, 1H); 6,85 (m, 2H); 7,25 (m, 2H) 14.09 пропил тетрагидротиопиранил-4 4–Cl 4,00 (m, 4H); 4,53 (m, 1H); 6,85 (m, 2H); 7,25 (m, 2H) 14.10 этил тетрагидротиопиранил-3 2–Сl 4,15 (m, 2H); 4,57 (m, 1H); 6,90 (m, 2H); 7,20 (m, 1H); 7,35 (m, 1H) 14.11 пропил тетрагидротиопиранил-3 2–Сl 4,15 (m, 2H); 4,57 (m, 1H); 6,90 (m, 2H); 7,20 (m, 1H); 7,35 (m, 1H) 14.12 этил тетрагидропиранил-3 2,4–Сl2 3,93 (m, 1H); 4,60 (m, 1H); 6,90 (d, 1H); 7,20 (dd, 1H); 7,40 (d, 1H) 14.13 этил тетрагидропиранил-4 2,4–Сl2 4,60 (m, 1H); 6,90 (d, 1H); 7,20 (dd, 1H); 7,40 (d, 1H) 14.14 пропил тетрагидропиранил-4 2,4–Сl2 4,60 (m, 1H); 6,90 (d, 1H); 7,20 (dd, 1H); 7,40 (d, 1H) 14.15 этил тетрагидротиопиранил-3 2,4–Сl2 4,60 (m, 1H); 6,90 (d, 1H); 7,20 (dd, 1H); 7,40 (d, 1H) Таблица 15 Нормы расхода 0,5 кг активного ве щества на 1 га; послевсхо довая обработка Соединение Поражение Echinochloa в % 1 2 2.08 85 2.11 90 2.17 75 2.18 75 2.19 85 2.23 98 2.69 75 2.70 65 2.73 80 2.74 85 2.77 90 2.78 90 5.05 70 5.44 70 5.47 80 5.48 90 7.16 65 7.41 85 9.19 90 Продолжение табл. 15 1 2 9.20 90 9.21 80 9.23 80 9.24 90 9.25 70 9.26 80 9.28 75 9.29 98 9.30 80 10.01 90 10.02 85 10.05 70 10.06 95 10.08 95 Таблица 16 Норма расхода 0,5 кг активного ве щества на 1 га; предвсхо довая обработка Соединение Поражение Echinochloa в % 2.03 70 2.26 80 2.30 75 6.31 70 6.32 70 7.07 65 7.11 65 7.12 85 7.15 65 7.20 65 7.38 65 7.42 65 7.52 75 7.54 70 10.12 98 Таблица 17 Норма расхода 0,5 кг активного ве щества на 1 га; предвсхо довая обработка Соединение Поражение Lolium multiflorum в % 1 2 2.14 80 2.17 85 2.73 100 2.74 100 5.15 80 5.24 98 Продолжение табл. 17 1 2 5.31 95 5.33 95 9.05 90 9.08 70 9.19 100 9.23 100 Таблица 18 Норма расхода 0,5 кг активного ве щества на 1 га; предвсхо довая обработка Соединение Испытуемые соединения и поражение в % Echinochloa Lolium multiflorum 2.04 70 100 2.07 100 100 2.09 100 100 2.10 100 100 2.12 95 100 2.13 98 100 2.15 100 100 2.16 85 95 2.19 75 100 2.20 75 100 2.21 75 98 2.23 85 100 2.24 90 100 2.37 90 100 2.38 95 100 2.39 95 100 2.40 98 100 2.41 98 100 2.42 100 100 2.61 100 100 2.62 100 98 2.63 98 100 2.64 100 100 2.65 95 100 2.66 90 100 2.75 95 100 2.76 75 95 3.15 100 100 3.16 100 100 3.17 80 95 3.18 95 98 4.13 85 100 4.14 95 Соединение 95 Продолжение табл. 18 Испытуемые соединения и поражение в % Echinochloa Lolium multiflorum 4.15 90 75 5.01 70 70 5.02 75 90 5.03 90 100 5.04 98 98 5.19 98 90 5.20 95 90 5.21 100 95 5.22 98 100 5.37 100 100 5.38 95 100 5.39 100 100 5.40 100 100 5.41 100 100 5.42 100 100 5.49 98 80 5.50 98 70 5.51 98 98 5.52 100 98 6.16 90 75 7.08 75 65 7.09 75 75 7.10 95 70 7.19 90 80 7.21 90 90 7.22 70 95 7.23 70 75 7.39 75 98 7.40 75 70 9.02 85 98 9.04 90 98 9.20 85 100 9.21 70 100 9.22 98 100 9.24 80 100 10.07 100 90 Таблица 19 Норма расхода 0,5 кг активного ве щества на 1 га; послевсхо довая обработка Cоединение Испытуемые соединения и поражение в % Bromus spp. Echinochloa 2.21 90 85 2.39 100 Cоединение 100 Продолжение табл. 19 Испытуемые соединения и поражение в % Bromus spp. Echinochloa 2.40 100 100 2.41 85 100 2.42 90 100 3.15 100 100 3.16 100 100 3.17 95 100 3.18 100 100 5.19 98 100 5.20 98 98 5.21 95 100 5.22 98 98 5.23 100 100 5.24 90 98 5.37 95 98 5.38 100 100 5.39 100 100 5.40 100 100 5.41 100 100 5.42 100 100 5.49 80 100 5.50 70 100 5.51 95 100 5.52 95 100 5.53 70 100 5.54 75 100 Таблица 20 1 Пример № R R 2.39 СН2СН2О–(4–Cl–C6H4) СН2СН3 A (пр. 30 на ЕР–А 218,233) СН2СН2ОСН3 СН2СН3 В (пр. 29 из ЕР–А 218,233) СН2ОСН3 СН2СН3 С (пр. 36 из ЕР–А 218,233) СН2СН2ОСН3 СН2СН2СН3 D (пр. 35 из ЕР–А 218,233 СН2ОСН3 СН2СН2СН3 Таблица 21 Сравнение результатов, полученных при опытах в теплицах при обработке после появления всхо дов и при норме расхо да от 0,03 до 0,06 кг/га активного вещества Соединение Кол-во, кг/га Повреж дение (%) ORYSA ALOMY DIGSA ECHCG SETIT 2.39 0,03 26 90 94 73 95 2.39 0,06 38 93 97 98 98 A 0,03 55 70 80 55 50 A 0,06 65 94 95 92 92 B 0,03 20 0 0 0 10 B 0,06 20 0 15 42 25 Таблица 22 Сравнение результатов, полученных при опытах в теплицах при обработке после появления всхо дов и при норме расхо да 0,03 до 0,06 кг/га активного ве щества Соединение Кол-во, кг/га Повреж дение (%) ORYSA ALOMY DIGSA ECHCG SETIT 2.39 0,03 11 80 78 70 91 2.39 0,06 18 91 93 98 100 С 0,03 55 75 80 70 50 С 0,06 65 87 92 92 86 D 0,03 10 0 0 0 10 D 0,06 20 25 20 10 50 Таблица 23 Латинское название Русское название Код Alopecurus myosuroides Лисохвост полевой ALOMY Digitaria sanguinalis DIGSA Echinochloa crus-galli Ежовник ECHCG Setaria italica Щетинник итальянский SETIT Oryza sativa Рис ORYSA Таблица 24 Гербицидная активность при обработке после появления всхо дов и при 0,5 кг/га активного ве щества в теплице № примера Повреж дение (%) ECHCG BROSS 3.20 100 50 5.92 98 5 9.40 85 0 9.38 98 55 11.20 30 0 7.77 85 0 9.39 85 10 9.37 90 30 3.22 30 20 3.21 95 20 3.27 100 75 3.28 100 60 3.25 100 98 3.26 100 70 3.23 100 60 3.24 100 20 6.44 40 0 BROSS – Bromus spp. (ви ды) ECHCG – Echinochloa crus-galli (ежовник) Таблица 25 Гербицидная активность при обработке после появления всхо дов и при 0,25 кг/га активного ве щества в теплице № примера Повреж дение (%) ECHCG SEFTA 5.91 99 100 3.19 99 99 SEFTA – Setaria faberii (ще тинник) Таблица 26 Соединение № Испытанные растения и повреждение (%) Озимая пшеница Digitaria sanguinalis Echinochloa crus-galli 12.01 0 90 30 12.02 10 90 75 13.01 0 90 60 13.02 0 85 85 Ботаническое название (латинское) Русское название 1 2 1. Allium cepa 1. Лук репчатый 2. Ananas comosus 2. Aна нас 3. Arachis hypogaea 3. Земляной орех 4. Asparagus officinalis 4. Овес 5. Avena sativa 5. Спаржа 6. Beta vulgaris spp. altissima 6. Са харная свекла 7. Beta vulgaris spp. rapa 7. Кормовая свекла 8. Beta vulgaris spp. esculenta 8. Красная свекла 9. Brassica napus var. napus 9. Ра пс 10. Brassica napus var. napobrassica 10. Брюква 11. Brassica napus var. rapa 11. Белая свекла 12. Brassica napa var. silvestris 12. Редис 13. Camellia sinensis 13. Чай 14. Carthamus tinctorius 14. Серпуха неколючая 15. Carya illinoinensis 15. Древесный пекановый орех 16. Citras limon 16. Лимон 17. Citrus maxima 17. Пампельмус 18. Citrus reticulata 18. Мандарины 19. Citrus sinensis 19. Апельсины 20. Coffea arabica (Coffea canephora, Coffea liberia) 20. Кофе 21. Cucumis melo 21. Дыня 22. Cucumis sativus 22. Огурцы 23. Cynodon dactilon 23. Бермудская трава 24. Daucus carota 24. Морковь 25. Elaeis guineensis 25. Масляная пальма 1 2 26. Fragaris vesea 26. Земляника 27. Glycine max 27. Соевые бобы 28. Gossypium hirsutum (Gossypium arboreum, (Gossypium herbaceum, Gossypium vitifolium) 28. Хлопчатник 29. Heliantus annuus 29. Подсолнечник 30. Helianthus tuberosus 30. Топинамбур 31. Hevea brasiliensis 31. Каучуковое дерево 32. Hordeum vulgare 32. Ячмень 33. Humulus lapulus 33. Хмель 34. Ipomoea batatas 34. Сладкий картофе ль 35. Juglans regia 35. Орех 36. Lactuca sativa 36. Кочанный салат 37. Lens culinaris 37. Чечевица 38. Linum usitatissimum 38. Лен 39. Lycopersicon 39. Томаты 40. Malus spp. 40. Яблоки 41. Manihot esculenta 41. Маниок 42. Medicago sativa 42. Люцерна 43. Mentha piperita 43. Перец 44. Musa spp. 44. Бананы 45. Nicotiana tabacum (N. rustica) 45. Табак 46. Olea europaca 46. Масляное дерево 47. Oryza sativa 47. Рис 48. Panicum miliaceum 48. Конопля 49. Phaseolus lunatus 49. Фа соль 50. Phaseolus mungo 50. Арахис 51. Phaseolus vulgaris 51. Фасоль кусто вая 52. Pennisetum glaucum 52. Щeтинник итальянский 53. Petroselinum crispum spp. tuberosum 53. Петрушка 54. Picea abies 54. Сосна 55. Abies alba 55. Голубая ель 56. Pinus spp. 56. Клевер 57. Pisum sativum 57. Цветной горошек 58. Prunus avium 58. Вишня 59. Prunus domestica 59. Слива 60. Prunus dulus 60. Миндаль 61. Prunus dulcis 61. Персики 62. Pyrus communis 62. Груша 63. Ribes sylvestra 63. Крыжовник 64. Ribes uva-crispa 64. Смо родина 65. Ricinus communis 65. Клеще вина 66. Saccharum officinarum 66. Сахар ный тростник 67. Secale cereale 67. Рожь 68. Sesamum indicum 68. Кунжут 69. Solanum tuberosum 69. Картофе ль 70. Sorghum bicolor (s. vulgare) 70. Сорго 1 2 71. Sorghum dochna 71. Сорго сахар ное 72. Spinacia oleracea 72. Шпинат 73. Theobroma cacao 73. Какао 74. Trifolium pratense 74. Клевер луговой 75. Triticum aestivum 75. Пше ница 76. Triticum durum 76. Твердая пшеница 77. Vaccinium corymbosum 77. Черника 78. Vaccinium corymbosum 78. Брусника 79. Vicia faba 79. Бобы конские 80. Vigna sinensis (V. unguiculata) 80. Вигна 81. Vitis vinifera 81. Виноградная лоза 82. Zea Ma ys 82. Кукуруза
ДивитисяДодаткова інформація
Назва патенту англійськоюCyclohexenone oxime ethers and herbicidal agent
Автори англійськоюMisslotz Ulf, Meier Norbert, Kast Jurgen, Goetz Norbert, Harreus Albrecht, Wurtzer Bruno, Walter Helmut, Westfalen Karl-Otto, Gerber Matthias
Назва патенту російськоюЭфиры циклогексаноноксимов и гербицидное средство
Автори російськоюМисслиц Ульф, Мейер Норберт, Каст Юрген, Гетц Норберт, Харреус Альбрехт, Вюрцер Бруно, Вальтер Хельмут, Вестфален Карль-Отто, Гербер Маттиас
МПК / Мітки
МПК: A01N 35/10
Мітки: ефіри, циклогексеноноксимів, засіб, гербіцидний
Код посилання
<a href="https://ua.patents.su/31-34414-efiri-ciklogeksenonoksimiv-ta-gerbicidnijj-zasib.html" target="_blank" rel="follow" title="База патентів України">Ефіри циклогексеноноксимів та гербіцидний засіб</a>