Застосування гетероциклічних бензопохідних сульфаміду для лікування тривожних розладів
Формула / Реферат
1. Спосіб лікування тривожного розладу або спорідненого патологічного розладу, який відрізняється тим, що потребуючому цього суб’єкту вводять терапевтично ефективну кількість сполуки формули (I)
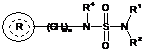 , (I)
, (I)
де
R1 і R2 кожний незалежно вибирають із групи, що складається з водню й нижчого алкілу;
R4 вибирають із групи, що складається з водню й нижчого алкілу;
a - це ціле число від 1 до 2;
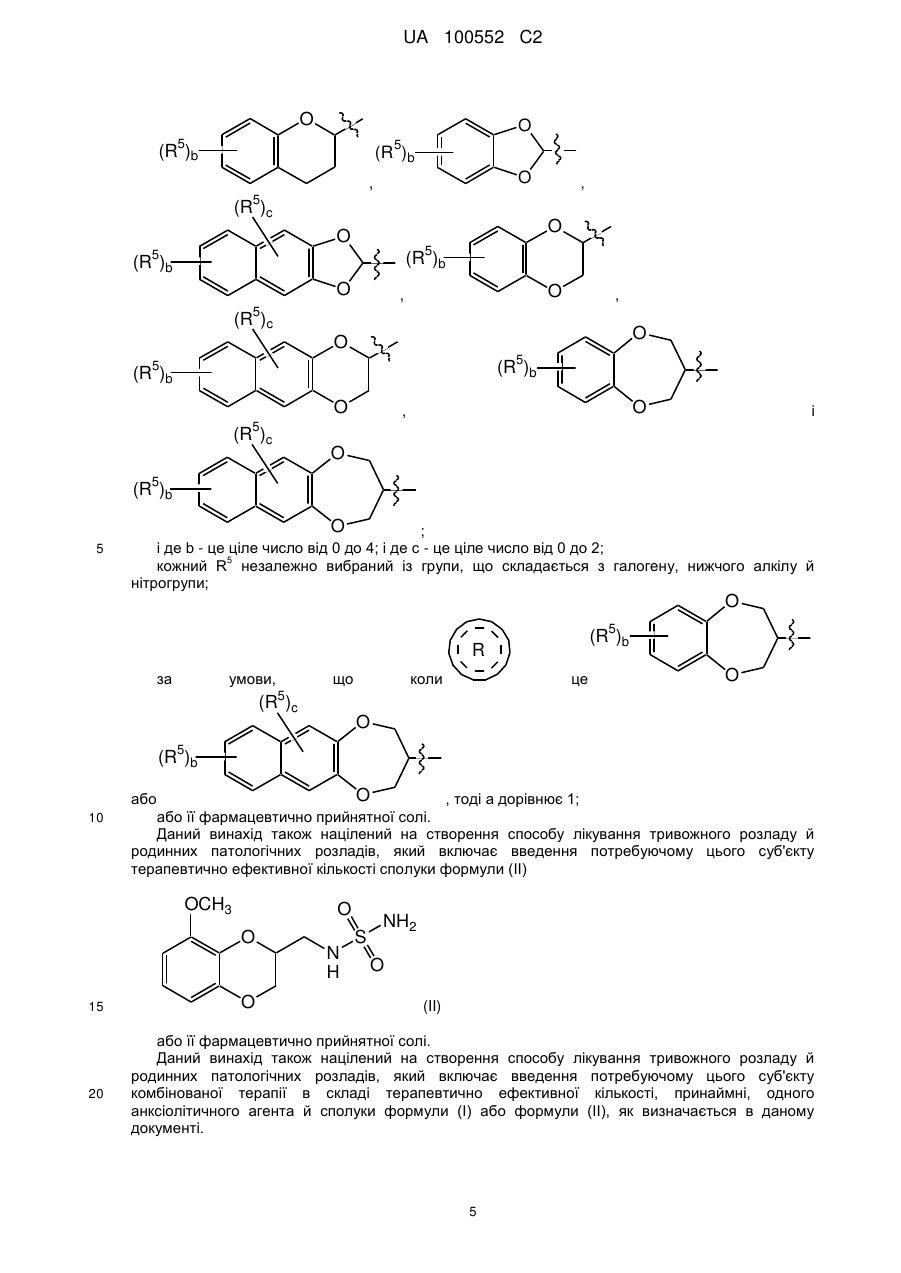
![]() являє собою
являє собою 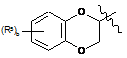 ,
,
де b - це ціле число від 0 до 4; кожний R5 незалежно вибирають із групи, що складається з галогену і нижчого алкілу;
або її фармацевтично прийнятної солі.
2. Спосіб за п. 1, де
R1 і R2 кожний незалежно вибирають із групи, що складається з водню й нижчого алкілу;
R4 вибирають із групи, що складається з водню й нижчого алкілу;
a - це ціле число від 1 до 2;
![]() являє собою
являє собою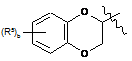 ,
,
де b - це ціле число від 0 до 2; кожний R5 незалежно вибирають із групи, що складається з галогену і нижчого алкілу.
3. Спосіб за п. 2, де
R1 і R2 кожний незалежно вибирають із групи, що складається з водню й нижчого алкілу;
R4 вибирають із групи, що складається з водню й нижчого алкілу;
a - це ціле число 1;
![]() являє собою
являє собою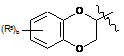 ,
,
де b - це ціле число від 0 до 2; кожний R5 незалежно вибирають із групи, що складається з галогену і нижчого алкілу.
4. Спосіб за п. 2, де
R1 і R2 кожний незалежно вибирають із групи, що складається з водню й нижчого алкілу;
R4 вибирають із групи, що складається з водню й метилу;
a - це ціле число від 1 до 2;
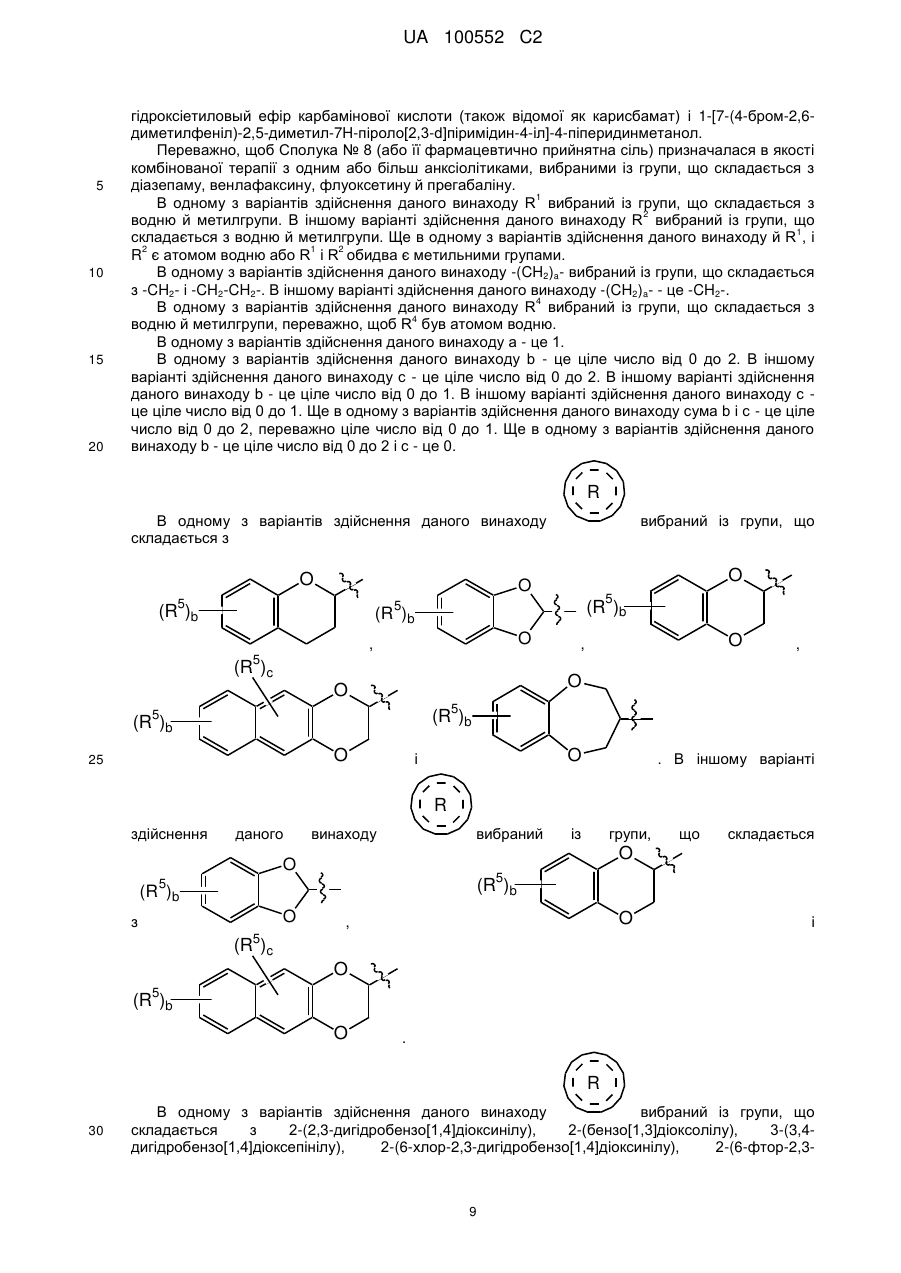
![]() вибирають із групи, що складається з
вибирають із групи, що складається з
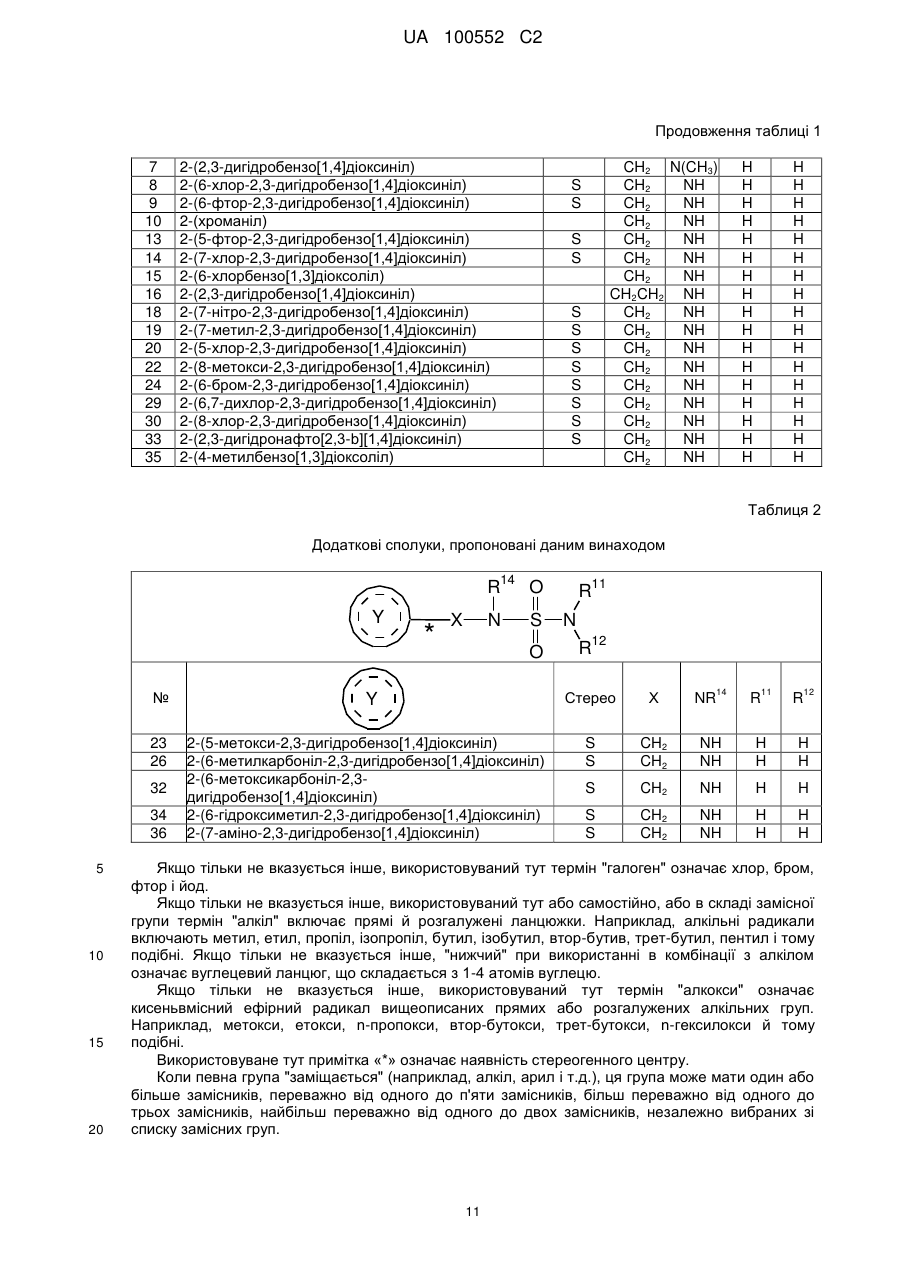
2-(2,3-дигідробензо[1,4]діоксинілу),
2-(6-хлор-2,3-дигідробензо[1,4]діоксинілу),
2-(6-фтор-2,3-дигідробензо[1,4]діоксинілу),
2-(5-фтор-2,3-дигідробензо[1,4]діоксинілу),
2-(7-хлор-2,3-дигідробензо[1,4]діоксинілу),
2-(7-метил-2,3-дигідробензо[1,4]діоксинілу),
2-(5-хлор-2,3-дигідробензо[1,4]діоксинілу),
2-(6-бром-2,3-дигідробензо[1,4]діоксинілу),
2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксинілу) і
2-(8-хлор-2,3-дигідробензо[1,4]діоксинілу).
5. Спосіб за п. 4, де
R1 і R2 кожний незалежно вибирають із групи, що складається з водню й метилу;
R4 вибирають із групи, що складається з водню й метилу;
a - це ціле число від 1 до 2;
![]() вибирають із групи, що складається з
вибирають із групи, що складається з
2-(2,3-дигідробензо[1,4]діоксинілу),
2-(6-хлор-2,3-дигідробензо[1,4]діоксинілу),
2-(7-хлор-2,3-дигідробензо[1,4]діоксинілу),
2-(7-метил-2,3-дигідробензо[1,4]діоксинілу),
2-(6-бром-2,3-дигідробензо[1,4]діоксинілу) і
2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксинілу).
6. Спосіб за п. 1, де сполука формули (I) вибрана із групи, що складається з (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфаміду і його фармацевтично прийнятних солей.
7. Спосіб за п. 1, де тривожний розлад або споріднений патологічний розлад вибирають із групи захворювань, що складається з генералізованого тривожного розладу, гострого стресового розладу, посттравматичного стресового розладу, обсесивно-компульсивного розладу, соціальної фобії, специфічних фобій, панічного розладу з агорафобією або без неї, агорафобії без супутнього панічного розладу, тривожного розладу внаслідок загального захворювання, тривожного розладу внаслідок залежності від речовин, а також тривожного розладу неясної етіології.
8. Спосіб за п. 1, де тривожний розлад або споріднений патологічний розлад вибирають із групи захворювань, що складається з генералізованого тривожного розладу, гострого стресового розладу, посттравматичного стресового розладу й обсесивно-компульсивного розладу.
9. Спосіб за п. 1, де тривожний розлад або споріднений патологічний розлад вибирають із групи захворювань, що складається з генералізованого тривожного розладу.
10. Спосіб лікування тривожного розладу або спорідненого патологічного розладу, який відрізніється тим, що потребуючому цього суб’єкту вводять терапевтично ефективну кількість сполуки, вибраної із групи, що складається (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфаміду і його фармацевтично прийнятних солей.
11. Спосіб за п. 10, де тривожний розлад або споріднений патологічний розлад вибирають із групи захворювань, що складається з генералізованого тривожного розладу, гострого стресового розладу, посттравматичного стресового розладу, обсесивно-компульсивного розладу, соціальної фобії, специфічних фобій, панічного розладу з агорафобією або без неї, агорафобії без супутнього панічного розладу, тривожного розладу внаслідок загального захворювання, тривожного розладу внаслідок залежності від речовин, а також тривожного розладу неясної етіології.
12. Спосіб за п. 11, де тривожний розлад або споріднений патологічний розлад вибирають із групи захворювань, що складається з генералізованого тривожного розладу, гострого стресового розладу, посттравматичного стресового розладу й обсесивно-компульсивного розладу.
13. Спосіб за п. 12, де тривожний розлад або споріднений патологічний розлад вибирають із групи захворювань, що складається з генералізованого тривожного розладу.
14. Спосіб лікування тривожного розладу або спорідненого патологічного розладу, який відрізняється тим, що потребуючому цього суб’єкту вводять терапевтично ефективну кількість сполуки формули (III)
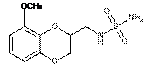 (III)
(III)
або її фармацевтично прийнятної солі.
15. Спосіб за п. 14, де тривожний розлад або споріднений патологічний розлад вибирають із групи захворювань, що складається з генералізованого тривожного розладу, гострого стресового розладу, посттравматичного стресового розладу, обсесивно-компульсивного розладу, соціальної фобії, специфічних фобій, панічного розладу з агорафобією або без неї, агорафобії без супутнього панічного розладу, тривожного розладу внаслідок загального захворювання, тривожного розладу внаслідок залежності від речовин, а також тривожного розладу неясної етіології.
16. Спосіб за п. 15, де тривожний розлад або споріднений патологічний розлад вибирають із групи захворювань, що складається з генералізованого тривожного розладу, гострого стресового розладу, посттравматичного стресового розладу й обсесивно-компульсивного розладу.
17. Спосіб за п. 16, де тривожний розлад або споріднений патологічний розлад є генералізованим тривожним розладом.
18. Спосіб лікування тривожного розладу або спорідненого патологічного розладу, який відрізняється тим, що потребуючому цього суб’єкту проводять комбіновану терапію терапевтично ефективною кількістю принаймні одного анксіолітика й сполуки формули (I)
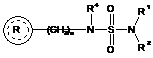 , (I)
, (I)
де
R1 і R2 кожний незалежно вибирають із групи, що складається з водню й нижчого алкілу;
R4 вибирають із групи, що складається з водню й нижчого алкілу;
a - це ціле число від 1 до 2;
![]() являє собою
являє собою 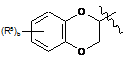 ;
;
де b - це ціле число від 0 до 4;
кожний R5 незалежно вибирають із групи, що складається з галогену і нижчого алкілу;
або її фармацевтично прийнятної солі.
19. Спосіб за п. 18, де сполуку формули (I) вибирають із групи, що складається з (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфаміду і його фармацевтично прийнятних солей.
20. Спосіб за п. 18, де тривожний розлад або споріднений патологічний розлад вибирають із групи захворювань, що складається з генералізованого тривожного розладу, гострого стресового розладу, посттравматичного стресового розладу, обсесивно-компульсивного розладу, соціальної фобії, специфічних фобій, панічного розладу з агорафобією або без неї, агорафобії без супутнього панічного розладу, тривожного розладу внаслідок загального захворювання, тривожного розладу внаслідок залежності від речовин, а також тривожного розладу неясної етіології.
21. Спосіб за п. 20, де тривожний розлад або споріднений патологічний розлад вибирають із групи захворювань, що складається з генералізованого тривожного розладу, гострого стресового розладу, посттравматичного стресового розладу й обсесивно-компульсивного розладу.
22. Спосіб за п. 21, де тривожний розлад або споріднений патологічний розлад є генералізованим тривожним розладом.
23. Спосіб за п. 18, де анксіолітик вибирають із групи, що включає бензодіазепіни, селективні інгібітори зворотного захоплення серотоніну, селективні інгібітори зворотного захоплення норадреналіну, антагоністи рецептора серотоніну, інгібітори зворотного захоплення норепінефрину, інгібітори зворотного захоплення допаміну, антагоніст рецептора допаміну, антагоністи кортикотропін-рилізинг фактора, інгібітори моноаміноксидази, 5HT1a агоністи, альфа-2 адренергічні антагоністи, агоністи ГАМКA, антагоністи ГАМКB, агоністи канабіноїдів, антагоністи нейрокініну, антагоністи каппа-опіоїдів і агоністи рецептора, подібного до опіоїдного-1 (ORL-1).
24. Спосіб за п. 23, де анксіолітик вибирають із групи, що включає бензодіазепіни, селективні інгібітори зворотного захоплення серотоніну (SSRI) і селективні інгібітори зворотного захоплення норадреналіну.
25. Спосіб за п. 18, де анксіолітик вибирають із групи, що включає діазепам, флуразепам, триазолам, лоразепам, алпразолам, хлордіазепам, оксазепам, темазепам, клоназепам, буспірон, флуоксетин, сертралін, пароксетин, циталопрам, флувоксамін, нефазадон, венлафаксин, мілнаципран, 3-(3-аміно-2-(R)-гідроксипропіл)-1-(4-фторфеніл)-8-(8-метилнафтален-1-ілметил)-1,3,8-триазаспіро[4,5]декан-4-он, 2-(2-хлорфеніл)-2-(S)-гідроксіетиловий ефір карбамінової кислоти і 1-[7-(4-бром-2,6-диметилфеніл)-2,5-диметил-7H-піроло[2,3-d]піримідин-4-іл]-4-піперидинметанол.
26. Спосіб за п. 25, де анксіолітик вибирають із групи, що включає діазепам, венлафаксин, флуоксетин і прегабалін.
27. Спосіб лікування тривожного розладу або спорідненого патологічного розладу, який відрізняється тим, що потребуючому цього суб’єкту проводять комбіновану терапію терапевтично ефективною кількістю принаймні одного анксіолітика і сполуки, вибраної із групи, що складається з (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфаміду і його фармацевтично прийнятних солей.
28. Спосіб за п. 27, де тривожний розлад або споріднений патологічний розлад вибирають із групи захворювань, що складається з генералізованого тривожного розладу, гострого стресового розладу, посттравматичного стресового розладу, обсесивно-компульсивного розладу, соціальної фобії, специфічних фобій, панічного розладу з агорафобією або без неї, агорафобії без супутнього панічного розладу, тривожного розладу внаслідок загального захворювання, тривожного розладу внаслідок залежності від речовин, а також тривожного розладу неясної етіології.
29. Спосіб за п. 28, де тривожний розлад або споріднений патологічний розлад вибирають із групи захворювань, що складається з генералізованого тривожного розладу, гострого стресового розладу, посттравматичного стресового розладу й обсесивно-компульсивного розладу.
30. Спосіб за п. 29, де тривожний розлад або споріднений патологічний розлад є генералізованим тривожним розладом.
31. Спосіб за п. 27, де анксіолітик вибирають із групи, що включає бензодіазепіни, селективні інгібітори зворотного захоплення серотоніну, селективні інгібітори зворотного захоплення норадреналіну, антагоністи рецептора серотоніну, інгібітори зворотного захоплення норепінефрину, інгібітори зворотного захоплення допаміну, антагоніст рецептора допаміну, антагоністи кортикотропін-рилізинг фактора, інгібітори моноаміноксидази, 5HT1a агоністи, альфа-2 адренергічні антагоністи, агоністи ГАМКA, антагоністи ГАМКB, агоністи канабіноїдів, антагоністи нейрокініну, антагоністи каппа-опіоїдів і агоністи рецептора, подібного до опіоїдного-1 (ORL-1).
32. Спосіб за п. 31, де анксіолітик вибирають із групи, що включає бензодіазепіни, селективні інгібітори зворотного захоплення серотоніну (SSRI) і селективні інгібітори зворотного захоплення норадреналіну.
33. Спосіб за п. 27, де анксіолітик вибирають із групи, що включає діазепам, флуразепам, триазолам, лоразепам, алпразолам, хлордіазепам, оксазепам, темазепам, буспірон, флуоксетин, сертралін, пароксетин, циталопрам, флувоксамін, нефазадон, венлафаксин, мілнаципран, 3-(3-аміно-2-(R)-гідроксипропіл)-1-(4-фторфеніл)-8-(8-метилнафтален-1-ілметил)-1,3,8-триазаспіро[4,5]декан-4-он, 2-(2-хлорфеніл)-2-(S)-гідроксіетиловий ефір карбамінової кислоти і 1-[7-(4-бром-2,6-диметилфеніл)-2,5-диметил-7H-піроло[2,3-d]піримідин-4-іл]-4-піперидинметанол.
34. Спосіб за п. 33, де анксіолітик вибирають із групи, що включає діазепам, венлафаксин, флуоксетин і прегабалін.
35. Спосіб лікування тривожного розладу або спорідненого патологічного розладу, який відрізняється тим, що потребуючому цього суб’єкту проводять комбіновану терапію терапевтично ефективною кількістю принаймні одного анксіолітика і сполуки формули (III)
 (III)
(III)
або її фармацевтично прийнятної солі.
Текст
Реферат: Даний винахід являє собою спосіб лікування тривожного розладу й споріднених патологічних розладів, що включає введення потребуючому цього суб'єкту терапевтично ефективних кількостей одного або більше нових гетероциклічних бензопохідних сульфаміду формули (І) R R (CH2)a N 4 O S O R 1 R 2 OCH3 N і формули (II) . UA 100552 C2 (12) UA 100552 C2 Даний винахід спрямований на створення способу лікування тривожного розладу й споріднених патологічних розладів, який включає введення монотерапії і, як варіант, комбінованої терапії принаймні одним анксіолітиком. UA 100552 C2 5 10 15 20 25 30 35 40 45 50 55 60 Галузь винаходу Даний винахід націлений на використання гетероциклічних бензопохідних сульфаміду при лікуванні тривожних розладів і родинних патологічних розладів, включаючи генералізований тривожний розлад, гострий стресовий розлад, посттравматичний стресовий розлад (ПТСР), обсесивно-компульсивний розлад, соціальну фобію, специфічні фобії, панічний розлад з агорафобією або без неї, агорафобію без супутнього панічного розладу, тривожний розлад внаслідок загального захворювання, тривожний розлад внаслідок залежності від речовин, а також тривожний розлад неясної етіології. Передумови створення винаходу Тривожні розлади, що є найбільш частими психіатричними розладами, зустрічаються в 1520 % пацієнтів лікувальних установ загального профілю. Тривога, обумовлена як суб'єктивне почуття дискомфорту, страху або поява дурних передчуттів, може вказувати на первинний психіатричний розлад, або бути компонентом первинної загальномедичної патології або реакцією на неї. Первинні тривожні розлади класифікуються залежно від тривалості й характеру протікання, а також наявності й природи загострюючого фактора. У пацієнтів з генералізованим тривожним розладом (ГТР) відзначаються постійні надлишкові й (або) необґрунтовані побоювання, що супроводжуються м'язовим напруженням, труднощами в зосередженні, вегетативною гіперактивністю, загальним порушенням або занепокоєнням і безсонням. Початок захворювання звичайно відзначається у віці до 20 років, при цьому в анамнезі може простежуватися наявність дитячих страхів і соціального гальмування. Частота зустрічальності ГТР становить від 5 до 6 %; ризик виникнення вище в родичів пацієнтів із уже встановленим діагнозом, що мають перший ступінь споріднення. Цікаво те, що як указують результати проведених сімейних досліджень, ГТР і панічний розлад розвиваються незалежно. Понад 80 % пацієнтів із ГТР також страждають вираженою тривожністю й родинними розладами, дистимією, або соціофобією. У цих пацієнтів часто відзначається супутнє зловживання психоактивними препаратами, особливо седативними/снотворними засобами й (або) алкоголем. Пацієнти із ГТР зайво тривожаться по дріб'язках, при цьому тривога виявляє істотний негативний вплив на повсякденне життя пацієнтів; на відміну від панічного розладу, скарги на ускладнення дихання, серцебиття й тахікардію відносно рідкі. Комбінація лікарських і психотерапевтичних впливів є найбільш ефективним підходом до лікування тривожних розладів, хоча повне рятування пацієнта від симптомів досягається рідко. Звичайно показане введення короткого курсового лікування бензодіазепіном, переважно лорезепамом, оксазепамом або темазепамом. Прийом препарату, як правило, починають із найменших можливих доз, а його введення здійснюється по потребі, з появою симптомів. Бензодіазепіни різняться питомою активністю (мг/кг), тривалістю періоду напівжиття, розчинністю в ліпідах, шляхами метаболізму й наявністю активних метаболітів. Швидкорозчинні і розчинні в ліпідах лікарські агенти, такі як діазепам, мають швидкий початок дії й більш високий потенційний ризик зловживання. Бензодіазепіни звичайно не призначаються на строк >4-6 тижнів, у зв'язку з можливим розвитком толерантності й ризиком зловживання й виникнення лікарської залежності. Також необхідно попереджати пацієнтів про неприпустимість одночасного прийому алкоголю або інших седативних препаратів, у зв'язку з можливістю розвитку нейротоксичної дії й функціональних порушень. Виразність побічних ефектів бензодіазепінів звичайно співвідноситься з відносною тривалістю періоду напівжиття. Довгостроково діючі агенти, такі як діазепам, хлордіазепоксид, флуразепам і клоназепам мають схильність акумулювати активні метаболіти, що приводить до розвитку вираженої седативної дії, погіршенню когнітивних функцій і психомоторних показників. Короткочасно діючі сполуки, такі як алпразолам і оксазепам, здатні викликати тривожні порушення в денний час доби, ранкове безсоння й, при припиненні прийому, поновлення симптомів тривожного розладу й безсоння. Хоча пацієнти привчаються переносити седативну дію бензодіазепінів, їм значно складніше звикати до їх побічних психомоторних ефектів. Припинення прийому бензодіазепінів із тривалим періодом напівжиття може бути досягнуте за допомогою поступового покрокового зниження дози (на 10 % кожні 1-2 тижні) протягом 6-12 тижнів. Звичайно більш важким є припинення прийому короткочасно діючих бензодіазепінів. Лікарям може знадобитися переведення пацієнта на прийом бензодіазепіну з більш тривалим періодом напівжиття, або застосування додаткового препарату, наприклад, бета-блокатора або карбамазепіну, перш ніж уживати спроби повного припинення прийому бензодіазепіну. Реакції, пов'язані із припиненням прийому препарату, варіюються по ступеню важкості й тривалості; вони можуть включати тривожні розлади й родинні патологічні розлади, тривожний розлад, маревний розлад свідомості, летаргію, діафорез, тинітус, вегетативну гіперактивність, мимовільні рухи й, зрідка, епілептичні припадки. 1 UA 100552 C2 5 10 15 20 25 30 35 40 45 50 55 60 Альтернативним є введення буспірону. Буспірон являє собою небензодіазепіновий анксіолітик. Цей препарат позбавлений седативної дії, не викликає звикання або лікарської залежності, не взаємодіє з рецепторами бензодіазепіну або алкоголем і не має потенціал для виникнення розгальмування або ризику зловживань. Однак цей препарат необхідно приймати протягом декількох тижнів для прояву його терапевтичної дії, при цьому його прийом здійснюється тричі на день. Пацієнти, в яких раніше досягався терапевтичний ефект від прийому бензодіазепіну, навряд чи вважатимуть буспірон рівноефективним, але пацієнти, що страждають травмою голови або деменцією, й мають симптоми тривожного розладу й (або) порушення, можуть добре відповідати на прийом даного лікарського агента. Введення бензодіазепінів пацієнтам літнього віку вимагає особливої обережності. У таких пацієнтів підвищена абсорбція лікарських препаратів; знижений печіночний метаболізм, білкове зв'язування й ниркова екскреція; а також збільшений рівень розподілу. Ці фактори, поряд із імовірною наявністю супутніх захворювань і прийомом інших лікарських засобів, різко збільшують імовірність токсичної дії препаратів. Ятрогенні психомоторні порушення можуть стати причиною падінь і переломів, поплутаного стану свідомості або автомобільних аварій. При призначенні прийому препаратів цього класу необхідно починати з найменшої можливої дози, здійснюючи пильне спостереження за побічними ефектами. Бензодіазепіни також протипоказані при вагітності й годуванні грудьми. Антиконвульсанти з ГАМК-ергічними властивостями також можуть бути ефективні при лікуванні тривожних розладів. Габапентин, окскарбазепін, тіагабін, прегабалін і дивальпроекс, як було показано, виявляють певну сприятливу дію при лікуванні різноманітних синдромів із тривожною симптоматикою. Агенти, що виявляють селективний вплив на ГАМКA рецептори, розробляються в цей час; існує надія, що ця остання група препаратів буде позбавлена побічних ефектів, властивих бензодіазепінам, у тому числі седативної дії, впливу на пам'ять і здатності викликати звикання. Панічний розлад визначається наявністю повторюваних і непередбачених панічних атак, що представляють собою чітко виражені періоди сильного страху й дискомфорту, пов'язаного із проявами різноманітних фізичних симптомів, що включають серцебиття, пітливість, тремтіння, задишку, біль у грудях, запаморочення й страх неминучого наближення смерті. Парестезії, порушення функцій шлунково-кишкового тракту, а також відчуття нереальності, що відбувається також є частими симптомами. Діагностичні критерії також включають наявність, що зберігається протягом не менш 1 місяця, стурбованості у зв'язку з виникненням панічних атак, або пов'язаних з ними змін поведінки. Частота зустрічності панічного розладу становить від 1 до 3 %. Панічні атаки мають раптовий початок, розвиваються протягом 10 хвилин і звичайно проходять протягом години, виникнення атак відрізняється непередбачуваністю. Частота й ступінь виразності панічних атак варіюються, коливаючись від одиничних щотижневих атак до серії багаторазових атак, які переміняються місяцями задовільного самопочуття. Перша атака, як правило, трапляється поза будинком, і її виникнення звичайно відзначається в пізньому підлітковому або ранньому зрілому віці. У деяких індивідуумів згодом розвивається тривога, пов'язана з очікуванням нападу, що приводить до виникнення генералізованого страху й прогресуючого прагнення уникати місць і ситуацій, у яких панічна атака може виникнути знову. Агорафобія, яка часто виникає в пацієнтів з панічним розладом, являє собою придбаний несвідомий страх перебування в місцях, де можливе виникнення відчуття відсутності виходу або неможливості втечі. Як правило, це приводить до прогресуючих обмежень, що стосуються способу життя пацієнта й, у буквальному значенні, до обмежень його переміщень у просторі. Найчастіше пацієнти соромляться такої прихильності до свого будинку й необхідності присутності інших осіб для виходу за його межі, і тому ні з ким не діляться своєю проблемою; як наслідок, лікарям найчастіше не вдається діагностувати даний синдром, якщо тільки вони не ставлять прямі запитання. Досяжними цілями лікування будуть зниження частоти й зменшення інтенсивності панічних атак. Основою лікарської терапії є призначення антидепресантів. Трициклічні антидепресанти (ТЦА) іміпрамін і кломіпрамін ефективні в 75-90 % пацієнтів з панічними розладами. Спочатку призначаються низькі дози (наприклад, від 10 до 25 мг/день), що дозволяють уникнути виникнення минущого посилення тривоги, пов'язаного зі збільшенням рівня моноамінів. Селективні інгібітори зворотного захоплення серотоніну (SSRI) є рівною мірою ефективними й не виявляють побічної дії, характерної для ТЦА. Прийом SSRI повинен починатися з однієї третьої до половини звичайної ефективної дози (наприклад, від 5 до 10 мг флуоксетину, від 25 до 50 мг сертраліну, 10 мг пароксетину). Інгібітори моноаміноксидази (ІМАО) також ефективні й можуть особливо бути корисні для пацієнтів із супутніми ознаками атипічної депресії (наприклад, гіперсомнією і збільшенням ваги тіла). Однак наявність інсомнії, ортостатичної 2 UA 100552 C2 5 10 15 20 25 30 35 40 45 50 55 60 гіпотензії й необхідності підтримки дієти зі зниженим вмістом тираміну (з виключенням сиру й вина) обмежує застосування цієї групи препаратів. При лікуванні антидепресантами звичайно потрібно від 2 до 6 тижнів для досягнення терапевтичного ефекту, при цьому може знадобитися корекція дози, залежно від виразності клінічних результатів. Основною характеристикою фобічних розладів є наявність значно вираженого постійного страху об'єктів або ситуацій, вплив яких приводить до появи негайної тривожної реакції. Такий пацієнт прагне уникати фобічного стимулу, і це прагнення звичайне негативно впливає на його професійні або соціальні функції. Панічні атаки можуть викликатися фобічним стимулом, або виникати спонтанно. На відміну від пацієнтів, що страждають на інші тривожні розлади, індивідууми з фобіями звичайно відчувають почуття тривоги тільки в специфічних ситуаціях. Широко розповсюджені фобії включають страх замкнених просторів (клаустрофобію), страх виду крові й страх польотів. Соціальна фобія, також відома як соціальний тривожний розлад, відрізняється специфічним страхом перебувати в товаристві або виступати перед групою людей, у ситуаціях, коли індивідуум виявляється в товаристві незнайомих осіб або зазнає екзаменаційної перевірки й оцінки з боку інших. Приклади включають необхідність підтримувати розмову на вечірці, користуватися суспільним туалетом і зустрічатися з незнайомцями. У кожному випадку, пацієнт усвідомлює те, що випробовуваний страх, з урахуванням реальних обставин, є надмірним і безпідставним. Специфічний характер фобії може варіюватися залежно від статі, етнічної приналежності й культурних традицій. Фобічні розлади досить широко поширені, вражаючи до 10 % населення. ІMAO зменшують виразність соціальної фобії незалежно від своєї антидепресантної активності, SSRI також виявляються ефективними. Бензодіазепіни можуть виявитися корисними для зниження прагнення уникати фобічного стимулу, але хронічна природа фобічних розладів обмежує корисність цієї групи препаратів. У пацієнтів також може розвиватися тривога після впливу екстремальних подій, що травмують, таких як погроза смерті або травми або загибель близьких. Реакція може розвитися незабаром після травми (гострий стресовий розлад), або може виникати й повторюватися пізніше (ПТСР). У випадку обох синдромів індивідууми відчувають асоційовані симптоми неемоційності й втрати сприйнятливості. Пацієнт може відчувати себе деперсоналізованим і нездатним згадати специфічні аспекти емоційної травми, хоча, як правило, вона нагадує про себе в думках, снах, або спогадах, особливо при наявності свідчень вихідної події. Пацієнти часто активно уникають стимулів, здатних викликати спогаду про травму, і в результаті проявляють підвищення пильності, порушення й старт-рефлексу. Пацієнти зі стресовими розладами піддаються ризику розвитку інших розладів, близьких до тривожних розладів, розладів настрою й хворобливим пристрастям (особливо до алкоголю). Від 5 до 10 % американців будуть відповідати в якийсь певний момент їх життя критеріям ПТСР, причому жінки мають більшу ймовірність розвитку цього розладу, ніж чоловіки. Фактори ризику розвитку ПТСР включають психіатричні епізоди в анамнезі й особистісні характеристики підвищеного невротизму й екстраверсії. Гострі стресові реакції звичайно відрізняються здатністю самообмеження, і лікування звичайне включає короткочасне застосування бензодіазепінів і підтримуючої/експресивної психотерапії. Хронічна й рецидивуюча природа ПТСР, однак, вимагає більш комплексного підходу із застосуванням лікарських і психотерапевтичних впливів. ПТСР має високий ступінь кореляції з перитравматичними дисоціативними симптомами й розвитком гострого стресового розладу в момент травми. ТЦА, такі як іміпрамін і амітриптилін, ІМАО фенелзин і SSRI (флуоксетин, сертралін, циталопрам, пароксетин), здатні знизити рівень тривоги, інтрузивну симптоматику й реакцію уникнення, що також властиво празозину, що є α1 антагоністом. Тразодон, антидепресант із седативною дією, часто призначається на ніч для купіювання інсомнії (від 50 до 150 мг на ніч). Карбамазепін, вальпроєва кислота й алпразолам також автономно викликали поліпшення в неконтрольованих дослідженнях. Обсесивно-компульсивний розлад (OКР) характеризується розвитком нав'язливих думок і дій, які здатні погіршувати повсякденне функціонування. Часто зустрічаються страхи забруднення й інфікування, також як і часте миття рук, повторне перераховування й потреба перевірки й повторного огляду таких дій, як запирання двері на замок. Ступінь, у якому даний розлад заважає життю індивідуума, варіюється, але у всіх випадках обсесивно-компульсивна активність займає до >1 години/день і відбувається з метою полегшення тривоги, викликаної основним страхом. Пацієнти часто приховують свої симптоми, звичайно у зв'язку зі сором'язливістю, викликаною змістом їх думок, або характером їх дій. Лікарям необхідно ставити спеціальні запитання, що стосуються рецидивуючих думок і дій, особливо, якщо присутні фізичні ознаки, такі як шорстка почервоніла шкіра рук або осередкова втрата волосся 3 UA 100552 C2 5 10 15 20 25 30 на голові (у зв'язку з постійним висмикуванням волосся, або трихотиломанією). Звичайно відзначаються супутні захворювання, серед яких найбільш частими є тривожні розлади й родинні патологічні розлади, інші розлади, що супроводжуються тривожним розладом, розлади харчової поведінки й тики. Частота зустрічальності ОКР у світі становить від 2 до 3 %. Початок захворювання, як правило, поступовий, з першими проявами в ранньому зрілому віці, хоча початок у дитячому віці також не є рідкістю. Захворювання звичайно протікає хвилеподібно з періодами загострення й зменшення симптоматики, але в деяких випадках відзначається неухильне погіршення психосоціальних функцій. Кломіпрамін, флуоксетин і флувоксамін схвалені для застосування при лікуванні ОКР. Кломіпрамін є ТЦА, часто погано стерпним внаслідок антихолінергічної й седативної побічних дій, що проявляються при введенні доз, необхідних для лікування даного захворювання (150250 мг/день). Ефективність препарату при лікуванні ОКР не пов'язана з антидепресантною активністю препарату. Флуоксетин (від 40 до 60 мг/день) і флувоксамін (від 100 до 300 мг/день) мають ефективність, яка дорівнює ефективності кломіпраміну, але виявляють більш м'яку побічну дію. Тільки від 50 до 60 % пацієнтів, що страждають на ОКР, демонструють адекватне поліпшення при введенні ізольованої фармакотерапії. При лікуванні резистентних випадків перевагу може мати комбінація з іншими серотонінергічними агентами, такими як буспірон, або з нейролептиками або бензодіазепінами. При досягненні терапевтичної відповіді звичайно показане проведення тривалої підтримуючої терапії. На додаток, у багатьох пацієнтів, що особливо страждають компульсивними розладами, що віднімають надмірно багато часу, поведінкова терапія викликає поліпшення стану, порівнянне з тим, яке досягається лікарською терапією. Ефективні психотерапевтичні підходи включають поступове збільшення впливу стресових ситуацій, ведення щоденника для уточнення стресових факторів, а також виконання домашніх завдань, які навчають новим діям замість проявів компульсивної поведінки. (Harrison's Online @ www.accessmedicine.com, 10 жовтня 2006 р.) Проте, зберігається потреба забезпечення ефективного лікування тривожного розладу й родинних патологічних розладів. Короткий опис винаходу Даний винахід спрямований на створення способу лікування тривожного розладу й родинних патологічних розладів, який включає введення потребуючому цього суб'єкту терапевтично ефективної кількості сполуки формули (I) R4 O R (CH2)a N S O 35 1 R N R2 (I), де 1 2 R і R кожний незалежно вибраний із групи, що складається з водню й нижчого алкілу; 4 R вибирається із групи, що складається з водню й нижчого алкілу; a - це ціле число від 1 до 2; R 40 вибраний із групи, що складається з 4 UA 100552 C2 O O 5 5 (R )b (R )b O , , 5 (R )c O O (R5)b 5 (R )b O O , , 5 (R )c O O (R5)b 5 (R )b O O , і 5 (R )c O (R5)b 5 O ; і де b - це ціле число від 0 до 4; і де c - це ціле число від 0 до 2; 5 кожний R незалежно вибраний із групи, що складається з галогену, нижчого алкілу й нітрогрупи; O (R5)b R за умови, що коли це O 5 (R )c O (R5)b O , тоді a дорівнює 1; або її фармацевтично прийнятної солі. Даний винахід також націлений на створення способу лікування тривожного розладу й родинних патологічних розладів, який включає введення потребуючому цього суб'єкту терапевтично ефективної кількості сполуки формули (II) або 10 OCH3 O O 15 20 O N H S NH2 O (II) або її фармацевтично прийнятної солі. Даний винахід також націлений на створення способу лікування тривожного розладу й родинних патологічних розладів, який включає введення потребуючому цього суб'єкту комбінованої терапії в складі терапевтично ефективної кількості, принаймні, одного анксіолітичного агента й сполуки формули (I) або формули (II), як визначається в даному документі. 5 UA 100552 C2 5 10 15 20 Прикладами, що ілюструють даний винахід, є способи лікування генералізованого тривожного розладу, гострого стресового розладу, посттравматичного стресового розладу, обсесивно-компульсивного розладу, соціальної фобії, специфічних фобій, панічного розладу з агорафобією або без неї, агорафобії без супутнього панічного розладу, тривожного розладу внаслідок загального захворювання, тривожного розладу, викликаного наркотичною залежністю або токсикоманією, а також тривожного розладу неясної етіології, при цьому способи включають введення потребуючому цього суб'єкту терапевтично ефективної кількості кожної з описаних вище сполук або фармацевтичних препаратів. В іншому прикладі даний винахід націлений на створення способів лікування генералізованого тривожного розладу, гострого стресового розладу, посттравматичного стресового розладу, обсесивно-компульсивного розладу, соціальної фобії, специфічних фобій, панічного розладу з агорафобією або без неї, агорафобії без супутнього панічного розладу, тривожного розладу внаслідок загального захворювання, тривожного розладу, викликаного наркотичною залежністю або токсикоманією, а також тривожного розладу неясної етіології, при цьому способи включають введення потребуючому цього суб'єкту, принаймні, одного анксіолітика в комбінації з кожною з описаних вище сполук або фармацевтичних препаратів. Докладний опис винаходу Даний винахід спрямований на створення способів лікування тривожного розладу й родинних патологічних розладів, при цьому способи включають введення потребуючому цього суб'єкту терапевтично ефективної кількості сполуки формули (I) R4 O R (CH2)a N S 1 R N R2 (I) O R 1 25 2 4 або її фармацевтично прийнятної солі, де , a, R , R і R визначені в даному документі. Даний винахід також ставить метою лікування тривожного розладу й родинних патологічних розладів, що включає введення потребуючому цього суб'єкту терапевтично ефективної кількості сполуки формули (I) або формули (II) у комбінації із щонайменше одним анксіолітиком. В одному з варіантів здійснення даного винаходу сполука формули (I) являє собою Сполуку № 8 або її фармацевтично прийнятну сіль, що має наступну структуру 30 O O (S) Cl 35 40 45 O N H S NH2 O (Спол. № 8) також відома як (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфамід. У даному документі терміни "тривожний розлад і родинні патологічні розлади" і "тривожний розлад або родинний патологічний розлад" визначаються так, щоб включати тривожний розлад і родинний патологічні розлади, включаючи генералізований тривожний розлад, гострий стресовий розлад, посттравматичний стресовий розлад, обсесивно-компульсивний розлад, соціальну фобію (також відомі як соціальний тривожний розлад),специфічні фобії, панічний розлад з агорафобією або без неї, агорафобію без супутнього панічного розладу, тривожний розлад внаслідок загального захворювання, тривожний розлад внаслідок залежності від речовин, а також тривожний розлад неясної етіології (у тому виді, як ці розлади описані за th діагностичними показниками в роботі Diagnostic and Statistical Manual of Mental Disorders, 4 Edition, Text Revision, American Psychiatric Association, 2000, включеної в даний документ у вигляді посилання). Переважно, щоб тривожний розлад або родинний патологічний розлад був вибраний із групи захворювань, що складається з генералізованого тривожного розладу, гострого стресового розладу, посттравматичного стресового розладу й обсесивно 6 UA 100552 C2 5 10 15 20 25 30 35 40 45 50 55 компульсивного розладу. Більш переважно, щоб тривожний розлад і родинний патологічний розлад був генералізованим тривожним розладом. Якщо тільки не зазначене інакше, використовуваний тут термін "анксіолітик" означає будьякий фармацевтичний агент, який може використовуватися для лікування тривожного розладу або родинних патологічних розладів, або для лікування симптомів тривожного розладу або родинного патологічного розладу. Термін "анксіолітик" також включає, але не обмежується цим, кожний фармацевтичний агент, що одержав схвалення FDA (Управління по контролю над продуктами й ліками) або іншого регулюючого відомства як лікарського засобу, призначеного для лікування тривожного розладу або родинного патологічного розладу. Фахівець в галузі може легко визначити такі фармацевтичні агенти, провівши пошук з використанням ресурсів Інтернету, фармацевтичних довідників (наприклад, Настільного довідника лікаря (Physician's Desk Reference)) і (або) довідкових посібників, виданих FDA (або іншим регулюючим відомством). Більше того, фахівець здатний легко визначити рівні доз, рекомендовані для відомих і (або) наявних на ринку анксіолітичних препаратів, за допомогою звертання до відповідної до довідкової інформації, такої як вкладиші лікарського впакування, рекомендації FDA, Настільний довідник лікаря й т.п. Припустимі приклади анксіолітиків включають, але не обмежуються цим, бензодіазепіни, селективні інгібітори зворотного захоплення серотоніну (SSRI), селективні інгібітори зворотного захоплення норадреналіну, антагоністи рецептора серотоніну, інгібітори зворотного захоплення норепінефрину, інгібітори зворотного захоплення допаміну, антагоніст рецептора допаміну (переважно, антагоністи рецепторів допаміну D1, D2 і (або) D3), антагоністи кортикотропінрилізинг фактора (КРФ), інгібітори моноаміноксидази (MAO), 5HT1a агоністи, альфа-2 адренергічні антагоністи, агоністи ГАМКA, антагоністи ГАМКB, агоністи канабіноїда (переважно, агоністи CB1 рецептора), антагоністи нейрокініну (переважно, антагоністи NK1 рецептора), антагоністи каппа-опіоїдів, агоністи рецептора, подібного опіоїдному -1 (ORL-1) (також відомі як агоністи ноцицептин/орфанін пептиду FQ (NOP) і тому подібні. Переважно, щоб анксіолітики були вибрані із групи препаратів, що складається з бензодіазепінів, селективних інгібіторів зворотного захоплення серотоніну (SSRI) і селективних інгібіторів зворотного захоплення норадреналіну. В одному з варіантів здійснення даного винаходу анксіолітик вибраний із групи препаратів, що складається з бензодіазепінів, таких як діазепам, флуразепам, триазолам, лоразепам, алпразолам, хлордіазепам, оксазепам, темазепам і клоназепам; не-бензодіазепінових препаратів, таких як буспірон; селективних інгібіторів зворотного захоплення серотоніну, таких як флуоксетин, сертралін, пароксетин, циталопрам, флувоксамін і їм подібні; антагоністів рецептора серотоніну, таких як нефазадон і тому подібні; інгібіторів зворотного захоплення серотоніну і норадреналіну, таких як венлафаксин, мілнаципран і тому подібні, 3-(3-аміно-2-(R)гідроксипропіл)-1-(4-фторфеніл)-8-(8-метилнафтален-1-ілметил)-1,3,8-триазаспіро[4,5]декан-4он, 2-(2-хлорфеніл)-2-(S)-гідроксіетиловый ефір карбамінової кислоти (також відомої як карисбамат) і 1-[7-(4-бром-2,6-диметилфеніл)-2,5-диметил-7H-піроло[2,3-d]піримідин-4-іл]-4піперидинметанол. Переважно, щоб анксіолітик був вибраний із групи, що складається з діазепаму, венлафаксину, флуоксетину й прегабаліну. Використовуваний тут термін "суб'єкт" означає експериментальну тварину, переважно ссавця (наприклад, свійську тварину, таку як собака, кішка і т.д.), найбільш переважно, людину, яка є об'єктом лікування, спостереження або експерименту. Використовуваний тут термін "терапевтично ефективна кількість" означає кількість активної сполуки або фармацевтичного агента, що викликає таку біологічно або медично значущу відповідь із боку системи тканин/органів, організму тварини або людини, що перебуває під спостереженням дослідника, ветеринара, лікаря або іншого клініциста, який включає полегшення симптомів захворювання або патологічного розладу, що піддалися лікуванню. Там, де даний винахід націлений на проведення комбінованої терапії, або комбінованої терапії, що включає введення однієї або більше сполук формули (I) або формули (II) і одного або більше анксіолітиків, "терапевтично ефективна кількість" означає таку кількість комбінованих агентів, прийнятих спільно, яка викликає бажаний біологічну або медичну відповідь. Наприклад, терапевтично ефективною кількістю при проведенні комбінованої терапії, що включає введення сполуки формули (I) або формули (II) і, принаймні, одним анксіолітиком, буде така кількість сполуки з формулою (I) або формулою (II) і кількість анксіолітика, яка, у випадку якщо препарати введені одночасно або послідовно, має комбінований ефект, що є терапевтично ефективним. Більше того, фахівцеві буде зрозуміло, що у випадку проведення комбінованої терапії з використанням терапевтично ефективних кількостей, як показано у 7 UA 100552 C2 5 10 15 20 25 30 35 40 45 50 55 вищенаведеному прикладі, кількість сполуки з формулою (I) або з формулою (II) і (або) кількість анксіолітика, взяті окремо, можуть бути, а можуть і не бути терапевтично ефективними. Використовуваний тут термін "комбінована терапія" означає лікування суб'єкта, що потребує цього, за допомогою однієї або більше сполук формули (I) або формули (II) у комбінації з одним або більш анксіолітиком, де сполука(-и) формули (I) або формули (II) і анксіолітик(-и) призначаються з використанням підходящих засобів доставки, одночасно, послідовно, роздільно або у вигляді єдиної лікарської форми. Там, де сполука(-и) формули (I) або формули (II) і анксіолітик(-и) призначаються у вигляді роздільних лікарських форм, добові дози кожної із сполук можуть бути або однаковими, або різними. Сполука(-и) формули (I) або формули (II) і анксіолітик(-и) можуть призначатися з використанням того самого, або різних шляхів уведення. Приклади підходящих способів введення включають, але не обмежуються цим, пероральний, внутрішньовенний (в/в), внутрішньом'язовий (в/м), підшкірний (п/ш), трансдермальний і ректальний. Сполуки також можуть вводитися безпосередньо в нервову систему з використанням способів, що включають, але не обмежуваних цим, інтрацеребральне, інтравентрикулярне, інтрацеребровентрикулярне, інтратекальне, інтрацистернальне, інтраспінальне й (або) периспінальне введення, з використанням інтракраніальних або інтравертебральних голок і (або) катетерів за допомогою або без допомоги насосних пристосувань. Сполука(-и) формули (I) або формули (II) і анксіолітик(-и) можуть призначатися відповідно до одночасних або чергу вальних режимів введення, у той самий або різний час протягом курсу лікування, одночасно у вигляді роздільних форм або в єдиній лікарській формі. В одному з варіантів здійснення даний винахід націлений на створення способу лікування тривожного розладу й родинних патологічних розладів, який включає введення потребуючому цього суб'єкту комбінованої терапії в складі однієї або більше сполук формули (I) або формули (II) і однієї або більше анксіолітичних сполук, вибраних із групи препаратів, що складається з бензодіазепінів, селективних інгібіторів зворотного захоплення серотоніну (SSRI) і селективних інгібіторів зворотного захоплення норадреналіну. В іншому варіанті здійснення даний винахід націлений на створення способу лікування тривожного розладу й родинних патологічних розладів, який включає введення потребуючому цього суб'єкту комбінованої терапії в складі однієї або більше сполук формули (I) або формули (II) і одного або більше анксіолітиків, вибраних із групи бензодіазепінів, таких як діазепам, флуразепам, триазолам, лоразепам, алпразолам, хлордіазепам, оксазепам, темазепам і клоназепам; не-бензодіазепінових препаратів, таких як буспірон; селективних інгібіторів зворотного захоплення серотоніну, таких як флуоксетин, сертралін, пароксетин, циталопрам, флувоксамін і тому подібні; антагоністів рецептора серотоніну, таких як нефазадон і тому подібних; інгібіторів зворотного захоплення серотоніну й норадреналіну, таких як венлафаксин, мілнаципран і тому подібних, 3-(3-аміно-2-(R)-гідроксипропіл)-1-(4-фторфеніл)-8-(8метилнафтален-1-ілметил)-1,3,8-триазаспіро[4,5]декан-4-он, 2-(2-хлорфеніл)-2-(S)гідроксіетиловый ефір карбамінової кислоти (також відомої як карисбамат) і 1-[7-(4-бром-2,6диметилфеніл)-2,5-диметил-7H-піроло[2,3-d]піримідин-4-іл]-4-піперидинметанол. Переважно, щоб одна або більше сполук формули (I) або формули (II) призначалися в якості комбінованої терапії з одним або більше анксіолітиків, вибраних із групи, що складається з діазепаму, венлафаксину, флуоксетину й прегабаліну. В одному з варіантів здійснення даний винахід націлений на створення способу лікування тривожного розладу й родинних патологічних розладів, який включає введення потребуючому цього суб'єкту комбінованої терапії в складі Сполуки № 8 або її фармацевтично прийнятної солі й однієї або декількох анксіолітичних сполук, вибраних із групи, що складається з бензодіазепінів, селективних інгібіторів зворотного захоплення серотоніну (SSRI) і селективних інгібіторів зворотного захоплення норадреналіну. В іншому варіанті здійснення, даний винахід націлений на створення способу лікування тривожного розладу й родинних патологічних розладів, який включає введення потребуючому цього суб'єкту комбінованої терапії в складі Сполуки № 8 або її фармацевтично прийнятної солі й одного або декількох анксіолітиків, вибраних із групи, що складається з бензодіазепінів, таких як діазепам, флуразепам, триазолам, лоразепам, алпразолам, хлордіазепам, оксазепам, темазепам і клоназепам; не-бензодіазепінових препаратів, таких як буспірон; селективних інгібіторів зворотного захоплення серотоніну, таких як флуоксетин, сертралін, пароксетин, циталопрам, флувоксамін і тому подібних; антагоністів рецептора серотоніну, таких як нефазадон і тому подібних; інгібіторів зворотного захоплення серотоніну й норадреналіну, таких як венлафаксин, мілнаципран і тому подібних, 3-(3-аміно-2-(R)-гідроксипропіл)-1-(4-фторфеніл)8-(8-метилнафтален-1-ілметил)-1,3,8-триазаспіро[4,5]декан-4-он, 2-(2-хлорфеніл)-2-(S) 8 UA 100552 C2 5 10 15 20 гідроксіетиловый ефір карбамінової кислоти (також відомої як карисбамат) і 1-[7-(4-бром-2,6диметилфеніл)-2,5-диметил-7H-піроло[2,3-d]піримідин-4-іл]-4-піперидинметанол. Переважно, щоб Сполука № 8 (або її фармацевтично прийнятна сіль) призначалася в якості комбінованої терапії з одним або більш анксіолітиками, вибраними із групи, що складається з діазепаму, венлафаксину, флуоксетину й прегабаліну. 1 В одному з варіантів здійснення даного винаходу R вибраний із групи, що складається з 2 водню й метилгрупи. В іншому варіанті здійснення даного винаходу R вибраний із групи, що 1 складається з водню й метилгрупи. Ще в одному з варіантів здійснення даного винаходу й R , і 2 1 2 R є атомом водню або R і R обидва є метильними групами. В одному з варіантів здійснення даного винаходу -(CH2)a- вибраний із групи, що складається з -CH2- і -CH2-CH2-. В іншому варіанті здійснення даного винаходу -(CH2)a- - це -CH2-. 4 В одному з варіантів здійснення даного винаходу R вибраний із групи, що складається з 4 водню й метилгрупи, переважно, щоб R був атомом водню. В одному з варіантів здійснення даного винаходу a - це 1. В одному з варіантів здійснення даного винаходу b - це ціле число від 0 до 2. В іншому варіанті здійснення даного винаходу c - це ціле число від 0 до 2. В іншому варіанті здійснення даного винаходу b - це ціле число від 0 до 1. В іншому варіанті здійснення даного винаходу c це ціле число від 0 до 1. Ще в одному з варіантів здійснення даного винаходу сума b і c - це ціле число від 0 до 2, переважно ціле число від 0 до 1. Ще в одному з варіантів здійснення даного винаходу b - це ціле число від 0 до 2 і c - це 0. R В одному з варіантів здійснення даного винаходу складається з O вибраний із групи, що O O (R5)b 5 (R )b (R5)b O , O , , 5 (R )c O O (R5)b 5 (R )b O 25 O і . В іншому варіанті R здійснення даного винаходу вибраний із групи, що складається O O 5 (R )b (R5)b O з O , і 5 (R )c O 5 (R )b O . R 30 В одному з варіантів здійснення даного винаходу вибраний із групи, що складається з 2-(2,3-дигідробензо[1,4]діоксинілу), 2-(бензо[1,3]діоксолілу), 3-(3,4дигідробензо[1,4]діоксепінілу), 2-(6-хлор-2,3-дигідробензо[1,4]діоксинілу), 2-(6-фтор-2,3 9 UA 100552 C2 5 дигідробензо[1,4]діоксинілу), 2-(хроманіл), 2-(5-фтор-2,3-дигідробензо[1,4]діоксинілу), 2-(7-хлор2,3-дигідробензо[1,4]діоксинілу), 2-(6-хлорбензо[1,3]діоксолілу), 2-(7-нітро-2,3дигідробензо[1,4]діоксинілу), 2-(7-метил-2,3-дигідробензо[1,4]діоксинілу), 2-(5-хлор-2,3дигідробензо[1,4]діоксинілу), 2-(6-бром-2,3-дигідробензо[1,4]діоксинілу), 2-(6,7-дихлор-2,3дигідробензо[1,4]діоксинілу), 2-(8-хлор-2,3-дигідробензо[1,4]діоксинілу), 2-(2,3-дигідронафто[2,3b][1,4]діоксинілу) і 2-(4-метилбензо[1,3]діоксолілу). R 10 В іншому варіанті здійснення даного винаходу вибраний із групи, що складається з 2-(бензо[1,3]діоксолілу), 2-(2,3-дигідробензо[1,4]діоксинілу), 2-(6-хлор-2,3дигідробензо[1,4]діоксинілу), 2-(7-хлор-2,3-дигідробензо[1,4]діоксинілу), 2-(7-метил-2,3дигідробензо[1,4]діоксинілу), 2-(6-бром-2,3-дигідробензо[1,4] діоксинілу) і 2-(6,7-дихлор-2,3 R 15 20 25 30 дигідробензо[1,4]діоксинілу). В іншому варіанті здійснення даного винаходу вибраний із групи, що складається з 2-(2,3-дигідробензо[1,4]діоксинілу), 2-(7-метил-2,3дигідробензо[1,4]діоксинілу) і 2-(6-бром-2,3-дигідробензо[1,4]діоксинілу). 5 В одному з варіантів здійснення даного винаходу R вибраний із групи, що складається з 5 галогену й нижчого алкілу. В іншому варіанті здійснення даного винаходу R вибраний із хлор-, фтор-, бром- і метилгруп. В одному з варіантів здійснення даного винаходу стереохімічний центр сполуки з формулою (I) має S-конфігурацію. В іншому варіанті здійснення даного винаходу стереохімічний центр сполуки з формулою (I) має R-конфігурацію. В одному з варіантів здійснення даного винаходу сполука формули (I) є присутньою у збагаченій енантіомерами суміші, де відсоток збагачення енантіомерами - більше 75 %, переважно - більше 90 %, більш переважно - більше 95 % і найбільше переважно - більше 98 %. Додаткові варіанти здійснення даного винаходу включають ті, де для однієї або більше 1 2 3 4 змінних, визначених тут, вибрані замісні групи (тобто R , R , R , R , X-Y і A) є незалежно вибраними в якості індивідуальних замісників, або є компонентами певної вибірки замісників, вибраної з повного списку, визначеного даним документом. Приклади сполук, пропонованих даним винаходом, перераховані нижче в таблиці 1. Додаткові сполуки, розглянуті в рамках даного винаходу, приводяться в таблиці 3. У нижчеподаних таблицях 1 і 2, у стовпчику, озаглавленому "стерео", визначається стереоконфігурація біля атома вуглецю гетероциклу в місці з'єднання. У випадку відсутності додаткових вказівок, сполука була приготовлена у вигляді суміші стереоконфігурацій. У випадках наявності приміток "R" або "S", стереоконфігурація визначалася на підставі збагачення вихідного матеріалу енантіомерами. Таблиця 1 Приклади сполук, описуваних формулою (I) R4 R № 1 2 3 4 5 6 * (CH2)a O N S 1 R N 2 R O Стерео (CH2)a R 2-(2,3-дигідробензо[1,4]діоксиніл) 2-(бензо[1,3]діоксоліл) 3-(3,4-дигідро2H-бензо[1,4]діоксепініл) 2-(2,3-дигідробензо[1,4]діоксиніл) 2-(2,3-дигідробензо[1,4]діоксиніл) 2-(2,3-дигідробензо[1,4]діоксиніл) S R 10 CH2 CH2 CH2 CH2 CH2 CH2 NR 4 NH NH NH NH NH NH R 1 R 2 H H H H H H H H H H метил метил UA 100552 C2 Продовження таблиці 1 7 8 9 10 13 14 15 16 18 19 20 22 24 29 30 33 35 2-(2,3-дигідробензо[1,4]діоксиніл) 2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл) 2-(6-фтор-2,3-дигідробензо[1,4]діоксиніл) 2-(хроманіл) 2-(5-фтор-2,3-дигідробензо[1,4]діоксиніл) 2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл) 2-(6-хлорбензо[1,3]діоксоліл) 2-(2,3-дигідробензо[1,4]діоксиніл) 2-(7-нітро-2,3-дигідробензо[1,4]діоксиніл) 2-(7-метил-2,3-дигідробензо[1,4]діоксиніл) 2-(5-хлор-2,3-дигідробензо[1,4]діоксиніл) 2-(8-метокси-2,3-дигідробензо[1,4]діоксиніл) 2-(6-бром-2,3-дигідробензо[1,4]діоксиніл) 2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл) 2-(8-хлор-2,3-дигідробензо[1,4]діоксиніл) 2-(2,3-дигідронафто[2,3-b][1,4]діоксиніл) 2-(4-метилбензо[1,3]діоксоліл) CH2 N(CH3) CH2 NH CH2 NH CH2 NH CH2 NH CH2 NH CH2 NH CH2CH2 NH CH2 NH CH2 NH CH2 NH CH2 NH CH2 NH CH2 NH CH2 NH CH2 NH CH2 NH S S S S S S S S S S S S H H H H H H H H H H H H H H H H H H H H H H H H H H H H H H H H H H Таблиця 2 Додаткові сполуки, пропоновані даним винаходом R14 O Y № 23 26 32 34 36 5 10 15 20 * N X S O 11 R N R12 14 11 12 Стерео Y 2-(5-метокси-2,3-дигідробензо[1,4]діоксиніл) 2-(6-метилкарбоніл-2,3-дигідробензо[1,4]діоксиніл) 2-(6-метоксикарбоніл-2,3дигідробензо[1,4]діоксиніл) 2-(6-гідроксиметил-2,3-дигідробензо[1,4]діоксиніл) 2-(7-аміно-2,3-дигідробензо[1,4]діоксиніл) Х S S CH2 CH2 NH NH H H H H S CH2 NH H H S S CH2 CH2 NH NH H H H H NR R R Якщо тільки не вказується інше, використовуваний тут термін "галоген" означає хлор, бром, фтор і йод. Якщо тільки не вказується інше, використовуваний тут або самостійно, або в складі замісної групи термін "алкіл" включає прямі й розгалужені ланцюжки. Наприклад, алкільні радикали включають метил, етил, пропіл, ізопропіл, бутил, ізобутил, втор-бутив, трет-бутил, пентил і тому подібні. Якщо тільки не вказується інше, "нижчий" при використанні в комбінації з алкілом означає вуглецевий ланцюг, що складається з 1-4 атомів вуглецю. Якщо тільки не вказується інше, використовуваний тут термін "алкокси" означає кисеньвмісний ефірний радикал вищеописаних прямих або розгалужених алкільних груп. Наприклад, метокси, етокси, n-пропокси, втор-бутокси, трет-бутокси, n-гексилокси й тому подібні. Використовуване тут примітка «*» означає наявність стереогенного центру. Коли певна група "заміщається" (наприклад, алкіл, арил і т.д.), ця група може мати один або більше замісників, переважно від одного до п'яти замісників, більш переважно від одного до трьох замісників, найбільш переважно від одного до двох замісників, незалежно вибраних зі списку замісних груп. 11 UA 100552 C2 5 Стосовно замісників термін "незалежно" означає, що коли можливе заміщення більш ніж одним замісником, ці замісники можуть бути однакові, або можуть відрізнятися один від іншого. У рамках стандартної номенклатури, використовуваної в даний заявці на винахід, кінцева частина певного бічного ланцюга описується першою, потім йде опис прилеглих функціональних груп, аж до точки прикріплення бічного ланцюга. Так, наприклад, "феніл-алкіламіно-карбоніл-алкіл" замісник описує групу формули (алкіл) (алкіл) . Наступні скорочення використані в технічному описі, особливо в схемах і прикладах: DCC DCE DCM DIPEA або DIEA DMF DMSO EDC Et3N або TEA Et2O EA або Etoac Etoh IPA Hept HOBT HPLC LAH M або Meoh NМР Pd-C RP HPLC RT або rt TEA TFA THF TLC = = = = = = = = = = = = = = = = = = = = = = = = = Дициклогексил карбодіімід Дихлоретан Дихлорметан Діізопропілетиламін N, N-Диметилформамід Диметилсульфоксид Етилкарбодіімід Триетиламін Діетиловий ефір Етилацетат Етанол 2-пропанол Гептан 1-гідроксибензотриазол Високоефективна рідинна хроматографія Алюмогідрид літію Метанол Ядерний магнітний резонанс Паладієвий каталізатор на вуглецевому носії Зворотно-фазоваа високоефективна рідинна хроматографія Кімнатна температура Триетиламін Трифтороцтова кислота Тетрагідрофуран Тонкошарова хроматографія 10 15 20 25 30 У тих випадках, коли сполуки, відповідно до даного винаходу, мають принаймні один хиральний центр, вони можуть відповідно існувати у формі енантіомерів. У тих випадках, коли сполуки мають два або більше хиральних центрів, вони додатково можуть існувати у формі діастереомерів. Необхідно розуміти, що всі подібні ізомери і їх суміші попадають у рамки даного винаходу. Більше того, деякі із кристалічних форм цих сполук можуть існувати у вигляді поліморфів, при цьому передбачається, що вони також підпадають під дію даного винаходу. На додаток, деякі із сполук можуть утворювати сольвати в поєднанні з водою (наприклад, гідрати) або широко розповсюдженими органічними розчинниками, при цьому також передбачається, що такі сольвати попадають у фокус даного винаходу. Для використання в медичних цілях солі сполук, розглянутих у рамках даного винаходу, описуються як нетоксичні "фармацевтично прийнятні солі". Інші солі можуть, однак, бути використані в процесі одержання сполук, описуваних даним винаходом, або їх фармацевтично прийнятних солей. Фармацевтично прийнятні солі таких сполук включають солі додаткових кислот, які можуть, наприклад, утворюватися при змішуванні розчину сполуки з розчином фармацевтично прийнятної кислоти, такої як соляна кислота, сірчана кислота, фумарова кислота, малеїнова кислота, бурштинова кислота, оцтова кислота, бензойна кислота, лимонна кислота, виннокам'яна кислота, вугільна кислота або фосфорна кислота. Більше того, у випадках, коли сполуки, описувані в рамках даного винаходу, несуть кислотний фрагмент, їх фармацевтично прийнятні солі можуть включати солі лужних металів, наприклад, солі натрію або калію; солі лужноземельних металів, наприклад, солі кальцію й магнію; а також солі, 12 UA 100552 C2 5 10 15 20 25 30 35 утворені прийнятними органічними лігандами, наприклад четвертинні амонієві солі. Так, приклади фармацевтично прийнятних солей включають наступні: ацетат, бензенсульфонат, бензоaт, бікарбонат, бісульфат, бітартрат, борат, бромід, кальцію едетат, камзилат, карбонат, хлорид, клавуланат, цитрат, дигідрохлорид, едетат, едизилат, естолат, езилат, фумарат, глюцептат, глюконат, глутамат, гліколіларсанілат, гексилрезорцинат, гідрабамін, гідробромід, гідрохлорид, гідроксинафтоат, йодид, ізотіонат, лактат, лактобіонат, лаурат, малат, малеат, манделат, мезилат, метилбромід, метилнітрат, метилсульфат, мукат, напсилат, нітрат, сіль N-метилглюкамін амонію, олеат, памоат (ембонат), пальмітат, пантотенат, фосфат/дифосфат, полігалактуронат, саліцилат, стеарат, сульфат, субацетат, сукцинат, танат, тартрат, теоклат, тозилат, триетйодид і валерат. Прикладами кислот і основ, які можуть використовуватися в процесі одержання фармацевтично прийнятних солей, є наступні: кислоти, включаючи оцтову кислоту, 2,2-дихлороцтову кислоту, ациловані амінокислоти, адипінову кислоту, альгінову кислоту, аскорбінову кислоту, L-аспарагінову кислоту, бензенсульфонову кислоту, бензойну кислоту, 4-ацетамідoбензойну кислоту, (+)-камфорну кислоту, камфорсульфокислоту, (+)-(1S)-камфор-10-сульфонову кислоту, капринову кислоту, капронову кислоту, каприлову кислоту, коричну кислоту, лимонну кислоту, цикламінову кислоту, додецилсірчану кислоту, етан--1,2-дисульфонову кислоту, етансульфонову кислоту, 2гідроксіетансульфонову кислоту, мурашину кислоту, фумарову кислоту, галактарову кислоту, гентизинову кислоту, глюкогептонову кислоту, D-глюконову кислоту, D-глюкоронову кислоту, Lглютамінову кислоту, α-оксо-глютарову кислоту, гліколеву кислоту, гіпуринову кислоту, гідробромову кислоту, соляну кислоту, (+)-L-молочну кислоту, (±)- DL-молочну кислоту, лактобіонову кислоту, малеїнову кислоту, (-)-L-оксибурштинову кислоту, малонову кислоту, (±)DL-мигдальну кислоту, метансульфонову кислоту, нафтален-2-сульфонову кислоту, нафтален1,5-дисульфонову кислоту, 2-нафтойну кислоту, нікотинову кислоту, азотну кислоту, олеїнову кислоту, оротову кислоту, щавлеву кислоту, пальмітинову кислоту, памову кислоту, фосфорну кислоту, L-піроглютамову кислоту, саліцилову кислоту, аміно-саліцилову кислоту, себацинову кислоту, стеаринову кислоту, бурштинову кислоту, сірчану кислоту, дигалову кислоту, (+)-Lвиннокам'яну кислоту, тіоціанову кислоту, p-толуенсульфонову кислоту й ундециленову кислоту; і основи, включаючи аміак, L-аргінін, бенетамін, бензатин, кальцію гідроксид, холін, динол, діетаноламін, діетиламін, 2-(діетиламіно)-етанол, етаноламін, етилендіамін, N-метилглюкамін, гідрабамін, 1H-імідазол, L-лізин, магнію гідроксид, 4-(2-гідроксіетил)-морфолін, піперазин, калію гідроксид, 1-(2-гідроксіетил)-піролідин, вторинний амін, натрію гідроксид, триетаноламін, трометамін і цинку гідроксид. Сполуки формули (I) можуть бути одержані в результаті процесу, представленого на схемі 1. R4 O O H2N * (CH2)a NH2 R * O R4 R S (CH2)a S NH2 O (Ia) NH (X) S R4 O 1 O Cl R N R * (CH2)a R O (XI) N S O 2 40 N R1 N R2 (I) Схема 1 Таким чином, належно заміщена сполука формули (X), відома сполука або сполука, одержана за допомогою відомих способів, реагує із сульфамідом, відомою сполукою, в якій сульфамід переважно присутній у кількості, що варіюється від 2 до 5 еквівалентів в органічному розчиннику, такому як THF, діоксан і їм подібні, переважно при підвищеній температурі, що 13 UA 100552 C2 5 варіюється в межах від 50 °C до 100 °C, більш переважно приблизно при температурі флегми, у результаті відбувається утворення відповідної сполуки формули (Ia). Як варіант належно заміщена сполука формули (X), відома сполука або сполука, одержана за допомогою відомих способів, реагує з належно заміщеною сполукою формули (XI), відомою сполукою або сполукою, одержаною за допомогою відомих способів, у присутності основи, такої як TEA, DIPEA, піридин і їм подібні, у присутності органічного розчинника, такого як DMF, DMSO і їм подібні, у результаті чого відбувається утворення відповідної сполуки формули (I). O 5 (R )b R 10 O Сполуки формули (X), де – це отримані відповідно до процесу, представленого на схемі 2. , можуть бути (нижчий алкіл) 15 20 Схема 2 Таким чином, належно заміщена сполука формули (XII), відома сполука або сполука, одержана за допомогою відомих способів (наприклад, як описано вище в схемі 3), реагує з NH4OH, відомою сполукою, причому можливою, але не обов'язковою, умовою є використання органічного розчинника, такого як ацетонітрил і йому подібні, у результаті чого відбувається утворення відповідної сполуки формули (XIII). Сполука формули (XIII) взаємодіє з належним чином вибраним відновником, таким як LAH і йому подібні, у присутності органічного розчинника, такого як THF, діетиловий ефір і подібні, у результаті чого відбувається утворення відповідної сполуки формули (Xa). O (R3)b R Сполука формули (X), де вибрано з отримані відповідно до процесу, представленого на схемі 3. , можуть бути 25 O O O (CH2)0-1 O OH 5 (R )b NH2 (R5)b (XIV) (XV) O (CH2)0-1 NH2 5 (R )b (Xb) Схема 3 14 (CH2)0-1 UA 100552 C2 5 Таким чином, належно заміщена сполука формули (XIV), відома сполука або сполука, одержана за допомогою відомих способів, взаємодіє з NH 4OH, у присутності єднального агента, такого як DCC і йому подібні, причому можливою, але не обов'язковою, умовою є використання органічного розчинника, такого як ацетонітрил і йому подібні, у результаті чого відбувається утворення відповідної сполуки формули (XV). Сполука формули (XV) взаємодіє з належним чином вибраним відновником, таким як LAH і йому подібні, у присутності органічного розчинника, такого як THF, діетиловий ефір і подібні, у результаті чого відбувається утворення відповідної сполуки формули (Xb). O (R5)b R 10 O Сполука формули (X), де вибраний з можуть бути отримані відповідно до процесу, представленого на схемі 4. O O J1 (R5)b і де a - це 2, CN 5 (R )b O (XVII) O (XVI) O NH2 (R5)b O (Xc) 15 20 Схема 4 1 Таким чином, належно заміщена сполука формули (XVI), де J є належною групою, що заміщається, такою як Br, Cl, I, тозил, мезил, трифліл і їм подібні, відома сполука або сполука, одержана за допомогою відомих способів (наприклад, за допомогою активації відповідної J сполуки, де 1 - це OH), взаємодіє із ціанідом, таким як ціанід калію, ціанід натрію і їм подібні, в органічному розчиннику, такому як DMSO, DMF, THF і їм подібні, у результаті чого відбувається утворення відповідної сполуки формули (XVII). Сполука формули (XVII) відновлюється згідно з відомими способами, наприклад, у результаті взаємодії з придатним відновником, таким як LAH, борган і їм подібні, у результаті чого відбувається утворення відповідної сполуки формули (Xc). 25 O (R5)b R O Сполука формули (X), де вибраний з можуть бути одержані відповідно до процесу, представленого на схемі 5. O 5 O OH 5 (R )b (R )b O (XIX) O (XVIII) 15 і де a - це 1, J2 UA 100552 C2 O N O O O (R5)b O (XX) 5 10 15 NH2 (R5)b O (Xd) Схема 5 Таким чином, належно заміщена сполука формули (XVIII), відома сполука або сполука, одержана за допомогою відомих способів, активується за допомогою відомого способу, у 2 результаті чого відбувається утворення відповідної сполуки формули (XIX), де J є групою, що заміщається, такою як тозилат, Cl, Br, I, мезилат, трифлат і їм подібні. Сполука формули (XIX) вступає у взаємодію із сіллю фталіміду, такою як фталімід калію, фталімід натрію і їм подібні, в органічному розчиннику, такому як DMF, DMSO, ацетонітрил і їм подібні, переважно при підвищеній температурі, що варіюється в межах від 50 °C до 200 °C, більш переважно, приблизно при температурі флегми, у результаті відбувається утворення відповідної сполуки формули (XX). Сполука формули (XX) вступає у взаємодію з N 2H4, відомою сполукою, в органічному розчиннику, такому як етанол, метанол і їм подібні, переважно при підвищеній температурі, що варіюється в межах від 50 °C до 100 °C, більш переважно приблизно при температурі флегми, у результаті відбувається утворення відповідної сполуки формули (Xd). R Фахівцеві буде зрозуміло, що сполуки формули (X), (R )c O O 5 (R )b (R )b O з O , 3 , 5 (R )c (R )c O O 3 5 (R )b (R )b O O , 3 (R )c , 5 (R )c O O (R5)b (R3)b 25 вибраний (R )c 3 20 де 5 3 O O або , можуть бути одержані подібним образочином, згідно з відомими способами, або, наприклад, відповідно до процесів, описаних вище, на схемах від 2 до 5, за допомогою відбору й заміщення відповідними нафтил-зв'язаними сполуками бензо-зв'язаних початкових матеріалів. Фахівцеві буде далі зрозуміло, що у випадку, коли бажане одержання одиничного енантіомеру (або суміші енантіомерів, в якій проведено збагачення у відношенні одного з енантіомерів) сполуки формули (X) можуть використовуватися вищевказані процеси, окреслені 16 UA 100552 C2 5 10 15 20 25 30 35 40 45 50 55 60 схемами з 1 по 5, при цьому відповідний початковий матеріал може заміщатися відповідним одиничним енантіомером (або сумішшю енантіомерів, в якій проведено збагачення у відношенні одного з енантіомерів). Фахівцеві буде зрозуміло, що в той час як реакційний стадія, описувана даним винаходом, може протікати в різноманітних розчинниках або системах розчинників, згадана реакційна стадія також може протікати в сумішах прийнятних розчинників або систем розчинників. У тих випадках, коли процеси одержання сполук відповідно до даного винаходу приводять до утворення суміші стереоізомерів, ці ізомери можуть бути ізольовані за допомогою широко відомих способів, таких як препаративна хроматографія. Сполуки можуть бути одержані в рацемічній формі, або індивідуальні енантіомери можуть бути одержані в результаті енантіоспецифічного синтезу, або за допомогою розділення. Сполуки можуть, наприклад, бути розділені на складаючі їх енантіомери за допомогою стандартних способів, таких як утворення діастереометричних пар за допомогою утворення солей з оптично активними кислотами, як, наприклад, (-)-ди-p-толуоїл-D-виннокам'яна кислота й (або) (+)-ди-p-толуоїл-L-виннокам'яна кислота з наступною фракційною кристалізацією й відновленням вільної основи. Сполуки можуть також бути розділені за допомогою утворення діастереометричних ефірів або амідів, з наступним хроматографічним розділенням і видаленням хирального партнера. Як варіант, сполуки можуть бути розділені за допомогою хиральної колонки для HPLC. У ході процесів одержання сполук, що становлять предмет даного винаходу, може виникнути необхідність у захисті чутливих або реакційних груп на кожній з розглянутих молекул. Це може бути досягнуте за допомогою використання стандартних захисних груп, таких як описані в роботі Protective Groups in Organic Chemistry, ed. J.F.W. Mcomie, Plenum Press, 1973; а також T.W. Greene & P.G.M. Wuts, Protective Groups in Organic Synthesis, John Wiley & Sons, 1991. Ці захисні групи можуть бути згодом вилучені, на будь-який зручній для цього стадії, з використанням відомих фахівцям способів. Даний винахід також описує фармацевтичні склади, що містять одну або більше сполук формули (I) разом з фармацевтично прийнятним носієм. Фармацевтичні склади, що містять як активні інгредієнти одну або більше сполук, описуваних даним винаходом, можуть бути приготовлені за допомогою ретельного змішування сполуки або сполук із фармацевтичним носієм, відповідно до стандартних фармацевтичних технологій готування сумішей. Носій може мати широку різноманітність форм, залежно від передбачуваного способу введення (наприклад, пероральний, парентеральний). Так, для рідких пероральних лікарських форм, таких як суспензії, еліксири й розчини, прийнятні носії й добавки включають воду, гліколі, масла, спирти, смакові добавки, консерванти, стабілізатори, барвники й тому подібні; для твердих пероральних лікарських форм, таких як порошки, капсули й таблетки, прийнятні носії й добавки включають крохмалі, цукри, розріджувачі, гранулоутворювальні агенти, змащувальні речовини, зв'язувальні речовини, добавки для поліпшення деградації таблеток і тому подібні. Тверді пероральні лікарські форми також можуть покриватися оболонками з таких речовин, як цукор, або покриватися кишково-розчинним покриттям, для модулювання основного місця усмоктування. Для парентерального введення носій буде, як правило, складатися зі стерильної води, при цьому з метою поліпшення розчинності або консервації можуть додаватися інші інгредієнти. Суспензії або розчини, що вводяться інъ'єційно, також можуть виготовлятися з використанням водних носіїв разом з відповідними добавками. Для готування фармацевтичних складів, описуваних даним винаходом, одна або більше сполук, описуваних даним винаходом як активні інгредієнти, ретельно змішуються з фармацевтичним носієм, відповідно до стандартних фармацевтичних технологій готування сумішей, при цьому такий носій може мати широку різноманітність форм, залежно від лікарської форми, необхідної для передбачуваного способу введення, наприклад, перорального або парентерального, такого як внутрішньом'язове введення. При виготовленні пероральних лікарських форм можуть використовуватися будь-які зі звичайних фармацевтичних середовищ. Так, для рідких пероральних лікарських форм, таких як суспензії, еліксири й розчини, прийнятні носії й добавки включають воду, гліколі, масла, спирти, смакові добавки, консерванти, барвники й тому подібні; для твердих пероральних лікарських форм, таких як порошки, капсули, таблетки у формі капсул, і таблетки, прийнятні носії й добавки включають крохмалі, цукри, розріджувачі, гранулоутворювальні агенти, змащувальні речовини, зв'язувальні речовини, добавки для поліпшення деградації таблеток і тому подібні. У зв'язку з легкістю введення, таблетки й капсули являють собою найбільш зручну у вживанні пероральну дозовану лікарську форму, в якій з очевидністю використовуються тверді фармацевтичні носії. При необхідності таблетки можуть покриватися оболонкою із цукрів або кишково-розчинним покриттям за допомогою стандартних способів. Для парентеральних лікарських форм носій буде, як правило, складатися зі 17 UA 100552 C2 5 10 15 20 25 30 35 40 45 50 55 60 стерильної води, хоча інші інгредієнти, наприклад, з метою поліпшення розчинності або для консервації, можуть також включатися до складу. Також можуть виготовлятися суспензії, що вводяться ін'єкційно, у цьому випадку можуть використовуватися відповідні рідинні носії, суспендуючі агенти й тому подібні компоненти. Описувані тут фармацевтичні склади будуть містити, розраховуючи на одиницю дози, наприклад, таблетку, капсулу, дозу порошку, ін'єкцію, чайну ложку й т.п., таку кількість активного інгредієнта, яка необхідна для забезпечення ефективної дози, відповідно до опису, наведеного вище. Описувані тут фармацевтичні склади будуть містити, розраховуючи на одиницю дози, наприклад, таблетку, капсулу, дозу порошку, ін'єкцію, супозиторій, чайну ложку й тому подібні одиниці, від 0,1 до 1000 мг і можуть призначатися в кількості приблизно від 0,01 до 200 мг/кг/день, переважно приблизно від 0,1 до 100 мг/кг/день, більш переважно приблизно від 0,5 до 50 мг/кг/день, більш переважно приблизно від 1,0 до 25,0 мг/кг/день, або в будь-яких описаних тут межах. Дози, однак, можуть варіюватися, залежно від потреби пацієнта, тяжкості розладу й використовуваної сполуки. Можливе щоденне дозування, або періодична ревізія дози. Переважне використання цих складів у вигляді дозованих лікарських форм, наприклад, у вигляді таблеток, пігулок, капсул, дозованих порошків, гранул, стерильних розчинів або суспензій для парентерального введення, дозованих аерозолів або рідин для розбризкування, крапель ампул, аутоін'єкторів або супозиторіїв; для перорального, парентерального, інтраназального, сублінгвального або ректального прийому, або для введення за допомогою інгаляції або вдування. Як варіант, склад може бути представлений у вигляді лікарської форми, що призначається один раз на тиждень або місяць; наприклад, нерозчинна сіль активної сполуки, така як деканоат, може бути адаптована для внутрішньом'язової ін'єкції з формуванням тканинного депо. Для виготовлення твердих лікарських форм, таких як таблетки, основний активний інгредієнт змішується з фармацевтичним носієм, наприклад, звичайними інгредієнтами, використовуваними для готування таблеток, такими як кукурудзяний крохмаль, лактоза, сахароза, сорбітол, тальк, стеаринова кислота, стеарат магнію, дикальцію фосфат або камедь, й іншими фармацевтичними розріджувачами, наприклад водою, з утворенням твердого переформулюючого складу, що містить гомогенну суміш сполук, що описуються даним винаходом, або їх фармацевтично прийнятних солей. Характеристика таких переформулюючих складів як гомогенних означає, що активні інгредієнти рівномірно дисперговані всередині складу, так що склад може бути негайно поділений на рівноефективні дозовані лікарські форми, такі як таблетки, пилюлі Такий твердий переформулюючий склад потім виявляється поділеним на дозовані лікарські форми описаних вище типів, що містять від 0,1 до приблизно 1000 мг активного інгредієнта, описуваного даним винаходом. Таблетки або пігулки такого нового складу можуть покриватися оболонкою, або інакше формуватися для того, щоб забезпечувати створення дозованої лікарської форми, що має переваги тривалої дії. Наприклад, таблетка або пігулка може включати внутрішній і зовнішній дозовані компоненти, останній з яких є свого роду конвертом, який містить попередній компонент. Ці два компоненти можуть бути розділені кишково-розчинним шаром, який служить для захисту від розщеплення в шлунку й дозволяє внутрішньому компоненту виявитися в просвіті дванадцятипалої кишки, зберігши свою інтактність, або сприяє його пролонгованому вивільненню. Для створення подібних кишковорозчинних оболонок або шарів можуть бути використані різні матеріали, що включають ряд полімерних кислот з такими матеріалами, як шелак, цетиловий спирт і ацетат целюлози. Рідкі лікарські форми, що містять нові склади даного винаходу, можуть бути інкорпоровані для перорального введення, або для введення ін'єкційним шляхом і включають водні розчини, сиропи з відповідними смаковими добавками, водні або масляні суспензії й емульсії з відповідними смаковими добавками і їстівними оліями, такими як бавовняна олія, кунжутна олія, кокосова олія або арахісова олія, також як і еліксири й подібні лікарські засоби доставки. Прийнятні диспергуючі або суспендуючі агенти для водних суспензій включають синтетичну або природну камедь, таку як трагакант, гуміарабік, альгінат, декстран, карбоксиметилцелюлозу натрію, метилцелюлозу, полівінілпіролідон або желатин. Спосіб лікування тривожного розладу й родинних патологічних розладів, описуваних даним винаходом, може також здійснюватися з використанням фармацевтичного складу, що містить кожну з описаних тут сполук і фармацевтично прийнятний носій. Фармацевтичний склад може містити від 0,1 до 1000 мг, переважно приблизно від 50 до 500 мг, сполуки й може бути сформований у вигляді будь-якої форми, придатної для цілей вибраного способу прийому ліків. Носії включають необхідні й інертні фармацевтичні наповнювачі, включаючи, але не обмежуючись цим зв'язувальні речовини, суспендуючі агенти, змащувальні речовини, ароматизатори, підсолоджувачі, консерванти, барвники й оболонки. Склади, прийнятні для перорального введення, включають тверді форми, такі як пігулки, таблетки, таблетки у формі 18 UA 100552 C2 5 10 15 20 25 30 35 40 45 50 55 60 капсул, капсули (кожна включає варіанти з негайним вивільненням, пролонгованим і вповільненим вивільненням), гранули, порошки, і рідкі форми, такі як розчини, сиропи, еліксири, емульсії й суспензії. Форми, прийнятні для парентерального введення, включають стерильні розчини, емульсії й суспензії. Переважно, сполуки, розглянуті даним винаходом, можуть призначатися у вигляді однократної денної дози, або сумарна денна доза може призначатися багаторазовими дозами двічі, тричі або чотири рази на день. Більше того, сполуки, розглянуті даним винаходом, можуть призначатися інтраназально за допомогою місцевого використання прийнятних інтраназальних засобів доставки, або за допомогою трансдермальних шкірних пластирів, добре відомих фахівцям у даній галузі. Для того щоб призначатися трансдермально, доставка повинна, без сумніву, бути безперервною, а не перемежованою протягом усього режиму дозування. Наприклад, для перорального введення у формі таблетки або капсули, активний компонент ліків може комбінуватися з пероральним, нетоксичним, фармацевтично прийнятним інертним носієм, таким як етанол, гліцерол, вода і їм подібні. Більше того, якщо буде потреба або за бажанням, можуть використовуватися відповідні зв'язувальні речовини; змащувальні речовини, дезінтегруючі агенти, барвники, також можуть бути включені в суміш. Придатні зв'язувальні речовини включають, без обмеження, крохмаль, желатин, природні цукри, такі як глюкоза або бета-лактоза, підсолоджувач із кукурудзи, природні й синтетичні камеді, такі як гуміарабік, трагакант або олеат натрію, стеарат натрію, стеарат магнію, бензоат натрію, ацетат натрію, хлорид натрію і їм подібні сполуки. Дезінтегратори включають, без обмеження, крохмаль, метилцелюлозу, агар, бентоніт, ксантанову камедь і їм подібні. Рідкі форми у відповідним чином ароматизованих суспендуючих або диспергуючих агентах, таких як синтетичні й природні камеді, наприклад, трагакант, гуміарабік, метилцелюлоза і їм подібні. Для парентерального введення необхідні стерильні суспензії й розчини. Ізотонічні середовища, що звичайно містять придатні консерванти, застосовуються в тих випадках, коли потрібне внутрішньовенне введення. Сполуки, що розглядаються даним винаходом, можуть призначатися в кожній зі згаданих вище композицій і відповідно до встановлених у даній галузі дозовими режимами, у випадках коли потрібне проведення лікування у зв'язку із тривожним розладом і родинними патологічними розладами. Добова доза препаратів може варіюватися в широких межах, що становлять для дорослого пацієнта від 0,01 до 200 мг/кг на день. Для перорального введення фармацевтичні склади переважно поставляються у вигляді таблеток, що містять 0,01, 0,05, 0,1, 0,5, 1,0, 2,5, 5,0, 10,0, 15,0, 25,0, 50,0, 100, 150, 200, 250, 500 і 1000 мг активного інгредієнта, з метою симптоматичної корекції дози в пацієнта, що одержує лікування. Ефективна кількість ліків звичайно забезпечується дозою на рівні приблизно від 0,01 мг/кг до 200 мг/кг ваги тіла на день, або в іншому діапазоні в цій межі. Переважно, щоб цей діапазон становив приблизно від 0,1 до 100,0 мг/кг ваги тіла на день, більш переважно, щоб він становив приблизно від 0,5 мг/кг до 50 мг/кг, більш переважно приблизно від 1,0 до 25,0 мг/кг ваги тіла на день. Сполуки можуть призначатися з режимом від 1 до 4 раз на день. Оптимальні призначувані дози можуть легко визначатися фахівцями й будуть варіюватися залежно від використовуваної сполуки, способу введення, сили препарату й ступені виразності патологічного розладу. На додаток, фактори, пов'язані з особистими особливостями конкретних пацієнтів, включаючи вік, вагу, особливості харчування й час введення препарату, у результаті зажадають корекції доз препаратів, що вводяться. Фахівцеві буде зрозуміло, що випробування як in vivo, так і in vitro, проведені з використанням придатних, відомих і загальноприйнятих клітинних і (або) тваринних моделей, дозволяють приблизно оцінювати здатність тестованої сполуки виявляти лікувальну або профілактичну дію стосовно даного захворювання. Фахівцеві також буде зрозуміло, що клінічні випробування на людях, включаючи первинні випробування на людині, оцінку ефективності доз, випробування на групах здорових добровольців і (або) пацієнтів, що страждають даним захворюванням, можуть здійснюватися відповідно до способів, добре відомих у медичній і клінічній практиці. Наступні приклади пропонуються з метою сприяння розумінню суті даного винаходу й не призначені для того (і не повинні бути так витлумачені), щоб обмежувати яким-небудь чином рамки даного винаходу, що розкривається в наведених далі пунктах його формули. Приклад 1 ((3,4-дигідро-2H-бензо[b][1,4]діоксипін-3-іл)метил)сульфамід (Сполука № 3) 19 UA 100552 C2 O O O HN S NH2 O 5 10 15 20 25 30 Катехол (5,09 г, 46,2 ммоль) і калію карбонат змішували в присутності ацетонітрилу й нагрівали до температури флегми протягом однієї години. Додавався 2-хлорметил-3-хлор-1пропен (5,78 г, 46,2 ммоль), і реакція була продовжена при температурі флегми протягом наступних 24 годин. Розчин був охолоджений до кімнатної температури й профільтрований. Фільтрат був підданий випаровуванню, залишок розведений водою й екстрагований за допомогою діетилового ефіру (3 x). Комбінований органічний розчин був висушений у присутності MgSO4 і піддадуть концентруванню. Хроматографія (2 % етилового ефіру в гексані) дозволила одержати 3-метилен-3,4-дигідро-2H-бензо[b][1,4]діоксипін у вигляді безбарвної маслянистої рідини. + MS (ESI) (мас-спектрометрія з іонізацією електророзпиленням): 163,2 (M+H ) 1H ЯМР (300 МГц, CdСl3), δ: 6,94 (м, 4H), 5,07 (с, 2H), 4,76 (с, 4H). 3-метилен-3,4-дигідро-2H-бензо[b][1,4]діоксепін (5,00 г, 30,8 ммоль) був розчинений у безводному THF (100 мол). Боран-THF (1,0 M в THF, 10,3 мл) був доданий при температурі 0 °C. Реакційна суміш була піддана перемішуванню при кімнатній температурі протягом 5 годин. Була додана аміносульфонова кислота (6,97 г, 61,6 ммоль). Реакційна суміш піддавалася нагріванню до температури флегми протягом ночі. Реакційна суміш була охолоджена до кімнатної температури, після чого був доданий водний розчин гідроксиду натрію (3,0 M, 100 мл). Розчин екстрагувався за допомогою етилацетату (3 × 100 мл). Комбінований органічний розчин був висушений у присутності MgSO4. Розчин був сконцентрований в умовах вакууму й очищений за допомогою хроматографії (від 2 % до 8 % метанолу в дихлорметані), що дозволило одержати ((3,4-дигідро-2H-бензо[b][1,4]діоксепін-3-іл)метил)амін у вигляді безбарвної маслянистої рідини. + MS (ESI): 180,1 (M+H ) 1H ЯМР (300 МГц, DMSO), δ: 6,92 (м, 4H), 4,21 (м, 2H), 4,07 (м, 2H), 3,33 (ш, 2H), 3,16 (д, J=4 Гц, 1H), 2,72 (д, J=4 Гц, 1H), 2,30 (м, 1H). ((3,4-дигідро-2H-бензо[b][1,4]діоксепін-3-іл)метил)амін (2,90 г, 16,2 ммоль) і сульфамід (3,11 г, 32,4 ммоль) змішували в присутності збезводненого діоксану (60 мл) і нагрівали до температури флегми протягом ночі. Хлороформ був доданий, і преципітат був вилучений за допомогою фільтрації. Фільтрат був сконцентрований в умовах вакууму й очищений за допомогою хроматографії (від 2 % до 8 % ацетону в дихлорметані), що дозволило одержати названу сполуку у вигляді твердого білуватого матеріалу. + 258,8 (M+H ) 1H ЯМР (300 Мгц, DMSO), δ: 6,92 (м, 4H), 6,71 (ш, 1H), 6,59 (ш, 2H), 4,19 (м, 2H), 4,04 (м, 2H), 3,00 (м, 2H), 2,39 (м, 1H). 35 Приклад 2 N-(2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфамід (Сполука № 1) O O H N O 40 45 O S NH2 Рацемічний 2,3-дигідро-1,4-бенздіоксин-2-ілметиламін (4,4 г, 26 ммоль) і сульфамід (5,1 г, 53 ммоль) змішували в присутності 1,4 діоксану (100 мл) і нагрівали до температури флегми протягом 2 год. Реакційну суміш охолоджували до кімнатної температури, і від невеликої кількості твердого осаду позбувалися за допомогою фільтрації. Фільтрат був підданий випарюванню в умовах вакууму й залишок очищений за допомогою хроматографії на випарній колонці (DCM:метанол - 10:1), що дозволило одержати твердий білий матеріал. Цей матеріал був рекристалізований з DCM з одержанням названої сполуки у вигляді твердого білого матеріалу. Т. пл.: 97,5-98,5 °C Аналіз елементного складу: Аналіз розрахунковий: C, 44,25; H, 4,95; N, 11,47; S, 13,13 20 UA 100552 C2 5 Аналіз одержаний: C, 44,28; H, 4,66; N, 11,21; S, 13,15 1 H ЯМР (DMSO д6) δ 6,85 (м, 4H), 6,68 (бд с, 3H, NH), 4,28 (м, 2H), 3,97 (дд, J=6,9, 11,4 Гц, 1H), 3,20 (м, 1H), 3,10 (м, 1H). Приклад 3 (Бензо[1,3]діоксол-2-ілметил)сульфамід (Сполука № 2) O O O HN S NH2 O 10 15 20 25 30 35 40 45 Катехол (10,26 г, 93,2 ммоль), метоксид натрію (25 % по вазі, у метанолі, 40,3 г, 186 ммоль), і метил дихлорацетат (13,3 г, 93,2 ммоль) змішували в присутності збезводненого метанолу (100 мл). Реакційну суміш піддавали нагріванню до температури флегми протягом ночі. Реакційна суміш була охолоджена до кімнатної температури, підкислена додаванням концентрованої соляної кислоти й потім піддана випарюванню в умовах вакууму до об'єму приблизно 50 мл. Після додавання води суміш піддавали екстрагуванню за допомогою діетилового ефіру (3 × 100 мл). Комбінований органічний розчин був висушений у присутності MgSO4, сконцентрований до стану твердого коричневого осаду й очищений за допомогою хроматографії (2 % етилацетату в гексані) з одержанням метилового ефіру бензо[1,3]діоксол-2карбонової кислоти у вигляді безбарвної маслянистої рідини. + MS (ESI): 195,10 (M+H ). 1H ЯМР (300 МГц, CdCl3), δ: 6,89 (ш, 4H), 6,29 (с, 1H), 4,34 (к, J=7 Гц, 2H), 1,33 (т, J=7 Гц, 3H). До метилового ефіру бензо[1,3]діоксол-2-карбонової кислоти (7,21 г, 40,0 ммоль) був доданий гідроксид амонію (29 % у воді, 10 мл) і достатню кількість ацетонітрилу (~5 мл), для того щоб додати суміші гомогенність. Розчин перемішувався при кімнатній температурі протягом двох годин з наступним додаванням дистильованої води. Амід бензо[1,3]диоксол-2карбонової кислоти зазнав преципітації з утворенням твердого білого осаду, який збирали за допомогою фільтрації й використовували без подальшого очищення. + MS (ESI): 160,00 (M+H ) 1 H ЯМР (300 Мгц, DMSO), δ: 7,99 (с, ш, 1H), 7,72 (с, ш, 1H), 6,94 (м, 2H) 6,86 (м, 2H), 6,30 (с, 1H). Амід бензо[1,3]діоксол-2-карбонової кислоти (5,44 г, 32,9 ммоль) розчиняли в тетрагідрофурані (THF, 100 мл). Алюмогідрид літію (LAH, 1M в THF, 39,5 мл, 39,5 ммоль) повільно додавався до розчину при кімнатній температурі. Реакційна суміш перемішувалася при кімнатній температурі протягом 24 годин. Додаванням дистильованої води відділявся надлишок LAH. Після додавання водного розчину гідроксиду натрію (3,0 M, 100 мл), проводилося екстрагування за допомогою етилацетату (3 × 100 мл). Комбінований органічний розчин промивався водою й висушувався в присутності MgSO4. Випарювання розчинника приводило до утворення C-бензо[1,3]діоксол-2-іл-метиламіну у вигляді безбарвної маслянистої рідини. + MS (ESI): 152,1 (M+H ) 1H ЯМР (300 МГц, CdCl3), δ: 6,87 (м, 4H), 6,09 (т, J=4 Гц, 1H), 3,13 (д, J=4 Гц, 2H) C-бензо[1,3]діоксол-2-іл-метиламін (2,94 г, 19,4 ммоль) і сульфамід (3,74 г, 38,9 ммоль) змішувалися в збезводненому діоксані (50 мл), після чого розчин нагрівався до температури флегми протягом ночі. Реакційна суміш була сконцентрована й піддана хроматографії (від 2 % до 10 % ацетону в дихлорметані), що дозволило одержати названу сполуку у вигляді твердого білого матеріалу. + MS (ESI): 230,0 (M+H ) 1H ЯМР (300 МГц, CdCl3), δ: 6,87 (м, 4H), 6,25 (т, J=4 Гц, 1H), 4,79 (ш, 1H), 4,62 (ш, 1H), 3,64 (д, J=4 Гц, 2H). Приклад 4 (2S)-(-)-N-(2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфамід (Сполука № 4) O (S) O 50 H N O O S NH2 21 UA 100552 C2 5 10 15 20 25 30 35 40 45 50 Катехол (13,2 г, 0,12 моль) і карбонат калію (16,6 г, 0,12 моль) перемішувалися в DMF (250 мл) і додавався (2R)-гліцидил тозилату (22,8 г, 0,10 моль), і реакційна суміш перемішувалася при 60 °C протягом 24 год. Реакційна суміш охолоджувалася до кімнатної температури, розбавлялася крижаною водою (1 л) і піддавалася екстрагуванню діетиловим ефіром (4 рази). Комбінований органічний розчин тричі промивався 10 % розчином карбонату калію, однократно водою, однократно сольовим розчином і випарювався в умовах вакууму з утворенням білого твердого матеріалу, який піддавали очищенню за допомогою хроматографії на випарній колонці (DCM:метанол - 50:1), з одержанням твердого ((2S)-2,3-дигідробензо[1,4]діоксин-2-іл)-метанолу. Твердий залишок (13,3 г, 68 ммоль) розчиняли в піридині (85 мл), охолодженому до 0 °C, з додаванням p-толуенсульфоніл хлориду (13,0 г, 68 ммоль) і наступним перемішуванням реакційної суміші при кімнатній температурі протягом 20 год. Реакційна суміш розбавлялася діетиловим ефіром (1 л) і 1N HCl (1,2 л). Органічний шар був відділений і двічі промитий 1N HCl (500 мл), 4 рази водою (150 мл), однократно сольовим розчином, висушений (MgSO4) і підданий випарюванню в умовах вакууму з утворенням білого твердого матеріалу, який піддавали очищенню за допомогою хроматографії на випарній колонці (Hept:EA-2:1) з утворенням (2S)-2,3дигідробензо[1,4]діоксин-2-ілметил ефіру толуен-4-сульфонової кислоти у вигляді твердого матеріалу білого кольору. Твердий білий залишок змішували із фталімідом калію (14,4 г, 78 ммоль) в DMF (250 мл) і нагрівали до температури флегми протягом 1 год., охолоджували до кімнатної температури, додавали у воду, що інтенсивно розмішується (1,5 л), перемішуючи протягом 30 хв. Білий осад відфільтровувався й промивався кілька разів водою, 2 % NaOH і знову водою, потім висушувався з одержанням (2S)-2-(2,3-дигідробензо[1,4]діоксин-2-ілметил)-ізоіндол-1,3-діoну у вигляді білого порошкоподібного матеріалу. Білий порошкоподібний матеріал змішували з гідразином (2,75 г, 86 ммоль) в EtOH (225 мл) і нагрівали до температури флегми протягом 2 год., охолоджували до кімнатної температури, додавали 1N HCl до pH 1,0 і перемішували протягом 15 хв. Білий осад відфільтровувався й промивався свіжою порцією EtOH (осад викидався) і фільтрат піддавали випарюванню в умовах вакууму з утворенням твердого залишку, який далі розділявся між діетиловим ефіром і водним розчином NaOH. Розчин діетилового ефіру висушували (Na2SO4) і піддавали випарюванню в умовах вакууму з утворенням ясно-жовтої маслянистої рідини. Масляниста рідина піддавалася очищенню за допомогою хроматографії на випарній колонці (DCM:MeOH – 10:1) з утворенням масла. Частина цього масла (4,82 г, 29 ммоль) в 2-пропанолі (250 мл) оброблялася 1N HCl (30 мл) і нагрівалася в паровій бані до досягнення гомогенного стану, а потім охолоджувалася до кімнатної температури. Через 3 год. суміш вміщували на лід на 2 год. Біла пластівчаста маса (відповідна солянокислій солі (2S)-C-(2,3-дигідробензо[1,4]діоксин-2-іл)-метиламіну) відфільтровувалася і потім піддавалася рекристалізації з розчину 2-пропанолу з утворенням білого твердого матеріалу. [α]D = -69,6 (c=1,06, EtOH) Білий твердий залишок далі розділявся між DCM і розчином NaOH, DCM висушували (NaSO4) і проводили випарювання в умовах вакууму з утворенням (2S)-C-(2,3дигідробензо[1,4]діоксин-2-іл)-метиламіну у вигляді масла. [α]D = -57,8 (c=1,40, CHCl3) Масло (2,1 г, 12,7 ммоль) і сульфамід (2,44 г, 25,4 ммоль) нагрівалися до температури флегми в діоксані (75 мл) протягом 2 год., і неочищений продукт піддавали очищенню за допомогою хроматографії на випарній колонці (DCM:MeOH 10:1) з утворенням білого твердого матеріалу, що піддавали далі рекристалізації з розчину DCM з одержанням названої сполуки у вигляді твердого білого кристалічного матеріалу. Т. пл. 102-103 °C [α]D = -45,1° (c=1,05, M); 1 H ЯМР (DMSO д6) δ 6,86 (м, 4H), 6,81 (бд с, 3H, NH), 4,3 (м, 2H), 3,97 (дд, J=6,9, 11,4 Гц, 1H), 3,20 (дд, J=5,5, 13,7 Гц, 1H), 3,10 (дд, J=6,9, 13,7 Гц, 1H) Аналіз елементного складу: Аналіз розрахунковий: C, 44,25; H, 4,95; N, 11,47; S, 13,13 Аналіз отриманий: C, 44,20; H, 4,69; N, 11,40; S, 13,22. 22 UA 100552 C2 Приклад 5 N-(2,3-дигідробензо[1,4]діоксин-2-ілметил)-N",N" диметилсульфамід (Сполука № 6) O O H N O S O 5 10 15 20 N Рацемічний 2,3-дигідро-1,4-бенздіоксин-2-ілметиламін (8,25 г, 5,0 ммоль) і триетиламін (1,52 г, 15 ммоль) змішували в DMF (10 мл) і охолоджували на льоді, в той час як додавався диметилсульфамоїл хлорид (1,44 г, 10 ммоль). Реакційна суміш потім перемішувалася протягом 3 год. з постійним охолодженням. Реакційна суміш розділялася між етилацетатом і водою, розчин етилацетату відмивався сольовим розчином, висушувався (MgSO 4) і піддавався випарюванню в умовах вакууму з утворенням масла. Масло очищалося за допомогою хроматографії на випарній колонці (етилацетат:гептан - 1:1) з одержанням білого твердого матеріалу, який далі піддавався рекристалізації (етилацетат/гексан) з одержанням названої сполуки у вигляді білої пластівчастої маси. Т. пл. 76-78 °C + MS 273 (MH ) Аналіз елементного складу: Аналіз розрахунковий: C, 48,52; H, 5,92; N, 10,29; S, 11,78 Аналіз отриманий: C, 48,63; H, 5,62; N, 10,20; S, 11,90 1 H ЯМР (CDCl3) δ 6,87 (м, 4H), 4,59 (бд м, 1H, NH), 4,35 (м, 1H), 4,27 (дд, J=2,3, 11,4 Гц, 1H), 4,04 (дд, J=7,0, 11,4, 1H), 3,36 (м, 2H), 2,82 (с, 6H). Приклад 6 N-(2,3-дигідробензо[1,4]діоксин-2-ілметил)-N-метилсульфамід (Сполука № 7) O O N H2N 25 30 35 40 45 O S O Рацемічний 2,3-дигідро-1,4-бенздіоксин-2-ілметиламін (825 мг, 5 ммоль) розчиняли в етилформіаті (15 мл), нагрівали до температури флегми протягом 30 хв. і піддавали випарюванню в умовах вакууму з одержанням N-(2,3-дигідробензо[1,4]діоксин-2-ілметил)формаміду у вигляді масла. Масло в діетиловому ефірі (25 мл) піддавали обробці 1M LAH в THF (9,0 мл, 9,0 ммоль) при 0 °C і подальшому перемішуванню протягом 5 год. при кімнатній температурі. Реакційна суміш охолоджувалася на льодовій бані й зупинялася додаванням води (0,50 мл), з наступним додаванням 3 N NaOH (0,50 мл) і води (0,50 мл). Потім суміш перемішувалася при кімнатній температурі протягом 1 год. Твердий осад відфільтровувався, і фільтрат піддавали випарюванню в умовах вакууму з утворенням залишку, який був розділений між 1N HCl і діетиловим ефіром. Водна фаза вилуговувалася додаванням 1N NaOH і піддавалася екстрагуванню діетиловим ефіром. Органічна фаза висушувалася (MgSO 4), піддавалася випарюванню в умовах вакууму з утворенням (2,3-дигідробензо[1,4]діоксин-2-ілметил)метиламіну у вигляді масла. + MS 180 (MH ) 1 H ЯМР (CDCl3) δ 6,85 (м, 4H), 4,30 (м, 2H), 4,02 (дд, J=7,9, 11,6 Гц, 1H), 2,85 (м, 2H), 2,50 (с, 3H) Масло (380 мг, 2,1 ммоль) і сульфамід (820 мг, 8,5 ммоль) змішували в діоксані (15 мл), нагрівали до температури флегми протягом 1,5 год. і піддавали випарюванню в умовах вакууму з утворенням неочищеного залишку. Залишок очищали за допомогою колонкової хроматографії (етилацетат/гептан 1:1), і одержаний у результаті твердий продукт піддавали рекристалізації з етилацетат/гептану з одержанням названої сполуки у вигляді білого твердого матеріалу. Т. пл. 97-98 °C -1 MS 257 (M ) 23 UA 100552 C2 5 Аналіз елементного складу: Аналіз розрахунковий: C, 46,50; H, 5,46; N, 10,85; S, 12,41 Аналіз отриманий: C, 46,48; H, 5,65; N, 10,90; S, 12,07 1 H ЯМР (CDCl3) δ 6,86 (м, 4H), 4,52 (бс, 2H), 4,46 (м, 1H), 4,29 (дд, J=2,3, 11,5 Гц, 1H), 4,05 (дд, J=6,5, 11,5 Гц, 1H), 3,51 (дд, J=6,7, 14,9 Гц, 1H), 3,40 (дд, J=5,9, 14,9 Гц, 1H), 2,99 (с, 3H). Приклад 7 (2S)-(-)-N-(6-хлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфамід (Сполука № 8) Cl O (S) O H N O 10 15 20 25 30 35 40 45 50 O S NH2 Слідуючи процедурі, описаній вище в Прикладі 4, 4-хлоркатехол вступав у реакцію з утворенням суміші (2S)-C-(7-хлор-2,3-дигідробензо[1,4]діоксин-2-іл)-метиламіну і (2S)-C-(6-хлор2,3-дигідробензо[1,4]діоксин-2-іл)-метиламіну (бл. 3:1 співвідношення 6-хлор:7-хлорізомерів за результатами RP HPLC). Суміш розчинялася в 2-пропанолі (100 мл) і 1N HCl у діетилефірі додавалося до досягнення pH=1,0. Утворююча преципітати сіль соляної кислоти відфільтровувалася (2,65 г) і піддавалася рекристалізації з метанолу/IPA з утворенням білих кристалів. Кристали розділялися між DCM і розчином NaOH. DCM висушувався й піддавався випарюванню в умовах вакууму з утворенням очищеного (2S)-C-(6-хлор-2,3-дигідробензо[1,4]діоксин-2-іл)-метиламіну у вигляді масла. [α]D = -67,8 (c=1,51, CHCl3) Масло (7,75 ммоль) і сульфамід (1,50 г, 15,5 ммоль) змішували в діоксані (50 мл) і нагрівали до температури флегми протягом 2 год., охолоджували до кімнатної температури й піддавали випарюванню в умовах вакууму з утворенням твердого залишку. Продукт очищали за допомогою хроматографії на випарній колонці з використанням DCM/метанолу 20:1 і одержували названу сполуку у вигляді білого твердого матеріалу. -1 MS 277 (M ) [α]D = -59,9° (c=1,11, M) 1 H ЯМР (CDCl3) δ 6,90 (д, J=2,2 Гц, 1H), 6,81 (м, 2H), 4,76 (м, 1H), 4,55 (с, 2H), 4,40 (м, 1H), 4,29 (дд, J=2,4, 11,5 Гц, 1H), 4,05 (дд, J=7,1, 11,5 Гц, 1H), 3,45 (м, 2H) Аналіз елементного складу: Аналіз розрахунковий: C, 38,78; H, 3,98; N, 10,05 Аналіз отриманий: C, 38,80; H, 3,67; N, 9,99. Фільтрати кристалізованої солі гідрохлориду (2S)-C-(6-хлор-2,3-дигідробензо[1,4]діоксин-2іл)-метиламіну, одержані вище, витягали (бл. 1:1 6-хлор: 7-хлорізомерів) і піддавали випарюванню в умовах вакууму з утворенням твердого осаду, який розділяли між DCM (200 мл) і розчином NaOH (0,5 M, 50 мл). Розчин DCM промивали однократно сольовим розчином, висушували (Na2SO4) і піддавали випарюванню в умовах вакууму з утворенням масла, яке очищали за допомогою зворотно-фазової рідинної хроматографії (10-50 % ACN з 0,16 % TFA у воді з 0,20 % TFA) з одержанням (2S)-C-(7-хлор-2,3-дигідробензо[1,4]діоксин-2-іл)-метиламіну в залишку. Залишок змішували із сульфамідом (0,90 г, 9,4 ммоль) в діоксані (25 мл) і нагрівали до температури флегми протягом 2,5 год., охолоджували до кімнатної температури й піддавали випарюванню в умовах вакууму з утворенням масла. Масло очищали за допомогою хроматографії на випарній колонці з використанням DCM/метанолу - 10:1 з утворенням (2S)-(-)N-(7-хлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфаміду у вигляді твердого білого матеріалу. -1 MS 277 (M ) 1 H ЯМР (CDCl3/CD3OD) δ 6,88 (д, J=0,7 Гц, 1H), 6,81 (м, 2H), 4,37 (м, 1H), 4,30 (дд, J=2,3, 11,6 Гц, 1H), 4,04 (дд, J=7,0, 11,6 Гц, 1H), 3,38 (м, 2H). Приклад 8 Хроман-2-ілметилсульфамід (Сполука № 10) 24 UA 100552 C2 O H N O S O 5 10 15 20 25 NH2 Хроман-2-карбонову кислоту (4,5 г, 25 ммоль) і HOBT (3,86 г, 25 ммоль) з'єднували в DCM (40 мл) і DMF (10 мл). Диметиламінопропіл етилкарбодіімід (EDC, 4,84 г, 25 ммоль) додавали при кімнатній температурі й перемішували реакційну суміш протягом 30 хв. Після додавання гідроксиду амонію (2,26 мл, 33,4 ммоль) реакційну суміш перемішували протягом 16 год. Реакційну суміш розбавляли DCM (50 мл) і водою (50 мл), pH суміші доводили приблизно до pH=3,0 за допомогою 1N HCl. DCM відокремлювали й водну фазу двічі екстрагували за допомогою DCM. Об'єднані фракції DCM висушували (Na2SO4) і піддавали випарюванню в умовах вакууму з утворенням масла, яке очищали за допомогою хроматографії на випарній колонці (етилацетат) з одержанням масла. Масло (5,35 г, 30 ммоль) в THF (90 мл) перемішували, додаючи при перемішуванні 1M LAH в THF (36 мл, 36 ммоль), після чого реакційна суміш перемішувалася при кімнатній температурі протягом 20 год. Реакцію зупиняли водою, перемішували протягом 2 годин, розчин зливали, висушували (Na2SO4) і піддавали випарюванню в умовах вакууму з утворенням C-хроман-2-ілметиламіну у вигляді масляного аміну. Масляний амін (1,63 г, 10 ммоль) і сульфамід (1,92 г, 20 ммоль) з'єднували в діоксані (50 мл) і доводили до температури флегми протягом 2 год. Розчин охолоджували й піддавали випарюванню в умовах вакууму з утворенням масла, яке очищали колонковою хроматографією (DCM:метанол 10:1) з утворенням твердого білого матеріалу. Білий матеріал піддавали рекристалізації з етилацетату/гексану з утворенням хроман-2-ілметилсульфаміду у формі твердого білого матеріалу. Т. пл. 100-101 °C -1 MS 241 (M ) Аналіз елементного складу: Аналіз розрахунковий: C, 49,57; H, 5,82; N, 11,56; S, 13,23 Аналіз отриманий: C, 49,57; H, 5,80; N, 11,75; S, 13,33. Приклад 9 2-(2,3-дигідробензо[1,4]діоксин-2-іл)-етилсульфамід (Сполука № 16) O H N O O S NH2 O 30 35 40 45 50 Ціанід калію (2,05 г, 31,5 ммоль) додавали до 2-бромметил-(2,3 дигідробензо[1,4]діоксину) (6,87 г, 30 ммоль) в DMSO (90 мл) і перемішували при кімнатній температурі протягом 20 год. Реакційна суміш була потім розведена водою (250 мл) і екстрагована двічі за допомогою діетилового ефіру. Діетиловий ефір промивали водою, потім двічі сольовим розчином, висушували (Na2SO4) і піддавали випарюванню в умовах вакууму з утворенням 2-ціанометил(2,3 дигідробензо[1,4]діоксину) у формі твердого білого матеріалу. 1 H ЯМР (CDCl3) δ 6,89 (м, 4H), 4,50 (м, 1H), 4,31 (дд, J=2,3, 11,5 Гц, 1H), 4,08 (дд, J=6,2, 11,6 Гц, 1H), 2,78 (д, J=6,1, Гц, 2H) 2-ціанометил-(2,3 дигідробензо[1,4]діоксин) розчиняли в THF (50 мл) і додавали 1M BH3 в THF (80 мл, 80 ммоль), потім реакційну суміш нагрівали до температури флегми протягом 5 год., після чого перемішували при кімнатній температурі протягом 16 год. Після охолодження на крижаній бані додавали 2N HCl до досягнення pH=1,0. Потім реакційну суміш перемішували протягом 1 год. при кімнатній температурі й випарювали в умовах вакууму з утворенням масла. Масло розділяли між 3N NaOH і діетиловим ефіром, розчин діетилового ефіру промивали сольовим розчином, висушували (Na2SO4) і піддавали випарюванню в умовах вакууму з утворенням неочищеного 2-(2,3 дигідробензо[1,4]діоксин-2-іл)етиламіну. + MS (M+H) 180. Неочищений 2-(2,3 дигідробензо[1,4]діоксин-2-іл)етиламін в діоксані (100 мл) з'єднували із сульфамідом (3,0 г, 31 ммоль) і нагрівали до температури флегми протягом 2 год. Розчин охолоджували й піддавали випарюванню в умовах вакууму з утворенням твердого жовтогарячого матеріалу, який очищали за допомогою колонкової хроматографії (DCM:MeOH – 25 UA 100552 C2 5 10 10:1) з утворенням твердого білого матеріалу. Цей матеріал був підданий рекристалізації з DCM з утворенням названої сполуки у формі твердого матеріалу. MS (M-1) 257 Т. пл. 101-103 °C (corr) 1 H ЯМР (CDCl3): δ 6,86 (м, 4H), 4,70 (м, 1H), 4,52 (с, 2H), 4,30 (м, 2H), 3,94 (дд, J=7,4, 11,3 Гц, 1H), 3,43 (дд, J=6,4, 12,9 Гц, 2H), 1,94 (дд, J=6,5, 12,9, 2H). Аналіз елементного складу: Одержаний: C, 46,48; H, 5,60; N, 10,81; S, 12,41 Розрахунковий: C, 46,50; H, 5,46; N, 10,85; S, 12,41 Приклад 10 (2S)-(-)-N-(6,7 дихлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфамід (Сполука № 29) O Cl O (S) Cl 15 20 25 30 35 40 45 50 55 N H S NH2 O O 4,5 Дихлоратекол (8,6 г, 48 ммоль) і карбонат калію (6,64 г, 48 ммоль) перемішували в DMF (200 мл). (2R)-Гліцидилу тозилат (9,12 г, 40 ммоль) додавали й перемішували реакційну суміш при 60 °C протягом 24 год. Реакційну суміш охолоджували до кімнатної температури й потім розводили крижаною водою (600 мл) і екстрагували діетиловим ефіром (4 рази). Комбінований органічний розчин тричі промивали 10 % розчином карбонату калію, двічі концентрованим сольовим розчином, висушували (MgSO4) і піддавали випарюванню в умовах вакууму з утворенням грузлої маслянистої сполуки - (2S)-2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксин) метанолу. Маслянистий розчин (2S)-2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксин) метанолу (6,4 г, 27 ммоль) розчиняли в піридині (50 мл) і охолоджували до 0 °C. Потім до реакційної суміші додавали p-толуенсульфоніл хлорид (5,2 г, 27 ммоль) і перемішували при кімнатній температурі протягом 20 год. Реакційну суміш розбавляли діетиловим ефіром і 1N HCl (750 мл), і органічний шар був відділений і дворазово промитий 1N HCl (250 мл), однократно водою (150 мл), двічі концентрованим сольовим розчином, висушений (MgSO4) і підданий випарюванню в умовах вакууму з утворенням твердого ясно-жовтого залишку (2S)-6,7-дихлор-2,3дигідробензо[1,4]діоксин-2-ілметилового ефіру толуен-4-сульфонової кислоти. 1 H ЯМР (CDCl3): δ 7,79 (д, J=8,3 Гц, 2H), 7,36 (д, J=8,0 Гц, 2H), 6,94 (с, 1H), 6,83 (с, 1H), 4,37 (м, 1H), 4,2 (м, 3H), 4,03 (дд, J=6,3, 11,7 Гц, 1H), 2,47 (с, 3H). (2S)-6,7-дихлор-2,3-дигідробензо[1,4]діоксин-2-ілметиловий ефір толуен-4-сульфонової кислоти (8,0 г, 20,5 ммоль) змішували із фталімідом калію (6,1 г, 33 ммоль) в DMF (75 мл) і нагрівали до температури флегми протягом 1 год., охолоджували до кімнатної температури, додавали у воду, що інтенсивно перемішується (0,5 л), і потім перемішували протягом 30 хв. Твердий білий осад відфільтровували й промивали кілька разів водою, 2 % NaOH і знову водою, потім залишали підсихати на відкритому повітрі з утворенням білої порошкоподібної твердої маси (2S)-2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)-ізоіндол-1,3-діoну (6,0 г, 80 %). Білу порошкоподібну тверду масу з'єднували з гідразином (1,06 г, 33 ммоль) в EtOH (80 мл) і нагрівали до температури флегми протягом 2 год., потім охолоджували до кімнатної температури. 1N HCl додавали для корекції pH реакційної суміші до 1,0 і перемішували реакційну суміш протягом 15 хв. Твердий білий осад відфільтровували й промивали свіжою порцією EtOH (твердий залишок відкидали), потім випарювали фільтрат в умовах вакууму з одержанням твердого залишку, який розділяли між діетиловим ефіром і водним розчином NaOH. Розчин діетилового ефіру висушували (Na2SO4) і випарювали в умовах вакууму з утворенням грузлої маслянистої сполуки (2S)-2-амінометил-(6,7-дихлор-2,3дигідробензо[1,4]діоксину). 1 H ЯМР (CDCl3): δ 6,98 (с, 1H), 6,96 (с, 1H), 4,25 (дд, J=2,0, 11,2 Гц, 1H), 4,15 (м, 1H), 4,0 (м, 1H), 2,97 (д, J=5,5 Гц, 2H) Порцію цього масла (3,8 г, 16 ммоль) і сульфамід (3,1 г, 32,4 ммоль) нагрівали до температури флегми в діоксані (100 мл) протягом 2 год. і неочищений продукт очищали за допомогою хроматографії на випарній колонці (DCM:MeOH 20:1) з одержанням названої сполуки у формі твердого білого продукту, який піддавали рекристалізації з етилацетату/гексану з одержанням названої сполуки у формі білого кристалічного матеріалу. MS [M-H] 311,0 26 UA 100552 C2 5 10 Т. пл. 119-121 °C [α]D = -53,4° (c=1,17, M) 1 H ЯМР (DMSO d6): δ 7,22 (с, 1H), 7,20 (с, 1H), 6,91 (бд с, 1H), 6,68 (бд с, 2H), 4,35 (м, 2H), 4,05 (дд, J=6,5, 11,5 Гц, 1H), 3,15 (м, 2H) Аналіз елементного складу: Виміряний: C, 34,52; H, 3,22; N, 8,95; Cl, 22,64; S, 10,24 Розрахунковий: C, 34,64; H, 2,68; N, 8,87; Cl, 22,94; S, 10,35. Приклад 11 (2S)-(-)-N-(7-аміно-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфамід (Сполука № 36) O H2N O (S) N H S NH2 O O 15 20 25 (2S)-(-)-N-(2,3-дигідро-7-нітро-бензо[1,4]діоксин-2-ілметил)сульфамід (1,2 г, 4,15 ммоль), був отриманий з 4-нітрокатехолу відповідно до процесу, описаного в прикладі 4. (2S)-(-)-N-(2,3дигідро-7-нітро-бензо[1,4]діоксин-2-ілметил)сульфамід був далі з'єднаний з 10 % Pd/C у метанолі (120 мл), і суміш перемішувалася хитанням в атмосфері водню (268,9 кПа (39 psi)) при кімнатній температурі протягом 3 год.Твердий матеріал відфільтровували й промивали 10 % M в DCM і фільтрат випарювали в умовах вакууму з одержанням неочищеного твердого продукту. Неочищений продукт розчиняли в 0,2 N HCl (25 мл), заморожували й ліофілізували з одержанням названої сполуки у формі пластівчастого твердого продукту, що відповідає його солянокислій солі. + MS (M+H) 260 1 H ЯМР (DMSO d6): δ 10,2 (бд с, 3H), 6,86 (м, 1H), 6,85 (с, 1H), 6,74 (дд, J=2,5, 8,4 Гц, 1H), 4,22 (м, 2H), 3,88 (дд, J=6,7, 11,4 Гц, 1H), 3,04 (м, 2H) Приклад 12 (2S)-(-)-N-(7-метил-2,3-дигідробензо[1,4]діоксин-2-ілметил)сульфамід (Сполука № 19) O H3C O (S) 30 35 40 45 N H S NH2 O O Названу сполуку одержували відповідно до процесу, описаного вище в прикладі 4, починаючи з 4-метилкатехолу, з одержанням твердого білого продукту, який піддавали рекристалізації з етилацетату/гексану з одержанням названої сполуки у формі білого матеріалу. MS [M-H] 257 1 H ЯМР (CDCl3): δ 6,76 (м, 1H), 6,66 (м, 2H), 4,80 (м, 1H), 4,57 (бд с, 1H), 4,40 (м, 1H), 4,28 (м, 1H), 4,03 (дд, J=6,9, 11,4 Гц, 1H), 3,45 (м, 2H), 2,25 (с, 3H). Аналіз елементного складу Розрахунковий: C, 46,50; H, 5,46; N, 10,85; S, 12,41 Отриманий: C, 46,65; H, 5,60; N, 10,84; S, 12,61 Приклад 13 Піднятий хрестоподібний лабіринт, миша (EPM) Аналіз EPM in vivo використовується для виявлення анксіолітичної (протитривожної) активності тестованої сполуки. Гризуни уникають відкритих просторів (у випадку апарату для проведення даного аналізу, відкриті сегменти піднятого хрестоподібного лабіринту). Сполуки, що володіють протитривожною активністю, підсилюють пошукову активність гризунів у відкритих сегментах піднятого хрестоподібного лабіринту. Аналіз EPM проводили відповідно до процедури, описаної Handley and Mithani (Naunyn. Schmied. Arch. Pharmacol., 327, 1-5, 1984). 27 UA 100552 C2 5 10 15 20 25 30 Миші Rj:NMRI чоловічої статі, вагою 20-30 г (макс. варіація в межах того самого експерименту = 5 г), були отримані з Elevage Janvier, 53940 Le Genest-Saint-Isle, France і використані для виконання аналізу. Тварини доставлялися в лабораторію, принаймні, за 5 днів до виконання експериментів, протягом цих днів вони проходили акліматизацію до лабораторних умов. Миші розміщалися групами по 10 особин у клітках Macrolon (25 × 19 × 13 см) на підстилках з тирси (Litalabo-SPPS, 95100 Argenteuil, France) з вільним доступом до їжі (Code 113-SAFE, 89290 Augy, France) і воді до моменту тестування (або, якщо зазначене, іншим способом). У віварії підтримувалося штучне освітлення (12 годин) в інтервалі між 7:00 і 19:00 і контролювалися температура приміщень на рівні 21±3 °C, а відносна вологість повітря - у межах 30-80 %. Піднятий хрестоподібний лабіринт складався з 4 сегментів рівної довжини й ширини (14 × 5 см), що розташовувалися у формі знака плюс (+). Два протилежні сегменти були укладені усередині стінок висотою 12 см (закриті сегменти). У двох інших сегментах стін не було (відкриті сегменти). Лабіринт був піднятий над рівнем підлоги на висоту 56 см. Миша вміщувалася в центрі піднятого хрестоподібного лабіринту, при цьому їй надавалося 5 хвилин для дослідження лабіринту. Реєструвалася кількість заходів у відкриті й закриті сегменти й час, проведений у відкритих сегментах. 10 (десять) мишей використовувалося в складі кожної експериментальної групи. Тестування проводилося з використанням сліпого способу. Сполука № 8 оцінювалася в дозах 30 мг/кг, 60 мг/кг і 120 мг/кг, призначуваних перорально за 60 хвилин до тестування, її ефект оцінювався в порівнянні з контрольною групою, що одержувала лише розчинник, використовуваний для розведення тестованої сполуки. Сполуку № 8 гомогенізували й диспергували з використанням ступки й товкачика в 0,2 % гідроксипропілметилцелюлозі (HPMC) у дистильованій воді, що служила розчинником. Як позитивний контролю використовувався клобазам (16 мг/кг перорально), який призначався в ідентичних експериментальних умовах. Клобазам у вигляді таблеток URBANYL® (16 мг/кг перорально) диспергували в 0,2 % гідроксипропілметилцелюлозі (HPMC) у дистильованій воді для прийому. Кожний експеримент, таким чином, включав 5 груп дослідження з 10 мишей у кожній. Дані аналізували за допомогою порівняння груп, що одержували Сполуку № 8 із групами, що одержували контрольний препарат у формі розчинника, з використанням непарного t-тесту Стьюдента. Результати (включаючи середній час, % відмінностей від контролю, а також зміни p критерію t-тесту Стьюдента) наведені в таблиці 4 нижче. Таблиця 4 Ефект сполуки № 8 в EPM Розчинник Спол. № 8 30 мг/кг Спол. № 8 60 мг/кг Спол. № 8 120 мг/кг Клобазам 16 мг/кг 35 40 45 Відкриті сегменти Кількість заходів % Серед. відмінносS.E.M. тей 2,6 0,4 3,90,7 (NS) +50 % 5,91,0 (**) +127 % +73 % 4,50,6 (*) 11,71,1 +350 % (***) Відкриті сегменти Закриті сегменти Витрачений час (сек.) Кількість заходів % % Серед. Серед. відмінносвідмінносS.E.M. S.E.M. тей тей 18,02,9 7,5 0,5 44,68,0 (**) +148 % 8,50,9 (NS) +13 % 54,110,6 (**) +201 % 10,30,8 (**) +37 % 38,65,2 (**) +114 % 10,01,1 (*) +33 % 120,113,1 +567 % 11,91,5 (*) +59 % (***) t-тест Стьюдента: (NS) = Статистично незначущий; (*) = p < 0,05; (**) = p < 0,01; (***) = p < 0,001 Приклад 14 Тест чотирьох пластин, миша Тест чотирьох пластин in vivo використовується для виявлення анксіолітичної (протитривожної) активності тестованої сполуки. Тест чотирьох пластин проводили відповідно до процедури, описаної Aron et al (Neuropharmacology, 10, 459-469, 1971). У цьому аналізі гризуни відчувають електричний шок при переході з однієї пластини на іншу. Анксіолітики (такі як бензодіазепіни) сприяють збільшенню кількості карних переходів. Тварини містилися індивідуально в білі пластикові загони, що мали підлогу, побудовану з 4 металевих пластин, приєднаних до генератора електричного струму (Apelex: Type 011346). 28
ДивитисяДодаткова інформація
Назва патенту англійськоюUse of benzo-fused heterocycle sulfamide derivatives for the treatment of anxiety and related disorders
Автори англійськоюSmith-Swintosky, Virginia L.
Назва патенту російськоюПрименение гетероциклических бензопроизводных сульфамида для лечения тревожных расстройств
Автори російськоюСмит-Свинтоски Вирджиния Л.
МПК / Мітки
МПК: A61P 25/22, A61K 31/357, A61K 31/353
Мітки: застосування, сульфаміду, бензопохідних, розладів, лікування, гетероциклічних, тривожних
Код посилання
<a href="https://ua.patents.su/35-100552-zastosuvannya-geterociklichnikh-benzopokhidnikh-sulfamidu-dlya-likuvannya-trivozhnikh-rozladiv.html" target="_blank" rel="follow" title="База патентів України">Застосування гетероциклічних бензопохідних сульфаміду для лікування тривожних розладів</a>
Попередній патент: Синбіотична суміш
Випадковий патент: Армуючі мікронаповнювачі для композиційних матеріалів на основі подрібнених мікро-, ультра- та супертонких мінеральних волокон