Застосування прогестерону для виробництва лікарського засобу
Формула / Реферат
1. Застосування прогестерону для виробництва лікарського засобу для мінімізації укорочення шийки матки у вагітних жінок з короткою шийкою матки від 1,0 см до 3,5 см, щоб таким чином лікувати чи попереджати настання передчасних пологів та наступного передчасного народження.
2. Застосування за п. 1, яке відрізняється тим, що лікарський засіб являє собою вагінальний гель, вагінальний супозиторій, вагінальний крем або вагінальну тверду дозовану форму.
3. Застосування за п. 1, яке відрізняється тим, що лікарський засіб сформований для введення внутрішньом'язовим, оральним, ректальним, підшкірним, вагінальним, інтрадермальним, місцевим, інтраназальним, інтраперітонеальним, внутрішньосуглобовим, внутрішньошлуночковим, інтратекальним, внутрішньовагінальним або внутрішньовенним шляхом.
4. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що прогестерон містить природний прогестерон або метаболіт прогестерону.
5. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що прогестерон містить синтетичний прогестерон, вибраний з 17-альфа-гідроксипрогестерону капроату, медроксипрогестерону ацетату, норетиндрону, норетиндрону ацетату, норетиндрону енантату, дезогестрелу, левоногестрелу, лінестренолу, етинодіолу діацетату, норгестрелу, норгестимату, норетинодрелу, гестодену, дроспіренону, тримегестону, леводезогестрелу, гестодину, нестерону, етоногестрелу і похідних 19-нортестостерону.
6. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що лікарський засіб призначений для щоденного введення.
7. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що лікарський засіб призначений для введення з приблизно 18-22 тижня вагітності аж до приблизно 37 тижня вагітності.
8. Застосування за п. 6, яке відрізняється тим, що лікарський засіб призначений для введення протягом від приблизно 14 до приблизно 19 тижнів.
9. Застосування за п. 6, яке відрізняється тим, що лікарський засіб призначений для введення з приблизно 16 тижня вагітності аж до приблизно 37 тижня вагітності.
10. Застосування за п. 6, яке відрізняється тим, що лікарський засіб призначений для введення протягом приблизно 21 тижня.
11. Застосування за п. 6, яке відрізняється тим, що лікарський засіб призначений для введення з моменту позитивного тесту на вагітність аж до приблизно 37 тижня вагітності.
12. Застосування за п. 6, яке відрізняється тим, що лікарський засіб призначений для введення з приблизно 2-го по 4-й тиждень вагітності.
13. Застосування за п. 6, яке відрізняється тим, що лікарський засіб призначений для введення протягом приблизно 33-35 тижнів.
14. Застосування за п. 6, яке відрізняється тим, що лікарський засіб призначений для введення залежно від гестаційного віку на початку лікування і на дату пологів.
15. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що лікарський засіб сформований для доставки дози прогестерону від приблизно 45 мг до приблизно 800 мг.
16. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що лікарський засіб знаходиться в формі або міститься в системі доставки ліків, що містить прогестерон, водорозчинний, водонабрякаючий перехресно зшитий полімер полікарбонової кислоти та принаймні один ад'ювант.
17. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що шийка матки вагітної жінки має довжину від 1,0 см до 3,0 см.
18. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що прогестерон містить природний прогестерон і 17-альфа-гідроксипрогестерон.
19. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що лікарський засіб сформований для доставки дози прогестерону приблизно 90 мг, і тим, що прогестерон є природним прогестероном.
20. Застосування за будь-яким із попередніх пунктів, щоб таким чином знизити дитячу захворюваність та смертність у недоношеного новонародженого, що очікується або пізніше народиться від вагітної жінки з короткою шийкою матки.
21. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що лікарський засіб призначений для введення в комбінації з однією або більше сполуками для лікування або профілактики передчасного народження.
22. Застосування за будь-яким із пп. 1-20, яке відрізняється тим, що лікарський засіб призначений для введення в комбінації з клінічною процедурою для лікування або профілактики передчасного народження.
23. Застосування за будь-яким з попередніх пунктів, яке відрізняється тим, що лікарський засіб вводиться у пристрої для вивільнення ліків, що має конфігурацію для введення у вагіну.
24. Застосування за п. 23, яке відрізняється тим, що пристрій являє собою або містить цервікальне кільце.
Текст
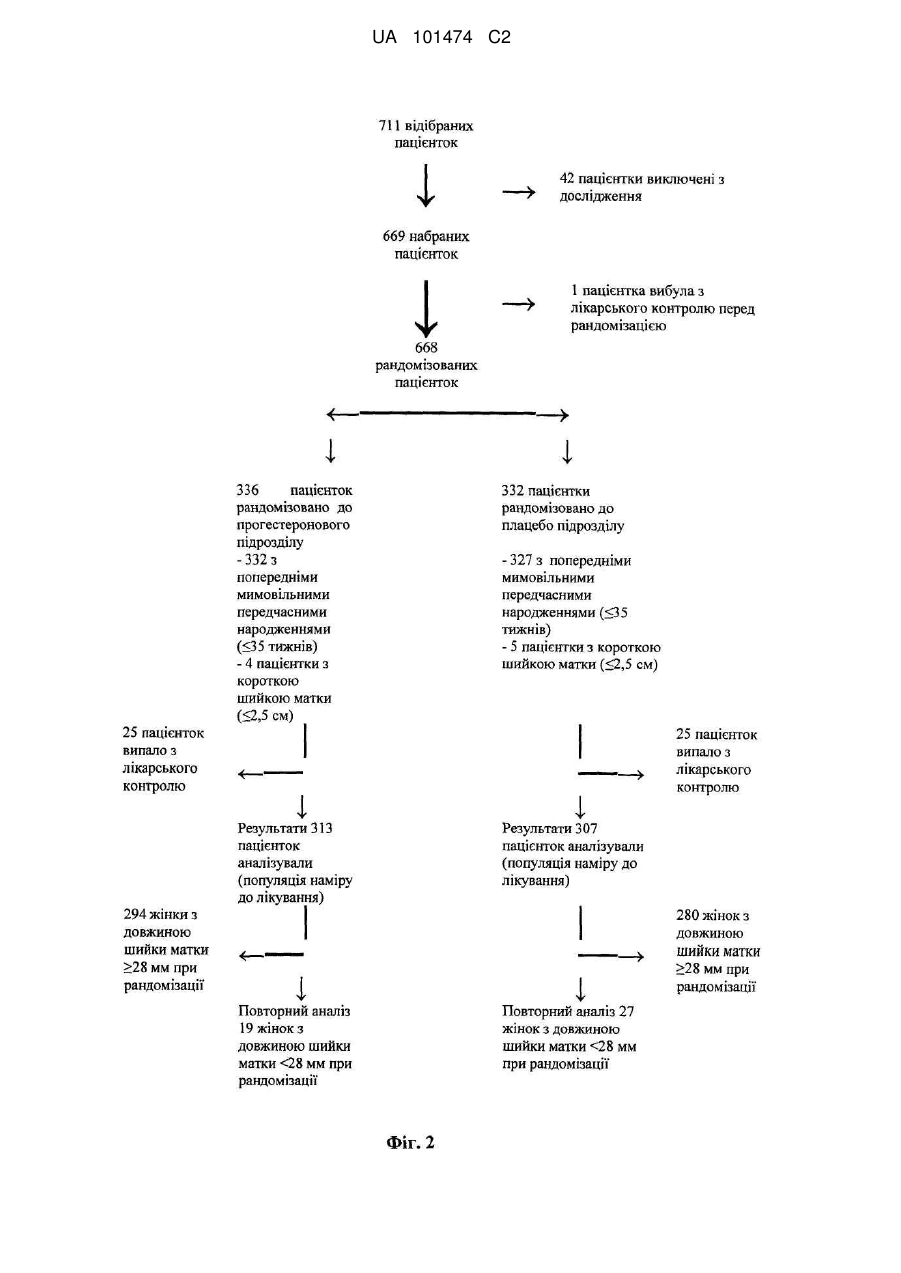
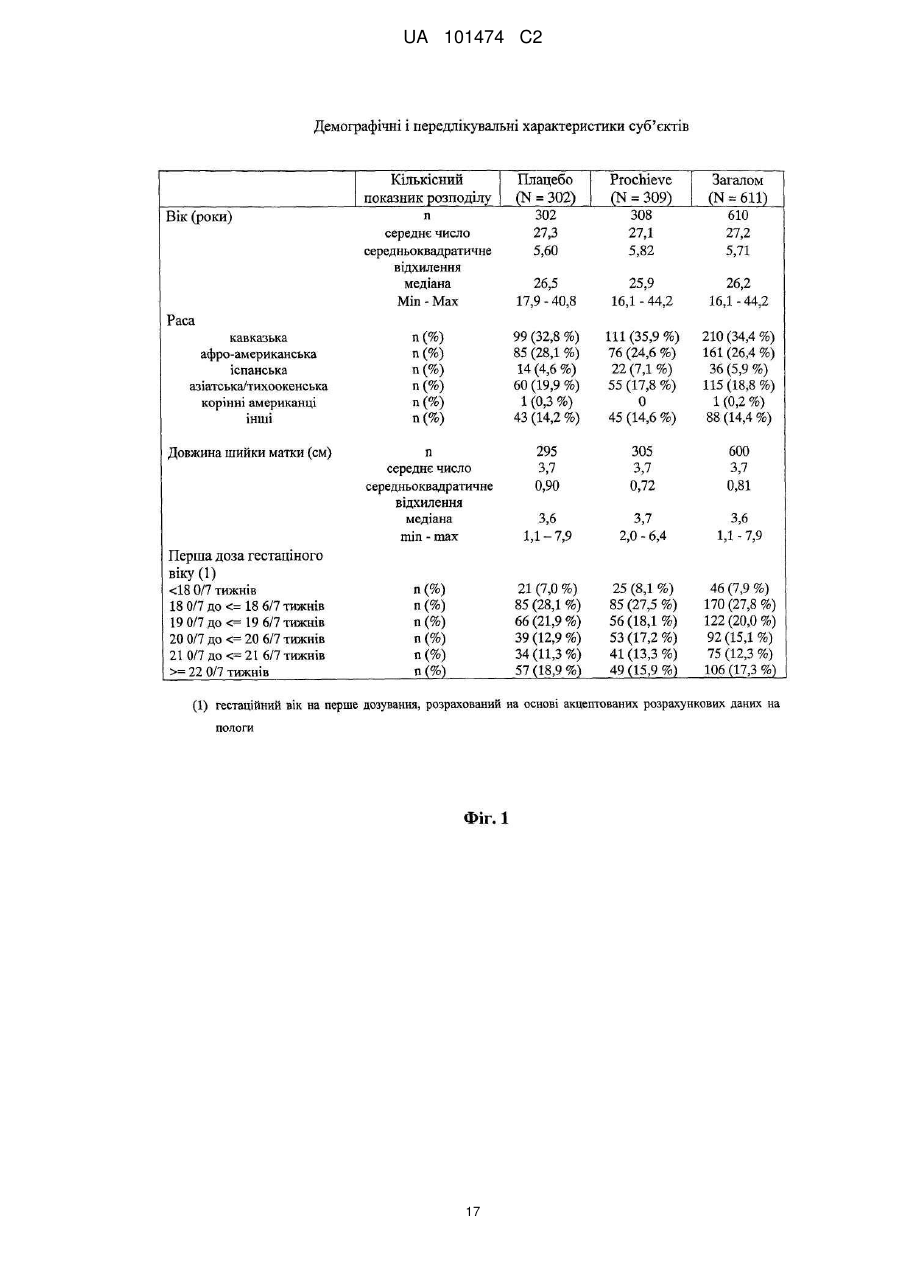
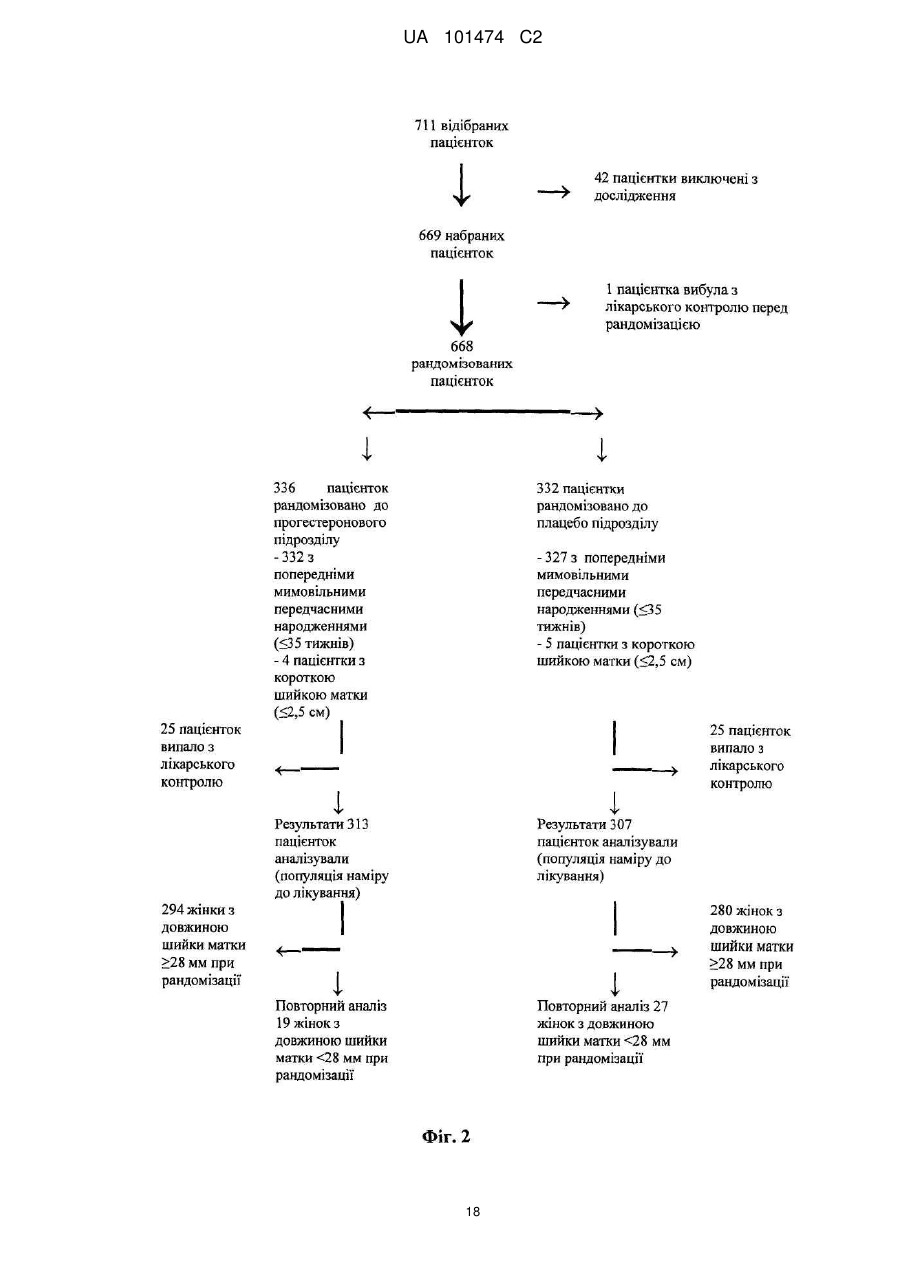
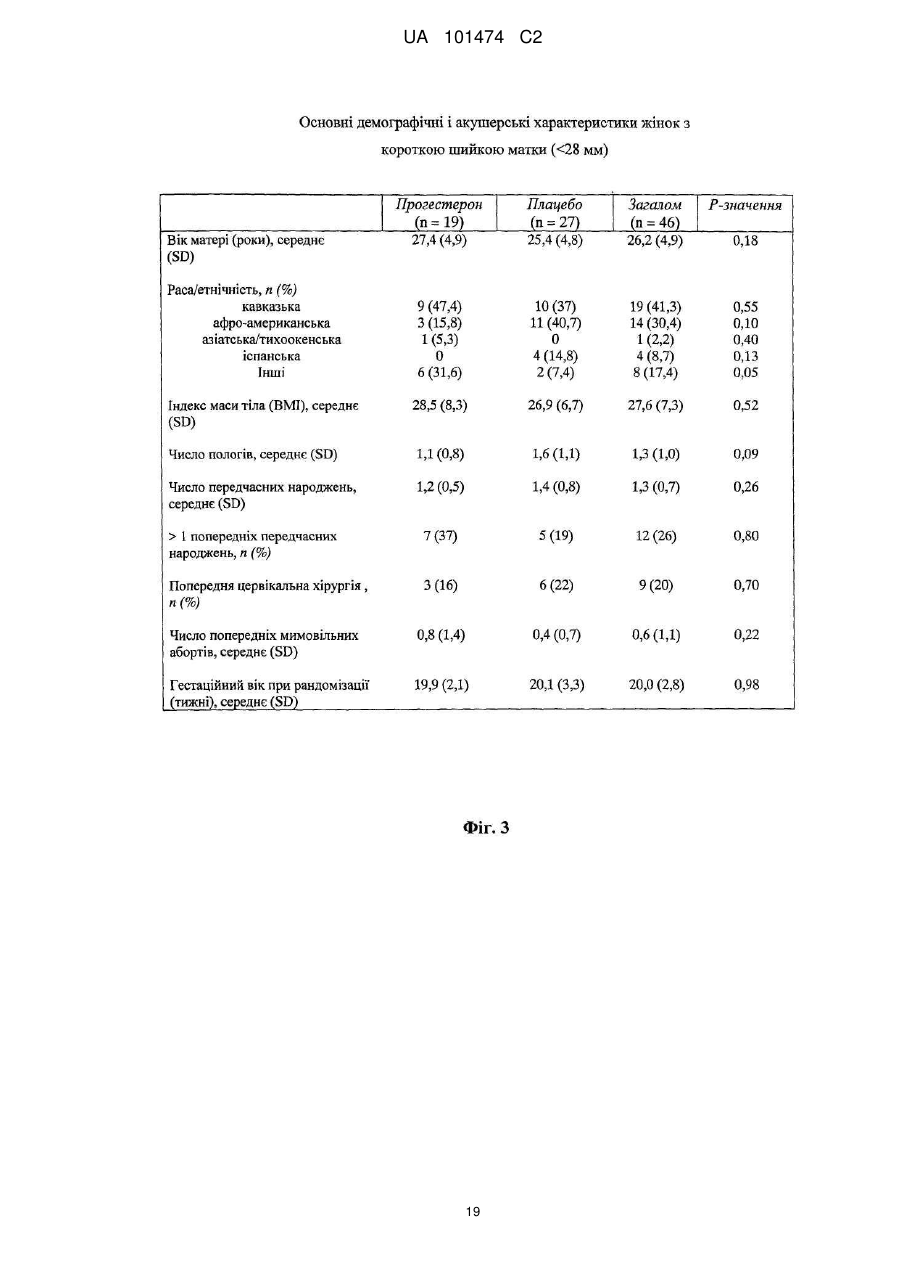
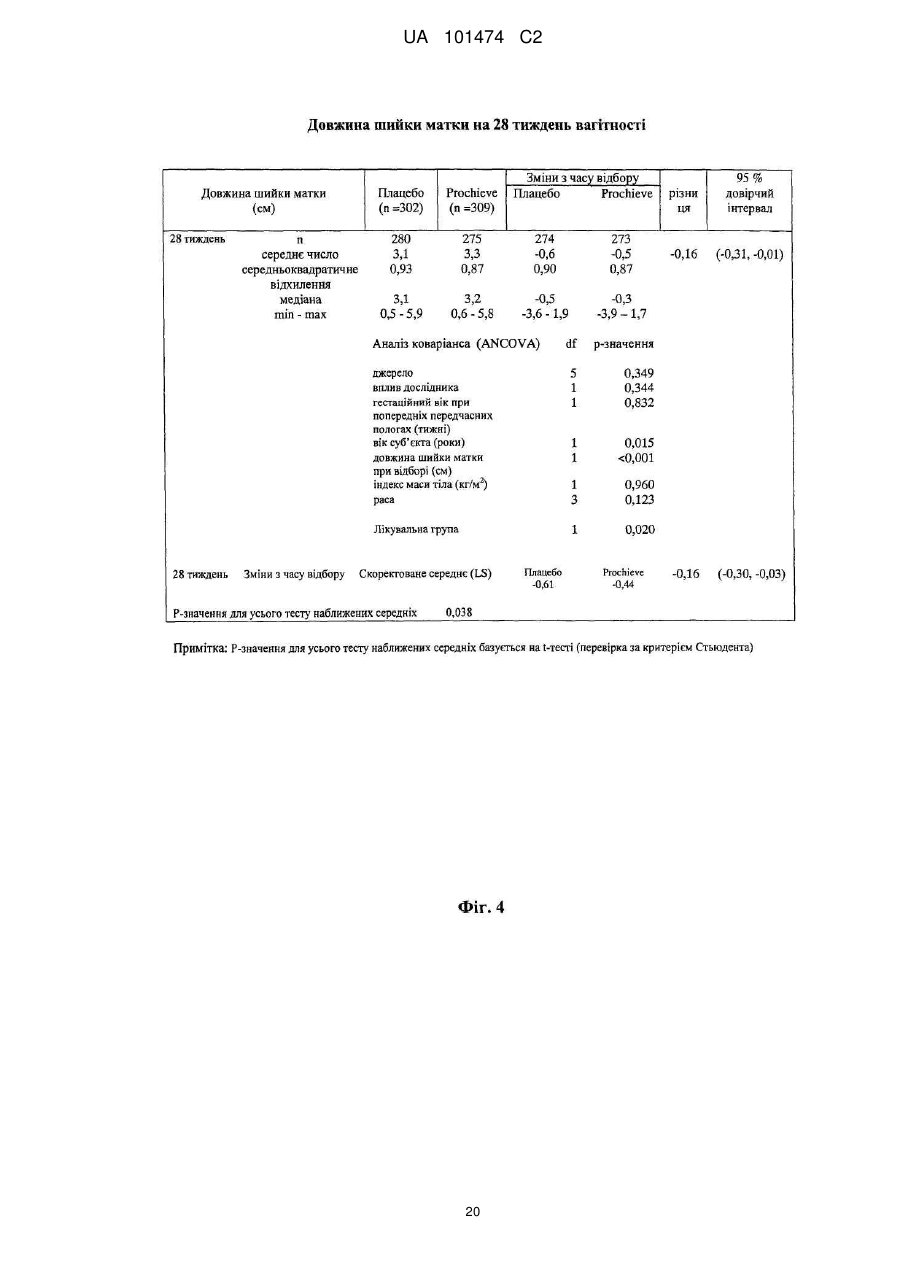
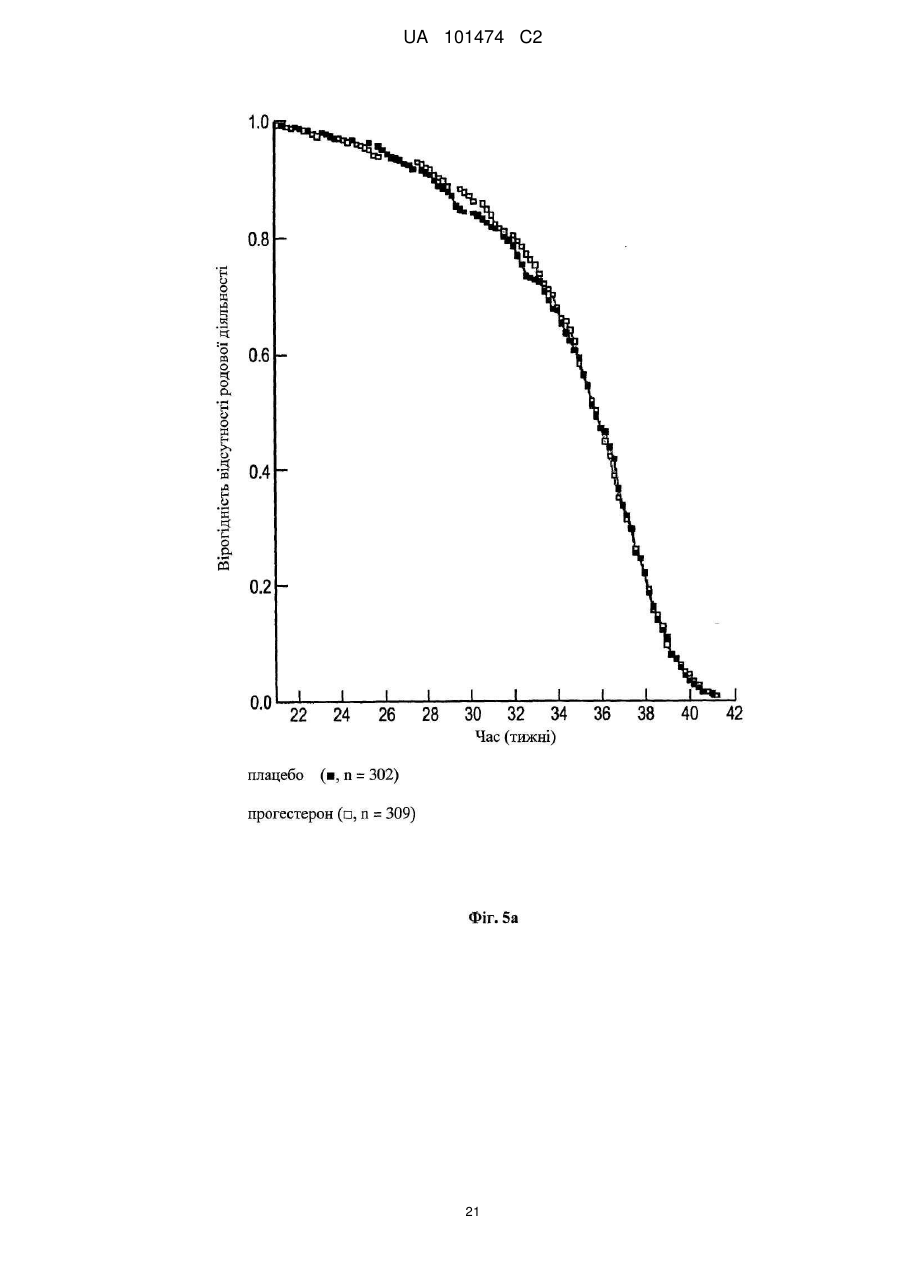
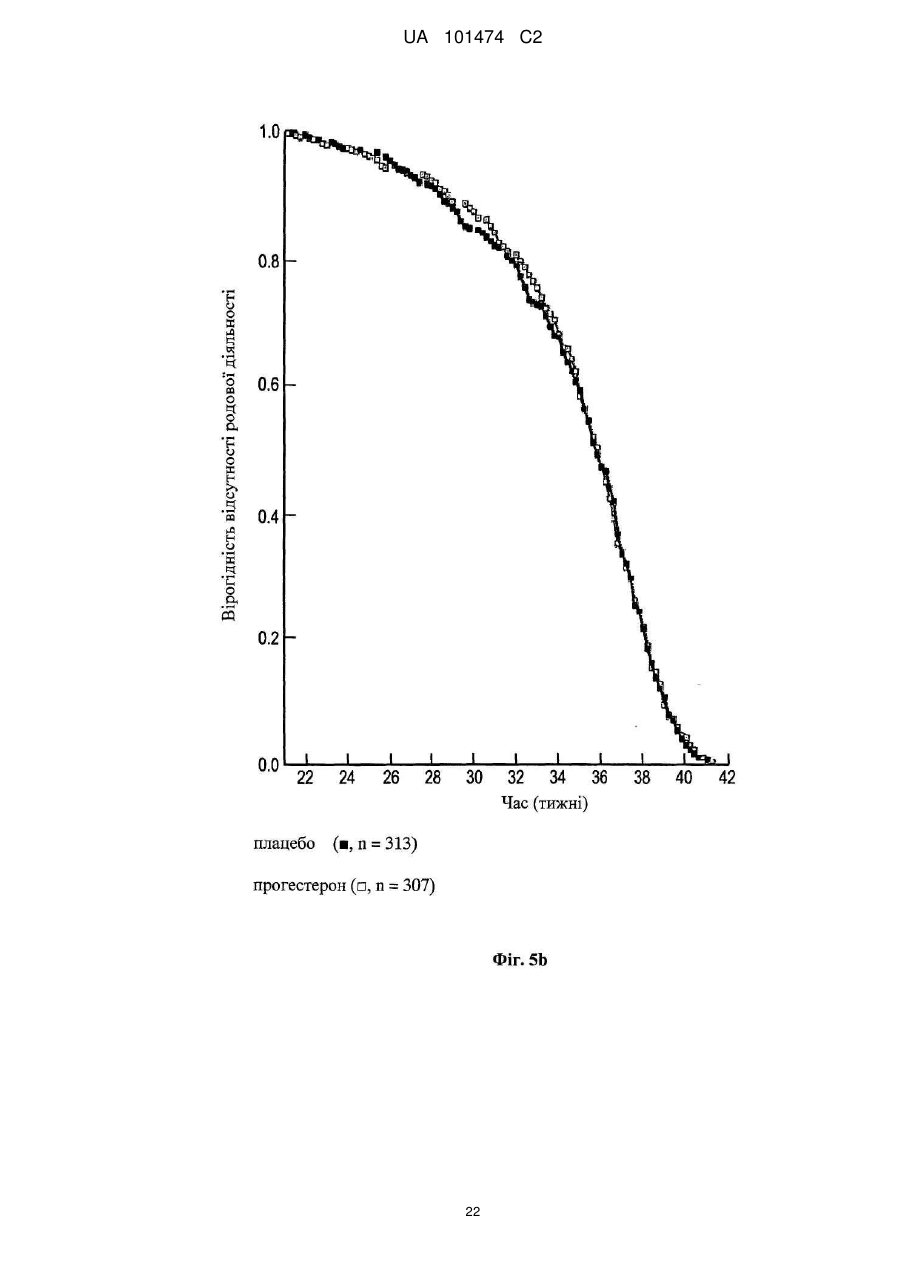
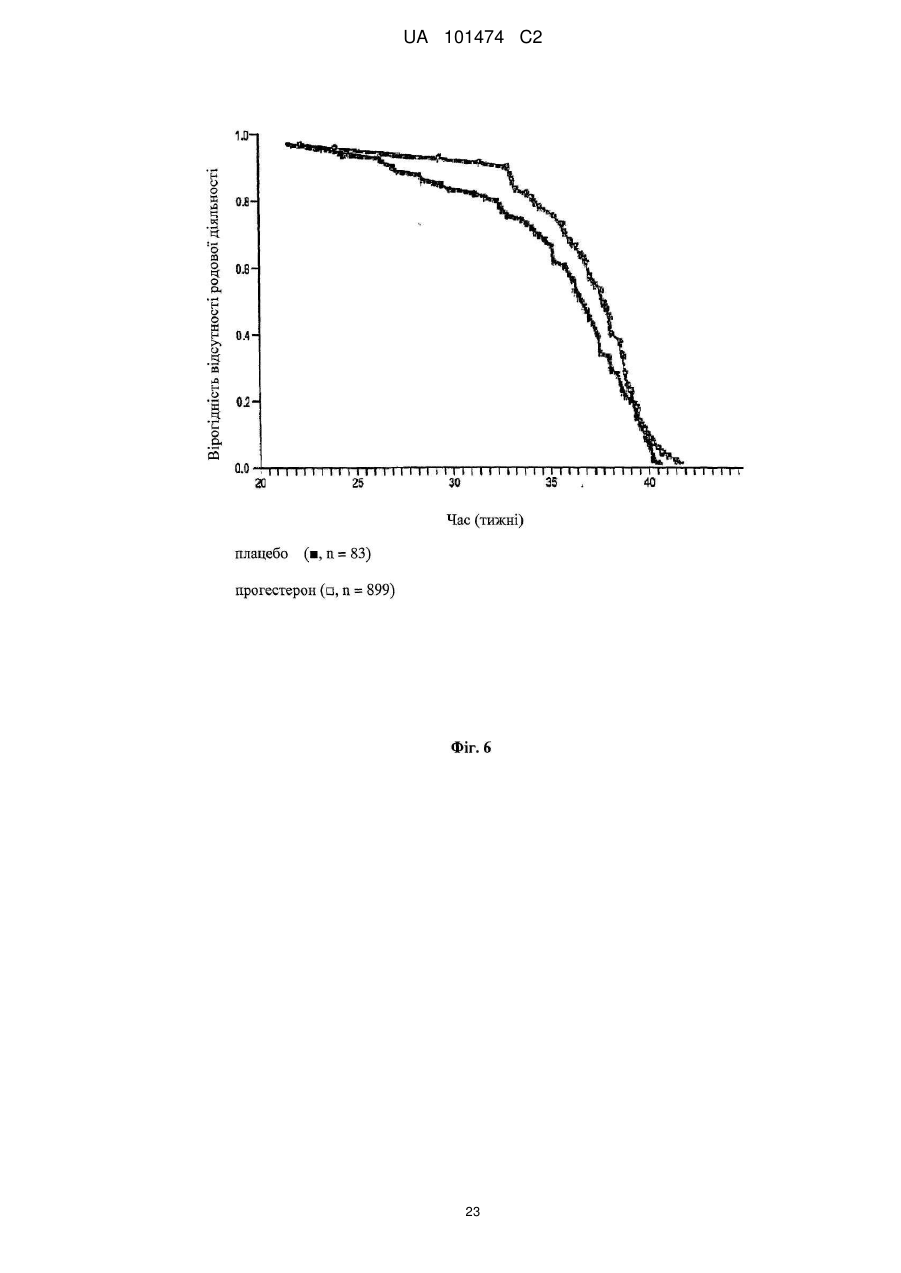
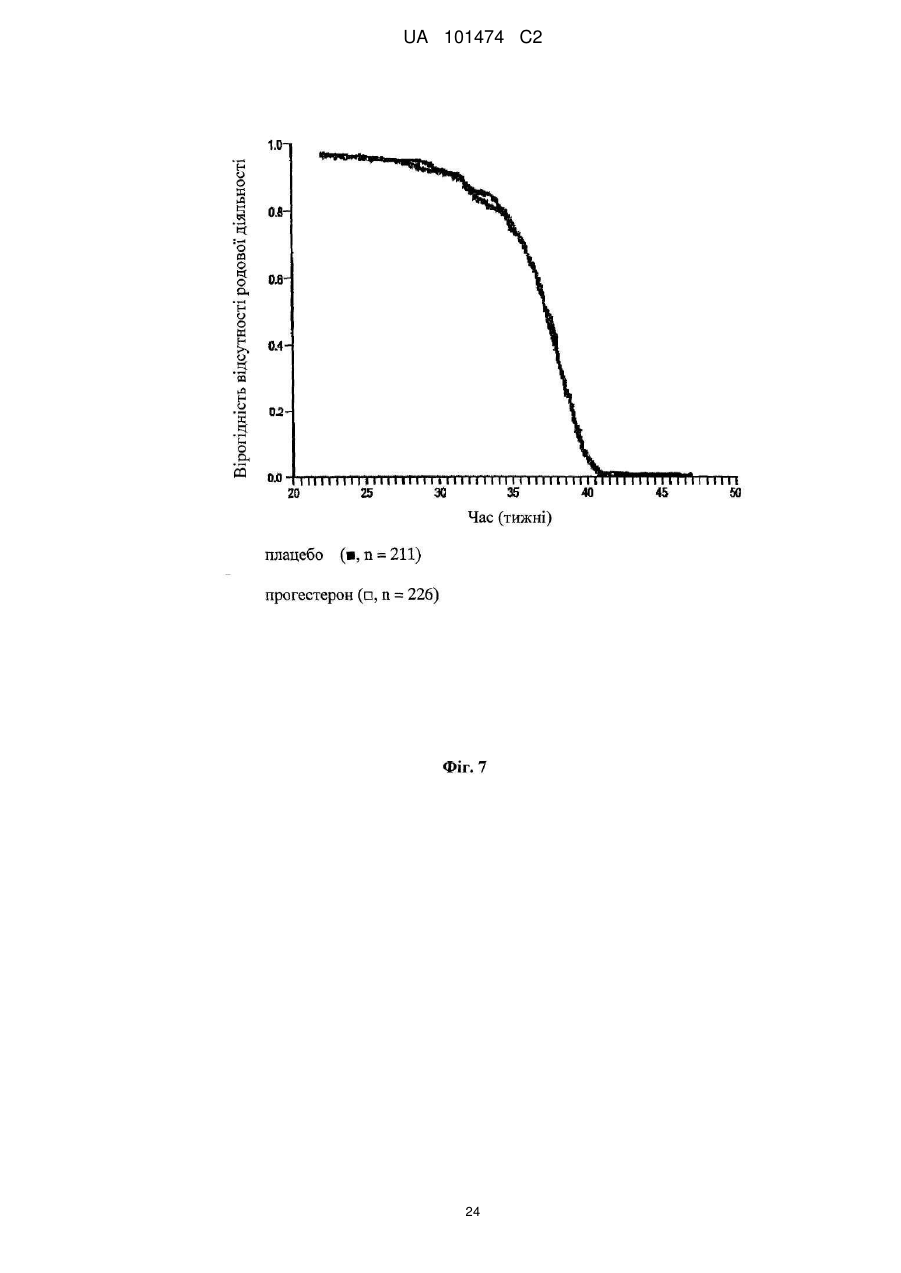
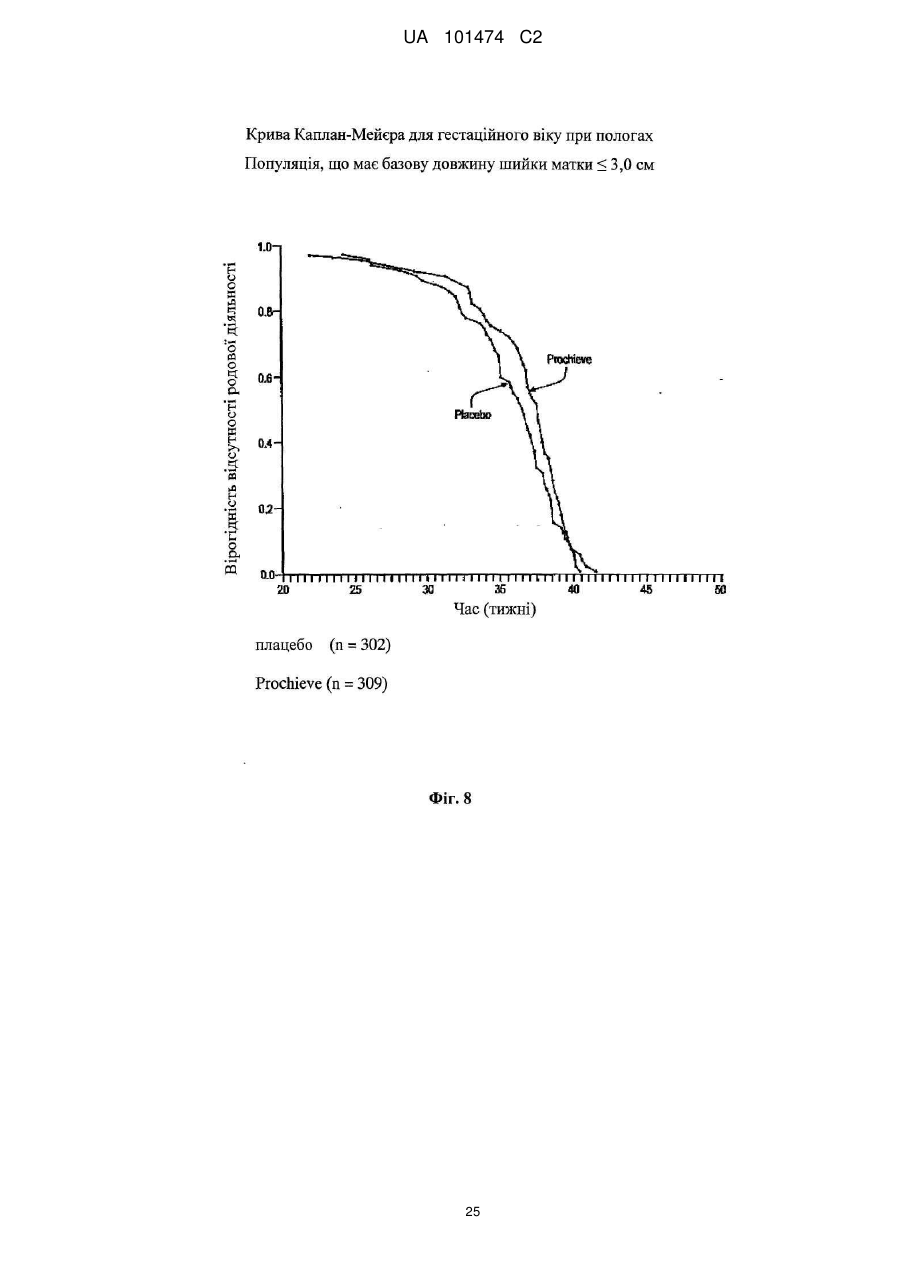
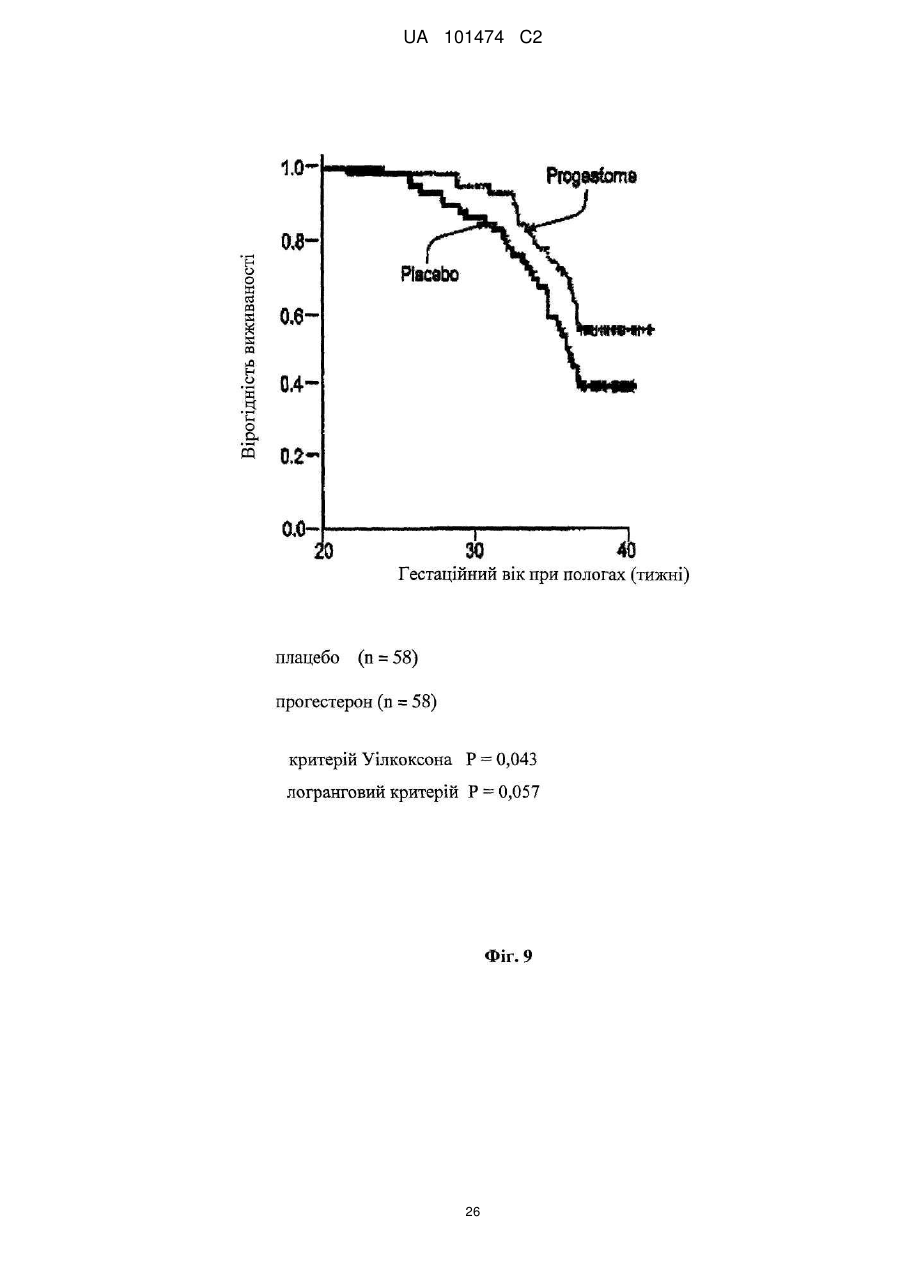
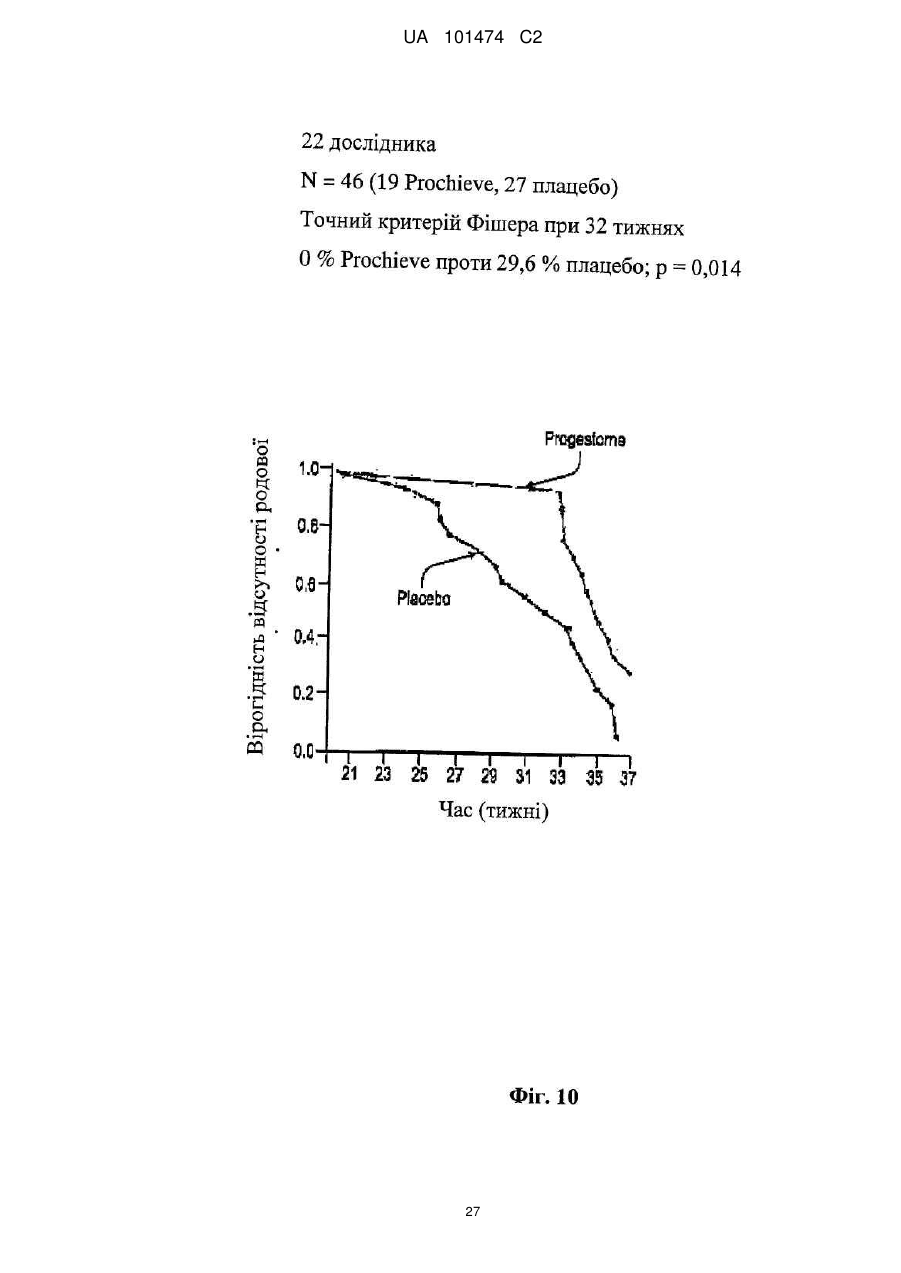
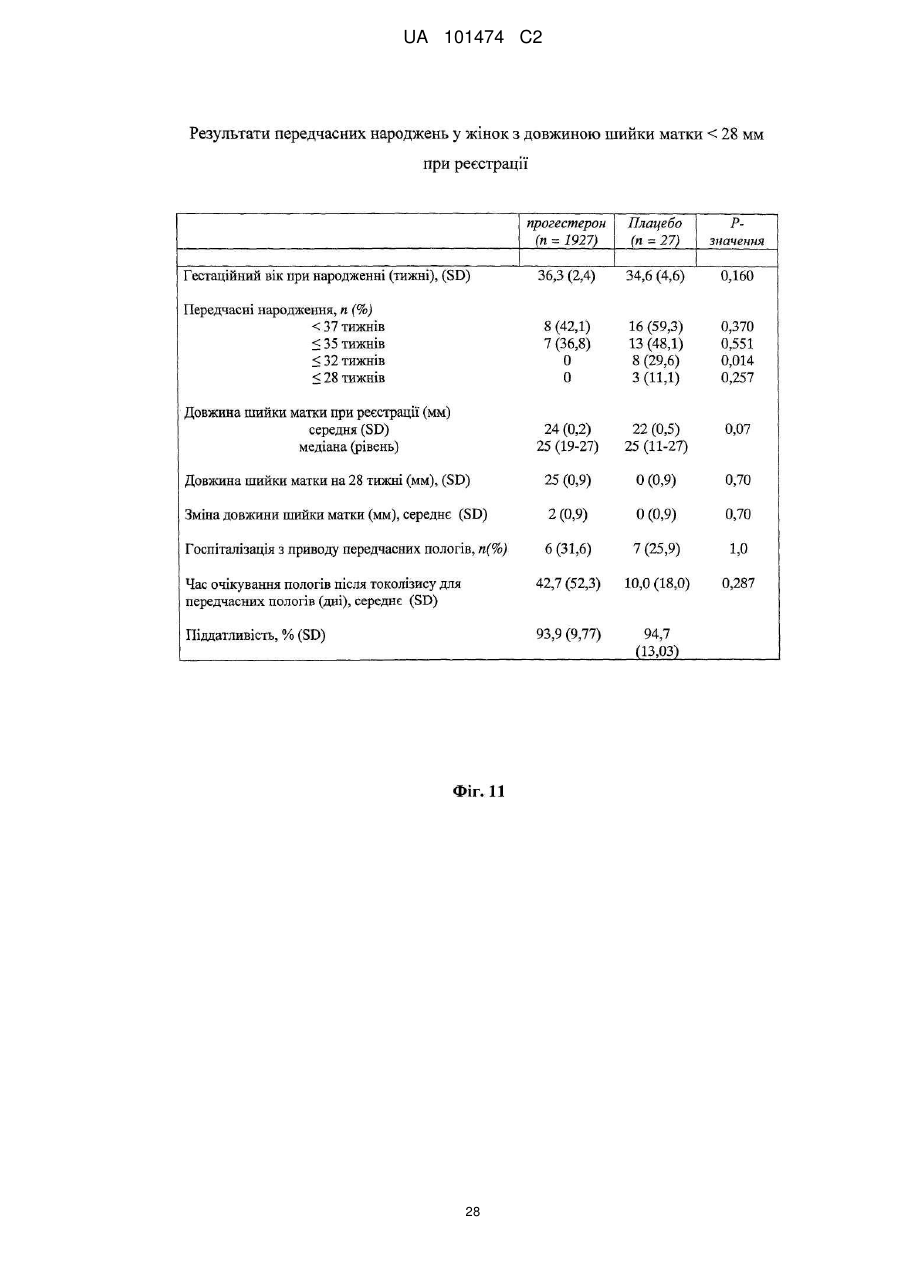
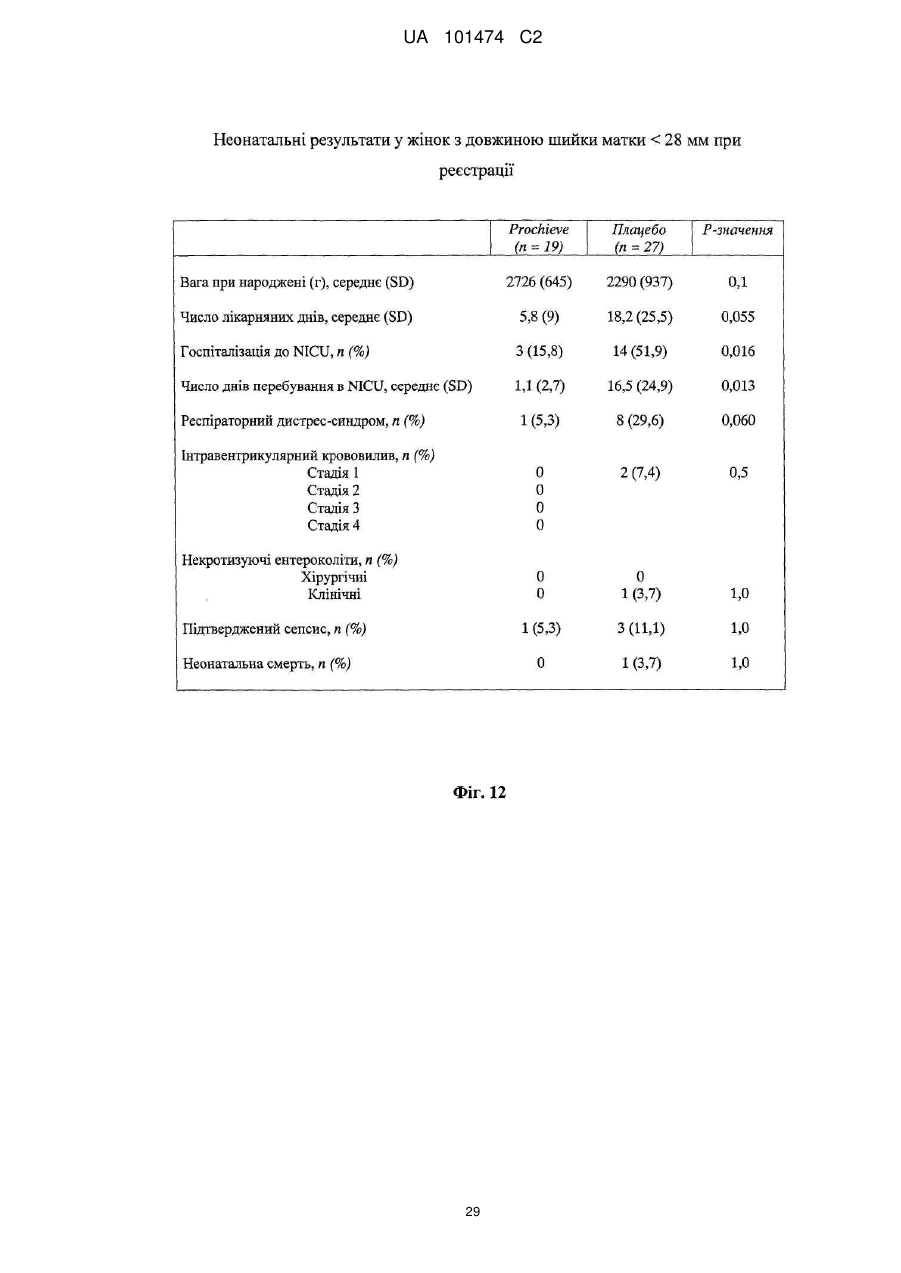
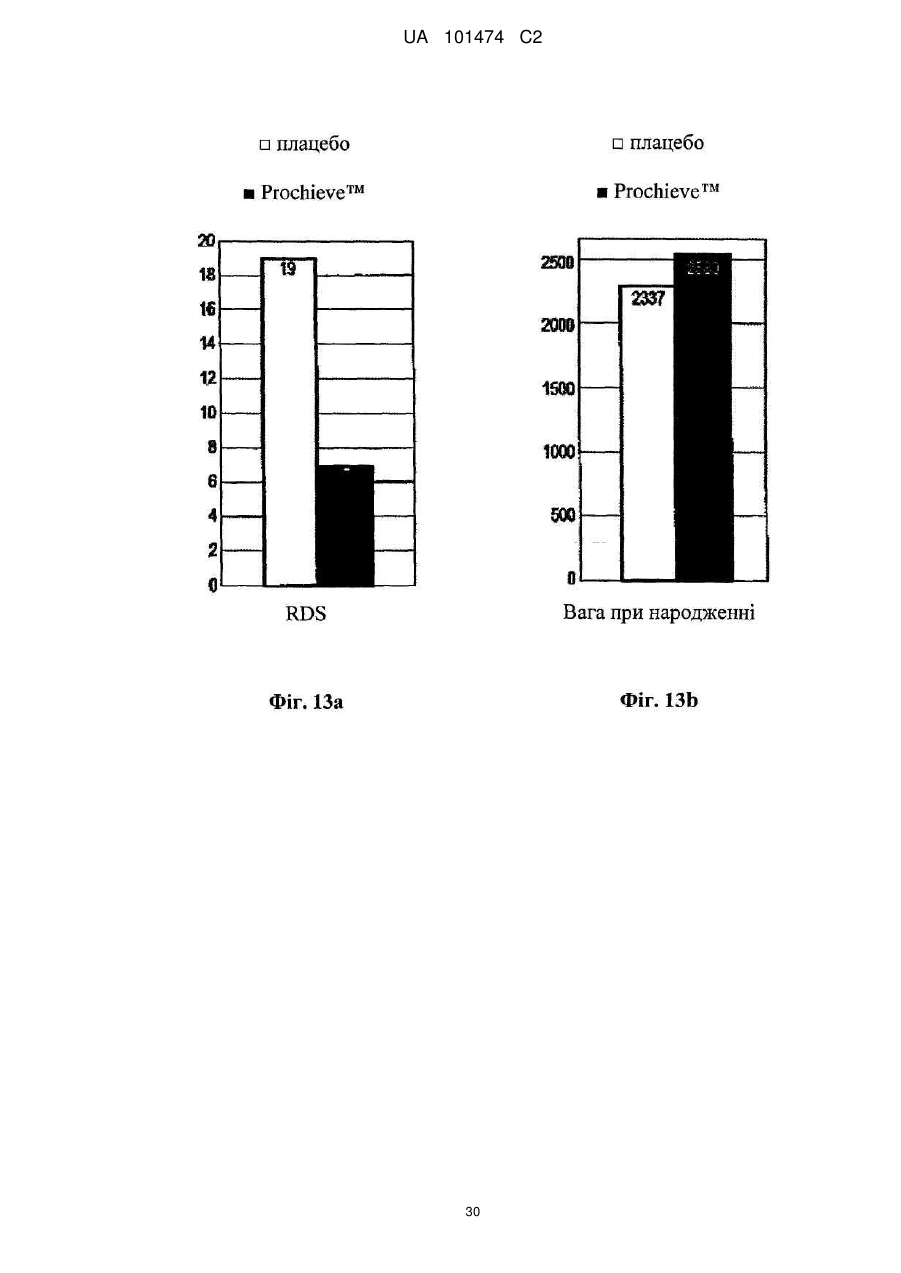
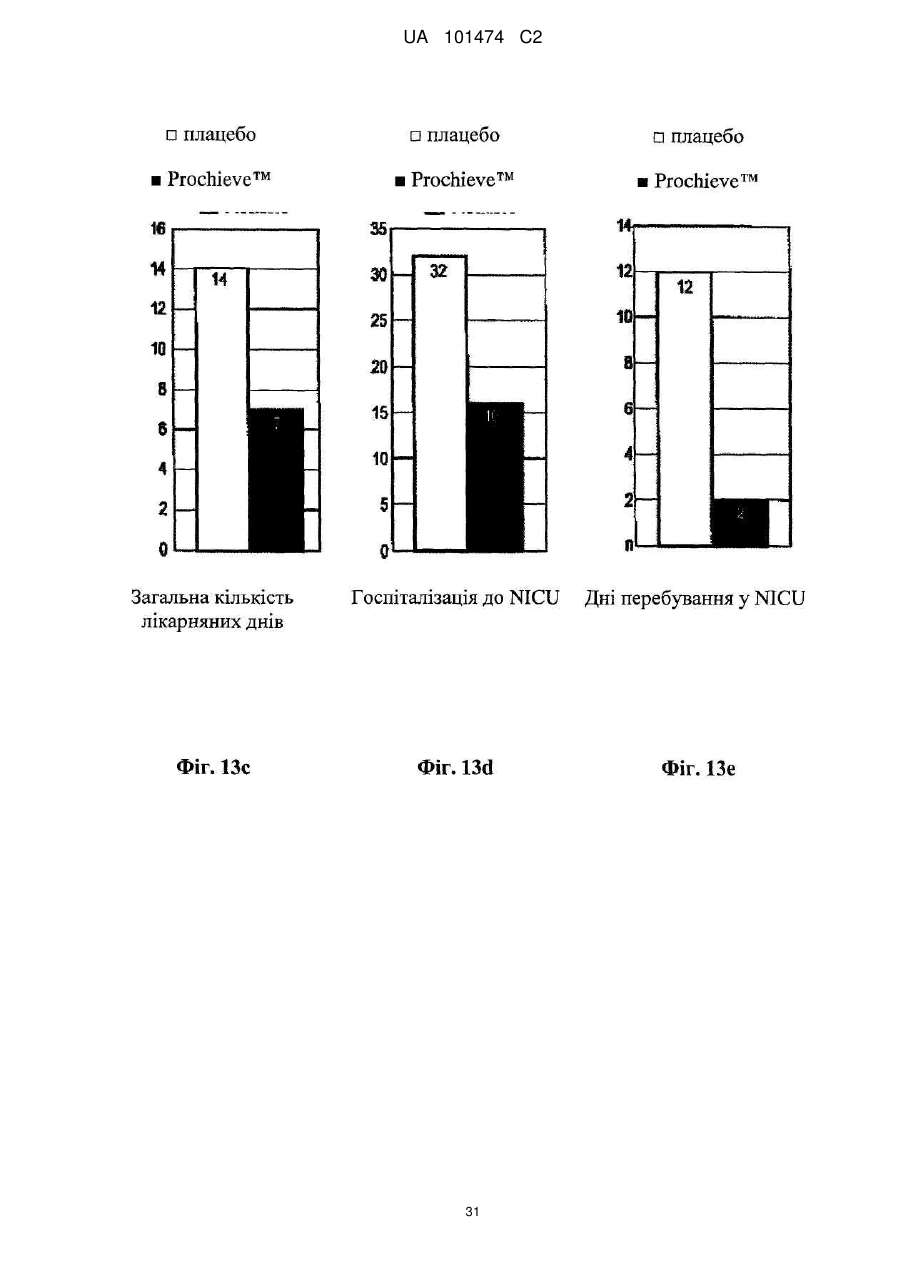
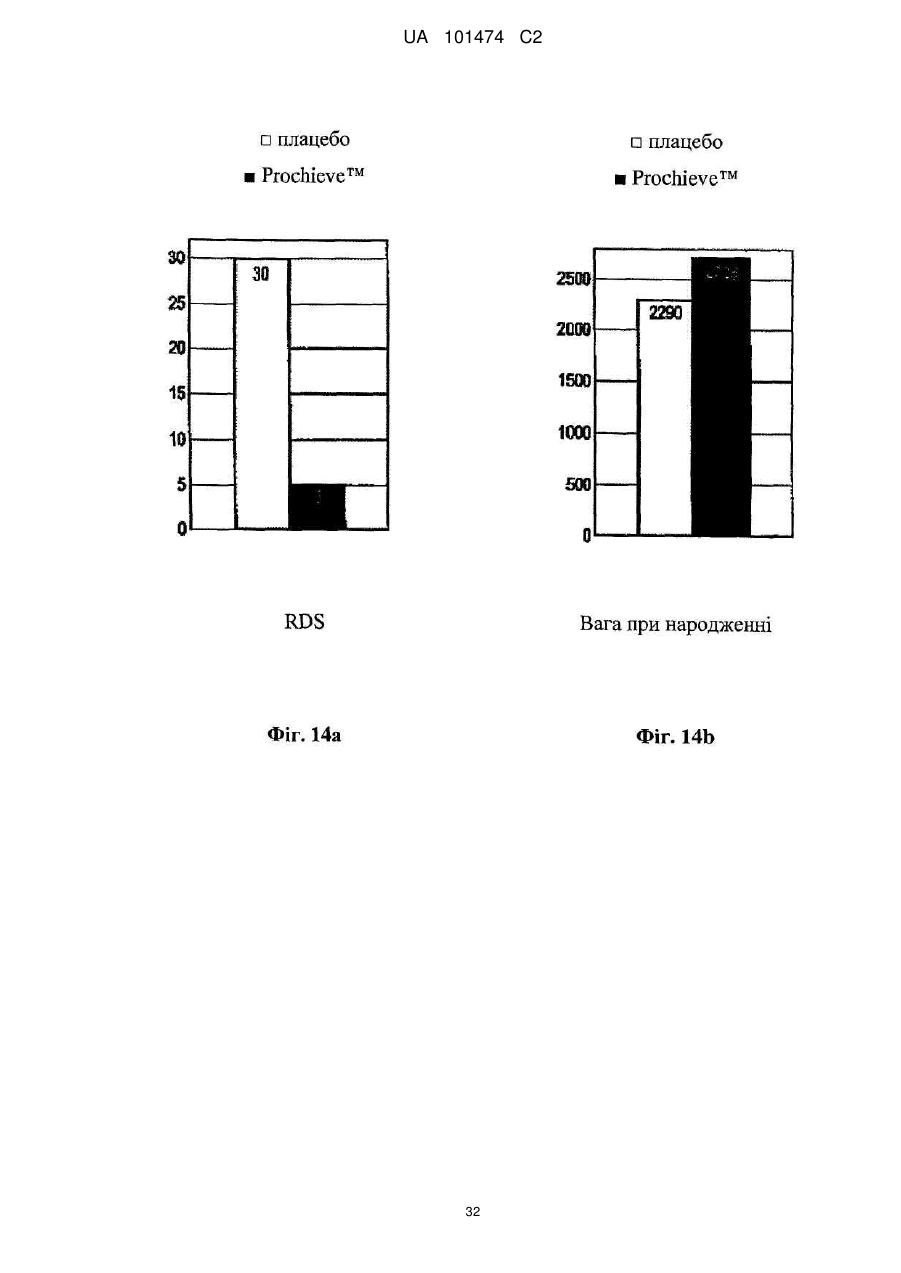
Реферат: Винахід належить до медицини, стосується застосування прогестерону для виробництва лікарського засобу для подовження вагітності шляхом мінімізації укорочення або стоншення шийки матки. UA 101474 C2 (12) UA 101474 C2 UA 101474 C2 5 10 15 20 25 30 35 40 45 50 55 60 Ця заявка претендує на пріоритет попередньої заявки на патент США № 60/888,480; що була подана 6 лютого 2007, і попередньої заявки на патент США № 60/973,667; що була подана 19 вересня 2007, описи яких в повному обсязі включені в дану заявку шляхом посилання. Галузь винаходу Даний винахід належить до способу лікування або попередження мимовільного передчасного народження у вагітних жінок з метою покращення здоров'я новонародженого. Більш конкретно, винахід належить до способу лікування або попередження настання передчасних пологів, що ведуть до передчасного народження, шляхом введення вагітній жінці такої кількості прогестерону, яка є достатньою для продовження вагітності, відстрочуючи укорочення або стирання її шийки матки. Додатково, винахід належить до способу лікування або попередження настання передчасних пологів з метою зниження дитячої смертності або захворюваності шляхом введення вагітній жінці з клінічно вираженою короткою шийкою матки ефективної кількості прогестерону для затримки пологів та зниження дитячої смертності та/або захворюваності. Попередній рівень техніки Загальновідомо, що у вагітних жінок, які зазнають мимовільне передчасне народження, починаються передчасні пологи (також рівноцінно названі в даній заявці "ранні пологи") і запускаються регулярні скорочення, що примушують їх шийку матки починати відкриватись або стоншуватись (названі розкриття і стоншення шийки матки) і розм'якшуватись до досягнення приблизно 37 тижнів вагітності. Якщо жінка народжує дитину раніше 37 тижнів, то це зазвичай і загальноприйнятно називається передчасним народженням і дитина вважається недоношеною. Передчасне народження залишається однією з найбільш серйозних проблем в акушерстві і жахливим ударом для немовлят, їх сімей і нашого суспільства. Згідно з недавнім дослідженням, оприлюдненим Інститутом Медицини, відсоток передчасних пологів зріс на 33 %, починаючи з 1981, і кожен рік тільки в одних США приблизно 500 тисяч жінок народжують передчасно, що приводить до 26 мільярдів доларів річних витрат на передчасне народження в національній системі охорони здоров'я. Недавно було повідомлено, що передчасні народження зустрічаються у 15 % вагітностей в світі і 12,7 % усіх народжень в Сполучених Штатах в 2006 році та 12,4 % усіх народжень в Сполучених Штатах в 2004. Дивись, наприклад, Use of progesterone to reduce preterm birth, American College of Obstetricians and Gynecologists Committee Opinion No. 291, Vol. 102, No. 5, November 2003, pages 1115-1116; Hamilton, В. Е., Annal Summary of Vital Statistics: 2005, Pediatrics, Vol. 119, No. 2, February 2007, pages 345-360. Вважається, що передчасне народження раніше 32 тижнів вагітності являє собою надзвичайно високий ризик захворюваності та смертності. Додатково, передчасне народження між 32 та 36 тижнями вагітності вважається особливо загрозливим, як таке, що має чисельні ризики для немовлят. Передчасні пологи несуть відповідальність за 60-70 % дитячої смертності і є причиною головних витрат на медичну допомогу як в перинатальний період, так і впродовж життя дітей, котрі вижили. Недавні досягнення в акушерстві та неонатальному догляді привели до покращення дитячої виживаності, проте 55 % новонароджених з екстремально низькою вагою при народженні (< 1000 г) або народжені дуже рано (< 28 тижнів), які дожили до середнього дитячого віку, демонструють виражену клінічно значиму пізнавальну, освітню та поведінкову недостатність. Приблизно 20 % - 30 % передчасних народжень є результатом рішення лікаря викликати пологи через материнські показники або показники плоду. Інша частина передчасних народжень є мимовільною, зазвичай після атаки передчасних пологів або внаслідок розриву мембран. Було ідентифіковано декілька факторів ризику для передчасних пологів, включаючи мультиембріональну вагітність, материнський стрес, системну та внутрішньоматкову інфекцію, расу та соціальноекономічний статус. Попереднє прогностичне дослідження показало, що історія попередніх мимовільних передчасних пологів є вагомим передбаченням наступних передчасних пологів з раннім народженням через 23-27 тижнів зі зростанням ризику вії разів. Проте, нажаль, методи оцінки ризиків із застосуванням лише історичних факторів ризику мають неприйнятно низьку чутливість і слабке прогностичне значення. Підкріплення історично обгрунтованої оцінки ризиків технологією, особливо ультразвуковим дослідженням шийки матки, додає вдосконалену чутливість і специфічність. Ультразвукова ідентифікація стоншення шийки матки корелює з логарифмічним підвищенням ризику передчасних пологів. Дивись lams et al, The length of the cervix and the risk of spontaneous premature delivery, N. Engl. J. Med. 1996; 334: 6 %7-572. Серед передчасно народжених дітей, що вижили, багато страждає від пожиттєвих труднощів, таких як церебральний параліч, розумове відставання, хронічні захворювання 1 UA 101474 C2 5 10 15 20 25 30 35 40 45 50 55 легень, дефіцит слуху і зору та нездатність до навчання. Більш зріла дитина при народженні, більш імовірно він або вона, виживає і, менш імовірно він або вона, має пов'язані зі здоров'ям проблеми. Недоношені діти, народжені між 34 і 37 тижнями, є загалом відносно здоровими. Проте, якщо жінка іде на пологи через 34 тижні, то ризики небезпечних впливів на здоров'я та/або медичних ускладнень зростають. Загальновідомо, що довжина шийки матки жінки є надійним показником того, чи вагітна жінка зазнає передчасні пологи і передчасне народження. Лікарі зазвичай перевіряють довжину шийки матки під час першого пренатального візиту і, таким чином, вони можуть контролювати зміни довжини шийки матки як прогресування вагітності. Якщо у жінки шийка матки стає коротшою в другий триместр вагітності, то це означає, що шийка матки починає згладжуватись (стоншуватись), і це є надійним показником того, що у жінки є високий ризик передчасних пологів. Укорочення шийки матки і, до деякої міри, такі характеристики, як історія попередніх передчасних народжень, вік, етнічна належність, індекс маси тіла (ВМІ) і хірургічне втручання з приводу шийки матки, є загальновідомими факторами ризику, що стосуються передчасного народження. Дані підтримують зворотній зв'язок між довжиною шийки матки і передчасними пологами. При перспективному дослідженні 2915 жінок, у яких вивчався взяємозв'язок між короткою довжиною шийки матки і передчасними пологами, дослідники знайшли, що навіть незначне зменшення довжини шийки матки між 24 і 28 тижнями вагітності було пов'язане зі зростанням ризику передчасного народження (RR 2,03; 95 % СІ, 1,28-3,22). Дивись lams et al, The length of the cervix and the risk of spontaneous premature delivery, N. Engl. J. Med. 1996; 334: 6 %7-572. При 24 тижнях, у порівнянні з жінками, у яких довжина шийки матки була вище приблизно 75 % норми, жінки, які мали довжину шийки матки 25 % від норми (< 3,0 см), мали відносний ризик передчасних пологів 3,79 (95 % СІ, 2,32-6,19); ті жінки, що мали довжину шийки матки 10 % від норми (< 2,6 см), мали відносний ризик передчасних пологів 6,19 (95 % СІ, 3,849,97); жінки, що мали довжину шийки матки 5 % від норми (< 2,2 см), мали відносний ризик 9,49 (95 % СІ, 5,95-15,15); і жінки, що мали довжину шийки матки 1 % від норми (< 1,3 см), мали відносний ризик 13,99 (95 % СІ, 7,89-24,78). Інші дослідження виявили, що моніторинг довжини шийки матки може допомогти ідентифікувати жінок з підвищеним ризиком рекурентного передчасного народження. Дивись, Spong, С, Prediction and prevention of recurrent spontaneous preterm birth, American College of Obstetricians and Gynecologists, Vol. 110, No. 2, Part 1, August 2007, pages 407-408. На сьогодні в Сполучених Штатах відсутня будь-яка схвалена терапія для запобігання передчасних народжень. Дивись доповідь по передчасному розродженню Інституту Медицини, 2006. Існуюча медична практика попереджувальних лікувань щодо короткої шийки матки в ранній вагітності залучає механічні/хірургічні лікування. Наприклад, цервікальний серкляж є хірургічною процедурою, при якій шийку матки зашивають або закривають накладенням швів, тким чином фізично захищаючи шийку матки від передчасного укорочення або стоншення. Шви потім видаляють, зазвичай приблизно на 37 тижні, щоб дозволити шийці матки нормально розкритися під час пологів. Нажаль, типові несприятливі ефекти, асоційовані з процедурою цервікального серкляжу, включають ризик передчасних скорочень, цервікальної дистоції (нездатність шийки матки нормально розкриватись під час пологів), цервікальні інфекції та інші ризики, зазвичай пов'язані з хірургічними процедурами, надодачу і викликають полеміку з приводу ефективності серкляжу в лікуванні короткої шийки матки. Декілька недавніх досліджень свідчать рпро те, що це хірургічне лікування не краще за плацебо. Хоча відомо, що довжина шийки матки, особливо укорочення шийки матки, корелює з передчасним народженням, але на сьогодні невідомо про ефективність якого-небудь нехірургічного втручання. Дивись Spong, C, pages 407-408. Тобто, зараз відсутня будь-яка загальноприйнятна лікувальна процедура для фактору ризику передчасних пологів та народження, відомого як "коротка шийка матки". Пропагується введення прогестерону длязапобігання передчасного народження у деяких жінок, для яких визнається високий ризик, хоча попередня увага фокусувалась на пацієнтках з попередньою історією передчасних народжень. Ефективність вагінального введення прогестерону для попередження передчасного народження у жінок з особливо високим ризиком передчасних пологів, особливо у жінок, що зазнають укорочення шийки матки, є далекою від реальної і в значній мірі невідома. O'Brien et al., наприклад, визначили, що профілактичне лікування вагінальним прогестероновим гелем фактично не знижує частоту рекурентних передчасних народжень у жінок з високим ризиком, вибраних з історичних та мимовільних передчасних народжень. Крім того, як передбачено Committee on Obstetric Practice of the American College of Obstetricians and Gynecologists в публікації Use of Progesterone to Reduce 2 UA 101474 C2 5 10 15 20 25 30 35 40 45 50 55 60 Preterm Birth, American College of Obstetricians and Gynecologists Committee Opinion No. 291, Vol. 102, No. 5, November 2003, pages 1115-1116, є невідомою ідеальна композиція прогестерону. Застосування прогестерону для лікування усіх жінок з ризиком передчасного народження на даний час не має абсолютної підтримки. Декілька авторів виразило необхідність в розроблених, рандомізованих дослідженнях на більших популяціях для ідентифікації ідеальної прогестеронової композиції та дозування, і для того, щоб продемонструвати зменшення передчасних народжень раніше 37 тижнів та зниження дитячої захворюваності і смертності. Дивись, наприклад, Dodd et al, Prenatal administration of progesterone for preventing preterm birth, Cochrane Database SystRev 2006. Хоча існує багато дебатів стосовно застосування прогестерону щодо народження, особливо щодо періоду вагітності, є небагато, якщо взагалі є, звичайних технологічних аналізуючих дій щодо неонатальних популяцій, що базуються на лікуванні для попередження передчасних народжень. Мета-аналіз рандомізованих досліджень із залученням жінок виявив, що може мати місце зниження ризику передчасного народження менше ніж за 37 тижнів і 34 тижні. Dodd, J.M. et al, Prenatal administration of progesterone for preventing preterm birth (Review), The Cochrane collaboration, John Wiley Sons, Ltd, 2006, pages 1-36. Однак, що важливо, не було статистично значущої різниці щодо частоти перинатальної смерті у жінок, яким вводили прогестерон, і тими, що приймали плацебо. Dodd, J.M. et al, pages 4-5. Фактично, не повідомлено про жодні відмінності щодо неонатальних результатів між плацебо і прогестероновими групами. Dodd, J.M. et al, pages 4-5; Mackenzie, R. et al., Progesterone for the prevention of preterm birth among women at increased risk: A systematic review and meta-analysis of randomized controlled trials, Journal of Obstetrics and Gynecology, 194, 2006, pages 1234-42. Одне дослідження надало інформацію стосовно пролонгації вагітності і дитячої захворюваності. Lam, F. et al, Evaluation of the pregnancy prolongation index (PPI) as a measure of success of obstetric interventions in the prevention of preterm birth and associated morbidities, Journal of Obstetrics and Gynecology, 192, 2005, 2047-54. Проте, це дослідження не забезпечило ніяких порівняльних експериментальних даних щодо лікувальних груп і контрольних груп. Окрім того, це вивчення не стосувалося застосування прогестерону для лікування або попередження передчасного народження. Кінець кінцем, це вивчення було обмежене дослідженням неонатального здоров'я просто як функції гестаційного віку при пологах, а не як наслідок лікувального/профілактичного агента. Тому, є потреба в методі лікування або запобігання настання передчасних пологів і передчасного народження у вагітних жінок, особливо жінок, які мають коротку шийку матки, без несприятливих для здоров'я наслідків, що на даний час зазвичай асоціюються з відомими методами. Окрім того, щоб тільки зосереджуватись на здоров'ї матері, яка народжує, є потреба зосередитись на та втрутитись в покращення неонатального результату. Тобто, передчасне народження асоціюється з високою перинатальною захворюваністю і смертністю і пригнічення передчасних пологів зазвичай не пов'язувалось з покращеними дитячими результатами. Традиційна технологія не демонструє жодної безпосередньої користі для здоров'я новонародженого. Тому існує потреба в технології лікування та/або профілактики з метою поліпшити натальне, особливо неонатальне, здоров'я під час народжень, які стались передчасно. Суть винаходу Даний винахід направлений на спосіб лікування або попередження настання передчасних пологів і наступного передчасного народження у вагітних жінок, в переважному втіленні спосіб включає введення вагітній жінці, яка цього потребує, ефективної кількості прогестерону, що є достатньою для того, щоб продовжити вагітність шляхом затягування укорочення і стоншення шийки матки. Переважно, прогестерон вводять як вагінальний гель, як вагінальний супозиторій, як вагінальний крем або вагінальна тверда дозована форма (така, як таблетка), або за допомогою вивільняючих пристроїв, введених у вагіну, таких як цервікальне кільце або інші пристрої, добре відомі з рівня техніки. Даний винахід забезпечує спосіб покращення неонатального здоров'я, тобто, зниження захворюваності та/або смертності у новонароджених жінками з короткою довжиною шийки матки в другому триместрі вагітності. Спосіб зниження неонатальної захворювальності і смертності включає введення вагітній жінці з короткою або стоншеною шийкою матки, яка цього потребує, ефективної кількості прогестерону, достатньої для подовження вагітності. В деяких втіленнях немовлята, народженні жінками, що отримували лікування та/або профілактику прогестероном, характеризувались зниженою неонатальною захворюваністю та смертністю, зменшенням кількості днів, проведених у відділенні інтенсивної терапії новонароджених (NICU), зниженням вірогідності госпіталізації до NICU або їх комбінацією у порівнянні з дітьми, 3 UA 101474 C2 5 10 15 20 25 30 35 40 45 50 55 народженими матерями, які не отримували ефективну кількість прогестерону під час вагітності. В переважних втіленнях, прогестерон, природний або синтетичний, або його похідні в кількості між приблизно 45 мг та приблизно 800 мг вводять як вагінальний гель. Ще в додаткових втіленнях прогестерон вводять щодня, починаючи приблизно з 18-22 тижня вагітності до приблизно 37 тижня вагітності, переважно приблизно 14-19 тижнів. Ще в інших втіленнях даного винаходу прогестерон вводять вагітній жінці, шийка матки якої має довжину більшу ніж приблизно 1,0 см і більше, переважніше більше ніж 1,5 см, де прогестерон вводять вагітній жінці, шийка матки якої має довжину між приблизно 1,0 см та приблизно 8,0 см. Як варіант, довжина шийки матки у жінки, якій вводять прогестерон, є меншою ніж або дорівнює приблизно 3,0 см, переважно меншою ніж 2,8 см ще більш переважно меншою ніж 2,5 см. У втіленні даного винаходу прогестерон, який вводять, може бути молекулою прогестерону (з будь-якого джерела, включаючи природний і синтетичний) або метаболітами прогестерону (з будь-якого джерела, включаючи природний і синтетичний), або будь-які інші прогестини. Сам прогестерон є переважним, хоче можуть бути застосовані інші прогестини. Коли застосовують синтетичний прогестин, переважно синтетичний прогестерон вибирають з групи, що складається з похідних прогестерону або тестостерону, або похідних інших молекул з прогестогенною активністю. Такі прогестини включають 17-альфа-гідроксипрогестерону капроат, медроксипрогестерону ацетат, норетиндрон, норетиндрону ацетат, норетиндрону енантат, дезогестрел, левоногестрел, лінестренол, етинодіолу діацетат, норгестрел, норгестимат, норетинодрел, гестоден, дроспіренон, тримегестон, леводезогестрел, гестодин, нестерон, етоногестрел і похідні 19-нортестостерону, але не обмежуються ними. В переважному втіленні прогестерон включає як природні прогестини, так і прогестерон або 17альфа-гідроксипрогестерон. Деякі прогестини можуть вивільнятись вагінально, деякі шляхом внутрішньом'язової ін'єкції, деякі шляхом орального введення, деякі шляхом ректального введення, хоча можуть бути застосовані інші шляхи введення, добре відомі з рівня техніки. В переважному втіленні прогестерон вводять через систему доставки ліків, що містить прогестерон, водорозчинний, водонабрякаючий поперечно зшитий полімер полікарбонової кислоти і принаймні один ад'ювант. В переважному втіленні прогестерон вводять щодня вагінальним шляхом. Проте, введення може бути як рідшим - щотижневим, так і частішим - 4 рази на день, залежно від характеристик прогестину та прогестинової композиції. Переважно прогестерон вводять, починаючи з приблизно 18-22 тижня вагітності і аж до 37 тижня вагітності, або приблизно 14-19 тижнів, залежно від гестаційного віку на початок лікування та дати пологів. В іншому втіленні прогестерон вводять, починаючи приблизно з 16 тижня вагітності і аж до 37 тижня вагітності, або приблизно 21 тиждень. Ще в іншому втіленні прогестерон вводять, починаючи приблизно з часу позитивного тесту на вагітність і аж до приблизно 37 тижня вагітності, або починаючи приблизно з 2-4 тижня вагітності і впродовж приблизно 33-35 тижнів. Кількість введеного прогестерону переважно знаходиться між приблизно 45 мг і приблизно 800 мг і, більш переважно, між приблизно 90 мг та приблизно 250 мг, базуючись на прогестиновій дії природного прогестерону, введеного вагінально, але ця кількість може бути меншою або більшою, залежно від ефективності прогестину та шляху введення. Прогестерон переважно вводять вагітним жінкам, починаючи так рано, як настає вагітність, і тим жінкам, шийка матки яких має довжину, більшу ніж приблизно 1,0 см. Більш переважно прогестерон вводять вагітним жінкам, починаючи так рано, як настає вагітність, і тим жінкам, шийка матки яких має довжину принаймні приблизно 1,0 см і не більше ніж приблизно 8,0 см, та ще більш переважно, прогестерон вводять вагітним жінкам, шийка матки яких має довжину меншу ніж або дорівнює 2,5 см або 3,0 см. Інше втілення даного винаходу забезпечує удосконалені способи лікування або запобігання настання передчасних пологів і передчасного народження шляхом введення вагітній жінці кількості прогестерону, що є достатньою для мінімізації або затримки укорочення або стоншення її шийки матки та можливості розм'якшення та розкриття. Перелік фігур Інші особливості і переваги винаходу стануть очевидними з наданого опису з посиланням на додані Фігури, що показують можливі втілення винаходу за допомогою прикладу, але не обмежуючи його. Фіг. 1 - це таблиця, що містить початкові дані учасників дослідження, яке порівнює ефективність лікування передчасних народжень шляхом плацебо і груп лікування, що отримували прогестерон, відповідно до одного втілення винаходу; 4 UA 101474 C2 5 10 15 20 25 30 35 40 45 50 55 Фіг. 2 - це таблиця, що ілюструє профілі випробувань учасників відповідно до одного втілення винаходу; Фіг. 3 - це таблиця даних учасників з короткою шийкою матки, менше ніж 2,8 см, відповідно до одного втілення винаходу; Фіг. 4 - це таблиця, що містить дані про довжину шийки матки на 28 тиждень вагітності груп учасників, що отримували плацебо і лікування відповідно до одного втілення винаходу; На Фігурах 5а та 5b зображена крива часу пологів груп учасників, що отримували плацебо і лікування прогестероном відповідно до одного втілення винаходу; Фіг. 6 являє собою криву часу пологів учасників з початковою довжиною шийки матки меншою ніж або дорівнює 3,2 см відповідно до одного втілення винаходу; Фіг. 7 являє собою криву часу пологів учасників з початковою довжиною шийки матки більшою ніж 3,2 см відповідно до одного втілення винаходу; Фіг. 8 являє собою криву часу пологів учасників з початковою довжиною шийки матки меншою ніж або дорівнює 3,0 см відповідно до одного втілення винаходу; Фіг. 9 являє собою криву виживаності, що оцінює передчасні пологи аж до 37 тижнів для учасників з довжиною шийки матки меншою ніж або дорівнює 3,0 см відповідно до одного втілення винаходу; Фіг. 10 являє собою криву часу пологів учасників, що мають довжину шийки матки меншу ніж 2,8 см відповідно до одного втілення винаходу; Фіг. 11 являє собою таблицю, яка підсумовує результати передчасних пологів учасників дослідження з довжиною шийки матки меншою ніж 2,8 см при реєстрації відповідно до одного втілення винаходу, Фіг. 12 являє собою таблицю, яка підсумовує неонатальні результати учасників з початковою довжиною шийки матки меншою ніж 2,8 см відповідно до одного втілення винаходу; Фігури 13а-е репрезентують графіки, на яких зображені результати новонароджених для пацієнтів, що отримували плацебо і лікування та мали початкову довжину шийки матки < 3,0 см відповідно до одного втілення даного винаходу; та Фігури 14а-е репрезентують графіки, на яких зображені результати новонароджених у пацієнтів, що отримували плацебо і лікування та мали початкову довжину шийки матки < 2.8 см відповідно до одного втілення даного винаходу. Детальний опис переважних втілень винаходу В галузі акушерства є загальновідомим введення прогестерону вагітній жінці з короткою та стоншеною шийкою матки з метою впливу на церві кальне розкриття і стоншення для лікування та попередження настання передчасних пологів і передчасного народження. Зокрема, наскільки нам відомо, відсутня будь-яка література або інші публікації, що стосуються або свідчать проте, що прогестерон можна вводити вагітній жінці з короткою шийкою матки з метою пролонгування вагітності шляхом мінімізації укорочення та стоншення шийки матки і можливості її розм'якшення і розкриття. Даний винахід направлений на покращення неонатального здоров'я шляхом введення ефективної кількості прогестерону або його похідних вагітним жінкам, які мають короткі або стоншені шийки матки. В переважних втіленнях застосування прогестерону знижує захворюваність та/або смерність немовлят, народжених вагітними жінками з клінічно вираженою укороченою шийкою матки. В деяких варіантах новонароджені, чиї матері лікувались прогестероном, демонстрували принаймні: 1) зменшення кількості днів, проведених у відділенні інтенсивної терапії новонароджених (NICU) та 2) менший відсоток госпіталізацій до NICU, (тобто, зниження відсотка малят, госпіталізованих до NICU). Немовлята, народжені жінками, яким вводився прогестерон впродовж вагітності, також демонструють нижчу інцідентність хвороб та розладів у немовлят, таких як післяпологова асфіксія (RDS), інтравентрикулярний крововилив, некротизуючий ентероколіт, сепсис та смерть, у порівнянні з немовлятами, народженими матерями, яким не вводили прогестерон під час вагітності. Ці дані є свідченням зниженого рівня захворюваності і демонструють, що менша кількість дітей захворіває завдяки лікуванню та/або профілактиці вагітних жінок, які мають симптоми короткої шийки матки, прогестероном. Згідно з даним винаходом лікування і профілактика матерів, у яких є симптоми короткої шийки матки, підвищує клінічне здоров'я новонароджених і знижує частоту народжень на 37 тижні вагітності або раніше 37 тижнів вагітності. Втілення данного винаходу свідчать, що застосування прогестерону у пацієнток з короткою шийкою матки спричиняє значне зниження передчасного народження (РТВ) менше ніж за 32 тижні вагітності або на 32 тижні вагітності та/або значне покращення відібраних дитячих результатів. Додатково, втілення винаходу свідчать, що жінки, які мають коротку довжину шийки 5 UA 101474 C2 5 10 15 20 25 30 35 40 45 50 55 60 матки, переважно менше ніж 3,0 см, і більш переважно менше ніж 2,8 см, отримували користь від прогестеронової терапії як РТВ стратегії втручання. Як використано в даному описі, термін "передчасний" загалом описує людську вагітність, що призводить до народження раніше 37 тижнів. Відповідно, "передчасні" охоплює народження, що настають раніше 35 тижнів вагітності або на 32 тижні вагітності. Додатково, інше визначення передчасних пологів включає розкриття та/або стоншення шийки матки, що виявляються пальпацією і пов'язані зі стійкою родовою діяльність раніше 37 тижнів вагітності. В деяких втіленнях, що обговорюються в даному винаході, передчасні пологи визначаються як шість або більше скорочень матки на годину, що супроводжуються задокументованими цервікальними змінами, розкриттям шийки матки на більше ніж 2 см, стоншенням шийки матки більше ніж на 80 % або задокументованою зміною стоншення шийки матки більше ніж на 50 %. Як використано в даному описі, коротка шийка матки означає довжину шийки матки від більше ніж 1,0 до 3,5 см, переважно від більше ніж 1,0 до 3,0 см, більш переважно від більше ніж 1,0 до 2,5 см та ще більш переважно від більше ніж 1,0 до 2,0 см. Шийка матки, що є меншою ніж 1,0 см зазвичай описується як "ультракоротка шийка" і клінічно відрізняється від "короткої шиїки." Спеціалісту, обізнаному в даній галузі, зрозуміло, що для ідентифікації і клінічної діагностики вагітних жінок, які мають коротку шийку матки, можна застосувати такі методи як ультразвукове дослідження і, наприклад, клінічне дослідження. Як використано вданому описі, термін "новонароджений" охоплює дітей віком від приблизно 6 місяців і менше, переважно приблизно віком від 3 місяців і менше, більш переважно віком від приблизно 2 місяців і менше, та ще більш переважно віком від приблизно 1 місяці і менше. В певних втіленнях термін "новонароджений" застосовують, щоб охопити перинатальний період, переважно період після народження. Як використано в даному описі, неонатальний результат (рівнозначно названий в даному описі як "неонатальне здоров'я") вимірюють рівнем, поширеністю та клінічним станом захворюваності та смертності. Наприклад, здоров'я може безпосередньо корелювати з вагою дитини. Здоров'я може бути обернено пов'язане з відсотком госпіталізації до спеціальних лікувальних відділень (тобто, NICU) при народженні, тривалістю стаціонарного перебування при народженні, відсотком RSD, відсотком інтравентрикулярних кровотеч, відсотком некротизуючих ентероколітів, відсотком сепсисів та відсотком неонатальної смерті. Спеціалістами в даній галузі можуть бути застосовані й інші вимірювання захворюванності. Термін "фармацевтично ефективна кількість" (або рівнозначно названа в даному описі як "ефективна кількість") має своє звичайне значення, відоме з рівня техніки, тобто, кількість фармацевтичного агента, яка здатна індукувати in vivo та/або клінічні відповіді, що сприяють контролю, профілактиці або лікувнню. Цей термін може охоплювати як терапевтично, так і профілактично ефективні кількості. Як використано в даному описі, термін "придатний" означає придатне для ссавців, переважно людини, застосування або для фармацевтичних цілей, описаних в даній заявці. Термін "лікування" означає будь-яке лікування захворювання або розладу у ссавця, включаючи: запобігання або захист від хвороби або порушення, тобто, примушуючи клінічні симптоми не розвиватись, пригнічуючи хворобу або порушення, тобто, затримуючи або пригнічуючи розвиток клінічних симптомів; та/або полегшення хвороби або порушення, тобто, викликаючи регрес клінічних симптомів. В деяких втіленнях термін "лікування" включає поліпшення симптомів, лікування або виліковування і запобігання розвитку даної хвороби. Термін "профілактика" задуманий як елемент "лікування", щоб охопити як "запобігання", так і "пригнічення", як визначено в даному описі. Для спеціаліста в даній галузі зрозуміло, що в людській медицині не завжди можна відрізнити "запобігання" від "пригнічення", так як початкова індуктивна подія або події можуть бути невідомими, латентними або пацієнт нез'ясований до тих пір, доки не стануться подія або події. Без зв'язку з будь-якою теорією думають, що усі передчасні народження, жінки, що мають коротку шийку матки, нараховують приблизно 20-30 %. Даний винахід несподівано і неочікувано виявив, що популяція жінок, які страждають від короткої шийки матки, серед жінок, сприйнятливих, схильних або пов'язаних з частотою виникнення передчасного народження, є чутливою до прогестеронового лікування, профілактики та/або інших терапій під час вагітності з метою запобігання або зниження частоти виникнення передчасних народжень. Цікаво, в рівні техніки ведеться багато дебатів з приводу застосування прогестерону для зниження частоти виникнення передчасних народжень. Фігури 5а та 5b в даному описі свідчать, що відсутні відмінності в період вагітності між популяцією вагітних жінок, що отримували лікування прогестероном, і контрольною популяцією, яка отримувала плацебо, коли жінки в обох групах мають середню початкову довжину шийки матки більшу ніж 3,2 см. Фігури 6 та 7 демонструють, 6 UA 101474 C2 5 10 15 20 25 30 35 40 45 50 55 60 що реагування популяції пацієнток з короткою шийкою матки (див. ФІГ. 6) приховані в загальній популяції результатів (див. Фігури 5а та 5b) і що популяція пацієнток з більш довгою шийкою матки (див. Фіг. 7) демонструє відсутність впливу прогестерону подібно до усієї популяції (див. Фігури 5а та 5b). Тобто, вірогідність відсутності пологів раніше строку в цілому є схожою для обох груп. Фактично, статистично результати є настільки прихованими, що попередній рівень техніки є далеким від очікування результатів, яких ми досягли. Проте, дослідження популяції жінок з короткою шийкою матки (наприклад, довжина шийки матки менша ніж або дорівнює 3,0 см, як показано на Фіг. 8) виявило, що жінки, які отримують прогестерон, мають більшу вірогідність для пологів на більш пізньому терміні вагітності ніж жінки, що отримують плацебо. На Фіг. 9 діти, народженні жінками, яким вводили прогестерон, мають більший шанс вижити ніж діти, народженні жінками, що отримували плацебо під час зниження передчасного народження. Дивись Фігури 10, 11 та 12. Подібні результати були отримані для жінок, що мають довжину шийки матки меншу ніж 2,8 см. Прогестерон, ведений згідно з даним винаходом, може бути молекулою прогестерону (з будь-якого джерела, включаючи природний і синтетичний) або метаболітами прогестерону (з будь-якого джерела, включаючи природний і синтетичний), або будь-які інші прогестини. Також може бути застосована будь-яка їх комбінація. В деяких втіленнях термін "природний прогестин" включає прогестерон та/або метаболіти природного прогестерону. Сам прогестерон є переважним, хоче можуть бути застосовані інші прогестини. Коли застосовують синтетичний прогестин, переважно синтетичний прогестерон вибирають з групи, що складається з похідних прогестерону або тестостерону, або похідних інших молекул з прогестогенною активністю. Термін "похідне" означає хімічну сполуку, що може бути утворена або походить з батьківської сполуки і отримана внаслідок однієї або кількох реакцій. Як використано в даному описі термін "прогестин" охоплює природний прогестерон, синтетичний прогестерон, природні або синтетичні похідні прогестерону та/або інші прогестогенні сполуки або їх комбінації. Такі прогестини включають 17-альфа-гідроксипрогестерону капроат, медроксипрогестерону ацетат, норетиндрон, норетиндрону ацетат, норетиндрону енантат, дезогестрел, левоногестрел, лінестренол, етинодіолу діацетат, норгестрел, норгестимат, норетинодрел, гестоден, дроспіренон, тримегестон, леводезогестрел, гестодин, нестерон, етоногестрел і похідні 19-нортестостерону, але не обмежуються ними. В переважному втіленні прогестерон включає як природні прогестини, так і прогестерон або 17-альфа-гідроксипрогестерон. Деякі прогестини можуть вивільнятись вагінально, деякі шляхом внутрішньом'язової ін'єкції, деякі шляхом орального введення, деякі шляхом ректального введення, хоча можуть бути застосовані інші шляхи введення, добре відомі з рівня техніки. В переважному втіленні прогестерон вводять через систему доставки ліків, що містить прогестерон, водорозчинний, водонабрякаючий поперечно зшитий полімер полікарбонової кислоти і принаймні один ад'ювант. В переважному втіленні прогестерон вводять щодня вагінальним шляхом. Проте, введення може бути як рідшим - щотижневим, так і частішим - 4 рази на день, залежно від характеристик прогестину та прогестинової композиції, включаючи концентрацію та шляхи введення. Переважно прогестерон вводять, починаючи з приблизно 18-22 тижня вагітності і аж до приблизно 37 тижня вагітності, або приблизно впродовж 14-19 тижнів, залежно від гестаційного віку на початок лікування та дати пологів. В іншому втіленні прогестерон вводять, починаючи приблизно з 16 тижня вагітності і аж до приблизно 37 тижня вагітності, або приблизно впродовж 21 тижня. Ще в іншому втіленні прогестерон вводять, починаючи приблизно з часу позитивного тесту на вагітність і аж до приблизно 37 тижня вагітності, або починаючи приблизно з 2-4 тижня вагітності і впродовж приблизно 33-35 тижнів. Прогестерон переважно вводять вагітним жінкам, починаючи так рано, як настає вагітність, і тим жінкам, шийка матки яких має довжину, більшу ніж приблизно 1,0 см, або більш переважно, більше ніж 1,5 см. Більш переважно прогестерон вводять вагітним жінкам, починаючи так рано, як настає вагітність, і тим жінкам, шийка матки яких має довжину принаймні приблизно 1,0 см і не більше ніж приблизно 8,0 см, та ще більш переважно, прогестерон вводять вагітним жінкам, шийка матки яких має довжину меншу ніж або дорівнює 3,0 см або меншу ніж або дорівнює 2,5 см в більш переважних втіленнях. Кількість введеного прогестерону переважно знаходиться між приблизно 45 мг і приблизно 800 мг і, більш переважно, між приблизно 90 мг та приблизно 250 мг, базуючись на прогестиновій дії природного прогестерону, введеного вагінально, але ця кількість може бути меншою або більшою, залежно від ефективності прогестину, системи вивільнення та шляху введення. Концентрація прогестерону складає від приблизно 0.01 % до приблизно 50 %, переважно від приблизно 1 % до приблизно 40 %, більш переважно від приблизно 2,5 % до 7 UA 101474 C2 5 10 15 20 25 30 35 40 45 50 55 приблизно 30 %, ще більш переважно від приблизно 5 % до приблизно 20 %, ще більш переважніше від приблизно 6 % до приблизно 15 %. В найбільш переважних втіленнях концентрація прогестерону складає від приблизно 1 % до приблизно 9 %. Для деяких втілень кількість і концентрація прогестерону повинна бути достатньою для того, щоб залишатися у суб'єкта для забезпечення профілактики або лікування, наприклад, впродовж приблизно 1 години або більше, переважно більше ніж приблизно 2 години, ще більш переважно більше ніж 6 годин, ще більш переважно більше ніж приблизно 12 годин, іще більш переважно більше ніж приблизно 24 години та найбільш переважно більше ніж приблизно 36 годин. Для деяких втілень спосіб введення може включати парентеральне введення, шляхом ін'єкції, оральне, місцеве, внутрішньовенне, внутрішньоочеревинне, підшкірне, черезшкірне, внутрішньошкірне, субдермальне, інтраартикулярне, інтравентрикулярне, інтратекальне, внутрішньовагінальне або внутрішньом'язове. Додаткові композиції, що є придатними для інших способів введення, включають супозиторії і, в деяких випадках, водяться трансбукально, сублінгвально, інтраперитоніально, внутрішньовагінально, анально або інтракарніально. В переважних втіленнях спосіб введення є вагінальним. У певних втіленнях прогестерон забезпечений в розчині, такому як олія або інший відповідний носій, що зрозуміло для спеціаліста в даній галузі. Інші способи доставки, такі як олійні капсули і супозиторії, також доступні в певних втіленнях. Для супозиторіїв можуть бути застосовані будь-які звичайні зв'язуюче та/або носій, наприклад, один або більше поліалкенілгліколів або тригліцеридів; такі супозиторії можуть бути зформовані з сумішей, які містять активний інгредієнт в межах переважно від приблизно 0,5 % до приблизно 10 %, більш переважно від приблизно 1 до приблизно 2 %. Оральні композиції можуть містити такі зазвичай використовувані ексципієнти, як наприклад, фармацевтично прийнятний манітол, лактоза, крохмаль, магнію стеарат, натрію цукроза, целюлоза, магнію карбонат і подібні або їх комбінації. Згідно зі втіленням даного винаходу прогестерон вводять стільки разів на день, скільки потрібно для ефективного попередження та/або лікування передчасного народження, тобто, затримки народження і збільшення гестації до переважно більше ніж 37 тижнів або дорінює 37 тижням, в деяких варіантах цих втілень дозування прогестерону складає від 1 до 4 разів на день. Для спеціаліста в даній галузі зрозуміло, що частота введення на добу змінюється в залежності від концентрації і кількості доставленого прогестерону. Наприклад, системи доставки, що містять 90 мг 8 % прогестерону, переважно вводять один раз на день. В інших втіленнях 200 мг прогестерону вводять 2-4 рази на день. Деякі втілення даного винаходу доставляють прогестерон разом з або в композиції, що має біоадгезивний носій, який містить перехресно зшитий полікарбоновий полімер. Деякі варіанти цих втілень включають водонабрякаючий полімер полікарбонової кислоти, що при введенні забезпечує локально направлені у тканину рівні та ефективність терапевтичного агента без шкідливих його рівнів у крові. В переважних втіленнях композиції даного винаходу є корисними для вагінального введення. Наприклад, вагінальний шлях введення може бути вибраний через його потенціал для більшого задоволення пацієнта у порівнянні з внутрішньом'язовим дозуванням та для покращення ефективності через підвищене вивільнення ліків у цільових тканинах. Біоадгезивні композиції згідно з винаходом можуть бути зформовані для забезпечення локального вагінального введення прогестерону з корисними локальними рівнями ліків, уникаючи рівнів, які дають початок небажаним побічним ефектам. Вагінальне введення також уникає проблем пресистемного метаболізму, наприклад, забезпечує ефект першого маткового проходу, і безпосередня доставка у матку дозволяє знизити системні концентрації ліків. В переважних втіленнях прогестерон вводять в біоадгезивній композиції прогестерону для вагінально застосування, яка містить заснований на полікарбофілі гель, що містить 8 % (за вагою) прогестерону, в більш переважних втіленнях прогестерон доставляється як 8 % прогестероновий гель або плацебо, зазвичай доступний як Prochieve® або Replens®, що виробляються Columbia Laboratories, Inc., NJ. В деяких втіленнях прогестерон доставляється в зазделегіть заповненому одноразовому пластиковому аплікаторі, який доставляє дозу 1,125 г гелю, що містить 90 мг прогестерону. Втілення даного винаходу доставляють прогестерон згідно з патентом США № 5,543,150, патентна заявка США № 08/122,371, які включені в даний опис повністю. Способи, розкриті в даному винаході, можуть бути застосовані в сполученні з іншими способами запобігання та/або лікування передчасного народження та/або короткої шийки матки у вагітних жінок, такі як хірургічний серкляж, введення додаткових/доповнюючих композицій, 8 UA 101474 C2 5 10 15 20 25 30 35 40 45 50 55 таких як антибіотики, наприклад, індометацин, і полімерних композицій. Відповідно даний винахід є придатним для комбінованої терапії. Приклади Даний винахід далі проілюстрований наступними прикладами, які наведені з метою продемонструвати винахід і не повинні розглядатись як такі, що обмежують обсяг винаходу і спосіб, в який він може бути застосований на практиці. Хоча результати дослідження показують, що прогестерон може бути ефективно введений вагітним жінкам, що мають початкову довжину шийки матки між приблизно 1.0 см та 8.0 см, для лікування або попередження зменшення довжини шийки матки під час вагітності і, таким чином, лікувати або попереджувати передчасні пологи і передчасне народження, наступні приклади демонструють підвищену ефективність в окремих підгрупах. Приклад Іа. Рандомізований, подвійний сліпий, контрольований плацебо тест на вплив прогестерону на передчасне народження З врахуванням сучасного рівня техніки дослідження проводили з метою перевірити вплив прогестерону на передчасні пологи і передчасне народження у жінок з історією попереднього передчасного народження. Початкові дані дослідження представлені на Фіг. 1. Учасники дослідження включають 611 придатних для оцінювання вагітних жінок, 308 з яких були відібрані у групу, що отримувала лікування, і 302 були відібрані у групу, що отримувала плацебо. Відбір, класифікація і розподіл на дві групи накреслені на схемі на Фіг. 2. Дослідження було проспективним, рандомізованим, контрольованим плацебо, подвійним сліпим, багатоцентровим випробовуванням у вагітних суб'єктів з високим ризиком мимовільних передчасних пологів. Учасники дослідження були відібрані з гестаційним віком з 16 0/7 до 22 6/7 тижнів. Суб'єкти були рандомізовані за ліками та плацебо з 18 0/7 до 22 6/7 тижнів. Суб'єкти, що відповідали критеріям дослідження, були зареєстровані дослідником між 18 0/7 та 22 6/7 тижнями вагітності і отримали ідентично запаковані, послідовно пронумеровані прогестероновий або плацебо вагінальний гель у співвідношенні 1:1. Процедура SAS (SAS Institute Inc., Cary, NC, USA) для блоку перемінного розміру була застосована для створення рандомізаційного переліку, стратифікованого за центром проведення клінічного дослідження та за критеріями включення (попереднє передчасне народження і коротка шийка матки). Quintiles, Inc. (Kansas City, MO, USA) створив рандомізаційні послідовності, які були конфіденційно забезпечені для пакувальної компанії. Розміщення ліків було приховане ідентичним пакуванням і процесом маркуванням, проведеним Aptuit, Inc. (Mount Laurel, NJ, USA). Досліджувані пацієнти, постачальники акушерської допомоги, дослідники, координатори дослідження та спостерігачі не були проінформовані щодо статусу впливу (прогестерон чи плацебо) усіх досліджуваних пацієнтів. Рандомізовані суб'єкти почали лікувння виділеними дослідними ліками і приймали їх щодня аж до 37 тижя гестаційного віку, розвитку передчасного розриву мембран або пологів. Суб'єкти були рандомізовані у співвідношенні 1:1 для одержання 8 % PROCHIEVE® (вагінально вводили 90 мг гелю природного прогестерону) або плацебо вагінального гелю. Усі жінки здійснювали самодозування щоденної базової дози призначених їм досліджуваних ліків - як PROCHIEVE® (прогестерон), так і плацебо. Приклад Іb. Стеження за рандомізованим, подвійним сліпим, контрольованим плацебо тестом на вплив прогестерону на передчасне народження Дані, представлені в цьому Прикладі, далі досліджують дані, репрезентовані в Прикладі Іа. Метою цього випробовування було визначити, чи профілактичне введення вагінального прогестерону знижує ризик передчасного народження у жінок з мимовільним передчасним народженням у минулому. Це дослідження було рандомізованим, подвійним сліпим, контрольованим плацебо, багатонаціональним випробуванням 659 вагітних жінок з мимовільним передчасним народженням у минулому, зареєстрованих і рандомізованих. Між 18 0/7 та 22 6/7 тижнями вагітності пацієнти були випадковим чином призначені на лікування або 8 % прогестероновим вагінальним гелем, або плацебо аж до настання пологів, 37 тижнів вагітності або розвитку передчасного розриву мембран (PROM). Основним результатом було передчасне народження через < 32 тижнів вагітності. Статистичний аналіз базувався на принципі наміру до лікування. Вагітні жінки були придатними для включення до випробовування, якщо їх вік складав від 18 до 45 років з встановленим гестаційним віком між 16 0/7 та 22 6/7 тижнями і мали в минулому мимовільне, синглетне передчасне народження між 20 0/7 та 35 0/7 тижнями вагітності, підтверджене записом в медичній документації щодо кваліфікованого передчасного народження. Також було необхідним, щоб пацієнти розуміли англійську мову або спільну 9 UA 101474 C2 5 10 15 20 25 30 35 40 45 50 55 місцеву мову, добровільно підписали форму про інформовану згоду, демонстрували розуміння мети дослідження і згоду дотримуватися протоколу вивчення. Пацієнти виключались з випробовування, якщо вони мали в минулому несприятливу реакцію на прогестерон або будь-який компонент, присутній у ліках, отримували лікування прогестероном протягом 4 тижнів, передуючих реєстрації, або були проліковані щодо епілептичного нападу, психіатричного порушення або хронічної гіпертензії при реєстрації. Пацієнти також виключались з випробовування, якщо вони мали у минулому гостру або хронічну застійну серцеву недостатність, ниркову недостатність або неконтрольований 3 цукровий діабет; активне печінкове порушення; ВІЛ-інфекцію з кількістю CD4 < 350 клітин/мм і потребують поліпротивірусних агентів; передлежачу плаценту або низько лежачу плаценту, що вимагає вагінальної профілактики; в минулому мали або підозрювались на наявність злоякісних пухлин молочної залози або статевих шляхів; в минулому мали або підозрювались на наявність тромбоемболічної хвороби або мюллерівської аномалії. Пацієнти, які на той час або раніше були зареєстровані в іншому дослідженні за один місяць до відбору у дане вивчення, не були включені до випробовування. Пацієнти були також обмежені від участі у випробуванні, якщо справжня вагітність була ускладнена основною ембріональною аномалією або відомим порушенням хромосоми, або була багатоембріональною вагітністю. Пацієнти з цервікальним серкляжем або ті, що мають намір розмістити один протягом поточної вагітності, були виключені з участі у випробовуванні як такі, що мають ознаки передчасного розриву мембран, вагінальної кровотечі, амніоніту або передчасних пологів при реєстрації. Нарешті, пацієнти, які не могли або були несхильні підкорятися процедурам випробовування, або мали кваліфіковане передчасне народження, яке сталося без передчасних пологів, не увійшли до випробування. Ліки для випробовування були запаковані і промарковані згідно зі схемою рандомізації 1:1, забезпеченою Quintiles, Inc (Kansas City, MO, USA). A SAS (SAS Institute Inc., Cary, NC, USA), процедура для блоку перемінного розміру була застосована для створення рандомізаційного переліку, стратифікованого за центром проведення клінічного дослідження. Тридцять три з 53 центрів укомплектували принаймні 1 рандомізаційний блок, розрахований на 92 % зареєстрованих пацієнтів. Досліджувані ліки (8 % прогестероновий гель Prochieve®) і пласебо (Replens®) були надані Columbia Laboratories, Inc. (Livingston, NJ, USA). Пацієнти були проінструктовані щодо самостійного введення заповненого вагінальним гелем аплікатора приблизно в той самий період доби, переважно вранці. Пацієнти одержали 2-тижневий набір для розприділеного під час рандомізації лікування та з того часу кожні 2 тижні дослідження відвідували відповідний центр. Всі упаковки ліків досталялись у всі дослідні центри при кожному візиті і дотримання дослідного лікування визначали за поверненими пустими упаковками та невикористаними упаковками. Відсоток дотримання оцінювали як загальну тривалість дотримання лікування: (загальна кількість використаних аплікаторів/загальна кількість добових дозувань) х 100. Загальну кількість добових дозувань визначали як інтервал від дати реєстрації до або дати передчасного розриву мембран, або дати передчасного народження без супроводжуючих розривів мембран, або 37 0/7 тижневої вагітності. Опитування щодо наявності несприятливих подій здійснювали при кожному двотижневому візиті у всіх дослідницьких центрах, запитуючи, чи мав пацієнт будь-які ускладнення або проблеми. Пацієнти отримували додатковий однотижневий набір ліків у випадку, коли лікування ініціювали через те, що вони не могли зробити наступне регулярне заплановане призначення. Досліджувані ліки являли собою біоадгезивну композицію прогестерону для вагінального застосування, що містить заснований на полікарбофілі гель, який містить 8 % (за вагою) прогестерону. Попередньо заповнений одноразовий пластиковий аплікатор доставляє 1,125 г гелю, який містить 90 мг прогестерону. Плацебо являє собою Replens - біоадгезивну систему доставки без прогестерону. Суб'єкти із задокументованим в минулому мимовільним передчасним народженням були відібрані в період між 16 0/7 та 22 6/7 тижнями вагітності дослідником або координатором випробовування. Гестаційний вік базувався на минулому менструальному періоді пацієнтки та корелював з ультразвуковим біометричним алгоритмом. Кожна пацієнтка мала принаймні одне ультразвукове дослідження перед рандомізацією для підтвердження гестаційного віку та виключення основних ембріональних аномалій і трансвагінальне сканування для визначення довжини шийки матки. Після рандомізації щоденне лікування ініціювалось пацієнткою і продовжувалось аж до 37 0/7 тижневого гестаційного віку, настання передчасного розриву мембран або передчасних пологів. Кожна пацієнтка оцінювалась з двотижневим інтервалом. Через 28 тижнів вагітності у всіх суб'єктів визначали довжину шийки матки за допомогою трансвагінального ультразвукового дослідження. 10 UA 101474 C2 5 10 15 20 25 30 35 40 45 50 55 60 Основні характеристики були схожими в обох групах дослідного лікування. Прогестерон не знижував частоту передчасного народження < 32 тижнів. Не було ніяких відмінностей у середньому гестаційному віці при пологах, дитячій захворюваності чи смертності або інших материнських чи неонатальних показниках. Поява несприятливих подій при лікуванні була схожою в обох групах. Виходячи з цих результатів, профілактичне лікування вагінальним прогестероновим гелем ефективно не знижувало частоту рекурентних передчасних народжень у жінок з високим ризиком, вибраних через мимовільні передчасні пологи в минулому. Необхідно вивчити інші методи оцінки ризиків. Визначення точної кількості пацієнтів, початково відібраних у всіх 53 дослідницькихцентрах, включаючи направлення фахівцями до цих центрів, не було реально продуманим. Оцінка 1500 початково відібраних суб'єктів була отримана шляхом запиту до дослідницьких центрів. В цілому 711 жінок було визначено як формально відібрані (отримана інформована згода, але не рандомізовані) та 42 жінки були в подальшому виключенні. Найбільш загальними причинами для виключення з випробовування були плановий серкляж, смертельний стан, відмова документувати попереднє мимовільне передчасне народження в кваліфікаціному гестаційному віці. Сумарно 669 пацієнток були реально придатними для реєстрації у дослідження, з 659 рандомізованих у лікувальні групи жінок лише для однієї була визначена історія материнства (Фіг. 2). П'ять пацієнток, зареєстрованих в планову підгрупу для дослідження з приводу короткої шийки матки, і одна кваліфікаційна пацієнтка, що випала з наступного лікарського контролю ще перед рандомізацією, були виключені з аналізу. Пацієнти, які отримали принаймні одну дозу досліджуваних ліків і передбачену дату пологів, були включені до популяції наміру до лікування (ІТТ). Пацієнтки без дати пологів обґрунтовано випали з наступного лікарського контролю. Популяція ІТТ пацієнток, що мали попередні передчасні пологи, налічувала 309 пацієнток в прогестероновій групі і 302 пацієнтки у групі плацебо. Рандомізація забезпечила лікувальні групи, які задовольняли щодо віку, етнічної приналежності та індексу маси тіла (ВМІ). Дані про наявність пологів в анамнезі, кількість попередніх передчасних народжень та мимовільні аборти були схожими. Середній гестаційний вік (± SD) при рандомізації складав 19,9 (± 2,1) і 20,1 (± 3,3) тижнів для прогестеронових і плацебо груп відповідно. Щодо історій попередніх вагітностей, то 76,4 % прогестеронових пацієнток та 74,5 % плацебо пацієнток в минулому мали одне мимовільне передчасне народження і 23,6 % та 25,5 % пацієнток в кожній групі зазнало по два і більше передчасних пологів в минулому відповідно. Рівень передчасних народжень < 32 0/7 тижні вагітності, попередній результат, суттєво не відрізнявся; 10,0 % (n = 31) в прогестероновій групі та 11,3 % (n = 34) в плацебо групі. Аналіз попередніх результатів відносно країни/регіону не продемонстрував ніяких значних відмінностей між країною або регіоном. Серередній гестаційний вік при пологах складав 36,6 тижнів як в прогестероновій, так і в плацебо групах. Рівні підатливості досліджуваним лікам також були схожими: 96,2 % для жінок в прогестероновій групі та 96,4 % для жінок в плацебо групі. Інші результати дослідження також не відрізнялись між прогестероновою і плацебо групами. Рівень передчасних пологів склав 41,7 % (n = 129) проти 40,7 % (n = 123) відповідно через < 37 0/7 тижнів вагітності; 22,7 % (n = 70) проти 26,5 % (n = 80) відповідно через < 35 0/7 тижнів вагітності; і 3,2 % (n = 10) проти 3,0 % (n = 9) відповідно через < 28 0/7 тижнів вагітності. Криві виживаності на час пологів показані на Фігурі 5а. Госпіталізація з приводу передчасних пологів (25,6 % для прогестерону проти 24,8 % для плацебо), введення засобів, що знижують родову діяльність, та застосування дородової кортикостероїдної терапії були схожими для обох груп. У пацієнток, госпіталізованих для лікування передчасних пологів, кількість днів перебування у лікарні до пологів склала 30 днів для прогестерону і 19,6 днів для плацебо (95 % СІ, -23-2.3). Крім того, відсутні відмінності в рівні передчасних розривів мембран (12,0 % проти 12,6 %) або мертвонароджуваності/внутрішньоутробної загибелі плоду (1,6 % проти 1,3 %) в прогестероновій та плацебо групах відповідно. Середня маса тіла немовлят при народженні в прогестероновій і плацебо групах була схожою (2680±710 прти 2661±738 г відповідно), так само як і окружність голови (32,3±3,34 проти 32,5±3,75 см відповідно). Були відсутні відмінності у групах, що одержували лікування прогестероном та плацебо, щодо 1-хвилинного (середній показник = 8 для кожної групи) та 5хвилинного (середній показник = 9 для кожної групи) показників APGAR або рівня госпіталізації до дитячого відділення інтенсивної терапії (17,5 % проти 21,5 %). Випадки діопатичного респіраторного дистрес-синдрому новонароджених (11,0 % проти 11,9 %), 3 або 4 рівня крововиливу у шлуночки головного мозку (0,3 % проти 0,3 %) та некротизаційного ентероколіту (1.0 % vs. 1.7 %) були також схожими в прогестероновій та плацебо групах. Аномалії розвитку, потенційно набуті на другому чи третьому триместрах вагітності, спостерігались у 2 11 UA 101474 C2 5 10 15 20 25 30 35 40 45 50 55 60 новонароджених: по 1 випадку неповного вивиху тазостегнового суглоба в кожній групі. Аномалії в процесі розвитку, що мали місце в першому триместрі органогенезу, такі як гіпоспадія, додаткові пальці та тетрада Фалло, не були включені. Дані лікарського контролю дітей віком 6, 12 та 24 місяці продовжують збиратись та не були доступними на час повідомлення цих результатів. Приклад 2. Рандомізоване випробовування, яке досліджує ефективність вагінального прогестерону щодо запобігання раннього передчасного народження у жінок з укороченою шийкою матки у другому триместрі вагітності. Дослідження надалі включало жінок без передчасних пологів у минулому і які мали коротку шийку матки на час реєстрації. Хоча популяція з короткою шийкою матки включала тільки 9 пацієнток, результати наводять на думку про можливий ефект прогестерону з огляду на 40 % (2/5) пологів раніше 32 тижнів вагітності в групі плацебо і 0 (0/4) пологів раніше 32 тижнів вагітності в прогестероновій групі. Оскільки деякі учасниці з історією передчасних пологів в минулому також мали коротку шийку матки, то популяцію для вивчення передчасних пологів поділили на квартилі, базуючись на довжині шийки матки. Найнижча квартиль (< 3,2 см) була згрупована тільки з пацієнток з короткою шийкою матки і послідовно поділена та аналізувались первинні і вторинні результати для жінок з довжиною шийки матки < 3,0 см та < 2,8 см на час реєстрації. Була недостатня кількість пацієнток з ще коротшими шийками матки, доступними для подальшого аналізу. Для цілей вивчення як критерій короткої шийки матки була встановлена довжина менша ніж 2,8 см. В цілому 46 учасниць підпало під цю категорію і їх демографічні дані і характеристики представлені на Фіг. 3. Загалом, довжина шийки матки менша ніж 2,8 см була ідентифікована у 46 рандомізованих жінок: 19 з 313, які отримували прогестерон, і 27 з 307, які отримували плацебо. Базові характеристики обох груп були схожими. Рівень передчасних пологів раніше 32 тижнів вагітності був значно нижчим для прогестерону ніж для плацебо (0 % проти 29,6 %, Р = 0.014). З прогестероном було менше госпіталізацій до відділення дитячої інтенсивної терапії (15,8 % проти 51,9 %, Р = 0.016) та коротше перебування у відділенні дитячої інтенсивної терапії (1,1 проти 16,5 днів, Р = 0,013). Спостерігалась також тенденція до зниженого рівня неонатального респіраторного дистрес-синдрому (5,3 % проти 29,6 %, Р = 0,060). Було встановлено, що вагінальний прогестероновий гель знижував рівень ранніх передчасних народжень і покращував неонатальні результати у жінок з укороченням шийки матки на другому триместрі вагітності. Дослідження включало жінок з задокументованим мимовільним передчасним народженням в минулому (< 35 тижнів) при одноембріональній вагітності в безпосередньо передуючих родах в анамнезі, незважаючи на довжину шийки матки, і жінок без передчасних народжень в минулому але з укороченням довжини шийки матки (< 2,5 см) на другому триместрі вагітності в поточній вагітності, яким було запропоновано зареєструватись до дослідження на 18 0/7-22 6/7 тижнях вагітності. Набір почався в квітні 2004 і остання пацієнтка народила 8 січня 2007. Жінки були виключені з дослідження, якщо вони мали стан або ускладнення вагітності перед відбором, що збільшував ризик несприятливого результату для матері або плоду, суттєво збільшував ризик медично показаних (немимовільних) передчасних пологів або можливий результат за відсутності підатливості або при ранньому припиненні дослідження. Відповідно, жінки були виключенні з дослідження, якщо була присутня будь-яка з наступних умов: вік 45 років; багатоембріональна вагітність; несприятлива реакція в минулому на прогестерон або будь-який компонент, присутній в ліках; лікування прогестероном протягом 4 тижнів, що передували реєстрації або поточне лікування епілептичних нападів, психіатричних розладів або хронічної гіпертензії. Пацієнти також виключались з випробовування, якщо вони мали у минулому гостру або хронічну застійну серцеву недостатність, ниркову недостатність або неконтрольований цукровий діабет; активне печінкове порушення; ВІЛ-інфекцію з кількістю CD4 3 < 350 клітин/мм і потребують поліпротивірусних агентів; передлежачу плаценту або низько лежачу плаценту, що вимагає вагінальної профілактики; в минулому мали або підозрювались на наявність злоякісних пухлин молочної залози або статевих шляхів; в минулому мали або підозрювались на наявність тромбоемболічної хвороби або мюллерівської аномалії. Пацієнти, які на той час або раніше були зареєстровані в іншому дослідженні за один місяць до відбору у дане вивчення, не були включені до випробовування. Пацієнти були також обмежені від участі у випробуванні, якщо справжня вагітність була ускладнена основною ембріональною аномалією або відомим порушенням хромосоми, або була багатоембріональною вагітністю. Пацієнти з цервікальним серкляжем або ті, що мають намір розмістити один протягом поточної вагітності, були виключені з участі у випробовуванні як такі, що мають ознаки передчасного розриву мембран, вагінальної кровотечі, амніоніту або передчасних пологів при реєстрації. 12 UA 101474 C2 5 10 15 20 25 30 35 40 45 50 55 60 Жінки із мимовільним передчасним народженням в минулому у передуючій вагітності, незважаючи на довжину шийки матки, і жінки без передчасних народжень в минулому але з укороченням довжини шийки матки на другому триместрі вагітності в поточній вагітності, були відібрані дослідником або координатором дослідження між 16 0/7 та 22 6/7 тижнями вагітності. Попередня історія мимовільних передчасних пологів була підтверджена оцінкою медичних записів пацієнта перед реєстрацією. Гестаціний вік базувався на минулому менструальному циклі пацієнток і корелював з ультразвуковим біометричним алгоритмом. Кожна пацієнтка мала принаймні одне ультразвукове дослідження перед рандомізацією для підтвердження гестаційного віку та виключення основних ембріональних аномалій і трансвагінальне сканування для визначення довжини шийки матки. Суб'єкти, що відповідали критеріям дослідження, були зареєстровані дослідником між 18 0/7 та 22 6/7 тижнями вагітності і отримали ідентично запаковані, послідовно пронумеровані прогестероновий або плацебо вагінальний гель у співвідношенні 1:1. Процедура SAS (SAS Institute Inc., Cary, NC, USA) для блоку перемінного розміру була застосована для створення рандомізаційного переліку, стратифікованого за центром проведення клінічного дослідження та за критеріями включення (попереднє передчасне народження і коротка шийка матки). Quintiles, Inc. (Kansas City, MO, USA) створив рандомізаційні послідовності, які були конфіденційно забезпечені для пакувальної компанії. Розміщення ліків було приховане ідентичним пакуванням і процесом маркуванням, проведеним Aptuit, Inc. (Mount Laurel, NJ, USA). Досліджувані пацієнти, постачальники акушерської допомоги, дослідники, координатори дослідження та спостерігачі не були проінформовані щодо статусу впливу (прогестерон чи плацебо) усіх досліджуваних пацієнтів. Після рандомізації щоденне лікування ініціювалось пацієнткою і продовжувалось аж до 37 0/7 тижневого гестаційного віку, настання передчасного розриву мембран або передчасних пологів. Кожна пацієнтка оцінювалась з двотижневим інтервалом. Через 28 тижнів вагітності у всіх суб'єктів визначали довжину шийки матки за допомогою трансвагінального ультразвукового дослідження. Перед початком дослідження були взяті базові виміри довжини шийки матки кожної учасниці і підсумовані на Фіг 1. Протягом дослідження за допомогою ультразвуку здійснювали вимірювання довжини шийки матки, як базової, так і через 28 тижнів вагітності після 6-10тижневого періоду дозування. Середня довжина шийки матки 3,7 см була такою як в групі, що отримувала лікування, так і в групі, що отримувала плацебо, рівень довжини шийки матки для всіх учасниць був між 1,1 см та 7,9 см. Через 28 тижнів вагітності довжину шийки матки кожної учасниці переміряли і дані порівняли з базовими даними і був виявлений неочікуваний і несподіваний результат. Як показано на Фіг. 4, середнє зниження довжини шийки матки після 28 тижнів у пацієнток, що отримували плацебо, склало 0,61 см, в той час як середнє зниження довжини шийки матки за той самий період часу у пацієнток в групі, яка отримувала лікування (тобто, була на прогестероновому режимі), склало тільки 0,44 см. Оскільки р-значення для усього випробовування було 0,038, то результати вказують на те, що має місце статистично значиме зниження кількості укорочення або стоншення шийки матки у жінок на прогестереновому режимі у порівнянні з жінками, що отримували плацебо. Результати дослідження змальовані з використанням кривих Каплан-Мейєра, як показано на Фігурах 5b-10, досліджуючи кінцеву точку передчасних пологів у вивченні. Фіг. 5b являє собою криву часу до пологів для усіх рандомізованих пацієнток. Хоча криві для кожної групи на Фіг. 5b здаються такими, що мають істотне перекриття, коли результати розбиті внизу додатково для аналізу довжини шийки матки пацієнток на базисі, різниця в результаті між групами лікування і плацебо явно видима. Для пацієнток, що мають базову довжину шийки матки меншу ніж або дорівнює 3,2 см, (Фіг. 6), меншу ніж або дорівнює 3,0 см (Фіг. 8 та 9), та меншу ніж 2,8 см (Фіг. 10), учасниці в групі, що отримувала лікування, ясно демонструють вірогідність ненастання пологів за довший період вагітності у порівнянні з учасницями групи, яка отримувала плацебо. Як показано на Фіг. 7, відсутня суттєва різниця в результаті між групами, що отримували лікування і плацебо, у пацієнток, що мали базову довжину шийки матки більшу ніж 3,2 см напочатку. Посилаючись на Фіг. 10, яка демонструє вірогідність пацієнток з базовою довжиною шийки матки меншою ніж 2.8 см залишатись нерозродженою, група учасників, що мають довжину шийки матки меншу ніж 2,8 см зазнала значне зниження частоти передчасних пологів. Як показано на. 10, серед 46 суб'єктів (19 пролікованих прогестероном, наприклад, прогестероном Prochieve®, і 27 плацебо) частота передчасних пологів в групі, що отримувала лікування, була 0 %, проти 29,6 % в плацебо групі (Р = 0.014). Для цілей цього дослідження, параметр передчасних пологів був встановлений менше ніж або дорівнює 32 тижням. Фіг. 11 включає більш детальний розподіл пологів при різних точках гестації для прогестеронової і плацебо груп, 13 UA 101474 C2 5 10 15 20 25 30 зокрема для менше ніж або дорівнює 37, 35, 32 та 28 тижням. Результат був помітно кращим для групи, що отримувала лікування, ніж для групи плацебо в кожній точці часу. Особливо, для менше ніж або дорівнює 37 тижнів та менше ніж 35 тижнів лікування знизило кількість передчасних пологів приблизно наполовину, для менше ніж або дорівнює 32 тижні та менше ніж або дорівнює 28 тижнів були відсутні передчасні пологи в групі, що отримувала лікування, хоча в групі плацебо було 8 та З передчасних пологів відповідно. Результати досліджень також виявили покращений результат для немовлят, народжених учасницями в прогестероновій групі, що продемонстровано на Фіг. 12, коли застосована до жінок з довжиною шийки матки < 2,8 см прогестеронова терапія знизила кількість госпіталізацій до NICU (15,8 % проти 51.9 %, Р = 0,016) та знизила перебування в NICU (1,1 проти 16,5 днів, Р = 0.013). Спостерігалась тенденція скорочення в цілому неонатальних госпіталізаційних днів (5,8 проти 18,2 днів, Р - 0,055) і скорочення випадків неонатального респіраторного дистрессиндрому (5,3 % проти 29,6 %, Р = 0,060) у випадку прогестеронової терапії. В підгрупі жінок, зареєстрованих з довжиною шийки матки < 2,8 см, сталися 2 смерті плоду/новонародженого в плацебо групі ([1] срок розродження, помер у віці 11 тижнів, SIDS; [2] 35 тижнів вагітності, аспіраційна пневмонія), а в групі, що отримувала вагінальний прогестерон, смертей не було. Ґрунтуючись на результатах цього дослідження, очевидно, що введення прогестерону вагітним жінкам ефективно знижує кількість укорочень або стоншень їх шийок матки, більш помітно у жінок з короткою шийкою матки. Приклад 3. Популяції, що мають базову довжину шийки матки < 2,8 см Дані підгрупи учасниць, що мали базову довжину шийки матки меншу ніж або дорівнює 2,8 см, надані в Таблиці 1 нижче. Результати показують, що 8 з 27 учасниць, які отримували режим плацебо, мали пологи раніше 32 тижнів, в той час як жодна з 19 учасниць, які отримували прогестероновий режим, не мала пологів раніше 32 тижнів. Як визначено за двостороннім р-значенням 0,014 і 95 % СІ -0,469,-0,124, результати вказують на статистично істотний ефект в зниженні народжень раніше 32 тижнів через введення прогестерону у порівнянні з плацебо серед популяції вагітних жінок, що мали базову довжину шийки матки < 2,8 см. Див. також Фігури 12 та 14а-е, які надають порівняння між лікуваннями немовлят, народжених пацієнтками, що отримували плацебо, і немовлят, народжених пацієнтками, що отримували прогестерон Prochieve®. Таблиця 1 19 19 Народження 32 тижнів Плацебо група Лікувальна група кількість кількість Загальна кількість Точний критерій 0,014 Фішера р-значення 95 % СІ -0,469,-0,124 35 40 Приклад 4. Популяція, що мала базову довжину шийки матки < 3,0 см Дані підгрупи учасниць, що мали базову довжину шийки матки меншу ніж або дорівнює 3,0 см, надані в Таблиці 2 нижче. Результати показали, що 11 з 58 учасниць, які отримували режим плацебо, мали пологи на 32 тижні вагітності або раніше, в той час як тільки 5 з 58 учасниць, які отримували прогестероновий режим, мали пологи на 32 тижні або раніше. Ці результати є суттєвими з огляду на 95 % СІ і двостороннє р-значення вказує на тенденцію зменшення пологів раніше 32 тижнів вагітності через застосування прогестерону у порівнянні з плацебо серед популяції вагітних жінок, що мали базову довжину шийки матки < 3,0 см. Див. також Фігури 3а-е, які надають порівняння між лікуваннями немовлят, народжених пацієнтками, що отримували плацебо, і немовлят, народжених пацієнтками, що отримували прогестерон Prochieve®. 45 14 UA 101474 C2 Таблиця 2 47 54 Народження 32 тижнів Плацебо група Лікувальна група кількість кількість Загальна кількість Точний критерій 0,094 Фішера р-значення 95 % СІ -0,214,-0,001 5 10 Термін "приблизно, " як використано в даному описі, потрібно розуміти як такий, що стосується як певної кількості, так і діапазону кількостей. Окрім того, усі діапазони числових значень в даному описі потрібно розуміти як такі, що включають кожне повне число в межах діапазону. Хоча в даному описі розкриті ілюстративні втілення винаходу, спеціаліст в даній галузі зможе розробити численні модифікації і інші його втілення. Особливості втілень, описаних в даній заявці, можуть комбінуватися, відбиратись, змінюватись та/або реорганізовуватись для генерування інших втілень. Відповідно, зрозуміло, що прикладена формула призначена охопити усі такі модифікації та втілення, що перебувають в межах сутності і духу даного винаходу. ФОРМУЛА ВИНАХОДУ 15 20 25 30 35 40 45 1. Застосування прогестерону для виробництва лікарського засобу для мінімізації укорочення шийки матки у вагітних жінок з короткою шийкою матки від 1,0 см до 3,5 см, щоб таким чином лікувати чи попереджати настання передчасних пологів та наступного передчасного народження. 2. Застосування за п. 1, яке відрізняється тим, що лікарський засіб являє собою вагінальний гель, вагінальний супозиторій, вагінальний крем або вагінальну тверду дозовану форму. 3. Застосування за п. 1, яке відрізняється тим, що лікарський засіб сформований для введення внутрішньом'язовим, оральним, ректальним, підшкірним, вагінальним, інтрадермальним, місцевим, інтраназальним, інтраперітонеальним, внутрішньосуглобовим, внутрішньошлуночковим, інтратекальним, внутрішньовагінальним або внутрішньовенним шляхом. 4. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що прогестерон містить природний прогестерон або метаболіт прогестерону. 5. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що прогестерон містить синтетичний прогестерон, вибраний з 17-альфа-гідроксипрогестерону капроату, медроксипрогестерону ацетату, норетиндрону, норетиндрону ацетату, норетиндрону енантату, дезогестрелу, левоногестрелу, лінестренолу, етинодіолу діацетату, норгестрелу, норгестимату, норетинодрелу, гестодену, дроспіренону, тримегестону, леводезогестрелу, гестодину, нестерону, етоногестрелу і похідних 19-нортестостерону. 6. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що лікарський засіб призначений для щоденного введення. 7. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що лікарський засіб призначений для введення з приблизно 18-22 тижня вагітності аж до приблизно 37 тижня вагітності. 8. Застосування за п. 6, яке відрізняється тим, що лікарський засіб призначений для введення протягом від приблизно 14 до приблизно 19 тижнів. 9. Застосування за п. 6, яке відрізняється тим, що лікарський засіб призначений для введення з приблизно 16 тижня вагітності аж до приблизно 37 тижня вагітності. 10. Застосування за п. 6, яке відрізняється тим, що лікарський засіб призначений для введення протягом приблизно 21 тижня. 11. Застосування за п. 6, яке відрізняється тим, що лікарський засіб призначений для введення з моменту позитивного тесту на вагітність аж до приблизно 37 тижня вагітності. 12. Застосування за п. 6, яке відрізняється тим, що лікарський засіб призначений для введення з приблизно 2-го по 4-й тиждень вагітності. 15 UA 101474 C2 5 10 15 20 25 30 13. Застосування за п. 6, яке відрізняється тим, що лікарський засіб призначений для введення протягом приблизно 33-35 тижнів. 14. Застосування за п. 6, яке відрізняється тим, що лікарський засіб призначений для введення залежно від гестаційного віку на початку лікування і на дату пологів. 15. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що лікарський засіб сформований для доставки дози прогестерону від приблизно 45 мг до приблизно 800 мг. 16. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що лікарський засіб знаходиться в формі або міститься в системі доставки ліків, що містить прогестерон, водорозчинний, водонабрякаючий перехресно зшитий полімер полікарбонової кислоти та принаймні один ад'ювант. 17. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що шийка матки вагітної жінки має довжину від 1,0 см до 3,0 см. 18. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що прогестерон містить природний прогестерон і 17-альфа-гідроксипрогестерон. 19. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що лікарський засіб сформований для доставки дози прогестерону приблизно 90 мг, і тим, що прогестерон є природним прогестероном. 20. Застосування за будь-яким із попередніх пунктів, щоб таким чином знизити дитячу захворюваність та смертність у недоношеного новонародженого, що очікується або пізніше народиться від вагітної жінки з короткою шийкою матки. 21. Застосування за будь-яким із попередніх пунктів, яке відрізняється тим, що лікарський засіб призначений для введення в комбінації з однією або більше сполуками для лікування або профілактики передчасного народження. 22. Застосування за будь-яким із пп. 1-20, яке відрізняється тим, що лікарський засіб призначений для введення в комбінації з клінічною процедурою для лікування або профілактики передчасного народження. 23. Застосування за будь-яким з попередніх пунктів, яке відрізняється тим, що лікарський засіб вводиться у пристрої для вивільнення ліків, що має конфігурацію для введення у вагіну. 24. Застосування за п. 23, яке відрізняється тим, що пристрій являє собою або містить цервікальне кільце. 16 UA 101474 C2 17 UA 101474 C2 18 UA 101474 C2 19 UA 101474 C2 20 UA 101474 C2 21 UA 101474 C2 22 UA 101474 C2 23 UA 101474 C2 24 UA 101474 C2 25 UA 101474 C2 26 UA 101474 C2 27 UA 101474 C2 28
ДивитисяДодаткова інформація
Назва патенту англійськоюUse of a progesterone in the manufacture of a medicament
Автори англійськоюCreasy, George
Назва патенту російськоюПрименение прогестерона для производства лекарственного средства
Автори російськоюКризи Джордж
МПК / Мітки
МПК: A61K 45/06, A61P 15/06, A61K 31/57
Мітки: засобу, застосування, виробництва, лікарського, прогестерону
Код посилання
<a href="https://ua.patents.su/35-101474-zastosuvannya-progesteronu-dlya-virobnictva-likarskogo-zasobu.html" target="_blank" rel="follow" title="База патентів України">Застосування прогестерону для виробництва лікарського засобу</a>
Попередній патент: Конструкція і спосіб встановлення керованого моста у транспортне положення та сільськогосподарська робоча машина, яка містить зазначений керований міст
Наступний патент: Спосіб одержання сірчаної кислоти та установка для його здійснення
Випадковий патент: Привідний газотурбінний двигун гтд-10в для газоперекачувальних агрегатів