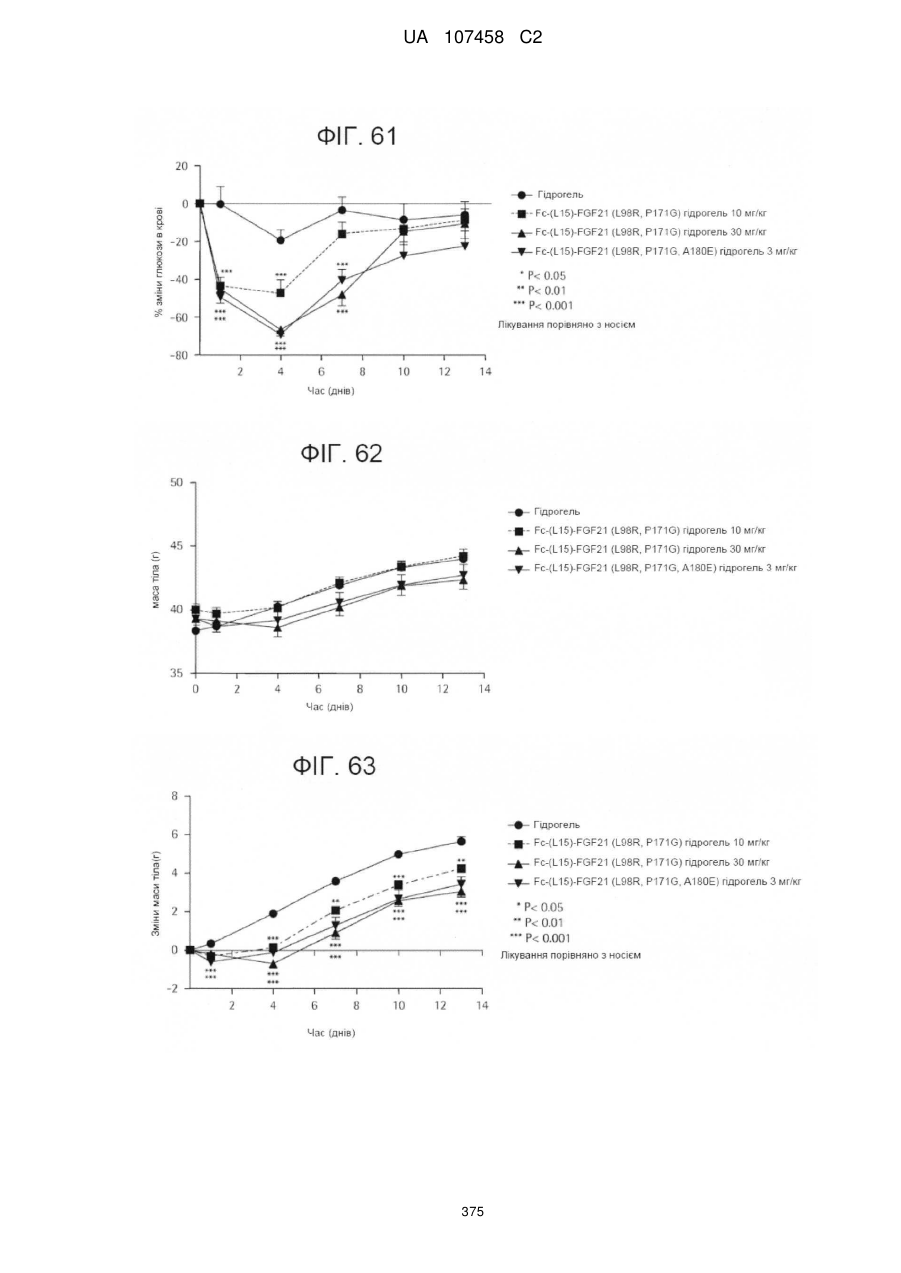
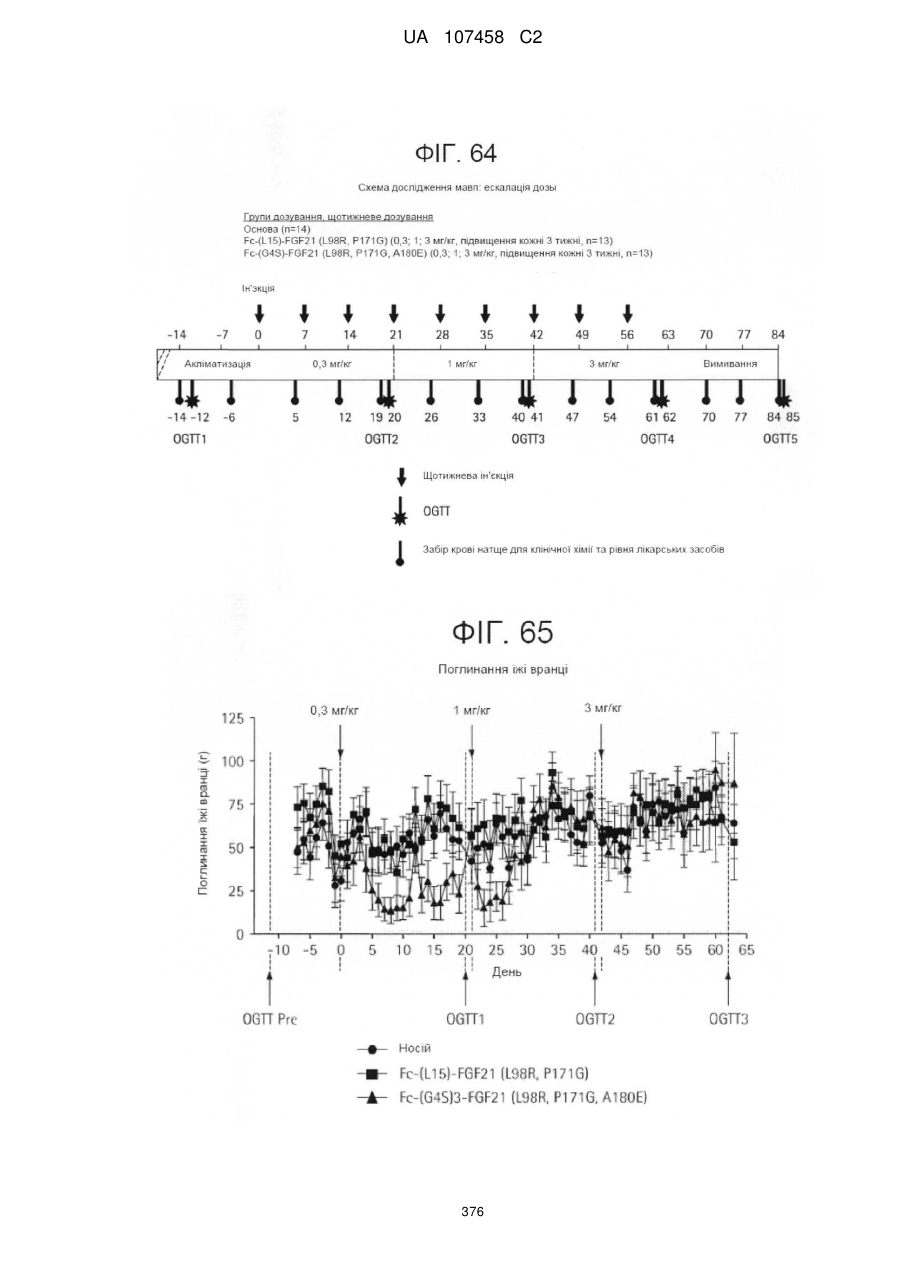
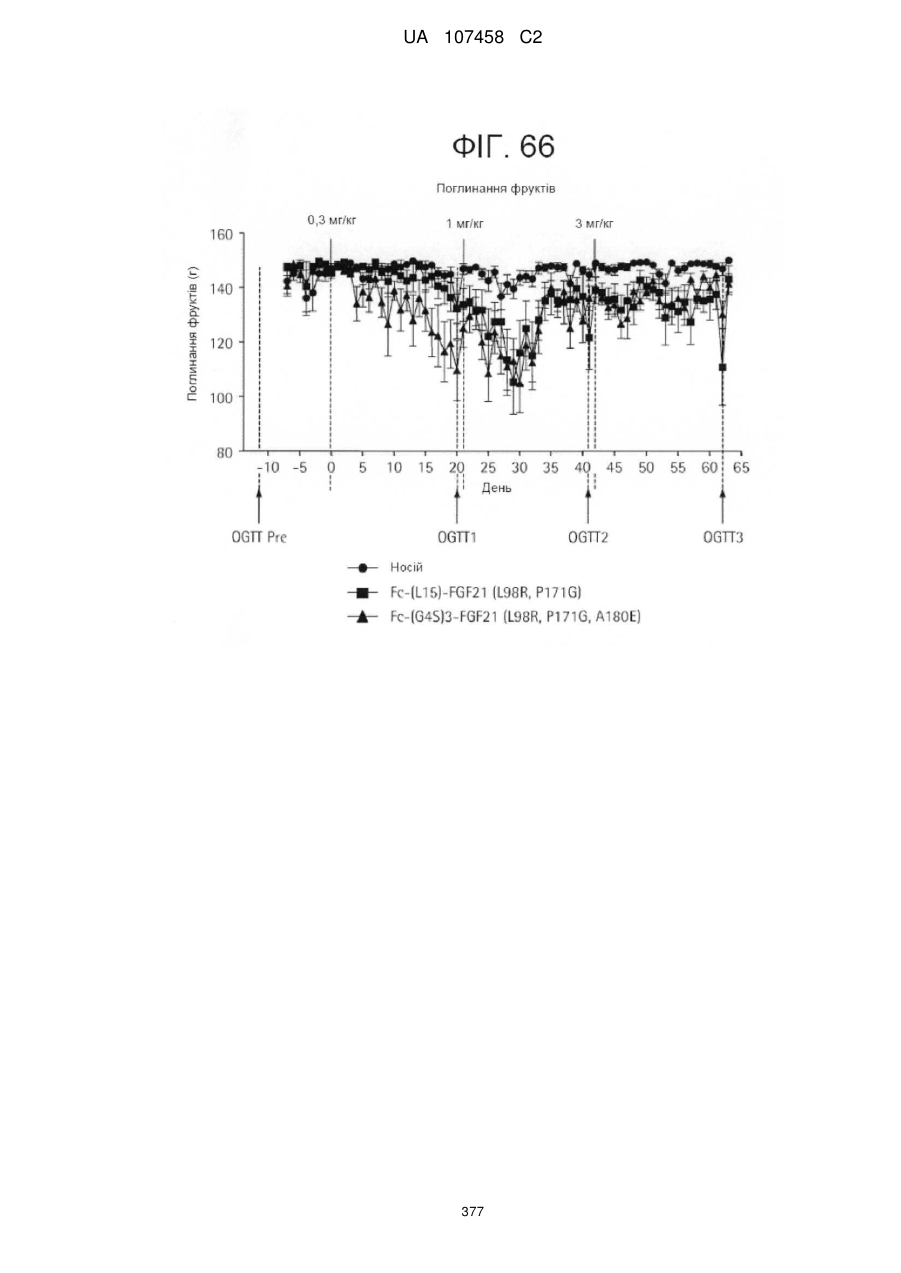
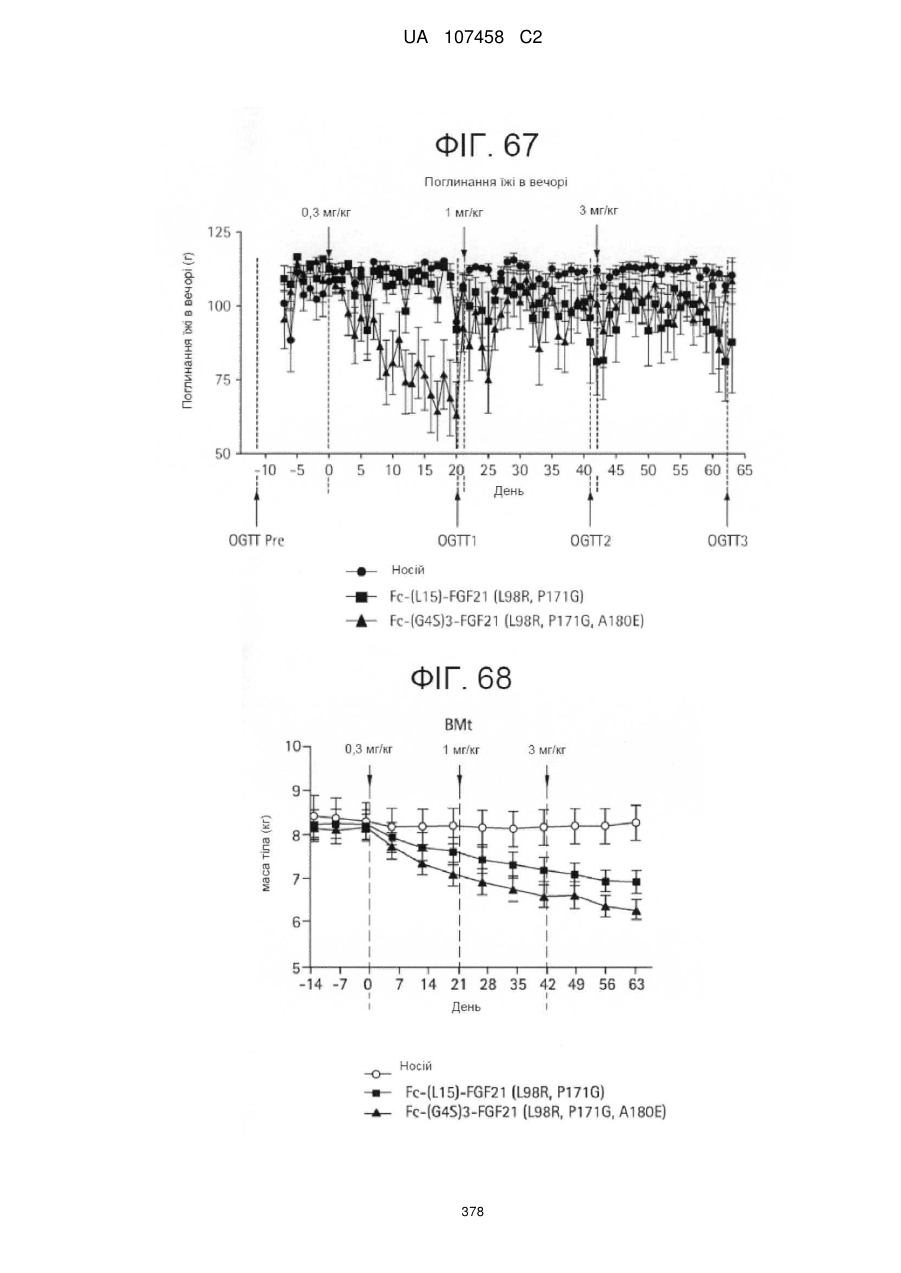
Мутанти fgf21 та їх застосування
Номер патенту: 107458
Опубліковано: 12.01.2015
Автори: Еллісон Мюріель Маріє, Лі Юе-Шенг, Сун Йеонгхун, Хетч Ренді Іра, Белоускі Едвард Джон, Ксу Йінг, Хамбургер Агнес Єва, Майклз Марк Лео
Формула / Реферат
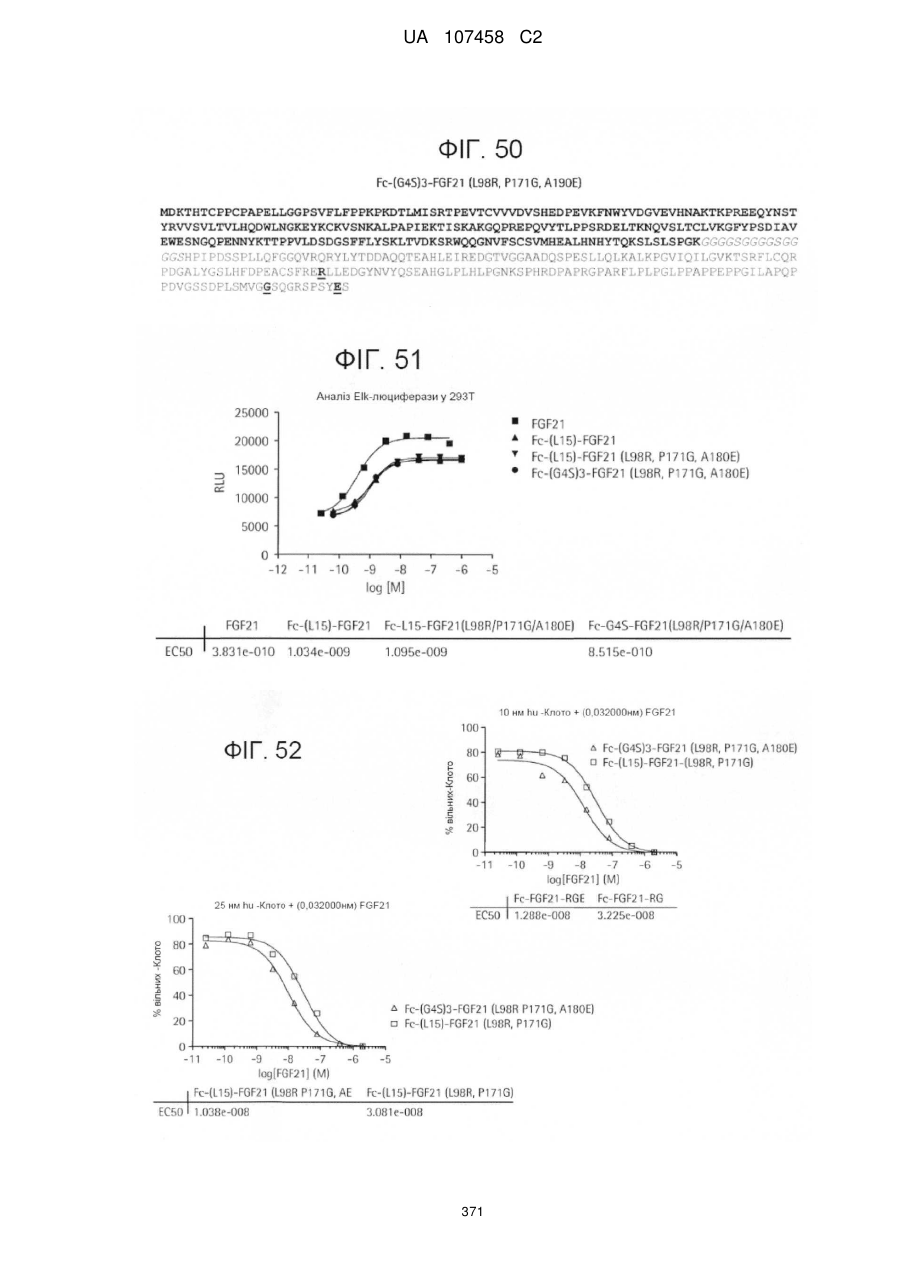
1. Поліпептид, що містить: (а) поліпептид SEQ ID NO:4, в якому (і) лейцин у положенні 98 заміщений на аргінін; (ii) пролін у положенні 171 заміщений на гліцин; та (iii) аланін у положенні 180 заміщений на глутамову кислоту; (b) лінкерну послідовність, яка містить SEQ ID NO:31; та (c) Fc домен, який містить SEQ ID NO:11.
2. Поліпептид за п. 1, де поліпептид ковалентно зв'язаний з одним або більше полімерів.
3. Поліпептид за п. 2, де полімером є ПЕГ.
4. Фармацевтична композиція, яка містить поліпептид за п. 1 і фармацевтично прийнятний формоутворюючий агент.
5. Фармацевтична композиція за п. 4, в якій фармацевтично прийнятним формоутворюючим агентом є гідрогель.
6. Спосіб зниження рівня глюкози у крові пацієнта, що страждає на метаболічний розлад, який включає введення пацієнтові, що того потребує, терапевтично ефективної кількості фармацевтичної композиції за п. 4.
7. Спосіб за п. 6, де метаболічним розладом є діабет 2 типу.
8. Спосіб за п. 6, де метаболічним розладом є ожиріння.
9. Спосіб лікування діабету 2 типу, який включає введення пацієнтові, що того потребує, терапевтично ефективної кількості фармацевтичної композиції за п. 4.
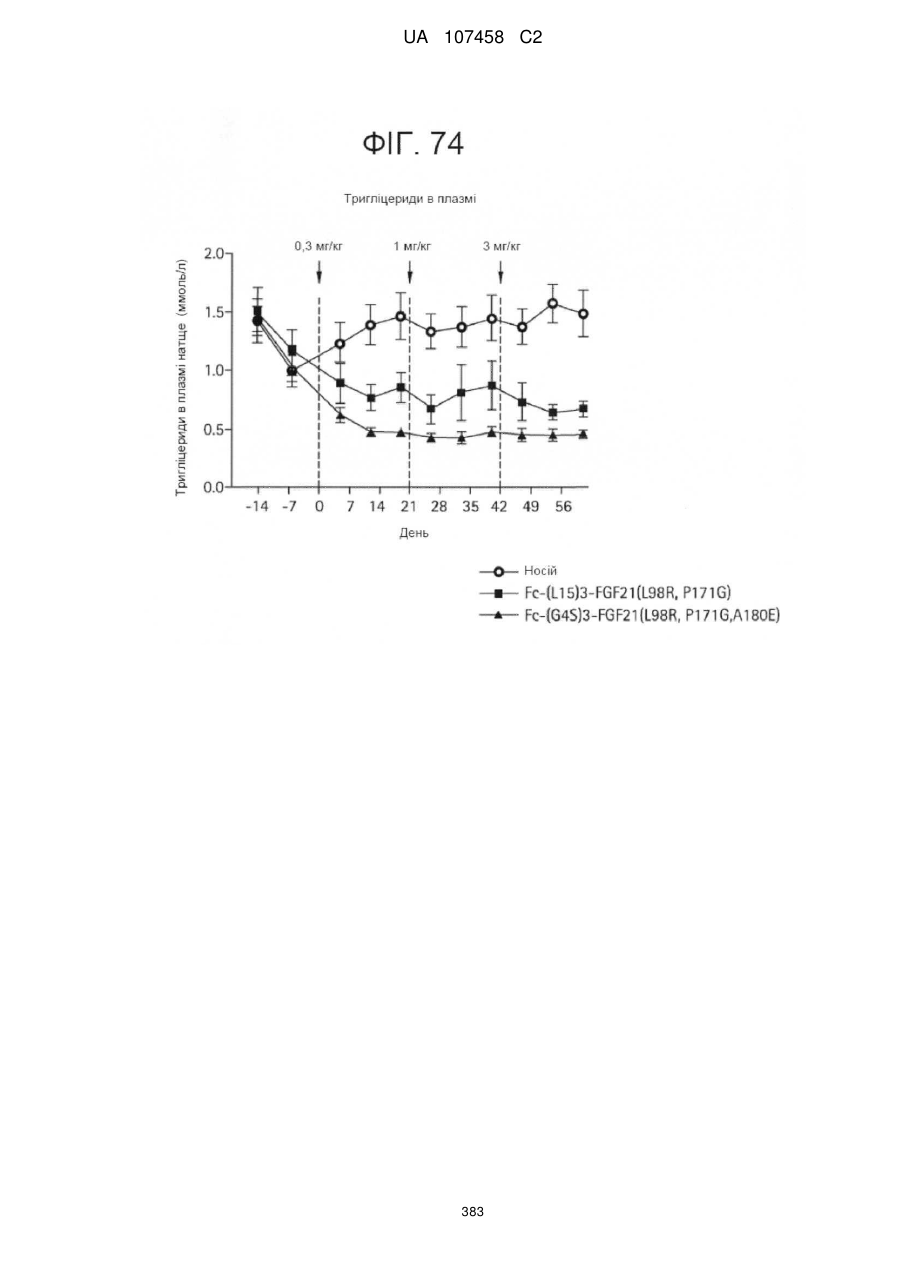
10. Спосіб зниження рівня тригліцеридів натще у пацієнта, який включає введення пацієнтові, що того потребує, терапевтично ефективної кількості фармацевтичної композиції за п. 4.
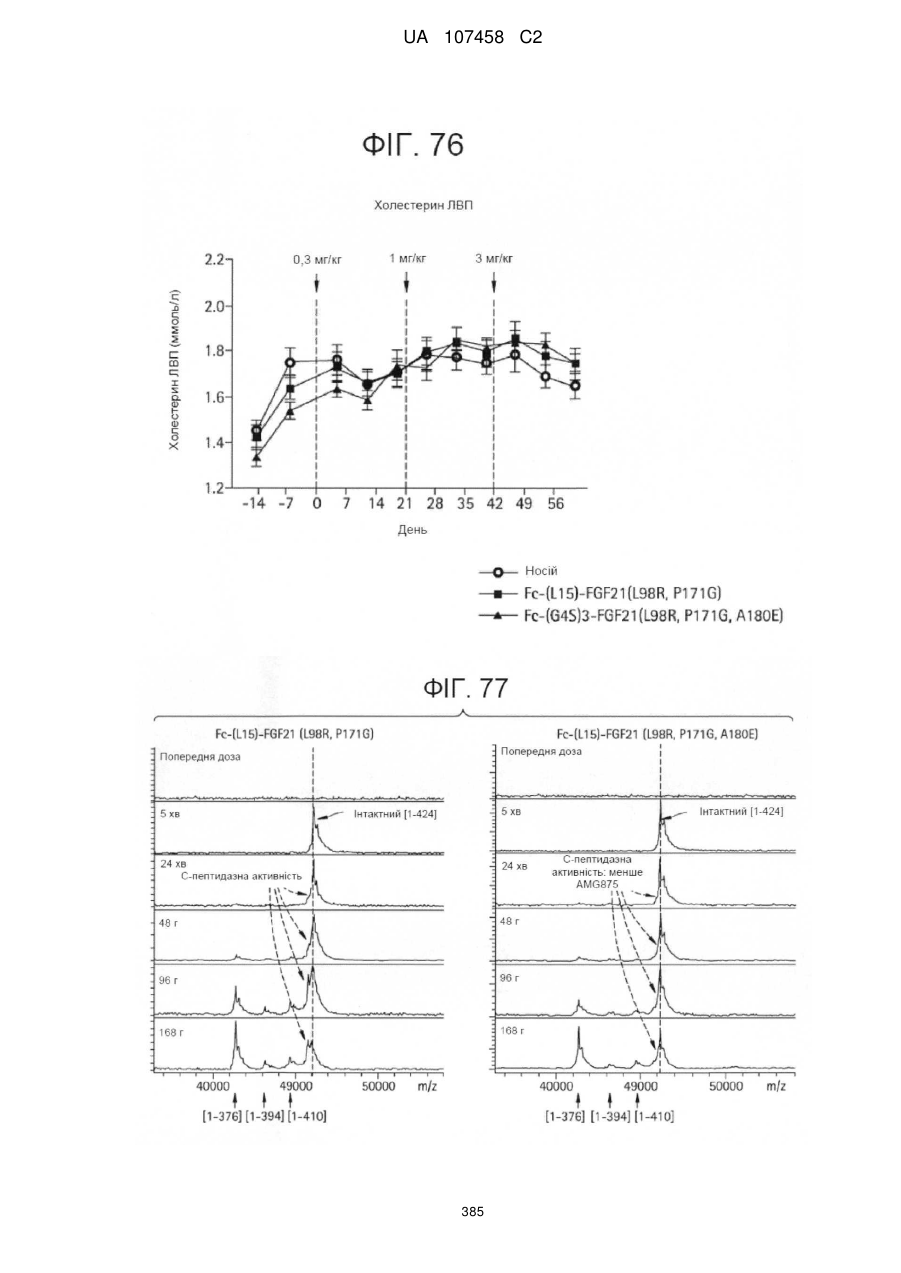
11. Спосіб підвищення рівнів холестерину ліпопротеїдів високої щільності у пацієнта, який включає введення пацієнтові, що того потребує, терапевтично ефективної кількості фармацевтичної композиції за п. 4.
12. Спосіб покращення толерантності до глюкози у пацієнта, який включає введення пацієнтові, що того потребує, терапевтично ефективної кількості фармацевтичної композиції за п. 4.
13. Поліпептид, що містить послідовність SEQ ID NO:47.
14. Поліпептид за п. 13, де поліпептид ковалентно зв'язаний з одним або більше полімерів.
15. Поліпептид за п. 14, де полімером є ПЕГ.
16. Фармацевтична композиція, яка містить поліпептид за п. 13 і фармацевтично прийнятний формоутворюючий агент.
17. Фармацевтична композиція за п. 16, в якій фармацевтично прийнятним формоутворюючим агентом є гідрогель.
18. Спосіб зниження рівня глюкози у крові пацієнта, що страждає на метаболічний розлад, який включає введення пацієнтові, що того потребує, терапевтично ефективної кількості фармацевтичної композиції за п. 16.
19. Спосіб за п. 18, де метаболічним розладом є діабет 2 типу.
20. Спосіб за п. 18, де метаболічним розладом є ожиріння.
21. Спосіб лікування діабету 2 типу, який включає введення пацієнтові, що того потребує, терапевтично ефективної кількості фармацевтичної композиції за п. 16.
22. Спосіб зниження рівня тригліцеридів натще у пацієнта, який включає введення пацієнтові, що того потребує, терапевтично ефективної кількості фармацевтичної композиції за п. 16.
23. Спосіб підвищення рівнів холестерину ліпопротеїдів високої щільності у пацієнта, який включає введення пацієнтові, що того потребує, терапевтично ефективної кількості фармацевтичної композиції за п. 16.
24. Спосіб покращення толерантності до глюкози у пацієнта, який включає введення пацієнтові, що того потребує, терапевтично ефективної кількості фармацевтичної композиції за п. 16.
25. Поліпептид, кодований нуклеїновокислотною послідовністю SEQ ID NO:46.
26. Нуклеїнова кислота, яка кодує (а) поліпептид SEQ ID NO:4, в якому (і) лейцин у положенні 98 заміщений на аргінін; (ii) пролін у положенні 171 заміщений на гліцин; та (iii) аланін у положенні 180 заміщений на глутамову кислоту; (b) лінкерну послідовність, яка містить SEQ ID NO:31; та (c) Fc домен, який містить SEQ ID NO:11.
27. Нуклеїнова кислота за п. 26, де нуклеїнова кислота містить SEQ ID NO:46.
28. Вектор, що містить молекулу нуклеїнової кислоти за п. 27.
29. Клітина-хазяїн, що містить молекулу нуклеїнової кислоти за п. 26 або п. 27.
30. Нуклеїнова кислота, яка кодує поліпептид SEQ ID NO:47.
31. Нуклеїнова кислота, яка містить нуклеотиди 1-1272 послідовності SEQ ID NO:46.
Текст
Реферат: Винахід пропонує молекули нуклеїнових кислот, що кодують мутантні поліпептиди FGF21, мутантні поліпептиди FGF21, як такі, фармацевтичні композиції, що включають мутантні поліпептиди FGF21, і способи лікування метаболічних захворювань із застосуванням таких нуклеїнових кислот, поліпептидів або фармацевтичних композицій. UA 107458 C2 (12) UA 107458 C2 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 МУТАНТИ FGF21 ТА ЇХ ЗАСТОСУВАННЯ У цій заявці заявлений пріоритет попередньої заявки США № 61/175,736, поданої 5 травня 2009 р., і попередньої заявки США № 61/285,118, поданої 9 грудня 2009 р., усі з яких включені в цю заявку шляхом посилання. ГАЛУЗЬ ВИНАХОДУ Даний винахід відноситься до молекул нуклеїнових кислот, що кодують мутантні поліпептиди FGF21, до мутантних поліпептидів FGF21, до фармацевтичних композицій, що містять мутантні поліпептиди FGF21 та до способів лікування метаболічних захворювань із застосуванням таких нуклеїнових кислот, поліпептидів або фармацевтичних композицій. ПЕРЕДУМОВИ СТВОРЕННЯ ВИНАХОДУ FGF21 є поліпептидом, що секретується, належить до підродини факторів росту фібробластів (FGF), які включають FGF19, FGF21 і FGF23 (Itoh et al., 2004, Trend Genet. 20: 56369). Поліпептид FGF21 є атиповим FGF в тому відношенні, що він незалежний від гепарину і функціонує як гормон в регуляції глюкози, ліпідів і енергетичного метаболізму. FGF21 був виділений з бібліотеки кДНК печінки як печінковий фактор, що секретується. Він високо експресується в печінці і підшлунковій залозі, та є єдиним членом сімейства FGF, що експресується, головним чином, в печінці. Трансгенні миші з надмірною експресією FGF21 демонструють метаболічні фенотипи уповільнених темпів росту, низького рівня глюкози і тригліцеридів в плазмі, а також відсутність пов'язаного з віком цукрового діабету 2 типу, гіперплазії острівкових клітин підшлункової залози та ожиріння. Фармакологічне введення рекомбінантного білку FGF21 в моделях гризунів і приматів призводить до нормалізації рівня глюкози в плазмі, до зниження рівня тригліцеридів і холестерину, а також до покращення толерантності до глюкози та чутливості до інсуліну. Додатково до цього, FGF21 знижує масу тіла і відкладення тілесного жиру за рахунок збільшення споживання енергії, фізичної активності і швидкості метаболізму. Експериментальні дослідження дають підтвердження фармакологічного введення FGF21 для лікування цукрового діабету 2 типу, ожиріння, дисліпидемії та інших метаболічних станів або захворювань у людини. FGF21 людини має короткий період напіввиведення in vivo. У мишей період напіввиведення FGF21 людини складає від 1 до 2 годин, а у мавп cynomolgus період напіввиведення складає від 2,5 до 3 годин. При розробці білкового препарату FGF21 для застосування як ліків при лікуванні цукрового діабету 2 типу було б бажано збільшити період напіввиведення. Білки FGF21, що мають подовжений період напіввиведення, дозволили б рідше вводити дози ліків хворим, що одержують такі препарати. Опис таких білків наводиться в цьому документі. СУТЬ ВИНАХОДУ Описано виділений поліпептид, що містить амінокислотну послідовність SEQ ID NO:4, що додатково містить: (а) щонайменше одне амінокислотне заміщення в положенні 180 та (b) щонайменше одне амінокислотне заміщення, вибране з групи, що складається з: (і) заміщення в положенні 171; та (іі) заміщення в положенні 98, та (с) їх комбінацій. В одному з варіантів здійснення даного винаходу виділений поліпептид включає заміщення в положенні 98, і заміщення в положенні 180, де (а) заміщення в положенні 98 вибирають із групи, що складається з аргініну, цистеїну, глутамової кислоти, глутаміну, лізину та треоніну; та (b) заміщення в положенні 180 вибирають із групи, що складається з гліцину, проліну, серину або глутамової кислоти; та (с) їх комбінацій. В одному з варіантів здійснення винаходу залишок у положенні 98 є аргініном, а залишок у положенні 180 є глутаміновою кислотою. Також представлено злитий поліпептид, що містить виділений поліпептид, злитий з гетерологічною амінокислотною послідовністю. В одному варіанті здійснення винаходу гетерологічна амінокислотна послідовність являє собою Fc домен або його фрагмент, і може містити амінокислотну послідовність SEQ ID NO:11. В іншому варіанті здійснення винаходу, поліпептид зливають з Fc доменом за допомогою лінкера та у ще одному варіанті здійснення винаходу лінкер містить GGGGSGGGGSGGGGS (SEQ ID NO:31). В одному конкретному варіанті здійснення винаходу поліпептид містить SEQ ID NO:47. Також описано мультимер, що містить два або більше злитих поліпептидів. Також описано фармацевтичну композицію, що містить виділений поліпептид та фармацевтично прийнятний формоутворюючий агент, такий, як гідрогель. В іншому аспекті представлено спосіб лікування метаболічного розладу, та в одному варіанті здійснення даний спосіб включає введення хворій людині, що потребує лікування, фармацевтичної композиції, що відповідає даному винаходу. В одному варіанті здійснення винаходу, метаболічним захворюванням є цукровий діабет, а іншим метаболічним захворюванням є ожиріння. Також представлені нуклеїнові кислоти, що кодують виділений поліпептид, та в одному варіанті здійснення нуклеїнова кислота містить SEQ ID NO:46. Нуклеїнова кислота може бути присутня у векторі, який сам по собі може бути присутнім у 1 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 клітині-хазяїні. У ще одному варіанті здійснення винаходу поліпептид містить (a) амінокінцеве усічення не більш ніж 8 амінокислотних залишків, при цьому поліпептид здатний знижувати рівень глюкози у крові ссавця, (b) карбоксикінцеве усічення не більш ніж 12 амінокислотних залишків, при цьому поліпептид здатний знижувати рівень глюкози у крові ссавця, або (c) амінокінцеве усічення не більш ніж амінокислотних залишків і карбоксикінцеве усічення не більш ніж 12 амінокислотних залишків, при цьому поліпептид здатний знижувати рівень глюкози в крові ссавця. В інших варіантах здійснення винаходу поліпептид ковалентно зв'язано з одним або більше полімерами, такими, як ПЕГ. В іншому варіанті здійснення виділений поліпептид містить заміщення в положенні 171 і заміщення в положенні 180, де: (a) заміщення в положенні 180 вибирають із групи, що складається з гліцину, проліну, серину і глутамової кислоти; (b) заміщення в положенні 171 вибирають із групи, що складається з аланіну, аргініну, аспарагіну, аспартамової кислоти, цистеїну, глутамової кислоти, глутаміну, гліцину, гістидину, лізину, серину, треоніну, триптофану та тирозину; та (c) їх комбінацій. В одному варіанті здійснення винаходу залишок у положенні 171 є гліцином, а залишок у положенні 180 є глутамовою кислотою. Також представлено поліпептид злиття, що містить виділений поліпептид, злитий з гетерологічною амінокислотною послідовністю. В одному варіанті здійснення винаходу гетерологічна амінокислотна послідовність є Fc доменом або його фрагментом, і може містити амінокислотну послідовність SEQ ID NO: 11. В іншому варіанті здійснення винаходу поліпептид зливають з Fc доменом за допомогою лінкера та у ще одному варіанті здійснення винаходу лінкер містить GGGGSGGGGSGGGGS (SEQ ID NO:31). В одному конкретному варіанті здійснення винаходу поліпептид містить SEQ ID NO:47. Також описано мультимер, що містить два або більше злитих поліпептидів. Також описано фармацевтичну композицію, що містить виділений поліпептид і фармацевтично прийнятний формоутворюючий агент, такий, як гідрогель. В іншому аспекті, представлено спосіб лікування метаболічного захворювання, та один варіант здійснення винаходу включає введення хворій людині, що потребує такого лікування, фармацевтичної композиції, що відповідає даному винаходу. В одному варіанті здійснення винаходу, метаболічним захворюванням є діабет, а іншим метаболічним захворюванням є ожиріння. Також представлені нуклеїнові кислоти, що кодують виділений поліпептид і в одному варіанті здійснення винаходу нуклеїнова кислота містить SEQ ID NO: 46. Нуклеїнова кислота може бути присутня у векторі, що сам по собі може бути присутнім у клітині-хазяїні. У ще одному варіанті здійснення винаходу поліпептид містить: (a) амінокінцеве усічення не більш ніж 8 амінокислотних залишків, при цьому поліпептид здатний знижувати рівень глюкози у крові ссавця, (b) карбоксикінцеве усічення не більш ніж 12 амінокислотних залишків, при цьому поліпептид здатний знижувати рівень глюкози у крові ссавця, або (c) амінокінцеве усічення не більш ніж 8 амінокислотних залишків і карбоксикінцеве усічення не усічення не більш ніж 12 амінокислотних залишків, при цьому поліпептид здатний знижувати рівень глюкози в крові ссавця. В інших варіантах здійснення винаходу поліпептид ковалентно зв'язаний з одним або більше полімерів, наприклад, ПЕГ. У ще одному варіанті здійснення винаходу поліпептид містить заміщення в положенні 98, заміщення в положенні 171 та заміщення в положенні 180, SEQ ID NO:4, де: (a) заміщення в положенні 171 вибирають із групи, що складається з аланіну, аргініну, аспарагіну, аспартамової кислоти, цистеїну, глутамової кислоти, глутаміну, гліцину, гістидину, лізину, серину, треоніну, триптофану або тирозину; (b) заміщення в положенні 98 вибирають із групи, що складається з аргініну, цистеїну, глутамової кислоти, глутаміну, лізину або треоніну; та (c) заміщення в положенні 180 вибирають з групи, що складається з гліцину, проліну, серину або глутамової кислоти, та їх комбінацій. У додатковому аспекті залишком у положенні 98 є аргінін, залишком у положенні 171 є гліцин і залишком у положенні 180 є глутамова кислота. Також розкрито злитий поліпептид, що містить виділений поліпептид, злитий з гетерологічною амінокислотною послідовністю. В одному варіанті здійснення винаходу гетерологічна амінокислотна послідовність є Fc доменом або його фрагментом, і може містити амінокислотну послідовність SEQ ID NO:11. У ще одному варіанті здійснення винаходу поліпептид злитий з Fc доменом за допомогою лінкера та у ще одному варіанті здійснення винаходу лінкер містить GGGGSGGGGSGGGGS (SEQ ID NO:31). В одному конкретному варіанті здійснення винаходу поліпептид містить SEQ ID NO:47. Також описано мультимер, що містить два або більш злитих поліпептиди. Також розкрито фармацевтичну композицію, що містить виділений поліпептид та фармацевтично прийнятний формоутворюючий агент, наприклад, гідрогель. В іншому аспекті, представлено спосіб лікування метаболічного захворювання, та один варіант здійснення винаходу включає введення хворій людині, що потребує такого лікування, фармацевтичної композиції, що відповідає даному 2 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 винаходу. В одному варіанті здійснення винаходу, метаболічним захворюванням є діабет, а іншим метаболічним захворюванням є ожиріння. Також представлені нуклеїнові кислоти, що кодують виділений поліпептид, і в одному варіанті здійснення нуклеїнова кислота містить SEQ ID NO: 46. Нуклеїнова кислота може бути присутня у векторі, що сам по собі може бути присутнім у клітині-хазяїні. У ще одному варіанті здійснення винаходу поліпептид містить: (a) амінокінцеве усічення не більш ніж 8 амінокислотних залишків, при цьому поліпептид здатний знижувати рівень глюкози у крові ссавця, (b) карбоксикінцеве усічення не більш ніж 12 амінокислотних залишків, при цьому поліпептид здатний знижувати рівень глюкози у крові ссавця, або (c) амінокінцеве усічення не більш ніж 8 амінокислотних залишків та карбоксикінцеве усічення не більш ніж 12 амінокислотних залишків, при цьому поліпептид здатний знижувати рівень глюкози в крові ссавця. У ще одних варіантах здійснення винаходу поліпептид ковалентно зв'язаний з одним або більше полімерів, наприклад, ПЕГ. Специфічні варіанти здійснення винаходи будуть очевидні з наступного більш детального опису деяких варіантів здійснення винаходу і з формули винаходу. СТИСЛИЙ ОПИС КРЕСЛЕНЬ На Фігурах 1A-1B показані результати аналізу активності ELK-люциферази, що був проведений на усічених мутантах FGF21 7-181 та 8-181 (Фіг. 1A) та усічених мутантах FGF21 1172, 1-171, 1-169 та 1-164 (Фіг. 1B); кожна панель показує результати, одержані на контрольних зразках FGF21 людини. На Фіг. 2 показані результати аналізу активності ELK-люциферази, що був проведений на контрольних зразках FGF21 людини і на усічених мутантах FGF21 3-181, 4-181, 5-181, 7-181, 8181, 1-180, 1-178, 1-177, 1-176, 1-175, 1-174, 1-173, 1-172, 9-181 та 1-149. На Фіг. 3 показані значення рівня глюкози в крові, вимірюваного у мишей, яким шляхом ін'єкції вводили PBS (зафарбований стовпчик), контрольний FGF21 людини (порожній стовпчик) або усічені мутанти FGF21 8-181 (сірий стовпчик) та 9-181 (стовпчик із шаховими клітками). На Фіг. 4 показано зміну у відсотках рівня глюкози в крові, вимірюваного у мишей, яким шляхом ін'єкції вводили PBS (зафарбовані кружки), контрольний Fc-FGF21 дикого типу (WT) (порожні кружки) або усічені гібридні білки Fc-FGF21, що включають амінокислотні залишки 5181 (зафарбовані трикутники) або 7-181 (порожні трикутники). На Фіг. 5 показано зміну у відсотках рівня глюкози в крові, вимірюваного у мишей, яким шляхом ін'єкції вводили PBS (зафарбовані кружки), контрольний FGF21-Fc (WT) (порожні кружки), усічений гібридний білок FGF21-Fc, що включає амінокислотні залишки 1- 175 (зафарбовані трикутники) або усічений білок Fc-FGF21, що включає залишки 1-171 (порожні трикутники). На Фігурах 6A-6D показано результати аналізу контрольного зразка Fc-(G5)-FGF21 (SEQ ID NO:107) людини (Фіг. 6A) та зразків Fc-(G5)-FGF21, одержаних від мишей через 6 годин (зразок D6, Фіг. 6B), 24 години (зразок D24, Фіг. 6C) та 48 годин (зразок D48, Фіг. 6D) після ін'єкції з застосуванням комбінованого способу рідинної хроматографії і мас-спектрометрії (LC-MS). На Фігурах 7A-7D показані результати аналізу контрольного зразка FGF21-(G3)-Fc (SEQ ID NO:105) людини (Фіг. 7A) та зразків FGF21-(G3)-Fc, одержаних від мишей через 6 годин (зразок E6, Фіг. 7B), 24 години (зразок E24, Фіг. 7C) та 48 годин (зразок E48, Фіг. 7D) після ін'єкції, способом LC-MS. На Фігурах 8A-8D показані результати аналізу контрольного зразка Fc-(L15)-FGF21 (SEQ ID NO: 49) (Фіг. 8A) і зразків Fc-(L15)-FGF21, одержаних від мишей через 6 годин (Фіг. 8B), 24 години (Фіг. 8C) та 48 годин (Фіг. 8D) після ін'єкції, способом LC-MS. На Фігурах 9A-9D показані результати аналізу контрольного зразка FGF21-(L15)-Fc (SEQ ID NO: 41) (Фіг. 9A) і зразків FGF21-(L15)-Fc, одержаних від мишей через 6 годин (Фіг. 9B), 24 години (Фіг. 9C) та 48 годин (Фіг. 9D) після ін'єкції, способом LC-MS. На Фігурах 10A-10B показані сайти розщеплення, ідентифіковані аналізом LC-MS гібридних білків Fc-(L15)-FGF21 (Фіг. 10A, SEQ ID NO:49) та Fc-(L15)-FGF21 (Фіг. 10B, SEQ ID NO:41), введених мишам шляхом ін'єкції. На Фіг. 11 показані результати вимірювань рівня глюкози в крові у мишей, яким шляхом ін'єкції вводили PBS (зафарбований стовпчик), Fc-(L15)-FGF21 (SEQ ID NO:49) (порожній стовпчик) або такі мутанти Fc-(L15)-FGF21, як Fc-(L15)-FGF21 G170E (SEQ ID NO:51) (сірий стовпчик), Fc-(L15)-FGF21 P171A (SEQ ID NO:53) (стовпчик із шаховими клітками), Fc-(L15)FGF21 S172L (SEQ ID NO:55) (порожній стовпчик з діагональними смужками), Fc-(L15)-FGF21 (G170E P171 S172L) (SEQ ID NO:59) (зафарбований стовпчик с горизонтальними смужками) або Fc-(L15)-FGF21 G151A (SEQ ID NO:61) (порожній стовпчик з діагональними смужками). На Фіг. 12 показано зміну у відсотках рівня глюкози в крові за результатами вимірювань у 3 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 мишей, яким шляхом ін'єкції вводили PBS (зафарбовані кружки), Fc-(L15)-FGF21 (SEQ ID NO:49) (порожні кружки) або такі мутанти Fc-(L15)-FGF21 як Fc-(L15)-FGF21 G170E (SEQ ID NO:51) (зафарбовані трикутники), Fc-(L15)-FGF21 P171A (SEQ ID NO:53) (порожні трикутники), Fc-(L15)-FGF21 S172L (SEQ ID NO:55) (зафарбовані ромби), Fc-(L15)-FGF21 G170E/P171A/S172L (SEQ ID NO:59) (порожні ромби) або Fc-(L15)-FGF21 G151A (SEQ ID NO:61) (зафарбовані квадрати). На Фіг. 13 показані результати вимірювань рівня глюкози в крові у мишей, яким шляхом ін'єкції вводили PBS (зафарбований стовпчик), Fc-(L15)-FGF21 (SEQ ID NO:49) (порожній стовпчик), або такі мутанти Fc-(L15)-FGF21, як Fc-(L15)-FGF21 P150A, G151A, I152V (сірий стовпчик), Fc-(L15)-FGF21 G170E (SEQ ID NO:51) (порожній стовпчик з діагональними смужками), Fc-(L15)-FGF21 G170E/P171A (SEQ ID NO:63) (сірий стовпчик з діагональними смужками) або Fc-(L15)-FGF21 G170E/S172L (SEQ ID NO:67) (порожній стовпчик з діагональними смужками). На Фіг. 14 показано зміну у відсотках рівня глюкози в крові за результатами вимірювань у мишей, яким шляхом ін'єкції вводили PBS (зафарбовані квадрати), Fc-(L15)-FGF21 (SEQ ID NO:49) (порожні квадрати) або такі мутанти Fc-(L15)-FGF21, як Fc-(L15)-FGF21 P150A, G151A, I152V (SEQ ID NO:65) (зафарбовані перевернені трикутники), Fc-(L15)-FGF21 G170E(SEQ ID NO:51) (порожні перевернені трикутники), Fc-(L15)-FGF21 G170E, P171A (SEQ ID NO:63) (зафарбовані кружки) або Fc-(L15)-FGF21 G170E, S172L (SEQ ID NO:67) (порожні кружки). На Фіг. 15 показані результати вимірювань рівня глюкози в крові у мишей, яким шляхом ін'єкції вводили PBS (зафарбований стовпчик), або такі мутанти Fc-(L15)-FGF21, як Fc-(L15)FGF21 G 170E (SEQ ID NO:51) (порожній стовпчик), Fc-(L15)-FGF21 G170A (SEQ ID NO:69) (сірий стовпчик), Fc-(L15)-FGF21 G170C (SEQ ID NO:71) (порожній стовпчик з діагональними смужками), Fc-(L15)-FGF21 G170D (SEQ ID NO:73) (сіро-білий стовпчик), Fc-(L15)-FGF21 G 170N (SEQ ID NO:75) (зафарбований стовпчик з діагональними смужками) або Fc-(L15)-FGF21 G 170S (SEQ ID NO:77) (порожній стовпчик з діагональними смужками). На Фіг. 16 показано зміну у відсотках рівня глюкози в крові за результатами вимірювань у мишей, яким шляхом ін'єкції вводили PBS (зафарбовані кружки) або такі мутанти Fc-(L15)FGF21, як Fc-(L15)-FGF21 G170E (SEQ ID NO:51) (порожні кружки), Fc-(L15)-FGF21 G170A (SEQ ID NO:69) (зафарбовані трикутники), Fc-(L15)-FGF21 G170C (SEQ ID NO:71) (порожні трикутники), Fc-(L15)-FGF21 G170D (SEQ ID NO:73) (зафарбовані ромби), Fc-(L15)-FGF21 G170N (SEQ ID NO:75) (порожні ромби) або Fc-(L15)-FGF21 G170S (SEQ ID NO:77) (перевернені порожні трикутники). На Фіг. 17 показані результати вимірювань рівня глюкози в крові у мишей, яким шляхом ін'єкції вводили PBS (зафарбований стовпчик) або такі мутанти Fc-(L15)-FGF21, як Fc-(L15)FGF21 G 170E (SEQ ID NO:51) (порожній стовпчик), Fc-(L15)-FGF21 P171E (SEQ ID NO:79) (сірий стовпчик), Fc-(L15)-FGF21 P171H (SEQ ID NO:81) (зафарбований стовпчик з діагональними смужками), Fc-(L15)-FGF21 P171Q (SEQ ID NO:83) (порожній стовпчик з діагональними смужками), Fc-(L15)-FGF21 P171T (SEQ ID NO:85) (стовпчик із шаховими клітками) або Fc-(L15)-FGF21 P171Y (SEQ ID NO:87) (сірий стовпчик з діагональними смужками). На Фіг. 18 показано зміну у відсотках рівня глюкози в крові за результатами вимірювань у мишей, яким шляхом ін'єкції вводили PBS (зафарбовані кружки) або такі мутанти Fc-(L15)FGF21, як Fc-(L15)-FGF21 G170E (SEQ ID NO:51) (порожні кружки), Fc-(L15)-FGF21 P171E P171E (SEQ ID NO:79) (SEQ ID NO:79) (зафарбовані трикутники), Fc-(L15)-FGF21 P171H (SEQ ID NO:81) (порожні трикутники), Fc-(L15)-FGF21 P171Q (SEQ ID NO:83) (зафарбовані ромби), Fc-(L15)-FGF21 P171T(SEQ ID NO:85) (порожні ромби) або Fc-(L15)-FGF21 P171Y (SEQ ID NO:87) (зафарбовані квадрати). На Фігурах 19A-19D показані результати аналізу контрольного зразка Fc-(L15)-FGF21 (Фіг. 19A, SEQ ID NO:49) і зразків, одержаних від мишей через 6 годин (Фіг. 19B), 24 години (Фіг. 19C) та 48 годин (Фіг. 19D) після ін'єкції, способом LC-MS. На Фігурах 20A-20D показані результати аналізу контрольного зразка Fc-(L15)-FGF21 G170E (Фіг. 20A, SEQ IDNO:51) та зразків Fc-(L15)-FGF21 G 170E, одержаних від мишей через 6 годин (Фіг. 20B), 24 години (Фіг. 20C) та 48 годин (Фіг. 20D) після ін'єкції, способом LC-MS. На Фігурах 21A-21D показані результати аналізу контрольного зразка Fc-(L15)-FGF21 P171A (Фіг. 21A, SEQ ID NO:53) та зразків Fc-(L15)-FGF21 P171A, одержаних від мишей через 6 годин (Фіг. 21B), 24 години (Фіг. 21C) та 48 годин (Фіг. 21D) після ін'єкції, способом LC-MS. На Фігурах 22A-22D показані результати аналізу контрольного зразка Fc-(L15)-FGF21 S172L (Фіг. 22A, SEQ ID NO:55) та зразків Fc-(L15)-FGF21 S172L, одержаних від мишей через 6 годин (Фіг. 22B), 24 години (Фіг. 22C) та 48 годин (Фіг. 22D) після ін'єкції, способом LC-MS. 4 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 На Фігурах 23A-23D показані сайти розщеплення, ідентифіковані аналізом LC-MS гібридних білків Fc-(L15)-FGF21 (Фіг. 23 A, SEQ ID NO: 49), Fc-(L15)-FGF21 G 170E (Фіг. 23B, SEQ ID NO: 51), Fc-(L15)-FGF21 P171A (Фіг. 23C, SEQ ID NO: 53) і Fc-(L15)-FGF21 S172L (Фіг. 23D, SEQ ID NO: 55), введених мишам шляхом ін'єкції. На Фігурах 24A-24C показані результати аналізу активності ELK-люциферази, проведеного на таких мутантах FGF21, як FGF21 L99R (SEQ ID NO:109), FGF21 L99D (SEQ ID NO:111), і FGF21 A111T (SEQ ID NO:113) (Фіг. 24A), на таких мутантах FGF21, як FGF21 A129D (SEQ ID NO:115), FGF21 A129Q (SEQ ID NO:117), та FGF21 A134K (SEQ ID NO:119) (Фіг. 24B) і на таких мутантах FGF21, як FGF21 A134Y (SEQ ID NO:121), FGF21 A134E (SEQ ID NO:123), та FGF21 A129K (SEQ ID NO:125) (Фіг. 24C), при цьому кожна панель показує результати, одержані на контрольних зразках FGF21 людини. На Фігурах 25A-25D показані результати аналізу активності ELK-люциферази, проведеного на таких мутантах Fc-(L15)-FGF21, як Fc-(L15)-FGF21 P171G (SEQ ID NO:89) Fc-(L15)-FGF21 P171S (SEQ ID NO:91), та Fc-(L15)-FGF21 P171T (SEQ ID NO:85) (Фіг. 25A), на таких мутантах Fc-(L15)-FGF21, як Fc-(L15)-FGF21 P171Y (SEQ ID NO:87), Fc-(L15)-FGF21 P171W (SEQ ID NO:93), та Fc-(L15)-FGF21 P171C (SEQ ID NO:95) (Фіг. 25B), на таких мутантах Fc-(L15)-FGF21 (SEQ ID NO:49), як Fc-(L15)-FGF21 A45K, G170E (SEQ ID NO:97), та FGF21 A45K (SEQ ID NO:99) (Фіг. 25C) та на таких мутантах Fc-(L15)-FGF21 (SEQ ID NO:49), як Fc-(L15)-FGF21 P171E (SEQ ID NO:79) та Fc-(L15)-FGF21 A45K/G170E (SEQ ID NO:97) (Фіг. 25D), при цьому кожна панель показує результати, одержані на контрольних зразках FGF21 людини. На Фігурах 26A-26B показано агрегацію, як функцію часу, для зрілого FGF21 дикого типу і для різних мутантів FGF21, Фіг. 26A показує зміну у відсотках агрегації для контрольного FGF21 (WT, зафарбовані ромби) і FGF21 A45K (зафарбовані кружки) після інкубації 65 мг/мл білка при 4 °C протягом 1, 2 і 4 днів, тоді як Фіг. 26B показує зміну у відсотках агрегації для контрольного FGF21 (WT) (SEQ ID NO:4) і варіантів FGF21 P78C (SEQ ID NO:127), FGF21, P78R (SEQ ID NO:129), FGF21 L86T (SEQ ID NO:131), FGF21 L86C (SEQ ID NO:133), FGF21 L98C (SEQ ID NO:135), FGF21 L98R (SEQ ID NO:137), FGF21 A111T (SEQ ID NO:113), FGF21 A129D (SEQ ID NO:115), FGF21 A129Q (SEQ ID NO:117), FGF21 A129K (SEQ ID NO:125), FGF21 A134K (SEQ ID NO:119), FGF21 A134Y (SEQ ID NO:121), та FGF21 A134E (SEQ ID NO:123) (усі маркіровані на графіку) після інкубації 65 мг/мл білка при 4 °C протягом 1, 6 та 10 днів. На Фіг. 27 показані результати аналізу активності ELK-люциферази, проведеного на контрольному FGF21 людини і на таких мутантах FGF21, як FGF21 A45K (SEQ ID NO:99), FGF21 L52T (SEQ ID NO:139), та FGF21 L58E (SEQ ID NO:141). На Фіг. 28 A представлений графік, що показує зміну рівня агрегації для таких мутантів Fc(L15)-FGF21, як Fc-(L15)-FGF21 6-181, G170E (SEQ ID NO:101) (зафарбовані ромби), Fc-(L15)FGF21 A45K, G170E (SEQ ID NO:97) (порожні квадрати), Fc-(L15)-FGF21 P171E (SEQ ID NO:79) (зафарбовані трикутники), Fc-(L15)-FGF21 P171A (SEQ ID NO:53) (хрестики), Fc-(L15)-FGF21 G 170E (SEQ ID NO:51) (порожні трикутники) і для контрольного FGF21 (зафарбовані кружки) після інкубації при 4 °C протягом 1, 4 та 8 днів, а Фіг. 28B являє собою гістограмму, що також показує результати інкубації. На Фіг. 29 показані результати вимірювання рівня глюкози в крові у мишей, яким шляхом ін'єкції вводили PBS (носій) (зафарбовані кружки) або такі мутанти Fc-(L15)-FGF21, як Fc-(L15)FGF21 A45K/G170E (SEQ ID NO:97) (порожні кружки), Fc-(L15)-FGF21 A45K, P171G (SEQ ID NO:103) (зафарбовані трикутники) або Fc-(L15)-FGF21 L98R, P171G (SEQ ID NO:43) (порожні трикутники). На Фіг. 30 представлений графік, що показує результати аналізу активності ELKлюциферази, проведеного на FGF21 людини (зафарбовані кружки, суцільна лінія), на Fc-(L15)FGF21 (SEQ ID NO:49) (порожні кружки, суцільна лінія) і на Fc-(L15)-FGF21 L98R, P171G (SEQ ID NO:43) (зафарбовані трикутники, пунктирна лінія). На Фіг. 31 представлено графік, що показує величину у відсотках агрегатів з високою молекулярною масою, що спостерігаються після дев'яти днів витримування при кімнатній температурі (Фіг. 31A) та 4 °C (Фіг. 31B) для Fc-(L15)-FGF21 (SEQ ID NO:4) (зафарбовані кружки, суцільна лінія), Fc-(L15)-FGF21 (SEQ ID NO:49) (порожні кружки, суцільна лінія) і Fc-(L15)-FGF21 L98R/P171G (SEQ ID NO:43) (зафарбовані трикутники, пунктирна лінія). На Фіг. 32 представлена серія трас МАЛДІ при мас-спектрометрії, що показує зміни, що спостерігаються, Fc-(L15)-FGF21 L98R, P171G (SEQ ID NO:43) у різних точках протягом 168годинного проміжку часу. На Фіг. 33 представлений графік, що показує зміну у відсотках рівня глюкози в крові у мишей ob/ob для контрольного носія PBS (порожні кружки), зрілого FGF21 дикого типу (зафарбовані квадрати) і таких мутантів FGF21, як Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) 5 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 (перевернені зафарбовані трикутники), Fc-(L15)-FGF21 (L98R, P171G, 182P) (SEQ ID NO:143) (порожні ромби) та Fc-(L15)-FGF21 (L98R, P171G, 182G) (SEQ ID NO:145) (зафарбовані кружки). На Фіг. 34 представлено графік, що показує зміну у відсотках рівня глюкози в крові у мишей ob/ob для контрольного носія PBS (зафарбовані кружки) та мутантів Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) (зафарбовані трикутники), Fc-(L15)-FGF21 (L98R, P171G, 182G, 183G) (SEQ ID NO:147) (порожні трикутники), Fc-(L15)-FGF21 (L98R, P171G, 182G) (SEQ ID NO:145) (зафарбовані ромби) і Fc-(L15)-FGF21 (L98R, P171G, 182P) (SEQ ID NO:143) (порожні ромби). На Фіг. 35 представлено графік, що показує зміну у відсотках рівня глюкози в крові у мишей ob/ob для контрольного носія PBS (порожні кружки) і мутантів Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) (зафарбовані квадрати), Fc-(L15)-FGF21 (L98R, P171G, Y179S) (SEQ ID NO:149) (порожні трикутники), Fc-(L15)-FGF21 (L98R, P171G, Y179A) (SEQ ID NO:153) (перевернені зафарбовані трикутники), c-(L15)-FGF21 (L98R, P171G, A180S) (SEQ ID NO:155) (порожні ромби) і Fc-(L15)-FGF21 (L98R, P171G, A180G) (SEQ ID NO:157) (зафарбовані кружки). На Фіг. 36 представлено графік, що показує зміну у відсотках рівня глюкози в крові у мишей ob/ob для контрольного носія PBS (зафарбовані кружки) і таких мутантів FGF21, як Fc-(L15)FGF21(L98R, P171G) (SEQ ID NO:43) (порожні квадрати), Fc-(L15)-FGF21 (L98R, P171G, Y179F) (SEQ ID NO:151) (зафарбовані трикутники) і c-(L15)-FGF21 (L98R, P171G, A180E) (SEQ ID NO:57) (порожні ромби). На Фіг. 37 представлена діаграма, що відображає схему шеститижневого дослідження з підвищенням дози, проведеного на мавпах резус. На зазначеній фігурі, напівтонові символи позначають узяття крові натще, а фактурні символи позначають узяття крові після годівлі. На Фігурах 38A-38D представлена серія графіків, що відображають рандомізацию мавп резус по профілях OGTT, AUC (площі під кривою) OGTT та масою тіла. Фіг. 38A відображає базовий рівень глюкози в OGTT1, при цьому зафарбовані квадрати відповідають групі A, зафарбовані кружки на суцільній лінії відповідають групі B, а порожні кружки на пунктирній лінії відповідають групі C перед розподілом випробуваних сполук і носія по групах. На Фіг. 38B відображено базовий рівень глюкози в OGTT2, при цьому зафарбовані квадрати відповідають групі A, зафарбовані кружки на суцільній лінії відповідають групі B, а порожні кружки на пунктирній лінії відповідають групі C перед розподілом випробуваних сполук і носія по групах. На Фіг. 38C показано базовий рівень глюкози в OGTT 1 і OGTT 2 у термінах AUC, при цьому фактурний стовпчик відповідає групі A, напівтоновий стовпчик відповідає групі B, а порожній стовпчик відповідає групі C. Фіг. 38D показує базову маса тіла, при цьому фактурний стовпчик відповідає групі A, напівтоновий стовпчик відповідає групі B, а порожній стовпчик відповідає групі C. На Фіг. 39 представлений графік, що показує відсоток зміни маси тіла щодо фонового носія, FGF21 (SEQ ID NO:4) і Fc-(L15)-FGF21 L98R, P171G) (SEQ ID NO:43) у мавп резус, при цьому напівтонові стовпчики 1 і 2 відповідають 1-му та 2-му тижням на низькій дозі, порожні стовпчики 3 і 4 відповідають 3-му та 4-му тижням на середній дозі, зафарбовані стовпчики 5 і 6 відповідають 5-му та 6-му тижням на високій дозі, а фактурні стовпчики 7, 8 і 9 відповідають періоду відмивання (з 7-го по 9-й тиждень). На Фіг. 40 представлено графік, що показує зміну у відсотках рівня інсуліну натще відносно базового рівня у мавп резус для носія, FGF21 (SEQ ID NO:4) та Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43), при цьому напівтонові стовпчики 1 і 2 відповідають 1-му та 2-му тижням на низькій дозі, порожні стовпчики 3 і 4 відповідають 3-мута 4-му тижням на середній дозі, зафарбовані стовпчики 5 і 6 відповідають 5-му та 6-му тижням на високій дозі, а фактурні стовпчики 7 і 8 відповідають 7-му і 8-му тижню в період відмивання. На Фіг. 41 представлений графік, що показує вплив носія, FGF21 (SEQ ID NO:4) і Fc-(L15)FGF21 (L98R, P171G) (SEQ ID NO:43) при введенні високої дози на рівень інсуліну в мавп резус після годівлі на 5-му та 6-му тижні дослідження, при цьому зафарбовані стовпчики відповідають 5-му тижню, а напівтонові стовпчики відповідають 6-му тижню. На Фіг. 42 представлено графік, що показує профілі глюкози в ході тесту OGTT5 (пероральний тест на толерантність до глюкози), проведеного наприкінці двотижневого лікування високими дозами Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43), при цьому зафарбовані кружки на суцільній лінії відповідають носію, порожні квадрати на пунктирній лінії відповідають FGF21, а зафарбовані трикутники на суцільній лінії відповідають Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43). На Фіг. 43 представлено графік, що показує профілі інсуліну в ході тесту OGTT5, проведеного наприкінці двотижневого лікування високими дозами Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43), при цьому зафарбовані кружки на суцільній лінії відповідають носію, порожні квадрати на пунктирній лінії відповідають FGF21, а зафарбовані трикутники на суцільній 6 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 лінії відповідають Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43). На Фіг. 44 представлено графік, що показує відсоток зміни від фонової лінії AUC3-5 глюкози в ході тесту OGTT, проведеному наприкінці кожного періоду введення доз (низької, середньої і високої дози) мавпам резус, при цьому порожні стовпчики відповідають AUC3, розрахованій за результатами вимірювань глюкози в OGTT3, зафарбовані стовпчики відповідають AUC4, розрахованій за результатами вимірювань глюкози в OGTT4, а напівтонові стовпчики відповідають AUC5, розрахованій за результатами вимірювань глюкози у OGTT5. На Фіг. 45 представлено графік, що показує вплив носія, FGF21 та Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) на зміну у відсотках рівня тригліцеридів у плазмі в порівнянні з базовим рівнем у кожній групі мавп резус, при цьому напівтонові стовпчики 1 і 2 відповідають 1-му та 2-му тижням на низькій дозі, порожні стовпчики 3 і 4 відповідають 3-му та 4-му тижням на середній дозі, зафарбовані стовпчики 5 і 6 відповідають 5-та 6-му тижням на високій дозі, а фактурні стовпчики 7, 8 і 9 відповідають періоду відмивання (з 7-го по 9-й тиждень). На Фіг. 46 представлено графік, що показує рівень тригліцеридів у плазмі після годівлі в кожній групі мавп резус за результатами вимірювань на п'ятому і шостому тижнях лікування носієм, FGF21 або Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) у високій дозі, при цьому напівтонові стовпчики відповідають 5-му тижню, а зафарбовані стовпчики відповідають 6-му тижню. Фіг. 47 являє собою графік, що показує рівень людського FGF21 в окремих мавп за результатами вимірювань перед початком введення доз, а також на 5-й, 12-й, 19-й та 26-й день при взятті зразків приблизно через 21 годину після кожної ін'єкції. На Фіг. 48 представлено графік, що показує індивідуальний рівень Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) у мавпи за результатами вимірювань перед початком введення доз, а також на 5-й, 12-й, 19-й та 26-й день при взятті зразків приблизно через 5 днів після кожної ін'єкції. На Фіг. 49 представлено графік, що показує середні концентрації FGF21 та Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) за результатами вимірювань у ході трьох тестів OGTT, проведених після введення кожної дози (низької, середньої і високої), при цьому напівтонові стовпчики відповідають OGTT3 з низькою дозою, зафарбовані стовпчики відповідають OGTT4 із середньою дозою, а порожні стовпчики відповідають OGTT5 з високою дозою. Фігура 50 являє собою амінокислотну послідовність Fc-(G4S)3-FGF21 (L98R, P171G, A180E) злитого білка (SEQ ID NO:47); де IgG1 Fc залишки (SEQ ID NO:11) зазначені жирним шрифтом, (G4S)3 лінкер (SEQ ID NO:31) зазначений курсивом, і крапкові мутації в FGF21 послідовності (SEQ ID NO:39) зазначені жирним шрифтом та підкреслені. Фігура 51 являє собою графік, де показана крива доза-відповідь проаналізованих сполук в аналізах Erk-люциферази, де були проаналізовані Fc-(G4S)3-FGF21 (L98R, P171G, A180E) (SEQ ID NO:47), Fc-(L15)-FGF21 (L98R, P171G, A180E) (SEQ ID NO:57), дикого типу FGF21, та Fc злиття з FGF21 дикого типу. Фігура 52 являє собою графік, де показані результати, одержані в аналізі зв'язування Біакор рівноваги розчину Fc-(G4S)3-FGF21 (L98R, P171G, A180E) (SEQ ID NO:47) і Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) для людини (праворуч) і β-Клото яванських макак (ліворуч). Фігура 53 являє собою пари графіків, де показано криву доза-відповідь Fc-(G4S)3-FGF21 (L98R, P171G, A180E) (SEQ ID NO:47) у мишей db/db після однієї ін'єкції; Фігура 53A показує рівні глюкози в крові у мишей db/db у різні моменти часу після ін'єкції носія або Fc-(G4S)3-FGF21 (L98R, P171G, A180E), у той час як Фігура 53B показує вплив Fc-(G4S)3-FGF21 (L98R, P171G, A180E) на масу тіла після однієї ін'єкції у мишей db/db. Фігура 54 схематично графічно представляє дослідження впливу частоти доз Fc-(G4S)3FGF21 (L98R, P171G, A180E) (SEQ ID NO:47) та Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) у DIO мишей. Фігура 55 являє собою графік, на якому показані профілі GTT мишей, яких лікували носієм, Fc-(G4S)3-FGF21 (L98R, P171G, A180E) (SEQ ID NO:47) або Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) при різних частотах введення доз. Фігура 56 являє собою графік, на якому показано зміну маси тіла в порівнянні з фоновою лінією (день 0) у мишей, яких лікували носієм, Fc-(G4S)3-FGF21 (L98R, P171G, A180E) (SEQ ID NO:47) або Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) при різних частотах введення доз. Фігура 57 являє собою графік, на якому показані результати дослідження in vitro гідрогелів, що містять FGF21 (L98R, P171G)) (SEQ ID NO:37) FGF21 мутант. Фігура 58 являє собою графік, на якому показано вплив на рівні глюкози в крові 8-тижневих мишей db/db, яким давали дозування різних композицій гідрогелю. Фігура 59 являє собою графік, на якому показано вплив на рівні глюкози в крові 8-тижневих 7 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 мишей db/db, яким давали дозування різних композицій гідрогелю. Фігура 60 являє собою графік, на якому показано вплив на рівні глюкози в крові 8-тижневих мишей db/B6, яким давали дозування різних композицій гідрогелю; зафарбовані кружки представляють мишей, яким давали дози гідрогелевого контролю, зафарбовані квадрати представляють мишей, яким давали дози FGF21 (L98R, P171G) (SEQ ID NO:37) у гідрогелі при 10 мг/кг, зафарбовані трикутники представляють мишей, яким давали дози FGF21 (L98R, P171G) у гідрогелі при 30 мг/кг, і перевернені трикутники представляють мишей, яким давали дози Fc-(L15)-FGF21 (L98R, P171G, A180E) (SEQ ID NO:57) окремо. Фігура 61 являє собою графік, на якому показано вплив на рівні глюкози в крові 8-тижневих мишей db/B6, яким давали дози різних гідрогелевих композицій; зафарбовані кружки представляють мишей, яким давали дози з гідрогелевим контролем, зафарбовані квадрати представляють мишей, яким давали дози FGF21 (L98R, P171G) (SEQ ID NO:37) у гідрогелі при 10 мг/кг, зафарбовані трикутники представляють мишей, яким давали дози FGF21 (L98R, P171G) у гідрогелі при 30 мг/кг, і перевернені трикутники представляють мишей, яким давали дози Fc-(L15)-FGF21 (L98R, P171G, A180E) (SEQ ID NO:57) окремо. Фігура 62 являє собою графік, на якому показано вплив на масу тіла 8-тижневих мишей db/B6, яким давали різні гідрогелеві композиції; зафарбовані кружки представляють мишей, яким давали дози гідрогелевого контролю, зафарбовані квадрати представляють мишей, яким давали дози FGF21 (L98R, P171G) (SEQ ID NO:37) у гідрогелі при 10 мг/кг, зафарбовані трикутники представляють мишей, яким давали дози FGF21 (L98R, P171G) у гідрогелі при 30 мг/кг, і перевернені трикутники представляють мишей, яким давали дози Fc-(L15)-FGF21 (L98R, P171G, A180E) (SEQ ID NO:57) окремо. Фігура 63 являє собою графік, на якому показаний відсоток зміни маси 8-тижневих мишей db/B6, яким давали дози різних гідрогелевих композицій; зафарбовані кружки представляють мишей, яким давали дози з гідрогелевим контролем, зафарбовані квадрати представляють мишей, яким давали дози FGF21 (L98R, P171G) (SEQ ID NO:37) у гідрогелі при 10 мг/кг, зафарбовані трикутники представляють мишей, яким давали дози FGF21 (L98R, P171G) у гідрогелі при 30 мг/кг, і перевернені трикутники представляють мишей, яким давали дози Fc(L15)-FGF21 (L98R, P171G, A180E) (SEQ ID NO:57) окремо. Фігура 64 являє собою діаграму, на якій графічно відображено план клінічного дослідження для дев'ятитижневого дослідження з ескалацією дози, що виконували для яванських макак з погіршеною толерантністю до глюкози (IGT). Фігура 65 являє собою графік, на якому відображено вплив носія, Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) і Fc-(G4S)3-FGF21 (L98R, P171G, A180E) (SEQ ID NO:47) на AM поглинання їжі досліджуваних яванських макак IGT. Фігура 66 являє собою графік, на якому відображено вплив носія, Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) та Fc-(G4S)3-FGF21 (L98R, P171G, A180E) (SEQ ID NO:47) на поглинання фруктів досліджуваних яванських макак IGT. Фігура 67 являє собою графік, на якому відображено вплив носія, Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) і Fc-(G4S)3-FGF21 (L98R, P171G, A180E) (SEQ ID NO:47) на PM поглинання їжі досліджуваних яванських макак IGT. Фігура 68 являє собою графік, на якому відображено вплив носія, Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) і Fc-(G4S)3-FGF21 (L98R, P171G, A180E) (SEQ ID NO:47) на масу тіла досліджуваних яванських макак IGT. Фігура 69 являє собою графік, на якому відображено вплив носія, Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) і Fc-(G4S)3-FGF21 (L98R, P171G, A180E) (SEQ ID NO:47) на індекс маси тіла досліджуваних яванських макак IGT. Фігура 70 являє собою графік, на якому відображено вплив носія, Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) і Fc-(G4S)3-FGF21 (L98R, P171G, A180E) (SEQ ID NO:47) на товщину шкірної складки досліджуваних яванських макак IGT. Фігура 71 являє собою графік, на якому відображено вплив носія, Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) і Fc-(G4S)3-FGF21 (L98R, P171G, A180E) (SEQ ID NO:47) на окружність живота досліджуваних яванських макак IGT. Фігура 72 являє собою графік, на якому відображено вплив носія, Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) і Fc-(G4S)3-FGF21 (L98R, P171G, A180E) (SEQ ID NO:47) на рівні глюкози в плазмі досліджуваних яванських макак IGT. Фігура 73 являє собою графік, на якому відображено вплив носія, Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) і Fc-(G4S)3-FGF21 (L98R, P171G, A180E) (SEQ ID NO:47) на толерантність до глюкози досліджуваних яванських макак IGT. Фігура 74 являє собою графік, на якому відображено вплив носія, Fc-(L15)-FGF21 (L98R, 8 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 P171G) (SEQ ID NO:43) і Fc-(G4S)3-FGF21 (L98R, P171G, A180E) (SEQ ID NO:47) на рівні тригліцеридів у плазмі досліджуваних яванських макак IGT. Фігура 75 являє собою графік, на якому відображено вплив носія, Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) і Fc-(G4S)3-FGF21 (L98R, P171G, A180E) (SEQ ID NO:47) на рівні загального холестерину в плазмі досліджуваних яванських макак IGT. Фігура 76 являє собою графік, на якому відображено вплив носія, Fc-(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) і Fc-(G4S)3-FGF21 (L98R, P171G, A180E) (SEQ ID NO:47) на рівні холестерину ЛПВЩ у плазмі досліджуваних яванських макак IGT. Фігура 77 являє собою серію слідових кількостей відповідно до мас-спектрометрії МАЛДІ, де показані зміни, що спостерігаються, Fc-(L15)-FGF21 (L98R, P171G) (ліва панель, SEQ ID NO:43) і Fc-(L15)-FGF21 (L98R, P171G, A180E) (права панель, SEQ ID NO:57) у різні моменти часу протягом 168-годинного періоду. Фігура 78 являє собою графік, на якому показано відносну поширеність (%) повноразмірного C-кінцевого пептиду в порівнянні з загальною кількістю фрагментів C-кінцевого пептиду, одержаних як з Fc-(L15)-FGF21 (L98R, P171G), так і з Fc-(L15)-FGF21 (L98R, P171G, A180E), відповідно до аналізів моніторингу множинних реакцій РХ/МС/МС після Asp-N дигестії. Фігура 79 являє собою графік, на якому показані результати твердофазного імуноферментного аналізу (ELISA) для концентрації в плазмі інтактного повноразмірного Fc(L15)-FGF21 (L98R, P171G) (SEQ ID NO:43) та Fc-(L15)-FGF21 (L98R, P171G, A180E) (SEQ ID NO:57) протягом 240-годинного періоду після внутрішньовенної ін'єкції у мишей. Фігура 80 являє собою графік, на якому показані результати аналізу ELK-люциферазної активності, виконаного на негативному контролі, людських FGF21 (SEQ ID NO:4) і FGF21 мутантів глікозилування FGF21 (Y179N, S181T) (SEQ ID NO:161), FGF21 Y179N (SEQ ID NO:163) і FGF21 P124S (SEQ ID NO:165). ДЕТАЛЬНИЙ ОПИС ВИНАХОДУ Білок людини FGF21, що має поліпшені властивості, зокрема, подовжений період напіввиведення та/або зменшену агрегацією, може бути виготовлений способами, розкритими в даному описі і стандартними способами молекулярної біології. Факультативно можна додатково збільшити період напіввиведення, гібридизуючи антитіло або його частину з N-кінцевою або Cкінцевою ділянкою послідовності FGF21 дикого типу. Також можна додатково збільшити період напіввиведення або зменшити агрегацію білка FGF21 дикого типу, вводячи в цей білок амінокислотні заміщення. Такі модифіковані білки згадуються в даному документі як мутанти або мутанти FGF21, та формують варіанти здійснення даного винаходу. Способи рекомбінантних нуклеїнових кислот, що згадуються в даному описі, включаючи приклади, у цілому являють собою способи, сформульовані в опублікованих джерелах Sambrook et al., Molecular Cloning: A Laboratory Manual (Cold Spring Harbor Laboratory Press, 1989) або Current Protocols in Molecular Biology (Ausubel et al., eds., Green Publishers Inc. and Wiley and Sons 1994), причому обидва зазначені джерела включені в даний опис як посилання для будь-яких цілей. 1. Загальні терміни і визначення Термін "виділена молекула нуклеїнової кислоти" відноситься до молекули нуклеїнової кислоти, представленої в даній заявці, що (1) була відділена, щонайменше, приблизно від 50 відсотків білків, ліпідів, або вуглеводів інших матеріалів, разом з якими вона зустрічається в природі, коли тотальну нуклеїнову кислоту виділяють із клітин-джерел, (2) не зчеплена з усім полінуклеотидом або частиною полінуклеотида, з якими "виділена молекула нуклеїнової кислоти" зчеплена в природі, (3) функціонально зв'язана з полінуклеотидом, з яким вона не зв'язана в природі, або (4) не зустрічається в природі як частина більшої полінуклеотидної послідовності. Переважним є, щоб виділена молекула нуклеїнової кислоти була, істотно, вільна від будь-яких інших забруднюючих молекул нуклеїнової кислоти або від інших забруднень, що виявляються в природному оточенні, і які могли б перешкодити її застосуванню у виробленні поліпептиду або її терапевтичному, діагностичному, профілактичному застосуванню або застосуванню в науково-дослідних цілях. Термін "вектор" вживається для позначення будь-якої молекули (наприклад, нуклеїнової кислоти, плазміди або вірусу), використовуваної для переносу інформації, що кодує, у клітинухазяїн. Термін "вектор експресії" відноситься до вектора, що придатний для трансформації клітинихазяїна і містить послідовності нуклеїнової кислоти, що направляють та/або контролюють експресію вставлених гетерологічних послідовностей нуклеїнової кислоти. Експресія включає, але не обмежуючись цим, такі процеси, як транскрипція, трансляція і сплайсинг РНК, якщо присутні інтрони. 9 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 Термін "функціонально зв'язаний(а, е)" вживається в даному документі для позначення компонування фланкуючих послідовностей, при цьому фланкуючі послідовності, описані таким чином, сконфігуровані або зібрані таким чином, що виконують свою звичайну функцію. Отже, фланкуюча послідовність, функціонально зв'язана з послідовністю, що кодує, може бути здатна викликати реплікацію, транскрипцію та/або трансляцію послідовності, що кодує. Наприклад, послідовність, що кодує, функціонально зв'язана з промотором, якщо промотор здатний керувати транскрипцією цієї послідовності, що кодує. Фланкуюча послідовність не обов'язково повинна примикати до послідовності, що кодує, доти, поки вона правильно функціонує. Так, наприклад, між промоторною послідовністю і послідовністю, що кодує, можуть бути вставлені проміжні не трансльовані, але такі, що можуть бути транскрибовані, послідовності, при цьому промоторна послідовність, як і раніше, може вважатися "функціонально зв'язаною" з послідовністю, що кодує. Термін "клітина-хазяїн" вживається для позначення клітини, що була трансформована або здатна до трансформації послідовністю нуклеїнової кислоти, такої, як нуклеїнова кислота, представлена в даній заявці, після чого вона експресує ген, що представляє інтерес. Цей термін включає потомство батьківської клітини незалежно від того, або воно ідентично або не ідентично первісному батьку за морфологією або генетичною структурою доти, поки клітина експресує обраний ген. Термін "виділений поліпептид" відноситься до поліпептиду, представленому в даній заявці, який (1) був відділений, щонайменше, приблизно, від 50 відсотків полінуклеотидів, ліпідів, вуглеводів або інших матеріалів, разом з якими він зустрічається в природі, коли його виділяють із клітин-джерел, (2) не зв'язаний (за допомогою ковалентної або нековалентної взаємодії) з усім поліпептидом або частиною поліпептиду, з якими "виділений поліпептид" зв'язаний у природі, (3) функціонально зв'язаний (за допомогою ковалентної або нековалентної взаємодії) з поліпептидом, з яким він не зв'язаний у природі, або (4) не зустрічається в природі. Переважним є, щоб виділений поліпептид був істотно вільний від будь-яких інших забруднюючих поліпептидів або від інших забруднень, що виявляються в природному оточенні, і які могли б перешкодити його застосуванню в терапевтичних, діагностичних, профілактичних або науководослідних цілях. Термін "що зустрічається в природі" стосовно до таких біологічних матеріалів, як молекули нуклеїнових кислот, поліпептиди, клітини-хазяєва і т.п., відноситься до матеріалів, що зустрічаються в природі і не піддаються маніпуляціям з боку людини. Подібним чином, термін "що не зустрічається в природі" при використанні в даному документі відноситься до матеріалу, що не зустрічається в природі або був структурно модифікований або синтезований людиною. При використанні по відношенню до нуклеотидів термін "що зустрічається в природі" відноситься до таких основ, як аденін (A), цитозін (З), гуанін (G), тимін (T) та урацил (U). При використанні по відношенню до амінокислот термін "що зустрічається в природі" відноситься до таких 20 амінокислот: аланін (A), цистеїн (C), аспарагінова кислота (D), глутамінова кислота (E), фенілаланін (F), гліцин (G), гістидин (H), ізолейцин (I), лізин (K), лейцин (L), метіонін (M), аспарагін (N), пролін (P), глутамін (Q), аргінін (R), серин (S), треонін (T), валін (V), триптофан (W) та тирозин (Y). Термін "поліпептид FGF21" відноситься до поліпептиду дикого типу, що зустрічається в природі, який експресується у людини. З метою цього розкриття винаходу термін "поліпептид FGF21" може використовуватися взаємозамінно з будь-яким повноразмірним поліпептидом FGF21, наприклад, SEQ ID NOs: 2 та 6, що складаються з 209 амінокислотних залишків, і які кодуються нуклеотидними послідовностями SEQ ID NOs: 1 та 5; відповідно, будь-яка зріла форма поліпептиду, SEQ ID NOs: 4 та 8, що складаються з 181 амінокислотних залишків, і які кодуються нуклеотидними послідовностями SEQ ID NOs: 3 та 7, та в який 28 амінокислотних залишків на аміно-кінці повноразмірного поліпептиду FGF21 (наприклад, які складають сигнальний пептид) були видалені. Повнорозмірні і зрілі FGF21 поліпептиди можуть, але не обов'язково, містити аміно-кінцевий метіонін, що вводять за допомогою методів інженерії або в результаті процесу бактеріальної експресії. Терміни "мутант поліпептиду FGF21" та "мутант FGF21" можуть бути використані як взаємозамінні і відносяться до поліпептиду FGF21, у якому природна амінокислотна послідовність FGF21 (наприклад, SEQ ID NOs:2, 4, 6, або 8) була модифікована. Такі модифікації включають, але не обмежуючись цим, одне або більше амінокислотних заміщень, включаючи заміщення на аналоги амінокислот, що не зустрічаються в природі, і аналоги амінокислот, що зустрічаються в природі, і усічення. Таким чином, мутанти поліпептиду FGF21 включають, але не обмежуючись цим, сайт-специфічні мутанти FGF21, усічені поліпептиди FGF21, мутанти FGF21, стійкі до протеолізу, мутанти FGF21 зі зниженою агрегацією, 10 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 комбінаторні мутанти FGF21 і гібридні білки FGF21, як описано в даному документі. З метою ідентифікації специфічних усічень і амінокислотних заміщень у мутантах FGF21 за даним винаходом нумерація усічених або мутованих амінокислотних залишків відповідає нумерації в зрілому поліпептиді FGF21, що складається з 181 амінокислотних залишків. FGF21 мутанти можуть, але необов'язково, містити аміно-кінцевий метіонін, що може бути введений за допомогою методів інженерії або в результаті процесу бактеріальної експресії. В інших варіантах здійснення даного винаходу мутант поліпептиду FGF21 включає амінокислотну послідовність, яка, щонайменше, на 85 відсотків ідентична мутантній FGF21’s амінокислотній послідовності, але в якій специфічні залишки, що надають мутантному поліпептиду FGF21 бажані властивості, наприклад, стійкість до протеолізу, збільшений період напіввиведення, знижену агрегацію або їх комбінації, не були додатково модифіковані. Іншими словами, за винятком тих залишків у мутантній послідовності FGF21, які були модифіковані для надання поліпептиду стійкості до протеолізу, зниженій здатності до агрегації інших властивостей, модифікованими можуть бути приблизно 15 відсотків всіх або інших амінокислотних залишків у мутантній послідовності FGF21. Наприклад, у мутанті FGF21 Q173E, можуть бути модифіковані до 15 відсотків всіх інших амінокислотних залишків додатково до залишку глутамінової кислоти, що був заміщений на глутамін у положенні 173. В інших варіантах здійснення винаходу мутантний поліпептид FGF21 включає амінокислотну послідовність, яка, щонайменше, приблизно, на 90 відсотків, або приблизно, на 95, 96, 97, 98 або 99 відсотків ідентична мутантній FGF21’s амінокислотній послідовності, але в якій специфічні залишки, що надають мутантному поліпептиду FGF21 властивості стійкості до протеолізу або зниженій здатності до агрегації, не були додатково модифіковані. Такі мутанти поліпептиду FGF21 мають, щонайменше, один вид активності поліпептиду FGF21 дикого типу. Даний винахід також охоплює молекулу нуклеїнової кислоти, що кодує мутант поліпептиду FGF21, що включає амінокислотну послідовність, яка, щонайменше, приблизно, на 85 відсотків ідентична мутантній FGF21’s амінокислотній послідовності, але в який специфічні залишки, що надають мутантному поліпептиду FGF21 бажані властивості, наприклад, стійкість до протеолізу, збільшений період напіввиведення, знижену агрегацію або їх комбінації, не були додатково модифіковані. Інакше кажучи, за винятком тих залишків у мутантній послідовності FGF21, які були модифіковані для надання поліпептиду стійкості до протеолізу, зниженій здатності до агрегації або інших властивостей, модифікованими можуть бути приблизно 15 відсотків всіх інших амінокислотних залишків у мутантній послідовності FGF21. Наприклад, у мутанті FGF21 Q173E, можуть бути модифіковані до 15 відсотків всіх інших амінокислотних залишків додатково до залишку глутамінової кислоти, що був заміщений на глутамін у положенні 173. Далі, даний винахід охоплює молекулу нуклеїнової кислоти, що включає нуклеотидну послідовність, яка, щонайменше, приблизно, на 90 відсотків, або приблизно, на 95, 96, 97, 98 або 99 відсотків ідентична амінокислотній послідовності, яка кодує FGF21 мутант, але в який нуклеотиди, що кодують амінокислотні залишки, які надають мутантному поліпептиду FGF21, який кодують, властивості стійкості до протеолізу або зниженій здатності до агрегації, не були додатково модифіковані. Такі молекули нуклеїнових кислот кодують мутанти FGF21, що мають, щонайменше, один вид активності поліпептиду FGF21 дикого типу. Термін "біологічно активний мутант поліпептиду FGF21" відноситься до будь-якого мутантного поліпептиду FGF21, описаного в даному документі, що має активність поліпептиду FGF21 дикого типу, зокрема, здатність знижувати рівень глюкози, інсуліну, тригліцеридів або холестерину в крові, зменшувати масу тіла і поліпшувати толерантність до глюкози, споживання енергії або чутливість до інсуліну незалежно від кількості модифікацій, введених у мутант поліпептиду FGF21. Мутантні поліпептиди FGF21, що мають деякою мірою знижений рівень активності FGF21 у порівнянні з поліпептидом FGF21 дикого типу, можуть, проте, вважатися біологічно активними мутантами поліпептиду FGF21. Кожний з термінів "ефективна кількість" і "терапевтично ефективна кількість" відноситься до мутантного поліпептиду FGF21, застосовуваному для підтримки рівня, що спостерігається, одного або більш видів біологічної активності поліпептиду FGF21 дикого типу, зокрема, здатності знижувати рівень глюкози, інсуліну, тригліцеридів або холестерину в крові, знижувати масу тіла або поліпшувати толерантність до глюкози, споживання енергії або чутливість до інсуліну. Термін "фармацевтично прийнятний носій" або "фізіологічно прийнятний носій" при використанні в даному документі відноситься до одного або більш рецептурних агентів, придатних для здійснення або покращення доставки мутантного поліпептиду FGF21 в організм людського або нелюдського суб'єкта. Термін включає будь-який та всі розчинники, дисперсійні 11 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 середовища, покриття, антибактеріальні і протигрибкові агенти, ізотонічні агенти та агенти, що сповільнюють поглинання, , та інш., що є фізіологічно несумісними. Приклади фармацевтично прийнятних носіїв включають один або більше з води, сольового розчину, фосфатного сольового буфера, декстрози, гліцерину, етанолу та інш., а також їх комбінації. У деяких випадках, кращим буде включення ізотонічних агентів, наприклад, цукрів, поліспиртів, таких, як манітол, сорбітол, або хлорид натрію, у фармацевтичну композицію. Фармацевтично прийнятні речовини, наприклад, що змочують, або незначні кількості допоміжних речовин, наприклад, агентів, що змочують, або агентів, що емульгують, консерватори або буфери, що збільшують термін придатності поліпептидного мутанта FGF21, можуть також діяти як носії, або утворювати компонент носія. Термін "антиген" відноситься до молекули або частини молекули, що здатні зв'язуватися з антитілом і, крім того, їх можна використовувати на тваринах для вироблення антитіл, що здатні зв'язувати епітоп антигена. Антиген може мати один або більше епітопів. Термін "нативний Fc" відноситься до молекули або послідовності, що включає послідовність неантигензвязуючого фрагмента та отриманої в результаті розщеплення цілого антитіла або виробленої іншими засобами, як у мономерной, так і в мультимерній формі, яка може містити шарнірну ділянку. Первісне імуноглобулінове джерело нативного Fc переважно, але не обов'язково, має людське походження і являє собою будь-який з імуноглобулінів, хоча більш кращими є IgG1 та IgG1. Також може бути використаний IgG4. Нативні молекули Fc складаються з мономерних поліпептидів, що можуть бути з'єднані в димерні або мультимерні форми за допомогою ковалентної (тобто, за типом дисульфідних зв'язків) і нековалентної асоціації. Кількість міжмолекулярних дисульфідних зв'язків між мономерними субодиницями нативних молекул Fc варіюється від 1 до 4 у залежності від класу (наприклад, IgG, IgA та IgE) або підкласу (наприклад, IgG1, IgG2, IgG3, IgG4, IgG1 та IgGA2). Один із прикладів нативного Fc являє собою дисульфидно зв'язаний димер, отриманий у результаті папаїнового розщеплення IgG (див. Ellison et al., 1982, Nucleic Acids Res. 10: 4071-9). Термін "нативний Fc" при використанні в даному документі узагальнює мономерні, димерні і мультимерні форми. Приклад поліпептидної послідовності Fc представлений у SEQ ID NO: 11, що отриманий з людської молекули IgG1. Нативний Fc може, але не обов'язково, містити аміно-кінцевий метіонін, що може бути введений за допомогою методів інженерії або в результаті процесу бактеріальної експресії; такі Fc продовжують розглядати як "нативні Fc" молекули. Термін "варіант Fc" відноситься до молекули або послідовності, що модифіковані з нативного Fc, але ще включають сайт зв'язування для рецептора утилізації, FcRn (рецептор Fc немовлят). Міжнародні патентні публікації №№ WO 97/34631 та WO 96/32478 описують типові варіанти Fc, а також їх взаємодію з рецептором утилізації, у зв'язку з чим зазначені публікації включені в цей документ як посилання. Таким чином, термін "варіант Fc" може включати молекулу або послідовність, що гуманізовані з нативного Fc нелюдського походження. Крім того, нативний Fc включає ділянки, які можна видалити, оскільки вони забезпечують структурні ознаки біологічної активності, що не є необхідними для гібридних молекул мутантів FGF21, що відповідають даному винаходу. Таким чином, термін "варіант Fc" включає молекулу або послідовність, у яких один або більш сайтів або залишків нативного Fc втрачені або модифіковані, що впливає на: (1) утворення дисульфідних зв'язків, (2) несумісність з обраної клітиною-хазяїном, (3) N-кінцеву гетерогенність при експресії в обраній клітині-хазяїні, (4) гліколизування, (5) взаємодія з комплементом, (6) зв'язування з рецептором Fc, іншим, ніж рецептор утилізації, або (7) антитілозалежну клітинну цитотоксичність (ADCC). Варіанти Fc більш детально описані в даному документі нижче. Варіант Fc може, але не обов'язково, містити аміно-кінцевий метіонін, що може бути введений методами інженерії або в результаті бактеріальної експресії; такі Fc молекули продовжують розглядати як "Fc варіанти.” Термін "домен Fc" охоплює нативний Fc, варіанти Fc і їх послідовності відповідно до наведених вище визначень. Як у відношенні варіантів Fc, так і у відношенні нативних молекул Fc, термін " домен Fc" включає молекули в мономерній або мультимерній формі, одержані в результаті розщеплення цілого антитіла або вироблені іншими засобами. У деяких варіантах здійснення даного винаходу домен Fc може бути з'єднаний з FGF21 або мутантом FGF21 (включаючи усічену форму FGF21 або мутанта FGF21) за допомогою, наприклад, ковалентного зв'язку між доменом Fc і послідовністю FGF21. Такі складені білки можуть утворювати мультимери через асоціацію доменів Fc, при цьому як складені білки, так і їх мультимери є аспектом даного винаходу. Fc домен може, але необов'язково, містити аміно-кінцевий метіонін, що може бути введений методами інженерії або в результаті процесу бактеріальної експресії. 2. Мутанти FGF21 Термін " мутант FGF21" відноситься до мутантного поліпептиду FGF21, що має 12 UA 107458 C2 5 10 15 20 25 амінокислотну послідовність, яка відрізняється від амінокислотної послідовності природного поліпептиду FGF21, наприклад, SEQ ID NOs: 2, 4, 6 або 8, однієї або більш амінокислот. Мутанти FGF21 можна створювати, вводячи одне або більше амінокислотних заміщень, консервативні або не консервативні, і використовуючи амінокислоти, що як зустрічаються, так і не зустрічаються в природі, в специфічних положеннях поліпептиду FGF21. "Консервативне амінокислотне заміщення" може включати заміщення нативного амінокислотного залишку (тобто, залишку, що виявляється в даному положенні поліпептидної послідовності FGF21 дикого типу) на ненативний залишок (т.зв. залишок, що не виявляється в даному положенні поліпептидної послідовності FGF21 дикого типу), при цьому не відбувається жодних впливів, або відбуваються дуже незначні впливи на полярність або заряд амінокислотного залишку в даному положенні. Консервативні амінокислотні заміщення також охоплюють амінокислотні залишки, які не зустрічаються в природі, що зазвичай вбудовуються за допомогою хімічного пептидного синтезу, а не синтезу в біологічних системах. Вони включають пептидоміметики та інші реверсовані або інвертовані форми амінокислотних компонентів. Амінокислотні залишки, що зустрічаються в природі, можна підрозділити на класи, ґрунтуючись на загальних властивостях бічного ланцюга: (1) гідрофобні: норлейцин (norleucine), Met, Ala, Va, Leu, Ile; (2) нейтральні гідрофільні: Cys, Ser, Thr; (3) кислотні: Asp, GIu; (4) основні: Asn, GIn, His, Lys, Arg; (5) залишки, що впливають на орієнтацію ланцюга: GIy, Pro; та (6) ароматичні: Trp, Tyr, Phe. Консервативні заміщення можуть включати заміну члена одного з цих класів на інший член того ж класу. Неконсервативні заміщення можуть включати заміну члена одного з цих класів на інший член іншого класу. Бажані амінокислотні заміщення (як консервативні, так і неконсервативні) можуть визначити компетентні фахівці в даній галузі в той час, коли такі заміни знадобляться. Типовий (але не обмежуючий) список амінокислотних заміщень представлений у таблиці 1. 30 Таблиця 1 Амінокислотні заміщення Первісний залишок Ala Arg Asn Asp Cys Gln Glu Gly His Ile Leu Lys Met Phe Pro Ser Thr Trp Tyr Val Типові заміщення Val, Leu, Ile Lys, Gln, Asn Gln Glu Ser, Ala Asn Asp Pro, Ala Asn, Gln, Lys, Arg Leu, Val, Met, Ala, Phe Ile, Val, Met, Ala, Phe Arg, Gln, Asn Leu, Phe, Ile Leu, Val, Ile, Ala, Tyr Ala Thr, Ala, Cys Ser Tyr, Phe Trp, Phe, Thr, Ser Ile, Met, Leu, Phe, Ala 3. Усічені поліпептиди FGF21 Один з варіантів здійснення даного винаходу відноситься до усічених форм зрілого поліпептиду FGF21 або мутанта FGF21. Цей варіант здійснення даного винаходу виник у зв'язку 13 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 зі спробою виявити усічені поліпептиди FGF21, що здатні забезпечувати активність, рівну активності не усічених форм зрілого поліпептиду FGF21, а в деяких випадках таку, що більша за неї. При використанні в даному описі термін "усічений поліпептид FGF21" відноситься до поліпептиду FGF21, у якого були вилучені амінокислотні залишки з амінокінцевої (чи N-кінцевої ділянки) поліпептиду FGF21, були вилучені амінокислотні залишки з карбоксикінцевої (чи Cкінцевого) ділянки поліпептиду FGF21 або були вилучені амінокислотні залишки як з амінокінцевої, так і з карбоксикінцевої ділянок поліпептиду FGF21. Різні усічення, розкриті в даному документі, були підготовлені так, як це викладено в Прикладах 3 і 6. Активність поліпептидів FGF21, усічених на N-кінці, і поліпептидів FGF21, усічених на C-кінці, можна оцінювати, застосовуючи аналіз на ELK-люциферазу in vitro, як це описано в прикладі 4. Специфічні подробиці аналізів in vitro, які можна застосовувати для дослідження активності усічених поліпептидів FGF21, можна знайти в прикладі 4. Активність усічених поліпептидів FGF21 за даним винаходом також можна оцінювати в аналізі in vivo, такому, як аналіз на мишах db/db або на мишах ob/ob, описаний у прикладах 5 і 7. У цілому, для оцінки активності усіченого поліпептиду FGF21 in vivo цей усічений поліпептид можна ввести тварині, використовуваній для тестування, внутрішньочеревно. Після необхідного періоду інкубації (наприклад, однієї години або більше), можна взяти зразок крові і вимірити рівень глюкози. Специфічні подробиці аналізів in vivo, які можна застосовувати для дослідження активності усічених поліпептидів FGF21, можна знайти в прикладах 5 і 7. a. N-кінцеві усічення У деяких варіантах здійснення даного винаходу N-кінцеві усічення включають 1, 2, 3, 4, 5, 6, 7 або 8 амінокислотних залишків з N-кінцевої ділянки зрілого поліпептиду FGF21 або мутанта FGF21. Як продемонстровано в прикладі 5 і на фігурі 3, усічені поліпептиди FGF21, що мають кінцеві усічення довжиною менше 9 амінокислотних залишків, зберігають здатність зрілого поліпептиду FGF21 знижувати рівень глюкози в крові суб'єкта. Відповідно до цього, у специфічних варіантах здійснення даний винахід охоплює усічені форми зрілого поліпептиду FGF21 або мутантних поліпептидів FGF21, що мають N- кінцеві усічення 1, 2, 3, 4, 5, 6, 7 або 8 амінокислотних залишків. b. C-кінцеві усічення У деяких варіантах здійснення даного винаходу C-кінцеві усічення включають 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 або 12 амінокислотних залишків з C-кінцевої ділянки зрілого поліпептиду FGF21. Як продемонстровано в прикладі 4 і на фігурі 1B, усічені поліпептиди FGF21, що мають Cкінцеві усічення довжиною менше 13 амінокислотних залишків, демонструють ефективність на рівні, щонайменше, 50 % ефективності FGF21 дикого типу в аналізі на ELK-люциферазу in vitro, що вказує на те, що ці мутанти FGF21 зберігають здатність зрілого поліпептиду FGF21 знижувати рівень глюкози в крові суб'єкта. Відповідно до цього, у специфічних варіантах здійснення даний винахід охоплює усічені форми зрілого поліпептиду FGF21 або мутантних поліпептидів FGF21, що мають C- кінцеві усічення 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 або 12 амінокислотних залишків. c. N-кінцеві і C-кінцеві усічення З деяких варіантах здійснення даного винаходу усічені поліпептиди FGF21 можуть мати скобміновані N-кінцеві і C-кінцеві усічення. Усічені поліпептиди FGF21, що мають сполучення Nкінцевих і C-кінцевих усікань, зберігають активність відповідних усічених поліпептидів FGF21, що мають тільки N- кінцеві або C-кінцеві усічення. Інакше кажучи, усічені поліпептиди FGF21, що мають як N-кінцеві усічення довжиною менше 9 амінокислотних залишків, так і C-кінцеві усічення довжиною менше 13 амінокислотних залишків, володіють такою ж або навіть більшою біологічною активністю, наприклад, за зниженню рівня глюкози в крові, ніж усічені поліпептиди FGF21, що мають тільки N-кінцеві усічення довжиною менше 9 амінокислотних залишків або Cкінцеві усічення довжиною менше 13 амінокислотних залишків. Відповідно до цього, у специфічних варіантах здійснення даний винахід охоплює усічені форми зрілого поліпептиду FGF21 або мутантних поліпептидів FGF21, що мають N-кінцеві усічення 1, 2, 3, 4, 5, 6, 7 або 8 амінокислотних залишків і C-кінцеві усічення 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 або 12 амінокислотних залишків. Як і у відношенні всіх мутантів FGF21 за даним винаходом, усічені поліпептиди FGF21 і мутанти FGF21 можуть у необов'язковому порядку включати амінокінцевий залишок метіоніну, який можна ввести за допомогою спрямованої мутації або в результаті процесу бактеріальної експресії. Усічені поліпептиди FGF21 за даним винаходом можна виготовити так, як це описано в прикладах 3 і 6. Середній фахівець у даній галузі, знайомий зі стандартними методиками 14 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 молекулярної біології, зможе використати свої знання разом з відомостями, представленими в даному розкритті винаходу, щоб виготовляти і застосовувати усічені поліпептиди FGF21 за даним винаходом. Для рекомбінантної ДНК, олигонуклеотидного синтезу, тканинної культури і трансформації можна використовувати стандартні методики (наприклад, електропорацію, ліпофекцію). Див., наприклад, публікацію Sambrook et al., Molecular Cloning: A Laboratory Manual, вище, що включена в цей документ як посилання для будь-яких цілей. Ферментативні реакції і методики очищення можна проводити у відповідності зі специфікаціями виробників, як це загальноприйнято в даній галузі техніки або описано у даному документі. Якщо не наведені спеціальні визначення, номенклатура, використовувана в даному документі стосовно лабораторних процедур і методик аналітичної хімії, синтетичної органічної хімії, медичної і фармацевтичної хімії, представлена добре відомою і загальноприйнятою номенклатурою в даній галузі. Для хімічного синтезу, хімічних аналізів, виготовлення фармацевтичних препаратів, рецептурних сполук, їх доставки і для лікування хворих можна використовувати стандартні методики. Усічені поліпептидиFGF21 за даним винаходом також можна з'єднувати з іншим компонентом, що здатний надавати усіченому поліпептиду FGF21 додаткові властивості. В одному з варіантів здійснення даного винаходу усічений поліпептид FGF21 може бути з'єднаний з послідовністю Fc. Таке злиття можна здійснити, застосовуючи відомі способи молекулярної біології та/або керівні вказівки, представлені в даному документі. Переваги таких складених поліпептидів, а також способи виготовлення таких складених поліпептидів будуть обговорюватися в даному документі більш детально. 4. Мутанти FGF21, стійкі до протеолізу Як зазначено в прикладі 8, було виявлено, що зрілий FGF21 піддається руйнуванню in vivo, що, в остаточному підсумку, є результатом протеолітичної атаки. Було виявлено, що руйнування зрілого FGF21 in vivo скорочує ефективний період його напіввиведення, а це, у свою чергу, негативно впливає на терапевтичний потенціал молекули. Відповідно до цього, було проведено цілеспрямоване дослідження з ідентифікації мутантів FGF21, що виявляють стійкість до протеолізу. У результаті цього дослідження було визначено, що сайти в молекулі зрілого поліпептиду FGF21, що особливо чутливі до протеолізу, включають амінокислотні залишки в положеннях 4-5, 20-21, 151-152, 171-172 та 178-181. Було проведене широке, але сфокусоване і цілеспрямоване дослідження з ідентифікації специфічних заміщень, що усувають протеолітичний ефект, що спостерігається, хоча при цьому не впливають на активність білка в неприпустимому ступені. Таблиці 8 і 11 представляють деякі з одержаних і протестованих мутантів. Як описано в прикладах 13 і 14, не всі мутанти FGF21 демонструють ідеальний профіль: одні мутанти, набуваючи стійкість до протеолізу, втрачали або знижували корисну активність FGF21, а інші мутанти зберігали активність FGF21, але не набували стійкості до протеолізу. Деякі мутанти, включаючи, наприклад, FGF21 P171G, зберігали рівень активності, подібний до FGF21 дикого типу, і в той же час демонстрували стійкість до протеолітичного руйнування. Один із критеріїв відбору при ідентифікації бажаних мутантів FGF21, стійких до протеолізу, полягав у тому, щоб активність мутанта FGF21 була істотно такою же або навіть більшою в порівнянні з активністю FGF21 дикого типу. Отже, ще один варіант здійснення даного винаходу спрямований на мутанти FGF21, що стійкі до протеолізу, але при цьому зберігають активність, яка істотно не відрізняється від активності FGF21 дикого або типу перевищує її. Хоча в деяких випадках це менш бажано, ще один варіант здійснення даного винаходу зв'язаний з мутантами FGF21, стійких до протеолізу, але таких, що виявляють деякою мірою знижену активність. У деяких випадках може виявитися бажаним підтримувати протеоліз, унаслідок чого мутанти FGF21, що припускають деякий ступінь протеолізу, формують ще один варіант здійснення даного винаходу. Як і всі мутанти FGF21, представлені в даній заявці, мутанти FGF21, стійкі до протеолізу, можна виготовити так, як описано в даному документі. Фахівці в даній галузі, наприклад, які знають стандартні методики молекулярної біології, зможуть використати свої знання разом з відомостями, представленими в даному розкритті винаходу, щоб виготовляти і застосовувати мутанти FGF21, стійкі до протеолізу, представлені в даній заявці. Для рекомбінантної ДНК, олігонуклеотидного синтезу, тканинної культури і трансформації можна використовувати стандартні методики (наприклад, електропорацію, ліпофекцію). Див., наприклад, публікацію Sambrook et al., Molecular Cloning: A Laboratory Manual, вище, що включена в даний документ як посилання для будь-яких цілей. Ферментативні реакції і методики очищення можна проводити у відповідності зі специфікаціями виробників, як це загальноприйнято в даній галузі техніки або описано в даному документі. Якщо не представлені спеціальні визначення, номенклатура, 15 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 використовувана в даному документі стосовно лабораторних процедур і методик аналітичної хімії, синтетичної органічної хімії, медичної і фармацевтичної хімії, представлена добре відомою і загальноприйнятою номенклатурою в даній галузі. Для хімічного синтезу, хімічних аналізів, виготовлення фармацевтичних препаратів, рецептурних сполук, їх доставки і для лікування хворих можна використовувати стандартні методики. Мутанти FGF21, стійкі до протеолізу, можна комбінувати з іншим компонентом, що здатний надавати мутанту FGF21, стійкому до протеолізу, додаткові властивості. В одному з варіантів здійснення даного винаходу стійкий до протеолізу мутант FGF21 можна скомбінувати з послідовністю Fc IgG, наприклад, SEQ ID NO: 11. Таке злиття можна здійснити, застосовуючи відомі способи молекулярної біології та/або керівні вказівки, представлені в даному документі. Переваги таких складених поліпептидів, а також способи виготовлення таких складених поліпептидів відомі і будуть обговорюватися в даному документі більш детально. 5. Мутанти FGF21 зі зниженою агрегацією Як описано в прикладі 15, однією з властивостей поліпептиду FGF21 дикого типу є його схильність до агрегації. При концентрації понад приблизно 5 мг/мл ступінь агрегації високий при кімнатній температурі. Як показано та описано в даному документі, ступінь агрегації для поліпептиду FGF21 дикого типу залежить як від концентрації, так і від температури. Агрегація може викликати проблеми при роботі з FGF21 дикого типу в цих концентраціях, наприклад, у контексті складання терапевтичної композиції. Відповідно до цього, було проведено цілеспрямоване дослідження з ідентифікації мутантів FGF21, що виявляють знижену схильність до агрегації. Потім виявлені мутанти FGF21 були протестовані на схильність до агрегації в різних концентраціях. Було проведене широке, але сфокусоване та цілеспрямоване дослідження з ідентифікації специфічних заміщень, що усувають ефект агрегації, що спостерігається, для FGF21 дикого типу, але при цьому не впливають на активність білка в неприпустимому ступені. Підхід до ідентифікації придатних мутантів зі зниженою агрегацією описано у прикладі 15. У таблиці 16 представлені деякі одержані та протестовані мутанти. Як показано в прикладі 17, не всі мутанти FGF21 виявляють ідеальний профіль. Одні мутанти, такі, як FGF21 L58E, мали знижену активність FGF21 і не досліджувалися далі, а інші мутанти, такі, як FGF21 A134E, зберігали активність FGF21, але не набували властивості зниженої схильності до агрегації. У той же час деякі мутанти, такі, як FGF21 L98R, не тільки зберігали активність FGF21, але й демонстрували знижену агрегацію. Один мутант, FGF21 A45K, несподівано виявив підвищену активність FGF21 поряд зі зниженою схильністю до агрегації. Один із критеріїв відбору при ідентифікації бажаних мутантів FGF21, не схильних до агрегації, полягав у тому, щоб активність мутанта FGF21 була, істотно, подібною або навіть більшою в порівнянні з активністю FGF21 дикого типу. Отже, ще один варіант здійснення даного винаходу спрямовано на мутанти FGF21, що мають знижену схильність до агрегації, але в той же час зберігають активність FGF21, що подібна до активності FGF21 дикого типу або перевищує її. Незважаючи на те, що в деяких випадках це менш бажано, ще один варіант здійснення даного винаходу зв'язаний з мутантами FGF21, що мають знижену схильність до агрегації, але виявляють деякою мірою знижену активність FGF21. У деяких випадках може виявитися бажаним підтримувати визначений рівень агрегації, внаслідок чого мутанти FGF21, що припускають деякий ступінь агрегації, формують ще один варіант здійснення даного винаходу. Як і всі мутанти FGF21, представлені в даній заявці, мутанти FGF21, що мають знижену схильністю до агрегації, можна виготовити так, як описано в даному документі. Середні фахівці в даній галузі, знайомі зі стандартними методиками молекулярної біології, зможуть використати свої знання разом з відомостями, представленими в даному розкритті винаходу, щоб виготовляти та застосовувати мутанти FGF21 зі зниженою схильністю до агрегації, представлені в даній заявці. Для рекомбінантної ДНК, олигонуклеотидного синтезу, тканинної культури і трансформації можна використовувати стандартні методики (наприклад, електропорацію, ліпофекцію). Див., наприклад, Sambrook et al., Molecular Cloning: A Laboratory Manual, вище, що включена в цей документ як посилання для будь-яких цілей. Ферментативні реакції і методики очищення можна проводити у відповідності зі специфікаціями виробників, як це загальноприйнято в даній галузі техніки або описано в даному документі. Якщо не представлені спеціальні визначення, номенклатура, використовувана в даному документі стосовно лабораторних процедур і методик аналітичної хімії, синтетичної органічної хімії, медичної і фармацевтичної хімії, представлена добре відомою й загальноприйнятою номенклатурою в даній галузі. Для хімічного синтезу, хімічних аналізів, виготовлення фармацевтичних препаратів, рецептурних сполук, їх доставки та для лікування хворих можна використовувати стандартні 16 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 методики. Мутанти FGF21, не схильні до агрегації, можна з'єднувати з іншим компонентом, що здатний надавати мутанту FGF21, не схильному до агрегації, додаткові властивості. В одному з варіантів здійснення даного винаходу не схильний до агрегації мутант FGF21 можна з'єднати з послідовністю Fc IgG, наприклад, SEQ ID NO: 11. Таке злиття можна здійснити, застосовуючи відомі способи молекулярної біології та/або керівні вказівки, представлені в даному документі. Переваги таких складених поліпептидів, а також способи виготовлення таких складених поліпептидів обговорюються в даному документі більш детально. 6. Комбіновані мутанти FGF21 Як описано в даному документі, послідовність FGF21 дикого типу має деякі властивості, що викликають значні проблеми при використанні FGF21 як терапевтичної молекули. Серед цих проблем необхідно згадати чутливість білка до руйнування та його схильність до агрегації у високих концентраціях. Після всебічних спроб ідентифікувати такі поліпептиди FGF21, що долають кожну з цих проблем, було проведено цілеспрямоване дослідження для визначення того, або можна скомбінувати амінокислотні заміщення, що надають білку стійкість до протеолізу, і заміщення, що знижують схильність до агрегації, щоб досягти адитивного або синергічного ефекту таких заміщень в одній поліпептидній послідовності, підтримуючи при цьому такий рівень активності, що відповідає активності FGF21 дикого типу або перевищує її. Ця задача складна для рішення, оскільки в даній галузі знань відомо, що введення множинних мутацій у визначений поліпептид іноді може негативно впливати на експресію, активність і наступне вироблення білка у виробничих масштабах. Несподівано, як це продемонстровано в прикладах 19 і 20, було виявлено, що бажані властивості декількох мутантів FGF21, дійсно, можна комбінувати адитивним або синергічним чином, щоб одержати такий мутант FGF21, що має поліпшені фармацевтичні властивості. У даному документі розкриті мутанти FGF21, які стійкі до протеолізу, мають знижений ступінь агрегації, але при цьому зберігають таку активність, що відповідає активності FGF21 дикого типу або перевищує її. Один із критеріїв відбору при ідентифікації бажаних комбінованих мутантів FGF21 полягав у тому, щоб активність мутанта FGF21 була, істотно, подібною або навіть більшою в порівнянні з активністю FGF21 дикого типу. Отже, ще один варіант здійснення даного винаходу спрямований на мутанти FGF21, стійкі до протеолізу і такі, що мають знижену схильність до агрегації, але в той же час такі, що зберігають активність FGF21, подібну за активність FGF21 дикого типу або перевищуючу її. Хоча в деяких випадках це менш бажано, ще один варіант здійснення даного винаходу зв'язаний з мутантами FGF21, що стійкі до протеолізу і мають знижену схильність до агрегації, але виявляють деякою мірою знижену активність FGF21. У деяких випадках може виявитися бажаним підтримувати визначений рівень протеолізу та/або агрегації, внаслідок чого мутанти FGF21, що припускають деякий ступінь протеолізу та/або агрегації, формують ще один варіант здійснення даного винаходу. Як і всі мутанти FGF21 за даним винаходом, комбіновані мутанти FGF21, що відповідають цьому винаходу, можна виготовити так, як описано в даному документі. Середні фахівці в даній галузі, знайомі зі стандартними методиками молекулярної біології, зможуть використати свої знання разом з відомостями, представленими в даному розкритті винаходу, щоб виготовляти і застосовувати комбіновані мутанти FGF21, що відповідають даному винаходу. Для рекомбінантної ДНК, олігонуклеотидного синтезу, тканинної культури і трансформації можна використовувати стандартні методики (наприклад, електропорацію, ліпофекцію). Див., наприклад, Sambrook et al., Molecular Cloning: A Laboratory Manual, вище, що включена в цей документ як посилання для будь-яких цілей. Ферментативні реакції і методики очищення можна проводити у відповідності зі специфікаціями виробників, як це загальноприйнято в даній галузі техніки або описано в даному документі. Якщо не представлені спеціальні визначення, номенклатура, використовувана в даному документі стосовно лабораторних процедур і методик аналітичної хімії, синтетичної органічної хімії, медичної і фармацевтичної хімії, представлена добре відомою і загальноприйнятою номенклатурою в даній галузі. Для хімічного синтезу, хімічних аналізів, виготовлення фармацевтичних препаратів, рецептурних сполук, їх доставки та для лікування хворих можна використовувати стандартні методики. Комбіновані мутанти FGF21, що відповідають даному винаходу, можна з'єднувати з іншим компонентом, що здатний надавати комбінованому мутанту FGF21 додаткові властивості. В одному з варіантів здійснення даного винаходу комбінований мутант FGF21 можна з'єднувати з послідовністю Fc IgG,наприклад, SEQ ID NO: 11. Таке злиття можна здійснити, застосовуючи відомі способи молекулярної біології та/або керівні вказівки, представлені в даному документі. Переваги таких складених поліпептидів, а також способи виготовлення таких складених поліпептидів обговорюються в даному документі більш детально. 17 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 7. Складені білки FGF21 При використанні в даному документі термін "складений поліпептид FGF21" або "складений білок FGF21" відноситься до сполуки одного або більш амінокислотних залишків (наприклад, з утворенням гетерологічного білка або пептиду) на N-кінці або C-кінці будь-якого мутантного поліпептиду FGF21, описаного в даному документі. Гетерологічні пептиди та поліпептиди включають, але не обмежуючись цим, епітоп, що дозволяє виявити та/або виділити мутантний поліпептид FGF21, трансмембранний рецепторний білок або його частину, таку як позаклітинний домен або трансмембранний і внутрішньоклітинний домен, ліганд або частина ліганду, які зв'язуються з трансмембранним рецепторним білком, фермент або частина ферменту, що каталітично активні, пептид або поліпептид, що стимулюють олігомерізацию, наприклад, домен лейцинової застібки, пептид або поліпептид, що підвищують стабільність, наприклад, константна ділянка імуноглобуліну (наприклад, Fc домен); що підвищує період напіввиведення послідовності, що містить комбінацію двох або більше (наприклад, 2, 5, 10, 15, 20, 25, та інш.) таких, що зустрічаються у природі або не зустрічаються в природі заряджених та/або незаряджених амінокислот (наприклад, серин, гліцин, глутамову або аспартамову кислоту), розроблену для утворення, головним чином, гідрофільного, чи, головним чином, гідрофобного партнера гібридизації для мутанта FGF21, функціональне або не функціональне антитіло або його важкий або легкий ланцюг, а також поліпептид, що має активність, зокрема, терапевтичну активністю, відмінну від мутантних поліпептидів FGF21 за даним винаходом. Даний винахід також охоплює мутантів FGF21, з'єднаних із сироватковим альбуміном людини (HSA). Складені білки FGF21 можна виготовити за допомогою з'єднання гетерологічних послідовностей або на N-кінці, або на C-кінці мутантного поліпептиду FGF21. Як описано в даному документі, гетерологічна послідовність може являти собою амінокислотну послідовність або полімер, що не містить амінокислот. Гетерологічні послідовності можна з'єднувати з мутантним поліпептидом FGF21 безпосередньо, або через лінкер/адаптерну молекулу. Лінкер або адаптерна молекула можуть являти собою один або більше амінокислотних залишків (або мерів), наприклад, 1, 2, 3, 4, 5, 6, 7, 8, або 9 залишків (або -мерів), переважно, від 10 до 50 амінокислотних залишків (або -мерів), наприклад, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30, 35, 40, 45 або 50 залишків (або -мерів) і, більш переважно, від 15 до 35 амінокислотних залишків (або -мерів). Лінкер або адаптерну молекулу також можна сконструювати із сайтом розщеплення для рестрикційної ДНК-ендонуклеази або для протеази, що дозволяє розділяти з'єднані компоненти. a. Сполуки з Fc У одному з варіантів здійснення даного винаходу мутантний поліпептид FGF21 з'єднано з Fc доменом, наприклад, одним або більше доменів ділянок Fc імуноглобуліну IgG людини. Антитіла включають дві функціонально незалежні частини, варіабельний домен, відомий як "Fab", що зв'язує антиген, і константний домен, відомий як "Fc", що задіяний у такі ефекторні функції, як активація комплементу та атака фагоцитарними клітинами. Домен Fc має довгий період напіввиведення із сироватки, тоді як домен Fab є короткоживучим (Capon et al., 1989, Nature 337: 525-31). При з'єднанні з терапевтичним білком домен Fc може забезпечити більш тривалий період напіввиведення або вбудувати такі функції, як зв'язування рецептора Fc, зв'язування білка A, фіксація комплементу та, можливо, навіть перенос через плаценту (Capon et al., 1989). Фармакокінетичний аналіз in vivo вказує на те, що FGF21 людини має короткий період напіввиведення, що становить у мишей приблизно 1 годину, що зв'язано зі швидким кліренсом і руйнуванням in vivo. Отже, для подовження періоду напіввиведення FGF21 нативну послідовність Fc приєднували до N- або C-кінцевої ділянки поліпептиду FGF21. Злиття послідовності Fc з FGF21 дикого типу, особливо, приєднання Fc до N-кінця FGF21 дикого типу, усупереч чеканням, не подовжувало період напіввиведення, однак це спостереження призвело до дослідження протеолітичного розпаду FGF21 in vivo і до ідентифікації мутантів FGF21, що були стійкими до такого розпаду. Такі мутанти, описані в прикладах 9 і 11, виявляють довший період напіввиведення в порівнянні з FGF21 дикого типу. Ці та інші складені білки FGF21 формують варіанти здійснення даного винаходу. По всьому тексту даного розкриття винаходу позначення Fc-FGF21 відноситься до складеного білка, у якому послідовність Fc приєднана до N-кінця FGF21. Подібним чином, позначення Fc-FGF21 відноситься до складеного білка, в якому послідовність Fc приєднана до C-кінця FGF21. Одержаний в результаті такого злиття складений білок FGF21 можна очистити, наприклад, застосовуючи колонку для афінної хроматографії з білком A. Було виявлено, що пептиди та 18 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 білки, до яких приєднана ділянка Fc, виявляють in vivo значно більш тривалий період напіввиведення в порівнянні з не з'єднаними аналогами. До того ж складання з ділянкою Fc створює можливість для димерізації/мультимерізації складеного поліпептиду. Ділянка Fc може являти собою ділянку Fc, що зустрічається в природі, але також може піддаватися змінам для покращення визначених якостей, таких як терапевтичні якості, час циркуляції або знижена агрегація. Корисні модифікації білкових терапевтичних засобів за рахунок злиття з доменом "Fc" антитіла детально обговорюються в Міжнародній патентній публікації № WO 00/024782, зміст якої повністю включено в цей документ як посилання. b. Лінкери складених білків При формуванні складених білків за даним винаходом можна, але не обов'язково, використовувати лінкер. Якщо лінкер представлено, його хімічна структура може бути принциповою, оскільки він, у першу чергу, слугує спейсером. Лінкер може складатися з амінокислот, зчеплених одна з одною за допомогою пептидних зв'язків. У деяких варіантах здійснення даного винаходу лінкер складений з 1–20 амінокислот, зчеплених за допомогою пептидних зв'язків, при цьому амінокислоти вибрані з 20 амінокислот, що зустрічаються в природі. У різних варіантах здійснення винаходу від 1 до 20 амінокислот вибрані з гліцину, серину, аланіну, проліну, аспарагіну, глутаміну та лізину. У деяких варіантах здійснення винаходу лінкер складений з більшості амінокислот, що не мають стеричних утруднень, таких як гліцин та аланін. У деяких варіантах здійснення винаходу лінкери являють собою полігліцини (такі, як (GIy)4 (SEQ ID NO: 29) та (Gly)5 (SEQ ID NO: 30)), поліаланіни, комбінації гліцину та аланіну (такі, як полі(Gly-AIa)) або комбінації гліцину та серину (такі, як полі(Gly-Ser)). Інші придатні лінкери включають: Gly)5-Ser-(Gly)3-Ser-(Gly)4-Ser (SEQ ID NO: 28), (GIy)4-Ser-(Gly)4-Ser(Gly)4-Ser (SEQ ID NO: 31), (GIy) 3-Lys-(GIy)4 (SEQ ID NO: 32), (Gly)3-Asn-Gly-Ser-(Gly)2 (SEQ ID NO: 33), (GIy)3-Cys-(GIy)4 (SEQ ID NO: 34), та Gly-Pro-Asn-Gly-GIy (SEQ ID NO: 35). Незважаючи на те, що було виявлено, що для складених білків FGF21 особливо придатним є лінкер з 15 амінокислот, даний винахід розглядає лінкери будь-якої довжини або будь-якого складу. При використанні лінкера для сполуки з гетерологічною послідовністю, такою, як Fc домен, та FGF21 поліпептид або FGF21 мутант, лінкер наведений у дужках. Лінкери, описані в даному документі, типові, але даний винахід також розглядає лінкери, що набагато довші та можуть включати інші амінокислотні залишки. Непептидні лінкери також розглядаються в даному винаході. Наприклад, можна використовувати алкильні лінкери, такі, як -NH-(CH2)S-C(O)-, у якому s = від 2 до 20. Далі, такі алкильні лінкери можуть бути заміщені будьякою стерично не утрудненою групою, включаючи, але не обмежуючись цим, нижчий алкіл (наприклад, C1-C6), нижчий ацил, галоген (наприклад, Cl, Br), CN, NH 2 або феніл. Типовим непептидним лінкером є поліетиленгліколевий лінкер, що має молекулярну масу від 100 до 5000 кДа, наприклад, від 100 до 500 кДа. 8. Хімічно модифіковані мутанти FGF21 Хімічно модифіковані форми мутантних поліпептидів FGF21, описані в даному документі, включаючи усічені форми FGF21, описані в даному документі, можуть бути виготовлені кваліфікованим фахівцем з урахуванням інформації, представленої в цьому розкритті винаходу. Такі хімічно модифіковані мутанти FGF21 змінені таким чином, що вони відрізняються від не модифікованих мутантів FGF21 не за типом, та не за локалізацією молекул, природним чином прикріплених до мутанта FGF21. Хімічно модифіковані мутанти FGF21 можуть включати молекули, що будуть утворені за допомогою видалення однієї або більше хімічних груп, прикріплених природним чином. В одному з варіантів здійснення винаходу мутантні поліпептиди FGF21 за даним винаходом можуть бути модифіковані за допомогою ковалентного приєднання одного або більше полімерів. Наприклад, у типовому випадку відібраний полімер розчинний у воді, тому білок, до якого він приєднується, не випадає в осад у водяному середовищі, такому, як фізіологічне середовище. У сферу придатних полімерів включені суміші полімерів. З метою терапевтичного використання препарату, що є кінцевим продуктом, переважно, щоб полімер був фармацевтично прийнятним. Нерозчинні у воді полімери, кон'юговані з мутантними поліпептидами FGF21 за даним винаходом, також формують один з аспектів винаходу. Типові полімери можуть мати будь-яку молекулярну масу і бути розгалуженими або нерозгалуженими. Кожний типовий полімер має середню молекулярну масу приблизно від 2 кДа до 100 кДа (термін "приблизно" вказує на те, що в препаратах водорозчинних полімерів маса деяких молекул буде відрізнятися у більшу або меншу сторону від заявленої молекулярної маси). Переважно, щоб середня молекулярна маса кожного полімер становила приблизно від 5 кДа до 50 кДа, більш переважно, приблизно від 12 кДа до 40 кДа та, найбільше переважно, 19 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 приблизно від 20 кДа до 35 кДа. Придатні водорозчинні полімери або їх суміші включають, але не обмежуючись цим, Nзчеплені або O-зчеплені вуглеводи, цукри, фосфати, поліетиленгліколь (ПЕГ) (включаючи такі форми ПЕГ, що були використані для одержання похідних білків, включаючи моно-(C1-C10), алкокси- або арилокси-поліетиленгліколь), монометокси-поліетиленгліколь, декстран (такий, як декстран низької молекулярної маси, наприклад, приблизно 6 кДа), целюлозу або інші полімери на вуглеводній основі, полі-(N-вінілпіролідон) поліетиленгліколь, гомополімери пропіленгликолю, кополімери пропіленоксида/етиленоксида, поліоксиетильовані поліоли (наприклад, гліцерин) і полівініловий спирт. Даний винахід також охоплює біфункціональні поперечно зшиті молекули, що можуть бути використані для одержання ковалентно зв'язаних мультимерів мутантних поліпептидів FGF21. Даний винахід також охоплює мутанти FGF21, ковалентно приєднані до полісіалової кислоти. У деяких варіантах здійснення даного винаходу мутант FGF21 ковалентно або хімічно модифікований із приєднанням одного або більш водорозчинних полімерів, включаючи, але не обмежуючись цим, поліетиленгліколь (ПЕГ), поліоксиетиленгліколь або пропіленгліколь. Див., наприклад, патенти США №№ 4640835, 4496689, 4301144, 4670417, 4791192 та 4179337. У деяких варіантах здійснення даного винаходу мутант FGF21 містить один або більше полімерів, включаючи, але не обмежуючи цим, монометокси-поліетиленгліколь, декстран, целюлозу, інший полімер на вуглеводній основі, полі-(N-вінілпіролідон)-поліетиленгліколь, гомополімери пропіленгліколя, кополімера поліпропіленоксида/етиленоксида, поліоксиетильовані поліоли (наприклад, гліцерин), полівініловий спирт або суміші таких полімерів. У деяких варіантах здійснення даного винаходу мутант FGF21 ковалентно модифікований субодиницями ПЕГ. У деяких варіантах здійснення винаходу один або більше водорозчинних полімерів зв'язані в одному або більше специфічних положень (наприклад, на N-кінці) мутанта FGF21. У деяких варіантах здійснення винаходу один або більше водорозчинних полімерів у випадковому порядку прикріплені до одного або більше бічних ланцюгів мутанта FGF21. У деяких варіантах здійснення винаходу ПЕГ використовується для покращення терапевтичної продуктивності мутанта FGF21. Деякі з таких способів обговорюються, наприклад, у патенті США № 6133426, що включений у цей документ як посилання для будь-яких цілей. У тих варіантах здійснення даного винаходу, де полімером є ПЕГ, група ПЕГ може мати будь-яку придатну молекулярну масу і може бути лінійною або розгалуженою. Переважно, щоб середня молекулярна маса групи ПЕГ варіювалася в приблизному діапазоні від 2 кДа до 100 кДа та, більш переважно, приблизно від 5 кДа до 50 кДа, наприклад, 10, 20, 30, 40 або 50 кДа. Групи ПЕГ зазвичай прикріплюються до мутанта FGF21 за допомогою ацилювання або відновлювального алкилування через реактивну групу на компоненті ПЕГ (наприклад, альдегідну, аміно, тіолову або ефірну групу), взаємодіючу з реактивною групою на мутанті FGF21 (наприклад, альдегідної, аміно або ефірною групою). ПЕГилювання (чи пегилювання) поліпептидів, включаючи мутанти FGF21 за даним винаходом, може специфічно здійснюватися із застосуванням будь-яких реакцій пегилювання, відомих у даній галузі знань. Такі реакції описані, наприклад, у таких посиланнях: Francis et al., 1992, Focus on Growth Factors 3: 4-10, європейські патенти №№ 0 154 316 і 0 401 384, патент США № 4179337. Наприклад, пегилювання можна здійснити за допомогою реакції ацилювання або реакції алкилування з реактивною молекулою поліетиленгліколя (чи аналогічного реактивного водорозчинного полімеру), як описано в даному документі. Для реакцій ацилювання обраний полімер повинен мати одну реактивну ефірну групу. Для відновлювального алкилування обраний полімер повинен мати одну реактивну альдегідну групу. Реактивним альдегідом є, наприклад, пропіональдегід поліетиленгліколя, що стабільний у воді, або його моно C1-C10 алкокси або арилокси похідні (див., наприклад, патент США № 5252714). У деяких варіантах здійснення даного винаходу корисна стратегія приєднання групи ПЕГ до поліпептиду включає комбінування через утворення конъюгатного зв'язку в розчині між пептидом та компонентом ПЕГ, при цьому кожен з них несе особливу функціональність із взаємною реактивністю по відношенню один до одного. Пептиди можна легко приготувати за допомогою традиційного твердофазного синтезу. Пептиди "попередньо активовані", тобто, мають відповідну функціональну групу в специфічному сайті. Перед реакцією з компонентом ПЕГ попередники очищають та одержують їх повні характеристики. Зшивання пептиду з ПЕГ зазвичай відбувається у водній фазі, і його можна легко контролювати за допомогою оберненофазової аналітичної ВЕРХ (високоефективна рідинна хроматографія). Пегильовані пептиди можна легко очистити за допомогою препаративної ВЕРХ і охарактеризувати за допомогою аналітичної ВЕРХ, амінокислотного аналізу і лазерної десорбційної мас-спектрометрії. 20 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 Полісахаридні полімери являють собою ще один тип водорозчинного полімеру, який можна застосовувати для модифікації білка. Отже, мутанти FGF21 за даним винаходом, з'єднані з полісахаридним полімером, формують варіанти здійснення даного винаходу. Декстрани являють собою полісахаридні полімери, що складаються з окремих субодиниць глюкози, переважно з'єднаних альфа 1-6 зв'язками. Декстран, як такий, доступний у широкому діапазоні молекулярної маси і легко доступний у діапазоні молекулярної маси приблизно від 1 кДа до 70 кДа. Декстран є придатним водорозчинним полімером для застосування як носія або самостійно в комбінації з іншим носієм (наприклад, Fc). Див., наприклад, Міжнародну патентну публікацію № WO 96/11953. У ній було описане застосування декстрана, кон'югованого з терапевтичними або діагностичними імуноглобулінами. Див., наприклад, Європейську патентну публікацію № 0 315 456, що включена в цей документ як посилання. Даний винахід також охоплює застосування декстрана з молекулярною масою приблизно від 1 кДа до 20 кДа. У цілому, хімічну модифікацію можна проводити у будь-яких придатних умовах, що сприяють реакції білка з активованою молекулою полімеру. Способи приготування хімічно модифікованих поліпептидів зазвичай включають наступні етапи: (a) реакція поліпептиду з активованою молекулою полімеру (такою, як реактивне ефірне або альдегідне похідне молекули полімеру) у таких умовах, за яких мутантний поліпептид FGF21 прикріплюється до однієї або більше молекул полімеру, та (b) одержання продуктів реакції. Оптимальні умови реакції можна визначити, ґрунтуючись на відомих параметрах і бажаному результаті. Наприклад, чим більше співвідношення між молекулами полімеру і білка, тим більшим є відсотковий показник приєднання молекул полімеру. В одному з варіантів здійснення даного винаходу, хімічно модифіковані мутанти FGF21 можуть мати одиничний компонент, представлений молекулою полімеру на аміно-кінці (див., наприклад, патент США № 5234784). В іншому варіанті здійснення даного винаходу мутантні поліпептиди FGF21 можуть бути хімічно з'єднані з біотином. Потім комплексам біотину з мутантними поліпептидами FGF21 дають можливість зв'язуватися з авидіном, що призводить до утворення тетравалента авидін/біотин/мутантний поліпептид FGF21. Мутантні поліпептиди FGF21 також можна ковалентно з'єднувати з динітрофенолом (DNP) або тринітрофенолом (TNP), а одержані в результаті кон'югати, що осаджуються антитілами IgM типу анти-DNP або анти-TNP утворять декамерні кон'югати з валентністю 10. У цілому, стани, які можна полегшити або модулювати введенням описаних хімічно модифікованих мутантів FGF21, включають ті ж стани, що описані в даному документі для мутантних поліпептидів FGF21. Однак хімічно модифіковані мутанти FGF21, розкриті в даному документі, можуть мати додаткові види активності, посиленої або послабленої біологічною активністю або іншими властивостями, такими, як подовжений або скорочений період напіввиведення в порівнянні з не модифікованими мутантами FGF21. 9. Фармацевтичні композиції мутантів FGF21 і їх введення Фармацевтичні композиції, що включають мутанти FGF21, відносяться до сфери даного винаходу і специфічно розглядаються у світлі ідентифікації різних мутантних послідовностей FGF21, що виявляють поліпшені властивості. Такі фармацевтичні композиції з мутантами FGF21 можуть включати терапевтично ефективну кількість мутантного поліпептиду FGF21 у суміші з фармацевтично або фізіологічно прийнятним формоутворюючим агентом, підібраним відповідно до передбачуваного способу введення. Переважним є, щоб прийнятні формоутворюючі агенти були нетоксичними для реципієнтів у застосовуваних дозах і концентраціях. Фармацевтична композиція може містити формоутворюючий агент(и) для модифікації, підтримання або збереження, наприклад, pН, осмолярності, в'язкості, прозорості, кольору, ізотонічності, запаху, стерильності, стабільності, швидкості розкладання або вивільнення, адсорбції або пенетрациії композиції. Відповідні формоутворюючі агенти включають, але не обмежуючи цим, амінокислоти (такі, як гліцин, глутамін, аспарагін, аргінін або лізин), протимікробні засоби, антиоксиданти (такі, як аскорбінова кислота, сульфіт натрію або гідросульфіт натрію), буфери (такі, як борати, бікарбонати, трис-HCl, цитрати, фосфати або інші органічні кислоти), наповнювачі (такі, як маніт або гліцин), хелатоутворюючі агенти (такі, як етилендіамінтетраоцтова кислота (EDTA)), комплексоутворюючі агенти (такі, як кофеїн, полівінілпіролідон, бета-циклодекстрин або гідроксипропіл-бета-циклодекстрин), заповнювачі, моносахариди, дисахариди та інші вуглеводи (такі, як глюкоза, маноза або декстрини), білки (такі, як сироватковий альбумін, желатин або імуноглобуліни), барвники, смако-ароматичні агенти, або агенти, що розбавляють, емульгуючі агенти, гідрофільні полімери (такі, як полівінілпіролідон), поліпептиди низької молекулярної маси, солеутворюючі протиіони (такі, як натрій), консерванти (такі, як бензалконій хлорид, бензойна кислота, саліцилова кислота, 21 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 тимеросал, фенілетиловий спирт, метилпарабен, пропілпарабен, хлоргексидин, сорбинова кислота або перекис водню), розчинники (такі, як гліцерин, пропіленгликоль або поліетиленгліколь), цукрові спирти (такі, як маніт або сорбіт), суспендуючі агенти, сурфактанти або змочувальні агенти (такі, як плюроники, ПЕГ, ефіри сорбіту, полісорбати, такі, як полісорбат 20 або полісорбат 80, тритон, трометамин, лецитин, або холестерин тилоксапол), агенти, що підсилюють стабільність (такі, як сахароза або сорбіт), агенти, що підсилюють тоничність (такі, як галіди лужних металів, переважно, хлорид натрію або калію, маніт, сорбіт), транспортні засоби для доставки, розріджувачі, наповнювачі та/або фармацевтичні ад'юванти (див., наприклад, Remington's Pharmaceutical Sciences (18th Ed., A.R. Gennaro, ed., Mack Publishing Company 1990) і наступні видання тієї ж книги, що включені в цей документ як посилання для будь-яких цілей). Оптимальну фармацевтичну композицію цілком може визначити кваліфікований фахівець у залежності, наприклад, від наміченого способу введення, формату доставки та бажаної дози (див., наприклад, Remington's Pharmaceutical Sciences, вище). Такі композиції можуть впливати на фізичний стан, стабільність, швидкість вивільнення in vivo, та швидкість кліренсу in vivo мутантного поліпептиду FGF21. Основний транспортний засіб або носій у фармацевтичній композиції може бути водним або не водним за своєю природою. Наприклад, придатним транспортним засобом або носієм для ін'єкцій може бути вода, фізіологічний сольовий розчин або штучна спинномозкова рідина, можливо з додаванням інших матеріалів, загальноприйнятих у композиціях для парентерального введення. Іншими типовими транспортувальними засобами є фізіологічний розчин з додаванням буферу, або фізіологічний розчин, змішаний із сироватковим альбуміном. Іншими типовими фармацевтичними композиціями є буфер трис із приблизним значенням pН 7,0-8,5 або ацетатний буфер із приблизним значенням pН 4,0-5,5, що додатково можуть включати сорбіт або його придатний замінник. В одному з варіантів здійснення даного винаходу композиції з мутантним поліпептидом FGF21 можна приготувати для зберігання, змішуючи вибрану композицію, що має бажаний ступінь чистоти, з факультативними формоутворюючими агентами (Remington's Pharmaceutical Sciences, вище) у виді лиіофілізованої таблетки або водяного розчину. Крім того, фармацевтичний продукт із мутантним поліпептидом FGF21 може випускатися у виді ліофилизата із застосуванням відповідних наповнювачів, таких, як сахароза. Фармацевтичні композиції з мутантним поліпептидом FGF21 можуть бути підібрані для парентеральної доставки. В альтернативному варіанті можна підібрати композиції для інгаляції або для доставки через травний тракт, наприклад, пероральної. Виготовлення таких фармацевтично прийнятних композицій відноситься до кваліфікації фахівців, що працюють у даній галузі. Формоутворюючі компоненти представлені в таких концентраціях, що прийнятні в місці введення композиції. Наприклад, буфери застосовують для підтримки pН композиції на фізіологічному рівні або трохи нижче, зазвичай в приблизному діапазоні pН від 5 до 8. Коли йдеться про парентеральне введення, терапевтична композиція для застосування за даним винаходом може являти собою апірогенний, парентерально прийнятний водний розчин, що містить бажаний мутантний поліпептид FGF21 і фармацевтично прийнятний транспортний засіб. Особливо придатним транспортним засобом для парентеральних ін'єкцій є стерильна дистильована вода, в якій розчиняють мутантний поліпептид FGF21, одержуючи в результаті стерильний ізотонічний розчин, законсервований відповідним чином. Ще один препарат може включати лікарську сполуку з бажаної молекули з таким агентом, як ін'єкційні мікросфери, частки, що біологічно розпадаються, полімерні сполуки (такі, як полімолочна кислота або полігликолева кислота), крапельки або ліпосоми, що забезпечують кероване і тривале вивільнення продукту, який можна доставляти за допомогою депонованих ін'єкцій. Також можна використовувати гіалуронову кислоту, яка може стимулювати тривале перебування композиції у кровотоці. Інші придатні засоби для введення бажаної молекули включають пристосування, що імплантуються, для доставки ліків. В одному з варіантів здійснення винаходу може бути складена фармацевтична композиція для інгаляції. Наприклад, мутантний поліпептид FGF21 може бути оформлений у вигляді сухого порошку для інгаляції. Також можна приготувати інгаляційні розчини мутантного поліпептиду FGF21 із пропелентом для аерозольної доставки. Ще в одному варіанті здійснення винаходу розчини можна розпорошувати за допомогою небулайзера. Пульмональне (легеневе) введення більш детально описано в Міжнародній патентній публікації № WO 94/20069, що описує пульмональне введення хімічно модифікованих білків. Також розглядається можливість перорального введення деяких лікарських сполук. В одному з варіантів здійснення даного винаходу мутантні поліпептиди FGF21, що вводять таким 22 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 способом, можна вводити в лікарські сполуки разом з носіями або без носіїв, що зазвичай використовують при виготовленні твердих лікарських форм, таких як таблетки і капсули. Наприклад, можна сконструювати капсулу для вивільнення активної частини лікарської сполуки в тому відділі шлунково-кишкового тракту, де біологічна доступність ліків буде максимальною, а розпад перед потраплянням у системний кровоток буде мінімальним. Для того щоб полегшити всмоктування мутантного поліпептиду FGF21, у лікарську сполуку можна включити додаткові агенти. Можна також використовувати розріджувачі, смако-ароматичні речовини, воски з низькою температурою плавлення, рослинні олії, змащення, суспендуючі агенти, агенти для розпаду таблеток і зв'язувальні речовини. Фармацевтична композиція іншого типу може включати ефективну кількість мутантного поліпептиду FGF21 у суміші з нетоксичними наповнювачами, що зручні для виробництва таблеток. Розчиняючи таблетки в стерильній воді або іншому придатному носії, можна приготувати розчини в стандартній дозованій формі. Придатні наповнювачі включають, але не обмежуючись цим, інертні розріджувачі, такі, як карбонат кальцію, карбонат або бікарбонат натрію, лактозу або фосфат кальцію, агенти зв'язування, такі, як крохмаль, желатин або гуміарабік, а також змащувальні речовини, такі, як стеарат магнію, стеаринову кислоту або тальк. Кваліфікованим фахівцям будуть очевидні додаткові варіанти фармацевтичних композицій з мутантними поліпептидами FGF21, включаючи лікарські сполуки з уповільненим або контрольованим вивільненням мутантних поліпептидів FGF21. Компетентним фахівцям також повинні бути відомі методики складання багатьох інших засобів з уповільненим або контрольованим вивільненням, таких як ліпосомні носії, мікрочастинки, що біологічно руйнуються, пористий бісер і депоновані ін'єкції (див., наприклад, такі посилання, як Міжнародна патентна публікація № WO 93/15722, що описує контрольоване вивільнення пористих полімерних мікрочастинок для доставки фармацевтичних композицій, Wischke & Schwendeman, 2008, Int. J. Pharm. 364: 298-327, а також Freiberg & Zhu, 2004, Int. J. Pharm. 282: 1-18, у яких обговорюється виготовлення і застосування мікросфер/мікрочастинок). Як описано в даній заявці, гідрогель являє собою приклад композиції з уповільненим або контрольованим вивільненням. Додаткові приклади препаратів з уповільненим вивільненням включають напівпроникні полімерні матриці у виді виробів з визначеною формою, наприклад плівок або мікрокапсул. Матриці з уповільненим вивільненням можуть включати поліефіри, гідрогелі, полілактиди (патент США № 3773919 і європейський патент № 0 058 481), кополімери L-глутамінової кислоти та гамма-етил-L-глутамата (Sidman et al., 1983, Biopolymers 22: 547-56), полі(2гідроксиетил-метакрилат) (Langer et al., 1981, J. Biomed. Mater. Res. 15: 167-277 і Langer, 1982, Chem. Tech. 12: 98-105), етиленвінілацетат (Langer et al., вище) або полі-D(-)-3-гідроксибутирову кислоту (європейський патент № 0 133 988). Композиції з уповільненим вивільненням також можуть включати ліпосоми, які можна виготовити кожним з множини способів, відомих у даній галузі техніки. Див., наприклад, Epstein et al., 1985, Proc. Natl. Acad. Sci. U.S.A. 82: 3688-92 та європейські патенти №№ 0 036 676, 0 088 046 і 0 143 949. Типова фармацевтична композиція з мутантним поліпептидом FGF21, застосовувана для введення in vivo, повинна бути стерильною. Цього можна досягти пропусканням через мембрани для стерильної фільтрації. При виготовленні ліофілізованої композиції стерилізацію із застосуванням цього способу можна проводити або до ліофилізації, або після ліофилізації і відновлення. Композицію для парентерального введення можна зберігати в ліофілізованому вигляді або у розчині. Додатково до цього, парентеральну композицію ззазвичай поміщають у контейнер, що має стерильний порт доступу, наприклад, у мішок для внутрішньовенного розчину або у флакон із пробкою, яку можна проколоти голкою для підшкірної ін'єкції. Після складання фармацевтичної композиції її можна зберігати в стерильних флаконах у вигляді розчину, суспензії, гелю, емульсії, твердої речовини, збезводненого або ліофілізованого порошку. Такі лікарські сполуки можна зберігати або в готовій для застосування формі, або у такій формі, що вимагає відновлення перед введенням (наприклад, у ліофілізованій). У специфічному варіанті здійснення даний винахід спрямований на набори для виготовлення модулів разових доз, призначених для введення. Такі набори можуть включати як перший контейнер із сухим білком, так і другий контейнер з водним складом. У сферу цього винаходу також входять набори, що включають однокамерні і багатокамерні попередньо заповнені шприци (наприклад, шприци з рідиною і шприци з ліофілізатом). Ефективна кількість фармацевтичної композиції з мутантним поліпептидом FGF21 для терапевтичного застосування буде залежати, наприклад, від терапевтичної ситуації і цільових об'єктів терапії. Кваліфікований фахівець зрозуміє, що придатні рівні доз для лікування будуть варіюватися, що частково залежить від молекули, яка вводиться, від показання до застосування 23 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 мутантного поліпептиду FGF21, від способу введення, а також від габаритів хворого (маси тіла, площі поверхні тіла або розміру органа) та від його/її медичного статусу (віку і загального стану здоров'я). Відповідно до цього, клініцист, прагнучи домогтися оптимального терапевтичного ефекту, може титрувати дозу і змінювати спосіб введення ліків. Типова доза може варіюватися в приблизному діапазоні від 0,1 мкг/кг до 100 мг/кг або більше, в залежності від вищезгаданих факторів. В інших варіантах здійснення винаходу доза може варіюватися в приблизному діапазоні від 0,1 мкг/кг до 100 мг/кг, від 1 мкг/кг до 100 мг/кг або від 5 мкг/кг, 10 мкг/кг, 15 мкг/кг, 20 мкг/кг, 25 мкг/кг, 30 мкг/кг, 35 мкг/кг, 40 мкг/кг, 45 мкг/кг, 50 мкг/кг, 55 мкг/кг, 60 мкг/кг, 65 мкг/кг, 70 мкг/кг, 75 мкг/кг до 100 мг/кг. В інших варіантах здійснення винаходу доза може складати 50 мкг/кг, 100 мкг/кг, 150 мкг/кг, 200 мкг/кг, 250 мкг/кг, 300 мкг/кг, 350 мкг/кг, 400 мкг/кг, 450 мкг/кг, 500 мкг/кг, 550 мкг/кг, 600 мкг/кг, 650 мкг/кг, 700 мкг/кг, 750 мкг/кг, 800 мкг/кг, 850 мкг/кг, 900 мкг/кг, 950 мкг/кг, 100 мкг/кг, 200 мкг/кг, 300 мкг/кг, 400 мкг/кг, 500 мкг/кг, 600 мкг/кг, 700 мкг/кг, 800 мкг/кг, 900 мкг/кг, 1000 мкг/кг, 2000 мкг/кг, 3000 мкг/кг, 4000 мкг/кг, 5000 мкг/кг, 6000 мкг/кг, 7000 мкг/кг, 8000 мкг/кг, 9000 мкг/кг або 10 мг/кг. Частота введення доз буде залежати від фармакокінетичних параметрів мутантного поліпептиду FGF21 у застосовуваній лікарській сполуці. У типовому випадку клініцист буде вводити композицію таким чином, щоб була досягнута доза, що дозволяє досягти бажаного лікувального ефекту. Отже, композицію можна вводити у виді разової дози, а також двох або більш доз, розділених за часом (які можуть містити таку саму або різну кількість потрібної молекули), або за допомогою безперервного вливання через пристосування, що імплантується, або катетер. Подальше доведення правильної дози зазвичай проводить середній фахівець, що знаходиться в межах його компетенції і входить у сферу його повсякденних задач. Правильну дозу встановлюють, виходячи з відповідних даних за дозовою залежністю реакції на лікування. Спосіб введення фармацевтичної композиції відповідає відомим способам, наприклад, перорально, через ін'єкцію: внутрішньовенну, внутрішньочеревну, внутрішньомозкову (інтрапаренхіматозну або інтравентрикулярну), внутрішньом'язову, внутрішньоочну, внутрішньоартеріальну, інтрапортальну (у воротну вену), усередину ушкодження, а також через системи з тривалим вивільненням (які можуть бути ін'єкційними або являти собою пристосування, які імплантують. При бажанні композиції можна вводити болюсну ін'єкцію, безперервним уливанням або через пристосування, яке імплантують. Альтернативно або додатково до цього, композицію можна вводити місцево через імплантацію мембрани, губки або іншого придатного матеріалу, який поглинає або інкапсулює необхідну молекулу. При використанні пристосування, що імплантують, це пристосування можна імплантувати у будь-яку придатну тканину або орган, при цьому доставка потрібної молекули може відбуватися через дифузію, розрахований за часом болюс або у вигляді безперервного введення. Для доставки лікарського засобу, наприклад, мутанта FGF21, описаного в даній заявці, з попередньо визначеною швидкістю, таким чином, що концентрація лікарського засобу може бути підтримана на бажаному терапевтично ефективному рівні протягом тривалого періоду часу, можуть бути застосовані різні підходи. В одному прикладі, може бути використаний гідрогель, що містить полімер, наприклад, желатин (наприклад, бичачий желатин, людський желатин, або желатин, одержаний з іншого джерела), або желатин, що зустрічається в природі або синтетично одержаний гідрогель. У гідрогелі може бути використаний будь-який відсотковий вміст полімеру (наприклад, желатину), наприклад, 5, 10, 15 або 20 %. Вибір відповідної концентрації може залежати від безлічі факторів, наприклад, бажаного терапевтичного профілю і фармакокінетичного профілю терапевтичної молекули. Приклади полімерів, що можуть бути включені в гідрогель, включають поліетиленгліколь ("ПЕГ"), поліетиленоксид, поліетиленоксид-ко-поліпропіленоксид, блок кополімери кополіетиленоксида або статистичні кополімери, полівініловий спирт, полі(вінілпіролідинон), полі(амінокислоти), декстран, гепарин, полісахариди, поліефіри та інш. Іншим фактором, що може бути прийнятий до уваги при одержанні гідрогелевої композиції, є ступінь перехресної зшивки в гідрогелі та в агенті перехресної зшивки. В одному варіанті здійснення винаходу, перехресне зшивання може бути одержане за допомогою реакції метакрилування з використанням метакрилового ангідриду. У деяких ситуаціях, може бути кращім високий ступінь перехресної зшивки, у той час як в інших ситуаціях кращим є більш низький ступінь перехресної зшивки. У деяких випадках більш високий ступінь перехресної зшивки забезпечує більш тривале уповільнене вивільнення. Більш високий ступінь перехресної зшивки може забезпечувати більш густий гідрогель і більш тривалий період доставки лікарського засобу. Для одержання гідрогелю з бажаними властивостями може бути використане будь-яке 24 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 співвідношення полімера та агента перехресної зшивки (наприклад, метакриловий ангідрид). Наприклад, співвідношення полімера та агента перехресної зшивки може бути, наприклад, 8:1, 16:1, 24:1, або 32:1. Наприклад, якщо гідрогелевим полімером є желатин, а агентом перехресної зшивки є метакрилат, то можуть бути використані співвідношення метакриловий ангідрид:желатин 8:1, 16:1, 24:1 або 32:1. 10. Можливості терапевтичного застосування мутантних поліпептидів FGF21 Мутантні поліпептиди FGF21 можна застосовувати для лікування, діагностики, полегшення або профілактики багатьох захворювань або патологічних станів, включаючи порушення обміну речовин, але не обмежуючись цим. В одному з варіантів здійснення винаходу порушення обміну речовин, що підлягає лікуванню, являє собою цукровий діабет, наприклад, діабет 2 типу. В іншому варіанті здійснення винаходу порушенням обміну речовин є ожиріння. Інші варіанти здійснення винаходу спрямовані на такі метаболічні стани або порушення як дисліпідемія, гіпертонія, гепатостеатоз, зокрема, неалкогольний гепатостеатоз (NASH), серцево-судинне захворювання, зокрема, атеросклероз, та вікові зміни обміну речовин. У прикладному варіанті здійснення винаходу таке захворювання/патологічний стан, як цукровий діабет або ожиріння, можна лікувати за допомогою введення хворому, що потребує такого лікування, мутантного поліпептиду FGF21 у терапевтично ефективній дозі, як описано в даному документі. Введення можна здійснити відповідно до способів, описаних в даному документі, зокрема, за допомогою внутрішньовенної ін'єкції, внутршньочеревної ін'єкції, внутрішньом'язової ін'єкції або перорально у вигляді таблеток або рідкого лікарського складу. У більшості ситуацій необхідну дозу може визначити клініцист, як описано в даному документі, при цьому необхідна доза являє собою терапевтично ефективну дозу мутантного поліпептиду FGF21. Кваліфікованому фахівцю буде очевидно, що терапевтично ефективна доза мутантного поліпептиду FGF21 буде залежати, серед всього іншого, від графіка введення, від стандартної дози агента, що вводиться, від того, або вводять молекулу нуклеїнової кислоти або поліпептиду в комбінації з іншими терапевтичними засобами, від імунного статусу і загального стану здоров'я реципієнта. Термін "терапевтично ефективна доза" при вживанні в даному документі означає, що кількість мутантного поліпептиду FGF21, що викликає біологічну або медичну реакцію в тканинній системі, в організмі тварини або людини, яку намагається визначити дослідник, лікар, який лікує, або інший клініцист, викликає полегшення симптомів захворювання або розладу, який підлягає лікуванню. 11. Антитіла В обсязі даного винаходу розглядаються антитіла та фрагменти антитіл, що специфічно зв'язуються з мутантними поліпептидами FGF21 за даним винаходом, але не дають специфічного зв'язування з поліпептидами FGF21 дикого типу. Антитіла можуть бути поліклональными, включаючи специфічні поліклональні, моноклональними (MAb), рекомбінантними, химерними, гуманізованимии, такими, як антитіла з пересадженою гіперваріабельною ділянкою (CDR), антитілами людини, одноланцюговими та/або біспецифічними, а також можуть являти собою їх фрагменти, варіанти або хімічно модифіковані молекули. Фрагменти антитіл включають ті частини антитіла, що специфічно зв'язуються з епітопом на мутантному поліпептиді FGF21. Приклади таких фрагментів включають фрагменти Fab і F(ab'), одержані в результаті ферментативного розщеплення поінорозмірних антитіл. Інші зв'язувальні фрагменти включають фрагменти, одержані методиками рекомбінантних ДНК, такими, як експресія рекомбінантних плазмід, що містять послідовності нуклеїнової кислоти, які кодують варіабельні ділянки антитіла. Термін "специфічне зв'язування, ” при використанні в контексті антитіла, означає, що антитіло зв'язує свою мішень у присутності гетерогенної популяції або білків іншого біологічного матеріалу. Більш конкретно, якщо антитіло специфічно зв'язує свою мішень, це означає, що в попередньо визначених умовах імуноаналізу, дане антитіло зв'язує свою мішень і не зв'язує в значній кількості інші білки, присутні в даній пробі. Для ідентифікації антитіла, що специфічно зв'язує свою мішень, може бути застосований будь-який зручний формат імуноаналізу, наприклад, твердофазні імуноаналізи ELISA. Див., наприклад, Harlow and Lane (1988) Antibodies, A Laboratory Manual, Cold Spring Harbor Publications, New York. Поліклональні антитіла, спрямовані на FGF21 мутантний поліпептид, загалом, продукуються у тварин (наприклад, кролики або миші) за допомогою множинних підшкірних або внутрішньочеревних ін'єкцій мутантного поліпептиду FGF21 та ад'юванта. Може виявитися корисним кон'югувати мутантний поліпептид FGF21 з білковим носієм, що є імуногеном для імунізованого біологічного виду, таким, як гемоціанин лімфи равлика, сироватковий альбумін, тіреоглобулин великої рогатої худоби або соєвий інгібітор трипсину. Для посилення імунної відповіді також використовують агрегуючі агенти, такі, як галун. Після імунізації у тварин беруть зразки крові і 25 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 проводять аналіз сироватки на титр антитіла проти мутантного FGF21. Моноклональні антитіла, спрямовані на мутантні поліпептиди FGF21, можна здійснювати будь-яким способом, що передбачає вироблення молекул антитіла безперервною клітинною лінією в культурі. Приклади придатних способів для вироблення моноклональних антитіл включають способи гибрідоми, описані Kohler et al., 1975, Nature 256: 495-97 і спосіб гибридоми з B-клітин людини (Kozbor, 1984, J. Immunol. 133: 3001; Brodeur et al., Monoclonal Antibody Production Techniques and Applications 51-63 (Marcel Dekker, Inc., 1987). Даний винахід також пропонує клітинні лінії, що виробляють моноклональні антитіла, що реагують з мутантними поліпептидами FGF21. Моноклональні антитіла за даним винаходом можна модифікувати для застосування як лікарських засобів. В одному з варіантів здійснення винаходу моноклональне антитіло являє собою "химерне" антитіло, в якому частина важкого (H) та/або легкого(L) ланцюга ідентична або гомологична відповідній послідовності в антитілах, одержаних від визначеного біологічного виду або належних до особливого класу/підкласу антитіл, тоді як інша частина ланцюга (ланцюгів) ідентична або гомологична відповідній послідовності в антитілах, одержаних від іншого біологічного виду або належних до іншого класу/ підкласу антитіл. Сюди ж можна включити фрагменти таких антитіл, що здатні виявляти необхідну біологічну активність. Див., наприклад, патент США № 4816567, Morrison et al., 1985, Proc. Natl. Acad. Sci. U.S.A. 81: 6851-55. В іншому варіанті здійснення моноклональне антитіло за даним винаходом являє собою "гуманізоване" антитіло. Способи гуманізації антитіл, що походять не від людини, добре відомі в даній галузі техніки. Див., наприклад, патенти США №№ 5585089 та 5693762. Зазвичай гуманізоване антитіло має один або більше амінокислотних залишків, вбудованих у нього з джерела нелюдського походження. Гуманізацію можна провести, наприклад, застосовуючи способи, описані в даній галузі техніки (див., наприклад, Jones et al., 1986, Nature 321: 522-25; Riechmann et al., 1998, Nature 332: 323-27; Verhoeyen et al., 1988, Science 239: 1534-36), за допомогою заміщення, щонайменше, частини гіперваріабельної ділянки антитіла гризуна відповідними ділянками з антитіла людини. Винахід також охоплює антитіла людини, що зв'язують мутантні поліпептиди FGF21 за даним винаходом. Використовуючи трансгенні тварини (наприклад, мишей), що здатні виробляти набір антитіл людини за відсутності ендогенного вироблення імуноглобуліну, такі антитіла одержують, шляхом імунізації тварин антигеном, одержаним з мутанта FGF21 (тобто, антигеном, що має, щонайменше, 6 суміжних амінокислот), факультативно з'єднаних з носієм. Див., наприклад, Jakobovits et al., 1993, Proc. Natl. Acad. Sci. U.S.A. 90: 2551-55; Jakobovits et al., 1993, Nature 362: 255-58; Bruggermann et al., 1993, Year in Immuno. 7:33. В одному зі способів такі трансгенні тварини одержують, виводячи з ладу ендогенні локуси, що кодують у них важкі та легкі ланцюги імуноглобуліну, і вставляючи в їх геном локуси, що кодують білки важких і легких ланцюгів людини. Потім частково модифіковані тварини, тобто, тварини, що мають неповний комплект модифікацій, схрещують, щоб одержати тварин, що мають всі необхідні модифікації імунної системи. При введенні імуногену ці трансгенні тварини виробляють антитіла з амінокислотними послідовностями людини (скоріше ніж, наприклад, з мишачими), включаючи варіабельні ділянки, імуноспецифічні для цих антигенів. Див., наприклад, міжнародні патентні публікації №№ WO 96/33735 та WO 94/02602. Додаткові способи описані в патенті США № 5545807, міжнародних патентних публікаціях №№ WO 91/10741 та WO 90/04036, а також в європейському патенті № 0 546 073. Антитіла людини також можна виробляти за допомогою експресії рекомбінантної ДНК у клітинах-хазяєвах або експресії в клітинах гибрідоми, як описано в даному документі. В альтернативному варіанті здійснення винаходу антитіла людини також можна одержувати з бібліотек фагового дисплея (див., наприклад, Hoogenboom et al., 1991, J. MoI Biol. 227: 381; Marks et al., 1991, J. MoI Biol. 222: 581). Ці процеси імітують імунний відбір через демонстрацію репертуару антитіл на поверхні нитковидного бактеріофага і наступний відбір фага за допомогою його зв'язування з антигеном відбору. Химерні антитіла, антитіла з пересадженим CDR та гуманізовані антитіла зазвичай одержують рекомбінантними способами. Нуклеїнові кислоти, що кодують антитіла, вводять в клітини-хазяєва та експресують, застосовуючи матеріали і процедури, описані в даному документі. В одному з варіантів здійснення винаходу антитіла виробляють у клітинах-хазяєвах ссавця, таких, як клітини CHO. Моноклональні (наприклад, людські) антитіла можна одержувати за допомогою експресії рекомбінантної ДНК у хазяєвах або у клітинах гибрідоми, як описано в даному документі. Антитіла проти мутанта FGF21 за даним винаходом можна використовувати в будь-якому відомому способі аналізу для виявлення і кількісної оцінки мутантних поліпептидів FGF21, 26 UA 107458 C2 5 10 15 20 25 30 35 40 45 50 55 60 такому, як аналізи конкурентного зв'язування, прямі і непрямі сендвич-аналізи та аналізи імунопреципітації (див., наприклад, публікацію Sola, Monoclonal Antibodies: A Manual of Techniques 147-158 (CRC Press, Inc., 1987), включену в цей документ як посилання у всій повноті її вмісту). Антитіла будуть зв'язувати мутантні поліпептиди FGF21 з афінністю, що відповідає використовуваному методу аналізу. При діагностичному використанні в деяких варіантах здійснення винаходу антитіла проти мутантів FGF21 можна позначити компонентом, що виявляють. Компонент, що виявляють, може являти собою будь-який компонент, що здатний створювати прямим або непрямим чином сигнал, що піддається виявленню. Наприклад, компонентом, що виявляють, може бути 3 14 32 35 125 99 111 67 радіоізотоп, такий як H, C, P, S, I, Tc, In або Ga, флуоресцентна або хемілюмінесцентна сполука, така, як флуоресцинізотіоціанат, родамін або люциферін, а також фермент, такий, як лужна фосфатаза, β-галактозидаза або пероксидаза хрону (Bayer et al., 1990, Meth. Enz. 184: 138-63). Аналізи з конкурентним зв'язуванням засновані на здатності міченого стандарту (наприклад, мутантного поліпептиду FGF21 або його імунологічно реактивної частини) конкурувати з випробуваним продуктом, який аналізують, (наприклад, мутантним поліпептидом FGF21) за зв'язування з обмеженою кількістю антитіла проти мутанта FGF21. Кількість мутантного поліпептиду FGF21 у випробуваному зразку зворотно пропорційно кількості стандарту, що вступає в зв'язок з антитілами. Для того, щоб полегшити визначення кількості зв'язаного стандарту, антитіла зазвичай інсобілізують (переводять у нерозчинну форму) до або після конкуренції, щоб стандарт та продукт, що аналізують, зв'язані з антитілами, було зручно відділити від стандарту та продукту, що аналізують, які залишилися незв'язаними. Сендвіч-аналізи зазвичай включають використання двох антитіл, кожне з який здатне зв'язуватися із самостійною імуногенною частиною або епітопом білка, що підлягає виявленню або кількісній оцінці. У сендвіч-аналізі зразок, який тестують, аналізованого продукту зазвичай зв'язується з першим антитілом, що іммобілізовано на твердій опорі, а потім друге антитіло зв'язується з аналізованим продуктом, формуючи в такий спосіб комплекс з трьох частин. Див., наприклад, патент США № 4376110. Друге антитіло, саме по собі, може бути мічено компонентом, що виявляють, (прямі сендвіч-аналізи) або вимірюватися із застосуванням антитіла проти імуноглобуліну, що мічено компонентом, що виявляють, (непрямі сендвічаналізи). Наприклад, одним з типів сендвіч-анализа є твердофазний імуноферментний аналіз (ELISA), у якому компонент, що виявляють, являє собою фермент. Антитіла проти мутанта FGF21 за даним винаходом також корисні для одержання візуальних зображень in vivo. Антитіло, мічене компонентом, що виявляють, можна ввести тварині, переважно в кровоток, з наступною оцінкою наявності і локалізації міченого антитіла в організмі хазяїна. Антитіло можна позначити будь-яким компонентом, що піддається виявленню у тварини, способами ядерного магнітного резонансу, радіології або іншими засобами виявлення, відомими в даній галузі техніки. Антитіла до мутантів FGF21 за даним винаходом можна використовувати як лікарські засоби. Терапевтичні агенти зазвичай є агоністами або антагоністами в тому сенсі, що вони або підсилюють, або послабляють, відповідно, щонайменше, одну з біологічних активностей мутантного поліпептиду FGF21. В одному з варіантів здійснення антагоністичні антитіла за даним винаходом являють собою антитіла або їх зв'язуючі фрагменти, що здатні до специфічного зв'язування з мутантним поліпептидом FGF21 і які здатні пригничувати або усувати функціональну активність мутантного поліпептиду FGF21 in vivo або in vitro. У деяких варіантах здійснення винаходу антагоністичне антитіло буде пригничувати функціональну активність мутантного поліпептиду FGF21, щонайменше, приблизно на 50 % та, переважно, щонайменше, приблизно на 80 %. Ще в одному варіанті здійснення винаходу антитіло проти мутанта здатно втручатися у взаємодію між мутантним поліпептидом FGF21 та рецептором FGF, таким чином, пригнічуючи або усуваючи активність мутантного поліпептиду FGF21 in vitro або in vivo. Агоністичні та антагоністичні антитіла проти мутанта FGF21 ідентифікують аналізами скринінгу, які добре відомі в даній галузі техніки. Винахід також відноситься до набору, що включає антитіла проти мутанта FGF21 і інші реактиви, корисні для виявлення рівня мутантного поліпептиду FGF21 у біологічних зразках. Такі реактиви можуть включати мітку, що виявляють, яка блокує сироватку, позитивні та негативні контрольні зразки, а також реактиви для виявлення. ПРИКЛАДИ Наведені нижче приклади ілюструють специфічні варіанти здійснення винаходу та різних варіантів його застосування. Вони сформульовані тільки з метою пояснення, і їх не слід сприймати як обмежуючу сферу дії винаходу будь-яким чином. 27 UA 107458 C2 5 ПРИКЛАД 1 Виготовлення конструкцій для експресії FGF21 Послідовність нуклеїнової кислоти, що кодує зрілий поліпептид FGF21, одержували за допомогою ампліфікації в полімеразній ланцюгової реакції (ПЦР) з використанням праймерів, що мають нуклеотидні послідовності, які відповідають 5' і 3' кінцям послідовності зрілого FGF21. Таблиця 2 перелічує праймери, використані ампліфікації послідовності зрілого FGF21. Таблиця 2 Праймери ПЦР для конструкції FGF21 Праймер Послідовність SEQ ID NO: Сенсовий 5'–AGGAGGAATAACATATGCATCCAATTOOAGATTCTTCTCC–3' 12 Антисенсовий 5'–TAGTGAGCTCGAATTCTTAGGAAGCGTAGCTGG–3' 13 10 15 20 25 30 35 40 45 50 Праймери, використані для виготовлення конструкції, що експресує зрілий FGF21, включали сайти рестрикційної ендонуклеази (сайт NdeI також містить N-кінцевий метіонін для бактеріальної експресії) для спрямованого клонування послідовності в придатний вектор експресії (наприклад, pET30 (Novagen/EMD Biosciences; Сан-Дієго, штат Каліфорнія) або pAMG33 (Amgen; Саузенд Оукс, штат Каліфорнія)). Вектор експресії pAMG33 містить низькокопійну точку початку реплікації R-100, модифікований промотор lac та ген стійкості до канаміцину. Вектор експресії pET30 містить точку початку реплікації, одержану з pBR322, індукуємий промотор T7 та ген стійкості до канаміцину. Було виявлено, що експресія з pAMG33 вище, але pET30 є більш надійним вектором для клонування. Таким чином, більшість конструкцій, описаних у даній заявці, спочатку були створені в pET30, а потім піддані скринінгу на ефективність. Після цього відібрані послідовності були перенесені в pAMG33 для подальшої ампліфікації. Послідовність FGF21 була ампліфікована в реакційній суміші, що містить 40,65 мкл dH 2O, 5 мкл реакційного буфера PfuUltra II Reaction Buffer (10×), 1,25 мкл суміші dNTP (40 мМ - 4×10 мМ), 0,1 мкл матриці (100 нг/мол), 1 мкл праймера 1 (10 мкм), 1 мкл праймера 2 (10 мкм) і 1 мкл з'єднуючої ДНК-полімерази HS PfuUltra II (Stratagene, Ла-Хойя, штат Каліфорнія). Реакції ампліфікації проводили з нагріванням протягом двох хвилин при 95 °C, що супроводжується десятьма циклами при 95 °C протягом 20 секунд, 60 °C протягом 20 секунд (з додатковим вирахуванням 1 °C на цикл) та 72 °C протягом 15 секунд на кілобазу потрібного продукту, після чого проводили 20 циклів при 94 °C протягом 20 секунд, 55 °C протягом 20 секунд та 72 °C протягом 15 секунд на кілобазу потрібного продукту, а потім 72 °C протягом 3 хвилин. Продукти ампліфікації розщеплювали рестрикційними ендонуклеазами Ndel, Dpnl та EcoRI, вшивали у придатний вектор, а потім вбудовували в компетентну клітину для її трансформації. ПРИКЛАД 2 Очищення білків FGF21, одержаних з бактерій У наступних прикладах різні білки FGF21, включаючи поліпептид FGF21 дикого типу, усічені поліпептиди FGF21, мутанти FGF21 і гібридні білки FGF21, були експресовані в бактеріальній системі експресії. Після експресії, що описана нижче, білки FGF21 були очищені, як описано в цьому прикладі, якщо спеціально не зазначене інше. Для очищення поліпептиду FGF21 дикого типу, усічених поліпептидів FGF21 та мутантів FGF21 від бактеріальних тілець включень двічі відмиті тільця включень (DWIB) солюбілізували в солюбілізаційному буфері, що містить гуанідину гідрохлорид та DTT у буфері Tris при pH 8,5. Їх потім перемішували протягом однієї години при кімнатній температурі, і солюбілізовану суміш додавали до буфера для рефолдингу, що містить сечовину, аргінін, цистеїн та цистаміну гідрохлорид при pН 9,5, а потім перемішували 24 години при 5 °C (див., наприклад, Clarke, 1998, Curr. Opin. Biotechnol. 9: 157-63; Mannall et al., 2007, Biotechnol. Bioeng. 97: 1523-34; Rudolph et al., 1997, "Folding proteins, " Protein Function: A Practical Approach (Creighton, ed., New York, IRL Press) 57-99; та Ishibashi et al., 2005, Protein Expr. Purif. 42: 1-6). Після солюбілізації та рефолдинга суміш пропускали через фільтр з розміром комірок 0,45 мікрона. Потім концентрацію пула рефолдинга збільшували приблизно в 10 разів, використовуючи для цього касету, що відокремлює, Pall Omega, з молекулярною масою 10 кДа при трансмембранному тиску (TMP) 20 psi, а також проводили діафільтрацію з 3 обсягами колонки 20 мм Tris, pН 8,0 при TMP 20 psi. Після цього очищений зразок піддавали аніонообмінній хроматографії (AEX) із застосуванням смоли Q Sepharose HP. Лінійний сольовий градієнт від 0 до 250 мМ NaCl у 20 мМ 28
ДивитисяДодаткова інформація
Назва патенту англійськоюMutants and uses thereof
Автори англійськоюBelouski, Edward, John, Ellison, Murielle, Marie, Hamburger, Agnes, Eva, Hecht, Randy Ira, Li, Yue-Sheng, Michaels, Mark Leo, Sun, Jeonghoon, Xu, Jing
Автори російськоюБелоуски Эдвард Джон, Эллисон Мюриель Марие, Хамбургер Агнес Ева, Хетч Ренди Ира, Ли Юе-Шенг, Майклз Марк Лео, Сун Йеонгхун, Ксу Йинг
МПК / Мітки
МПК: A61K 38/18, C07K 14/50
Мітки: застосування, fgf21, мутанти
Код посилання
<a href="https://ua.patents.su/389-107458-mutanti-fgf21-ta-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Мутанти fgf21 та їх застосування</a>
Попередній патент: Похідні піразолу
Наступний патент: Карбоксамідні сполуки і їх застосування як інгібіторів кальпаїну
Випадковий патент: Спосіб екстракції днк з тканин тваринного походження для генетичного аналізу за допомогою полімеразної ланцюгової реакції