Спосіб одержання 3-трихлорометил-1,4,2-бензодитіазин-1,1-діоксидів і 3-трихлорометил-4,1,2-бензоксатіазин-1,1-діоксидів
Номер патенту: 57364
Опубліковано: 25.02.2011
Автори: Шалімов Олександр Олександрович, Онисько Петро Петрович, Синиця Анатолій Данилович, Лобанов Сергій Володимирович
Формула / Реферат
Спосіб одержання 3-трихлорометил-1,4,2-бензодитіазин-1,1-діоксидів і 3-трихлорометил-4,1,2-бензоксатіазин-1,1-діоксидів загальної формули (1):
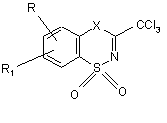 , (1)
, (1)
де: Х = О; R = Н, R1 = 6-ОН; R = Н, R1 = 6-OCH3; R = 6-OCH3, R1 = 8-OCH3,
Х = S; R = R1= H; R = H, R1 = 5-Cl; R = H, R1 = 7-Cl; R = H, R1 = 6-OCH3; R = 5-CH3,
R1 = 7-CH3; R = 5-СН3, R1 = 8-CH3,
який відрізняється тим, що препаративно доступний N-хлоросульфонілтрихлороацетимідоїлхлорид вводять в реакцію з фенолами або тіофенолами, з подальшою обробкою проміжних імідатів або тіоімідатів хлоридом алюмінію в органічному розчиннику при температурі 15-83 °С протягом 12-96 годин, з наступним виділенням цільових продуктів звичайними методами.
Текст
Спосіб одержання 3-трихлорометил-1,4,2бензодитіазин-1,1-діоксидів і 3-трихлорометил4,1,2-бензоксатіазин-1,1-діоксидів загальної формули (1): де: Х = О; R = Н, R1 = 6-ОН; R = Н, R1 = 6-OCH3; R = 6-OCH3, R1 = 8-OCH3, Х = S; R = R1= H; R = H, R1 = 5-Cl; R = H, R1 = 7-Cl; R = H, R1 = 6-OCH3; R = 5-CH3, R1 = 7-CH3; R = 5-СН3, R1 = 8-CH3, який відрізняється тим, що препаративно доступний N-хлоросульфонілтрихлороацетимідоїлхлорид вводять в реакцію з фенолами або тіофенолами, з подальшою обробкою проміжних імідатів або тіоімідатів хлоридом алюмінію в органічному розчиннику при температурі 15-83 °С протягом 1296 годин, з наступним виділенням цільових продуктів звичайними методами. R N (13) S O I 57364 Корисна модель відноситься до органічної хімії, а саме до нового та зручного методу синтезу 4,1,2-бензоксатіазинів та 1,4,2-бензодітіазинів загальної формули (1): R CCl3 X S R1 O N O , I (1) де: Х=О; R=H, R1=6-OH; R=H, R1=6-OCH3; R=6OCH3, R1=8-OCH3. Х=S; R=R1=Н; R=Н, R1=5-Сl; R=H, R1=7-Cl; R=H, R1=6-OCH3; R=5-CH3, R1=7-CH3; R=5-СН3, R1=8CH3. Названі сполуки, їх властивості та застосування в патентних виданнях і науковій літературі не описані. Чисельні публікації за останнє десятиліття свідчать, що гетероциклічні системи з 1,4,2бензодітіазиновим і 4,1,2-бензоксатіазиновим циклом можуть знайти застосування як біологічно активні речовини, а також як базові системи для дизайну та синтезу речовин із потенційною фармакологічною дією. Зокрема, в ряду похідних наведених гетероциклічних систем виявлені високоселективні інгібітори росту лейкемічних клітин [1], а також ефективні (11) , , (1) UA O (19) R1 U CCl3 X 3 57364 інгібітори ферменту ВІЛ-1 інтегрази [2], що створює позитивні передумови для їх використання при лікуванні раку та СНІДу. В той же час представники 4,1,2-бензоксатіазинів проявляють гіпоглікемічну активність [3]. Найближчими структурними аналогами сполук, які заявляються, є похідні (2), де Х=О,S; R=Alk,Ar,NAlk2. R X S N O O , (2) II В науковій літературі описані два підходи до синтезу сполук формули (2), ці підходи є багатоступеневими і вимагають застосування важкодоступних реагентів. У першому [1] використовуються 2-меркапто- або 2-гідроксибензолсульфаміди, які одержуються багатостадійними синтезами. Другий метод [4] базується на циклізації продуктів реакції хлоросульфонілізоціанату і S-(О)-арил-N,Nдіалкіл(ді)тіокарбаматів. Суттєвим недоліком такого підходу є те, що він придатний лише для синтезу похідних (2), де R=NAlk2. При цьому очистка цільових продуктів здійснюється за допомогою (3) + Ar 4 колонкової хроматографії, що значно обмежує їх препаративні масштаби. До недоліків способу слід також віднести використання хлоросульфонілізоціанату, вартість якого достатньо висока. Задачею корисної моделі є спосіб отримання гетероциклічних систем ряду 4,1,2бензоксатіазина та 1,4,2-бензодітіазина на основі нового біелектрофільного реагенту CCl3C(Cl)=NSO2Cl (3). Задача досягається за рахунок циклізації продуктів реакції N-хлоросульфонілтрихлороацетімідоїлхлориду з комерційно доступними фенолами або тіофенолами в умовах реакції ФріделяКрафтса. Спосіб одержання сполук, які заявляються, полягає в тому, що N-хлоросульфонілтрихлороацетімідоїлхлорид (3), який може бути одержаний з доступних трихлороацетилізоціанату та хлоросульфонової кислоти, вводять в реакцію з фенолами або тіофенолами, з подальшою обробкою проміжних імідатів або тіоімідатів (4) хлоридом алюмінію в органічному розчиннику при температурі 15-83°С протягом 12-96 годин. Виходи кінцевих продуктів сягають 19-79%. Метод реалізований в однореакторному варіанті без виділення проміжних імідатів й тіоімідатів (4). CCl3 XH AlCl3 N SO2Cl - HCl (1) - HCl X Ar (4) Х=О, S; Аr=С6Н5, 3-НОС6Н4, 3-СН3ОС6Н4, 3,5(СН3О)2С6Н3, 2-СlС6Н4, 4-СlС6Н4, 2,4-(СН3)2С6Н3, 2,5-(СН3)2С6Н3 Запропонований підхід є синтетичною реалізацією хемоселективного заміщення імідоїльного атому хлору в біелектрофільному реагенті (3) з наступною внутрішньо-молекулярною електрофільною циклізацією проміжних імідатів або тіоімідатів (4) з утворенням гетероциклічних сполук формули (1), які можуть знайти практичне застосування як перспективні біорегулятори. Отриманий результат не був заздалегідь передбачуваним, оскільки, базуючись на літературних даних [5], не виключалась можливість реакції на першій стадії по сульфонільному реакційному центру. Не було також очевидним утворення циклу на другій стадії, враховуючи можливість одержання сполук лінійного типу. Насправді ж, обидві стадії процесу в запропонованій схемі характеризується високою регіоселективністю. Його первинними продуктами є імідати та тіоімідати (4), які при дії хлориду алюмінію з високими виходами перетворюються в цільові сполуки формули (1). Будова та склад всіх отриманих сполук доведені даними спектрів ядерного магнітного резонансу та елементним аналізом. Додатковим підтвердженням утворення 1,4,2-бензодітіазинової системи є також розщеплення 3-трихлорометил1,4,2-бензодітіазин-1,1-діоксиду під дією лугу з утворенням відомого [6] 2-меркаптобензолсульфаміду. Корисна модель ілюструється загальними методами одержання 6-гідрокси-, 6-метокси-, 6,8діметокси-3-трихлорометил-4,1,2-бензоксатіазин1,1-діоксидів, 5-хлоро-, 7-хлоро- та 5,7-диметил-3трихлорометил-1,4,2-бензодітіазин-1,1-діоксидів, та фізико-хімічними характеристиками всіх синтезованих сполук. Приклад 1. N-Хлоросульфонілтрихлороацетамід CCl3CONHSO2Cl. До 0,503 моля трихлороацетилізоціанату [7] додають при перемішуванні 0,518 моля свіжоперегнаної хлоросульфонової кислоти, суміш нагрівають протягом 30 хвилин при 130°С до початку екзотермічної реакції та бурхливого виділення діоксиду вуглецю. Через 3 години реакційну суміш розтирають з 150 см3 дихлорометану, осад відфільтровують та промивають 50 см3 дихлорометану. Вихід 86%, т. топл. 125-127°С. Спектр ЯМР1Н (CDCl3), , м.ч.: 9,65 уш.с. Спектр ЯМР 13С (CDCl3), , м.ч.: 89,39 (ССl3), 164,83 (С=О). Знайдено, %: СІ 53,57; N 5,31; S 12,56. C2HCl4NO3S. Вирахувано, %: СІ 54,35; N 5,37; S 12,29. Приклад 2. 5 N-Хлоросульфонілтрихлороацетімідоїлхлорид (3). Суміш 0,138 моля N-хлоросульфонілтрихлороацетаміду, 0,138 моля пентахлориду фос3 фору та 50 см хлороксиду фосфору нагрівають при кипінні протягом 20 годин. Хлороксид фосфору відганяють при атмосферному тиску, залишок переганяють у вакуумі. Вихід 93%, т. кип. 131132°С (10 мм рт.ст.), т. топл. 47-48°С. Спектр ЯМР 13 С (CDCl3), , м.ч.: 91,34 (ССl3), 156,73 (C=N). Знайдено, %: СІ 62,45; S 11,42. C2Cl5NO2S. Вирахувано, %: СІ 63,45; S 11,48. Приклад 3. Загальний спосіб одержання 3трихлорометил-4,1,2-бензоксатіазин-1,1-діоксидів. До розчину 0,01 моля N-хлоросульфонілтрихлороацетімідоїлхлориду в 20 см3 дихлороетана при перемішуванні додають 0,01 моля відповідного фенолу в 20 см3 дихлороетана, суміш нагрівають при 83°С 4 години, до охолодженої суміші додають 2 г безводного хлориду алюмінію та залишають на 3 доби при кімнатній температурі. Розчинник видаляють у вакуумі, залишок розтирають з 50 см3 води. Суміш декантують, осад обробляють 30 см3 50% холодного водного метанолу, швидко відфільтровують, промивають на фільтрі холодним 50% метанолом (35 см3). 6-Гідрокси-3-трихлорометил-4,1,2-бензоксатіазин-1,1-діоксид. Вихід 56%, т. топл. 144°С. Спектр ЯМР1Н (CDCl3), , м.ч.: 6,80 д, (J 2,0 Гц) 1Н (Н5), 6,85 дд, (J 9,5 Гц, J 2,0 Гц) 1Н (Н7), 8,26 д, (J 9,5 Гц) 1H (Н8), 11,30 с, 1Н (НО). Спектр ЯМР 13С (CDCl3), , м.ч.: 93,81, 103,74, 106,08, 114,45, 132,47, 157,68, 166,20, 168,16. Знайдено, %: S 10,19; СІ 33,57. C8H4Cl3NO4S. Вирахувано, %: S 10,12; СІ 33,60. 6-Метокси-3-трихлорометил-4,1,2-бензоксатіазин-1,1-діоксид. Вихід 54%, т. топл. 119°С (бензол). Спектр ЯМР 1Н (CDCl3), , м.ч.: 3,95 с, 3Н, (ОСН3), 6,83 д, (J 2,4 Гц) 1Н (Н5), 6,92 дд, (J 9,3 Гц, J 2,4 Гц) 1Н (H7), 8,36 д, (J 9,3 Гц) 1Н (Н8). Спектр ЯМР 13С (CDCl3), 6, м.ч.: 56,70, 93,76, 103,92, 104,55, 113,37, 132,03, 157,81, 167,26, 167,86. Знайдено, %: S 9,74; С1 32,11. C9H6Cl3NO4S. Вирахувано, %: S 9,70; С1 32,17. 6,8-Діметокси-3-трихлорометил-4,1,2-бензоксатіазин-1,1-діоксид. Вихід 48%, т. топл. 158°С (бензол). Спектр ЯМР 1Н (CDCl3), , м.ч.: 3,91 с, 3Н, (6-ОСН3), 3,93 с, 3Н, (8-ОСН3), 6,35 д, (J 2,3 Гц) 1Н (Н5), 6,49 д, (J 2,3 Гц) 1H (Н7). Знайдено, %: S 8,90; СІ 29,52. C10H8Cl3NO5S. Вирахувано, %: S 8,89; СІ 29,49. Приклад 4. Загальний спосіб одержання 3трихлорометил-1,4,2-бензодітіазин-1,1-діоксидів. До розчину 0,05 моля N-хлоросульфоніл3 трихлороацетімідоїлхлориду в 75 см дихлороетана додають 0,05 моля відповідного тіофенолу, через 4 години до суміші додають 7 г безводного хлориду алюмінію і реакційну суміш нагрівають при 83°С протягом 96 годин. Розчинник видаляють у вакуумі, до залишку додають 200 см3 води, осад відфільтровують, промивають водою (550 см3) та 57364 6 розтирають з 50 см3 метанолу. Осад відфільтровують, промивають бензолом (320 см3), розчиняють в 60 см3 дихлорометана, домішки відфільтровують, продукт одержують після випарювання фільтрату. За необхідності продукт кристалізують з бензолу. 5-Хлоро-3-трихлорометил-1,4,2-бензодітіазин1,1-діоксид. Вихід 25%, т. топл. 153°С. Спектр ЯМР1H (CDCl3), , м.ч.: 7,69 т, (J 7,9 Гц) 1H (Н7), 7,80 дд, (J 7,9 Гц, J 1,3 Гц) 1Н (Н6), 8,18 дд, (J 7,9 Гц, J 1,3 Гц) 1Н (Н8). Знайдено, %: S 18,40; СІ 40,37. C8H3Cl4NO2S2. Вирахувано, %: S 18,27; СІ 40,40. 7-Хлоро-3-трихлорометил-1,4,2-бензодітіазин1,1-діоксид. Вихід 19%, т. топл. 235-236°С (розкл). Спектр ЯМР 1Н (CDCl3+DMSO-D6 (20:1)), , м.ч.: 7,48 дд, (J 8,6 Гц, J 2,3 Гц) 1Н (H5), 7,76 д, (J 8,6 Гц) 1Н (Н6), 8,15 д, (J 2,3 Гц) 1Н (Н8). Спектр ЯМР 13С (DMSO-D6), , м.ч.: 97,11 (ССl3), 128,21 (СН), 129,84 (СН), 131,18 (С7), 131,78 (СН), 133,64 (C-S), 142,46 (C-SO2), 164,22 (C=N). Знайдено, %: S 18,33; СІ 40,42. C8H3Cl4NO2S2. Вирахувано, %: S 18,27; СІ 40,40. 5,7-Диметил-3-трихлорометил-1,4,2-бензодітіазин-1,1-діоксид. Вихід 43%, т. топл. 142°С. Спектр ЯМР 1Н (CDCl3), , м.ч.: 2,47 с, 3Н, (СН3), 2,49 с, 3Н, (СН3), 7,39 с, 1H (Н6), 7,91 с, 1Н (Н8). Спектр ЯМР 13С (CDCl3), , м.ч.: 19,30 (СН3), 21,30 (СН3), 95,01 (ССl3), 124,12 (СН), 124,87 (С-СН3), 127,00 (С-СН3), 135,94 (СН), 136,81 (C-S), 141,27 (C-SO2), 173,05 (C=N). Знайдено, %: S 18,74; СІ 30,91. C10H8Cl3NO2S2. Вирахувано, %: S 18,61; СІ 30,86. Приклад 5. 3-Трихлорометил-1,4,2-бензодітіазин-1,1-діоксид. До розчину 0,052 моля N-хлоросульфонілтрихлороацетімідоїлхлориду в 50 см3 дихлорометана при 15°С і перемішуванні додають 0,052 моля тіофенолу в 20 см3 дихлорометана, через 4 години до суміші добавляють 7 г безводного хлориду алюмінію та залишають на ніч. Розчинник видаляють у вакуумі, залишок розтирають з 150 см3 льодяної води, осад промивають водою та відфільтровують. Вихід 79%, т. топл. 118-119°С (ССl4). Спектр ЯМР 1Н (CDCl3), , м.ч.: 7,28 тд, (J 7,6 Гц, J 1,2 Гц) 1Н (H6), 7,38 тд, (J 7,6 Гц, J 1,2 Гц) 1Н (Н7), 7,45 дд, (J 7,6 Гц, J 1,2 Гц) 1Н (Н5), 8,01 дд, (J 7,6 Гц, J 1,2 Гц) 1Н (Н8). Знайдено, %: С 30,27; Н 1,21; С1 33,72; S 20,49. C8H4Cl3NO2S2 Вирахувано, %: С 30,35; Н 1,27; С1 33,59; S 20,26. Приклад 6. 5,8-Диметил-3-трихлорометил-1,4,2-бензодітіазин-1,1-діоксид. До розчину 0,01 моля N-хлоросульфонілтрихлороацетімідоїлхлориду в 20 см3 дихлорометана при перемішуванні додають 0,01 моля 2,53 диметилтіофенолу в 3 см дихлорометана, через 1 годину до суміші добавляють 1,5 г безводного хлориду алюмінію та залишають на 2 доби при кімнатній температурі (15°С). Розчинник видаляють у вакуумі, залишок обробляють 100 см3 води, осад відфільтровують, промивають водою (620 см3) та метанолом (310 см3). Вихід 78%, т. 7 57364 топл. 183°С (бензол). Спектр ЯМР 1Н (CDCl3), , м.ч.: 2,47 с, 3Н, (5-СН3), 2,79 с, 3Н, (8-СН3), 7,36 д, (J 7,8 Гц) 1Н (Н6), 7,40 д, (J 7,8 Гц) 1Н (Н7). Спектр ЯМР 13С (CDCl3+DMSO-D6 (20:1)), , м.ч.: 20,69 (СН3), 22,61 (СН3), 95,52 (ССІ3), 133,38 (СН), 133,82 (С-СН3), 133,86 (СН), 135,34 (С-СН3), 139,93 (C-S), 143,95 (C-SO2), 168,36 (C=N). Знайдено, %: S 18,66; СІ 30,82. C10H8Cl3NO2S2. Вирахувано, %: S 18,61; СІ 30,86. Приклад 7. 6-Метокси-3-трихлорометил-1,4,2-бензодітіазин-1,1-діоксид. До розчину 0,033 моля N-хлоросульфонілтрихлороацетімідоїлхлориду в 50 см3 дихлороетана при перемішуванні додають 0,033 моля 3метокситіофенолу, через 1 годину до суміші додають 4 г безводного хлориду алюмінію та залишають на 3 доби при кімнатній температурі (20°С). Розчинник видаляють у вакуумі, залишок обробляють 150 см3 води, осад відфільтровують, промивають водою (550 см3) та 50% водним метанолом (220 см3). Вихід 65%, т. топл. 169-170°С (бензол). Спектр ЯМР 1Н (CDCl3), , м.ч.: 3,95 с, 3Н, (СН3), 6,82 д, (J 2,4 Гц) 1Н (Н5), 6,91 дд, (J 9,3 Гц, J 2,4 Гц) 1H, (H7), 8,35 д, (J 9,3 Гц) 1Н, (Н8). Спектр ЯМР 13С (CDCl3+DMSO-D6 (20:1)), , м.ч.: 55,64 (ОСН3), 91,48 (ССІ3), 111,42 (СН), 112,37 (СН), 126,59 (С6) 134,71 (СН), 137,96 (C-S), 159,21 (C-SO2), 163,91(C=N). Знайдено, %: S 18,55; СІ 30,60 C9H6Cl3NO3S2. Вирахувано, %: S 18,50; СІ 30,68. Приклад 8. 2-Меркаптобензолсульфамід. До розчину 0,01 моля 3-трихлорометил-1,4,2бензодітіазин-1,1-діоксиду в 30 см3 метанолу при Комп’ютерна верстка Л. Ціхановська 8 перемішуванні додають 10 см3 20% водного розчину КОН та залишають суміш на ніч. Осад відфільтровують, до фільтрату при 5-10°С додають 20 см3 соляної кислоти, осад, який випав відфільтровують, промивають водою та двічі кристалізують з водного метанолу. Вихід 30%, т. топл. 221-223°С (розкл). Спектр ЯМР 1Н (CDCl3+DMSO-D6 (10:1)), , м.ч.: 6,92 уш.с, 2Н, (NH2), 7,41 т, (J 7,8 Гц) 1H, 7,54 т, (J 7,8 Гц) 1Н, 7,91 д, 1Н, 7,97 д, 1Н. Спектр ЯМР 13С (DMSO-D6), , м.ч.: 127,13 (СН), 127,45 (СН), 128,64 (СН), 132,81 (СН), 134,48 (C-S), 141,87 (C-SO2). Знайдено, %: S 33,65; N 7,31 C6H7NO2S2. Вирахувано, %: S 33,89; N 7,40. Джерела інформації: 1. Brzozowski Z. and Saczewski F. // J. Heterocyclic Chem. - 2005 - V.42 - P.1297-1303. 2. Chih-Ling Kuo, Assefa H., Kamath S., Brzozowski Z., Slawinski J., Saczewski F., Buolamwini J. K., and Neamati N. // J. Med. Chem. 2004 - V.47 - P.385-399 3. Suzue S. and Irikura T. // Chem. Pharm. Bull. 1968. - V. 16(5) - P.806-813. 4. Iwakawa Т., Tamura H., Murabayashi A. and Hayase Y. // Chem. Pharm. Bull - 1991 - V.39(8) P.1939-1943 5. Марковский Л.Н., Шермолович Ю.Г., Шевченко В.И. // ЖОХ. - 1974 - Т.10. - №3. - С.488-493. 6. Willy Meyer, Патент США, US5163996, Publ. 17.11.1992. 7. Зверев В.В., Ильясов А.В., Аминова P.M., Зобова Н.Н., Сагитова Р.Н. // ЖОХ. - 1991 - Т.61. №4. - С.1031-1032. Підписне Тираж 23 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of 3-trichloromethyl-1,4,2-benzodithiazine-1,1-dioxides and 3-trichloromethyl-4,1,2-benzoxathiazine-1,1-dioxides
Автори англійськоюShalimov Oleksandr Oleksandrovych, Lobanov Serhii Volodymyrovych, Onysko Petro Petrovych, Synytsia Anatolii Danylovych
Назва патенту російськоюСпособ получения 3-трихлорометил-1,4,2-бензодитиазин-1,1-диоксидов и 3-трихлорометил-4,1,2-бензоксатиазин-1,1-диоксидов
Автори російськоюШалимов Александр Александрович, Лобанов Сергей Владимирович, Онисько Петр Петрович, Синица Анатолий Данилович
МПК / Мітки
МПК: C07D 285/00, C07D 279/00, C07D 339/00, C07D 327/00
Мітки: спосіб, 3-трихлорометил-4,1,2-бензоксатіазин-1,1-діоксидів, одержання, 3-трихлорометил-1,4,2-бензодитіазин-1,1-діоксидів
Код посилання
<a href="https://ua.patents.su/4-57364-sposib-oderzhannya-3-trikhlorometil-142-benzoditiazin-11-dioksidiv-i-3-trikhlorometil-412-benzoksatiazin-11-dioksidiv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 3-трихлорометил-1,4,2-бензодитіазин-1,1-діоксидів і 3-трихлорометил-4,1,2-бензоксатіазин-1,1-діоксидів</a>
Попередній патент: Пристрій для міжрядної обробки ґрунту афанасьєва
Наступний патент: Спосіб експрес-діагностики порушень ритму серця
Випадковий патент: Магнітний фільтр-осаджувач








