Спосіб одержання заміщених 2-метилсульфоніл-1,3-діарил(гетерил)-проп-2-ен-1-онів
Номер патенту: 57633
Опубліковано: 10.03.2011
Автори: Десенко Сергій Михайлович, Гладков Євгеній Станіславович, Сірко Світлана Миколаївна, Афанасіаді Людмила Михайлівна
Формула / Реферат
Спосіб одержання заміщених 2-метилсульфоніл-1,3-діарил(гетерил)-проп-2-ен-1-онів загальної формули І:
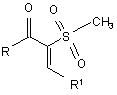 I,
I,
де R=С6Н5, 4-СН3-С6Н4;
R1=С6Н5, 4-СН3-С6Н4, 4-Сl-С6Н4,
4-ОСН3-С6Н4, 4-Вr-С6Н4,
4-F-С6Н4, 3-СН3-С6Н4,
2-СН3-С6H4,
 ,
,
що включає взаємодію відповідної метиленактивної сполуки і альдегідів в органічному розчиннику при нагріванні і перемішуванні у присутності каталізатора, який відрізняється тим, що як метиленактивну сполуку використовують R-заміщені ![]() -метилсульфонілацетофенони формули R-CO-CH2-SO2-CH3, як альдегіди - R1-заміщені ароматичні або гетероциклічні альдегіди у рівномолярних кількостях, як каталізатор - піперидин, реакцію конденсації проводять в етанолі при температурі 120 °С у закритій посудині при мікрохвильовому опроміненні до утворення цільового продукту.
-метилсульфонілацетофенони формули R-CO-CH2-SO2-CH3, як альдегіди - R1-заміщені ароматичні або гетероциклічні альдегіди у рівномолярних кількостях, як каталізатор - піперидин, реакцію конденсації проводять в етанолі при температурі 120 °С у закритій посудині при мікрохвильовому опроміненні до утворення цільового продукту.
Текст
Спосіб одержання заміщених 2метилсульфоніл-1,3-діарил(гетерил)-проп-2-ен-1онів загальної формули І: O O CH3 S R O 2 3 кислоти 133-136°С. Вихід технічного продукту складає 55%. Автори відомого джерела інформації не вказують умови проведення реакції, часовий і температурний режими. Недоліком відомого способу одержання (у відсутності вказівок на умови проведення синтезу) є використання вогненебезпечного розчинника бензолу, токсичної речовини з гранично допустимою концентрацією у повітрі 5 мг/м3. Крім того, в результаті реакції одержують нечистий продукт, оскільки необхідна додаткова перекристалізація із оцтової кислоти. Вихід кінцевого продукту після перекристалізації низький і складає менше 55%. Відомий спосіб одержання 1-(5-бром-2фурил)-2-метилсульфоніл-2фуроїлкарбонілетилену формули III: описаний у [К. Spirkova, P. Bobal et al., Collect. Czech. Chem. Commun., 57, 2157-2165(1992)]. На першій стадії розчин 2-бромацетилфурану (0,1 моль) у 50 мл метанолу додають при перемішуванні до суспензії метилсульфінату натрію (0,11-0,15 моль) у 80 мл сухого метанолу, і реакційну суміш нагрівають 2,5 години. Після відгону розчинника технічний продукт 2-(2-фурил)-2оксоетилметилсульфону кристалізують із етанолу. Т. пл. складає 122-123°С, вихід 48%. Час протікання реакції на першій стадії приблизно 3,5-4 години. На другій стадії розчин тетрахлориду титану (0,1 моль) у сухому тетрахлорметані (25 мл) додають при перемішуванні у сухий тетрагідрофуран (200 мл) при 0°С. Потім додають 2-бромфурфурол (0,05 моль) і 2-(2-фурил)-2-оксиетилметилсульфон (0,05 моль), видержують при цьому температуру у межах -5-10°С. Після додавання піридину (0,2 моль) у тетрагідрофурані реакційну суміш перемішують при -5-10°С протягом 48 годин і розбавляють 50 мл води. Продукт екстрагують ефіром, ефірний розчин сушать і концентрують, видаляючи розчинник. Після стояння протягом 2-4 днів утворюються кристали 1-(5-бром-2-фурил)-2метилсульфоніл-2-фуроїлкарбонілетилену. Т.пл. 125-126°С, вихід складає 50 %. Час реакції на другій стадії приблизно 100-150 годин. Загальний час одержання 1-(5-бром-2фурил)-2-метилсульфоніл-2фуроїлкарбонілетилену складає 110-160 годин. Недоліком відомого способу є тривалий, двостадійний процес, пов'язаний з виділенням продуктів шляхом екстракції розчинниками, їх концентруванням і наступною перекристалізацією із етанолу, що ускладнює реакцію, а використання вибухових (тетрагідрофуран має властивість утворювати з часом пероксиди), горючих (піридин, метанол) і легкозаймистих (ефір) розчинників обмежує використання відомого способу одержання навіть у лабораторних умовах. 57633 4 Проведення реакції при низьких температурах (-5-10°С), низький вихід (50%) кінцевого продукту, використання осушених розчинників також слід віднести до суттєвих недоліків відомого способу одержання сполуки формули III. У якості прототипу за технічною суттю нами обрано перший із наведених аналогів. В основу корисної моделі поставлено задачу розробки способу одержання заміщених 2метилсульфоніл-1,3-діарил(гетерил)-проп-2-ен-1онів, який дозволяє підвищити вихід і якість кінцевого продукту без використання легкозаймистих, вибухових і токсичних розчинників. Крім того спосіб, що заявляється, дозволяє скоротити час реакції. Рішення поставленої задачі забезпечується тим, що за способом одержання заміщених 2метилсульфоніл-1,3-діарил(гетерил)-проп-2-ен-1онів, що включає взаємодію відповідної метиленактивної сполуки і альдегідів в органічному розчиннику при кипінні в присутності каталізатора упродовж часу, необхідного для утворення продукту, згідно з корисною моделлю, реакцію взаємодії проводять протягом 50-60 хвилин, в якості метиленактивної сполуки використовують R-заміщені -метил-сульфонилацетофенони формули R-COCH2-SO2-CH3, в якості альдегідів -R1-заміщені ароматичні або гетероциклічні альдегіди у рівномолярних кількостях, як каталізатор - піперидин; реакцію конденсації проводять в етанолі при температурі 120°С у закритому сосуді при мікрохвильовому опроміненні до утворення цільового продукту. Вибір компонентів реакції конденсації - метилсульфонілзаміщених ацетофенонів, розчинника для реакції - етанолу, основного каталізатора піперидину дозволяє здійснювати синтез в одну стадію протягом 50-60 хвилин у мікрохвильовому реакторі. За способом, що заявляється, заміщені 2-метилсульфоніл-1,3-діарил(гетерил)-проп-2-ен1-они одержують з високими виходами (85-92%), виключається додаткова очистка кінцевих продуктів та скорочується час реакції. В залежності від замісника R (у залишку метилсульфоніл-ацетофенона) і R1 (в альдегідній компоненті) спосіб, що заявляється, дозволяє широко модифікувати хімічну структуру кінцевого продукту і одержувати великий набір заміщених 2метилсульфоніл-1,3-діарил-(гетерил)-проп-2-ен-1онів - потенційних біологічно активних речовин. Проведення реакції в умовах основного каталізу при мікрохвильовому опромінюванні, що заявляються, забезпечує високу швидкість її протікання, що приводить до мінімальної тривалості одностадійного технологічного процесу (50-60 хвилин) у порівнянні з часом другого відомого аналога (110-160 годин), виключає використання легкозаймистих, горючих і отруйних розчинників і лакриматорів і дозволяє при необхідності швидко розробити промислову методику синтезу таких сполук в промисловому мікрохвильовому реакторі. Експериментальне варіювання температурного режиму реакції показало, що температура 120°С в умовах закритого мікрохвильового реактора є оптимальною, при якій сполуки можна оде 5 57633 ржувати чистими, що не потребують додаткової перекристалізації, і з високими, майже кількісними виходами. Усі сполуки, що одержано за способом, що заявляється, ідентифіковано за допомогою 1Н ЯМР спектрів. У таблиці 1 дано порівняльні характеристики способу, що заявляється, і способів одержання відомих аналогів. У таблиці 2 наведено характеристики (температура плавлення, виходи і спектри ЯМР) деяких основних продуктів реакції, які одержані за способом, що заявляється. Спосіб, що заявляється, здійснюється за схемою O O O CH3 O CH3 S piperidine + R O S R R1CHO ethanol O R1 0,1 моль R-заміщеного метилсульфонілацетофенона і 0,1 моль R1заміщеного альдегіду розчиняють у 300 мл етанолу, додають 0,01 моль піперидину. Реакційну суміш нагрівають при 120°С у закритому сосуді у мікрохвильовому реакторі при перемішуванні протягом 50-60 хвилин. Після охолодження осад, що випав, відфільтровують, промивають спиртом і сушать. Нижче приведено приклади конкретного виконання. Приклад 1. Одержання 2-метилсульфоніл-1,3дифеніл-проп-2-ен-1-ону. 19,8 г (0,1 моль) метилсульфонілацетофенона і 10,6 г (0,1 моль) бензальдегіду розчиняють у 300 мл. етанолу і після цього додали 0,85 г (0,01 моль) піперидину. Реакційну суміш нагрівають при 120°С в зачиненому сосуді у мікрохвильовому реакторі при перемішуванні на протязі однієї години. Після охолодження до кімнатної температури, осад що випав, відфільтровують, промивають спиртом та сушать. Вихід 28,3 г (92%). Вихідні дані: вихід 28,3 г ( 92%), т.пл. 141142°С. Елементний аналіз на вміст: С, %: обчислено 67,11; C16H14O3S; знайдено 67,51 S, %: обчислено 11,20; знайдено 11,34 Приклад 2. Одержання 2-метилсульфоніл-1-(4метилфеніл)-3-(4-фторфеніл)-проп-2-ен-1-ону. 6 21,2 г (0,1 моль) -метилсульфоніл-4метилацетофенону і 12,4 г (0,1 моль) 4фторбензальдегіду розчиняють у 300 мл етанолу і після цього додають 0,85 г (0,01 моль) піперидину. Реакційну суміш нагрівали при 120°С в зачиненому сосуді у мікрохвильовому реакторі при перемішуванні на протязі 50 хвилин. Після охолодження до кімнатної температури осад що випав, відфільтровують, промивають спиртом та сушать. Вихід 27,0 г (85%). Вихідні дані: вихід 27,0 г (85%), т.пл. 150151°С. Елементний аналіз на вміст: С, %: обчислено 64,14; C17H15FO3S знайдено 64,03 S, %: обчислено 10,07; знайдено 10,16 Приклад 3. Одержання 2-метилсульфоніл-1феніл-3-(-тієніл)-проп-2-ен-1-ону. 19,8г (0,1моль) метилсульфонілацетофенону і 11,2 г (0,1 моль) тіофенового альдегіду розчиняють у 300 мл етанолу і після цього додають 0,85 г (0,01 моль) піперидину. Реакційну суміш нагрівали при 120°С в зачиненому сосуді у мікрохвильовому реакторі при перемішуванні на протязі 50 хвилин. Після охолодження до кімнатної температури, осад, що випав, відфільтровують, промивають спиртом та сушать. Вихід 25,4 г (87 %). Вихідні дані: вихід 25,4 г (87 %), Т.пл. 127128°С. Елементний аналіз на вміст: С, %: обчислено 57,51; C14H12O3S2; знайдено 57,69 S, %: обчислено 21,93; знайдено 21,88 Як видно із тексту матеріалів, що заявляються, технічне рішення, що пропонується, має наступні переваги: - тривалість синтезу складає 50-60 хвилин (за другим відомим аналогом - 110-160 годин); - дозволяє підвищити вихід і якість кінцевих продуктів до 85-92% (у порівнянні зі способомпрототипом -55%, з другим відомим аналогом 50%); - широко варіювати у молекулі замісники різної електронної природи. Спосіб одержання сполук структури І, що заявляється, простий у технологічному плані, здійснюється в одну стадію і може легко відтворюватись як у лабораторії, так і в умовах виробництва. 7 57633 8 Таблиця 1 Розчинник Час реакції Вихід, % Кількість стадій етанол 50-60 хвилин 85-92 1 бензол Спосіб, що заявляється Спосіб-прототип [K.Spirkova, P. Bobal et al., Collect. Czech. Chem. Commun., 57, 2157-2165 (1992)] 55 1 тетрагідрофуран 110-160 годин 50 2 Мікрохвильове опромінення при 120°С Умови не описано Реакцію проводять при низьких температурах 5-10°С, екстракція, конденсування розчинника, перекристалізація Таблиця 2 Сполука Т.пл., °С 141-142 92 138-139 85 O O CH3 S 1 Вихід, % C6H5 O C6H5 O O CH3 S 2 C6H5 O O O O 90 3.31 (s, 3Н, СН3), 7.34 (d, 2H, Аr), 7.36 (d, 2H, Аr), 7.47 (m, 2Н, Аr), 7.64 (m, 1H, Аr), 7.85 (dd, 2H, Аr), 7.98 (s, 1H, СН) 87 3.31(s,3H,CH3), 7.31 (t, 1Н, Аr), 7.51 (m, 3H, Ar), 7.65 (m, 2Н, Аr), 7.79 (m, 2Н, Аr), 8.01 (s, 1Н,СН) 85 2.37 (s, 3Н, СН3), 3.32 (s, 3Н, СН3), 6.92 (m, 2Н, Аr), 7.21(m,2Н, Аr), 7.27 (d, 2H, Аr), 7.71 (d,2H, Ar), 7.98 (s, 1Н, СН) CH3 S C6 H5 3 O 181-182 Cl O O S C6 H5 4 127-128 O S O O S O 5 150-151 CH3 Комп’ютерна верстка Л. Купенко Спектр ЯМР 1H, (м.ч.) 3.31 (s, 3Н, СН3), 7.31 (m, 5H, Аr), 7.46 (m, 2H, Аr), 7.63 (m, 1H, Аr), 7.86 (m, 2H, Аr), 7.96 (s, 1Н, СН) 3.27 (s, 3Н, СН3), 3.69 (s, 3Н, ОСН3), 6.85 (d, 2H, Аr), 7.30 (d, 2H, Аr), 7.49 (m, 2H, Аr), 7.65 (m, 1H, Аr), 7.87 (s, 1H, СН), 7.89 (m, 3Н, Аr), 7.90 (s, 1Н,СН) Підписне Тираж 23 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of 2-methylsulfonyl-1,3-diaryl(heteryl)-prop-2-ene-1-ones
Автори англійськоюHladkov Yevhenii Stanislavovych, Sirko Svitlana Mykolaivna, Desenko Serhii Mykhailovych, Afanasiadi Luidmyla Mykhailivna
Назва патенту російськоюСпособ получения замещенных 2-метилсульфонил-1,3-диарил(гетерил)-проп-2-эн-1-онов
Автори російськоюГладков Евгений Станиславович, Сирко Светлана Николаевна, Десенко Сергей Михайлович, Афанасиади Людмила Михайловна
МПК / Мітки
МПК: C07C 317/08
Мітки: заміщених, одержання, 2-метилсульфоніл-1,3-діарил(гетерил)-проп-2-ен-1-онів, спосіб
Код посилання
<a href="https://ua.patents.su/4-57633-sposib-oderzhannya-zamishhenikh-2-metilsulfonil-13-diarilgeteril-prop-2-en-1-oniv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання заміщених 2-метилсульфоніл-1,3-діарил(гетерил)-проп-2-ен-1-онів</a>
Попередній патент: Коток
Випадковий патент: Пристрій для навчання письму з звуковим супроводженням