Спосіб отримання полімерних мембран
Номер патенту: 69337
Опубліковано: 16.08.2004
Автори: Брик Михайло Теодорович, Бурбан Анатолій Флавіанович, Коновалова Вікторія Валеріївна, Вортман Марина Яківна, Клименко Ніна Сергіївна, Вакулюк Поліна Василівна, Шевченко Валерій Васильович
Формула / Реферат
Спосіб отримання полімерних мембран, виготовлених з поліетилентерефталату, для процесів розділення, який відрізняються тим, що трекові поліетилентерефталатні мембрани витримують у водних розчинах гуанідинвмісних олігомерів з концентраціями 200, 500, 1000 ppm з тривалістю адсорбції 0,08 - 72 годин.
Текст
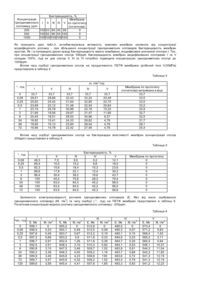
Винахід відноситься до напівпроникних мембран для процесів розділення, що відрізняються присутністю специфічних груп, що забезпечують бактерицидну дію і призначений для отримання біологічно чистої води. Біологічне забруднення полімерних мембран є однією з головних проблем мембранних технологій. В процесі експлуатації мембрани мікроорганізми осідають на її поверхні. За рахунок постійного підводу субстрату до поверхні мембрани, мікроорганізми інтенсивно розмножуються та утворюють біоплівку, що руйнує поверхню мембрани, викликає падіння продуктивності за рахунок блокування пор та спричинює вторинне забруднення очищеної води продуктами метаболізму [1]. Відомо, що більшість мембран, що випускаються промисловістю, не виявляють антимікробних властивостей і тому потребують модифікування бактерицидними агентами. Модифікування гідрофобних мембран дозволяє, з одного боку, гідрофілізувати їх поверхню (в т.ч. поверхню пор), а з іншого - надати мембранам специфічних розділювальних характеристик за рахунок утворення на їх поверхні ти х чи інших функціональних груп [2]. Бактеріальне забруднення та деструкція характерні в тій чи іншій мірі для всіх відомих полімерних мембран. Прототипом запропонованого винаходу є спосіб отримання трекових поліетилентерефталатних (ПЕТФ) мембран. Він полягає в тому, що пори отримують дією високоенергетичних (направлений пучок електронів) частинок, які під час обробки направлені перпендикулярно плівці. Частинки пошкоджують поліетилентерефталатну плівку та формують треки. Після цього її занурюють в ванну з кислотою (або лугом), та піддають травленню [3]. Отримані мембрани характеризуються вузьким розподілом пор за розмірами, що дозволяє виключити проблеми пов'язані із неоднорідністю пор та звивистістю порових каналів полімерних мембран, що робить їх особливо зручними для дослідження. Недоліком є те, що вони не проявляють бактерицидних властивостей, що в результаті призводить до зниження терміну їх експлуатації. Задачею винаходу є модифікування поверхні полімерних мембран, що забезпечує надання їм бактерицидних властивостей, подовження терміну експлуатації шляхом зменшення їх біологічного забруднення продуктами життєдіяльності мікроорганізмів, та зменшення біологічної деструкції полімеру мембрани. Поставлена задача реалізується тим, що по способу отримання полімерних мембран одержаних з поліетилентерефталату для процесів розділення, згідно з запропонованим винаходом, трекові поліетилентерефталатні мембрани витримують у водних розчинах гуанідинвмісних олігомерів з концентраціями 200; 500 і 1000ppm з тривалістю адсорбції олігомерів 0,08-72 годин. Для надання мембранам бактерицидних властивостей використовували поліетилентерефталатні (ПЕТФ) трекові мембрани (виробництво ОІЯД м. Дубна, Росія) з розміром пор 0,05мкм та гуанідинвмісні олігомери загальної формули: H 2N C NH CH 2 CH R OH NH.HCl CH CH2 NH OH C NH 2 NH.HCl де R CH 3 CH 2 C O O CH 2 CH 3 (I) CH3 CH2 C O CH CH2 NH C NH O CH2 OH CH3 5 NH.HCl (II) CH3 CH2 O CH2 C O CH2OOCC 6H4(CH2-O) n CH 3 -C6H 4COOCH 2-CH-CH 2-O C OH O CH3 CH3 n=50 CH 2 - O - [ CH 2 - CH - O]x - CH2 CH3 CH OH CH 3 (III) CH3 CH - [OCH - CH 2]y - O - CH 2 - CH - CH 2 - NH - C - NH 2 OH CH 2 - O - [CH 2 - CH - O]z - CH2 CH 3 NH.HCl x+y+z=10 (IV) CH 3 CH3 CH2 O C O CH2 CH CH 2O OCC 6H4(CH 2-O)m-(CH 2-CH-O) n OH CH3 CH 3 -C 6H4COOCH2-CH-CH 2-OOH C CH3 O CH3 m+n=30 (V) Гуанідинвмісні олігомери є порошкоподібними речовинами добре розчинними у воді. Запропонований спосіб реалізується наступним чином. Зразки трекових поліетилентерефталатних мембран площею 26,4.10-4м 2 витримували у водних розчинах гуанідинвмісних олігомерів з початковими концентраціями 200; 500 і 1000ppm з тривалістю адсорбції 0,08-72 годин, об'єм модифікуючого розчину гуанідинвмісних олігомерів складав 20см 3. Протягом адсорбційної модифікації через певні проміжки часу мембрани виймали з розчину гуанідинвмісних олігомерів, промивали дистильованою водою і використовували для подальших досліджень. Модифікування проводили до повного адсорбційного насичення поверхні мембрани (в т.ч. поверхні пор) гуанідинвмісними олігомерами, тобто коли подальша сорбція олігомеру вже не відбувається. Концентрацію водних розчинів гуанідинвмісних олігомерів в початковому розчині і розчині після адсорбції визначали за їх електропровідністю кондуктометричним методом з використанням кондуктометра НІ 9032 (HANNA INSTRUMENTS). Всі показники отримання полімерних мембран дані в таблиці 2-7. Для дослідження бактерицидної активності використовували штам Escherichia coli HB 101 (Тип-штам, типовий для виду). Для культивування кишкової палички застосовували середовище Ендо. Мінімальну пригнічувальну концентрацію гуанідинвмісних сполук визначали методом розведень в агаризованому середовищі в модифікації реплік [4]. Мінімальною пригнічувальною концентрацією (МПК) вважали ту найменшу концентрацію сполук в середовищі, за якою був відсутній ріст мікроорганізмів на поживному середовищі. Досліди проводили у 3-х повторах. Суспензії добових тест-к ультур готували у стерильному фізичному розчині (1´109кл/мл), в об'ємі 0,2мл вносили у лунки реплікатора та висівали паралельно на три чашки Петрі відповідно до схеми експерименту. Результати обраховували через 24 та 48 годин культивування бактерій, при 32-37°С. Як контроль використовували середовище Ендо без додавання гуанідинвмісних сполук. Результати дослідження бактерицидної активності сполук по відношенню до грамнегативної бактерії Escherichia coli HB 101, так як ця культура є санітарно-показовою мікробіологічної якості води, наведені в таблиці 1. Таблиця 1 Сполука І II III IV V 10 ++++ ++++ ++++ ++++ ++++ Концентрація сполук у середовищі (ppm): 25 50 100 120 140 ++++ ++++ +++ ++ + ++++ +++ ++ + ++++ ++++ ++++ +++ ++ +++ ++ 180 + 200 Контроль ++++ ++++ ++++ ++++ ++++ Примітка: в таблиці наведені зведені дані, після висіву культур на 3-х чашках Петрі; "-" - ріст мікроорганізмів відсутній; "+" - поодинокі колонії; "++++" - суцільний ріст; З таблиці видно, що бактерицидна активность гуанідинвмісних сполук по відношенню до грамнегативної бактерії Escherichia coli HB 101 була найвищою для всіх сполук при концентрації 200ppm, тобто не росла жодна культура. Бактерицидну активність модифікованих мембран визначали фільтруванням суспензії Escherichia coli HB 101 в фізіологічному розчині через досліджувану мембрану з відомим розміром пор. Фільтрацію проводили в установці непроточного типу з використанням термостатування і перемішування об'ємом 0,15дм 3 і площею мембрани 26,4×10-4м 2. Робочий тиск становив 0,05МПа. Робоча температура 25°С. Культур у вирощували на селективному середовищі Ендо та вносили в фізіологічний розчин в концентрації близько 106 клітин/мл. Після розведення до концентрації 103 клітин/л 100мл суспензії фільтрували через досліджувану мембрану до сухого залишку. Контролем слугувала мембрана по прототипу, тобто немодифікована. Після фільтрації мембрану інкубували на твердому середовищі Ендо при 28°С протягом доби. Бактерицидну активність визначали як відсоток колонієутворюючи х одиниць на модифікованій мембрані до немодифікованої. Таким чином, виявлено, що при концентрації гуанідинвмісних сполук 200ppm всі проявляють максимальну бактерицидну дію. Тому подальші наші дослідження включали вивчення бактерицидної активності поліетилентерефталатних мембран модифікованих гуанідинвмісними сполуками починаючи з концентрації їх 200ppm. В таблиці 2 наведені результати бактерицидної активності поліетилентерефталатних мембран модифікованих гуанідинвмісними сполуками до грамнегативної бактерії Escherichia coli HB 101, концентрація розчину 200ppm. Час сорбції 24год. Початкова продуктивність мембрани 33,7л/м 2×год. Робочий тиск 0,05МПа. Таблиця 2 Гуанідинвмісний олігомер І II III IV V Мембрана по прототипу (початкова) JV, л/м 2×год 18,9 15,4 22,2 29,8 4,7 31,7 Бактерицидність, % 100 63 84 45 98 0 Як видно з табл.2, адсорбція БАС з водних розчинів на поверхні і в порах мембрани зменшує ефективний радіус пор, що в свою чергу призводить до падіння об'ємного потоку. Таким чином, ступінь модифікування мембрани ПАР можна характеризувати за зміною об'ємного потоку води крізь мембрану до та після сорбції. Мембрани, модифіковані сполуками І та V, виявляють найвищу бактерицидну дію по відношенню до Е. coli - 100 та 98% відповідно. Продуктивність мембран знижується до 18,9 та 4,7л/м 2×год. Вплив концентрації модифікуючого розчину гуанідинвмісних олігомерів на бактерицидні властивості мембрани представлені в таблиці 3. Початкова продуктивність мембрани 33,7л/м 2×год. Час сорбції 24год. Робочий тиск 0,05МПа. Таблиця 3 Бактерицидність, % Концентрація Мембрана гуанідинвмісного І II III IV V по прототипу олігомеру, ppm (початкова) 200 100 63 84 45 98 0 500 100 82 98 65 100 0 1000 100 100 100 100 100 0 Як показують дані табл.3, антибактеріальна активність трекових мембран залежить від концентрації модифікуючого розчину - при збільшенні концентрації гуанідинвмісних олігомерів бактерицидність мембран зростає. Як і в попередніх даних кращу бактерицидність мають мембрани, модифіковані розчином сполуки І. Так, при концентрації гуанідинвмісних сполук 500ppm бактерицидність мембран модифікованих сполуками І та V складає 100%, тоді як для сполук II, III та IV потрібно підвищити концентрацію гуанідинвмісних сполук до 1000ppm. Вплив часу сорбції гуанідинвмісних сполук на продуктивність ПЕТФ мембрани (робочий тиск 0,05МПа) представлено в таблиці 4. Таблиця 4 t , год 0 0,08 0,25 0,5 1 3 6 24 48 72 Jv, л/м 2×год I II III IV 33,7 29,51 25,62 23,69 23,19 21,66 20,45 18,92 18,95 18,96 33,7 28,66 24,42 22,12 20,78 19,56 18,51 15,41 15,12 14,78 33,7 32,43 31,64 31,48 30,86 29,67 28,52 24,33 23,84 22,42 33,7 33,22 32,85 32,54 32,18 31,47 30,96 29,82 28,54 27,48 Мембрана по прототипу (початкова) витримана в воді 33,7 33,5 33,5 33,2 32,9 32,7 32,5 31,7 29,1 25,4 V 33,7 25,48 22,75 20,64 15,32 11,66 9,37 4,78 4,78 4,78 Вплив часу сорбції гуанідинвмісних сполук на бактерицидні властивості мембран (концентрація сполук 200ppm) представлені в таблиці 5. Таблиця 5 t , год 0,08 0,25 0,5 1 3 6 24 48 72 I 48,3 68,4 82,3 88,6 96,4 100 100 100 100 II 7,0 10,5 15,6 17,6 30,4 45,4 63,0 63,4 63,5 III 9,5 15,2 18,4 22,1 38,2 75,8 84,3 84,5 84,5 Бактерицидність, % IV V 5,2 12,1 8,6 18,5 10,3 23,6 12,4 30,2 18,6 43,7 28,3 79,4 45,2 98,5 45,2 98,5 45,3 98,6 Мембрана по прототипу 0 0 0 0 0 0 0 0 0 Залежність електропровідності розчинів гуанідинвмісних олігомерів (Е, Ms) від маси сорбованого гуанідинвмісного олігомеру (М, г/м 2) та часу сорбції ( t , год) на ПЕТФ мембрані представлені в таблиці 6. Початкова концентрація водного розчину гуанідинвмісного олігомеру - 200ppm. Таблиця 6 Час, год 0 0,08 0,25 0,5 1 3 6 24 48 72 120 I Е, Ms 599,1 598,5 597,8 597,3 596,7 592,5 590,8 590,2 589,9 589,7 589,6 М, г/м 2 0 0,23 0,49 0,68 0,91 2,51 3,15 3,38 3,49 3,57 3,59 II Е, Ms 655,2 654,1 653,7 653,2 652,4 648,3 647,5 646,3 645,8 645,6 645,4 М, г/м 2 0 0,49 0,67 0,9 1,26 3,10 3,46 4,00 4,23 4,32 4,41 III Е, Ms 512,8 512,5 512,2 511,8 511,6 510,3 509,7 509,2 508,6 508,2 507,8 М, г/м 2 0 0,09 0,19 0,33 0,39 0,82 1,02 1,16 138 1,52 1,65 IV Е, Ms 485,5 485,3 485,1 484,9 484,7 484,1 483,9 483,7 483,6 483,4 483,3 М, г/м 2 0 0,07 0,15 0,23 0,30 0,53 0,61 0,68 0,72 0,79 0,83 V Е, Ms 573,4 571,2 569,4 565,2 560,4 546,1 544,3 542,2 541,3 541,3 541,2 М, г/м 2 0 0,83 1,52 3,11 4,94 10,37 11,04 11,85 12,19 12,19 12,23 240 589,6 3,59 645,4 4,41 507,6 1,71 483,1 0,91 541,2 12,23 Як видно з даних про кількість адсорбованого гуанідинвмісного олігомеру в залежності від тривалості сорбції (табл.6), розрахованої за зміною електропровідності модифікуючих розчинів, максимальну адсорбцію до поверхні ПЕТФ мембран має сполука V. За 48год сорбції мембрана досягає піку адсорбційної ємності - 12,19г/м 2 речовини, що обумовлено найвищою молекулярною масою V. Набагато нижчу сорбційну активність проявляли гуанідинвмісні олігомери І та II, які сорбувалися за 48год 3,49 та 4,23г/м 2 речовини відповідно. А гуанідинвмісні олігомери III і IV за 240год модифікування сорбувалися лише 1,71 та 0,91г/м 2 речовини відповідно. Таким чином приведені дані свідчать, що незважаючи на високу поверхневу та абсорбційну активність V, модифіковані ним мембрани мають нижчу бактерицидність. Така ж картина спостерігається і для II, що проявляє вищу адсорбційну здатність та нижчу бактерицидну активність до мембрани в порівняні з сполукою І (табл.2). Вивчення впливу часу десорбції гуанідинвмісних олігомерів на бактерицидні властивості мембран представлено в таблиці 7. Початкова концетрація БАС 200ppm. Час модифікування 24 години. Ми вибрали мембрани, що виявили найкращу бактерицидну активність, тобто мембрани модифіковані сполуками І та V. Таблиця 7 Час десорбції, діб 0 1 2 3 5 7 10 Jv, л/м 2×год 18,96 18,55 18,32 18,25 18,22 18,18 18,15 I Бактерицидність, % 100 100 100 100 100 100 100 Jv, л/м 2×год 4,78 7,75 8,85 9,76 9,82 9,85 9,87 V Бактерицидність, % 98 95 93 92,8 92,7 92,5 92,5 Як свідчать дані табл.7, до десорбції більш схильні мембрани модифіковані сполукою V, продуктивність мембрани зростає з 4,7 до 9,7л/м 2×год через 3 доби і в подальшому майже не змінюється, а бактерицидність мембрани за цей час знижується з 98 до 92%. В той час, як мембрана модифікована сполукою І, бактерицидна дія її залишалася стабільною, а продуктивність майже не зросла 18,9 до 18,1л/м 2×год за 10 діб роботи мембрани. Полімерні мембрани одержані запропонованим способом забезпечують: - бактерицидні властивості; - подовження терміну експлуатації мембран шляхом зменшення їх біологічного забруднення продуктами життєдіяльності мікроорганізмів; - зменшення біологічної деструкції полімеру мембрани; Джерела: 1. Н. -С. Flemming, G. Schaule, Biofouling on membranes - a microbiological approach, Desalination 70 (1988) 95. 2. Вакулюк П.В, Бурбан А.Ф, Брик М.Т, Протасова Н.В, Шевченко В.В. Модифікування трекових мембран аніонними біанкерними сполуками та вивчення їх розділювальних характеристик. Доповіді НАН України. -2002. №10. -С.133-138. 3. Ione M.Yamazaki, A new generation of track etched membranes for microfiltration and ultrafiltration. Part I. Preparation and characterisation, J. Membr. Sci. 118 (1996) 239-245. 4. Василевская И.А., Сергейчук М.Г., Згонник В.В., Фуртат И.М., Ми хальский Л.А. Усовершенствование метода бактериологического контроля в производстве лизина // Мікробіол. журн. -1996. -58, №5. -С.66.
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for production of polymeric membranes
Автори англійськоюVakuliuk Polina Vasylivna, Vortman Maryna Yakivna, Konovalova Viktoria Valeriivna, Burban Anatolii Flavianovych, Klymenko Nina Serhiivna, Bryk Mykhailo Teodorovych, Shevchenko Valerii Vasyliovych
Назва патенту російськоюСпособ получения полимерных мембран
Автори російськоюВакулюк Полина Васильевна, Вортман Марина Яковлевна, Коновалова Виктория Валерьевна, Бурбан Анатолий Флавианович, Клименко Нина Сергеевна, Брик Михаил Теодорович, Шевченко Валерий Васильевич
МПК / Мітки
МПК: B01D 71/00
Мітки: отримання, спосіб, полімерних, мембран
Код посилання
<a href="https://ua.patents.su/4-69337-sposib-otrimannya-polimernikh-membran.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання полімерних мембран</a>
Попередній патент: Спосіб мікрохірургічного лікування птеригіуму
Наступний патент: Інструмент для об’ємної обробки матеріалу
Випадковий патент: Відцентровий тепломасообмінний апарат