Спосіб одержання 4-аміно-3-галогенпіколінової кислоти селективним електрохімічним відновленням
Номер патенту: 70405
Опубліковано: 15.10.2004
Автори: Ботт Крейг Джозеф, Гулло Майкл Фредерік, Халл Джон Уеслі, мол., Крумел Карл Леопольд, Скортічіні Кері Лі
Формула / Реферат
1. Спосіб одержання 4-аміно-3-галогенпіколінової кислоти формули І
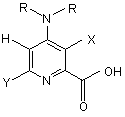 , I
, I
де
Х означає Сl або Вr;
Y означає Н, F, Сl, Вr або С1-С4-алкіл; і
R незалежно означає Н або С1-С4-алкіл, що включає
пропускання постійного або змінного електричного струму від анода до катода через розчин 4-аміно-3,5-дигалогенпіколінової кислоти формули II
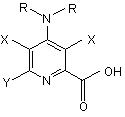 , II
, II
де
X, Y і R є такими, як визначено вище, причому обидва Х означають або Сl, або Вr,
при катодному потенціалі від -0,4 до -1,7 В відносно Ag/AgCl (3,0 М Сl-)-електрода порівняння,
і вилучення продукту, при умові, що, коли Х є хлором, то Y не є бромом.
2. Спосіб за п. 1, в якому сполукою формули II є
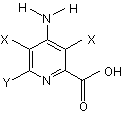 ,
,
де Х і Y є такими, як визначено вище.
3. Спосіб за будь-яким з пп. 1, 2, в якому розчин 4-аміно-3,5-дигалогенпіколінової кислоти є основним водним розчином.
4. Спосіб за будь-яким з пп. 1-3, в якому Х означає Сl, і катодний потенціал складає від -0,8 до -1,7 В.
5. Спосіб за будь-яким з пп. 1-4, в якому Y означає Сl.
6. Спосіб за будь-яким з пп. 1-3, в якому Х означає Вr, і катодний потенціал складає від -0,4 до -1,1 В.
7. Спосіб за п. 6, в якому Y означає Вr.
8. Спосіб за будь-яким з пп. 1-7, в якому катодом є срібло.
9. Спосіб за будь-яким з пп. 1-8, в якому срібний катод активують анодуванням у водному лужному розчині при потенціалі не менш ніж від +0,3 до +0,7 В з подальшою зворотною поляризацією.
Текст
Даний винахід відноситься до одержання деяких 4-амінопіколінових кислот електрохімічним відновленням. Більш конкретно даний винахід відноситься до селективного відновлення галогенних заступників в 5положенні галогенованих 4-амінопіколінових кислот в присутності галогенних заступників в 3- і 6-положеннях. Недавно було встановлено, що деякі похідні 4-аміно-3-галогенпіколшової кислоти, що містять водень в 5положенні, використовуються як гербіциди. Було б бажано мати можливість одержувати вказані гербіциди з відповідних 5-галогенпохідних, багато які з яких є комерційно доступними, такі як 4-аміно-3,5,6-трихлорпіколінова кислота (піклорам). Хоч хімічне відновлення галогенованих піридинів є відомим, дивись, наприклад, патент США 4087431, в якому гідразин використовується як відновник, ефективність використання матеріалу є низькою, і вартість є відносно високою. Електролітичне відновлення, з іншого боку, може бути дуже ефективним, а також селективним. Патент США 3694332 розглядає селективне електролітичне відновлення галогенованих піридинів і галогенованих ціанпіридинів в 4-положенні. Патент США 4217185 розглядає електролітичне відновлення тетрахлорпіколінової кислоти в 4- і 5-положеннях. Патент США 4242183 розглядає електролітичне відновлення симетричного тетрахлорпіридину до 2,3,5-трихлорпіридину з використанням активованого срібного сітчастого електрода. Вказаний патент також патентує способи активування срібного катода. Російський патент SU 1807686 А1 розглядає електролітичне відновлення поліхлорованих піридинкарбонових кислот. Такі селективні електролітичні відновлення обмежуються галогенованими піридинами, які містять тільки карбонову кислоту або ціанзамісники. Було б бажано мати електрохімічні способи, які можуть селективно відновлювати галогеновані піридини, що містять інші заступники. Тепер встановлено згідно з даним винаходом, що 4-аміно-3-галогенпіколінові кислоти можуть бути одержані електрохімічним відновленням відповідних 4-аміно-3,5-дигалогенпіколінових кислот. Більш конкретно, даний винахід відноситься до способу одержання 4-аміно-3-галогеншколінової кислоти формули I: в якій X представляє СІ або Вr; Υ представляє Н, F, СІ, Вr або С 1-С4-алкіл; і R незалежно представляє Η або С1-С4-алкіл, при цьому спосіб передбачає пропущення постійного або змінного електричного струму від анода до катода через розчин 4-аміно-3,5-дигалогенпіколінової кислоти формули II: в якій Χ, Υ і R є такими, як визначено раніше, і в якій обидва X представляють або СІ, або Вr, при катодному потенціалі від -0,4 до -1,7В відносно електрода порівняння Ag/AgCl (3,0Μ Сl-) і витягання продукту при умові, що, коли X представляє СІ, тоді Υ не є Вr, Несподівано було виявлено, що галоген в 5положенні селективно віддаляється в присутності 4-аміногрупи з високим виходом. Як використано тут, термін "галоген" відноситься до СІ або Вr. Реакції, що полягають у відновленні 4-аміно-3,5-дигалогенпіколінової кислоти, можуть бути зображені таким чином: A) Нейтралізація: B) Катодна реакція: C) Анодна реакція: 2 (ОН-) 1/2 О2+Н2О+2е-; D) Сумарна реакція: Карболову кислоту витягують підкисленням реакційної суміші і витяганням продукту по традиційній технології. Необхідне електролітичне відновлення здійснюють по технології, яка добре відома в техніці. У загальному випадку початкову 4-аміно-3,5-дигалоґенпіколінову кислоту розчиняють в розчиннику з одержанням електроліту, який вводять в електролітичний осередок, після чого через електроліт пропускають достатній електричний струм до одержання необхідної міри відновлення. Фахівці в даній області техніки зазначать, що відновний потенціал брому приблизно на 0,5В перевищує (менш негативний) порівняльний потенціал хлору. Бром завжди буде відновлюватися першим. Таким чином, коли X є СІ, Υ не може бути Вr. Конструкція електролізера не є визначальною. Електроліз може проводитися періодичним, безперервним або напівбезперервним способом. Електролізером може бути реактор з перемішуванням, що містить електроди, або проточний електролізер будь-якої традиційної конструкції. У деяких випадках може бути бажано використати сепаратор для розділення електролізера на окремі анодний відсік і катодний відсік. Прикладами сепараторних матеріалів, що використовуються є різні аніонообмінні і катіонообмінні мембрани, пористий тефлон, азбести і скло. Хоч використання трьох електродів, коли катодний потенціал регулюється відносно електрода порівняння, є переважним, електроліз альтернативно може здійснюватися з використанням тільки двох електродів (анода і катода) з регулюванням або струму електролізера, або напруження електролізера, або того і іншого. Для зручності 3-х електродний неподілений електролізер, в якій електроліт служить як католітом, так і анолітом, є переважним. Анодом може бути будь-який хімічно інертний матеріал, включаючи, наприклад, платину, графіт, вуглець, оксиди металів, такі як оксид срібла на сріблі, або сплави, такий як сплав Хастелой С, причому графіт, вуглець і сплав Хастелой С є переважними. Аналогічно катод може бути виконаний з ряду матеріалів, включаючи ртуть, свинець, залізо, олово, цинк або срібло, причому срібло є переважним. Електроди можуть бути у вигляді пластин, стрижнів, дроту, екранів, тонкої сітки, вати або шарів, причому екрани з тягнутої сітки є переважними. Анод або катод може також складатися з покриття, нанесеного на інший матеріал, прикладом якого є оксид благородного металу, такий як оксид рутенію, нанесений на титан. Найбільш переважними катодами є активовані срібні катоди, одержані, як описано в патентах США 4217185 і 4242183. Такі активовані катоди можуть бути одержані нанесенням шару мікрокристалів срібла на провідну підкладку з формуванням композитного електрода або анодуванням самого срібного електрода. Наприклад, для ілюстрації останнього неактивований срібний електрод можна занурити або завантажити в лужний водний каталітичний розчин і анодувати з перетворенням внаслідок частини срібла на поверхні електрода в колоїдний оксид срібла і з одночасним придбанням поверхні шорсткості. Полярність електрода потім міняється на протилежну, і оксид електролітично перетворюється в частки мікрокристалічного срібла, адгезовані до поверхні електрода. Методика активування полягає в збільшенні потенціалу від початкового значення 0В до кінцевого значення не менше за +0,3В і, переважно, +0,7В. Відновлення оксидного шару вимагає негативної поляризації катода. Катодний потенціал поступово знижується від значення +(0,3-0,7)В, очікуваного в процесі стадії окислення, до значення -0,5В або нижче. У даному способі немає необхідності вводити яку-небудь кількість срібла в католіт або водну основу. Вода є найбільш переважним розчинником для електролізу, але в деяких випадках можна використати органічний розчинник або нарізно, або як співрозчинник. Розчинник або система із співрозчинником повинні розчиняти весь або велику частину початкового матеріалу і електроліту або, щонайменше, достатню для забезпечення протікання відновлення з прийнятною швидкістю. Крім того, розчинник або система із співрозчинником повинні бути інертними до умов електролізу, тобто вони не повинні негативно впливати або взаємодіяти з матеріалами катода або католіта в недопустимій мірі. Інші, чим вода, переважні розчинники/співрозчинники змішуються з водою і включають низькомолекулярні спирти, прості ефіри, такі як тетрагідрофуран, діоксан і ефіри полігліколю, і нижчі аміди, такі як диметилформамід або диметилацетамід. Гідроксиди лужних металів є переважними як фоновий електроліт, але можуть бути використані багато які інші речовини, такі як гідроксиди, хлориди, карбонати четвертинного амонію або металів і т.д. NaOH є найбільш переважним фоновим електролітом. У реакції один еквівалент основи потрібний для нейтралізації початкового матеріалу, і додатковий еквівалент потрібний для генерування гідроксильних іонів, які споживаються в електролізі. Реакція звичайно протікає з надлишком основи, переважно, з 0,05-2% мас. надлишку основи в процесі реакції. Концентрація галогенованої 4-амінопіколінової кислоти в католіті або живленні може бути від 1 до 20%мас, переважно, від 8 до 12%мас. Низькі концентрації знижують продуктивність, тоді як високі концентрації звичайно дають більш низькі виходи, чистоту продукту і електричну ефективність. Відповідні температури для електролізу звичайно знаходяться в інтервалі від 5 до 90°С. Переважний температурний інтервал складає від 20 до 60°С. Найбільш переважним є інтервал від 20 до 40°С. Фахівець в даній області техніки зазначить, що уявний катодний потенціал, при якому галоген буде селективно відновлюватися, залежить від цілого ряду чинників, що включають, наприклад, структур у конкретної підкладки, конфігурацію електролізера і відстань, що розділяє електроди. У загальному випадку катодний потенціал відносно стандартного Ag/AgCl (3,0Μ Сl-)- електроду повинен знаходитися в інтервалі від 0,4 до -1,1В для Вr і в інтервалі від -0,8 до -1,7В для СІ. Для Вr катодний потенціал, переважно, складає від 0,6 до -0,9В. Для СІ катодний потенціал, переважно, складає від -1,0 до -1,4В. Щільність струму в амперах на квадратний сантиметр (А/см 2) повинна бути не менше за 0,005, переважно, 0,05А/см 2 або більше. Хоч виділення молекулярного кисню є переважним, можуть бути використані багато які інші анодні реакції. Приклади включають виділення молекулярного хлору або брому, окислення часток, що втрачаються, таких як форміат або оксалат, з одержанням вуглекислого газу, або окислення органічного субстрату з утворенням цінного співпродукту. У переважному в цей час варіанті галогеновану 4-амінопіколінову кислоту розчиняють у водному лузі з утворенням лужного водного розчину, який безперервно циркулює через розділений електролізер, що має срібний катод з тягнутої сітки, активований анодуванням при +0,7В у водному лужному електроліті. При підтримці реакційної суміші лужний електроліз при катодному потенціалі від -0,6 до -1,5В відносно Ag/AgCl (3,0Μ Сl-)- електроду порівняння продовжують до досягнення необхідної міри відновлення. Необхідний продукт витягують по традиційній технології. Наприклад, кислота може бути висаджена з реакційної суміші підкисленням з подальшою або фільтрацією, або екстракцією органічним розчинником, що не змішується з водою. Наступні приклади ілюструють даний винахід. Приклади Приклад 1 Одержання 4-аміно-3,6-дихдорпіридин-2-карбонової кислоти (проточний електролізер) У 3-літрову (л) хімічну склянку завантажують 2000г гарячої води, 115,1г 50%мас. NaOH і 200г сирої 4аміно-3,5,6-трихлорпіридин-2-карбонової кислоти (79,4%). Розчин перемішують протягом 30хв., фільтрують через паперовий фільтр і транспортують в 5л місткість живлення/рециркуляції. Вказаний розчин має масу 2315г і містить 6,8% 4-аміно-3,5,6-трихлорпіридин-2-карбонової кислоти. Вказане живлення рециркулюють з швидкістю приблизно 9,46л/хв. і при температурі 30°С через розділений електролізер, що має анод з сплаву Хастелой С (15см х4см) і срібний катод з тягнутої сі тки (15см х4см). Після звичайного анодування при +0,7В міняють полярність електролізера на протилежну і починають електроліз. Робочий катодний потенціал регулюють в інтервалі від -1,1 до -1,4В відносно Ag/AgCl (3,0Μ Сl-)- електроду порівняння. Електрод порівняння фізично розміщують безпосередньо позаду срібного електрода і з'єднують електрично з водним сольовим містком. При рециркуляції живлення 50% розчин NaOH повільно прокачують в місткість рециркуляції з підтримкою концентрації NaOH при надлишку 1,5-2,0%. Струм знаходиться в інтервалі від 1,0 до 5,2А. Після приблизно 15 годин (год.) і пропущення приблизно 213100Кл через систему електроліз припиняють і потік, що виходить з електролізера фільтрують через паперовий фільтр. Розчин нейтралізують концентрованою НСl і концентрують його до приблизно 750г сирого концентрату. Концентрат підігрівають при 85°С при перемішуванні і рН коректують до менше за 1 за допомогою концентрованої НСl протягом 30хв. Одержану суспензію охолоджують до температури навколишнього середовища і фільтрують. Залишок на фільтрі промивають 3x200мл порціями води і сушать у вакуумі при 80°С. Висушений продукт, 118,1г, визначений при 90,6% необхідного продукту; газовою хроматографією (ГХ) показане, що приблизно 4% 4аміно-3,5,6-трихлорпіридин-2-карбонової кислоти залишається як домішка. Очищений зразок 4-аміно-3,6дихлорпіридин-2-карбонової кислоти має температур у плавлення 185-187°С (декалін). 1 H-ЯМР (ДМСO-d6): δ 5 13,9 (шир, 1Н), 7,0 (шир м, 2Н), 6,8 (с, 1H); 13 С-ЯМР {1H} (ДМСО-d6): δ 165,4 (1С), 153,4 (1С), 149,5 (1С), 147,7 (1С), 111,0 (1С), 108,1 (1С). Приклад 2 Одержання 4-аміно-3,6-дихдорпіридин-2-карбонової кислоти (електролізер періодичної дії) Електролізером є 180мл хімічна склянка (2 дюйми (5,1см) діаметр x4,5 дюйми (11,4см) висота). Срібний сітчастий катод складається з стрічки 1 дюйм (2,5см)x4 дюйми (10,2см), вміщеної навколо внутрішньої стінки хімічної склянки приблизно на 0,5 дюйма (1,3см) від дна, і має стрічку шириною 0,5 дюйма (1,3см), що відходить від вер ху хімічної склянки, до якого підключена подача енергії. Анодом є графітовий стрижень діаметром 0,75 дюйми (1,9см) і довжиною 6 дюймів (15,2см), що підтримується гумовою пробкою в середині хімічної склянки і віддалений приблизно на 0,5 дюйма (1,3см) від дна. Робочий потенціал катода регулюють відносно Ag/AgCl (3,0Μ Сl-)- електроду порівняння, розташованого між срібною сіткою і стінкою хімічної склянки. Срібний сітчастий катод активують анодуванням при +0,7В в 2%-ному розчині гідроксиду натрію і 1%-ому розчині хлориду натрію у воді з подальшою зворотною поляризацією. Після активування розчин замінюють розчином 81мл води, 5,1г (0,0213моль) 4-аміно-3,5,6-трихлорпіколінової кислоти і 2,8г (0,0426моль) 85% КОН. Після продування повільним струмом азоту проводять електроліз при робочому потенціалі від -1,3 до -1,5В протягом 2 годин при температурі навколишнього середовища. Струм має початкове значення 0,83А, яке поступово знижується до 0,25А після 2 годин. Сумарну кількість 5000Кл пропускають через розчин (теоретична кількість для відновлення одного хлору з піридинового кільця становить 2050Кл). Аналіз сирого продукту методом градієнтного елюювання ВЕРХ показує зникнення початкового матеріалу і появу одиничного піка, пізніше ідентифікованого як 4-аміно-3,6-дихлорпіколіновая кислота. Приклад 3 Одержання 4-аміно-3,6-дибромпіридин-2-карбонової кислоти (електролізер періодичної дії) Використовують такий же електролізер періодичної дії, як описано в прикладі В електролізер завантажують 75мл розчину 1% хлориду натрію і 2% гідроксиду натрію у воді. Активують срібний катод і потім в розчин в електролізері вводять 0,635г метилового ефіру 4-аміно-3,5,6трибромпіколінової кислоти. Після нагрівання розчину приблизно при 75°С протягом 30хв. з гідролізом складного ефіру до карбоксилатного аніона розчин охолоджують до кімнатної температури. Проводять електроліз протягом 45хв. при робочому катодному потенціалі -0,7В. Струм становить 0,44А на початку і падає до 0,12А в кінці реакції. Пропускають сумарно 400Кл. Витягують електролітичний розчин, коректують рН розчину до нейтрального і випаровують розчин до висихання. Витягнуту тверду речовину розчиняють в суміші ацетонітрил-вода і витягують продукт препаративною ВЕРХ. Одержують зразок 110мг єдиного ізомеру з чистотою >98% по ВЕРХ і 1Н-ЯМР, ідентифікованого як 4аміно-3,6-дибромпіколінова кислота.
ДивитисяДодаткова інформація
Назва патенту англійськоюA method for preparation of 4-amino-3-halogenpicolinic acid by selective electrochemical reduction
Назва патенту російськоюСпособ получения 4-амино-3-галогенпиколиновой кислоты селективным электрохимическим восстановлением
МПК / Мітки
МПК: C07D 213/79, C25B 3/00, C07D 213/803
Мітки: електрохімічним, одержання, селективним, 4-аміно-3-галогенпіколінової, відновленням, кислоти, спосіб
Код посилання
<a href="https://ua.patents.su/4-70405-sposib-oderzhannya-4-amino-3-galogenpikolinovo-kisloti-selektivnim-elektrokhimichnim-vidnovlennyam.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 4-аміно-3-галогенпіколінової кислоти селективним електрохімічним відновленням</a>
Попередній патент: Термічно і механічно стабільний нітрат амонію та спосіб його одержання
Наступний патент: Аналоговий інтерфейс для багатоточкової інформаційно-вимірювальної системи централізованого типу
Випадковий патент: Спосіб поліпшення функціонального стану людини








