Анальгетична та антипіретична фармацевтична композиція та спосіб її виготовлення
Номер патенту: 72535
Опубліковано: 15.03.2005
Автори: Якаб Богларка, Вітаньіне Морваї Магдольна, Вегелі Ержебет, Кальманне Мате Ірма, Ковач Петерне
Формула / Реферат
1. Стабільна тверда фармацевтична композиція, що містить як активні інгредієнти парацетамол і гідрохлорид дротаверину в суміші з однією або більше органічними кислотами або сорбатом калію як стабілізатором, одну або більше допоміжних сполук, що звичайно використовуються в фармацевтиці, і необов'язково додатковий активний інгредієнт.
2. Композиція за п. 1, яка відрізняється тим, що як додатковий активний інгредієнт, містить фосфат кодеїну.
3. Композиція за п. 1 або п. 2, яка відрізняється тим, що як органічну кислоту містить органічну кислоту, що має константу дисоціації (К) у межах 10-3-10-12.
4. Композиція за п. 3, яка відрізняється тим, що як органічну кислоту містить аскорбінову або лимонну кислоту.
5. Композиція за п. 1 або п. 2, яка відрізняється тим, що містить як наповнювач і як носій, що полегшує розклад, крохмаль і як змащувальну речовину - стеаринову кислоту, її солі або ефіри, або гідровані рослинні олії.
6. Композиція за п. 1, яка відрізняється тим, що містить як активні інгредієнти парацетамол і гідрохлорид дротаверину, як стабілізатори - аскорбінову кислоту, лимонну кислоту або сорбат калію, як наповнювач і як носій, що полегшує розклад, - крохмаль, як змащувальну речовину - стеарат магнію, стеаринову кислоту, гідровану рослинну олію або тальк, як барвник - оксид заліза (III) або Ariavit Sunset Yellow.
7. Композиція за п. 1 або п. 2, яка відрізняється тим, що містить парацетамол, гідрохлорид дротаверину і фосфат кодеїну як активні інгредієнти, аскорбінову кислоту, лимонну кислоту або сорбат калію як стабілізатор, крохмаль як наповнювач і як носій, що полегшує розклад, стеарат магнію, стеаринову кислоту, гідровану рослинну олію або тальк як змащувальну речовину, оксид заліза (ІІІ) або Ariavit Sunset Yellow як барвник і полі(вінілпіролідон).
8. Композиція за п. 1, яка відрізняється тим, що вона знаходиться у формі гранулята, який може бути наповнено в капсули або спресовано в таблетки.
9. Спосіб одержання композиції за п. 1, який відрізняється тим, що використовують вологу грануляцію.
10. Спосіб за п. 9, який відрізняється тим, що парацетамол, гідрохлорид дротаверину, крохмаль, оброблений крохмаль, стабілізуючу органічну кислоту і полівінілпіролідон змішують у сухій формі, потім суміш гранулюють, використовуючи вологу грануляцію, висушують, відсортовують, змішують зі змащувальною речовиною і речовиною, що полегшує розклад, а потім пресують у таблетки.
Текст
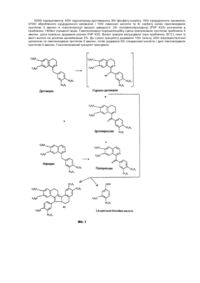
Об'єктом даного винаходу є нова анальгетична/антипіретична композиція у формі таблетки, що містить як активний інгредієнт парацетамол і гідрохлорид дротаверину або парацетамол, гідрохлорид дротаверину і кодеїн у комбінації. Нова комбінація може бути застосована орально, вона є також стійкою в фізико-хімічному значенні і швидко всмоктується. Винахід також належить до способу одержання нової композиції. Відомо, що цілий ряд фармацевтичних препаратів з різними хімічними структурами і їх комбінаціями застосовується для лікування хвороб, що супроводжуються болями різного походження, наприклад, головним болем, або лихоманкою, гарячковими станами (наприклад, парацетамол, новамінофеназон, феназон, ацетилсаліцилова кислота і їх комбінації, а саме, парацетамол + кодеїн, парацетамол + кофеїн або новамінофеназон + кофеїн, використовуються для зменшення лихоманки та/або болю). Комбінації сприяють зниженню доз окремих активних інгредієнтів, стримуючи таким чином їх шкідливі побічні ефекти, та ефективно зменшують болі через короткий час. Один з активних інгредієнтів композиції даного винаходу є парацетамол (п-ацетиламінофенол), що має сильний жарознижувальний і анальгетичний ефект. Іншим активним інгредієнтом композиції даного винаходу є гідрохлорид дротаверину, сполука, що містить ізохіноліновий скелет (хлороводнева сіль 3,4-дигідроперпарину), оригінальна молекула фірми Chinoin Pharmaceutical and Chemical Works Co. Ltd., Budapest., що використовується в терапії як спазмолітик під торговою назвою NO-SPA. Вона використовується сама по-собі або в комбінації з анальгетичним агентом (наприклад, новамінофеназон). Додатковим активним інгредієнтом, що використовується в композиції даного винаходу, є кодеїн, 3метиловий ефір морфію. Від добре поглинається орально, придатний для припинення болю середньої сили, є частим компонентом не наркотичних анальгетиків. Хімічна стабільність окремих інгредієнтів, що використовуються в комбінаціях даного винаходу, є різною. Відповідно до літературних даних парацетамол є несумісним з сильними кислотами, тому що кислотні умови сприяють його гідролізу, що призводить до виділення отруйного побічного продукту, п-амінофенолу. Щоб зменшити побічний ефект парацетамолу розроблено численні композиції, які містять поряд з парацетамолом кофеїн, допоміжний компонент (компоненти), що зв'язує кислоту, лимонну кислотну і аскорбінову кислоту (вітамін С). У цих композиціях корисною властивістю парацетамолу в порівнянні з аспірином є те, що він не ушкоджує слизову оболонку шлунку. Суміш парацетамолу, ацетилсаліцилової кислоти і кофеїну широко використовується для полегшення болю. У згаданій вище композиції полувінілбутират використовується для забезпечення хімічної стабільності ацетилсаліцилової кислоти і гідроксипропілцелюлоза для полегшення розкладення. У нейтральному і лужному середовищі гідрохлорид дротаверину окисляється до дротаверальдину за механізмом окислювального розкладення, в той час під впливом світла він розкладається до перпарину і остаточно до перпаральдину шляхом дегідрогенування молекули (Фіг.1). Обидва види розкладання можуть бути інгібовані шляхом застосування антиоксиданту або допоміжного компоненту, що зв'язує кислоту. Під час перевірок на сумісність ми знайшли, що на хімічну стабільність фармацевтичних препаратів у твердому стані, що містять гідрохлорид дротаветину, значно впливають носії таблеток, вміст вологи в гранулах та таблетках, до того ж рН-умови формули. Ми вивчили взаємодію гідрохлориду дротаверину і ряд шляхів одержання таблеток і знайшов, що розкладання гідрохлориду дротаверину істотно збільшується стеаратом магнію, змащувальною речовиною, що широко використовується під час виготовлення таблетки і що гідролізує лужним шляхом. Фосфат кодеїну не показує істотного розкладання в твердій фармацевтичній композиції для орального застосування. Відповідно до літературних даних реакція фосфату кодеїну в твердому стані з органічними кислотами, наприклад, лимонною кислотою, або змащувальними речовинами, що найбільш часто використовуються, -стеаратом магнію або стеариновою кислотою, може трансетерифікуватися [J.Pharm. Sci., Vol.76. No.1., січень, 1987]. Патентна специфікація Mallinckrodt Inc. (ЕР 0 040 472 А2) описує приготування композиції, що містить 300650мг парацетамолу і 15-60мг фосфату кодеїну. Під час приготування використовувались спрей-сушильна виробнича технологія і від 1.5% до 25% попередньо обробленого крохмалю як наповнювача. Парацетамол (100-600мг) і фосфа т кодеїну (5-60мг) також придатні для використання в м'язово-релаксаційних композиціях. Метою нашого винаходу було отримання оральних хімічно стабільних фармацевтичних композицій, що містять парацетамол і гідрохлорид дротаверину, або парацетамол, гідрохлорид дротаверину і фосфат кодеїну. Фармацевтична композиція відповідно до винаходу містить наповнювачі і носії, що звичайно використовуються, наприклад лактозу, манітол, сорбітол, змащувальні речовини, наприклад, стеарат магнію, стеаринову кислоту і тальк, до того ж речовини, що полегшують дезинтеграцію, наприклад, полі(вінілполіпіролідон), крохмаль, целюлозу і пігменти, наприклад, оксиди заліза (ІІІ), або органічні барвники. Кількість продуктів розкладання в композиціях даного винаходу є низькою, навіть після довгого зберігання. Ми знайшли, що стійкі фармацевтичні композиції можуть бути одержані за допомогою використання поряд з парацетамолом і гідрохлоридом дротаверину наповнювачів сахаридного типу, що звичайно використовуються, і як стабілізатора -органічної кислоти. Згадане вище ствердження є правдивим навіть у випадку, коли зовнішня або внутрішня фаза композиції містить інший активний інгредієнт, наприклад, фосфат кодеїну, і як носій - стеарат магнію або іншу сполуку (сполуки), що впливає на стабільність активних інгредієнтів, що використовуються. Крім того, ми знайшли, що стабільну оральну композицію, що можна спресувати в таблетку або помістити в капсулу, може бути отримано грануляцією активних інгредієнтів, парацетамолу і гідрохлориду дротаверину, окремо з наповнювачами сахаристого типу, що звичайно використовуються, використанням полі(вінілпіролідону) як носія, з наступною гомогенізацією двох типів гранул з речовинами, що полегшують дезинтеграцію, та носіями. Відповідно до наших дослідів композиції з відповідною стабільністю також можуть бути отримані шляхом пресування двох сортів гранул, що містять парацетамол і гідрохлорид дротаверину, в таблетки, що складаються з шарів. Відповідно до переважного втілення нашого винаходу як наповнювачі можуть використовува тись необроблений і оброблений крохмаль і мікрокристалічна целюлоза, як носій - крохмаль і полі(вінілпіролідон), як речовини, що полегшують дезинтеграцію, - полі(вінілпіролідон), як змащувальна речовина - стеарат магнію та/або стеаринова кислота, тальк, як стабілізатори - фармацевтично прийнятні органічні кислоти, наприклад, лимонна кислота, малеїнова кислотна або винна кислота, необов'язково аскорбінова кислота, крім того, пігменти, що звичайно використовуються, наприклад, оксид заліза (III). Додаткові допоміжні матеріали, які можуть бути застосовані, перелічуються в Угорській Фармакопеї або Європейській Фармакопеї. Переважним втіленням нашого винаходу є композиція, що містить парацетамол, гідрохлорид дротаверину, необов'язково фосфат кодеїну і крохмаль, мікрокристалічну целюлозу, стеарат магнію і стабілізуючий агент, у формі таблетки або композиція, що гранулюється для наповнення в капсули. Передбачений стабілізуючий механізм органічних кислот, використаних відповідно до винаходу, може бути інтерпретовано наступним чином: у присутності вологи стеарат магнію та сахариди сприяють, завдяки їх протон-зв'язувальному характеру, гідролізу гідрохлоридної солі дротаверину, який затримується органічними кислотами як донорами протонів. Волога може бути з повітря та/або з рідини, що гранулюється, до того ж -з допоміжних продуктів. Як стабілізатори такі органічні кислоти можуть бути застосовані в композиціях даного винаходу, що містять гідрохлорид дротаверину і парацетамол у комбінації, ступінь кислотних констант дисоціації (К) яких є 10-3-10-12, переважно менш за 10-4, і в той же час вони мають антиоксидантний характер. Наступним об'єктом нашого винаходу є спосіб одержання вищеописаних фармацевтичних композицій, відповідно до якого парацетамол, гідрохлорид дротаверину і органічну кислоту, що застосована як стабілізатор, гомогенізують разом з наповнювачем (наповнювачами), потім гранулюють для наповнення капсул та/або пресують в таблетки, що отримують вологою грануляцією. Таблетки, вироблені відповідно до винаходу, є однаково стійким з фізичних і хімічних аспектів. Вони зберігають свою стабільність довгий час в умовах прискорених і також довготривалих випробувань стабільності. Ми виконали наступні випробування, щоб порівняти здатність до зберігання композицій, що містить стабілізатор і вироблені відповідно до нашого винаходу, і композиції без стабілізатора a) Дослідження на домішки методом спектрометрії (пара-амінофенол) і рідинної хроматографії високої роздільної здатності (продукти розкладення гідрохлориду дротаверину): нижче наведено кількісну зміну під час досліджень характеристичних продуктів розкладання препаратів, а саме, пара-амінофенолу, головного продукту розкладання парацетамолу, і продукту розкладання гідрохлориду дротаверину. b) 3 випробувань фармацевтичних композицій, перш за все, було вивчено розкладання таблетки відповідно до вимог фармакопеї. c) 3 фізичних особливостей ми, в першу чергу, розглянули зовнішні прояви таблеток. Результати підсумовано в таблиці 1. З даних таблиці можна побачити, що хімічна стабільність препаратів, які містять лимонну кислоту або аскорбінову кислоту, відповідає вимогам. Таблиця 1 Дані стабільності таблеток, що містять парацетамол, дротаверин і кодеїн, які зберігались при 40°C/75%RH протягом 1 місяця Технологія Умови зберігання: 40°C/75%RH, 1 місяць Кодеїн Кодеїн Кодеїн Панадол Кодеїн Кодеїн внут- Панадол + NOзоввнутТаблетки зов- внутрішня SPA нішня рішня покриті нішня рішня фаза + фаза фаза плівкою. фаза фаза Sterotex Стабілізатор К-сорбат темноЗовнішній вигляд коричневий Дезинтегра ція (хв) 13 РАР (%) 0.0025 DROT домішка (%) 5.5 відсутній темнокоричневий 9 0.0025 7.9 Аскорбінова кислота + + Жов- темно- Жов-тий темно- темно- темно- корич- темнотий коричкорич- корич- корич- невий коричневий невий невий невий невий 3 13 2 8 15 17 9 12 0.0025 0.0025 0.0025 0.01 0.01 0.01 0.0025 0.0025 9.2 9.6 2.9 2.1 1.6 2.1 2.0 1.6 покриті таблетки темнокоричневий 24 0.0025 5.2 Кодеїн Кодеїн Кодеїн внутзов- внутрішня нішня рішня фаза фаза фаза Лимонна кислота Пояснення: РАР: пара-амінофенол DROT: дротаветин Наступні деталі винаходу показані на прикладах, але без обмежевання ними обсягу винаходу. Активні інгредієнти та допоміжні продукти і інші добавки, що використовуються в прикладах, були фармакопейної або придатної якості для фармацевтичного використання. Приклад 1 5000г парацетамолу, 400г гідрохлориду дротаверину, 190г кукурудзяного крохмалю, 500г обробленого кукурудзяного крохмалю і 100г аскорбінової кислоти гомогенізували протягом 5 хвилин в гомогенізаторі високої швидкості. 20г полі(вінілпіролідону) (PVP K25) розчиняли в приблизно 1300мл очищеної води. Гомогенізовану порошкоподібну суміш гранулювали протягом приблизно 5 хвилин, доти повільно додавали розчин PVP K25. Вологі гранули висушували (при приблизно 30°С), поки вміст їх вологи не досягав щонайменше 2%. До сухого грануляту додавали 80г фосфату кодеїну, 150г тальку, 200г мікрокристалічної целюлози і 130г полі(вінілпіролідону), гомогенізували протягом 5 хвилин, потім додавали 30г стеарату магнію і далі гомогенізували протягом 5 хвилин. Гомогенізований гранулят пресували. Приклад 2 5000г парацетамолу, 400г гідрохлориду дротаверину, 190г кукурудзяного крохмалю, 480г обробленого кукурудзяного крохмалю і 100г аскорбінової кислоти гомогенізували протягом 5 хвилин в гомогенізаторі високої швидкості. 20г полі(вінілпіролідону) (PVP K25) розчиняли в приблизно 1300мл очищеної води. Гомогенізовану порошкоподібну суміш гранулювали протягом приблизно 5 хвилин, доки повільно додавали розчин PVP K25. Вологі гранули висушували (при приблизно 30°С), поки вміст їх вологи не досягав як мінімум 2%. До сухого грануляту додавали 80г фосфату кодеїну, 150г тальку, 200г мікрокристалічної целюлози і 130г полі(вінілпіролідону), гомогенізували від 5 до 10 хвилин, потім додавали 30г стеарату магнію і далі гомогенізували протягом 5 хвилин. Гомогенізований гранулят пресували. Приклад 3 5000г парацетамолу, 400г гідрохлориду дротаверину, 130г кукурудзяного крохмалю, 390г обробленого кукурудзяного крохмалю і 100г аскорбінової кислоти гомогенізували протягом 5 хвилин в гомогенізаторі високої швидкості. 20г полі(вінілпіролідону) (PVP K25) розчиняли в приблизно 1300мл очищеної води. Гомогенізована порошкоподібна суміш гранулювали протягом приблизно 5 хвилин, доки повільно додавали розчин PVP K25. Вологі гранули висушували (при приблизно 30°С), поки вміст їх вологи не досягав щонайменше 2%. До сухого грануляту додавали 80г фосфату кодеїну, 150г тальку, 200г мікрокристалічної целюлози і 130г полі(вінілпіролідону), гомогенізували протягом 5 хвилин, потім додавали 200г гідрованої рослинної олії і далі гомогенізували протягом 10 хвилин. Гомогенізований гранулят пресували. Приклад 4 5000г парацетамолу, 400г гідрохлориду дротаверину, 160г кукурудзяного крохмалю, 500г обробленого кукурудзяного крохмалю і 100г аскорбінової кислоти гомогенізували протягом 5 хвилин в гомогенізаторі високої швидкості. 20г полі(вінілпіролідону) (PVP K25) розчиняли в приблизно 1300мл очищеної води. Гомогенізовану порошкоподібну суміш гранулювали протягом приблизно 5 хвилин, доки повільно додавали розчин PVP K25. Вологі гранули висушували (при приблизно 30°С), поки вміст їх вологи не досягав щонайменше 2%. До сухого грануляту додавали 80г фосфату кодеїну, 150г тальку, 200г мікрокристалічної целюлози, 30г жовтого оксиду заліза і 130г полі(вінілпіролідону), гомогенізували протягом 5 хвилин, потім додавали 30г стеарату магнію і далі гомогенізували протягом 5 хвилин. Гомогенізований гранулят пресували. Приклад 5 5000г парацетамолу, 400г гідрохлориду дротаверину, 214г кукурудзяного крохмалю, 500г обробленого кукурудзяного крохмалю і 100г аскорбінової кислоти гомогенізували протягом 5 хвилин в гомогенізаторі високої швидкості. 20г полі(вінілпіролідону) (PVP K25) розчиняли в приблизно 1300мл очищеної води. Гомогенізовану порошкоподібну суміш гранулювали протягом приблизно 5 хвилин, доки повільно додавали розчин PVP K25. Вологі гранули висушували (при приблизно 30°С), поки вміст їх вологи не досягав щонайменше 2%. До сухого грануляту додавали 80г фосфату кодеїну, 150г тальку та 200г мікрокристалічної целюлози та гомогенізували протягом 5 хвилин, потім додавали 10г стеарату магнію та 50г стеаринової кислоти і далі гомогенізували протягом 4-5 хвилин. Гомогенізований гранулят пресували. Приклад 6 5000г парацетамолу, 400г гідрохлсриду дротаверину, 214г кукур удзяного крохмалю, 500г обробленого кукурудзяного крохмалю та 500г аскорбінової кислоти гомогенізували протягом 5 хвилин в гомогенізаторі високої швидкості. 20г полі(вінілпіролідону) (PVP K25) розчиняли в приблизно 1300мл очищеної води. Гомогенізовану порошкоподібну суміш гранулювали протягом приблизно 5 хвилин, доки повільно додавали розчин PVP K25. Вологі гранули висушували (при приблизно 30°С), поки вміст їх вологи не досягав щонайменше 2%. До сухого грануляту додавали 80г фосфату кодеїну, 150г тальку, 200г мікрокристалічної целюлози та гомогенізували протягом 5 хвилин, потім додавали 10г стеарату магнію та 50г стеаринової кислоти і далі гомогенізували протягом 5 хвилин. Гомогенізований гранулят пресували. Приклад 7 5000г парацетамолу, 400г гідрохлориду дротаверину, 217.5г кукур удзяного крохмалю, 500г обробленого кукурудзяного крохмалю і 100г аскорбінової кислоти гомогенізували протягом 5 хвилин в гомогенізаторі високої швидкості. 20г полі(вінілпіролідону) (PVP K25) розчиняли в приблизно 1300 мл очищеної води. Гомогенізовану порошкоподібну суміш гранулювали протягом приблизно 5 хвилин, доки повільно додавали розчин PVP K25. Вологі гранули висушували (при приблизно 30°С), поки вміст їх вологи не досягав щонайменше 2%. До сухого грануляту додавали 80г фосфату кодеїну, 150г тальку, 200г мікрокристалічної целюлози і 130г полі(вінілпіролідону), гомогенізували протягом 5 хвилин, потім додавали 50г стеаринової кислоти і далі гомогенізували протягом 5 хвилин. Гомогенізований гранулят пресували. Приклад 8 5000г парацетамолу, 400г гідрохлориду дротаверину, 214г кукурудзяного крохмалю, 500г обробленого кукурудзяного крохмалю, 100г лимонної кислоти та 6г сорбату калію гомогенізували протягом 5 хвилин в гомогенізаторі високої швидкості. 20г полі(вінілпіролідону) (PVP K25) розчиняли в приблизно 1300мл очищеної води. Гомогенізовану порошкоподібну суміш гранулювали протягом приблизно 5 хвилин, доки повільно додавали розчин PVP K25. Вологі гранули висушували (при приблизно 30°С), поки вміст їх вологи не досягав як мінімум 2%. До сухого грануляту додавали 80г фосфату кодеїну, 150г тальку, 200г мікрокристалічної целюлози та гомогенізували протягом 5 хвилин, потім додавали 50г стеаринової кислоти і далі гомогенізували протягом 5 хвилин. Гомогенізований гранулят пресували. Приклад 9 5000г парацетамолу, 400г гідрохлориду дротаверину, 80г фосфату кодеїну, 164г кукурудзяного крохмалю, 4700г обробленого кукурудзяного крохмалю і 100г лимонної кислоти та 6г сорбату калію гомогенізували протягом 5 хвилин в гомогенізаторі високої швидкості. 20г полі(вінілпіролідону) (PVP K25) розчиняли в приблизно 1300мл очищеної води. Гомогенізовану порошкоподібну суміш гранулювали протягом приблизно 5 хвилин, доки повільно додавали розчин PVP K25. Вологі гранули висушували (при приблизно 30°С), поки їх вміст вологи не досягав щонайменше 2%. До сухого грануляту додавали 150г тальку, 200г мікрокристалічної целюлози та гомогенізували протягом 5 хвилин, потім додавали 50г стеаринової кислоти і далі гомогенізували протягом 5 хвилин. Гомогенізований гранулят пресували.
ДивитисяДодаткова інформація
Назва патенту англійськоюAnalgesic and antipyretic pharmaceutical composition and method for its manufacture
Назва патенту російськоюАнальгетическая и антипиретическая фармацевтическая композиция и способ ее изготовления
МПК / Мітки
МПК: A61K 31/47, A61K 31/165, A61P 29/00
Мітки: фармацевтична, спосіб, виготовлення, антипіретична, композиція, анальгетична
Код посилання
<a href="https://ua.patents.su/4-72535-analgetichna-ta-antipiretichna-farmacevtichna-kompoziciya-ta-sposib-vigotovlennya.html" target="_blank" rel="follow" title="База патентів України">Анальгетична та антипіретична фармацевтична композиція та спосіб її виготовлення</a>
Попередній патент: Пристрій обмеження параметрів електромагнітних процесів у високовольтних мережах
Наступний патент: Вимірювач магнітної індукції
Випадковий патент: Платіжний термінал