Похідні (1,2,4-триазоло[1,5-c]хіназолін-5-іл)-алкілкарбонової кислоти
Номер патенту: 91318
Опубліковано: 12.07.2010
Автори: Бабанін Анатолій Анатолійович, Сапегін Ігор Дмитрович, Волошина Вікторія Олександрівна, Коваленко Сергій Іванович, Берест Галина Григорівна, Литвиненко Микита Олексійович
Формула / Реферат
(2-R-7-R1-8-R2-9-R3-10-R4-[1,2,4]-триазоло[1,5-с]хіназолін-5-іл)алкілкарбонові кислоти формули І
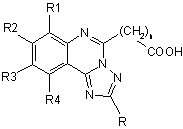 , І
, І
в якій n позначає 2, 3; R позначає алкіл-, галогеналкіл-, гідроксоалкіл-, аміноалкіл-, арилалкіл-, гетерилалкіл-, арил-, гетерил-, R1, R2, R3, R4, кожний незалежно один від одного, позначає водень, галоген, алкіл-, алкокси-.
Текст
(2-R-7-R1-8-R2-9-R3-10-R4-[1,2,4]триазоло[1,5-с]хіназолін-5-іл)алкілкарбонові кислоти формули І 2 3 use /Schlecker R., Treiber H.-J., Behl В., Hofmann H.P. (Germany); BASF AG (Germany); Заявл. 27.11.1993; Опубл. 20.05.1997], які рекомендуються для лікування нейродегенеративних хвороб, нейротоксичних розладів ЦНС, проявляють антиалергійну активність. Методи їх синтезу також зводяться до взаємодії заміщених 4-гідразинохіназолінів з хлорангідридами моноефірів дикарбонових кислот та їх діефірами, через проміжні N-ацилпохідні, які піддавали в подальшому циклізації. Спільною суттєвою ознакою прототипу та винаходу, що заявляється є те, що сполуки за прототипом та винаходом відносяться до 5заміщених [1,2,4]тріазоло[1,5-с]хіназолінів. Проте прототип, а саме [5-оксо-5,6-дигідро[1,2,4]тріазоло[1,5-с]хіназолін-2іл)]алкіл(гетерил)карбонові кислоти в положенні 5 (п'ять) містять оксогрупу, а не карбоксіалкільну групу та її функціональні похідні, по-друге, методи синтезу сполук що заявляються, зводяться до прямої циклоконденсації заміщених 2-(5-R-2H[1,2,4]тріазол-3-іл)феніламінів з ангідридами дикарбонових кислот. Крім того, введення 5карбоксіалкільного замісника до 2-R[1,2,4]тріазоло[1,5-с]хіназолінової системи суттєво впливає на направленість біологічної дії. Виходячи із зазначеного, в основу винаходу поставлено задачу створення нових (2-R-7-Rl-8R2-9-R3-10-R4-[1,2,4]-тpiaзoлo[15-c]xiнaзoлін-5iл)aлкiлкapбонових кислот, які можуть бути використані як вихідні сполуки для одержання 91318 4 функціональних похідних та пошуку біологічно активних речовин з антигіпоксичною, антиамнестичною та ноотропною дією. У відповідності з цим у винаході пропонуються нові сполуки - (2-R-7-R1-8-R2-9-R3-10-R4-[1,2,4]тріазоло[1,5-с]хіназолін-5-іл)алкілкарбонові кислоти, формули І: R1 R2 (CH2)n N COOH N R3 N R4 N R , в яких n, позначає 2, 3; R позначає алкіл-, галогеналкіл-, гідроксоалкіл-, аміноалкіл-, арилалкіл-, гетерилалкіл-, арил-, гетерил-, R1, R2, R3, R4, кожний незалежно один від одного, позначає водень, галоген, алкіл-, алкокси-. Винахід ілюструється загальною схемою та загальними способами одержання сполук. Сполуки що заявляються одержують шляхом взаємодії відповідного заміщеного [2-(5-R-2H[1,2,4]тріазол-3-іл)феніл]аміну (II) з ангідридами дикарбонових кислот (III) у киплячому органічному розчиннику (льодяна оцтова кислота, діоксан, ДМФА тощо) протягом 1-6 годин (схема). При цьому утворюються відповідні (2-R-7-R1-8-R2-9R3-10-R4-[1,2,4]-тріазоло-[1,5-с]хіназолін-5іл)алкілкарбонові кислоти з високими виходами. Схема Загальний спосіб одержання (2-R-7-R1-8-R2-9R34-10-R4-[1,2,4]-тріазоло[1,5-с]хіназолін-5іл)пропанових кислот (І). До розчину 0,01М заміщеного [2-(5-R-2H-[1,2,4]тріазол-3іл)феніл]аміну (II) в 15мл ДМФА або льодяної оцтової кислоти додають 1,10г (0,011М) янтарного ангідриду (III) та кип'ятять протягом 4-6 годин. Розчинник видаляють у вакуумі і після охолодження додають метанол. Утворений осад відфільтровують та промивають на фільтрі 10мл діетилового ефіру, сушать. 3-(2-Метил-[1,2,4]-тріазоло[1,5-с]хіназолін-5іл)пропанова кислота. Вихід: 60,9%; Т. пл. 230-232°С (уксусная кислота); ИК, см-1: 3089, 3034, 2922, 2847, 2760, 2678, 2581, 2526, 1714, 1627, 1565, 1532, 1499, 1471, 1425, 1392, 1347, 1310, 1278, 1226, 1186, 1115, 1041, 1000, 968, 922, 881, 791, 770, 726, 713, 679, 650, 630; 1H ЯМР: δ=11.70 (с, 1Н, -СООН), 8.39 (д, 1H, J=8.0, H-10), 7.97 (д, 1Н, J=8.0, Н-7), 7.88 (т, 1H, J=7.8, Н-8), 7.75 (т, 1H, J=7.8, Н-9), 3.55 (т, 2Н, 7=6.6, -СH2СН2СООН), 2.98 (т, 2Н, J=6.6, СН2СH2СООН), 2.61 (с, 3Н, СH3); LC-MS, m/z=258 [М+2], 257 [М+1]; Емпірична формула C13H12N4O2; Вирахувано: N, 21,84; Знайдено: N, 21,86. 3-(2-(Піперидін-1-іл)метил-[1,2,4]-тріазоло[1,5с]хіназолін-5-іл)пропанова кислота. Вихід: 54,8%; Т.пл. 198-200°С (уксусная кислота); ИК, см-1: 3069, 3032, 2988, 2922, 2857, 2764, 2678, 2586, 2532, 1744, 1718, 1623, 1565, 1538, 1499, 1474, 1425, 1389, 1367, 1323, 1298, 1268, 1236, 1196, 1156, 1117, 1041, 1000, 964, 932, 881, 798, 787, 726, 717, 679, 656, 630; LC-MS, m/z=341 [М+2], 340 [М+1]; Емпірична формула C18H21N5O2; Вирахувано: N, 20,63; Знайдено: N, 20,61. 3-(2-Бензил-7-метил-[1,2,4]-тріазоло[1,5с]хіназолін-5-іл)пропанова кислота. Вихід: 78,3%; Т.пл. 210-212°С (уксусная кислота); ИК, см-1: 3030, 3008, 2925, 2851, 2526, 1714, 1625, 1561, 1530, 1492, 1466, 1432, 1394, 1343, 1324, 1294, 1262, 5 1189, 1155, 1120, 1032, 1023, 1003, 986, 966, 926, 878, 838, 809, 796, 771, 745, 731, 705, 697, 661, 636, 609; 1H ЯМР: δ = 11.67 (с, 1H, -СООН), 8.42 (д, 1H, J=8.0, Н-10), 7.69 (д, 1Н, J=7.8, Н-8), 7.45 (т, 1H, J=7.8, Н-9), 7.32-7.27 (м, 4Н, Н-2΄, 3΄, 5΄, 6΄), 7.20 (м, 1Н, Н-4΄), 4.01 (с, 2Н, -СH2Рh), 3.54 (т, 2Н, J=6.6, -СH2СН2СООН), 2.97 (т, 2Н, J=6.6, СН2СH2СООН)б 2.46 (с, 3Н, СН3); LC-MS, m/z=348 [М+2], 347 [М+1]; Емпірична формула C20H18N4O2; Вирахувано: N, 16.17; Знайдено: N, 16.18. 3-(2-Фенетіл-[1,2,4]-тріазоло[1,5-с]хіназолін-5іл)пропанова кислота. Вихід: 86,7%; Т.пл. 126128°С (уксусная кислота); ИК, см-1: 3207, 3155, 3085, 3062, 3026, 2925, 2858, 2653, 2510, 1712, 1682, 1628, 1587, 1563, 1496, 1469, 1455, 1422, 1391, 1364, 1346, 1320, 1289, 1271, 1224, 1201, 1183, 1159, 1125, 1076, 1065, 1040, 1027, 985, 959, 909, 870, 843, 779, 768, 752, 699, 673, 655, 618; LCMS, m/z=348 [M+2], 347 [M+l]; Емпірична формула C20H18N4O2; Вирахувано: N, 16.18; Знайдено: N, 16.17. 3-(2-Феніл-[1,2,4]-тріазоло[1,5-с]хінозол ін-5-іл) пропанова кислота. Вихід: 72,3%; Т.пл. 240-241°С (уксусная кислота); ИК, см-1: 2902, 1713, 1623, 1606, 1561, 1525, 1477, 1445, 1429, 1384, 1350, 1320, 1300, 1274, 1175, 1151, 1136, 1111, 1100, 1077, 1026, 988, 957, 921, 877, 787, 771, 743, 722, 690, 671, 630, 614; 1H ЯМР: δ=12.34 (с, 1H, -СООН), 8.52 (д, 1Н, 7=8.0, Н-10), 8.33 (д, 2Н, Н-2΄, 6΄), 8.02 (д, 1Н, 7=8.0, Н-7), 7.94 (т, 1H, 7=7.8, Н-8), 7.81 (т, 1Н, J=7.8, Н-9), 7.62-7.58 (м, 3Н, Н-3΄, 4΄, 5΄), 3.63 (т, 2Н, 7=6.6, - СH2СН2СООН), 3.03 (т, 2Н, 7=6.6, СH2СH2СООН); LC-MS, m/z=320 [M+2], 319 [M+l]; Емпірична формула C18H14N4O2; Вирахувано: N, 17.62; Знайдено: N, 17.60. 3-(2-(Тієніл-2)-[1,2,4]тріазоло[1,5-с]хіназолін-5іл)пропанова кислота: Виход 69,6%, Т.пл. 284286°С (уксусна кислоат). ИК, см-1: 2915; 1731; 1633; 1617; 1600; 1570; 1531; 1519; 1485; 1464; 1407; 1344; 1296; 1249; 1224; 1178; 1165; 1110; 1095; 1045; 993; 968; 928; 887; 852; 795; 772; 750; 736; 725; 691; 668; 626. 1H ЯМР: δ=12.34 (с, 1Н, СООН), 8.52 (д, 1H, J=8.0, Н-10), 8.39 (d, 1H, 7=3.9, Н-3΄), 8.02 (д, 1Н, 7=8.0, Н-7), 7.94 (м, 2Н, Н-8, 5΄), 7.81 (т, 1Н, J=7.8, H-9), 7.30 (т, 1H, 7=3.9, Н-4΄), 3.63 (т, 2Н, 7=6.6, -СH2СН2СООН), 3.03 (т, 2Н, 7=6.6, -СH2СH2СООН); LC-MS, m/z=355 ([МН+3]+), 353 (МH+). Емпірична формула C15H11N4O2S; Вирахувано: N, 18.62; Знайдено: N, 18.60. Загальний спосіб одержання (2-R1-7-R2-8-R39-R4-10-R5-[1,2,4]-тріазоло[1,5-с]хіназолін-5іл)бутанових кислот (І). До розчину 0,01М заміщеного [2-(5-R-2H-[1,2,4]тріазол-3-іл)феніл] аміну (II) в 15мл ДМФА або діоксану або льодяної оцтової кислоти додають 1,25г (0,011М) глутарового ангідриду (III) та кип'ятять протягом 46 годин. Розчинник видаляють у вакуумі і після охолодження додають метанол. Утворений осад відфільтровують та промивають на фільтрі 10мл діетилового ефіру, сушать. (2-Метил-8-етокси-[1,2,4]-тріазоло[1,5с]хіназолін-5-іл)бутанова кислота. Вихід: 86,7%; Т.пл. 191-194°С (уксусная кислота); ИК, см-1: 2917, 2849, 2715, 2649, 2577, 2509, 1720, 1626, 1563, 91318 6 1536, 1504, 1472, 1455, 1415, 1396, 1378, 1347, 1332, 1307, 1279, 1250, 1181, 1114, 1060, 1043, 999, 981, 941, 908, 878, 784, 770, 745, 710, 670, 634; LC-MS, m/z=392 [M+2], 391 [M+l]; Емпірична формула C22H22N4O3; Вирахувано: N, 14.35; Знайдено: N, 14.37. (2-Бензил-[1,2,4]-тріазоло[1,5-с]хіназолін-5іл)бутанова кислота. Вихід: 86,6%; Т.пл. 167-169°С (уксусная кислота); ИК, см-1: 3031, 3009, 2971, 2921, 2655, 2584, 1717, 1630, 1562, 1532, 1495, 1468, 1457, 1430, 1416, 1398, 1367, 1337, 1312, 1278, 1253, 1198, 1185, 1158, 1115, 1057, 1035, 985, 968, 911, 881, 776, 738, 731, 706, 693, 673, 658, 636, 614; LC-MS, m/z=348 [М+2], 347 [М+1]; Емпірична формула C20H18N4O2; Вирахувано: N, 16.14; Знайдено: N, 16.17. (2-Фенетіл-[1,2,4]-тріазоло[1,5-с]хіназолін-5іл)бутанова кислота. Вихід: 61,1%; Т.пл. 186-190°С (уксусная кислота); ИК, см-1: 3022, 2973, 2940, 2861, 2821, 2736, 2660, 2591, 1716, 1627, 1612, 1562, 1535, 1500, 1470, 1454, 1416, 1400, 1371, 1343, 1317, 1279, 1255, 1220, 1199, 1189, 1158, 1143, 1117, 1073, 1058, 1029, 985, 969, 913, 850, 776, 747, 696, 675, 664, 638, 614; LC-MS, m/z=362 [М+2], 361 [М+1]; Емпірична формула C21H20N4O2; Вирахувано: N, 15.53; Знайдено: N, 15.54. (2-Феніл-8,9-диметокси-[1,2,4]-тріазоло[1,5с]хіназолін-5-іл)бутанова кислота. Вихід: 52,4%; Т.пл. 199-202°С (уксусная кислота); ИК, см-1: 3056, 2982, 2931, 2908, 2864, 2847, 2720, 2652, 2604, 1713, 1628, 1605, 1565, 1534, 1519, 1478, 1443, 1393, 1350, 1321, 1299, 1282, 1272, 1222, 1174, 1134, 1105, 1070, 1037, 1022, 991, 961, 923, 892, 877, 851, 791, 782, 765, 747, 721, 689, 669, 653; LCMS, m/z=408 [М+2], 407 [М+1]; Емпірична формула C22H22N4O4; Вирахувано: N, 13.78; Знайдено: N, 13.76. Дослідження антигіпоксичної активності в умовах моделювання порушень мозкового кровообігу за допомогою антиортостатичної гіпокінезії. Досліди проводились на кролях породи «Шиншилла» з попередньо вживленими у кору великих напівкуль, таламус та гіпоталамус ігольчатими платиновими електродами [Бекетов А.И., Сапегин И.Д., Полевик И.В. Экспериментальное (доклиническое) изучение фармакологических средств, влияющих на мозговое кровообращение: методические рекомендации. - Киев: "Авиценна", 2002. - 33с.]. Координати структур визначали відповідно до атласу стерео-таксичних досліджень на мозку кролика [Monier M., Gangloff M. Atlas for stereotaxic brain research on the conscious rabbit. - Amsterdam: Elsevier Publishing Company, 1961. - 145р.]. Напруга кисню у тканинах вказаних структур вивчали методом полярографії [Березовский В.А. Напряжение кислорода в тканях животных и человека. - Киев: Наукова думка, 1975. - 280с.; Коваленко Е.А., Березовский В.А., Эпштейн И.М. Полярографическое определение кислорода в организме. - М.: Медицина, 1975. – 231 с.]. Одержані дані без вирахувань абсолютних значень рО2, безпосередньо призводили до ± % до 7 91318 вихідного рівня, який приймали за 100 %. Моделювання антиортостатичної гіпокінезії з кутом нахилу 45° головою донизу, проводили на спеціальному стенді (розроблений на кафедрі фармакології КДМУ ім. С.І.Георгиєвського) [Полевик И.В. Влияние верапамила и нимодипина на мозговой кровоток и цереброваскулярную реактивность в покое и при антиортостатическом воздействии: Автореферат дисс. ... канд. мед. наук: 14.00.25 /Ростов-на Дону, 1991. - 21с.; Сапегин И.Д. Влияние пикамилона и фенибута на мозговое кровообращение при моделировании гемодинамических нарушений, связанных с болезнью движения: Автореф. дисс.... канд. мед. наук: 14.00.25 /Киев, 1993. – 20с.]. Досліджувані сполуки вводили у вигляді суспензій (до наважки речовини додавали 0,3мл ТВІН-80) перорально у дозі 10мг/кг за 30 хвилин до 8 переводу тварин в антиортостатичне положення. У якості препарату порівняння використовували пірацетам у дозі 250мг/кг, який вводили у вигляді водного розчину перорально, також за 30 хвилин до переводу тварин в антиортостатичне положення. Препарат порівняння «Пірацетам» проявляє помірну антигіпоксичну активність, зменшуючи при цьому рО2 найбільш виражено у гіпоталамусі (табл.). Досліджувані сполуки найбільш ефективно сприяли зниженню рО2 у даній структурі, що можна пояснити їх кращим проникненням через гематоенцефалічний бар'єр у гіпоталамусі. Важливим є те, що досліджувані сполуки у більшості випадків суттєво відрізнялись від пірацетаму як по ступеню антигіпоксичної активності, так і по її прояву у відповідних структурах мозку. Таблиця Зміни напруги кисню (рО2) у тканинах мозку кролів при АОП без застосування препаратів і на фоні дії досліджуваних сполук Показник М ±m Р М ±m Р М ±m Р М ±m Р Зміни показника у ± % до вихідного рівня (через 2 години впливу) Сполука Кора Таламус Гіпоталамус -29,22 -25,13 -19,28 Контроль 1,97 1,32 0,51
ДивитисяДодаткова інформація
Назва патенту англійською(1,2,4-triazolo[1,5-c]quinazoline-5-yl)alkylcarboxylic acid derivatives
Автори англійськоюKovalenko Serhii Ivanovych, Voloshyna Viktoria Oleksandrivna, Lytvynenko Mykyta Oleksiiovych, Sapehin Ihor Dmytrovych, Babanin Anatolii Anatoliiovych, Berest Halyna Hryhorivna
Назва патенту російськоюПроизводные (1,2,4-триазоло[1,5-с]хиназолин-5-ил)-алкилкарбоновой кислоты
Автори російськоюКоваленко Сергей Иванович, Волошина Виктория Александровна, Литвиненко Никита Алексеевич, Сапегин Игорь Дмитриевич, Бабанин Анатолий Анатолиевич, Берест Галина Григорьевна
МПК / Мітки
МПК: C07D 487/04
Мітки: похідні, кислоти, 1,2,4-триазоло[1,5-c]хіназолін-5-іл)-алкілкарбонової
Код посилання
<a href="https://ua.patents.su/4-91318-pokhidni-124-triazolo15-ckhinazolin-5-il-alkilkarbonovo-kisloti.html" target="_blank" rel="follow" title="База патентів України">Похідні (1,2,4-триазоло[1,5-c]хіназолін-5-іл)-алкілкарбонової кислоти</a>
Попередній патент: Упаковка для стрижнеподібних курильних виробів і заготовка для неї
Наступний патент: Спіральна антена
Випадковий патент: Аераційний пристрій до апаратів для вирощування мікроорганізмів








