N3 алкіловані похідні бензимідазолу як інгібітори мек
Номер патенту: 77765
Опубліковано: 15.01.2007
Автори: Воллас Елі М., Герлі Брайан Т., Ліссікатос Джозеф П., Марлоу Еллісон Л.
Формула / Реферат
1. Сполука формули
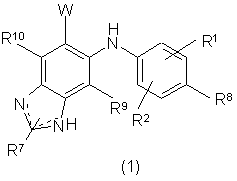
і її фармацевтично прийнятні солі, проліки і сольвати, де:
----- означає, як варіант, зв'язок, за умови, що один і лише один нітроген кільця приєднаний подвійним зв'язком;
R1, R2, R9 і R10 незалежно вибрані з гідрогену, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -OR3, -C(O)R3, -C(O)OR3, -NR4C(O)OR,
-OC(O)R3, -NR4SO2R6, -SO2NR3R4, -NR4C(O)R3, -C(O)NR3R4, -NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -NR3R4, і
С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3-С10циклоалкілалкілу,
-S(O)j(С1-С6алкіл), -S(O)j(CR4R5)m-арилу, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу, гетероциклілалкілу, -O(CR4R5)m-арилу, -NR4(CR4R5)m- арилу, - O(CR4R5)m-гетероарилу, -NR4(CR4R5)m-гетероарилу, -O(CR4R5)m-гeтepoциклiлy і -NR4(CR4R5)m-гeтepoциклiлy, де кожна алкільна, алкенільна, алкінільна, циклоалкільна, арильна, гетороарильна і гетероциклільна частина, як варіант, заміщена 1-5 групами, незалежно вибраними з оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR4SO2R6, -SO2NR3R4, -C(O)R3, -C(O)OR3, -OC(O)R3, NR4C(O)OR6, -NR4C(O)R3, - C(O)NR3R4, -NR3R4, -NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу;
R3 вибрана з гідрогену, трифлуорметилу, і
С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3-С10циклоалкілалкілу, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу, де кожна алкільна, алкенільна, алкінільна, циклоалкільна, арильна, гетороарильна і гетероциклільна частина, як варіант, заміщена 1-5 групами, незалежно вибраними з оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR'SO2R"", -SO2NR'R", -C(O)R', -C(O)OR', -OC(O)R', -NR'C(O)OR"", -NR'C(O)R", -C(O)NR'R", -SR', -S(O)R"", -SO2R"", -NR'R", -NR'C(O)NR"R'", -NR'C(NCN)NR"R'", -OR', арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу;
R', R" і R'" незалежно вибрані з гідрогену, нижчого алкілу, нижчого алкенілу, арилу і арилалкілу;
R"" вибрана з нижчого алкілу, нижчого алкенілу, арилу і арилалкілу, або
будь-які дві з R', R", R'" або R"" можуть разом з атомом, до якого вони приєднані, утворювати 4-10-членне карбоциклічне, гетероарильне або гетероциклічне кільце, кожне з яких, як варіант, заміщене 1-3 групами, незалежно вибраними з галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу, або
R3 і R4 можуть разом з атомом, до якого вони приєднані, утворювати 4-10-членне карбоциклічне, гетероарильне або гетероциклічне кільце, кожне з яких, як варіант, заміщене однією-трьома групами, незалежно вибраними з галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи,
-NR'SO2R"", -SO2NR'R", -C(O)R', -C(O)OR', -OC(O)R', -NR'C(O)OR"", -NR'C(O)R", -C(O)NR'R", -SO2R"", -NR'R", -NR'C(O)NR"R'", -NR'C(NCN)NR"R'", -OR', арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероцикпілалкілу; або
R4 і R5 незалежно є гідрогеном або С1-С6алкілом; або
R4 і R5 разом з атомом, до якого вони приєднані, утворюють 4-10-членне карбоциклічне, гетероарильне або гетороциклічне кільце, кожне з яких, як варіант, заміщене 1-3 групами, незалежно вибраними з галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR'SO2R"", -SO2NR'R", -C(O)R"", -C(O)OR', -OC(O)R', -NR'C(O)OR"", -NR'C(O)R", -C(O)NR'R", -SO2R"", -NR'R", -NR'C(O)NR"R"', -NR'C(NCN)NR"R"', -OR', арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу;
R6 вибрана з трифлуорметилу і
С1-С10алкілу, С3-С10циклоалкілу, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу, гетероциклілалкілу, де кожна алкільна, циклоалкільна, арильна, гетероарильна і гетероциклільна частина, як варіант, заміщена 1-5 групами, незалежно вибраними з оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR'SO2R"", -SO2NR'R", -C(O)R', -C(O)OR', -OC(O)R', -NR'C(O)OR"", -NR'C(O)R", -C(O)NR'R", -SO2R"", -NR'R', -NR'C(O)NR"R'", -NR'C(NCN)NR"R"',
-OR', арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу,
R7 вибрана з гідрогену і
С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3-С10циклоалкілалкілу, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу, гетероциклілалкілу, де кожна алкільна, алкенільна, алкінільна, циклоалкільна, арильна, гетороарильна і гетероциклільна частина, як варіант, заміщена 1-5 групами, незалежно вибраними з оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу,
трифлуорметоксилу, азидогрупи, -R4SO2R6, -SO2NR3R4, -C(O)R3, -C(O)OR3, -OC(O)R3 , -NR4C(O)OR6, -NR4C(O)R3, -C(O)NR3R4, -SO2R6, -NR3R4, -NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу,
W вибрана з гетероарилу, гетероциклілу, -C(O)OR3, -C(O)NR3R4, -C(O)NR4OR3, -C(O)R4OR3, -С(O)(С3-С10циклоалкіл), -С(O)(С1-С10алкіл), -С(O)(арил), -С(O)(гетероарил) і -С(O)(гетероцикліл), кожне з яких, як варіант, заміщене 1 -5 групами, незалежно вибраними з -NR3R4, -OR3, -R2 і
С1-С10алкілу, С2-С10алкенілу і С2-С10алкінілу, кожне з яких, як варіант, заміщене 1 або 2 групами, незалежно вибраними з -NR3R4 і -OR3,
R8 вибрана з гідрогену, -SCF3, -Сl, -Br, -F, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -OR3, -С(O)R3, -C(O)OR3, -NR4C(O)OR6, -OC(O)R3, -NR4SO2R6, -SO2NR3R4, -NR4C(O)R3, -C(O)NR3R4, -NR5C(O)NR3R4, -NR3R4 і
С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3-С10циклоалкіл-алкілу, -S(O)j(С1-С6алкіл), -S(O)j(CR4R5)m-арилу, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу, гетероциклілалкілу, -O(CR4R5)m-арилу, -NR4(CR4R5)m-арилу, -O(CR4R5)m-гетероарилу, -NR4(CR4R5)m-гeтepoapилy, -O(CR4R5)m-гeтepoциклілy і -NR4(CR4R5)m-гeтepoциклілy, де кожна алкільна, алкенільна, алкінільна, циклоалкільна, арильна, гетороарильна і гетероциклільна частина, як варіант, заміщена 1-5 групами, незалежно вибраними з оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR4SO2R6, -SO2NR3R4, -C(O)R3, -C(O)OR3, -OC(O)R3, -NR4C(O) OR6, -NR4C(O)R3, -C(O)NR3R4, -NR3R4, -NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу,
m дорівнює 0, 1, 2, 3, 4 або 5, і
j дорівнює 1 або 2.
2. Сполука формули
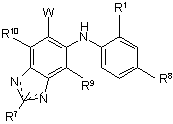
і її фармацевтично прийнятні солі, проліки і сольвати, де
------ означає, як варіант, зв'язок, за умови, що один і лише один нітроген кільця приєднаний подвійним зв'язком,
R1, R9 і R10 незалежно вибрані з гідрогену, галогену, ціаногрупи, нітрогрупи трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -OR3, -C(O)R3, -C(O)OR3, -NR4C(O)OR6,
-OC(O)R3, -NR4SO2R6, -SO2NR3R4, -NR4C(O)R3, -C(O)NR3R4, -NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -NR3R4 і
С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3-С10циклоалкілалкілу, -S(O)j(С1-С6алкіл), S(О)j(CR4R5)m-арилу, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу, гетероциклілалкілу, -O(CR4R5)m-арилу, -NR4(CR4R5)m-арилу, -O(CR4R5)m-гетероарилу, -NR4(CR4R5)m-гетероарилу, -O(CR4R5)m-гетероциклілу і -NR4(CR4R5)m-гетероциклілу, де кожна алкільна, алкенільна, алкінільна, циклоалкільна, арильна, гетероарильна і гетероциклільна частина, як варіант, заміщена 1-5 групами незалежно вибраними з оксогрупи,галогену, ціаногрупи, нітрогрупи, трифлуорметилу дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR4SO2R6, -SO2NR3R4, -C(O)R4, -C(O)OR3, -OC(O)R3, -NR4C(O)OR6, -NR4C(O)R3, -C(O)NR3R4, -NR3R4, -NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу,
R3 вибрана з гідрогену, трифлуорметилу і
С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3-С10циклоалкілалкілу, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу, де кожна алкільна, алкенільна, алкінільна, циклоалкільна, арильна, гетороарильна і гетероциклільна частина, як варіант, заміщена 1-5 групами, незалежно вибраними з оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу трифлуорметоксилу, азидогрупи, -NR'SO2R""', -SO2NR'R", -C(O)R', -C(O)OR', -OC(O)R', -NR'C(O)OR"", -NR'C(O)R", -C(O)NR'R", -SR', -S(O)R"", -SO2R"", -NR'R", -NR'C(О)R"R'", -NR'C(NCN)NR"R'", -OR', арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу,
R', R" і R'" незалежно вибрані з гідрогену, нижчого алкілу, нижчого алкенілу, арилу і арилалкілу,
R"" незалежно вибрана з нижчого алкілу, нижчого алкенілу, арилу і арилалкілу,
будь-які дві з R', R", R'" або R"" можуть разом з атомом, до якого вони приєднані, утворювати 4-10-членне карбоциклічне, гетероарильне або гетероциклічне кільце, кожне з яких, як варіант, заміщене 1-3 трьома групами, незалежно вибраними з галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу, або
R3 і R4 можуть разом з атомом, до якого вони приєднані, утворювати 4-10-членне карбоциклічне, гетероарильне або гетероциклічне кільце, кожне з яких, як варіант, заміщене 1-3 групами, незалежно вибраними з галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR'SO2R"", -SO2NR'R", -C(O)R', -C(O)OR', -OC(O)R', -NR'C(O)OR"", -NR'C(O)R", -C(O)NR'R", -SO2R"", -NR'R", -NR'C(O)NR"R'", -NR'C(NCN)NR"R'", -OR', арилу, гетероарилу арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу, або
R4 і R5 незалежно є гідрогеном або С1-С6алкілом, або
R4 і R5 разом з атомом, до якого вони приєднані, утворюють 4-10-членне карбоциклічне, гетероарильне або гетороциклічне кільце, кожне з яких, як варіант, заміщене 1-3 трьома групами, незалежно вибраними з галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR'SO2R"",
-SO2NR'R", -C(O)R', -C(O)OR', -OC(O)R', -NR'C(O)OR"", -NR'C(O)R", -C(O)NR'R", -SO2R"", -NR'R", -NR'C(O)NR"R"', -NR'C(NCN)NR"R"', -OR', арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу,
R6 вибрана з трифлуорметилу і
С1-С10алкілу, С3-С10циклоалкілу, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу, гетероциклілалкілу, де кожна алкільна, циклоалкільна, арильна, гетероарильна і гетероциклільна частина, як варіант, заміщена 1-5 групами, незалежно вибраними з оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR'SO2R"", -SO2NR'R", -C(O)R', -C(O)OR', -OC(O)R', -NR'C(O)OR"", -NR'C(O)R", -C(O)NR'R", -SO2R"", -NR'R', -NR'C(O)NR"R"', -NR'C(NCN)NR"R"',
-OR', арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу,
R7 вибрана з гідрогену і
С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3-С10циклоалкілалкілу, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу, гетероциклілалкілу, де кожна алкільна, алкенільна, алкінільна, циклоалкільна, арильна, гетороарильна і гетероциклільна частина, як варіант, заміщена 1-5 групами, незалежно вибраними з оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу трифлуорметоксилу, азидогрупи, -NR4SO2R6, -SO2NR3R4, -C(O)R3, -C(O)OR3, -OC(O)R3, -NR4C(O)OR6, -NR4C(O)R3, -C(O)NR3R4, -SO2R6, -NR3R4, -NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу,
W вибрана з гетероарилу, гетероциклілу, -C(O)OR3, -C(O)NR4R3, -C(O)NR4OR3, -C(O)R4OR3, -С(O)(С3-С10циклоалкіл), -С(O)(С1-С10алкіл), -С(O)(арил), -С(O)(гетероарил) і -С(O)(гетероцикліл), кожне з яких, як варіант, заміщене 1 -5 групами, незалежно вибраними з –NR3R4, -OR3, -R2 і С1-С10алкілу, С2-С10алкенілу і С2-С10алкінілу, кожне з яких, як варіант, заміщене однією або двома групами, незалежно вибраними з -NR3R4 і -OR3,
R8 вибрана з гідрогену, -SСF3, -Сl, -Br, -F, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -OR3, -C(O)R3, -C(O)OR3, -NR4C(O)OR6, -OC(O)R3, -NR4SO2R6, -SO2NR3R4, -NR4C(O)R3, -C(O)NR3R4, -NR5C(O)NR3R4, -NR3R4 і
С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3-С10циклоалкіл-алкілу, -S(O)j(С1-С6алкіл), -S(O)j(CR4R5)m-apилy, арилу, арилалкілу, гетероарилу гетероарилалкілу, гетероциклілу, гетероциклілалкілу, -O(CR4R5)m-арилу, -NR4(CR4R5)m-арилу, -O(CR4R5)m-гeтepoapилy, -NR4(CR4R5)m-гeтepoapилy, -O(CR4R5)m-гетероциклілу і -NR4(CR4R5)m-гетероциклілу, де кожна алкільна, алкенільна, алкінільна, циклоалкільна, арильна, гетероарильна і гетероциклільна частина, як варіант, заміщена 1-5 групами, незалежно вибраними з оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, –NR4SO2R6, -SO2NR3R4, -C(O)R3, -C(O)OR3, -OC(O)R3, -NR4C(O)OR6, -NR4C(O)R3, -C(O)NR3R4, -NR3R4, -NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу,
m дорівнює 0, 1, 2, 3, 4 або 5, і
j дорівнює 1 або 2.
3. Сполука формули
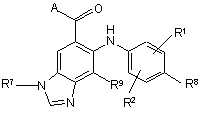
і її фармацевтичнo прийнятні солі, проліки і сольвати, де
R1, R2, і R9 незалежно вибрані з гідрогену, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи,
-OR3, -C(O)R3, -C(O)OR3, -R4C(O)OR6, -OC(O)R3, -NR4SO2R6, -SO2NR3R4, -NR4C(O)R3, -С(O)NR3R4, -NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -NR3R4 і
С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3-С10циклоалкіл-алкілу, -S(O)j(С1-С6алкіл), -S(O)j(CR4R5)m-apилy, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу, гетероциклілалкілу, -O(CR4R5)m-арилу, -NR4(CR4R5)m-арилу, -O(CR4R5)m-гeтepoapилy, -NR4(CR4R5)m-гeтepoapилy, -O(CR4R5)m-гeтepoциклілу і -NR4(CR4R5)m-гетероциклілу, де кожна алкільна, алкенільна, алкінільна, циклоалкільна, арильна, гетороарильна і гетероциклільна частина, як варіант, заміщена 1-5 групами, незалежно вибраними з оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR4SO2R6, -SO2NR3R4, -C(O)R3, -C(O)OR3, -OC(O)R3, -NR4C(O)OR6, -NR4C(O)R3, -C(O)NR3R4, -NR3R4,
-NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, гетероарилу, арилалкілу, гетероарил-алкілу, гетероциклілу і гетероциклілалкілу;
R3 вибрана з гідрогену, трифлуорметилу і
С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3-С10циклоалкілалкілу, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу, де кожна алкільна, алкенільна, алкінільна, циклоалкільна, арильна, гетороарильна і гетероциклільна частина, як варіант, заміщена 1-5 групами, незалежно вибраними з оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR'SO2R"", -SO2NR'R", -C(O)R', -C(O)OR', -OC(O)R', -NR'C(O)OR"", -NR'C(O)R", -C(O)NR'R", -SR"", -S(O)R"", -SO2R', -NR'R", -NR'C(O)NR"R'", -NR'C(NCN)NR"R'", -OR', арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу,
R', R" і R"' незалежно вибрані з гідрогену, нижчого алкілу, нижчого алкенілу арилу і арилалкілу,
R"" вибрана з нижчого алкілу, нижчого алкенілу, арилу і арилалкілу, або
будь-які дві з R', R", R"' або R"" можуть разом з атомом, до якого вони приєднані, утворювати 4-10-членне карбоциклічне, гетероарильне або гетероциклічне кільце, кожне з яких, як варіант, заміщене 1-3 групами, незалежно вибраними з галогену ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу, або
R3 і R4 можуть разом з атомом, до якого вони приєднані, утворювати 4-10-членне карбоциклічне, гетероарильне або гетороциклічне кільце, кожне з яких, як варіант, заміщене 1-3 групами, незалежно вибраними з галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR'SO2R"", -SO2NR'R", -C(O)R', -C(O)OR', -OC(O)R', -NR'C(O)OR"", -NR'C(O)R", -C(O)NR'R", -SO2R"", -NR'R", -NR'C(O)NR"R'", -NR'C(NCN)NR"R'", -OR', арилу, гетероарилу, арилалкілу гетероарилалкілу, гетероциклілу і гетероциклілалкілу, або
R4 і R5 незалежно є гідрогеном або С1-С6алкілом, або
R4 і R5 разом з атомом, до якого вони приєднані, утворюють 4-10-членне карбоциклічне, гетероарильне або гетороциклічне кільце, кожне з яких, як варіант, заміщене 1-3 трьома групами, незалежно вибраними з галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR'SO2R"", -SO2NR'R", -C(O)R', -C(O)OR', -OC(O)R', -NR'C(O)OR"", -NR'C(O)R", -C(O)NR'R", -SO2R"", -NR'R", -NR'C(O)NR"R'", -NR'C(NCN)NR"R'", -OR', арилу, гетероарилу арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу,
R6 вибрана з трифлуорметилу і
С1-С10алкілу, С3-С10циклоалкілу, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу, гетероциклілалкілу, де кожна алкільна, циклоалкільна, арильна, гетероарильна і гетероциклільна частина, як варіант, заміщена 1-5 групами, незалежно вибраними з оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR'SO2R"", -SO2NR'R", -C(O)R', -C(O)OR', -OC(O)R', -NR'C(O)OR"", -NR'C(O)R", -C(O)NR'R", -SO2R"", -NR'R', -NR'C(O)NR"R"', -NR'C(NCN)NR"R"', -OR', арилу, гетероарилу, арилалкілу, гетероарилалкілу гетероциклілу і гетероциклілалкілу,
R7 вибрана з гідрогену і
С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3-С10циклоалкілалкілу арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу, гетероциклілалкілу, де кожна алкільна, алкенільна, алкінільна, циклоалкільна, арильна, гетороарильна і гетероциклільна частина, як варіант, заміщена 1-5 групами, незалежно вибраними з оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR4SO2R6, -SO2NR3R4, -C(O)R3, -C(O)OR3, -OC(O)R3, -NR4C(O)OR6, -NR4C(O)R3, -C(O)NR3R4, -SO2R6, -NR3R4, -NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу,
А вибрана з -C(O)OR3 або -C(O)NR4OR3,
R8 вибрана з гідрогену, -SCF3, -Сl, -Br, -F, ціаногрупи нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -OR3, -С(O)R3, -C(O)OR3, -NR4C(O)OR6, -OC(O)R3, -NR4SO2R6, -SO2NR3R4, -NR4C(O)R3, -C(O)NR3R4, -NR5C(O)NR3R4, -NR3R4 і
С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3-С10циклоалкілалкілу, -S(О)J(С1-С6алкіл), -S(O)j(CR4R5)m-apилy, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу, гетероциклілалкілу, -O(CR4R5)m-арилу, -NR4(CR4R5)m-арилу, -O(CR4R5)m-гетероарилу, -NR4(CR4R5)m-гетероарилу, -O(CR4R5)m-гетероциклілу і -NR4(CR4R5)m-гетероциклілу, де кожна алкільна, алкенільна, алкінільна, циклоалкільна, арильна гетороарильна і гетероциклільна частина, як варіант, заміщена 1-5 групами, незалежно вибраними з оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR4SO2R6, -SO2NR3R4, С(O)R3, -C(O)OR3, -OC(O)R3, -NR4C(O)OR6, -NR4C(O)R3, -C(O)NR3R4, -NR3R4, -NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу,
m дорівнює 0, 1, 2, 3, 4 або 5, і
j дорівнює 1 або 2.
4. Сполука за п. 3, яка відрізняється тим, що має формулу
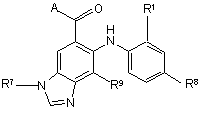 .
.
5. Сполука за п 4., яка відрізняється тим, що
R7 є С1-С10алкілом, С3-С7циклоалкілом, С3-С7циклоалкілалкілом, С3-С7гетероциклоалкілом або С3-С7гетероциклоалкілалкілом, кожний з яких може бути, як варіант, заміщений 1-3 групами, незалежно вибраними з оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR4SO2R6, -SO2NR3R4, -C(O)R3, -C(O)OR3, -OC(O)R3, -SO2R6, -NR4C(O)OR6, -NR4C(O)R3, -C(O)NR3R4, -NR3R4, -NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу,
R9 є гідрогеном або галогеном,
R1 є нижчим алкілом або галогеном, і
R8 є –ОСF3 або галогеном.
6. Сполука за п. 5, яка відрізняється тим, що R9 є флуором.
7. Сполука за п. 6, яка відрізняється тим, що R1 є метилом або хлором.
8. Сполука за п. 7, яка відрізняється тим, що R8 є хлором або бромом.
9. Сполука за п. 5, яка відрізняється тим, що А є -С(O)NR4ОR3.
10. Сполука за п. 1, яка відрізняється тим, що
R7 є С1-С10алкілом, С3-С7циклоалкілом, С3-С7циклоалкілалкілом, С3-С7гетероциклоалкілом або С3-С7гетероциклоалкілалкілом, кожний з яких може бути, як варіант, заміщений 1-3 групами, незалежно вибраними з оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR4SO2R6, -SO2NR3R4, -C(O)R3, -C(O)OR3, -OC(O)R3, -SO2R6, -NR4C(O)OR6, -NR4C(O)R3, -C(O)NR3R4, -NR3R4, -NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу,
R8 є -ОСF3, -Вr або -Сl, R2 є гідрогеном і R1 є нижчим алкілом або галогеном,
R9 є гідрогеном або галогеном,
R10 є гідрогеном, і
W є -C(O)OR3 або -C(O)NR4OR3
11. Сполука за п. 10, яка відрізняється тим, що W є -C(O)NR4R3.
12. Сполука за п. 2, яка відрізняється тим, що
R7 є С1-С10алкілом, С3-С7циклоалкілом або С3-С7циклоалкілалкілом, кожний з яких може бути, як варіант, заміщений 1-3 групами, незалежно вибраними з оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR4SO2R6, -SO2NR3R4, -C(O)R3, -C(O)OR3, -OC(O)R3, -SO2R3, -NR4C(O)OR6, -NR4C(O)R3, -C(O)NR3R4, -NR3R4, -NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу,
R8 є –OCF3, -Br або -Сl, і R1 є нижчим алкілом або галогеном,
R9 є гідрогеном або галогеном,
R10 є гідрогеном, і
W є -C(O)OR3 або –C(O)NR4OR3.
13. Сполука за п. 12, яка відрізняється тим, що W є -C(O)NR4OR3.
14. Сполука за п. 1, яка відрізняється тим, що вибрана з групи, яку складають
циклопропілметоксіамід 7-флуор-6-(4-бром-2-метилфеніламіно)-3Н-бензоімідазол-5-карбонової кислоти,
циклопропілметоксіамід 6-(4-бром-2-хлорфеніламіно)-7-флуор-3Н-бензоімідазол-5-карбонової кислоти,
(2-гідроксіетоксі)-амід 6-(4-бром-2-хлорфеніламіно)-7-флуор-3-метил-3Н-бензоімідазол-5-карбонової кислоти,
(2,3-дигідроксипропокси)-амід 6-(4-бром-2-хлорфеніламіно)-7-флуор-3-метил-3Н-бензоімідазол-5-карбонової кислоти,
(2-гідроксіетоксі)-амід 6-(4-бром-2-хлорфеніламіно)-7-флуор-3-(тетрагідропіран-2-ілметил)-3Н-бензоімідазол-5-карбонової кислоти,
[6-(5-аміно-[1,3,4]оксадіазол-2-іл)-4-флуор-1Н-бензоімідазол-5-іл]-(4-бром-2-метилфеніл)-амін,
1-[6-(4-бром-2-хлорфеніламіно)-7-флуор-3-метил-3Н-бензоімідазол-5-іл]-2-гідроксиетанон,
1-[6-(4-бром-2-хлорфеніламіно)-7-флуор-3Н-бензоімідазол-5-іл]-2-метоксіетанон,
(2-гідрокси-1,1-диметилетоксі)-амід 6-(4-бром-2-хлорфеніламіно)-7-флуор-3-метил-3Н-бензоімідазол-5-карбонової кислоти,
(2-гідроксіетокси)-амід 6-(4-бром-2-хлорфеніламіно)-7-флуор-3-(тетрагідрофуран-2-ілметил)-3Н-бензоімідазол-5-карбонової кислоти,
(2-гідроксіетокси)-амід 6-(4-бром-2-хлорфеніламіно)-7-флуор-3Н-бензоімідазол-5-карбонової кислоти,
(2-гідроксіетокси)-амід 6-(4-бром-2-флуорфеніламіно)-7-флуор-3-метил-3Н-бензоімідазол-5-карбонової кислоти і
(2-гідроксіетокси)-амід 6-(2,4-дихлорфеніламіно)-7-флуор-3-метил-3Н-бензоімідазол-5-карбонової кислоти.
15. Композиція, яка містить сполуку за п. 1 і фармацевтично прийнятний носій.
16. Спосіб інгібування активності МЕК ссавців, який включає введення ефективної кількості сполуки за п. 1 цьому ссавцю.
17. Спосіб лікування гіперпроліферативного розладу у ссавців, який включає введення ефективної кількості сполуки за п. 1 цьому ссавцю.
Текст
1. Сполука формули W H 10 R R1 N C2 2 (19) 1 3 77765 4 роциклілу і гетероциклілалкілу, де кожна алкільна, R7 вибрана з гідрогену і алкенільна, алкінільна, циклоалкільна, арильна, С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3гетороарильна і гетероциклільна частина, як варіС10циклоалкілу, С3-С10циклоалкілалкілу, арилу, ант, заміщена 1-5 групами, незалежно вибраними арилалкілу, гетероарилу, гетероарилалкілу, гетез оксогрупи, галогену, ціаногрупи, нітрогрупи, трироциклілу, гетероциклілалкілу, де кожна алкільна, флуорметилу, дифлуорметоксилу, трифлуорметоалкенільна, алкінільна, циклоалкільна, арильна, ксилу, азидогрупи, -NR'SO2R"", -SO2NR'R", -C(O)R', гетороарильна і гетероциклільна частина, як варі-C(O)OR', -OC(O)R', -NR'C(O)OR"", -NR'C(O)R", ант, заміщена 1-5 групами, незалежно вибраними C(O)NR'R", -SR', -S(O)R"", -SO2R"", -NR'R", з оксогрупи, галогену, ціаногрупи, нітрогрупи, триNR'C(O)NR"R'", -NR'C(NCN)NR"R'", -OR', арилу, флуорметилу, ди флуорметоксилу, гетероарилу, арилалкілу, гетероарилалкілу, гететрифлуорметоксилу, азидогрупи, -R4SO2R6, роциклілу і гетероциклілалкілу; SO2NR3R4, -C(O)R3 , -C(O)OR 3, -OC(O)R 3 , R', R" і R'" незалежно вибрані з гідрогену, нижчого NR4C(O)OR 6, -NR4C(O)R3, -C(O)NR3R4, -SO2R6 , алкілу, нижчого алкенілу, арилу і арилалкілу; NR3R4, -NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, R"" вибрана з нижчого алкілу, нижчого алкенілу, арилу, гетероарилу, арилалкілу, гетероарилалкілу, арилу і арилалкілу, або гетероциклілу і гетероциклілалкілу, будь-які дві з R', R", R'" або R"" можуть разом з W вибрана з гетероарилу, гетероциклілу, атомом, до якого вони приєднані, утворювати 4C(O)OR 3, -C(O)NR3R4, -C(O)NR4 OR3, -C(O)R4 OR3, 10-членне карбоциклічне, гетероарильне або геС(O)(С3-С10циклоалкіл), -С(O)(С1-С10алкіл), тероциклічне кільце, кожне з яких, як варіант, заС(O)(арил), -С(O)(гетероарил) і міщене 1-3 групами, незалежно вибраними з галоС(O)(гетероцикліл), кожне з яких, як варіант, замігену, ціаногрупи, нітрогрупи, трифлуорметилу, щене 1 -5 групами, незалежно вибраними з дифлуорметоксилу, трифлуорметоксилу, азидогNR3R4, -OR3, -R2 і рупи, арилу, гетероарилу, арилалкілу, гетероариС1-С10алкілу, С2-С10алкенілу і С2-С10алкінілу, кожне лалкілу, гетероциклілу і гетероциклілалкілу, або з яких, як варіант, заміщене 1 або 2 групами, незаR3 і R4 можуть разом з атомом, до якого вони прилежно вибраними з -NR3R4 і -OR3, єднані, утворювати 4-10-членне карбоциклічне, R8 вибрана з гідрогену, -SCF3, -Сl, -Br, -F, ціаноггетероарильне або гетероциклічне кільце, кожне з рупи, нітрогрупи, трифлуорметилу, дифлуорметояких, як варіант, заміщене однією-трьома групами, ксилу, трифлуорметоксилу, азидогрупи, -OR3, незалежно вибраними з галогену, ціаногрупи, нітС(O)R3, -C(O)OR 3, -NR4C(O)OR 6 , -OC(O)R3, рогрупи, трифлуорметилу, ди флуорметоксилу, NR4SO2R6, -SO 2NR3R4, -NR4C(O)R3, -C(O)NR3R4, трифлуорметоксилу, азидогрупи, NR5C(O)NR3R4, -NR 3R4 і -NR'SO2R"", -SO2NR'R", -C(O)R', -C(O)OR', С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3OC(O)R', -NR'C(O)OR"", -NR'C(O)R", -C(O)NR'R", С10циклоалкілу, С3-С10циклоалкіл-алкілу, -S(O)j(С1SO2R"", -NR'R", -NR'C(O)NR"R'", С6алкіл), -S(O)j(CR4R5)m-арилу, арилу, арилалкілу, NR'C(NCN)NR"R'", -OR', арилу, гетероарилу, аригетероарилу, гетероарилалкілу, гетероциклілу, лалкілу, гетероарилалкілу, гетероциклілу і гетерогетероциклілалкілу, -O(CR4R5)m-арилу, 4 4 5 цикпілалкілу; або NR (CR R )m-арилу, -O(CR4R5) m-гетероарилу, R4 і R5 незалежно є гідрогеном або С 1-С6алкілом; NR4(CR4R5)m-гeтepoapилy, -O(CR4R5)m4 4 5 або гeтepoциклілy і -NR (CR R )m-гeтepoциклілy, де R4 і R5 разом з атомом, до якого вони приєднані, кожна алкільна, алкенільна, алкінільна, циклоалкіутворюють 4-10-членне карбоциклічне, гетероарильна, арильна, гетороарильна і гетероциклільна льне або гетороциклічне кільце, кожне з яких, як частина, як варіант, заміщена 1-5 групами, незаваріант, заміщене 1-3 групами, незалежно вибралежно вибраними з оксогрупи, галогену, ціаногруними з галогену, ціаногрупи, нітрогрупи, трифлуопи, нітрогрупи, трифлуорметилу, ди флуорметокрметилу, дифлуорметоксилу, трифлуорметоксилу, силу, три флуорметоксилу, азидогрупи, -NR4SO2R6, азидогрупи, -NR'SO2R"", -SO2NR'R", -C(O)R"", -SO2NR3R4, -C(O)R3, -C(O)OR3, -OC(O)R 3, -NR4C(O) C(O)OR', -OC(O)R', -NR'C(O)OR"", -NR'C(O)R", OR6, -NR4C(O)R3, -C(O)NR3R4, -NR3R4, C(O)NR'R", -SO2R"", -NR'R", -NR'C(O)NR"R"', NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, NR'C(NCN)NR"R"', -OR', арилу, гетероарилу, аригетероарилу, арилалкілу, гетероарилалкілу, гетелалкілу, гетероарилалкілу, гетероциклілу і гетеророциклілу і гетероциклілалкілу, циклілалкілу; m дорівнює 0, 1, 2, 3, 4 або 5, і R6 вибрана з трифлуорметилу і j дорівнює 1 або 2. С1-С10алкілу, С3-С10циклоалкілу, арилу, арилалкі2. Сполука формули лу, гетероарилу, гетероарилалкілу, гетероциклілу, R1 W гетероциклілалкілу, де кожна алкільна, циклоалкіH льна, арильна, гетероарильна і гетероциклільна R10 N частина, як варіант, заміщена 1-5 групами, незалежно вибраними з оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, ди флуорметокR8 N R9 силу, три флуорметоксилу, азидогрупи, N NR'SO2R"", -SO2NR'R", -C(O)R', -C(O)OR', 7 OC(O)R', -NR'C(O)OR"", -NR'C(O)R", -C(O)NR'R", R SO2R"", -NR'R', -NR'C(O)NR"R'", -NR'C(NCN)NR"R"', і її фармацевтично прийнятні солі, проліки і соль-OR', арилу, гетероарилу, арилалкілу, гетероаривати, де лалкілу, гетероциклілу і гетероциклілалкілу, 5 77765 6 ------ означає, як варіант, зв'язок, за умови, що C(O)R', -C(O)OR', -OC(O)R', -NR'C(O)OR"", один і лише один нітроген кільця приєднаний поNR'C(O)R", -C(O)NR'R", -SO2R"", -NR'R", двійним зв'язком, NR'C(O)NR"R'", -NR'C(NCN)NR"R'", -OR', арилу, R1, R9 і R10 незалежно вибрані з гідрогену, галогегетероарилу арилалкілу, гетероарилалкілу, гетену, ціаногрупи, нітрогрупи трифлуорметилу, дифроциклілу і гетероциклілалкілу, або луорметоксилу, трифлуорметоксилу, азидогрупи, R4 і R5 незалежно є гідрогеном або С 1-С6алкілом, 3 3 3 4 6 OR , -C(O)R , -C(O)OR , -NR C(O)OR , або -OC(O)R3, -NR4SO2R6 , -SO2NR3R4, -NR4C(O)R3 , R4 і R5 разом з атомом, до якого вони приєднані, 3 4 5 3 4 5 3 4 C(O)NR R , -NR C(O)NR R , -NR C(NCN)NR R , утворюють 4-10-членне карбоциклічне, гетероариNR3R4 і льне або гетороциклічне кільце, кожне з яких, як С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3варіант, заміщене 1-3 трьома групами, незалежно С10циклоалкілу, С3-С10циклоалкілалкілу, -S(O)j(С1вибраними з галогену, ціаногрупи, нітрогрупи, С6алкіл), S(О)j(CR4R5)m-арилу, арилу, арилалкілу, трифлуорметилу, дифлуорметоксилу, трифлуоргетероарилу, гетероарилалкілу, гетероциклілу, метоксилу, азидогрупи, -NR'SO2R"", гетероциклілалкілу, -O(CR4R5)m-арилу, -SO2NR'R", -C(O)R', -C(O)OR', -OC(O)R', NR4(CR4R5)m-арилу, -O(CR4R5) m-гетероарилу, NR'C(O)OR"", -NR'C(O)R", -C(O)NR'R", -SO2R"", NR4(CR4R5)m-гетероарилу, -O(CR4R5)mNR'R", -NR'C(O)NR"R"', -NR'C(NCN)NR"R"', -OR', гетероциклілу і -NR4(CR4R5)m-гетероциклілу, де арилу, гетероарилу, арилалкілу, гетероарилалкілу, кожна алкільна, алкенільна, алкінільна, циклоалкігетероциклілу і гетероциклілалкілу, льна, арильна, гетероарильна і гетероциклільна R6 вибрана з трифлуорметилу і частина, як варіант, заміщена 1-5 групами незалеС1-С10алкілу, С3-С10циклоалкілу, арилу, арилалкіжно вибраними з оксогрупи, галогену, ціаногрупи, лу, гетероарилу, гетероарилалкілу, гетероциклілу, нітрогрупи, трифлуорметилу ди флуорметоксилу, гетероциклілалкілу, де кожна алкільна, циклоалкітрифлуорметоксилу, азидогрупи, -NR4SO2R6, льна, арильна, гетероарильна і гетероциклільна SO2NR3R4, -C(O)R4 , -C(O)OR 3, -OC(O)R 3, частина, як варіант, заміщена 1-5 групами, незаNR4C(O)OR 6, -NR4C(O)R3, -C(O)NR3R4, -NR3R4, лежно вибраними з оксогрупи, галогену, ціаногруNR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, пи, нітрогрупи, трифлуорметилу, ди флуорметокгетероарилу, арилалкілу, гетероарилалкілу, гетесилу, три флуорметоксилу, азидогрупи, роциклілу і гетероциклілалкілу, NR'SO2R"", -SO2NR'R", -C(O)R', -C(O)OR', R3 вибрана з гідрогену, трифлуорметилу і OC(O)R', -NR'C(O)OR"", -NR'C(O)R", -C(O)NR'R", С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3SO2R"", -NR'R', -NR'C(O)NR"R"', -NR'C(NCN)NR"R"', С10циклоалкілу, С3-С10циклоалкілалкілу, арилу, -OR', арилу, гетероарилу, арилалкілу, гетероариарилалкілу, гетероарилу, гетероарилалкілу, гетелалкілу, гетероциклілу і гетероциклілалкілу, роциклілу і гетероциклілалкілу, де кожна алкільна, R7 вибрана з гідрогену і алкенільна, алкінільна, циклоалкільна, арильна, С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3гетороарильна і гетероциклільна частина, як варіС10циклоалкілу, С3-С10циклоалкілалкілу, арилу, ант, заміщена 1-5 групами, незалежно вибраними арилалкілу, гетероарилу, гетероарилалкілу, гетез оксогрупи, галогену, ціаногрупи, нітрогрупи, трироциклілу, гетероциклілалкілу, де кожна алкільна, флуорметилу, дифлуорметоксилу трифлуорметоалкенільна, алкінільна, циклоалкільна, арильна, ксилу, азидогрупи, -NR'SO2R""', -SO2NR'R", гетороарильна і гетероциклільна частина, як варіC(O)R', -C(O)OR', -OC(O)R', -NR'C(O)OR"", ант, заміщена 1-5 групами, незалежно вибраними NR'C(O)R", -C(O)NR'R", -SR', -S(O)R"", -SO2R"", з оксогрупи, галогену, ціаногрупи, нітрогрупи, триNR'R", -NR'C(О)R"R'", -NR'C(NCN)NR"R'", -OR', флуорметилу, дифлуорметоксилу трифлуорметоарилу, гетероарилу, арилалкілу, гетероарилалкілу, ксилу, азидогрупи, -NR4SO2R6, -SO2NR3R4 , гетероциклілу і гетероциклілалкілу, C(O)R3, -C(O)OR 3, -OC(O)R 3, -NR4C(O)OR 6, R', R" і R'" незалежно вибрані з гідрогену, нижчого NR4C(O)R3, -C(O)NR3R4, -SO2R6, -NR3R4, алкілу, нижчого алкенілу, арилу і арилалкілу, NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, R"" незалежно вибрана з нижчого алкілу, нижчого гетероарилу, арилалкілу, гетероарилалкілу, гетеалкенілу, арилу і арилалкілу, роциклілу і гетероциклілалкілу, будь-які дві з R', R", R'" або R"" можуть разом з W вибрана з гетероарилу, гетероциклілу, атомом, до якого вони приєднані, утворювати 4C(O)OR 3, -C(O)NR4R3, -C(O)NR4 OR3, -C(O)R4 OR3, 10-членне карбоциклічне, гетероарильне або геС(O)(С3-С10циклоалкіл), -С(O)(С1-С10алкіл), тероциклічне кільце, кожне з яких, як варіант, заС(O)(арил), -С(O)(гетероарил) і міщене 1-3 трьома групами, незалежно вибраними С(O)(гетероцикліл), кожне з яких, як варіант, заміз галогену, ціаногрупи, нітрогрупи, трифлуорметищене 1 -5 групами, незалежно вибраними з – лу, ди флуорметоксилу, трифлуорметоксилу, азиNR3R4, -OR3 , -R2 і С1-С10алкілу, С2-С10алкенілу і С 2догрупи, арилу, гетероарилу, арилалкілу, гетероС10алкінілу, кожне з яких, як варіант, заміщене арилалкілу, гетероциклілу і гетероциклілалкілу, однією або двома групами, незалежно вибраними або з -NR3R4 і -OR3, 3 4 R і R можуть разом з атомом, до якого вони приR8 вибрана з гідрогену, -SСF3, -Сl, -Br, -F, ціаногєднані, утворювати 4-10-членне карбоциклічне, рупи, нітрогрупи, трифлуорметилу, дифлуорметогетероарильне або гетероциклічне кільце, кожне з ксилу, трифлуорметоксилу, азидогрупи, -OR3, яких, як варіант, заміщене 1-3 групами, незалежно C(O)R3, -C(O)OR 3, -NR4C(O)OR 6 , -OC(O)R3, вибраними з галогену, ціаногрупи, нітрогрупи, NR4SO2R6, -SO 2NR3R4, -NR4C(O)R3, -C(O)NR3R4, трифлуорметилу, дифлуорметоксилу, трифлуорNR5C(O)NR3R4, -NR 3R4 і метоксилу, азидогрупи, -NR'SO2R"", -SO2NR'R", 7 77765 8 С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3дифлуорметоксилу, трифлуорметоксилу, азидогС10циклоалкілу, С3-С10циклоалкіл-алкілу, -S(O)j(С1рупи, -NR'SO2R"", -SO2NR'R", -C(O)R', -C(O)OR', С6алкіл), -S(O)j(CR4R5)m-apилy, арилу, арилалкілу, OC(O)R', -NR'C(O)OR"", -NR'C(O)R", -C(O)NR'R", гетероарилу гетероарилалкілу, гетероциклілу, геSR"", -S(O)R"", -SO2R', -NR'R", -NR'C(O)NR"R'", тероциклілалкілу, -O(CR4R5)m-арилу, NR'C(NCN)NR"R'", -OR', арилу, гетероарилу, ариNR4(CR4R5)m-арилу, -O(CR4R5) m-гeтepoapилy, лалкілу, гетероарилалкілу, гетероциклілу і гетероNR4(CR4R5)m-гeтepoapилy, -O(CR4R5)mциклілалкілу, гетероциклілу і -NR4(CR4R5)m-гетероциклілу, де R', R" і R"' незалежно вибрані з гідрогену, нижчого кожна алкільна, алкенільна, алкінільна, циклоалкіалкілу, нижчого алкенілу арилу і арилалкілу, льна, арильна, гетероарильна і гетероциклільна R"" вибрана з нижчого алкілу, нижчого алкенілу, частина, як варіант, заміщена 1-5 групами, незаарилу і арилалкілу, або лежно вибраними з оксогрупи, галогену, ціаногрубудь-які дві з R', R", R"' або R"" можуть разом з пи, нітрогрупи, трифлуорметилу, ди флуорметокатомом, до якого вони приєднані, утворювати 4силу, трифлуорметоксилу, азидогрупи, – 10-членне карбоциклічне, гетероарильне або геNR4SO2R6, -SO2NR3R4, -C(O)R3, -C(O)OR 3, тероциклічне кільце, кожне з яких, як варіант, заOC(O)R3, -NR4C(O)OR 6 , -NR4C(O)R3, -C(O)NR 3R4, міщене 1-3 групами, незалежно вибраними з галоNR3R4, -NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, гену ціаногрупи, нітрогрупи, трифлуорметилу, арилу, гетероарилу, арилалкілу, гетероарилалкілу, дифлуорметоксилу, трифлуорметоксилу, азидоггетероциклілу і гетероциклілалкілу, рупи, арилу, гетероарилу, арилалкілу, гетероариm дорівнює 0, 1, 2, 3, 4 або 5, і лалкілу, гетероциклілу і гетероциклілалкілу, або j дорівнює 1 або 2. R3 і R4 можуть разом з атомом, до якого вони при3. Сполука формули єднані, утворювати 4-10-членне карбоциклічне, гетероарильне або гетороциклічне кільце, кожне з A O яких, як варіант, заміщене 1-3 групами, незалежно H R1 вибраними з галогену, ціаногрупи, нітрогрупи, N трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, -NR'SO2R"", -SO2NR'R", C(O)R', -C(O)OR', -OC(O)R', -NR'C(O)OR"", 7 8 9 R R R N NR'C(O)R", -C(O)NR'R", -SO2R"", -NR'R", NR'C(O)NR"R'", -NR'C(NCN)NR"R'", -OR', арилу, N R2 гетероарилу, арилалкілу гетероарилалкілу, гетеі її фармацевтичнo прийнятні солі, проліки і сольроциклілу і гетероциклілалкілу, або вати, де R4 і R5 незалежно є гідрогеном або С 1-С6алкілом, R1, R2, і R9 незалежно вибрані з гідрогену, галогеабо ну, ціаногрупи, нітрогрупи, трифлуорметилу, дифR4 і R5 разом з атомом, до якого вони приєднані, луорметоксилу, трифлуорметоксилу, азидогрупи, 3 3 3 4 6 3 утворюють 4-10-членне карбоциклічне, гетероари-OR , -C(O)R , -C(O)OR , -R C(O)OR , -OC(O)R , льне або гетороциклічне кільце, кожне з яких, як NR4SO2R6, -SO 2NR3R4, -NR4C(O)R3, -С(O)NR3R4, варіант, заміщене 1-3 трьома групами, незалежно NR5C(O)NR3R4, -NR 5C(NCN)NR3R4, -NR 3R4 і вибраними з галогену, ціаногрупи, нітрогрупи, С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3трифлуорметилу, дифлуорметоксилу, трифлуорС10циклоалкілу, С3-С10циклоалкіл-алкілу, -S(O)j(С1метоксилу, азидогрупи, -NR'SO2R"", -SO2NR'R", С6алкіл), -S(O)j(CR4R5)m-apилy, арилу, арилалкілу, C(O)R', -C(O)OR', -OC(O)R', -NR'C(O)OR"", гетероарилу, гетероарилалкілу, гетероциклілу, NR'C(O)R", -C(O)NR'R", -SO2R"", -NR'R", гетероциклілалкілу, -O(CR4R5)m-арилу, NR'C(O)NR"R'", -NR'C(NCN)NR"R'", -OR', арилу, NR4(CR4R5)m-арилу, -O(CR4R5) m-гeтepoapилy, 4 4 5 4 5 гетероарилу арилалкілу, гетероарилалкілу, гетеNR (CR R )m-гeтepoapилy, -O(CR R )mроциклілу і гетероциклілалкілу, гeтepoциклілу і -NR4(CR4R5)m-гетероциклілу, де R6 вибрана з трифлуорметилу і кожна алкільна, алкенільна, алкінільна, циклоалкіС1-С10алкілу, С3-С10циклоалкілу, арилу, арилалкільна, арильна, гетороарильна і гетероциклільна лу, гетероарилу, гетероарилалкілу, гетероциклілу, частина, як варіант, заміщена 1-5 групами, незагетероциклілалкілу, де кожна алкільна, циклоалкілежно вибраними з оксогрупи, галогену, ціаногрульна, арильна, гетероарильна і гетероциклільна пи, нітрогрупи, трифлуорметилу, ди флуорметокчастина, як варіант, заміщена 1-5 групами, незасилу, три флуорметоксилу, азидогрупи, -NR4SO2R6, лежно вибраними з оксогрупи, галогену, ціаногру-SO2NR3R4, -C(O)R3 , -C(O)OR 3, -OC(O)R 3, пи, нітрогрупи, трифлуорметилу, ди флуорметокNR4C(O)OR 6, -NR 4C(O)R3, -C(O)NR 3R4, -NR 3R4, силу, три флуорметоксилу, азидогрупи, -NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, NR'SO2R"", -SO2NR'R", -C(O)R', -C(O)OR', гетероарилу, арилалкілу, гетероарил-алкілу, гетеOC(O)R', -NR'C(O)OR"", -NR'C(O)R", -C(O)NR'R", роциклілу і гетероциклілалкілу; SO2R"", -NR'R', -NR'C(O)NR"R"', -NR'C(NCN)NR"R"', R3 вибрана з гідрогену, трифлуорметилу і -OR', арилу, гетероарилу, арилалкілу, гетероариС1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3лалкілу гетероциклілу і гетероциклілалкілу, С10циклоалкілу, С3-С10циклоалкілалкілу, арилу, R7 вибрана з гідрогену і арилалкілу, гетероарилу, гетероарилалкілу, гетеС1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3роциклілу, де кожна алкільна, алкенільна, алкініС10циклоалкілу, С3-С10циклоалкілалкілу арилу, льна, циклоалкільна, арильна, гетороарильна і арилалкілу, гетероарилу, гетероарилалкілу, гетегетероциклільна частина, як варіант, заміщена 1-5 роциклілу, гетероциклілалкілу, де кожна алкільна, групами, незалежно вибраними з оксогрупи, галоалкенільна, алкінільна, циклоалкільна, арильна, гену, ціаногрупи, нітрогрупи, трифлуорметилу, 9 77765 10 гетороарильна і гетероциклільна частина, як варі6. Сполука за п. 5, яка відрізняється тим, що R9 є ант, заміщена 1-5 групами, незалежно вибраними флуором. з оксогрупи, галогену, ціаногрупи, нітрогрупи, три7. Сполука за п. 6, яка відрізняється тим, що R1 є флуорметилу, дифлуорметоксилу, трифлуорметометилом або хлором. ксилу, азидогрупи, -NR4SO2R6, -SO2NR3R4 , 8. Сполука за п. 7, яка відрізняється тим, що R8 є 3 3 3 4 6 C(O)R , -C(O)OR , -OC(O)R , -NR C(O)OR , хлором або бромом. NR4C(O)R3, -C(O)NR3R4, -SO2R6, -NR3R4, 9. Сполука за п. 5, яка відрізняється тим, що А є NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, С(O)NR4ОR3. гетероарилу, арилалкілу, гетероарилалкілу, гете10. Сполука за п. 1, яка відрізняється тим, що роциклілу і гетероциклілалкілу, R7 є С1-С10алкілом, С3-С7циклоалкілом, С33 4 3 А вибрана з -C(O)OR або -C(O)NR OR , С7циклоалкілалкілом, С3-С7гетероциклоалкілом R8 вибрана з гідрогену, -SCF3, -Сl, -Br, -F, ціаногабо С3-С7гетероциклоалкілалкілом, кожний з яких рупи нітрогрупи, трифлуорметилу, ди флуорметокможе бути, як варіант, заміщений 1-3 групами, несилу, трифлуорметоксилу, азидогрупи, -OR3, залежно вибраними з оксогрупи, галогену, ціаногС(O)R3, -C(O)OR 3, -NR4C(O)OR 6 , -OC(O)R3, рупи, нітрогрупи, трифлуорметилу, дифлуорметоNR4SO2R6, -SO 2NR3R4, -NR4C(O)R3, -C(O)NR3R4, ксилу, трифлуорметоксилу, азидогрупи, NR5C(O)NR3R4, -NR 3R4 і NR4SO2R6, -SO2NR3R4, -C(O)R3, -C(O)OR 3, С1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3OC(O)R3, -SO2R 6, -NR4C(O)OR 6, -NR4C(O)R3, С10циклоалкілу, С3-С10циклоалкілалкілу, -S(О)J(С1C(O)NR3R4, -NR3R4, -NR5C(O)NR3R4, С6алкіл), -S(O)j(CR4R5)m-apилy, арилу, арилалкілу, NR5C(NCN)NR3R4, -OR3, арилу, ге тероарилу, аригетероарилу, гетероарилалкілу, гетероциклілу, лалкілу, гетероарилалкілу, гетероциклілу і гетерогетероциклілалкілу, -O(CR4R5)m-арилу, циклілалкілу, NR4(CR4R5)m-арилу, -O(CR4R5) m-гетероарилу, R8 є -ОСF3 , -Вr або -Сl, R2 є гідрогеном і R1 є ниж4 4 5 4 5 NR (CR R )m-гетероарилу, -O(CR R )mчим алкілом або галогеном, гетероциклілу і -NR4(CR4R5)m-гетероциклілу, де R9 є гідрогеном або галогеном, кожна алкільна, алкенільна, алкінільна, циклоалкіR10 є гідрогеном, і льна, арильна гетороарильна і гетероциклільна W є -C(O)OR 3 або -C(O)NR4OR3 частина, як варіант, заміщена 1-5 групами, неза11. Сполука за п. 10, яка відрізняється тим, що W лежно вибраними з оксогрупи, галогену, ціаногрує -C(O)NR4R3. пи, нітрогрупи, трифлуорметилу дифлуорметокси12. Сполука за п. 2, яка відрізняється тим, що лу, трифлуорметоксилу, азидогрупи, -NR4SO2R6, R7 є С1-С10алкілом, С3-С7циклоалкілом або С3SO2NR3R4, С(O)R3 , -C(O)OR 3, -OC(O)R 3, С7циклоалкілалкілом, кожний з яких може бути, як NR4C(O)OR 6, -NR4C(O)R3, -C(O)NR3R4, -NR3R4, варіант, заміщений 1-3 групами, незалежно вибраNR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, ними з оксогрупи, галогену, ціаногрупи, нітрогрупи, гетероарилу, арилалкілу, гетероарилалкілу, гететрифлуорметилу, дифлуорметоксилу, трифлуорроциклілу і гетероциклілалкілу, метоксилу, азидогрупи, -NR4SO2R6, -SO2NR3R4, m дорівнює 0, 1, 2, 3, 4 або 5, і C(O)R3, -C(O)OR 3 , -OC(O)R 3 , -SO 2R3, -NR4C(O)OR 6, j дорівнює 1 або 2. -NR4C(O)R3, -C(O)NR3R4, -NR3R4, -NR5C(O)NR3R4, 4. Сполука за п. 3, яка відрізняється тим, що має NR5C(NCN)NR3R4, -OR3, арилу, ге тероарилу, ариформулу лалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу, A O R1 R8 є –OCF3, -Br або -Сl, і R1 є нижчим алкілом або H галогеном, N R9 є гідрогеном або галогеном, R10 є гідрогеном, і W є -C(O)OR 3 або –C(O)NR 4OR3. R7 R8 R9 N 13. Сполука за п. 12, яка відрізняється тим, що W N є -C(O)NR4OR3. . 14. Сполука за п. 1, яка відрізняється тим, що 5. Сполука за п 4., яка відрізняється тим, що 7 вибрана з групи, яку складають R є С1-С10алкілом, С3-С7циклоалкілом, С3циклопропілметоксіамід 7-флуор-6-(4-бром-2С7циклоалкілалкілом, С3-С7гетероциклоалкілом метилфеніламіно)-3Н-бензоімідазол-5-карбонової або С3-С7гетероциклоалкілалкілом, кожний з яких кислоти, може бути, як варіант, заміщений 1-3 групами, нециклопропілметоксіамід 6-(4-бром-2залежно вибраними з оксогрупи, галогену, ціаногхлорфеніламіно)-7-флуор-3Н-бензоімідазол-5рупи, нітрогрупи, трифлуорметилу, дифлуорметокарбонової кислоти, ксилу, трифлуорметоксилу, азидогрупи, (2-гідроксіетоксі)-амід 6-(4-бром-2NR4SO2R6, -SO2NR3R4, -C(O)R3, -C(O)OR 3, 3 6 4 6 4 3 хлорфеніламіно)-7-флуор-3-метил-3НOC(O)R , -SO2R , -NR C(O)OR , -NR C(O)R , бензоімідазол-5-карбонової кислоти, C(O)NR3R4, -NR3R4, -NR5C(O)NR3R4, 5 3 4 3 (2,3-дигідроксипропокси)-амід 6-(4-бром-2NR C(NCN)NR R , -OR , арилу, ге тероарилу, арихлорфеніламіно)-7-флуор-3-метил-3Нлалкілу, гетероарилалкілу, гетероциклілу і гетеробензоімідазол-5-карбонової кислоти, циклілалкілу, 9 (2-гідроксіетоксі)-амід 6-(4-бром-2R є гідрогеном або галогеном, хлорфеніламіно)-7-флуор-3-(тетрагідропіран-2R1 є нижчим алкілом або галогеном, і ілметил)-3Н-бензоімідазол-5-карбонової кислоти, R8 є –ОСF3 або галогеном. 11 77765 12 [6-(5-аміно-[1,3,4]оксадіазол-2-іл)-4-флуор-1Н(2-гідроксіетокси)-амід 6-(4-бром-2бензоімідазол-5-іл]-(4-бром-2-метилфеніл)-амін, флуорфеніламіно)-7-флуор-3-метил-3Н1-[6-(4-бром-2-хлорфеніламіно)-7-флуор-3-метилбензоімідазол-5-карбонової кислоти і 3Н-бензоімідазол-5-іл]-2-гідроксиетанон, (2-гідроксіетокси)-амід 6-(2,4-дихлорфеніламіно)-71-[6-(4-бром-2-хлорфеніламіно)-7-флуор-3Нфлуор-3-метил-3Н-бензоімідазол-5-карбонової бензоімідазол-5-іл]-2-метоксіетанон, кислоти. (2-гідрокси-1,1-диметилетоксі)-амід 6-(4-бром-215. Композиція, яка містить сполуку за п. 1 і фархлорфеніламіно)-7-флуор-3-метил-3Нмацевтично прийнятний носій. бензоімідазол-5-карбонової кислоти, 16. Спосіб інгібування активності МЕК ссавців, (2-гідроксіетокси)-амід 6-(4-бром-2який включає введення ефективної кількості спохлорфеніламіно)-7-флуор-3-(тетрагідрофуран-2луки за п. 1 цьому ссавцю. ілметил)-3Н-бензоімідазол-5-карбонової кислоти, 17. Спосіб лікування гіперпроліферативного роз(2-гідроксіетокси)-амід 6-(4-бром-2ладу у ссавців, який включає введення ефективної хлорфеніламіно)-7-флуор-3Н-бензоімідазол-5кількості сполуки за п. 1 цьому ссавцю. карбонової кислоти, Винахід стосується ряду алкілованих похідних (1Н-бензоімідозол-5-іл)-(4-іодофеніл)-аміну, які можуть бути використані у лікуванні таких гіперпроліферативних хвороб, як рак і запалення, у ссавців. Винахід стосується також способу використання таких сполук у лікуванні гіперпроліферативних хвороб у ссавців, зокрема у людини, і фармацевтичних композицій, що містять такі сполуки. Клітинна сигналізація через рецептори фактора росту і кінази протеїну є важливим регулятором росту клітин, їх проліферації і диференціації. При нормальному рості клітин фактори росту через активування рецептора (тобто PDGF або EOF та ін.) активують шляхи кінази МАР. Одним з найважливіших і найкраще зрозумілих шляхів кінази МАР, які беруть участь у нормальному і неконтрольованому рості клітин є шлях кінази Ras/Raf Активна з'єднана GTP Ras призводить до активування і непрямого фосфорилування кінази Raf. Тоді Raf фосфорилує МЕК1 і 2 на двох серинових залишках (S218 і S222 для МЕК1 і S222 і S226 для МЕК2) [Ann et al, Methods in Enzymology 2001, 332, 417-431]. Активована МЕК фосфорилує її єдині відомі субстрати, кінази MAP, ERK1 і 2. Фосфорилування ERK через МЕК відбувається на Υ204 і Τ202 для ERK1 і Υ185 і Τ183 для ERK2 [Ann et al, Methods in Enzymology 2001 332 417-431]. Фосфорилована ERK димеризує і здійснює транслокацію до ядра, де вона накопичується [Khokhlatchev et al, Cell 1998, 93, 605-615]. У ядрі ERK бере участь у декількох важливих функціях клітини, включаючи (але без обмеження) ядерне транспортування трансдукцію сигналів, відновлення ДНК, складання і транслокацію нуклеосоми і обробку і трансляцію mRNA [Ann et al, Molecular Cell 2000, 6, 1343-1354]. Взагалі обробка клітини факторами росту призводить до активування ERK1 і 2, що викликає проліферацію і, у деяких випадках, диференціацію [Lewis et al, Adv Cancer Res 1998, 74, 49-139]. При проліферативних хворобах генетичні мутації і/або надекспресія рецепторів фактора росту, протеїнів сигналізації униз або кінази протеїну, які беруть участь у створенні шляху кінази ERK, призводить до неконтрольованої проліферації клітин і, як результат до утворення пухлини. Наприклад, деякі раки містять мутації, результатом яких є без перервне активування цього шляху, зумовлене безперервним продукуванням факторів росту. Ін ші мутації можуть викликати дефективне деактивування активованого комплексу з'єднаного GTP Ras, що знову викликає активування шляху кінази МАР. Онкогенні форми Ras, що зазнали мутації, знаходять у 50% випадків раку ободової кишки і більш, як у 90% випадків раку підшлункової залози, а також у багатьох інших типах раку [Kohl et al, Science 1993 260 1834-1837]. Нещодавно мутації bRaf були ідентифіковані у більш, як 60% випадків злоякісної меланоми [Davies, Η. et al, Nature 2002, 417, 949-954]. Ці мутації bRaf призводять до нерегульованого активного каскаду кінази МАР. Вивчення зразків первинних пухлин і ліній клітин також показало нерегульоване або надмірне активування шляху кінази МАР у випадках раків підшлункової залози, ободкової кишки, легенів, яєчника і нирок [Hoshino, R et al, Oncogene 1999, 18, 813-822]. Тому існує сильна кореляція між раками і надактивним шляхом кінази МАР як результатом генетичних мутацій. Оскільки неконтрольоване або надмірне активування каскаду кінази МАР грає вирішальну роль у проліферації і диференціації клітин, вважають, що інгібування цього шляху може бути корисним у випадках пперпроліферативних хвороб. МЕК є ключовим фактором у цьому шля ху, оскільки він є нижчим за Ras і Raf. Крім того, вона є привабливим об'єктом терапії, оскільки єдиними відомими субстрати для фосфорилування МЕК є кінази MAP ERK1 і 2. Було показано декількома дослідженнями, що інгібування МЕК є потенційно терапевтично цінним. Наприклад, було показано, що інгібітори малих молекул МЕК інгібують розвиток пухлини у людини на ксеротрансплантатах у голих мишей [Sebolt-Leopold et al, Nature-Medicine 1999, 5 (7), 810-816; Trachet et al., AACR April 6-10, 2002, Poster #5426; TeCle Η. ІВС 2nd International Conference of Protein Kmases, September 9-10 2002], блокують статичн у алодинію у тварин [WO 01/05390, 25/01/2001] і інгібують ріст клітин гострої мі'лоїдної лейкемії [Milella et al., JClin Invest 2001,108 (6), 851-859]. Інгібітори малих молекул МЕК були описані. Принаймні 13 заявок на патенти були подані про 13 77765 14 тягом останніх років: US 5 525 625 від 24/01/1995, C1-С10алкілу, С2-С10алкенілу, С2-С10алкінілу, С3WO 98/43960 від 8/10/1998 WO 99/01421 від С10циклоалкілу, С3-С10циклоалкілалкілу, арилу, 14/01/1999, WO 99/01426 від 14/01/1999, WO арилалкілу, гетероарилу, гетероарилалкілу, гете00/41505 від 20/07/2000, WO 00/42002 від роциклілу і гетероциклілалкілу, де кожна алкільна, 20/07/2000, WO 00/42003 від 20/07/2000, WO алкенільна, алкінільна, циклоалкільна, арильна, 00/41994 від 20/07/2000 WO 00/42022 від гетороарильна і гетероциклільна частина, як варі20/07/2000, WO 00/42029 від 20/07/2000, WO ант, заміщена 1-5 групами, незалежно вибраними 00/68201 від 16/11/2000 WO 01/68619 від серед оксогрупи, галогену, ціаногрупи, нітрогрупи, 20/09/2001, і WO 02/06213 від 24/01/2002. трифлуорметилу, дифлуорметоксилу, трифлуорВинахід стосується алкілованих (1Нметоксилу, азидогрупи, -NR'SO2R'''', -SO 2NR'R", бензоімідазол-5-іл)-(4-заміщений феніл)-амінових C(O)R', -C(O)OR', -OC(O)R', -NR'C(O)OR'''', сполук формули І і їх фармацевтично прийнятних NR'C(O)R", -C(O)NR'R", -SR', -S(O)R'''', -SO 2R'''', солей і проліків, які є корисними при лікуванні ппеNR'R", -NR'C(O)NR"R''', -NR'C(NCN)NR"R''', -OR', рпроліферативних хвороб. арилу, гетероарилу, арилалкілу, гетероарилалкілу, Зокрема, винахід стосується сполук формули гетероциклілу і гетероциклілалкілу; І, які діють як інгібітори МЕК, а також способів лікуR', R" і R''' незалежно вибрані серед гідрогену, вання раку. Винахід включає також рецептури, які нижчого алкілу, нижчого алкенілу, арилу і арилалмістять сполуки формули l i способи застосування кілу; цих сполук для лікування пацієнтів, що потребують R'''' вибрана серед нижчого алкілу, нижчого такого лікування. Крім того, описано способи алкенілу, арилу і арилалкілу; або отримання інгібіторних сполук формули І. будь-які дві з R', R", R''' або R'''' можуть разом з Відповідно, винахід стосується сполук формуатомом, до якого вони приєднані, утворювати 4ли І: 10-членне карбоциклічне, гетероарильне або гетороциклічне кільце, кожне з яких, як варіант, заміщене однією-трьома групами, незалежно вибраними серед галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорметоксилу, трифлуорметоксилу, азидогрупи, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу, або R3 і R4 можуть разом з атомом, до якого вони приєднані, утворювати 4-10-членне карбоциклічне, гетероарильне або гетороциклічне кільце, кожне з яких, як варіант, заміщене однією-трьома групами, незалежно вибраними серед галогену, ціаногрупи, і їх фармацевтично прийнятних солей, проліків нітрогрупи, трифлуорметилу, ди флуорметоксилу, і сольватів, де: трифлуорметоксилу, азидогрупи, -NR'SO2R'''', ----- позначає, як варіант, зв'язок, за умови, що один і лише один нітроген кільця приєднаний поSO2NR'R", -C(O)R', -C(O)OR', -OC(O)R', NR'C(O)OR'''', -NR'C(O)R", C(O)NR'R", -SO2R'''', двійним зв'язком; NR'R", -NR'C(O)NR"R''', -NR'C(NCN)NR"R''', -OR', R1, R2, R9 і R10 незалежно вибрані серед гідроарилу, гегероарилу, арилалкілу, гетероарилалкілу, гену, галогену, ціаногрупи, нітрогрупи, трифлуоргетероциклілу і гетероциклілалкілу; або метилу, дифлуорметоксилу, три флуорметоксилу, азидогрупи, -OR3, -C(O)R3, -C(O)OR 3, NR4C(O)OR 6, R4 і R5 незалежно є гідрогеном або C13 4 6 3 4 4 3 С6алкілом; або -OC(O)R , -NR SO2R , -SO2NR R , -NR C(O)R , R4 і R5 разом з атомом, до якого вони приєдC(O)NR3R4, -NR5C(O)NR3R4, -NR5C(NCN)NR3R4, 3 4 нані, утворюють 4-10-членне карбоциклічне, гетеNR R і C1-С10алкілу, С2-С10алкенілу, С2роарильне або гетороциклічне кільце, кожне з С10алкінілу С 3-С10циклоалкілу, С3С10циклоалкілалкілу, -S(О)j(C1-С6алкіл), яких, як варіант, заміщене однією-трьома групами, незалежно вибраними серед галогену, ціаногрупи, S(О)j(СR4R5)m-арилу, арилу, арилалкілу, гетеронітрогрупи, трифлуорметилу, ди флуорметоксилу, арилу, гетероарилалкілу, гетероциклілу, гетероцитрифлуорметоксилу, азидогрупи, -NR'SO2R'''', клілалкілу, -O(CR4R5)m-арил, -NR4(CR4R5)m-apилy, SO2NR'R", -C(O)R'''', -C(O)OR', -OC(O)R', O(CR4R5)m-reTepoapnny, -NR4(CR4R5)mгeτepoapилy, -O(CR4Rb)m-гетероциклілу і NR'C(O)OR'''', -NR'C(O)R", -C(O)NR'R", -SO2R'''', NR'R", -NR'C(O)NR"R''', -NR'C(NCN)NR"R", -OR', NR4(CR4R5)m-гетероарилу, де кожна алкільна, аларилу, гетероарилу, арилалкілу, гетероарилалкілу, кенільна, алкінільна циклоалкільна, арильна, гетогетероциклілу і гетероциклілалкілу; роарильна і гетероциклільна частина, як варіант, R6 вибрана серед трифлуорметилу і C1заміщена 1-5 групами, незалежно вибраними серед оксогрупи, галогену, ціанорупи, нітрогрупи, С10алкілу, С3-С10циклоалкілу, арилу, арилалкілу, гетероарилу, гетероарилалкілу, гетероциклілу, трифлуорметилу, дифлуорметоксилу, трифлуоргетероциклілалкілу, де кожна алкільна, циклоалкіметоксилу, азидогрупи, -NR4SO2R6, SO2NR3R4, льна, арильна, гетероалильна і гетероциклільна C(O)R3, -C(O)OR 3, -OC(O)R 3, -NR4C(O)OR 6, частина, як варіант, заміщена 1-5 групами, незаNR4C(O)R3, -C(O)NR3R4, -NR3R4, -NR5C(O)NR3R4, NR5C(NCN)NR3R4, -OR3, арилу, ге тероарилу, арилежно вибраними серед оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, дифлуорлалкілу, гетероарилалкілу, гетероциклілу і гетерометоксилу, трифлуорметоксилу, азидогрупи, циклілалкілу; NR'SO2R'''', SO2NR'R", -C(O)R', -C(O)OR', -OC(O)R', R3 вибрана серед гідрогену, трифлуорметилу і 15 77765 16 -NR'C(O)OR'''', -NR'C(O)R", -C(O)NR'R", -SO2R'''', ціаногрупи, нітрогрупи, трифлуорметилу, дифлуоNR'R", -NR'C(O)NR"R''', -NR'C(NCN)NR"R''', -OR', рметоксилу, трифлуорметоксилу, азидогрупи, арилу, гетероарилу, арилалкілу, гетероарилалкілу, NR4SO2R6, -SO2NR3R4, -C(O)R3, -C(O)OR 3, гетероциклілу і гетероциклілалкілу; OC(O)R3, -SO2R 3, -NR4C(O)OR 6, -NR4C(O)R3, 7 R вибрана серед гідрогену і C1-С10алкілу, С2C(O)NR3R4, -NR3R4, -NR5C(O)NR3R4, 5 3 4 3 С10алкенілу, С2-С 10алкінілу, С3-С10циклоалкілу, -С3NR C(NCN)NR R , -OR , арилу, ге тероарилу, ариС10циклоалкілалкілу, арилу, арилалкілу, гетеролалкілу, гетероарилалкілу, гетероциклілу і гетероарилу, гетероарилалкілу, гетероциклілу, гетероцициклілалкілу. клілалкілу, де кожна алкільна, алкенільна, алкініВинахід включає також сполуки формули І, де льна, циклоалкільна, арильна, гетороарильна і R8 є -OCF3 , -Br або -СІ, R2 є гідрогеном і R1 є нижгетероциклільна частина, як варіант, заміщена 1-5 чим алкілом або галогеном. групами, незалежно вибраними серед оксогрупи, Винахід також включає сполуки формули І, де галогену, ціаногрупи, нітрогрупи, трифлуорметилу, R9 є гідрогеном або галогеном, і R10 є гідрогеном. дифлуорметоксилу, трифлуорметоксилу, азидогВинахід включає також сполуки формули І, де рупи, -NR4SO2R6, -SO2NR3R4, -C(O)R3, C(O)OR 3 , W є -C(O)OR 3 або -C(O)NR4OR3. OC(O)R3, -NR4C(O)OR 6 , -NR4C(O)R3, -C(O)NR 3R4, Винахід стосується також сполук формули II: SO2R6, -NR3R4, -NR 5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу; W вибрана серед гетероарилу, гетероциклілу, -C(O)OR3, -C(O)NR3R4, -C(O)NR4OR3, -C(O)R4OR3, -С(О)(С3-С10циклоалкіл), -С(О)(C1-С10алкіл), С(О)(арил), -С(О)(гетероарил) і С(O)(гетероцикліл), кожне з яких, як варіант, заміщене 1-5 групами, незалежно вибраними серед NR3R4, -OR3 , -R2 і С1-С10алкілу, С2-С10алкенілу і С 2С10алкінілу, кожне з яких, як варіант, заміщене 1 або 2 групами, незалежно вибраними cepefl-NR3R4 і -OR3; R8 вибрана серед гідрогену, -SCF3, -СІ, -Br, -F, де W, R1, R7, R8, R9 і R10 є такими, що були виціаногрупи, нітрогрупи, трифлуорметилу, дифлуозначені вище для формули І. рметоксилу, трифлуорметоксилу, азидогрупи, Винахід також включає сполуки формули II, у OR3, -C(O)R3 , -C(O)OR 3 , -NR4C(O)OR 6 , -OC(O)R 3, якій R7 є C1-С10алкілом, С3-С7циклоалкілом або С 34 6 3 4 4 3 3 4 NR SO2R , -SO 2NR R , -NR C(O)R , -C(O)NR R , С7циклоалкілалкілом, кожний з яких може бути, як NR5C(O)NR3R4, -NR3R4 і C1-С10алкілу, С2варіант, заміщений 1-3 групами, незалежно вибраС10алкенілу, С2-С10алкінілу, С3-С10циклоалкілу, С3ними серед оксогрупи, галогену, ціаногрупи, нітроС10циклоалкілалкілу, -S(О)j(С1-С6алкіл), групи трифлуорметилу, дифлуорметоксилу, трифS(O)j(CR4R5)m-арилу, арилу, арилалкілу, гетеролуорметоксилу, азидогрупи, NR4SO2R6, 3 4 3 3 арилу, гетероарилалкілу, гетероциклілу, гетероциSO2NR R , -C(O)R , -C(O)OR , -OC(O)R 3, -SO2R3 , 4 5 4 4 5 клілалкілу, -O(CR R )m-арилу, NR (CR R )m-арилу, NR4C(O)OR 6, -NR4C(O)R3, C(O)NR3R4, -NR3R4, -O(CR4R5)m-гетероарилу, -NR4(CR4R5)mNR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, гетероарилу, - -O(CR4R5)m-гетероциклілу і гетероарилу, арилалкілу, гетероарилалкілу, гетеNR4(CR4R5)m-гетероциклілу, де кожна алкільна, роциклілу і гетероциклілалкілу. алкенільна, алкінільна, циклоалкільна, арильна, Винахід також включає сполуки формули II, де гетороарильна і гетероциклільна частина, як варіR8 є -OCF 3, -Br або -СІ, і R1 є нижчим алкілом або ант, заміщена 1-5 групами, незалежно вибраними галогеном. серед оксогрупи, галогену, ціаногрупи, нітрогрупи, Винахід також включає сполуки формули II, де трифлуорметилу, дифлуорметоксилу, трифлуорR9 є гідрогеном або галогеном, і R10 є гідрогеном. 4 6 3 4 метоксилу, азидогрупи -NR SO2R , -SO2NR R , Винахід також включає сполуки формули II, де C(O)R3, -C(O)OR 3, -OC(O)R 3, -NR4C(O)OR 6, W є -C(O)OR 3 або -C(O)NR4OR3. 4 3 3 4 3 4 5 3 4 NR C(O)R , -C(O)NR R , -NR R , -NR C(O)NR R , Винахід також включає сполуки формули III: NR5C(NCN)NR3R4, -OR3, арилу, ге тероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу; m дорівнює 0, 1,2, 3, 4 або 5; і j дорівнює 1 або 2. Новими сполуками, що входять в об'єм винаходу, є ті, що описуються загальною формулою І, наведеною вище, і їх фармацевтично прийнятні солі і проліки. Винахід також включає сполуки формули І, де R7 є C1-С10алкілом, С3-С7циклоалкілом, С3С7циклоалкілалкілом, С3-С7гетероциклоалкілом або С3-С7гетероциклоалкілалкілом, кожний з яких може бути, як варіант, заміщений 1-3 групами, незалежно вибраними серед оксогрупи, галогену, де R1, R2, R7, R 8 і R9 є такими, що визначені 17 77765 18 вище для формули І, і А є -OR3 або NR4OR3, де R3 і R4 є такими, що визначені вище для формули І. Винахід також включає сполуки формули III, у якій R7 є C1-С10алкілом, С3-С7циклоалкілом або С 3С7циклоалкілалкілом, кожний з яких може бути, як варіант, заміщений 1-3 групами, незалежно вибраними серед оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, ди флуорметоксилу, трифлуорметоксилу, азидогрупи, -NR4SO2R 6, SO2NR3R4, -C(O)R3, -C(O)OR 3, -OC(O)R 3, -SO2R3 , NR4C(O)OR 6, -NR4C(O)R3, -C(O)NR3R4, -NR3R4, NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетеде R1 R7 R81 R9 є такими, що визначені вище роциклілу і гетероциклілалкілу. для формули І і А є -OR3 або -NR4OR3 де R31 R4 є Винахід також включає сполуки формули III, такими, що визначені вище для формули І. де R8 є -OCF3, -Br або -СІ, R2 є гідрогеном і R1 є Винахід також включає сполуки формули ІІІb, у нижчим алкілом або галогеном. якій R7 є C1-С10алкілом С3-С7циклоалкілом або С 3Винахід також включає сполуки формули III, С7циклоалкілалкілом, кожний з яких може бути як де R9 є гідрогеном або галогеном. варіант заміщений 1-3 групами незалежно вибраВинахід також включає сполуки формули III, ними серед оксогрупи, галогену ціаногрупи нітро3 де R є гідрогеном або нижчим алкілом, коли А є групи три флуорметилу, ди флуорметоксилу, три3 4 4 3 OR ; і R є гідрогеном, коли А є -NR OR . флуорметоксилу, азидогрупи, -NR4SO2R6, Винахід також включає сполуки формули IlIa: SO NR3R4, -C(O)R3 -C(O)OR3, -OC(O)R3 , -SO R3, 2 де R1, R2, R7, R 8 і R9 є такими, що визначені вище для формули І, і А є -OR3 або -NR 4OR3, де R3 і R4 є такими, що визначені вище для формули І. Винахід також включає сполуки формули ІІІа, у якій R є C1-С10алкілом, С3-С7циклоалкілом або С 3С7циклоалкілалкілом, кожний з яких може бути, як варіант, заміщений 1-3 групами, незалежно вибраними серед оксогрупи, галогену, ціаногрупи, нітрогрупи, трифлуорметилу, ди флуорметоксилу, трифлуорметоксилу, азидогрупи, -NR4SO2R 6, SO2NR3R4, -C(O)R3, -C(O)OR 3, -OC(O)R 3, -SO2R3 , NR4C(O)OR 6, -NR4C(O)R3, -C(O)NR3R4, -NR3R4, NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, гетероарилу, арилалкілу, гетероарилалкілу, гетероциклілу і гетероциклілалкілу. Винахід також включає сполуки формули IlIa, де R8 є -OCF3, -Br або -СІ, R2 є гідрогеном, і R1 є нижчим алкілом або галогеном. Винахід також включає сполуки формули IlIa, де R9 є гідрогеном або галогеном. Винахід також включає сполуки формули IlIa, де R3 є гідрогеном або нижчим алкілом, коли А є OR3; і R4 є гідрогеном, коли А є -NR 4OR3. Винахід також включає сполуки формули ІІІb: 2 NR4C(O)OR 6, -NR4C(O)R3, -C(O)NR3R4, -NR3R4, NR5C(O)NR3R4, -NR5C(NCN)NR3R4, -OR3, арилу, гетероарилу, арилалкілу гетероарилалкілу, гетероциклілу і гетероциклілалкілу Винахід також включає сполуки формули ІІІb, де R8 є -OCF3 , -Br або -СІ і R1 є нижчим алкілом або галогеном. Винахід також включає сполуки формули ІІІb, де R9 є флуором або хлором. Винахід також включає сполуки формули ІІІb, де R3 є гідрогеном або нижчим алкілом коли А є OR3, і R4 є гідрогеном, коли А є -NR 4OR3. Якщо не визначено інакше, у цьому описі використано такі терміни. Терміни "C1-С10алкіл", "алкіл" і "нижчий алкіл" визначають лінійні або розгалужені ланцюгові алкільні групи з 1-10 атомами карбону, наприклад, метил, етил, пропіл, ізопропіл n-бутил, втор-бутил, трет-бутил, пентил, 2-пентил, ізопентил, неопентил, гексил 2-гексил 3-гексил, 3-метилпентил, гептил, октил тощо. Бажаним алкільним радикалом є C1-С6алкіл, зокрема C1-С3алкіл. Терміни "С2-С10алкеніл", "нижчий алкеніл" і "алкеніл" визначають лінійні або розгалужені гідрокарбонові радикали з 2-10 атомами карбону і принаймні одним подвійним зв'язком і включають етеніл пропеніл, 1-бут-3-еніл 1-пент-3-еніл, 1-гекс5-еніл тощо. Бажаним є нижчий алкеніл з 3-5 атомами карбону. Терміни "С2-С10алкініл", "нижчий алкініл" і "алкініл" визначають лінійні або розгалужені гідрокарбонові радикали з 2-10 атомами карбону і принаймні одним потрійним зв'язком і включають етиніл, пропиніл, бутиніл, пентин-2-іл тощо. Бажаним є алкініл з 3-5 атомами карбону. Термін "галоген" означає флуор, бром, хлор і ioд. Термін "арил" визначає ароматичну карбоциклічну гр уп у з одним кільцем (наприклад, феніл), декількома кільцями (наприклад, біфеніл), або декількома конденсованими кільцями в яких принаймні одне є ароматичним, (наприклад, 1,2,3,4тетрагідронафтил, нафтил), як варіант, моно-, ди, 19 77765 20 або тризаміщеним, наприклад, галогеном нижчим азабіцикло[3,1,0]гексаніл, 3алкілом нижчим алколсиііом, трифлуорметилом, азабіцикло[4,1,0]гептаніл, азабіцикарилом, гетероарилом і гідроксилом. ло[2,2,2]гексаніл, 3Н-індоліл і хінолізиніл. Винахід Термін "гетероарил" означає системи одного включає також спірокомпоненти. Вищезазначені або більше ароматичних кілець тобто 5-, 6-, або 7групи як похідні груп, перелічених вище, можуть членних кілець, включаючи системи злитих кілець бути С-приєднаними або N-приєднаними, коли це (принаймні одне з яких є ароматичним) з 5-10 атоможливо. Наприклад, групи, що походять від піромами, які містять принаймні 1-4 гетероатоми, виблу можуть бути пірол-1-ілом (N-приєднаним) або рані серед нітгрогену, оксигену або сульфур у. пірол-3-ілом (С-приєднаним). Групи, що походять Прикладами гетероарильних груп є піридиніл, імівід імідазолу, можуть бути імідазол-1-ілом (Nдазоліл, піримідиніл, піразоліл, триазоліл, піразиприєднаним) або імідазол-3-ілом (С-приєднаним). ніл, тетразоліл, фурил, тієніл, ізоксазоліл, тіазоліл, Прикладом гетероциклічної групи, у якій 2 кільцеві оксазоліл, ізотіазоліл, піроліл, хінолініл, ізохіноліатоми карбону заміщено оксо-(=О)компонентом, є ніл, індоліл, бензоімідазоліл, бензофураніл, цино1,1-діоксотіоморфолініл. Тут ге тероцикличні групи лініл, індазоліл, індолізиніл, фталазиніл, пірадазиє незаміщеними або, якщо зазначено, заміщеними ніл, триазиніл, ізоіндоліл, піридиніл, пуриніл, в одній або більше придатних для заміщення пооксадіазоліл, триазоліл, тіадіазоліл, фуразиніл, зиціях різними групами. Наприклад, такі гетероцибензофуразиніл, бензотіофеніл, бензотіазоліл, клічні групи можуть бути, як варіант, заміщені, набензоксазоліл, хіназолініл, хіноксалініл, нафтириприклад, C1-С6алкілом, C1-С6алкоксилом, диніл і фуропіридиніл. Це визначення включає галогеном, гідроксилом, ціаногрупою, нітрогрупою, спірокомпоненти. Гетероарильні групи є, як варіаміногрупою, моно(С1-С6)алкіламіногрупою, ди(C1ант, моно- ди- або тризаміщеними, наприклад, С6)алкіламіногрупою, С2-С6алкенілом, С2галогеном, нижчим алкілом, нижчим алкоксилом, С6алкінілом, C1-С6галогеналкілом, C1-С6 галогенагалогеналкілом, арилом, гетероарилом і гідроксилкоксилом, аміно(C1-С6)алкілом, моно(C1лом. С6)алкіламіно(С1-С6)алкілом або ди(С 1Термін "карбоцикл", "карбоцикліл", "циклоалС6)алкіламіно(С1-С6)алкілом. кіл" або "С3-С10циклоалкіл" означає насичені карТермін "арилалкіл" означає алкільний компобоциклічні радикали з 3-10 атомами карбону. Цикнент (визначений вище), заміщений одним або лоалкіл може бути моноциклічною або більше арильними компонентами (визначеними поліциклічною злитою системою і може бути зливище). Бажаними арилалкільними радикалами є тим з ароматичним кільцем. Прикладами таких арил-С 1-3алкіли. Прикладами є бензил, фенілетил радикалів є циклопропіл, циклобутил, циклопентил тощо. і циклогексил. Тут циклоалкільні групи є незаміщеТермін "гетероарилалкіл" означає алкільний ними або, якщо вказано, заміщеними в одній або компонент (визначений вище), заміщений гетеробільше придатних для заміщення позиціях різними арильним компонентом (також визначеним вище). групами. Наприклад, такі циклоалкільні групи моБажаними гетероарилалкільними радикалами є 5жуть бути, як варіант, заміщені, наприклад, С1або 6-членні гетероарил-С1-3алкіли. Прикладами є С6алкілом, C1-С6алкоксилом, галогеном, гідроксиоксазолілметил, піридилетил тощо. лом, ціаногрупою, нітрогрупою, аміногрупою, моТермін "гетероциклілалкіл" означає алкільний но(C1-С6)алкіламіногрупою, ди(С1компонент (визначений вище), заміщений гетероС6)алкіламіногрупою, С2-С6алкенілом, С2циклільним компонентом (також визначеним виС6алкінілом, C1-С6галогеналкілом, C1ще). Бажаними гетероциклілалкільними радикаС6галогеналкоксилом, аміно(C1-С6)алкілом, молами є 5- або 6-членні гетероцикліл-С1-3алкіли. но(С1-С6)алкіламіно(С 1-С6)алкілом або ди(C1Прикладом є тетрагідропіранілметил. С6)алкіламіно(С1-С6)алкілом. Термін "циклоалкілалкіл" означає алкільний Термін "гетероцикл" або "гетероцикліл" ознакомпонент (визначений вище), заміщений циклоачає одну або більше карбоциклічних кільцевих лкільним компонентом (також визначеним вище). систем з 5-, 6-, або 7-членними кільцями, що Бажаними гетероциклільними радикалами є 5- або включають злиті кільцеві системи з 4-10 атомів, які 6-членні циклоалкіл-С 1-3алкіли. Прикладом є цикмістять принаймні 1-4 гетероатоми, вибрані серед лопропілметил. нітрогену, оксигену або сульфур у, за умови, що "Me" означає метил, "Et" - етил, "Вu" - бутил і кільце групи не містить двох суміжних атомів О "Ас" - ацетил. або S. Злитою системою може бути гетероцикл, Вираз "фармацевтично прийнятна сіль", якщо злитий з ароматичною групою. Бажані гетероцикли не вказано інше, означає солі кислотних і основних включають але без обмеження піролідиніл, тетрагруп, які можуть бути присутні у сполуках винахогідрофураніл, дигідрофураніл, тетрагідротієніл, ду. Сполуки винаходу, які є природно основними тетрагідропіраніл, дигідропіраніл, тетрагідротіопіможуть утворювати багато солей з різними неорраніл, піперидин, морфолін, тіоморфолін, тіоксаганічними і органічними кислотами. Кислотами, які ніл, піперазиніл, гомопіперазиніл, ацетидиніл, окможуть бути використані для приготування фарсетаніл, тієтаніл, гомопіперидиніл, оксепаніл, мацевтично прийнятних адитивно-кислотних солей тієпаніл, оксазепініл, діазепініл, тіазепініл, 1,2,3,6з такими основними сполуками винаходу, є ті, які тетрагідропіридиніл 2-піролініл, 3-піролініл, індоліутворюють нетоксичні адитивно-кислотні солі, тобніл, 2Н-піраніл, 4Н-піраніл, діоксаніл, 1,3то солі, що містять такі фармацевтично прийнятні діоксоланіл, піразолініл, дитіаніл, дитіоланіл, дигіаніони, як ацетат, бензолсульфонат, бензоат, бідропіраніл, дигідротієніл, дигідрофураніл, піразокарбонат, бісульфат, бітартрат, борат, бромід лідинілімідазолініл, імідазолідиніл, 3кальцію, камсилат, карбонат, хлорид, клавуланат, 21 77765 22 цитрат, дигідрохлорид, едисліат, естолат, езилат, луки, ідентичні згаданим у винаході, але такі, в етилсукцинат, фумарат, глюцептат, глюконат, глюяких один або більше атомів заміщені атомами з тамат, гліколіларсанілат, гексилресорцинат, гідраатомною масою або масовим числом відмінними бамін, гідробромід, гідрохлорид, іодид, ізотіонат, від атомної маси або масового числа, які звичайно лактат, лактобіонат, лаурат, малат, малеат, манзустрічаються у природі. Приклади ізотопів які моделат, мезилат, метилсульфат, мукат, напсилат, жна вводити у сполуки винаходу, включають ізотонітрат, олеат, оксалат, памоат (ембонат), пальміпи гідрогену карбону, нітрогену, оксигену, фосфотат, пантотенат, фосфа т/ди фосфат, полігалактуру, суль фуру, флуору і хлору, наприклад, 2Н, 3Н, 13 ронат, силіцилат, стеарат, субацетат, сукцинат, С, 14С, 15Ν, 18О, 17О, 31Р, 32Р, 35S, 18 F, і 36СІ, відпотаннат, тартрат, теоклат, тозилат, триетіодод і відно. Сполуки винаходу, їх проліки і фармацевтивалератові солі. Оскільки окремі сполуки винаходу чне прийнятні солі цих сполук або цих проліків, які можуть включати декілька кислотних або основних містять вищезгадані ізотопи і/або інші ізотопи інкомпонентів, в окремих випадках сполуки винахоших атомів, входять в об'єм винаходу. Деякі мічені ду можуть включати моно, ди- або три-солі. ізотопами сполуки винаходу, наприклад, ті що місУ випадку кислотного компонента у сполуці тять такі радіоактивні ізотопи, як 3Н і 14C, є корисвинаходу сіль можна одержати обробкою сполуки ними у ліках і/або субстратах тканин при аналізі. винаходу основною сполукою, зокрема неорганічІзотопи 3Н і карбону-14, тобто 14С, є особливо баною основою. Бажаними є неорганічні солі, утвожаними завдяки легкості їх отримання і виявлення. рені такими лужними і лужноземельними металаКрім того, заміщення важчими ізотопами наприми, як літій, натрій, калій, барій і кальцій. Бажані клад, дейтерієм тобто 2Н, може дати певні терапеорганічні основи включають, наприклад, солі амовтичні переваги внаслідок більшої метаболічної нію, дибензиламонію, бензиламонію, 2стабільності, наприклад, збільшення in vivo напівгідроксиетиламонію, біс(2-гідроксиетил)амонію, періоду або зменшення потрібної дози і тому мофенілетилбензиламіну, дибензилетилендіаміну жуть бути бажаними у деяких випадках. Мічені тощо. Інші солі кислотних компонентів можуть ізотопами сполуки винаходу і їх проліки можна включати, наприклад, солі, утворені прокаїном, звичайно приготувати, використовуючи процедури, хініном і N-метилглюкозаміном, плюс солі основописані у Схемах і/або у Прикладах і Препаратах них амінокислот, наприклад, гліцину, орнітину, нижче, шляхом заміщення неміченого реагента гістидину, фенілгліцину, лізину і аргініну. Бажаниміченим ізотопами реагентом. ми є натрієва або калієва сіль сполуки винаходу. Винахід також включає фармацевтичні компоУ випадку основних компонентів сіль одержузиції, які містять сполуки формул І-ІІІb і способи ють обробкою сполуки винаходу кислотною сполулікування проліферативних розладів або анормакою, зокрема неорганічною кислотою. Бажані нельного росту клітин, введенням проліків сполук органічні солі цього типу можуть включати, винаходу. Сполуки винаходу, які мають вільні амінаприклад, гідрохлорні, гідробромні, гідроіодні, но-, амідо-, гідрокси- або карбогрупи, можуть бути сульфурові, фосфатні то що солі. Бажані органічні перетворені у проліки. Проліки включають сполусолі цього типу, можуть включати, наприклад, солі ки, в яких амінокислотний залишок або поліпептимурашиної, оцтової, бурштинової, лимонної, молодний ланцюг з двох або більше (наприклад, двох, чної, малеїнової, фумарової, пальмітинової, холетрьох або чотирьох) амінокислотних залишків костирової, памоєвої, муцинової, D-глютамової, Dвалентно приєднані амідним або естеровим зв'язкамфорної, глютарової, гліколевої, фталевої, винком до вільної аміно-, гідрокси- або карбонокислоної, лауринової, стеаринової, салі циклічної, метатної групи сполук винаходу. Амінокислотні нсульфонової, бензолсульфонової, паратолуолсузалишки включають, але без обмеження, 20 прильфонової, сорбінової, пуринової, бензойної, родних амінокислот, які звичайно позначають коричної органічних кислот тощо. Особливо бажатрьома літерами, і також включають 4ними є гідрохлоридні або сульфатні солі сполуки гідроксипролін, гідроксилізин, демозин, ізодемовинаходу. зин, 3-метилпстидин, норвалін, бета-аланін, гамУ сполуках винаходу, які містять такі компонема-аміномасляну кислоту, циртулін, гомоцистеїн, нти, як (CR4R5)m або (CR4R5)t, R4 і R5 можуть змігомосерин, орнітин і метioнінсульфон. Припустинюватись з кожною ітерацією m або t вище 1. Намими є і інші типи проліків. Наприклад, вільні карприклад, коли m або t дорівнює 2, компоненти боксигрупи можуть бути дериватизовані як аміди (CR4R5)m або (CR4R5)t можуть бути -СН2СН2- або або алкільні естери. Вільні гідроксигрупи можуть СН(СН3)С(СН2СНз)(СН2СН2СН3)- або будь-якими бути дериватизовані через застосування груп, які подібними компонентами, що відповідають визнавключають, але без обмеження, гемісукцинати, ченням R4 і R5 у межах винаходу. фосфа тні естери, диметиламіноацетати і фосфоДеякі сполуки винаходу можуть мати асиметрилоксиметилоксикарбоніли, згідно з [Advanced ричні центри і, отже, існувати у різних енантіомерDrug Delivery Reviews 1996, 19, 115]. Сюди входять них формах. Всі оптичні ізомери і стереоізомери також карбаматні проліки гідрокси- i аміногруп, а сполук винаходу і їх суміші входять в об'єм винатакож карбонатні проліки сульфонатні естери і ходу. Щодо сполук винаходу, винахід включає висульфатні естери гідрокси груп. Дериватизація користання рацемату, однієї або більше енантіогідроксигруп як (ацилокси)метилових і (ацилокмерних форм, однієї або більше діастереомерних си)етилових етерів, де ацильна група може бути форм або їх сумішей. Сполуки винаходу можуть алкіловим естером, як варіант, заміщеним групатакож існувати як таутомери. Винахід включає вими, включаючи, але без обмеження, етерові, амікористання всіх таких та утомерів і їх сумішей. нові і карбонокислотні функціональності, або де Винахід також включає мічені ізотопами споацильна група є амінокислотним естером, описа 23 77765 24 ним вище, також входить в об'єм винаходу. Пролігіперпроліферативного розладу у ссавців, який ки такого типу описані у [J. Med. Chem. 1996, 39, включає введення зазначеному ссавцю терапев10]. Вільні аміни можуть також бути дериватизоватично ефективної кількості сполуки-вина-ходу або ні як аміди, сульфонаміди або фосфонаміди. Всі ці її фармацевтично прийнятної солі проліків або проліки можуть містити групи, включаючи, але без гідрату. У одному з втілень зазначений спосіб стообмеження, етерові, амінові і карбонокислотні фусується лікування раку, наприклад, мозку, легенів; нкціональності. лускатих клітин, сечового міхура, шлунку, підшлунЗрозуміло, що у випадках, коли для визначенкової залози, грудей, голови, шиї, нирок, яєчника, ня замісника, приєднаного до структури, викориспростати, прямої кишки, стравоходу, яєчок, гінекотано у послідовності два або більше радикалів, логічного раку або раку щитовидної залози, у інперший поімєнований радикал вважається термішому втіленні зазначений спосіб стосується лікунальним, а останній поімєнований радикал вважавання таких неракових гіперпроліферативних ється приєднаним до цієї структури. Наприклад, розладів, як доброякісна гіперплазія шкіри (наприрадикал арилалкіл приєднаний до структури алкіклад, псоріаз), рестенозу або простати (наприклад, льною групою. доброякісної гіпертрофії простати (ДГП)). Винахід також стосується фармацевтичної Винахід також стосується способу лікування композиції для лікування гіперпроліферативного гіперпроліферативного розладу у ссавців, який розладу у ссавців, яка містить терапевтично ефеквключає введення зазначеному ссавцю терапевтивну кількість сполуки винаходу або її фармацевтично ефективної кількості сполуки винаходу або її тично прийнятної солі, проліків або гідрату і фарфармацевтично прийнятної солі, проліків або гідмацевтично прийнятного носія. У одному з втілень рату у комбінації з антипухлинним агентом, вибразазначена фармацевтична композиція призначаним з групи, яку складають мітотичні інгібітори, ється для лікування раку, наприклад, мозку, легеалкілювальні агенти, антиметаболіти, додаткові нів, лускатих клітин, сечового міхура, шлунку, підантибіотики, інгібітори фактора росту, інгібітори шлункової залози, грудей, голови, шиї, нирок, клітинного циклу, ензимні інгібітори, інгібітори тояєчника, простати, прямої кишки, стравоходу, яєпоізомерази, модифікатори біологічної реакції, чок, гінекологічного раку або раку щи товидної заантигормони, інгібітори ангіогенезу і антиандрогелози. У іншому втіленні зазначена фармацевтична ни. композиція призначається для лікування таких Винахід також стосується способу лікування неракових гіперпроліферативних розладів, як добпанкреатиту або ниркової хвороби у ссавців, який роякісна гіперплазія шкіри (наприклад, псоріаз), включає введення зазначеному ссавцю терапеврестеноз або простата (наприклад, доброякісна тично ефективної кількості сполуки винаходу або її гіпертрофія простати (ДГП)). фармацевтично прийнятної солі, проліків або гідВинахід також стосується фармацевтичної рату. композиції, призначеної для лікування панкреатиту Винахід також стосується способу профілактиабо хвороб нирок (включаючи проліферативний ки імплантування бластоциту у ссавців, який вклюгломерулонефрит і викликану діабетом хворобу чає введення зазначеному ссавцю терапевтично нирок), або для полегшення болю у ссавців, яка ефективної кількості сполуки винаходу або її фармістить терапевтично ефективну кількість сполуки мацевтично прийнятної солі, проліків або гідрату. винаходу або її фармацевтично прийнятної солі, Винахід також стосується способу лікування проліків або гідрату і фармацевтично прийнятного хвороб, пов'язаних з васкулогенезом або ангіогеносія. незом у ссавців, який включає введення зазначеВинахід також стосується фармацевтичної ному ссавцю ефективної кількості сполуки винахокомпозиції для профілактики імплантування бласду або її фармацевтично прийнятної солі, проліків тоциту у ссавців, яка містить терапевтично ефекабо гідрату. У одному з втілень спосіб призначативну кількість сполуки винаходу або її фармацевється для лікування хвороб, вибраних з гр упи, яку тично прийнятної солі, проліків або гідрату і складають ангіогенезна пухлини, хронічна запальфармацевтично прийнятного носія. на хвороби, наприклад, ревматоїдний артрит, атеВинахід також стосується фармацевтичної росклероз, запальна кишкова хвороба, такі шкіряні композиції для лікування хвороб, пов'язаних з васхвороби, як псоріаз, екзема і склеродерма, діабет, кулогенезом або ангіогенезом у ссавців, яка місдіабетична ретинопатія, ретинопатія передчасного тить терапевтично ефективну кількість сполуки розвитку, вікова макулярна дегенерація, гемангіовинаходу або її фармацевтично прийнятної солі, ма, гліома, меланома, саркома Капосі і рак яєчнипроліків або гідрату і фармацевтично прийнятного ка, грудей, легенів, підшлункової залози, простати носія. У одному з втілень зазначена фармацевтиі епідерми. чна композиція призначається для лікування хвоПацієнтами, яких можна лікувати сполуками роб, вибраних з групи, яку складають ангіогенезна винаходу або їх фармацевтично прийнятними сопухлини, хронічна запальна хвороби, наприклад, лями, проліками і гідратами з використанням відревматоїдний артрит, атеросклероз, запальна киповідних способів згідно з винаходом, є такі, у яких шкова хвороба, такі шкіряні хвороби, як псоріаз, були діагнозовані псоріаз, рестеноз, атеросклероз, екзема і склеродерма, діабет, діабетична ретиноВРН, рак легенів, рак кістки, CMML, рак підшлунпатія, ретинопатія передчасного розвитку, вікова кової залози, рак шкіри, рак голови і шиї, меланомакулярна дегенерація, гемангіома, гліома, мелама шкіри або ока, рак матки, рак яєчника, рак прянома, саркома Капосі і рак яєчника, грудей, легемої кишки, рак анальної зони, рак шлунку, рак нів, підшлункової залози, простати і епідерми. товстої кишки, рак грудей, пухлини яєчника і гінеВинахід також стосується способу лікування кологічні пухлини (наприклад, саркоми матки, кар 25 77765 26 цинома фаллопієвої труби, карцинома ендометтрансдукції сигналів і антипроліферативних агенрію, карцинома шийки, карцинома вульви або піхтів. ви), хвороба Ходжкіна, рак стравоходу, рак тонких Такі антиангіогенезійні агенти, як інгібітори кишок, рак ендокринної системи (наприклад, рак ММР-2 (матрична металопротієназа 2), інгібітори щитовидної залози, навколощитовидної залози ММР-9 (матрична металопротієназа 9) і інгібітори або надниркової залози), саркоми м'яких тканин, СОХ-ІІ (циклооксигеназа II), можна використовуварак уретри, рак пеніса, рак простати, хронічна або ти разом з сполукою винаходу і фармацевтичними гостра лейкемію, дитячі тверді пухлини, лімфоциткомпозиціями, описаними тут. Приклади придатні лімфоми, рак сечового міхура, рак нирки або них інгібіторів СОХ-ІІ включають CELEBREXÔ сечового каналу (наприклад, карциноми ниркових (алекоксиб), вальдекоксиб і рофекоксиб. Приклади клітин, карцинома ниркової лоханки) або неоплазпридатних інгібіторів матричної металопротієнази ми центральної нервової системи (наприклад, пеможна знайти у WO 96/33172 (від 24/10/1996), WO рвинна лімфома ЦНС, пухлини хребта, гліоми сто96/27583 (від 7/03/1996), європейських заявках No. вбура мозку або аденоми слизової). 97304971,1 (від 8/07/1997), No. 99308617,2 (від Винахід також стосується фармацевтичної 29/10/1999), WO 98/07697 (від 26/02/1998), WO композиції для інгібування анормального росту 98/03516 (від 29/01/1998), WO 98/34918 (від клітин у ссавців, яка містить сполуку винаходу або 13/08/1998), WO 98/34915 (від 13/08/1998), WO її фармацевтично прийнятну сіль або сольват або 98/33768 (від 6/08/1998), WO 98/30566 (від проліки у комбінації з хемотерапевтичним препа16/07/1998), публікаціях 606046 (від 13/07/1994), ратом, причому кількості сполуки, солі, сольвату 931788 (від 28/07/1999), WO 90/05719 (від або проліків і хемотерапевтичного препарату за31/05/1990), WO 99/52910 (від 21/10/1999), WO безпечують ефективне інгібування анормального 99/52889 (від 21/10/1999), WO 99/29667 (від росту клітин. Відомими є численні хемотерапевти17/06/199.9), заявці РСТ/ІВ98/01113 (від чні препарати. У одному з втілень хемотерапевти21/07/1998), європейській заявці No. 99302232,1 чний препарат вибирають з групи, яку складають (від 25/03/1999), британській заявці No. 9912961,1 мітотичні інгібітори, алкілювальні агенти, антиме(від 3/06/1999), заявці США No. 60/148464 (від таболіти, додаткові антибіотики, інгібітори фактора 12/08/1999), патентах США 5863949 (від росту, інгібітори циклу клітин, інгібітори топоізоме26/08/1999), 5861510 (від 19/01/1999) і європейсьрази, модифікатори біологічної реакції, антигормокій публікації 780386 (від 25/06/1997), включених ни, інгібітори ангіогенезу і антиандрогени. посиланням. Бажаними інгібіторами ММР-2 і ММРВинахід, крім того, стосується способу інгібу9 є ті, що є неактивними або малоактивними в інгівання анормального росту клітин у ссавців або буванні ММР-1. лікування гіперпроліферативного розладу, який Більш бажаними є ті, що інгібують ММР-2 і/або включає введення ссавцю певної кількості сполуки ММР-9 селективно відносно інших матричних мевинаходу або її фармацевтично прийнятної солі талопротієназ (тобто ММР-1, ММР-3, ММР-4, або сольвату або проліків у комбінації з радіаційММР-5, ММР-6, ММР-7, ММР-8, ММР-10, ММРною терапією, причому кількості сполуки, солі, со11,ММР-12 і ММР-13). львату або проліків у комбінації з радіаційною теДеякими конкретними прикладами інгібіторів рапією забезпечують ефективне інгібування ММР, придатних для використання у винаході, є анормального росту клітин або лікування гіперAG-3340, RO 32-3555 і RS 13-0830. проліферативного розладу у ссавців. Способи раТерміни "ріст анормальних клітин" і "гіперпродіаційної терапії є відомими, і вони можуть бути ліферативний розлад" у цьому описі є взаємозазастосовані у комбінації з описаною терапією. мінними. Введення сполуки винаходу у цій комбінованій "Ріст анормальних клітин" тут означає, якщо терапії можна здійснювати, як це описано тут. не визначене інше, ріст клітин, який відбувається Вважають, що сполуки винаходу можуть піднезалежно від нормальних регуляторних механізвищити чутливість анормальних клітин до радіамів (наприклад, з втратою контактного інгібуванційного лікування з метою припинення і/або інгібуня). Це включає, наприклад, анормальний ріст: (1) вання росту ци х клітин. Відповідно, винахід пухлинних клітин (пухлини), які проліферують чевключає спосіб підвищення чутливості анормальрез експресію кінази тирозину, що зазнав мутації, них клітин у ссавців до радіаційного лікування, або через надекспресію рецептора кінази тирозиякий включає введення ссавцю кількості сполуки ну; (2) доброякісних і злоякісних пухлин при інших винаходу або її фармацевтично прийнятної солі проліферативних хворобах, коли відбувається або сольвату або проліків, яка ефективно підвиненормальне активування кінази тирозину; (3) щує чутливість анормальних клітин до радіації. будь-яких пухлин, що проліферують через рецепКількість сполуки, солі або сольват згідно з цим тор кінази тирозину; (4) будь-яких пухлин, що проспособом може бути визначена засобами встаноліферують через ненормальне активування кінази влення ефективних кількостей таких сполук, описерину/треоніну; і (5) доброякісних і злоякісних саними тут. пухлин при інших проліферативних хворобах, коли Винахід також стосується способу застосуванвідбувається ненормальне активування кінази сеня і фармацевтичної композиції для інгібування рину/треоніну. анормального росту клітин у ссавців, яка містить Термін "лікування" тут означає, якщо не висполуку винаходу або її фармацевтично прийнятну значене інше, засоби обернення, припинення, інгісіль або сольват, її проліки або її мічені ізотопами бування розвитку або профілактику розладу або похідні, і містить одну або більше речовин, вибрастану, яких стосується цей термін, або одного або них серед антиангіогенезійних агентів, інгібіторів більше симптомів таких розладу або стану. 27 77765 Типові сполуки винаходу включають, але без обмеження, сполуки прикладів і їх фармацевтично прийнятні солі приєднання кислоти або основи, або ίχ проліки. Наведені нижче приклади ілюструють втілення винаходу, не обмежуючи об'єму опису або Формули винаходу. Схеми 1-4 ілюструють приготування сполук винаходу. 28 29 77765 30 до рН приблизно 0. Операцією 3 одержують естер стандартними методами, наприклад, естерифікацією Фішера (МеОН, H2SO4) і реакцією з TMSCHN2 у придатному органічному розчиннику, наприклад, PhMe/MeOH або ТГФ/МеОН. Операцією 4 одержують похідну діаніліну нагріванням (60-200°С) естеру з надлишком відповідного аніліну чисто або у органічному розчиннику, наприклад, ксилолах. Наприклад, коли R1 є Me і R2 є Η, бажаним методом є перемішування естеру з 10 еквівалентами аніліну у ксилолах під зворотним холодильником до завершення реакції. Операцією 5 нітроарен відновлюють для одержання діаміну стандартним відновленням, використовуючи (без обмеження) Н2 і Pd/C або Pd(OH)2/C або нікель Рейні в органічному розчиннику, наприклад, ЕtOН або ТГФ, Fe у АсОН, Zn у АсОН або Zn, NH4CI (водн) у МеОН. Операцією 6 діамін циклізують нагріванням з мурашиною кислотою або формамідинацетатом у належному розчиннику, наприклад, ЕtOН. У іншому варіанті, коли R1 або R2 не є галогеном, нітроарен може бути перетворений безпосередньо у бензоімідазол операцією 7, а саме, нагріванням у мурашиній кислоті з Pd(OH)2/C або іншим джерелом паладію наприклад, Pd/C. Операцією 8 галогенід можна вводити стандартними методами, використовуючи, але без обмеження, NBS або NCS і pTsOH в органічних співрозчинниках наприклад, ТГФ і МеОН. Операцією 9 бензоімідазол алкілюють, одержуючи приблизно рівну суміш продуктів N1 і N3, які можна розділити стандартними методами, наприклад, хроматографією і перетиранням. Алкілювання здійснюється з використанням алкілювального агента, наприклад, алкілгалогеніду, і основи, наприклад, NaH, або К2СО3 у придатному органічному розчиннику, наприклад, ДМФ або ТГФ при температурах від 0 до 80°С. R7 можна потім модифікувати різними відомими методами синтезу, як це показано нижче. Операцією 10 естер гідролізують стандартним омиленням. Операцією 11 кислоту перетворюють у бажаний гідроксамат, використовуючи стандартні процедури сполучення, з, наприклад (але без обмеження) EDCІ, HOEt або РуВОР і з належним гідроксиламіном у придатному органічному розчиннику, наприклад, ДМФ, ТГФ або метиленхлориді. Схема 2 ілюструє приклад, в якому замісник R8 знаходиться на аніліні перед процедурою сполучення з нітроестером. Реакцію проводять, як, наприклад, у Схемі 1, але без введення R8, яка є в аніліні з самогопочатку. Схема 3 ілюструє отримання похідних N3 алкіламінобензоімідазолу. Операцією 1 термінальний алкен N3 алкілованого бензоімідазолгідроксамату дигідроксилують, застосовуючи придатний окисДля отримання деяких сполук винаходу молювач, наприклад, OsO4 у придатному розчиннику жуть бути застосовані загальні методи синтезу, або КМnО4, або l2, AgOAc, АсОН, воді. Діол далі наприклад, описані у публікації WO 00/42022 (від окислюють операцією 2, використовуючи NalO4 20/07/2000), включеній посиланням. або Рb(ОАс)4 у придатній біфазній суміші для одеСхема 1 ілюструє синтез сполук винаходу ржання альдегіду. У іншому варіанті (опер. 3), алОперацією 1 здійснюється нітрування кислоти у кен може бути безпосередньо перетворений в стандартних умовах, бажано, паруючою нітрогенальдегід стандартними методами, використовуюною кислотою у H2SO4. Операцією 2 готують анілін чи, але без обмеження, озон/MeaS, NalO4/OsO4 заміщенням флуориду NH4OH при кімнатній темабо КМnО4. Операцією 4 одержують амін відновпературі у воді з подальшим обережним підкислювальним амінуванням, застосовуючи стандартні ленням концентрованою неорганічною кислотою методи, наприклад, з Na(CN)BHs, Na(OAc)3BH, 31 77765 32 NMe4BH(OAc)3 з або без АсОН, у придатному розвідні чисті енантіомери. Всі такі ізомери, чиннику, наприклад, метиленхлориді, ацетонітрилі включаючи діастереомерні суміші і чисті енантіоабо ТГФ. Бажаним відновлювальним амінуванням мери, входять в об'єм винаходу. є обробка альдегіду аміном, Me4NBH(OAc) 3 i оцтоАктивність сполук винаходу можна визначити вою кислотою у MeCN при кімнатній температурі. за допомогою описаної далі процедури. NСхема 4 ілюструє отримання сполук винаходу, термінал 6 His-міченої, структурно активної МЕК1 у яких W є гетероциклом. Операцією 1 метиловий (2-393) експресують у Е. соlі і протеїн очищають естер перетворюють у гідразид перемішуванням з звичайними методами [Ahn et al, Science 1994, гідразином у придатному розчиннику, наприклад, 265, 966-970]. Активність МЕК1 оцінюють вимірюЕtOН, при температурі від 50 до 100°С. Бажану ванням введення g-33Р-фосфату з g-33Ρ-ΑΤΡ у Nгетероциклічну похідну потім одержують циклізацітермінал His-міченої ERK2, експресованої у Е. соlі єю належним реагентом. Для оксадіазолу 21 гідраз очищенням звичайними методами у присутності зид обробляють ортоформатом, наприклад, триМЕК1. Дослідження виконували у 96-комірковій етилортоформатом з кислотним каталізатором, поліпропіленовій платі. Інкубаційна суміш (100мкл) наприклад, pTsOH, у придатному органічному розмістила 25мМ Hepes, pH 7,4, 10мМ МgСІ2 , 5мМ рчиннику, наприклад, ЕtOН, при підвищених темпегліцеринфосфату, 100мкМ Na-ортованадату, 5мМ ратурах (50-100°С). Для гідроксиоксадіазолу 22 DTT, 5нМ МЕК1, і 1мкМ ERK2. Інгібітори були сугідразид може бути циклізований фосгеном або спендовані у ДМСО, і всі реакції, включаючи контфосгеновим еквівалентом, наприклад, трифосгерольну, проводили при кінцевій концентрації 1% ном або карбонілдіімідазолом у придатному оргаДМСО. Реакцію ініціювали доданням 10мкМ АТР (з нічному розчиннику, наприклад, толуолі при тем0,5мкСі g-33Р-АТР/комірка) і інкубували при зовнішпературах від 50 до 120°С. Меркаптооксадіазол 23 ній температурі протягом 45хвил. Такий же об'єм може бути приготовлений реакцією з карбондису25%-ї ТСА додавали для припинення реакції і осальфідом і основою, наприклад, КОН, у придатному дження протеїнів. Осаджені протеїни затримуютьорганічному розчиннику, наприклад, ЕtOН, при ся у скловолоконних В-фільтр-платах, і надлишок підвищеній температурі (50-100°С). Амінооксадіаміченої АТР промивають, застосовуючи апарат зол 24 може бути приготовлений реакцією з BrCN і Tomtec МАСH II. Плати сушили повітрям і потім основою, наприклад, NaHCO3, у придатній біфаздодавали 30мкл/комірка Packard Microscint 20 і ній системі розчинників, наприклад, діоксані і воді плати підраховували, застосовуючи Packard Topпри кімнатній температурі. Нарешті, заміщений Count. У цьому дослідженні сполуки винаходу поамінооксадіазол 25 може бути приготовлений споказали ІК50 менше 50мкМ. Далі наведено приклади чатку реакцією гідразиду з належним ізотіоціанасполук такої активності. том у придатному органічному розчиннику, наприклад, ДМФ або ТГФ при температурах від 25 до Сполука 100°С. Інтермедіат можна ізолювати або циклізу-8n вати безпосередньо обробкою EDCI або іншим 11b карбодіімідом у придатному органічному розчин11с нику, наприклад, ТГФ або ДМФ, при температурах 11р від кімнатної до 80°С. 18i Схема 5 ілюструє отримання похідних кетобе29с нзоімідазолу. Операцією 1 метиловий естер пере29і творюють у бензиловий спирт стандартними ме29s тодами відновлення, бажано, з використанням 29t LAH у ТГФ при 0°С або NaBH4 у ЕtOН/ТГФ при 29bb кімнатній температурі. Окислювання до альдегіду може бути здійснене операцією 2 з застосуванням 29111 МnОа в ацетон/ТГФ при 50°С. Операцією 3 у ТГФ 29mmm до альдегіду можуть бути додані органометалеві реагенти, наприклад, органолітій і реагенти ГриньВведення сполук винаходу (далі - "активні яра при низькій-температурі (наприклад, -78°С), з сполуки") можна здійснювати будь-яким методом, одержанням бензилового або заміщеного бензиякий забезпечує доставку сполук до місця дії. Ці лового спирту. Кетопохідні можуть бути приготовметоди включають оральне і внутрішньодуоденалені в операції 4 окислюванням бензилового спирльне введення, парентеральну ін'єкцію (включаюту в стандартних умовах, наприклад, чи внутрішньовенну, підшкірну, внутрішньом'язову, окислюванням Свема або Дес-Мартина. внутрішньосудинну ін'єкцію або інфузію), локальне Сполуки винаходу можуть мати асиметричні і ректальне введення. атоми карбону. Діастереомерні суміші можна розКількість введеної активної сполуки залежить діляти на окремі діастереомери, базуючись на їх від суб'єкта, що одержує лікування, важкості розфізико-хімічних відмінностях, методами, відомими ладу або стану, частоти введення, розміщення фа хівцям, наприклад, хроматографією або фраксполуки і призначень лікаря. Ефективні дози стаційною кристалізацією. Енантіомери можна роздіновлять від приблизно 0,001 до приблизно 100мг ляти перетворенням енантіомерної суміші у діасна кг маси тіла на день, бажано, приблизно від 1 тереомерну реакцією з належною оптично до приблизно 35мг/кг/день одиничними або подріактивною сполукою (наприклад, спиртом), роздібненими дозами. Для людини масою 70кг це відленням діастере-омерів і перетворенням (наприповідає кількості приблизно 0,05-7г/день, бажано, клад, гідролізом) окремих діастереомерів у відпоприблизно від 0,05 до приблизно 2,5г/день. У де 33 77765 34 яких випадках адекватними можуть бути дози, ниного типу можуть також мати форму м'яких і жчі за наведену нижчу межу, а в інши х випадках жорстких наповнених желатинових капсул. Бажаадекватними можуть бути дози, вищі за наведену ними матеріалами можуть бути лактоза або моловерхню межу без появи будь-яких шкідливих побічний цукор і високомолекулярні поліетиленгліколі. чних явищ, за умови, що такі великі дози будуть При використанні для орального введення водних розділені на декілька менших доз при введення суспензій або еліксирів активну сполуку можна протягом дня. комбінувати з різними підсолоджувачами або смаАктивна сполука може бути застосована як ковими агентами, забарвлювачами і, якщо бажано, єдина терапія або може сполучатись з однією або емульгаторами або суспендуючими агентами, рабільше іншими антипухлинними препаратами, назом з такими розріджувачами, як вода, етанол, приклад, вибраними серед мітотичних інгібіторів, пропіленгліколь, гліцерин або їх комбінації. наприклад, вінбластину; алкілювальних агентів, Методи отримання фармацевтичних композинаприклад, цис-платину, карбоплатину і циклофоцій з визначеною кількістю активної сполуки є вісфаміду; антиметаболітів, наприклад, 5домими. [Див., наприклад, Remington's флуорурацилу, арабінсиду цитозину і гідроксимоPharmaceutical Sciences, Mack Publishing Company, чевини, або, наприклад, одного з бажаних антимеEster, Pa., 15 th Edition (1975)]. таболітів, описаних у європейській заявці No. Приклади і приготування, наведені нижче, ілю239362, наприклад, з N-(5-[N-(3,4-дигідро-2-метилструють сполуки винаходу і методи отримання 4-оксохіназолін-6-ілметил)-N-метиламіно]-2таких сполук. Зрозуміло, що об'єм винаходу не теноїл)-L-глутамовою кислотою; інгібіторів фактообмежується наведеними прикладами і приготура росту; інгібіторів циклу клітин; додаткових антиваннями. У цих прикладах, якщо не визначено інбіотиків, наприклад, адріаміцину і блеоміцину, енше, молекули з одним хіраль-ним центром існують зимів, наприклад, інтерферону; і антигормонів, як рацемічна суміш. Молекули з декількома хіранаприклад, антиестрогенів, наприклад, льними центрами, якщо не визначено інше, існуNolvadexTM (тамоксифен) або, наприклад, антиють як рацемічна суміш діастереомерів. Одиничні андрогенів, наприклад, CasodexTM (4'-ціано-3-(4енантіомери/діастереомери можна отримати відофлуорфенілsмкпрhоніл)-2-гідрокси-2-метил-3'мими методами. (трифлуорметил)пропіонанілід). Таке комбіноване У цьому описі всі статті і посилання,· включалікування можна проводити з одночасним або поючи патенти, включені посиланням. слідовним введенням, або з окремим дозуванням Винахід ілюструється наведеними далі приіндивідуальних компонентів лікування. кладами,які не обмежують об'єм або концепції Фармацевтична композиція може, наприклад, винаходу описаними конкретними процедурами. мати форму, придатну для орального введення у Вихідні матеріали і різні інтермедіати можна вигляді таблетки, капсули, пігулки, порошку, рецепридбати з комерційних джерел приготува ти з коптури безперервного вивільнення, розчину або мерційно доступних органічних сполук, або синтесуспензії, придатної для парентеральної ін'єкції у зувати добре відомими методами. вигляді стерильного розчину, суспензії або емульДалі наведено приклади. сії, для локального введення у вигляді мазі або Приклади крему, або придатну для ректального введення Приклад 1 супозиторієм. Фармацевтична композиція може, бути у одиничній дозованій формі, придатній для одиничного введення точної дози. Фармацевтична композиція включає звичайні фармацевтичні носії або наповнювачі і сполуку винаходу як активний інгредієнт. Вона може також включати інші медичні або фармацевтичні агенти, носії, ад'юванти тощо. Типовими формами для парентерального введення є розчини або суспензії активної сполуки у стерильних водних розчинах, наприклад, водноЦикпопропілметоксиамід 7-флуор-6-(4-бром-2метилфеніламіно)-3Н-бензоімідазол-5-карбонової му пропіленгліколі або розчинах декстрози. За кислоти (11а) бажанням такі дозовані форми можуть бути буфеЕтап А: 2,3,4-трифлуор-5-нітробензойна кисровані. лота 2 Придатними фармацевтичними носіями можуть бути інертні розріджувачі або наповнювачі, У 3-літрову тригорлу круглодонну колбу вносять 125мл H2SO4, додають паруючу нітрогенну вода і різні органічні розчинники. Фармацевтичні кислоту (8,4мл, 199ммоль) і суміш обережно пекомпозиції можуть містити додаткові інгредієнти, ремішують. Порціями по 5г додають 2,3,4наприклад, смакові добавки, зв'язуючі, ексципієнти трифлуорбензойну кислоту 1 (25г, 142ммоль) протощо. Таблетки для орального введення можуть містити різні ексципієнти, наприклад, лимонну кистягом 90хвил. Темний коричнево-жовтува тий розчин перемішують протягом 60хвил. до завершення лоту разом з різними розпушувачами, наприклад, реакції. Реакційну суміш вливають у 1л водольокрохмалем, альгіновою кислотою і деякими комдової суміші і екстрагують діетилетером плексними силікатами, з зв'язуючими агентами, (3х600мл). Об'єднані органічні екстракти сушать наприклад, сахарозою, желатином і гуміарабіком, з змащувачами, наприклад, стеаратом магнію, лау(MgSO4) і концентрують під зниженим тиском, одержуючи жовту тверду речовину, яку суспендують у рилсульфатом натрію і тальком, які сприяють ввегексанах і перемішують протягом 30хвил. і потім денню ліків таблетками. Тверді композиції подіб 35 77765 36 фільтрують, одержуючи 29г (92%) чистого бажано95°С з перемішуванням. Через 16год. реакційну го продукту як жовтуватої твердої речовини: MS суміш охолоджують до кімнатної температури і APCI (-) m/z 220 (М-І-структура). фільтрують через Celite і промивають ЕtOН. ФільЕтап В: 4-аміно-2,3-дифлуор-5-нітробензойна трат концентрують під зниженим тиском до осакислота 3 дження бажаного продукту, який збирають фільтРозчин гідроксиду амонію (прибл. 30% у воді) руванням. Фільтрат концентрують знову до (35мл, 271ммоль) додають до розчину 2,3,4більшого осадження бажаного продукту. Продукт трифлуор-5-нітробензойної кислоти 2 (15г, збирають фільтруванням і декілька разів концент67,8ммоль) у 30мл води при 0°С з перемішуванрують ЕtOН і фільтрують, одержуючи 1,09г (74%) ням. Після цього реакційну суміш доводять до кімчистого бажаного продукту: MS АРСІ (+) m/z 300 натної температури з перемішуванням. Через (М+1-стр уктура); MS АРСІ (-) m/z 298 (М-І2,5год. суміш охолоджують до 0°С і обережно доструктура). дають конц. НСІ до досягнення рН прибл. 0. РеакЕтап F: метиловий естер 7-флуор-6-(4-бром-2ційну суміш розбавляють водою (30мл) і екстрагуметилфеніламіно)-1Н-бензоімідазол-5-карбонової ють діетилетером (3х50мл). Об'єднані органічні кислоти 8а екстракти сушать (MgSO4) і концентрують під зниМетиловий естер 7-флуор-6-о-толіламіно-1Нженим тиском, одержуючи 14г (95%) чистого бабензоімідазол-5-карбонової кислоти 7а (2,00г, жаного продукту: MS APCI (-) m/z 211 (М-І6,68ммоль) суспендують у суміші 1:1 ТГФ:МеОН структура). (60мл) і охолоджують до -78°С в атмосфері нітроЕтап С: метиловий естер 4-аміно-2,3-дифлуоргену. Додають розчин NBS (1,20г, 6,75ммоль) у 1:1 5-нітробензойної кислоти 4 ТГФ/МеОН (5мл) і потім МеОН (5мл) розчин 2М розчин TMS діазометану у гексанах TsOH·H2O (1,9г, 10,0ммоль). Через 30хвил. реак(6,88мл, 13,75ммоль) додають до суспензії 4ційну суміш доводять до 0°С і через 1год. довоаміно-2,3-дифлуор-5-нітробензойної кислоти 3 дять до кімнатної температури. Через 16год. до(2,00г, 9,17ммоль) у 25мл 4:1 ТГФ:МеОН при 0°С в дають ще NBS (0,12г, 0,67ммоль) і реакційну суміш атмосфері нітрогену. Після цього реакційну суміш залишають перемішува тись протягом 3год. Реакпідігрівають до кімнатної температури і через ційну суміш гасять доданням 10%-го розчину 0,5год. надлишок TMS діазометану нейтралізують Na2S2O4. Через 30хвил. реакційну суміш розбавобережним доданням оцтової кислоти. Реакцію ляють водою і етилацетатом і шари розділяють. концентрують під зниженим тиском і сушать у ваВодний шар екстрагують етилацетатом. Об'єднані куумі, одержуючи 1,95г (92%) чистого бажаного органічні екстракти суша ть (Na2SO4) і концентрупродукту: MS АРСІ (-) m/z 231 (М-І). ють під зниженим тиском. Одержану тверду речоЕтап D: метиловий есгпер 4-аміно-3-флуор-5вину перетирають з метиленхлоридом, одержуючи нітро-2-о-толіламінобензойної кислоти 5а 2,00г (79%; чистого бажаного продукту: MS АРСІ Метиловий естер 4-аміно-2,3-дифлуор-5(+) m/z 380, 378 (М+1 Вr-структура). нітробензойної кислоти 4 (12,0г, 51,7ммоль) суЕтап G: 7-флуор-6-(4-бром-2спендують у ксилолах (60мл) і додають ортометилфеніламіно)-1Н-бензоімідазол-5-карбонова толуїдин (55,2мл, 517ммоль). Реакційну суміш кислота 10а гріють під зворотним холодильником з перемішуМетиловий естер 7-флуор-6-(4-бром-2ванням в атмосфері нітрогену. Через 36год. реакметилфеніламіно)-1Н-бензоімідазол-5-карбонової ційну суміш охолоджують до кімнатної температукислоти 8а (63мг, 0,167ммоль) суспендують у Мери, розбавляють діетилетером і промивають 10%ОН (1,5мл) і додають 20% NaOH (400мкл). Через м водним розчином НСІ. Водні змивки екстрагують 16год. реакційну суміш охолоджують до 0°С і крадіетилетером, об'єднані органічні екстракти концеплями додають розчин 1N НСІ до досягнення рН нтрують під зниженим тиском, залишок розчиня2-3. Реакційну суміш розбавляють етилацетатом і ють у метиленхлориді, фільтрують через силікаводою і шари розділяють. Органічний шар промигель у фритованій воронці і промивають вають розсолом, сушать (Na2SO4) і концентрують метиленхлоридом, одержуючи три фракції. Перша під зниженим тиском, одержуючи 58мг (95%) ба(2л) є майже чистою, згідно з ВЕРХ. Друга (1л) і жаного продукту: MS АРС І (+) m/z 366, 364 (М+1 третя (1л) фракції є чистими лише частково. ПерВr-структура); MS АРСІ (-) m/z 364, 362 (М-І Вгшу фракцію концентрують під зниженим тиском і структура). розтирають з діетилетером, одержуючи 11,2г Етап Н: Циклопропілметоксиамід 7-флуор-6(68%) чистого бажаного продукту як яскраво жов(4-бром-2-метилфеніламіно)-1Н-бєнзоімідазол-5тої твердої речовини: MS АРСІ (-) m/z 318 (М-Ікарбонової кислоти 11а структура). 7-флуор-6-(4-бром-2-метилфеніламіно)-1НЕтап Е: метиловий естер 7-флуор-6-обензоімідазол-5-карбонову кислоту 10а (48мг, толіламіно-1Н-бензоімідазол-5-карбонової кислоти 0,132ммоль) розчиняють у 1:1 ТГФ: метиленхло7а рид (1мл) і додають основу Гуніга (0,23мкл, Метиловий естер 4-аміно-3-флуор-5-нітро-2-о1,32ммоль) і потім РуВОР (82мг, 0,158ммоль). Четоліламінобензойної кислоти 5а (1,57г, рез декілька хвил. додають циклопропілметилгід4,92ммоль), мурашину кислоту (25мл, 26,5ммоль) і роксиламінгідрохлорид (20мг, 0,158ммоль) (WO 20% Pd(OH)2/C (1,57г, 2,95ммоль) у 25мл ЕtOН 0042022). Після завершення реакції суміш роздінагрівають з перемішуванням до 95°С. Через ляють між метиленхлоридом і насиченим розчи16год. реакційну суміш о холоджують до кімнатної ном NaHCO3. Шари розділяють і органічний шар температури і додають 0,5г 20% Pd(OH)2/C і 10мл промивають насиченим NaHCO3 і розсолом. Оргамурашиної кислоти. Реакційну суміш доводять до нічний шар сушать (Na2SO4) і концентрують під 37 77765 38 зниженим тиском. Очищенням колонною флешхроматографією (елюент - 20:1 метиленхлорид:МеОН) одержують 25мг (45%) чистого бажаного продукту: MS ESI (+) m/z 435, 433 (М+1 Вrструктура); MS ESI (-) m/z 433, 431 (М-І Вrструктура); 1Н ЯМР (400МГц, CDCI3) d 8,15 (s, 1H), 8,02 (s, 1H), 7,28 (s, 1H), 7,43 (d, 1H), 7,07 (dd, 1H), Метиловий естер 6-(4-бром-26,36 (m, 1H), 3,70 (d, 2H), 2,38 (s, ЗН), 0,86 (m, 1H), хлорфеніламіно)-7-флуор-3Н-бензоімідазол-519 0,41 (m, 2H), 0,13 (m, 2H); F ЯМР (376МГц, карбонової кислоти (8b) CDCI3)-134,05 (s). Етап А: метиловий естер 6-(4Приклад 2 бромфеніламіно)-7-флуор-3Н-бензоімідазол-5карбонової кислоти 28а Метиловий естер 7-флуор-6-феніламіно-3Нбензоімідазол-5-карбонової кислоти 27а (4,99г, 17,51ммоль) розчиняють у Ν,Ν-ДМФ (275мл). Додають твердий N-бромсукцинімід (3,15г, 17,70ммоль) і реакційну суміш перемішують при кімнатній температурі під N2. Через 30хвил. реакційну суміш гасять доданням водного насиченого Метиловий естер 7-флуор-6-феніламіно-3Нрозчину бісульфі ту натрію. Реакційну суміш влибензоімідазол-5-карбонової кислоти (27а) вають у сепараторну воронку, розбавляють водою Етап А: метиловий естер 4-аміно-3-флуор-5і етилацетатом , шари ризл'ляють. Водний шар нітро-2-феніламінобензойної кислоти 26а екстрагують етилацетатом, об'єднані органічні Метиловий естер 4-аміно-2,3-дифлуор-5екстракти промивають тричі водою, розсолом, сунітробензойної кислоти 4 (23,48г, 101,1ммоль), шать (Na2SO4) і концентрують під зниженим тиспродукт Прикладу 1, Етапу С, суспендують у ксиком, одержуючи 6,38г (100%) чистого бажаного лолах (125мл) і додають анілін (92мл, 1011ммоль). продукту як тверду речовину. MS ESI (+) m/z 364, Реакційну суміш перемішують при 125°С протягом 366 (М+ Br). 16год. під Ν2 і потім охолоджують до кімнатної теЕтап В: метиловий естер 6-(4-6ром-2-хлормператури і тверду речовину осаджують з розчину. феніламіно)-7-флуор-3Н-бензоімідазол-5Тверду речовину збирають фільтруванням і прокарбонової кислоти 8b мивають ксилолами і потім діетилетером. ОдерМетиловий естер 6-(4-бром-феніламіно)-7жана 22,22г (72,78ммоль) жовта тверда речовина флуор-3Н-бензоімідазол-5-карбонової кислоти 28а є чистим бажаним продуктом. Фільтрат концент(6,38г, 17,51ммоль) розчиняють у Ν,Ν-ДМФ рують під зниженим тиском, розчиняють у мети(275мл). Додають твердий N-хлорсукцинімід (2,36г, ленхлориді і пропускають через пробку силікаге17,70ммоль) і реакційну суміш перемішують при лю, елююючи метиленхлоридом. Бажані фракції кімнатній температурі під N2 до завершення реакконцентрують під зниженим тиском, одержуючи ції (5-6 днів). Реакційну суміш гасять доданням коричневу тверду речовину, яку перетирають з водного насиченого розчину бісульфіту натрію, діетилетером, одержуючи 5,47г (17,91ммоль) жоводержуючи суспензію. Одержану тверду речовину тої твердої речовини, яка є чистим бажаним поодзбирають фільтруванням, промивають водою і уктом. Вихід об'єднаного продукту 27,69г (90%). діетилетером і сушать під зниженим тиском, одерMS APCI (-) m/z 304 (М-І-стр уктура). жуючи 6,07г (87%) чистого бажаного продукту як Етап В: метиловий естер 7-флуор-6тверду речовину. MS ESI (+) m/z 398, 400 (М+ Brфеніламіно-3Н-бензоімідазол-5-карбонової кислоструктура). ти 27а Приклад 4 Метиловий естер 4-аміно-3-флуор-5-нітро-2феніламіно-бензойної кислоти 26а (16,70г, 54,71ммоль), мурашину кислоту (250мл, 6,63моль) і 20% Pd(OH)2/C (9,00г, 16,91ммоль) у етанолі (250мл) перемішують при 40°С 2год. під N 2 і потім при 95°С протягом 16год. Реакційну суміш охолоджують до кімнатної температури і фільтрують через Celite, промиваючи етилацетатом. Фільтрат концентрують під зниженим тиском, одержуючи Метиловий естер 6-(2,4-Дихлор-феніламіно)-7жовту тверду речовину, яку перетирають з діетифлуор-3Н-бензоімідазол-5-карбонової кислоти (8с) летером, одержуючи 13,47г (86%) бажаного проМетиловий естер 27-флуор-6-феніламіно-3Ндукту як коричневу тверду речовину. MS APCI (+) бензоімідазол-5-карбонової кислоти 7а (1,00г, m/z 286 (М+1-структура); MS APCI (-) m/z 284 (М-І3,51ммоль) суспендують у 1:1 ТГФ/метанол (20мл) структура). і охолоджують до -78°С під N2. Додають TsOH·H2O Приклад 3 (3,00г, 10,50ммоль) і потім N-хлорсукцинімід (0,95г, 7,08ммоль). Через 10хвил. реакційну суміш підігрівають до 0°С, одержуючи розчин, і через 30хвил. підігрівають до кімнатної температури. Після перемішування протягом 16год. реакція завершується. Реакційну суміш гасять доданням водного на 39 77765 40 сиченого розчину бісульфіту натрію і розбавляють етилацетатом і водою і шари розділяють. Водний шар екстрагують етилацетатом, об'єднані органічні екстракти промивають розсолом, сушать (Na2SO4) і концентрують під зниженим тиском. Одержану твердий залишок перетирають з метиленхлоридом, одержуючи білу тверду речовину, яку збирають фільтруванням, одержуючи 1,05г (85%) чистоМетиловий естер 7-флуор-6-(2-метил-4го бажаного продукту. MS ESI (+) m/z 355, 357 трифлуорметоксифеніламінс)-3Н-бензоімідазол-5(М+СІ-структура). карбонової кислоти (8f) Приклад 5 Етап А: метиловий естер 4-аміно-3-флуор-2(2-метил-4-трифлуорметоксифеніламіно)-5-нітробензойної кислоти 12а Метиловий естер 4-аміно-2,3-дифлуор-5нітробензойної кислоти 4 (0,50г, 2,15ммоль) суспендують у ксилолах (3мл) і додають 2-метил-4трифлуорметоксифеніламін (1,00г, 5,23ммоль). Реакційну суміш перемішують при 140°С під N2. Після 7-денного перемішування реакція стає суміМетиловий естер 6-(4-6ром-2-флуоршшю ви хідного матеріалу і продукту. Реакційну феніламіно)-7-флуор-3Н-бензоімідазол-5суміш охолоджують до кімнатної температури, карбонової кислоти (8d) вливають у сепараторну воронку, додають діетиЕтап А: метиловий естер 4-аміно-3-флуор-2летер і 10%-у водну НСІ і шари розділяють. Водну (2-флуор-феніламіно)-5-нітробензойної кислоти 5b фазу екстрагують тричі діетилетером. Об'єднані Метиловий естер 4-аміно-2,3-дифлуор-5діетилетерові шари сушать (MgSO4) і концентрунітробензойної кислоти 4 (1,50г, 6,46ммоль) сують під зниженим тиском. Залишок розчиняють у спендують у ксилолах (7,5мл) і додають 2метиленхлориді і проводять через пробку силікафлуорфеніламін (6,24мл, 64,6ммоль). Реакційну гелю, елююючи метиленхлоридом. Фільтрат консуміш перемішують при 140°С під N2. Після 6центрують під зниженим тиском, одержуючи яскденного перемішування реакція завершується. равожовту тверду речовину, яку промивають Реакційну суміш охолоджують до кімнатної темпедіетилетером, фільтрат концентрують під знижератури, розбавляють метиленхлоридом і фільтруним тиском і залишок очищають колонною флешють через силікагелеву пробку, елююючи метихроматографією (елюент -100% метиленхлориду), ленхлоридом (1л) і одержують оранжевий одержуючи 0,39г (45%) бажаного чистого продукту фільтрат, який концентрують до сухості і перетияк жовту тверду речовину. MS АРСІ (-) m/z 402 (Мрають з діетилетером, одержуючи яскравожовту 1-структура). тверду речовину. Перетирання повторюють і жовЕтап В: метиловий естер7-флуор-6-(2-метилту тверду речовину збирають, одержуючи 1,08г 4-трифлуорметокси-феніламіно)-3Н(52%) чистого бажаного продукту. MS АРСІ (-) m/z бензоімідазол-5-карбонової кислоти 8f 322 (М-І-стр уктура). Метиловий естер 4-аміно-3-флуор-2-(2-метилЕтап В: метиловий естер 6-(4-бром-2-флуор4-трифлуорметоксифеніламіно)-5-нітробензойної феніламіно)-7-флуор-3Н-бензоімідазол-5кислоти 12а перетворюють описаними вище відкарбонової кислоти 8d новленням/циклізацією, одержуючи бажаний проМетиловий естер 4-аміно-3-флуор-2-(2дукт. MS АРСІ (+) m/z 384 (М+1-стр уктура); MS флуорфеніламіно)-5-нітробензойної кислоти 5b APCI (-)m/z 382 (М-І-стр уктура). перетворюють відновленням/циклізацією і бромуПриклад 8. Отримання гідроксиламичів ванням, описаними вище, і одержують бажаний Гідроксиламіни для синтезування сполук випродукт. MS ESI (+) m/z 382, 384 (М+, Brнаходу можуть бути приготовлені, як описано далі. структура). (і) О-(2-метоксиетил)-гідроксиламін Приклад 6 Етап А: 2-(2-метокси-етокси)-ізоіндол-1,3-діон DEAD (10мл, 63ммоль) додають до суміші 2метоксиетанолу (5,0мл, 63ммоль), PPh3 (17г, 63ммоль), і N-гідроксифталіміду (10г, 62ммоль) у ТГФ (170мл). Одержаний оранжевий розчин перемішують 16год. при кімнатній температурі. Реакційну суміш концентрують у вакуумі і тверду речовину фільтрують, промиваючи СНСІ3. Фільтрат Метиловий естер 6-(4-хлор-2знову концентрують і тверду речовину фільтрують, метилфеніламіно)-7-флуор-3Н-бензоімідазол-5промиваючи СНСІ3. Ці дії повторюють до появи карбонової кислоти (8е) осаду. Жовтувату тверду речовину рекристалізуМетиловий естер 7-флуор-6-о-толіламіно-3Нють з ЕtOН, одержуючи бажаний продукт (7,7г, бензоімідазол-5-карбонової кислоти 7а перетво55%). рюють описаним вище бромуванням, використоЕтап В: О-(2-метоксиетил)-гідроксиламін вуючи N-хлорсукцинімід замість NДо розчину 2-(2-метоксиетокси)-ізоіндол-1,3бромсукциніміду, і одержують бажаний продукт. діону (7,7г, 35ммоль) у СН2СІ2 (30мл) при кімнатній MS ESI (+) m/z 334, 336 (М+, СІ-стр уктура). температурі додають мегилгідразин (2,0мл, Приклад 7 41 77765 42 36ммоль). Одержаний розчин перемішують протя(ν) О-(2-морфолін-4-іл-етил)гом 16год. 'при кімнатній температурі. Білу тверду гідроксиламіндигідрохлорид речовину відфільтровують. Розчинник обережно Етап А: О-(2-бром-етил)рщділяють під зниженим тиском, концентрат диисгідроксиламінгідробромід тилюють під вакуумом (20Тор. 57-58°С), одержую2-(2-бром-етокси)-ізоіндол-1,3-діон, приготовчи бажаний продукт (2,2г, 68%). лений з 1,2-диброметану і Ν-гідроксифталіміду (іі) Наведені далі гідроксиламіни одержують, [див. WO 0018790] обробляють за процедурою, як описано вище, застосовуючи належні спирти. описаною у Org. Chem. 1963,28,1604, одержуючи Ізоіндол-1,3-діонні інтермедіати очищають флешбажаний продукт. хроматографією. Етап В: Трет-бутиловип естер (2-брометокси)карбамової кислоти До розчину O-(2-брометил)О(2-ізобутокситил)гідроксиламінгідроброміду (100мг, 0,45ммоль) і дигідроксиламін використовують безпосередньо, без t-бутилдикарбонату (110мг, 0,49ммоль) у СН 2СІ2 очищення. (1мл) при кімнатній температурі додають EtsN (0,08мл, 0,56ммоль). Одержану суспензію, перемішують 16год. при кімнатній температури. РеакО-(2-піролідин-1-ілетил)ційну суміш розбавляють ЕtOАс, промивають 1N гідроксиламін використовують безпосередньо, без водн. НСІ і розсолом, сушать над MgSO4, фільточищення. рують, концентрують і очищають флешхроматографією (100% СН2СІ2), одержуючи бажаний продукт (81мг, 75%). О-(2-піперидин-1-ілетил)Етап С: Трет-бутиловий естер (2-морфолін-4гідроксиламін очищають дистиляцією Кугельрора іл-етокси)-карбамовоїкислоти (температура камери 140°С, 1Тор.). До розчину трет-бутилового естеру (2О-(2-метилсульфанілетил)брометокси)-карбамової кислоти (252мг, гідроксиламін очищають вакуумною дистиляцією 1,05ммоль) у ДМФ (2мл) при кімнатній температурі (76-78°С, 20Тор.). додають морфолін (0,14мл, 1,6ммоль). Реакційну суміш перемішують протягом 7год. при 50°С і поО-(2-фенілсульфанілетил)тім розбавляють ЕtOАс і промивають водою. Оргідроксиламін використовують безпосередньо, без ганічний шар сушать над MgSO4, фільтр ують, коночищення. центрують і очищають флеш-хроматографією (2% О-(3-метилсульфанілпропіл)МеОН у СН 2СІ2), одержуючи бажаний продукт гідроксиламін використовують безпосередньо, без (118мг, 46%) MS АРСІ (+) m/z 247. очищення. Етап D: О-(2-морфолін-4-ілетил)(ііі) Наведені далі гідроксиламіни одержують з гідроксиламіндигідрохлорид відповідних ізоіндол-1,3-діонів окислюванням, заДо розчину трет-бутилового естеру (2стосовуючи оксон [Tetrahedron Lett. 1981, 22, морфолін-4-ілетокси)-карбамової кислоти (118мг, 1287], з подальшим зняттям захисту, як це описа0,48ммоль) у МеОН (1мл) додають 4М діоксановий но вище. розчин НСІ (2,4мл, 9,60ммоль) при кімнатній температурі. Одержаний розчин перемішують протягом 16год. при кімнатній температурі. Після доО-(2-метансульфонілетил)дання НСІ (2,4мл) з наступним перемішуванням гідроксиламін використовують безпосередньо, без протягом 4год. реакційну суміш концентрують у очищення. вакуумі, одержуючи жовту тверду речовину (82мг, 78%). О-(2-бензолсульфонілетил)(vi) Інтермедіати ізоіндол-1,3-діони для гідрогідроксиламін очищають флеш-хроматографією ксиламінів одержують з належного алкілгалогеніду (1% МеОН у СН 2СІ2). і N-гідроксифталіміду за процедурою, описаною у [J. Hetercyclic Chem., 2000, 37, 827-830]. Ізоіндол1,3-діони позбавляють захисту за процедурою, О-(3-метансульфонілпропіл)описаною вище: О-бут-3-енілгідроксиламін; Огідроксиламін використовують безпосередньо, без (ТГФ-2-ілметил)-гідроксилзмін; О-(3-метоксиочищення. пропіл)-гідроксиламін; і О-(3-бензилоксипропіл)·О-(3гідроксиламін. фенілсульфанілпропіл)-гідроксиламін одержують з (vii) Наведені далі гідроксиламіни одержують, PhSCH2CH2CH2Br і N-гідроксифталіміду за процеяк це описано у WO 0206213: О-(2-вінілоксиетил)дурою WO 0018790 з подальшим зняттям захисту, гідроксиламін; 2-аміноокси-2-метилпропан-1-ол; 1як описано вище, і використовують без очищення. аміноокси-2-метилпропан-2-ол; 3амінооксипропан-1-ол; і (трет-бутиловий естер 2аміноксиетил)-метилкарбамової кислоти . (iv) О-(3Приклад 9 бензолсульфонілнілпропіл)-гідроксиламін одержують з ізоіндол-1,3-діону окислюванням оксоном з подальшим зняттям захисту і очищають флешхроматографією (100% СН2СІ2 до 2% МеОН у СН2СІ2). 43 77765 44 татом і водою. Шари розділяють і водний шар екстрагують етилацетатом. Об'єднані органічні екстракти сушать (MgSO4) і концентрують під зниженим тиском. Сирий продукт перетирають з метиленхлоридом, одержуючи 58мг (85%) чистого бажаного продукту як коричневу тверду речовину. Етап Е: 6-(4-бром-2-хлорфеніламіно)-7-флуорЦиклопропілметоксиамід 6-(4-бром-23Н-бензоімідазол-5-карбонова кислота 10b хлорфеніламіно)-7-флуор-3Н-бензоімідазол-5Метиловий естер 8b 6-(4-бром-2карбонової кислоти (11b) хлорфеніламіно)-7-флуор-3Н-бензоімідазол-5Етап А: Метиловий естер 4-аміно-2-(2карбонової кислоти (58мг, 0,146ммоль) суспендухлорфеніламіно)-3-флуор-5-нітробензойної кислоють у ЕtOН (2мл) і додають 1мл 2N NaOH. Через ти 5b 16год., реакційну суміш розбавляють етилацетаМетиловий естер 4-аміно-2,3-дифлуор-5том, водою, і 10%-м розчином НСІ. Шари розділянітробензойної кислоти 4 (2,00г, 8,62ммоль) сують і органічний шар промивають розсолом. Оргаспендують у ксилолах (15мл) і додають 2нічний шар сушать (MgSO4) і концентрують під хлоранілін (9,06мл, 86,15ммоль). Реакційну суміш зниженим тиском. Перетирання з МеОН дає 22мг нагрівають до 140°С в атмосфері нітрогену. Через (39%) чистого бажаного продукту. 6 днів реакційну суміш о холоджують до кімнатної Етап F: циклопропілметоксиамід 6-(4-бром-2температури і розбавляють етилацетатом, потім хлорфеніламіно)-7-флуор-3Н-бензоімідазол-5промивають водою, 10%-м розчином НСІ і розсокарбонової кислоти (lІb) лом. Органічний шар сушать (MgSO4) і концентру6-(4-бром-2-хлорфеніламіно)-7-флуор-3Нють під зниженим тиском. Сирий продукт двічі пебензоімідазол-5-карбонову кислоту 10b (22мг, ретирають з діетилетером, одержуючи 0,35г (12%) 0,057ммоль) розчиняють у ДМФ (1мл) і HOBt (9мг, чистого бажаного продукту як коричневату тверду 0,062ммоль) і додають триетиламін (18мкл, речовину. 0,132ммоль), циклопропілметилгідроксиламіЕтап В: Метиловий естер 4,5-діаміно-2-(2нгідрохлорид (8мг, 0,062ммоль) і EDCI (14мг, хлорфеніламіно)-3-флуорбензойної кислоти 6а 0,074ммоль). Через 16год. реакційну суміш розбаМетиловий естер 4-аміно-2-(2вляють етилацетатом і водою і шари розділяють. хлорфеніламіно)-3-флуор-5-нітробензойної кислоОрганічний шар промивають насиченим NH4CI, ти 5b (0,30г, 0,88ммоль) суспендують у АсОН (5мл) розсолом, насиченим NaHCO3, водою і розсолом. і додають цинковий порошок (0,29г, 4,42ммоль). Органічний шар сушать (MgSO4) і концентрують Через 15хвил. реакція завершується. Реакційну під зниженим тиском, одержуючи 23мг (89%) чиссуміш розбавляють етилацетатом і фільтрують того бажаного продукту. MS APCI (+) m/z 455, 453 через Celite. Фільтрат промивають водою, насиче(М+ Вr-структура); MS APCI (-) m/z 453, 451 (М-Brним NHCO3 10%-м K2СО3 і розсолом. Органічний структура); 1Н Я МР (400МГц, ДМСО-d6) d 11,69 шар сушать (MgSO4) і концентрують під зниженим (шир. s, 1Η), 8,43 (s, 1Η), 7,62 (d, 1Η), 7,28 (dd, 1Η), тиском, одержуючи 0,13г (48%) чистого бажаного 6,42 (m, 1Η), 3,63 (d, 2H), 1,03 (m, 1Н), 0,48 (m, 2H), продукту як білувату коричневу піну. 0,19 (m, 2H); 19F ЯМР (376МГц, ДМСО-d 6)-132,95 Етап С: Метиловий естер 6-(2(s). хлорфеніламіно)-7-флуор-3Н-бензоімідазол-5Наведені далі сполуки одержують, як це було карбонової кислоти 7b описано у Приклад 1 і у Прикладі 9, застосовуючи Метиловий естер 4,5-діаміно-2-(2належні карбонові кислоти і належні гідроксиламіхлорфеніламіно)-3-флуорбензойної кислоти 6а ни: (0,125г, 0,404ммоль) суспендують у ЕtOН (2мл) і додають формамідинацетат(63мг, 0,605ммоль). Реакційну суміш гріють під зворотним холодильником. Через 16год. реакційну суміш охолоджують до кімнатної температури, і розбавляють етилацетатом. Органічний шар промивають водою, насиченим NaHCO3, 10%-м K2СО3 і розсолом. Органічний шар сушать (MgSO4) і концентрують під зниженим тиском, одержуючи 0,109г (85%) чистого бажаного продукту. Етап D: метиловий естер 6-(4-бром-2хлорфеніламіно)-7-флуор-3Н-бензоімідазол-5карбонової кислоти 8b Метиловий естер 6-(2-хлорфеніламіно)-7флуор-3Н-бензоімідазол-5-карбонової кислоти 7b (55мг, 0,172ммоль) розчиняють у 1:1 ТГФ:МеОН (2мл) і охолоджують до -78°С в атмосфері нітрогену. Додають TsOH·H2O (49мг, 0,258ммоль) і потім Приклад 10 NBS (31мг, 0,174ммоль). Через 10хвил. реакційну суміш доводять до 0°С і через 2год. - до кімнатної температури. Через 16год. реакційну суміш гасять доданням 10%-го Na2S2O3 і розбавляють етилаце 45 77765 46 зниженим тиском до одержання твердої речовини, перетирання якої з діетилетером дає 2,18г (90%) бажаного продукту як білуватої твердої речовини. MS ESI (+) m/z 483, 485 (М+ Br-стр уктура). Етап D: (2-гідроксиетокси)-амід 6-(4-бром-2хлорфеніламіно)-7-флуор-3-метил-3Нбензоімідазол-5-карбонової кислоти 29с (2-гідроксиетокси)-амід 6-(4-бром-2-хлорГідрохлорну кислоту (14мл, 1,0Μ водний розфеніламіно)-7-флуор-3-метил-3Н-бензоімідазол-5чин, 14ммоль) додають до суспензії 6-(4карбонової кислоти (29с) вінілоксиетокси)-аміду 29а бром-2Етап А. метиловий естер 6-(4-бром-2хлорфеніламіно)-7-флуор-3-метил-3Нхлорфеніламіно)-7-флуор-3-метил-3Нбензоімідазол-5-карбонової кислоти (2-(2,18г, бензоімідазол-5-карбонової кислоти 9а і метил4,50ммоль) в етанолі (50мл) і реакційну суміш заовий естер 6-(4-бром-2-хлорфеніламіно)-7-флуорлишають перемішуватись протягом 24год. Реак1-метил-1Н-бензоімідазол-5-карбонової кислоти ційну суміш концентрують до сухості роторним Розчин метилового естеру 6-(4-бром-2випарюванням і тверду речовину розділяють між хлорфеніламіно)-7-флуор-3Н-бензоімідазол-53:1 етил ацетат/ТГФ і насиченим карбонатом калію карбонової кислоти 8b (150мг, 0,38ммоль), іодомеВодну фаз у екстрагують 3:1 етилацетат/ТГФ (3х), тану (28мкл, 0,45ммоль) і карбонату калію (78мг, об'єднану органіку сушать (Na2SO4) і концентру0,56ммоль) у ДМФ (1,5мл) перемішують при 75°С ють, одержуючи 2,11г (100%) (2-гідроксиетокси)1год. Реакційну суміш розбавляють етилацетатом, аміду 6-(4-бром-2-хлорфеніламіно)-7-флуор-3промивають насиченим водним карбонатом калію метил-3Н-бензоімідазол-5-карбоновоі кислоти як (2х), розсолом і сушіть (Na2SO4). Колонна флешбілуватої твецдог речовини. MS ESI (+) m/z 457, хроматографія (20:1 метиленхлорид/етилацетат) 459 (М+, Br-структура). дає 56мг (36%) більш мобільного метилового ес1 Н ЯМР (400МГц, МеОН-d4) d 8,26 (s, 1H), 7,78 теру 9а 6-(4-бром-2-хлорфеніламіно)-7-флуор-3(s, 1H), 7,57 (d, 1H), 7,24 (dd, 1H), 6,40 (dd, 1Н), метил-3Н-бензоімідазол-5-карбонової кислоти як 3,86 (s, ЗН), 3,79 (m, 2Н), 3,49 (m, 2Н). 19F ЯМР білої твердої речовини. 19F ЯМР (376МГц, CD3OD) (376МГц, MeOH-d4) -133,68 (s). -133,5 (s). MS АРСІ (+) m/z 412, 414 (M+, BrПриклад 11 структура). Також одержують 54мг (35%) метилНаведені далі сполуки одержують, як це було ового естеру 6-(4-бром-2-хлорфеніламіно)-7описано у Прикладэ 10, з застосуванням метилфлуор-1-метил-1Н-бензоімідазол-5-карбонової овийого естеру 8b і належного алкілювального кислоти як білої твердої речовини. 19F ЯМР агента (Етап А) і належного гідроксиламіну (Етап (376МГц, CD3OD) -139,9 (s). MS АРСІ (+) m/z С): 412,414 (M+, Br-стр уктура). Етап В. 6-(4-бром-2-хлор-феніламіно)-7флуор-3-метил-3Н-бензоімідазол-5-карбонова кислота 10с Метиловий естер 6-(4-бром-2-хлорфеніламіно)-7-флуор-3-метил-3Н-бензоімідазол-5карбонової кислоти 9а (56мг, 0,14ммоль) розчиняють у 2:1 ТГФ/воді (3мл) і додають водний розчин NaOH (0,55мл, 1,0М, 0,55ммоль). Після двогодинного перемішування роторним випарюванням реакцію зменшують до 1/4 початкового об'єму і залишок розбавляють до 50мл водою. Водний розчин підкислюють до рН 2 доданням 1,0Μ водної НСІ і екстрагують 1:1 ТГФ/етилацетатом (3х), сушать (Na2SO4) і концентрують під зниженим тиском, одержуючи 43мг (79%) чистої карбонової кислоти як білуватої твердої речовини. MS ESI (+) m/z 397, 398 (М+, Br-структура). Етап С: (2-вінілоксиетокси)-амід 6-(4-бром-2хлорфеніламіно)-7-флуор-3-метил-3Нбензоімідазол-5-карбонової кислоти 29а 6-(4-бром-2-хлорфеніламіно)-7-флуор-3метил-3Н-бензоімідазол-5-карбонову кислоту 10с (2,00г, 5,0ммоль), О-(2-вінілоксиетил)гідроксиламін (0,776г, 7,5ммоль), HOBt (0,88г, 6,5ммоль), триетиламін (1,61мл, 2,3ммоль) і EDCI (1,3г, 6,5ммоль) розчиняють у ДМФ (52мл) і перемішують при кімнатній температурі протягом 48год. Реакційну суміш розбавляють етилацетатом, промивають водою (3х), насиченим карбонатом калію (2х), насиченим хлоридом амонію (2х), розсолом, сушать (Na2SO4) і концентрують під 47 77765 48 Приклад 12 (2,3-дигідроксипропокси)-амід 6-(4-бром-2хлорфеніламіно)-7-флуор-3-метил-3Нбензоімідазол-5-карбонової кислоти (29hhh) До розчину алілоксиаміду 6-(4-бром-2-хлорфеніламіно)-7-флуор-3-метил-3Н-бензоімідазол-5карбонової кислоти 29tt (20мг, 0,04ммоль) у 0,50мл 4:1 ТГФ/вода додають OsO4 (41мкл, 0,054М розчин у t-BuOH, 0,002ммоль) і потім NMO (7мг, 0,06ммоль). Розчин перемішують при кімнатній температурі 8год. і потім аналіз ВЕРХ показує повне перетворення у продукт. Розчин перемішують 49 77765 50 з насиченим NaHSO3 і розбавляють етилацетатом. належний гідроксиламін (Етап С). Органічну фаз у сушать (Na2SO4). Очи щення колонною флеш-хроматографією (DCM -> 20:1 DCM/MeOH) дає 16мг бажаного продукту як білуватої твердої речовини. MS ESI (+) m/z 487, 489 (М+, Br-стр уктура). Приклад 13 (3,4-дигідроксибутокси)-амід 6-(4-бром-2хлорфеніламіно)-7-флуор-3-метил-3Нбензоімідазол-5-карбонової кислоти (29ііі) Бут-3-енілоксиамід 6-(4-бром-2-хлорфеніламіно)-7-флуор-3-метил-3Н-бензо-імідазол5-карбонової кислоти 29uu піддають дигідроксилюванню методом, описаним у Прикладі 12. MS АРСІ (+) m/z 501, 503 (М+ Вг-структура). Приклад 14 Приклад 17 Наведені далі сполуки одержують, як це описано у Прикладі 10, застосовуючи метиловий естер 8с, належний алкілювальний агент (Етап А) і належний гідроксиламін (Етап С): Приклад 18 Наведені далі сполуки одержують, як це описано у Прикладі 10, застосовуючи метиловий естер 8d, належний алкілювальиий агент (Етап А), і належний гідроксиламін (Етап С): (2-мутиламіноетокси)-амід 6-(4-бром-2хлорфеніламіно)-7-флуор-3-метил-3Нбензоімідазол-5-карбонової кислоти ( сіль TFA, 29jjj) Одержують з (трет-бутилового естеру 2-{[6-(4бром-2-хлорфеніламіно)-7-флуор-3-метил-3Нбензоімідазол-5-карбоніл]-аміноокси}-етил)метилкарбамової кислоти 29ww зняттям захисту з трифлуооцтової кислоти у метиленхлориді. MS APCI (+) m/z 470, 472 (Mt, Вк-стр уктура); 1Н ЯМР (400МГц, CD3OD) d 8,31 (s, 1H), 7,74 (s, 1H), 7,51 (d, 1H), 7,19 (dd, 1H), 6,39 (dd, 1H), 4,11 (m, 2H), 3,97 (s, 3Н), 3,12 (m, 2H), 2,72 (s, 3H); 19F ЯМР (376МГц, CD3OD) -77,41 (s, 3F), -134,79 (s, 1F). Приклад 15 Наведені далі сполуки одержують, як це описано у Прикладі 10, застосовуючи метиловий естер 8а, належний алкілювальний агент (Етап А) і належний гідроксиламін (Етап С): Приклад 16 Наведені далі сполуки одержують, як це описано у Прикладі 10, застосовуючи метиловий естер 8е, належний алюлювальний агент (Етап Α) і Приклад 19 Цикпопропілметоксиамід 6-(4-бром-2метилфеніламіно)-7-флуор-3-[4-(4-метилпіперазин-1-іл)-бутил]-3Н-бензоімідазол-5карбонової кислоти (11о) Етап А: метиловий естер 6-(4-бром-2метилфеніламіно)-7-флуор-3-пент-4-еніл-3Нбензоімідазол-5-карбонової кислоти 9b Метиловий естер 7-флуор-6-(4-бром-2метилфеніламіно)-1Н-бензоімідазол-5-карбонової кислоти 8а (0,915г, 2,419ммоль) суспендують у ДМФ (18мл) в атмосфері нітрогену. Додають бромпентен (0,430мл, 3,629ммоль) і K2СО3 (0,502г, 3,629ммоль) і реакційну суміш нагрівають до 80°С. Через 1год. реакційну суміш охолоджують до кімнатної температури і вливають у 100мл 1:1 етилацетат:діетилетеру. Органічний шар промивають водою і розсолом, сушать (Na2SO4) і концентрують під зниженим тиском N3 і N1 алкіловані продукти розділяють колонною флеш-хроматографією, 51 77765 52 елююючи 20:1 метиленхлорид:етилацетатом. По2-метилфеніламіно)-3-(4,5-дигідроксипентил)-7вне розділення ізомерів здійснюють двома хромафлуор-3Н-бензоімідазол-5-карбонової кислоти тографічними розділеннями. Продукт з вищим Rf є 11m (0,244г, 0,456ммоль), ТГФ (5мл) і фосфатного N3-продуктом 9b, а продукт з нижчим Rf є N1буфера з рН 7 (3мл) додають періодат натрію продуктом. Вихід N3-продукту 9b - 0,415г (38%). (0,195г, 0,911ммоль). Через 16год. реакційну суміш LC/MS ESI (+) m/z 448, 446 (M+1 Br-стр уктура) розбавляють етилацетатом і промивають NaHCO3 Вихід N1-продукту - 0,486г (45%) LC/MS ESI (+) m/z і розсолом. Органічний шар сушать (Na2SO4) і кон448,446 (M+1 Вr-стр уктура). центрують під зниженим тиском, одержуючи оранЕтап В: 6-(4-бром-2-метилфеніламіно)-7жеву тверду речовину. Очи щення колонною флуор-3-пент-4-еніл-3Н-бензоімідазол-5флеш-хроматографією з елюентом 4:1 метиленкарбонова кислота 10d хлорид:МеОН дає 0,189г (82%) чистого бажаного Метиловий естер 6-(4-бром-2продукту як жовту тверду речовину: MS АРСІ (+) метилфеніламіно)-7-флуор-3-пент-4-еніл-3Нm/z 505, 503 (М+1 Вr-стр уктура); MS APCI (-) m/z бензоімідазол-5-карбонової кислоти 9b розчиня503, 501 (М-І Вr-стр уктура). ють у 1:1 ТГФ:МеОН (10мл) і додають розчин 1N Етап F. циклопропілметоксиамід 6-(4-бром-2МаОН (2,3мл). Через 5год. органічні розчинники метилфеніламіно)-7-флуор-3-[4-(4видаляють під зниженим тиском і залишок розбавметилпіперазин-1-іл)-бутил]-3Н-бензоімідазол-5ляють водою і 100мл 1:1 ТГФ:етилацетат. Шари карбонової кислоти 11о розділяють і водний шар екстрагують етилацетаЦиклопропілметоксиамід 6-(4-бром-2том. Об'єднані органічні екстракти сушать метилфеніламіно)-7-флуор-3-(4-оксобутил)-3Н(Na2SO4) і концентрують під зниженим і тиском, бензоімідазол-5-карбонової кислоти 11n (15мг, одержуючи 0,35г (100%) чистого бажаного продук0,030моль) розчиняють у MeCN (500мкл) і додають ту як світложовту тверду речовину. метилпіпераіим (10мкл, 0,089ммоль) і потім АсОН Етап С: циклопропілметоксиамід 6-(4-бром-2(5мкл, 0,089ммоль) Через 5хвил. додають триацеметилфеніламіно)-7-флуор-3-пент-4-еніл-3Нтоксиборгідрид тетраметиламонію (12мг, бензоімідазол-5-карбонової кислоти 11f 0,045ммоль) Через 5хвил. реакційну суміш розба6-(4-бром-2-метилфеніламіно)-7-флуор-3вляють етилацетатом і промивають NaHCO3 і розпент-4-еніл-3Н-бензоімідазол-5-карбонову кислоту солом. Органічний шар сушать (Na2SO4) і концент10d (0,390г, 0,902ммоль) розчиняють у 1:1 рують під зниженим тиском, одержуючи 12мг ТГФ:метиленхлориді (6мл) і додають основу Гуніга (69%) чистого бажаного продукту як білу тверду (0,346мл, 1,985ммоль) і потім РуВОР (0,563г, речовину MS АРСІ (-) m/z 587, 585 (М-І Вr1,083ммоль). Через 10хвил. додають циклопропіструктура), 1Н ЯМР (400МГц, CDCI3) d 7,99 (s, 1H), лметилгідроксиламінгідрохлорид (0,134г, 7,98 (s, 1H), 7,30 (d, 1H), 7,08 (dd, 1H), 6,30 (d, 1H), 1,083ммоль). Через 16год. реакційну суміш розба6,1 (шир. синглет, 1Н), 4,26 (t, 2H), 3,64 (d, 2H), вляють етилацетатом і промивають 0,1N НСІ, на3,37 (s, 1H), 2,45 (шир. d, 8H), 2,41 (s, 3H), 2,38 (t, сиченим NaHCO3 і розсолом. Органічний шар су2Н), 2,28 (s, 3Н), 1,95 (квін., 2Н), 1,55 (квін., 2Н), шать (Na2SO4) і концентрують під зниженим 0,98 (m, 1H), 0,50 (qt, 2H), 0,22 (qt, 2H.) тиском. Сирий жовтий залишок очищають колонПриклад 20 ною флеш-хроматографією, елююючи етилацетаНаведені далі сполуки одержують, як це опитом, і одержують 0,315г (70%) чистого бажаного сано у Прикладі 19 by, застосовуючи бензоімідапродукту як жовту тверду речовину: MS APCI (+) зол, заміщений належним алкенілом, і належний m/z 503, 501 (М+1 Вr-стр уктура). амін у відновлювальному амінуванні (Етап F): Етап D: циклопропілметоксиамід 6-(4-бром-2метилфеніламіно)-3-(4,5-дигідроксипентил)-7флуор-3Н-бензоімідазол-5-карбонової кислоти 11m Циклопропілметоксиамід 6-(4-бром-2метилфеніламіно)-7-флуор-3-пент-4-еніл-3Нбензоімідазол-5-карбонової кислоти 11f (0,307г, 0,612ммоль) розчиняють у 4:1 ТГФ/вода (8мл) і додають розчин 1,134мл (0,061ммоль) 0,054М OsO4 у t-BuOH і потім NMO (0,093г, 0,796ммоль). Через 5год. реакційну суміш гасять доданням 10%го розчину NaHS2O3. Через 10хвил. реакційну суміш фільтрують через Celite, промиваючи етилацетатом і метиленхлоридом. Фільтрат розбавляють етилацетатом і промивають 0,01N НСІ і розсолом. Органічний шар сушать (Na2SO4) і концентрують під зниженим тиском. Сирий продукт очищають колонною флеш-хроматографією з елюентом 9:1 етилацетат:МеОН, одержуючи 0,244г (74%) чистого бажаного продукту. Етап Е: циклопропілметоксиамід 6-(4-бром-2метилфеніламіно)-7-флуор-3-(4-оксобутил)-3Нбензоімідазол-5-карбонової кислоти 11n До суміші циклопропілметоксиаміду 6-(4-бром 53 77765 54 тіоморфолін-4-іл)-бутил]-7-флуор-3Нбензоімідазол-5-карбонової кислоти (18сс) До розчину циклопропілметоксиамід 6-(4бром-2-метилфеніламіно)-7-флуор-3-(4тioморфолін-4-іл-бутил)-3Н-бензоімідазол-5карбонової кислоти 181 (8мг, 0,014ммоль) у 1:1:1 вода/ацетон/МеОН (1мл) додають NMO (1,6мг, 0,014ммоль) і тетроксид осмію (250мкл, 0,054М розчин у t-BuOH, 0,014ммоль). Після перемішування протягом 24год. розчин розбавляють насиченим тіосульфатом натрію, перемішують протягом 10хвил. і розбавляють етилацетатом. Розчин промивають розсолом (2х), сушать (Na2SO4) і концентрують під зниженим тиском до сірої твердої речовини, колонною флеш-хроматографією (10:1 дихлорметан/метанол) дає 6мг (71%) бажаного продукту як білувату тверду речовину. MS ESI (+) m/z 622, 624 (М+, Br-стр уктура). Πриклад 22 Приклад 21 Циклопропілметоксиамід 6-(4-6ром-2метилфеніламіно)-3-[4-(1,1-діоксо-1l6 Циклопропілметоксиамід 6-(4-бром-2хлорфеніламіно)-7-флуор-3-[4-(4-метил-піперазин1-іл)-бутил]-3Н-бензоімідазол-5-карбонової кислоти (18dd) Розчин циклопропілметоксиаміду 6-(4-бром-2хлорфеніламіно)-3-(4-хлорбутил)-7-флуор-3Нбензоімідазол-5-карбонової кислоти 18ее (10мг, 0,018ммоль), іодиду натрію (14мг, 0,092ммоль) і 1метилпіперазину (10мкл, 0,092ммоль) перемішують при 85°С 3год. Реакційну суміш розбавляють етилацетатом і промивають тричі водою, двічі насиченим водним карбонатом калію, сушать (Na2SO4) і концентрують під зниженим тиском до жовтого масла. Колонна флеш-хроматографія (1:1 дихлорметан/метанол, потім метанол, потім 20:1 метанол/триетиланілін) дає чистий продукт (8мг, 72%) як білувату піну. MS ESI (+) m/z 607, 609 (М+, Br-структура). 1Н ЯМР (400МГц, ДMCO-d 6) d 8,37 (s, 1H), 7,71 (s, 1Н), 7,49 (d, 1H), 7,18 (dd, 1H), 6,40 (dd, 1H), 4,38 (t, 2H), 3,62 (d, 2H), 2,45 (шир. d, 8H), 2,41 (t, 2H), 2,28 (s, ЗН), 1,96 (m, 2H), 1,54 (m, 2H), 1,07 (m, 1H), 0,50 (d,2H), 0,22 (d,2H). Приклад 23 Наведені далі сполуки одержують, як це було описано у Прикладі 22, застосовуючи належний амін і первинний алкіл хлорид 55 77765 56 Циклопропілметоксиамід 6-(4-хлор-2метилфеніламіно)-7-флуор-3-оксазол-5-ілметил3Н-бензоїмідазол-о-карбонової кислоти (18ggg) Циклопропілметоксиамід 6-(4-хлор-2метилфеніламіно)-7-флуор-3-(2-оксоетил)-3Нбензоімідазол-5-карбонової кислоти (0,020г, 0,046ммоль) розчиняють у метанолі (2мл) Додають карбонат калію (0,013г, 0,093ммоль) і 1ізоціанометансульфоніл-4-метилбензол (0,010г, 0,051ммоль), реакційну суміш перемішують під зворотним холодильником протягом 16год. під N2, потім концентрують під зниженим тиском. Залишок розчиняють в етилацетаті, вливають у сепараторну воронку і промивають водою і розсолом. Об'єднані водні шари екстрагують етилацетатом (2х). Об'єднані етилацетатні шари сушать (Na2SO4) і концентрують під зниженим тиском. Одержану тверду речовину очи щають колонною флешхроматографією (елюент - 15:1 метиленхлорид:метанол) і одержують 0,011г (50%) бажаного продукту. MS АРСІ (+) m/z 470, 472 (М+, СІструктура), 1Н ЯМР (400МГц, CDCI3) d 10,51 (br s, 1H), 8,07 (s, 1H), 8,02 (s, 1H), 7,89 (s, 1H), 7,23 (s, 1H), 7,15 (d, 1H), 6,92 (dd, 1H), 6,31 (d, 1H), 6,11 (br s, 1H), 5,45 (s, 2H), 3,62 (d, 2H), 2,40 (s, 3H), 0,87 (m, 1H), 0,49 (m, 2H), 0,20 (m, 2H). 19F ЯМР (376МГц, CDCI3) -134,54 (s). Приклад 25 Приклад 24 Циклопропілметоксиамід 6-(4-бром-2хлорфеніламіно)-7-флуор-3-(3-оксо-3-піролідин-1іл-пропіл)-3Н-бензоімідазол-5-карбонової кислоти (18hhh) Етап А: метиловий естер 6-(4-бром-2хлорфеніламіно)-3-(2-трет-бутоксикарбонілетил)7-флуор-3Н-бензоімідазол-5-карбонової кислоти Метиловий естер 6-(4-бром-2-хлорфеніламіно)-7-флуор-3Н-бензоімідазол-5карбоновоі кислоти 8b (0,50г, 1,25ммоль) розчиняють у ДМФ (8мл) під Ν2 і додають K2СО3 (0,26г, 1,88ммоль) і потім t-бутилакрилат (1,84мл, 12,54ммоль). Реакційну суміш нагрівають до 90°С з перемішуванням. Через 4год. реакційну суміш охолоджують до кімнатної температури і розбавляють етилацетатом. Органічний шар промивають водою (3х) і розсолом, сушать (MgSO 4) і концентрують під зниженим тиском. Очищення колонною флеш-хроматографією з елюентом 19:1 метиленхлорид:етилацетат дає 0,41г (62%) бажаного продукту. Етап В: Метиловий естер 6-(4-бром-2 57 77765 58 хлорфеніламіно)-3 (2-карбоксиетил)-7-флуор-3ННаведені далі сполуки одержують, як це опибензоімідазол-5-карбонової кислоти, сіль ΤFA сано у Прикладі 25, застосовуючи метиловий есМетиловий естер 6-(4-бром-2тер 8b і відповідні аміни: хлорфеніламіно)-3-(2-трет-бутоксикарбонілєтил)-7флуор-3Н-бензоімідазол-5-карбонової кислоти: (0,50г, 0,095ммоль) розчиняють у метиленхлориді (0,5мл) і додають TFA (0,5мл). Через 45хвил. реакційну суміш концентрують до сухості, одержуючи 0,49г (88%) бажаного продукту: LC/MS ESI (+) m/z 472,470 (М+ Вr-структура); 1Н Я МР (400МГц, ДMCO-d6) d 8,51 (s, 1Н), 8,20 (s, 1 Η), 8,13 (s, 1H), 7,64 (d, 1H), 7,29 (dd, 1H), 6,45 (dd, 1H), 4,55 (t, 2H), 2,89 (t, 2H). Приклад 27 Етап С: метиловий естер 6-(4-бром-2хлорфеніламіно)-7-флуор-3-(3-оксо-3-піролідин-1ілпропіл)-3Н-бензоімідазол-5-карбонової кислоти До розчину метилового естеру 6-(4-бром-2хлорфеніламіно)-3-(2-карбоксиетил)-7-флуор-3Нбензоімідазол-5-карбонової кислоти (60мг, 0,13ммоль) у ДМФ (1,8мл) додають HOBt-H2O (24мг, 0,16ммоль), Et3N (0,043мл, 0,31ммоль), піролідин (0,011мл, 0,13ммоль) і EDCI (34мг, 0,18ммоль) при кімнатній температурі. Одержаний (2-гідроксиетокси)-амід 6-(4-бром-2жовтий розчин перемішують 16год. при кімнатній хлорфеніламіно)-7-флуор-3-(тетрагідропіран-2температурі. Реакційну суміш розбавляють EtOAc і ілметил)-3Н-бензоімідазол-5-карбонової кислоти водою, промивають насиченим водним NFLiCI, (11p) розсолом, насиченим водним NaHCO3 і розсолом. Етап А: 6-(4-бром-2-хлорфеніламіно)-7-флуорОрганічний шар сушать над MgSO 4, фільтр ують і 3-(тетрагідропіран-2-ілметил)-3Н-бензоімідазол-5концентрують у вакуумі, одержуючи сирий матерікарбонової кислоти метиловий естер 11q ал, який очищають флеш-хроматографією (3% Метиловий естер 6-(4-бром-2МеОН у СН2СІ2), одержуючи 45мг (67%) бажаного хлорфеніламіно)-7-флуор-3Н-бензоімідазол-5продукту: MS АРСІ (+) m/z 523, 525 (М+, Вrкарбонової кислоти 8b (0,25г, 0,63ммоль) розчиструктура). няють у Ν,Ν-ДМФ (5мл). Додають 2Етап D: 6-(4-бром-2-хлорфеніламіно)-7-флуорбромметилтетрагідропіран (0,34г, 1,88ммоль) і 3-(3-оксо-3-піролідин-1-ілпропіл)-3Нкарбонат калію (0,26г, 1,88ммоль) і реакційну субензоімідазол-5-карбонова кислота міш перемішують при 60°С протягом 12год. під N 2. До розчину метилового естеру 6-(4-бром-2Реакційну суміш вливають у сепараторну ворснку, хлорфеніламіно)-7-флуор-3-(3-оксо-3-піролідин-1розбавляють етилацетатом і водою і шари роздііл-пропіл)-3Н-бензоімідазол-5-карбонової кислоти ляють Етилаце-татний шар промивають водою і (41мг, 0,079ммоль) у ТГФ/Н2О (1,5мл/0,75мл) дорозсолом, сушать (Na2SO4) і концентрують під дають 0,20мл (0,20ммоль) 1N водн. LiOH при кімзниженим тиском Одержану тверду речовину пенатній температурі. Одержаний розчин перемішуретирають з діетилетером, одержуючи блідожовту ють 16год. Реакційну суміш підкислюють доданням тверду речовину (N3 регіоізомер - ЯМР) і жовтий 1N водної НСІ (рН прибл. 2-3) і розбавляють фільтрат (суміш N1 і N3 регіоізомерів - ЯМР) ТвеEtOAc. Органічний шар суша ть над MgSO4 , фільтрду речовину збирають і промивають діетилетерують і концентрують у вакуумі, одержуючи сирий ром, одержуючи 0,12г (37%) чистого бажаного N3 продукт (42мг), який використовують без очищенрегіоізомерного продукту як блідожовту тверду ня. речовину. MS ESI (+) m/z 496,498 (М+, BrЕтап Е: циклопропілметоксиамід 6-(4-бром-2структура). хлорфеніламіно)-7-флуор-3-(3-оксо-3-піролідин-1Етап В: 6-(4-бром-2-хлорфентаміно)-7-флуорілпропіл)-3Н-бензоімідазол-5-карбонової кислоти 3-(тетрагідропіран-2ілметил)-3Н-бензоімідазол-518hhh карбонова кислота 11r Цю сполуку приготовляють з 6-(4-бром-2Метиловий естер 6-(4-бром-2-хлорхлорфеніламіно)-7-флуор-3-(3-оксо-3-піролідин-1феніламіно)-7-флуор-3-(тетрагідропіран-2іл-пропіл)-3Н-бензоімідазол-5-карбонової кислоти і ілметил)-3Н-бензоімідазол-5-карбоновоі кислоти О-циклопропілметилгідроксиламінгідрохлорид за 11q суспендують у 4:1 ТГФ/воді (2,5мл) і додають процедурою стандартного сполучення, описаною у водний 1М LiCH (2,5мл)ю Після 16-годинного пеЕтапі А. MS АРСІ (+) m/z 578, 580 (М+, Brремішування при кімнатній температурі реакційна 1 структура); Н Я МР (400МГц, ДMCO-d 6) d 11,66 (s, суміш стає гомогенною і реакція завершується. 1H), 8,42 (s, 1H), 8,01 (s, 1H), 7,76 (s, 1H), 7,62 (s, Реакційну суміш охолоджують до 0°С, розбавля1H), 7,28 (d, 1H), 6,39 (m, 1H), 4,52 (t, 2H), 3,66 (d ють водою і краплями додають водну 2М НС до 2Н), 3,33 (t, 2Н), 3,28 (t, 2Н), 2,89 (t, 2Н), 1,83 (m, досягнення рН 1-2, внаслідок чого вона перетво2Н), 1,76 (m, 2Н), 1,06 (m, 1Н), 0,49 (m, 2Н), 0,22 рюється у суспензію. Реакційну суміш вливають у 19 (m, 2Н); F ЯМР (376МГц, ДMCO-d6) -132-,94 (s, сепараторну воронку і розбавляють етилацета1F). том/ТГФ і водою і шари розділяють Водний шар Приклад 26 59 77765 60 екстрагують етилацетатом, об'єднані органічні шари промивають розсолом, сушать (Na2SO4) і концентрують під зниженим тиском, одержуючи 0,11г (100%) чистого бажаного продукту як білої твердої речовини. MS ESI (+) m/z 482,484 (М+, Brструктура). Етап С. (2-вінілоксиетокси)-амід 6-(4-бром-2хлорфеніламіно)-7-флуор-3-(тетрагідропіран-2ілметил)-3Н-бензоімідазол-5-карбонової кислоти 11s 6-(4-бром-2-хлор-феніламіно)-7-флуор-3(тетрагідропіран-2-ілметил)-3Н-бензо-імідазол-5карбонову кислоту 11г (0,11г, 0,23ммоль) розчиняють у Ν,Ν-ДМФ (2мл) Додають НОВТ (0,037г, 0,27ммоль) і триетиламін (0,094мл, 0,68ммоль). Додають О-(2-вінілоксиетил)-гідроксиламін (0,028г, 0,27ммоль) і EDCI (0,056г, 0,29ммоль) і реакційну суміш перемішують при кімнатній температурі під N2 до завершення реакції (ВЕРХ) (2-3 дні). РеакПриклад 29 ційну суміш вливають у сепараторну воронку, розбавляють етилацетатом і водою і шари розділяють. Етилацетатний шар промивають послідовно водним насиченим NH 4CI (2x), розсоло'м, водним насиченим бікарбонатом натрію (2х), водою і розсолом, сушать (Na2SO4) і концентрують під зниженим тиском. Одержану тверду речовину очи щають колонною флеш-хроматографією (елюент - 15:1 метиленхлорид:метанол), одержуючи 0,039г (79%) Циклопрoпілметоксиамід 6-(4-бром-2чистого бажаного продукту як білувату тверду рехлорфеніламіно)-7-флуор-3-(2-метанчовину. MS ESI (+) m/z 567, 569 (М+, Br-структура). сульфонілетил)-3Н-бензоімідазол-5-карбонової Етап D: (2-гідроксиетокси)-амід 6-(4-бром-2кислоти (11bb) хлорфеніламіно)-7-флуор-3-(тетрагідропіран-2Етап А: метиловий естер 6-(4-бром-2ілметил)-3Н-бензоімідазол-5-карбонової кислоти хлорфеніламіно)-7-флуор-3-(211р метансульфонілетил)-3Н-бензоімідазол-5(2-вінілокси-етокси)-амід 6-(4-бром-2карбонової кислоти 11се хлорфеніламіно)-7-флуор-3-(тетрагідро-піран-2Метиловий естер 6-(4-бром-2ілметил)-3Н-бензоімідазол-5-карбонової кислоти хлорфеніламіно)-7-флуор-3Н-бензоімідазол-511s (0,039г, 0,068ммоль) розчиняють в етанолі карбонової кислоти 8b (1,55г, 3,89ммоль) розчи(2мл) і додають водну 2М НСІ (200мкл). Реакційну няють у 15мл ДМФ під N2. Додають K2СО3 (0,70г, суміш перемішують при кімнатній температурі про5,06ммоль) і потім метилвінілсульфон (0,41мл, тягом 30хвил., потім розбавляють зодою, нейтра4,67ммоль). Після 16-годинного перемішування лізують водним 2М NaOH (прибл. 200мкл) до рН 7 при кімнатній температурі реакційну суміш розбаі концентрують під зниженим тиском Залишок розвляють етилацетатом і водою. Шари розділяють і діляють між етилацетат і розсолом у сепараторній органічний шар промивають водою (3х) і розсоворонці і шари розділяють Етилацетатний шар лом. Об'єднані водні змивки екстрагують етилацесушать (Na2SO4) і концентрують під зниженим тистатом, об'єднані органічні екстракти сушать ком, одержуючи 0,034г (91%) чистого бажаного (MgSO4) і концентрують під зниженим тиском. Бапродукту як білувату тверду речовину MS ESI (+) гаторазове очищення розчиненням залишку у ме1 m/z 541, 543 (М+, Br-стр уктура), Н ЯМР (400МГц, тиленхлориді і осадження діетилетером дає 1,16г CD3OD) d 8,29 (s, 1H), 7,75 (s, 1H), 7,49 (d, 1H), (59%) чистого бажаного продукт як жовту тверду 7,18 (dd, 1Η), 6,40 (dd, 1Η), 4,40 (dd, А АВХречовину MS АРСІ (+) m/z 506, 504 (М+ Br pattern) і структури, 1Н), 4,28 (dd, В АВХ-структури, 1Н), 400, 398 (Μ - метилетилсульфоне-Вr-структура). 3,92 (m, X АВХ-стр уктури, 1Η), 3,66 (t, 2Н), 3,35 (m, Етап В: циклопропілметоксиамід 6-(4-бром-21Н) 1,89 (m, 1Н) 1,76 (m, 1Н) 2,28 (s, 3Н), 1,54 (m, хлорфеніламіно)-7-флуор-3-(219 3Н), 1,30 (m, 1Н). F ЯМР (376МГц, CD3OD) метансульфонілетил)-3Н-бензоімідазол-5134,87 (s). карбонової кислоти 11bb Приклад 28 Метиловий естер 6-(4-бром-2Наведені далі сполуки одержують, як було хлорфеніламіно)-7-флуор-3-(2-метансульфонілописано у Прикладі 27 застосовуючи належний етил)-3Н-бензоімідазол-5-дарбонової кислоти 11сс метиловий естер і алкіілювальний агент (Етап Α) і обробляють, як було описано, і одержують циклоналежний гідроксиламін (Етап С). пропілметоксиамід 6-(4-бром-2-хлорфеніламіно)-7флуор-3-(2-метансульфоніл-етил)-3Нбензоімідазол-5-карбонової кислоти : MS АРСІ (+) m/z 561, 559 (М+ Вr-стр уктура) і MS АРСІ (-) m/z 559, 557 (Μ- Br-структура); 1Н ЯМР (400МГц, ДMCO-d6) d 11,75 (s, 1H), 8,47 (s, 1H), 8,04 (s, 1H),
ДивитисяДодаткова інформація
Назва патенту англійськоюN3 alkylated derivatives of benzimidazole as mek inhibitors
Автори англійськоюLYSSIKATOS JOSEPH P., Marlow Allison L.
Назва патенту російськоюN3 алкилированные производные бензимидазола как ингибиторы мэк
Автори російськоюЛиссикатос Джозеф П., Марлоу Эллисон Л.
МПК / Мітки
МПК: A61K 31/4245, A61P 17/04, A61P 1/00, A61P 35/00, C07D 401/12, C07D 417/06, A61P 3/10, A61P 27/02, A61K 31/454, A61K 31/427, A61K 31/4439, C07D 413/04, A61P 9/10, C07D 417/12, A61P 17/00, A61K 31/541, A61K 31/4184, A61P 9/08, C07D 401/06, C07D 235/08, A61P 43/00, A61K 31/496, A61P 19/02, A61P 29/00, C07D 405/06, A61P 1/18, A61K 31/422, A61K 31/5377, C07D 403/04, C07D 413/06, A61P 13/12, A61P 17/06, A61P 13/08, C07D 235/06
Мітки: алкіловані, інгібітори, мек, похідні, бензимідазолу
Код посилання
<a href="https://ua.patents.su/40-77765-n3-alkilovani-pokhidni-benzimidazolu-yak-ingibitori-mek.html" target="_blank" rel="follow" title="База патентів України">N3 алкіловані похідні бензимідазолу як інгібітори мек</a>
Попередній патент: Спосіб прискорення випробувань виробів на старіння
Наступний патент: Пристрій для зміни напряму смуги у змотувальному пристрої
Випадковий патент: Спосіб застосування органо-мінерального добрива із шламу хімводопідготовки тец












