Застосування сполук порфірину
Номер патенту: 94027
Опубліковано: 11.04.2011
Автори: Лав Уільям Г., Ріс-Уільямс Уільям, Брандіш Дерек
Формула / Реферат
1. Застосування сполуки формули І або II, наведеної нижче, у приготуванні лікарського засобу для знищення або атенуації росту мікроорганізмів способом, який включає використання власної антимікробної активності цієї сполуки,
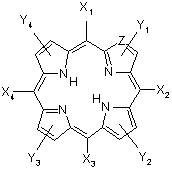 , I
, I 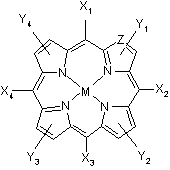 , II
, II
де:
Х1, Х2, Х3 та Х4 незалежно позначають атом водню, ліпофільну частину молекули, фенільну групу, нижчу алкільну, алкарильну чи аралкільну групу або катіонну групу такої формули:
-L-R1-N+(R2)(R3)R4,
де:
L означає з'єднувальну (лінкерну) частину молекули або відсутній;
R1 означає нижчий алкілен, нижчий алкенілен або нижчий алкінілен, який необов'язково заміщений одним чи декількома замісниками, вибраними з нижчого алкілу, нижчого алкілену (необов'язково перериваного киснем), фтору, OR5, C(O)R6, C(O)OR7, C(O)NR8R9, NR10R11 та N+R12R13R14; і
R2, R3 та R4 незалежно означають Н, арил, нижчий алкіл, нижчий алкеніл або нижчий алкініл, останні три з яких необов'язково заміщені одним або декількома замісниками, вибраними з нижчого алкілу, нижчого алкілену (необов'язково перериваного киснем), арилу, OR5, C(O)R6, C(O)OR7, C(O)NR8R9, NR10R11 та N+R12R13R14;
Z означає -СН або N;
Y1, Y2, Y3 та Y4 відсутні або незалежно означають арил, нижчий алкіл, нижчий алкеніл або нижчий алкініл, останні три з яких необов'язково заміщені одним або декількома замісниками, вибраними з нижчого алкілу, нижчого алкілену (необов'язково перериваного киснем), арилу, OR5, C(O)R6, C(O)OR7, C(O)NR8R9, NR10R11, N+R12R13R14, або, узяті разом з пірольним кільцем, до якого вони приєднані, можуть утворювати циклічну групу; і
R5, R6, R7, R8, R9, R10, R11, R12, R13 та R14 незалежно означають Н або нижчий алкіл;
М означає елемент металу або металоїду;
за умови, що щонайменше один з Х1, Х2, Х3 та Х4 є катіонною групою, визначеною вище, і щонайменше один з Х1, Х2, Х3 та Х4 означає атом водню, фенільну групу, ліпофільну частину молекули або нижчу алкільну, алкарильну чи аралкільну групу.
2. Застосування за п. 1, де М означає двовалентний або тривалентний металевий елемент.
3. Застосування за п. 2, де М вибраний з Zn(II), Cu(II), La(III), Lu(III), Y(III), In(III), Cd(II), Mg(II), Al(III), Ru, Ni(II), Mn(III), Fe(III) і Pd(II).
4. Застосування за п. 1, де М означає металоїдний елемент, наприклад, кремній (Si) або германій (Ge).
5. Застосування за п.1, де Y1, Y2, Y3 та Y4 відсутні.
6. Застосування за п. 1, де Z означає -СН.
7. Застосування за п. 1, де R1 означає незаміщену нижчу алкіленову, нижчу алкеніленову або нижчу алкініленову групу.
8. Застосування за п. 7, де R1 означає -(СН2)m- і "m" дорівнює цілому числу 1-20.
9. Застосування за п. 8, де "m" дорівнює цілому числу 1-10, наприклад 1-6, 1-5, 1-4 або 1-3.
10. Застосування за п. 9, де "m" дорівнює 3.
11. Застосування за п. 1, де R2, R3 та/або R4 означають нижчу алкільну, нижчу алкенільну або нижчу алкінільну групи.
12. Застосування за п. 11, де R2, R3 та/або R4 означають незаміщені нижчі алкільні групи.
13. Застосування за п. 12, де щонайменше один з R2, R3 та R4 означає алкільну групу, заміщену первинною, вторинною або третинною аміногрупою або четвертинною амонієвою групою.
14. Застосування за п. 1, де R1 означає -(СН2)3-, R2 та R3 означають СН3 і R4 означає -(CH2)3-N(CH3)2.
15. Застосування за п. 1, де R1 означає -(СН2)3- і R2, R3 та R4 означають, кожен, СН3.
16. Застосування за п. 1, де R1 означає -(СН2)3- і R2, R3 та R4 означають, кожний, C2H5.
17. Застосування за п. 1, де L вибраний з групи, що складається зі з'єднувальних груп фенокси, фенілену, сульфоніламідо, аміносульфонілу, сульфоніліміно, фенілсульфоніламідо, феніламіносульфонілу, сечовини, уретану та карбамату.
18. Застосування за п. 17, де Х1, Х2, Х3 та/або Х4 означають:
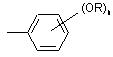 ,
,
де R означає R1-N+(R2)(R3)R4, як визначено в п. 1, і "n" дорівнює цілому числу 1-3.
19. Застосування за п. 17, де Х1, Х2, Х3 та/або Х4 означають:
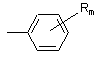 ,
,
де R означає R1-N+(R2)(R3)R4, як визначено в п. 1, і "m" дорівнює цілому числу 1-3.
20. Застосування за п. 17, де Х1, Х2, Х3 та Х4 означають:
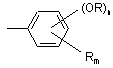 ,
,
де кожен R незалежно означає R1-N+(R2)(R3)R4, як визначено в п. 1, і "n" та "m" дорівнюють цілим числам 1-3, і де сума "n+m" дорівнює цілому числу 1-3.
21. Застосування за будь-яким з пп. 18-20, де "n" або "m" дорівнює 3.
22. Застосування за будь-яким з пп. 18-20, де "n" або "m" дорівнює 2.
23. Застосування за будь-яким з пп. 18-20, де "n" та/або "m" дорівнює 1.
24. Застосування за будь-яким з пп. 18-20, де L є монозаміщеним у пара-положенні.
25. Застосування за будь-яким з пп. 18-20, де L є монозаміщеним або дизаміщеним у мета-положенні (мета-положеннях).
26. Застосування за будь-яким з пп. 18-20, де L є монозаміщеним або дизаміщеним в орто-положенні (орто-положеннях).
27. Застосування за п. 1, де ця сполука включає дві катіонні групи, як визначено в п. 1, з протилежних боків порфіринового кільця, тобто, в положеннях кільця 5 та 15 або положеннях кільця 10 та 20.
28. Застосування за п. 27, де Х1 та Х3 є атомом водню, ліпофільною групою, фенільною групою, нижчою алкільною, алкарильною або аралкільною групою, а Х2 та Х4 є катіонними групами, або навпаки.
29. Застосування за п. 1, де ця сполука може містити дві катіонні групи, як визначено в п. 1, на сусідніх положеннях порфіринового кільця, тобто, в положеннях кільця 5 та 10 або положеннях кільця 10 та 15, або положеннях кільця 15 та 20, або положеннях кільця 20 та 5.
30. Застосування за п. 29, де Х1 та Х2 означають водень, а Х3 та Х4 означають катіонні групи, або Х2 та Х3 означають водень, а Х4 та Х1 означають катіонні групи.
31. Застосування за п. 1, де щонайменше один з Х1, Х2, Х3 та Х4 означає ліпофільну частину молекули.
32. Застосування за п. 31, де ця ліпофільна частина молекули є насиченою алкільною групою з розгалуженим ланцюгом формули -(СН2)pСН3, де "р" дорівнює цілому числу 1-22.
33. Застосування за п. 32, де "р" дорівнює 1-18, наприклад 2-16 або 4-12.
34. Застосування за п. 1, де жоден з Х1, Х2, Х3 та Х4 не є ліпофільною частиною молекули.
35. Застосування за п. 1, де жоден з Х1, Х2, Х3 та Х4 не є фенільною групою.
36. Застосування за п. 1, де ця сполука є водорозчинною.
37. Застосування за п. 1, де цією сполукою є дихлорид 5,15-біс-(4-{3-[(3-диметиламінопропіл)диметиламоніо]пропілокси}феніл)порфірину.
38. Застосування за п. 1, де цією сполукою є дихлорид 5,15-біс-[4-(3-триетиламоніопропілокси)феніл]порфірину.
39. Застосування за п. 1, де цією сполукою є дихлорид 5,15-біс-[3-(3-триметиламоніопропілокси)феніл]порфірину.
40. Застосування за п. 1, де цією сполукою є дихлорид 5,15-біс-[4-(3-триметиламоніопропілокси)феніл]порфірину.
41. Застосування за п. 1, де цією сполукою є дихлорид 5-[3,5-біс-(3-триметиламоніопропілокси)феніл]-15-ундецилпорфірину.
42. Застосування за п. 1, де цією сполукою є хлорид 5-{4-[3-диметил-(3-диметиламінопропіл)амоніопропілокси]феніл}-15-(4-додецилоксифеніл)порфірину.
43. Застосування за п. 1, де цією сполукою є трихлорид 3-[({3-[(3-{4-[15-(4-додецилоксифеніл)порфірин-5-іл]фенокси}пропіл)диметиламоніо]пропіл}диметиламоніо)-пропіл]триметиламонію.
44. Застосування за п. 1, де цією сполукою є дихлорид 5,15-біс-[3-(3-триметиламоніопропілокси)феніл]-10-ундецилпорфірину.
45. Застосування за п. 1, де цією сполукою є дихлорид 5-{4-[3-диметил-(3-триметиламоніопропіл)амоніопропілокси]феніл}-15-(4-додецилоксифеніл)-порфірину.
46. Застосування за п. 1, де цією сполукою є дихлорид 5-[4-(3-диметилдециламоніопропілокси)феніл]-15-{4-[3-диметил-(3-диметиламінопропіл)-амоніопропілокси]феніл}порфірину.
47. Застосування за будь-яким з пп. 37-46, де ця сполука знаходиться в металованій формі.
48. Застосування за п. 1, де ця сполука є нетоксичною по відношенню до клітин ссавців.
49. Застосування за п. 1, де цей лікарський засіб призначений для перорального введення.
50. Застосування за п. 1, де цей лікарський засіб призначений для парентерального введення.
51. Застосування за п. 1, де цей лікарський засіб призначений для місцевого (топічного) введення.
52. Застосування за п. 1, де ці мікроорганізми вибрані із групи, що складається з бактерій, мікоплазм, дріжджів, грибків і вірусів.
53. Застосування за п. 1, де ці мікроорганізми є бактеріями, стійкими до одного або декількох загальноприйнятих антибіотичних агентів.
54. Застосування за п. 1, де ці мікроорганізми знаходяться на недоступній для світла поверхні або в недоступній для світла ділянці.
55. Застосування за п. 1, де цей лікарський засіб призначений для застосування в лікуванні та/або профілактиці мікробних інфекцій.
56. Застосування за п. 55, де ця мікробна інфекція є системною інфекцією.
57. Застосування за п. 1, де цей лікарський засіб призначений для попередження та/або лікування дерматологічної інфекції.
58. Застосування за п. 1, де цей лікарський засіб призначений для попередження та/або лікування інфекції легенів.
59. Застосування за п. 1, де цей лікарський засіб призначений для попередження та/або лікування ранової інфекції та/або виразок.
60. Спосіб лікування пацієнта, що потребує лікування антимікробним агентом, при якому вводять цьому пацієнту сполуку, описану в будь-якому з пунктів 1-48, де цей спосіб включає використання власної антимікробної активності цієї сполуки.
61. Спосіб за п. 60, де цю сполуку вводять перорально.
62. Спосіб за п. 60, де цю сполуку вводять парентерально.
63. Спосіб за п. 60, де цю сполуку вводять місцево (топічно).
64. Спосіб за п. 60, де цей пацієнт має дерматологічну інфекцію або інфекцію легенів.
65. Спосіб за п. 60, де цей пацієнт має ранову інфекцію.
66. Спосіб знищення мікроорганізмів in vitro, при якому здійснюють контактування цих мікроорганізмів зі сполукою, описаною в будь-якому з пунктів 1-48, де цей спосіб включає використання власної антимікробної активності цієї сполуки.
67. Спосіб лікування пацієнта, що потребує лікування антимікробним агентом, при якому вводять цьому пацієнту сполуку, описану в будь-якому з пунктів 1-48, де цей спосіб передбачає першу фазу лікування, під час якої спосіб використовує власну антимікробну активність цієї сполуки, з наступною другою фазою лікування, коли цю сполуку опромінюють стимулом, що активує антимікробну активність.
68. Спосіб за п. 67, де стимулом, що активує антимікробну активність, є ультразвук та/або світло.
69. Спосіб за п. 67, де перша фаза лікування триває щонайменше 10 хвилин, наприклад, щонайменше 20 хвилин, 30 хвилин, 40 хвилин, 50 хвилин, 1 годину, 2 години, 3 години, 5 годин, 12 годин або 24 години.
Текст
1. Застосування сполуки формули І або II, наведеної нижче, у приготуванні лікарського засобу для знищення або атенуації росту мікроорганізмів способом, який включає використання власної антимікробної активності цієї сполуки, X1 Y4 Y1 Z C2 2 (19) 1 3 7. Застосування за п. 1, де R1 означає незаміщену нижчу алкіленову, нижчу алкеніленову або нижчу алкініленову групу. 8. Застосування за п. 7, де R1 означає -(СН2)m- і "m" дорівнює цілому числу 1-20. 9. Застосування за п. 8, де "m" дорівнює цілому числу 1-10, наприклад 1-6, 1-5, 1-4 або 1-3. 10. Застосування за п. 9, де "m" дорівнює 3. 11. Застосування за п. 1, де R2, R3 та/або R4 означають нижчу алкільну, нижчу алкенільну або нижчу алкінільну групи. 12. Застосування за п. 11, де R2, R3 та/або R4 означають незаміщені нижчі алкільні групи. 13. Застосування за п. 12, де щонайменше один з R2, R3 та R4 означає алкільну групу, заміщену первинною, вторинною або третинною аміногрупою або четвертинною амонієвою групою. 14. Застосування за п. 1, де R1 означає -(СН2)3-, R2 та R3 означають СН3 і R4 означає -(CH2)3-N(CH3)2. 15. Застосування за п. 1, де R1 означає -(СН2)3- і R2, R3 та R4 означають, кожен, СН3. 16. Застосування за п. 1, де R1 означає -(СН2)3- і R2, R3 та R4 означають, кожний, C2H5. 17. Застосування за п. 1, де L вибраний з групи, що складається зі з'єднувальних груп фенокси, фенілену, сульфоніламідо, аміносульфонілу, сульфоніліміно, фенілсульфоніламідо, феніламіносульфонілу, сечовини, уретану та карбамату. 18. Застосування за п. 17, де Х1, Х2, Х3 та/або Х4 означають: (OR)n , де R означає R1-N+(R2)(R3)R4, як визначено в п. 1, і "n" дорівнює цілому числу 1-3. 19. Застосування за п. 17, де Х1, Х2, Х3 та/або Х4 означають: Rm , де R означає R1-N+(R2)(R3)R4, як визначено в п. 1, і "m" дорівнює цілому числу 1-3. 20. Застосування за п. 17, де Х1, Х2, Х3 та Х4 означають: (OR)n Rm , де кожен R незалежно означає R1-N+(R2)(R3)R4, як визначено в п. 1, і "n" та "m" дорівнюють цілим числам 1-3, і де сума "n+m" дорівнює цілому числу 1-3. 21. Застосування за будь-яким з пп. 18-20, де "n" або "m" дорівнює 3. 22. Застосування за будь-яким з пп. 18-20, де "n" або "m" дорівнює 2. 23. Застосування за будь-яким з пп. 18-20, де "n" та/або "m" дорівнює 1. 24. Застосування за будь-яким з пп. 18-20, де L є монозаміщеним у пара-положенні. 94027 4 25. Застосування за будь-яким з пп. 18-20, де L є монозаміщеним або дизаміщеним у метаположенні (мета-положеннях). 26. Застосування за будь-яким з пп. 18-20, де L є монозаміщеним або дизаміщеним в ортоположенні (орто-положеннях). 27. Застосування за п. 1, де ця сполука включає дві катіонні групи, як визначено в п. 1, з протилежних боків порфіринового кільця, тобто, в положеннях кільця 5 та 15 або положеннях кільця 10 та 20. 28. Застосування за п. 27, де Х1 та Х3 є атомом водню, ліпофільною групою, фенільною групою, нижчою алкільною, алкарильною або аралкільною групою, а Х2 та Х4 є катіонними групами, або навпаки. 29. Застосування за п. 1, де ця сполука може містити дві катіонні групи, як визначено в п. 1, на сусідніх положеннях порфіринового кільця, тобто, в положеннях кільця 5 та 10 або положеннях кільця 10 та 15, або положеннях кільця 15 та 20, або положеннях кільця 20 та 5. 30. Застосування за п. 29, де Х1 та Х2 означають водень, а Х3 та Х4 означають катіонні групи, або Х2 та Х3 означають водень, а Х4 та Х1 означають катіонні групи. 31. Застосування за п. 1, де щонайменше один з Х1, Х2, Х3 та Х4 означає ліпофільну частину молекули. 32. Застосування за п. 31, де ця ліпофільна частина молекули є насиченою алкільною групою з розгалуженим ланцюгом формули -(СН2)pСН3, де "р" дорівнює цілому числу 1-22. 33. Застосування за п. 32, де "р" дорівнює 1-18, наприклад 2-16 або 4-12. 34. Застосування за п. 1, де жоден з Х1, Х2, Х3 та Х4 не є ліпофільною частиною молекули. 35. Застосування за п. 1, де жоден з Х1, Х2, Х3 та Х4 не є фенільною групою. 36. Застосування за п. 1, де ця сполука є водорозчинною. 37. Застосування за п. 1, де цією сполукою є дихлорид 5,15-біс-(4-{3-[(3диметиламінопропіл)диметиламоніо]пропілокси}феніл)порфірину. 38. Застосування за п. 1, де цією сполукою є дихлорид 5,15-біс-[4-(3триетиламоніопропілокси)феніл]порфірину. 39. Застосування за п. 1, де цією сполукою є дихлорид 5,15-біс-[3-(3триметиламоніопропілокси)феніл]порфірину. 40. Застосування за п. 1, де цією сполукою є дихлорид 5,15-біс-[4-(3триметиламоніопропілокси)феніл]порфірину. 41. Застосування за п. 1, де цією сполукою є дихлорид 5-[3,5-біс-(3триметиламоніопропілокси)феніл]-15ундецилпорфірину. 42. Застосування за п. 1, де цією сполукою є хлорид 5-{4-[3-диметил-(3диметиламінопропіл)амоніопропілокси]феніл}-15(4-додецилоксифеніл)порфірину. 43. Застосування за п. 1, де цією сполукою є трихлорид 3-[({3-[(3-{4-[15-(4додецилоксифеніл)порфірин-5 5 94027 6 іл]фенокси}пропіл)диметиламоніо]пропіл}диметил амоніо)-пропіл]триметиламонію. 44. Застосування за п. 1, де цією сполукою є дихлорид 5,15-біс-[3-(3триметиламоніопропілокси)феніл]-10ундецилпорфірину. 45. Застосування за п. 1, де цією сполукою є дихлорид 5-{4-[3-диметил-(3триметиламоніопропіл)амоніопропілокси]феніл}15-(4-додецилоксифеніл)-порфірину. 46. Застосування за п. 1, де цією сполукою є дихлорид 5-[4-(3диметилдециламоніопропілокси)феніл]-15-{4-[3диметил-(3-диметиламінопропіл)амоніопропілокси]феніл}порфірину. 47. Застосування за будь-яким з пп. 37-46, де ця сполука знаходиться в металованій формі. 48. Застосування за п. 1, де ця сполука є нетоксичною по відношенню до клітин ссавців. 49. Застосування за п. 1, де цей лікарський засіб призначений для перорального введення. 50. Застосування за п. 1, де цей лікарський засіб призначений для парентерального введення. 51. Застосування за п. 1, де цей лікарський засіб призначений для місцевого (топічного) введення. 52. Застосування за п. 1, де ці мікроорганізми вибрані із групи, що складається з бактерій, мікоплазм, дріжджів, грибків і вірусів. 53. Застосування за п. 1, де ці мікроорганізми є бактеріями, стійкими до одного або декількох загальноприйнятих антибіотичних агентів. 54. Застосування за п. 1, де ці мікроорганізми знаходяться на недоступній для світла поверхні або в недоступній для світла ділянці. 55. Застосування за п. 1, де цей лікарський засіб призначений для застосування в лікуванні та/або профілактиці мікробних інфекцій. 56. Застосування за п. 55, де ця мікробна інфекція є системною інфекцією. 57. Застосування за п. 1, де цей лікарський засіб призначений для попередження та/або лікування дерматологічної інфекції. 58. Застосування за п. 1, де цей лікарський засіб призначений для попередження та/або лікування інфекції легенів. 59. Застосування за п. 1, де цей лікарський засіб призначений для попередження та/або лікування ранової інфекції та/або виразок. 60. Спосіб лікування пацієнта, що потребує лікування антимікробним агентом, при якому вводять цьому пацієнту сполуку, описану в будь-якому з пунктів 1-48, де цей спосіб включає використання власної антимікробної активності цієї сполуки. 61. Спосіб за п. 60, де цю сполуку вводять перорально. 62. Спосіб за п. 60, де цю сполуку вводять парентерально. 63. Спосіб за п. 60, де цю сполуку вводять місцево (топічно). 64. Спосіб за п. 60, де цей пацієнт має дерматологічну інфекцію або інфекцію легенів. 65. Спосіб за п. 60, де цей пацієнт має ранову інфекцію. 66. Спосіб знищення мікроорганізмів in vitro, при якому здійснюють контактування цих мікроорганізмів зі сполукою, описаною в будь-якому з пунктів 1-48, де цей спосіб включає використання власної антимікробної активності цієї сполуки. 67. Спосіб лікування пацієнта, що потребує лікування антимікробним агентом, при якому вводять цьому пацієнту сполуку, описану в будь-якому з пунктів 1-48, де цей спосіб передбачає першу фазу лікування, під час якої спосіб використовує власну антимікробну активність цієї сполуки, з наступною другою фазою лікування, коли цю сполуку опромінюють стимулом, що активує антимікробну активність. 68. Спосіб за п. 67, де стимулом, що активує антимікробну активність, є ультразвук та/або світло. 69. Спосіб за п. 67, де перша фаза лікування триває щонайменше 10 хвилин, наприклад, щонайменше 20 хвилин, 30 хвилин, 40 хвилин, 50 хвилин, 1 годину, 2 години, 3 години, 5 годин, 12 годин або 24 години. Область техніки, до якої належить винахід Даний винахід стосується нових застосувань сполук порфірину і, зокрема, застосування таких сполук у лікувальній або профілактичній терапії мікробної колонізації та інфекції. Рівень техніки Визнається, що стійкість до антибіотиків, що розвивається зростаючим числом мікроорганізмів, є всесвітньою проблемою охорони здоров'я (Tunger et al., 2000, Int. J. Microb. Agents 15:131135; Jorgensen et al., 2000, Clin. Infect. Dis. 30:799808). Внаслідок цього розвиток нових підходів до вбивання мікроорганізмів є вкрай необхідним. Лікування мікробних інфекцій фотодинамічною терапією (PDT) є важливим недавно розробленим способом знищення бактерій, тому що включає механізм, який явно відрізняється від механізму, типового для більшості антибіотиків. Так, PDT за снована на застосуванні фотосенсибілізувальної молекули, яка, після активації світлом, генерує реакційноздатні різновиди кисню, що є токсичними для різноманітних прокаріотичних та еукаріотичних клітин, у тому числі бактерій, мікоплазм і дріжджів (Malik et al., 1990, J. Photochem. Photobiol. В Biol. 5:281-293; Bertoloni et al., 1992, Mickrobios 71:3346). Важливо, що ця фотосенсибілізувальна активність багатьох фотодинамічних агентів проти бактерій не руйнується стійкістю до антибіотиків, а навпроти, залежить в основному від їхньої хімічної структури (Malik et al., 1992, J. Photochem. Photobiol. B. Biol. 14:262-266). Різні типи нейтральних та аніонних фотосенсибілізувальних агентів виявляють явну фототоксичну активність проти грампозитивних бактерій. Однак такі фотосенсибілізувальні агенти не виявляють прийнятної цитотоксичної активності проти 7 грамнегативних бактерій, поки проникність зовнішньої мембрани не буде змінена обробкою етилендіамінтетраоцтовою кислотою (ЕДТА) або полікатіонами (Bertoloni et al., FEMS Microbiol. Lett. 71: 149-156; Nitzan et al., 1992, Photochem. Photobiol. 55:89-97). Вважається, що клітинна оболонка грамнегативних бактерій, яка є більш складною та більш товстою, ніж клітинна оболонка грампозитивних бактерій, запобігає ефективному зв'язуванню фотосенсибілізувального агента або затримує чи дезактивує цитотоксичні реакційноздатні частинки, фотогенеровані фотосенсибілізувальним агентом (Ehrenberg et al., 1985, Photochem. Photobiol. 41:429-435; Valduga et al., 1993, J. Photochem. Photobiol. B. Biol. 21:81-86). На противагу цьому, позитивно заряджені (катіонні) фотосенсибілізувальні агенти, у тому числі порфірини та фталоціаніни, стимулюють ефективну інактивацію грамнегативних бактерій без необхідності модифікації природної структури клітинної оболонки (Mervhat et al., J. Photochem. Photobiol. B. Biol. 32:153-157; Minnok et al., 1996, J. Photochem. Photobiol. B. Biol. 32:159-164). Очевидно, позитивний заряд сприяє зв'язуванню фотосенсибілізувального агента в критичних клітинних сайтах, які, після ушкодження під дією світла, викликають втрату життєздатності клітин (Merchat et al., 1996, J. Photochem. Photobiol. B. Biol. 35:149157). Так, повідомлялося, що Escherichia coli ефективно інактивується видимим світлом після інкубації з катіонним 5,10,15,20-тетракіс-(4-Nметилпіридил)порфіном (Т4МРуР) (Valduga et al., 1999, Biochem. Biophys. Res. Commun. 256:84-88). Фототоксична активність цього порфірину опосередкована в основному руйнуванням ферментативної та транспортної функцій як зовнішньої, так і цитоплазматичної мембран, а не зв'язуванням із ДНК. Однак застосовність відомих антимікробних агентів на основі порфірину є обмеженою внаслідок їхньої токсичності проти клітин тканин хазяїнассавця, тобто, ці сполуки не здатні розрізняти між мікробними клітинами-мішенями та клітинамихазяями. Крім того, застосовність відомих антимікробних агентів на основі порфірину додатково обмежується їхньою відносно низкою активністю по відношенню до мікробних клітин-мішеней. Крім того, не всі мікробні інфекції є придатними для лікування з використанням фотодинамічної терапії, наприклад, сайт інфекції може бути недоступним для світла. Таким чином, існує необхідність у нових способах вбивання та атенуації росту мікробних агентів. Розкриття винаходу Відповідно до першого аспекту даного винаходу, забезпечене застосування сполуки формули І у приготуванні лікарського засобу для вбивання або атенуації росту мікроорганізмів у спосіб, який не включає піддавання цієї сполуки дії джерела світла фотодинамічної терапії або джерела ультразвуку ультразвукової (сонодинамічної) терапії, 94027 8 де: Χ1, Х2, Х3 та Х4 незалежно позначають (тобто, є однаковими чи різними) атом водню, ліпофільну частину молекули, фенільну групу, нижчу алкільну, алкарильну чи аралкільну групу, або катіонну групу такої формули: -L-R1-N+(R2)(R3)R4 де: L позначає з'єднувальну (лінкерну) частину молекули або відсутній; R1 позначає нижчий алкілен, нижчий алкенілен або нижчий алкінілен, необов'язково заміщений одним або декількома замісниками, вибраними з нижчого алкілу, нижчого алкілену (необов'язково перериваного киснем), фтору, OR5, C(O)R6, C(O)OR7, C(O)NR8R9, NR10R11 та N+R12R13R14; і R2, R3 та R4 незалежно позначають (тобто, є однаковими чи різними) Н, арил, нижчий алкіл, нижчий алкеніл або нижчий алкініл, останні три з яких необов'язково заміщені одним або декількома замісниками, вибраними з нижчого алкілу, нижчого алкілену (необов'язково перериваного киснем), арилу, OR5, C(O)R6, C(O)OR7, C(O)NR8R9, NR10R11 та N+R12R13R14; Ζ позначає -СН або Ν; Υ1, Υ2, Υ3 та Υ4 відсутні або незалежно позначають арил, нижчий алкіл, нижчий алкеніл або нижчий алкініл, останні три з яких необов'язково заміщені одним або декількома замісниками, вибраними з нижчого алкілу, нижчого алкілену (необов'язково перериваного киснем), арилу, OR5, C(O)R6, C(O)OR7, C(O)NR8R9, NR10R11 та N+R12R13R14, або, узяті разом з пірольним кільцем, до якого вони приєднані, можуть утворювати циклічну групу; і R5, R6, R7, R8, R9, R10, R11, R12, R13 та R14 незалежно позначають Н або нижчий алкіл; за умови, що, щонайменше, один з Χ1, Х2, Х3 та Х4 є катіонною групою, визначеною вище, і, щонайменше, один з Χ1, Х2, Х3 та Х4 позначає атом водню, фенільну групу, ліпофільну частину молекули або нижчу алкільну, алкарильну чи аралкільну групу. Термін "нижчий алкіл" включає лінійний або розгалужений, циклічний або ациклічний С1-С20алкіл, який може бути перерваний киснем (краще, не більш ніж п'ять атомів вуглецю присутні в кожному алкільному ланцюзі). Нижчі алкільні групи, які можуть представляти R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11, R12, R13 та R14, включають С1-С18алкіл, С1-С16-алкіл, С1-С14-алкіл, С1-С12-алкіл, С1С10-алкіл, С1-С9-алкіл, С1-С8-алкіл, С1-С7 алкіл, С1 9 94027 10 С6-алкіл, С1-С5-алкіл, С1-С4-алкіл, С1-С3-алкіл і С1С2-алкіл. Кращі нижчі алкільні групи, що можуть представляти R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11, R12, R13 та R14, включають С1, C2, C3, C4, C5, С6, С7, С8, C9, С10, С11, C12, C13, C14, C15 та С16алкіл. Таким чином, будь-які один чи кілька N+R2R3R4 та/або N+R12R13R14 можуть представляти групи циклічного аміну/амонію, наприклад, Має бути зрозуміло, що групи циклічного аміну/амонію можуть також містити менше чи більше, ніж шість членів, наприклад, такі групи можуть містити 4-, 5-, 7-, 8-, 9- або 10-членні кільця. Термін «нижчий алкілен» повинен розумітися відповідним чином. Терміни «нижчий алкеніл» та «нижчий алкініл» включають лінійний або розгалужений, циклічний або ациклічний С2-С20-алкеніл та С2-С20-алкініл, відповідно, кожний з яких може перериватися киснем (краще, не більш ніж п'ять атомів кисню присутні в кожному алкенільному чи алкінільному ланцюзі). Термін «нижчий алкеніл» включає також як цис-, так і транс-геометричні ізомери. Нижчі алкенільні групи, які можуть представляти R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11, R12, R13 та R14, включають С2-С18-алкеніл, С2-С17-алкеніл, С1-С16алкеніл, С2-С14-алкеніл, С2-С12-алкеніл, С2-С10алкеніл, С2-С8-алкеніл, С2-С7-алкеніл, С2-С6алкеніл, С2-С5-алкеніл, С2-С4-алкеніл, С2-С3алкеніл та С3-С4-алкеніл. Кращі нижчі алкенільні групи, які можуть представляти R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11, R12, R13 та R14, включають C2, C3, C4, C5, С6, С7, С8, C9, С10, С11, C12, C13 та С14-алкеніл. Термін "нижчий алкенілен" повинен розумітися відповідним чином. «Нижчі алкінільні» групи, які можуть представляти R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11, R12, R13 та R14, включають С2-С18-алкініл, С2-С16алкініл, С2-С14-алкініл, С2-С12-алкініл, С2-С10алкініл, С2-С9-алкініл, С2-С8-алкініл, С2-С7-алкініл, С2-С6-алкініл, С2-С5-алкініл, С2-С4-алкініл, С2-С3алкініл та С3-С4-алкініл. Кращі нижчі алкінільні групи, які можуть представляти R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11, R12, R13 та R14, включають C2, C3, C4, C5, С6, С7, С8, C9, С10, С11, C12, C13 та С14алкініл. Термін "нижчий алкінілен" повинен розумітися відповідним чином. Термін "арил" включає шести-десятичленні карбоциклічні ароматичні групи, такі як феніл і нафтил, необов'язково заміщені одним або декількома замісниками, вибраними з фтору, ціано, нітро, нижчого алкілу (тобто, алкарилу), OR5, C(O)R6, C(O)OR7, C(O)NR8R9 та NR10R11. Термін «аралкіл» включає арильні групи, приєднані до порфіринового кільця через нижчу алкільну групу. Другий аспект даного винаходу забезпечує застосування сполуки формули II у приготуванні лі карського засобу для вбивання або атенуації росту мікроорганізмів способом, який не включає піддавання цієї сполуки дії джерела світла фотодинамічної терапії або джерела ультразвуку ультразвукової (сонодинамічної) терапії: де Μ позначає металевий елемент або металоїдний елемент і X1, Х2, Х3, Х4, Υ1, Υ2, Υ3, Υ4 та Ζ мають визначені вище значення. Краще, у першому та другому аспектах даного винаходу лікарський засіб призначений для вбивання або атенуації росту мікроорганізмів способом, який не включає піддавання цієї сполуки дії стимулу, що активує антимікробну активність. Під «стимулом, що активує антимікробну активність» автори мають на увазі стимул, який підвищує здатність зазначеної сполуки вбивати або атенуювати ріст мікробних агентів, такий як освітлення джерелом світла фотодинамічної терапії або піддавання дії джерелом ультразвуку. Інакше кажучи, цей лікарський засіб виявляє власну антимікробну активність, тобто, цей лікарський засіб (і конкретно активна сполука в ньому) має властиву йому активність. Така активність може бути визначена способами, добре відомими в даній області, наприклад, див. приклад В. Таким чином, цей лікарський засіб призначений для вбивання або атенуації росту мікроорганізмів способом, іншим, ніж фотодинамічна або ультразвукова терапія. Однак має бути зрозуміло, що не виключаються способи вбивання або атенуації росту мікроорганізмів, у яких цей лікарський засіб піддається дії нормального світла навколишнього середовища (тобто, сонячного світла або штучного світла навколишнього середовища). Краще, цей лікарський засіб піддають дії світла/радіації з інтенсивністю, меншою, ніж 10 мВт/см2, наприклад, меншою, ніж 20 мВт/см2, меншою, ніж 25 мВт/см2, меншою, ніж 30 мВт/см2 11 (тобто, меншою, ніж 300 Вт/м2), меншою, ніж 40 мВт/см2, меншою, ніж 50 мВт/см2, меншою, ніж 60 мВт/см2, меншою, ніж 70 мВт/см2, меншою, ніж 80 мВт/см2, меншою, ніж 90 мВт/см2, або меншою, ніж 2 100 мВт/см . Краще, цей лікарський засіб піддають дозі світла/радіації, меншій, ніж 100 Дж/см2, наприклад, меншій, ніж 90 Дж/см2, меншій, ніж 80 Дж/см2, меншій, ніж 70 Дж/см2, меншій, ніж 60 Дж/см2, меншій, ніж 50 Дж/см2, меншій, ніж 40 Дж/см2, меншій, ніж 30 Дж/см2, меншій, ніж 20 Дж/см2, або меншій, ніж 10 Дж/см2. Крім того, фахівцям з кваліфікацією в даній області буде зрозуміло, що цей лікарський засіб може бути застосовним в схемі лікування, що використовує як його власну активність, так і його фотодинамічну та/або сонодинамічну активність. Наприклад, цей лікарський засіб може спочатку використовуватися під час відсутності активуючого стимулу, так що використовується його власна антимікробна активність, а потім він може піддаватися дії активуючого стимулу, так що використовується його фотодинамічна та/або сонодинамічна активність. Термін «металевий елемент» включає двовалентний або тривалентний металевий елемент. Краще, цей металевий елемент є діамагнітним. Ще краще, цей металевий елемент вибраний з Zn(ll), Cu(ll), La(lll), Lu(lll), Y(lll), In(lll), Cd(ll), Mg(ll), Al(lll), Ru, Ni(ll), Mn(lll), Fe(lll) і Pd(ll). Найкраще, металевим елементом є Ni(ll), Mn(lll), Fe(lll) або Pd(ll). Термін «металоїд» включає елемент, який має такі фізичні та хімічні властивості, як здатність проводити електрику, що є проміжними між властивостями як металів, так і неметалів. Термін «металоїдний елемент» включає атоми кремнію (Si) і германію (Ge), які необов'язково заміщені одним або декількома лігандами. Має бути зрозуміло, що терміни металевий елемент і металоїдний елемент включають металевий елемент або металоїдний елемент, які мають позитивний окиснений стан, усі з яких можуть бути заміщені одним або декількома лігандами, вибраними з фтору, ОН, OR15, де R15 позначає нижчий алкіл, нижчий алкеніл, нижчий алкініл, аралкіл, арил або алкарил, визначені вище (де арил та алкарил є монозаміщеними). Сполуки формул І та II містять, щонайменше, одну катіонну групу. Таким чином, сполуки за даним винаходом можуть нести результуючий (загальний) позитивний заряд, наприклад, заряд +1, +2, +3, +4, +5, +6 чи більше. У кращому варіанті здійснення, ці сполуки несуть загальний заряд, менший, ніж +4, наприклад, +1, +2 або +3. В особливо кращому варіанті здійснення, ці сполуки несуть загальний заряд +2. Фахівцям із кваліфікацією в даній області буде зрозуміло, що сполуки формул І та II можуть бути врівноважені протианіонами. Приклади протианіонів включають, без обмеження ними, галогеніди (наприклад, фторид, хлорид і бромід), сульфати (наприклад, децилсульфат), нітрати, перхлорати, сульфонати (наприклад, метансульфонат) і трифторацетат. Інші придатні протианіони будуть до 94027 12 бре відомі особам із кваліфікацією в даній області. Таким чином, фармацевтично або ветеринарно прийнятні похідні сполук формул І та II, такі як солі та сольвати, також включені в об'єм цього винаходу. Солі, що можуть бути згадані, включають кислотно-адитивні солі, наприклад, солі, утворені з неорганічними кислотами, такими як хлористоводнева, бромистоводнева, сірчана та фосфорна кислота, з карбоновими кислотами або органосульфоновими кислотами; основно-адитивні солі; солі металів, утворені з основами, наприклад, солі натрію та солі калію. Крім того, особам із кваліфікацією в даній області буде зрозуміло, що сполуки формули І можуть виявляти таутомерію. Всі таутомерні форми та їхні суміші включені в об'єм даного винаходу. Сполуки формул І та II можуть також містити один або кілька асиметричних атомів вуглецю і, отже, можуть виявляти оптичну ізомерію або діастереоізомерію. Діастереоізомери можуть бути розділені з використанням загальноприйнятих способів, наприклад, хроматографії та фракційної кристалізації. Різні стереоізомери можуть бути виділені розділенням рацемічної або іншої суміші цих сполук з використанням загальноприйнятих способів, наприклад, фракційної кристалізації або ВЕРХ. Альтернативно, бажані оптичні ізомери можуть бути одержані реакцією відповідних оптично активних вихідних матеріалів в умовах, які не будуть викликати рацемізації або епімеризації, або дериватизацією, наприклад, гомохіральною кислотою з наступним розділенням діастереомерних ефірів загальноприйнятими способами (наприклад, ВЕРХ, хроматографією на силікагелі). Всі стереоізомери включені в об'єм даного винаходу. В одному кращому варіанті здійснення першого та другого аспектів даного винаходу Ζ позначає -СН. Характерною ознакою першого та другого аспектів даного винаходу є те, що, щонайменше, одна із груп-замісників Χ1, Х2, Х3 і Х4 є катіонною групою четвертинного амонію формули -L-R1N+(R2)(R3)R4, визначеною вище. Краще, жоден з Χ1, Х2, Х3 та Х4 не є катіонною групою анілінію або піридинію. В кращому варіанті здійснення, R1 позначає незаміщену нижчу алкіленову, нижчу алкеніленову або нижчу алкініленову групу. Краще, R1 позначає нижчу алкіленову групу з розгалуженим ланцюгом формули: -(СН2)m-. Краще, "m" дорівнює цілому числу 1-20. Ще краще, "m" дорівнює цілому числу 1-10, наприклад, 1-6, 1-5, 1-4, або 1-3. Кращі нижчі алкіленові групи з розгалуженим ланцюгом, які може представляти R1, включають групи наведеної вище формули, де m дорівнює 2, 3, 4, 5, 6, 7, 8, 9 або 10. Найкраще, "m" дорівнює 2 або 3. Інші три групи-замісники радикала четвертинного амонію, тобто, R2, R3 та R4, можуть бути однаковими чи різними і вибрані з Н, нижчого алкілу, нижчого алкенілу та нижчого алкінілу, останні три з яких необов'язково заміщені одним або декількома замісниками, вибраними з нижчого алкілу, OR5, 13 C(O)R6, C(O)OR7, C(O)NR8R9, NR10R11 та N+R12R13R14. В кращому варіанті здійснення, R2, R3 та/або R4 позначають нижчу алкільну, нижчу алкенільну або нижчу алкінільну групу. Краще, R2, R3 та/або R4 позначають незаміщені нижчі алкільні групи. Необов'язково, щонайменше, один з R2, R3 та R4 позначає алкільну групу, заміщену первинною, вторинною або третинною аміногрупою або четвертинною амонієвою групою. В кращому варіанті першого та другого аспектів даного винаходу, R1 позначає -(СН2)3-, R2 та R3 позначають СН3 і R4 позначає -(CH2)3-N(CH3)2. В альтернативному кращому варіанті першого та другого аспектів даного винаходу, R1 позначає (СН2)3- і R2, R3 та R4 позначають кожен СН3. У наступному альтернативному кращому варіанті першого та другого аспектів даного винаходу R1 позначає -(СН2)3- і R2, R3 та R4 позначають кожен С2Н5. Краще, щонайменше один з Χ1, Х2, Х3 та Х4 є катіонною групою, визначеною вище, і, щонайменше один з Χ1, Х2, Х3 та Х4 є атомом водню. Краще, кожний з Χ1, Х2, Х3 та Х4 позначає атом водню або катіонну групу, визначену вище. Краще, величини pK будь-якої первинної, вторинної або третинної аміногруп, якщо вони присутні в сполуках даного винаходу, є більшими, ніж 8, для гарантії того, що ця група є протонованою, коли вона перебуває у фізіологічному середовищі. Четвертинна амонієва катіонна група необов'язково приєднана до порфіринового кільця через з'єднувальну групу L. Кращі з'єднувальні групи L включають з'єднувальні групи фенокси, фенілен, сульфоніламідо, аміносульфоніл, сульфоніліміно, фенілсульфоніламідо, феніламіносульфоніл, сечовину, уретан і карбамат. В кращому варіанті здійснення, четвертинна амонієва катіонна група приєднана до порфіринового кільця через з'єднувальну феноксигрупу. Таким чином, Χ1, Х2, Х3 та/або Х4 можуть мати таку формулу: де R позначає R1-N+(R2)(R3)R4, як визначено вище, і "n" дорівнює цілому числу 1-3. В альтернативному кращому варіанті здійснення, четвертинна амонієва катіонна група приєднана до порфіринового кільця через з'єднувальну феніленову групу. Таким чином, Χ1, Х2, Х3та/або Х4 можуть мати таку формулу: де R позначає R1-N+(R2)(R3)R4, як визначено вище, і "m" дорівнює цілому числу 1-3. Краще, "m" дорівнює 2, найкраще, 1. 94027 14 В альтернативному кращому варіанті здійснення, Χ1, Х2, Х3 та Х4 можуть мати таку формулу: де R позначає R1-N+(R2)(R3)R4, "n" та "m" відповідають визначеним вище і сума n+m дорівнює 1-3. Краще, L містить бензольне кільце (наприклад, фенокси, фенілен, фенілсульфоніламідо або феніламіносульфоніл), монозаміщене в параположенні. Альтернативно, L може бути моно- або дизаміщеним у мета- чи орто-положеннях. L може бути також як пара-, так і орто-заміщеним. В альтернативному кращому варіанті здійснення, четвертинна амонієва катіонна група приєднана безпосередньо до порфіринового кільця, тобто, L відсутній. В кращому варіанті першого та другого аспектів даного винаходу, ця сполука містить дві катіонні групи, визначені вище, з протилежних боків порфіринового кільця, тобто, в положеннях кільця 5 та 15 або положеннях кільця 10 та 20. Наприклад, Χ1 та Х3 можуть бути атомом водню, ліпофільною групою, фенільною групою, нижчою алкільною, алкарильною чи аралкільною групою, а Х2 та Х4 можуть бути катіонними групами, або навпаки. Краще, Χ1 та Х3 є обидва атомами водню, а Х2 та Х4 є обидва катіонними групами, чи навпаки. Альтернативно, ця сполука може містити дві катіонні групи, як визначено вище, в сусідніх положеннях порфіринового кільця, тобто, в положеннях кільця 5 та 10, або положеннях кільця 10 та 15, або положеннях кільця 15 та 20, або положеннях кільця 20 та 5. Наприклад, Χ1 та Х2 можуть бути атомами водню, а Х3 та Х4 можуть бути катіонними групами, або Х2 та Х3 можуть бути атомами водню, а Х4 та Χ1 можуть бути катіонними групами і т.д. Особам із кваліфікацією в даній області буде зрозуміло, що коли Ζ позначає азот, виникають додаткові ізомерні структурні можливості. Такі можливості включені в об'єм даного винаходу. В наступному кращому варіанті здійснення першого та другого аспектів даного винаходу, ця сполука заміщена на одному чи більше з пірольних кілець, що входять до її складу. Так, Υ1, Υ2, Υ3 та Υ4 можуть бути відсутніми або незалежно позначають арил, нижчий алкіл, нижчий алкеніл чи нижчий алкініл, останні три з яких необов'язково заміщені одним або декількома замісниками, вибраними з нижчого алкілу, нижчого алкілену (необов'язково перериваного киснем), арилу, OR5, C(O)R6, C(O)OR7, C(O)NR8R9, NR10R11 та N+R12R13R14. Особам із кваліфікацією в даній області буде зрозуміло, що Υ1, Υ2, Υ3 та/або Υ4 можуть містити циклічні групи, які можуть бути насиченими або ароматичними. Наприклад, одне чи більше з пірольних кілець можуть бути заміщеними з утворенням ізоіндольної групи, тобто, Υ1, Υ2, Υ3 та/або Υ4 разом з пірольним кільцем, до якого вони приєднані, можуть бути циклічними. В альтернативному кращому варіанті здійснення першого та другого аспектів даного винахо 15 ду, Υ1, Υ2, Υ3 та Υ4 відсутні. Таким чином, порфіринове кільце, краще, заміщене тільки в одному чи більше з положень 5, 10, 15 або 20. В наступному кращому варіанті здійснення першого та другого аспектів даного винаходу, щонайменше, один з Χ1, Х2, Х3 та Х4 позначає або містить ліпофільну групу. Під «ліпофільною групою» автори мають на увазі групи, які мають коефіцієнт розподілу між 1н-октанолом та водою, виражений в log P, більший, ніж 1,0 при фізіологічному pH та 25 °С. Краще, цією ліпофільною частиною є насичена алкільна група з розгалуженим ланцюгом формули -(СН2)pСН3, або еквівалентна алкіленова група формули (СН2)p-, де "p" дорівнює цілому числу 122, наприклад, 1-18. Краще, "р" дорівнює 1-18, ще краще, 2-16, 4-16, 6-18, 8-16, або 4-12. Найкраще, "р" дорівнює 10-12. Має бути зрозуміло, що Χ1, Х2, Х3 та/або Х4 може бути катіонною групою, визначеною вище, яка також містить ліпофільну групу. В альтернативному кращому варіанті здійснення першого та другого аспектів даного винаходу жоден з Χ1, Х2, Х3 та Х4 не є ліпофільною групою. Краще, сполуки, використовувані в першому та другому аспектах даного винаходу, є розчинними у воді. Краще, ці сполуки можуть бути розчинені у воді до концентрації, щонайменше, 5 мкг/л, наприклад, щонайменше, 10 мкг/л, 15 мкг/л або 20 мкг/л. Ще краще, ці сполуки можуть бути розчинені у воді до концентрації, щонайменше, 100 мкг/л, наприклад, 200 мкг/л, 300 мкг/л, 400 мкг/л, 500 мкг/л, 1 мг/мл, 5 мг/мл, 10 мг/мл, 20 мг/мл, 50 мг/мл або 100 мг/мл. Краще, сполуки, використовувані в першому та другому аспектах даного винаходу, виявляють селективну токсичність по відношенню до мікробних агентів. Під терміном "селективний" автори мають на увазі, що ця сполука є, краще, токсичною по відношенню до одного або декількох мікроорганізмів (таких як бактерії, мікоплазми, дріжджі, гриби та/або віруси) у порівнянні з клітинами-хазяями ссавців, наприклад, людини. Краще, токсичність цієї сполуки по відношенню до мікроорганізмумішені є, щонайменше, удвічі вищою, ніж токсичність цієї сполуки по відношенню до клітин ссавців, ще краще, щонайменше, утричі, щонайменше, у чотири рази, щонайменше, у п'ять разів, щонайменше, у шість разів, щонайменше, у вісім разів, щонайменше, у десять разів, щонайменше, у п'ятнадцять разів, або, щонайменше, у двадцять разів. Найкраще, сполука даного винаходу є по суті нетоксичною по відношенню до клітин ссавців. Таким чином, коли ці сполуки використовуються, наприклад, для лікування бактеріальних інфекцій, схеми введення доз можуть бути вибрані таким чином, що бактеріальні клітини руйнуються з мінімальним ушкодженням здорової тканини хазяїна. Таким чином, сполуки для застосування в першому та другому аспектах даного винаходу, краще, виявляють "терапевтичне вікно". В кращому варіанті здійснення, ця сполука є токсичною по відношенню до мікроорганізмумішені (наприклад, бактеріальної клітини) при ни 94027 16 зьких дозах. Краще, ця сполука є токсичною по відношенню до мікроорганізму-мішені при концентрації, меншій, ніж 10 мкМ, наприклад, меншій, ніж 1 мкМ, меншій, ніж 0,1 мкМ, меншій, ніж 0,01 мкМ, меншій, ніж 0,005 мкМ, або меншій, ніж 0,001 мкМ (див. приклад В). Кращі сполуки для застосування в першому та другому аспектах цього винаходу включають такі сполуки: (а) дихлорид 5,15-біс-(4-{3-[(3диметиламінопропіл)диметиламоніо]пропілокси}феніл)порфірину («Сполука 8») Краще, ця Сполука забезпечена у вигляді дихлоридної або тетрахлоридної солі. (b) дихлорид 5,15-біс-[4-(3триетиламоніопропілокси)феніл]порфірину («Сполука 9») Краще, ця сполука забезпечена у вигляді дихлоридної солі. (с) дихлорид 5,15-біс-[3-(3триметиламоніопропілокси)феніл]порфірину («Сполука 12») Краще, ця сполука забезпечена у вигляді дихлоридної солі. (d) дихлорид 5,15-біс-[4-(3триметиламоніопропілокси)феніл]порфірину («Сполука 10») Краще, ця сполука забезпечена у вигляді дихлоридної солі. (e) дихлорид 5-[3,5-біс-(3триметиламоніопропілокси)феніл]-15-ундецилпорфірину («Сполука 6») 17 Краще, ця сполука забезпечена у вигляді дихлоридної солі. (f) хлорид 5-{4-[3-диметил-(3диметиламінопропіл)амоніопропілокси]феніл}-15(4-додецилоксифеніл)порфірину («Сполука 23») Краще, ця Сполука забезпечена у вигляді хлоридної чи дихлоридної солі. (д) трихлорид 3-[({3-{4-[15-(4додецилоксифеніл)порфірин-5-іл]фенокси}пропіл)диметиламоніо]пропіл}диметиламоніо)пропіл]т риметиламонію («Сполука 25») 94027 18 Краще, ця сполука забезпечена у вигляді трихлоридної солі. (h) дихлорид 5,15-біс-[3-(3триметиламоніопропілокси)феніл]-10-ундецилпорфірину («Сполука 28») Краще, ця сполука забезпечена у вигляді дихлоридної солі. (і) дихлорид 5-{4-[3-диметил-(3триметиламоніопропіл)амоніопропілокси]-феніл}15-(4-додецилоксифеніл)порфірину («(Сполука 31») Краще, ця сполука забезпечена у вигляді дихлоридної солі. (j) дихлорид 5-[4-(3диметилдециламоніопропілокси)феніл]-15-{4-[3 диметил-(3диметиламінопропіл)амоніопропілокси]феніл}порфірину 32») Краще, ця сполука забезпечена у вигляді дихлоридної солі. Має бути зрозуміло, що наведені вище сполуки можуть бути альтернативно в металованій формі, тобто, вони можуть містити хелатований металевий елемент або металоїдний елемент у порфіриновому кільці. Лікарський засіб, приготовлений відповідно до першого або другого аспектів даного винаходу, може бути приготовлений в різних концентраціях залежно від ефективності/токсичності використовуваної сполуки та показання, за яким його використовують. Краще, цей лікарський засіб містить дану сполуку в концентрації 0,1 мкМ - 1 мкМ, ще краще, 1 мкМ - 100 мкМ, 5 мкМ - 50 мкМ, 10 мкМ 50 мкМ, 20 мкМ - 40 мкМ, і найкраще, приблизно 30 мкМ. Для застосувань in vitro, готові форми мо («Сполука 19 жуть містити більш низьку концентрацію сполуки, наприклад, 0,0025 мкМ - 1 мкМ. Особі із кваліфікацією в даній області буде зрозуміло, що сполука, використовувана в першому та другому аспектах даного винаходу, буде звичайно вводитися в суміші з придатним фармацевтичним ексципієнтом, розріджувачем або носієм, вибраним з урахуванням передбачуваного способу введення та стандартної фармацевтичної практики (наприклад, див. Remington: The Science and Practice of Pharmacy, 19th edition, 1995, Ed. Alfonso Gennaro, Mack Publishing Company, Pensylvania, USA). Придатні способи введення обговорюються нижче та включають місцеву (локальну), внутрішньовенну, пероральну, легеневу, назальну, вушну, очну доставку, введення в сечовий міхур та в центральну нервову систему. Наприклад, для локального введення, наприклад, на ділянку шкіри або ділянку рани, ці сполуки можуть вводитися у формі лосьйону, розчину, крему, гелю, мазі або порошку-присипки (наприклад, див. Remington, supra, pages 1586-1597). Таким чином, ці сполуки можуть бути приготовлені у вигляді придатної мазі, що містить активну сполуку, суспендовану або розчинену, наприклад, у суміші з одним або декількома з таких компонентів: мінеральним маслом, рідким вазеліном, білим вазеліном, пропіленгліколем, поліоксіетиленомполіоксипропіленом, емульгуючим воском та водою. Альтернативно, вони можуть бути приготовлені у вигляді придатного лосьйону або крему, що містять активну сполуку, суспендовану або розчинену, наприклад, у суміші з одним або декількома з таких компонентів: мінеральним маслом, моностеаратом сорбітану, поліетиленгліколем, рідким парафіном, полісорбатом 60, воском, що містить цетилові ефіри, -лаурилсульфатом, спиртом (наприклад, етанолом, цетеариловим спиртом, 2октилдодеканолом, бензиловим спиртом) і водою. В кращому варіанті здійснення, цей лікарський засіб (наприклад, лосьйон, розчин, крем, гель або мазь) має водну основу. Готові форми, придатні для локального введення в порожнину рота, додатково включають таблетки, що містять активний інгредієнт в ароматизованій основі, звичайно, сахарозі або аравійській чи трагакантовій камеді; пастилки, що містять активний інгредієнт в інертній основі, такій як желатин та гліцерин, або сахароза чи аравійська камедь; і рідини для полоскання ротової порожнини, що містять активний інгредієнт у придатному рідкому носії. Лікарський засіб, приготовлений відповідно до першого або другого аспектів даного винаходу, може також вводитися інтраназально або за допомогою інгаляції і, краще, доставлятися у формі презентації інгаляційного сухого порошку або аерозольного спрею з контейнера, що перебуває під тиском, помпи, пульверизатора або розпилювача з використанням придатного пропелента, наприклад, дихлордифторметану, трихлорфторметану, дихлортетрафторетану, гідрофторалкану, такого як 1,1,1,2-тетрафторетан (HFA 134A3) або 1,1,1,2,3,3,3-гептафторпропан (HFA 227EA3), діоксиду вуглецю або іншого придатного газу. У випа 94027 20 дку аерозолю, що перебуває під тиском, одиниця дози може бути визначена забезпеченням клапана для доставки відміряної кількості. Контейнер, що перебуває під тиском, помпа, спрей або розпилювач можуть містити розчин або суспензію активної сполуки, наприклад, з використанням як розчинника суміші етанолу та пропелента, що можуть додатково містити пом'якшуючий компонент, наприклад, тріолеат сорбітану. Можуть бути приготовлені капсули та картриджі (виготовлені, наприклад, з желатину) для використання в інгаляторі або інсуфляторі, які містять порошкоподібну суміш сполуки за даним винаходом та придатну порошкоподібну основу, таку як лактоза або крохмаль. Аерозольні або сухі порошкоподібні форми, краще, готовлять таким чином, що кожна відміряна доза або «викид» містить щонайменше 1 мг сполуки для доставки пацієнту. Має бути зрозуміло, що загальна доза, надана з аерозолем, буде варіюватися від пацієнта до пацієнта та від показання до показання і може вводитися у вигляді єдиної дози або, частіше, розділеними дозами протягом дня. Альтернативно, можуть бути також використані інші загальноприйняті способи введення, відомі в даній області; наприклад, лікарський засіб, приготовлений відповідно до першого або другого аспектів даного винаходу, може доставлятися перорально, букально або під'язично у формі таблеток, капсул, овальних коржів, еліксирів, розчинів або суспензій, які можуть містити ароматизуючі та барвні агенти, для негайного, затриманого або контрольованого вивільнення. Цей лікарський засіб може також вводитися внутрішньоочним способом (див. нижче), внутрішньовушним способом або за допомогою внутрішньопорожнинної ін'єкції. Цей лікарський засіб може також вводитися парентерально, наприклад, внутрішньовенно, внутрішньоартеріально, внутрішньоочеревинно, внутрішньооболонково, інтравентрикулярно, внутрішньогрудинно, інтракраніально, внутрішньом'язово або підшкірно (у тому числі за допомогою набору тонких голок або з використанням безголкової технології Powderject®), або він може вводитися інфузійними способами. Ці лікарські засоби найкраще використовувати у формі стерильного водного розчину, який може містити інші речовини, наприклад, достатню кількість солей або глюкози, щоб зробити цей розчин ізотонічним із кров'ю. Ці водні розчини повинні бути придатним образом забуференими (краще, до pH 3-9), якщо це необхідно. Приготування придатних парентеральних форм при стерильних умовах легко здійснюється стандартними фармацевтичними способами, добре відомими фахівцям із кваліфікацією в даній області. Композиції, придатні для парентерального введення, включають водні та неводні стерильні ін'єкційні розчини, які можуть містити антиоксиданти, буфери, бактеріостати та розчинені речовини, що роблять цю композицію ізотоничною із кров'ю передбачуваного реципієнта; і водні та неводні стерильні суспензії, які можуть включати суспендувальні агенти та загусники. Ці композиції можуть бути представлені в уніфікованій (стандартній) 21 дозі або в багатодозових контейнерах, наприклад, у запаяних ампулах та флаконах, і можуть зберігатися у висушеному заморожуванням (ліофілізованому) стані, що потребує тільки додавання стерильного рідкого носія, наприклад, води для ін'єкційних розчинів, безпосередньо перед використанням. Розчини та суспензії для незапланованих ін'єкцій можуть бути приготовлені зі стерильних порошків, гранул і таблеток описаного раніше типу. Цей лікарський засіб може також вводитися внутрішньоочним способом, зокрема, для лікування очних захворювань. Для офтальмічного застосування ці сполуки можуть бути приготовлені у вигляді мікронізованих суспензій в ізотонічному стерильному сольовому розчині, що має доведений pH, або, краще, у вигляді розчинів в ізотонічному стерильному сольовому розчині, що має доведений pH, необов'язково, в комбінації з консервантом, таким як хлорид бензилалконію. Альтернативно, вони можуть бути приготовлені в мазі, такій як вазелін. Для ветеринарного застосування сполуку вводять у вигляді придатної прийнятної композиції відповідно до звичайної ветеринарної практики, і ветеринар-хірург буде визначати схему введення доз та спосіб введення, які будуть найбільш придатними для конкретної тварини. В кращому варіанті здійснення першого та другого аспектів даного винаходу, цей лікарський засіб є засобом для перорального або парентерального введення. Таким чином, ці лікарські засоби призначені, краще, для лікування системних мікробних інфекцій. Ці лікарські засоби можуть зберігатися в будьякому придатному контейнері або посудині, відомих в даній області. Особам із кваліфікацією в даній області буде зрозуміло, що цей контейнер або посудина повинен бути, краще, герметичним та/або стерилізованим. Краще, цей контейнер або посудина виготовлені із пластику, такого як поліетилен. Має бути зрозуміло, що лікарські засоби, приготовлені відповідно до першого або другого аспектів даного винаходу, можуть бути також використані для вбивання ряду бактерій, мікоплазм, дріжджів, грибків та/або вірусів. Крім того, має бути зрозуміло, що ці лікарські засоби можуть бути використані для попередження та/або лікування інфекції такими мікроорганізмами, тобто, ці лікарські засоби придатні для профілактичної та/або терапевтичної терапії. Наприклад, такий лікарський засіб може бути використаний для попередження або зменшення поширення чи перенесення патогену до інших суб'єктів, наприклад, пацієнтів, працівників охорони здоров'я і т.д. Краще, лікарські засоби, приготовлені відповідно до першого або другого аспектів даного винаходу, призначені для застосування в лікувальній та/або профілактичній терапії бактеріальних інфекцій, таких як грампозитивні коки (наприклад, Streptococcus), грамнегативні коки (наприклад, Neisseria), грампозитивні бацили (наприклад, види Corynebacterium), грамнегативні бацили (наприклад, Escherichia coli), кислотостійкі бацили (на 94027 22 приклад, типовий Mycobacterium), і в тому числі інфекцій, що спричинюють абсцеси, кісти, інфекцій крові (бактеріємій), дерматологічних інфекцій, раневих інфекцій, артриту, інфекцій сечових шляхів, панкреатиту, запального захворювання тазової області, перитоніту, простатиту, інфекцій вагіни, порожнини рота (у тому числі зубних інфекцій), ока та/або вуха, виразок та інших локалізованих інфекцій; інфекцій Actinomyces; грибкових інфекцій, таких як Candida albicans, Aspergillus та Blastomyces; вірусних інфекцій, таких як ВІЛ, енцефаліт, гастроентерит, геморагічна лихоманка, хантавірус, вірусний гепатит, герпесвірус (наприклад, цитомегаловірус, вірус Епштейна-Барр, герпесвірус мавп, простий герпес і вірус вітряної віспи); протозойних інфекцій, таких як амебіаз, бабезіоз, кокцидіоз, криптоспоридіоз, лямбліоз, лейшманіоз, трихомоніаз, токсоплазмоз і малярія; спричинюваних гельмінтами інфекцій, таких як інфекції, спричинювані нематодами, цестодами та трематодами, наприклад, аскаридоз, анкілостомна анемія, лімфатичний філяріатоз, онхоцеркоз, шистосомоз і токсокароз; спричинюваних пріонами захворювань і запальних захворювань, таких як ревматизм м'яких тканин, остеоартрит, ревматоїдний артрит та спонділоартропатії. Ще краще, ці лікарські засоби призначені для застосування в лікуванні та/або профілактиці інфекцій, спричинюваних грампозитивними бактеріями та/або грамнегативними бактеріями. Найкраще, сполуки за даним винаходом призначені для застосування в лікуванні та/або профілактиці інфекцій, спричинюваних грампозитивними бактеріями. Ці лікарські засоби використовують, краще, для вбивання мікроорганізмів, наприклад, бактерій, мікоплазм, дріжджів, грибків і вірусів. Ці лікарські засоби особливо придатні для вбивання бактерій, які розвили стійкість до загальноприйнятих антибіотичних способів лікування, таких як метицилін-стійкий Staphylococcus aureus (MRSA). Особам із кваліфікацією в даній області буде зрозуміло, що ці лікарські засоби придатні для лікування всіх мікробних інфекцій, незалежно від того, є ділянка інфекції легко доступною чи ні. Таким чином, ці лікарські засоби можуть знайти застосування в лікуванні інфекцій, які не можуть лікуватися загальноприйнятими агентами фотодинамічної терапії. Краще, ця мікробна інфекція находиться на недоступній для світла поверхні або в недоступній для світла ділянці. Дози розглянутих сполук у лікарських засобах, приготовлених відповідно до першого або другого аспектів даного винаходу, будуть залежати від декількох факторів, у тому числі від конкретних використовуваних сполук, композиції, способу введення та показання, за яким використовується ця сполука. Однак, дози будуть звичайно находитися в діапазоні 0,01-20 мг сполуки на кілограм маси тіла, краще, 0,1-15 мг/кг, наприклад, 1-10 мг/кг маси тіла. В кращому варіанті здійснення, лікарські засоби відповідно до першого або другого аспектів даного винаходу використовують у комбінації із загальноприйнятими антимікробними агентами. 23 Наприклад, ці сполуки можуть бути використані в комбінації з одним чи декількома з таких загальноприйнятих антибіотиків: антибактеріальними агентами, наприклад, такими як природні та синтетичні пеніциліни та цефалоспорини, сульфонаміди, еритроміцин, каноміцин, тетрациклін, хлорамфенікол, рифаміцин та, в тому числі, гентаміцин, ампіцилін, бензипеніцилін, бенетамін-пеніцилін, бензатинпеніцилін, фенетицилін, феноксиметилпеніцилін, прокаїнпеніцилін, клоксацилін, флуклоксацилін, метицилін-натрій, амоксицилін, бакампіциліну гідрохлорид, циклацилін, мезлоцилін, півампіцилін, талампіциліну гідрохлорид, карфецилін-натрій, піперацилін, тикарцилін, мецилінам, пірмецилінан, цефаклор, цефадроксил, цефотаксим, цефокситин, цефсулодин-натрій, цефтазидим, цефтизоксим, цефуроксим, цефалексин, цефалотин, цефамандол, цефазолін, цефрадин, латамоксефдинатрій, азтреонам, хлортетрацикліну гідрохлорид, кломоциклін-натрій, демеклоцидину гідрохлорид, доксициклін, лімециклін, міноциклін, окситетрациклін, амікацин, фраміцетину сульфат, неоміцину сульфат, нетилміцин, тобраміцин, колістин, натрію фусидат, сульфат поліміксину В, спектиноміцин, ванкоміцин, сульфалоксат кальцію, сульфаметопіразин, сульфадіазин, сульфадимідин, сульфагуанідин, сульфасечовина, капреоміцин, метронідазол, тинідазол, циноксацин, ципрофлоксацин, нітрофурантоїн, гексамін, стрептоміцин, карбеніцилін, колістиметат, поліміксин В, фуразолідон, налідиксова кислота, триметоприм-сульфаметоксазол, кліндаміцин, лінкоміцин, циклосерин, ізоніазид, етамбутол, етіонамід, піразинамід і т.п.; протигрибковими агентами, наприклад, такими як міконазол, кетоконазол, ітраконазол, флуконазол, амфотерицин, флуцитозин, гризеофулвін, натаміцин, ністатин і т.п.; та антивірусними агентами, такими як ацикловір, AZT, ddl, амантадину гідрохлорид, інозин-пранобекс, відарабін і т.п. У наступному кращому варіанті здійснення, ці лікарські засоби включають агенти посилення проникності та/або вводяться разом з агентами посилення проникності, такими як полі(етиленімін), або антибіотичними агентами, які виявляють здатність посилювати проникність (наприклад, поліміксином або колістином). Лікарські засоби, приготовлені відповідно до першого або другого аспектів даного винаходу, є особливо придатними для застосування в лікуванні чи профілактиці одного чи декількох з таких показань: Імпетиго Імпетиго є у високому ступені заразною інфекцією. Воно є найбільш частою інфекцією у дітей. Імпетиго має дві класичні форми: небульозне імпетиго та бульозне імпетиго. Небульозне імпетиго, також назване контагіозним (заразним) імпетиго, є відповідальним за приблизно 70% випадків імпетиго. Ушкодження звичайно зникають за 2-3 тижні без лікування. Імпетиго може бути також ускладненням інших шкірних захворювань, таких як короста, вітряна віспа, атопічний дерматит і хвороба Дар'є. 94027 24 (а) Небульозне імпетиго Тип бактерій Небульозне імпетиго є інфекцією, спричинюваною в основному бета-гемолітичними стрептококами Групи A (Streptococcus pyogenes), Staphylococcus aureus або комбінацією цих двох організмів (див. Andrews' diseases of the skin: Clinical dermatology, 9th ed. (2000) edited by Odom R.B. editor Saunders p.312-4). Стрептококи, що не належать до групи А (Групи В, С та D), можуть бути відповідальними за рідкі випадки імпетиго, а стрептококи Групи В асоційовані з імпетиго у немовлят. Типи ран Небульозне імпетиго є поверхневою, інтраепідермальною, унілокулярною везикулопустулярною інфекцією. Ураження небульозного імпетиго звичайно починаються на шкірі особи або на кінцівках після травми. Як правило, інтактна шкіра є стійкою до ураження імпетиго. Клінічні вияви імпетиго розвиваються впорядковано від невеликого пухирця або пустули, які прогресують до лускатих струпів кольору меду. Ці ушкодження звичайно мають 2 см у діаметрі. Ушкодження мають тенденцію висихати, залишаючи дрібні струпи без рубцювання. Ушкодження звичайно є мінімально симптоматичними. Рідко може бути присутньою еритема, асоційована зі слабким болем або слабкою сверблячкою. Ця інфекція поширюється на суміжні та дистальні області внаслідок інокуляції іншого поранення через розчісування. Місцерозташування бактерій Небульозне імпетиго є поверхневою стрептококовою або стафілококовою інфекцією, що локалізується в субкорнеальному (безпосередньо під роговим шаром) шарі шкіри (див. фігуру 1). Більш конкретно, інфекція у випадку імпетиго обмежена гістопатологічно високо диференційованими, верхніми епідермальними кератиноцитами. Як тільки бактерії проникають у шкіру, вони починають розмножуватися. Гістопатологія полягає у вкрай поверхневому запаленні біля воронкоподібної верхньої частини пухирців, які належать волосяним фолікулам і сальним залозам. Утворюється субкорнеальна везикопустула, що містить невелику кількість розсіяних коків, разом із залишками поліморфно-ядерних лейкоцитів та епідермальних клітин. У дермі спостерігається слабка запальна реакція - розширення судин, набряк та інфільтрація поліморфноядерних лейкоцитів (Andrews' diseases of the skin, supra, p. 312-4). (b) Бульозне імпетиго Тип бактерій Бульозне імпетиго викликається насамперед штамами Staphylococcus aureus, які продукують ексфоліативні токсини (Sadick et al., 1997, Dermatologic Clinics 15(2):341-9). Типи ран Бульозне імпетиго гістологічно характеризується субкорнеальним розщепленням та інфільтратом поліморфно-ядерних лейкоцитів, які мігрують крізь епідерміс та накопичуються між 25 зернистим та роговим шарами шкіри. Невеликі або великі поверхневі тендітні пухирі присутні на тулубі та кінцівках. В'ялі пухирі та вологі ерозії з навколишньою еритемою є характерними для цих субкорнеальних інфекцій. Часто в момент прояву видні тільки залишки розірваних пухирів. Це відділення епідермісу обумовлене екзотоксином, продукованим Staphylococcus aureus. Місцерозташування бактерій Бульозне імпетиго є поверхневою стафілококовою інфекцією, що має місце в роговому шарі та безпосередньо під роговим шаром (див. фігуру 1). Вважається, що бульозне імпетиго обумовлене ексфоліативним токсином, продукованим деякими Staphylococcus aureus, прикріпленими до клітин рогового шару. Атопічний дерматит (АР) Атопічний дерматит, також названий атопічною екземою, є хронічним запаленням шкіри, що приводить до сверблячого висипу, особливо в згинах, тобто, під коліньми, у передній частині ліктів, кистях, шиї та очних віках. Інфекція цього висипу є звичайною і викликає додаткове запалення та сверблячку. Звичайно екзема виявляється у віці 1-6 місяців. Приблизно 60% пацієнтів мають перший прояв у віці 1 року, і 90% - у віці 5 років. Поява атопічного дерматиту в підлітковому віці або пізніше є незвичайною і повинна спонукати до розгляду іншого діагнозу. Маніфестації хвороби змінюються з віком. Тип бактерій Бактерії та їхні суперантигени сприяють патогенезу AD. Staphylococcus aureus колонізує шкіру 90% пацієнтів з AD (хронічні екзематозні ушкодження) і тільки 5% неатопічних пацієнтів. Щільність колонізації Staphylococcus aureus може досягати 107 колонієутворювальних одиниць на см2 без клінічних ознак інфекції у пацієнтів з AD. Крім того, нормальна на вигляд шкіра атопічних пацієнтів, що не має ушкоджень, містить збільшені кількості Staphylococcus aureus. Причина надлишкового росту Staphylococcus aureus при атопічному дерматиті, хоч і набагато менш тяжкому або взагалі не спостережуваному при таких захворюваннях, як псоріаз, є невідомою. Білок А індукує набагато менш сильну реакцію у атопічних пацієнтів, ніж у здорових людей або пацієнтах із псоріазом, але це може бути результатом, а не причиною колонізації. Недавно увага була привернута до ліпідів шкіри, і є певні докази того, що у пацієнтів з атопічним дерматитом існує недостатність деяких жирних кислот, які можуть контролювати стафілококову колонізацію. Суперантигени є унікальною групою білків, продукованих бактеріями та вірусами, які обходять деякі елементи звичайної, антигенопосередкованої послідовності імунних реакцій. У той час як звичайні антигени активують приблизно 0,01%-0,1% Т-клітин організму, суперантиген є здатним стимулювати 5%-30% популяції Т-клітин. S. aureus може загострювати або підтримувати запалення шкіри при AD за рахунок секреції групи 94027 26 екзотоксинів, що діють як суперантигени. Пацієнти з AD мають змінений шкірний бар'єр, вторинний відносно недостатності церамідів у роговому шарі. Було зроблене припущення, що проникнення через шкіру цих екзотоксинів може викликати активацію Т-клітин, макрофагів, LC і гладких клітин, що приводить до вивільнення цитокінів та медіаторів гладких клітин. Зрозуміло, що ці події можуть забезпечувати основу для запалення при хронічному AD. Триває обговорення того, чи є колонізація S. Aureus і локальна секреція суперантигену первинним або вторинним явищем при AD (Andrew's diseases of skin, Chap. 5, Atopic Dermatitis, Eczema, and non-infectious immunodeficiency disorders, p.6976). Шкірні вірусні, грибкові та бактеріальні інфекції зустрічаються частіше у пацієнтів з AD. Вірусні інфекціїузгоджуються з недостатністю Т-клітин і включають простий герпес (місцевий або генералізований, тобто, герпетиформну екзему), контагіозний молюск і папіломавірус людини. Поверхневі грибкові інфекції Trichophyton rubrum та Pityrosporon ovale також часто зустрічаються. Бактеріальні інфекції, зокрема, інфекції S. aureus, є надзвичайно частими. Суперінфекція приводить до утворення струпів медяного кольору, сильної серозної мокнучої екземи або фолікуліту. Тип ран Гострі ушкодження мають вигляд еритематозних папул, пухирців та ерозій; хронічне захворювання складається з фібротичних папул і стовщеної, ліхеніфікованої шкіри. Виявлення збільшених кількостей патогенних стафілококів часто зв'язане з мокнуттям, струпоутворенням, фолікулітом та аденопатією. Під час атопічного дерматиту частою є вторинна стафілококова інфекція та часто зустрічаються локальний набряк і регіонарна аденопатія. Імпетиго може бути різновидом вторинної інфекції атопічного дерматиту. Гістологія атопічного дерматиту находиться в діапазоні від гострого губкоподібного дерматиту до ліхеноїдної простої хронічної екземи, залежно від морфології біопсії шкірного ушкодження. Місцерозташування бактерій Клітинні стінки Staphylococcus aureus мають рецептори, так звані адгезини, для епідермального та дермального фібронектину та фібриногену. Було показано, що зв'язування Staphylococcus aureus опосередковане фібриногеном і фібронектином у пацієнтів з AD. Оскільки шкіра пацієнтів з AD не має інтактного рогового шару, дермальний фібронектин може не мати покриття, і це збільшує прикріплення Staphylococcus aureus. Фібрилярні та аморфні структури були простежені між клітинами Staphylococcus aureus і корнеоцитами, і вони можуть приводити до бактеріальної біоплівки. Спостерігали, що Staphylococcus aureus проникає у внутрішньошньоклітинні простори, що дозволяє припустити, що ліпіди поверхні шкіри є ушкодженими у пацієнтів з AD (див. Breuer K. et al., 2002, British Journal of Dermatology, 147: 55-61). Виразки Шкірні виразки, такі як діабетичні виразки підошов, пролежні та хронічні венозні виразки, є 27 відкритими ураженнями або ушкодженнями шкіри, що характеризуються виснаженням тканини та іноді супроводжуються утворенням гною. Шкірні виразки можуть мати різні причини та впливати на різні популяції, але всі вони мають тенденцію дуже повільного загоєння, якщо взагалі гояться, і їхнє лікування може бути дуже важким і дорогим. Тип бактерій Поверхневі пролежні не пов'язані з проблемами основної інфекції. Аеробні мікроорганізми при низьких рівнях будуть забруднювати пролежні, але не будуть перешкоджати своєчасному загоєнню. Однак, глибокі пролежні можуть вторинно інфікуватися і може виникати остеомієліт. Пролежні з некротичною тканиною містять високі рівні аеробних та анаеробних мікроорганізмів у порівнянні з некротичними виразками; часто є присутнім гнильний запах при інвазії тканин анаеробними мікроорганізмами. Таким чином, стратегія лікування полягає у видаленні некротичної тканини з рани, що зменшує присутність анаеробних мікроорганізмів. Інфекції пролежнів звичайно є полімікробними і можуть містити Streptococcus pyogenes, ентерококи, анаеробні стрептококи, Enterobacteriaceae, Pseudomonas aeruginosa, Bacteroides fragilis та Staphylococcus aureus. Тип ран Пролежень стадії І: набряк інтактної шкіри, що не блідне, який вважається ушкодженням, що передвіщає утворення виразки шкіри. Пролежень стадії II: часткова втрата товщини шкіри, що охоплює епідерміс та/або дерму. Ця виразка є поверхневою і представлена клінічно у вигляді садна, пухиря або дрібного кратера. Оскільки епідерміс може втрачати цілісність через подряпини, пухирі або дрібні кратери, ці виразки треба оцінювати на наявність ознак вторинних інфекцій. Пролежень стадії III: повна втрата товщини шкіри, що включає ушкодження або некроз підшкірної тканини, що може простиратися вниз до підстильної фасції, але не через неї. Ця виразка представлена клінічно у вигляді глибокого кратера, який може заходити під сусідню тканину чи ні. Стадія IV: повна втрата товщини шкіри із сильною деструкцією, некрозом тканини або ушкодженням м'яза, кістки або підтримуючих структур, таких як сухожилля або суглобні капсули. Місцерозташування бактерій Існують три мікробіологічних стани, які є можливими в рані: забруднення, колонізація та інфекція. Забруднення характеризується як проста присутність мікроорганізмів у рані, але без проліферації. Звичайно приймається, що всі рани, незалежно від етіології, є забрудненими. Колонізація характеризується як наявність розмноження мікроорганізмів у рані, але без реакції хазяїна. Колонізація є звичайним станом у хронічних ранах, таких як венозні виразки та пролежні, і вона необов'язково затримує процес загоєння. Коли бактерії інвазують здорові тканини та продовжують проліферувати у них настільки, що їхня присутність та їхні побічні продукти індукують або пригнічують імунну реакцію хазяїна, цей мікробний стан відомий як інфекція. Класичні ознаки та симптоми 94027 28 інфекції включають місцеве почервоніння, біль і набрякання, лихоманку і зміни кількості та характеру раневих ексудатів. Легеневі інфекції Лікарські засоби за даним винаходом є придатними також для лікування пацієнта, що має інфекційне захворювання легень. Легенева інфекція може мати місце з різними бактеріальними родами та видами, які включають Mycobacterium tuberculosis (tuberculosis), Pseudomonas (первинна причина смерті пацієнтів з муковісцидозом), Streptococcus, Staphylococcus pneumoniae, Klebsiella, Toxoplasma і т.д. Легенева інфекція може також зустрічатися з різними вірусними штамами та умовними патогенами (грибками, паразитами). Оскільки стійкість патогенів легень до класичних антибіотичних способів терапії зростає, фотодинамічна терапія представляє альтернативний спосіб елімінації цих шкідливих організмів. Лікарські засоби за даним винаходом можуть вводитися в легені різними способами. Наприклад, ця сполука може вводитися через дихальні шляхи (наприклад, інтратрахеально, інтрабронхіально або інтраальвеолярно) або через стінку грудної клітки тіла. Додаткові показання Лікарські засоби за даним винаходом придатні також для лікування та/або профілактики таких інфекцій: системних інфекцій, бактеріємії (інфекції крові), періодонтиту та інших зубних інфекцій, каріозного розпаду та зубних бляшок, інфекцій сечових шляхів, вагінальних інфекцій, захворювань, спричинюваних всіма мікроорганізмами, у тому числі пріонами, вірусних інфекцій, дріжджових інфекцій, інфекцій горла, виразок шлунка (спричинюваних Heliobacter pylori), інфекцій опікових вогнищ і трансплантатів шкіри, отиту (вушної інфекції), бактеріального кон'юнктивіту та інших очних хвороб, інфікованих кісток, що зазнали дії мікроорганізмів під час хірургічних процедур, і атак біотероризму. Придатні ветеринарні застосування включають лікування та/або профілактику ящуру, BSE та інвазії паразитів тварин. Таким чином, наступні аспекти даного винаходу забезпечують таке: (і) Застосування сполуки, описаної вище, у приготуванні лікарського засобу для лікування та/або профілактики дерматологічної інфекції; (іі) Застосування сполуки, описаної вище, у приготуванні лікарського засобу для лікування та/або профілактики інфекції легенів; (ііі) Застосування сполуки, описаної вище, у приготуванні лікарського засобу для лікування та/або профілактики раневої інфекції та/або виразки; (iv) Спосіб лікування пацієнта, що потребує лікування, антимікробним агентом, який передбачає введення цьому пацієнту сполуки, описаної вище, причому спосіб не включає опромінення цієї сполуки стимулом, активуючим антимікробну активність; і (ν) Спосіб лікування пацієнта, що потребує лікування, антимікробним агентом, що передбачає введення цьому пацієнту сполуки, описаної вище, 29 причому спосіб включає першу фазу лікування, під час якої цю сполуку не опромінюють стимулом, що активує антимікробну активність, з наступною другою фазою лікування, коли цю сполуку опромінюють стимулом, що активує антимікробну активність (таким як ультразвук та/або світло). Краще, перша фаза лікування триває щонайменше 10 хвилин, наприклад, щонайменше 20 хвилин, 30 хвилин, 40 хвилин, 50 хвилин, 1 годину, 2 години, 3 години, 5 годин, 12 годин та 24 години. Лікарські засоби, приготовлені відповідно до першого та другого аспектів даного винаходу, можуть бути також використані для вбивання мікроорганізмів in vitro. Наприклад, цей лікарський засіб може бути також використаний у формі стерилізуючого розчину або промивання для попередження росту мікроорганізмів на поверхні чи субстраті, наприклад, у клінічному середовищі (наприклад, в операційній) або домашньому середовищі (наприклад, на робочій поверхні кухні, при пранні білизни, наприклад, постільної білизни). Краще, такий лікарський засіб включає антимікробну сполуку в розчині в концентрації 1-100 мкг/мл. Краще, цей розчин додатково включає поверхнево-активний агент або сурфактант. Придатні сурфактанти включають аніоногенні сурфактанти (наприклад, аліфатичний сульфонат), амфотерні та/або цвітеріонні сурфактанти (наприклад, похідні аліфатичного четвертинного амонію, сполуки фосфонію та сульфонію) і неіоногенні сурфактанти (наприклад, аліфатичні спирти, кислоти, аміди або алкілфеноли з алкіленоксидами). Краще, цей поверхнево-активний агент присутній у концентрації 0,5-5 % мас. Ці стерилізуючі розчини є особливо придатними для застосування в умовах лікарні. Наприклад, ці стерилізуючі розчини можуть бути використані для стерилізації хірургічних інструментів і поверхонь операційної, а також рук і рукавичок персоналу операційної. Крім того, ці стерилізуючі розчини можуть бути використані під час хірургії, наприклад, для стерилізації оголених кісток. В усіх випадках, цей розчин наносять на поверхню, що підлягає стерилізації. Цей лікарський засіб може бути також використаний для дезінфекції крові та продуктів крові та у діагностиці бактеріального забруднення або інфекції. У застосуваннях як in vitro, так і in vivo лікарським засобом, приготовленим відповідно до першого та другого аспектів даного винаходу, краще, обробляють мікроорганізми-мішені (або поверхні/області, що підлягають обробці) протягом щонайменше п'яти хвилин. Наприклад, час обробки може становити щонайменше 10 хвилин, 20 хвилин, 30 хвилин, 40 хвилин, 50 хвилин, 1 годину, 2 години, 3 години, 5 годин, 12 годин та 24 години. Далі будуть описані кращі, необмежуючі варіанти здійснення даного винаходу за допомогою прикладів з посиланням на супутні креслення, на яких: Фігура 1 показує схематично структуру шкіри. 94027 30 Фігура 2 показує клітинну токсичність дермальних фібробластів здорової людини після 5 хвилин, 1 години і 4 годин інкубації зі сполукою 10. NHDF інкубували з різними концентраціями сполуки 10 протягом 5 хв., 1 год. та 4 год. (0 мкМ, 0,01 мкМ, 0,1 мкМ, 1,0 мкМ, 10 мкМ). Потім клітини інкубували протягом 24 год. у темряві. Токсичність вимірювали стандартним МТТ-аналізом. Життєздатність клітин нормалізували відносно 1, тобто, значення для контрольних клітин приймали за 1. Сіра пунктирна лінія: 5-хвилинна інкубація; чорна пунктирна лінія: 1-годинна інкубація; чорна лінія: 4годинна інкубація; (n=3, середнє ± SD (стандартне відхилення)). Фігура 3 показує клітинну токсичність епідермальних кератиноцитів здорової людини після 5 хвилин, 1 години та 4 годин інкубації зі сполукою 10. NHEK інкубували з різними концентраціями сполуки 10 протягом 5 хв., 1 год. та 4 год. (0 мкМ, 0,01 мкМ, 0,1 мкМ, 1,0 мкМ, 10 мкМ). Потім клітини інкубували протягом 24 год. у темряві. Токсичність вимірювали стандартним МТТ-аналізом. Життєздатність клітин нормалізували відносно 1, тобто, значення для контрольних клітин приймали за 1. Червона пунктирна лінія: 5-хвилинна інкубація; чорна пунктирна лінія: 1-годинна інкубація; синя пунктирна лінія: тільки 4-годинна інкубація; (n=3, середнє ± SD (стандартне відхилення)). Фігура 4 показує хімічну стабільність сполуки 10, приготовленої (А) у вигляді твердої речовини, (В) у воді та (С) у забуференому фізіологічному розчині (ЗФР). Фігура 5 показує тривимірний графік стабільності (вимірюваної методом ВЕРХ) сполуки 10 після 21 дня в буфері ЗФР. Фігура 6 показує стабільність протягом 8 тижнів різних композицій (А) сполуки 1, (В) сполуки 8, (С) сполуки 12 та (D) сполуки 10. Фігура 7 показує пролонговану стабільність протягом 17 тижнів різних композицій (А) сполуки 10 та (В) сполуки 8. Приклади Приклад А: Синтез типових сполук Матеріали та способи Виміри ЯМР 1 Н ЯМР-спектри реєстрували на приладі Brucker B-ACS60 (300 МГц) з використанням TMS як внутрішнього стандарту. Хімічні зсуви наведені в м.ч., а константи зв'язування - в Гц у зазначеному розчиннику. Деякі абревіатури для ЯМР: синглет (с), широкий синглет (шир.с), дублет (д), триплет (т), квартет (к), квінтет (квінт), мультиплет (м). Хімічні препарати Всі розчинники та реагенти купували у Aldrich, Fluka, Merck та Lancaster і використовували без додаткового очищення. Дипіролметан одержували, як описано С. Brucker et al., J. Porphyrins Phthalocyanines, 2:455 (1998). Хроматографія Хроматографію на колонці проводили з використанням силікагелю (Merck Silicagel 60, Fluka 60, 0,040-0,063 мм) і Sephadex LH-20 (Pharmacia). Всі 31 розчинники (Synopharm) для хроматографії були технічної чистоти. Абревіатури DDQ: 2,3-дихлор-5,5-диціано-п-бензохінон DMF: Ν,Ν-диметилформамід TFA: трифтороцтова кислота Способи синтезу для тест-сполук Синтезували такі тест-сполуки: Приклади сполук для використання в даному винаході Сполуки 6, 8-10, 12, 23, 25, 28, 31 та 32. Посилальні сполуки (для використання як порівняльні контролі) Сполуки 1, 3, 16, 19, 26, 29, 33, 36, 37, 41 та 46-51. Хімічні проміжні продукти Сполуки 2, 4, 5, 7, 11, 13-15, 17, 18, 20-22, 24, 27, 30, 34, 35, 38, 40 та 42-45. Сполука 1 Тетрахлорид 5,10,15,20-тетракіс-[4-(3триметиламоніопропілокси)феніл]-порфірину До сильно перемішуваної суспензії 5,10,15,20тетракіс-(4-гідроксифеніл)-порфірину (50 мг, 0,07 ммоль) і K2СО3 (230 мг, 1,7 ммоль) у ДМФ (20 мол) додають по краплях розчин (1бромпропіл)триметиламонійброміду (0,27 г, 1,05 ммоль) у ДМФ (5 мл) при 50 °С протягом 30 хвилин. Цю суміш перемішують при 50 °С протягом 15 годин. Після видалення ДМФ при зниженому тиску одержаний залишок розчиняють у метанолі (5 мл) і фільтрують через шар силікагелю (товщина 2 см), підтримуваний на сталевій фриті (з діаметром 3,5 см). Після промивання метанолом (1 л) цей шар елююють оцтовою кислотою. Після випарювання розчинника з елюату одержаний залишок очищають хроматографією на колонці (2,540 см) Sephadex LH20 з елюцією сумішшю нбутанол:вода:оцтова кислота (4:5:1, по об'єму, верхня фаза). Видобутий матеріал розчиняють у мінімальному об'ємі метанолу і цей розчин пропускають через коротку колонку (3,520 см) аніонообмінної смоли (Amberlite IRA 400, хлоридна форма). Видобуту тетрахлоридну сіль сушать під високим вакуумом та одержують у вигляді фіолетової твердої речовини. 1 Н-ЯМР (300 МГц, CD3OD): 2,35-2,50 (bs, 8Н), 3,25-3,35 (bs, 36H), 3,65-3,75 (bs, 8Н), 4,35 (m, 8Н), 7,30, 8,10 (2d, 3J 8,5 Гц, 16Н), 8,80-9,00 (bs, 8H). Сполука 2 5,10,15-трис-(4-гідроксифеніл)-20-(4ундецилоксифеніл)порфірин 94027 32 До сильно перемішуваної суспензії 5,10,15,20тетракіс-(4-гідроксифеніл)-порфірину (400 мг, 0,59 ммоль) і K2СО3 (1,0 г, 7,1 ммоль) у ДМФ (75 мл) додають по краплях розчин 1-бромундекану (0,1 мл, 0,45 ммоль) у ДМФ (10 мл) при 50 °С протягом 30 хвилин і цю суміш перемішують при тій же самій температурі протягом 1,5 годин. Після видалення фільтруванням К2СО3 і видалення при зниженому тиску ДМФ одержаний залишок розчиняють у дихлорметані (200 мл), промивають водою (3150 мл) і розчин сушать (Na2SO4). Розчинник випарюють при зниженому тиску та одержаний залишок розчиняють у суміші толуол:етанол (5:1 по об'єму, приблизно 10 мл) і очищають хроматографією з використанням колонки (550 см) силікагелю (Merck 60). Колонку елююють толуолом з наступною елюцією сумішшю толуол:етилацетат (2:1 по об'єму) і бажаний матеріал, видобутий випарюванням розчинника з придатних фракцій, сушать під високим вакуумом. Продукт одержують у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, d6-ацетон): 0,95 (t, 3J 7,5 Гц, 3Н), 1,25-1,55 (m, 14H), 1,58 (quint, 3J 7,5 Гц, 2H), 1,85 (quint, 3J 7,5 Гц, 2H). 4,16 (t, 3J 7,5 Гц, 2H), 7,20 (d, 3J 8,1 Гц, 2H), 7,25 (d, 3J 8,2 Гц, 6H), 8,008,15 (m, 8H), 8,80-9,10 (m, 8H). Сполука 3 Трихлорид 5,10,15-трис-[4-(3триметиламоніопропілокси)феніл]-20-(4ундецилоксифеніл)порфірину До сильно перемішуваної суспензії сполуки 2 (100 мг, 0,12 ммоль) і K2СО3 (230 мг, 1,7 ммоль) у ДМФ (30 мл) додають розчин (1-бромпропіл)триметиламонійброміду (0,3 г, 16,6 ммоль) у ДМФ (10 мл) при 50 °С протягом 30 хвилин. Цю суміш перемішують при вказаній температурі протягом 12 годин. Після видалення ДМФ при зниженому тиску одержаний залишок розчиняють у метанолі (5 мл) і фільтрують через шар силікагелю (товщи 33 на 2 см), підтримуваний на сталевій фриті (з діаметром 3,5 см). Після промивання метанолом (приблизно 1 л) цей шар елююють сумішшю оцтова кислота:метанол:вода (3:2:1 по об'єму). Після випарювання розчинника з елюату при зниженому тиску одержаний залишок очищають хроматографією на колонці (2,540 см) Sephadex LH20 з елюцією сумішшю н-бутанол:вода:оцтова кислота (5:4:1, по об'єму, верхня фаза). Після видалення розчинника з придатних фракцій елюату при зниженому тиску одержаний залишок розчиняють у метанолі (5 мл) і цей розчин пропускають через коротку колонку (3,520 см) аніонообмінної смоли (Amberlite IRA 400, хлоридна форма). Кінцевий продукт одержують у вигляді трихлоридної солі після видалення розчинника та сушіння під високим вакуумом у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, CD3OD): 0,80 (t, 3J 7,5 Гц, 3Н), 1,15-1,45 (m, 16Н), 1,50-1,60 (bs, 2H), 2,252,45 (bs, 6H), 3,25-3,35 (bs, 27Н), 3,75-3,85 (bs, 6H), 4,18 (t, 3J 7,5 Гц, 2H), 4,40-4,45 (bs, 6H), 7,20-7,40, 7,95-8,15 (2m, 16Н), 8,60-9,00 (bs, 8H). Сполука 4 5-(3,5-диметоксифеніл)-15-ундецилпорфірин До перемішуваного розчину дипіролметану (0,62 г, 4,2 ммоль) у дихлорметані (5 мл) додають 3,5-диметоксибензальдегід (0,35 г, 2,1 ммоль) і додеканаль (0,464 г, 2,52 ммоль) у дегазованому дихлорметані (1 л). Додають по краплях ТФО (0,07 мл, 3,0 ммоль). Цей розчин перемішують при кімнатній температурі в темряві протягом 17 годин в атмосфері аргону. Після додавання DDQ (2,7 г, 12 ммоль) суміш перемішують при кімнатній температурі ще протягом години. Очищення матеріалу, одержаного після видалення розчинника при зниженому тиску, хроматографією на колонці (400 г) силікагелю (Merck 60) з використанням толуолу для елюції дає продукт у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, CDCI3): 0,80 (t, 3J 7,5 Гц, 3Н), 1,10-1,25 (m, 12Н), 1,40 (m, 2H), 1,75 (quint, 3J 7,5 Гц, 2H), 2,45 (quint, 3J 7,5 Гц, 2H), 3,90 (s, 6H), 4,90 (t, 3J 7,5 Гц, 2H), 6,80 (m, 1H), 7,35 (m, 2H), 9,00, 9,25, 9,30, 9,50 (4d, 3J 4,7 Гц, 42Н), 10,15 (s, 2H). Сполука 5 5-(15-ундецилпорфірин-5-іл)бензол-1,3-діол До розчину сполуки 4 (80 мг, 0,133 ммоль) у безводному дихлорметані (80 мл) в атмосфері аргону додають по краплях ВВr3 (5 мл,1М у дихлорметані) при -70 °С і суміш перемішують протя 94027 34 гом 1 години при цій температурі, а потім нагрівають до кімнатної температури та перемішують протягом ночі. Суміш охолоджують до -10 °С і гідролізують додаванням води (2 мл) і перемішуванням протягом 1 години. Додають NаНСО3 (3 г) безпосередньо для нейтралізації. Суміш перемішують протягом додаткових 12 годин і після фільтрування NаНСО3 та видалення дихлорметану під вакуумом одержаний залишок очищають хроматографією на колонці з використанням силікагелю з елюцією дихлорметаном. Після випарювання розчинника з придатних об'єднаних фракцій і сушіння одержаного залишку під високим вакуумом продукт одержують у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, d6-ацетон): 0,75 (t, 3J 7,5 Гц, 3Н), 1,05-1,25 (m, 12H), 1,30-1,40 (m, 2Н), 1,451,50 (m, 2Н), 2,40 (quint, 3J 7,5 Гц, 2H), 4,90 (t, 3J 7,5 Гц, 2Н), 6,65 (m, 1H), 7,18 (m, 2H), 8,60-8,65, 9,00-9,05, 9,35-9,40, 9,55-9,60 (4m, 8H), 10,25 (s, 2H). Сполука 6 Дихлорид 5-[3,5-біс-(3триметиламоніопропілокси)феніл]-15-ундецилпорфірину До сильно перемішуваної суспензії сполуки 5 (80 мг, 0, 14 ммоль) і K2СО3 (230 мг, 1,7 ммоль) у ДМФ (30 мл) додають розчин (1бромпропіл)триметиламонійброміду (0,3 г, 16,6 ммоль) при 50 °С. Цю суміш перемішують при вказаній температурі протягом 18 годин. Після видалення ДМФ при зниженому тиску одержаний залишок розчиняють у метанолі (5 мл) і фільтрують через шар силікагелю (товщина 2 см), підтримуваний на сталевій фриті (з діаметром 3,5 см). Після промивання цього шару метанолом (приблизно 1 л) неочищений продукт елююють сумішшю оцтова кислота:метанол:вода (3:2:1 по об'єму). Придатні фракції збирають і після випарювання розчинника при зниженому тиску одержаний залишок очищають хроматографією на колонці (2,540 см) Sephadex LH-20 з елюцією сумішшю нбутанол:вода:оцтова кислота (5:4:1, по об'єму, верхня фаза). Після видалення розчинника з придатних фракцій при зниженому тиску одержаний залишок розчиняють у метанолі (5 мл) і цей розчин пропускають через коротку колонку (3,520 см) аніонообмінної смоли (Amberlite IRA 400, хлоридна форма). Після збирання елюату, розчинник видаляють при зниженому тиску та одержаний залишок сушать під високим вакуумом з одержанням дихлоридної солі у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, CD3OD): 0,75 (t, 3J 7,5 Гц, 3Н), 1,05-1,20 (m, 14Н), 1,45-1,50 (m, 2H), 2,052,15 (m, 4H), 2,15-2,20 (m, 2H), 2,95 (s, 18Н), 3,353,45 (m, 4H), 3,95 (t, 3J 7,5 Гц, 4H), 4,55 (t, 3J 7,5 Гц, 35 2H), 6,85 (m, 1H), 7,35 (m, 2H), 8,85-8,90, 9,15-9,20, (3m, 8H), 10,10 (s, 2H). Сполука 7 5,15-біс-[4-(3-бромпропілокси)феніл]порфірин До перемішуваного розчину дипіролметану (0,61 г, 4,1 ммоль) і 4-(3бромпропілокси)бензальдегіду (1,03 г, 4,2 ммоль) у дегазованому дихлорметані (1 л) додають по краплях ТФО (0,07 мл, 1,5 ммоль). Розчин перемішують при кімнатній температурі в темряві в атмосфері аргону протягом 17 годин. Після додавання DDQ (2,76 г, 0,012 ммоль) цю суміш перемішують при кімнатній температурі додатково протягом години. Фільтрування через силікагель (Fluka 60, 100 г) з використанням дихлорметану для елюції дає неочищений продукт, що після обробки сумішшю дихлорметан:н-гексан дає чистий продукт у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, C6D6): -3,15 (2Н, s), 2,00 (quint, 3J 7,5 Гц, 4H), 3,30 (t, 3J 7,5 Гц, 4H), 3,90 (t, 3 J 7,5 Гц, 4Н), 7,15-7,18, 7,95-8,15 (2m, 24Η), 9,15-9,20 (m, 8H), 10,05 (s, 2H). Сполука 8 Дихлорид 5,15-біс-(4-{3-[(3диметиламінопропіл)диметиламоніо]пропілокси}феніл)порфірину Сполуку 7 (200 мг, 0,27 ммоль) розчиняють в абсолютному ДМФ (40 мл) з N,N,N',N'-тетраметил1,3-пропандіаміном (5 мл, 13,9 ммоль) і цей розчин перемішують при 50 °С в атмосфері аргону протягом ночі. Після випарювання розчинника при зниженому тиску, одержаний залишок розчиняють у метанолі (5 мл) і фільтрують через шар силікагелю (товщина 2 см), підтримуваний на сталевій фриті (з діаметром 3,5 см). Шар елююють метанолом (приблизно 1 л) і потім сумішшю оцтова кислота:метанол:вода (3:2:1 по об'єму). Після випарювання розчинника з придатних фракцій неочищений продукт розчиняють у метанолі (5 мл) і додатково очищають хроматографією на колонці (2,540 см) Sephadex LH-20 з використанням суміші н-бутанол:вода:оцтова кислота (4:5:1, по об'єму, верхня фаза) як проявної фази. Після видалення розчинника при зниженому тиску одержаний залишок розчиняють у метанолі (5 мл) і розчин пропускають через коротку колонку (3,520 см) аніонообмінної смоли (Amberlite IRA 400, хлоридна форма). Після видалення розчинника при зниже 94027 36 ному тиску із цього елюату залишок обробляють діетиловим ефіром і сушать під високим вакуумом з одержанням продукту у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, CD3OD): 2,20-2,35 (m, 4H), 2,40-2,50 (m, 4H), 2,80 (s, 12Н), 3,05 (4H, 3J 7,8, 2Н), 3,25 (s, 12Н), 3,45-3,55 (bs, 4Н), 3,65-3,75 (m, 4Н), 4,30 (t, 3J 4,2 Гц, 4H), 7,40, 8,10 (2d, 3J 7,5 Гц, 24Η), 8,95, 9,45 (2d, 3J 4,2 Гц, 8Н), 10,40 (s, 2H). Сполука 9 Дихлорид 5,15-біс-[4-(3триетиламоніопропілокси)феніл]порфірину До розчину сполуки 7 (50 мг, 0,068 ммоль) в абсолютному ДМФ (20 мл) додають триетиламін (4,7 мл, 0,034 моль, 500 екв.). Цю суміш перемішують при 60 °С протягом 24 годин. Розчинник видаляють при зниженому тиску та одержаний залишок розчиняють у метанолі (5 мл) і фільтрують через шар силікагелю (товщина 2 см), підтримуваний на сталевій фриті (з діаметром 3,5 см). Після промивання метанолом (приблизно 1 л) шар елююють сумішшю оцтова кислота:метанол:вода (3:2:1, по об'єму). Після випарювання розчинника з елюйованої фракції одержаний неочищений продукт розчиняють у метанолі (5 мл) і очищають хроматографією на колонці (2,540 см) Sephadex LH-20 з елюцією сумішшю н-бутанол:вода:оцтова кислота (4:5:1, по об'єму, верхня фаза). Розчинники видаляють при зниженому тиску з придатних фракцій, одержаний залишок розчиняють у метанолі (5 мл) і цей розчин пропускають через коротку колонку (3,520 см) аніонообмінної смоли (Amberlite IRA 400, хлоридна форма) з одержанням продукту у вигляді фіолетової твердої речовини після випарювання розчинника. 1 Н-ЯМР: δΗ (300 МГц, CD3OD): 1,25 (m, 18Н), 2,13 (m, 4H), сигнали -CH2NCH2 (16Н) знаходяться в області 3,00-3,40 як частина мультиплету, що перекривається сигналами розчинника, 4,15 (t, 4Н, 3 J = 7,5 Гц), 7,36 (d, 4Н, 3J = 7,5 Гц), 8,15 (d, 4H, 3J = 7,5 Гц), 9,05 (d, 4Н, 3J = 7,5 Гц), 9,54 (d, 4Н, 3J = 7,5 Гц), 10,45 (s, 2H). Сполука 10 Дихлорид 5,15-біс-[4-(3триметиламоніопропілокси)феніл]порфірину Розчин сполуки 7 (300 мг, 0,41 ммоль) в абсолютному ДМФ (50 мл) переносять в автоклав на 100 мл. Після додавання триметиламіну (4,5 г) суміш перемішують при 50 °С протягом 16 годин. Після випарювання розчинника одержаний залишок розчиняють у метанолі (5 мл) і розчин фільтрують через шар силікагелю (товщина 2 см), підт 37 римуваний на сталевій фриті (з діаметром 3,5 см). Після промивання метанолом (приблизно 1 л) шар елююють сумішшю оцтова кислота:метанол:вода (3:2:1, по об'єму). Після випарювання розчинника з придатних фракцій одержаний залишок розчиняють у метанолі (5 мл) і очищають хроматографією на колонці (2,540 см) Sephadex LH-20 з елюцією сумішшю н-бутанол:вода:оцтова кислота (4:5:1, по об'єму, верхня фаза). Одержують дві фракції, з яких перша елюйована фракція є бажаним продуктом. Розчинник видаляють при зниженому тиску та одержаний залишок повторно розчиняють у метанолі (5 мл) і цей розчин пропускають через коротку колонку (3,520 см) аніонообмінної смоли (Amberlite IRA 400, хлоридна форма). Після випарювання розчинника при зниженому тиску залишок обробляють сумішшю метанол:діетиловий ефір і сушать під високим вакуумом з одержанням продукту у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, CD3OD): 2,40-2,60 (m, 4H), 3,30-3,25 (bs, 18Н), 3,75-3,80 (m, 4H), 4,40 (t, 3 J 7,5 Гц, 4H), 7,40, 8,20 (2d, 3J 8,5 Гц, 8Н), 9,05, 9,50 (2d, 3J 4,5 Гц, 8H), 10,45 (s, 2H). Альтернативний спосіб синтезу сполуки 10 Сполуку 42 (100 мг, 0,2 ммоль; див. нижче) розчиняють і карбонат калію (230 мг, 1,7 ммоль) суспендують у ДМФ (30 мл) і до цієї суміші при сильному перемішуванні додають по краплях розчин (1-бромпропіл)триметиламонійброміду (350 мг, 1,3 ммоль) у ДМФ (5 мл) при 50 °С протягом 30 хвилин. Суміш нагрівають протягом 15 годин. ДМФ видаляють на роторному випарнику, а одержаний залишок розчиняють в метанолі і цей розчин фільтрують через шар силікагелю (товщина 2 см), підтримуваний на сталевій фриті (з діаметром 3,5 см). Після промивання метанолом (приблизно 1 л) шар елююють сумішшю оцтова кислота:метанол:вода (3:2:1, по об'єму). Після випарювання розчинника з придатних фракцій одержаний залишок розчиняють у метанолі (5 мл) і очищають хроматографією на колонці (2,540 см) Sephadex LH-20 з елюцією сумішшю н-бутанол:вода:оцтова кислота (4:5:1, по об'єму, верхня фаза). Одержують дві фракції, з яких перша елюйована фракція є бажаним продуктом. Розчинник видаляють при зниженому тиску, одержаний залишок повторно розчиняють у метанолі (5 мл) і цей розчин пропускають через коротку колонку (3,520 см) аніонообмінної смоли (Amberlite IRA 400, хлоридна форма). Після випарювання розчинника при зниженому тиску залишок обробляють сумішшю метанол:діетиловий ефір і сушать під високим вакуумом з одержанням продукту у вигляді фіолетової твердої речовини. Сполука 11 5,15-біс-[3-(3-бромпропілокси)феніл]порфірин 94027 38 До перемішуваного розчину дипіролметану (1,22 г, 8,2 ммоль) і 3-(3бромпропілокси)бензальдегіду (2,06 г, 8,2 ммоль) у дегазованому дихлорметані (2 л) додають по краплях ТФО (0,14 мл, 3 ммоль). Цей розчин перемішують при кімнатній температурі в темряві протягом 17 годин в атмосфері аргону. Після додавання DDQ (5,4 г, 0,024 моль) цю суміш перемішують при кімнатній температурі додатково протягом 1 години. Після видалення розчинників при зниженому тиску одержаний залишок розчиняють у дихлорметані (5 мл) і пропускають через колонку (300 г) силікагелю (Fluka 60) з використанням дихлорметану як елюенту з одержанням неочищеного продукту, який обробляють сумішшю дихлорметан:метанол з одержанням чистого матеріалу у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, CDCI3): -3,20 (2Н, s), 2,40 (quint, 3J 7,5 Гц, 4Н), 3,65 (t, 3J 7,5 Гц, 4H), 4,25 (t, 3J 7,5 Гц, 4H), 7,20-7,25, 7,60-7,65, 7,75-7,80 (3m, 8H), 9,05, 9,25 (2d, 3J 4,2 Гц, 8H), 10,25 (s, 2H). Сполука 12 Дихлорид 5,15-біс-[3-(3триметиламоніопропілокси)феніл]порфірину Розчин сполуки 11 (400 мг, 0,543 ммоль) у ДМФ (50 мл) переносять в автоклав на 100 мл. Після додавання триетиламіну (6,3 г) цю суміш перемішують при 50 °С протягом 8 годин. Після випарювання розчинника при зниженому тиску залишок розчиняють у метанолі (5 мл) і розчин фільтрують через шар силікагелю (товщина 2 см), підтримуваний на сталевій фриті (з діаметром 3,5 см). Після промивання шару метанолом (приблизно 1 л) елюція сумішшю оцтова кислота:метанол:вода (3:2:1, по об'єму) дає фракції, які після випарювання розчинника при зниженому тиску дають твердий залишок. Його розчиняють у метанолі (5 мл) і очищають хроматографією на колонці (2,540 см) Sephadex LH-20 з елюцією сумішшю н-бутанол:вода:оцтова кислота (4:5:1, по об'єму, верхня фаза). Одержують дві фракції, з яких перша елюйована фракція є бажаним продуктом. Після видалення розчинника при зниженому тиску одержаний залишок розчиняють у метанолі (5 мл). Цей розчин пропускають через коротку колонку (3,520 см) аніонообмінної смоли (Amberlite IRA 400, хлоридна форма), розчинник видаляють при зниженому тиску і неочищений продукт обробляють сумішшю метанол:діетиловий ефір з одержанням фіолетової твердої речовини, яку сушать під високим вакуумом. 1 Н-ЯМР: δΗ (300 МГц, CD3OD): 2,30-2,35 (m, 4H), 3,15 (s, 18Н), 3,95-4,05 (m, 4H), 4,20-4,25 (m, 4H), 7,40-7,45, 7,65-7,70, 7,80-7,85 (3m, 8H), 9,009,05, 9,40-9,45, (2m, 8H), 10,40 (m, 2H). Сполука 13 39 94027 40 5,15-біс-(4-гідроксифеніл)-10,20-біс-(4ундецилоксифеніл)порфірин Третя фракція, елюйована з колонки під час хроматографічного розділення, описаного для синтезу сполуки 2, характеризується як 5,15-біс-(4гідроксифеніл)-10,20-біс-(4ундецилоксифеніл)порфірин. 1 Н-ЯМР: δΗ (300 МГц, CDCI3): -2,88 (2Н, s), 0,85 (t, 3J 7,5 Гц, 6Н), 1,20-1,40 (m, 28Н), 1,55 (br.m, 4H), 1,80 (quint, 3J 7,5 Гц, 4Н), 4,15 (t, 3J 7,5 Гц, 4Н), 6,65, 7,15 (d, 3J 8,1 Гц, 8Н), 7,80, 8,00 (d, 3J 8,1 Гц, 8Η), 8,75-8,80 (m, 8H). Геометрія транс-региоізомера була визначена за допомогою 1Н-13С-2D-ЯМР в d-оцтовій кислоті. Сполука 14 5,10-біс-(4-гідроксифеніл)-15,20-біс-(4ундецилоксифеніл)порфірин Четверта фракція, елюйована з колонки під час хроматографічного розділення, описаного для синтезу сполуки 2, характеризується як 5,10-біс-(4гідроксифеніл)-15,20-біс-(4-ундецилоксифеніл)порфірин. 1 Н-МНР: δΗ (300 МГц, CDCI3): -2,80 (2Н, s), 0,90 (t, 3J 7,5 Гц, 6Н), 1,20-1,60 (m, 28Н), 1,65 (quint, 3J 7,5 Гц, 4H), 2,00 (quint, 3J 7,5 Гц, 4H), 4,22 (t, 3J 7,5 Гц, 4Н), 7,15 (d, 3J 8,1 Гц, 4H), 7,25 (d, 3J 8,2 Гц, 4H), 8,10 (d, 3J 8,2 Гц, 4H), 8,15 (d, 3J 8,2 Гц, 4Н), 8,80-8,90 (m, 8H). Геометрія цис-региоізомера була визначена за допомогою 1Н-13С-2D-ЯМР в d-оцтовій кислоті. Сполука 15 5,10,15-трис-[4-(3-бромпропілокси)феніл]-20(4-ундецилоксифеніл)порфірин В атмосфері аргону сполуку 2 (200 мг, 0,24 ммоль) розчиняють в абсолютному ДМФ (40 мл) у присутності K2СО3 (500 мг) і 1,3-дибромпропану (1,02 мл, 10 ммоль). Цю суміш нагрівають протягом ночі при 80 °С. Доопрацювання проводять за процедурою, наведеною для сполуки 2 вище. Продукт очищають хроматографією на колонці з силікагелем (Merck 60) з елюцією сумішшю гексан:етилацетат (5:1, по об'єму). 1 Н-ЯМР: δΗ (300 МГц, CDCI3): -2,75 (2Н, s), 0,85 (t, 3J 7,5 Гц, 3Н), 1,20-1,45 (m, 14Н), 1,50 (quint, 3J 7,5 Гц, 2H), 1,90 (quint, 3J 7,5 Гц, 2H), 2,40 (quint, 3J 7,4 Гц, 6Н), 3,65 (t, 3J 7,4 Гц, 6H), 4,16 (t, 3 J 7,5 Гц, 2H), 4,25 (t, 3J 7,5 Гц, 6H), 7,18-7,20 (m, 8H), 8,00-8,05 (m, 8H), 8,75-8,85 (m, 8H). Сполука 16 Трихлорид 5,10,15-трис-[4-(3триетиламоніопропілокси)феніл]-20-(4ундецилоксифеніл)порфірину Сполуку 15 (200 мг, 0,17 ммоль) розчиняють в абсолютному ДМФ (40 мл) з триетиламіном (5 мл, 34,5 ммоль, 208 екв.). Цю суміш нагрівають до 50 °С протягом 48 годин. Після видалення ДМФ під вакуумом одержаний залишок розчиняють в метанолі та очищають хроматографією на колонці на силікагелі (Merck 60) з елюцією сумішшю метанол:вода:оцтова кислота (2:1:3, по об'єму), а потім сумішшю оцтова кислота:піридин (1:1, по об'єму). Видалення розчинника з придатних фракцій під вакуумом дає неочищений продукт, який розчиняють у суміші метанол:водний NaCI (1M) (5 мл, 1:1, по об'єму). Цю суміш перемішують протягом 30 хвилин і фільтрують через шар силікагелю (товщина 2 см), підтримуваний на сталевій фриті (з діаметром 3,5 см). Після промивання шару метанолом (200 мл) його елююють сумішшю метанол:вода:оцтова кислота (2:1:3, по об'єму). Після випарювання розчинника з придатних об'єднаних 41 фракцій одержаний залишок розчиняють у метанолі (2 мл) і додають по краплях дихлорметан (5 мл). Осаджений білий гель збирають фільтруванням і розчинник видаляють під високим вакуумом. 1 3 Н-ЯМР: δΗ (300 МГц, CD3OD): 0,90 (t, J 7,5 Гц, 3Н), 1,20-1,45 (m, 43Н), 1,45-1,65 (bs, 2H), 2,252,40 (bs, 6H), 3,35-3,45 (bs, 24Н). 3,50-3,60 (bs, 6H), 4,25 (t, 3J 7,5 Гц, 2H), 4,40-4,45 (bs, 6Н), 7,25-7,40, 8,10-8,20 (m, 16Н), 8,80-9,10 (bs, 8H). Сполука 17 5-[4-(3-гідроксифеніл)]-15-(3ундецилоксифеніл)порфірин 5-15-біс-(3-гідроксифеніл)порфірин (Wiehe, Α., Simonenko, E.J., Senge, M.О. and Roeder, В., Journal of Porphyrins and Phthalocyanines, 5, 758761 (2001)) (86 мг, 0,17 ммоль) розчиняють і K2СО3 (250 мг, 7,1 ммоль) суспендують у ДМФ (40 мл). До цієї суміші при сильному перемішуванні додають по краплях розчин 1-бромундекану (0,04 мл, 0,17 ммоль) у ДМФ (5 мл) при 50 °С протягом 30 хвилин і цю суміш нагрівають при цій температурі під високим вакуумом. Одержаний залишок очищають хроматографією на колонці з використанням силікагелю (Merck 60) з елюцією сумішшю нгексан:етилацетат (10:1, по об'єму). Другу фракцію збирають і сушать під високим вакуумом з одержанням продукту. 1 Н-ЯМР: δΗ (300 МГц, CDCI3): -3,15 (2Н, s), 0,75 (t, 3J 7,5 Гц, 3Н), 1,10-1,30 (m, 14Н), 1,35 (m, 2H), 1,80 (quint, 3J 7,5 Гц, 2H), 4,05 (t, 3J 7,5 Гц, 2Н), 6,85-6,90, 7,20-7,25, 7,35-7,45, 7,50-7,65, 7,75-7,80 (5m, 8H), 8,85, 8,95, 9,10, 9,20 (4d, 3J 4,9 Гц, 42Н), 10,15 (s, 2H). Сполука 18 5,10,15-трис-(3-гідроксифеніл)-20-(3додецилфеніл)порфірин 3-гідроксибензальдегід (1,8 г, 14,9 ммоль, 3 екв.) і 3-додецилоксибензальдегід (1,35 г, 4,9 ммоль, 1 екв.) розчиняють у суміші оцтової кислоти (145 мл) та нітробензолу (98 мл, 960 ммоль) і нагрівають до 120 °С. Додають пірол (1,35 мл, 19,6 ммоль, 4 екв.) однією порцією і цю суміш перемішують при 120 °С протягом 1 години. Після охолодження до кімнатної температури розчинники видаляють під вакуумом при 50 °С. Продукт виділяють хроматографією на колонці (500 г) силікагелю з використанням толуолу як елюенту. Бажаний продукт одержують у вигляді п'ятої фракції із цієї колонки і повторно хроматографують з використанням меншої (200 г) колонки силікагелю з елюцією толуолом. Продукт одержують у вигляді фіолетової твердої речовини після випарювання розчинника. 1 Н-ЯМР: δΗ (300 МГц, CDCI3): 0,64 (t, 3Н, 3J 6,8 Гц), 0,94-1,15 (m, 16H), 1,25 (bs, 2H), 1,62 (bs, 2H), 3,90 (bs, 2H), 6,33-6,95 (m, 8H), 7,08-7,60 (m, 8H), 8,20-8,47 (m,4H), 8,51-8,70 (m,4H). 94027 42 Сполука 19 5-{3-[біс-(2-діетиламіноетил)амінопропілокси] феніл}-15-(3-ундецилоксифеніл)порфірин Сполуку 17 (50 мг, 0,065 ммоль) розчиняють із Ν,Ν,Ν',Ν'-тетраетилдіетилентриаміном (1 мл, 39 ммоль) у ТГФ (10 мл) і цю суміш перемішують при кімнатній температурі протягом 4 днів. Після випарювання розчинника залишок розчиняють у діетиловому ефірі (20 мл) і цей розчин промивають водою (530 мл). Органічну фазу сушать (Na2SO4) і концентрують при зниженому тиску. Цю суміш очищають хроматографією на колонці (силікагель, Merck 60) з елюцією сумішшю н-гексан:етилацетат (5:1, по об'єму) і потім сумішшю нгексан:етилацетат:триетиламін (10:10:1, по об'єму). Після збирання придатних фракцій і видалення розчинника при зниженому тиску чистий продукт одержують обробкою залишку сумішшю діетиловий ефір:метанол. 1 Н-ЯМР: δΗ (300 МГц, CDCI3): 0,80 (t, 3J 7,5 Гц, 3Н), 0,9 (t, 3J 7,5 Гц, 12Н), 1,20-1,40 (m, 14Н), 1,45 (quint, 3J 7,5 Гц, 2 Η), 1,80 (quint, 3J 7,5 Гц, 2Н), 1,95 (quint, 3J 7,5 Гц, 2 Η), 2,40-2,60 (m, 16H), 2,65 (t, 3J 7,5 Гц, 2Н), 4,10 (t, 3J 7,5 Гц, 2Н), 4,20 (t, 3J 7,5 Гц, 2H), 7,30-7,40, 7,55-7,65, 7,75-7,80 (3m, 8Н), 9,109,15, 9,20-9,25 (2m, 24Η), 10,15 (s, 2H). Сполука 20 5-[4-(3-бромпропілокси)феніл]-15-(4додецилоксифеніл)порфірин До перемішуваного розчину дипіролметану (0,31 г, 2,1 ммоль), 4-(3бромпропілокси)бензальдегіду (0,27 г, 1,1 ммоль) та 4-додецилоксибензальдегіду (0,32 г, 1,1 ммоль) у дегазованому дихлорметані (500 мл) додають по краплях ТФО (0,035 мл, 1,5 ммоль). Цей розчин перемішують при кімнатній температурі в темряві протягом 17 годин в атмосфері аргону. Після додавання DDQ (1,38 г, 6 ммоль) цю суміш перемішують при кімнатній температурі ще протягом години. Очищення хроматографією на колонці з використанням силікагелю (Merck 60, 400 г) з толуолом як елюенту дають продукт (2-а фракція) разом зі сполукою 7 (3-я фракція). 1 Н-ЯМР: δΗ (300 МГц, CDCI3): -3,15 (2Н, s), 0,90 (t, 3J 7,5 Гц, 3Н), 1,20-1,40 (m, 16H), 1,55 (quint, 3J 7,5 Гц, 2Н), 1,90 (quint, 3J 7,5 Гц, 2Н), 2,40 3 3 (quint, J 7,5 Гц, 2Н), 3,75 (t, J 7,5 Гц, 2Н), 4,20 (t, 3 3 J 7,5 Гц, 2Н), 4,35 (t, J 7,5 Гц, 2Н), 7,20-7,30, 8,108,15 (2m, 8H), 9,10-9,15, 9,25-9,30 (2m, 24H), 10,20 (s, 2H). СполукА 21 5,10,15,20-тетракіс-(3-гідроксифеніл)порфірин 43 3-гідроксибензальдегід (0,910 г, 7,45 ммоль) розчиняють у пропіоновій кислоті (50 мл) і нагрівають до 140 °С. Пірол (0,52 мл, 7,45 ммоль) додають однією порцією і цю суміш нагрівають зі зворотним холодильником при дефлегмації протягом 2 годин. Перемішування продовжують протягом додаткових 12 годин при кімнатній температурі. Пропіонову кислоту видаляють під вакуумом і залишок розчиняють в ацетоні та очищають хроматографією на колонці (250 г) силікагелю, яку елююють толуолом, що включає безперервно зростаючу частку етилацетату. Продукт елююють сумішшю толуол:етилацетат (6:1 по об'єму). Розчинник видаляють під вакуумом з одержанням продукту у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, d6-ацетон): 7,18 (d, 4Н, 3 J = 8,25 Гц), 7,49 (t, 4Н, 3J = 8,25 Гц), 7,56-7,62 (m, 8H), 8,81 (m, 8H). Сполука 22 5,10,15-трис-[4-(3-бромпропілокси)феніл]-20(4-додецилоксифеніл)порфірин До перемішуваного розчину піролу (0,7 мл, 10 ммоль), 4-(3-бромпропілокси)-бензальдегіду (1,8 г, 7,5 ммоль) та 4-(н-додецилокси)бензальдегіду (0,725 г, 2,5 ммоль) у дегазованому дихлорметані (1 л) додають по краплях ТФО (0,085 мл, 10 ммоль). Реакційний розчин перемішують в атмосфері аргону при кімнатній температурі в темряві протягом 17 годин. Після додавання DDQ (6,9 г, 30 ммоль) реакційну суміш перемішують при кімнатній температурі ще протягом 1 години. Розчинники видаляють при зниженому тиску і залишок перерозчиняють у толуолі. Хроматографічне очищення на колонці (3,530 см) силікагелю (Merck 60) з використанням суміші толуол:н-гексан (1:4 по об'єму) як розчинника дає неочищений продукт, який очищають обробкою сумішшю метанол:дихлорметан з одержанням фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, CDCI3): 0,90 (t, 3J 7,5 Гц, 3Н), 1,20-1,45 (m, 16H), 1,60 (quint, 3J 7,5 Гц, 2H), 1,90 (quint, 3J 7,5 Гц, 2H), 2,50 (quint, 3J 7,4 Гц, 6H), 3,75 (t, 3J 7,4 Гц, 6Н), 4,20 (t, 3J 7,5 Гц, 2Н), 4,35 (t, 3 J 7,5 Гц, 6Н), 7,25-7,30 (m, 8H), 8,15-8,30 (m, 8H), 8,80-8,85 (m, 8H). Сполука 23 Хлорид 5-{4-[3-диметил-(3диметиламінопропіл)амоніопропілокси]феніл}-15(4-додецилоксифеніл)порфірину 94027 44 Сполуку 20 (30 мг, 0,038 ммоль) розчиняють із Ν,Ν,Ν',Ν'-тетраметил-1,3-пропандіаміном (156 мг, 1,2 ммоль) у суміші ТГФ:ДМФ (1:1 по об'єму, 20 мл) і перемішують при 50 °С протягом 18 годин. Після випарювання розчинника при зниженому тиску залишок розчиняють у дихлорметані та очищають хроматографією на колонці (силікагель Merck 60) з елюцією сумішшю оцтова кислота:метанол:вода (3:2:1, по об'єму). Після об'єднання придатних фракцій і видалення розчинника при зниженому тиску залишок обробляють сумішшю дихлорметан:гексан з одержанням продукту у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, CDCI3 + 1% оцтової кислоти): 0,85 (m, 3Н), 1,20-1,40 (m, 18Н), 1,55-1,60 (m, 2Н), 1,60-1,65 (m, 4Н), 2,10-2,20 (bs, 8Н), 3,153,25 (m, 8Н), 3,75 (bs, 2Н), 4,20 (bs, 2Н), 4,35 (bs, 2Н), 7,15-7,20, 8,10-8,15 (2m, 8Н), 8,95-9,00, 9,109,15, 9,25-9,30 (3bs, 8H), 10,20 (s, 2H). Сполука 24 5,15-біс-(3-метоксифеніл)-10-ундецилпорфірин В колбу на 50 мл, що містить літій (500 мг, 71 ммоль), додають свіжоперегнаний діетиловий ефір (15 мл) в атмосфері аргону. Цю суспензію нагрівають зі зворотним холодильником при дефлегмації протягом 1 години, охолоджують до 15 °С та обробляють розчином н-ундецилброміду (6,58 г, 71 ммоль) в ефірі (6 мл), який додають по краплях через шприц. Цю суміш охолоджують до 7-10 °С і через 5 хвилин, коли ця суспензія стає трохи мутною, а на металевому літії з'являються яскраві плями, додають решту розчину н-ундецилброміду при рівномірній швидкості протягом періоду 30 хвилин при підтриманні внутрішньої температури нижче 10 °С. Після завершення додавання суміш перемішують додатково протягом 1 години при 10 °С. Суспензію фільтрують в атмосфері аргону для видалення надлишку літію та броміду літію. 5,15-біс-(3-метоксифеніл)порфірин (100 мг, 0,19 ммоль) розчиняють у безводному ТГФ (30 мл) при -50 °С в атмосфері аргону, літійорганічний реагент, описаний вище (5 мл), додають по краплях до цієї суміші. Через 5 хвилин охолодну баню забирають і суміш нагрівають до кімнатної температури. Після перемішування при кімнатній температурі протягом 15 хвилин реакцію гасять повільним додаванням води (2 мл). Через 15 хвилин суміш окисляють додаванням DDQ (4 мл, 0,4 ммоль, 0,1 Μ у ТГФ) та перемішують ще протягом 15 хвилин. Суміш фільтрують через оксид алюмі 45 нію (нейтральний, категорії "+" за Брокманом) і очищають хроматографією на колонці на силікагелі з елюцією сумішшю гексан:дихлорметан (4:1 по об'єму). Першу фракцію збирають та обробляють сумішшю метанол:дихлорметан з одержанням продукту у вигляді твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, CDCI3): -3,05 (bs, 2H, s), 0,80 (t, 3J 7,5 Гц, 3Н), 1,10-1,20 (m, 12H), 1,25 (m, 2H), 1,70 (quint, 3J 7,5 Гц, 2Н), 2,40 (quint, 3J 7,5 Гц, 2Н), 3,85 (s, 6H), 4,95 (t, 3J 7,5 Гц, 2H), 7,20-7,23, 7,50-7,60, 7,65-7,75 (3m, 8H), 8,85-8,90, 9,10-9,15, 9,35-9,40 (3m, 8H), 9,95 (s, 1H). Сполука 25 Трихлорид 3-[({3-[(3-{4-[15-(4додецилоксифеніл)порфірин-5-іл]фенокси}пропіл)диметиламоніо]пропіл}диметиламоніо)пропіл]т риметиламонію Сполуку 23 (20 мг, 0,022 ммоль) і (1бромпропіл)триметиламонійбромід (26 мг, 0,1 ммоль) розчиняють у ДМФ (15 мл) і перемішують протягом ночі при 50 °С. Після випарювання розчинника при зниженому тиску залишок розчиняють у метанолі (5 мл) і наносять на шар (глибина 3 см) силікагелю, який промивають метанолом (500 мл) і потім сумішшю оцтова кислота:метанол:вода (3:2:1 по об'єму). Після випарювання розчинника залишок очищають хроматографією на колонці (силікагель Merck 60) з використанням спочатку суміші оцтова кислота: метанол:вода (3:2:1 по об'єму), а потім суміші піридин:оцтова кислота (1:1 по об'єму). Другу елюйовану фракцію збирають і сушать під вакуумом. Залишок розчиняють у метанолі (2 мл) і очищають хроматографією на колонці (2,540 см) Sephadex LH-20, яку елююють сумішшю н-бутанол:оцтова кислота:вода (5:1:4 по об'єму, верхня фаза). Після видалення розчинника при зниженому тиску залишок сушать під вакуумом при 80 °С. ЯМР-спектроскопія показує, що цей продукт забруднений невеликою часткою елімінованих продуктів. Сполука 26 5,10,15-трис-[4-(3-діетиламінопропілокси)феніл]-20-(4-додецилоксифеніл)-порфірин Сполуку 22 (50 мг, 0,06 ммоль) і свіжоперегнаний діетиламін (5 мл) розчиняють в абсолютному 94027 46 ДМФ (30 мл) в атмосфері аргону. Реакційну суміш перемішують при кімнатній температурі протягом 20 годин і виливають в етилацетат (50 мл). Цю суміш промивають водою (450 мл) і після сушіння об'єднаних органічних фаз (Na2SO4) випарювання розчинника дає залишок, який очищають хроматографією на колонці (2,530 см) силікагелю (Merck 60), що елююють сумішшю етилацетат:гексан:триетиламін (10:10:1, по об'єму). Фракції об'єднують при необхідності, розчинник випарюють при зниженому тиску і залишок сушать під високим вакуумом. Обробка сумішшю дихлорметан:н-гексан дає чистий продукт. 1 Н-ЯМР: δΗ (300 МГц, CDCI3): 0,85 (t, 3J 7,5 Гц, 3Н), 1,05 (m, 18Н), 1,20-1,45 (m, 18Н), 1,55 (quint, 3 J 7,5 Гц, 2Н), 2,15 (quint, 3J 7,5 Гц, 6Н), 2,75 (quint, 3 J 7,4 Гц, 6H), 3,15-3,25 (m, 12Н), 4,15 (t, 3J 7,5 Гц, 2H), 4,25 (t, 3J 7,5 Гц, 6Н), 7,15-7,20 (m, 8H), 8,008,05 (m, 8H), 7,95-8,05 (m, 8H). Сполука 27 5,15-біс-(3-гідроксифеніл)-10-ундецилпорфірин До розчину сполуки 24 (95 мг, 0,14 ммоль) у безводному дихлорметані (80 мл) в атмосфері аргону додають по краплях ВВr3 (6 мл, 1М у дихлорметані) при -70 °С і цю суміш перемішують протягом 1 години. Суміш нагрівають до кімнатної температури та перемішують протягом ночі, а потім охолоджують до -10 °С і гідролізують додаванням 2 мл води протягом 1 години. Додають NaHCO3 (3 г) безпосередньо для нейтралізації. Суміш перемішують ще протягом 12 годин. Після видалення NaHCO3 фільтруванням і дихлорметану під вакуумом одержаний залишок очищають хроматографією на колонці з використанням силікагелю з елюцією дихлорметаном. Після видалення розчинника з придатних об'єднаних фракцій і сушіння під високим вакуумом продукт одержують у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, CDCI3): -3,05 (bs, 2Н, s), 0,85 (t, 3J 7,5 Гц, 3Н), 1,20-1,40 (m, 12Н), 1,50 (m, 2H), 1,80 (quint, 3J 7,5 Гц, 2H), 2,55 (quint, 3J 7,5 Гц, 2H), 5,00 (t, 3J 7,5 Гц, 2H), 7,15-7,25, 7,50-7,60, 7,80-7,90 (3m, 8H), 8,95-9,00, 9,20-9,25, 9,50-9,60 (3m, 8H), 10,15 (s, 1H). Сполука 28 Дихлорид 5,15-біс-[3-(3-триметиламоніопропілокси)феніл]-10-ундецилпорфірину До розчину сполуки 27 (50 мг, 0,08 ммоль) у ДМФ (20 мл) в атмосфері аргону додають K2СО3 47 (100 мг, 0,72 ммоль) та (3бромпропіл)триметиламонійбромід (300 мг, 1,2 ммоль) і цю суміш перемішують при 50 °С протягом 18 годин. Після видалення розчинника під високим вакуумом одержаний залишок розчиняють у метанолі (5 мл) і фільтрують через шар силікагелю (товщина 2 см), підтримуваний на сталевій фриті (з діаметром 3,5 см). Після промивання шару метанолом (500 мл) його елююють сумішшю оцтова кислота:метанол:вода (3:2:1, об./об.). Після сушіння придатних об'єднаних фракцій під високим вакуумом залишок розчиняють у метанолі та очищають хроматографією на колонці на Sephadex LH20 з елюцією сумішшю н-бутанол:оцтова кислота:вода (5:1:4, по об'єму, верхня фаза). Після випарювання розчинника залишок, одержаний з першої елюйованої фракції, розчиняють у метанолі та пропускають через коротку колонку аніонообмінної смоли (Amberlite IRA 400, хлоридна форма) з одержанням, після випарювання розчинника, чистого продукту. 1 Н-ЯМР: δΗ (300 МГц, CD3OD): 0,85 (t, 3J 7,5 Гц, 3Н), 1,20-1,40 (m, 12Н), 1,50 (m, 2H), 1,80 (m, 2H), 2,40 (bs, 4H), 2,55 (m, 2H), 3,20 (bs, 18Н), 3,65 (bs, 4H), 4,35 (bs, 4H), 5,10 (m, 2H), 7,50-7,55, 7,707,85 (2m, 8H), 8,95-9,00, 9,25-9,24, 9,50-9,70 (3bs, 8H), 10,15 (bs, 1H). Сполука 29 Дихлорид 5,10-біс-[4-(3триметиламоніопропілокси)феніл]-15,20-біс-(4ундецилфеніл)порфірину Сполуку 14 (50 мг, 0,05 ммоль) розчиняють і K2СО3 (150 мг, 1,1 ммоль) суспендують у ДМФ (30 мл). До цієї суміші при сильному перемішуванні додають по краплях розчин (1бромпропіл)триметиламонійброміду (0,3 г, 16,6 ммоль) у ДМФ (10 мл) при 50 °С і цю суміш нагрівають протягом 18 годин. Після видалення ДМФ під високим вакуумом одержаний залишок розчиняють у метанолі (5 мл) і фільтрують через шар силікагелю (товщина 2 см), підтримуваний на сталевій фриті (діаметр 3,5 см). Після промивання шару метанолом (приблизно 500 мл) його елююють сумішшю оцтова кислота:метанол:вода (3:2:1, по об'єму). Після випарювання розчинника з при 94027 48 датних об'єднаних фракцій одержаний залишок очищають хроматографією на колонці (2,540 см) Sephadex LH-20 з елюцією сумішшю нбутанол:вода:оцтова кислота:вода (5:4:1, по об'єму, верхня фаза) для додаткового очищення від надлишку солі амонію та інших побічних продуктів. Після видалення розчинника при зниженому тиску одержаний залишок розчиняють у метанолі та пропускають через коротку колонку (3,520 см) аніонообмінної смоли (Amberlite IRA 400, хлоридна форма). Після випарювання розчинника при зниженому тиску продукт сушать під високим вакуумом. 1 Н-ЯМР: δΗ (300 МГц, CD3OD): 0,80 (t, 3J 7,5 Гц, 6Н), 1,15-1,35 (m, 28Н), 1,35-1,45 (bs, 4H), 1,701,80 (bs, 4H), 2,30-2,40 (bs, 4H), 3,15-3,30 (bs, 18Н), 3,65-3,75 (bs, 4H), 4,00-4,05 (m, 4H), 4,30-4,40 (bs, 4H), 7,00-7,15, 7,20-7,30, 7,80-95, 7,95-8,15 (4m, 44Η), 8,60-9,00 (bs, 8H). Сполука 30 5,10,15-трис-(3-гідроксифеніл)-20-(3ундецилоксифеніл)порфірин Пірол (1,31 г, 19,6 ммоль) додають однією порцією до суміші 3-гідроксибензальдегіду (1,8 г, 14,8 ммоль) та 3-ундецилоксибензальдегіду (1,36 г, 4,9 ммоль) в оцтовій кислоті (145 мл) і нітробензолі (118 г, 960 ммоль), попередньо нагрітої до 130 °С, і цю суміш перемішують протягом 1 години при 120 °С. Суміш охолоджують і розчинник видаляють під високим вакуумом. Залишок розчиняють у дихлорметані (5 мл) і очищають хроматографією на колонці з використанням силікагелю (Merck 60) з елюцією сумішшю гексантолуол (4:1, по об'єму). Продукт одержують після видалення розчинника з елюату при зниженому тиску та сушіння одержаного залишку під вакуумом. 1 Н-ЯМР: δΗ (300 МГц, CDCI3): 0,75-0,80 (m, 3H), 1,05-1,35 (m, 14Н), 1,40-1,50 (m, 2H), 1,75-1,85 (m, 2H), 3,90-4,10 (m, 2H), 6,90- 7,70 (m, 16Н), 8,458,80 (m, 8H). Сполука 31 Дихлорид 5-{4-[3-диметил-(3триметиламоніопропіл)амоніопропілокси]-феніл}15-(4-додецилоксифеніл)порфірину 49 Сполуку 23 (50 мг, 0,055 ммоль) розчиняють у метилйодиді (5 мл, 80 ммоль) в абсолютному ДМФ (30 мл) і цю суміш перемішують при 40 °С протягом 3 годин. Після випарювання розчинника одержаний залишок розчиняють у метанолі (5 мл) і фільтрують через шар силікагелю (товщина 2 см), підтримуваний на сталевій фриті (з діаметром 3,5 см). Після промивання шару метанолом (приблизно 1 л) його елююють сумішшю дихлорметан:метанол (2:3, по об'єму, 500 мл), а потім сумішшю оцтова кислота:вода:метанол (3:1:2, по об'єму). Після видалення розчинника з придатних об'єднаних фракцій одержаний залишок розчиняють в оцтовій кислоті та очищають з використанням хроматографії на колонці Sephadex LH-20 з елюцією оцтовою кислотою. Після випарювання розчинника з придатних об'єднаних фракцією та сушіння одержаного залишку під високим вакуумом залишок розчиняють у метанолі та пропускають через невелику колонку (3,520 см) аніонообмінної смоли (Amberlite IRA 400, хлоридна форма). Після випарювання розчинника з елюату продукт сушать під високим вакуумом. Сполука 32 Дихлорид 5-[4-(3диметилдециламоніопропілокси)феніл]-15-{4-[3диметил-(3диметиламінопропіл)амоніопропілокси]феніл}порфірину Сполуку 23 (50 мг, 0,068 ммоль) розчиняють із N,N,N',N'-тетраметил-1,3-пропандіаміном (354 мг, 1536 ммоль) та Ν,Ν-диметилдециламіном (1 г, 2,72 ммоль) в суміші ДМФ:ТГФ (30 мл, 1:1 по об'єму) і цю суміш перемішують при 50 °С протягом ночі. Після випарювання розчинника при зниженому тиску залишок розчиняють у метанолі (10 мл) і фільтрують через шар силікагелю (товщина 2 см), підтримуваний на сталевій фриті (з діаметром 3,5 см). Після промивання шару метанолом (приблизно 500 мл) його елююють сумішшю оцтова кислота:метанол:вода (3:2:1, по об'єму). Перші дві елюйовані фракції об'єднують і після випарювання розчинника при зниженому тиску одержаний залишок розчиняють в метанолі та очищають хроматографією на колонці (2,540 см) Sephadex LH-20 з елюцією сумішшю н-бутанол:вода:оцтова кислота (4:5:1, по об'єму). Після видалення розчинника при зниженому тиску із другої елюйованої фракції залишок розчиняють у метанолі (5 мл) і пропускають через коротку колонку (3,520 см) аніонообмінної смоли (Amberlite IRA 400, хлоридна форма). Елюат упарюють досуха і одержаний залишок сушать під високим вакуумом з одержанням продукту. 1 Н-ЯМР: δΗ (300 МГц, CD3OD): 0,80 (m, 3Н), 1,05-1,25 (m, 10Н), 1,25-1,40 (bs, 2H), 1,80-1,90 (bs, 94027 50 4H), 2,15-2,30 (bs, 2H), 2,80-3,60 (m, 20Н), 3,803,95 (bs, 4H), 7,05-7,15, 7,85-8,00 (2m, 24Η), 8,75-8,90, 9,20-9,35 (2bs, 24Η), 10,15 (bs, 2H). Сполука 33 Трихлорид 5,10,15-трис-[3-(3триметиламоніопропілокси)феніл]-20-(3ундецилоксифеніл)порфірину Сполуку 30 (100 мг, 0,12 ммоль) розчиняють і K2СО3 (230 мг, 1,7 ммоль) суспендують у ДМФ (30 мл). До цієї суміші при сильному перемішуванні додають по краплях розчин (1бромпропіл)триметиламонійброміду (0,3 г, 16,6 ммоль) у ДМФ (10 мл) при 50 °С протягом 30 хвилин і цю суміш нагрівають протягом 18 годин. Після видалення ДМФ при зниженому тиску одержаний залишок розчиняють у метанолі (5 мл) і фільтрують через шар силікагелю (товщина 2 см), підтримуваний на сталевій фриті (з діаметром 3,5 см). Після промивання шару метанолом (приблизно 500 мл) його елююють сумішшю оцтова кислота:метанол:вода (3:2:1, по об'єму). Після випарювання розчинника з придатних об'єднаних фракцій при зниженому тиску залишок очищають хроматографією на колонці (2,540 см) Sephadex LH-20 з елюцією сумішшю н-бутанол:вода:оцтова кислота (5:4:1, по об'єму, верхня фаза). Після видалення розчинника при зниженому тиску з елюату одержаний залишок розчиняють у метанолі і цей розчин пропускають через коротку колонку (3,520 см) аніонообмінної смоли (Amberlite IRA 400, хлоридна форма). Випарювання розчинника із цього елюату дає продукт, який сушать під високим вакуумом. 1 Н-ЯМР: δΗ (300 МГц, CD3OD): 0,75-0,80 (m, 3H), 1,00-1,40 (m, 18Н), 1,60-1,80 (bs, 2H), 2,252,40 (bs, 6H), 3,29 (bs, 27Н), 3,40-3,60 (m, 6H), 3,904,00 (m, 2H), 4,05-4,25 (m, 6H), 7,10-7,20, 7,25-7,40, 7,60-7,80, 7,80-7,90 (4m, 16Н), 8,70-9,00 (bs, 8H). Сполука 34 5,15-біс-(3-гідроксифеніл)порфірин Цю сполуку одержували, як описано Wiehe, Α., Simonenko, E.J., Senge, M.О. and Roeder, В. Journal of Porphyrins and Phthalocyanines 5, 758761 (2001). 51 Сполука 35 5,10,15-трис-(4-гідроксифеніл)-20-(4тетрадецилоксифеніл)порфірин 5,10,15,20-тетракіс-(4-гідроксифеніл)порфірин (170 мг, 0,25 ммоль) розчиняють і K2СО3 (0,65 г, ммоль) суспендують у ДМФ (30 мл). До цієї реакційної суміші при сильному перемішуванні додають по краплях розчин 1-бромтетрадекану (0,1 мл, 0,45 ммоль) у ДМФ (10 мл) при 50 °С протягом 30 хвилин і цю суміш нагрівають протягом 1,5 годин. Після випарювання розчинника залишок розчиняють у суміші толуол:етанол (1:1 по об'єму, приблизно 5 мл) і очищають хроматографією з використанням колонки (525 см) силікагелю (Merck 60), яку промивають толуолом. Після елюції перших 3 фракцій елюцію продовжують із використанням суміші толуол:етилацетат (2:1 по об'єму). П'яту елюйовану сполуку збирають, розчинник випарюють і залишок сушать під високим вакуумом з одержанням продукту у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, d6-ацетон): 0,85 (t, 3J 7,5 Гц, 3Н), 1,15-1,55 (m, 20H), 1,45 (quint, 3J 7,5 Гц, 2H), 1,75 (quint, 3J 7,5 Гц, 2H), 4,10 (t, 3J 7,5 Гц, 2H), 7,20 (d, 3J 8,5 Гц, 2H), 7,25 (d, 3J 8,5 Гц, 6H), 8,008,15 (m, 8H), 8,80-9,10 (m, 8H). Сполука 36 Трихлорид 5,10,15-трис-[4-(3триметиламоніопропілокси)феніл]-20-(4тетрадецилоксифеніл)порфірину н-тетрадецилокси-аналог сполуки 2, одержаний аналогічно сполуці 2, але з використанням, замість 1-бромундекану, 1-бромтетрадекану (50 мг, 0,057 ммоль) і (1бромпропіл)триметиламонійброміду (210 мг, 0,8 ммоль) розчиняють і K2СО3 (230 мг, 1,7 ммоль) суспендують у ДМФ (20 мл). Цю суміш сильно перемішують при цій температурі протягом 18 годин. Після видалення ДМФ при зниженому тиску одер 94027 52 жаний залишок розчиняють у метанолі (5 мл) і фільтрують через шар силікагелю (товщина 2 см), підтримуваний на сталевій фриті (з діаметром 3,5 см). Після промивання цього шару метанолом (приблизно 500 мл) його елююють сумішшю оцтова кислота:метанол:вода (3:2:1, по об'єму). Після випарювання розчинника з придатним чином об'єднаних фракцій одержаний залишок очищають хроматографією на колонці Sephadex LH-20 з елюцією сумішшю н-бутанол:вода:оцтова кислота (4:5:1, по об'єму, верхня фаза) для відокремлення від надлишку амонієвої солі та інших забруднюючих матеріалів. Після елюції та видалення розчинника з придатних фракцій одержаний залишок розчиняють у метанолі (5 мл) і пропускають через коротку колонку (3,520 см) аніонообмінної смоли (Amberlite IRA 400, хлоридна форма). Розчинник видаляють при зниженому тиску і одержаний залишок сушать під високим вакуумом з одержанням продукту у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, CD3OD): 0,75 (t, 3J 7,5 Гц, 3Н), 0,95-1,25 (m, 22Н), 1,50-1,65 (bs, 2H), 2,202,40 (bs, 6H), 3,05-3,15 (bs, 27Н), 3,45-3,60 (bs, 6H), 3,60-3,80 (bs, 2H), 4,05-4,25 (bs, 6H), 6,80-7,25, 7,65-8,05, (2m, 16Н), 8,45-8,95 (bs, 8H). Сполука 37 5-(4-{3-[2,4,6-трис(диметиламінометил)фенілокси]пропілокси}феніл)15-(4-додецилоксифеніл)порфірин Сполуку 20 (50 мг, 0,063 ммоль) розчиняють у ДМФ (20 мл) в присутності 2,4,6-трис(диметиламінометил)фенолу (1 мл, 3,7 ммоль) і перемішують при 50 °С протягом ночі. Після випарювання розчинника залишок отверджують обробкою цього залишку сумішшю дихлорметан:метанол для видалення надлишку аміну. Після фільтрування порфірини перерозчиняють у дихлорметані та очищають хроматографією на колонці силікагелю (Merck 60), яку промивають дихлорметаном. Випарювання розчинника при зниженому тиску та обробка цього залишку сумішшю дихлорметан:метанол дає продукт у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, CDCI3): -3,15 (2Н, s), 0,85 (t, 3J 4,5 Гц, 3Н), 1,20-1,40 (m, 18Н), 1,55 (quint, 3J 4,5 Гц, 2H), 1,90 (quint, 3J 4,5 Гц, 2H), 2,20 (s, 18Н), 2,55 (t, 3J 5,2 Гц, 2H), 3,45 (s, 6H), 4,15 (t, 3 J 5,5 Гц, 2H), 4,20 (t, 3J 5,5 Гц, 2H), 4,35 (t, 3J 7,5 Гц, 2H), 6,85 (2s, 2H), 7,20-7,30, 8,10-8,15 (2m, 8H), 9,00-9,05, 9,25-9,30 (2m, 24Η), 10,20 (s, 2H). 53 Сполука 38 5,10,15-трис-(4-гідроксифеніл)-20-(4децилоксифеніл)порфірин 5,10,15,20-тетракіс-(4-гідроксифеніл)порфірин (100 мг, 0,15 ммоль) розчиняють і K2СО3 (230 мг) суспендують у ДМФ (30 мл). До цієї реакційної суміші при сильному перемішуванні додають по краплях розчин 1-бромдекану (0,016 мл, 0,11 ммоль) у ДМФ (10 мл) при 70 °С протягом 30 хвилин і цю суміш перемішують протягом 1,5 годин. Після випарювання розчинника залишок розчиняють у суміші толуол:етанол (1:1 по об'єму, приблизно 3 мл) і очищають хроматографією на колонці (150 г) силікагелю (Merck 60) з використанням толуолу як елюенту. Після елюції перших 3 фракцій колонку елююють сумішшю толуол:етилацетат (2:1 по об'єму) і 5-у елюйовану фракцію збирають, розчинник видаляють і залишок сушать під високим вакуумом з одержанням продукту у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, d6-ацетон): 0,95 (t, 3J 7,5 Гц, 3Н), 1,25-1,55 (m, 12H), 1,55 (quint, 3J 7,5 Гц, 2H), 1,85 (quint, 3J 7,5 Гц, 2H), 4,15 (t, 3J 7,5 Гц, 2H), 7,20 (d, 3J 8,5 Гц, 2H), 7,25 (d, 3J 8,5 Гц, 6H), 8,008,15 (m, 8H), 8,80-9,10 (m, 8H). Сполука 39 Трихлорид 5,10,15-трис-[4-(3триметиламоніопропілокси)феніл]-20-(4децилоксифеніл)порфірину Сполуку 38 (50 мг, 0,061 ммоль) і (1бромпропіл)триметиламонійбромід (210 мг, 0,8 ммоль) розчиняють і K2СО3 (230 мг, 1,7 ммоль) суспендують у ДМФ (20 мл). Цю реакційну суміш при сильному перемішуванні нагрівають при 50 °С протягом 18 годин. Після випарювання розчинника 94027 54 неочищений продукт розчиняють у метанолі та очищають хроматографією на колонці (2,540 см) Sephadex LH-20 з елюцією сумішшю нбутанол:вода:оцтова кислота (4:5:1, по об'єму, верхня фаза). Після видалення розчинника залишок розчиняють у метанолі та пропускають через коротку колонку (3,520 см) аніонообмінної смоли (Amberlite IRA 400, хлоридна форма). Після випарювання розчинника продукт сушать під високим вакуумом та одержують фіолетову тверду речовину. 1 Н-ЯМР: δΗ (300 МГц, CD3OD): 0,90 (t, 3J 7,5 Гц, 3Н), 1,20-1,40 (m, 12Н), 1,45-1,60 (bs, 2H), 1,801,90 (bs, 2H), 2,45-2,55 (bs, 6H), 3,25-3,35 (bs, 27Н), 3,75-3,85 (bs, 6H), 4,05-4,25 (m, 2H), 4,35-4,40 (bs, 6H), 7,10-7,40, 7,95-8,15 (2m, 16Н), 8,60-9,00 (bs, 8H). Сполука 40 5,10,15-трис-(4-гідроксифеніл)-20-(4тридецилоксифеніл)порфірин 5,10,15,20-тетракіс-(4-гідроксифеніл)порфірин (400 мг, 0,59 ммоль) розчиняють і K2СО3 (1,0 г, 7,1 ммоль) суспендують у ДМФ (75 мл). До цієї реакційної суміші при сильному перемішуванні додають по краплях розчин 1-бромтридекану (0,1 мл, 0,45 ммоль) у ДМФ (10 мл) при 50 °С протягом 30 хвилин і потім цю суміш нагрівають протягом 1,5 годин. Реакційну суміш охолоджують до кімнатної температури та виливають у воду (150 мл). Порфірини екстрагують етилацетатом (100 мл) і екстракт промивають сольовим розчином (350 мл) та сушать (Na2SO4). Після випарювання розчинника залишок розчиняють у суміші толуол:етанол (1:1, по об'єму, приблизно 10 мл) і очищають хроматографією з використанням колонки (200 г) силікагелю (Merck 60) з толуолом як елюентом. Після елюції перших трьох сполук цей елюент заміняють на суміш толуол:етилацетат (2:1, по об'єму). П'яту елюйовану сполуку збирають і сушать під високим вакуумом з одержанням продукту у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, d6-ацетон): 0,85 (t, 3J 7,5 Гц, 3Н), 1,20-1,60 (m, 18H), 1,50 (quint, 3J 7,5 Гц, 2H), 1,80 (quint, 3J 7,5 Гц, 2H), 4,14 (t, 3J 7,5 Гц, 2H), 7,20 (d, 3J 8,5 Гц, 2H), 7,25 (d, 3J 8,5 Гц, 6H), 8,008,15 (m, 8H), 8,80-9,10 (m, 8H). 55 94027 56 Сполука 41 Трихлорид 5-(4-тридецилоксифеніл)-10,15,20трис-[4-(3-триметиламоніопропілокси)феніл]порфірину Сполуку 40 (50 мг, 0,057 ммоль) та (1бромпропіл)триметиламонійбромід (210 мг, 0,8 ммоль) розчиняють і K2СО3 (230 мг, 1,7 ммоль) суспендують у ДМФ (20 мл). Цю суміш при сильному перемішуванні нагрівають при 50 °С протягом 18 годин. Після видалення ДМФ залишок розчиняють у метанолі (5 мл) і наносять на шар силікагелю (товщина 2 см), який промивають метанолом (приблизно 1000 мл) і потім елююють сумішшю оцтова кислота:метанол:вода (3:2:1 по об'єму). Після випарювання розчинника залишок розчиняють у метанолі та додатково очищають хроматографією на колонці (2,540 см) Sephadex LH-20 з елюцією сумішшю н-бутанол:вода:оцтова кислота (4:5:1, по об'єму, верхня фаза). Після видалення розчинника залишок розчиняють у метанолі та пропускають через коротку колонку (3,520 см) аніонообмінної смоли (Amberlite IRA 400, хлоридна форма). Після випарювання розчинника продукт сушать під високим вакуумом з одержанням фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, CD3OD): 0,90 (t, 3J 7,5 Гц, 3Н), 1,20-1,40 (m, 18Н), 1,45-1,60 (m, 2H), 1,801,90 (bs, 2H), 2,40-2,55 (bs, 6H), 3,25-3,35 (bs, 27Н), 3,75-3,85 (bs, 6H), 4,05-4,25 (m, 2H), 4,35-4,40 (bs, 6H), 7,10-7,40, 7,90-8,15 (2m, 16Н), 8,60-9,00 (bs, 8H). Сполука 42 5,15-біс-(4-гідроксифеніл)порфірин Цю сполуку одержують, як описано Mehta, Goverdhan; Muthusamy, Sengodagounder; Maiya, Bhaskar G.; Arounaguiri, S., J. Chem. Soc. Perkin Trans. 14 2177-2182(1999). Сполука 43 5,10,15-трис-(4-гідроксифеніл)-20-(4октилоксифеніл)порфірин 5,10,15,20-тетракіс-(4-гідроксифеніл)порфірин (200 мг, 0,294 ммоль) розчиняють і карбонат калію (487 мг, 3,53 ммоль, 12 екв.) суспендують в атмосфері аргону в абсолютному ДМФ (50 мл) і цю суміш нагрівають до 55 °С. Додають по краплях розчин октилброміду (35,8 мкл, 0,206 ммоль, 0,7 екв.) в абсолютному ДМФ (10 мл) протягом 30 хвилин і цю суміш перемішують при 55 °С протягом 2 годин. Розчинник видаляють під вакуумом при 50 °С, додають воду (80 мл) і цю суміш екстрагують етилацетатом (340 мл). Об'єднану органічну фракцію сушать (Na2SO4) і розчинник випарюють. Залишок очищають хроматографією на колонці (300 г) силікагелю. Тетраалкіловані та триалкіловані сполуки елююють сумішшю толуол: етил ацетат (30:1 по об'єму). Третю фракцію (дизаміщена сполука, транс-ізомер) елююють сумішшю толуол:етилацетат (15:1 по об'єму). Четверту фракцію (дизаміщена сполука, цис-ізомер) елююють сумішшю толуол:етилацетат (10:1 по об'єму) і бажаний продукт (моноалкілована сполука) елююють сумішшю толуол:етилацетат (5:1 по об'єму). Розчинник видаляють при зниженому тиску і залишок сушать під високим вакуумом з одержанням продукту у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, d6-ацетон): 0,75 (t, 3Н, 3J = 6,8 Гц), 1,13-1,25 (m, 8H), 1,43 (quint, 2H, 3J = 7,5 Гц), 1,73 (quint, 2H, 3J = 7,5 Гц), 3,50 (t, 2H, 3J = 8 Гц), 7,11 (d, 2H, 3J = 7,5 Гц), 7,16 (d, 6H, 3J = 7,5 Гц), 7,90-7,94 (m, 8H), 8,80-8,90 (m, 8H). Сполука 44 5-(4-додецилоксифеніл)-10,15,20-трис-(4гідроксифеніл)порфірин 5,10,15,20-тетракіс-(4-гідроксифеніл)порфірин (200 мг, 0,294 ммоль) розчиняють і карбонат калію (487 мг, 3,53 ммоль, 12 екв.) суспендують в атмосфері аргону в абсолютному ДМФ (50 мл) і цю суміш нагрівають до 55 °С. Додають по краплях розчин додецилброміду (49,4 мкл, 0,206 ммоль, 0,7 57 екв.) в абсолютному ДМФ (10 мл) протягом 30 хвилин. Цю суміш перемішують при 55 °С протягом 2 годин. Розчинник видаляють під вакуумом при 50 °С, додають воду (80 мл) і цю суміш екстрагують етилацетатом (340 мл). Об'єднані органічні фракції сушать (Na2SO4) і розчинник випарюють. Продукт виділяють хроматографією на колонці (300 г) силікагелю. Тетраалкіловані та триалкіловані сполуки елююють сумішшю толуол:етилацетат (30:1 по об'єму), дизаміщену сполуку (транс-ізомер) -сумішшю толуол: етил ацетат (15:1 по об'єму), дизаміщену сполуку (цис-ізомер) сумішшю толуол:етилацетат (10:1 по об'єму) і бажаний продукт (моноалкілована сполука) - сумішшю толуол:етилацетат (5:1 по об'єму). Розчинник видаляють під вакуумом і залишок сушать під високим вакуумом з одержанням продукту у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, d6-ацетон): 0,75 (t, 3Н, 3J = 6,8 Гц), 1,13-1,25 (m, 16H), 1,41 (quint, 2H, 3J = 7,5 Гц), 1,63 (quint, 2H, 3J = 7,5 Гц), 3,89 (t, 2H, 3J = 6 Гц), 7,11 (d, 2H, 3J = 7,5 Гц), 7,16 (d, 6H, 3J = 7,5 Гц), 7,9-7,94 (m, 8H), 8,78-8,83 (m, 8H) Сполука 45 5,10,15-трис-(4-гідроксифеніл)-20-(4нонілоксифеніл)порфірин 5,10,15,20-тетракіс-(4-гідроксифеніл)порфірин (200 мг, 0,294 ммоль) розчиняють і карбонат калію (487 мг, 3,53 ммоль, 12 екв.) суспендують в атмосфері аргону в абсолютному ДМФ (50 мл) і цю суміш нагрівають до 55 °С. Додають по краплях розчин нонілброміду (49,4 мкл, 0,206 ммоль, 0,7 екв.) в абсолютному ДМФ (10 мл) протягом 30 хвилин. Цю суміш перемішують при 55 °С протягом 2 годин. Розчинник видаляють під вакуумом при 50 °С, додають воду (80 мл) і цю суміш екстрагують етилацетатом (340 мл). Об'єднані органічні фракції сушать (Na2SO4) і розчинник видаляють при зниженому тиску. Продукт виділяють хроматографією на колонці (300 г) силікагелю. Тетраалкіловані та триалкіловані сполуки елююють сумішшю толуол:етилацетат (30:1 по об'єму), дизаміщену сполуку (транс-ізомер) - сумішшю толуол:етилацетат (15:1 по об'єму), дизаміщену сполуку (цис-ізомер) сумішшю толуол:етилацетат (10:1 по об'єму) і бажаний продукт (моноалкілована сполука) - сумішшю толуол:етилацетат (5:1 по об'єму). Розчинник видаляють при зниженому тиску і залишок сушать під високим вакуумом з одержанням продукту у вигляді фіолетової твердої речовини. 94027 58 1 Н-ЯМР: δΗ (300 МГц, d6-ацетон): 0,87 (t, 3Н, 3J = 7,5 Гц), 1,14-1,26 (m, 10H), 1,41 (quint, 2H), 1,70 (quint, 2H, 3J = 7,5 Гц), 3,92 (t, 2H, 3J = 7,5 Гц), 7,02 (d, 2H, 3J = 8,25 Гц), 7,15 (d, 6H, 3J = 7,5 Гц), 7,85 3 3 (d, 2H, J = 8,25 Гц), 7,91 (d, J = 7,5 Гц), 8,76-8,84 (m, 8H). Сполука 46 Трихлорид 5-(4-октилоксифеніл)-10,15,20трис-[4-(3-триметиламоніопропілокси)феніл]порфірину Сполука 43 (50 мг, 0,063 ммоль) та (3бромпропіл)триметиламонійбромід (164 мг, 0,63 ммоль, 10 екв.) розчиняють і карбонат калію (130 мг, 0,95 ммоль, 15 екв.) суспендують в атмосфері аргону в абсолютному ДМФ (30 мл) і цю суміш перемішують при 55 °С протягом 12 годин. Розчинник видаляють під вакуумом при 50 °С і залишок наносять на шар (товщина 2 см) силікагелю. Непрореаговані солі амонію вимивають метанолом (1000 мл) і продукт елююють сумішшю оцтова кислота:метанол:вода (3:2:1 по об'єму). Розчинник видаляють при зниженому тиску, а потім очищають хроматографією на колонці (100 г) Sephadex LH-20 з використанням суміші нбутанол:вода:оцтова кислота (4:5:1, по об'єму, верхня фаза) як елюенту. Розчинники видаляють при зниженому тиску і залишок розчиняють в метанолі та пропускають через коротку колонку аніонообмінної смоли (Amberlite IRA 400, хлоридна форма) з використанням метанолу як елюенту. Після випарювання розчинника неочищений продукт розчиняють у мінімальній кількості метанолу та додають діетиловий ефір (50 мл). Цей розчин центрифугують протягом 15 хвилин. Надосадну рідину упарюють досуха і залишок сушать під високим вакуумом з одержанням продукту у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, CD3OD): 0,90 (t, 3H, 3J = 7,5 Гц), 1,25-1,41 (m, 8H), 1,45 (bs, 2H), 1,87 (bs, 2H), 2,38 (bs, 6H), 3,29 (bs, 27Н), 3,67 (t, 6H, 3J = 7,5 Гц), 4,01 (t, 2H, 3J = 7,5 Гц), 4,30 (t, 6H, 3J = 7,5 Гц), 7,11 (d, 2H, 3J = 7,5 Гц), 7,38 (d, 6H, 3J = 7,5 Гц), 7,95 (d, 2H, 3J = 7,5 Гц), 8,11 (d, 6H, 3J = 7,5 Гц), 8,93 (bs, 8H). 59 94027 60 Сполука 47 Трихлорид 5-(4-додецилоксифеніл)-10,15,20трис-[4-(3-триметиламоніопропілокси)феніл)порфірину Сполуку 44 (50 мг, 0,059 ммоль) та (3бромпропіл)триметиламонійбромід (154 мг, 0,59 ммоль, 10 екв.) розчиняють і карбонат калію (122 мг, 0,885 ммоль, 15 екв.) суспендують в атмосфері аргону в абсолютному ДМФ (30 мл) і цю суміш перемішують при 55 °С протягом 12 годин. Розчинник видаляють під вакуумом при 50 °С і залишок повторно розчиняють у невеликій кількості метанолу та наносять на шар силікагелю (товщина 2 см). Непрореаговані солі амонію вимивають метанолом (1000 мл). Продукт елююють сумішшю оцтова кислота:метанол:вода (3:2:1 по об'єму). Розчинники видаляють при зниженому тиску та неочищений продукт додатково очищають хроматографією на колонці (100 г) Sephadex LH-20 з використанням суміші н-бутанол:вода:оцтова кислота (4:5:1, по об'єму, верхня фаза) як елюенту. Розчинники видаляють при зниженому тиску і залишок розчиняють у невеликій кількості метанолу та пропускають цей розчин через коротку колонку аніонообмінної смоли (Amberlite IRA 400, хлоридна форма) з використанням метанолу як елюенту. Після випарювання розчинника неочищений продукт повторно розчиняють у мінімальній кількості метанолу та додають діетиловий ефір (50 мл). Цей розчин центрифугують протягом 15 хвилин. Надосадну рідину упарюють досуха та залишок сушать під високим вакуумом з одержанням продукту у вигляді фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, CD3OD): 0,88 (t, 3Н, 3J = 7,5 Гц), 1,25-1,37 (m, 16H), 1,48 (bs, 2H), 1,93 (bs, 2H), 2,42 (bs, 6H), 3,28 (bs, 27H), 3,68-3,75 (m, 6H), 4,05 (t, 2Н), 4,33 (t, 6H), 7,17 (d, 2H, 3J = 7,5 Гц), 7,33 (d, 6H, 3J = 7,5 Гц), 7,99 (d, 2H, 3J = 7,5 Гц), 8,08 (d, 6Н, 3J = 7,5 Гц), 8,85 (bs, 8H). Сполука 48 Трихлорид 5-(4-нонілоксифеніл)-10,15,20-трис[4-(3-триметиламоніо-пропілокси)феніл]порфірину Сполуку 45 (50 мг, 0,062 ммоль) та (3бромпропіл)триметиламонійбромід (162 мг, 0,62 ммоль, 10 екв.) розчиняють і карбонат калію (128 мг, 0,93 ммоль, 15 екв.) суспендують в атмосфері аргону в абсолютному ДМФ (30 мл) і цю суміш перемішують при 55 °С протягом 12 годин. Розчинник видаляють під вакуумом при 50 °С і залишок повторно розчиняють у невеликій кількості метанолу та наносять на шар силікагелю (товщина 2 см). Непрореаговані солі амонію вимивають метанолом (1000 мл). Продукт елююють сумішшю оцтова кислота:метанол:вода (3:2:1 по об'єму). Розчинники видаляють при зниженому тиску і цей продукт додатково очищають хроматографією на колонці (100 г) Sephadex LH-20 з елюцією сумішшю н-бутанол:вода:оцтова кислота (4:5:1, по об'єму, верхня фаза). Розчинники видаляють при зниженому тиску і залишок розчиняють у невеликій кількості метанолу та пропускають цей розчин через коротку колонку аніонообмінної смоли (Amberlite IRA 400, хлоридна форма) з використанням метанолу як елюенту. Після видалення розчинника продукт сушать під високим вакуумом з одержанням фіолетової твердої речовини. 1 Н-ЯМР: δΗ (300 МГц, CD3OD): 0,89 (t, 3H, 3J = 7,5 Гц), 1,18-1,34 (m, 10Н), 1,41 (bs, 2H), 1,73 (quint, 2H, 3J = 7,5 Гц), 2,30-2,44 (m, 6H), 3,31 (bs, 27Н), 3,65-3,73 (m, 6H), 3,93 (t, 2H, 3J = 7,5 Гц), 4,25-4,42 (m, 6H), 7,08 (d, 2H, 3J = 7,5 Гц), 7,30 (d, 6H, 3J = 7,5 Гц), 7,93 (d, 2H, 3J = 7,5 Гц), 8,05 (d, 6H, 3 J = 7,5 Гц), 8,94 (bs, 8H). Сполука 49 Трихлорид 5-(4-октилоксифеніл)-10,15,20трис-[4-(5-триметиламоніопентилокси)феніл]порфірину Сполуку 43 (23 мг, 0,03 ммоль) та (5бромпентил)триметиламонійбромід (84 мг, 0,3
ДивитисяДодаткова інформація
Назва патенту англійськоюNovel uses of porphyrin compounds
Автори англійськоюLove William G., Rhys-Williams William, Brundish Derek
Назва патенту російськоюПрименение соединений порфирина
Автори російськоюЛав Уильям Г., Рис-Уильямс Уильям, Брандиш Дерек
МПК / Мітки
МПК: A61K 31/409, A61P 31/00
Мітки: сполук, застосування, порфірину
Код посилання
<a href="https://ua.patents.su/40-94027-zastosuvannya-spoluk-porfirinu.html" target="_blank" rel="follow" title="База патентів України">Застосування сполук порфірину</a>
Попередній патент: Боковина з пристосуваннями для закріплення поверхневих накладок
Наступний патент: Амідосполуки та їх застосування як лікарських засобів
Випадковий патент: Спосіб екстреної адаптації практично здорових осіб до короткочасного перебування у льодяній воді без наслідків застудних захворювань












