Застосування сполук аміноадамантану як імунорегуляторів
Формула / Реферат
1. Застосування похідного аміноадамантану формули (І)
,
де R1, R2, R3 і R4 незалежно вибрані з –NR5R6, -NR5R6R7+, водню, арилу або гетероарилу,що містить до 7 членів, С1-С20-алкілу, С1-С20-алкенілу і С1-С20-алкінілу, де залишки алкілу, алкенілу та алкінілу можуть бути розгалуженими, нерозгалуженими або циклізованими і необов'язково заміщеними галогеном, арилом або гетероарилом, що містить 7 членів, за умови, що принаймні один із залишків R1, R2, R3 і R4 являє собою -NR5R6 або -NR5R6R7, і
R5, R6 і R7 незалежно вибрані з водню, арилу або гетероарилу з кільцем, що містить до 7 членів, С1-С20-алкілу, С1-С20-алкенілу та С1-С20-алкінілу, де залишки алкілу, алкенілу та алкінілу можуть бути розгалуженими, нерозгалуженими або циклізованими та необов'язково заміщеними галогеном, арилом або гетероарилом, що містить до 7 членів, або R5 і R6 разом з атомом азоту утворюють гетероциклічну групу,що містить до 7 членів, для збільшення активності вже активованих нейтрофілів.
2. Застосування за п. 1, яке відрізняється тим, що похідне аміноадамантану формули (І) вибране з
1-аміно-3-етил-5,7-диметиладамантану,
1-аміно-3-циклогексиладамантану,
1-аміно-3-етиладамантану,
1-аміно-3,5-диметиладамантану,
1-аміно-3,5-диетиладамантану,
1-N-метиламіно-3,5-диметиладамантану,
1-N-етиламіно-3,5-диметиладамантану.
3. Спосіб збільшення активності вже активованих нейтрофілів, який передбачає контакт вказаних нейтрофілів з похідним аміноадамантану формули (І) у концентрації від 10-6 до 10-5 М у плазмі крові.
4. Фармацевтична композиція, яка включає похідне аміноадамантану формули (І) у терапевтично ефективній кількості, що забезпечує концентрацію вказаного похідного аміноадамантану у плазмі крові у межах від 10-6 до 10-5 М.
5. Фармацевтична композиція за п. 4, яка відрізняється тим, що додатково включає активатор нейтрофілів.
6. Фармацевтична композиція за п. 5, яка відрізняється тим, що активатор вибирають з зимозану, N-форміл-Меt-Leu-Phe та A23187.
7. Фармацевтична композиція за будь-яким з пунктів 4, 5 та 6, яка відрізняється тим, що її застосовують для лікування агрануломатозу, грануломатозу Вегенера та імунодефіцитів, зокрема синдрому набутого імунодефіциту.
Текст
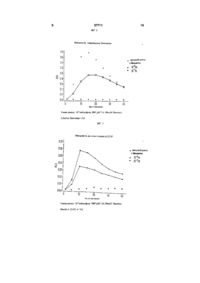
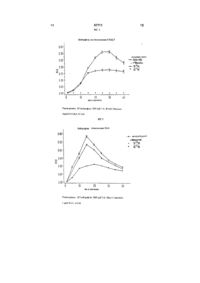
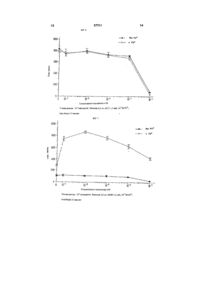
1 Застосування похідного аміноадамантану формули (І) R, (ї) де R-і, R2, R3 1 R4 незалежно вибрані з -NR5R6, NRsR6R7+, водню, арилу або гетероарилу.що містить до 7 членів, Сі-Сго-алкілу, Сі-Сго-алкенілу і Сі-Сго-алкінілу, де залишки алкілу, алкенілу та алкінілу можуть бути розгалуженими, нерозгалуженими або циклізованими і необов'язково заміщеними галогеном, арилом або гетероарилом, що містить 7 членів, за умови, що принаймні один із залишків Ri, R2, R3 і R4 являє собою -NR5R6 або -NR5R6R7, і R5, R6 і R7 незалежно вибрані з водню, арилу або гетероарилу з кільцем, що містить до 7 членів, С г Сго-алкілу, Сі-Сго-алкенілу та Сі-Сго-алкінілу, де залишки алкілу, алкенілу та алкінілу можуть бути розгалуженими, нерозгалуженими або циклізованими та необов'язково заміщеними галогеном, арилом або гетероарилом, що містить до 7 членів, або Rs 1 R6 разом з атомом азоту утворюють гетероциклічну групу.що містить до 7 членів, для збільшення активності вже активованих нейтрофілів 2 Застосування за п 1, яке відрізняється тим, що похідне аміноадамантану формули (І) вибране з 1-амшо-3-етил-5,7-диметиладамантану, 1 -аміно-3-циклогексиладамантану, 1 -аміно-3-етиладамантану, 1-амшо-3,5-диметиладамантану, 1 -амшо-3,5-диетиладамантану, 1-І\І-метиламіно-3,5-диметиладамантану, 1-І\І-етиламіно-3,5-диметиладамантану 3 Спосіб збільшення активності вже активованих нейтрофілів, який передбачає контакт вказаних нейтрофілів з похідним аміноадамантану формули (І) у концентрації від 10 6 до 10 Му плазмі крові 4 Фармацевтична композиція, яка включає похідне аміноадамантану формули (І) у терапевтично ефективній КІЛЬКОСТІ, ЩО забезпечує концентрацію вказаного похідного аміноадамантану у плазмі крові у межах від 10 6 до 105М 5 Фармацевтична композиція за п 4, яка відрізняється тим, що додатково включає активатор нейтрофілів 6 Фармацевтична композиція за п 5, яка відрізняється тим, що активатор вибирають з зимозану, І\І-форміл-МеМ_еи-Ргіе та А23187 7 Фармацевтична композиція за будь-яким з пунктів 4, 5 та 6, яка відрізняється тим, що и застосовують для лікування агрануломатозу, грануломатозу Вегенера та імунодефіцитів, зокрема синдрому набутого імунодефіциту О і ю 57711 Винахід стосується застосування аміноадамантанових похідних у якості імунорегуляторів зокрема, для регулювання і модулювання вже активованих нейтрофілів Нейтрофіли, підклас лейкоцитів, утягнуті в процеси імунного захисту і ІНШІ реакції в кровоносній системі і навколишніх тканинах (Roitt, І М Leitfaden, der Immunologie, Steinkopf-Verlag Darmstadt, 2 n d edition 1984) Нейтрофіли можуть активуватися екзогенними речовинами, наприклад, такими як компоненти стінок клітин (промислове виробленим продуктом є «Зимозан» («Zymosan»),) У зв'язку з цим утворюються реакційноздатні частинки кисню в так званому респіраторному вибуху На Фіг 1 показана спрощена схема стимуляції нейтрофілів Після зв'язування ліганду (наприклад, Зимозану А) із специфічним рецептором мембрани нейтрофілу активується гуанозинтрифосфат (GTP), який, в свою чергу, активує специфічну до фосфатидил-шозитол-4,5біфосфату (РІРг) фосфоліпазу С (PLC) Фосфоліпаза С каталізує гідроліз фосфатидилшозитол-4,5-біфосфату до шозитол-1,4,5трифосфату (ІРз) і діацилгліцерину (DG) Інозитол4,5-трифосфат стимулює виділення ІОНІВ Са 2+ із внутрішньоклітинних запасів Іони Са2+, з діацил гліцерином, активують протешкіназу С (РКС), яка фосфорилює багато білків і таким чином активує, серед інших, комплекс* NADPH (відновлений нікотин-амідаденшдинуклеотидфосфат) і оксидази В свою чергу, комплекс NADPH-оксидаза каталізує реакцію 2О2 + NADPH 2 + NADP+ Н+ в якій утворюються реакційно-здатні кисневі частинки Ог Хоча активовані нейтрофіли є важливими для функціонування імунного захисту, в результаті надлишкових реакцій, що викликаються особливо реакційноздатними кисневими частинками, можуть з'являтися симптоми захворювання, такі як гострі або хронічні запалення або ІНШІ алергічні реакції З іншого боку, активність нейтрофілів може бути занадто низькою або недостатньої для успішного імунного захисту при наявності загального імунодефіциту, наприклад, як це має місце при СНІДі Отже, існує потреба, особливо з медичної точки зору, у можливості впливати на регулятивну і/або модулюючу активність нейтрофілів in vivo і in vitro У зв'язку з цим, активність нейтрофілів потрібно підвищувати або знижувати в залежності від показань, тобто потрібно, щоб нею можна було керувати довільно Отже, метою цього винаходу є розробка засоб\ для регулювання і/або модулювання активності нейтрофілів Несподівано, в останній час було встановлено, що певні ПОХІДНІ адамантану мають регулятивний і/або модулюючий вплив на активність нейтрофілів Цей винахід пов'язаний з цим відкриттям Вирішальна обставина в зв'язку з цим полягає в тому, щоб нейтрофіли вже були активовані іншими стимуляторами Самі по собі аміноадамантани не виявляють якого б то не було активуючого впливу на нейтрофіли ВІДПОВІДНО, вказана вище вирішується шляхом застосування аміноадамантану формули (І) проблема похідного І) де R-i, R2, R3 і R4 незалежно обрані з -NR5R6, NR5R6R7, водню, арилу або гетероарилу з кільцем аж до 7-членного, Сі-Сго-алкілу, Сі-Сго-алкенілу і Сі-Сго-алкінілу, де залишки алкіл, алкеніл і алкініл можуть бути розгалуженими, нерозгалуженими або циклізованими і необов'язково заміщені галогеном, арилом або гетероарилом з кільцем аж до 7-членного, за умови, що принаймні, один із залишків R-i, R2, R3 і R4 являє собою -NR5R6 або NR5R6R7 і R5, R6 і R7 незалежно обрані з водню, арилу або гетероарилу з кільцем аж до 7-членного, d Сго-алкілу, Сі-Сго-алкенілу і Сі-Сго-алкінілу, де залишки алкіл, алкеніл і алкініл можуть бути розгалуженими, нерозгалуженими або циклізованними і необов'язково заміщеними галогеном, арилом або гетероарилом з кільцем аж до 7-членного або Rs 1 R6, разом з атомом азоту утворять гетероциклічну групу з кільцем аж до 7членного, для регулювання активності вже активованих нейтрофілів ВІДОМІ ПОХІДНІ аміноадаманту цього типу Так 1 -аміноадамантани описані в DE 2219256, DE 2856393 DE 2232735 US 3450761 або 4122193 Одержання сполук формули (І) звичайно здійснюється відомими методами, такими як, наприклад, алкілювання галогенадамантанів Наступне потім подальше галогенування і алкілювання дає окремі ди-і/або тризаміщені адамантани Патент ЕР 392 059, зміст якого недвозначним чином включено тут для відома, відноситься до одержання аміноадамантанів ПОХІДНІ аміноадамантану також вже використовувалися у фармацевтичних цілях Так, в ЕР 392059 описується застосування похідних аміноадамантану для лікування хвороби Альцгеймера або ушкодження клітин головного мозку в результаті церебральної ішемії У патенті US 3450761 описуються аміноадамантани з противірусною активністю Чи відбувається підвищення або часткове або повне придушення активності" нейтрофілів, залежить від концентрації використаного похідного аміноадамантану Так концентрації від 10 6 до 10 5 М мають дію, що підвищує активність Показано, що концентрація біля 5 10 6 М особливо ефективна для підвищення активності нейтрофілів, причому ця концентрація цілком може бути досягнута m vivo у плазмі крові На противагу цьому, в результаті підвищення концентрації амшоадамантаиу відбувається гальмування 57711 6 активності Підхожа для цієї ЦІЛІ концентрація аміноадамантан можуть особливо ефективно становить від 10 4 до 10 3 М боротися зі станами зовнішнього і внутрішнього запалення, наприклад, коліна, тазостегнового Винахід включає ПОХІДНІ адамантану, що суглоба або щелепи, а також з аутоімунними заміщені однією або декількома аміногрупами, захворюваннями Іншою областю застосування є серед яких моноаміноадамантани є кращими лікування паразитарних захворюванні, таких як Отже придатними сполуками формули (І) є ті, у лейшманіоз яких Ri являє собою аміногрупу, наприклад, такі як 1-амшо-5-етил-5,7-диметиладамантан, а також В зв'язку з цим, забезпечення подхожої сполуки, у яких Ri являє собою аміногрупу, a R3 і концентрації похідних аміноадамантану для R4 представляють атом водню, наприклад, такі як регулювання і модулювання активності 1 -аміно-3-циклогексиладамантан, 1 -аміно-3 нейтрофілів шляхом вибору підхожої дози і форми етиладамантан введення залишається на розсуд лікаря У залежності від області застосування, тут можливі Кращими похідними адамантану є 1-амшо-3,5парентеральні форми, наприклад, внутрішньовенні диметиладамантан 1-амшо-3,5-диетиладамантан або пероральні форми введення, придатними є і N-заміщені сполуки 1-І\І-метиламшо-3,5також форми тривалої дії Винахід включає також диметиладамантан і сполука 1-Х-етиламшо-З 5сполучення похідних аміноадамантану ВІДПОВІДНО диметиладамантан Найкращими кращим є 1до винаходу, а також їх фармацевтичне аміно-3 5-диметиладамантан названий мемантин прийнятних солей, особливо кислотно-адитивних (INN, Akatmol Memantme) В роботі Gortelmeyer R , солей, як приклад тут повинні бути названі* et al Spectrum of Neurorehabihtation W пдрохлориди пдроброміди, сульфати, ацетати, Zuckscrmerdt Publishers Munich, 1993 50ff сукцинати, тартрати або сполуки приєднання описане лікування мемантином синдрому Деменса фумарової, малеїнової, лимонної або фосфорної (Demens syndrome) кислот Фармацевтичні композиції можуть Як пояснювалося вище, ПОХІДНІ додатково містити активатор нейтрофілів, у аміноадамантану ВІДПОВІДНО ДО ЦЬОГО винаходу залежності від кола показань Для виготовлення здійснюють регулюючий вплив тільки на складу використовуються звичайні нейтрофіли, які попередньо активовані або були стимульовані спеціальними активаторами У якості активаторів ВІДОМІ речовини природного походження, такі як Зимозан, Nформіл-Met-Leu-Phe (N-FMLP) або А 23187 (антагоніст Са) Ці речовини можуть застосовуватися, якщо хто-небудь має намір здійснити специфічне і більш сильне активування нейтрофілів як in vitro, так і in vivo Завдяки цьому можливо виявлення нейтрофілів у зразку, наприклад, у зразку рідини з організму, зокрема в зразку крові, навіть у тому випадку, коли є в наявності лише мала КІЛЬКІСТЬ нейтрофілів або коли їхня активність дуже слабка В зв'язку з цим, у сполученні з похідними аміноадамантану може бути присутнім активатор Ступінь активації нейтрофілів, що викликана активатором, збільшується шляхом одночасного додавання похідного аміноадамантану Наступною областю застосування є поліпшення імунного захисту для пацієнтів із різноманітними формами імунної недостатності, особливо для пацієнтів із СНІДом В такому випадку може вводитися фармацевтична композиція, що містить похідне аміноадамантану ВІДПОВІДНО до винаходу, необов'язково в сполученні з активатором нейтрофілів Крім того, можливо застосування при таких захворюваннях агрануломатоз (CGD) грануломатоз Вегенера і/або накопичення глікогену Саме собою зрозуміло, нейтрофіли можуть також активуватися внаслідок природної імунної реакції організму, як наприклад, реакція на різноманітні імуногени і алергічні реакції, запалення і ревматичні симптоми, що ініційовані внаслідок надлишкової реакції У таких випадках активність нейтрофілів може послаблятися аміноадамантаном \ підвищений до підхожого рівня концентрації, і пацієнт може одержати полегшення Лікарські препарати, що містять фармацевтично прийнятні носи і ад'юванти Наступний приклад ілюструє за допомогою певної сполуки - мемантину - залежність впливу похідних аміноадамантану на підвищення або придушення активності Приклад Принцип виміру Визначення активності стимульованих нейтрофілів при різних концентраціях мемантину проводили шляхом виміру із застосуванням хемілюмінесценції Активовані нейтрофіли утворюють реакційноздатні кисневі частинки при респіраторному вибуху, які реєструються у виді дуже слабкої хемілюмінесценції - так званий низький рівень зверх слабкої хемілюмінесценції Щоб підвищити вихід фотонів, у якості сенсибілізатору додають люмінол (залежна від індикатора хемілюмінесценція) Люмінол являє собою циклічний гідразид, що може окислятися реакційно-здатними кисневими частинками до діазохшону При нуклеофільній атаці аніону перекису водню цей діазохшон далі перетворюється в а-пдроксипдропероксид, що при висиланні світла розкладається до амінофталату Суміш для реакції Нейтрофіли 10 6 і А (?) ЗФР-буфер, рН (7,4) до 250мл люмінол 80мМ мемантин змінювана концентрація стимулюючий засіб зимозан 2,5мг/мл або РМА 1мМ або А 23 187 20мМ a6oN-FLMP 10м ЗФР - забуферений фосфатом фізіологічний розчин РіМА - Форбол-Містрат-Ацетат (PhprbolMystrate- Acetate) Ангалопчні реакційні суміші можуть бути 57711 виготовлені з іншими похідними адамантану Вимір Вимір здійснювали за допомогою високочутливих фото-множників з низьким рівнем шуму, які перетворюють фотони на фото-катоді в первинні електрони і потім багаторазово посилюють останні до сигналу у виді електричного імпульсу Реакцію починали за допомогою стимулятору і здійснювали виміри без інкубаційного періоду протягом 40 хвилин (= 80 циклів) Результати 8 Для нейтрофілів, що були активовані природними стимуляторами (Зимозан А, А 23187, М-форміл-Met-Leu-Phe) вихідний показник RLU (RLU = Relative Light Units, ВІДНОСНІ СВІТЛОВІ одиниці) може бути додатково підвищений за допомогою 1 0 6 М метамшу (для Зимозану А приблизно на 90%, для А 23187 приблизно на 60%, для N-FMLP приблизно на 78% від вихідної стимуляції) [Фіг 2-4] Це припускає підвищений респіраторний вибух і підвищену активність фагоцитозу Ця реакція не відбувається при стимуляції токсичною сполукою Форбол-МістратАцетат (Phorbol-Mystrate-Acetate) (біля -20% від вихідної стимуляції) [Фіг 5] На противагу цьому, мемантин у концентрації 1 0 3 майже цілком придушує вихідну стимуляцію будь-якими стимуляторами В контрольному експерименті можна показати, що сам по собі мемантин не має хемілюмінесценції і не гасить хемілюмінесценцію (не показане) Специфічність регуляції активації Регулятивний вплив похідних аміноадамантану ВІДПОВІДНО ДО винаходу є дуже 8 специфічним для нейтрофілів Так, у похідних аміноадамантану не виявляється ніякого впливу на ефект дерегулювання активованих лейкоцитів З фіг 6 випливає, що сама по собі АСС (1 аміноциклопропан-1-карбонова кислота) не взаємодіє з мемантином у відносно високих концентраціях АСС є специфічним індикатором для мієлопероксидази що виділяється за допомогою дегрануляцм лейкоцитів і утворює в міжклітинному просторі руйнівний гіпохлорит Мієлопероксидаза специфічно взаємодіє з АСС з утворенням етилену, який може детектуватися газохроматографічним способом Внаслідок цього, КІЛЬКІСТЬ етилену, що утворюється, являє непрямий вимір КІЛЬКІСНОГО вираження активності лейкоцитів На противагу цьому, індикатор для респіраторного вибуху і виникаючі з нього кисневі радикали (супероксид, ОН-радикали і пдропероксид) активуються мемантином Це 7 виявляється вже при концентрації лише 10 М, яка може бути легко отримана in vivo Вплив активації може бути зроблений видимим шляхом додавання Fe+3 який зрушує рівновагу реакції завдяки реакції Хабера-Вайса (Haber-Weib reaction) від супероксиду і пдропероксиду в напрямку ОКрадикалів Чутливим індикатором для частинок кисню є КМВ (a-KCTO-g-метилтіобутират), який розкладається в окисних умовах, у числі іншого, до етилену, і який може легко детектуватися [фіг 7] В якості контрольного експерименту на фіг 8 показано, що при додаванні Fe+3 у концентрації > 5 х10 4 М першою стимулюється реакція КМВ, але не реакція АСС Самий по собі Fe впливу не здійснює ФІГ І 57711 10 ФІГ 2 Нейтрофіли, стимульовані Зимозаном я вихдашй рівень + Мвяаятин 2(3 З О час в чвилнна\ Умови реакції іО°кейірофпи І ЗФР(рН74) 80мкМ Люміноі, 2,5мг/чл Знмочакрі- 2ч6 ФІГ З Неитрсфпн, які стмм\ іьоваш А 2 вихідний рівень + Мемантин Умови реакції ІС'нейтрофши ЗФР (рН 7,4), 80мкМ Люмшоя, 20мкМА23Ш,п-2х6 57711 11 12 ФІГ 4 Нейтрофпи, які стимульован! F-FMLP 10 20 ЗЕ час в хвилинам Умови реакції 10'нейтрофіли, 1ФР(рН7 4) КОмкМЛюмтол ФІГ 5 Нейтрофіли стимульовані РМА вичщішй рм Мемантин ІО'ВМ 10"3М 10 20 ЗО час в хвичинах Умови реаьцн Ю'кейтрофпн ЗФР(рН7.4) 80міЛїЛюміноі. 14 57711 13 Ф!Гб 3 —я— без Fe *" концентрація мемзнїііиу в М 3 3i Умов» реакції 10 'лейкоцити, Зимозан 2,5 мг,АСС 1,5 мМ, 1 0 M F e , Інкубація 15 чвияни < ФІГ? —и— -о— £.00 ~ Q 10-1 10 Концентрація мемантину в М Улшаи реачші Ш'ленкоикти, Зимозвн 2,5 иг, КМВ І,5мМ, І 0 ' 3 М Р е 3 ' , Інкубація 15 хвилин без F e a i с Fe3i 15 16 57711 "•ЭЕ 2500 зг Індикатор КМВ 20 0C Індикатор АСС 10 00 Ю ,0Ч Концентрація Ге' в М Умови радиш " 0 ' л Є И к о и т , , З к Ч о Ю я 2 , 5 м г , і В Д Ш » ю р 1,5 мМ. /-h/бащябОхвипия Комп'ютерна верстка О В Курасв Підписано до друку 05 08 2003 Тираж39 прим Міністерство освіти і науки України Державний департамент інтелектуальної власності, Львівська площа, 8, м Київ, МСП, 04655, Україна ТОВ "Міжнародний науковий комітет", вул Артема, 77, м Київ, 04050, Україна
ДивитисяДодаткова інформація
Назва патенту англійськоюAminoadamantane compounds as immunomodulators
Назва патенту російськоюПрименение соединений аминоадамантана как иммунорегуляторов
МПК / Мітки
МПК: A61K 38/06, A61P 7/00, A61P 31/00, A61K 31/14, A61P 31/18, A61P 33/02, A61K 31/132, A61P 29/00, A61K 31/135, A61K 31/42, G01N 33/49, A61K 31/00, A61P 37/00, A61P 33/00, A61P 35/00, A61K 31/13
Мітки: застосування, сполук, імунорегуляторів, аміноадамантану
Код посилання
<a href="https://ua.patents.su/8-57711-zastosuvannya-spoluk-aminoadamantanu-yak-imunoregulyatoriv.html" target="_blank" rel="follow" title="База патентів України">Застосування сполук аміноадамантану як імунорегуляторів</a>
Попередній патент: Пневмоакумулятор для пуску дизельного двигуна
Наступний патент: Фармацевтична композиція, що містить похідну гідроксамової кислоти, спосіб лікування з її використанням та протектор мітохондріального геному та/або мітохондрій
Випадковий патент: Спосіб улаштування зовнішньої теплоізоляції будинку