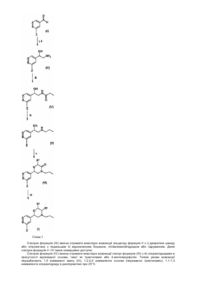
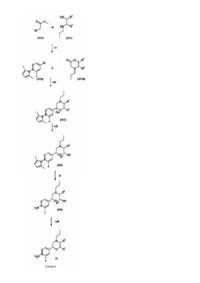
Похідні морфоліну для застосування як агоністів допаміну при лікуванні статевої дисфункції
Номер патенту: 79024
Опубліковано: 10.05.2007
Автори: Бакстер Ендрю Дуглас, Кук Ендрю Саймон, Хепворт Девід, Аллєртон Шарлотт Мойра Норфор, Вон Стефен Квок-Фун
Формула / Реферат
1. Сполуки формули (І), (Іа) і (Іb)
 , (I)
, (I)
 , (Ia)
, (Ia)
 , (Ib)
, (Ib)
де
А вибраний з С-Х і N,
В вибраний з C-Y і N,
R1 вибраний з Н і (С1-С6)алкілу,
R2 вибраний з Н і (С1-С6)алкілу,
Х вибраний з Н, HO, C(O)NH2, NH2,
Y вибраний з Н, НО, NH2, Br, Cl і F,
Z вибраний з Н, НО, F, CONH2 і CN;
і їх фармацевтично прийнятні солі, сольвати і проліки;
за умови, що
для сполуки формули (І), (Іа) або (Іb), коли А являє собою С-Х, В являє собою C-Y, R1 являє собою Н або (С1-С6)алкіл і R2 являє собою Н або (С1-С6)алкіл, щонайменше один з X, Y і Z повинен являти собою ОН;
для сполуки формули (І), коли А являє собою С-Х і В являє собою C-Y, Y являє собою Н, Z являє собою Н, R1 являє собою Н і R2 являє собою Н, Х не може являти собою ОН.
2. Сполуки формули (І), (Іа) і (Іb) за п.1, де А являє собою С-Х або N, і В являє собою C-Y.
3. Сполуки формули (І), (Іа) і (Іb) за пп.1-2, де R1 являє собою Н, метил і етил.
4. Сполуки формули (І), (Іа) і (Іb) за пп.1-3, де R2 вибраний з Н і метилу.
5. Сполуки формули (І), (Іа) і (Іb) за пп.1-4, де Х вибраний з Н, ОН і NH2.
6. Сполуки формули (І), (Іа) і (Іb) за пп.1-5, де Y вибраний з Н, NH2, Cl і F.
7. Сполуки формули (І), (Іа) і (Іb) за пп.1-6, де Z вибраний з Н, НО і F.
8. Сполука за п. 1 вибрана з
R-(-)-3-(4-пропілморфолін-2-іл)фенолу,
S-(+)-3-(4-пропілморфолін-2-іл)фенолу,
гідрохлориду R-(-)-3-(4-пропілморфолін-2-іл)фенолу,
R-5-(4-пропілморфолін-2-іл)бензол-1,3-діолу,
S-5-(4-пропілморфолін-2-іл)бензол-1,3-діолу,
R-(+)-2-фтор-5-(4-пропілморфолін-2-іл)фенолу,
S-(-)-2-фтор-5-(4-пропілморфолін-2-іл)фенолу,
5-(4-пропілморфолін-2-іл)піридин-2-іламіну,
2-хлор-5-(4-пропілморфолін-2-іл)фенолу,
5-[(2S, 5S)-5-метил-4-пропілморфолін-2-іл]піридин-2-аміну,
5-[(2R, 5S)-5-метил-4-пропілморфолін-2-іл]піридин-2-аміну.
9. Сполуки формули (І), (Іа) і (Іb) за будь-яким з пп. 1-8 для застосування як лікарського засобу.
10. Застосування сполук формули (І), (Іа) і (Іb) за будь-яким з пп. 1-8 для одержання лікарського засобу для лікування стану, вибраного з порушення статевої функції, порушення статевої функції у жінок, включаючи розлад у вигляді зниженої активності сексуального бажання, розладу сексуального збудження, порушення оргазму і сексуального больового розладу; порушення еректильної функції у чоловіків, гіпертензії, нейродегенерації, психіатричних розладів, депресії (наприклад, депресії у ракових пацієнтів, депресії у пацієнтів з хворобою Паркінсона, депресії після інфаркту міокарда, субсиндромної симптоматичної депресії, депресії у жінок з безпліддям, депресії у дітей, великої депресії, одиночних епізодів депресії, рецидивуючої депресії, депресії, викликаної грубим поводженням з дітьми, післяпологової депресії і синдрому роздратованості у людей похилого віку), генералізованого тривожного розладу, фобій (наприклад, агорафобії, соціальної фобії і простих фобій), синдрому посттравматичного стресу, розладів особистості у вигляді уникнення, передчасної еякуляції, розладів споживання їжі (наприклад, невротичної анорексії і невротичної булімії), ожиріння, залежності від хімічних сполук (наприклад, пристрасті до алкоголю, кокаїну, героїну, фенобарбіталу, нікотину і бензодіазепінів), «гістамінового» головного болю, мігрені, болю, хвороби Альцгеймера, нав'язливо-компульсивного розладу, панічного розладу, розладів пам'яті (наприклад, деменції, амнестичних розладів і вікового зниження пам'яті (ACRD)), хвороби Паркінсона (наприклад, деменції при хворобі Паркінсона, паркінсонізму, викликаного нейролептиками, і пізніх дискінезій), ендокринних розладів (наприклад, гіперпролактинемії), судинного спазму (зокрема, судин головного мозку), мозочкової атаксії, розладів шлунково-кишкового тракту (включаючи зміни моторики і секреції), негативних симптомів шизофренії, передменструального синдрому, синдрому фіброміалгії, стресового нетримання, синдрому Турета, трихотиломанії, клептоманії, імпотенції у чоловіків, розладів у вигляді дефіциту уваги з гіперактивністю (ADHD), хронічної пароксизмальної гемікранії, головного болю (пов'язаного з судинними розладами), емоційної лабільності, патологічного плачу, розладу сну (каталепсії) і шоку.
11. Застосування за п. 10, де стан являє собою порушення статевої функції у жінок, порушення еректильної функції у чоловіків, нейродегенерацію, депресію і психіатричні розлади.
12. Застосування за п. 10, де стан являє собою порушення еректильної функції у чоловіків.
13. Застосування за п. 10, де стан являє собою розлад у вигляді зниженої активності сексуального бажання, розлад сексуального збудження, порушення оргазму і сексуальний больовий розлад у жінок.
14. Застосування за п. 13, де стан являє собою розлад сексуального збудження у жінок і супутній розлад у вигляді зниженої активності сексуального бажання.
15. Композиція, що містить сполуки формули (І), (Іа) і (Іb) за будь-яким з пп. 1-8 і фармацевтично прийнятний розріджувач або носій.
Текст
Даний винахід відноситься до класу агоністів допаміну, конкретніше, до класу агоністів, які вибіркові для D2 і D3. Ці сполуки також можна застосовувати для лікування і/або запобігання статевій дисфункції, наприклад, статевій дисфункції у жінок (FSD), зокрема, статевій дисфункції у жінок у вигляді розладу сексуального збудження (FSAD) і статевій - дисфункції у чоловіків, зокрема, еректильній дисфункції у чоловіків (MED). Під статевою дисфункцією, що згадується в даному описі, у чоловіків маються на увазі еякуляторні розлади, такі як передчасна еякуляція, аноргазмія (нездатність досягнути оргазму) або розлади сексуального бажання, такі як розлад у вигляді гіпоактивного сексуального бажання (HSDD; відсутність інтересу до сексу). Ці сполуки можна також застосовувати при лікуванні нейропсихіатричних розладів і нейродегенеративних розладів. Даним винаходом передбачені сполуки формули (І), (Іа) і (Іb) де А вибраний з С-Х і N, В вибраний з С-Υ і Ν, R1 вибраний з Н і (C1-C6) алкілу, R2 вибраний з Η і (C1-C6) алкілу, X вибраний з Н, HO, C(O)NH2 , NH2 Υ вибраний з Н, HO, NH2, Br, Cl і F Ζ вибраний з Η, HO, F, CONH2 і CN; і їх фармацевтично прийнятні солі, сольвати і проліки; за умови, що для сполуки (І), (Іа) або (Іb), коли А являє собою С-Х, В являє собою C-Y, R1 являє собою Η або (C1C6)алкіл і R2 являє собою Η або (C1-C6)алкіл, щонайменше один з Χ, Υ і Ζ повинен являти собою ОН; для сполуки формули (І), коли А являє собою С-Х і В являє собою C-Y, Y являє собою Η, Υ являє собою Н, R1 являє собою Η і R2 являє собою Н, то X не може являти собою ОН. Фармацевтично прийнятні солі сполук формули (І) включають в себе їх кислотно-адитивні солі і основні солі. Фармацевтично прийнятні солі сполук формули (І) можна легко отримати шляхом змішування разом розчинів сполуки формули (І) і, за необхідності, бажаної кислоти або основи. Сіль можна осадити з розчину і зібрати шляхом фільтрації або можна витягнути шляхом випаровування розчинника. Відповідні кислотно-адитивні солі утворюються з кислот, які утворюють нетоксичні солі, і прикладами є гідрохлорид, гідробромід, гідройодид, сульфат, бісульфат, нітрат, фосфат, гідрофосфат, ацетат, малеат, фумарат, лактат, тартрат, цитрат, глюконат, сукцинат, сахарат, бензоат, метансульфонат, етансульфонат, бензолсульфонат, паратолуолсульфонат і памоат. Відповідні основні солі утворюються з основ, які утворюють нетоксичні солі, і прикладами є солі натрію, калію, алюмінію, кальцію, магнію, цинку і діетаноламіну. Огляд відповідних солей можна знайти в публікації [Berge et al, J. Pharm. Sci., 66, 1-19, 1977]. Фармацевтично прийнятні сольвати сполук формули (І) включають в себе їх гідрати. В об'єм сполук формули (І) згідно з винаходом також включені їх поліморфи. Сполука формули (І) містить один або більше асиметричних атомів вуглецю і тому існує в двох або більше стереоізомерних формах. Виділення діастереоізомерів можна досягнути звичайними методиками, наприклад, фракційною кристалізацією, хроматографією або ВЕРХ стереоізомерної суміші сполуки формули (І) або її відповідної солі або похідного. Окремий енантіомер сполуки формули (І) можна отримати з відповідної оптично чистої проміжної сполуки або шляхом розділення, такого як ВЕРХ, відповідного рацемату з використанням відповідної хиральної підкладки, або шляхом фракційної кристалізації діастереоізомерних солей, утворених взаємодією відповідного рацемату з відповідною оптично активною кислотою або основою, в залежності від доцільності. Переважними сполуками згідно з винаходом є сполуки формули (Іа) і (Іb). Особливо переважними є сполуки формули (Іа). Переважно, якщо А являє собою С-Х, і В являє собою C-Y. Переважніше, якщо А являє собою N, і В являє собою C-Y. Переважніше, коли А являє собою С-Х, і В являє собою C-Y. Переважно, щоб R1 був вибраний з Η і (С1-С4) алкілу. Переважніше, коли R1 являє собою Н, метил і етил. Ще переважніше, коли R1 являє собою Η або метил. Найбільш переважно, коли R1 являє собою Н. Переважно, щоб R2 вибраний з Η і (С1-С4) алкілу. Переважніше, коли R2 вибраний з Н, метилу і етилу. Найбільш переважно, щоб R2 був вибраний з Η і метилу. В особливо переважному варіанті здійснення R2 являє собою Н. У ще одному переважному варіанті здійснення R2 являє собою метил. Переважно, якщо X вибраний з Н, ОН і ΝΗ2. Найбільш переважно, щоб X був вибраний з Η і ОН. В особливо переважному варіанті здійснення X являє собою Н. У ще одному особливо переважному варіанті здійснення X являє собою ОН. Переважно, якщо Υ вибраний з Η, ΝΗ2, СІ і F. Найбільш переважно, якщо Υ вибраний з Η і ΝΗ2. В особливо переважному варіанті здійснення Υ являє собою Н. У ще одному особливо переважному варіанті здійснення Υ являє собою ΝΗ2. Переважно, якщо Ζ вибраний з Η, ΗΟ і F. Найбільш переважно, щоб Ζ був вибраний з Η або НО. В особливо переважному варіанті здійснення Ζ являє собою Н. У ще одному особливо переважному варіанті здійснення Ζ являє собою НО. Особливо переважними є сполуки (і їх солі) згідно з винаходом, проілюстровані в даному описі; більш переважними є R-(-)-3-(4-пpoпiлмopфoлiн-2-iл) фенол (Приклад 7А) S-(+)-3-(4-пропілморфолін-2-іл) фенол (Приклад 7В) гідрохлорид R-(-)-3-(4-пpoпiлмopфoлiн-2-iл) фенолу (Приклад 8) R-5-(4-пропілмopфoлiн-2-iл)бензол-1,3-діол (Приклад 15А) S-5-(4-пропілморфолін-2-іл)бензол-1,3-діол (Приклад 15В) R-(+)-2-фтop-5-(4-пpoпiлмopфoлiн-2-iл)фенол (Приклад 23А) S-(-)-2-фтор-5-(4-пропілморфолін-2-іл)фенол (Приклад 23В) 2-бром-4-(4-пропілморфолін-2-іл)фенол (Приклад 30) 2-гідрокси-5-(4-пропілморфолін-2-іл)бензамід (Приклад 35) 2-нітро-4-(4-пропілморфолін-2-іл)фенол (Приклад 36) 2-аміно-4-(4-пропілморфолін-2-іл)фенол (Приклад 37) 5-(4-пропілморфолін-2-іл)піридин-2-іламін (Приклад 44А і 44В) 2-хлор-5-(4-пропілморфолін-2-іл)фенол (Приклад 54) 3-[(5S)-5-метил-4-пропілморфолін-2-іл]фенол (Приклад 60) 5-[(2S,5S)-5-метил-4-пропілморфолін-2-іл]піридин-2-амін (Приклад 66) 5-[(2R,5S)-5-метил-4-пропілморфолін-2-іл]піридин-2-амін (Приклад 67) Найбільш переважними є R-(-)-3-(4-пропілморфолін-2-іл)фенол (Приклад 7А) S-(+)-3-(4-пропілморфолін-2-іл)фенол (Приклад 7В) гідрохлорид R-(-)-3-(4-пpoпiлмopфoлін-2-iл)фенолу (Приклад 8) R-5-(4-пpoпiлмopфoлiн-2-iл)бензол-1,3-діол (Приклад 15А) S-5-(4-пропілморфолін-2-іл)бензол-1,3-діол (Приклад 15В) R-(+)-2-фтор-5-(4-пропілморфолін-2-іл)фенол (Приклад 23А) S-(-)-2-фтор-5-(4-пропілморфолін-2-іл)фенол (Приклад 23В) 5-(4-пропілморфолін-2-іл)піридин-2-іламін (Приклад 44А і 44В) 2-хлор-5-(4-пропілморфолін-2-іл)фенол (Приклад 54) 5-[(2S,5S)-5-метил-4-пропілморфолін-2-іл]піридин-2-амін (Приклад 66) 5-[(2R,5S)-5-метил-4-пропілморфолін-2-іл]піридин-2-амін (Приклад 67) Сполуки згідно з винаходом можна отримати відомим чином різними шляхами. Описані нижче шляхи ілюструють способи синтезу сполуки формули (І); фахівцеві в даній галузі буде зрозуміло, що сполуки формули (Іа) і (Іb) можна виділити, використовуючи відповідні методи розділення. Сполуки загальної формули І, де А являє собою С-Х, В являє собою C-Y, R1 являє собою Η або (C1C6)алкіл, R2 являє собою Н, і де Χ, Υ і Ζ мають значення, що визначаються в даному описі, можна отримати відповідно до схеми реакції 1. Сполуки формули (III) можна отримати внаслідок взаємодії альдегіду формули II з і) джерелом ціаніду або нітрометану з подальшим іі) відновленням бораном, літійалюмінійгідридом або гідруванням. Деякі сполуки формули II і III також комерційно доступні. Сполуки формули (IV) можна отримати внаслідок взаємодії сполук формули (III) з ііі) хлорангідридами в присутності відповідної основи, такої як триетиламін або 4-метилморфолін. Типові умови взаємодії передбачають 1,0 еквівалент аміну (III), 1,2-2,0 еквіваленти основи (переважно триетиламін), 1,1-1,3 еквіваленти хлорангідриду в дихлорметані при 25°С. Сполуки формули (V) можна отримати шляхом відновлення сполук формули (IV) з iv) відновлювальним агентом, таким як боран або літійалюмінійгідрид. Типові умови передбачають 1,0 еквівалент аміду (IV), 1,23,0 еквіваленти борану в ТГФ (тетрагідрофуран) при кип'ятінні із зворотним холодильником. Сполуки формули (V) можна також отримати шляхом відновного амінування сполук формули (III) відповідним альдегідом в присутності ціанборгідриду натрію. Сполуки формули (VI) можна отримати внаслідок взаємодії сполук формули V з ν) хлорацетилхлоридом або 2-заміщеними хлорацетилхлоридами (такими як 2-хлорпропіонілхлорид або 2-хлорбутирилхлорид) в присутності основи, такої як триетиламін, карбонат натрію і гідроксид калію. Типові умови передбачають 1,0 еквівалент аміну IV, 1,0-1,3 еквіваленти хлорангідриду, 1,2-2,0 еквіваленти триетиламіну в дихлорметані при 25°С, неочищену реакційну суміш потім розчиняють в ІРА (ізопропіловий спирт) з 1,2-3,0 еквівалентами водного гідроксиду калію. Сполуки формули (І) можна отримати внаслідок взаємодії сполук формули (VI) з vi) відновлювальними агентами, такими як боран або літійалюмінійгідрид. Типові умови передбачають 1,0 еквівалент аміду VI, 1,23,0 еквіваленти борану в ТГФ при кип'ятінні із зворотним холодильником. Фахівцеві в даній галузі буде зрозуміло, що в зв'язку з тим, що один з Χ, Υ або Ζ являє собою гідроксигрупу, буде необхідно захистити гідроксигрупу (групи) відповідною захисною групою по ходу трансформацій по схемі 1, потім видалити захисну групу. Способи зняття захисту фенольної групи залежать від захисної групи. Приклади методів захисту/зняття захисту [див. в "Protective groups in Organic synthesis" TW Greene and PGM Wutz]. Наприклад, коли гідроксигрупа захищена у вигляді простого метилового ефіру, умови зняття захисту включають в себе кип'ятіння із зворотним холодильником у 48% водному НВr протягом 1-24год. або перемішування з трибромідбораном в трихлорметані протягом 1-24год. Альтернативно, коли гідроксигрупа захищена у вигляді простого бензилового ефіру, умови зняття захисту включають в себе гідрування паладієвим каталізатором в атмосфері водню. Сполуки загальної формули (І), де А або В являє собою N, R1 являє собою Η або (C1-C6)алкіл, R являє собою Η і Χ, Υ і Ζ мають значення, що визначаються в даному описі, за умови, що один з Χ, Υ або Ζ являє собою ΝΗ2, можна отримати у відповідності до схеми реакції 2. Схема проілюстрована для сполук, де В являє собою C-Y, і де Υ являє собою ΝΗ2; фахівцеві в даній галузі буде зрозуміло, що в рівній мірі можна використати альтернативні сполуки. Сполуки формули (VII) можна отримати з використанням способу, описаного в [JP 2001048864]. Сполуки формули (VIII) можна отримати внаслідок взаємодії епоксиду (VII) з vii) пропіламіном. Типові умови взаємодії передбачають перемішування епоксиду з надлишком аміну або чистого або в диметилсульфоксиді. Сполуки формули (IX) можна отримати внаслідок взаємодії сполук формули (VIII) з ν) хлорацетилхлоридом або 2-заміщеними хлорацетилхлоридами (таким як 2-хлорпропіонілхлорид або 2хлорбутилілхлорид) в присутності основи, такої як триетиламін, карбонат натрію і гідроксид калію. Типові умови реакції передбачають 1,0 еквівалент аміну (VIII), 1,2-2,0 еквіваленти триетиламіну в дихлорметані при 25°С, потім неочищену реакційну суміш розчиняють в ІРА з 1,2-3,0 еквівалентами водного гідроксиду калію. Сполуки формули (X) можна отримати внаслідок взаємодії сполук формули (IX) з відновлювальними агентами, такими як літійалюмінійгідрид. Типові умови реакції передбачають 1,0 еквівалент аміду (X), 1,2 еквіваленти літійалюмінійгідриду в ТГФ при кип'ятінні із зворотним холодильником. Сполуки формули (І) можна отримати шляхом іх) зняття захисту. Типові умови передбачають 1,0 еквівалент сполуки X і 5 еквівалентів гідрохлориду гідроксиламіну в етанолі при кип'ятінні із зворотним холодильником. Сполуки загальної формули І, де А являє собою С-Х, В являє собою C-Y, R1 1 являє собою Η і R2 являє собою Η або (C1-C6)алкіл, і де Χ, Υ і Ζ мають значення, що визначаються в даному описі, можна отримати у відповідності до схеми реакції 3. Сполуки формули (XII) можна отримати внаслідок взаємодії складного ефіру амінокислоти (XI) з х) хлорангідридами в присутності відповідної основи, такої як триетиламін і 4-метилморфолін. Типові умови реакції передбачають 1 еквівалент складного ефіру амінокислоти (XI), 1 еквівалент хлорангідриду і 3 еквіваленти основи в дихлорметані при 25°С. Деякі сполуки формули (XI) комерційно доступні. Сполуки формули (XIII) можна отримати внаслідок взаємодії сполук формули (XII) з хі) комплексом боран-ТГФ з подальшим руйнуванням боран-азотного комплексу кислотою і захистом третбутилоксикарбонілом утвореного аміну. Типові умови взаємодії передбачають 1 еквівалент аміду (XII) з 3 еквівалентами ВН3-ТГФ при кип'ятінні із зворотним холодильником, охолоджування, обережне додавання 6М водної НСl і нагрівання при кип'ятінні із зворотним холодильником протягом ще 6год. Подальше випаровування розчинника, повторне розчинення в суміші метанол:вода (8:1) і додання 5 еквівалентів основи, такої як гідроксид калію, і 1,5 еквівалентів ди-трет-бутилдикарбонату і перемішування суміші протягом 72год. Сполуки формули (XIV) можна отримати внаслідок взаємодії сполук формули (XIII) з хіі) органічним розчином НСl. Типові умови взаємодії передбачають 1 еквівалент карбамата (XIII) і 1-10 еквівалентів 4М розчину НСl в диоксане при 25°С. Сполуки формули (XV) можна отримати внаслідок взаємодії сполук формули (XIV) з хііі) 2бромацетофеноном в присутності основи, такої як триетиламін або 4-метилморфолін. 2-бромацетофенони можна отримати з комерційних джерел або, альтернативно, отримати з початкового ацетофенону методом стандартного бронювання, добре відомим фахівцям в даній галузі. Типові умови передбачають 1 еквівалент аміноспирту (XIV) з 1-3 еквівалентами триетиламіну і 1 еквівалентом 2-бромацетофенону при 65°С. Сполуки формули (І) можна отримати внаслідок взаємодії сполук формули (XV) з xiv) триетилсиланом і триметилсилілтрифлатом. Типові умови передбачають додання 5-10 еквівалентів триетилсилану до 1 еквівалента морфолінолу (XV) в дихлорметані при -78°С, з подальшим доданням 2 еквівалентів триметилсилілтрифлату. Фахівцеві в даній галузі буде зрозуміло, що в зв'язку з тим, що один з Χ, Υ або Ζ являє собою гідроксигрупу, буде необхідно захистити гідроксигрупу (групи) відповідною захисною групою в ході трансформацій по схемі 3, потім видалити захисну групу. Способи зняття захисту фенольної групи залежать від захисної групи. Приклади методів захисту/зняття захисту [див. в "Protective groups in Organic synthesis" TW Greene and PGM Wutz]. Наприклад, коли гідроксигрупа захищена у вигляді простого метилового ефіру, умови зняття захисту включають в себе кип'ятіння із зворотним холодильником у 48% водному НВr протягом 1-24год., або перемішування з борантрибромідом в трихлорметані протягом 1-24год. Альтернативно, коли гідроксигрупа захищена у вигляді простого бензилового ефіру, умови зняття захисту включають в себе гідрування паладієвим каталізатором в атмосфері водню. Сполуки загальної формули (І), де стереоцентр альфа для азоту морфоліну абсолютно визначений, можна отримати, виходячи з гомохиральних сполук формули (XI), які можуть бути комерційно доступні або бути отримані способами, легко доступними для фахівця в даній галузі з хімічної літератури. Отримані сполуки формули (І) будуть містити суміш діастереоізомеров, які можна виділити на колонці ВЕРХ. Типові умови передбачають елюювання через колонку Chiralcel OJ-H з рухомою фазою 100% МеОН. Сполуки загальної формули (І), де один з А або В являє собою N, R1 являє собою Н, R являє собою Η або (C1-C6)алкіл, і Χ, Υ і Ζ мають значення, описані вище, за умови, що один з Χ, Υ і Ζ являє собою ΝΗ2, можна отримати у відповідності до схеми реакції 4. Схема проілюстрована для сполук, де В являє собою CY, і де Υ являє собою ΝΗ2; фахівцеві в даній галузі буде зрозуміло, що в рівній мірі можна використати альтернативні сполуки. Сполуки формули (XVIII) можна отримати внаслідок взаємодії сполук формули (XVI) з xv) аміноспиртами формули (XIV) в присутності основи, такої як триетиламін або 4-метилморфолін. Типові умови передбачають 1 еквівалент аміноспирту (XIV) з 1-3 еквівалентами триетиламіну і 1 еквівалентом сполуки формули (XVI) з використанням толуолу як розчинника при кімнатній температурі або вище. Сполуки формули (XVI) комерційно доступні. Сполуки формули (XIX) можна отримати внаслідок взаємодії сполук формули (XVIII) з xvi) металоорганічним реагентом, утвореним з броміду формули (XVII). Відповідні металоорганічні реагенти включають в себе реагенти Гріньяра (магнійорганічна сполука) або літійорганічні сполуки, які можна отримати з . броміду шляхом галогенметалічного обміну. Типові умови передбачають додання ізопропілмагнійхлориду до броміду (XVII) в безводному ефірному розчиннику, такому як тетрагідрофуран, при кімнатній температурі (для здійснення реакції галогенметалічного обміну) з подальшим доданням морфолінону (XVIII). Бромід (XVII) можна отримати, використовуючи спосіб, описаний в [W09932475]. Морфолінол (XIX) можна відновити до діолу (XX), вводячи його у взаємодію з гідридним відновлювальним агентом, таким як боргідрид натрію, в спиртовому розчиннику, такому як метанол. Сполуки формули (XXI) можна отримати з діолу (XX) шляхом іх) зняття захисту. Типові умови передбачають 1,0 еквівалент сполуки (XX) і 5 еквівалентів гідрохлориду гідроксил аміну в етанолі при кип'ятінні із зворотним холодильником. Сполуки формули (І) можна отримати шляхом xviii) циклізації сполук формули (XXI) при обробці кислотою. Типові умови передбачають концентровану сірчану кислоту і дихлорметан як розчинник при кімнатній температурі або вище. Всі з вказаних вище взаємодій і способів отримання нових початкових речовин, що використовуються в попередніх способах, реагенти і умови взаємодії є звичайними і відповідними їх функції або отриманню, а також методи виділення бажаних продуктів добре відомі фахівцям в даній галузі, з посиланням на літературні джерела, а також приклади і способи отримання, представлені в даному описі. Сполуки згідно з винаходом використовуються як селективні агоністи D3 для лікування патологічних станів. Існує ряд сполук з активністю обох агоністів, D2 і D3; однак застосування таких сполук пов'язане з великою кількістю побічних ефектів, включаючи нудоту, блювання, непритомність, гіпотонію і брадикардію, деякі з яких викликають серйозне занепокоєння. Раніше вважалося, що ефективність сполук попереднього рівня техніки була пов'язана з їх здатністю надавати агоністичну дію на D2; однак Б2-агонізм вважають причиною побічних ефектів, перерахованих вище. Даний винахід пов'язаний з класом селективних D3-агоністів. Несподівано, було виявлено, що вони ефективні при одночасному зниженні побічних ефектів, пов'язаних з неселективними сполуками попереднього рівня техніки. Сполуки згідно з винаходом можна застосовувати при лікуванні статевої дисфункції, статевої дисфункції у жінок, включаючи розлад у вигляді гіпоактивного сексуального бажання, розлад сексуального збудження, розлад оргазму і статевий больовий розлад; розлади еректильної функції у чоловіків, гіпертонії, нейродегенерації, психіатричних розладів, депресії (наприклад, депресії у ракових хворих, депресії у пацієнтів з хворобою Паркінсона, депресії після інфаркту міокарда, субсиндромної симптоматичної депресії, депресії у безплідних жінок, депресії у дітей, великої депресії, депресії у вигляді одиночних епізодів, рецидивуючої депресії, депресії, викликаної грубим поводженням з дітьми, післяпологової депресії і синдрому роздратованості у немолодих людей), розладу в формі генералізованої тривоги, фобій (наприклад, агорафобії, соціальної фобії і сенільних фобій), синдрому посттравматичного стресу, розлад особистості у вигляді уникнення, передчасної еякуляції, розладів споживання їжі (наприклад, невротичної анорексії і невротичної булімії), ожиріння, залежності від хімічних речовин (наприклад, залежність від алкоголю, кокаїну, героїну, фенобарбіталу, нікотину і бензодіазепінів), «гістамінового» головного болю, мігрені, болю, хвороби Альцгеймера, нав'язливо-компульсивного розладу, панічного розладу, розладів пам'яті (наприклад, деменції, амнестичних розладів і вікового зниження пізнавальної функції (ARCD)), хвороби Паркінсона (наприклад, деменції при хворобі Паркінсона, паркінсонізму, викликаного нейролептиками, і повільних дискінезій), ендокринних розладів (наприклад, гіперпролактинемії), судинного спазму (зокрема, судинної мережі мозку), мозжечкової атаксії, розладів шлунково-кишкового тракту (включаючи зміни моторики і секреції), негативних симптомів шизофренії, передменструального синдрому, синдрому фіброміалгії, стресового нетримання сечі, синдрому Турета, трихотиломанії, клептоманії, імпотенції у чоловіків, розлади дефіциту уваги з гіперактивністю (ADHD), хронічної пароксизмальної гемікранії, головного болю (пов'язаного з судинними розладами), емоційної лабільності, патологічного плачу, розладу сну (катаплексії) і шоку. Сполуки згідно з винаходом особливо підходять для лікування статевої дисфункції у жінок, порушення еректильної функції у чоловіків, нейродегенерації, депресії і психіатричних розладів. Сполуки згідно з винаходом можна застосовувати при статевій дисфункції у чоловіків, особливо при порушенні еректильної функції у чоловіків. Статеву дисфункцію у чоловіків (MED), інакше відому як порушення еректильної функції у чоловіків, визначають як «нездатність досягнути ерекції статевого члена і/або її підтримки для задовільної статевої функції» (NIH Consensus Panel on Impotence, 1993). За оцінками, поширеність порушення еректильної функції (ED) всіх мір (мінімальної, помірної і повної імпотенції) становить 52% у чоловіків у віці 40-70 років при більш високих частотах в осіб старших за 70 років [Melman et al 1999, J. Urology, 161, p.5-11]. Цей стан надає істотний негативний вплив на якість життя індивідуума і його партнера, часто приводячи до підвищеної тривоги і напруження, що веде до депресії і низької самооцінки. Хоча 2 десятиріччя тому MED вважали насамперед психологічним розладом [Benet et al 1994 Сотр. Ther., 20: 669-673], в цей час відомо, що у більшості індивідуумів є органічна причина, що лежить в основі цього явища. В результаті був досягнутий великий прогрес в ідентифікації механізму нормальної ерекції статевого члена і патофізіологічних механізмів MED. Ерекція статевого члена являє собою гемодинамічне явище, яке залежить від балансу скорочення і розслаблення гладкої мускулатури печеристих тіл і судинної мережі статевого члена [Lemer et al 1993, J. Urology, 149, 1255-1256]. Гладка мускулатура печеристих тіл також іменується в даному описі гладкою мускулатурою тіла або у множині печеристих тіл. Розслаблення гладкої мускулатури печеристих тіл веде до збільшеного кровотоку в трабекулярні простори кавернозного тіла, спричиняючи їх розширення до навколишньої оболонки, і здавлюють дренуючі вени. Це спричиняє велике підвищення артеріального тиску, яке приводить до ерекції [Naylor, 1998, J. Urology, 81, 424-431]. Зміни, які відбуваються під час процесу ерекції, складні і вимагають високої міри координованої регуляції, що залучає периферичну і центральну нервову системи і ендокринну систему [Naylor, 1998, J. Urology, 81, 424-431]. Скорочення гладкої мускулатури печеристих тіл модулюється симпатичною норадренергічною іннервацією за допомогою активації постсинаптичних a 1-адренорецепторів. MED може бути пов'язано із збільшенням ендогенного тонусу гладкої мускулатури печеристого тіла. Однак процес розслаблення гладкої мускулатури печеристого тіла частково опосередкований не-адренергічною, нехолінергічною (NANC) нейропередачею. Є ряд інших нейромедіаторів NANC, що виявляються в статевому членові, відмінних від NO, таких як пептид, пов'язаний з геном кальцитоніну (CGRP), і вазоактивний кишковий пептид (VIP). Основним розслабляючим фактором, відповідальним за опосередковування цього розслаблення, є окис азоту (NO), який синтезується з L-аргініну синтазою окису азоту (NOS) [Taub et al 1993 Urology, 42, 698-704]. Вважають, що зниження тонусу гладкої мускулатури печеристих тіл може сприяти NO в індукції розслаблення печеристого тіла. Під час сексуального збудження у чоловіків NO вивільняється з нейронів і ендотелію і зв'язується з розчинної гуанілатциклазою (sGC) і активує її в гладком'язових клітинах і ендотелії, приводячи до підйому рівнів внутрішньоклітинної циклічної гуанозин-3',5'-монофосфату (cGMP). Цей підйом рівня cGMP веде до розслаблення печеристого тіла внаслідок зниження внутрішньоклітинного кальцію ([Са2+]), за допомогою невідомих механізмів, які, як вважають, включають в себе активацію протеїнкінази G (ймовірно, внаслідок активації насосів Са2+ і Са2+-активованих К+-каналів). Всередині центральної нервової системи були ідентифіковані множинні потенційні ділянки для модуляції статевої поведінки. Вважають, що ключовими нейромедіаторами є серотонін, норепінефрин, окситоцин, окис азоту і допамін. Шляхом імітації видів дії одного з цих нейромедіаторів можна регулювати статеву функцію. Допамінові D3-рецептори експресовані майже виключно в лімбічній зоні головного мозку, в ділянках, що беруть участь в заохоченні, емоційних і пізнавальних процесах. Безвідносно до якої-небудь теорії, виявляється, що «завдяки його ролі в регуляції рухової активності, єдність нігростріального допамінергічного шляху також істотна для вияву поведінки спаровування. Якимсь чином, специфічніше для статевої функції, ймовірно, що допамін може запускати ерекцію статевого члена впливом на окситоцинергічні нейрони, розташовані в навколошлуночковому ядрі гіпоталамусу, і, можливо, на сприяюче ерекції крестцеве парасимпатичне ядро всередині спинного мозку». У цей час виявляється, що значною ділянкою є D3, а не D2, як вважалося раніше. По суті, D3 є ініціатором статевої поведінки. Відповідно, даним винаходом передбачено застосування сполуки формули (І) у виготовленні лікарського засобу для лікування або запобігання еректильній дисфункції. На пацієнтів з MED від легкої до помірної міри тяжкості повинні надавати сприятливий ефект сполуки відповідно до даного винаходу, і на лікування можуть реагувати пацієнти також і з важкою формою MED. Однак ранні дослідження свідчать про те, що частота реакції пацієнтів на лікування легкої, помірної і важкої форми MED може збільшуватися при впливі комбінації селективний агоніст D3/інгібітор PDE5. Легка, помірна і важка форма MED являють собою терміни, відомі фахівцеві в даній галузі, але керівництво можна знайти в [The Journal of Urology, vol. 151, 54-61 (Jan 1994)]. Ранні дослідження свідчать про те, що на згадані нижче групи пацієнтів з MED може надати сприятливий ефект селективний В3-агоніст і інгібітор PDE5 (або інші комбінації, представлені нижче в даному описі). До цієї групи пацієнтів, детально описаних в [Clinical Andrology vol.23, no.4 p.773-782 і розділу 3 книги І. Eardley and К. Sethia "Erectile Dysfunction-Current Investigation and Management", видавництво Mosby-Wolfe], відносяться пацієнти з психогенною, органічною, судинною, ендокринною, нейрогенною, артеріогенною, викликаною лікарськими засобами (ятрогенною) статевою дисфункцією і статевою дисфункцією, пов'язаною із печеристими факторами, зокрема, веногенними причинами. Відповідно, даний винахід передбачає застосування сполуки формули (І), (Іа) або (Іb) у виготовленні лікарського засобу в комбінації з інгібітором PDE5 для лікування еректильної дисфункції. Відповідні інгібітори PDE5 описані в даному описі. Сполуки згідно з винаходом можна застосовувати при лікуванні або запобіганні статевій дисфункції у жінок (FSD), зокрема, FSAD. Відповідно до винаходу, FSD можна визначити як ускладнення або нездатність жінки досягнути сексуального задоволення. FSD являє собою колективний термін для декількох різноманітних статевих розладів [Leiblum, S.R. (1998)-Definition and classification of female sexual disorders. Int. J. Impotence Res., 10, S104-S106; Berman, J.R., Berman, L. & Goldstein, I. (1999)-Female sexual dysfunction: Incidence, pathophysiology, evaluations and treatment options. Urology, 54, 385-391]. У жінки може бути відсутнім бажання, спостерігатися ускладнення в досягненні збудження або оргазму, біль при статевому акті або комбінація цих проблем. Декілька типів захворювань, видів медикаментозного лікування, травм або психологічних проблем можуть викликати FSD. Способи лікування при розвитку розладу направлені на лікування певних підтипів FSD, переважно розладів бажання і збудження. Категорії FSD найкращим чином визначаються шляхом зіставлення їх з фазами нормальної статевої реакції жінок: бажанню, збудженню і оргазму [Leiblum, S.R. (1998)-Defmition and classification of female sexual disorders. Int. J. Impotence Res., 10, S104-S106]. Бажання або прагнення являє собою спонукання до сексуального вираження. Його вияви часто включають в себе сексуальні думки або при наявності в компанії зацікавленого партнера, або при впливі інших еротичних стимулів. Збудження являє собою судинну реакцію на сексуальну стимуляцію, і важливим його компонентом є гіперемія статевих органів, і воно включає в себе збільшену змазку піхви, подовження піхви і підвищене відчуття/чутливість статевих органів. Оргазм являє собою зняття статевого напруження, що досягло кульмінації під час збудження. Отже, FSD відбувається, коли жінка має неадекватну або незадовільну реакцію в будь-якій з цих фаз, звичайно бажання, збудження або оргазму. Категорії FSD включають в себе розлад сексуального бажання, розлад сексуального збудження, розлади оргазму і сексуальні больові розлади. Хоча сполуки згідно з винаходом поліпшують реакцію статевих органів на сексуальну стимуляцію (як при розладі сексуального збудження у жінок), при цьому вони можуть також полегшити пов'язаний з нею біль, дисфункцію і дискомфорт, пов'язані з статевим актом і, таким чином, лікувати інші сексуальні розлади у жінок. Розлад у вигляді гипоактивного сексуального бажання має місце, якщо у жінки немає бажання бути сексуальною або воно невелике, і у неї немає сексуальних думок або фантазій або їх небагато. Цей тип FSD може бути викликаний низькими рівнями тестостерону або внаслідок природної менопаузи, або хірургічної менопаузи. Інші причини включають в себе захворювання, види медикаментозної терапії, втому, депресію і тривогу. Статева дисфункція у жінок у вигляді розладу сексуального збудження (FSAD) характеризується неадекватною реакцією статевих органів на сексуальну стимуляцію. Статеві органи не зазнають гиперемії, яка характеризує нормальне сексуальне збудження. Стінки піхви погано змащуються, і тому статевий акт хворобливий. Оргазми можуть бути пригнічені. Розлад збудження може бути викликаний зниженим рівнем естрогену при менопаузі або після пологів і під час лактації, а також захворюваннями з судинним компонентом, такими як цукровий діабет і атеросклероз. Інші причини виникають внаслідок лікування діуретичними засобами, антигістамінними препаратами, антидепресантами, наприклад, селективними інгібіторами зворотного захоплення серотоніну (SSRI) або гіпотензивними засобами. Сексуальні больові розлади (включаючи диспареунію і вагінізм) характеризуються болем внаслідок проникнення статевого члена у піхву, і вона може бути викликана видами медикаментозної терапії, які зменшують змазку, ендометріозом, запальними захворюванням тазових органів, запальними кишковими захворюваннями або патологією сечовивідних шляхів. Як обговорювалося раніше, вважають, що D3 є ініціатором сексуальної поведінки. Клітор вважають гомологом пеніса [Levin, R.J. (1991), Ехр. СНп. Endocrinol., 98, 61-69]; такий же механізм, який забезпечує еректильну реакцію у чоловіків, спричиняє збільшення кровотоку в статевих органах у жінок з пов'язаним ефектом на FSD. Крім того, є зміни процептивності і рецептивності. Таким чином, відповідно до переважного аспекту винаходу, пропонується застосування сполуки формули (І), (Іа) або (Іb) у виготовленні лікарського засобу для лікування або профілактики статевої дисфункції у жінок, конкретніше, розладу у вигляді гіпоактивного сексуального бажання, розладу сексуального збудження, розладу оргазму і сексуального больового розладу. Переважно сполуки формули (І) можна застосовувати при лікуванні або профілактиці розладу сексуального збудження, розладу оргазму і розладу у вигляді гіпоактивного сексуального бажання, а найбільш переважно, при лікуванні або профілактиці розладу сексуального збудження. У переважному варіанті здійснення сполуки формули (І), (Іа) або (Іb) можна застосовувати при лікуванні жінок з розладом сексуального збудження і супутнім розладом у вигляді гіпоактивного сексуального бажання. У керівництві ["The Diagnostic and Statistical Manual (DSM) IV of the American Psychiatric Association"] статева дисфункція у жінок у вигляді розладу сексуального збудження (FSAD) визначається як «... стійка або рецидивуюча нездатність придбати або підтримувати адекватну реакцію сексуального збудження у вигляді змазки-набряку до завершення сексуальної активності. Розлад повинний викликати виражену дисфункцію або ускладнення в міжособовому спілкуванні...». Реакція збудження складається з наповнення судин тазової порожнини, змазки піхви і збільшення об'єму і набряку зовнішніх статевих органів. Цей розлад викликає виражену дисфункцію або ускладнення міжособового спілкування. FSAD являє собою дуже поширений сексуальний розлад, що вражає жінок перед, під час і після менопаузи (при наявності і відсутності гормональної заміщувальної терапії (HRT)). Він пов'язаний з супутніми розладами, такими як депресія, серцево-судинні захворювання, нукровий діабет і сечостатеві (UG) розлади. Первинними наслідками FSAD є відсутність гіперемії/набряку, відсутність змазки і відсутність приємного відчуття з боку статевих органів. Вторинними наслідками FSAD є знижене сексуальне бажання, біль під час статевого акту і ускладнення в досягненні оргазму. Недавно була висловлена гіпотеза, що існує судинна основа щонайменше у частини пацієнтів з симптомами FSAD [Goldstein et al., Int. J. Impot. Res., 10, S84-S90, 1998], причому експериментальні дані підтверджують цю точку зору [Park et al., Int. J. Impot. Res, 9, 27-37, 1997]. R.J. Levin повідомляє, що в зв'язку з тим, що «... чоловічі і жіночі статеві органи розвиваються ембріологічно із загального тканинного зачатка, то ведуться дискусії про те, що структури чоловічих і жіночих статевих органів є гомологами один одного. Таким чином, клітор є гомологом статевого члена, а статеві губи є гомологами мошонкового мішка ...» [Levin, R.J. (1991), Exp. Clin. Endocrinol, 98, 61-69]. Перспективні препарати для лікування FSAD, які досліджуються для визначення ефективності, являють собою насамперед засоби для лікування еректильної дисфункції, які стимулюють кровопостачання чоловічих статевих органів. Сполуки згідно з винаходом мають переваги, забезпечуючи засіб для відновлення нормальної реакції статевого збудження, а саме, збільшеного кровотоку в статевих органах, який веде до гіперемії клітора і статевих губ. Це приводить до збільшеної змазки піхви внаслідок транссудації плазми, зростаючої розтяжності піхви і збільшеній чутливості статевих органів. Отже, даний винахід передбачає засіб для відновлення або посилення нормальної реакції сексуального збудження. Таким чином, відповідно до переважного аспекту винаходу, пропонується застосування сполуки формули (І), (Іа) або (Іb) у виготовленні лікарського засобу для лікування або профілактики розладу сексуального збудження у жінок. Жіночі статеві органи в даному описі відповідають наступному визначенню: «Статеві органи складаються з внутрішньої і зовнішньої групи. Внутрішні органи розташовані всередині таза і складаються з яєчників, маточних труб, матки і піхви. Зовнішні органи розташовані поверхово відносно сечостатевої діафрагми і під тазовою дугою. Вони включають в себе лобкове піднесення, статеві великі губи і статеві малі губи, клітор, переддвер'я, цибулину переддвер'я і великі залози переддвер'я» [Gray's Anatomy, CD. Clemente, 13th American Edition]. Сполуки згідно з винаходом знаходять застосування у наступних субпопуляцій пацієнток з FSD: молодих, немолодих жінок, жінок перед менопаузою, під час менопаузи, після менопаузи, жінок одержуючих гормональну заміщувальну терапію, і без неї. Сполуки згідно з винаходом знаходять застосування у пацієнток з FSD, що виникає в результаті і) Судинних етіологій, наприклад, серцево-судинних або атеросклеротичних захворювань, гіперхолестеринемії, куріння, цукрового діабету, гіпертонії, опромінення і травм промежини, травматичного пошкодження підклубово-підчеревної статевої судинної системи. іі) Нейрогенних етіологій, таких як травми спинного мозку або захворювання центральної нервової системи, включаючи розсіяний склероз, цукровий діабет, паркінсонізм, цереброваскулярні явища, периферичні нейропатії, травму або радикальні операції на тазових органах. ііі) Гормональних/ендокринних етіологій, таких як дисфункція осі гіпоталамус-гіпофіз-статеві залози, або дисфункція яєчників, дисфункція підшлункової залози, хірургічна або медикаментозна кастрація, недостатність андрогенів, високі рівні пролактину в циркулюючій крові, наприклад, гіперпролактинемія, природна менопауза, передчасна яєчникова недостатність, гіпер- і гіпотиреоз. iv) Психогенних етіологій, таких як депресія, нав'язливо-компульсивний розлад, тривожний розлад, післяпологова депресія/«туга після народження немовляти», емоційні проблеми і проблеми, пов'язані з міжособовими відносинами, тривога, пов'язана з виконанням сексуальної функції, сімейні розлади, дисфункціональні відношення, сексуальні фобії, релігійне придушення або травмуючий минулий досвід. ν) Сексуальної дисфункцій, викликаної лікарськими засобами, внаслідок лікування селективними інгібіторами зворотного захоплення серотоніну (SSRI) і іншими засобами для лікування депресії (трициклічні препарати і великі транквілізатори), засобами для лікування гіпертонії, сімпатолітичними препаратами, хронічної терапії пероральними протизаплідними засобами. Сполуки згідно з винаходом можна також застосовувати при лікуванні депресії. Допамінові В3-рецептори експресовані майже виключно в лімбічній зоні головного мозку, ділянках, що беруть участь в заохоченні, емоційних і пізнавальних процесах. Відомо, що хронічне лікування декількома класами антидепресантів збільшує експресію D3 в лімбічній зоні, і антидепресивні ефекти дезипраміну можна блокувати сулпридом (антагоністом D2/D3) при ін'єкції в ядро Accumbens (зону, багату на D3), але не хвостате ядро-павутину (зону, багату на допамінові D2-рецептори). Крім того, антидепресантні ефекти спостерігалися на передклінічних моделях депресії і у пацієнтів, що отримували лікування праміпексолом, агоністом, що віддає перевагу D3-рецепторам. Доступна інформація свідчить про те, що D3-рецептори опосередковують антидепресантну активність, і що селективні агоністи D3-рецепторів являють собою новий клас антидепресантних препаратів. Оскільки відомо, що антидепресанти ефективні при інших психіатричних розладах, D3-агоністи могли б використовуватися для лікування психіатричних захворювань. У даному винаході мається на увазі застосування селективного D3-агоніста у виготовленні лікарського засобу для лікування депресії і психіатричних захворювань. Переважно, якщо вказаний D3-агоніст виявляє функціональну активність на D3-рецепторі, що виявляється у вигляді ЕС50 нижче ніж 1000нМ, переважніше - нижче ніж 100нМ, ще переважніше - нижче ніж 50нМ, найбільш переважно - нижче ніж 10нМ. Переважно, якщо вказаний D3-агоніст має селективність у відношенні D3, в порівнянні з D2, де вказаний агоніст допамінового D3-агоніста щонайменше приблизно в 15 разів, переважно щонайменше приблизно в 27 разів, переважніше - щонайменше приблизно в 30 разів, найбільш переважно щонайменше приблизно в 100 разів функціонально більш вибірковий у відношенні допамінового D3рецептора, в порівнянні з допаміновим D2-рецептором. Відповідні стани включають в себе депресію (наприклад, депресію у ракових хворих, депресію при хворобі Паркінсона, депресію після інфаркту міокарда, субсиндромну симптоматичну депресію, депресію у безплідних жінок, депресію у дітей, велику депресію, депресію у вигляді одиночних епізодів, рецидивуючу депресію, депресію, викликану грубим поводженням з дітьми, післяпологову депресію і синдром роздратованості у немолодих людей), розлад у вигляді генералізованої тривоги, фобії (наприклад, агорафобію, соціальну фобію і сенільні фобії), синдром посттравматичного стресу, розлад особистості у вигляді уникнення, розладу споживання їжі (наприклад, невротичну анорексію і невротичну булімію), ожиріння, залежність від хімічних речовин (наприклад, залежність від алкоголю, кокаїну, героїну, фенобарбіталу, нікотину і бензодіазепінів), хворобу Альцгеймера, нав'язливо-компульсивний розлад, панічний розлад, розлади пам'яті (наприклад, деменцію, амнестичній розлади і вікове зниження пізнавальної функції (ARCD)), хворобу Паркінсона (наприклад, деменцію при хворобі Паркінсона, паркінсонізм, викликаний нейролептиками, і повільні дискінезії), ендокринні розлади (наприклад, гіперпролактинемію), судинний спазм (зокрема, судин головного мозку), мозжечкову атаксію, негативні симптоми шизофренії, стресове нетримання сечі, синдром Турета, трихотиломанію, клептоманію, розлад дефіциту уваги з гіперактивністю (ADHD), хронічну пароксизмальну гемікранію, емоційну лабільність, патологічний плач, розлади сну (каталепсію) і шок. У переважному варіанті здійснення даний винахід призначений для застосування сполуки формули (І), (Іа) і (Іb) у виготовленні лікарського засобу для лікування депресії або психіатричних розладів. Відповідні депресивні стани і психіатричні розлади описані вище. Сполуки згідно з винаходом можуть також застосовуватися при лікуванні нейродегенеративних процесів; джерела нейродегенеративних процесів включають в себе отруєння нейротоксинами; втрату зору, викликану нейродегенерацією зорового шляху, наприклад, інсультом в зоровому шляху, наприклад, в сітчатці, зоровому нерві і/або потиличній частці; епілептичними нападами; і внаслідок порушення постачання головного мозку глюкозою і/або киснем. Відповідно, даним винаходом передбачено застосування селективного D3-агоніста у виготовленні лікарського засобу для лікування нейродегенерації. Переважно вказаний D3-агоніст виявляє функціональну активність на D3-рецепторі, що виявляється у вигляді ЕС50 нижче ніж 1000нМ, переважніше - нижче ніж 100нМ, ще переважніше - нижче ніж 50нМ, найбільш переважно - нижче ніж 10нМ. Переважно, вказаний D3-агоніст має селективність у відношенні D3, в порівнянні з D2, де вказаний агоніст допамінового D3-агоніста щонайменше приблизно в 15 разів, переважно щонайменше приблизно в 27 разів, переважніше щонайменше приблизно в 30 разів, найбільш переважно щонайменше приблизно в 100 разів функціонально більш вибірковий у відношенні допамінового D3-рецептора, в порівнянні з допаміновим D2-рецептором. У переважному варіанті здійснення D3-агоніст являє собою сполуку формули (І), (Іа) або (Іb). У доповнення до їх ролі при лікуванні статевої дисфункції, депресії, нейродегенерації і психіатричних розладів, сполуки згідно з винаходом, ймовірно, мають ряд додаткових показань. Відповідно, даний винахід надає застосування сполук формули (І), (Іа) або (Іb) у виготовленні лікарського засобу для лікування гіпертонії, передчасної еякуляції, ожиріння, «гістамінового» головного болю, мігрені, болю, ендокринних розладів (наприклад, гіперпролактинемії), судинного спазму (зокрема, судин головного мозку), мозжечкової атаксії, розладів шлунково-кишкового тракту (включаючи зміни моторики і секреції), передменструального синдрому, синдрому фіброміалгії, стресового нетримання сечі, трихотиломанії, клептоманії і хронічної пароксизмальної гемікранії, головного болю (пов'язаного з судинними розладами). Аналіз зв'язування D3/D2-агоністів Gonazalez et al [Eur. J Pharmacology 272 (1995) R1-R3] описаний спосіб аналізу для визначення здатності зв'язування сполуки з D3 і/або D2-допаміновимими рецепторами і, таким чином, селективності зв'язування таких сполук. Таким чином, цей аналіз іменується в даному описі аналізом зв'язування. Функціональний аналіз D3/D2-агоністів Відповідний аналіз для функціонального.визначення активності сполуки на D3 і/або D2-допамінових рецепторах детально описаний нижче. Сполуки оцінюють як агоністи або антагоністи на допамінових рецепторах D2 і D3, вивчаючи рівні сАМР (цАМФ) в лініях клітин GH4Cl і СНО, які експресують, відповідно, людські D2 і D3-рецептори. Експериментальні методики Інгібування за допомогою допамінових D3-рецепторів активності аденілат-циклази, стимульованої форсколіном Матеріали Середовища для клітинних культур: Середовище hD3CHO DMEM, високий вміст глюкози (Sigma D5671) 2мМ L-глутамін (Sigma G7513) 10% діалізована FBS (Sigma F0392) Клітини Hd3CHO (яєчників китайського хом'ячка), які експресують людський допаміновий D3-рецептор були генеровані на місці. Ці клітини позбавлені гена дигідрофолат-редуктази. Свіжі середовища готують кожний тиждень, як описано нижче, і фільтрують через фільтр 0,22мкм перед використанням. Середовища зберігають при 4°С і нагрівають до 37°С перед додаванням до клітин. Розчин для дисоціації клітин (CDS): (Sigma C-5914) 5мл використовують для збору клітин з колби об'ємом 225см2 (37°С, 5хв. для клітин hD2LGH4Cl і 10хв. для клітин hD3CHO). Забуферений фосфатом сольовий розчин (PBS): (Gibco. 14040-091) Триптановий синій: (Sigma T8154) Форсколін (Calbiochem 3442t3) Розчиняють до концентрацій 20мМ в дистильованій воді. (Цей маточний розчин зберігають при +4°С). 4х аналітичних маточних розчини по 40мкМ готують шляхом 500-кратного розведення в буфері PBS. 25мкл маточного розчину 40мкМ додають до кінцевого аналітичного об'єму 100мкл, отримуючи кінцеву аналітичну концентрацію 10мкМ. Сполуки, що тестуються Розчиняють в 100% ДМСО (Диметилсульфоксид) для отримання концентрації маточного розчину 10мМ. Стандарт праміпексолу Розчиняють в 100% ДМСО для отримання концентрації маточного розчину 10мМ. Аналіз активації циклази на флеш-планшеті (NEN SMP004B) Постачається компанією Perkjin-Elmer Life Sciences, Inc [125I]- циклічний аденозинмонофосфат (cAMP) (NEX 130) Постачається компанією Perkjin-Elmer Life Sciences, Inc Спеціальне обладнання Шейкер/інкубатор титрувальних мікропланшетів Westbart Packard Topcount NXT (програма, сумісна з ECADA) Tecan Genesis Labsystems Multi-drop DW Протокол тестування активності сполук на клітинах hD3CHO Розведення сполук Прамепіксол включений як еталонний стандарт. 10-точкову, напівлогарифмічну криву будують для кожних 4 планшетів. Результати по сполуках нормалізують до мінімальних (0нМ праміпексолу) і до максимальних (100нМ праміпексолу) реакцій, генерованих клітинами. Усі випробувані сполуки можна також тестувати за допомогою 10-точкової (напівлогарифмічної) кривої. Випробувані сполуки розчиняють в 100% ДМСО для отримання концентрації маточного розчину 10мМ. Ці розчини потім розводять в 100% ДМСО до 1мМ за допомогою 10-кратного розведення (необхідна кінцева аналітична концентрація 1000х, наприклад, 1мМ, дає верхню концентрацію 1мкМ). Прамепіксол розчиняють в 100% ДМСО для отримання концентрації 10мМ. Прамепіксол додатково розводять до 0,1мМ в 100% ДМСО за допомогою 100-кратного розведення. Подальше розведення і додавання проводять в 0,4% ДМСО/PBS з використанням протоколу відповідно до рекомендацій Tecan Genesis для виконання серійних розведень в 3,159 разів (напівлогарифмічна одиниця). Розведення відповідно до рекомендацій Tecan Genesis 10мкл випробуваних сполук додають в стовпця 1 мікропланшету. До них додають 240мкл 0,4% ДМСО/PBS для отримання 25-кратного розведення (0,04мМ). 20мкл розведення 0,04мМ переносять в ямки стовпця 2, куди додають 180мкл 0,4% ДМСО/PBS, даючи подальше 10-кратне розведення, для досягнення 4-кратної верхньої аналітичної концентрації (0,004мМ). Виконують серійні розведення (в 3,159 рази) для досягнення серії напівлогарифмічних розведень: 4мкМ, 1,27мкМ, 400нМ, 127нМ, 40нМ, 13нМ, 3нМ, 1,27нМ, 0,4нМ, 0,1нМ. 25мкл (в двох повторах) серійних розведень переносять в стовпці 2-11 флеш-планшету (см. Додаток). Оскільки кінцевий аналітичний об'єм становить 100мл, кінцеві аналітичні концентрації будуть становити 1000мкМ, 317нМ, 100нМ, 32нМ, 10нМ, 3,2нМ, 1нМ, 0,3нМ, 0,1нМ, 0,03нМ. Мінімальний контроль (низький контроль): 25мкл 0,4% ДМСО/PBS (носій) додають в наступну ямку (стовпець 1 ямка Е-Н і стовпець 2 ямка A-D). Клітини+форсколін додають пізніше. Максимальний контроль (високий контроль): 10мМ праміпексолу розводять в PBS за допомогою 250кратного розведення (10мкл+2490мкл PBS) для генерування 40мкМ праміпексолу. 40мкМ праміпексол далі розводять за допомогою 100-кратного розведення в 0,4% ДМСО/PBS (100мкл+9900мкл носія) для генерування 400нМ (4-кратна аналітична концентрація стандартного праміпексолу). 25мкл 400нМ праміпексолу додають в наступну ямку флеш-планшету для отримання кінцевої концентрації праміпексолу 100нМ; стовпець 1 ямка A-D і стовпець 12 ямка Е-Н. Клітини+форсколін додають пізніше. Аналіз активації циклази у флеш-планшеті ΓΝΕΝ SMP004B) Як описано в розділі «Матеріали», форсколін розчиняють в дистильованій воді для досягнення концентрації маточного розчину 20мМ. Його далі розводять до 40мкМ (4-кратна аналітична концентрація) з використанням PBS. 25мкл 40мкМ маточного розчину додають у всі ямки з використанням Multi-drop, отримуючи кінцеву концентрацію 10мкМ. Потім планшети герметизують і інкубують при 37°С в інкубаторі Westbart, в той час як клітини збирають. Клітини, які на 70%-80% є такими, що злилися, збирають з колб. Істотно, що всі компоненти, які додаються до клітин, нагріті до 37°С. 5мл CDS додають на колбу Т225 і інкубують при 37°С протягом 5хв. перед нейтралізацією 5мл PBS. Клітини потім центрифугують при 160g (1000об./хв.) протягом 5хв. Отриману надосадову рідину виливають і клітини повторно суспендують в стимуляційному буфері (нагрітому до 37°С) для досягнення концентрації 5´105клітин/мл. 50мкл клітинної суспензії потім розподілять у всі ямки флеш-планшету. Планшети відразу інкубують при 37°С на струшуючому інкубаторі протягом 15хв. Реакцію зупиняють 100 мкл детекторної суміші у всіх ямках (100мкл 125І цАМФ:11мл детекторного буфера на планшет). Планшети повторно герметизують і інкубують в темряві протягом 3год. для забезпечення можливості досягнення рівноваги між антитілом проти цАМФ (що покриває ямки), міткою [125І] цАМФ і клітинним цАМФ. Підрахунок імпульсів в планшетах проводять на приладі Packard Topcount NXT з використанням відповідного протоколу, сумісного з ECADA (протокол 75). Відновлення життєздатності заморожених клітин в ампулах Видаляють ампули з рідкого азоту і дають їм можливість урівноважитися протягом 2хв., оскільки захоплений газ або рідина можуть спричинити швидке розширення і вибух ампул. їх можна також вмістити при -20°С на 2хв. перед відтаванням. Швидко і повністю відтають ампули при 37°С на водяній бані. Переносять клітинну суспензію в колбу об'ємом 75см2, що містить 10мл ростового середовища і інкубують протягом 24год. при 37°С, 5% СО2. Після прикріплення клітин (3-6год.) середовище видаляють і замінюють свіжим середовищем (для видалення ДМСО). Через 24год. при наближенні до злиття клітини переносять в колбу об'ємом 225см2. Якщо ні, клітини зберігають доти, поки вони не будуть такими, що злилися на 70%-80%. Збірі розділення клітин Клітини розділяють в п'ятницю для забезпечення клітин для аналізів в понеділок і вівторок. Клітини, необхідні для інших днів тижня, розділяють в понеділок. Суттєво не дати можливості клітинам hD3CHO досягнути більш ніж 80%-ного злиття або зробити розділення >1:20, оскільки це надає шкідливі впливи на їх проліферативну реакцію, і в подальшому вплине на здатність клітин функціонувати при аналізі. Клітини вирощують в колбах об'ємом 225см2 (Jumbos). Кожний компонент, що додається до клітин, повинен бути нагрітий до 37°С перед використанням. Збір клітин Ростове середовище видаляють з колб, клітини промивають теплим PBS (Gibco. 14040-091) і видаляють. 5мл буфера для дисоціації клітин додають до клітин і вміщують в інкубатор приблизно на 5хв. У колбах роблять прокол для видалення будь-яких клітин, що залишилися з пластика для культури тканини. 5мл PBS додають до клітин і використовують для промивання основи і колби. Клітини центрифугують протягом 5хв. при 160g (1000об./хв.) для осадження клітин. Надосадову рідину видаляють і 5мл стимулюючого буферу використовують для повторного суспендування клітин. Аналіз виключення трипанового синього проводять для визначення кількості життєздатних клітин. Клітини розбавляють стимулюючим буфером до отримання концентрації 5´105клітин/мл. Для переходу до клітин стадію центрифугування опускають, і клітинну суспензію вводять в нові колби об'ємом Т225, що містять 50мл середовища. Співвідношення при розділенні клітин hD3CHO розділяються в співвідношенні від 1:5 до 1:10. Культуру не можна продовжувати після 30-го пасажа, оскільки характеристики лінії клітин втрачаються при більшій кількості пасажів. Кріоконсервування ліній клітин Істотно створити банк власних клітин для оживлення з метою подальшого використання. Клітини збирають, як описано в попередньому розділі. Після аналізу виключення трипанового синього клітини розбавляють в середовищі, що містить 10% ДМСО, для досягнення концентрації 2-4´106клітин/мл. Клітини ділять на аліквоти по 1мл і негайно поступово заморожують в середовищі "Mr Frosty", (що містить свіжий IРА (ізопропіловий спирт)) при -80°С перед перенесенням в посудину для зберігання в газоподібній фазі рідкого азоту. (Клітини можна зберігати в середовищі "Mr Frosty" протягом періоду до 2 днів). Рекомендується тестувати життєздатність клітин відтаванням однієї ампули після заморожування. Показники життєздатності нижче за 70% можуть викликати проблеми при відновленні внаслідок низького числа клітин і присутності клітинних фрагментів. Аналіз даних Дані аналізують з використанням ECADA. % нормалізації (відносно праміпексолу) визначають для всіх сполук за допомогою наступної формули: % нормалізації (Х-ВО)/(Мах-В0)´100, де x - середні сумарні кількості імпульсів для даної концентрації сполуки, що тестується, ВО = середні сумарні кількості імпульсів мінімального контролю (0нМ праміпексолу) і Мах = середні сумарні кількості імпульсів, отримані від максимального контролю (100нМ праміпексолу) Криві можна побудувати нанесенням на графік % нормалізації (у) в залежності від концентрації агоніста в нМ (х). Дані підігнані з використанням нелінійної регресії при крутості нахилу кривої, що втримується в межах 1. По ним визначаються ЕС50 і %Емах для сполуки, що тестується. MAX - максимальний MIN - мінімальний Стовпець 1: Ямки A-D = МАХ: високі контролі (клітини+форсколін+100нМ праміпексол) Ямки Е-Н = MIN: низькі контролі (клітини+форсколін+носій) Стовпець 12: Ямки A-D = MIN: низькі контролі (клітини+форсколін+носій) Ямки Е-Н = МАХ: високі контролі (клітини+форсколін+100нМ праміпексол) Стовпці 2-11: 10-точкове серійне розведення (в двох повторах) сполук, що тестуються. Зменшувані концентрації від стовпця 2 до стовпця 11 (від 1000нМ до 0,03нМ). Праміпексол заміняє Сів першій планшеті. Інгібування через допамінові D2-рецептори стимульованої форсколіном активності аденілатциклази Матеріали Середовища для клітинної культури: Середовище HD2 GH4Cl/hD2L Hams F-12 (Sigma N6013) 2мМ L-глутамін (Sigma G7513) 10% FBS(Gibco 10106-169) 700мкг/мл генетицина (Gibco 10131-019) GH4Cl/hD 2L являють собою клітини гіпофіза щурів, які експресують людський допаміновий рецептор D2long. Свіже середовище готують кожний тиждень, як зазначено нижче, і фільтрують через фільтр 0,22мкМ перед використанням. Середовище зберігають при 4°С і нагрівають до 37°С для додавання до клітин. Розчин для дисоціації клітин (CDS): (Sigma C-5914) 5мл використовують для збору клітин з колби об'ємом 225см2. Забуферений фосфатом сольовий розчин (PBS): (Gibco. 14040-091) Триптановий синій: (Sigma T8154) Форсколін (Calbiochem 344273) Розчиняють до концентрації 20мМ в дистильованій воді. (Цей маточний розчин зберігають при +4°С). 4х аналітичних маточних розчини по 20мкМ готують шляхом 1000-кратного розведення в буфері PBS. 25мкл маточного розчину 20мкМ додають до кінцевого аналітичного об'єму 100мкл, отримуючи кінцеву аналітичну концентрацію 5мкМ. Сполуки, що тестуються Розчиняють до концентрації 10мМ в 100% ДМСО. Стандарт праміпексолу Розчиняють в 100% ДМСО для отримання концентрації маточного розчину 10мМ. Аналіз активації циклази на флеш-планшеті (NEN SMP004B) Постачається компанією Perkin-Elmer Life Sciences, Inc [125І]- циклічний аденозинмонофосфат (cAMP) (NEX 130) Постачається компанією Perkin-Elmer Life Sciences, Inc Спеціальне обладнання Шейкер/інкубатор титрувальних мікропланшетів Westbart Packard Topcount NXT (програма, сумісна з ECADA) Tecan Genesis Labsystems Multi-drop DW Протокол операцій Розведення сполук Прамепіксол включений як еталонний стандарт. 10-точкову, напівлогарифмічну криву будують для кожних 4 планшетів. Реакції сполук нормалізують до мінімальних (0 нМ праміпексолу) і до максимальних (1000нМ праміпексолу) реакцій, генерованими клітками. Всі випробувані сполуки можна також тестувати за допомогою 10-точкової (напівлогарифмічної) кривої. Випробувані сполуки розчиняють в 100% ДМСО для отримання концентрації маточного розчину 10мМ (необхідна кінцева аналітична концентрація 1000х, наприклад, 10мМ дає верхню концентрацію 10000нМ). Прамепіксол розчиняють в 100% ДМСО для отримання концентрації 10мМ. Прамепіксол додатково розводять до 1мМ в 100% ДМСО за допомогою 10-кратного розведення. Подальші розведення і додавання проводять в 0,4% ДМСО/PBS з використанням протоколу відповідно до рекомендацій Tecan Genesis для виконання серійних розведень в 3,159 разів (напівлогарифмічна одиниця). Розведення відповідно до рекомендацій Tecan Genesis 10мкл випробуваних сполук додають в стовпець 1 мікропланшету. До них додають 240мкл 0,4% ДМСО/PBS для отримання 25-кратного розведення (0,04мМ). 20мкл розведення 0,04мМ переносять в ямки стовпця 2, куди додають 180мкл 0,4% ДМСО/PBS, даючи подальше 10-кратне розведення, для досягнення 4-кратної верхньої аналітичної концентрації (0,04мМ). Виконують серійне розведення (в 3,159 рази) для досягнення серій напівлогарифмічних розведень: 40мкМ, 12,7мкМ, 4мкМ, 1,27мкМ, 400нМ, 130нМ, 40нМ, 13нМ, 4нМ, 1,3нМ. 25мкл (в двох повторах) серійних розведень переносять в стовпці 2-11 флеш-планшету (см. Додаток). Оскільки кінцевий аналітичний об'єм становить 100мл, кінцеві аналітичні концентрації будуть становити 10000мкМ, 3170нМ, 1000нМ, 320нМ, 100нМ, 32нМ, 10ним, 3нМ, 1нМ, 0,3нМ. Мінімальний контроль (низький контроль): 25мкл 0,4% ДМСО/PBS (носій) додають в наступні ямки (стовпець 1 ямки Е-Н і стовпець 2 ямки A-D). Клітини і форсколін додають пізніше. Максимальний контроль (високий контроль): 10мМ праміпексолу розводять в PBS за допомогою 250кратного розведення (10мкл+2490мкл PBS) для генерування 40мкМ праміпексолу. 40мкМ праміпексолу далі розводять за допомогою 10-кратного розведення в 0,4% ДМСО/PBS (100мкл+990мкл носія) для генерування 4000нМ (4-кратна аналітична концентрація стандартного праміпексолу). 25мкл 4000нМ праміпексолу додають в наступні ямки флеш-планшету для отримання кінцевої концентрації праміпексолу 1000нМ; стовпець 1 ямки A-D і стовпець 12ямки Е-Н. Клітини+форсколін додають пізніше. Аналіз активації циклази у флеш-планшеті (NEN SMP004B) Як описано в розділі «Матеріали», форсколін розчиняють в дистильованій воді для досягнення концентрації маточного розчину 20мМ. Його далі розводять до 20мкМ (4-кратна аналітична концентрація) з використанням PBS. 25мкл 40мкМ маточного розчину додають у всі ямки з використанням Multi-drop, отримуючи кінцеву концентрацію 0,5мкМ. Потім планшети герметизують і інкубують при 37°С в інкубаторі Westbart, в той час як клітини збирають. Клітини, які на 70%-80% є такими, що злилися, збирають з колб. Істотно, що всі компоненти, які додаються до клітин, нагріті до 37°С. 5мл CDS додають на колбу об'ємом 225см2 і інкубують при 37°С протягом 5хв. перед нейтралізацією 5мл PBS. Клітини потім центрифугують при 160g (1000об./хв.) протягом 5хв. Отриману надосадову рідину виливають, і клітини повторно суспендують в стимулюючому буфері (нагрітому до 37°С) для досягнення концентрації 1´105клітин/мл. 50мкл клітинної суспензії потім розподілять у всі ямки флеш-планшету. Планшети відразу інкубують при 37°С на струшуючому інкубаторі протягом 15хв. Реакцію зупиняють 100мкл детекторної суміші у всі ямки (100мкл 125І цАМФ:11мл детекторного буферу на планшет). Планшети повторно герметизують і інкубують в темряві протягом 3год. для забезпечення можливості досягнення рівноваги між антитілом проти цАМФ (що покриває ямки), міткою [І25І] цАМФ і клітинним цАМФ. Підрахунок імпульсів в планшетах проводять на приладі Packard Topcount NXT з використанням відповідного протоколу, сумісного з ECADA (протокол 75). Відновлення життєздатності заморожених клітин в ампулах Видаляють ампули з рідкого азоту і дають їм можливість урівноважитися протягом 2хв., оскільки захоплений газ або рідина можуть спричинити швидке розширення і вибух ампул. їх можна також вмістити при -20°С на 2хв. перед відтаванням. Швидко і повністю відтають ампули при 37°С на водяній бані. Переносять клітинну суспензію в колбу об'ємом 75см2, що містить 10мл ростового середовища і інкубують протягом 24год. при 37°С, 5% СО2. Після прикріплення клітин (3-6год.) середовище видаляють і замінюють свіжим середовищем (для видалення ДМСО). Через 24год. при наближенні до злиття клітини переносять в колбу об'ємом 225см2. Якщо ні, клітини зберігають доти, поки вони не будуть такими, що злилися на 60%. Збір і розділення клітин Клітини розділяють в п'ятницю для забезпечення клітин для аналізів в понеділок і вівторок. Клітини, необхідні для інших днів тижня, розділяють в понеділок. Суттєво не дати можливість клітинам досягнути більш ніж 60%-ного злиття, оскільки це надає шкідливі впливи на їх проліферативну реакцію і в подальшому вплине на здатність клітин функціонувати при аналізі. Клітини вирощують в колбах 225см2 (Jumbos). Кожний компонент, що додається до клітин, повинен бути нагрітий до 37°С перед використанням. Збір клітин Ростове середовище видаляють з колб, клітини промивають теплим PBS (Gibco. 14040-091) і видаляють. 5мл буфера для дисоціації клітин додають до клітин і вміщують в інкубатор приблизно на 5хв. У колбах роблять прокол для видалення будь-яких залишкових клітин з пластику для культури тканини. 5мл PBS додають до клітин і використовують для промивання основи і колби. Клітини центрифугують протягом 5хв. при 160g (1000об./хв.) для осадження клітин. Надосадову рідину видаляють, і 5мл стимулюючого буферу використовують для повторного суспендування клітин. Аналіз виключення трипанового синього проводять для визначення кількості життєздатних клітин. Клітини розбавляють стимулюючим буфером до отримання концентрації 1´105клітин/мл. Для переходу до клітин стадію центрифугування опускають, і клітинну суспензію вводять в нові колби об'ємом Т225, що містять 50мл середовища. Співвідношення при розділенні клітин GH4C1/D2 розділяють в співвідношенні від 1:3 до 1:5. Кріоконсервування ліній клітин Істотно створити банк власних клітин для оживлення з метою подальшого використання. Клітини збирають, як описано в попередньому розділі. Після аналізу виключення трипанового синього клітини розбавляють в середовищі, що містить 10% ДМСО, для досягнення концентрації 2-4´106клітин/мл. Клітини ділять на аліквоти по 1мл і негайно поступово заморожують в середовищі "Mr Frosty", (що містить свіжий IPА) при -80°С перед перенесенням в посудину для зберігання в газоподібній фазі рідкого азоту. (Клітини можна зберігати в середовищі "Mr Frosty" протягом періоду до 2 днів). Рекомендується тестувати життєздатність клітин відтаванням однієї ампули після заморожування. Показники життєздатності нижче за 70% можуть викликати проблеми при відновленні внаслідок низького числа клітин і присутності клітинних фрагментів. Аналіз даних Дані аналізують з використанням ECADA. % нормалізації (відносно праміпексолу) визначають для всіх сполук за допомогою наступної формули: % нормалізації=(Х-ВО)/(Мах-В0)´100, де x = середні сумарні кількості імпульсів для даної концентрації сполуки, що тестується, ВО = середні сумарні кількості імпульсів мінімального контролю (0нМ праміпексолу)і Мах = середні сумарні кількості імпульсів, отримані від максимального контролю (100нМ праміпексолу) Криві можна побудувати нанесенням на графік % нормалізації (у) в залежності від концентрації агоніста в нМ (х). Дані підігнані з використанням нелінійної регресії при крутості нахилу кривої, що втримується в межах 1. По ним визначаються ЕС50 і %Емах для сполуки, що тестується. MAX - максимальний MIN - мінімальний Стовпець 1: Ямки A-D = МАХ: високі контролі (клітини+форсколін+100нМ праміпексолу) Ямки Е-Н = MIN: низькі контролі (клітини+форсколін+носій) Стовпець 12: Ямки A-D = MIN: низькі контролі (клітини+форсколін+носій) Ямки Е-Н = МАХ: високі контролі (клітини+форсколін+100нМ праміпексол) Стовпці 2-11: 10-точкове серійне розведення (в двох повторах) сполук, що тестуються. Зменшувані концентрації від стовпця 2 до стовпця 11 (від 1000нМ до 0,03нМ). Праміпексол заміняє С1 в першій планшеті. При використанні описаного вище аналізу всі сполуки згідно з винаходом виявляють функціональну активність на D3-рецепторі, що виявляється у вигляді ЕС50 нижче, ніж 1000нМ, і 10-кратну селективність у відношенні D3, в порівнянні з D2. Сполука прикладу 8 має функціональну активність на D3-рецепторі, що виявляється у вигляді ЕС50 7,6нМ і селективність у відношенні D3, в 1315,8 разів перевищуючу D2. Селективність розраховують як величину ЕС50 D2, ділену на величину ЕС50 D3. Коли величина ЕС50 D2 становила >10000, при розрахунку використали число 10000. Потрібно розуміти, що всі посилання в даному описі на лікування включають в себе радикальне, паліативне і профілактичне лікування. Відповідні допоміжні активні речовини для застосування в комбінаціях згідно з винаходом включають в себе 1) природні або синтетичні простагландини або їх складні ефіри. Відповідні простагландини для застосування в даному винаході включають в себе такі сполуки як алпростадил, простагландин Е1, простагландин Е0, 13,14-дигідропростагландин Е1, простагландин Е2, епростинол, натуральні, синтетичні і напівсинтетичні простагландини і їх похідні, включаючи ті, які описані в [WO-00033825 і/або в патенті США № 6037346, виданому 14 березня 2000p.], які всі включені в даний опис як посилання, PGE0, PGE1, PGA1, PGB1, PGF1,a, 19-гідрокси-PGA1, 19-гідрокси-РGВ1, PGE2, PGB2, 19-гідрокси-РGА2, 19-гідрокси-PGB2, PGE3a, карбопрост трометамін динопрост, трометамін, динопростон, ліпопрост, гемепрост, метенопрост, сулпростун, тіапрост і моксисилат; 2) сполуки-антагоністи α-адренергічних рецепторів, також відомі як a-адреноцептори або a-рецептори або a-блокатори. Придатні сполуки для застосування в даному винаході включають в себе: блокатори aадренергічних рецепторів, як описано в заявці [РСТ W099/30697, опублікованій 14 червня 1998p.], положення якої, що відносяться до a-адренергічних рецепторів, включені в даний опис як посилання і включають в себе селективні блокатори a 1-адреноцепторів або a 2-адреноцепторів і неселективні блокатори адренорецепторів, приклади відповідних блокаторів а1-адреноцепторів включають в себе: фентоламін, месилат фентоламіну, тразодон, алфузосин, індорамін, нафтопідил, тамсулозин, дапіпразол, феноксибензамін, ідазоксан, ефараксан, йохимбін, алкалоїди раувольфії, Recordati 15/2739, SNAP 1069, SNAP 5089, RS17053, SL 89.0591, доксазосин, теразосин, абанохіл і проазосин; блокатори a 2адреноцепторів з [патенту США №6037346 [14 березня 2000p.]] дибенамін, толазолін, тримазосин і дибенамін; a-адренергічні рецептори, як описано в [патентах США №№: 4188390, 4026894, 3511836, 4315007, 3527761, 3997666, 2503059, 4703063, 3381009, 4252721 і 2599000], кожний з яких включений в даний опис як посилання; блокатори агадреноцепторів включають в себе: клонідин, папаверин, гідрохлорид папаверину, необов'язково в присутності каріотонічного засобу, такого як пірксамін; 3) сполуки-донори NO (NO-агоністи). Відповідні сполуки-донори NO для застосування в даному винаході включають в себе органічний нітрат, такі як моно-, ди- і тринітрати, або складні ефіри органічного нітрату, включаючи тринітрат гліцерилу (також відомий як нітрогліцерин), 5-мононітрат ізосорбіду, динітрат ізосорбіду, тетранітрат пентаеритриолу, тетранітрат еритритилу, нітропрусид натрію (SNP), 3морфоліносиднонімін молсидимін, S-нітрозо-N-ацетилпенициламін (SNAP), 5-нітрозо-N-глутатіон (SNOGLU), N-оксі-L-аргінін, амілнітрат, лінсидомін, хлоргідрат лінсидоміну, (SIN-1) 3-нітрозо-N-цистеїн, діолати діазенію, (NONОати), 1,5-пентандинітрат, L-аргінін, женьшень, плід зізфи, молсидомін, Re-2047, похідні нітрозильованого максисиліту, такі як NMI-678-11 і NMI-937, як описано в [опублікованій заявці РС-Т WO 0012075]; 4) засоби, що відкривають або модулють калієві канали. Відповідні засоби, що відкривають або модулють калієві канали, для застосування в даному винаході, виключають нікорандил, кромокалим, левкромакалим, лемакалим, пінацидил, кліазоксид, миноксидил, чарибдотоксин, глібурид, 4-амінопіридин, ВаСI 2; 5) судинорозширювальні засоби. Відповідні судинорозширювальні засоби для використання в даному винаході включають в себе німодепин, пінацидил, цикланделат, ізоксуприн, хлорпромазин, галоперидол, Rec 15/2739, тразодон; 6) агоністи тромбоксану А2; 7) засоби, діючі на ЦНС; 8) алкалоїди полину; відповідні алкалоїди полину описані в [патенті США №6037346, виданому 14 березня 2000p.], і включають в себе ацетергамін, бразерголін, бромергурид, ціанерголін, делорготрил, дисулергін, малеат ергоновіну, тартрат ерготаміну, етисулергін, лерготрил, лізергід, месулергін, метерголін, метерготамін, ніцерголін, перголід, пропісергід, протергурид і тергурид; 9) сполуки, які модулюють дію натрійуретичних факторів, зокрема, передсердного натрійуретичного фактора (також відомого як передсердний натрійуретичний пептид), натрійуретичні фактори типу В і типу С, такі як інгібітори нейтральної ендопептидази; 10) сполуки, які інгібують ангіотензин-перетворюючий фермент, такі як енаприл, і комбіновані інгібітори ангіотензин-перетворюючого ферменту і нейтральної ендопептидази, такі як омапатрилат; 11) антагоністи рецепторів ангіотензину, такі як лосартан; 12) субстрати для NO-синтази, такі як L-аргінін; 13) блокатори кальцієвих каналів, такі як амлодипін; 14) антагоністи рецепторів ендотеліну і інгібітори ендотелін-перетворюючого ферменту; 15) засоби, що знижують рівень холестерину, такі як статини (наприклад, аторвастатин/Lipitor - торгова марка) і фібрати; 16) антитромбоцитарні і антитромботичні засоби, наприклад, tPA, uPA, варфарин, гірудин і інші інгібітори тромбіну, гепарин, інгібітори фактора, що активує тромбопластин; 17) засоби, сенсибілізуючі до інсуліну, такі як резулин, і гіпоглікемічні засоби, такі як гліпізид; 18) L-DOPA або карбідопа; 19) інгібітори ацетилхолінестерази, такі як донезипіл; 20) стероїдні або нестероїдні протизапальні засоби; 21) модулятори естрогенових рецепторів і/або агоністи естрогенів і/або антагоністи естрогенів, переважно, ралоксифен або ласофоксифен, (-)-цис-6-феніл-5-[4-(2-піролідин-1-ілетокси)феніл]-5,6,7,8тетрагідронафталін-2-ол і їх фармацевтично прийнятні солі, отримання яких детально описано в [WO 96/21656]; 22) інгібітор PDE (фосфодіестерази), конкретніше, інгібітор PDE 2, 3, 4, 5, 7 або 8, переважно, інгібітор PDE2 або PDE5, і найбільш переважно, інгібітор PDE5 (див. нижче в даному описі), причому вказані інгібітори переважно мають ІС50 проти відповідного ферменту менше ніж 100нМ (за умови, що інгібітор PDE2 або PDE3 і 4 інгібітори вводяться тільки місцево або ін'єкцією в пеніс); 23) вазоактивні кишковий білок (VIP), міметик VIP, аналог VIP, конкретніше, опосередковані одним або декількома підтипами рецепторів VIP VPAC1, VPAC або РАСАР (пептид, що активує гіпофізарну аденілатциклазу), один або декілька агоністів рецепторів VIP або аналогів VIP (наприклад, Ro-125-1553) або фрагмент VIP, один або декілька антагоністів a-адреноцепторів з комбінацією VIP (наприклад, Invicorp, Aviptadil); 24) агоніст або модулятор рецепторів меланокортину або підсилювач меланокортину, такий як меланотан II, РТ-14, РТ-141 або сполуки, заявлені в [WO-09964002, WO-00074679, WO-09955679, WO00105401, WO-00058361, WO-00114879, WO-00113112, WO-09954358]; 25) агоніст, антагоніст або модулятор серотонінових рецепторів, конкретніше, агоністи, антагоністи або модулятори рецепторів 5НТ1А (включаючи VML 670), 5НТ2А, 5НТ2С, 5НТЗ і/або 5НТ6, включаючи рецептори, описані в [WO-09902159, WO-00002550 і/або WO-00028993]; 26) засіб, що заміняє тестостерон (включаючи дигідроандростендіон), тестостерон (Tostrelle), дигідротестостерон або імплантат тестостерону; 27) естроген, естроген і медроксипрогестерон або ацетат медроксипрогестерону (МРА) (тобто, у . вигляді комбінації), або засіб заміщувальної гормональної терапії естроген і метилтестостерон (наприклад, HRT, зокрема, премарин, ценестин, естрофемінал, еквін, естрейс, естрофем, елесте соло, естринг, естрадерм TTS, естрадерм матриця, дерместрил, премфейз, примпро, премпак, премік, естратест, естратест HS, тиболон); 28) модулятор транспортерів для норадреналіну, допаміну і/або серотоніну, такий як бупропіон, GW320659; 29) агоніст і/або модулятор пуринергічних рецепторів; 30) антагоніст рецепторів нейрокініну (NK), включаючи антагоністи, описані в [WO-09964008]; 31) агоніст, антагоніст або модулятор опіоїдних рецепторів, переважно, агоністи для рецептора ORL-1; 32) агоніст або модулятор для рецепторів окситоцину/вазопресину, переважно, селективний агоніст або модулятор окситоцину; 33) модулятори канабіоїдних рецепторів; 34) інгібітор SEP (SEPi), наприклад, SEPi, що має ІС50 нарівні менше ніж 100нМ, переважніше, на рівні менше ніж 50нМ. Переважно, інгібітори SEP відповідно до даного винаходу мають селективність для SEP більш ніж в 30 разів, переважніше, більше ніж в 50 разів, в порівнянні з нейтральною пептидазою ΝΕΡ EC 3.4.24.11 і ангіотензин-перетворюючим ферментом (АСЕ). Переважно, SEPi також має селективність, в 100 разів вищу, ніж для ендотелін-перетворюючого ферменту (ЕСЕ). У даному описі під перехресним посиланням на сполуки, що містяться в патентах і патентних заявках, які можна використати відповідно до винаходу, заявники мають на увазі терапевтично активні сполуки, визначені в формулі винаходу (зокрема, в п.1), і в конкретних прикладах (які все включені в даний опис як посилання). Якщо вводиться комбінація активних засобів, то їх можна вводити одночасно, роздільно або послідовно. Допоміжні засоби-інгібітори PDE5 Придатність будь-якого конкретного cGMP інгібітора PDE5 можна легко визначити оцінкою його активності і селективності з використанням способів, описаних в літературі, з подальшою оцінкою його токсичності, всмоктування, метаболізму, фармакокінетики і т.д. у відповідності до стандартної фармацевтичної практики. Величини ІС50 для cGMP інгібіторів PDE5 можна визначити з використанням аналізу PDE5 (див. нижче в даному описі). Переважно, cGMP інгібітори PDE5, що використовуються в фармацевтичних комбінаціях відповідно до даного винаходу, є селективними для ферменту PDE5. Переважно (при пероральному введенні), вони більш вибіркові, ніж для PDE3, переважніше, чим для PDE3 і для PDE4. Переважно (при застосуванні перорально), cGMP інгібітори PDE5 винаходу мають співвідношення селективності більше ніж 100, переважніше, більше ніж 300, в порівнянні з PDE3, переважніше, з PDE3 і PDE4. Співвідношення селективності може легко визначити фахівець в даній галузі. Величини ІС50 для ферменту PDE3 і PDE4 можна визначити з використанням встановленої, описаної в літературі методології [див. S.A. Ballard et al, Journal of Urology, 1998, vol. 159, pages 2164-2171] і як детально описано нижче в даному описі. Відповідні cGMP інгібітори PDE5 для застосування відповідно до даного винаходу включають в себе піразоло[4,3-d]піримідин-7-они, розкриті в [ЕР-А-0463756]; піразоло[4,3-d]піримідин-7-они, розкриті в [ЕР-А-0526004]; піразоло[4,3-d]піримідин-7-они, розкриті в опублікованій міжнародній патентній заявці [WO 93/06104]; ізомерні піразоло[3,4-d]піримідин-4-они, розкриті в опублікованій міжнародній патентній заявці [WO 93/07149]; хіназолін-4-они, розкриті в опублікованій міжнародній патентній заявці [WO 93/12095]; піридо[3,2-d]піримідин-4-они, розкриті в опублікованій міжнародній патентній заявці [WO 94/05661]; пурин-6-они, розкриті в опублікованій міжнародній патентній заявці [WO 94/00453]; піразоло[4,3-d]піримідин-7-они, розкриті в опублікованій міжнародній патентній заявці [WO 98/49166]; піразоло[4,3-d]піримідин-7-они, розкриті в опублікованій міжнародній патентній заявці [WO 99/54333]; піразоло[4,3-d]піримідин-4-они, розкриті в [ЕР-А-0995751]; піразоло[4,3-d]піримідин-7-они, розкриті в опублікованій міжнародній патентній заявці [WO 00/24745]; піразоло[4,3-d]піримідин-4-они, розкриті в [ЕР-А-0995750]; сполуки, розкриті в опублікованій міжнародній патентній заявці [WO 95/19978]; сполуки, розкриті в опублікованій міжнародній патентній заявці [WO 99/24433], і сполуки, розкриті в опублікованій міжнародній патентній заявці [WO 93/07124]; піразоло[4,3-d]піримідин-7-они, розкриті в опублікованій міжнародній патентній заявці [WO 01/27112]; піразоло[4,3-d] піримідин-7-они, розкриті в опублікованій міжнародній патентній заявці [WO 01/27113]; сполуки, розкриті в [ЕР-А-1092718], і сполуки, розкриті в [ЕР-А-1092719]. Інші відповідні інгібітори PDE5 для застосування відповідно до даного винаходу включають в себе 5-[2-етокси-5-(4-метил-1-піперазинілсульфоніл)феніл]-1-метил-3-н-пропіл-1,6-дигідро-7Н-піразоло[4,3d]піримідин-7-он (силденафіл), також відомий як 1-[[3-(6,7-дигідро-1-метил-7-оксо-3-пропіл-1Н-піразоло[4,3d]піримідин-5-іл)-4-етоксифеніл]сульфоніл]-4-метилпіперазин [див. ЕР-А-0463756]; 5-(2-етокси-5-морфолінацетилфеніл)-1-метил-3-н-пропіл-1,6-дигідро-7Н-піразоло[4,3-d]піримідин-7-он [див. ЕР-А-0526004]; 3-етил-5-[5-(4-етилпіперазин-1-ілсульфоніл)-2-н-пропоксифеніл]-2-(піридин-2-іл)метил-2,6-дигідро-7Нпіразоло[4,3-d]піримідин-7-он [див. WO98/49166]; 3-етил-5-[5-(4-етилпіперазин-1-ілсульфоніл)-2-(2-метоксіетокси)піридин-3-іл]-2-(піридин-2-іл)метил-2,6дигідро-7Н-піразоло[4,3-d]піримідин-7-он [див. W099/54333]; (+)-3-етил-5-[5-(4-етилпіперазин-1-ілсульфоніл)-2-(2-метокси-1(R)-метилетокси)піридин-3-іл]-2-метил2,6-дигідро-7Н-піразоло[4,3-d]піримідин-7-он, також відомий як 3-етил-5-{5-[4-етилпіперазин-1-ілсульфоніл]2-([(1R)-2-метокси-1-метилетил]окси)піридин-3-іл}-2-метил-2,6-дигідро-7Н-піразоло[4,3-d]піримідин-7-он [див. W099/54333]; 5-[2-етокси-5-(4-етилпіперазин-1-ілсульфоніл)піридин-3-іл]-3-етил-2-[2-метоксіетил]-2,6-дигідро-7Нпіразоло[4,3-d]піримідин-7-он, також відомий як 1-{6-етокси-5-[3-етил-6,7-дигідро-2-(2-метоксіетил)-7-оксо2Н-піразоло[4,3-d] піримідин-5-іл]-3-піридилсульфоніл}-4-етилпіперазин [див. WO 01/27113, приклад 8]; 5-[2-ізобутокси-5-(4-етилпіперазин-1-ілсульфоніл)піридин-3-іл]-3-етил-2-(1-метилпіперазин-4-іл)-2,6дигідро-7Н-піразоло[4,3-d]піримідин-7-он [див. WO 01/27113, приклад 15]; 5-[2-етокси-5-(4-етилпіперазин-1-ілсульфоніл)піридин-3-іл]-3-етил-2-феніл-2,6-дигідро-7Н-піразоло[4,3d]піримідин-7-он [див. WO 01/27113, приклад 66]; 5-(5-ацетил-2-пропокси-3-піридиніл)-3-етил-2-(1-ізопропіл-3-азетидиніл)-2,6-дигідро-7Н-піразоло[4,3d]піримідин-7-он [див. WO 01/27112, приклад 124]; 5-(5-ацетил-2-бутокси-3-піридиніл)-3-етил-2-(1-етил-3-азетидиніл)-2,6-дигідро-7Н-піразоло[4,3d]піримідин-7-он [див. WO 01/27112, приклад 132]; (6R,12aR)-2,3,6,7,12,12a-гeкcaгiдpo-2-мeтил-6-(3,4-мeтилeндioкcифeнiл)піразино[2',1':6,1]піридо[3,4b]індол-1,4-діон (ІС-351), тобто, сполуки прикладів 78 і 95 опублікованої міжнародної заявки [W095/19978], а також сполука прикладів 1, 3,7 i 8; 2-[2-етокси-5-(4-етилпіперазин-1-іл-1-сульфоніл)феніл]-5-метил-7-пропіл-3Н-імідазо[5,1-f][1,2,4]триазин4-он (варденафіл), також відомий як 1-[[3-(3,4-дигідро-5-метил-4-оксо-7-пропілімідазо[5,1-f]-асиметричн.триазин-2-іл)-4-етоксифеніл]сульфоніл]-4-етилпіперазин, тобто, сполука прикладів 20, 19, 337 і 336 опублікованої міжнародної заявки [W099/24433]; і сполука прикладу 11 опублікованої міжнародної заявки [W093/07124 (EISAI)]; і сполуки 3 і 14 з публікації [Rotella D. P., J. Med. Chem., 2000, 43, 1257]. Ще відповідні інгібітори PDE5 включають в себе 4-бром-5-(піридилметиламіно)-6-[3-(4-хлорфеніл)пропокси]-3(2Н) піридазинон; мононатрієву сіль 1-[4-[(1,3-бензодіоксол-5-ілметил)аміно]-6-хлор-2-хінозолініл]-4-піперидинкарбонової кислоти; (+)-цис-5,6а,7,9,9,9а-гексагідро-2-[4-(трифторметил)фенілметил-5-метилциклопент[4,5]імідазо[2,1b]пурин-4(ЗН)он; фуразлоцилін; цис-2-гексил-5-метил-3,4,5,6а,7,8,9,9а-октагідроциклопент[4,5]імідазо[2,1-b]пурин-4-он; 3-ацетил-1-(2-хлорбензил)-2-пропіліндол-6-карбоксилат; 3-ацетил-1-(2-хлорбензил)-2-пропіліндол-6-карбоксилат; 4-бром-5-(3-піридилметиламіно)-6-(3-(4-хлорфеніл)пропокси)-3-(2Н)піридазинон; мононатрієву сіль 1-метил-5-(5-морфолінацетил-2-н-пропоксифеніл)-3-н-пропіл-1,6-дигідро-7Нпіразол(4,3-d)тримідин-7-ону; 1-[4-[(1,3-бензодіоксол-5-ілметил)аміно]-6-хлор-2-хіназолініл]-4-піперидинкарбонову кислоту; фармацевтичні проекти №4516 (Glaxo Wellcome); фармацевтичні проекти №5051 (Bayer); фармацевтичні проекти №5064 [Kyowa Hakko; див. WO 96/26940]; фармацевтичні проекти №5069 (Schering Plough); GF-196960 (Glaxo Wellcome); E-8010 і E-4010 (Eisai); Bay-38-3045 & 38-9456 (Bayer) і Sch-51866. Сполуки формули (І) можна вводити окремо, але в основному їх потрібно вводити в суміші з відповідним фармацевтичним ексципієнтом, розріджувачем або носієм, вибраним з урахуванням передбачуваного шляху введення і стандартної фармацевтичної практики. Відповідно, даний винахід передбачає композицію, що включає в себе сполуки формули (І), (Іа) або (Іb) і фармацевтично прийнятний розріджувач або носій. Наприклад, сполуки формули (І), (Іа) або (Іb) можна вводити перорально, букально або сублінгвально у вигляді таблеток, капсул, кульок, еліксирів, розчинів або суспензій, які можуть містити ароматизуючі або фарбувальні речовини, з негайним, відстроченим, модифікованим, пролонгованим, пульсуючим або вивільненням, що контролюється. Такі таблетки можуть містити ексципієнти, такі як мікрокристалічна целюлоза, лактоза, цитрат натрію, карбонат кальцію, двохосновний фосфат кальцію і гліцин, розпушувачі, такі як крохмаль (переважно крохмаль з кукурудзи, картоплі або тапіоки), гліколаткрохмаль натрію, натрійкроскармелоза і певні складні силікати і грануляційні зв'язуючі речовини, такі як полівінілпіролідон, гідроксипропілметилцелюлоза (НРМС), гідроксипропілцелюлоза (НРС), сахароза, желатин і акація. Крім того, можуть, бути включені змащувальні речовини, такі як стеарат магнію, стеаринова кислота, бегенат гліцерилу і тальк. Тверді композиції аналогічного типу можна також використовувати як наповнювачі в желатинових капсулах. Переважні в цьому відношенні ексципієнти включають в себе лактозу, крохмаль, целюлозу, молочний цукор або поліетиленгліколі з високою молекулярною масою. Для водних суспензій і/або еліксирів сполуки формули (І), (Іа) або (Іb) можна комбінувати з різними підсолоджуючими або ароматизуючими речовинами, фарбувальною речовиною або барвниками, з емульгуючими і/або суспендуючими речовинами і з розріджувачами, такими як вода, етанол, пропіленгліколь і гліцерин, і їх комбінаціями. Сполуки формули (І), (Іа) або (Іb) можна також вводити парентерально, наприклад, внутрішньовенно, внутрішньоартеріально, внутрішньочеревинно, підоболонково, в шлуночки головного мозку, внутрішньоуретрально, інтрастернально, інтракраніально, внутрішньом'язово або підшкірно, або їх можна вводити методами вливання. Для такого парентерального введення вони найкращим чином застосовуються у вигляді стерильного водного розчину, який може містити інші речовини, наприклад, достатньо солей або глюкози для того, щоб зробити розчин ізотонічним з кров'ю. За необхідності, водним розчинам треба відповідним чином надати буферні властивості (переважно при рН від 3 до 9). Отримання відповідних парентеральних композицій в стерильних умовах легко здійснюється стандартними фармацевтичними методиками, добре відомими фахівцям в даній галузі. Сполуки формули (І), (Іа) або (Іb) можна також вводити інтраназально або шляхом інгаляції, звичайно у вигляді сухого порошку (або окремо, у вигляді суміші, наприклад, в сухій суміші з лактозою, або у вигляді змішаної компонентної частки, наприклад, змішаної з фосфоліпідами) з інгалятора сухого порошку або у вигляді аерозолю, що розпилюється з контейнера з вмістом під надмірним тиском, насосу, спрею, розпилювача (переважно розпилювача, в якому використана електрогідродинаміка для створення туману з дрібних крапель), або розбризкувача з використанням відповідного газу-витискувача, такого як дихлорфторметан, або без нього. Контейнер з вмістом під надмірним тиском, насос, спрей, розпилювач або розбризкувач містить розчин або суспензію активної сполуки, що включає в себе, наприклад, етанол (необов'язково водний етанол) або відповідну альтернативну речовину для диспергування, солюбілізації або подовження вивільнення активної речовини, газ(и)-витискувач як розчинник і необов'язково поверхнево-активну речовину, таку як триолеат сорбітану або олігомолочна кислота. Перед застосуванням в композиції у вигляді сухого порошку або суспензії лікарський продукт мікронізують до розміру, придатного для доставки шляхом інгаляції (звичайно менше ніж 5мкм). Цього можна досягнути будь-яким відповідним способом подрібнення, таким як помел в спіральному вихровому млині, помел псевдозрідженим шаром у вихровому млині, переробкою поверхневої рідини для утворення наночастинок, гомогенізацією при високому тиску або сушінням розпилюванням. Відповідна композиція у вигляді розчину для застосування в розпилювачі з використанням електрогідродинаміки для створення туману з дрібних крапель може містити від 1мкг до 10мг сполуки згідно з винаходом на запуск, а об'єм запуску може варіюватися від 1мкл до 100мкл. Звичайно композиція може включати в себе сполуки формули (І), (Іа) або (Іb), пропіленгліколь, стерильну воду, етанол і хлориди натрію. Альтернативні розчинники, які можна використати замість пропіленгліколю, включають в себе гліцерин і поліетиленгліколь. Капсули, блістери і картріджи (виготовлені, наприклад, з желатину або НРМС) для застосування в інгаляторі або інсуфляторі, можуть заповнюватися вмістом у вигляді порошкової суміші сполуки згідно з винаходом, відповідної порошкової основи, такої як лактоза або крохмаль, і функціонального модифікатора, такого як І-лейцин, маніт або стеарат магнію. Композиції для інгаляційного/інтраназального введення можна складати для негайного і/або модифікованого вивільнення. Альтернативно, сполуки формули (І), (Іа) або (Іb) можна вводити у вигляді супозиторію або песарію, або вони можуть наноситися місцево у вигляді гелю, гідрогелю, лосьйону, розчину, крему, мазі або порошка для присипки. Сполуки формули (І), (Іа) або (Іb) можна також вводити дермально або трансдермально, наприклад, з використанням шкірної накладки. їх можна також вводити легеневим або ректальним шляхом. Їх можна також вводити очним шляхом. Для офтальмологічного застосування сполуки можуть бути включені в композицію у вигляді мікронізованих суспензій в ізотонічному, стерильному сольовому розчині з доведеним рН або, переважно, у вигляді розчинів в ізотонічному, стерильному сольовому розчині з доведеним рН, необов'язково в комбінації з консервантом, таким як хлорид бензалконію. Альтернативно, вони можуть складатися в композицію у вигляді мазі, такої як вазелін. Для місцевого нанесення на шкіру сполуки формули (І), (Іа) або (Іb) можуть бути складені в композиції у вигляді відповідної мазі, що містить активну сполуку, суспендовану або розчинену, наприклад, в суміші з одним або декількома з наступних речовин: мінеральне масло, рідкий вазелін, білий вазелін, пропіленгліколь, сполуки поліоксіетилену-поліоксипропілену, емульгуючий віск і вода. Альтернативно, вони можуть бути складені в композицію у вигляді лосьйону або крему, суспендовані або розчинені, наприклад, суміші з одним або декількома з наступних речовин: мінеральне масло, моностеарат сорбітану, поліетиленгліколь, рідкий парафін, полісорбат 60, віск складних цетилових ефірів, цетеариловий спирт, 2октилдодеканол, бензиловий спирт і вода. Сполуки формули (І), (Іа) або (Іb) можна також застосовувати в комбінації з циклодекстрином. Відомо, що циклодекстрини утворюють сполуки включення і не включення з молекулами лікарської речовини. Утворення комплексу лікарська речовина-циклодекстрин може модифікувати розчинність, швидкість розчинення, біологічну доступність і/або стабільність молекули лікарського засобу. Комплекси лікарська речовина-циклодекстрин в основному корисні для більшості лікарських форм і шляхів введення. Як альтернатива прямому утворенню комплексів з лікарською речовиною, циклодекстрин можна використати як допоміжну домішку, наприклад, у вигляді носія, розріджувача або солюбілізатора. Альфа-, бета- і гаммациклодекстрини найбільш широко використовуються, і відповідні приклади описані в [WO- А-91/11172, WOA-94/02518 і WO-A-98/55148]. Даний винахід далі ілюструється наступними необмежувальними прикладами, в яких використані наступні абревіатури і визначення: оптичне обертання при 587нм aD ArbacelÒ фільтруючий агент уш Широкий Вос трет-бутоксикарбоніл СDСІ 3 хлороформ-d1 CD3OD метанол-d4 хімічний зсув d д дублет дд дублет дублетів DCM дихлорметан ДМФА Ν,Ν-диметилформамід ДМСО диметилсульфоксид год. години НСl хлористий водень LRMS мас спектр низького розрізнення м мультиплет m/z пік мас спектра хв. хвилини Т.пл. точка плавлення NaOH гідроксид натрію ЯМР ядерний магнітний резонанс KB квартет с синглет τ триплет Tf трифторметансульфоніл TFA трифтороцтова кислота ΤΓΦ тетрагідрофуран ТШХ тонкошарова хроматографія Точки плавлення визначали з використанням пристрою Perkin Elmer DSC7 при швидкості нагрівання 20°С/хв. Дані дифракція рентгенівських променів реєстрували при кімнатній температурі з використанням дифрактометру BROKER AXS SMART-APEX CCD AREA-DETECTOR (випромінювання MO Κa). Показники інтенсивності інтегрували по декількох серіях впливів. Кожний вплив покривав 0,3° в W, при часі впливу 60сек., і повний набір даних був більшим ніж сфера. Приклад 1 2-аміно-1-(3-метоксифеніл)етанол 3-метоксибензальдегід (27,2г, 0,2моль) в ТГФ (150мл) додають до перемішуваного розчину 3Ν НСl (водн.) (150мл, 0,3моль) і сульфату натрію (37,8г, 0,3моль) при кімнатній температурі. Через 10хв. порціями додають ціанід калію (19,53г, 0,3моль), і реакційну суміш потім перемішують протягом 30хв. Додають діетиловий ефір (800мл) і воду (300мл) і шари, що утворилися, розділяють. Повторну екстракцію водного розчину проводять діетиловим ефіром (500мл), органічні шари об'єднують, сушать над водним сульфатом магнію, фільтрують, потім концентрують у вакуумі з отриманням проміжної сполуки ціангідрину у вигляді безбарвної олії (35,57г, 0,22моль, >100%). Комплекс боран-тетрагідрофуран (1М в ТГФ) (400мл, 0,4моль) потім обережно додають до ціангідрину в ТГФ (100мл). Після припинення бурхливого виділення газу, перемішування продовжують при кип'ятінні із зворотним холодильником протягом 1,5год. в атмосфері азоту. Реакційну суміш охолоджують, потім реакцію гасять метанолом (400мл) перед концентруванням у вакуумі з отриманням безбарвної олії. Додають 6М НСl (водн.) (200мл) і реакційну суміш перемішують при кип'ятінні із зворотним холодильником протягом 2год. перед концентруванням у вакуумі з отриманням білої твердої речовини. Його заздалегідь абсорбують на діоксид кремнію, потім очищають колонковою хроматографією, елююючи сумішшю дихлорметан:метанол:аміак (90:10:1), з отриманням вказаної в заголовку сполуки у вигляді безбарвної олії (31,3г, 0,19моль, 94%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 1,60 (уш.с, 2Н), 2,80 (дд, 1Н), 3,02 (дд, 1Н), 3,46 (с, 1Н), 3,81 (с, 3Н), 4,60 (дд, 1Н), 6,81 (д, 1Н), 6,91 (д, 1Н), 6,93 (с, 1Н), 7,22 (т, 1Η). LRMS: m/z 168 (М-H+). Аналіз знайдено С, 56,66; Н, 8,28; N, 6,91%. C9H13NO2»·1, 33Н2О обчислено С, 56,33; Н, 8,27; N, 7,30%. Приклад 2 N-[2-гідрокси-2-(3-метоксифеніл)етил]пропіонамід Триетиламін (52мл, 0,37моль) додають до аміну прикладу 1 (31,3г, 0,19моль) в дихлорметані (400мл) і реакційну суміш перемішують в атмосфері газоподібного азоту при 0°С протягом 10хв. Додають хлорид пропіонілу (16,3мл, 0,19моль) і після перемішування протягом 30хв. температуру реакційної суміші підвищують до кімнатної температури протягом ще 5год. Реакційну суміш гасять 1N HCI (водн.) (100мл) і потім екстрагують дихлорметаном (2´50мл). Органічні фракції об'єднують, сушать над водним сульфатом магнію, фільтрують і концентрують у вакуумі з отриманням вказаної в заголовку сполуки у вигляді безбарвного масла, яке кристалізується при стоянні з утворенням білих кристалів (28г, 0,13моль, 67%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 1,18 (т, 3Н), 2,22 (кв, 2Н), 2,51 (уш.с, 1Н), 3,31 (м, 1Н), 3,71 (дд, 1Н), 3,80 (с, 3Н), 4,81 (м, 1Н), 5,95 (уш.с, 1Н), 6,80 (д, 1Н), 6,90 (д, 1Н), 6,91 (с, 1Н), 7,22 (т, 1Н). LRMS: m/z 224, Т.пл.: 7778°С. Аналіз знайдено С, 63,86; Н, 7,82; N, 6,28%. C12H17NO3·0,1H2O обчислено С, 64,04; Н, 7,70; N, 6,22%. Приклад 3 1-(3-метоксифеніл)-2-пропіламіноетанол Комплекс боран-тетрагідрофуран (1М в ТГФ) (376мл, 0,4моль) додають до аміду прикладу 2 (28г, 0,13моль) в сухому ТГФ (100мл), потім реакційну суміш перемішують в атмосфері газоподібного азоту, кип'ятять із зворотним холодильником протягом 2,5год. Реакційну суміш охолоджують, потім гасять метанолом (40мл) перед концентруванням у вакуумі з отриманням каламутного білого масла. Додають 6Ν НСI (води.) (200мл) і реакційну суміш перемішують при кип'ятінні із зворотним холодильником протягом 2год. Реакційну суміш охолоджують, потім додають дихлорметан (200мл) і шари розділяють. Водному шару додають основні властивості додаванням карбонату калію, потім повторно екстрагують дихлорметаном (2´200мл). Органічні екстракти об'єднують, сушать над безводним сульфатом магнію, фільтрують і концентрують у вакуумі з отриманням вказаної в заголовку сполуки у вигляді безбарвного масла, яке кристалізується при стоянні з утворенням безбарвних кристалів (15,3г, 0,07моль, 59%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 0,93 (т, 3Н), 1,62 (кв, 2Н), 2,71 (кв, 2Н), 2,81 (т, 2Н), 3,00 (д, 1Н), 3,80 (с, 3Н), 4,30 (уш.с, 1Н), 4,89 (д, 1Н), 6,81 (д, 1Н), 6,91 (д, 1Н), 6,93 (с, 1Н), 7,22 (т, 1Η). LRMS: m/z 210, Т.пл.: 50-51°С. Аналіз знайдено С, 67,47; Н, 9,02; N, 6,45%. C12H19NO2·0,2H2O обчислено С, 67,70; Н, 9,19; N, 6,58%. Приклад 4 2-N-[2-гідрокси-2-(3-метоксифеніл)етил]-N-пропілацетамід Гідроксид натрію (15,1г, 0,38моль) у воді (180мл) додають до аміну прикладу 3 (15,8г, 0,08моль) в дихлорметані (500мл) і розчин енергійно перемішують при кімнатній температурі. Потім додають хлорацетилхлорид (7,22мл, 0,09моль), і реакційну суміш перемішують ще протягом 30хв. Шари розділяють і водний шар повторно екстрагують дихлорметаном (200мл). Органічні екстракти об'єднують, сушать над безводним сульфатом магнію, фільтрують і концентрують у вакуумі з отриманням вказаної в заголовку сполуки у вигляді безбарвного масла (17,8г, 0,06моль, 83%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 0,96 (т, 3Н), 1,62 (кв, 2Н), 3,21 (кв, 2Н), 3,57-3,71 (м, 2Н), 3,82 (с, 3Н), 4,014,21 (уш.кв, 1Н), 4,16 (с, 2Н), 5,00 (м, 1Н), 6,82 (м, 1Н), 6,91-6,99 (м, 2Н), 7,22 (м, 1Н). LRMS: m/z 286, Аналіз знайдено С, 57,38; Н, 6,95; N, 4,67%. C14H2ONO3CI·0,33H2O обчислено С, 57,64; Н, 7,14; N, 4,80%. Приклад 5 6-(3-метоксифеніл)-4-пропілморфолін-3-он Гідроксид калію (4,2г, 0,07моль), ізопропіловий спирт (500мл) і амід прикладу 4 (17,8г, 0,06моль) перемішують разом у вигляді каламутного розчину з водою (15мл) протягом 2год. Реакційну суміш концентрують у вакуумі і жовтий залишок розчиняють в етилацетаті (200мл). Його розділяють водою (200мл), потім насиченим розчином солі (200мл). Органічну фракцію сушать над безводним сульфатом магнію, фільтрують і концентрують у вакуумі з отриманням вказаної в заголовку сполуки у вигляді жовтого масла (15,8г, 0,06моль, 100%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 0,96 (т, 3Н), 1,62 (м, 2Н), 3,36 (м, 2Н), 3,51 (кв, 2Н), 3,81 (с, 3Н), 4,30-4,62 (уш.кв, 2Н), 4,79 (д, 1Н), 6,85 (д, 1Н), 6,91 (д, 1Н), 6,95 (с, 1Н), 7,29 (т, 1Н). LRMS: m/z 272, Аналіз знайдено С, 66,80; Н, 7,78; N, 5,52%. C14H19NO3·0,1H2O обчислено С, 66,96; Н, 7,71; Ν, 5,58%. Приклад 6 2-(3-метоксифеніл)-4-пропілморфолін Комплекс боран-тетрагідрофуран (1М в ТГФ) (200мл, 0,19моль) (200мл, 0,19моль) додають по краплях до морфолін-3-ону прикладу 5 (15,8г, 0,06моль) в сухому ТГФ (100мл) в атмосфері азоту протягом 30хв. Реакційну суміш кип'ятять із зворотним холодильником протягом 3год., потім охолоджують і реакцію гасять доданням метанолу (30мл). Потім реакційну суміш концентрують у вакуумі і безбарвний залишок обережно суспендують в 4Ν НСI (водн.) (400мл) перед кип'ятінням із зворотним холодильником протягом 2,5год. Реакційну суміш охолоджують і додають дихлорметан (200мл). Шари розділяють і водному шару додають основні властивості доданням карбонату калію перед повторною екстракцією дихлорметаном (3´100мл). Органічні екстракти об'єднують, сушать над безводним сульфатом магнію, фільтрують і концентрують у вакуумі з отриманням вказаної в заголовку сполуки у вигляді безбарвного масла (12,51г, 0,05моль, 84%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 0,95 (т, 3Н), 1,59 (кв, 2Н), 2,05 (т, 1Н), 2,23 (т, 1Н), 2,40 (т, 2Н), 2,81 (д, 1Н), 2,98 (д, 1Н), 3,80 (с, 3Н), 3,85 (т, 1Н), 4,05 (д, 1Н), 4,60 (д, 1Н), 6,81 (д, 1Н), 6,91 (д, 1Н), 7,21 (т, 1Н), 7,23 (с, 1Н). LRMS: m/z 236, Аналіз знайдено С, 68,94; Н, 8,80; N, 5,79%. C 14H21NO2·0,5H2O обчислено С, 68,82; Н, 9,08; N, 5,73%. Приклад 7А R-(-)-3-(4-пpoпiлмopфoлiн-2-iл)фенол Приклад 7В S-(+)-3-(4-пропілморфолін-2-іл)фенол Бромистоводневу кислоту (250мл) і анізол прикладу 6 (8,62г, 0,03моль) нагрівають при кип'ятінні із зворотним холодильником разом протягом 1год. Після охолоджування реакційну суміш розбавляють водою (100мл), потім нейтралізують доданням NH4OH (20мл). Жовтий каламутний розчин потім екстрагують дихлорметаном (2´100мл). Органічні екстракти об'єднують, потім сушать над безводним сульфатом магнію, фільтрують і концентрують у вакуумі з отриманням рацемічної суміші сполуки у вигляді жовтого масла (7,78г, 0,03моль, 96%). Енантіомери розділяють хиральною хроматографією (колонка Chiralpak AD 250*20мм), елююючи сумішшю гексан:ізопропіловий спирт:діетиламін (70:30:0,05), з отриманням енантіомеру 1 (ее >95%) і енантіомеру 2 (ее >99%). Кожний енантіомер очищають колонковою хроматографією на діоксиді кремнію, елююючи сумішшю дихлорметан:метанол (95:5), з отриманням енантіомеру 1 (7а) (3,02г, 0,014моль, 39%) і енантіомеру 2 (7b) (3,15г, 0,014моль, 40%) у вигляді безбарвного масла. Енантіомер 1 (7а): 1 Н ЯМР (СDСІ 3, 400МГц) d: 0,96 (т, ЗН), 1,60 (кв, 2Н), 2,13 (т, 1Н), 2,31 (т, 1Η), 2,41 (т, 2Н), 2,85 (д, 1Н), 3,02 (д, 1Н), 3,90 (т, 1Н), 4,02 (дд, 1Н), 4,60 (д, 1Н), 6,78 (д, 1Н), 6,80 (с, 1Н), 6,91 (д, 1Н), 7,20 (т, 1Н). LRMS: m/z 222 (М-Н+). Енантіомер 2: 1 Н ЯМР (СDСІ 3, 400МГц) d: 0,96 (т, 3Н), 1,60 (кв, 2Н). 2,13 (т, 1Н), 2,31 (т, 1Н), 2,41 (т, 2Н), 2,85 (д, 1Н), 3,02 (д, 1Н), 3,90 (т, 1Н), 4,02 (дд, 1Н), 4,60 (д, 1Н), 6,78 (д, 1Н), 6,80 (с, 1Н), 6,91 (д, 1Н), 7,20 (т, 1Н). LRMS: m/z 222 (М-Н+). Приклад 8 Гідрохлорид R-(-)-3-(4-пpoпiлмopфoлiн-2-iл)фeнoлy Енантіомер 1 (7а) прикладу 7 (3,00г, 0,014моль) розчиняють в діетиловому ефірі (180мл) і додають хлористий водень (2,0М розчин в діетиловому ефірі) (10мл). Реакційну суміш перемішують при кімнатній температурі протягом 30хв., потім розчинник декантують і сушать у вакуумі, отримуючи вказану в заголовку сполуку у вигляді білої твердої речовини (3,115г, 0,012моль, 90%). 1 Н ЯМР (CD3OD, 400МГц) d: 1,06 (т, 3Н), 1,81 (м, 2Н), 3,02 (т, 1Н), 3,16 (т, 2Н), 3,20 (т, 1Н), 3,60 (т, 2Н), 4,01 (т, 1Н), 4,26 (д, 1Н), 4,71 (д, 1Н), 6,78 (д, 1Н), 6,82 (с, 1Н), 6,83 (д, 1Н), 7,21 (т, 1Н). LRMS: m/z 222 (МН+). Аналіз знайдено С, 59,74; Н, 7,98; N, 5,25%. C13H19NO2·0,18H2O обчислено С, 59,82; Н, 7,86; N, 5,37%. [a]D=-5,66° (метанол 10,6мг/10мл). Зразок вказаної в заголовку сполуки повторно кристалізують паровою дифузією з використанням суміші метанол:діетиловий ефір і отримують рентгенівську кристалічну структуру. Абсолютну стереохімію вказаної в заголовку сполуки визначають за даними дифракції способом FLACK1, і показано, що вона має "R" конфігурацію. [Посилання 1: H.D.Flack, Acta Cryst. 1983, 439, 876-881] Приклад 9 г 2-аміно-1-(3,5-диметоксифеніл)етанол Отримують, відповідно до аналогічної методики прикладу 1, виходячи з 3,5-диметоксибензальдегіду (5,00г, 0,03моль). Після кип'ятіння із зворотним холодильником в 6М НСl (водн.) реакційну суміш охолоджують і екстрагують діетиловим ефіром (2´80мл). Органічні шари відкидають і водному шару додають основні властивості додаванням карбонату калію. Водний залишок потім екстрагують етилацетатом (3´70мл). Органічні екстракти об'єднують і сушать над безводним сульфатом магнію, фільтрують і концентрують у вакуумі з отриманням вказаної в заголовку сполуки у вигляді блідо-жовтого масла (3,47г, 0,018моль, 59%). 1 Н ЯМР (CD3OD, 400МГц) d: 2,77-2,86 (м, 2Н), 3,78 (с, 6Н), 4,60 (м, 1Н), 6,38 (с, 1Н), 6,52 (с, 2Н). LRMS: m/z 198 (М-Н+). Приклад 10 N-[2-(3,5-диметоксифеніл)-2-гідроксіетил]пропіонамід Отримують, відповідно до аналогічної методики прикладу 2, виходячи з аміну прикладу 9 (3,41г, 0,017моль). Неочищену реакційну суміш очищають колонковою хроматографією на діоксиді кремнію, елююючи сумішшю дихлорметан:метанол (95:5), з отриманням вказаної в заголовку сполуки у вигляді яскраво-жовтого масла (3,08г, 0,12моль, 70%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 1,18 (м, 3Н), 2,24 (м, 2Н), 3,34 (м, 1Н), 3,68 (м, 1Н), 3,81 (с, 6Н), 4,80 (дд, 1Н), 5,95 (уш.с, 1Н), 6,39 (с, 1Н), 6,51 (с, 2Н). LRMS: m/z 252 (М-H-). Приклад 11 1-(3,5-диметоксифеніл)-2-пропіламінетанол Отримують, відповідно до аналогічної методики прикладу 3, виходячи з аміду прикладу 10 (3,06г, 0,012моль), з отриманням вказаної в заголовку сполуки у вигляді оранжевого масла (2,72г, 0,011моль, 94%). 1 Н ЯМР (CD3OD, 400МГц) d: 0,95 (т, 3Н), 1,56 (м, 2Н), 2,61 (м, 2Н), 2,77 (д, 2Н), 3,78 (с, 6Н), 4,70 (т, 1Н), 6,38 (с, 1Н), 6,51 (с, 2Н). LRMS: m/z 240 (М-Н+). Приклад 12 2-хлор-N-[2-(3,5-диметоксифеніл)-2-гідроксіетил]-N-пропілацетамід Отримують, відповідно до аналогічної методики прикладу 4, виходячи з аміну прикладу 11 (2,70г, 0,011моль), з отриманням вказаної в заголовку сполуки у вигляді жовтого масла (3,56г, 0,011моль, 100%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 0,92 (т, 3Н), 1,61 (м, 2Н), 3,20 (м, 2Н), 3,51-3,64 (м, 2Н), 3,80 (д, 6Н), 4,13 (с, 2Н), 4,95 (м, 1Н), 6,40 (м, 1Н), 6,55 (с, 2Н). LRMS: m/z 316(М-Н+). Приклад 13 6-(3,5-диметоксифеніл)-4-пропілморфолін-3-он і Отримують, відповідно до аналогічної методики прикладу 5, виходячи з аміду прикладу 12 (3,43г, 0,011моль), з отриманням вказаної в заголовку сполуки у вигляді жовтого масла (2,44г, 0,009моль, 78%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 0,94 (т, 3Н), 1,61 (м, 2Н), 3,30 (м, 2Н), 3,49 (м, 2Н), 3,80 (с, 6Н), 4,30 (д, 1Н), 4,42 (д, 1Н), 4,73 (дд, 1Н), 6,42 (с, 1Н), 6,53 (с, 2Н). LRMS: m/z 280 (М-Н+). Приклад 14 2-(3,5-диметоксифеніл)-4-пропілморфолін Отримують, відповідно до аналогічної методики прикладу 6, виходячи з аміду прикладу 13 (23,42г, 0,009моль). Після кип'ятіння із зворотним холодильником в 6М НСI (водн.) охолоджену реакційну суміш екстрагують діетиловим ефіром (2´80мл). Органічні шари відкидають і водному шару додають основні властивості додаванням карбонату калію. Водний залишок потім екстрагують етилацетатом (3´80мл) і органічні екстракти об'єднують, сушать над сульфатом магнію, фільтрують, потім концентрують у вакуумі з отриманням вказаної в заголовку сполуки у вигляді блідо-оранжевого масла (2,14г, 0,008моль, 93%). 1 Н ЯМР (CD3OD, 400МГц) d: 0,95 (т, 3Н), 1,58 (м, 2Н), 2,01 (м, 1Н), 2,22 (дт, 1Н), 2,38 (т, 2Н), 2,83 (д, 1Н), 2,93 (д, 1Н), 3,78 (м, 7Н), 4,01 (дд, 1Н), 4,45 (дд, 1Н), 6,39 (с, 1Н), 6,49 (с, 2Н). LRMS: m/z 266 (М-Н+). Приклад 15А R-5-(4-пpomлмopфoлiн-2-iл)бeнзoл-1,3-діол Приклад 15В S-5-(4-пропілморфолін-2-іл)бензол-1,3-діол Отримують, відповідно до аналогічної методики прикладу 7, виходячи з 3,5-диметоксифенільної сполуки прикладу 14 (1,00г, 0,004моль), отримуючи вказану в заголовку рацемічну сполуку у вигляді коричневого масла (145мг, 0,61ммоль, 16%). Енантіомери розділяють хиральною хроматографією (колонка Chiralpak AD 250*20мм), елююючи сумішшю гексан:ізопропіловий спирт (80:20), з отриманням енантіомеру 1 (15а) (5,2мг) (ее >98,94%) і енантіомеру 2 (15b) (5,1мг) (ее >96,46%), обидва у вигляді коричневого масла. Енантіомер 1 (15а): 1 Н ЯМР (CD3OD, 400МГц) d: 0,96 (т, 3Н), 1,58 (м, 2Н), 2,01 (т, 1Н), 2,20 (дт, 1Н), 2,37 (т, 2Н), 2,81-2,92 (м, 2Н), 3,89 (дт, 1Н), 3,99 (дд, 1Н), 4,38 (дд, 1Н), 6,18 (т, 1Н), 6,26 (с, 2Н). LRMS: m/z 238 (М-Н+). Енантіомер 2 (15b): 1 Н ЯМР (CD3OD, 400МГц) d: 0,95 (т, 3Н), 1,58 (м, 2Н), 2,01 (т, 1Н), 2,20 (дт, 1Н), 2,38 (т, 2Н), 2,80-2,92 (кв, 2Н), 3,78 (дт, 1Н), 3,98 (дд, 1Н), 4,38 (дд, 1Н), 6,18 (с, 1Н), 6,25 (с, 2Н). LRMS: m/z 238 (М-Н+). Приклад 16 4-фтор-3-метоксибензальдегід (4-фтор-3-метоксифеніл)метанол (5,00г, 0,03моль) і діоксид марганцю (33,4г, 0,38моль) перемішують в дихлорметані (100мл) в атмосфері азоту при обережному кип'ятінні із зворотним холодильником протягом 16год. Охолоджену реакційну суміш потім фільтрують через арбацел і концентрують у вакуумі з отриманням вказаної в заголовку сполуки у вигляді білої твердої речовини (4,18г, 0,027моль, 85%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 3,96 (с, 3Н), 7,23 (д, 1Н), 7,43 (м, 1Н), 7,50 (д, 1Н) 9,91 (с, 1Н). Т.пл.: 61-63°С. Аналіз знайдено С, 62,18; Н, 4,54%. C8H7FO2 обчислено С, 62,34; Н, 4,58%. Приклад 17 2-аміно-1-(4-фтор-3-метоксифеніл)етанол Отримують, відповідно до аналогічної методики прикладу 1, виходячи з 4-фтор-3-метоксибензальдегіду (4,17г, 0,03моль). Після кип'ятіння із зворотним холодильником в 6М НСl (водн.) реакційну суміш охолоджують і екстрагують діетиловим ефіром (2´60мл). Органічні шари відкидають і водному шару додають основні властивості доданням карбонату калію. Водний залишок потім екстрагують етилацетатом (3´80мл). Органічні екстракти об'єднують і сушать над безводним сульфатом магнію, фільтрують, потім концентрують у вакуумі з отриманням вказаної в заголовку сполуки у вигляді оранжевого масла (2,36г, 0,013моль, 47%). 1 Н ЯМР (CD3OD, 400МГц) d: 2,80-2,91 (м, 2Н), 3,86 (с, 3Н), 4,64 (м, 1Н), 6,89 (м, 1Н), 7,03 (т, 1Н), 7,11 (дд, 1Н). LRMS: m/z L86 (М-Н+). Приклад 18 N-[2-(4-фтор-3-метоксифеніл)-2-гідроксіетил]пропіонамід Отримують, відповідно до аналогічної методики прикладу 2, виходячи з аміну прикладу 17 (1,32г, 0,007моль). Неочищену реакційну суміш очищають колонковою хроматографією на діоксиді кремнію, елююючи сумішшю етилацетат:пентан (2:1), з отриманням вказаної в заголовку сполуки у вигляді жовтого масла, яке кристалізується при стоянні (0,59г, 0,002моль, 35%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 1,18 (т, 3Н), 2,24 (кв, 2Н), 2,58 (уш.с, 1Н), 3,34 (м, 1Н), 3,63 (м, 1Н), 3,88 (с, 3Н), 4,82 (дд, 1Н), 5,98 (уш.с, 1Н), 6,82 (м, 1Н), 7,01 (м, 2Н). LRMS: m/z 242 (М-Н+). Приклад 19 1-(4-фтор-3-метоксифеніл)-2-пропіламіноетанол Отримують, відповідно до аналогічної методики прикладу 3, виходячи з аміду прикладу 18 (585мг, 2,42ммоль). Після кип'ятіння із зворотним холодильником в 6М НСI (водн.) реакційну суміш охолоджують і екстрагують діетиловим ефіром (2´50мл). Органічні шари відкидають і водному шару додають основні властивості доданням карбонату калію. Водний залишок потім екстрагують етилацетатом (3´50мл). Органічні екстракти об'єднують і сушать над безводним сульфатом магнію, фільтрують, потім концентрують у вакуумі з отриманням вказаної в заголовку сполуки у вигляді блідо-жовтого масла (448мг, 1,97моль, 81%). 1 Н ЯМР (CD3OD, 400МГц) d: 0,96 (т, 3Н), 1,58 (м, 2Н), 2,63 (м, 2Н), 2,79 (д, 2Н), 3,96 (с, 3Н), 4,77 (т, 1Н), 6,90 (м, 1Н), 7,03 (т, 1Н), 7,11 (д, 1Н). LRMS: m/z 228 (М-Н+). Приклад 20 2-хлор-N-[2-(4-фтор-3-метоксифеніл)-2-гідроксіетил]-N-пропілацетамід Отримують, відповідно до аналогічної методики прикладу 4, виходячи з аміну прикладу 19 (0,84т. 4,00моль), з отриманням вказаної в заголовку сполуки у вигляді жовтого масла (0,97г, 3,00ммоль, 87%). LRMS: m/z 304 (М-Н+). Далі використовують в неочищеному вигляді. Приклад 21 6-(4-фтор-3-метоксифеніл)-4-пропілморфолін-3-он Отримують, відповідно до аналогічної методики прикладу 5, виходячи з аміду прикладу 20 (0,96г, 3,00ммоль), з отриманням вказаної в заголовку сполуки у вигляді жовтого масла (0,64г, 2,40ммоль, 75%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 0,94 (т, 3Н), 1,62 (м, 2Н), 3,33 (м, 2Н), 3,48 (м, 2Н), 3,91 (с, 3Н), 4,34 (д, 1Н), 4,43 (д, 1Н), 4,76 (дд, 1Н), 6,85 (м, 1Н), 7,01-7,08 (м, 2Н). LRMS: m/z 268. Приклад 22 2-(4-фтор-3-метоксифеніл)-4-пропілморфолін Отримують, відповідно до аналогічної методики прикладу 6, виходячи з морфолін-3-ону прикладу 21 (633мг, 2,37ммоль). Після кип'ятіння із зворотним холодильником в 6М НСI (водн.) реакційну суміш охолоджують і екстрагують діетиловим ефіром (2´20мл). Органічні шари відкидають і водному шару додають основні властивості доданням карбонату калію. Водний залишок потім екстрагують етилацетатом (3´20мл). Органічні екстракти об'єднують і сушать над безводним сульфатом магнію, фільтрують і концентрують у вакуумі з отриманням вказаної в заголовку сполуки у вигляді жовтого масла (552мг, 2,18ммоль, 92%). 1 Н ЯМР (CD3OD, 400МГц) d: 0,95 (т, 3Н), 1,58 (м, 2Н), 2,02 (т, 1Н), 2,22 (дт, 1Н), 2,38 (т, 2Н), 2,85 (д, 1Н), 2,93 (д, 1Н), 3,80 (м, 1Н), 3,84 (с, 3Н), 4,01 (дд, 1Н), 4,50 (дд, 1Н), 6,88 (м, 1Н), 7,02 (т, 1Н), 7,09 (д, 1Н). LRMS: m/z 254 (М-Н+). Приклад 23А R-(+)-2-фтop-5-(4-пpoпiлмopфoлiн-2-iл)фeнoл Приклад 23В S-(-)-2-фтор-5-(4-пропілморфолін-2-іл)фенол Отримують, відповідно до того ж способу, як в прикладі 7, виходячи з анізолу прикладу 22 (200мг, 0,789ммоль). Неочищену реакційну суміш очищають колонковою хроматографією на діоксиді кремнію, елююючи сумішшю дихлорметан:метанол (90:10), з отриманням вказаної в заголовку сполуки у вигляді темно-жовтого в'язкого масла (149мг, 0,62ммоль, 79%). Енантіомери розділяють хиральною хроматографією (колонка Chiralpak AD 250*20мм), елююючи сумішшю гексан:ізопропіловий спирт (90:10), з отриманням енантіомеру 1 (23а) у вигляді каламутного масла (15мг) (ее >99,5%) і енантіомеру 2 (23b) у вигляді кристалічної твердої речовини (16мг) (ее >99%). Енантіомер 1 (23a): 1 Н ЯМР (CD3OD, 400МГц) d: 0,95 (т, 3Н), 1,58 (м, 2Н), 2,01 (т, 1Н), 2,21 (дт, 1Н), 2,37 (т, 2Η), 2,82-2,97 (уш.кв, 2Н), 3,78 (дт, 1Н), 3,99 (дд, 1Н), 4,43 (д, 1Н), 6,78 (м, 1Н), 6,89-7,01 (м, 2Н). LRMS: m/z 240 (М-Н+). a D=+0,91 (етанол 1,10мг/мл). Енантіомер 2 (23b): 1 Н ЯМР (CD3OD, 400МГц) d: 0,96 (т, 3Н), 1,58 (м, 2Н), 2,01 (т, 1Η), 2,22 (дт, 1Н), 2,38 (т, 2Н), 2,78 (дд, 2Н), 3,78 (дт, 1Н), 4,00 (дд, 1Н), 4,43 (дд, 1Н), 6,78 (м, 11Н, 6,91 (д, 1Н), 6,98 (т, 1Н). LRMS: m/z 240 (М-Н+). a D=-0,40 (етанол 1,00мг/мл). Приклад 24 2-аміно-1-(4-бензилоксифеніл)етанол Ціанід калію (20,15г, 0,31моль) і хлорид амонію (16,4г, 0,31моль) розчиняють у воді (60мл), до якої додають 4-бензилоксибензальдегід (32,9г, 0,155моль) з подальшим доданням діетилового ефіру (100мл). Реакційну суміш енергійно перемішують протягом 48год. при кімнатній температурі перед екстрагуванням етилацетатом (2´200мл). Об'єднані органічні шари сушать над безводним сульфатом магнію, фільтрують і концентрують у вакуумі з отриманням ціангідринного проміжного продукту у вигляді жовтої твердої речовини (34,2г, 0,14моль, 90%). Потім циангідрин розчиняють в сухому ТГФ (300мл) і додають комплекс боран-метилсульфід (26,6мл, 0,28моль). Реакційну суміш кип'ятять із зворотним холодильником протягом 2год. перед гасінням метанолом (50мл). Додають воду (50мл) з подальшим доданням конц. НСl (40мл) і реакційну суміш перемішують протягом 2год. доти, поки екзотермічна реакція не слабшає. Потім реакційну суміш концентрують у вакуумі І залишок розбавляють водою (100мл). Потім водному розчину додають основні властивості доданням NH4OH (30мл) і екстрагують етилацетатом (3´150мл). Органічні екстракти сушать над безводним сульфатом магнію, фільтрують і концентрують у вакуумі з отриманням вказаної в заголовку сполуки у вигляді білої твердої речовини (24,8г, 0,10моль, 73%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 1,62 (уш.с, 3Н), 2,81 (дд, 1Н), 2,99 (д, 1Н), 4,61 (кв, 1Н), 5,07 (с, 2Н), 6,95 (д, 2Н), 7,22-7,45 (м, 7Н). LRMS: m/z 244 (М-H+). Приклад 25 N-[2-(4-бензилоксифеніл)-2-гідроксіетил)пропіонамід Амін прикладу 24 (24,8г, 0,10моль) розчиняють в дихлорметані (700мл) і додають триетиламін (20,86мл, 0,15моль). Реакційну суміш перемішують і охолоджують до 0°С перед доданням по краплях пропіонілхлориду (7,12мл, 0,082моль). Потім реакційній суміші дають можливість нагрітися до кімнатної температури протягом 16год. перед гасінням 3М НСI (водн.) (20мл) і водою (100мл). Потім реакційну суміш екстрагують дихлорметаном (3´200мл) і об'єднані органічні шари сушать над безводним сульфатом магнію, фільтрують і концентрують у вакуумі з отриманням сполуки у вигляді прозорої в'язкої смоли (27,5г, 0,092моль, 90%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 1,10 (т, 3Н), 2,19 (кв, 2Н), 3,32-3,43 (м, 4Н), 4,81 (с, 2Н), 5,11 (м, 1Н), 6,99 (д, 2Н), 7,25-7,42 (м, 7Н). LRMS: m/z 298 (М-H-). Приклад 26 1-(4-бензилоксифеніл)-2-пропіламіноетанол До аміду прикладу 25 (27,5г, 0,092моль) в сухому ТГФ (10мл) додають комплекс боран-метилсульфід (17,5мл, 0,18моль). Реакційну суміш охолоджують і потім реакцію гасять метанолом (3мл). Додають воду (50мл) і конц. НСI (35мл) і реакційну суміш перемішують доти, поки не припиниться виділення пухирців, потім концентрують у вакуумі. До залишку додають воду (250мл) і потім додають основні властивості додаванням NH4OH (30мл). Водний шар екстрагують етилацетатом (3´200мл і об'єднані органічні екстракти сушать над безводним сульфатом магнію, фільтрують і концентрують у вакуумі з отриманням вказаної в заголовку сполуки у вигляді білої твердої речовини (26,1г, 0,09моль, 99%). 1 Н ЯМР (CD3OD, 400МГц) d: 0,95 (т, 3Н), 1,58 (кв, 2Н), 2,6; (м, 2Н), 2,81 (м, 2Н), 4,72 (дд, 1Н), 5,05 (с, 2Н), 6,95 (д, 2Н), 7,24 (м, 3Н), 7,35 (т, 2Н), 7,41 (д, 2Н). LRMS: m/z 286 (М-Н+). Приклад 27 6-(4-бензилоксифеніл)-4-пропілморфолін-3-он Гідроксид натрію (22,5г, 0,56моль) у воді (100мл) додають до аміну прикладу 26 (26,0г, 0,09моль) в дихлорметані (400мл) і розчин енергійно перемішують при кімнатній температурі. Потім додають хлорацетилхлорид (8,6мл, 0,11моль) і реакційну суміш перемішують протягом ще 60хв. Шари розділяють і водний шар повторно екстрагують дихлорметаном (200мл). Органічні екстракти об'єднують, сушать над безводним сульфатом магнію, фільтрують і концентрують у вакуумі з отриманням безбарвного масла. Гідроксид калію (15,0г, 0,27моль), ізопропіловий спирт (400мл) і залишок безбарвного масла перемішують разом у вигляді каламутного розчину з водою (30мл) протягом 2год. Реакційну суміш концентрують у вакуумі і жовтий залишок розчиняють в етилацетаті (200мл). Його розділяють водою (200мл), потім насиченим розчином солі (200мл). Органічну фракцію сушать над безводним сульфатом магнію, фільтрують і концентрують у вакуумі з отриманням вказаної в заголовку сполуки у вигляді білої твердої речовини (19,9г, 0,06моль, 67%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 0,95 (т, 3Н), 1,62 (м, 2Н), 3,34 (м, 2Н), 3,51 (м, 2Н), 4,32 (д, 1Н), 4,41 (д, 1Н), 4,72 (дд, 1Н), 5,04 (с, 2Н), 6,98 (д, 2Н), 7,31-7,43 (м, 7Н). LRMS: m/z 326 (М-Н+). Приклад 28 2-(4-бензилоксифеніл)-4-пропілморфолін Отримують, відповідно до аналогічної методики прикладу 26, з використанням морфолін-3-ону прикладу 27 (19,9г, 0,061моль), з отриманням вказаної в заголовку сполуки у вигляді безбарвного масла (17г, 0,055моль, 90%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 0,95 (т, ЗН), 1,55 (кв, 2Н), 2,06 (т, 1Н), 2,21 (дт, 1Н), 2,35 (дд, 2Н), 2,80 (д, 1Н), 2,91 (д, 1Н), 3,82 (дт, 1Н), 4,02 (дд, 1Н), 4,52 (дд, 1Н), 5,05 (с, 2Н), 6,98 (т, 2Н), 7,24-7,42 (м, 7Н). LRMS: m/z 312 (М-Н+). Приклад 29 4-(4-пропілморфолін-2-іл)фенол Простий бензиловий ефір прикладу 28 (3,0г, 9,64ммоль) розчиняють в метанолі (150мл) і додають 10% паладій на активованому вугіллі (800мг). Реакційну суміш перемішують протягом декількох хвилин перед додаванням порціями форміату амонію (6,17г, 96,4ммоль). Реакційну суміш обережно нагрівають до 80°С доти, поки не припиниться виділення газу. Після охолоджування реакційну суміш фільтрують через арбацел, промивають метанолом (50мл) і концентрують у вакуумі з отриманням вказаної в заголовку сполуки у вигляді білої кристалічної твердої речовини (1,51г, 6,83ммоль, 71%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 0,91 (т, 3Н), 1,58 (кв, 2Н), 2,10 (τ, 1Η), 2,22 (τ, 1Η), 2,40 (дд, 2Н), 2,81 (д, 1Н), 2,93 (д, 1Н), 3,85 (т, 1Н), 4,02 (дд, 1Н), 4,57 (д, 1Н), 6,79 (д, 2Н), 7,21 (д, 2Н). LRMS: m/z 222 (М-Н+). Приклад 30 2-бром-4-(4-пропілморфолін-2-іл)фенол До фенолу прикладу 29 (200мл, 0,9ммоль) в дихлорметані (5мл) додають N-бромсукцинімід (161мг, 0,9ммоль). Реакційну суміш перемішують при кімнатній температурі протягом 55год. перед концентруванням у вакуумі. Неочищений продукт очищають колонковою хроматографією на діоксиді кремнію, елююючи сумішшю дихлорметан:метанол (95:5), з отриманням вказаної в заголовку сполуки у вигляді білої піни (117,5мг, 0,39ммоль, 44%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 0,96 (т, 3Н), 1,59 (кв, 2Н), 2,03 (т, 1Н), 2,23 (т, 1Н), 2,40 (т, 2Н), 2,81 (д, 1Н), 2,98 (д, 1Н), 3,82 (т, 1Н), 4,01 (д, 1Н), 4,56 (д, 1Н), 6,96 (д, 1Н), 7,20 (д, 1Н), 7,49 (с, 1Н). LRMS: m/z 302 (МН+, Вr ізотоп). Приклад 31 2-(4-бензилокси-3-бромфеніл)-4-пропілморфолін До фенолу прикладу 30 (117,5мг, 0,39моль) в сухому ДМФА (10мл) в атмосфері азоту додають карбонат калію (75мг, 0,54ммоль) і бензилброміду (0,07мл, 0,54ммоль). Реакційну суміш нагрівають до 150°С протягом 48год. Після охолоджування реакційну суміш концентрують у вакуумі і залишок розподіляють між етилацетатом (50мл) і водою (50мл). Водний шар потім повторно екстрагують етилацетатом (2´20мл). Потім об'єднані органічні екстракти сушать над безводним сульфатом магнію, фільтрують і концентрують у вакуумі з отриманням неочищеного продукту у вигляді коричневого масла. Масло очищають колонковою хроматографією на діоксиді кремнію, елююючи сумішшю дихлорметан:метанол (98:2), з отриманням вказаної в заголовку сполуки у вигляді безбарвного масла (153мг, 0,39ммоль, 100%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 0,93 (т, 3Н), 1,56 (кв, 2Н), 2,05 (т, 1Н), 2,25 (т, 1Н), 2,37 (т, 2Н), 2,82 (д, 1Н), 2,92 (д, 1Н), 3,85 (т, 1Н), 4,02 (д, 1Н), 4,52 (д, 1Н), 5,15 (с, 2Н), 6,87 (д, 1Н), 7,20 (д, 1Н), 7,30 (д, 1Н), 7,37 (т, 2Н), 7,45 (д, 2Н), 7,58 (с, 1Н). LRMS: m/z 392 (М-Н+). Приклад 32 Метиловий ефір 2-бензилокси-5-(4-пропілморфолін-2-іл)бензойної кислоти До броміду прикладу 31 (153мг, 0,39ммоль) в сухому ДМФА (4мл) додають триетиламін (2,1мл, 0,78ммоль) і метанол (2мл) і реакційну суміш перемішують протягом 5хв. Комплекс [1,1'біс(дифенілфосфін)фероцен]дихлорпаладію (II) і дихлорметану (1:1) (16мг, 0,02ммоль) додають перед барботуванням монооксиду вуглецю (газ) (3 заповнених балона) через реакційну суміш. Потім реакційну суміш нагрівають до 100°С протягом 16год. в атмосфері монооксиду вуглецю. Після охолоджування реакційну суміш концентрують у вакуумі і залишок розподіляють між етилацетатом (25мл) і водою (20мл). Органічний шар відділяють, промивають насиченим розчином солі (20мл) і сушать над безводним сульфатом магнію, фільтрують і концентрують у вакуумі з отриманням чорної твердої речовини. Очищення колонковою хроматографією на діоксиді кремнію при елююванні сумішшю дихлорметан:метанол:аміак (90:10:1) дає вказану в заголовку сполуку у вигляді безбарвного масла (105мг, 0,28ммоль, 73%). 1 Н ЯМР (СDСІ 3, 400МГц) d: 0,94 (т, 3Н), 1,60 (м, 2Н), 2, 18 (с, 4Н), 2,43 (м, 2Н), 3,00 (м, 2Н), 3,90 (с, 3Н), 4,04 (д, 1Н), 5,18 (с, 2Н), 5,97 (д, 1Н), 7,26-7,47 (м, 6Н), 7,82 (с, 1Н). LRMS: m/z 370 (М-Н+). Приклад 33 2-бензилокси-5-(4-пропілморфолін-2-іл)бензойна кислота
ДивитисяДодаткова інформація
Назва патенту англійськоюMorpholine derivatives as dopamine agonists for treating sexual dysfunction
Назва патенту російськоюПроизводные морфолина в качестве агонистов допамина для лечения половой дисфункции
МПК / Мітки
МПК: A61P 15/00, C07D 413/04, C07D 265/30
Мітки: лікуванні, агоністів, допаміну, дисфункції, застосування, статевої, похідні, морфоліну
Код посилання
<a href="https://ua.patents.su/41-79024-pokhidni-morfolinu-dlya-zastosuvannya-yak-agonistiv-dopaminu-pri-likuvanni-statevo-disfunkci.html" target="_blank" rel="follow" title="База патентів України">Похідні морфоліну для застосування як агоністів допаміну при лікуванні статевої дисфункції</a>
Попередній патент: Похідні індолінфенілсульфонаміду
Випадковий патент: Лікування шийного і грудного остеохондрозу хребта з неврологічними проявами способом інтегративної кінезітерапії