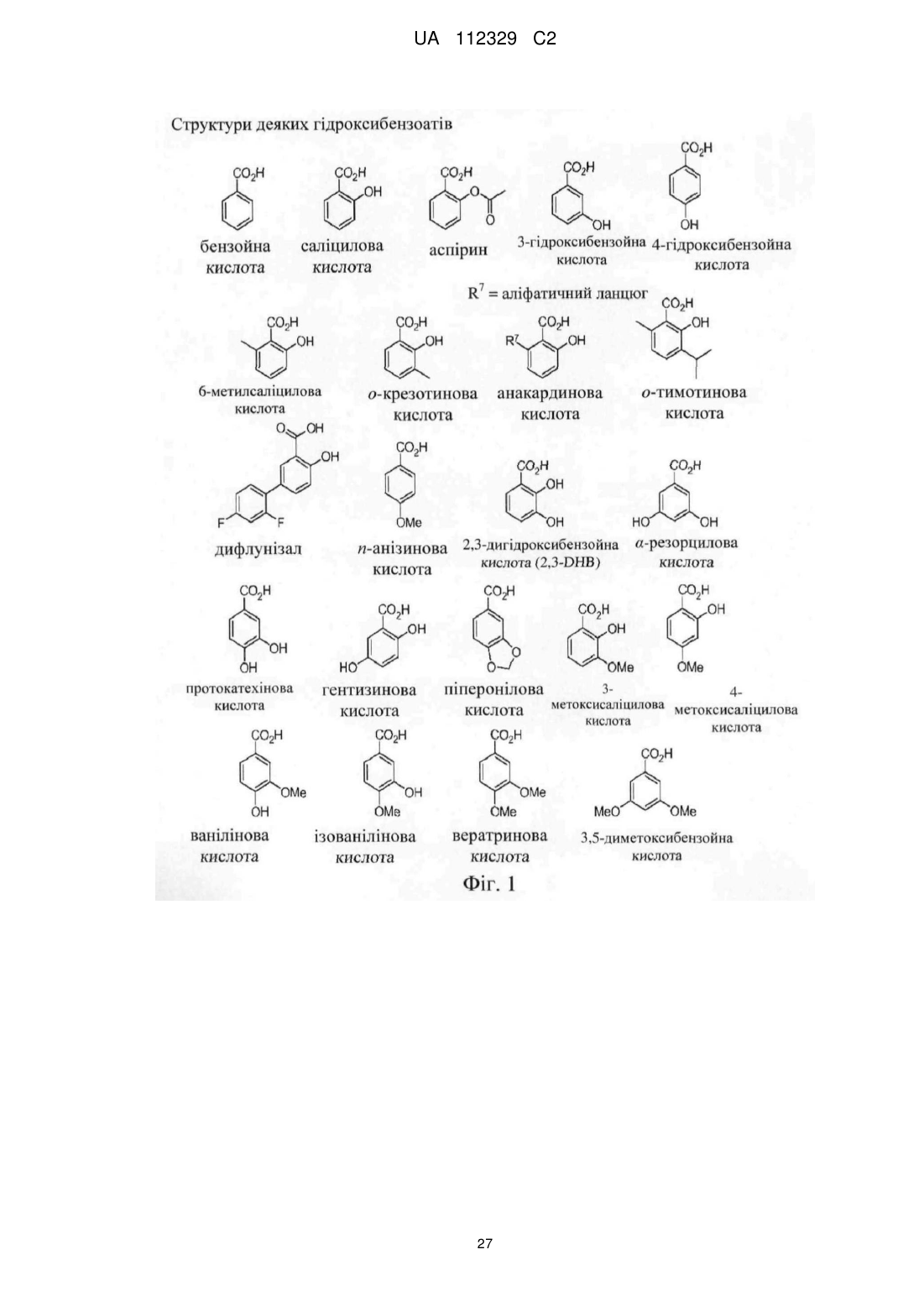
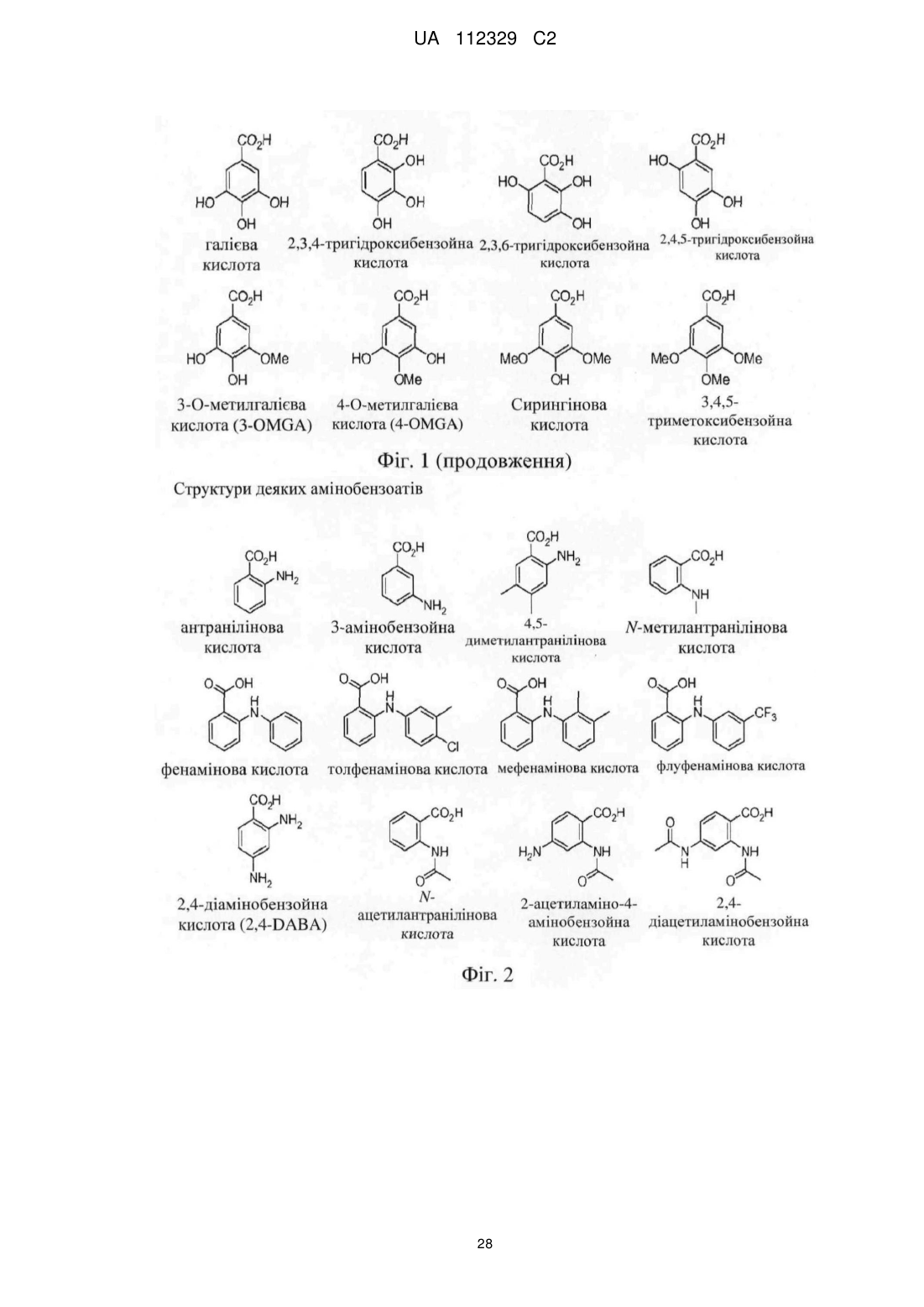
Композиція проліків, що містить кон’югат аспірину з гідроморфоном, та спосіб лікування захворювання
Номер патенту: 112329
Опубліковано: 25.08.2016
Автори: Бера Бінду, Чі Гочень, Гюнтер Свен, Мартін Андреа К., Каньскі Ярослав, Мікл Тревіс
Формула / Реферат
1. Композиція проліків, яка містить щонайменше один кон'югат, де щонайменше одним кон'югатом є 3,6-діаспірингідроморфон.
2. Композиція проліків за п. 1, де щонайменше один кон'югат застосовують для лікування наркотичного або опіоїдного зловживання; для запобігання наркотичній або опіоїдній відміні; для лікування від помірного до гострого болю; для зниження або запобігання пероральній, інтраназальній або внутрішньовенній лікарській залежності або для отримання стійкості до пероральної, інтраназальної або внутрішньовенної лікарської залежності.
3. Композиція проліків за п. 1, де пероральне введення щонайменше одного кон'югата дає поліпшену ППК і швидкість виділення протягом часу в порівнянні з некон'югованим гідроморфоном протягом одного і того ж періоду часу.
4. Композиція проліків за п. 1, де пероральне введення щонайменше одного кон'югата дає меншу варіабельність в пероральному профілі ФК в порівнянні з некон'югованим гідроморфоном.
5. Композиція проліків за п. 1, де пероральне введення щонайменше одного кон'югата викликає менші побічні ефекти в порівнянні з некон'югованим гідроморфоном.
6. Композиція проліків за п. 5, де зниженим побічним ефектом є знижена викликана опіоїдом констипація.
7. Композиція проліків за п. 1, де щонайменше один кон'югат представлений в лікарській формі, вибраній з групи, яка включає таблетки, капсули, каплети, супозиторії, пастилки, таблетки для розсмоктування, пероральний порошок, розчин, пероральну плівку, тонку смужку, завись і суспензію.
8. Композиція проліків за п. 1, де пероральне введення щонайменше одного кон'югата дає терапевтично біоеквівалентну ППК і/або біоеквівалентний або більш низький Сmах в порівнянні з еквівалентною молярною кількістю некон'югованого гідроморфону.
9. Композиція проліків за п. 1, де інтраназальне або внутрішньовенне введення щонайменше одного кон'югата дає більш низьку ППК і/або Сmах в порівнянні з еквівалентною молярною кількістю некон'югованого гідроморфону.
10. Композиція проліків за п. 1, де пероральне введення щонайменше одного кон'югата забезпечує знижену можливість передозування в порівнянні з еквівалентною молярною кількістю некон'югованого гідроморфону.
11. Композиція проліків за п. 1, де щонайменше один кон'югат забезпечує підвищену стійкість до втручання в порівнянні з некон'югованим гідроморфоном.
12. Спосіб лікування пацієнта, який страждає на захворювання, розлад або стан, опосередкований зв'язуванням опіоїду з рецепторами опіоїду пацієнта, що включає пероральне введення пацієнту фармацевтично ефективної кількості композиції проліків, яка містить щонайменше один кон'югат за п. 1.
Текст
Реферат: Даний винахід стосується композицій, які містять арилкарбонові кислоти, хімічно кон'юговані з гідроморфоном (4,5--епокси-3-гідрокси-17-метилморфінан-6-оном) з отриманням нових проліків/композицій гідроморфону. Проліки гідроморфону відповідно до даного винаходу викликають знижені побічні ефекти і знижений потенціал до виникнення залежності в порівнянні з некон'югованим гідроморфоном. У даному винаході також представлені способи лікування пацієнтів, фармацевтичні набори і способи синтезу кон'югатів відповідно до даного винаходу. UA 112329 C2 (12) UA 112329 C2 UA 112329 C2 5 10 15 20 25 30 35 40 45 50 55 60 Споріднені заявки У даній заявці заявлений пріоритет по попередній заявці на патент США № 61/551,600, поданій 26 жовтня 2011 року, озаглавленій "Бензойна кислота, похідні бензойної кислоти і кон'югати гетероарилкарбонової кислоти з гідроморфоном, їх проліки, способи отримання і застосування", ідентифікованій патентним реєстром № 24553US01 в юридичному бюро McAndrews, Held and Malloy, Ltd., і по попередній заявці на патент США № 61/657,201, поданій 8 липня 2012 року, озаглавленій "Бензойна кислота, похідні бензойної кислоти і кон'югати гетероарилкарбонової кислоти з гідроморфоном, їх проліки, способи отримання і застосування", ідентифікованій патентним реєстром № 24553US03 в юридичному бюро McAndrews, Held and Malloy, Ltd., опис яких включений сюди як посилання повністю. Дослідження і розробки, які фінансуються з федерального бюджету [не застосовується] Мікрофіша/авторське право [не застосовується] Рівень техніки Опіоїди є високо ефективними анальгетиками і їх часто призначають для лікування гострого і хронічного болю. Їх також часто застосовують як протикашльові засоби. Опіоїди, однак, також викликають ейфорію і/або "ефект схильності до лікарського препарату" і можуть викликати сильну залежність. У результаті вони часто викликають залежність з соціальними і пов'язаними зі здоров'ям наслідками. Через властиву їм тенденцію до викликання залежності, бажано, щоб будь-які фармацевтичні композиції, що містять опіоїдний агоніст, були настільки резистентними до залежності або стримуючими залежність, наскільки це можливо на практиці. Злочинці часто роблять спроби вдихати, вводити ін'єкцією або іншим чином незаконно використовувати продукт для досягнення більш сильного або негайного ефекту від опіоїдного агоніста. Незважаючи на те, що вони можуть спричиняти звикання і, потенційно, наркотичну залежність, морфіноподібні лікарські засоби, особливо, кодеїн, гідрокодон, гідроморфон і оксикодон звичайно призначають для лікування тяжкого, гострого і хронічного болю протягом десятиріч. Зокрема через те, що в цей час немає кращої альтернативи для полегшення сильного болю, який не піддається іншим, менш сильним знеболюючим засобам, таким як нестероїдні протизапальні лікарські засоби (НПЗЛЗ). У зв'язку з цим існує необхідність в зниженні потенційної залежності до опіоїдних знеболюючих засобів. На сьогоднішній день робилося декілька спроб, які, на жаль, не вирішили проблему. Гідроморфон (4,5-α-епокси-3-гідрокси-17-метилморфінан-6-он) є гідрованим кетоном морфіну, який застосовують як опіоїдний анальгетик центральної дії і протикашльовий засіб. Гідроморфон є напівсинтетичним наркотичним анальгетиком, що отримується з морфіну, який має велику кількість дій, якісно схожих на дію морфіну, і його застосовують в медицині як альтернативу морфіну. Його в основному застосовують для полегшення болю і як наркотичний протикашльовий засіб у випадку сухого, викликаючого біль кашлю. Гідроморфон взаємодіє переважно з опіоїдними рецепторами в центральній нервовій системі (ЦНС). Його знеболюючі властивості переважно основані на агоністичній дії на μ-опіоїдний рецептор. Гідроморфон також є частковим агоністом δ-опіоїдного рецептора і агоністом κ-опіоїдного рецептора. Додатково, гідроморфон має протикашльові властивостями, які придушують кашльовий рефлекс в медулярному кашльовому центрі мозку. Пацієнти, що приймають опіоїдні знеболюючі засоби, такі як гідроморфон, для полегшення болю і/або кашлю, можуть ненавмисно стати залежними від них. При розвитку толерантності до опіоїдів, вищі кількості лікарського засобу стають необхідними для полегшення симптомів і створення почуття стану, який спочатку досягався з призначеною дозою. Це веде до збільшення дози, яке, при відсутності контролю, може швидко привести до виникнення залежності. У деяких випадках пацієнти отримують залежність менше ніж за тридцять днів. Викликана опіоїдом констипація (ВОК) є частим побічним ефектом лікування болю опіоїдами. Він виникає у приблизно 40-90 % пацієнтів, які постійно отримують опіоїдні лікарські засоби. Крім того, пацієнти, які страждають на ВОК, можуть стати резистентними до проносних засобів. Хоча механізм ще до кінця не зрозумілий, вважають, що зв'язування агоністів з периферійними μ-опіоїдними рецепторами в шлунково-кишковому тракті (ШКТ) є першопричиною ВОК. Активація цього опіоїдного рецептора погіршує координацію функції ШКТ ентеричною частиною вегетативної нервової системи (ЕЧВНС), що знижує перистальтику кишечника через затримку часу проходження фекалій при взаємодії з нормальним тонусом і скорочуваністю товстого кишечника. У той час як скорочення кругового шару м'язової оболонки посилюються, спричиняючи не пропульсивне розминання і просування (застій) і підвищену 1 UA 112329 C2 5 10 15 20 25 30 35 40 45 50 55 абсорбцію рідини, тонус подовжніх гладких м'язів знижується, викликаючи знижену просуваючу уперед перистальтику і додатковий час для зневоднення фекалій. Більше того, тонус анального сфінктера підвищується, що ще більше утруднює дефекацію. Клінічний прояв цих ефектів звичайно виражається у вигляді симптомів тяжкого/сухого випорожнення, напружування, неповного випорожнення, здуття і збільшення розмірів живота. Короткий опис винаходу У представленій методиці застосовується кон'югація опіоїду гідроморфону з певними арилкарбоновими кислотами для зниження потенційного передозування або залежності, яка досягається необхідністю виділення активного гідроморфону через ферментне або метаболічне розщеплення кон'югата in vivo. Дана методика також представляє способи доставки гідроморфону у вигляді кон'югатів, які вивільняють гідроморфон після перорального введення, одночасно будучи резистентними до звикання при введенні обхідними шляхами, такими як внутрішньовенна ін'єкція ("вколювання") і інтраназальне введення ("нюхання"). Переваги певних варіантів гідроморфонових проліків відповідно до даної методики включають, але не обмежені ними, зниження потенційного звикання, зниження або виключення викликаної опіоїдом констипації (ВОК), зниження ризику хімічного або фізичного маніпулювання, що дає повну дозу гідроморфону, який виділяється, зниження зміни концентрації в плазмі у різних пацієнтів в порівнянні із звичайним гідроморфоном, поліпшені лікарські форми внаслідок модифікації фізичних і хімічних властивостей і поліпшений профіль побічних ефектів через знижене перетворення гідроморфонових проліки до небажаного гідроморфон-3-глюкуроніду. У деяких аспектах в даній методиці представлені композиції для негайного виділення кон'югованого гідроморфону, що дозволяє доставку гідроморфону в кровоносну систему людини або тварини терапевтично біоеквівалентним методом при пероральному введенні. У щонайменше одному аспекті, композиції/склади даної методики можуть зменшити звичайні побічні ефекти, характерні для некон'югованого гідроморфону і подібних сполук. Описана методика в щонайменше одному аспекті забезпечує повільне/сповільнююче/контролююче виділення композиції кон'югованого гідроморфону, яке забезпечує повільну/сповільнюючу/контролюючу доставку гідроморфону в кровоносну систему людини або тварини з безпечним терапевтичним вікном при, наприклад, пероральному введенні. Принаймні деякі композиції/склади даної методики можуть знизити потенціал до звикання/залежності, характерний для некон'югованого гідроморфону і подібних сполук. У додаткових аспектах в даній методиці застосовують кон'югацію природних не токсичних лігандів з гідроморфоном для створення нового класу проліків. Проліки відповідно до даної методики можуть легко розпізнаватися метаболічними системами і гідролізуються з виділенням активного опіоїду контрольованим чином при пероральному введенні. Інші шляхи введення є для сполук відповідно до даного винаходу не ефективними або менш ефективними, що дозволяє запобігти або знизити звикання до лікарського засобу. Додаткові способи звикання до лікарського засобу також усуваються через резистентність до фізичних змін і запобігання або зниження ейфорії при проковтуванні високих доз проліків відповідно до даного винаходу. Залежно від вибору ліганду, профілі фармакокінетики (ФК) гідроморфону, що вивільняється з проліків відповідно до даного винаходу, можуть бути змінені для оптимізації рівнів в крові з плином часу для конкретних показань і для поліпшення профілю безпеки. Крім того, при виборі відповідних лігандів проліки відповідно до даного винаходу можуть доставляти гідроморфон в системний кровотік без взаємодії з опіоїдними рецепторами в ентеричній частині вегетативної нервової системи, тим самим знижуючи або запобігаючи викликану опіоїдом констипацію (ВОК). У іншому аспекті, в даній методиці представлені арилкарбонові кислоти, хімічно приєднані до гідроморфону для отримання проліків, які можуть виділяти активний опіоїд. Проліки відповідно до даного винаходу не мають значної знеболюючої дії і при виборі відповідних лігандів значно знижують кількості гідроморфону, виділені в системний кровотік при введенні інтраназально або внутрішньовенно. Більше того, наркотик не може бути "екстрагований" з проліків відповідно до даного винаходу простим фізичним пошкодженням через природу ковалентного зв'язку енольного ефіру і/або фенольного ефіру між гідроморфоном і арилкарбоновою кислотою. Такий клас сполук відповідно до даного винаходу може бути менш привабливим для потенційно наркозалежних людей, ніж традиційні лікарські форми, і можуть мати поліпшений профіль безпеки і знижену кількість побічних ефектів. Крім того, при виборі відповідних лігандів всі або більшість неактивних проліків відповідно до даного винаходу можуть переносити прохід через шлунково-кишковий тракт (ШКТ) доти, поки вони не абсорбуються, тим самим запобігаючи взаємодії гідроморфону з опіоїдними рецепторами в ентеричній частині вегетативної нервової системи. Така відсутність зв'язування з 2 UA 112329 C2 5 10 15 20 25 30 35 40 периферійними опіоїдними рецепторами може значно знизити або навіть запобігти викликаній опіоїдом констипації. У щонайменше одному аспекті, в даному винаході представлена щонайменше одна композиція проліків, що містить щонайменше один кон'югат, де кон'югат містить щонайменше один гідроморфон, і щонайменше одну арилкарбонову кислоту. У іншому аспекті, в даному винаході представлена щонайменше одна композиція проліків гідроморфону, що містить арилкарбонову кислоту, хімічно зв'язану з гідроморфоном взаємодією групи карбонової кислоти арилкарбонової кислоти з С-6 енольним таутомером гідроморфону. У іншому аспекті, в даному винаході представлені щонайменше одні проліки, що містять щонайменше один гідроморфон, хімічно зв'язаний з щонайменше однією арилкарбоновою кислотою через взаємодію групи карбонової кислоти арилкарбонової кислоти з С-3 гідроксилом гідроморфону. У іншому аспекті, в даному винаході представлені проліки, які містять щонайменше один гідроморфон, хімічно зв'язаний з щонайменше однією арилкарбоновою кислотою через взаємодію групи карбонової кислоти арилкарбонової кислоти з С-6 енольним таутомером гідроморфону і взаємодію щонайменше однієї арилкарбонової кислоти з С-3 гідроксилом гідроморфону. У інших аспектах, в даному винаході представлені щонайменше одні проліки з щонайменше однією арилкарбоновою кислотою, що містить карбоксильну групу, приєднану безпосередньо до щонайменше однієї арильної групи. У іншому аспекті, в даному винаході представлені щонайменше одні проліки з щонайменше одним гідроморфоном, хімічно приєднаним до щонайменше одного бензоату загальної формули I: , 1 2 3 де R , R і R незалежно вибирають з групи, яка включає водень, гідроксил, аміно, амін, амід, тіол, ціано, нітро, галоген, імін, алкіл, алкокси, арил, алкеніл, алкініл, галогеналкіл, алкіларил, арилалкіл, гетероцикл, арилалкокси, циклоалкіл, циклоалкеніл, циклоалкініл, карбоніл, тіоефір, селеноефір, силіл, силілокси, сульфоніл, фосфонат. У щонайменше одному аспекті даного винаходу представлені проліки гідроморфону з щонайменше однією арилкарбоновою кислотою, що містить карбоксильну групу, яка сполучена одним карбоновим містком з арильною групою. У іншому аспекті, в даному винаході представлені щонайменше одні проліки гідроморфону, хімічно приєднані до щонайменше одного фенілацетату наступної загальної формули II: , 1 2 3 4 де R , R , R і R незалежно вибирають з групи, яка включає водень, гідроксил, аміно, амін, амід, тіол, ціано, нітро, галоген, імін, алкіл, алкокси, арил, алкеніл, алкініл, галогеналкіл, алкіларил, арилалкіл, гетероцикл, арилалкокси, циклоалкіл, циклоалкеніл, циклоалкініл, карбоніл, тіоефір, селеноефір, силіл, силілокси, сульфоніл, фосфонат. У інших аспектах, в даному винаході представлені проліки гідроморфону, що містять щонайменше одну арилкарбонову кислоту, що містить карбоксильну групу, яка сполучена двома вуглецевими містками з арильною групою. У додаткових аспектах в даному винаході представлені композиції проліків гідроморфону, що містять бензилацетати і цинамати, що мають наступну загальну формулу III або IV або їх поєднання: 3 UA 112329 C2 5 10 15 20 25 , 1 2 3 4 де R , R , R і R незалежно вибирають з групи, яка включає водень, гідроксил, аміно, амін, амід, тіол, ціано, нітро, галоген, імін, алкіл, алкокси, арил, алкеніл, алкініл, галогеналкіл, алкіларил, арилалкіл, гетероцикл, арилалкокси, циклоалкіл, циклоалкеніл, циклоалкініл, карбоніл, тіоефір, селеноефір, силіл, силілокси, сульфоніл, фосфонат. У інших аспектах, проліки гідроморфону відповідно до даного винаходу включають щонайменше одну арилкарбонову кислоту, що містить карбоксильну групу, приєднану до арильної групи алкільним ланцюгом. У інших аспектах, проліки гідроморфону відповідно до даного винаходу включають щонайменше одну арилкарбонову кислоту, що містить карбоксильну групу, приєднану до арильної групи алкенільним ланцюгом. У додаткових аспектах, проліки гідроморфону відповідно до даного винаходу містять щонайменше одну арилкарбонову кислоту, яка містить вуглецевий ланцюг між арильним кільцем і карбоксильну групу з одним або більше бічними ланцюгами. У додаткових аспектах, проліки гідроморфону відповідно до даного винаходу містять щонайменше одну арилкарбонову кислоту, яка містить одну або більше функціональних груп в доповнення до щонайменше однієї карбоксильної групи. У інших аспектах, проліки гідроморфону відповідно до даного винаходу містять щонайменше одну арилкарбонову кислоту, яка містить щонайменше одну гетероарилкарбонову кислоту. У додаткових аспектах, в даному винаході представлені композиції проліків гідроморфону, що містять гетероарилкарбонову кислоту наступної загальної формули V, VI, VII, VIII, IX, X, XI, XII або XIII або їх поєднання: , 1 2 3 де R , R і R незалежно вибирають з групи, яка включає водень, гідроксил, аміно, амін, амід, тіол, ціано, нітро, галоген, імін, алкіл, алкокси, арил, алкеніл, алкініл, галогеналкіл, 4 UA 112329 C2 5 10 15 20 25 30 35 40 45 50 55 алкіларил, арилалкіл, гетероцикл, арилалкокси, циклоалкіл, циклоалкеніл, циклоалкініл, карбоніл, тіоефір, селеноефір, силіл, силілокси, сульфоніл, фосфонат. У інших аспектах, в даному винаході представлені щонайменше одні проліки гідроморфону, які містять арилкарбонову кислоту, що містить шестичленне кільце. У інших аспектах, в даному винаході представлені щонайменше одні проліки гідроморфону, які містять арилкарбонову кислоту, що містить тільки одну вільну групу карбонової кислоти. У додаткових аспектах, в даному винаході представлені щонайменше одні проліки гідроморфону, які містять арилкарбонову кислоту, що містить від 1 до 4 фенільних замісників. У певних аспектах, в даному винаході представлений щонайменше один кон'югат проліків гідроморфону, які є нейтральними проліками. У певних аспектах, в даному винаході представлений щонайменше один кон'югат проліків гідроморфону, які є вільною кислотою. У певних аспектах, в даному винаході представлений щонайменше один кон'югат проліків гідроморфону, які є вільною основою. У додаткових аспектах, в даному винаході представлений щонайменше один кон'югат проліків гідроморфону, які є фармацевтично прийнятною аніонною або катіонною сольовою формою або сумішшю солей. У певних аспектах, композиції проліків гідроморфону відповідно до даного винаходу руйнуються in vivo, виділяючи активний гідроморфон і арилкарбонову кислоту або її похідні або метаболіти. У певних аспектах, композиції проліків гідроморфону відповідно до даного винаходу вводять перорально і вони гідролізуються in vivo, виділяючи гідроморфон з проліків. У інших аспектах, композиції проліків гідроморфону відповідно до даного винаходу демонструють відсутність або незначну фармакологічну дію при введенні. У інших аспектах, композиції проліків гідроморфону відповідно до даного винаходу таким чином виділяють гідроморфон, який аналогічний вільному або немодифікованому гідроморфону при введенні в еквімолярних дозах. У додаткових аспектах, композиції проліків гідроморфону відповідно до даного винаходу контролюють і обмежують виділення гідроморфону в системний кровотік, якщо проліки вводять шляхами, відмінними від перорального. У певних аспектах, композиції проліків гідроморфону відповідно до даного винаходу виділяють гідроморфон контрольованим або уповільненим чином при введенні. У інших аспектах, композиції проліків гідроморфону відповідно до даного винаходу демонструють відсутність або знижені побічні ефекти в порівнянні з немодифікованим гідроморфоном при введенні в еквімолярних дозах. У додаткових аспектах, введення композицій проліків гідроморфону відповідно до даного винаходу дає концентрації гідроморфону в плазмі або крові, які значно знижені в порівнянні з немодифікованим гідроморфоном при введенні в еквімолярних дозах при внутрішньовенному або інтраназальному введенні. У інших аспектах, введення композицій проліків гідроморфону відповідно до даного винаходу не викликає або викликає знижену ейфорію або наркотичну дію в порівнянні з немодифікованим гідроморфоном при інтраназальному або внутрішньовенному введенні в еквімолярних дозах. У деяких аспектах введення композицій проліків гідроморфону відповідно до даного винаходу не викликає швидкого піку концентрації гідроморфону (C max) в крові або плазмі при пероральному введенні. У інших аспектах, введення композицій проліків гідроморфону відповідно до даного винаходу дає уповільнений T max в порівнянні з немодифікованим гідроморфоном при пероральному введенні в еквімолярних дозах. У додаткових аспектах, введення композицій проліків гідроморфону відповідно до даного винаходу дає більш низьке значення Cmax в порівнянні з немодифікованим гідроморфоном при пероральному введенні в еквімолярних дозах. У інших аспектах, фізичні маніпуляції з композиціями проліків гідроморфону відповідно до даного винаходу не спричиняють вивільнення вільного гідроморфону. У інших аспектах, композицій проліків гідроморфону відповідно до даного винаходу демонструють резистентність до певних хімічних маніпуляцій, призначених для вивільнення вільного гідроморфону. У інших аспектах, введення композицій проліків гідроморфону відповідно до даного винаходу не викликає або не дає незначну активність на μ-опіоїдних рецепторах. 5 UA 112329 C2 5 10 15 20 25 30 35 40 45 50 55 60 У інших аспектах, композиції проліків гідроморфону відповідно до даного винаходу не схильні або обмежено схильні до ферментного гідролізу до абсорбції в кишечнику. У інших аспектах, композиції проліків гідроморфону відповідно до даного винаходу демонструють знижене перетворення в гідроморфон-3-глюкуронід (H3G) в порівнянні з немодифікованим гідроморфоном при пероральному введенні в еквімолярних дозах. У інших аспектах, композиції проліків гідроморфону відповідно до даного винаходу запобігають або знижують викликану опіоїдом констипацію (ВОК) в порівнянні з немодифікованим гідроморфоном при пероральному введенні в еквімолярних дозах. У інших аспектах, композиції проліків гідроморфону відповідно до даного винаходу містять додаткові активні фармацевтичні інгредієнти (АФІ), включаючи, наприклад, ібупрофен, ацетамінофен або аспірин. У певних аспектах, композиціями проліків гідроморфону відповідно до даного винаходу можуть бути 3-аспірин-гідроморфон, 3,6-ді-аспірин-гідроморфон, 6-o-саліцилат-гідроморфон, 3цинамат-гідроморфон, 6-напроксен-гідроморфон, 3-ізоніацин-гідроморфон, 3-п-саліциловийгідроморфон, 3-фенамат-гідроморфон, 3-бензоат-гідроморфон і 3,6-ди-бензоат-гідроморфон. У інших аспектах, композиції проліків гідроморфону відповідно до даного винаходу мають пероральну лікарську форму. У деяких аспектах, пероральні лікарські форми відповідно до даного винаходу є твердими лікарськими формами. У додаткових аспектах, наповнювачами відповідно до даного винаходу є антиадгезиви, зв'язувальні агенти, покриття, розпушувачі, наповнювачі, смакові добавки, барвники, гліданти, мастильні агенти, консерванти, сорбенти і підсолоджувачі. У додаткових аспектах, композиції проліків гідроморфону відповідно до даного винаходу представлені у вигляді таблеток, капсул, м'яких желатинових капсул, капсул з модифікованим вивільненням, таблеток з уповільненим вивільненням, капсул з контрольованим вивільненням, супозиторіїв, порошків для ін'єкцій, пероральних рідин, сиропів від кашлю, черезшкірної плівки, пероральної тонкої плівки, суспензії або ін'єкції. У певних аспектах, композиції проліків гідроморфону відповідно до даного винаходу представлені з ефективністю пероральної лікарської форми, яка еквімолярна від близько 0,1 мг до близько 200 мг немодифікованого гідроморфону. У інших аспектах, в даному винаході представлений спосіб лікування пацієнта, якому необхідно знеболююча дія, введенням кількості щонайменше однієї композиції проліків гідроморфону відповідно до даного винаходу, яка терапевтично еквівалентна ефективній кількості некон'югованого гідроморфону. У інших аспектах, в даному винаході представлений спосіб синтезу композицій проліків гідроморфону відповідно до даного винаходу. У інших аспектах, в даному винаході представлений спосіб лікування пацієнта, який потребує знеболюючої дії, шляхом введення кількості 3-аспірин-гідроморфону, 3,6-ді-аспірингідроморфону, 6-саліцилат-гідроморфону, 3-цинамат-гідроморфону або 3-бензоатгідроморфону, яка терапевтично еквівалентна ефективній кількості некон'югованого гідроморфону. У додаткових аспектах, в даному винаході представлений фармацевтичний набір, що містить певну кількість окремих доз, що містять кількість щонайменше одного кон'югата, яка терапевтично еквівалентна ефективній кількості некон'югованого гідроморфону, де щонайменше один кон'югат містить щонайменше один гідроморфон і щонайменше одну арилкарбонову кислоту. Короткий опис декількох видів креслень Фігура 1. Приклад хімічних структур деяких гідроксибензоатів для застосування в отриманні композицій проліків гідроморфону відповідно до даного винаходу. Фігура 2. Приклад хімічних структур деяких амінобензоатів для застосування в отриманні композицій проліків гідроморфону відповідно до даного винаходу. Фігура 3. Приклад хімічних структур деяких аміногідроксибензоатів для застосування в отриманні композицій проліків гідроморфону відповідно до даного винаходу. Фігура 4. Приклад хімічних структур деяких гетероарилкарбонових кислот для застосування в отриманні композицій проліків гідроморфону відповідно до даного винаходу. Фігура 5. Приклад хімічних структур деяких фенілацетатів для застосування в отриманні композицій проліків гідроморфону відповідно до даного винаходу. Фігура 6. Приклад хімічних структур деяких бензилацетатів для застосування в отриманні композицій проліків гідроморфону відповідно до даного винаходу. Фігура 7. Приклад хімічних структур деяких цинаматів для застосування в отриманні композицій проліків гідроморфону відповідно до даного винаходу. 6 UA 112329 C2 5 10 15 20 25 30 35 40 45 50 55 60 Фігура 8. Фармакокінетичний профіль виділеного гідроморфону (ГМ) в плазмі щурів, яким дають перорально дози 3-аспірин-ГМ, 3,6-ді-аспірин-ГМ і ГМ, еквімолярні 2,0 мг/кг гідроморфону. Фігура 9. Фармакокінетичний профіль виділеного гідроморфону (ГМ) в плазмі щурів, яким дають перорально дози 6-o-саліцилат-ГМ і ГМ, еквімолярні 2,0 мг/кг гідроморфону. Фігура 10. Фармакокінетичний профіль виділеного гідроморфону (ГМ) в плазмі щурів, яким дають перорально дози 3-цинамат-ГМ і ГМ, еквімолярні 2,0 мг/кг гідроморфону. Фігура 11. Фармакокінетичний профіль виділеного гідроморфону (ГМ) в плазмі щурів, яким дають перорально дози 6-напроксен-ГМ і ГМ, еквімолярні 2,0 мг/кг гідроморфону. Фігура 12. Фармакокінетичний профіль виділеного гідроморфону (ГМ) в плазмі щурів, яким дають перорально дози 3-ізоніацин-ГМ і ГМ, еквімолярні 2,0 мг/кг гідроморфону. Фігура 13. Фармакокінетичний профіль виділеного гідроморфону (ГМ) в плазмі щурів, яким дають перорально дози 3-п-саліцилат-ГМ і ГМ, еквімолярні 2,0 мг/кг гідроморфону. Фігура 14. Фармакокінетичний профіль виділеного гідроморфону (ГМ) в плазмі щурів, яким дають перорально дози 3-фенамат-ГМ і ГМ, еквімолярні 2,0 мг/кг гідроморфону. Фігура 15. Фармакокінетичний профіль виділеного гідроморфону (ГМ) в плазмі щурів, яким дають перорально дози 3-бензоат-ГМ, 3,6-ди-бензоат-ГМ і ГМ, еквімолярні 2,0 мг/кг гідроморфону. Фігура 16. Фармакокінетичний профіль виділеного гідроморфону (ГМ) в плазмі щурів, яким дають перорально дози 3,6-ді-аспірин-ГМ і ГМ, еквімолярні 2,0 мг/кг гідроморфону. Фігура 17. Фармакокінетичний профіль виділеного гідроморфону (ГМ) в плазмі щурів, яким дають перорально дози 3,6-ді-аспірин-ГМ і ГМ, еквімолярні 2,0 мг/кг гідроморфону. Фігура 18. Площа під кривою (ППК) виділеного гідроморфону (ГМ) в плазмі щурів, яким дають перорально підвищені еквімолярні дози ГМ і 3,6-ді-аспірин-ГМ. Фігура 19. Площа під кривою (ППК) і пікові концентрації в плазмі (C max) в плазмі щурів, яким дають перорально еквімолярні дози ГМ, незмінений 3,6-ді-аспірин-ГМ і продукти гідролітичного розпаду 3,6-ді-аспірин-ГМ. Фігура 20. Відстань проходження в шлунково-кишковому тракті (ШКТ), отримана в підтвердженому дослідженні скорочувальної здатності у щурів, яким дають перорально еквімолярні дози ГМ і 3,6-ді-аспірин-ГМ. Фігура 21. Приклади схем синтезу для синтезу деяких проліків гідроморфону відповідно до даного винаходу. Докладний опис винаходу Композиція У даному винаході представлені композиції, які містять арилкарбонові кислоти, які хімічно кон'юговані з гідроморфоном (4,5-α-епокси-3-гідрокси-17-метилморфінан-6-оном) з отриманням нових проліків і композицій гідроморфону. У деяких варіантах хімічний зв'язок між цими двома групами може бути встановлений взаємодією функціональної групи карбонової кислоти арилкарбонової кислоти з однією з наступних функціональних груп гідроморфону: (a) С-6 енольним таутомером гідроморфону (b) С-3 гідроксилом гідроморфону, (с) або обох С-3 гідроксилу і С-6 енольного таутомера гідроморфону. Застосування "опіоїду" включає будь-який лікарський засіб, який активує опіоїдні рецептори, знайдені в мозку, спинному мозку і кишечнику. Існує чотири широкі класи опіоїдів: природні алкалоїди опію, такі як морфін (прототипний опіоїд) кодеїн і тебаїн; ендогенні опіоїдні пептиди, такі як ендорфіни; напівсинтетичні, такі як героїн, оксикодон і гідрокодон, які отримують модифікацією природних алкалоїдів опію (опіатів) і які мають схожі структури; і чисті синтетичні, такі як фентаніл і метадон, які не отримують з опію, і які можуть мати сильно відмінні від алкалоїдів опію хімічні структури. Додаткові приклади опіоїдів включають гідроморфон, оксиморфон, метадон, леворфанол, дигідрокодеїн, меперидин, дифеноксилат, суфентаніл, алфентаніл, пропоксифен, пентазоцин, налбуфин, буторфанол, бупренорфин, мептазинол, дезоцин і їх фармацевтично прийнятні солі. Застосування "терапевтичного еквівалента" означає лікарські продукти, які є фармацевтичними еквівалентами і мають таку ж клінічну дію при введенні пацієнтам в умовах, вказаних на етикетці. Застосування "біоеквівалента" означає фармацевтичний еквівалент або фармацевтичні альтернативні продукти, які демонструють порівнянну біодоступність (тобто системні концентрації гідроморфону в плазмі) при вивченні в схожих експериментальних умовах. Застосування "гідроморфону" включає напівсинтетичний наркотичний знеболюючий засіб, який має множинну дією, якісно подібну до дії морфіну і застосовується в медицині як 7 UA 112329 C2 5 10 15 20 25 30 35 40 45 50 альтернатива морфіну. Його в основному застосовують для полегшення болю і як наркотичний протикашльовий засіб у випадках сухого хворобливого кашлю. Торгові найменування ® ® ® ® включають Dilaudid , Exalgo , Hydrostat і Palladone (уповільнене вивільнення). Інші фармацевтично прийнятні солі гідроморфону також включені в певні варіанти даного винаходу. Хімічною структурою гідроморфону є: . Арилкарбонові кислоти відповідно до даного винаходу можуть бути згруповані в різні категорії і субкатегорії. У певних варіантах карбоксильна група може бути приєднана безпосередньо до ароматичного кільця або відділена алкільним або алкенільним ланцюгом. У інших варіантах даного винаходу, довжина ланцюга алкільної або алкенільної групи не повинна перевищувати два нерозгалужені вуглеці, але не обмежена по кількості атомів потенційних бічних ланцюгів або додаткових функціональних груп. У інших варіантах, даний винахід включає тільки вуглецеві арильні групи і арильні групи з гетероатомами (гетероарил). Арильна або гетероарильна група певних варіантів відповідно до даного винаходу, яка зв'язана безпосередньо або через алкільну або алкенільну групу з карбоксильною функціональною групою, може бути 6-членним кільцем і містити нуль, один або більше одного гетероатома. Додаткові заміщені або незаміщені ароматичні або аліфатичні кільця можуть бути конденсовані з цим 6-членним арилом або гетероарилом в певних варіантах даного винаходу. У деяких варіантах даного винаходу, арилкарбонові кислоти можуть мати одну або більше груп вільної карбонової кислоти, і загальна кількість фенільних замісників на 6-членному кільці може бути чотири або менше. Залежно від окремих арилкарбонових кислот, які зв'язані з гідроморфоном, проліки відповідно до даного винаходу можуть бути нейтральними, вільною кислотою, вільною основою або різними фармацевтично прийнятними аніонними або катіонними солями або сумішами солей в будь-якому співвідношенні позитивних і негативних компонентів. У певних варіантах, солі проліків відповідно до даного винаходу включають, але не обмежені ними: ацетат, l-аспартат, безилат, бікарбонат, карбонат, d-камзилат, l-камзилат, цитрат, едизилат, форміат, фумарат, глюконат, гідробромід/бромід, гідрохлорид/хлорид, dлактат, l-лактат, d, l-лактат, d, l-малат, l-малат, d-малат, мезилат, памоат, фосфат, сукцинат, сульфат, бісульфат, d-тартрат, l-тартрат, d, l-тартрат, мезо-тартрат, бензоат, глуцептат, dглюкуронат, гібензат, ізетіонат, малонат, метилсульфат, 2-напсилат, нікотинат, нітрат, оротат, стеарат, тозилат, тіоціанат, ацефілінат, ацетурат, аміносаліцилат, аскорбат, борат, бутират, камфорат, камфокарбонат, деканоат, гексаноат, холат, ципіонат, дихлорацетат, едентат, етилсульфат, фурат, фузидат, галактарат (мукат), галактуронат, галлат, гентизат, глутамат, глутарат, гліцерофосфат, гептаноат (енантат), гідроксибензоат, гіпурат, фенілпропіонат, йодид, ксинафоат, лактобіонат, лаурат, малеат, міндалят, метансульфонат, міристат, нападизилат, олеат, оксалат, пальмітат, пікрат, півалат, пропіонат, пірофосфат, саліцилат, саліцилсульфат, сульфосаліцилат, танат, терефталат, тіосаліцилат, триброфенат, валерат, вальпроат, адипат, 4-ацетамідобензоат, камзилат, октаноат, естолат, езилат, гліколят, тіоціанат, ундециленат, натрій, калій, кальцій, магній, цинк, алюміній, литий, холінат, лізиній, амоній і трометамін. Проліки певних варіантів даного винаходу створені так, щоб розкладатися in vivo або ферментами, або іншим способом з виділенням активного гідроморфону і відповідної арилкарбонової кислоти(кислот) або їх метаболітів. Арилкарбонові кислоти відповідно до даного винаходу повинні бути не токсичними при даних рівнях дозування і, переважно, відомими лікарськими засобами, натуральними продуктами, метаболітами або ЗВЯБ (загальновизнаними як безпечні) сполуками (наприклад, консервантами, барвниками, смаковими добавками і т. д.) або їх не токсичними міметиками. У деяких варіантах, арилкарбонові кислоти відповідно до даного винаходу містять карбоксильну групу, яка приєднана безпосередньо до арильної групи. Ці арилкарбонові кислоти можуть бути розділені на дві субкатегорії: бензоати і гетероарилкарбонові кислоти. Бензоати Бензоати певних варіантів даного винаходу включають амінобензоати (наприклад, аналоги антранілінової кислоти, такі як фенамати) і гідроксибензоати (наприклад, аналоги саліцилової 8 UA 112329 C2 кислоти). Загальна хімічна структура бензоатів відповідно до даного винаходу представлена наступною загальною формулою I: 5 10 15 20 25 30 35 40 , 1 2 3 де R , R і R незалежно вибирають з групи, яка включає водень, гідроксил, аміно, амін, амід, тіол, ціано, нітро, галоген, імін, алкіл, алкокси, арил, алкеніл, алкініл, галогеналкіл, алкіларил, арилалкіл, гетероцикл, арилалкокси, циклоалкіл, циклоалкеніл, циклоалкініл, карбоніл, тіоефір, селеноефір, силіл, силілокси, сульфоніл, фосфонат. Бензоати широко поширені в природі у вигляді натуральних продуктів і метаболітів. Множинні аналоги бензойної кислоти також застосовують в харчовій і фармацевтичній промисловості. Деякі з найбільш численних бензоатів є похідними з гідроксильними або аміногрупами або їх поєднанням. Гідроксильні і аміно функціональні групи можуть бути присутніми у вільній формі або з іншими хімічними групами на кінцях. У певних варіантах даного винаходу іншими хімічними групами переважно є, але не обмежені ними, метильна або ацетильна групи. У деяких варіантах даного винаходу фенільне кільце може мати додаткові замісники. Деякі приклади гідроксибензоатів відповідно до даного винаходу включають, але не обмежені ними, бензойну кислоту, саліцилову кислоту, ацетилсаліцилову кислоту (аспірин), 3гідроксибензойну кислоту, 4-гідроксибензойну кислоту, 6-метилсаліцилову кислоту, o, м,пкрезотинову кислоту, анакардинову кислоту, 4,5-диметилсаліцилову кислоту, o, м,п-тимотинову кислоту, дифлузинал, o, м,п-анізинову кислоту, 2,3-дигідроксибензойну кислоту (2,3-ДГБ), α,β,γрезорцилову кислоту, протокатехову кислоту, гентизинову кислоту, піперонілову кислоту, 3метоксисаліцилову кислоту, 4-метоксисаліцилову кислоту, 5-метоксисаліцилову кислоту, 6метоксисаліцилову кислоту, 3-гідрокси-2-метоксибензойну кислоту, 4-гідрокси-2метоксибензойну кислоту, 5-гідрокси-2-метоксибензойну кислоту, ванілінову кислоту, ізованілінову кислоту, 5-гідрокси-3-метоксибензойну кислоту, 2,3-диметоксибензойну кислоту, 2,4-диметоксибензойну кислоту, 2,5-диметоксибензойну кислоту, 2,6-диметоксибензойну кислоту, вератрову кислоту (3,4-диметоксибензойну кислоту), 3,5-диметоксибензойну кислоту, галієву кислоту, 2,3,4-тригідроксибензойну кислоту, 2,3,6-тригідроксибензойну кислоту, 2,4,5тригідроксибензойну кислоту, 3-O-метилгалієву кислоту (3-OMGA), 4-O-метилгалієву кислоту (4OMGA), 3,4-O-диметилгалієву кислоту, бузкову кислоту і 3,4,5-триметоксибензойну кислоту. Деякі приклади амінобензоатів відповідно до даного винаходу включають, але не обмежені ними, антранілінову кислоту, 3-амінобензойну кислоту, 4,5-диметилантранілінову кислоту, Nметилантранілінову кислоту, N-ацетилантранілінову кислоту, фенамінові кислоти (наприклад, толфенамінову кислоту, мефенамінову кислоту, флуфенамінову кислоту), 2,4-діамінобензойну кислоту (2,4-DABA), 2-ацетиламіно-4-амінобензойну кислоту, 4-ацетиламіно-2-амінобензойну кислоту і 2,4-діацетиламінобензойну кислоту. Деякі приклади аміногідроксибензоатів відповідно до даного винаходу включають, але не обмежені ними, 4-аміносаліцилову кислоту, 3-гідроксіантранілінову кислоту і 3метоксіантранілінову кислоту. Гетероарилкарбонові кислоти Загальні структури деяких гетероарилкарбонових кислот відповідно до даного винаходу представлені наступними загальними формулами V, VI, VII, VIII, IX, X, XI, XII або XIII: 9 UA 112329 C2 5 10 15 20 25 30 35 , 1 2 3 де R , R і R такі, як визначені вище. Прийнятні приклади гетероарилкарбонових кислот відповідно до даного винаходу включають похідні піридину, деякі з яких залучені до метаболізму нікотинату і триптофану. У цих сполуках щонайменше один атом вуглецю фенільного кільця заміщений атомом азоту. Крім карбоксильної групи, даний ряд сполук відповідно до даного винаходу може мати додаткові замісники, переважно, але не обмежуючись ними, гідроксильні групи. Деякі приклади гетероарилкарбонових кислот відповідно до даного винаходу включають, але не обмежені ними, нікотинову кислоту (ніацин), ізонікотинову кислоту, піколінову кислоту, 3гідроксипіколінову кислоту, 6-гідроксинікотинову кислоту, цитразинову кислоту, 2,6дигідроксинікотинову кислоту, кінуренову кислоту, ксантуренову кислоту, 6-гідроксикінуренову кислоту, 8-метоксикінуренову кислоту, 7,8-дигідроксикінуренову кислоту і 7,8-дигідро-7,8дигідроксикінуренову кислоту. Фенілацетати У деяких варіантах даного винаходу арилкарбонові кислоти відповідно до даного винаходу включають карбоксильну групу, яка відділена одним атомом вуглецю від арильної частини. Ці арилкарбонові кислоти включають розгалужені фенілпропіонові кислоти (тобто, 2-метил-2фенілацетати) або інші похідні фенілацетату (Фігура 4). Загальна структура щонайменше одного фенілацетату відповідно до даного винаходу представлена наступною загальною формулою II: , 1 2 3 4 де R , R , R і R такі, як визначені вище. Фенілоцтові кислоти охоплюють різні підвиди природних продуктів, метаболітів і фармацевтичних препаратів. Одним з таких фармацевтично важливих підвидів є "профени", тип НСПЗЗ і похідних певних фенілпропіонових кислот (наприклад, аналоги 2-метил-2-фенілоцтової кислоти). Деякі інші фенілацетати мають центральні функції в метаболізмі фенілаланіну і тирозину. Деякі приклади фенілацетатів відповідно до даного винаходу включають, але не обмежені ними, фенілоцтову кислоту (гідратропову кислоту), 2-гідроксифенілоцтову кислоту, 3гідроксифенілоцтову кислоту, 4-гідроксифенілоцтову кислоту, гомопротокатехінову кислоту, гомогентизинову кислоту, 2,6-дигідроксифенілоцтову кислоту, гомованілінову кислоту, гомоізованілінову кислоту, гомовератринову кислоту, атропову кислоту, d, l-тропову кислоту, диклофенак, d, l-мигдалеву кислоту, 3,4-дигідрокси-d, l-мигдалеву кислоту, ваніліл-d, lмигдалеву кислоту, ізованіліл-d, l-мигдалеву кислоту, ібупрофен, фенопрофен, карпрофен, флурбіпрофен, кетопрофен і напроксен. Бензилацетати У додаткових варіантах, арилкарбонові кислоти відповідно до даного винаходу містять карбоксильну групу, яка відділена двома атомами вуглецю від арильної частини. Ці арилкарбонові кислоти включають бензилацетати і їх заміщені похідні, і аналоги цинамінової 10 UA 112329 C2 кислоти (Фігура 5). Обидва класи сполук широко поширені в природі в формі натуральних продуктів або метаболітів (наприклад, метаболізм фенілаланіну). Загальні структури деяких бензилацетатів і цинаматів відповідно до даного винаходу представлені наступними загальними формулами (III) і (IV): 5 10 15 20 25 30 35 40 45 50 , 1 2 3 4 де R , R , R і R такі, як визначені вище. Бензилоцтові кислоти визначені етиленовою групою між карбоксильною функціональною групою і фенільним кільцем. І алкільний ланцюг і арильна частина можуть мати замісники, переважно, гідроксильні групи. Деякі сполуки цього класу можуть бути знайдені при метаболізмі фенілаланіну. Деякі приклади бензилацетатів відповідно до даного винаходу включають, але не обмежені ними, бензилоцтову кислоту, метилоцтову кислоту, 3-гідроксифенілпропанову кислоту, 4гідроксифенілпропанову кислоту, 2,3-дигідроксифенілпропанову кислоту, d, l-фенілмолочну кислоту, o, м,п-гідрокси-d, l-фенілмолочну кислоту, фенілпіровиноградну кислоту. Цинамати Коричні кислоти (3-фенілакрилові кислоти) включають ненасичені аналоги бензилоцтових кислот. Цинамати існують в двох ізомерних формах: цис (Z) і транс (Е). Ізомери цинамату певних варіантів відповідно до даного винаходу переважно мають, але не обмежені нею, транс конфігурацію. Так само як і бензилацетати, похідні коричної кислоти можуть бути заміщені на алкенільну або арильну частину молекули. Переважні замісники деяких варіантів відповідно до даного винаходу включають гідроксильну і метоксигрупи. Вважається, що певні цинамати відіграють ключову роль в метаболізмі фенілаланіну. Деякі приклади цинаматів відповідно до даного винаходу включають, але не обмежені ними, коричну кислоту, o, м,п-кумаринову кислоту, 2,3-дигідроксикоричну кислоту, 2,6дигідроксикоричну кислоту, кофеїнову кислоту, ферулінову кислоту, ізоферулінову кислоту, 5гідроксиферулінову кислоту, синапову кислоту, 2-гідрокси-3-фенілпропенову кислоту. Фізіологічні переваги У певних варіантах, проліки гідроморфону і композиції відповідно до даного винаходу можуть вводитися перорально і, при введенні, виділяти активний гідроморфон після гідролізу в тілі. Оскільки арилкарбонові кислоти відповідно до даного винаходу є природними метаболітами або їх міметиками або фармацевтично активними сполуками, ці проліки можуть легко розпізнаватися фізіологічними системами, що викликає гідроліз і виділення гідроморфону. Проліки відповідно до даного винаходу, в певних варіантах, є або не активними, або мають обмежену фармакологічну активність і, отже, можуть проходити метаболічний шлях, який відрізняється від вихідного лікарського засобу. При виборі відповідних арилкарбонових кислот ("лігандів") відповідно до даного винаходу виділення гідроморфону в системний кровотік може контролюватися, навіть якщо проліки вводять шляхами, відмінними від перорального. У щонайменше одному варіанті проліки гідроморфону відповідно до даного винаходу виділяють гідроморфон так само, як вільний або немодифікований гідроморфон. У іншому варіанті, проліки гідроморфону відповідно до даного винаходу виділяють гідроморфон в контрольованій або уповільненій формі. Таке контрольоване виділення може потенційно полегшувати певні побічні ефекти і поліпшувати профіль безпеки вихідного лікарського засобу. Побічні ефекти, які полегшуються відповідно до даного винаходу, можуть включати запаморочення, нудоту, сонливість, блювання, застій шлунка, біль в шлунку, висипання, утруднене сечовипускання, утруднене дихання і втрату свідомості. Крім того, гідроморфон і інші опіоїди також сильно спричиняють звикання і схильні до виникнення залежності. Зловживання рекреаційними опіоїдами є загальною проблемою і звичайно починається з пероральних доз, що приймаються з метою досягнення ейфорії. Протягом часу наркозалежна людина часто підвищує пероральні дози для досягнення більш сильного "кайфу" або для компенсації підвищеної стійкості до опіоїду. Швидкий метаболізм і коротка тривалість дії гідроморфону знеславлює його схильність до виникнення залежності. 11 UA 112329 C2 5 10 15 20 25 30 35 40 45 50 55 60 Така поведінка може посилюватися і викликає перехід до інших способів введення, таких як інтраназальне ("нюхання") і внутрішньовенне ("вколювання"). У деяких варіантах даного винаходу, гідроморфон, який кон'югований з прийнятним лігандом арилкарбонової кислоти, не демонструє швидких піків в рівні крові при пероральному введенні, які необхідні потенційній наркозалежній людині. У певних варіантах, проліки відповідно до даного винаходу демонструють уповільнений T max і низькі значення Cmax в порівнянні з еквімолярною дозою вихідного лікарського засобу. Тому почуття "кайфу" втрачається при пероральному прийомі проліків відповідно до даного винаходу навіть в більш високих дозах, при одночасності полегшення болю. У інших варіантах, кон'югати гідроморфону відповідно до даного винаходу не гідролізуються ефективно при введенні не пероральним шляхом. У результаті проліки відповідно до даного винаходу не створюють високі концентрації в крові або плазмі виділеного гідроморфону при ін'єкції або вдиханні в порівнянні з вільним гідроморфоном, що вводиться цими шляхами. Більше того, оскільки ліганди в певних варіантах даного винаходу зв'язані ковалентно з гідроморфоном, опіоїд не вивільняється будь-якими фізичними маніпуляціями. Це є перевагою проліків відповідно до даного винаходу в порівнянні з іншими складами гідроморфону, які виділяють вільний гідроморфон за допомогою фізичних маніпуляцій (наприклад, розмелювання, розфарбування і т. д.). У щонайменше одному варіанті проліки відповідно до даного винаходу не надають або надають незначну дію на μ-опіоїдні рецептори. У іншому варіанті проліки відповідно до даного винаходу не піддаються ферментному гідролізу доти, поки вони не адсорбуються в кишечнику. Не прив'язуючись до певної теорії вважають, що активні проліки гідроморфону відповідно до даного винаходу ефективно "маскуються" приєднаною арилкарбоновою кислотою і можуть обходити периферійні μ-опіоїдні рецептори, не впливаючи на ШКНС, тим самим знижуючи або запобігаючи ВОК. Гідроморфон значною мірою метаболізується в печінці до гідроморфон-3-глюкуроніду (H3G). Хоча H3G не має знеболюючої дії, він може викликати нейрозбудження, збудження, сплутаність свідомості і галюцинації. Якщо H3G може долати гематоенцефалічний бар'єр (ГЕБ), він може акумулюватися в центральній нервовій системі (ЦНС) і викликати міоклонію, алодинію і пароксизм, які спостерігають у пацієнтів, яким хронічно вводять високі дози гідроморфону. Цей ефект може бути посилений у пацієнтів з нирковою дисфункцією. У щонайменше одному іншому варіанті, проліки відповідно до даного винаходу викликають знижене перетворення гідроморфону в H3G після перорального введення в порівнянні з некон'югованим гідроморфоном. Не прив'язуючись до певної теорії, вважають, що вони можуть мати поліпшений профіль побічних ефектів, особливо поліпшувати нейрозбуджену поведінку в порівнянні з вільним гідроморфоном. Композиції Композиції і проліки відповідно до даного винаходу можуть бути у вигляді пероральних лікарських форм. Такі лікарські форми включають, але не обмежені ними, таблетки, капсули, м'які желатинові капсули, каплети, коржики, пастилки, порошок, суспензію, сироп, розчин або пероральні тонкі плівки (ПТП). Переважними формами для перорального введення є капсули, таблетки, розчини і ПТП. Композиції і проліки відповідно до даного винаходу також можуть мати тверді лікарські форми, які включають наповнювачі. Наповнювачі відповідно до даного винаходу включають, але не обмежені ними, антиадгезиви, зв'язувальні агенти, покриття, розпушувачі, наповнювачі, смакові добавки і барвники, гліданти, мастильні агенти, консерванти, сорбенти і підсолоджувачі. Пероральні композиції відповідно до даного винаходу також можуть бути включені в розчин або суспензію у водній рідині або не водній рідині. Композицією може бути емульсія, така як масло у воді рідка емульсія і вода в маслі рідка емульсія. Масла можуть вводитися додаванням очищених і стерилізованих рідин в готову ентеральну формулу, яку потім вміщують в зонд для штучного годування пацієнта, який не здатний ковтати. М'які таблетки або м'які желатинові капсули можуть бути отримані, наприклад, диспергуванням композиції у прийнятній посудині (звичайно застосовують рослинні олії) для отримання високов'язкої суміші. Цю суміш потім інкапсулюють в плівку на основі желатину із застосуванням методики і обладнання, відомого в галузі виробництва м'якого желатину. Отримані таким чином лікарські форми потім сушать до постійної ваги. Жувальні таблетки, наприклад, можуть бути отримані змішуванням композицій з наповнювачами, складеними так, щоб отримати відносно м'які, ароматизовані, таблетовані лікарські форми, які призначені для розжовування, а не для проковтування. Можна застосовувати звичайне обладнання і методики для отримання таблеток, наприклад, 12 UA 112329 C2 5 10 15 20 25 30 35 40 45 50 55 60 безпосереднє пресування і гранулювання, тобто брикетування, перед пресуванням. Фахівці, що займаються виробництвом твердих лікарських форм, обізнані в застосовуваних методиках і обладнанні, і жувальні лікарські форми є широко застосовуваними лікарськими формами в фармацевтичній промисловості. Таблетки в плівковій оболонці, наприклад, можуть бути отримані нанесенням покриття на таблетки із застосуванням методик, таких як методи нанесення покриттів із застосуванням обертової чаші або методів повітряної суспензії для нанесення шару контактуючої плівки на таблетку. Пресовані таблетки, наприклад, можуть бути отримані змішуванням композиції з наповнювачами, які додають зв'язувальних властивостей або розпушувальних властивостей. Суміш або безпосередньо пресують із застосуванням методів і обладнання, відомих фахівцям в даній галузі техніки. Отримані пресовані таблетовані лікарські форми потім упаковують відповідно до потреб ринку, наприклад, в окремі упаковки, рулони, об'ємні пляшки, блістери і т. д. Дана методика також включає застосування біологічно прийнятних носіїв, які можуть бути отримані з множини матеріалів. Не обмежуючись ними, такі матеріали включають розріджувачі, зв'язувальні агенти і адгезиви, мастильні агенти, пластифікатори, розпушувачі, барвники, об'ємоутворювальні препарати, смакові добавки, підсолоджувачі і різні матеріали, такі як буфери і адсорбенти для отримання конкретної лікарської композиції. Зв'язувальні агенти відповідно до даного винаходу можуть бути вибрані з широкого спектра матеріалів, таких як гідроксипропілметилцелюлоза, етилцелюлоза або інші прийнятні похідні целюлози, повідон, співполімери акрилової і метакрилової кислоти, фармацевтична глазур, камеді, похідні молока, такі як сироватка, крохмаль і похідні, а також інші звичайні зв'язувальні агенти, відомі фахівцям в даній галузі техніки. Типові не обмежувальні розчинники включають воду, етанол, ізопропіловий спирт, метиленхлорид або їх суміші і поєднання. Приклади не обмежувальних об'ємоутворювальних речовин включають цукор, лактозу, желатин, крохмаль і двоокис кремнію. Повинно бути зрозуміло, що при додаванні до вказаних вище інгредієнтів композиції відповідно до даного винаходу можуть включати інші прийнятні агенти, такі як смакові добавки, консерванти і антиоксиданти. Такі антиоксиданти можуть бути прийнятні як продукти харчування і можуть включати вітамін Е, каротин, БГТ і інші антиоксиданти. Інші сполуки, які можуть бути додані домішуванням, включають, наприклад, медичні інертні інгредієнти, наприклад, тверді і рідкі розріджувачі, такі як лактоза, декстроза, сахароза, целюлоза, крохмаль або фосфат кальцію для таблеток або капсул, оливкову олію або етилолеат для м'яких капсул і води або рослинну олію для суспензій або емульсій; мастильні агенти, такі як двоокис кремнію, тальк, стеаринова кислота, стеарат магнію або кальцію і/або поліетиленгліколі; желатинуючі агенти, такі як колоїдні глини; загущувальні агенти, такі як трагакант або альгінат натрію, зв'язувальні агенти, такі як крохмаль, аравійські камеді, желатин, метилцелюлоза, карбоксиметилцелюлоза або полівінілпіролідон; розпушувальні агенти, такі як крохмаль, альгінова кислота, альгінати і гліколят крохмалю натрію; шипучі суміші; барвники; підсолоджувачі; змочувальні агенти, такі як лецитин, полісорбати або лаурилсульфати; і інші терапевтично прийнятні додаткові інгредієнти, такі як зволожувачі, консерванти, буфери і антиоксиданти, які є відомими добавками для таких композицій. Для перорального введення тонкоподрібнені порошки або гранули, що містять розріджувальні, диспергуючі і/або поверхнево-активні агенти, можуть бути представлені в сухій формі, у воді або в сиропі, в капсулах або саше в сухому стані, в неводній суспензії, в яку можуть бути включені суспендуючі агенти, або в суспензії у воді або сиропі. Якщо бажано, можуть бути додані смакові добавки, консерванти, суспендуючі агенти, загусники або емульгуючі агенти. Рідкі дисперсії для перорального введення можуть включати сиропи, емульсії або суспензії. Сиропи можуть містити, як носій, наприклад, сахарозу або сахарозу з гліцерином і/або манітом, і/або сорбітом. Зокрема, сироп для пацієнтів з діабетом може містити як носії тільки ті продукти, наприклад сорбіт, які не метаболізуються до глюкози або які метаболізуються тільки в дуже невеликих кількостях до глюкози. Суспензії і емульсії можуть містити носій, наприклад, натуральну камедь, агар, альгінат натрію, пектин, метилцелюлозу, карбоксиметилцелюлозу або полівініловий спирт. Схвалені в цей час композиції гідроморфону включають таблетки, капсули, капсули з модифікованим вивільненням, таблетки з уповільненим вивільненням, капсули з контрольованим вивільненням, супозиторії, порошки для ін'єкцій, пероральні рідини, сироп від кашлю і форми для ін'єкцій. Кон'югований гідроморфон відповідно до даного винаходу в певних 13 UA 112329 C2 5 10 15 20 25 30 35 40 45 50 55 варіантах може бути складений в будь-які з вказаних, схвалених в цей час, композицій некон'югованого гідроморфону. Інші, схвалені в цей час, композиції гідроморфону включають поєднання терапії гідроморфоном і одним або більше іншими не наркотичними активними інгредієнтами залежно від призначеного застосування. Приклади таких активних лікарських препаратів включають, але не обмежені ними, ацетамінофен, ібупрофен і аспірин. Кон'югований гідроморфон відповідно до даного винаходу може бути складений з одним або більше сполученнями цих і інших активних речовин або у вигляді окремого активного інгредієнта без будь-яких інших активних речовин. Способи застосування Композиції кон'югата або проліків відповідно до даного винаходу можуть застосовуватися в способах лікування пацієнта, який страждає на захворювання, розлад або стан, які вимагають або опосередковані зв'язуванням або інгібують зв'язуванням опіоїду з опіоїдними рецепторами пацієнта.Лікування включає пероральне введення пацієнту щонайменше одного кон'югата гідроморфону, як описано відповідно до даного винаходу, в кількості, терапевтично еквівалентній ефективній кількості некон'югованого гідроморфону. Кон'югат може демонструвати знижені пікові концентрації в плазмі (Cmax) і низьку площу під кривою (ППК) виділеного гідроморфону при введенні через не пероральні шляхи, такі як інтраназальний і внутрішньовенний, в порівнянні з еквівалентною молярною кількістю некон'югованого гідроморфону. У деяких аспектах пероральне введення щонайменше одного кон'югата може забезпечити уповільнену швидкість виділення гідроморфону протягом часу і терапевтично біоеквівалентну ППК з незначним або відсутністю піка в Cmax або еквівалентного значення Cmax в порівнянні з іншими формами з контрольованим вивільненням гідроморфону (наприклад, ® Exalgo ). У інших варіантах щонайменше один кон'югат може демонструвати меншу варіабельність в концентраціях гідроморфону в плазмі після перорального введення в порівнянні з некон'югованим гідроморфоном. У інших варіантах щонайменше представлений один кон'югат в кількості, достатній для отримання терапевтично біоеквівалентної ППК (площі під кривою) гідроморфону в порівнянні з молярною еквівалентною кількістю некон'югованого гідроморфону. У інших варіантах представлений кон'югат в кількості, достатній для отримання терапевтично біоеквівалентної ППК гідроморфону в порівнянні з молярною еквівалентною кількістю некон'югованого гідроморфону, але що має більш низьке значення Cmax (пікову концентрацію) гідроморфону в плазмі або не забезпечує еквівалентне значення Cmax в плазмі. У деяких аспектах представлений кон'югат в кількості, достатній для отримання терапевтично еквівалентного значення Cmax гідроморфону в порівнянні з молярною еквівалентною кількістю некон'югованого гідроморфону. У інших варіантах щонайменше представлений один кон'югат в кількості, достатній для отримання підвищеної ППК або підвищеного значення C max гідроморфону, або обох, в порівнянні з молярною еквівалентною кількістю некон'югованого гідроморфону. У інших аспектах представлений щонайменше один кон'югат в кількості, терапевтично еквівалентній ефективній кількості некон'югованого гідроморфону, але знижує або запобігає викликаній опіоїдом констипації (ВОК). У деяких варіантах щонайменше представлений один кон'югат в кількості, терапевтично еквівалентній ефективній кількості некон'югованого гідроморфону, але яка знижує або запобігає нейрозбуджувальній токсичності, викликаній гідроморфон-3-глюкуронідом. Прийнятні захворювання, розлади або стани, які можна лікувати проліками або композиціями відповідно до даного винаходу, включають наркотичну або лікарську залежність, гострий або хронічний біль і тяжкий кашель. Дози кон'югатів відповідно до даного винаходу залежать від їх молекулярної маси і відповідного масового процента гідроморфону як частини цілого кон'югата, і тому можуть бути вищим, ніж дози вільного гідроморфону. Пероральна доза для дорослої людини, в перерахунок на гідрохлорид гідроморфону, становить від 2 мг до 16 мг на дозу для композицій з негайним вивільненням, і від 8 мг до 64 мг на дозу для композицій з уповільненим вивільненням. Педіатрична пероральна доза становить від 0,03 мг/кг/доза до 0,08 мг/кг/доза для дітей і підлітків з масою тіла менше 50 кг і від 1 мг до 2 мг на дозу для дітей і підлітків з масою тіла більше 50 кг. Педіатричні пероральні дози для придушення кашлю варіюються від 0,5 мг до 1 мг на дозу. Дози повинні бути відтитровані до відповідної знеболюючої дії при мінімізації побічних ефектів. Дози для проліків відповідно до даного винаходу можуть бути вищими, залежно від їх молекулярної маси і відповідної масової частки гідроморфону в кон'югаті. Перерахунок дози з гідрохлориду гідроморфону в проліки гідроморфону може бути здійснений із застосуванням наступної формули: 14 UA 112329 C2 доза (проліки ГМ) fBA дозу(ГМ HCl) 5 10 15 20 25 30 35 40 45 50 55 (ММ (проліки ГМ) г 321,80 моль ГМ = гідроморфон HCl = гідрохлорид ММ = молекулярна маса fBА = поправний коефіцієнт, розрахований для різниць в біодоступності між немодифікованим гідроморфоном і проліками відповідно до даного винаходу. Цей поправний коефіцієнт визначений для кожних проліків відповідно до даного винаходу. Прийнятні дози кон'югованого гідроморфону відповідно до даного винаходу включають, але не обмежені ними, композиції, що містять від близько 0,1 мг або вище, альтернативно, від близько 0,5 мг або вище, альтернативно, відблизько 2,5 мг або вище, альтернативно, від близько 5,0 мг або вище, альтернативно, від близько 7,5 мг або вище, альтернативно, від близько 10 мг або вище, альтернативно, від близько 20 мг або вище, альтернативно, від близько 30 мг або вище, альтернативно, від близько 40 мг або вище, альтернативно, від близько 50 мг або вище, альтернативно, від близько 60 мг або вище, альтернативно, від близько 70 мг або вище, альтернативно, від близько 80 мг або вище, альтернативно, від близько 90 мг або вище, альтернативно, від близько 100 мг або вище, альтернативно, від близько 150 мг або вище, альтернативно, від близько 200 мг або вище, і включають будь-які додаткові прирости, наприклад, 0,1, 0,2, 0,25, 0,3, 0,4, 0,5, 0,6, 0,7, 0,75, 0,8, 0,9 або 1,0 мг і їх різноманітні множники (наприклад, ×1, ×2, ×2,5, ×5, ×10, ×100, і т. д.). У іншому аспекті, кількість на лікарську форму основана на вмісті вільного або некон'югованого гідроморфону в кон'югаті гідроморфону. Дана технологія також включає лікарські композиції, що включають схвалені в цей час композиції гідроморфону, де доза може бути розрахована із застосуванням вказаної вище формули, визначеної через кількість гідроморфону. У даному винаході представлені лікарські форми, складені у вигляді монотерапії або комбінованої терапії з іншими активними фармацевтичними інгредієнтами (АФІ). Проліки відповідно до даного винаходу можуть вводитися для полегшення болю або придушення кашлю або для лікування будь-якого стану, який може вимагати блокування опіоїдних рецепторів. Кон'югати відповідно до даного винаходу можуть знижувати побічні ефекти опіоїдних знеболюючих засобів, включаючи знижені або інгібовані констипаційні ефекти. Загальні методи синтезу У даному винаході також представлений спосіб синтезу для отримання кон'югованого гідроморфону відповідно до даного винаходу. У певних варіантах, синтез проліків відповідно до даного винаходу включає стадії: Кон'югати з фенольним складним ефіром (3-ліганд-ГМ): 1. Захист ліганду, при необхідності. 2. Активація групи карбонової кислоти ліганду, при необхідності. 3. Додання активованого ліганду до гідроморфону або навпаки в присутності основи. 4. Видалення захисної групи(груп) ліганду, якщо застосовно. Кон'югати з енольним складним ефіром (6-ліганд-ГМ): 1. Захист ліганду, при необхідності. 2. Активація групи карбонової кислоти ліганду, при необхідності. 3. Захист фенольної (3-OH) гідроксильної групи гідроморфону, при необхідності. 4. Додання активованого ліганду до гідроморфону або навпаки в присутності основи. 5. Видалення захисної групи(груп) ліганду і/або гідроморфону, якщо застосовується. Дикон'югати фенольного складного ефіру/енольного складного ефіру (3,6-ди-ліганд-ГМ): 1. Захист ліганду, при необхідності. 2. Активація групи карбонової кислоти ліганду, при необхідності. 3. Додання активованого ліганду до гідроморфону або навпаки в присутності основи. 4. Видалення захисної групи(груп) ліганду, якщо застосовно. Якщо арилкарбонова кислота містить будь-які додаткові реакційноздатні функціональні групи, які можуть втручатися в поєднання з гідроморфоном, може бути необхідним спочатку приєднувати одну або більш захисних груп. Можуть застосовуватися будь-які відповідні захисні групи, залежно від типу функціональної групи і умов реакції. Деякі приклади захисних груп включають: ацетил (Ac), β-метоксіетоксиметиловий ефір (МЕМ), метоксиметиловий ефір (МОМ), п-метоксибензиловий ефір (ПМБ), триметилсиліл (ТМС), трет-бутилдиметилсиліл (ТБДМС), триізопропілсиліл (ТІПС), карбобензилокси (Cbz), п-метоксибензилкарбоніл (Moz), 15 UA 112329 C2 5 10 15 20 25 30 35 40 45 50 55 трет-бутилоксикарбоніл (Boc), 9-флуоренілметилоксикарбоніл (Fmoc), бензил (Bn), пметоксибензил (MPM), тозил (Ts). Також може застосовуватися тимчасове утворення ацеталів або кеталів з функціональних груп карбонілу. Може бути необхідним активувати групу карбонової кислоти лігандів для того, щоб взаємодіяти з гідроморфоном і утворювати прийнятні кількості кон'югатів. Така активація може проводитися множиною методів із застосуванням різних поєднувальних агентів, відомих фахівцеві в даній галузі техніки. Приклади таких поєднувальних агентів включають: N, Nдициклогксилкарбодіімід (ДЦК), N-(3-диметиламінопропіл)-N'-етилкарбодіімід (EDCI), N, N'діізопропілкарбодіімід (ДІК), 1,1'-карбонілдіімідазол (КДІ) або інші карбодііміди; гексафторфосфат (бензотриазол-1-ілокси)тріс(диметиламіно)фосфонію (BOP), гексафторфосфат бромтрипіролідинофосфонію (PyBroP), гексафторфосфат (бензотриазол-1ілокси)трипіролідинофосфонію (PyBOP) або інші реагенти на основі фосфонію; гексафторфосфат О-(бензотриазол-1-іл)-N, N, N', N'-тетраметилуронію (HBTU), тетрафторборат О-(бензотриазол-1-іл)-N, N, N', N'-тетраметилуронію (TBTU), гексафторфосфат фтор-N, N, N', N'-тетраметилформамідинію (TFFH), тетрафторборат N, N, N', N'-тетраметил-O-(Nсукцинімідил)уронію (TSTU) або інші реагенти на основі амінію. Арилкарбонова кислота також може бути перетворена у відповідний ацилгалогенід, ацилазид або змішаний ангідрид. Основа може вимагатися на будь-якій стадії в схемі синтезу кон'югата арилкарбонової кислоти з гідроморфоном. Прийнятні основи включають, але не обмежені ними: 4метилморфолін (NMM), 4-(диметиламіно)піридин (DMAP), N, N-діізопропілетиламін, біс(триметилсиліл)амід літію, діізопропіламід літію (LDA), трет-бутоксид будь-якого лужного металу (наприклад, трет-бутоксид калію), будь-який гідрид лужного металу (наприклад, гідрид натрію), алкоксид будь-якого лужного металу (наприклад, метоксид натрію), триетиламін або будь-який інший третинний амін. Прийнятні розчинники, які можуть застосовуватися для будь-якої реакції в схемі синтезу кон'югата арилкарбонової кислоти з гідроморфоном, включають, але не обмежені ними: ацетон, ацетонітрил, бутанол, хлороформ, дихлометан, диметилформамід (ДМФ), диметилсульфоксид (ДМСО), діоксан, етанол, етилацетат, діетиловий ефір, гептан, гексан, метанол, метил-третбутиловий ефір (МТБЕ), ізопропанол, ізопропілацетат, діізопропіловий ефір, тетрагідрофуран, толуол, ксилол або воду. Фармацевтичні набори У даному винаході також представлені фармацевтичні набори для лікування або профілактики симптомів відміни лікарського засобу або болю у пацієнта. Пацієнтом може бути людина або тварина. Відповідні пацієнти включають дітей, немолодих людей і звичайних пацієнтів. Набір містить певну кількість окремих доз в упаковці, що містить фармацевтично ефективну кількість щонайменше одного кон'югата гідроморфону відповідно до даного винаходу. Набір також може включати інструкції по застосуванню набору. Певна кількість окремих доз може містити від близько 1 до близько 100 окремих доз, альтернативно, від близько 1 до близько 60 окремих доз, альтернативно, від близько 10 до близько 30 окремих доз, включаючи близько 1, близько 2, близько 5, близько 10, близько 15, близько 20, близько 25, близько 30, близько 35, близько 40, близько 45, близько 50, близько 55, близько 60, близько 70, близько 80, близько 100, і включають будь-які їх додаткові прирости, наприклад, 1, 2, 5, 10 і їх множники (наприклад, ×1, ×2, ×2,5, ×5, ×10, ×100, і т. д.). Описаний винахід і його переваги будуть краще зрозумілі з представлених нижче прикладів. Ці приклади представлені для опису конкретних варіантів даного винаходу. Дані конкретні приклади не призначені для обмеження об'єму і суті даного винаходу. Фахівець в даній галузі техніки зрозуміє, що повний об'єм даного винаходу охоплює об'єкт, визначений формулою винаходу, прикладеною до даного опису, і будь-які зміни, модифікації або еквіваленти цієї формули. Приклади Приклад 1: Аналіз пероральної фармакокінетики Певні кон'югати проліків відповідно до даного винаходу дозують у вигляді пероральних розчинів щурам і порівнюють з еквімолярним розчином гідрохлориду гідроморфону. Пероральні дослідження проводять в дозах, еквімолярних 2,0 мг/кг гідроморфону. Виділення гідроморфону з проліків варіюється залежно від ліганду, приєднаного до гідроморфону. Вплив гідроморфону, виділеного з проліків в представлених прикладах варіюється від 45 % ППК до 113 % ППК, %Cmax від 37 % до 185 % і %-Tmax від 13 % до 200 % в порівнянні з некон'югованим гідрохлоридом гідроморфону. Криві ФК профілю представлені на фігурах 8-15 і параметри ФК підсумовані в таблиці 1 нижче. 60 16 UA 112329 C2 Таблиця 1 ФК параметри гідроморфону, виділені з кон'югатів гідроморфону (дослідження у щурів). Кон'югат 3-аспірин-ГМ 3,6-ди-аспірин-ГМ 6-о-саліцилат-ГМ 3-цинамат-ГМ 6-напроксен-ГМ 3-ізоніацин-ГМ 3-п-саліциловий-ГМ 3-фенамат-ГМ 3-бензоат-ГМ 3,6-дибензоат-ГМ 5 10 15 20 25 30 35 40 ППК (нг/мл×год.) 55,9 82,4 33,3 25,3 31,6 25,1 31,4 44,6 41,2 30,1 Сmax (нг/мл) 44,3 36,5 14,1 28,3 19,1 18,5 17,2 30,6 19,8 11,3 Тmax (год.) 0,250 0,250 0,250 0,250 0,250 0,250 0,250 0,250 0,500 0,250 % ППК ГМ % Сmax ГМ % Тmax ГМ 76 % 113 % 101 % 45 % 54 % 76 % 60 % 94 % 72 % 53 % 133 % 109 % 51 % 62 % 94 % 66 % 74 % 185 % 64 % 37 % 25 % 25 % 100 % 100 % 100 % 100 % 100 % 13 % 200 % 100 % Концентрації гідроморфону в плазмі, викликані 3-цинамат-ГМ, 3-п-саліцилат-ГМ, 3-бензоатГМ і 3,6-дибензоат-ГМ, були нижчими у всі інтервали часу в порівнянні з некон'югованим гідроморфоном. Значення Cmax гідроморфону, виділеного з 6-напроксен-ГМ, було таким же, як пікова концентрація в плазмі некон'югованого гідроморфону, але загальний вплив після перорального введення цього кон'югата був значно нижчим в порівнянні з вихідними ліками. Концентрації гідроморфону в плазмі, викликані 6-о-саліцилат-ГМ і 3-ізоніацин-ГМ, були такими ж, як для некон'югованого гідроморфону, за винятком значного зниження в перший момент часу (0,25 години), що дало більш низьке значення Cmax для цих двох кон'югатів. Концентрації в плазмі гідроморфону, виділеного з 3-фенамат-ГМ, були підвищені протягом першої години після перорального введення і потім знизилися швидко в порівнянні з некон'югованим гідроморфоном. Концентрації гідроморфону в плазмі були порівнянні після перорального введення 3-аспірин-ГМ, 3,6-діаспірин-ГМ і некон'югованого гідроморфону. Приклад 2: Аналіз інтраназальної фармакокінетики Певні кон'югати проліків відповідно до даного винаходу дозують в інтраназальних розчинах щурам і порівнюють з еквімолярним розчином гідрохлориду гідроморфону. Інтраназальне дослідження проводять в дозах, еквімолярних 2,0 мг/кг гідроморфону. Виділення гідроморфону з проліків варіюється залежно від ліганду, приєднаного до гідроморфону. Концентрації гідроморфону в плазмі після інтраназального введення 3,6-діаспірин-ГМ були значно знижені в порівнянні з вихідним лікарським засобом (Фігура 16). Значення ППК і C max 3,6діаспірин-ГМ становлять 17 % і 20 % від відповідних параметрів ФК некон'югованого гідроморфону. Приклад 3: Аналіз внутрішньовенної фармакокінетики Певні кон'югати проліків відповідно до даного винаходу дозують у внутрішньовенних розчинах щурам і порівнюють з еквімолярним розчином гідрохлориду гідроморфон. Виділення гідроморфону з проліків варіюється залежно від ліганду, приєднаного до гідроморфону. Гідроморфон і 3,6-діаспірин-ГМ дозують внутрішньовенно щурам в дозі 0,20 мг/кг. Концентрації гідроморфону в плазмі після внутрішньовенного введення 3,6-діаспірин-ГМ значно нижчі в порівнянні з некон'югованим гідроморфоном (Фігура 17). Значення ППК і C max 3,6діаспірин-ГМ становлять 6 % і 3 % від відповідних параметрів ФК некон'югованого гідроморфону. Приклад 4: Аналіз збільшення дози Певні кон'югати проліків відповідно до даного винаходу дозують в підвищених дозах у вигляді пероральних розчинів щурам. Коли 3,6-діаспірин-ГМ дозують вище терапевтичного рівня, дія (ППК) гідроморфону досягає плато. Однак після перорального введення гідрохлориду гідроморфону, дія (ППК) гідроморфону залишається приблизно пропорційною дозі навіть для доз вище терапевтичного рівня і викликає смерть тестованих тварин при дозах вищих 14 мг/кг (див. Фігуру 18). Ці дані підтверджують, що 3,6-діаспірин-ГМ має знижений потенціал до передозування в порівнянні з гідрохлоридом гідроморфону. Не прив'язуючись до певної теорії, вважають, що плато впливу (ППК) спостерігається, коли 3,6-діаспірин-ГМ дозують в кількості вище терапевтичного рівня, завдяки насиченню гідролітичних ферментів. Приклад 5: Аналіз захищеності від несанкціонованого доступу 17 UA 112329 C2 5 10 Певні кон'югати проліків відповідно до даного винаходу піддають різним відомим широко застосовуваним "методам екстракції" для тестування гідролізу і/або розкладання проліків. Екстрагування розчину 3,6-діаспірин-ГМ з композиції дає тільки неактивні проліки з невід'ємним захистом від фармакологічно неправильного вживання. Це показує, що гідроморфон не може бути виділений з 3,6-діаспірин-ГМ за допомогою фізичних маніпуляцій або екстракції розчину. Крім того, 3,6-діаспірин-ГМ є хімічно стабільним при застосуванні звичайних "методів екстракції" і гідролізується і/або розкладається тільки в надто важких умовах, даючи комплексну суміш продуктів розкладання у вигляді високо кислих або лужних розчинів. Крім того, продукти розкладання мають знижену пероральну, ІН і ВВ біодоступність, що робить екстрагування неефективним і безглуздим. Результати аналізу екстрагування підсумовані в таблиці 2 нижче. Таблиця 2 Виділення 3,6-діаспірин-ГМ з композиції Умови (відомі способи) 1 н HCl Крижана оцтова кислота 5 % оцтова кислота Вода Насич. NaHCO3 1 н NaOH 4 н NaOH Температура навколишнього середовища 30 хв. 60 хв. 0 0 0 0 0 0 0 0 0 0 1% 1% 1% 6% Числа представляють кількість гідроморфону, виділеного з 3,6-діаспірин-ГМ (у вигляді % ППК по ВЕРХ) 15 20 25 30 35 40 Крім того, 3,6-діаспірин-ГМ піддають 16 жорстким гідролітичним умовам і отримані продукти розпаду відстежують і підраховують ВЕРХ. Крім гідроморфону спостерігають три проміжні продукти розпаду і потім синтезують і дозують перорально щурам. Для кожного гідролітичного стану розраховують віртуальні значення ППК і C max на основі композиції отриманої суміші і індивідуальних параметрів ФК для кожного з її компонентів (див. Фігуру 19). Ці дані показують, що руйнування 3,6-діаспірин-ГМ дає суміш сполук, які при пероральному введенні демонструють вплив (ППК) гідроморфону, який нижчий, ніж вплив (ППК) гідрохлориду гідроморфону або не зруйнованого 3,6-діаспірин-ГМ, і максимальний вплив (Cmax) гідроморфону, який нижчий максимального впливу (Cmax) гідрохлориду гідроморфону. Приклад 6: Аналіз викликаної опіоїдом констипації Аналізи зв'язування рецепторів і аналізи підтвердженої рухової активності шлунковокишкового тракту (ШКТ) у щурів проводять для певних кон'югатів проліків відповідно до даного винаходу. Аналізи зв'язування рецепторів показали, що 3,6-діаспірин-ГМ має незначну спорідненість до тонкокишкових μ-опіоїдних рецепторів, які розташовані в кишечнику. Аналіз підтвердженої рухової активності ШКТ у щурів демонструє, що в еквімолярних дозах 3,6-діаспірин-ГМ знижує транзит ШКТ в меншій мірі, ніж гідрохлорид гідроморфону. Дія 3,6діаспірин-ГМ на рухову активність ШКТ така ж, як у гідрохлориду гідроморфону тільки коли 3,6діаспірин-ГМ дають в дозі в два рази більшій еквімолярної дози вихідного лікарського засобу (Фігура 20). Ці дані дозволяють передбачити, що 3,6-діаспірин-ГМ має потенціал до зниження або виключення викликаної опіоїдом констипації (ВОК), пов'язаної з введенням некон'югованого гідроморфону. Не прив'язуючись до певної теорії вважають, що 3,6-діаспірин-ГМ залишається практично неторканим до абсорбції в слизову кишечника, де він перетворюється в гідроморфон після того, як обійде периферійні опіоїдні рецептори. Знов, не прив'язуючись до певної теорії, також вважають, що виділений гідроморфон потім проходить через базолатеральну мембрану в системний кровотік. Цей теоретичний механізм узгоджується з потенціалом до зниження або запобігання викликаній опіоїдом констипації, пов'язаної з введенням 3,6-діаспірин-ГМ в порівнянні з некон'югованим гідроморфоном. Приклад 7: Певні схеми синтезу Синтез 3-аспірин-ГМ·HCl (Фігура 21A): Триетиламін (0,42 мл, 3 ммоль) додають до гідрохлориду гідроморфону (0,322 г, 1 ммоль) в дихлорметані (10 мл), потім хлорид О-ацетілсаліцилоїлу (0,248 г, 1,25 ммоль). Реакційну суміш 18 UA 112329 C2 5 10 15 20 25 30 35 40 45 50 55 перемішують при кімнатній температурі протягом 4 годин. Суміш виливають в етилацетат (100 мл) і промивають водним насиченим NaHCO3 (30 мл × 3) і насиченим розчином солі (30 мл). Органічний шар сушать над безводним Na2SO4 і концентрують. Залишок очищають хроматографією на колонці (8 % метанол в дихлорметані) з отриманням 0,385 г аморфної твердої речовини, яку розчиняють в метанолі (6 мл) і потім обробляють 1N HCl/MeOH (1,3 мл). Розчинник випарюють, і TBME (6 мл) додають до залишку. Отриману білу тверду речовину збирають і обполіскують TBME (1 мл × 2). Вихід становить 0,395 г (81,6 %). Синтез 3-цинамат-ГМ·HCl (Фігура 21B): Сполуку синтезують із застосуванням методики, що застосовується для 3-аспірин-ГМ, за винятком того, що хлорид О-ацетилсаліцилоїлу замінюють на хлорид цинамоїлу. Вихід становить 65,2 %. Синтез 3-бензоат-ГМ·HCl (Фігура 21C): Сполуку синтезують із застосуванням методики, що застосовується для 3-аспірин-ГМ, за винятком того, що хлорид О-ацетилсаліцилоїлу замінюють на хлорид бензоїлу. Вихід становить 58,9 %. Синтез 3,6-ді-аспірин-ГМ·HCl (Фігура 21D): Триетиламін (0,70 мл, 5 ммоль) додають до гідрохлориду гідроморфону (0,322 г, 1 ммоль) в дихлорметані (15 мл), потім ДМАП (48,9 мг, 0,4 ммоль) і хлорид О-ацетилсаліцилоїлу (0,794 г, 4 ммоль). Реакційну суміш перемішують при кімнатній температурі протягом 48 годин. Суміш виливають в етилацетат (100 мл) і промивають водним насиченим NaHCO 3 (30 мл × 3) і насиченим розчином солі (30 мл). Органічний шар сушать над безводним Na 2SO4 і концентрують. Залишок очищають хроматографією на колонці (етилацетат і потім 8 % метанол в дихлорметані) і потім далі очищають ПТСХ (8 % метанол в дихлорметані). Бажану фракцію концентрують і перетворюють в її HCl сіль додаванням 1N HCl (1 мл). Розчинник випарюють і до залишку додають простий ефір (15 мл). Отриману тверду речовину збирають і обполіскують простим ефіром (2 мл × 3). Вихід становить 0,203 г (31,4 %). Синтез 6-саліцилат-ГМ·HCl (Фігура 21E): Стадія 1 (3-MOM-ГМ): 0,5M MeONa/MeOH (80 мл, 40 ммоль) додають до гідрохлориду гідроморфону (6,436 г, 20 ммоль) в метанолі (50 мл). Розчинник випарюють, і залишок спільно випарюють з толуолом (25 мл × 2). MOMCl (1,691 г, 21 ммоль) в хлороформі (5 мл) додають до отриманої твердої речовини в хлороформі (100 мл) протягом більше 5 хвилин при охолоджуванні на крижаній бані. Реакційну суміш перемішують при кімнатній температурі протягом ночі. Розчинники випарюють, і отриманий залишок очищають на колонці (8 % метанол в хлороформі) з отриманням 5,77 г (87,5 %) масла. Стадія 2 (сукцинімідиловий ефір 2-MOM-саліцилової кислоти):2-MOM саліцилову кислоту (3,2 г, 17,6 ммоль) і N-гідроксисукцинімід (NHS, 2,23 г, 19,36 ммоль) розчиняють в ТГФ (безводний, 40 мл). Додають ДЦК (3,99 г, 19,36 ммоль) однією порцією. Реакційну суміш перемішують протягом ночі. Тверді речовини відфільтровують. Фільтрат концентрують досуха, і залишок перекристалізовують з метанолу (10 мл). Отриману білу тверду речовину збирають і обполіскують метанолом (3 мл × 2). Вихід становить 2,599 г (52,8 %). Стадія 3 (3-MOM-6-(2-MOM-саліцилат)-ГМ): 1M LiHMDS/ТГФ (3 мл, 3 ммоль) додають до 3-MOM-захищеного гідроморфону (0,329 г, 1 ммоль) в ТГФ (безводний, 8 мл) протягом більше 5 хвилин при охолоджуванні на крижаній бані. Суміш потім перемішують протягом 20 хвилин при кімнатній температурі. При охолоджуванні на крижаній бані додають сукцинімідиловий ефір 2-MOM-саліцилової кислоти (0,838 г, 3 ммоль) однією порцією. Реакційну суміш перемішують протягом 6 годин. Насичений NH 4Cl (30 мл) додають для гасіння реакції. Суміш перемішують протягом 30 хвилин і екстрагують етилацетатом (100 мл). Шар ацетату промивають насиченим NaHCO 3 (30 мл × 2) і насиченим розчином солі (30 мл), сушать над безводним Na 2SO4 і концентрують. Залишок очищають на колонці (етилацетат і потім 7 % метанол в дихлорметані) з отриманням 100 мг сиропу (20,2 %). Стадія 4 (6-Саліцилат-ГМ·HCl): Захищений 3-MOM-6-(2-MOM-саліцилат)-ГМ (100 мг), отриманий на стадії 3, розчиняють в метанолі (1 мл). 1,25N HCl/MeOH (3 мл) додають до розчину, і реакційну суміш перемішують протягом 3 годин. Розчинники випарюють, і залишок розчиняють в метанолі (0,5 мл). Додають простий ефір (15 мл), і отриману тверду речовину збирають фільтрацією і промивають простим ефіром (1 мл × 3). Вихід становить 75 мг (83,7 %). У даному описі застосування однини включає множину, якщо чітко не вказане інакше. 19 UA 112329 C2 5 10 15 20 25 30 35 40 45 50 Композиції, проліки і способи, описані тут, можуть бути ілюстровані наступними варіантами, перерахованими в пронумерованих параграфах, представлених нижче. У одному типовому варіанті, даний винахід стосується композиції проліків, яка містить щонайменше один кон'югат, де кон'югат містить щонайменше один гідроморфон і щонайменше одну арилкарбонову кислоту. Далі, композиція проліків також може містити щонайменше один гідроморфон і щонайменше одну арилкарбонову кислоту, хімічно зв'язані одне з одним взаємодією групи карбонової кислоти арилкарбонової кислоти з С-6 енольним таутомером гідроморфону. Далі, композиція проліків може включати або використовувати щонайменше один гідроморфон і щонайменше одну арилкарбонову кислоту, хімічно зв'язані одне з одним взаємодією групи карбонової кислоти арилкарбонової кислоти з С-3 гідроксилом гідроморфону. Більше того, такі типові композиції проліків також можуть містити або застосовувати щонайменше один гідроморфон і щонайменше одну арилкарбонову кислоту, хімічно зв'язані одне з одним взаємодією групи карбонової кислоти однієї арилкарбонової кислоти з С-6 енольним таутомером гідроморфону і однієї арилкарбонової кислоти з С-3 гідроксилом гідроморфону. Повинно бути зрозуміло, що будь-який з описаних вище типових варіантів/композицій може включати або застосовувати щонайменше одну арилкарбонову кислоту, що містить карбоксильну групу, приєднану до щонайменше однієї арильної групі. У щонайменше одному альтернативному варіанті таких композицій проліків щонайменше одна арилкарбонова кислота може бути вибрана з групи, яка включає, наприклад, бензоати і гетероарилкарбонові кислоти. У інших варіантах композицій проліків гетероарилкарбонову кислоту вибирають з групи, яка включає піридин, діазин і триазин. У деяких варіантах композицій проліків, бензоат має наступну загальну формулу I: , 1 2 3 де R , R і R незалежно вибирають з групи, яка включає водень, гідроксил, аміно, амін, амід, тіол, ціано, нітро, галоген, імін, алкіл, алкокси, арил, алкеніл, алкініл, галогеналкіл, алкіларил, арилалкіл, гетероцикл, арилалкокси, циклоалкіл, циклоалкеніл, циклоалкініл, карбоніл, тіоефір, селеноефір, силіл, силілокси, сульфоніл, фосфонат. У додаткових варіантах композицій проліків бензоат можуть бути вибрані з групи, яка включає, наприклад, амінобензоати, гідроксибензоати і аміногідроксибензоати, їх суміші і їх похідні. Більше того, композиції проліків можуть містити або застосовувати амінобензоат, який вибирають з групи, що включає, наприклад, антранілінову кислоту, 3-амінобензойну кислоту, 4,5-диметилантранілінову кислоту, N-метилантранілінову кислоту, N-ацетилантранілінову кислоту, фенамінові кислоти, 2,4-діамінобензойну кислоту (2,4-DABA), 2-ацетиламіно-4амінобензойну кислоту, 4-ацетиламіно-2-амінобензойну кислоту і 2,4-діацетиламінобензойну кислоту, їх суміші їх похідні. Більше того, композиції проліків можуть містити або застосовувати гідроксибензоат, який вибирають з групи, що включає, наприклад, бензойну кислоту, саліцилову кислоту, ацетилсаліцилову кислоту (аспірин), 3-гідроксибензойну кислоту, 4-гідроксибензойну кислоту, 6-метилсаліцилову кислоту, o, м,п-крезотинову кислоту, анакардинові кислоти, 4,5диметилсаліцилову кислоту, o, м,п-тимотинову кислоту, дифлузинал, o, м,п-анізинову кислоту, 2,3-дигідроксибензойну кислоту (2,3-DHB), α,β,γ-резорцилову кислоту, протокатехову кислоту, гентизинову кислоту, піперонілінову кислоту, 3-метоксисаліцилову кислоту, 4метоксисаліцилову кислоту, 5-метоксисаліцилову кислоту, 6-метоксисаліцилову кислоту, 3гідрокси-2-метоксибензойну кислоту, 4-гідрокси-2-метоксибензойну кислоту, 5-гідрокси-2метоксибензойну кислоту, ванілінову кислоту, ізованілінову кислоту, 5-гідрокси-3метоксибензойну кислоту, 2,3-диметоксибензойну кислоту, 2,4-диметоксибензойну кислоту, 2,5диметоксибензойну кислоту, 2,6-диметоксибензойну кислоту, вератринову кислоту (3,4диметоксибензойну кислоту), 3,5-диметоксибензойну кислоту, галієву кислоту, 2,3,4тригідроксибензойну кислоту, 2,3,6-тригідроксибензойну кислоту, 2,4,5-тригідроксибензойну кислоту, 3-O-метилгалієву кислоту (3-OMGA), 4-O-метилгалієву кислоту (4-OMGA), 3,4-Oдиметилгалієву кислоту, бузкову кислоту і 3,4,5-триметоксибензойну кислоту, їх суміші і їх похідні. У інших альтернативних варіантах, композиції проліків можуть містити або застосовувати аміногідроксибензоат, який вибирають з групи, що включає, наприклад, 4аміносаліцилову кислоту, 3-гідроксіантранілінову кислоту і 3-метоксіантранілінову кислоту, їх суміші і їх похідні. 20 UA 112329 C2 5 10 15 20 25 30 35 40 45 У додаткових варіантах, композиції проліків можуть містити або застосовувати щонайменше одну арилкарбонову кислоту, яка включає карбоксильну групу, яка зв'язана вуглецевим зв'язком з арильною групою. У інших варіантах, композиції проліків можуть містити або застосовувати щонайменше, одну арилкарбонову кислоту, яку вибирають з групи, яка включає розгалужені фенілпропіонові кислоти і фенілацетати, їх суміші і їх похідні. Більше того, композиції проліків можуть містити або застосовувати фенілацетат, що має наступну загальну структуру II: , 1 2 3 4 де R , R , R і R незалежно вибирають з групи, що включає, наприклад, водень, гідроксил, аміно, амін, амід, тіол, ціано, нітро, галоген, імін, алкіл, алкокси, арил, алкеніл, алкініл, галогеналкіл, алкіларил, арилалкіл, гетероцикл, арилалкокси, циклоалкіл, циклоалкеніл, циклоалкініл, карбоніл, тіоефір, селеноефір, силіл, силілокси, сульфоніл, фосфонат. У додаткових варіантах, композиції проліків можуть містити або застосовувати фенілацетат, який вибирають з групи, що включає, наприклад, фенілоцтову кислоту (гідратропову кислоту), 2гідроксифенілоцтову кислоту, 3-гідроксифенілоцтову кислоту, 4-гідроксифенілоцтову кислоту, гомопротокатехову кислоту, гомогентизинову кислоту, 2,6-дигідроксифенілоцтову кислоту, гомованілінову кислоту, гомоізованілінову кислоту, гомовалератринову кислоту, атропову кислоту, d, l-тропову кислоту, диклофенак, d, l-мигдалеву кислоту, 3,4-дигідрокси-d, l-мигдалеву кислоту, ваніліл-d, l-мигдалеву кислоту, ізованіліл-d, l-мигдалеву кислоту, ібупрофен, фенопрофен, карпрофен, флурбіпрофен, кетопрофен і напроксен, їх суміші і їх похідні. У деяких додаткових варіантах, композиції проліків можуть містити або застосовувати щонайменше одну арилкарбонову кислоту, яка містить карбоксильну групу, яка зв'язана двовуглецевим зв'язком з арильною групою. Крім того, композиції проліків можуть містити або застосовувати щонайменше одну арилкарбонову кислоту, яку вибирають з групи, яка включає бензилацетати і цинамати, їх суміші і їх похідні. Далі, композиції проліків можуть містити або застосовувати щонайменше, одну арилкарбонову кислоту, яку вибирають з групи, що включає, наприклад, бензилацетати і цинамати, що мають наступну загальну формулу III або IV або їх поєднання: , 1 2 3 4 де R , R , R і R незалежно вибирають з групи, яка включає водень, гідроксил, аміно, амін, амід, тіол, ціано, нітро, галоген, імін, алкіл, алкокси, арил, алкеніл, алкініл, галогеналкіл, алкіларил, арилалкіл, гетероцикл, арилалкокси, циклоалкіл, циклоалкеніл, циклоалкініл, карбоніл, тіоефір, селеноефір, силіл, силілокси, сульфоніл, фосфонат. У додаткових варіантах, композиції проліків можуть містити або застосовувати бензилацетат, який вибирають з групи, що включає, наприклад, бензилоцтову кислоту, мелілотову кислоту, 3-гідроксифенілпропанову кислоту, 4-гідроксифенілпропанову кислоту, 2,3дигідроксифенілпропанову кислоту, d, l-фенілмолочну кислоту, o, м,п-гідрокси-d, l-фенілмолочну кислоту і фенілпіровиноградну кислоту, їх суміші і їх похідні. У альтернативних варіантах, композиції проліків можуть містити або застосовувати цинамат, який вибирають з групи, що включає, наприклад, коричну кислоту, o, м,п-кумаринову кислоту, 2,3-дигідроксикоричну кислоту, 2,6-дигідроксикоричну кислоту, кофеїнову кислоту, ферулінову кислоту, ізоферулінову кислоту, 5-гідроксиферулінову кислоту, синапову кислоту і 2-гідрокси-3-фенілпропеноеву кислоту, їх суміші і їх похідні. У деяких варіантах, композиції проліків можуть містити або застосовувати щонайменше одну арилкарбонову кислоту, яка містить карбоксильну групу, приєднану до арильної групи кільця 21 UA 112329 C2 5 10 15 20 25 30 алкільним ланцюгом. У інших варіантах, композиції проліків можуть містити або застосовувати алкільний ланцюг, який містить один вуглець. У інших варіантах, композиції проліків можуть містити або застосовувати алкільний ланцюг, який містить два вуглеці. У інших варіантах, композиції проліків можуть містити або застосовувати щонайменше одну арилкарбонову кислоту, яка містить карбоксильну групу, приєднану до арильної групи алкенільним ланцюгом. У інших варіантах, композиції проліків можуть містити або застосовувати алкенільний ланцюг, який містить два вуглеці. У інших варіантах, композиції проліків можуть містити або застосовувати щонайменше одну арилкарбонову кислоту, яка містить один або більше бічних ланцюгів. У додаткових варіантах, композиції проліків можуть містити або застосовувати щонайменше одну арилкарбонову кислоту, яка містить одну або більше функціональних груп. У альтернативних варіантах, композиції проліків можуть містити або застосовувати щонайменше одну арилкарбонову кислоту, яка містить щонайменше одну гетероарилкарбонову кислоту. У деяких варіантах, композиції проліків можуть містити або застосовувати гетероарилкарбонову кислоту, яка має, наприклад, одну з наступних загальних формул V, VI, VII, VIII, IX, X, XI, XII або XIII або їх поєднання: , 1 2 3 де R , R і R незалежно вибирають з групи, яка включає водень, гідроксил, аміно, амін, амід, тіол, ціано, нітро, галоген, імін, алкіл, алкокси, арил, алкеніл, алкініл, галогеналкіл, алкіларил, арилалкіл, гетероцикл, арилалкокси, циклоалкіл, циклоалкеніл, циклоалкініл, карбоніл, тіоефір, селеноефір, силіл, силілокси, сульфоніл, фосфонат. У інших варіантах, композиції проліків можуть містити або застосовувати гетероарильну групу, яка містить один гетероатом. У інших варіантах, композиції проліків можуть містити або застосовувати гетероарилкарбонову кислоту, тобто, наприклад, щонайменше один піридин або похідне піридину. У додаткових варіантах, композиції проліків можуть містити або застосовувати гетероарилкарбонову кислоту, яку вибирають з групи, що включає, наприклад, нікотинову кислоту (ніацин), ізонікотинову кислоту, піколінову кислоту, 3-гідроксипіколінову кислоту, 6гідроксинікотинову кислоту, цитразинову кислоту, 2,6-дигідроксинікотинову кислоту, кінуренову кислоту, ксантуренову кислоту, 6-гідроксикінуренову кислоту, 8-метоксикінуренову кислоту, 7,8дигідроксикінуренову кислоту і 7,8-дигідро-7,8-дигідроксикінуренову кислоту, їх суміші і їх похідні. У інших варіантах, композиції проліків можуть містити або застосовувати гетероарильну групу, яка містить два гетероатоми. У інших варіантах, композиції проліків можуть містити або застосовувати гетероарилкарбонову кислоту, наприклад, щонайменше один піразин, піримідин, 22 UA 112329 C2 5 10 15 20 25 30 35 40 45 50 55 60 піридазин або їх похідні. У інших варіантах, композиції проліків можуть містити або застосовувати гетероарильну групу, яка містить три гетероатоми. У додаткових варіантах, композиції проліків можуть містити або застосовувати гетероарилкарбонову кислоту, яка є щонайменше однією з 1,2,3-триазину, 1,2,4-триазину, 1,3,5-триазину або їх похідних. У інших варіантах, композиції проліків можуть містити або застосовувати щонайменше одну арилкарбонову кислоту, що містить шестичленне кільце. Більше того, композиції проліків можуть містити або застосовувати шестичленне кільце, яке містить додаткові заміщені або незаміщені ароматичні або аліфатичні кільця. У інших варіантах, композиції проліків можуть містити або застосовувати щонайменше, одну арилкарбонову кислоту, яка містить тільки одну вільну групу карбонової кислоти. У інших варіантах, композиції проліків можуть містити або застосовувати щонайменше одну арилкарбонову кислоту, яка містить, наприклад, від 1 до 4 замісників на арильному кільці. У інших варіантах, композиції проліків відповідно до даного винаходу можуть бути у вигляді кон'югата, який є нейтральними проліками. У інших варіантах, композиції проліків відповідно до даного винаходу можуть бути в формі кон'югата, який є вільною кислотою. У інших варіантах, композиції проліків відповідно до даного винаходу можуть бути в формі кон'югата, який є вільною основою. У інших варіантах, композиції проліків відповідно до даного винаходу можуть бути в формі кон'югата, який є фармацевтично прийнятною аніонною або катіонною сольовою формою або сумішшю солей. У деяких варіантах, композиції проліків відповідно до даного винаходу можуть бути в формі солі, яку вибирають з групи, що включає, наприклад, ацетат, lаспартат, безилат, бікарбонат, карбонат, d-камзилат, l-камзилат, цитрат, едизилат, формиат, фумарат, глюконат, гідробромід/бромід, гідрохлорид/хлорид, d-лактат, l-лактат, d, l-лактат, d, lмалат, l-малат, d-малат, мезилат, памоат, фосфат, сукцинат, сульфат, бісульфат, d-тартрат, lтартрат, d, l-тартрат, мезотартрат, бензоат, глуцептат, d-глюкуронат, гібензат, ізетіонат, малонат, метилсульфат, 2-напсилат, нікотинат, нітрат, оротат, стеарат, тозилат, тіоціанат, ацефілінат, ацетурат, аміносаліцилат, аскорбат, борат, бутират, камфорат, камфокарбонат, деканоат, гексаноат, холат, ципіонат, дихлорацетат, едентат, етилсульфат, фурат, фузидат, галактарат (мукат), галактуронат, галат, гентизат, глутамат, глутарат, гліцерофосфат, гептаноат (енантат), гідроксибензоат, гіпурат, фенілпропіонат, йодид, ксинафоат, лактобіонат, лаурат, малеат, міндалят, метансульфонат, міристат, нападизилат, олеат, оксалат, пальмітат, пікрат, півалат, пропіонат, пірофосфат, саліцилат, саліцилсульфат, субсаліцилат, танат, терефталат, тіосаліцилат, триброфенат, валерат, вальпроат, адипат, 4-ацетамідобензоат, камзилат, октаноат, естолат, езилат, гліколят, тіоціанат, ундециленат, натрій, калій, кальцій, магній, цинк, алюміній, літій, холінат, лізиній, амоній і трометамін, їх суміші і їх похідні. У певних варіантах даного винаходу композиції проліків можуть розкладатися in vivo з виділенням активного гідроморфону, арилкарбонової кислоти, їх похідних і їх метаболітів. У інших варіантах, композиції проліків відповідно до даного винаходу можуть бути у вигляді проліків, які вводять перорально і гідролізують in vivo з виділенням гідроморфону з проліків. У додаткових варіантах, композиції проліків відповідно до даного винаходу можуть бути у вигляді проліків, які демонструють відсутність або обмежену фармакологічну дію при введенні. У інших варіантах, композиції проліків відповідно до даного винаходу можуть бути у вигляді проліків, які виділяють гідроморфон так само, як і вільний або немодифікований гідроморфон при введенні в еквімолярних дозах. У інших варіантах, композиції проліків відповідно до даного винаходу можуть виділяти гідроморфон в системний кровотік в знижених/контрольованих кількостях при введенні проліків шляхом, відмінним від перорального. У інших варіантах, композиції проліків відповідно до даного винаходу можуть бути у вигляді проліків, які виділяють гідроморфон контрольованим або уповільненим чином при введенні. У певних варіантах відповідно до даного винаходу, композиції проліків можуть бути у вигляді проліків, які не викликають або викликають незначні побічні ефекти в порівнянні з немодифікованим гідроморфоном при введенні в еквімолярних дозах. У інших варіантах, композиції проліків можуть бути у вигляді проліків, які демонструють відсутність або знижені побічні ефекти, вибрані з, наприклад, запаморочення, нудоти, сонливості, блювання, констипації, болю в шлунку, висипу, утрудненого сечовипускання, утрудненого дихання, нейрозбуджувальної дії або непритомності. У інших варіантах відповідно до даного винаходу, композиції проліків не дають високі концентрації гідроморфону в плазмі або крові в порівнянні з немодифікованим гідроморфоном при введенні в еквімолярних дозах внутрішньовенним або інтраназальним способами. У інших варіантах, композиції проліків не викликають або знижують ейфорію або подібні ефекти при інтраназальному введенні. У інших варіантах, композиції проліків не викликають або знижують ейфорію або подібні ефекти при внутрішньовенному введенні. У альтернативних варіантах, 23 UA 112329 C2 5 10 15 20 25 30 35 40 45 50 55 60 композиції проліків не дають швидкий пік концентрації гідроморфону (Cmax) в крові або плазмі при пероральному введенні. У додаткових варіантах, композиції проліків демонструють відкладений Tmax в порівнянні з немодифікованим гідроморфоном при пероральному введенні в еквімолярних дозах. У інших варіантах, композиції проліків демонструють більш низьке значення Cmax в порівнянні з немодифікованим гідроморфоном при пероральному введенні в еквімолярних дозах. У додаткових варіантах, композиції проліків демонструють підвищену відносну біодоступність гідроморфону в порівнянні з немодифікованим гідроморфоном при пероральному введенні в еквімолярних дозах. У інших варіантах, композиції проліків демонструють більш високе значення Cmax в порівнянні з немодифікованим гідроморфоном при пероральному введенні в еквімолярних дозах. У альтернативних варіантах, композиції проліків мають більш високе значення ППК в порівнянні з немодифікованим гідроморфоном при пероральному введенні в еквімолярних дозах. У додаткових варіантах, композиції проліків демонструють більш високі значення Cmax і ППК в порівнянні з немодифікованим гідроморфоном при пероральному введенні в еквімолярних дозах. У інших варіантах відповідно до даного винаходу композиції проліків не вивільняють гідроморфон при фізичних маніпуляціях з композицією. У додаткових варіантах, композиції проліків демонструють стійкість до певних хімічних маніпуляцій з метою вивільнення вільного гідроморфону. У додаткових варіантах відповідно до даного винаходу композиції проліків не надають або надають незначну дію на μ-опіоїдні рецептори. У інших варіантах, композиції проліків не схильні або обмежено схильні до ферментного гідролізу доти, поки вони не адсорбуються в кишечнику. У додаткових варіантах, композиції проліків демонструють знижене перетворення в гідроморфон-3-глюкуронід (H3G) в порівнянні з немодифікованим гідроморфоном при пероральному введенні в еквімолярних дозах. У інших варіантах відповідно до даного винаходу композиції проліків запобігають або знижують викликану опіоїдом констипацію (ВОК) в порівнянні з немодифікованим гідроморфоном при пероральному введенні в еквімолярних дозах. У певних варіантах відповідно до даного винаходу композиції проліків, крім того, містять, наприклад, ібупрофен, ацетамінофен або аспірин. У деяких варіантах даного винаходу, композиції проліків містять або застосовують кон'югат, який вибирають з групи, що включає, наприклад, 3-аспірин-гідроморфон, 3,6-діаспірин-гідроморфон, 6-oсаліцилат-гідроморфон, 3цинамат-гідроморфон, 6-напроксен-гідроморфон, 3-ізоніацин-гідроморфон, 3-п-саліциловийгідроморфон, 3-фенамат-гідроморфон, 3-бензоат-гідроморфон і 3,6-ди-бензоат-гідроморфон. У інших варіантах відповідно до даного винаходу композиції проліків мають пероральну лікарську форму. У додаткових варіантах, композиції проліків мають пероральну лікарську форму, яку вибирають з групи, що включає, наприклад, таблетки, капсули, каплети, пастилки, таблетки для розсмоктування, порошок, суспензію, сироп, розчин, м'які желатинові капсули, суспензію, під'язикові краплі і пероральні тонкі плівки (ПТП). У певних варіантах, композиції проліків мають пероральну лікарську форму, яка є твердою лікарською формою. У інших варіантах, композиції проліків мають тверду лікарську форму і також містять щонайменше один наповнювач. У інших варіантах, композиції проліків містять наповнювач, який вибирають з групи, що включає, наприклад, антиадгезиви, зв'язувальні агенти, покриття, розпушувачі, наповнювачі, смакові добавки, барвники, гліданти, мастильні агенти, консерванти, сорбенти і підсолоджувачі. У додаткових варіантах, композиції проліків складені в таблетки, капсули, капсули з модифікованим вивільненням, м'які желатинові капсули, таблетки з пролонгованим виділенням, капсули з контрольованим вивільненням, супозиторії, порошки для ін'єкцій, пероральні рідини, сиропи від кашлю, черезшкірні плівки, суспензії або ін'єкції. У інших варіантах відповідно до даного винаходу композиції проліків мають пероральну дозу, яка еквімолярна від близько 0,1 мг до близько 200 мг немодифікованого гідроморфону. У додаткових варіантах, композиції проліків мають пероральну дозу, еквімолярну від близько 1 мг до близько 200 мг немодифікованого гідроморфону. У інших варіантах, композиції проліків мають пероральну дозу, еквімолярну від близько 2 мг до близько 8 мг немодифікованого гідроморфону. У інших варіантах, композиції проліків мають пероральну дозу, еквімолярну від близько 8 мг до близько 60 мг немодифікованого гідроморфону. У додаткових варіантах, композиції проліків мають пероральну дозу, еквімолярну від близько 60 мг до близько 200 мг немодифікованого гідроморфону. Інші варіанти відповідно до даного винаходу стосуються способів лікування пацієнта, потребуючого знеболюючої дії, введенням ефективної кількості будь-якої композиції проліків відповідно до даного винаходу. Додаткові варіанти відповідно до даного винаходу стосуються лікування пацієнта, потребуючого придушення кашлю, введенням ефективної кількості будь 24 UA 112329 C2 5 10 15 20 25 30 35 40 45 50 55 якої композиції проліків відповідно до даного винаходу. У додаткових варіантах, даний винахід стосується способу лікування пацієнта, потребуючого терапії наркотичної і лікарської залежності, введенням ефективної кількості будь-якої композиції проліків відповідно до даного винаходу. У певних способах лікування відповідно до даного винаходу композиції проліків мають пероральну лікарську форму. У інших способах відповідно до даного винаходу, композиції проліків мають пероральну лікарську форму, яку вибирають з групи, що включає, наприклад, таблетки, капсули, каплети, пастилки, таблетки для розсмоктування, порошок, суспензію, сироп, розчин, м'які желатинові капсули, суспензію, під'язикові краплі і пероральні тонкі плівки (ПТП). У додаткових способах лікування відповідно до даного винаходу композиції проліків мають тверду лікарську форму. У інших варіантах, способи лікування відповідно до даного винаходу включають композиції проліків в твердій лікарській формі, які також містять наповнювач. У додаткових варіантах, способи лікування відповідно до даного винаходу включають композиції проліків в твердій лікарській формі, які також містять наповнювач, який вибирають з групи, що включає, наприклад, антиадгезиви, зв'язувальні агенти, покриття, розпушувачі, наповнювачі, смакові добавки, барвники, гліданти, мастильні агенти, консерванти, сорбенти і підсолоджувачі. У інших варіантах, в способах відповідно до даного винаходу застосовують композиції проліків, які складені в, наприклад, таблетки, капсули, капсули з модифікованим вивільненням, м'які желатинові капсули, таблетки з пролонгованим виділенням, капсули з контрольованим вивільненням, супозиторії, порошки для ін'єкцій, пероральні рідини, сиропи від кашлю, черезшкірні плівки, суспензії або ін'єкції. У інших варіантах, в способах відповідно до даного винаходу застосовують композиції проліків, які мають пероральну дозу, еквімолярну від близько 0,1 мг до близько 200 мг немодифікованого гідроморфону. У додаткових варіантах, в способах відповідно до даного винаходу застосовують композиції проліків, які мають пероральну дозу, еквімолярну від близько 2 мг до близько 8 мг немодифікованого гідроморфону. У інших варіантах, в способах відповідно до даного винаходу застосовують композиції проліків, які мають пероральну дозу, еквімолярну від близько 8 мг до близько 60 мг немодифікованого гідроморфону. У інших варіантах, в способах відповідно до даного винаходу застосовують композиції проліків, які мають пероральну дозу, еквімолярну від близько 60 мг до близько 200 мг немодифікованого гідроморфону. Додаткові варіанти відповідно до даного винаходу стосуються способів синтезу будь-яких композицій проліків відповідно до даного винаходу, де синтез включає стадії хімічного зв'язування щонайменше однієї арилкарбонової кислоти з щонайменше одним гідроморфоном. У інших варіантах, способи синтезу будь-якої композиції проліків відповідно до даного винаходу стосуються синтезу, наприклад, 3-аспірин-гідроморфону, 3,6-діаспірин-гідроморфону, 6саліцилат-гідроморфону, 3-цинамат-гідроморфону і 3-бензоат-гідроморфону. Інші варіанти відповідно до даного винаходу стосуються фармацевтичного набору, що містить певну кількість окремих доз композиції проліків відповідно до даного винаходу в упаковці, що містить фармацевтично ефективну кількість щонайменше одного кон'югата, де кон'югат містить щонайменше один гідроморфон і щонайменше одну арилкарбонову кислоту. У інших варіантах, набори відповідно до даного винаходу включають спосіб лікування або профілактики болю у людини або тварини. У додаткових варіантах, набори відповідно до даного винаходу призначені для лікування дітей, немолодих пацієнтів і/або пацієнтів середнього віку. У інших варіантах, набори відповідно до даного винаходу включають окремі дози композиції проліків відповідно до даного винаходу, що містять щонайменше близько 0,1 мг або вище щонайменше одного кон'югата відповідно до даного винаходу. У інших варіантах, набори відповідно до даного винаходу включають окремі дози композиції(ій) проліків відповідно до даного винаходу, що містять щонайменше близько 1 мг, близько 2,5 мг, близько 5,0 мг, близько 10 мг, близько 20 мг, близько 50 мг, близько 100 мг, близько 200 мг, близько 500 мг або вище щонайменше одного кон'югата відповідно до даного винаходу. У додаткових варіантах, набори відповідно до даного винаходу включають від близько 1 до близько 90, близько 1 до близько 60 або близько 10 до близько 30 окремих доз щонайменше однієї композиції проліків відповідно до даного винаходу. Описаний тут винахід описаний за допомогою повних, однозначних, чітких і точних термінів, зрозумілих фахівцям в даній галузі техніки, для яких він призначений, для його застосування на практиці. Повинно бути зрозуміло, що представлені вище переважні варіанти винаходу, і в нього можуть бути внесені модифікації, що не виходять за суть або об'єм винаходу, представлені в формулі винаходу. 60 25 UA 112329 C2 ФОРМУЛА ВИНАХОДУ 5 10 15 20 25 30 35 1. Композиція проліків, яка містить щонайменше один кон'югат, де щонайменше одним кон'югатом є 3,6-діаспірингідроморфон. 2. Композиція проліків за п. 1, де щонайменше один кон'югат застосовують для лікування наркотичного або опіоїдного зловживання; для запобігання наркотичній або опіоїдній відміні; для лікування від помірного до гострого болю; для зниження або запобігання пероральній, інтраназальній або внутрішньовенній лікарській залежності або для отримання стійкості до пероральної, інтраназальної або внутрішньовенної лікарської залежності. 3. Композиція проліків за п. 1, де пероральне введення щонайменше одного кон'югата дає поліпшену ППК і швидкість виділення протягом часу в порівнянні з некон'югованим гідроморфоном протягом одного і того ж періоду часу. 4. Композиція проліків за п. 1, де пероральне введення щонайменше одного кон'югата дає меншу варіабельність в пероральному профілі ФК в порівнянні з некон'югованим гідроморфоном. 5. Композиція проліків за п. 1, де пероральне введення щонайменше одного кон'югата викликає менші побічні ефекти в порівнянні з некон'югованим гідроморфоном. 6. Композиція проліків за п. 5, де зниженим побічним ефектом є знижена викликана опіоїдом констипація. 7. Композиція проліків за п. 1, де щонайменше один кон'югат представлений в лікарській формі, вибраній з групи, яка включає таблетки, капсули, каплети, супозиторії, пастилки, таблетки для розсмоктування, пероральний порошок, розчин, пероральну плівку, тонку смужку, завись і суспензію. 8. Композиція проліків за п. 1, де пероральне введення щонайменше одного кон'югата дає терапевтично біоеквівалентну ППК і/або біоеквівалентний або більш низький С mах в порівнянні з еквівалентною молярною кількістю некон'югованого гідроморфону. 9. Композиція проліків за п. 1, де інтраназальне або внутрішньовенне введення щонайменше одного кон'югата дає більш низьку ППК і/або Сmах в порівнянні з еквівалентною молярною кількістю некон'югованого гідроморфону. 10. Композиція проліків за п. 1, де пероральне введення щонайменше одного кон'югата забезпечує знижену можливість передозування в порівнянні з еквівалентною молярною кількістю некон'югованого гідроморфону. 11. Композиція проліків за п. 1, де щонайменше один кон'югат забезпечує підвищену стійкість до втручання в порівнянні з некон'югованим гідроморфоном. 12. Спосіб лікування пацієнта, який страждає на захворювання, розлад або стан, опосередкований зв'язуванням опіоїду з рецепторами опіоїду пацієнта, що включає пероральне введення пацієнту фармацевтично ефективної кількості композиції проліків, яка містить щонайменше один кон'югат за п. 1. 26 UA 112329 C2 27 UA 112329 C2 28
ДивитисяДодаткова інформація
Автори англійськоюMickle, Travis, Guenther, Sven, Chi, Guochen, Kanski, Jaroslaw, Martin, Andrea K., Bera, Bindu
Автори російськоюМикл Трэвис, Гюнтер Свэн, Чи Гочень, Каньски Ярослав, Мартин Андреа К., Бэра Бинду
МПК / Мітки
МПК: A61K 31/485, C07D 489/00
Мітки: лікування, гідроморфоном, кон'югат, захворювання, проліків, містить, композиція, спосіб, аспірину
Код посилання
<a href="https://ua.patents.su/43-112329-kompoziciya-prolikiv-shho-mistit-konyugat-aspirinu-z-gidromorfonom-ta-sposib-likuvannya-zakhvoryuvannya.html" target="_blank" rel="follow" title="База патентів України">Композиція проліків, що містить кон’югат аспірину з гідроморфоном, та спосіб лікування захворювання</a>
Попередній патент: Ментолвмісний курильний виріб
Наступний патент: З’єднувальний пристрій для причепів самохідної робочої машини
Випадковий патент: Спосіб виробництва прокату з кольорового металу