Солі [1,3,4]оксадіазоло[2,3-b][1,4,3]тіаселеназин-4-ію і [1,3]тіазоло[2,3-b][1,4,3]оксадіазол-4-ію, що мають антимікробну активність
Номер патенту: 61996
Опубліковано: 10.08.2011
Автори: Лендєл Василь Георгійович, Сливка Михайло Васильович, Кривов'яз Андрій Олександрович, Коваль Галина Миколаївна
Формула / Реферат
Солі [1,3,4]оксадіазоло[2,3-b][1,4,3]тіаселеназин-4-ію й [1,3]тіазоло[2,3-b][1,4,3]-оксадіазол-4-ію, загальної формули (І, II):
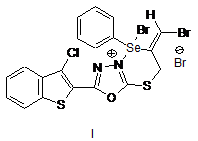 ,
,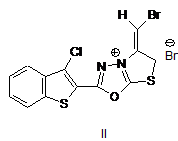 ,
,
що мають бактерицидну та бактеріостатичну активність по відношенню до грампозитивних й грамнегативних мікроорганізмів, включаючи збудників нозокоміальних госпітальних інфекцій.
Текст
Солі [1,3,4]оксадіазоло[2,3b][1,4,3]тіаселеназин-4-ію й [1,3]тіазоло[2,3b][1,4,3]оксадіазол-4-ію, загальної формули (І, II): H Br Se Cl II , що мають бактерицидну та бактеріостатичну активність по відношенню до грампозитивних й грамнегативних мікроорганізмів, включаючи збудників нозокоміальних госпітальних інфекцій. H Br N N Br S Br O Cl S , U 61996 Br Cl H Br N N Br N N S S I S Br Br Br S O , II S що мають бактерицидну та бактеріостатичну актиO вність по відношенню до грампозитивних й грамнегативних мікроорганізмів, включаючи збудників нозокоміальних госпітальних інфекцій. II Відомі бактерицидні речовини, які містять фрагмент 1,3,4-оксадіазолу, але вони містять сульфогетарільні замісники складної будови і тому їх UA Br Se H (11) II Корисна модель належить до органічної хімії, H а саме до солей [1,3,4]оксадіазоло[2,3Br b][1,4,3]тіаселеназин-4-ію й [1,3]тіазоло[2,3Se b][1,4,3]-оксадіазол-4-ію, загальної формули (І, II): Cl N N H I (13) S O S O Br N N , S O S S I Cl Br N N S Cl Br O Br Br N N S H (19) Cl [1,3]ТІАЗОЛО[2,3 3 61996 одержання характеризуються складним багатоступінчатим синтезом [1, 2]. Найбільш близькими за технічною суттю до заявлених є похідні 2-аміно1,3,4-оксадіазолів, які характеризуються низькою токсичністю, і які мають високу бактерицидну й бактеріостатичну активність до грам позитивних бактерій лише при відносно високих (вище 400 мкг/мл) концентраціях [3]. Ці солі характеризуються простотою синтезу, низькою токсичністю і є активними лише по відношенню до грам позитивних мікроорганізмів, тобто, вони не виявляють антимікробну активність по H відношенню до грамнегативних мікроорганізмів. Br Задачею корисної моделі є створення речовин Se Cl класу оксадіазолу, а саме конденсованих оксадіаN N золів, які мають бактерицидну та бактеріостатичну активність по відношенню до всіх прокаріотичних S мікроорганізмів, а особливо збудників нозокоміаO S льних госпітальних інфекцій. Поставлена задача вирішується синтезом та I використанням солей [1,3,4]оксадіазоло[2,3b][1,4,3]тіаселеназин-4-ію й [1,3]тіазоло[2,3b][1,4,3]-оксадіазол-4-ію, загальної формули (І, II): 4 H Br Se Cl , H O S Br N N O S II , що мають бактерицидну та бактеріостатичну активність по відношенню до грампозитивних й грамнегативних мікроорганізмів, включаючи збудників нозокоміальних госпітальних інфекцій. Суть корисної моделі досягається наступними прикладами: Приклад 1 Загальна схема синтезу сполук (І, II) Se Br Cl S III H Cl H Br Se Br S O Br N N O Br S I Br N N S Br N N S + S Br Br Cl , CH3COCH3 -C6H5SeBr II Склад сполук (І, II) підтверджено даними елементного аналізу; будову доведено методом спектроскопії протонного магнітного резонансу (ПМР) високого розділення (300 МГц); просторову геометрію олефінового протону доведено гомоядерним спектральним NOESY експериментом (ефект Оверхаузера, рис. 1). Методики синтезу сполук (І, II) 5-Бромо-6-[(E)-1-бромометиліден1-2-(3хлоробензо[b]тіофен-2-іл)-6,7-дигідро-5феніл[1,3,4]оксадіазоло[2,3-b][1,4,3]тіаселеназин4-ій бромід (І). До розчину 0,015 моль сполуки (III) [4] в 15 мл сухого хлороформу або оцтової кислоти при постійному перемішуванні протягом 30 хвилин прикапують розчин 0,015 моль фенілселентриброміду в 20 мл хлороформу або оцтової O S I Br N N S O Br Cl Cl Br N N S H Br кислоти відповідно. Вміст реакційної колби перемішують 6 години, а потім утворений світложовтий осад сполуки (II) відфільтровують та промивають діетиловим етером. З фільтрату розчинник повністю видаляють у вакуумі. Коричневий маслоподібний залишок обробляють 30 мл діетилового етеру і залишають для кристалізації. Утворений темно-жовтий порошок сполуки (І) відфільтровують, промивають діетиловим етером та сушать в ексикаторі над фосфор (V) оксидом. Порошок жовтого кольору. Вихід 47%, Ттопл. 9496°С (хлороформ). Спектр ПМР в CHCl3-D (, м.ч., J, Гц): 4,50 роз. С (2Н, СН2); 6,70 с (1Н, =CHBr); 7,39 м (3Н, 3СН, 7,2); 7,81-7,88 м (2Н, 2СН); 7,54 м (2Н, 2СН, 9,0); 7,81-7,88, 7,96 2м (4Н, 4СН). Знай II 5 61996 дено, %: С 32,23; Н 1,65; N 3,89; S 10,99; Se 9,03. С19Н12Вr3СlN2ОS2Sе. Вирахувано, %: С 32,46; Н 1,71; N 3,99; S 11,25; Se 9,11. 5-[(E)-1-бромометиліден]-2-(3хлоробензо[b]тіофен-2-іл)-5,6-дигідро[1.3]тіазоло[2.3-b][1,3,4]оксадіазол-4-ій бромід (II). До 0,015 моль сполуки (І) приливають 20 мл ацетону, інтенсивно перемішують до повного розчинення вихідної сполуки. Ацетоновий розчин знебарвлюється через 30 хвилин. Білий осад відфільтровують, промивають ацетоном та сушать на повітрі при 60°С. Кристали білого кольору. Вихід 87%, Ттопл. 112114°С (хлороформ). Спектр ПМР в CHCl3-D (, м.ч., J, Гц): 4,51 с (2Н, СН2); 6,70 с (1H, =СНВr); 7,54 д (2Н, 2СН, 9,3); 7,85, 7,96 м (2Н, 2СН). Знайдено, %: С 33,38; Н 1,45; N 5,94; Вr 34,18; S 13,69. C13H7Br2ClN2OS2 Вирахувано, %: С 33,43; Н 1,50; N 6,00; Вr 34,29; S 13,72. Для підтвердження E-конфігурації олефінового фрагменту було проведено вимірювання величини стаціонарного гомоядерного ефекту Оверхаузера для олефінового протону, при насиченні сигналу метиленових протонів основного компоненту. Виявилось, що величина зростання інтенсивності сигналу олефінового протону СН в такому експерименті не перевищує 1% (креслення - двомірний NOESY спектр сполуки II). Це свідчить про відносну віддаленість даних протонів, тобто про їх антиперипланарну орієнтацію (для альтернативного Zізомеру ефект Оверхаузера повинен був би бути в декілька разів більшим). Для дослідження бактерицидної та бактеріостатичної активності синтезованих сполук (І, II) по відношенню до запатентованих музейних штамів грампозитивних й грамнегативних мікроорганізмів, які зберігаються на кафедрі мікробіології, вірусології, імунології з курсом інфекційних хвороб медичного факультету ДВНЗ УжНУ використовували Staphylococcus aureus ATCC 25923, Sarcina flava, Pseudomonas aeruginosa ATCC 27853, Escherichia coli ATCC 25922; Bacillus subtilis 934; Klebsiella pneumoniae 5056, Klebsiella oxytoca ATCC 13182, Candida albicans ATCC 663-885, та 34 клінічні ізоляти із множинною стійкістю до антибіотиків, серед яких 9 належали до Staphylococcus spp., 17 Klebsiella spp., 5 - Escherichia coli, Pseudomonas aeruginosa - 3. Синьогнійну паличку і бацили культивували на м'ясо-пептонному агарі (МПА), для культивування кишкової застосовували середовище Ендо, грампозитивні кокові - на жовтково 6 яєчному агарі (ЖСА), кандіди вирощували на середовищі Сабуро [5]. Для вивчення ультраструктурних змін у клітинах бактерій, що відбуваються внаслідок дії досліджуваних речовин виготовляли мазки і фарбували по Граму [5]. Для визначення чутливості мікроорганізмів до новосинтезованих речовин використовували метод двократних серійних розведень в рідкому поживному середовищі, яке є оптимальним для росту тест-мікроорганізмів [6]. Під час дослідів ставили контроль середовища на стерильність, контроль розчинника. Досліди проводили у 3-х повторах, отримані результати обробляли математично. Оптимальний час дії речовин (І, II) за певних концентрацій визначали через 15 та 30 хвилин шляхом висіву на чашки Петрі з середовищем МПА, ЖСА, Сабуро чи Ендо за методом Yould [7]. Мікробне число (МЧ) - визначали за числом колонієутворюючих одиниць (КУО/мл), тобто враховувалися всі бактерії, що вижили після такої обробки і виростали на чашці з агаром через 24 години інкубації при температурі 37°С за методом [5]. Суспензії добових тест-культур готували у стерильному фізіологічному розчині NaCl, концентрацією 9 10 кл/мл та в об'ємі 0,3 мл вносили у лунки реплікатора, після чого висівали паралельно на три чашки Петрі відповідно до схеми експерименту. Результати обраховували через 24 години культивування бактерій за температури 37°С. Як контроль використовували середовище МПА без додавання синтезованих сполук (І, II). Результати порівняльної оцінки чутливості культур - представників грампозитивних й грамнегативних мікроорганізмів представлено в таблиці 1. Як видно із таблиці, сполука (І) виявила надзвичайно високий антимікробний ефект по відношенню до сапрофітних мікроорганізмів - Sarcina flava та по відношенню до грам негативних мікроорганізмів Klebsiella oxytoca ATCC 13182, Pseudom. aeruginosa ATCC 27853. Для грибків роду Candida, які є стійкими навіть до антибіотиків III-IV покоління, сполуки (І, II) виявили помірну активність. Pseudomonas aeruginosa ATCC 27853 - паличка синьо-зеленого гною, виявилась практично на 100% чутливою до сполук (І, II). Речовина (II) виявилась нейтральною для росту і розмноження Escherichia coli ATCC 25922, а сполука (II) виявила помірний ефект пригнічення росту даних бактерій. Таблиця Антимікробна активність сполук (І, II) щодо грампозитивних та грамнегативних мікроорганізмів (КУО) Вид бактерій 1 Сполука I 2 II 3 1 8 0 42 10 17 45 94 Грампозитивні мікроорганізми Staphylococcus aureus ATCC 25923 Staphylococcus albus Sarcina flava Candida albicans ATCC 653-885 7 61996 8 Продовження таблиці 1 2 8 3 14 7 0 0 24 Bacillus subtilis 934 22 8 2 CP Грамнегативні мікроорганізми Klebsiella pneumoniae 5056 Klebsiella oxytoca ATCC 13182 Pseudom. aeruginosa ATCC27853 Escherichia coli A TCC 25922 Примітка: у таблиці наведено зведені дані після висіву культури на 3-х чашках Петрі: концентрація сполук (І, II) складає 300 мкг/мл; СР - суцільний ріст бактерій. Для золотистого стафілококу (Staphylococcus aureus ATCC 25923) високу бактерицидну дію проявили як сполука (І), так і сполука (II), а для сапрофіта - білого стафілококу (Staphylococcus albus) аналогічна дія виявилась слабшою. Як бачимо дія сполук (І, II) на різні штами є не однаковою за ступенем пригнічення життєдіяльності мікроорганізмів, але спостерігається загальна закономірність щодо дії даних речовин на збудників одного й того ж виду: сполука (І) має більш широкий спектр антимікробної активності, активніше пригнічує ріст музейних штамів і клінічних ізолятів умовно патогенних мікроорганізмів з множинною стійкістюдо антибіотиків, що імовірно пов'язано із вмістом селену в її складі. В результаті цього постає питання про розробку комплексних лікарських препаратів, адже в лікарнях дані мікроорганізми перебувають в основному в складі стійких мікробних ценозів, про що свідчать проведені нами дослідження. При мікроскопічному дослідженні мазків із всіх дослідних культур під впливом новосинтезованих речовин у клітинах бактерій відбуваються ультраструктурні зміни, які вказують на порушення внутрішньоклітинного метаболізму та інгібування синтезу клітинних компонентів, що можуть бути факторами патогенності. Таким чином, позитивний ефект корисної моделі полягає в розширенні асортименту антимікробних препаратів, які мають високу активність по відношенню до прокаріотних мікроорганізмів, як музейних так і свіжовиділених штамів. Дослідження антибактеріальних властивостей новосинтезованих речовин по відношенню до збудників опортуністичних інфекцій дозволяють рекомендувати їх для подальших доклінічних та клінічних досліджень з можливим наступним застосуванням для терапії опортуністичних інфекцій. Пропоновані сполуки можуть бути використані для створення нових засобів дезінфекції, як антисептики для боротьби з патогенними мікроорганізмами, збудниками госпітальних інфекцій. Джерела інформації: 1. V. Padmavathi, G. Sudhakar Reddy, A. Padmaja, P. Kondaiah, Ali-Shazia. Synthesis, antimicrobial and cytotoxic activities of 1,3,4oxadiazoles, 1,3,4-thiadiazoles and 1,2,4-triazoles. // European Journal of Medicinal Chemistry. - V. 44 (2009), P. 2106-2112. 2. Padmavathi, A.V. Nagendra Mohan, P. Thriveni, A. Shazia. Synthesis and bioassay of a new class of heterocycles pyrrolyl oxadiazoles/thiadiazoles/triazoles. // European Journal of Medicinal Chemistry - V. 44 (2009), P. 2313-2321. 3. N.C. Desai, A.M. Bhavsar, M.D. Shah, Anil K. Saxena. Synthesis and QSAR studies of thiosemicarbazides, 1,2,4-triazoles, 1,3,4-thiadiazoles and 1,3,4-oxadiazoles derivatives as potential antibacterial agents. // Indian Journal of Chemistry. V. 47B, April 2008. - P. 579-589. - Прототип. 4. Кривов'яз А.О. Дисертація на здобуття наукового ступеня кандидата хімічних наук: 02.00.03. Київ, 2005. - 146 с. 5. Биргер М.О. Справочник по микробиологическим и вирусологическим методам исследования. - М.: Медицина, 1982. - 264 с. 6. Авдєєва Л.В., Овруцький В.М., Козлов С.Н. та співав. Скринінг антимікробної активності нових хімічних сполук. Актуальные проблемы медицины и биологии. 2000 г., №2, С. 298-302. 7. Yauld J.P. Quantity and anality in the diagnosis or ururory troot infection. // Brit. J. Urol. - 1965. - V. 37, №1. - P. 7-12. 9 Комп’ютерна верстка А. Рябко 61996 Підписне 10 Тираж 23 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюSalts of [1,3,4]oxadiazolo[2,3-b][1,4,3]thiaselenazin-4-ium and [1,3]thiazolo[2,3-b][1,4,3]-oxadiazol-4-ium exhibiting antimicrobial activity
Автори англійськоюKryvoviaz Andrii Oleksandrovych, Koval Halyna Mykolaivna, Slyvka Mykhailo Vasyliovych, Lendiel Vasyl Heorhiiovych
Автори російськоюКривовьяз Андрей Александрович, Коваль Галина Николаевна, Сливка Михаил Васильевич, Лендел Василий Георгиевич
МПК / Мітки
МПК: C12Q 1/18, C07D 517/00, C07D 498/00, C07D 513/00
Мітки: 1,3,4]оксадіазоло[2,3-b][1,4,3]тіаселеназин-4-ію, 1,3]тіазоло[2,3-b][1,4,3]оксадіазол-4-ію, солі, антимікробну, активність, мають
Код посилання
<a href="https://ua.patents.su/5-61996-soli-134oksadiazolo23-b143tiaselenazin-4-iyu-i-13tiazolo23-b143oksadiazol-4-iyu-shho-mayut-antimikrobnu-aktivnist.html" target="_blank" rel="follow" title="База патентів України">Солі [1,3,4]оксадіазоло[2,3-b][1,4,3]тіаселеназин-4-ію і [1,3]тіазоло[2,3-b][1,4,3]оксадіазол-4-ію, що мають антимікробну активність</a>
Наступний патент: Спосіб одержання діагностичної сироватки кампілобактеріозної аглютинуючої
Випадковий патент: Глибинний пробовідбірник









