Азольні і тіазольні похідні і їх застосування
Номер патенту: 95255
Опубліковано: 25.07.2011
Автори: ван ден Хевел Марко, Фінч Геррі, Булл Річард Джеймс, Браво Хосе Антоніо, Рей Ніколас Чарльз
Формула / Реферат
1. Сполука формули (І):
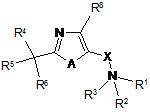 , (I)
, (I)
в якій
(і) R1 являє собою С1-С6-алкіл або водень; і R2 являє собою водень або групу -R7, -Z-Y-R7, -Z-NR9R10, -Z-CO-NR9R10, -Z-NR9-C(O)O-R7 або -Z-C(O)-R7; і R3 являє собою неподілену пару або С1-С6-алкіл; або
(іі) R1 і R3 утворюють разом з атомом азоту, до якого вони приєднані, гетероциклоалкільне кільце; і R2 являє собою неподілену пару або групу -R7, -Z-Y-R7, -Z-NR9R10, -Z-CO-NR9R10, -Z-NR9-C(O)O-R7 або -Z-C(O)-R7; або
(ііі) R1 і R2 утворюють разом з атомом азоту, до якого вони приєднані, гетероциклоалкільне кільце, причому згадане кільце заміщене групою -Y-R7, -Z-Y-R7, -Z-NR9R10, -Z-CO-NR9R10, -Z-NR9-C(O)O-R7 або -Z-C(O)-R7; і R3 являє собою неподілену пару або С1-С6-алкіл;
комбінації R4 і R5 являють собою комбінації, коли (і) кожний з R4 і R5 являє собою моноциклічний гетероарил, який містить 5 або 6 кільцевих атомів; (іі) кожний з R4 і R5 являє собою феніл; (ііі) один з R4 і R5 являє собою феніл, а інший являє собою циклоалкіл; і
(іv) один з R4 і R5 являє собою моноциклічний гетероарил, який містить 5 або 6 кільцевих атомів, а інший являє собою циклоалкіл;
R6 являє собою -ОН, С1-С6-алкіл, С1-С6-алкокси, гідроксі-С1-С6-алкіл, нітрил, групу CONR82 або атом водню;
А являє собою атом кисню або сірки;
X являє собою алкіленову, алкеніленову або алкініленову групу;
R7 являє собою С1-С6-алкільну, арильну, конденсовану з циклоалкілом арильну, конденсовану з гетероциклоалкілом арильну, гетероарильну, арил(С1-С8-алкіл)-, гетероарил(С1-С8-алкіл)-, циклоалкільну або гетероциклоалкільну групу;
R8 являє собою С1-С6-алкіл або атом водню;
Z являє собою С1-С16-алкіленову, С2-С16-алкеніленову або С2-С16-алкініленову групу;
Y являє собою зв'язок або атом кисню;
R9 і R10 незалежно являють собою атом водню, С1-С6-алкільну, арильну, конденсовану з гетероциклоалкілом арильну, конденсовану з циклоалкілом арильну, гетероарильну групу, арил(С1-С6-алкіл)- або гетероарил(С1-С6-алкіл)-; або
R9 і R10 утворюють разом з атомом азоту, до якого вони приєднані, гетероциклічне кільце яке містить 4-8 атомів і яке необов'язково містить додатковий атом азоту або кисню;
де будь-яка арильна, гетероарильна, циклоалкільна, конденсована з циклоалкілом арильна, гетероциклоалкільна і конденсована з гетероциклоалкілом арильна група може бути заміщена однією або декількома замісними групами, вибраними з ацилу, алкокси, алкоксикарбонілу, алкоксикарбоніл-N-(алкіл)аміноалкілу, алкіламіно, алкілсульфінілу, алкілсульфонілу, алкілтіо, -NH2, аміноацилу, аміноалкілу, алкіламіноалкілу, арилалкілу, ціано, діалкіламіно, галогену, галогеналкокси, галогеналкілу, алкілу, -ОН, -СНО, -СООН, -NO2, арилу (необов'язково заміщеного алкокси, галогеналкокси, галогеном, алкілом або галогеналкілом), гетероарилу (необов'язково заміщеного алкокси, галогеналкокси, галогеном, алкілом або галогеналкілом), гетероциклоалкілу, аміноацилу, аміносульфонілу, ациламіно, сульфоніламіно, гетероарилалкілу, циклічного аміну, арилокси, гетероарилокси, арилалкілокси або гетероарилалкілокси;
або її фармацевтично прийнятна сіль, сольват або N-оксид.
2. Сполука за п. 1, де:
R1 являє собою С1-С6-алкіл або атом водню;
R2 являє собою С1-С6-алкіл, атом водню або групу -Z-Y-R7, і
R3 являє собою неподілену пару або С1-С6-алкіл, або
R1 і R2 являють собою разом з атомом азоту, до якого вони приєднані, гетероциклоалкільне кільце, або
R1 і R3 утворюють разом з атомом азоту, до якого вони приєднані, гетероциклоалкільне кільце;
комбінації R4 і R5 являють собою комбінації, коли
(і) кожний з R4 і R5 являє собою моноциклічний гетероарил, який містить 5 або 6 кільцевих атомів;
(іі) кожний з R4 і R5 являє собою феніл;
(ііі) один з R4 і R5 являє собою феніл, а інший являє собою циклоалкіл; і
(іv) один з R4 і R5 являє собою моноциклічний гетероарил, який містить 5 або 6 кільцевих атомів, а інший являю собою циклоалкіл;
R6 являє собою -ОН, С1-С6-алкіл, гідроксі-С1-С6-алкіл або атом водню;
А являє собою атом кисню або сірки;
X являє собою алкіленову, алкеніленову або алкініленову групу;
Z являє собою алкіленову, алкеніленову або алкініленову групу;
Y являє собою зв'язок або атом кисню;
R7 являє собою арил, гетероарил, гетероциклоалкіл, причому арил, гетероарил або гетероциклоалкіл можуть бути заміщені однією або декількома замісними групами, визначеними в п. 1.
3. Сполука за п. 1 або п. 2, в якій R1 являє собою метил або етил, або атом водню; R2 являє собою водень, С1-С6-алкіл або групу -R7, -Z-Y-R7, -Z-NR9R10, -Z-CO-NR9R10, -Z-NR9-C(O)O-R7 або -Z-C(O)-R7; і R3 являє собою неподілену пару або С1-С6-алкіл, і в цьому випадку атом азоту, до якого він приєднаний, є четвертинним атомом азоту і несе позитивний заряд.
4. Сполука за п. 3, в якій R3 являє собою метил, тому атом азоту, до якого він приєднаний, є четвертинним атомом азоту і несе позитивний заряд.
5. Сполука за п. 1 або п. 2, в якій R1 і R3 утворюють разом з атомом азоту, до якого вони приєднані, моноциклічне гетероциклоалкільне кільце, що містить від 3 до 7 кільцевих атомів, в якому гетероатоми являють собою атоми азоту; і R2 являє собою неподілену пару або С1-С6-алкіл, або групу -R7, -Z-Y-R7, -Z-NR9R10, -Z-NR9-C(O)O-R7 або -Z-C(O)-R7.
6. Сполука за п. 5, в якій R1 і R3 утворюють разом з атомом азоту, до якого вони приєднані, азетидинільне, піперидинільне, піперазинільне, N-метилпіперазинільне або піролідинільне кільце.
7. Сполука за п. 5, в якій атом азоту, до якого приєднані R1 і R3 або R1 і R2, є четвертинним атомом азоту і несе позитивний заряд.
8. Сполуки за п. 1, в якій в будь-якій групі -R7, -Y-R7, -Z-Y-R7, -Z-NR9R10, -Z-CO-NR9R10, -Z-NR9-C(O)O-R7 або -Z-C(O)-R7:
Z являє собою -(СН2)1-8-, до трьох атомів вуглецю якої необов'язково заміщені метилом;
Y являє собою зв'язок або -О-;
R7 являє собою
метил, етил, н- або ізопропіл, н-, втор- або трет-бутил; або
феніл, 3,4-метилендіоксифеніл, 3,4-етилендіоксифеніл, дигідробензофураніл, нафтил; або
піридил, піроліл, піримідиніл, оксазоліл, ізоксазоліл, бензізоксазоліл, бензоксазоліл, тіазоліл, бензотіазоліл, хіноліл, тієніл, бензотієніл, фурил, бензофурил, імідазоліл, бензімідазоліл, ізотіазоліл, бензізотіазоліл, піразоліл, ізотіазоліл, триазоліл, бензотриазоліл, тіадіазоліл, оксадіазоліл, піридазиніл, триазиніл, індоліл або індазоліл; або
арил(С1-С6-алкіл), в якому арильна частина являє собою феніл або нафтил, і -(С1-С6-алкіл)- являє собою -СН2- або -СН2СН2-; або
гетероарил(С1-С6-алкіл), в якому гетероарильна частина являє собою піридил, піроліл, піримідиніл, оксазоліл, ізоксазоліл, бензізоксазоліл, бензоксазоліл, тіазоліл, бензотіазоліл, хіноліл, тієніл, бензотієніл, фурил, бензофурил, імідазоліл, бензімідазоліл, ізотіазоліл, бензізотіазоліл, піразоліл, ізотіазоліл, триазоліл, бензотриазоліл, тіадіазоліл, оксадіазоліл, піридазиніл, триазиніл, індоліл або індазоліл, і -(С1-С6-алкіл)- являє собою -СН2- або -СН2СН2-; або
інданіл або 1,2,3,4-тетрагідронафталеніл; або
циклопропіл, циклобутил, циклопентил або циклoгeксил; і
R9 і R10 незалежно являють собою
водень, метил, етил або н- або ізопропіл;
феніл, дигідробензофураніл, нафтил;
піридил, піроліл, піримідиніл, оксазоліл, ізоксазоліл, бензізоксазоліл, бензоксазоліл, тіазоліл, бензотіазоліл, хіноліл, тієніл, бензотієніл, фурил, бензофурил, імідазоліл, бензімідазоліл, ізотіазоліл, бензізотіазоліл, піразоліл, ізотіазоліл, триазоліл, бензотриазоліл, тіадіазоліл, оксадіазоліл, піридазиніл, триазиніл, індоліл або індазоліл; або
арил(С1-С6-алкіл), в якому арильна частина являє собою феніл або нафтил, і -(С1-С6-алкіл)- являє собою -СН2- або -СН2СН2-; або R9 і R10 утворюють разом з атомом азоту, до якого вони приєднані, азетидинільне, піперидинільне, піперазинільне, N-метилпіперазинільне, піролідинільне, морфолінільне або тіоморфолінільне кільце;
R9 і R10 незалежно вибирають з водню, С1-С6-алкілу або будь-якого з необов'язково заміщеного арилу, конденсованого з гетероциклоалкілом арилу, гетероарилу або арил(С1-С6-алкіл)-, значення яких точно визначене в цьому пункті при розгляді R7; або
R9 і R10 утворюють разом з атомом азоту, до якого вони приєднані, гетероциклічне кільце, яке містить 4-8 кільцевих атомів і яке необов'язково містить додатковий атом азоту або кисню;
і якщо R7 являє собою гетероарил, циклоалкіл, конденсований з циклоалкілом арил, гетероциклоалкіл або конденсований з гетероциклоалкілом арил, то він може бути заміщений однією або декількома замісними групами, значення яких визначене в п. 1.
9. Сполука за п. 1, в якій в групі -NR1R2R3
R1 являє собою метил або етил, R2 являє собою -Z-NR9R10 або -Z-Y-R7, Y являє собою зв'язок або -О-, і -Z- являє собою нерозгалужений або розгалужений алкіленовий радикал, який зв'язує атом азоту і -NR9R10 або -YR7 ланцюгом, що містить до 16 атомів вуглецю, і R3 являє собою метил.
10. Сполука за п. 9, в якій R7 являє собою феніл, бензил, дигідробензофурил або фенілетил, причому феніл, бензил, дигідробензофурил або фенілетил можуть бути заміщені однією або декількома замісними групами, значення яких визначене в п. 1.
11. Сполука за п. 9 або п. 10, в якій значення R9 і R10 визначені вище в п. 8.
12. Сполука за п. 1, в якій в групі -NR1R2R3
R2 являє собою -Z-NR9R10 або -Z-Y-R7, Y являє собою зв'язок або -О-, і -Z- являє собою нерозгалужений або розгалужений алкіленовий радикал, який зв'язує атом азоту і -NR9R10 або -YR7 , і є ланцюгом, що містить до 16 атомів вуглецю, і R1 і R3 утворюють разом з атомом азоту, до якого вони приєднані, гетероциклічне кільце, яке містить 4-8 кільцевих атомів і яке необов'язково містить додатковий атом азоту або кисню.
13. Сполука за п. 12, в якій R1 і R3 утворюють разом з атомом азоту, до якого вони приєднані, азетидинільне, піперидинільне, піперазинільне, N-метилпіперазинільне, піролідинільне, морфолінільне або тіоморфолінільне кільце.
14. Сполука за п. 12 або п. 13, в якій R7 переважно являє собою циклічну ліпофільну групу, таку як феніл, бензил, дигідробензофурил або фенілетил, причому фенільна, бензильна, дигідробензофурильна або фенілетильна група може бути заміщена однією або декількома замісними групами, значення яких визначене в п. 1.
15. Сполука за п. 12, в якій значення R9 і R10 визначені в п. 8.
16. Сполука за будь-яким з попередніх пунктів, в якій (і) кожний R4 і R5 являє собою тієніл; або (іі) кожний R4 і R5 являє собою феніл; або (ііі) один з R4 і R5 являє собою феніл, а інший являє собою циклопентил або циклогексил; або (iv) один з R4 і R5 являє собою тієніл, а інший являє собою циклопентил або циклогексил.
17. Сполука за п. 16, в якій R6 являє собою -ОН.
18. Сполука за будь-яким з попередніх пунктів, в якій R8 являєсобою водень.
19. Сполука за будь-яким з попередніх пунктів, в якій X являє собою -СН2- або -СН2СН2-.
20. Сполука за п. 1, яка має формулу (ІА)
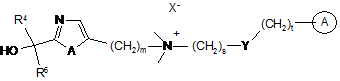 , (IA)
, (IA)
в якій А являє собою -О- або -S-;
m дорівнює 1 або 2;
кільце А являє собою необов'язково заміщене фенільне кільце або моноциклічне гетероциклічне кільце, яке містить 5 або 6 кільцевих атомів, або систему конденсованого з гетероциклоалкільним кільцем фенілу, де гетероциклоалкільне кільце являє собою моноциклічне гетероциклічне кільце, яке містить 5 або 6 кільцевих атомів;
R4 являє собою феніл, тієніл, циклопентил або циклогексил;
R5 являє собою феніл, тієніл, циклопентил або циклогексил;
s дорівнює 1, 2, 3, 4, 5, 6 або 7, і
t дорівнює 0, 1, 2, 3, 4, 5, 6 або 7,
за умови, що s+t не більше 16;
Y являє собою зв'язок або -О-, і
X- являє собою фармацевтично прийнятний аніон.
21. Сполука за п. 1, яка має формулу (IB)
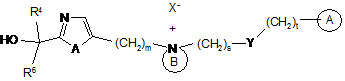 , (ІВ)
, (ІВ)
в якій А являє собою -О- або -S-; m дорівнює 1 або 2; кільце В являє собою піролідинієве або піперидинієве кільце; кільце А являє собою необов'язково заміщене фенільне кільце або моноциклічне гетероциклічне кільце, яке містить 5 або 6 кільцевих атомів, або систему конденсованого з гетероциклоалкільним кільцем фенілу, де гетероциклоалкільне кільце являє собою моноциклічне гетероциклічне кільце, яке містить 5 або 6 кільцевих атомів; R4 являє собою феніл, тієніл, циклопентил або циклогексил; R5 являє собою феніл, тієніл, циклопентил або циклогексил; s дорівнює 1, 2, 3, 4, 5, 6 або 7, і t дорівнює 0, 1, 2, 3, 4, 5, 6 або 7, за умови, що s+t не більше 16; Y являє собою зв'язок або -О-, і X- являє собою фармацевтично прийнятний аніон.
22. Сполука за п. 20 або п. 21, в якій кільце А являє собою (і) необов'язково заміщений феніл, де необов'язкові замісники вибирають з С1-С3-алкокси, галогену, С1-С3-алкілу, аміно-С1-С3-ацилу і аміно-С1-С3-алкілу, або (іі) систему конденсованого з гетероциклоалкільним кільцем фенілу, де гетероциклоалкільне кільце являє собою моноциклічне гетероциклічне кільце, яке містить 5 або 6 кільцевих атомів.
23. Сполука за будь-яким з пп. 20-22, в якій t дорівнює 0, 1, 2, 3, 4, 5 або 6, і s дорівнює 1, 2, 3, 4, 5, 6 або 7, і s+t дорівнює 1, 2, 3, 4, 5, 6 або 7.
24. Сполука за п. 20 або п. 21, в якій t дорівнює 0, s дорівнює 3, і Y являє собою -О-.
25. Сполука за п. 20 або п. 21, в якій Y являє собою зв'язок, і s+t дорівнює 2, 3 або 4.
26. Сполука за п. 1, вибрана з групи, що складається з:
солей [2-(гідроксидифенілметил)оксазол-5-ілметил]диметил(3-феноксипропіл)амонію;
солей [2-((R)-циклогексилгідроксифенілметил)oксазол-5-ілметил]диметил(3-феноксипропіл)-амонію;
солей [2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]диметилфенетиламонію;
солей [2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]диметил(4-метилпент-3-еніл)амонію;
солей [2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]-[2-(2,3-дигідробензофуран-5-іл)етил]диметиламонію;
солей [2-((R)-циклогексилгідроксифенілметил)oксазол-5-ілметил]диметил(6-метилпіридин-2-ілметил)амонію;
солей [2-(циклопентилгідроксифенілметил)оксазол-5-ілметил]диметил(3-феноксипропіл)-амонію;
солей [2-(циклопентилгідроксифенілметил)оксазол-5-ілметил]диметил(3-феноксипропіл)-амонію;
солей 1-[2-(циклогексилгідроксифенілметил)оксазол-5-ілметил]-1-(3-феноксипропіл)-піролідинію;
солей [2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]диметил(4-феноксибутил)-амонію;
солей (2-бензилоксіетил)-[2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]-диметиламонію;
солей [2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]диметил(4-фенілбутил)-амонію;
солей [2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]-[3-(4-фторфенокси)пропіл]-диметиламонію;
солей [2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]диметил(3-фенілпропіл)-амонію;
солей [2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]диметил(2-феноксіетил)-амонію;
солей [2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]диметил(3-пара-толілоксипропіл)амонію;
солей [3-(4-хлорфенокси)пропіл]-[2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]-диметиламонію;
солей [2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]-[3-(3,4-дихлорфенокси)-пропіл]диметиламонію;
солей [2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]диметил(8-метиламінооктил)амонію;
солей [2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]диметил-[2-(4-метиламінометилфеніл)етил]амонію;
солей {2-[2-(циклогексилгідроксифенілметил)оксазол-5-іл]етил}диметил(3-феноксипропіл)-амонію;
солей {2-[2-(циклогексилгідроксифенілметил)оксазол-5-іл]етил}диметил(3-феноксипропіл)-амонію;
солей {2-[2-(гідроксидифенілметил)оксазол-5-іл]етил}диметил(3-феноксипропіл)амонію;
солей [2-(гідроксидифенілметил)тіазол-5-ілметил]диметил(3-феноксипропіл)амонію;
солей (3-бензилоксипропіл)-[2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]-диметиламонію;
солей [2-(4-хлорбензилокси)етил]-[2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]-диметиламонію.
27. Сполука за п. 1, яка являє собою сіль [2-((R)-циклогексилгідроксифенілметил)oксазол-5-ілметил]диметил(3-феноксипропіл)амонію.
28. Сполука за п. 1, яка являє собою сіль [2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]-[3-(3,4-дихлорфенокси)пропіл]-диметиламонію.
29. Сполука за п. 1, яка являє собою сіль [2-(4-хлорбензилоксі)етил]-[2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]диметиламонію.
30. Сполука за п. 1, яка являє собою сіль [2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]диметил(2-фенетилоксіетил)амонію.
31. Сполука за п. 1, яка являє собою сіль [2-((R)-циклогексилгідроксифенілметил)оксазол-5-ілметил]-[2-(3,4-дихлорбензилокси)пропіл]-диметиламонію.
32. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-31 і фармацевтично прийнятний носій або наповнювач.
33. Фармацевтична композиція за п. 32 в формі, придатній для інгаляції.
34. Застосування сполуки за будь-яким з пп. 1-31 для отримання лікарського засобу для застосування для лікування або профілактики захворювання або стану, вибраного з порушення дихальних шляхів, порушення шлунково-кишкового тракту і порушення серцево-судинної системи.
35. Застосування за п. 34, де захворювання або стан являє собою порушення дихальних шляхів.
36. Застосування за п. 34, де захворювання або стан являє собою порушення шлунково-кишкового тракту.
37. Застосування за п. 34, де захворювання або стан являє собою порушення серцево-судинної системи.
38. Застосування за п. 34, де захворювання або стан являє собою хронічне неспецифічне захворювання легенів, хронічний бронхіт, бронхіальну астму, хронічну обструкцію дихальних шляхів, бронхіальну гіперактивність, фіброз легенів, емфізему легенів і алергічний риніт.
39. Застосування сполуки за будь-яким з пп. 1-31 для отримання лікарського засобу для лікування або профілактики захворювання або стану, де захворювання або стан являє собою синдром подразненої кишки, спастичний коліт, виразки шлунка і дванадцятипалої кишки, спазми або підвищену перистальтику шлунково-кишкового тракту, дивертикуліт, біль, супроводжуючий спазми гладкої мускулатури шлунково-кишкового тракту; супроводжуючі порушення сечовипускання, порушення сечовивідних шляхів, включаючи неврогенне почастішання сечовипускання, неврогенний сечовий міхур, нічне нетримання сечі, психосоматичний сечовий міхур, асоційоване зі спазмами сечового міхура або хронічним циститом нетримання сечі, невідкладний позив до сечовипускання або почастішання сечовипускання; закачування; і порушення серцево-судинної системи, такі як індукована блукаючим нервом синусова брадикардія.
40. Спосіб лікування захворювання або стану, в який залучена активність мускаринового М3 рецептора, що включає введення суб'єкту, який потребує цього, ефективної кількості сполуки за будь-яким з пп. 1-31.
41. Спосіб за п. 40, де захворювання або стан являє собою порушення дихальних шляхів.
42. Спосіб за п. 40, де захворювання або стан являє собою порушення шлунково-кишкового тракту.
43. Спосіб за п. 40, де захворювання або стан являє собою порушення серцево-судинної системи.
44. Спосіб за п. 40, де захворювання або стан являє собою хронічне неспецифічне захворювання легень, хронічний бронхіт, бронхіальну астму, хронічну обструкцію дихальних шляхів, бронхіальну гіперактивність, фіброз легенів, емфізему легенів і алергічний риніт.
45. Спосіб за п. 40, де захворювання або стан являє собою синдром подразненої кишки, спастичний коліт, виразки шлунку і дванадцятипалої кишки, спазми або підвищену перистальтику шлунково-кишкового тракту, дивертикуліт, біль, супроводжуючий спазми гладкої мускулатури шлунково-кишковоготракту; супроводжуючі порушення сечовипускання, порушення сечовивідних шляхів, включаючи неврогенне почастішання сечовипускання, неврогенний сечовий міхур, нічне нетримання сечі, психосоматичний сечовий міхур, асоційоване зі спазмами сечового міхура або хронічним циститом нетримання сечі, невідкладний позив до сечовипускання або почастішання сечовипускання; закачування; і порушення серцево-судинної системи, такі як індукована блукаючим нервом синусова брадикардія.
Текст
1. Сполука формули (І): R8 2 3 обов'язково заміщеного алкокси, галогеналкокси, галогеном, алкілом або галогеналкілом), гетероарилу (необов'язково заміщеного алкокси, галогеналкокси, галогеном, алкілом або галогеналкілом), гетероциклоалкілу, аміноацилу, аміносульфонілу, ациламіно, сульфоніламіно, гетероарилалкілу, циклічного аміну, арилокси, гетероарилокси, арилалкілокси або гетероарилалкілокси; або її фармацевтично прийнятна сіль, сольват або N-оксид. 2. Сполука за п. 1, де: 1 R являє собою С1-С6-алкіл або атом водню; 2 R являє собою С1-С6-алкіл, атом водню або групу 7 -Z-Y-R , і 3 R являє собою неподілену пару або С1-С6-алкіл, або 1 2 R і R являють собою разом з атомом азоту, до якого вони приєднані, гетероциклоалкільне кільце, або 1 3 R і R утворюють разом з атомом азоту, до якого вони приєднані, гетероциклоалкільне кільце; 4 5 комбінації R і R являють собою комбінації, коли 4 5 (і) кожний з R і R являє собою моноциклічний гетероарил, який містить 5 або 6 кільцевих атомів; 4 5 (іі) кожний з R і R являє собою феніл; 4 5 (ііі) один з R і R являє собою феніл, а інший являє собою циклоалкіл; і 4 5 (іv) один з R і R являє собою моноциклічний гетероарил, який містить 5 або 6 кільцевих атомів, а інший являю собою циклоалкіл; 6 R являє собою -ОН, С1-С6-алкіл, гідроксі-С1-С6алкіл або атом водню; А являє собою атом кисню або сірки; X являє собою алкіленову, алкеніленову або алкініленову групу; Z являє собою алкіленову, алкеніленову або алкініленову групу; Y являє собою зв'язок або атом кисню; 7 R являє собою арил, гетероарил, гетероциклоалкіл, причому арил, гетероарил або гетероциклоалкіл можуть бути заміщені однією або декількома замісними групами, визначеними в п. 1. 1 3. Сполука за п. 1 або п. 2, в якій R являє собою 2 метил або етил, або атом водню; R являє собою 7 7 водень, С1-С6-алкіл або групу -R , -Z-Y-R , -Z9 10 9 10 9 7 NR R , -Z-CO-NR R , -Z-NR -C(O)O-R або -Z7 3 C(O)-R ; і R являє собою неподілену пару або С1С6-алкіл, і в цьому випадку атом азоту, до якого він приєднаний, є четвертинним атомом азоту і несе позитивний заряд. 3 4. Сполука за п. 3, в якій R являє собою метил, тому атом азоту, до якого він приєднаний, є четвертинним атомом азоту і несе позитивний заряд. 1 3 5. Сполука за п. 1 або п. 2, в якій R і R утворюють разом з атомом азоту, до якого вони приєднані, моноциклічне гетероциклоалкільне кільце, що містить від 3 до 7 кільцевих атомів, в якому гетероа2 томи являють собою атоми азоту; і R являє собою 7 неподілену пару або С1-С6-алкіл, або групу -R , -Z7 9 10 9 7 7 Y-R , -Z-NR R , -Z-NR -C(O)O-R або -Z-C(O)-R . 1 3 6. Сполука за п. 5, в якій R і R утворюють разом з атомом азоту, до якого вони приєднані, азетидинільне, піперидинільне, піперазинільне, Nметилпіперазинільне або піролідинільне кільце. 95255 4 7. Сполука за п. 5, в якій атом азоту, до якого при1 3 1 2 єднані R і R або R і R , є четвертинним атомом азоту і несе позитивний заряд. 7 8. Сполуки за п. 1, в якій в будь-якій групі -R , -Y7 7 9 10 9 10 9 R , -Z-Y-R , -Z-NR R , -Z-CO-NR R , -Z-NR 7 7 C(O)O-R або -Z-C(O)-R : Z являє собою -(СН2)1-8-, до трьох атомів вуглецю якої необов'язково заміщені метилом; Y являє собою зв'язок або -О-; 7 R являє собою метил, етил, н- або ізопропіл, н-, втор- або третбутил; або феніл, 3,4-метилендіоксифеніл, 3,4етилендіоксифеніл, дигідробензофураніл, нафтил; або піридил, піроліл, піримідиніл, оксазоліл, ізоксазоліл, бензізоксазоліл, бензоксазоліл, тіазоліл, бензотіазоліл, хіноліл, тієніл, бензотієніл, фурил, бензофурил, імідазоліл, бензімідазоліл, ізотіазоліл, бензізотіазоліл, піразоліл, ізотіазоліл, триазоліл, бензотриазоліл, тіадіазоліл, оксадіазоліл, піридазиніл, триазиніл, індоліл або індазоліл; або арил(С1-С6-алкіл), в якому арильна частина являє собою феніл або нафтил, і -(С1-С6-алкіл)- являє собою -СН2- або -СН2СН2-; або гетероарил(С1-С6-алкіл), в якому гетероарильна частина являє собою піридил, піроліл, піримідиніл, оксазоліл, ізоксазоліл, бензізоксазоліл, бензоксазоліл, тіазоліл, бензотіазоліл, хіноліл, тієніл, бензотієніл, фурил, бензофурил, імідазоліл, бензімідазоліл, ізотіазоліл, бензізотіазоліл, піразоліл, ізотіазоліл, триазоліл, бензотриазоліл, тіадіазоліл, оксадіазоліл, піридазиніл, триазиніл, індоліл або індазоліл, і -(С1-С6-алкіл)- являє собою -СН2- або СН2СН2-; або інданіл або 1,2,3,4-тетрагідронафталеніл; або циклопропіл, циклобутил, циклопентил або циклoгeксил; і 9 10 R і R незалежно являють собою водень, метил, етил або н- або ізопропіл; феніл, дигідробензофураніл, нафтил; піридил, піроліл, піримідиніл, оксазоліл, ізоксазоліл, бензізоксазоліл, бензоксазоліл, тіазоліл, бензотіазоліл, хіноліл, тієніл, бензотієніл, фурил, бензофурил, імідазоліл, бензімідазоліл, ізотіазоліл, бензізотіазоліл, піразоліл, ізотіазоліл, триазоліл, бензотриазоліл, тіадіазоліл, оксадіазоліл, піридазиніл, триазиніл, індоліл або індазоліл; або арил(С1-С6-алкіл), в якому арильна частина являє собою феніл або нафтил, і -(С1-С6-алкіл)- являє 9 10 собою -СН2- або -СН2СН2-; або R і R утворюють разом з атомом азоту, до якого вони приєднані, азетидинільне, піперидинільне, піперазинільне, Nметилпіперазинільне, піролідинільне, морфолінільне або тіоморфолінільне кільце; 9 10 R і R незалежно вибирають з водню, С1-С6алкілу або будь-якого з необов'язково заміщеного арилу, конденсованого з гетероциклоалкілом арилу, гетероарилу або арил(С1-С6-алкіл)-, значення яких точно визначене в цьому пункті при розгляді 7 R ; або 9 10 R і R утворюють разом з атомом азоту, до якого вони приєднані, гетероциклічне кільце, яке містить 4-8 кільцевих атомів і яке необов'язково містить додатковий атом азоту або кисню; 5 95255 7 і якщо R являє собою гетероарил, циклоалкіл, конденсований з циклоалкілом арил, гетероциклоалкіл або конденсований з гетероциклоалкілом арил, то він може бути заміщений однією або декількома замісними групами, значення яких визначене в п. 1. 1 2 3 9. Сполука за п. 1, в якій в групі -NR R R 1 2 R являє собою метил або етил, R являє собою 9 10 7 Z-NR R або -Z-Y-R , Y являє собою зв'язок або О-, і -Z- являє собою нерозгалужений або розгалужений алкіленовий радикал, який зв'язує атом 9 10 7 азоту і -NR R або -YR ланцюгом, що містить до 3 16 атомів вуглецю, і R являє собою метил. 7 10. Сполука за п. 9, в якій R являє собою феніл, бензил, дигідробензофурил або фенілетил, причому феніл, бензил, дигідробензофурил або фенілетил можуть бути заміщені однією або декількома замісними групами, значення яких визначене в п. 1. 9 11. Сполука за п. 9 або п. 10, в якій значення R і 10 R визначені вище в п. 8. 1 2 3 12. Сполука за п. 1, в якій в групі -NR R R 2 9 10 7 R являє собою -Z-NR R або -Z-Y-R , Y являє собою зв'язок або -О-, і -Z- являє собою нерозгалужений або розгалужений алкіленовий радикал, 9 10 7 який зв'язує атом азоту і -NR R або -YR , і є лан1 3 цюгом, що містить до 16 атомів вуглецю, і R і R утворюють разом з атомом азоту, до якого вони приєднані, гетероциклічне кільце, яке містить 4-8 R4 кільцевих атомів і яке необов'язково містить додатковий атом азоту або кисню. 1 3 13. Сполука за п. 12, в якій R і R утворюють разом з атомом азоту, до якого вони приєднані, азетидинільне, піперидинільне, піперазинільне, Nметилпіперазинільне, піролідинільне, морфолінільне або тіоморфолінільне кільце. 7 14. Сполука за п. 12 або п. 13, в якій R переважно являє собою циклічну ліпофільну групу, таку як феніл, бензил, дигідробензофурил або фенілетил, причому фенільна, бензильна, дигідробензофурильна або фенілетильна група може бути заміщена однією або декількома замісними групами, значення яких визначене в п. 1. 9 10 15. Сполука за п. 12, в якій значення R і R визначені в п. 8. 16. Сполука за будь-яким з попередніх пунктів, в 4 5 якій (і) кожний R і R являє собою тієніл; або (іі) 4 5 кожний R і R являє собою феніл; або (ііі) один з 4 5 R і R являє собою феніл, а інший являє собою 4 циклопентил або циклогексил; або (iv) один з R і 5 R являє собою тієніл, а інший являє собою циклопентил або циклогексил. 6 17. Сполука за п. 16, в якій R являє собою -ОН. 18. Сполука за будь-яким з попередніх пунктів, в 8 якій R являє собою водень. 19. Сполука за будь-яким з попередніх пунктів, в якій X являє собою -СН2- або -СН2СН2-. 20. Сполука за п. 1, яка має формулу (ІА) X N HO 6 A (CH2)m N + (CH2)t (CH2)s A Y R6 , (IA) 4 в якій А являє собою -О- або -S-; m дорівнює 1 або 2; кільце А являє собою необов'язково заміщене фенільне кільце або моноциклічне гетероциклічне кільце, яке містить 5 або 6 кільцевих атомів, або систему конденсованого з гетероциклоалкільним кільцем фенілу, де гетероциклоалкільне кільце являє собою моноциклічне гетероциклічне кільце, яке містить 5 або 6 кільцевих атомів; R4 HO R являє собою феніл, тієніл, циклопентил або циклогексил; 5 R являє собою феніл, тієніл, циклопентил або циклогексил; s дорівнює 1, 2, 3, 4, 5, 6 або 7, і t дорівнює 0, 1, 2, 3, 4, 5, 6 або 7, за умови, що s+t не більше 16; Y являє собою зв'язок або -О-, і X являє собою фармацевтично прийнятний аніон. 21. Сполука за п. 1, яка має формулу (IB) X N (CH2)t + A (CH2)m R6 в якій А являє собою -О- або -S-; m дорівнює 1 або 2; кільце В являє собою піролідинієве або піперидинієве кільце; кільце А являє собою необов'язково заміщене фенільне кільце або моноциклічне гетероциклічне кільце, яке містить 5 або 6 кільцевих атомів, або систему конденсованого з гетероциклоалкільним кільцем фенілу, де гетероциклоалкільне кільце являє собою моноциклічне гетероциклічне кільце, яке містить 5 або 6 кільце4 вих атомів; R являє собою феніл, тієніл, циклопе5 нтил або циклогексил; R являє собою феніл, тієніл, циклопентил або циклогексил; s дорівнює 1, 2, N B (CH2)s A Y , (ІВ) 3, 4, 5, 6 або 7, і t дорівнює 0, 1, 2, 3, 4, 5, 6 або 7, за умови, що s+t не більше 16; Y являє собою зв'язок або -О-, і X являє собою фармацевтично прийнятний аніон. 22. Сполука за п. 20 або п. 21, в якій кільце А являє собою (і) необов'язково заміщений феніл, де необов'язкові замісники вибирають з С1-С3алкокси, галогену, С1-С3-алкілу, аміно-С1-С3-ацилу і аміно-С1-С3-алкілу, або (іі) систему конденсованого з гетероциклоалкільним кільцем фенілу, де гетероциклоалкільне кільце являє собою моноцик 7 лічне гетероциклічне кільце, яке містить 5 або 6 кільцевих атомів. 23. Сполука за будь-яким з пп. 20-22, в якій t дорівнює 0, 1, 2, 3, 4, 5 або 6, і s дорівнює 1, 2, 3, 4, 5, 6 або 7, і s+t дорівнює 1, 2, 3, 4, 5, 6 або 7. 24. Сполука за п. 20 або п. 21, в якій t дорівнює 0, s дорівнює 3, і Y являє собою -О-. 25. Сполука за п. 20 або п. 21, в якій Y являє собою зв'язок, і s+t дорівнює 2, 3 або 4. 26. Сполука за п. 1, вибрана з групи, що складається з: солей [2-(гідроксидифенілметил)оксазол-5ілметил]диметил(3-феноксипропіл)амонію; солей [2-((R)циклогексилгідроксифенілметил)oксазол-5ілметил]диметил(3-феноксипропіл)-амонію; солей [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметилфенетиламонію; солей [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметил(4-метилпент-3-еніл)амонію; солей [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]-[2-(2,3-дигідробензофуран-5іл)етил]диметиламонію; солей [2-((R)циклогексилгідроксифенілметил)oксазол-5ілметил]диметил(6-метилпіридин-2ілметил)амонію; солей [2(циклопентилгідроксифенілметил)оксазол-5ілметил]диметил(3-феноксипропіл)-амонію; солей [2(циклопентилгідроксифенілметил)оксазол-5ілметил]диметил(3-феноксипропіл)-амонію; солей 1-[2(циклогексилгідроксифенілметил)оксазол-5ілметил]-1-(3-феноксипропіл)-піролідинію; солей [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметил(4-феноксибутил)-амонію; солей (2-бензилоксіетил)-[2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]-диметиламонію; солей [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметил(4-фенілбутил)-амонію; солей [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]-[3-(4-фторфенокси)пропіл]диметиламонію; солей [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметил(3-фенілпропіл)-амонію; солей [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметил(2-феноксіетил)-амонію; солей [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметил(3-пара-толілоксипропіл)амонію; солей [3-(4-хлорфенокси)пропіл]-[2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]-диметиламонію; 95255 8 солей [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]-[3-(3,4-дихлорфенокси)пропіл]диметиламонію; солей [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметил(8-метиламінооктил)амонію; солей [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметил-[2-(4метиламінометилфеніл)етил]амонію; солей {2-[2(циклогексилгідроксифенілметил)оксазол-5іл]етил}диметил(3-феноксипропіл)-амонію; солей {2-[2(циклогексилгідроксифенілметил)оксазол-5іл]етил}диметил(3-феноксипропіл)-амонію; солей {2-[2-(гідроксидифенілметил)оксазол-5іл]етил}диметил(3-феноксипропіл)амонію; солей [2-(гідроксидифенілметил)тіазол-5ілметил]диметил(3-феноксипропіл)амонію; солей (3-бензилоксипропіл)-[2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]-диметиламонію; солей [2-(4-хлорбензилокси)етил]-[2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]-диметиламонію. 27. Сполука за п. 1, яка являє собою сіль [2-((R)циклогексилгідроксифенілметил)oксазол-5ілметил]диметил(3-феноксипропіл)амонію. 28. Сполука за п. 1, яка являє собою сіль [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]-[3-(3,4-дихлорфенокси)пропіл]диметиламонію. 29. Сполука за п. 1, яка являє собою сіль [2-(4хлорбензилоксі)етил]-[2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметиламонію. 30. Сполука за п. 1, яка являє собою сіль [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметил(2-фенетилоксіетил)амонію. 31. Сполука за п. 1, яка являє собою сіль [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]-[2-(3,4-дихлорбензилокси)пропіл]диметиламонію. 32. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-31 і фармацевтично прийнятний носій або наповнювач. 33. Фармацевтична композиція за п. 32 в формі, придатній для інгаляції. 34. Застосування сполуки за будь-яким з пп. 1-31 для отримання лікарського засобу для застосування для лікування або профілактики захворювання або стану, вибраного з порушення дихальних шляхів, порушення шлунково-кишкового тракту і порушення серцево-судинної системи. 35. Застосування за п. 34, де захворювання або стан являє собою порушення дихальних шляхів. 36. Застосування за п. 34, де захворювання або стан являє собою порушення шлунково-кишкового тракту. 37. Застосування за п. 34, де захворювання або стан являє собою порушення серцево-судинної системи. 9 95255 10 38. Застосування за п. 34, де захворювання або стан являє собою хронічне неспецифічне захворювання легенів, хронічний бронхіт, бронхіальну астму, хронічну обструкцію дихальних шляхів, бронхіальну гіперактивність, фіброз легенів, емфізему легенів і алергічний риніт. 39. Застосування сполуки за будь-яким з пп. 1-31 для отримання лікарського засобу для лікування або профілактики захворювання або стану, де захворювання або стан являє собою синдром подразненої кишки, спастичний коліт, виразки шлунка і дванадцятипалої кишки, спазми або підвищену перистальтику шлунково-кишкового тракту, дивертикуліт, біль, супроводжуючий спазми гладкої мускулатури шлунково-кишкового тракту; супроводжуючі порушення сечовипускання, порушення сечовивідних шляхів, включаючи неврогенне почастішання сечовипускання, неврогенний сечовий міхур, нічне нетримання сечі, психосоматичний сечовий міхур, асоційоване зі спазмами сечового міхура або хронічним циститом нетримання сечі, невідкладний позив до сечовипускання або почастішання сечовипускання; закачування; і порушення серцево-судинної системи, такі як індукована блукаючим нервом синусова брадикардія. 40. Спосіб лікування захворювання або стану, в який залучена активність мускаринового М3 рецептора, що включає введення суб'єкту, який потребує цього, ефективної кількості сполуки за будьяким з пп. 1-31. 41. Спосіб за п. 40, де захворювання або стан являє собою порушення дихальних шляхів. 42. Спосіб за п. 40, де захворювання або стан являє собою порушення шлунково-кишкового тракту. 43. Спосіб за п. 40, де захворювання або стан являє собою порушення серцево-судинної системи. 44. Спосіб за п. 40, де захворювання або стан являє собою хронічне неспецифічне захворювання легень, хронічний бронхіт, бронхіальну астму, хронічну обструкцію дихальних шляхів, бронхіальну гіперактивність, фіброз легенів, емфізему легенів і алергічний риніт. 45. Спосіб за п. 40, де захворювання або стан являє собою синдром подразненої кишки, спастичний коліт, виразки шлунку і дванадцятипалої кишки, спазми або підвищену перистальтику шлунково-кишкового тракту, дивертикуліт, біль, супроводжуючий спазми гладкої мускулатури шлунково-кишкового тракту; супроводжуючі порушення сечовипускання, порушення сечовивідних шляхів, включаючи неврогенне почастішання сечовипускання, неврогенний сечовий міхур, нічне нетримання сечі, психосоматичний сечовий міхур, асоційоване зі спазмами сечового міхура або хронічним циститом нетримання сечі, невідкладний позив до сечовипускання або почастішання сечовипускання; закачування; і порушення серцевосудинної системи, такі як індукована блукаючим нервом синусова брадикардія. Галузь техніки, якої стосується винахід Даний винахід стосується оксазольних і тіазольних похідних, фармацевтичних композицій, способів їх отримання і застосування для лікування захворювань, в які залучена посилена активація M3 рецептора. Передумови створення винаходу Антихолінергічні засоби попереджають проходження імпульсів по парасимпатичних нервах або ефекти, що відбувається внаслідок їх проходження. Це є наслідком здатності цих сполук інгібувати дію ацетилхоліну (Ach) шляхом блокування його зв'язування з мускариновими холінергічними рецепторами. Існує п'ять підтипів мускаринових холінергічних рецепторів (mAChR), що позначаються М1-М5, і кожний з них є продуктом окремого гена, і кожний їх них володіє унікальними фармакологічними властивостями. mAChR широко поширені в органах хребетних, і ці рецептори можуть опосередковувати як інгібуючу, так і збудливу дію. Наприклад, в гладкій мускулатурі дихальних шляхів, сечового міхура і шлунково-кишкового тракту M3 mAChR опосередковують скорочувальні відповіді (огляд Caulfield, 1993, Pharmac. Ther., 58, 319-379). Було показано, що в легенях важливі мускаринові M1, M2 і M3 рецептори, які розташовані в трахеї, бронхах, підслизових залозах і парасимпатичних гангліях (огляд представлений в Fryer and Jacoby, 1998. Am J Resp Crit Care Med., 158 (5 part 3), S154-160). M3 рецептори в гладкій мускулатурі дихальних шляхів опосередковують скорочення, а тому звуження просвіту бронхів. Стимуляція M3 рецепторів, розташованих в підслизових залозах приводить до секреції слизу. Посилена передача сигналів через мускаринові ацетилхолінові рецептори була відмічена при цілому ряді різних патофізіологічних станів, включаючи астму і ХНЗЛ. При ХНЗЛ тонус блукаючого нерва може бути підвищений (Gross et al.. 1989, Chest, 96:984-987) і/або може провокувати у високій мірі обструкцію легенів з геометричних міркувань при впливі на поверхню набряклих або просочених слизом стінок дихальних шляхів (Gross et al., 1984, Am Rev Respir Dis, 129:856-870). Крім того, запальні стани можуть приводити до втрати інгібуючої активності М2 рецептора, що приводить до збільшення кількості ацетилхоліну, що вивільняється при стимуляції блукаючого нерва (Fryer et al., 1999, Life Sci., 64, (6-7) 449-455). Посилена в результаті активація M3 рецепторів приводить до посилення обструкції дихальних шляхів. Таким чином, визначення можливих антагоністів мускаринових рецепторів може бути застосовне для терапевтичного лікування тих хворобливих станів, в які залучена посилена активність M3 рецептора. Насправді, сучасні стратегії лікування підтримує в цей час регулярне використання бронхолітичних засобів-антагоністів M3 як терапія першого ряду у хворих на ХНЗЛ (Pauwels et al., 2001, Am Rev Respir Crit Care Med, 163:1256-1276). 11 Також було показано, що нетримання сечі внаслідок підвищеної скорочуваності сечового міхура опосередковується підвищеною стимуляцією M3 mAChR рецепторів. Таким чином, антагоністи M3 mAChR можуть бути застосовні як терапевтичні засоби при лікуванні таких mAChRопосредованних захворювань. Незважаючи на значне число доказів в підтримку застосування терапії проти мускаринових рецепторів для лікування хворобливих станів дихальних шляхів, порівняно небагато антимускаринових сполук застосовуються в клініці з легеневих показань. Таким чином, залишається потреба в нових сполуках, здатних викликати блокаду мускаринових M3 рецепторів, особливо в сполуках з тривалим періодом дії, що дозволяють застосування схеми однократного прийому лікарського засобу. Оскільки мускаринові рецептори широко розподілені по організму, виграшною є можливість доставки антихолінергічних ліків безпосередньо в дихальні шляхи, оскільки це дозволяє вводити менші дози ліків. Розробка і застосування місцево активних ліків з тривалим періодом дії і ліків, що втримуються на рецепторі або в легенях, могло б знизити небажані побічні ефекти, які можуть спостерігати при системному введенні тих же ліків. Тіотропій (Spiriva) є представленим в цей час на ринку антагоністом мускаринових рецепторів тривалої дії для лікування хронічного неспецифічного захворювання легенів, який вводиться шляхом інгаляції. Крім того, іпратропій є представленим на ринку антагоністом мускаринових рецепторів для лікування ХНЗЛ. 95255 12 У ЕР0323864 як антагоністи мускаринових рецепторів описані оксадіазоли, пов'язані в моноабо біциклічному кільці. Добре відомим є клас агоністів 2 адренергічного рецептора. Багато які відомі 2-агоністи, зокрема 2-агоністи тривалої дії, такі як салметерол і формотерол, грають роль при лікуванні астми і ХНЗЛ. Ці сполуки, як правило, також вводять шляхом інгаляції. Сполуки, що знаходяться в цей час на випробуванні як такі, що приймаються один раз на добу 2-агоністи, описані в Expert Opin. Investig. Drugs 14 (7), 775-783 (2005). Добре відомим фармакофором з 2-агоністичною дією є фрагмент: Також відомими в даній галузі техніки є фармацевтичні композиції, що містять і агоніст мускаринових рецепторів, і 2-агоніст, для використання при лікуванні респіраторних порушень. Наприклад, в US2005/0025718 описаний 2-агоніст в поєднанні з тіотропієм, оксотропієм, іпратропієм і іншими мускариновими антагоністами; в WO02/060532 описано ... поєднання оксотропію з 2-агоністами. Інші поєднання М3-антагоністу/2-агоністу описані в WO04/105759 і WO03/087097. Також відомими в даній галузі техніки є сполуки, що діють і як антагоніст мускаринових рецепторів, і як 2-агоніст. Такі біфункціональні молекули забезпечують бронходилатацію двома різними способами дії, володіючи при цьому фармакокінетикою однієї молекули. У порівнянні з двома окремими сполуками така молекула може бути легше включена в склад для терапевтичного застосування, і може бути легше включена в склад з третім активним інгредієнтом, наприклад, зі стероїдом. Такі молекули описані, наприклад, в WO04/074246, WO04/089892, WO05/111004, WO06/023457 і WO06/023460, в кожній з яких використовуються різні лінкерні радикали для ковалентного зв'язування M3-антагоніста з 2-агоністом, вказуючи на те, що структура лінкерного радикала не є критичною для збереження активності. Це не є несподіваним, оскільки молекулі не потрібна одночасна взаємодія з M3- і 2-рецепторами. Короткий опис суті винаходу Даний винахід стосується сполуки формули (І): У Chem. Pharm. Bull., 27(12) 3149-3152 (1979) і J. Pharm. Sci., 69(5) 534-537 (1980) описані фурильні похідні, що володіють атропіно-подібною активністю. У Med. Chem. Res., 10 (9), 615-633 (2001) як антагоністи мускаринових рецепторів описані ізоксазоли і 2-ізоксазоліни. У WO97/30994 як антагоністи мускаринових рецепторів описані оксадіазоли і тіадіазоли. в якій 13 1 95255 2 (і) R являє собою С1-С6-алкіл або водень; і R 7 7 являє собою водень або групу -R , -Z-Y-R , -Z9 10 9 10 9 7 NR R , -Z-CO-NR R , -Z-NR -C(O)O-R або -Z7 3 C(O)-R ; і R являє собою невизначену пару або С1-С6-алкіл; або 1 3 (іі) R і R утворюють разом з атомом азоту, до якого вони приєднані, гетероциклоалкільне кільце; 2 7 і R являє собою невизначену пару або групу -R , 7 9 10 9 10 9 7 Z-Y-R , -Z-NR R , -Z-CO-NR R , -Z-NR -C(O)O-R 7 або -Z-C(O)-R ; або 1 2 (iii) R і R утворюють разом з атомом азоту, до якого вони приєднані, гетероциклоалкільне кільце, 7 причому згадане кільце заміщене групою -Y-R , -Z7 9 10 9 10 9 7 Y-R , -Z-NR R , -Z-CO-NR R , -Z-NR -C(O)O-R 7 3 або -Z-C(O)-R ; і R являє собою невизначену пару або С1-С6-алкіл; 4 5 R і R незалежно вибирають з групи, що складається з арилу, конденсованого з гетероциклоалкілом арилу, гетероарилу, С1-С6-алкілу, циклоалкілу; 6 R являє собою -ОН, С1-С6-алкіл, С1-С6алкокси, гідрокси-С1-С6-алкіл, нітрил, групу CONR82 або атом водню; А являє собою атом кисню або сірки; X являє собою алкіленову, алкеніленову або алкініленову групу; 7 R являє собою С1-С6-алкільну, арильну, конденсовану з циклоалкілом арильну, конденсовану з гетероциклоалкілом арильну, гетероарильну, арил(С1-С8-алкіл)-, гетероарил(С1-С8-алкіл)-, циклоалкільну або гетероциклоалкільну групу; 8 R являє собою С1-С6-алкіл або атом водню; Ζ являє собою С1-С16-алкіленову, С2-С16алкеніленову або С2-С16-алкініленову групу; Υ являє собою зв'язок або атом кисню; 9 10 R і R незалежно являють собою атом водню, С1-С6-алкільну, арильну, конденсовану з гетероциклоалкілом арильну, конденсовану з циклоалкілом арильну, гетероарильну групу, арил(С1-С69 10 алкіл)- або гетероарил(С1-С6-алкіл)-; або R і R утворюють разом з атомом азоту, до якого вони приєднані, утримуюче 4-8 атомів гетероциклічне кільце, що необов'язково містить додатковий атом азоту або кисню; або її фармацевтично прийнятної солі, сольвату, N-оксиду або пролікам. В одному підкласі сполук згідно з даним винаходом: 1 R являє собою С1-С6-алкіл або атом водню; 2 R являє собою С1-С6-алкіл, атом водню або групу 7 3 -Z-Y-R , і R являє собою невизначену пару або С1-С6-алкіл, або 1 2 R і R являють собою разом з атомом азоту, до якого вони приєднані, гетероциклоалкільне кі1 3 льце, або R і R утворюють разом з атомом азоту, до якого вони приєднані, гетероциклоалкільне кільце; 4 5 R і R незалежно вибирають з групи, що складається з арилу, гетероарилу, С1-С6-алкілу, циклоалкілу; 6 R являє собою -ОН, галоген, С1-С6-алкіл, гідрокси-С1-С6-алкіл або атом водню; А являє собою атом кисню або сірки; X являє собою алкіленову, алкеніленову або алкініленову групу; 14 Ζ являє собою алкіленову, алкеніленову або алкініленову групу; Υ являє собою зв'язок або атом кисню; 7 R являє собою арил, гетероарил, гетероциклоалкіл. Потрібно враховувати, що атом вуглецю, до 4 5 6 якого приєднані R , R і R , може бути асиметричним центром, тому сполуки згідно з даним винаходом можуть знаходитися в формі окремих енантіомерів або суміші енантіомерів. Переважний клас сполук згідно з даним винаходом складається з четвертинних амонієвих солей формули (І), в якій представлений в формулі (І) атом азоту являє собою четверинний атом азоту, несучий позитивний заряд. Сполуки згідно з даним винаходом можуть бути застосовні при лікуванні або профілактиці захворювань, в які залучена активація мускаринових рецепторів, наприклад, сполуки згідно з даним винаходом застосовні для лікування при цілому ряді показань, включаючи без обмеження порушення дихальних шляхів, такі як хронічне неспецифічне захворювання легенів, хронічний бронхіт всіх типів (включаючи асоційовану з ними задишку), бронхіальну астму (алергічну і неалергічну; «бронхіт новонароджених»), синдром дихальних розладів дорослих/гострих респіраторний дистрес синдром (ARDS), хронічну обструкцію дихальних шляхів, бронхіальну гіперактивність, фіброз легенів, емфизему легенів і алергічний риніт, загострення гіперреактивності дихальних шляхів внаслідок іншої лікарської терапії, особливо іншої лікарської терапії шляхом інгаляцій, пневмоконіоз (наприклад, алюміноз, антракоз, асбестоз, халікоз, птилоз, сидероз, силікоз, табакоз і біссиноз); порушення шлунково-кишкового тракту, такі як синдром подразненої кишки, спастичний коліт, виразки шлунка і дванадцятипалої кишки, спазми або підвищена перистальтика шлунковокишкового тракту, дивертикуліт, біль, супроводжуючий спазми гладкої мускулатури шлунковокишкового тракту; супроводжуючі порушення сечовипускання порушення сечовивідних шляхів, включаючи неврогенне частішання сечовипускання, неврогенний сечовий міхур, нічне нетримання сечі, психосоматичний сечовий міхур, асоційоване зі спазмами сечового міхура або хронічним циститом нетримання сечі, невідкладний позив до сечовипускання або частіше сечовипускання; заколисування; і порушення серцево-судинної системи, такі як індукована блукаючим нервом синусова брадикардія. Для лікування респіраторних станів звичайно переважно інгаляційне введення, і в таких випадках звичайно є переважним введення сполук формули (І), які є четвертинними амонієвими солями. У багатьох випадках тривалість дії четвертинних амонієвих солей згідно з даним винаходом, що вводяться інгаляційним шляхом, може складати більше 12, або більше 24 годин для звичайної дози. Для лікування порушень шлунково-кишкового тракту і порушень серцево-судинної системи пе 15 реважним може бути введення парентеральним шляхом, звичайно пероральним шляхом. Інший аспект даного винаходу стосується фармацевтичної композиції, що містить сполуки згідно з даним винаходом і фармацевтично прийнятний носій або наповнювач. Інший аспект даного винаходу стосується використання сполуки згідно з даним винаходом для виробництва лікарського засобу для лікування або профілактики захворювання або стану, в який залучена активність мускаринового M3 рецептора. Опис визначень Якщо інше не обумовлене інакше в контексті, в якому вони використовуються, то при використанні в цьому документі наступні терміни мають наступні значення: Термін «ацил» означає -СО-алкільну групу, де значення алкільної групи визначене в цьому документі. Приклади ацильних груп включають -СОСН3 і -СОСН(СН3)2. Термін «ациламіно» означає -NR-ацильну групу, в якій значення R і ацилу визначені в цьому документі. Приклади ациламіногруп включають NHCOCH3 і -N(CH3)COCH3. Терміни «алкокси» і «алкілокси» означають -Оалкільну групу, в якій значення алкілу описане нижче. Приклади алкоксигруп включають метокси (ОСН3) і етокси (-ОС2Н5). Термін «алкоксикарбоніл» означає -СООалкільну групу, в якій значення алкілу визначене нижче. Приклади алкілкарбонільних груп включають метоксикарбоніл і етоксикарбоніл. Термін «алкіл», що використовується для позначення як групи, так і частини групи, стосується нерозгалуженої або розгалуженої насиченої вуглеводневої групи, що містить в складі ланцюга від 1 до 12, переважно 1-6, атомів вуглецю. Приклади алкільних груп включають метил, етил, 1-пропіл і 2-пропіл. Термін «алкеніл», що використовується для позначення як групи, так і частини групи, стосується нерозгалуженої або розгалуженої вуглеводневої групи, що містить в складі ланцюга від 2 від 12, перевалено 2-6, атомів вуглецю і один вуглецьвуглецевий подвійний зв'язок. Приклади алкенільних груп включають етеніл, 1-пропеніл і 2пропеніл. Термін «алкіламіно» означає -NH-алкільну групу, в якій значення алкілу визначене вище. Приклади алкіламіногруп включають метиламіно і етиламіно. Термін «алкілен» означає групу -алкіл-, в якій значення алкілу визначене вище. Приклади алкіленових груп включають -СН2-. -(СН2)2- і С(СН3)НСН2-. Термін «алкенілен» означає групу -алкеніл-, в якій значення алкенілу визначене вище. Приклади алкеніленових груп включають -СН=СН-, СН=СНСН2- і -СН2СН=СН-. Термін «алкінілен» означає групу -алкініл-, в якій -алкініл- стосується нерозгалуженої або розгалуженої вуглеводневої групи, що містить в складі ланцюга від 2 до 12, переважно 2-6, атомів вуглецю і один вуглець-вуглецевий потрійний зв'язок. 95255 16 Приклади алкініленових груп включають етиніл і пропаргіл. Термін «алкілсульфініл» означає -SO-алкільну групу, в якій значення алкілу визначене вище. Приклади алкілсульфінільних груп включають метилсульфініл і етилсульфініл. Термін «алкілсульфоніл» означає -SO2алкільну групу, в якій значення алкілу визначене вище. Приклади алкілсульфонільних груп включають метилсульфоніл і етилсульфоніл. Термін «алкілтіо» означає -S-алкільну групу, в якій значення алкілу визначене вище. Приклади алкілтіогруп включають метилтіо і етилтіо. Термін «аміноацил» означає групу -CO-NRR, в якій значення R описане в цьому документі. Приклади аміноацильних груп включають -CONH2 і CONHCH3. Термін «аміноалкіл» означає групу алкіл-NН2, в якій значення алкілу описане вище. Приклади аміноалкільних груп включають -CH2NH2. Термін «аміносульфоніл» означає групу -SO2NRR, в якій значення R описане в цьому документі. Приклади аміносульфонільних груп включають SO2NH2 і -SO2NHCH3. Термін «арил», що використовується для позначення як групи, так і частини групи, означає необов'язково заміщений моноциклічний або поліциклічний ароматичний карбоциклічний фрагмент, що містить від 6 до 14 атомів вуглецю, переважно від 6 від 10 атомів вуглецю, такий як феніл або нафтил. Арильна група може бути заміщена однією або декількома замісними групами. Термін «арилалкіл» означає групу арил-алкіл-, в якій значення арильного і алкільного фрагментів описані вище. Переважні арилалкільні групи містять С1-С4алкільнийфрагмент. Приклади арилалкільних груп включають бензил, фенетил і нафталінметил. Термін «арилалкілокси» означає арилалкілокси- групу, в якій значення арильного і алкілокси- фрагментів описані вище. Переважні арилалкілоксигрупи містять С1-С4алкільнийфрагмент. Приклади арилалкільних груп включають бензилокси. Термін «конденсований з циклоалкілом арил» означає моноциклічне арильне кільце, таке як феніл, конденсоване з циклоалкільною групою, де значення арилу і циклоалкілу визначені в цьому документі. Приклади конденсованих з циклоалкілом арильних груп включають тетрагідронафтил і інданіл. Кожне арильне і циклоалкільне кільце може бути заміщене однією або декількома замісними групами. Конденсована з циклоалкілом арильна група може бути приєднана до частини сполуки, що залишилася, через будь-який прийнятний атом вуглецю. Термін «конденсований з гетероциклоалкілом арил» означає моноциклічне арильне кільце, таке як феніл, конденсоване з гетероциклоалкільною групою, де значення арилу і гетероциклоалкілу визначені в цьому документі. Приклади конденсованих з гетероциклоалкілом арильних груп включають тетрагідрохінолініл, індолініл, бензодіоксиніл, бензодіоксоліл, дигідробензофураніл і ізоіндолоніл. Кожне арильне і гетероциклоалкільне 17 кільце може бути заміщене однією або декількома замісними групами. Конденсована з гетероциклоалкілом арильна група може бути приєднана до частини сполуки, що залишилася, через будь-який прийнятний атом вуглецю або азоту. Термін «арилокси» означає -О-арильну групу, в якій значення арилу описане вище. Приклади арилоксигруп включають фенокси. Термін «циклічний амін» означає необов'язково заміщену 3-8-членну моноциклічну циклоалкільну кільцеву систему, в якій один з кільцевих атомів вуглецю заміщений азотом, і яка може необов'язково містити додатковий гетероатом, вибраний з О, S або NR (де значення R визначене в цьому документі). Приклади циклічних амінів включають піролідин, піперидин, морфолін, піперазин і N-метилпіперазин. Циклічна аміногрупа може бути заміщена однією або декількома замісними групами. Термін «циклоалкіл» означає необов'язково заміщену насичену моноциклічну або біциклічну кільцеву систему, що містить від 3 до 12 атомів вуглецю, переважно від 3 до 8 атомів вуглецю, і більш переважно від 3 до 6 атомів вуглецю. Приклади моноциклічних циклоалкільних кілець включають, циклопропіл, циклопентил, циклогексил і циклопентил. Циклоалкільна група може бути заміщена однією або декількома замісними групами. Термін «циклоалкілалкіл» означає циклоалкілалкіл- групу, в якій значення циклоалкільного і алкільного фрагментів описані вище. Приклади моноциклічних циклоалкілалкільних груп включають циклопропілметил, циклопентилметил, циклогексил метил і циклогептилметил. Термін «дендример» означає центральну групу з декількома функціональними дільницями з приєднаною до кожної функціональної дільниці групою, що відгалужується. Колена дільниця відгалуження може бути сполучена з іншою молекулою, що відгалужується, і цей процес може повторюватися багато разів. Термін «діалкіламіно» означає -N(алкіл)2 групу, в якій значення алкілу визначене вище. Приклади діалкіламіногруп включають диметиламіно і діетиламіно. Терміни «гало» або «галоген» означає фтор, хлор, бром або йод. Переважними є фтор або хлор. Термін «галогеналкокси» означає -О-алкільну групу, в якій алкіл заміщений одним або декількома атомами галогену. Приклади галогеналкільних груп включають трифторметокси і дифторметокси. Термін «галогеналкіл» означає алкільну групу, яка заміщена одним або декількома атомами галогену. Приклади галогеналкільних груп включають трифторметил. Термін «гетероарил», що використовується для позначення як групи, так і частини групи, означає необов'язково незаміщений ароматичний моноциклічний або поліциклічний органічний фрагмент, що містить від 5 до 14 кільцевих атомів, переважно від 5 до 10 кільцевих атомів, в якому один або декілька кільцевих атомів являє (являють собою) собою елемент (елементи), відмінні від вуглецю, наприклад, азот, кисень або сірку. Прик 95255 18 лади таких груп включають бензімідазолільну, бензоксазолільну, бензотіазолільну, бензофуранільну, бензотієнільну, фурильну, імідазолільну, індолільну, індолізинільну, ізоксазолільну, ізохінолінільну, ізотіазолільну, оксазолільну, оксадіазолільну, піразинільну, піридазинільну, піразолільну, піридильну, піримідинільну, пірол ільну, хіназолінільну, хінолінільну, тетразолільну, 1,3,4тіадіазолільну, тіазолільну, тієнільну і триазолільну групи. Гетероарильна група може бути заміщена однією або декількома замісними групами. Гетероарильна група може бути приєднана до частини, що залишилася, молекули сполуки згідно з даним винаходом по будь-якому прийнятному атому вуглецю або азоту. Термін «гетероарилалкіл» означає гетероарил-алкіл- групу, в якій значення гетероарильного і алкільного фрагментів описані вище. Переважні гетероарилалкільні групи містять фрагмент нижчого алкілу. Приклади гетероарилалкільних груп включають піридилметил. Термін «гетероарилалкілокси» означає гетероарил-алкілокси- групу, в якій значення гетероарильного і алкілокси- фрагментів описані вище. Переважні гетероарилалкілоксигрупи містять фрагмент нижчого алкілу. Приклади гетероарилалкілоксигруп включають піридилметилокси. Термін «гетероарилокси» означає гетероарилокси- групу, в якій значення гетероарилу описане вище. Приклади гетероарил оксигруп включають піридилокси. Термін «конденсований з циклоалкілом гетероарил» означає моноциклічну гетероарильну групу, таку як піридил або фураніл, конденсовану з циклоалкільною групою, де значення гетероарилу і циклоалкілу описані вище. Приклади конденсованих з циклоалкілом гетероарильних груп включають тетрагідрохінолініл і тетрагідробензофураніл. Гетероарильне і циклоалкільне кільця можуть бути заміщені однією або декількома замісними групами. Конденсовані з циклоалкілом гетероарильні групи можуть бути приєднані до частини сполуки, що залишилася, по будь-якому прийнятному атому вуглецю або азоту. Термін «конденсований з гетероциклоалкілом гетероарил» означає моноциклічну гетероарильну групу, таку як піридил або фураніл, конденсовану з гетероциклоалкільною групою, де значення гетероарилу і гетероциклоалкілу описані вище. Приклади конденсованих з гетероциклоалкілом гетероарильних груп включають дигідродіоксинопіридиніл, дигідропіролопіридиніл, дигідрофуранопіридиніл і діоксолопіридиніл. Гетероарильне і гетероциклоалкільне кільця можуть бути заміщені однією або декількома замісними групами. Конденсовані з гетероциклоалкілом гетероарильні групи можуть бути приєднані до частини сполуки, що залишилася, по будь-якому прийнятному атому вуглецю або азоту. Термін «гетероциклоалкіл» означає: (і) необов'язково заміщену циклоалкільну групу, що містить від 4 до 8 кільцевих атомів і один або декілька гетероатомів, вибраних з О, S або NR; (іі) циклоалкільну групу, що містить від 4 до 8 кільцевих атомів і CONR і CONRCO (приклади таких груп включають 19 сукцинімідил і 2-оксопіролідиніл). Гетероциклоалкільна група може бути заміщена однією або декількома замісними групами. Гетероциклоалкільна група може бути приєднана до частини сполуки, що залишилася, по будь-якому прийнятному атому вуглецю або азоту. Термін «гетероциклоалкілалкіл» означає гетероциклоалкіл-алкіл- групу, в якій значення гетероциклоалкільного і алкільного фрагментів описані вище. Якщо інше не вказане інакше, то термін «нижчий алкіл», що використовується для позначення групи означає аліфатичну вуглеводневу групу, яка може бути нерозгалуженою або розгалуженою, що містить в складі ланцюги від 1 до 4 атомів вуглецю, тобто метил, етил, пропіл (пропіл або ізопропіл) або бутил (бутил, ізобутил або трет-бутил). Термін «сульфоніл» означає -SO2-алкільну групу, в якій значення алкілу визначене в цьому документі. Приклади сульфонільних груп включають метансульфоніл. Термін «сульфоніламіно» означає -NRсульфонільну групу, в якій значення R і сульфонілу визначені в цьому документі. Приклади сульфоніламіногруп включають -NHSO2CH3. R означає алкіл, арил або гетероарил, описані в цьому документі. Термін «фармацевтично прийнятна сіль» означає фізіологічно або токсикологічно прийнятну сіль і включає, коли це доцільне, фармацевтично прийнятні солі додання основи, фармацевтично прийнятні солі додання кислоти і фармацевтично прийнятні солі четвертинного амонію. Наприклад, (і) якщо сполука згідно з даним винаходом містить одну або декілька кислотних груп, наприклад, карбоксигруп, то фармацевтично прийнятні солі додання основи, які можуть бути утворені, включають солі натрію, калію, кальцію, магнію і амонію, або солі з органічними амінами, такими як діетиламін, N-метил-глюкамін, діетаноламін або амінокислоти (наприклад, лізин), і тому подібне; (іі) якщо сполука згідно з даним винаходом містить основну групу, таку як аміногрупу, то фармацевтично прийнятні солі додання кислоти, які можуть бути утворені, включають гідрохлориди, гідроброміди, сульфати, фосфати, ацетати, цитрати, лактати, тартрати, мезилати, малеати, фумарати, сукцинати, і тому подібне; (ііі) якщо сполука містить четвертинну амонієву групу, то відповідними протиіонами можуть бути, наприклад, хлориди, броміди, сульфати, метансульфонати, бензолсульфонати, толуолсульфонати (тозилати), фосфати, ацетати, цитрати, лактати, тартрати, мезилати, малеати, фумарати, сукцинати, і тому подібне. Потрібно враховувати, що посилання, які використовуються в цьому документі на сполуки згідно з даним винаходом також передбачають включення фармацевтично прийнятних солей. Термін «проліки» стосується сполуки, яка здатна перетворюватися in vivo метаболічним шляхом (наприклад, шляхом гідролізу, відновлення або окислення) в сполуку згідно з даним винаходом. Придатні для утворення проліків групи описані в 'The Practice of Medicinal Chemistry, 2nd Ed. pp 561 95255 20 585 (2003) і в F. J. Leinweber, Drug Metab. Res., 18, 379, (1987). Потрібно враховувати, що посилання, які використовуються в цьому документі на сполуки згідно з даним винаходом також передбачають включення форм проліків. Термін «насичений» стосується сполук і/або груп, які не містять вуглець-вуглецевих подвійних або вуглець-вуглецевих потрійних зв'язків. Описані вище циклічні групи, а саме арил, гетероарил, циклоалкіл, конденсований з циклоалкілом арил, конденсований з циклоалкілом гетероарил, гетероциклоалкіл, конденсований з гетероциклоалкілом арил, конденсований з гетероциклоалкілом гетероарил і циклічний амін, можуть бути заміщені однією або декількома замісними групами. Придатні необов'язкові замісні групи включають ацил (наприклад, -СОСН3), алкокси (наприклад, -ОСН3), алкоксикарбоніл (наприклад, -СООСН3), алкіламіно (наприклад, -NHCH3), алкілсульфініл (наприклад, -SOCH3), алкілсульфоніл (наприклад, -SO2CH3), алкілтіо (наприклад, SCH3), -NH2, аміноацил (наприклад, -CON(CH3)2), аміноалкіл (наприклад, -CH2NH2), арилалкіл (наприклад, -CH2Ph або -CH2-CH2-Ph), ціано, діалкіламіно (наприклад, -N(CH3)2), галоген, галогеналкокси (наприклад, -OCF3 або -OCHF2), галогеналкіл (наприклад, -CF3), алкіл (наприклад, СН3 або -СН2СН3), -ОН, -СНО, -NO2, арил (необов'язково заміщений алкокси, галогеналкокси, галогеном, алкілом або галогеналкілом), гетероарил (необов'язково заміщений алкокси, галогеналкокси, галогеном, алкілом або галогеналкілом), гетероциклоалкіл, аміноацил (наприклад, -CONH2, CONHCH3), аміносульфоніл (наприклад, -SO2NH2, -SO2NHCH3), ациламіно (наприклад, -NHCOCH3), сульфоніламіно (наприклад, -NHSO2CH3), гетероарилалкіл, циклічний амін (наприклад, морфолін), арилокси, гетероарилокси, арилалкілокси (наприклад, бензилокси) і гетероарилалкілокси. Алкіленові і алкеніленові групи можуть бути необов'язково заміщені. Придатні необов'язкові замісні групи включають алкокси (наприклад, ОСН3), алкіламіно (наприклад, -NHCH3), алкілсульфініл (наприклад, -SOCH3), алкілсульфоніл (наприклад, -SO2CH3), алкілтіо (наприклад, -SCH3), NH2, аміноалкіл (наприклад, -CH2NH2), арилалкіл (наприклад, -CH2Ph або -CH2-CH2-Ph), ціано, діалкіламіно (наприклад, -N(CH3)2), галоген, галогеналкокси (наприклад, -ОСF3 або -OCHF2), галогеналкіл (наприклад, -CF3), алкіл (наприклад, -СН3 або СН2СН3), -ОН, -СНО і -NO2. Сполуки згідно з даним винаходом можуть існувати в одній або декількох геометричних, оптичних, енантіомерних, діастереоізомерних і таутомерних формах, включаючи без обмеження цис- і транс-форми, Е- і Z-форми, R-, S- і мезо-форми, кето- і енольні форми. Якщо інше не вказується особливо, то посилання на конкретну сполуку включає всі такі ізомерні форми, включаючи їх рацемічні і інші суміші. Коли це доцільне, такі ізомери можуть бути виділені з утримуючих їх сумішей шляхом застосування або модифікації відомих способів (наприклад, хроматографічних методик і методик перекристалізації). Коли це до 21 цільне, такі ізомери можуть бути отримані шляхом застосування або модифікації відомих способів (наприклад, асиметричного синтезу). 1 2 3 Групи R , R і R 1 2 3 Існують три комбінації груп R , R і R . 1 У комбінації (і) R являє собою С1-С6-алкіл або 2 7 водень; і R являє собою водень або групу -R , -Z7 9 10 9 10 9 7 Y-R , -Z-NR R , -Z-CO-NR R , -Z-NR -C(O)O-R 7 3 або -Z-C(O)-R ; i R являє собою невизначену пару або С1-С6-алкіл, і в цьому випадку атом азоту, до якого він приєднаний, є четвертинним атомом азоту і несе позитивний заряд. 1 3 У комбінації (іі) R і R утворюють разом з атомом азоту, до якого вони приєднані, гетероцикло2 алкільне кільце, і R являє собою невизначену 2 7 пару (тобто замісник R відсутній) або групу -R , 7 9 10 9 10 9 7 Z-Y-R , -Z-NR R , -Z-CO-NR R , -Z-NR -C(O)O-R 7 або -Z-C(O)-R . У цьому випадку, зрозуміло, якщо 2 R не являє собою невизначену пару, то атом азоту, до якого він приєднаний, є четвертинним ато1 мом азоту і несе позитивний заряд. Зокрема, R і 3 R утворюють разом з атомом азоту, до якого вони приєднані, утримуюче від 3 до 7 кільцевих атомів моноциклічне кільце, в якому гетероатоми являють собою атоми азоту. Приклади таких кілець включають азетидинільне, піперидинільне, піперазинільне, N-заміщене піперазинільне, таке як метилпіперазинільне, і піролідинільне кільця. 1 2 У комбінації (ііі) R і R утворюють разом з атомом азоту, до якого вони приєднані, гетероциклоалкільне кільце, причому згадане кільце замі7 7 9 10 щене групою -Y-R , -Z-Y-R , -Z-NR R , -Z-CO9 10 9 7 7 3 NR R , -Z-NR -C(O)O-R або -Z-C(O)-R , і R являє 3 собою невизначену пару (тобто замісник R відсу1 тній), або С1-С6-алкіл, зокрема метил. Зокрема, R 2 і R утворюють разом з атомом азоту, до якого вони приєднані, утримуюче від 3 до 7 кільцевих атомів моноциклічне кільце, в якому гетероатоми являють собою атоми азоту. Приклади таких кілець включають азетидинільне, піперидинільне, піперазинільне, N-заміщене піперазинільне, таке як метилпіперазинільне, і піролідинільне кільця. 3 Зрозуміло, якщо R не являє собою невизначену пару, то атом азоту, до якого він приєднаний, є четвертинним атомом азоту і несе позитивний заряд. 2 7 7 Якщо замісник R містить групу -R , або -Y-R , 7 9 10 -Z-Y-R , або групу -Z-NR R ; або групу -Z-CO9 10 9 7 NR R ; або групу -Z-NR -C(O)O-R або групу -Z7 1 2 CO2-R ; або R , R і атом азоту, до якого вони приєднані, утворюють кільце, то: Ζ може являти собою, наприклад, -(СН2)1-8-, причому до трьох атомів вуглецю в ланцюгу останнього необов'язково заміщені метилом; Υ являє собою зв'язок або -О-; 7 R може являти собою С1-С6-алкіл, такий як метил, етил, н- або ізопропіл, н-, втор- або трет-бутил; необов'язково заміщений арил, такий як феніл або нафтил, або конденсований з гетероциклоалкілом арил, такий як 3,4-метилендіоксифеніл, 3,4етилендіоксифеніл або дигідробензофураніл; необов'язково заміщений гетероарил, такий як піридил, піроліл, піримідиніл, оксазоліл, ізоксазоліл, бензізоксазоліл, бензоксазоліл, тіазоліл, бен 95255 22 зотіазоліл, хінолил, тієніл. бензотієніл, фурил, бензофурил, імідазоліл, бензімідазоліл, ізотіазоліл, бензізотіазоліл, піразоліл, ізотіазоліл, триазоліл, бензотриазоліл, тіадіазоліл, оксадіазоліл, піридазиніл, піридазиніл, триазиніл, індоліл і індазоліл; необов'язково заміщений арил(С1-С6-алкіл)-, такий як замісник, в якому арильна частина являє собою будь-яку з спеціально згаданих вище арильних груп, і -(С1-С6-алкіл)- являє собою -СН2- або -СН2СН2-; необов'язково заміщений конденсований з циклоалкілом арил, такий як інданіл або 1,2,3,4тетрагідронафталеніл; необов'язково заміщений гетероарил(С1-С8алкіл)-, такий як замісник, в якому гетероарильна частина являє собою будь-яку з спеціально згаданих вище гетероарильних груп, і -(С1-С6-алкіл)являє собою -СН2- або -СН2СН2-; необов'язково заміщений циклоалкіл, такий як циклопропіл, циклобутил, циклопентил або циклогексил; або необов'язково заміщений гетероциклоалкіл(С1С8-алкіл)-, такий як замісник, в якому гетероциклоалкільна частина являє собою азетидиніл, піперидиніл, піперазиніл, N-заміщений піперазиніл, такий як метилпіперазиніл, або піролідиніл, і -(С1-С6алкіл)- являє собою -СН2- або -СН2СН2-; 9 10 R і R можуть бути незалежно вибрані з водню; С1-С6-алкілу, такого як метил, етил або н- або ізопропіл; або будь-якого з необов'язково заміщеного арилу, конденсованого з гетероциклоалкілом арилу, гетероарилу або арил(С1-С8-алкіл)-, зна7 чення яких точно згадане вище при розгляді R ; або 9 10 R і R можуть утворювати разом з атомом азоту, до якого вони приєднані, гетероциклічне кільце, що містить 4-8 кільцевих атомів, переважно 4-6 кільцевих атомів, і що необов'язково містить додатковий атом азоту або кисню, таке як азетидиніл, піперидиніл, піперазиніл, N-заміщений піперазиніл, такий як метилпіперазиніл, піролідиніл, морфолініл і тіоморфолініл. В одному переважному прикладі здійснення 1 2 3 1 винаходу в групі -NR R R R являє собою метил 2 або етил, R являє собою визначені або розглянуті 9 10 7 вище -Z-NR R або -Z-Y-R , Υ являє собою зв'язок або -О-, і -Ζ- являє собою нерозгалужений або розгалужений алкіленовий радикал, зв'язуючий 9 10 7 атом азоту і -NR R або -YR ланцюгом, що міс3 тить до 16, наприклад, до 10, атомів вуглецю, і R являє собою метил, щоб атом азоту був кватерні7 зований і ніс позитивний заряд. У цих випадках R переважно являє собою циклічну ліпофільну групу, таку як феніл, бензил, дигідробензофурил або 9 10 фенілетил, а значення R і R визначені і розглянуті вище. В іншому переважному прикладі здійснення в 1 2 3 2 групі -NR R R R являє собою визначені або розг9 10 7 лянуті вище -Z-NR R або -Z-Y-R , Υ являє собою зв'язок або -О-, і -Ζ- являє собою нерозгалужений або розгалужений алкіленовий радикал, зв'язую9 10 7 чий атом азоту і -NR R або -YR ланцюгом, що містить до 16, наприклад, до 10, атомів вуглецю, a 1 3 R і R утворюють разом з атомом азоту, до якого вони приєднані, гетероциклічне кільце, що містить 23 4-8 кільцевих атомів, переважно 4-6 кільцевих атомів, і що необов'язково містить додатковий атом азоту або кисню, таке як азетидинільне, піперидинільне, піперазинільне, N-заміщене піперазинільне, таке як метилпіперазинільне, піролідинільне, морфолінільне і тіоморфолінільне кільце, щоб атом азоту був кватернізований і ніс позитивний 7 заряд. У цих випадках R переважно являє собою циклічну ліпофільну групу, таку як феніл, бензил, 9 дигідробензофурил або фенілетил; значення R і 10 R визначені вище. В одному підкласі сполук за 1 3 даним прикладом здійснення R і R утворюють разом з атомом азоту, до якого вони приєднані, піперидинільне або піролідинільне кільце. 4 5 6 Групи R , R і R 4 5 R і R можуть бути незалежно вибрані з будьякої з арильної, конденсованої з гетероциклоалкілом арильної, конденсованої з циклоалкілом арильної, гетероарильної, С1-С6-алкільної або циклоалкільної груп, значення яких точно згадане вище 5 6 при розгляді R . R може являти собою -ОН, атом водню, С1-С6-алкіл, такий як метил або етил, С1С6-алкокси, таку як метокси або етокси, гідроксиС1-С6-алкіл, такий як гідроксиметил, нітрил, або 8 8 групу CONR 2, в якій кожний R незалежно являє собою С1-С6-алкіл, такий як метил або етил, або атом водню. У даному винаході переважним є ви6 падок, коли R являє собою -ОН. Переважні поєд4 5 6 нання R і R , особливо, якщо R являє собою -ОН, 4 5 включають ті поєднання, коли (і) кожний з R і R являє собою необов'язково заміщений моноциклічний гетероарил, що містить 5 або 6 кільцевих атомів, такий як піридил, оксазоліл, тіазоліл, фурил і, особливо, тієніл, такій як 2-тієніл; (іі) кожний 4 5 з R і R являє собою необов'язково заміщений 4 5 феніл; (ііі) один з R і R являє собою необов'язково заміщений феніл, а інший являє собою циклоалкіл, такий як циклопропіл, циклобутил або, особ4 ливо, циклоиентил або циклогексил; і (iv) один з R 5 і R являє собою необов'язково заміщений моноциклічний гетероарил, що містить 5 або 6 кільцевих атомів, такий як піридил, тісніл, оксазоліл, тіазоліл або фурил, а інший являє собою циклоалкіл, такий як циклопропіл, циклобутил, циклопентил або циклогексил. Кільцевий атом А А може являти собою атом кисню або сірки. 8 Замісник R 8 Хоч R може являти собою С1-С6-алкіл, такий як метил або етил, в даному винаході переважно, 8 якщо R являє собою атом водню. Радикал X Хоч X може являти собою алкіленовий, алкеніленовий або алкініленовий радикал, в даному винаході переважно, якщо він являє собою алкілен, наприклад, етилен або метилен. Переважний підклас сполук, до яких належить даний винахід, складається із сполук формули (ІА) 95255 24 в якій А являє собою -О- або -S-; m дорівнює 1 або 2; кільце А являє собою необов'язково заміщене фенільне кільце, або утримуюче 5 або 6 кільцевих атомів моноциклічне гетероциклічне кільце, або систему конденсованого з гетероциклоалкільним кільцем фенілу, де гетероциклоалкільне кільце являє собою утримуюче 5 або 6 кільцевих атомів моноциклічне гетероциклі4 чне кільце; R являє собою феніл, тієніл, циклопе5 нтил або циклогексил; R являє собою феніл, тієніл, циклопентил або циклогексил; s дорівнює 1, 2, 3, 4, 5, 6 або 7, і t дорівнює 0, 1,2, 3, 4, 5, 6 або 7, за умови, що s+t не більше 16; Υ являє собою зв'язок або -О-, і X являє собою фармацевтично прийнятний аніон. Інший переважний підклас сполук, до яких належить даний винахід, складається із сполук формули (IB) в якій А являє собою -О- або -S-; m дорівнює 1 або 2; кільце В являє собою піролідинієве або піперидинієве кільце; кільце А являє собою необов'язково заміщене фенільне кільце, або утримуюче 5 або 6 кільцевих атомів моноциклічне гетероциклічне кільце, або систему конденсованого з гетероциклоалкільним кільцем фенілу, де гетероциклоалкільне кільце являє собою утримуюче 5 або 6 кільцевих атомів моноциклічне гетероциклічне 4 кільце; R являє собою феніл, тієніл, циклопентил 3 або циклогексил; R являє собою феніл, тієніл, циклопентил або циклогексил; s дорівнює 1, 2, 3, 4, 5, 6 або 7, і t дорівнює 0, 1,2, 3, 4, 5, 6 або 7, за умови, що s+t не більше 16; Υ являє собою зв'язок або -О-, і X являє собою фармацевтично прийнятний аніон. Інший переважний підклас сполук, до яких належить даний винахід, складається із сполук формули (IС) в якій А являє собою -О- або -S-; m дорівнює 1 або 2; кільце В являє собою піролідинієве або пі4 перидинієве кільце; R являє собою феніл, тієніл, 5 циклопентил або циклогексил; R являє собою 9 феніл, тієніл, циклопентил або циклогексил; R і 10 R незалежно являють собою атом водню, або необов'язково заміщений С1-С6-алкіл або арил, такий як необов'язково заміщений феніл; s дорівнює 1, 2, 3, 4, 5, 6 або 7, і t дорівнює 0, 1, 2, 3, 4, 5, 6 або 7, за умови, що s+t не більше 16; Υ являє 25 собою зв'язок або -О-, і X являє собою фармацевтично прийнятний аніон. У сполуках (ІА) і (IB) згідно з даним винаходом переважно, якщо кільце А являє собою (і) необов'язково заміщений феніл, де необов'язкові замісники вибрані з алкокси, галогену, особливо, фтору або хлору, С1-С3-алкілу, аміноС1-С3-ацилу, аміноС1-С3-алкілу, або (іі) систему конденсованого з гетероциклоалкільним кільцем фенілу, де гетероциклоалкільне кільце являє собою утримуюче 5 або 6 кільцевих атомів моноциклічне гетероциклічне кільце, таке як дигідробензофураніл. У кожному з підкласів (ІА), (IB) і (IС) s+t може дорівнювати, наприклад, 1, 2, 3, 4, 5, 6 або 7, і може зростати при відповідних поєднаннях t і s, де t дорівнює 0, 1, 2, 3, 4, 5 або 6, і s дорівнює 1, 2, 3, 4, 5, 6 або 7. У сполуках (ІА) і (IB) згідно з даним винаходом переважним є поєднання t, Υ і s, де t дорівнює 0, s дорівнює 3, і Υ являє собою -О-. Додатковим переважним згідно з даним винаходом є поєднання, де Υ являє собою зв'язок, і s+t дорівнює 2, 3 або 4. У сполуках (IС) згідно з даним винаходом переважним є поєднання t, Y і s, де Υ являє собою зв'язок, і s+t дорівнює 8, 9 або 10. Потрібно розуміти, що визначені поєднання 4 3 6 R , R і R можуть приводити до утворення оптичних енантіомерів. У таких випадках, як правило, обидва енантіомери згідно з даним винаходом, володіють спорідненістю до М3 рецептору, хоч один енантіомер, як правило, є більш переважним по критерію активності відносно М3 рецептора і/або вибірковості дії проти М2 рецептора. У декількох прикладах здійснення даного винаходу відома абсолютна стереохімія переважного енантіомеру. Наприклад, в одному переважному 4 прикладі здійснення R являє собою фенільну гру5 пу; R являє собою циклогексильну або циклопен6 тильну групу; R являє собою гідроксильну групу; і атом вуглецю, до якого вони приєднані має абсолютну R-конфігурацію, що визначається правилами Кана-Інгольда-Прелога. Приклади сполук згідно з даним винаходом включають поєднання викладених в цьому документі прикладів. Переважні сполуки згідно з даним винаходом включають: солі [2-(гідроксидифенілметил)оксазол-5ілметил]диметил(3-феноксипропіл)амонію; солі [2-((R)циклогексилгідроксифенілметил)oксазол-5ілметил]диметил(3-феноксипропіл)амонію; солі [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметилфенетиламонію; солі [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметил(4-метилпент-3-еніл)амонію; солі [2-((R)циклогексилгідроксифенілметил)oксазол-5ілметил]-[2-(2,3-дигідробензофуран-5іл)етил]диметиламонію; солі [2-((R)циклогексилгідроксифенілметил)оксазол-5 95255 26 ілметил]диметил(6-метилпіридин-2ілметил)амонію; солі [2(циклопентилгідроксифенілметил)оксазол-5ілметил]диметил(3-феноксипропіл)амонію; солі 1-[2(циклогексилгідроксифенілметил)оксазол-5ілметил]-1-(3-феноксипропіл)піролідинію; солі [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметил(4-феноксибутил)амонію; солі (2-бензилоксіетил)-[2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметиламонію; солі [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметил(4-фенілбутил)амонію; солі [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]-[3-(4фторфенокси)пропіл]диметиламонію; солі [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметил(3-фенілпропіл)амонію; солі [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметил(2-феноксіетил)амонію; солі [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметил(3-пара-толілоксипропіл)амонію; солі [3-(4-хлорфенокси)пропіл]-[2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметиламонію; солі [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]-[3-(3,4дихлорфенокси)пропіл]диметиламонію; солі [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметил(8-метиламінооктил)амонію; солі [2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметил-[2-(4метиламінометилфеніл)етил]амонію; солі {2-[2(циклогексилгідроксифенілметил)оксазол-5іл]етил}диметил(3-феноксипропіл)амонію; солі {2-[2-(гідроксидифенілметил)оксазол-5іл]етил}диметил(3-феноксипропіл)амонію; солі [2-(гідроксидифенілметил)тіазол-5ілметил]диметил(3-феноксипропіл)амонію; солі (3-бензилоксипропіл)-[2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметиламонію; солі [2-(4-хлорбензилокси)етил]-[2-((R)циклогексилгідроксифенілметил)оксазол-5ілметил]диметиламонію. Як повідомлялося вище в розділі «Передумови створення винаходу», відомі сполуки, що одночасно є антагоністами M3 рецептора і агоністами 2-адренорецептора, і лікування респіраторного захворювання такими сполуками з подвійною активністю є визнаною формою лікування. Відомою стратегією отримання сполук, що володіють такими подвійними механізмами дії, є просте ковален 27 95255 тне зв'язування сполуки-антагоніста M3 рецептора із сполукою-агоністом 2-адренорецептора. Такі ковалентні кон'югати сполуки (І), що є агоністом M3 рецептора, яка визначена і розглянута вище, і агоніста 2-адренорецептора також становлять частину даного винаходу. Наприклад, такі кон'югати з подвійною активністю включають сполуки формули (І), визначені і розглянуті вище, модифіко2 вані шляхом заміни групи R групою -L-B, де L являє собою лінкерний радикал, і В являє собою фрагмент, що володіє агоністичною активністю у відношенні 2-адренорецептора. Структурно, такі кон'югати з подвійною активністю можуть бути представлені у вигляді формули (III): 1 3 4 5 6 8 в якій значення R , R , R , R , R і R визначені і розглянуті вище відносно сполук (І) згідно з даним винаходом, L являє собою двовалентний лінкерний радикал, і В являє собою фрагмент, що володіє агоністичною активністю у відношенні 2адренорецептора, такий як 2-агоністичний фармакофор, про який йде мова вище в розділі «Передумови створення винаходу». Такі сполуки (III) утворюють інший аспект даного винаходу. Прикладом такої сполуки є сполука викладеного в цьому документі прикладу 77. Даний винахід також стосується фармацевтичних складів, що містять як активний інгредієнт сполуку згідно з даним винаходом. Для профілактики і лікування запальних захворювань легенів інші сполуки можуть бути об'єднані із сполуками згідно з даним винаходом. Тому, даний винахід також стосується фармацевтичних композицій для профілактики і лікування порушень дихальних шляхів, таких як хронічне неспецифічне захворювання легенів, хронічний бронхіт, бронхіальна астма, хронічна обструкція дихальних шляхів, фіброз легенів, емфізема легенів і алергічний риніт, що містить терапевтично ефективну кількість сполуки згідно з даним винаходом і один або декілька інших терапевтичних засобів. Для профілактики і лікування запальних захворювань легенів інші сполуки можуть бути об'єднані із сполуками згідно з даним винаходом. Отже, даний винахід включає поєднання засобу згідно з даним винаходом, описаного вище в цьому документі, з одним або декількома протизапальними, бронхолітичними, антигістаміновими, протизастійними або протикашлевими засобами, причому згадані засоби згідно з даним винаходом, описані вище в цьому документі, і згадані засоби, що поєднуться існують в одній і тій же або в різних фармацевтичних композиціях, що вводяться окремо або одночасно. Переважні поєднання повинні включати дві або три різних фармацевтичних композиції. Відповідні терапевтичні засоби для 28 комбінованої терапії разом із сполуками згідно з даним винаходом включають: один або декілька бронхолітичних засобів, таких як інгібітори PDE3; метилксантини, такі як теофілін; інші інгібітори мускаринових рецепторів; кортикостероїд, наприклад, флутиказону пропіонат, циклезонід, мометазону фуроат або будесонід, або стероїди, описані в WO02/88167, WO02/12266, WO02/100879, WO02/00679, WO03/35668, WO03/48181, WO03/62259, WO03/64445, WO03/72592, WO04/39827 і WO04/66920; нестероїдний агоніст глюкокортикоїдного рецептора; агоніст 2-адренорецептора, наприклад, альбутерол (сальбутамол), сальметерол, метапротеренол, тербуталін, фенотерол, прокатерол, кармотерол, індакатерол, формотерол, арформотерол, пикуметерол, GSK-159797, GSK-597901, GSK159802, GSK-64244, GSK-678007, ТА-2005, а також сполуки за ЕР1440966, JP05025045, WO93/18007, WO99/64035, US2002/0055651, US2005/0133417, US2005/5159448, WO00/075114, WO01/42193, WO01/83462, WO02/66422, WO02/70490, WO02/76933, WO03/24439, WO03/42160, WO03/42164, WO03/72539, WO03/91204, WO03/99764, WO04/16578, WO04/016601, WO04/22547, WO04/32921, WO04/33412, WO04/37768, WO04/37773, WO04/37807, WO0439762, WO04/39766, WO04/45618, WO04/46083, WO04/71388, WO04/80964, EP1460064, WO04/087142, WO04/89892, EP01477167, US2004/0242622, US2004/0229904, WO04/108675, WO04/108676, WO05/033121, WO05/040103, WO05/044787, WO04/071388, WO05/058299, WO05/058867, WO05/065650, WO05/066140, WO05/070908, WO05/092840, WO05/092841, WO05/092860, WO05/092887, WO05/092861, WO05/090288, WO05/092087, WO05/080324, WO05/080313, US20050182091. US20050171147, WO05/092870, WO05/077361, DE10258695, WO05/111002, WO05/111005, WO05/110990, US2005/0272769 WO05/110359, WO05/121065, US2006/0019991, WO06/016245, WO06/014704, WO06/031556, WO06/032627, US2006/0106075, US2006/0106213, WO06/051373, WO06/056471; модулятор лейкотрієнів, наприклад, монтелукаст, зафірлукаст або пранлукаст; інгібітори протеаз, такі як інгібітори металопротеаз матриксу. наприклад, інгібітори ММР12 і ТАСЕ, такі як марімастат, DPC-333, GW-3333; інгібітори еластази нейтрофілів людини, такі як сивелестат і описані в WO04/043942, WO05/021509, WO05/021512, WO05/026123, WO05/026124, WO04/024700, WO04/024701, WO04/020410, WO04/020412, WO05/080372, WO05/082863, WO05/082864, WO03/053930; інгібітори фосфодіестерази-4 (PDE4), наприклад, рофлуміласт, арофілін, циломіласт, ONO6126 або ІС-485; інгібітори фосфодіестерази-7; протикашлевий засіб, такий як кодеїн або декстраморфан: 29 інгібітори кіназ, особливо інгібітори Р38 МАРK; антагоністи Р2Х7; інгібітори iNOS; нестероїдний протизапальний засіб (NSAID), наприклад, ібупрофен або кетопрофен; антагоніст допамінового рецептора; інгібітори TNF-, наприклад анти-TNF моноклональні антитіла, такі як ремікад і CDP-870, і молекули імуноглобуліну TNF-рецептора, такі як енбрел; агоністи А2а, такі як описані в ЕР 1052264 і ЕР 1241176; антагоністи А2b, такі як описані в WO2002/42298; функціональні модулятори хемокінових рецепторів, наприклад, антагоністи CCR1, CCR2, CCR3, CXCR2, CXCR3, CX3CR1 і CCR8, такі як SB332235, SB-656933, SB-265610, SB-225002, МСР1(9-76), RS-504393, MLN-1202, INCB-3284; сполуки, що модулюють дію простаноїдних рецепторів, наприклад PGD2 (DPI або CRTH2), або антагоніст тромбоксану А2, наприклад, раматробант; сполуки, що модулюють функції Тh1 або Th2, наприклад, агоністи PPAR; антагоністи рецептору до інтерлейкіну 1, такі як кінерет; агоністи інтерлейкіну 10, такі як ілодекакін; інгібітори (статини) HMG-CoA-редуктази, наприклад, розувастатин, мевастатин, ловастатин, симвастатин, правастатин і флувастатин; регулювальники слизеутворення, такі як INS37217, диквафосол, сибенадет, CS-003, талнетант, DNK-333, MSI-1956, гефітиніб; протиінфекційні засоби (антибактерійні або противірусні), і протиалергічні засоби, включаючи без обмеження антигистамінні засоби. Масові частки першого і другого активних інгредієнтів можуть варіювати і залежать від ефективної дози кожного інгредієнта. Як правило, використовують ефективну дозу кожного інгредієнта. Будь-який придатний шлях введення може використовуватися для забезпечення ссавця, особливо людини, ефективною дозою сполуки згідно з даним винаходом. У терапевтичній практиці активна сполука може вводитися будь-яким зручним, придатним або ефективним шляхом. Придатні шляхи введення відомі фахівцям в даній галузі техніки, і включають пероральний, внутрішньовенний, ректальний, парентеральний, місцевий, офтальмічний, назальний, букальний і пульмонарний. Розміри профілактичної або терапевтичної дози сполуки згідно з даним винаходом, без всякого сумніву, варіюють в залежності від цілого ряду чинників, включаючи активність сполуки, що конкретно використовується, вік, масу тіла, раціон, загальний стан здоров'я і стать пацієнта, час введення, шлях введення, швидкість виведення, застосування інших ліків і тяжкості захворювання, що піддається лікуванню. Як правило, діапазон добової дози для інгаляції лежить в межах від приблизно 0,1 мкг до приблизно 10 мг на кг маси тіла людини, переважно від 0,1 мкг до приблизно 0,5 мг на кг, і більш переважно від 0,1 мкг до 50 мкг на кг, в однократній або дробових дозах. З іншого боку, в 95255 30 деяких випадках може бути необхідне використання дозування, що виходить за вказані межі. Композиції, придатні для введення шляхом інгаляції, відомі і можуть містити носії і/або розріджувачі, відомі для використання в таких композиціях. Композиція може містити 0,01-99 мас.% активної сполуки. Переважно, однократна доза містить активну сполуку в кількості від 1 мкг до 10 мг. Для перорального введення відповідні дози складають від 10 мкг на кг до 100 мг на кг, переважно від 40 мкг на кг до 4 мг на кг. Інший аспект даного винаходу стосується фармацевтичних композицій, які містять сполуки згідно з даним винаходом і фармацевтично прийнятний носій. Термін «композиція», як в «фармацевтична композиція», має на меті охопити продукт, що містить активний інгредієнт (інгредієнти) і інертний інгредієнт (інгредієнти) (фармацевтично прийнятні наповнювачі), що складають носій, а також будь-який продукт, є результатом, прямо або опосередковано, поєднання, комплексування або агрегації будь-яких двох або декількох з інгредієнтів, або дисоціації одного або декількох інгредієнтів, або інших типів реакцій або взаємодій одного або декількох з інгредієнтів. Отже, фармацевтичні композиції згідно з даним винаходом охоплюють будь-яку композицію, отриману шляхом змішування сполуки згідно з даним винаходом, додаткового активного інгредієнта (інгредієнтів) і фармацевтично прийнятнихнаповнювачів. Фармацевтичні композиції згідно з даним винаходом містять сполуку згідно з даним винаходом як активний інгредієнт або її фармацевтично прийнятну сіль, і також можуть містити фармацевтично прийнятний носій і необов'язково інші терапевтичні інгредієнти. Термін «фармацевтично прийнятні солі» стосується солей, отриманих з фармацевтично прийнятних нетоксичних основ або кислот, включаючи неорганічні основи і кислоти і органічні основи і кислоти, і солі четвертинного амонію з фармацевтично прийнятними протиіонами. Для доставки шляхом інгаляції активна сполука переважно знаходитися в формі мікрочастинок. Вони можуть бути отримані шляхом цілого ряду методик, включаючи сушіння розпиленням, ліофілізацію і мікронізацію. Як приклад, композиція згідно з даним винаходом може бути приготована у вигляді суспензії для доставки за допомогою небулайзера або у вигляді аерозолю в рідкому пропеленті, наприклад, для використання в дозуючому інгаляторі під тиском (PMDI). Пропеленти, придатні для використання в PMDI, відомі фахівцям і включають CFC-12, HFA134a, HFA-227, HCFC-22 (CCl2F2) і HFA-152 (C2H4F2) і ізобутан. У переважному прикладі здійснення даного винаходу композиція згідно з даним винаходом являє собою суху порошкову форму для доставки з використанням інгалятора сухого порошку (DPI). Відомо багато типів DPI. Мікрочастинки для доставки можуть бути включені в склад з наповнювачами, які сприяють доставці і вивільненню. Наприклад, в сухому порошковому складі мікрочастинки можуть бути 31 включені в склад з великими частинками носія, які сприяють потоку з DPI в легені. Відповідні частинки носія відомі і включають частинки лактози; вони можуть мати середній масовий аеродинамічний діаметр понад 90 мкм. Приклад складу на основі аерозолю містить наступне: сполука згідно з даним винаходом - 24 мг/балон; лецитин, NF рідк. конц. 1,2 мг/балон; трихлорфторметан, NF 4,025 г/балон; дихлордифторметан, NF - 12,15 г/балон. Активні сполуки можуть дозовано вводитися, як це було описане, в залежності від типу інгаляційної системи. У доповнення до активних сполук форми, що вводяться, можуть додатково містити наповнювачі, такі як, наприклад, пропеленти (наприклад, фриген у випадку дозуючих аерозолів), поверхнево-активні речовини, емульгатори, стабілізатори, консерванти, ароматизатори, наповнювачі (наприклад, лактозу у випадку порошкових інгаляторів) або, якщо це доцільне, додаткові активні сполуки. Для цілей інгаляції доступний великий ряд систем, за допомогою яких аерозолі з оптимальним розміром частинок можуть бути отримані і введені з використанням методики інгаляційного введення, придатної для пацієнта. У доповнення до використання адапторів (роздільників, розширювачів) і грушовидних контейнерів (наприклад, Nebulator, Volumatic), і автоматичних пристроїв розпилення (Autohaler) для дозуючих аерозолів, зокрема, у випадку порошкових інгаляторів, доступним є цілий ряд технічних рішень (наприклад, Diskhaler, Rotadisk, Turbohaler або інгалятори, наприклад, описані в ЕР-А-0505321). Крім того, сполуки згідно з даним винаходом можуть доставлятися в бага 95255 32 токамерні пристрої, дозволяючи тим самим доставку поєднання агентів. Способи синтезу Сполуки згідно з даним винаходом можуть бути отримані відповідно до методик, представлених на подальших схемах і прикладах, з використанням відповідних матеріалів, і додатково проілюстровані подальшими конкретними прикладами. Більше того з використанням методик, описаних в розкритті, що міститься в цьому документі, фахівець в даній галузі техніки може легко отримати додаткові сполуки згідно з даним винаходом, заявлені в цьому документі. Однак сполуки, проілюстровані прикладами, не повинні тлумачитися як єдиний тип, який розглядається як винахід. Далі в прикладах проілюстровані подробиці отримання сполук згідно з даним винаходом. Фахівці в даній галузі техніки повинні ясно розуміти, що для отримання вказаних сполук можуть використовуватися відомі варіанти умов і процесів подальших методик отримання. Сполуки згідно з даним винаходом можуть бути виділені в формі їх фармацевтично прийнятних солей, таких як описані раніше в цьому документі. Щоб уникнути їх небажаної участі в реакції, що приводить до утворення сполук, може бути необхідно захистити реакційноспроможні функціональні групи (наприклад, гідрокси, аміно, тіо або карбокси) в проміжних продуктах, що використовуються для отримання сполуки згідно з даним винаходом. Можуть використовуватися захисні групи, що традиційно застосовуються, наприклад, описані в Т. W. Greene and P. G. M. Wuts in «Protective groups in organic chemistry» John Wiley and Sons, 1999. Сполуки згідно з даним винаходом можуть бути отримані відповідно до шляхів синтезу, проілюстрованим на схемах 1-4. 33 95255 34 35 95255 36 37 95255 c d Сполуки формули (I-b), в якій значення R , R і 1 2 3 R визначені для R , R і R і не являють собою атом водню, можуть бути отримані із сполук формули (I-а) шляхом взаємодії з алкілуючим агентом формули (XXI): e e R -W 38 (XXI) в якої W являє собою відхідну групу, таку як галоген, тозилат, мезилат. Взаємодія може проводитися в ряді розчинників, переважно в DMF, хлороформі або ацетонітрилі, при температурі від 0°С до температури сублімації розчинника. Аналогічно, сполуки формули (I-е), (I-g), (I-і), (I-k) і (І-n) можуть бути отримані із сполук формули (I-d), (l-f), (I-h), (Ij) і (I-m), відповідно. Повинно бути зрозуміло, що деякі сполуки можуть містити хиральний центр, а тому існувати в енантіомерних формах, які можуть бути розділені за допомогою методик хиральної препаративної ВЕРХ з використанням умов, відомих фахівцям в даній галузі техніки і проілюстрованих нижче. Сполуки загальної формули (I-а) можуть бути отримані із сполук загальної формули (II): b RM (XXII) a 4 5 шляхом взаємодії з аміном формули (XXIII): c d R R NH (XXIII) c шляхом взаємодії із сполукою загальної формули (XXII): b в якій значення R і R визначені для R і R в загальній формулі (І), і Μ являє собою протиіон металу, такий як Li або MgBr. Реакція може бути проведена в апротонному органічному розчиннику, такому як THF або діетиловий ефір, в діапазоні температур переважно від -78°С до температури сублімації розчинника. Сполуки загальної формули (XXII) добре відомі в даній галузі техніки і є легкодоступними, або можуть бути отримані відомими способами. Сполуки загальної формули (II) можуть бути отримані із сполук загальної формули (III): d 1 2 в якій значення R і R визначені для R і R в загальній формулі (І). Реакцію проводять в ряді розчинників, переважно в THF/DCM, в діапазоні температур, переважно від 0 до 100°С. Сполуки загальної формули (XXIII) є добре відомими в даній галузі техніки і можуть бути отримані відомими способами, або с комерційно доступними. 39 Сполуки формули (III) можуть бути отримані із сполук загальної формули (IV): шляхом взаємодії з бромуючим агентом, таким як N-бромсукцинімід в присутності ініціатора вільнорадикальних реакцій, такого як AIBN або перекис бензоїлу. Реакція може проводитися у відповідних розчинниках, таких як ССl4, в діапазоні температур, переважно від температури навколишнього середовища до температури сублімації розчинника. Сполуки формули (IV) можуть бути отримані із сполук загальної формули (V): шляхом взаємодії з кислотою, такою як соляна кислота, сірчана кислота, метансульфонова або трифторметансульфонова кислота, в ряді розчинників, таких як THF, DCM, вода і, переважно, 1,4діоксан, в діапазоні температур, переважно від температури навколишнього середовища до температури сублімації розчинника. Як альтернатива, сполуки формули (IV) можуть бути отримані із сполук загальної формули (V) шляхом каталізованої паладієм циклізації з використанням паладієвого каталізатора, такого як біс(дибензиліденацетон)паладій, в присутності ліганда, такого як трифенілфосфін, і основи, такої як трет-бутоксид натрію, в розчиннику, такому як THF, при температурі від кімнатної температури до температури сублімації розчинника. Як альтернатива, сполуки формули (IV) можуть бути отримані із сполук формули (XVI): відповідно до способу, описаного в J. Chem. Soc. 1948, 1960. Сполуки загальної формули (XVI) є відомими в даній галузі техніки і можуть бути отримані відомими способами, такими як описані в Tetrahedron 2002, 58(14). 2813. Як альтернатива, сполуки формули (IV) можуть бути отримані із сполук формули (XVII): відповідно до способу, описаного в J. Org. Chem., 1938, 2, 319. Сполуки загальної формули 95255 40 (XVII) є добре відомими в даній галузі техніки і можуть бути отримані відомими способами, такими як описані в GB2214180. Сполуки загальної формули (V) можуть бути отримані із сполук загальної формули (VI): шляхом взаємодії з пропаргиламіном в присутності відповідного агента реакції поєднання, такого як DCC/HOBt, або іншими відомими методиками поєднання. Як альтернатива, сполуки формули (VI) можуть бути перетворені, наприклад, в хлорангідрид, і в добре відомих умовах відбувається утворення аміду, необов'язково в присутності відповідної ненуклеофільної основи і відповідного розчинника. Сполуки загальної формули (VI) є легкодоступними або можуть бути отримані відомими способами. Як альтернатива, сполуки загальної формули (I-а) можуть бути отримані із сполук загальної формули (VII): відповідно до способів, описаних вище для отримання сполук формули (II) із сполук формули (III). Сполуки загальної формули (VII) можуть бути отримані із сполук формули (VIII): відповідно до способів, схожих з описаними для отримання сполук формули (III) із сполук формули (IV), як описано вище. Сполуки загальної формули (VIII) можуть бути отримані із сполук формули (IV) з використанням способів, описаних вище для отримання сполук формули (I-а) із сполук формули (II). Як альтернатива, сполуки формули (VIII) можуть бути отримані із сполук формули (XIX): з використанням способів, описаних вище для отримання сполук формули (IV) із сполук формули (XVII). Сполуки загальної формули (XIX) можуть бути отримані відомими способами, такими як описані в GB2214180. Як альтернатива, сполуки формули (VIII) можуть бути отримані із сполук формули (XX): 41 95255 42 кімнатної температури до температури сублімації розчинника. Сполуки формули (I-h) можуть бути отримані із сполук формули (I-a) шляхом взаємодії з алкілуючим агентом формули (XXIV): з використанням способів, описаних вище для отримання сполук формули (IV) із сполук формули (V). Сполуки загальної формули (XX) можуть бути отримані із сполук формули (XVIII) з використанням способів, описаних вище для отримання сполук формули (V) із сполук формули (VI). Як альтернатива, сполуки формули (І-b) можуть бути отримані безпосередньо із сполук формули (VII) шляхом кватернізації описаним вище і відповідним чином заміщеним третинним аміном. Як альтернатива, сполуки формули (I-а), в якій c d -NR R являє собою вторинний амін (тобто один з c d R або R являє собою атом водню), можуть бути c d отримані із сполук формули (I-а), в якій -NR R являє собою групу -NH2, шляхом відновного алкілування відповідним чином заміщеним альдегідом. Взаємодію проводять в присутності відновника, такого як ціаноборгідрид або боргідрид натрію, переважно триацетоксиборгідрид натрію, в ряді органічних розчинників, переважно в дихлоретані. Сполуки формули (I-d) і (I-е) можуть бути отримані із сполук формули (I-е) методами описаного вище алкілування або відновного алкілування і відповідно до стандартних способів, добре відомих фахівцям в даній галузі техніки. Сполуки формули (I-е) можуть бути отримані із сполук загальної формули (IX): шляхом здійснення взаємодії з відновником, таким як літійалюмінійгідрид, діізобутилалюмінійгідрид або боран, в ряді апротонних розчинників, таких як діетиловий ефір або THF, або, переважно, шляхом гідрування в присутності каталізатора, такого як нікель Ренея, у відповідному розчиннику, такому як EtOAc або EtOH, в діапазоні температур від кімнатної температури до температури сублімації розчинника. Сполуки загальної формули (IX) можуть бути отримані із сполук загальної формули (VIII) шляхом здійснення взаємодії з джерелом ціаніду-іону, таким як ціангідрин ацетону або неорганічний ціанід, переважний ціанід натрію, в присутності ненуклеофільної основи, такої як тетраметилгуанідин, в ряді розчинників, переважно в етанолі, в діапазоні температур переважно від температури навколишнього середовища до температури сублімації розчинника. Сполуки формули (I-f) можуть бути отримані із сполук формули (I-a) шляхом здійснення взаємодії з відновником, таким як триетилсилан, в присутності кислоти, такої як трифтороцтова кислота, в розчиннику, такому як DCM, при температурі від f RY (XXIV) f 6 в якій значення R визначене для R в загальній формулі (І), і Υ являє собою відхідну групу, таку як галоген, тозилат. мезилат. Реакцію проводять в присутності основи, такої як гідрид натрію, в розчиннику, такому як THF, при температурі від 0°С до температури сублімації розчинника. Сполуки загальної формули (Θ-m) можуть бути отримані із сполук формули (I-l) з використанням способів, описаних вище для отримання сполук формули (I-d) із сполук формули (I-е). Сполуки загальної формули (I-l) можуть бути отримані із сполук формули (XIV) з використанням способів, описаних вище для отримання сполук формули (I-с) із сполук формули (IX). Сполуки загальної формули (XIV) можуть бути отримані із сполук формули (XIII) з використанням способів, описаних вище для отримання сполук формули (IX) із сполук формули (VII). Як альтернатива, сполуки формули (Θ-k) можуть бути отримані безпосередньо із сполук формули (XIII) шляхом кватернізації описаним вище і відповідним чином заміщеним третинним аміном. Сполуки загальної формули (I-j) можуть бути отримані із сполук формули (XIII) з використанням способів, описаних вище для отримання сполук формули (I-а) із сполук формули (VII). Сполуки загальної формули (XIII) можуть бути отримані із сполук формули (XII) з використанням способів, описаних вище для отримання сполук формули (III) із сполук формули (IV). Сполуки загальної формули (XII) можуть бути отримані із сполук загальної формули (XI): шляхом здійснення взаємодії з відновником, таким як нікель Ренея, в розчиннику, такому як етанол, при температурі від кімнатної температури до температури сублімації розчинника відповідно до способу, описаним в J. Org. Chem. 2006, 71(8), 3026. Сполуки загальної формули (XI) можуть бути отримані із сполук загальної формули (X): шляхом здійснення взаємодії з 1(метилтіо)ацетоном в присутності ангідрида трифторметансульфонової кислоти, в розчиннику, такому як DCM, при температурі від 0°С до темпе 43 95255 44 ратури сублімації розчинника відповідно до способу, описаного в J. Org. Chem. 2006, 71(8), 3026. Сполуки загальної формули (X) є добре відомими в даній галузі техніки і можуть бути отримані відомими способами, або є комерційно доступними. Сполуки формули (XXIX) можуть бути отримані із сполук формули (XXVI) з використанням послідовності реакцій, схожої з тією, що використовується для отримання сполук формули (І-b) із сполук формули (VIII) на представленій вище схемі 1. a b Сполуки формули (XXVI), в якій R і R є однаковими, можуть бути отримані із сполук формули (XXV), в якій R являє собою відповідну алкільну групу (таку як етил або метил), шляхом обробки відповідною металоорганічною сполукою, такою як реактив Гріньяра, у відповідному розчиннику, такому як THF або діетиловий ефір. Сполуки форa b мули (XXVI), в якій R і R є різними, можуть бути отримані із сполук формули (XXV) шляхом перетворення в проміжний амід, переважно в амід Вайb нреба, і проведення поетапного введення R" і R за допомогою їх відповідних металоорганічних сполук. Сполуки формули (XXV) добре відомі з літератури, наприклад, з Helv. Chim. Acta 1946, 29, 1957. Подальші необмежувальні приклади ілюструють даний винахід. Загальні деталі проведення експериментів: Всі реакції проводили в атмосфері азоту, якщо інше не вказане особливо. ЯМР-спектри отримували на спектрометрі Varian Unity Inova 400 з реєстрацією інверснодетектованого потрійного резонансу в зразку (5 мм), працюючому при 400 МГц, або на спектрометрі Bruker Avance DRX 400 з реєстрацією інверснодетектованого потрійного резонансу в зразку (5 мм), працюючому при 400 МГц, або на спектрометрі Bruker Avance DPX 300 зі стандартною реєстрацією подвійного резонансу в зразку (5 мм), працюючому при 300 МГц. Зсуви представлені в м.ч. відносно тетраметилсилану. Якщо продукти очищали по методу колонкової хроматографії, то термін «флеш-хроматографія на силікагелі» стосується силікагелю для хроматографії з розміром частинок від 0,035 до 0,070 мм (220-440 mesh) (наприклад, силікагель 60 виробництва Fluka) і прискорене елюювання під впли вом тиском азоту до 10 фунтів/дюйм . Якщо використовувалася тонкошарова хроматографія (ТШХ), то вона стосується ТШХ на силікагелі з використанням пластин (звичайно 3x6 см) силікагелю на алюмінієвій фользі з флуоресцентним індикатором (254 нм), (наприклад, Fluka 60778). Всі розчинники і комерційні реагенти використали в стані постачання. Все сполуки, що містили основний центр (центри), які очищали по методу ВЕРХ, отримували у вигляді TFA-солі, якщо інше не вказане особливо. Умови проведення препаративної ВЕРХ: С18-зворотно-фазна колонка (колонка 10022,5 мм Genesis з розміром частинок 7 мкм). УФ-детекція при 230 нм. РХ/МС системи Використані системи для проведення рідинної хроматографії/мас-спектрометр ії (РХ/МС): Спосіб проведення РХ/МС № 1 Waters Platform LCT з С18-зворотно-фазною колонкою (1003,0 мм Higgins Clipeus з розміром частинок 5 мкм), елюювання А: вода + 0,1% мурашина кислота; В: ацетонітрил + 0,1% мурашина кислота. Градієнт: 2 Градієнтний час 0.00 1,00 15,00 20,00 22,00 25,00 потік мл/хв 1,0 1,0 1,0 1,0 1,0 1,0 %А 95 95 5 5 95 95 %В 5 5 95 95 5 5 Виявлення - МС, ELS, УФ (відбір 100 мкл для проведення МС і вбудований УФ-детектор при 254 нм) Метод іонізації при проведенні МС - електророзпиленням (позитивний іон) Спосіб проведення РХ/МС № 2 Waters Platform LC з С18-зворотно-фазною колонкою (304,6 мм Phenomenex Luna з розміром частинок 3 мкм), елюювання А: вода + 0,1% мура 45 95255 шина кислота; В: ацетонітрил + 0,1% мурашина кислота. Градієнт: Градієнтний час 0,00 0,50 4,50 5,50 6,00 потік мл/хв. 2,0 2,0 2,0 2,0 2,0 %А 95 95 5 5 95 %В 5 5 95 95 5 Виявлення - МС, ELS, УФ (відбір 100 мкл для проведення МС і вбудований УФ-детектор) Метод іонізації при проведенні МС - електророзпиленням (позитивний і негативний іон) Спосіб проведення РХ/МС № 3 Waters Micromass ZQ з С18-зворотно-фазною колонкою (304,6 мм Phenomenex Luna з розміром частинок 3 мкм), елюювання А: вода + 0,1% мурашина кислота; В: ацетонітрил + 0,1% мурашина кислота. Градієнт: Градієнтний час 0,00 0,50 4,50 5,50 6,00 потік мл/хв. 2,0 2,0 2,0 2,0 2,0 %А 95 95 5 5 95 %В 5 5 95 95 5 Виявлення - МС, ELS, УФ (відбір 100 мкл для проведення МС і вбудований УФ-детектор) Метод іонізації при проведенні МС - електророзпиленням (позитивний і негативний іон) Спосіб проведення РХ/МС № 4 Waters ZMD з С18-зворотно-фазною колонкою (304,6 мм Phenomenex Luna з розміром частинок 3 мкм), елюювання розчинником А (вода з 0,1% мурашиною кислотою) і розчинником В (ацетонітрил з 0,1% мурашиною кислотою). Ерадієнт: Градієнтний час 0,00 0,50 4,50 5,50 6,00 потік мл/хв. 2,0 2,0 2,0 2,0 2,0 %А 95 95 5 5 95 %В 5 5 95 95 5 Виявлення - МС, ELS, УФ (відбір 200 мкл для проведення МС і вбудований діодно-матричний детектор Waters 996) Метод іонізації при проведенні МС - електророзпиленням (позитивний і негативний іон) Спосіб проведення РХ/МС № 5 Waters Micromass ZQ з С18-зворотно-фазною колонкою (1003,0 мм Higgins Clipeus з розміром частинок 5 мкм), елюювання А: вода + 0,1% мурашина кислота; В: ацетонітрил + 0,1% мурашина кислота. Градієнт: Градієнтний час 0,00 1,00 15,00 20,00 22,00 25,00 потік мл/хв. 1,0 1.0 1.0 1,0 1,0 1,0 %А 95 95 5 5 95 95 %В 5 5 95 95 5 5 46 Виявлення - МС, ELS, УФ (відбір 100 мкл для проведення МС і вбудований УФ-детектор при 254 нм) Метод іонізації при проведенні МС - електророзпиленням (позитивний іон) Спосіб проведення РХ/МС № 6 Waters Micromass ZQ з С18-зворотно-фазною колонкою (1003,0 мм Higgins Clipeus з розміром частинок 5 мкм), елюювання А: вода + 0,1% мурашина кислота; В: ацетонітрил + 0,1% мурашина кислота. Градієнт: Градієнтний час 0,00 1,00 15,00 20,00 22,00 25,00 потік мл/хв. 1,0 1,0 1,0 1,0 1,0 1,0 %А 95 95 5 5 95 95 %В 5 5 95 95 5 5 Виявлення - МС, ELS, УФ (відбір 100 мкл для проведення МС і вбудований УФ-детектор при 254 нм) Метод іонізації при проведенні МС - електророзпиленням (позитивний іон) Скорочення, що використовуються в експериментальному розділі: DСМ=дихлорметан DІРЕА=діізопропілетиламін DМАР=диметиламінопіридин DМF=диметилформамід EtOAc=етилацетат EtOH=етанол ІМS=промисловий денатурований спірит МеОН=метанол RТ=кімнатна температура (к.т.) Rt=чac втримання ТFА=трифтороцтова кислота ТНF=тетрагідрофуран Sаt=насичений (нас.) Отримання проміжних продуктів Проміжний продукт 1 2-Оксо-2-феніл-N-проп-2-инілацетамід (V): a R =Ph До розчину фенілгліоксилової кислоти (6,0 г, 40 ммоль) і 3 крапель DMF в безводному DCM (50 мл) додавали оксалілхлорид (6,1 г, 48 ммоль). Реакційну суміш перемішували при кімнатній температурі протягом 3 годин, а потім видаляли розчинник. Залишок поглинали безводним DCM (50 мл), і охолоджували розчин до 0°С. Обережно протягом 10 хвилин додавали суміш пропаргіламіну (2,2 г, 40 ммоль) і триетиламіну (4,05 г, 40 ммоль), а потім залишали суміш нагріватися до кімнатної температури. Продовжували перемішування протягом 2,5 годин, а потім додавали воду (10 мл). Суміш промивали 1M HCl (220 мл), нас. 47 гідрокарбонатом натрію (водн.) (220 мл), а потім сольовим розчином. Потім органічну фазу сушили (Na2SO4), і видаляли розчинник. Залишок кристалізували з циклогексану з отриманням продукту у вигляді ясно-коричневої твердої речовини. Вихід: 5,75 г, 76%. + РХ/МС (Спосіб 3): Rt 2,47 хв., m/z 188 [МН ]. Проміжний продукт 2 (5-Метилоксазол-2-іл)фенілметанон (IV): a R =Ph До розчину 2-оксо-2-феніл-N-проп-2инілацетаміду (проміжний продукт 1) (2,4 г, 12,83 ммоль) в 1,4-діоксані (20 мл) по краплях додавали метансульфонову кислоту (10 г, 104 ммоль). Отриманий розчин нагрівали при 90°С протягом 66 годин. Реакційну суміш охолоджували і видаляли розчинник. Темний залишок розподіляли між DCM і водою. DCM фракцію промивали 1M HCl (2), нас. гідрокарбонатом натрію (2), а потім сольовим розчином. Розчин сушили (Na2SO4) і видаляли розчинник з отриманням неочищеного продукту. Проводили очищення по методу колонкової хроматографії, елююючи циклогексаном/етилацетатом (4/1). Отримували продукт у вигляді не зовсім білої твердої речовини. Вихід: 1,0 г (41%). + РХ/МС (Спосіб 3): Rt 2,94 хв., m/z 188 [МН ]. Проміжний продукт 3 (5-Бромметилоксазол-2-іл)фенілметанон (III): a R =Ph Суміш (5-метилоксазол-2-іл)фенілметанону (проміжний продукт 2) (0,8 г, 4,28 ммоль), Nбромсукциніміду (0,9 г, 5,06 ммоль) і 2,2'-азобіс(2метилпропіонітрилу) (56 мг, 0,34 ммоль) в тетрахлориді вуглецю (8 мл) нагрівали із зворотним холодильником протягом 1,5 год. Реакційну суміш охолоджували до температури навколишнього середовища і фільтрували. Фільтрат розбавляли DCM (20 мл) і промивали водою, нас. гідрокарбонатом натрію і сольовим розчином. Сушили (Na2SO4) і видаляли розчинник. Проводили очищення по методу колонкової хроматографії, елююючи циклогексаном/етилацетатом (4/1). Отримували продукт у вигляді жовтої твердої речовини. Вихід: 0,9 г (79%). РХ/МС (Спосіб 3): Rt 3,26 хв., m/z 266, 268 + [МН ]. Проміжний продукт 4 95255 48 (5-Диметиламінометилоксазол-2a c d іл)фенілметанон (II): R =Ph, R , R =CH3 (5-Бромметилоксазол-2-іл)фенілметанон (проміжний продукт 3) (0,18 г, 0,68 ммоль) розчиняли в 2М розчині диметиламіну в THF (3 мл, 6 ммоль). Суміш перемішували при температурі навколишнього середовища протягом 1 год., при цьому майже відразу утворювався осад. Видаляли розчинник і розподіляли залишок між DCM і насиченим гідрокарбонатом натрію (водн., 5 мл). Водну фазу екстрагували DCM, об'єднану органічну фазу сушили (Na2SO4) і видаляли розчинник з отриманням продукту у вигляді оранжевого масла, яке кристалізувалося при відстоюванні. Вихід: 0,16 г (99%). + РХ/МС (Спосіб 2): Rt 1,22 хв, m/z 231 [МН ]. Аналогічним способом шляхом здійснення взаємодії проміжного продукту 3 з метиламіном також отримували проміжний продукт 5 (5-Метиламінометилоксазол-2a C d іл)фенілметанон (II): R =Ph, R =CH3, R =H Вихід: 2,37 г (83%) РХ/МС (Спосіб 3): Rt 0,26 і 1,44 хв., m/z 217 + [МН ]. Проміжний продукт 6 Циклогексил(5-метилоксазол-2a b іл)фенілметанол (VIII): R =Ph, R =циклогексил Розчин (5-метилоксазол-2-іл)фенілметанону (проміжний продукт 2) (3,0 г, 16 ммоль) в 32 мл безводного THF при 0°С в атмосфері азоту протягом 10 хвилин по краплях обробляли 2М розчином циклогексилмагнійхлориду в діетиловому ефірі (10 мл, 20 ммоль). Отриманий темно-жовтий розчин перемішували при 0°С протягом приблизно 30 хв., в процесі чого утворювався осад, а потім при кімнатній температурі протягом 1,5 годин. Реакційну суміш знов охолоджували до 0°С і обережно обробляли нас. розчином хлориду амонію (водн.) (10 мл). Суміш перемішували при кімнатній температурі протягом 10 хв., а потім розбавляли водою (10 мл). Фази розділяли, і промивали органічну фазу 49 сольовим розчином. Об'єднану водну фазу екстрагували DCM (320 мл), об'єднану органічну фазу сушили (MgSO4) і концентрували у вакуумі з отриманням неочищеного продукту, який розтирали з ефіром (10 мл), відфільтровувати і сушили. Вихід: 3,65 г (84%). + РХ/МС (Спосіб 3): Rt 3,78 хв., m/z 272 [МН ]. Аналогічним способом шляхом здійснення взаємодії проміжного продукту 2 з циклопентилмагнійхлоридом отримували проміжний продукт 7 Циклопентил(5-метилоксазол-2a b іл)фенілметанол (VIII): R =Ph, R =циклопентил Вихід: 3,82 г (70%) + РХ/МС (Спосіб 2): Rt 3,68 хв., m/z 258 [МН ]. Аналогічним способом шляхом здійснення взаємодії проміжного продукту 2 з фенілмагнійбромідом отримували проміжний продукт 8. (5-Метилоксазол-2-іл)дифенілметанол (VIII): a b R , R =Ph Вихід: 2,06 г (73%) + РХ/МС (Спосіб 3): Rt 3,78 хв., m/z 272 [МН ]. Проміжний продукт 9 (5-Бромметилоксазол-2a іл)циклогексилфенілметанол (VII): R =Ph, b R =циклогексил Розчин циклогексил(5-метил оксазол-2іл)фенілметанолу (проміжний продукт 6) (3,0 г, 11,1 ммоль) в 1,2-дихлоретані (22 мл) обробляли N-бромсукцинімідом (2,16 г, 12,2 ммоль), а потім 2,2'-азобіс(2-метилпропіонітрилом) (0,18 г, 2,1 ммоль). Суміш нагрівали до 80°С протягом 2,5 год., а потім залишали охолоджуватися до кімнатної температури. Додавали нас. розчин гідрокарбонату натрію, і розділяли фази. Органічний шар промивали сольовим розчином, і екстрагували об'єднані водні шари DCM. Об'єднану органічну фазу сушили (MgSO4) і концентрували у вакуумі з отриманням неочищеного продукту у вигляді коричневого масла. Проводили очищення по методу колонкової хроматографії, елююючи 33-100% DCM/циклогексаном, а потім 25% EtOAc/DCM. 95255 50 Вихід: 1,85 г (48%). РХ/МС (Спосіб 3): Rt 4.27 хв., m/z 350, 352 + [МН ]. Аналогічним способом з проміжного продукту 7 отримували проміжний продукт 10 (5-Бромметилоксазол-2a іл)циклопентилфенілметанол (VII): R =Ph, b R =циклопентил Вихід: 10,7 г (83%) РХ/МС (Спосіб 3): Rt 3,90 хв., m/z 336, 338 + [МН ]. Аналогічним способом з проміжного продукту 8 отримували проміжний продукт 11 (5-Бромметилоксазол-2-іл)дифенілметанол a b (VII): R , R =Ph Вихід: 1,63 г (63%) РХ/МС (Спосіб 4): Rt 3,53 хв., m/z 326, 328 + [МН -Н2О]. Проміжний продукт 12 [2-(Циклогексилгідроксифенілметил)оксазол-5a b іл]ацетонітрил (IX): R =Ph, Н =циклогексил До розчину ±-(5-бромметилоксазол-2іл)циклогексилфенілметанолу (проміжний продукт 9) (1,05 г, 3,0 ммоль) в IMS (15 мл) додавали ціанід натрію (169 мг, 3,45 ммоль). Суміш нагрівали при 70°С протягом 1 години, потім концентрували у вакуумі і розподіляли між етилацетатом (30 мл) і водою (30 мл). Водну фазу екстрагували етилацетатом (230 мл), об'єднані органічні фази сушили над сульфатом натрію, фільтрували і упарювали до отримання оранжевого масла. Використовучи як елюент суміш 40% етилацетат/60% циклогексан, проводили очищення по методу колонкової флеш-хроматографії на силікагелі, а потім перекристалізацію з DCM з використанням гексана з отриманням вказаної в заголовку сполуки у вигляді білої кристалічної твердої речовини. Вихід: 700 мг (79%). + РХ/МС (Спосіб 3): Rt 3,66 хв., m/z 279 [МН Н2О]. 51 95255 Аналогічним способом з проміжного продукту 11 отримували Проміжний продукт 13 [2-(Гідроксидифенілметил)оксазол-5a b іл]ацетонітрил (IX): R , R =Ph Вихід: 0,11 г (54%) + РХ/МС (Спосіб 3): Rt 2,96 хв., m/z 291 [МН ]. Проміжний продукт 14 2-(1,1-Дифенілетил)-5-метил-4a b g метилсульфанілоксазол (XI): R , R =Ph, R =CH3 До безбарвного розчину 1-метилтіо-2пропанону (0,98 мл, 9,7 ммоль) в 13 мл безводного DCM при 0°С в атмосфері азоту по краплях додавали розчин ангідриду трифторметансульфонової кислоти (1,62 мл, 9,7 ммоль) в 10 мл безводного DCM. Отриманий жовтий розчин перемішували при 0°С протягом 1 год., а потім швидко по краплях додавали розчин 2,2-дифенілпропіонітрилу (1 г, 4,8 ммоль) в 10 мл безводного DCM. Реакційну суміш перемішували при 0°С протягом 2 год., потім протягом 5 діб при температурі від 0°С до кімнатної температури, і вона ставала темночервоною. Реакційну суміш охолоджували до 0°С і обережно обробляли нас. розчином бікарбонату натрію. Фази розділяли, і екстрагували водний шар DCM (2). Об'єднану органічну фазу промивали водою, нас. розчином бікарбонату натрію і сольовим розчином, сушили (Na2SO4) і упарювали до отримання темного в'язкого масла (1,67 г). Неочищений продукт очищали по методу хроматографії на силікагелі, елююючи 5% діетиловим ефіром/циклогексаном (Rf=0,25), з отриманням вказаної в заголовку сполуки у вигляді блідо-жовтого масла, яке кристалізувалося при відстоюванні. Вихід: 0,79 г (53%). + РХ/МС (Спосіб 2): Rt 4,37 хв., m/z 310 [МН ]. Проміжний продукт 15 a 2-(1,1-Дифенілетил)-5-метилоксазол (XII): R , g R =Ph, R =CH3 Суспензію 2-(1,1-дифенілетил)-5-метил-4метилсульфанілоксазолу (проміжний продукт 14) (0,70 г, 2,3 ммоль) в 15 мл IMS нагрівали до розb 52 чинення. Додавали нікель Ренея 2800 (~3 г), що спричиняло швидке виділення газу. Реакційну суміш перемішували при нагріванні із зворотним холодильником в атмосфері азоту. Через 1,25 год. по методу РХ/МС була показана наявність суміші вихідний матеріал/продукт (1/1), а ще через 1 год. ніяких змін не спостерігалося. Додавали ще 3 г нікеля Ренея 2800 і перемішували реакційну суміш при нагріванні із зворотним холодильником протягом 1 год. По методу ТШХ було показано, що весь вихідний матеріал прореагував. Каталізатор відфільтровували через високопродуктивний фільтр, і випаровували леткі речовини з отриманням безбарвного в'язкого масла (0,57 г). Масло очищали по методу хроматографії на силікагелі, елююючи 15% EtOAc/циклогексаном (Rf=0,36), з отриманням вказаної в заголовку сполуки у вигляді безбарвного масла. Вихід: 0,57 г (89%). + РХ/МС (Спосіб 2): Rt 3,96 хв., m/z 264 [МН ]. Проміжний продукт 16 5-Бромметил-2-(1,1-дифенілетил)оксазол a b g (XIII): R , R =Ph, R =CH3 Отримували з проміжного продукту 15 відповідно до способу, що використовується для отримання проміжного продукту 9. Вихід: 0,75 г (кількісн.) РХ/МС (Спосіб 2): Rt 4,06 хв., m/z 342, 344 + [МН ]. Проміжний продукт 17 Складний 8-метоксіоктиловий ефір метансульфонової кислоти До розчину 8-метоксіоктан-1-олу (217 мг, 1,35 ммоль) в безводному DCM (1 мл) додавали діізопропілетиламін (170 мг, 1,49 ммоль). Розчин охолоджували на бані з льодом і додавали в атмосфері азоту метансульфонілхлорид (170 мг, 1,49 ммоль). Розчин залишали нагріватися протягом ночі до температури навколишнього середовища. По методу ТШХ була показана наявність деякої кількості вихідного матеріалу. Додатково додавали метансульфонілхлорид (231 мг, 2,01 ммоль), і перемішували розчин при температурі навколишнього середовища протягом ночі. Реакційну суміш обробляли водою, і розділяли фази. Органічний шар сушили (MgSO4), і випаровували розчинник. Неочищений продукт очищали по методу хроматографії на силікагелі, елююючи діетиловим ефіром/циклогексаном (1/1), а потім діетиловим ефіром/циклогексаном (2/1), з отриманням вказаної в заголовку сполуки у вигляді масла. 8 53 Метоксіоктан-1-ол може бути отриманий відповідно до способів, описаних в Synthesis 2004, 4, 595. Вихід: 135 мг (42%). РХ/МС (Спосіб 2): Rt 3,14 хв., іона молекули не спостерігали. Проміжний продукт 18 Складний 8-(третбутоксикарбонілметиламіно)октиловий ефір метансульфонової кислоти Вказану в заголовку сполуку отримували відповідно до методики, описаної для отримання проміжного продукту 17, з використанням складного трет-бутилового ефіру (8гідроксіоктил)метилкарбамінової кислоти замість 8-метоксіоктан-1-олу. Складний трет-бутиловий ефір (8-гідроксіоктил)метилкарбамінової кислоти може бути отриманий відповідно до способів, описаних в US2005277688 або US2004254219. Вихід: 225 мг (71%). 1 H-ЯМР (CDCl3): 1,20-1,57 (м, 19Н), 1,75 (м, 2Н), 2,83 (с, 3H), 3,01 (с, 3H), 3,19 (т, 2Н), 4,22 (т, 2Н). Проміжний продукт 19 2-(4-Бромметилфеніл)етанол Розчин 4-(бромметил)фенілоцтової кислоти (458 мг, 2,0 ммоль) в 10 мл толуолу і 8 мл THF в атмосфері азоту обробляли 2М розчином борандиметилсульфідного комплексу в THF (2 мл, 4,0 ммоль), і перемішували реакційну суміш при кімнатній температурі протягом ночі. По методу РХ/МС взаємодія не спостерігалася. Додатково додавали 1,5 мл (3,0 ммоль) борандиметилсульфідного комплексу, і перемішували реакційну суміш протягом 2 год. Додавали EtOAc і воду, і розділяли фази. Органічний шар сушили (MgSO4), і випаровували розчинник з отриманням вказаної в заголовку сполуки. Вихід: 347 мг (81%). 1 H-ЯМР (CDCl3): 2,89 (т, 2Н), 3,49 (с, 1Н), 3,86 (т, 2H), 4,49 (с, 2Н), 7,21 (д, 2Н), 7.35 (д, 2Н). Проміжний продукт 20 2-{4-[(Бензилметиламіно)метил]феніл}етанол Розчин 2-(4-бромметилфеніл)етанолу (проміжний продукт 19) (347 мг, 1,6 ммоль) в 15 мл ацетонітрилу обробляли карбонатом калію (557 мг, 4,0 ммоль), а потім N-метилбензиламіном (293 мг, 2,4 ммоль). Реакційну суміш перемішували при нагріванні із зворотним холодильником протягом 6 год., коли по методу РХ/МС було показане повне перетворення вихідного матеріалу. Реакційну су 95255 54 міш залишали охолоджуватися до кімнатної температури і випаровували розчинник. Залишок розподіляли між EtOAc і водою, і розділяли фази. Органічний шар сушили (MgSO4) і випаровували розчинник. Неочищений продукт очищали по методу хроматографії на силікагелі, елююючи від DCM до 1% MeOH/DCM, з отриманням вказаної в заголовку сполуки у вигляді масла. Вихід: 258 мг (63%). 1 H-ЯМР (CDCl3): 2,09 (ушир.с, 1Н), 2,16 (с, 3H), 2,81 (т, 2Н), 3,48 (с, 2Н), 3,50 (с, 2Н), 3,79 (т, 2Н), 7,15 (д, 2Н), 7,20-7,25 (м, 1Н), 7,26-7,37 (м, 6Н). Проміжний продукт 21 2-(4-Метиламінометилфеніл)етанол Розчин 2-{4[(бензилметиламіно)метил]феніл}етанолу (проміжний продукт 20) (258 мг, 1,0 ммоль) в 10 мл IMS обробляли 20% гідроксидом паладію на вугіллі (50 мг). Реакційну суміш перемішували в атмосфері водню протягом 3 год., коли по методу РХ/МС було показане повне перетворення вихідного матеріалу. Реакційну суміш фільтрували через целіт і випаровували розчинник. Неочищений продукт наносили на картрідж SCX-2, використовучи 10% MeOH/DCM, і видаляли домішки шляхом промивання колонки MeOH/DCM. Елюювали 2М аміаком в метанолi/DCM (1/1), і видаляли розчинник з отриманням вказаної в заголовку сполуки. Вихід: 91 мг (55%). 1 H-ЯМР (MeOD): 2,35 (с, 3H), 2,79 (т, 2Н), 3,65 (с, 2Н), 3,72 (т, 2Η), 7,18-7,25 (м, 4Н). Проміжний продукт 22 Складний трет-бутиловий ефір [4-(2гідроксіетил)бензил]метилкарбамінової кислоти Розчин 2-(4-метиламінометилфеніл)етанолу (проміжний продукт 21) (91 мг, 0,55 ммоль) в 3 мл безводного DCM при 0°С по краплях обробляли розчином ди-трет-бутилкарбонату (144 мг, 0,66 ммоль) в 2 мл безводного DCM, і залишали реакційну суміш нагріватися до кімнатної температури. Через 2 год. додавали воду, і перемішували суміш протягом 10 хв. Розділяли два шари, органічний шар сушили (MgSO4), і випаровували розчинник з отриманням вказаної в заголовку сполуки. Вихід: 146 мг (кількісн.). 1 H-ЯМР (CDCl3): 1,48 (с, 9Н), 2,81 (ушир.с, 3H), 2,86 (т, 2Н), 3,86 (ушир.т, 2Н), 4,40 (ушир.с, 2Н), 7,14-7,22 (м, 4Н). Проміжний продукт 23 55 Складний 2-{4-[(третбутоксикарбонілметиламіно)метил]феніл}етиловий ефір метансульфонової кислоти Вказану в заголовку сполуку отримували відповідно до методики, описаної для отримання проміжного продукту 17, з використанням проміжного продукту 22 замість 8-метоксіоктан-1-олу. Вихід: 106 мг (50%). 1 H-ЯМР (CDCl3): 1,48 (с, 9Н), 2,75-2,84 (ушир.с, 3H), 2,87 (с, 3H), 3,04 (т, 2Н), 4,36-4,44 (м, 4Н), 7,15-7,22 (м, 4Н). Проміжний продукт 24 4-(3-Бромпропокси)бензолсульфонамід Суспензію 4-гідроксибензолсульфонаміду (4,1 г, 23 ммоль), 1,3-дибромпропану (6,83 г, 34 ммоль) і карбонату калію (3,17 г, 23 ммоль) в ацетонітрилі (35 мл) нагрівали при 55°С протягом ночі. Суміш залишали охолоджуватися до температури навколишнього середовища і фільтрували. Фільтрат упарювали з отриманням залишку, який розподіляли між DCM і 0,1 Μ NaOH (водн.). Органічний шар сушили (MgSO4) і випаровували розчинник. Проводили очищення по методу колонкової хроматографії на силікагелі, елююючи циклогексаном, потім діетиловим ефіром, а потім перекристалізовували з ізопропанолу. Вихід: 483 мг (7%). РХ/МС (Спосіб 2): Rt 3,01 хв., іона молекули не спостерігали. Проміжний продукт 25 Бромід (9-гідроксиноніл)метиламонію До розчину 9-бром-1-нонанолу (10,2 г, 45,7 ммоль) в IMS (50 мл) при 0°С додавали розчин метиламіну (57 мл, 8М в EtOH, 456 ммоль). Через 30 хвилин при 0°С реакційну суміш залишали нагріватися до к.т. і перемішували протягом 26 год. Розчинник випаровували з отриманням білої твердої речовини, яку розтирали з діетиловим ефіром з отриманням вказаної в заголовку сполуки у вигляді білої твердої речовини. Вихід: 9,97 г, 86%. + РХ/МС (Спосіб 3): Rt 1,51 хв., m/z 174 [МН ]. Проміжний продукт 26 95255 56 9-{[2(Циклогексилгідроксифенілметил)оксазол-5ілметил]метиламіно}нонан-1-ол До розчину броміду (9гідроксиноніл)метиламонію (686 мг, 2,86 ммоль) і N, N-діізопропілетиламіну (1,0 мл, 5,7 ммоль) в безводному DCM додавали (5-бромметилоксазол2-іл)циклогексилфенілметанол (1,0 г, 2,86 ммоль). Після перемішування суміші при к.т. протягом 4 год. додавали нас. NaHCO3 (водн.). Фази розділяли і екстрагували водний шар DCM. Об'єднані органічні шари сушили (Na2SO4), фільтрували і концентрували досуха з отриманням жовтого масла. Проводили очищення по методу колонкової хроматографії на силікагелі, використовучи як елюент градієнт 5-10% MeOH/DCM, і отримували вказану в заголовку сполуку у вигляді безбарвного масла. Вихід: 0,80 г, 63%. + РХ/МС (Спосіб 2): Rt 2,42 хв., m/z 443 [МН ]. Проміжний продукт 27 9-{[2(Циклогексилгідроксифенілметил)оксазол-5ілметил]метиламіно}нонаналь До розчину оксалілхлориду (94 мкл) в безводному DCM (3 мл) при -78°С в атмосфері азоту по краплях додавали розчин DMSO (0,17 мл, 2,3 ммоль) в безводному DCM (3 мл). Потім додавали розчин 9-{[2(циклогексилгідроксифенілметил)оксазол-5ілметил]метиламіно}нонан-1-олу (0,49 г, 1,1 ммоль) в безводному DCM (5 мл), і перемішували реакційну суміш при -78°С протягом 15 хв. Додавали триетиламін (0,62 мл, 4,4 ммоль), і залишали реакційну суміш нагріватися до к.т. Через 1 год. додавали нас. NaHCO3 (водн.), розділяли фази, і екстрагували водний шар DCM. Об'єднані органічні шари промивали сольовим розчином, сушили (Na2SO4), фільтрували і концентрували досуха з отриманням жовтого/коричневого в'язкого масла. Неочищений продукт повторно переносили в ті ж самі реакційні умови для додаткового перетворення вихідного матеріалу з отриманням жовтого в'язкого масла і твердих речовин. Тверді речовини розтирали з діетиловим ефіром і концентрували надосадову рідину досуха з отриманням твердої піни, яку використали без додаткового очищення. Вихід: 0,59 м. + РХ/МС (Спосіб 2): Rt 2,74 хв., m/z 441 [МН ]. Проміжний продукт 28 57 5-[(R)-1-(Бутилдиметилсиланілокси)-2-(9-{[2(циклогексилгідроксифенілметил)оксазол-5ілметил]метиламіно}ноніламіно)етил]-8-гідрокси1Н-хінолін-2-он Суміш 9-{[2(циклогексилгідроксифенілметил)оксазол-5ілметил]метиламіно}нонаналю (0,49 г, 1,1 ммоль), 5-[(R)-2-аміно-1-(третбутилдиметилсиланілокси)етил]-8-гідрокси-1Нхінолін-2-ону (0,37 г, 1,1 ммоль) і триацетоксиборгідриду натрію (0,33 г, 1,6 ммоль) в безводному DCE (10 мл) перемішували в атмосфері азоту при к.т. протягом 19 год. Розчинники випаровували у вакуумі і очищали залишок по методу колонкової хроматографії на силікагелі, використовучи як елюент суміш DCM/MeOH/оцтова кислота/вода (120/15/3/2), з отриманням продукту у вигляді дещо коричнюватої смоли. Залишок поглінали МеОН, пропускали через картрідж SCX-2 і вивільняли з використанням 2М розчину аміаку в МеОН. Шляхом випаровування розчинника у вакуумі отримували вказану в заголовку сполуку у вигляді суміші діастереоізомерів у вигляді жовто-зеленої смоли. Вихід: 78 мг, 9%. + РХ/МС (Спосіб 2): Rt 2,64 хв., m/z 760 [МН ]. Проміжний продукт 29 95255 58 розчином, сушили (MgSO4) і упарювали. Залишок піддавали колонковій хроматографії (SiO2, 40 г), елююючи 10% EtOAc в ізогексані, з отриманням необхідної речовини. Вихід=0,27 г (67%). РХ/МС (Спосіб 6): Rt 3,20 хв., m/z 282 [МН]+. 1 H-ЯМР, 400 МГц, ДМСО-d6: 7,4 (1Н, м), 7,3 (4Н, м), 7,3-7,2 (6Н, м), 7,1 (1Н, с) і 2,4 (3H, д). Проміжний продукт 31 Складний 2-(4-метилбензилокси)етиловий ефір метансульфонової кислоти Отримували аналогічно методиці, описаній в J. Am. Chem. Soc. 2002, 124(28), 8206. РХ/МС (Спосіб 4): Rt 2,44 хв., іона молекули не спостерігали. Проміжний продукт 32 Складний 2-(4-хлорбензилокси)етиловий ефір метансульфонової кислоти Отримували аналогічно проміжному продукту 31. РХ/МС (Спосіб 2): Rt 3,34 хв., іона молекули не спостерігали. Проміжний продукт 33 Складний етиловий ефір 5-метилтіазол-2карбонової кислоти Отримували відповідно до Helv. Chim. Acta., 1946 (29), 1957. Проміжний продукт 30 Складний 2-(4-хлорбензилокси)етиловий ефір метансульфонової кислоти Отримували аналогічно проміжному продукту 31. РХ/МС (Спосіб 4): Rt 3,59 хв., іона молекули не спостерігали. Проміжний продукт 34 (5-Метилтіазол-2-іл)дифенілметанол У крижаний розчин проміжного продукту 29 (0,24 г, 1,402 ммоль) в безводному THF (7 мл) в атмосфері азоту по краплях додавали 3М розчин фенілмагнійброміду в діетиловому ефірі (0,934 мл, 2,80 ммоль). Відразу після завершення додання реакційну суміш залишали нагріватися до к.т. і перемішували протягом 20 хв. Після цього розчин виливали в 1M HCl і двічі екстрагували діетиловим ефіром. Об'єднані органічні шари промивали нас. гідрокарбонатом натрію (водн.), водою і сольовим 1-Бензилокси-3-метил-3-феноксибутан До розчину (3-метилбут-3енілоксиметил)бензолу (4,22 г, 23,9 ммоль) і фенолу (2,25 г, 23,9 ммоль) в 20 мл безводного DCM в атмосфері азоту додавали BF3·Et2O (0,582 мл, 4,78 ммоль). Розчин перемішували при температурі навколишнього середовища протягом ночі, додавали Н2О і розділяли фази. Водну фазу екстрагували DCM (2), органічний шар сушили (MgSO4), і видаляли розчинник з отриманням масла. Неочищений продукт очищали по методу колонкової хроматографії на силікагелі, елююючи 59 градієнтом від циклогексану до 5% діетилового ефіру в циклогексані. Вихід: 0,9 г (14%). РХ/МС (Спосіб 4): Rt 4,47 хв., іона молекули не спостерігали. Проміжний продукт 35 3-Метил-3-феноксибутан-1-ол В інертній атмосфері в колбу додавали гідроксид паладію (II) на вугіллі (20 мас.%) (150 мг), а потім охолоджений IMS (5 мл) і (3-бензил окси-1,1диметилпропокси)бензол (0,73 г, 2,7 ммоль). Колбу продували воднем (3), і перемішували суміш при температурі навколишнього середовища протягом ночі з підключеним балоном водню. Суміш фільтрували через целіт в інертній атмосфері, і упарювали фільтрат з отриманням неочищеного продукту, який очищали по методу колонкової хроматографії, використовучи як елюент градієнт від циклогексану до 50% діетилового ефіру в циклогексані. Вихід: 71 мг, 14%. РХ/МС (Спосіб 4): Rt 2,87 хв., іона молекули не спостерігали. Проміжний продукт 36 Приклад 1 (5-Диметиламінометилоксазол-2a b c d іл)дифенілметанол (I-a): R , R =Ph, R , R =CH3 До холодного (0°С) розчину (5диметиламінометилоксазол-2-іл)фенілметанону (проміжний продукт 4) (0,15 г, 0,65 ммоль) в безводному THF (1,5 мл) по краплях додавали фенілмагнійбромід (0,75 мл 1M розчину в THF, 0,75 ммоль). Суміш перемішували холодної протягом 1,5 год., а потім по краплях додатково додавали фенілмагнійбромід (0,4 мл 1M розчину в THF, 0,4 ммоль). Суміш перемішували при 0°С протягом 0,5 год., а потім обробляли надлишком нас. розчину 95255 60 Складний 3-метил-3-феноксибутиловий ефір метансульфонової кислоти Вказану в заголовку сполуку отримували відповідно до методики, описаної для отримання проміжного продукту 17. Вихід: 37 мг, 37%. РХ/МС (Спосіб 2): Rt 3,45 хв., іона молекули не спостерігали. Проміжний продукт 37 [2-(Циклопентилгідроксифенілметил)оксазолa b 5-іл]ацетонітрил (IX): R =Ph, R =циклопентил Отримували відповідно до способу, що використовується для отримання проміжного продукту 12. Вихід: 0,75 г (57%). + РХ/МС (Спосіб 4): Rt 3,47 хв., m/z 265 [МН Н2О]. Приклади Наступні сполуки отримували з використанням шляху синтезу, представленого на схемі 5. хлориду амонію (водн.). Суміш екстрагували DCM (2), об'єднану органічну фазу промивали сольовим розчином, сушили (Na2SO4) і видаляли розчинник з отриманням неочищеного продукту. Проводили очищення по методу ВЕРХ, елююючи протягом 18,5 хв. 5-70% ацетонітрилом/вода, що містить 0,1% TFA. Вихід: 0,19 г (69%, у вигляді TFA-солі) + РХ/МС (Спосіб 1): Rt 5,56 хв., m/z 309 [МН ]. + РХ/МС (Спосіб 3): Rt 1,72 хв., m/z 309 [МН ]. 1 H-ЯМР (ДМСО-d6): 2,74 (с, 6Н), 4,48 (с, 2Н), 7,25-7,37 (м, 10Н), 7,40 (с, 1Н), 10,23 (ушир.с, 1Н). Зразок цієї речовини перетворювали у вільну основу, пропускаючи через картрідж SCX-2 і елююючи МеОН (3), а потім 2М аміаком/МеОН (3), з отриманням бажаної сполуки у вигляді білої твердої речовини. + РХ/МС (Спосіб 1): Rt 5,68 хв., m/z 309 [МН ]. 1 H-ЯМР (ДМСО-d6): 2,12 (с, 6Н), 3,47 (с, 2Н), 6,98 (с, 1Н), 7,02 (с, 1Н), 7,22-7,34 (м, 10Н). Приклад 2
ДивитисяДодаткова інформація
Назва патенту англійськоюAzole and thiazole derivatives and their use
Автори англійськоюRay Nicholas Charles, Bull Richard James, Finch Harry, Van Den Heuvel Marco, Bravo Jose Antonio
Назва патенту російськоюАзольные и тиазольные производные и их применение
Автори російськоюРей Николас Чарльз, Булл Ричард Джеймс, Финч Герри, ван ден Хевел Марко, Браво Хосе Антонио
МПК / Мітки
МПК: C07D 277/30, C07D 263/32, A61K 31/426, A61K 31/421
Мітки: азольні, тіазольні, похідні, застосування
Код посилання
<a href="https://ua.patents.su/51-95255-azolni-i-tiazolni-pokhidni-i-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Азольні і тіазольні похідні і їх застосування</a>
Попередній патент: Сполуки аналога камптотецину, спосіб їх одержання і фармацевтична композиція, яка їх містить
Наступний патент: Спосіб підвищення експлуатаційних якостей поршневих двигунів внутрішнього згорання
Випадковий патент: Блок керування гідравлічний












