Фторметил-5,6-дигідро-4н-[1,3]оксазини
Формула / Реферат
1. Сполука формули І
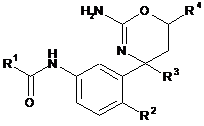 , I
, I
де
R1 вибрано з групи, що складається з
і) арилу,
іі) арилу, що включає 1-4 замісники, індивідуально вибрані з ціаногрупи, ціано-С1-6-алкілу, галогену, галоген-С1-6-алкоксигрупи, галоген-С1-6-алкілу, С1-6-алкоксигрупи, С1-6-алкоксі-С1-6-алкілу, С2-6-алкініл-С1-6-алкоксигрупи, С2-6-алкінілу і С1-6-алкілу
ііі) гетероарилу і
іv) гетероарилу, що включає 1-4 замісники, індивідуально вибрані з ціаногрупи, ціано-С1-6-алкілу, галогену, галоген-С1-6-алкоксигрупи, галоген-С1-6-алкілу, С1-6-алкоксигрупи, С1-6-алкоксі-С1-6-алкілу, С2-6-алкініл-С1-6-алкоксигрупи, С2-6-алкінілу і С1-6-алкілу;
R2 вибрано з групи, що складається з
і) водню,
іі) С1-6-алкілу і
ііі) галогену;
R3 вибрано з групи, що складається з
і) С1-6-алкілу і
іі) галоген-С1-6-алкілу;
R4 позначає галоген-С1-6-алкіл;
або її фармацевтично прийнятні солі.
2. Сполука за п. 1, де R1 позначає гетероарил, що містить 1-2 замісники, індивідуально вибрані з ціаногрупи, ціано-С1-6-алкілу, галогену, галоген-С1-6-алкоксигрупи, галоген-С1-6-алкілу, С1-6-алкоксигрупи, С1-6-алкоксі-С1-6-алкілу, С2-6-алкініл-С1-6-алкоксигрупи, С2-6-алкінілу і С1-6-алкілу.
3. Сполука за будь-яким з пп. 1-2, де R2 позначає галоген.
4. Сполука за будь-яким з пп. 1-3, де R2 позначає F.
5. Сполука за будь-яким з пп. 1-4, де R3 позначає фтор-С1-6-алкіл.
6. Сполука за будь-яким з пп. 1-5, де R3 позначає фторметил.
7. Сполука за будь-яким з пп. 1-4, де R3 позначає С1-6-алкіл.
8. Сполука за будь-яким з пп. 1-4 і 7, де R3 позначає метил.
9. Сполука за будь-яким з пп. 1-8, де R4 позначає фтор-С1-6-алкіл.
10. Сполука за будь-яким з пп. 1-9, де R4 позначає трифторметил.
11. Сполука за будь-яким з пп. 1-10, що позначає сполуку формули Іа-1
 , Ia-1
, Ia-1
де
R1 вибрано з групи, що складається з
і) арилу,
іі) арилу, що містить 1-2 замісники, індивідуально вибрані з ціаногрупи, ціано-С1-6-алкілу, галогену, галоген-С1-6-алкоксигрупи, галоген-С1-6-алкілу, С1-6-алкоксигрупи, С1-6-алкоксі-С1-6-алкілу, С2-6-алкініл-С1-6-алкоксигрупи, С2-6-алкінілу і С1-6-алкілу,
ііі) гетероарилу і
iv) гетероарилу, що містить 1-2 замісники, індивідуально вибрані з ціаногрупи, ціано-С1-6-алкілу, галогену, галоген-С1-6-алкоксигрупи, галоген-С1-6-алкілу, С1-6-алкоксигрупи, С1-6-алкоксі-С1-6-алкілу, С2-6-алкініл-С1-6-алкоксигрупи, С2-6-алкінілу і С1-6-алкілу; і
R3 вибрано з групи, що складається з
і) С1-6-алкілу і
іі) галоген-С1-6-алкілу,
або її фармацевтично прийнятні солі.
12. Сполука за будь-яким з пп. 1-11, де R1 позначає гетероарил, що містить 1-2 замісники, індивідуально вибрані з ціаногрупи, галогену, галоген-С1-6-алкоксигрупи, галоген-С1-6-алкілу, С1-6-алкоксигрупи, С2-6-алкініл-С1-6-алкоксигрупи і С1-6-алкілу.
13. Сполука за будь-яким з пп. 1-12, де R1 позначає гетероарил, що містить 1-2 замісники, індивідуально вибрані з ціаногрупи, галогену, галоген-С1-6-алкоксигрупи і С1-6-алкоксигрупи.
14. Сполука за будь-яким з пп. 1-13, де R1 позначає 1-(дифторметил)-1Н-піразол-3-іл, 2-(фторметил)оксазол-4-іл, 3,5-дихлорпіридин-2-іл, 3-хлор-5-ціанопіридин-2-іл, 3-метилпіразин-2-іл, 4-хлор-1-(дифторметил)-1Н-піразол-3-іл, 5-(2,2,2-трифторетокси)піразин-2-іл, 5-(2,2-дифторетокси)піразин-2-іл, 5-(бут-2-инілокси)піразин-2-іл, 5-(дифторметокси)піразин-2-іл, 5-(дифторметил)піразин-2-іл, 5-(фторметокси)піразин-2-іл, 5-(фторметил)піразин-2-іл, 5-хлорпіридин-2-іл, 5-ціано-3-метилпіридин-2-іл, 5-ціанопіридин-2-іл, 5-дифторметоксипіразин-2-іл, 5-дифторметоксипіридин-2-іл, 5-дифторметилпіридин-2-іл, 5-фторметоксипіридин-2-іл, 5-метоксипіразин-2-іл, 5-метоксипіридин-2-іл, 5-метилпіразин-2-іл, 5-трифторетоксипіридин-2-іл, 5-трифторметоксипіразин-2-іл або 5-трифторметоксипіридин-2-іл.
15. Сполука за будь-яким з пп. 1-14, де R1 позначає 5-ціанопіридин-2-іл, 5-хлорпіридин-2-іл, 5-(2,2-дифторетокси)піразин-2-іл, 5-(2,2,2-трифторетокси)піразин-2-іл або 5-метоксипіразин-2-іл.
16. Сполука за будь-яким з пп. 1-15, де R1 позначає 5-ціанопіридин-2-іл.
17. Сполука за будь-яким з пп. 1-16, яку вибирають з групи, що включає:
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-ціанопіколінамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-хлорпіколінамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-ціанопіколінамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-хлорпіколінамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-метоксипіразин-2-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(2,2-дифторетокси)піразин-2-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(2,2,2-трифторетокси)піразин-2-карбоксамід,
N-(3-((4S,6R)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-ціанопіколінамід,
N-(3-((4S,6R)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-хлорпіколінамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-3,5-хлорпіколінамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(фторметокси)піколінамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-ціано-3-метилпіколінамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-3-хлор-5-ціанопіколінамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-метоксипіколінамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(дифторметокси)піколінамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(трифторметокси)піколінамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(дифторметил)піколінамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(2,2,2-трифторетокси)піколінамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(фторметил)піразин-2-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(дифторметил)піразин-2-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-метилпіразин-2-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(бут-2-инілокси)піразин-2-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(фторметокси)піразин-2-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(дифторметокси)піразин-2-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-2-(фторметил)оксазол-4-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-4-хлор-1-(дифторметил)-1Н-піразол-3-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-ціано-3-метилпіколінамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-3-хлор-5-ціанопіколінамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-3,5-дихлорпіколінамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-метоксипіколінамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(дифторметокси)піколінамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(трифторметокси)піколінамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(дифторметил)піколінамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(2,2,2-трифторетокси)піколінамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(фторметокси)піколінамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-метоксипіразин-2-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(фторметил)піразин-2-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(бут-2-инілокси)піразин-2-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(дифторметокси)піразин-2-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(2,2-дифторетокси)піразин-2-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(2,2,2-трифторетокси)піразин-2-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-метилпіразин-2-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(фторметокси)піразин-2-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-3-метилпіразин-2-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(дифторметил)піразин-2-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-4-хлор-1-(дифторметил)-1Н-піразол-3-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-2-(фторметил)оксазол-4-карбоксамід,
N-(3-((4S,6R)-2-аміно-4-(дифторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-ціанопіколінамід і
N-(3-((4S,6S)-2-аміно-4-(дифторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-ціанопіколінамід
або її фармацевтично прийнятна сіль.
18. Сполука за будь-яким з пп. 1-17, яку вибирають з групи, що включає:
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-ціанопіколінамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-хлорпіколінамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-ціанопіколінамід,
N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-хлорпіколінамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-метоксипіразин-2-карбоксамід,
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(2,2-дифторетокси)піразин-2-карбоксамід і
N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4Н-1,3-оксазин-4-іл)-4-фторфеніл)-5-(2,2,2-трифторетокси)піразин-2-карбоксамід,
або її фармацевтично прийнятна сіль.
19. Спосіб одержання сполуки формули І за будь-яким з пп. 1-18, згідно з яким вводять в реакцію сполуку формули ХI’ із сполукою формули ХІI’ з утворенням сполуки формули І
 ’
’
де R1, R2, R3 і R4 розкриті в будь-якому з пп. 1-16.
20. Сполука формули І за будь-яким з пп. 1-18, у всіх випадках, коли вона одержана способом, розкритим в п. 19.
21. Сполука формули І за будь-яким з пп. 1-18 для застосування як терапевтично активної речовини.
22. Сполука формули І за пп. 1-18 для застосування як терапевтично активної речовини для терапевтичного та/або профілактичного лікування захворювань і розладів, що характеризуються підвищеним рівнем b-амілоїду та/або олігомерів b-амілоїду, та/або b-амілоїдних бляшок та інших відкладень, або хвороби Альцгеймера.
23. Сполука формули І за пп. 1-18 для застосування як терапевтично активної речовини для терапевтичного та/або профілактичного лікування аміотрофічного бічного склерозу (ALS), артеріального тромбозу, аутоімунних/запальних захворювань, раку, наприклад раку молочної залози, серцево-судинних захворювань, таких як інфаркт міокарда та інсульт, дерматоміозиту, синдрому Дауна, захворювань шлунково-кишкового тракту, мультиморфної гліобластоми, базедової хвороби, хвороби Гентінгтона, міозиту з включеними тільцями (IBM), запальних реакцій, саркоми Капоші, хвороби Костманна, еритематозного вовчака, міофасциту макрофагового, ювенільного ідіопатичного артриту, гранулематозного артриту, злоякісної меланоми, множинної мієломи, ревматоїдного артриту, синдрому Шегрена, спіноцеребелярної атаксії 1, спіноцеребелярної атаксії 7, хвороби Уіппла або хвороби Вільсона.
24. Фармацевтична композиція, яка включає сполуку формули І за будь-яким з пп. 1-18 і фармацевтично прийнятний носій та/або фармацевтично прийнятну допоміжну речовину.
25. Застосування сполуки формули І за будь-яким з пп. 1-18 для виготовлення лікарського засобу для терапевтичного та/або профілактичного лікування хвороби Альцгеймера.
26. Застосування сполуки формули І за будь-яким з пп. 1-18 для виготовлення лікарського засобу для терапевтичного та/або профілактичного лікування аміотрофічного бічного склерозу (ALS), артеріального тромбозу, аутоімунних/запальних захворювань, раку, наприклад раку молочної залози, серцево-судинних захворювань, таких як інфаркт міокарда і інсульт, дерматоміозиту, синдрому Дауна, захворювань шлунково-кишкового тракту, мультиморфної гліобластоми, базедової хвороби, хвороби Гентінгтона, міозиту з включеними тільцями (IBM), запальних реакцій, саркоми Капоші, хвороби Костманна, еритематозного вовчака, міофасциту макрофагового, ювенільного ідіопатичного артриту, гранулематозного артриту, злоякісної меланоми, множинної мієломи, ревматоїдного артриту, синдрому Шегрена, спіноцеребелярної атаксії 1, спіноцеребелярної атаксії 7, хвороби Уіппла або хвороби Вільсона.
27. Спосіб для застосування в терапевтичному та/або профілактичному лікуванні хвороби Альцгеймера або аміотрофічного бічного склерозу (ALS), артеріального тромбозу, аутоімунних/запальних захворювань, раку, наприклад раку молочної залози, серцево-судинних захворювань, таких як інфаркт міокарда та інсульт, дерматоміозиту, синдрому Дауна, захворювань шлунково-кишкового тракту, мультиморфної гліобластоми, базедової хвороби, хвороби Гентінгтона, міозиту з включеними тільцями (IBM), запальних реакцій, саркоми Капоші, хвороби Костманна, еритематозного вовчака, міофасциту макрофагового, ювенільного ідіопатичного артриту, гранулематозного артриту, злоякісної меланоми, множинної мієломи, ревматоїдного артриту, синдрому Шегрена, спіноцеребелярної атаксії 1, спіноцеребелярної атаксії 7, хвороби Уіппла або хвороби Вільсона, що включає введення сполуки формули І за будь-яким з пп. 1-18 людині або тварині.
Текст
Реферат: Даний винахід пропонує сполуки формули І R H N 1 O R O H2N 4 N R R 3 2 ,I (72) Винахідник(и): Хільперт Ханс (CH), Хумм Роланд (DE), Волтерінг Томас (DE) (73) Власник(и): Ф. ХОФФМАНН-ЛЯ РОШ АГ, Grenzacherstrasse 124, CH-4070 Basel, Switzerland (CH), СІЄНА БІОТЕК С.П.А, Strada del Petriccio e Belriguardo 35, I-53100 Siena, Italy (IT) (74) Представник: Новiкова Лiдiя Аркадiївна, реєстр. №36 (56) Перелік документів, взятих до уваги експертизою: WO 2011/069934 A1 (HOFFMANN LA ROCHE [CH]; SIENA BIOTECH SPA [IT]; BANNER DAVID [CH]; GUB), 16.06.2011 WO 2011/009943 A1 (NOVARTIS AG [CH]; BADIGER SANGAMESH [IN]; CHEBROLU MURALI [IN]; FREDER), 27.01.2011 WO 2011/020806 A1 (HOFFMANN LA ROCHE [CH]; SIENA BIOTECH SPA [IT]; ANDREINI MATTEO [IT]), 24.02.2011 WO 2010/128058 A1 (HOFFMANN LA ROCHE [CH]; BANNER DAVID [CH]; HILPERT HANS [CH]; HUMM ROL), 11.11.2010 UA 113538 C2 (12) UA 113538 C2 які мають активність інгібітора ВАСЕ1, їх одержання, фармацевтичні композиції, що містять такі сполуки, та їх застосування як терапевтично активних речовин. Діючі сполуки за даним винаходом корисні в терапевтичному та/або профілактичному лікуванні, наприклад, хвороби Альцгеймера. UA 113538 C2 5 10 15 20 25 30 35 40 45 50 55 60 Попередній рівень техніки Хвороба Альцгеймера (ХА) представляє собою нейродегенеративне захворювання центральної нервової системи і є основною причиною прогресуючого недоумства у літніх людей. Її клінічними симптомами є порушення пам'яті, когнітивних функцій, орієнтації в часі і просторі, помутніння свідомості і порушення інтелектуальної діяльності, а також серьйозні емоційні розлади. В даний час не існує ефективної терапії для профілактики виникнення або прогресу даного захворювання або ж стабільної ремісії його клінічних симптомів. ХА стала головною медичною проблемою у всіх соціумах з високим показником середньої тривалості життя, а також значним економічним тягарем для їх систем охорони здоров'я. ХА характеризується двома основними патологіями в центральній нервовій системі (ЦНС): виникненням амілоїдних бляшок і нейрофібрилярних клубків (Hardy et al., The amyloid hypothesis of Alzheimer's disease: progress and problems on the road to therapeutics, Science. 2002 Jul 19;297(5580):353-6, Selkoe, Cell biology of the amyloid beta-protein precursor and the mechanism of Alzheimer's disease, Annu Rev Cell Biol. 1994;10:373-403). Обидві патології часто виявляються у пацієнтів з синдромом Дауна (трисомія 21), у яких в молодості розвиваються симптоми, схожі з симптомами хвороби Альцгеймера. Нейрофібрилярними клубками є внутріклітинні агрегати асоційованого з мікротрубочками тау-білка (MAPT). Амілоїдні бляшки зустрічаються в екстрацелюлярному просторі; їх основними компонентами є Аβ-пептиди. Останні є групою протеолітичних фрагментів, які утворюються з попередника білка бета-амілоїду (APP) в декілька стадій протеолітичного розщеплювання. Ідентифіковано декілька форм APP, з яких найбільш поширені білки довжиною 695, 751 і 770 амінокислот. Вони всі походять з одного і того ж гена за рахунок диференціального сплайсингу. Аβ-пептиди утворюються з одного і того ж домена APP, але розрізняються на N- і C-кінцях, при цьому переважаючі молекули мають довжину 40 і 42 амінокислот. Є цілий ряд даних, виразно вказуючих на те, що агреговані Аβпептиди є молекулами, що відіграють ключову роль в патогенезі ХА: 1) амілоїдні бляшки, утворені Аβ-пептидами, є невід'ємною частиною патології ХА; 2) Аβ-пептиди токсичні для нейронів; 3) при спадковій хворобі Альцгеймера (СХА) мутації в генах схильності до захворювання APP, PSN1, PSN2 приводять до підвищеного рівня Аβ-пептидів і раннього амілоїдозу головного мозку; 4) у трансгенних мишей, експресуючих такі гени СХА, розвивається патологія, яка багато в чому нагадує хворобу людини. Аβ-пептиди утворюються з APP за рахунок послідовної дії двох протеолітичних ферментів, що позначаються як β- і γ-секретаза. Під дією β-секретази спочатку відбувається розщеплювання в позаклітинному домені APP, на відстані приблизно 28 амінокислот від трансмембранного домена (ТМ), з утворенням Cкінцевого фрагмента APP, що містить трансмембранний і цитоплазматичний домен (CTFβ). Доменом CTFβ є субстрат для γ-секретази, яка здійснює розщеплювання за декількома суміжними положеннями усередині ТМ з утворенням Aβ-пептидів і фрагмента цитоплазми. γСекретаза є комплексом, що складається щонайменше з чотирьох різних білків; її каталітична субодиниця дуже близька за структурою до білка пресеніліну (PSEN1, PSEN2). β-Секретаза (BACE1, Asp2; BACE позначає β-сайт APP-розщеплюючого ферменту) є аспартил-протеазою, яка зафіксована на мембрані за рахунок трансмембранного домена (Vassar et al., Beta-secretase cleavage of Alzheimer's amyloid precursor protein by the transmembrane aspartic protease BACE, Science. 1999 Oct 22;286(5440):735). Вона експресується в багатьох тканинах людського організму, але її рівень особливо високий в ЦНС. Шляхом генетичного видалення гена BACE1 у мишей було чітко показано, що активність цього гена відіграє ключову роль в процесуванні APP, яке приводить до утворення Аβ-пептидів; у відсутність BACE1 Аβ-пептиди не продукуються (Luo et al., Mice deficient in Bace1, the Alzheimer's beta-secretase, have normal phenotype and abolished beta-amyloid generation, Nat Neurosci. 2001 Mar;4(3):231-2, Roberds et al., BACE knockout mice are healthy despite lacking the primary beta-secretase activity in brain: implications for Alzheimer's disease therapeutics, Hum Mol Genet. 2001 Jun 1;10(12):1317-24). У мишей, які були генетично модифіковані так, щоб вони експресували людський ген APP, і у яких з віком утворюються обширні амілоїдні бляшки і розвиваються патології, схожі з хворобою Альцгеймера, цього не відбувається, якщо активність β-секретази знижена за рахунок генетичного видалення одного з алелів BACE1 (Mcconlogue et al., Partial reduction of Bace1 has dramatic effects on Alzheimer plaque and synaptic pathology in APP Transgenic Mice. J Biol Chem. 2007 Sep 7;282(36):26326). У зв'язку з цим припускають, що інгібітори активності BACE1 можуть бути ефективними агентами для терапевтичного лікування хвороби Альцгеймера (ХА). Крім того, запропоновані сполуки інгібують утворення або ж утворення і відкладення βамілоїдних пептидів в, на або в області нервової тканини (наприклад, в головному мозку), тобто вони інгібують продукцію Аβ-пептидів з APP або фрагмента APP. Крім цього, інгібітори BACE1 можна застосовувати для лікування наступних захворювань: 1 UA 113538 C2 5 10 15 20 25 30 35 40 45 IBM (міозит з включеними тільцями) (Vattemi G. et al., Lancet. 2001 Dec 8; 358(9297):1962-4), синдром Дауна (Barbiero L. et al, Exp Neurol. 2003 Aug; 182(2):335-45), хвороба Вільсона (Sugimoto I. et al., J Biol Chem. 2007 Nov 30; 282(48):34896-903), хвороба Уіппла (Desnues B. et al., Clin Vaccine Immunol. 2006 Feb; 13(2):170-8), спіноцеребелярна атаксія 1 і спіноцеребелярна атаксія 7 (Gatchel J.R. et al., Proc Natl Acad Sci U S A 2008 Jan 29; 105(4):1291-6), дерматоміозит (Greenberg S.A. et al., Ann Neurol. 2005 Can; 57(5):664-78; Greenberg S.A. et al., Neurol 2005 Can; 57(5):664-78), саркома Капоши (Lagos D. et al, Blood, 2007 Feb 15; 109(4):1550-8), мультиформна гліобластома (E-MEXP-2576, http://www.ebi.ac.uk/microarrayas/aer/result?queryFor=PhysicalArrayDesign&aAccession=A-MEXP-258),ревматоїдний артрит (Ungethuem U. et al, Gse2053), аміотрофічний бічний склероз (Koistinen H. et al., Muscle Nerve. 2006 Oct; 34(4):444-50; Li Q.x. et al, Aging Cell. 2006 Apr; 5(2):153-65), хвороба Гентінгтона (Kim Y.j. et al., Neurobiol Dis. 2006 Can; 22(2):346-56. Epub 2006 Jan 19; Hodges A. et al., Hum Mol Genet. 2006 Mar 15;15(6):965-77. Epub 2006 Feb 8), множинна мієлома (Kihara Y. et al, Proc Natl Acad Sci U S A. 2009 Dec 22; 106(51): 21807-12), злоякісна меланома (Talantov D. et al, Clin Cancer Res. 2005 Oct 15; 11(20):7234-42), синдром Шегрена (Basset C. et al., Scand J Immunol. 2000 Mar; 51(3): 307-11), еритематозний вовчак (Grewal P.K. et al, Mol Cell Biol. 2006, Jul; 26(13):4970-81), міофасцит макрофаговий, ювенільний ідіопатичний артрит, гранулематозний артрит, рак молочної залози (Hedlund M. et al, Cancer Res. 2008 Jan 15; 68(2):388-94; Kondoh K. et al., Breast Cancer Res Treat. 2003 Mar; 78(1):37-44), захворювання шлунково-кишкового тракту (Hoffmeister A. et al, JOP. 2009 Sep 4; 10(5): 501-6), аутоімунні/запальні захворювання (Woodardgrice A.v. et al., J Biol Chem. 2008 Sep 26; 283(39): 26364-73. Epub 2008 Jul 23), ревматоїдний артрит (Toegel S. et al, Osteoarthritis Cartilage. 2010 Feb; 18(2): 240-8. Epub 2009 Sep 22), запальні реакції (Lichtenthaler S.f. et al., J Biol Chem. 2003 Dec 5; 278(49): 48713-9. Epub 2003 Sep 24), артеріальний тромбоз (Merten M. et al., Z Kardiol. 2004 Nov; 93(11): 855-63), серцевосудинні захворювання, такі як інфаркт міокарда та інсульт (Maugeri N. et al., Srp Arh Celok Lek. 2010 Jan; 138 Suppl 1:50-2) і базедова хвороба (Kiljaсski J. et al, Thyroid. 2005 Jul; 15(7): 645-52). Даний винахід пропонує нові сполуки формули I, їх одержання, лікарські засоби на основі сполук за винаходом та їх виготовлення, а також застосування сполук формули I для здійснення контролю або профілактики захворювань, таких як хвороба Альцгеймера. Крім того, запропоновано застосування сполук формули I в лікуванні аміотрофічного бічного склерозу (ALS), артеріального тромбозу, аутоімунних/запальних захворювань, раку, наприклад раку молочної залози, серцево-судинних захворювань, таких як інфаркт міокарда або інсульт, дерматоміозиту, синдрому Дауна, захворювань шлунково-кишкового тракту, мультиморфної гліобластоми, базедової хвороби, хвороби Гентінгтона, міозиту з включеними тільцями (IBM), запальних реакцій, саркоми Капоши, хвороби Костманна, еритематозного вовчаку, міофасциту макрофагового, ювенільного ідіопатичного артриту, гранулематозного артриту, злоякісної меланоми, множинної мієломи, ревматоїдного артриту, синдрому Шегрена, спіноцеребелярної атаксії 1, спіноцеребелярної атаксії 7, хвороби Уіппла або хвороби Вільсона. Нові сполуки формули I мають покращувані фармакологічні властивості. Область техніки Даний винахід пропонує фторметил-5,6-дигідро-4H-[1,3]оксазин-2-іламіни, що мають властивості інгібіторів BACE1, їх одержання, фармацевтичні композиції, що містять такі сполуки, а також їх застосування як терапевтично активних речовин. Суть винаходу Даний винахід пропонує сполуку формули I, H2N H N 1 R O 50 4 R O N 3 R 2 R I, де замісники та змінні описані нижче, а також у формулі винаходу, або їх фармацевтично прийнятні солі. Заявлені сполуки мають активність інгібіторів Asp2 (β-секретази, BACE1 або Мемплазину-2), і тому їх можна застосовувати для терапевтичного та/або профілактичного лікування захворювань і розладів, які характеризуються підвищеним рівнем β-амілоїду та/або олігомерів β-амілоїду та/або β-амілоїдних бляшок та інших відкладень, зокрема, хвороби Альцгеймера. Докладний опис винаходу 2 UA 113538 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід пропонує сполуку формули I та її фармацевтично прийнятні солі, одержання вище зазначених сполук, що містять їх лікарські засоби і виготовлення, а також застосування вище зазначених сполук для терапевтичного та/або профілактичного лікування захворювань і розладів, які пов'язані з інгібуванням BACE1, наприклад хвороби Альцгеймера. Крім того, утворення або ж утворення і відкладення β-амілоїдних бляшок в, на або в області нервової тканини (наприклад, в головному мозку) інгібуються запропонованими сполуками, за рахунок інгібування продукції Аβ-пептидів з APP або фрагмента APP. Нижче наступні визначення загальних термінів використовуваних в даному описі, застосовуються незалежно від того, чи зустрічається обговорюваний термін окремо або у поєднанні з іншими групами. Якщо не зазначено інше, нижче наступні терміни, використовувані в даній Заявці, включаючи опис і формулу винаходу мають значення, розкриті нижче. Слід відмітити, що використовувані в даному описі і наданій формулі винаходу форми однини включають посилання на форми множини, окрім тих випадків, коли з контексту не виходить протилежне. Термін "C1-6-алкіл", окремо або у поєднанні з іншими групами, позначає вуглеводневий радикал, який може бути лінійним або розгалуженим, з єдиним або декількома розгалуженнями, причому зазначений алкіл в загальному випадку включає від 1 до 6 атомів вуглецю, наприклад, метил (Me), етил (Et), пропіл, ізопропіл, н-бутил, ізобутил, 2-бутил (втор-бутил), трет-бутил, ізопентил, 2-етилпропіл (2-метилпропіл), 1,2-диметилпропіл і т.п. Зокрема, “C1-6-алкіл” позначає "C1-3-алкіл". У окремому випадку, такими групами є метил і етил. Окремим прикладом є метил. Термін “галоген-C1-6-алкіл”, окремо або у поєднанні з іншими групами, позначає C1-6-алкіл, розкритий в даному описі, який заміщений одним або декількома атомами галогену, зокрема 1-5 атомами галогену, в окремому випадку 1-3 атомами галогену. Зокрема, галогеном є фтор. У окремому випадку, “галоген-C1-6-алкіл” позначає фтор-C1-6-алкіл, і в окремому випадку, “галогенC1-3-алкіл” позначає фтор-C1-3-алкіл. Прикладами є трифторметил, дифторметил, фторметил і т.п. У окремому випадку, такою групою є трифторметил. Термін “ціано-C1-6-алкіл”, окремо або у поєднанні з іншими групами, позначає C1-6-алкіл, розкритий в даному описі, який заміщений однією або декількома ціаногрупами, зокрема однією ціаногрупою. Прикладами є ціанометил, ціаноетил і т. п. Термін “C1-6-алкокси-C1-6-алкіл”, окремо або у поєднанні з іншими групами, позначає C1-6алкіл, розкритий в даному описі, який заміщений одним або декількома C1-6-алкоксигрупами, розкритими в даному описі, зокрема, однією C1-6-алкоксигрупою. У окремому випадку, “C1-6алкокси-C1-6-алкіл” позначає метокси-C1-6-алкіл. Прикладами є метоксиметил, метоксиетил і т. п. Термін “ціано”, окремо або у поєднанні з іншими групами, позначає групу N≡C-(NC-). Термін "галоген", окремо або у поєднанні з іншими групами, позначає хлор (Cl), йод (I), фтор (F) і бром (Br). Зокрема, “галоген” позначає Cl і F. У окремому випадку, такою групою є атом F. Термін "гетероарил", окремо або у поєднанні з іншими групами, позначає ароматичну карбоциклічну групу, що містить єдине кільце, що включає від 4 до 8 членів, зокрема, від 3 до 5 членів, або декількох конденсованих кілець, що включають від 6 до 14, зокрема, від 6 до 10 кільцевих атомів, і що містить 1, 2 або 3 гетероатоми індивідуально вибраних з N, O і S, зокрема з одного або двох атомів N, причому в цій групі щонайменше одне гетероциклічне кільце є ароматичним. Приклади "гетероарилу" включають бензофурил, бензоімідазоліл, 1Hбензоімідазоліл, бензоксазиніл, бензоксазоліл, бензотіазиніл, бензотіазоліл, бензотієніл, бензотриазоліл, фурил, імідазоліл, індазоліл, 1H-індазоліл індоліл, ізохінолініл, ізотіазоліл, ізоксазоліл, оксазоліл, піразиніл, піразоліл (піразил), 1H-піразоліл, піразоло[1,5-a]піридиніл, піридазиніл, піридиніл, піримідиніл, піроліл, хінолініл, тетразоліл, тіазоліл, тиєніл, триазоліл, 6,7дигідро-5H-[1]піриндиніл і т. п. Зокрема, "гетероарил" є піридинілом і піразинілом, а також оксазолілом і 1H-піразолілом. В окремому випадку, "гетероарил" позначає піридин-2-іл і піразин2-іл, а також 1H-піразол-3-іл і оксазол-4-іл. Термін C1-6-алкоксигрупа", окремо або у поєднанні з іншими групами, позначає -O-C1-6алкільний радикал, який може бути лінійним або розгалуженим, з єдиним або декількома розгалуженнями, при цьому зазначена алкільна група в загальному випадку включає від 1 до 6 атомів вуглецю, наприклад, метокси- (OMe, MeO), етокси- (OEt), пропокси-, ізопропокси-, нбутокси-, ізобутокси-, 2-бутокси- (втор-бутокси-), трет-бутокси-, ізопентилоксигрупа і т. п. Зокрема, “ C1-6-алкоксигрупа” позначає групу, що включає від 1 до 4 атомів вуглецю. Окремим випадком є метоксигрупа. Термін “галоген-C1-6-алкоксигрупа”, окремо або у поєднанні з іншими групами, позначає C1-6алкоксигрупу, яка розкрита в даному описі, містить як замісника один або декілька атомів галогену, зокрема, фтору. У окремому випадку, “галоген-C1-6-алкоксигрупа” позначає фтор-C1-6алкоксигрупу. Зокрема, “галоген-C1-6-алкокси” позначає трифторметоксигрупу. 3 UA 113538 C2 5 10 15 20 25 30 35 40 45 50 55 60 Термін “C2-6-алкініл-C1-6-алкокси”, окремо або у поєднанні з іншими групами, позначає C1-6-алкоксигрупу, розкриту в даному описі, яка заміщена одним або декількома C2-6алкінілами, розкритими в даному описі, зокрема, одним C2-6-алкінілом. Термін “ C2-6-алкініл”, окремо або у поєднанні з іншими групами, позначає моновалентну лінійну або розгалужену насичену вуглеводневу групу, що включає від 2 до 6 атомів вуглецю, зокрема, від 2 до 4 атомів вуглецю, і що включає один, два або три потрійних зв'язків. Приклади C2-6-алкінілу включають етиніл, пропініл і н-бутиніл. Термін “арил” позначає моновалентну ароматичну карбоциклічну моно- або біциклічну кільцеву систему, що включає від 6 до 10 кільцевих атомів вуглецю. Приклади арильних груп включають феніл і нафтил. Зокрема, “арил” позначає феніл. Термін "фармацевтично прийнятні солі" позначає солі, які підходять для застосування у контакті з тканинами людини або тварини. Прикладами відповідних солей з неорганічними і органічними кислотами є, без обмеження, солі оцтової кислоти, лимонної кислоти, мурашиної кислоти, фумарової кислоти, хлороводневої кислоти, молочної кислоти, малеїнової кислоти, яблучної кислоти, метансульфонової кислоти, азотної кислоти, фосфорної кислоти, птолуолсульфонової кислоти, янтарної кислоти, сірчаної кислоти (сірчистої кислоти), винної кислоти, трифтороцтової кислоти і т. п. Зокрема, така кислота є мурашиною кислотою, трифтороцтовою кислотою і хлороводневою кислотою. Зокрема, такою кислотою є хлороводнева кислота, трифтороцтова кислота і фумарова кислота. Терміни “фармацевтично прийнятний носій” і “фармацевтично прийнятну допоміжну речовину” позначають носії і допоміжні речовини, такі як розчинники або наповнювачі, сумісні з іншими компонентами лікарської форми. Термін "фармацевтична композиція" включає продукт, що містить зазначені інгредієнти в заздалегідь певних кількостях або пропорціях, а також будь-який продукт, який можна одержати, прямо або опосередковано, шляхом комбінації зазначених інгредієнтів в заданих кількостях. Зокрема, він охоплює продукт, що включає один або більше активних інгредієнтів і, можливо, носій, що включає інертні інгредієнти, а також будь-який продукт, який можна одержати, прямо або опосередковано, в результаті поєднання, комплексування або агрегації будь-яких двох або більше інгредієнтів або в результаті дисоціації одного або більше інгредієнтів або за рахунок інших типів реакцій або взаємодій одного або більше інгредієнтів. Термін “інгібітор” позначає сполуку, яка конкурує із зв’язуванням, знижує зв’язування або перешкоджає зв'язанню конкретного ліганда із заданим рецептором або яке знижує або перешкоджає інгібуванню функції конкретного білка. Термін “напівмаксимальна інгібуюча концентрація” (IC50) позначає концентрацію конкретної сполуки, яка необхідна для досягнення 50% інгібувань біологічного процесу in vitro. Величини IC50 можна логарифмічно перетворювати у величини pIC50 (-log IC50), для яких вищі значення відповідають більшій активності, за експоненціальною залежністю. Величина IC50 є не абсолютною величиною, але залежить від експериментальних умов, наприклад від використовуваних концентрацій. Величину IC50 можна перетворити в абсолютну константу інгібування (Ki) за допомогою рівняння Ченга-Прусоффа (Biochem. Pharmacol. (1973) 22:3099). Термін “константа інгібування” (Ki) позначає абсолютний ступінь спорідненості конкретного інгібітора до рецептора. Її визначають кількісно за допомогою конкурентного аналізу зв’язування, і вона рівна концентрації, при якій конкретний інгібітор зв'язав би 50% рецепторів у відсутності конкуруючого ліганда (наприклад, радіоліганда). Величини Ki можна логарифмічно перетворити у величини pKi (-log Ki), для яких більш високі значення відповідають більшій активності, за експоненціальною залежністю. “Терапевтично ефективна кількість” позначає таку кількість сполуки, якої, при введенні її суб'єктові з метою лікування хворобливого стану, виявляється достатньо для проведення такого лікування для даного хворобливого стану. “Терапевтично ефективна кількість” варіюється залежно від сполуки, хворобливого стану, на який направлено лікування, тяжкості захворювання, на яке направлено лікування, віку і відносного здоров'я суб'єкта, способу і форми введення, думки лікаря-куратора або ветеринара та інших факторів. Термін “розкритий в даному описі” і “описаний в даному тексті” у випадках, коли вони відносяться до змінної, включає за допомогою посилання широке визначення цієї змінної, а також конкретне, конкретніше і найбільш конкретніше визначення, якщо такі є. Терміни “обробка”, “введення в контакт” і “введення в реакцію” в тих випадках, коли вони відносяться до хімічної реакції, означають додавання або змішування двох або більше реагентів у відповідних умовах з одержанням зазначеного та/або бажаного продукту. Слід розуміти, що реакція, яка приводить до зазначеного та/або бажаного продукту, не завжди є безпосереднім результатом поєднання двох реагентів, які були спочатку додані, тобто, можливе утворення в 4 UA 113538 C2 5 10 15 20 25 30 35 реакційній суміші одного або більше проміжних продуктів, що зрештою приводить до одержання зазначеного та/або бажаного продукту. Термін “захисна група” позначає групу, яка селективно блокує реакційноздатний сайт в сполученні з декількома функціональними групами так, щоб можна було селективно провести хімічну реакцію на іншому незахищеному реакційноздатному сайті, в загальноприйнятому значенні, що відноситься до області синтетичної хімії. Захисні групи можна видаляти в потрібний момент. Прикладами захисних груп є аміно-протекторні групи, карбокси-протекторні 1 групи або гідрокси-протекторні групи. Термін “аміно-протекторна група” (тут також P ) позначає групи, призначені для захисту аміногрупи, і включає наступні приклади: бензил, бензилоксикарбоніл (карбобензилокси, CBZ), 9-флюоренілметилоксикарбоніл (FMOC), пметоксибензилоксикарбоніл, п-нітробензилоксикарбоніл, трет-бутоксикарбоніл (ВОС) і трифторацетил. Додаткові приклади таких груп можна знайти в літературі (T. W. Greene and P. G. M. Wuts, “Protective Groups in Organic Synthesis”, 2nd ed., John Wiley & Sons, Inc., New York, NY, 1991, chapter 7; E. Haslam, “Protective Groups in Organic Chemistry”, J. G. W. Mcomie, Ed., Plenum Press, New York, NY, 1973, Chapter 5; T.w. Greene, “Protective Groups in Organic Synthesis”, John Wiley and Sons, New York, NY, 1981). Термін “захищена аміногрупа” позначає аміногрупу, що містить як замісника аміно-протекторні групи. Зокрема, амінопротекторними групами є трет-бутоксикарбонільна група і диметокситритіл. Термін ”група, що підлягає заміщенню“, позначає групу в загальноприйнятому значенні, що відноситься до області синтетичної хімії, тобто атом або групу, які можна замістити в умовах реакції заміщення. Прикладами груп, що підлягають заміщенню, є: атом галогену, зокрема, брому, алканабо ариленсульфонілоксигрупа, наприклад метансульфонілокси-, етансульфонілокси-, тіометил, бензолсульфонілокси-, тозілокси-, дигалогенфосфіноілокси-, можливо, заміщена бензилокси-, ізопропілокси- і ацилоксигрупа. Термін “ароматичний” пов'язаний із загальноприйнятим поняттям ароматичності, розкритим в літературі, зокрема, в IUPAC - Compendium of Chemical Terminology, 2nd, A. D. Mcnaught & A. Wilkinson (Eds). Blackwell Scientific Publications, Oxford (1997). Термін “фармацевтично прийнятна допоміжна речовина” позначає будь-який інгредієнт, що не має терапевтичної активності і що не має токсичності, наприклад розпушувачі, що пов'язуючі речовини, наповнювачі, розчинники, буфери, речовини, регулюючі тонічність, стабілізатори, антиоксиданти, поверхнево-активні речовини або лубріканти, вживаний при виготовленні лікарських форм фармацевтичних продуктів. У всіх випадках, коли в хімічній структурі присутній хіральний атом вуглецю, мається на увазі, що даною структурою охоплені всі стереоізомери, зв'язані з цим хіральним атомом вуглецю, у вигляді чистих стереоізомерів, а також їх сумішей. Даний винахід пропонує також фармацевтичні композиції, способи застосування і способи одержання зазначених вище сполук. Окремі варіанти здійснення можна комбінувати. В одному втіленні даного винаходу запропоновано сполуку формули I, H2N H N 1 R O 40 45 50 4 R O N 3 R 2 R I де 1 R вибирають з групи, що складається з і) арилу, іі) арилу, що включає 1-4 замісники, індивідуально вибрані з ціаногрупи, ціано-C1-6-алкілу, галогену, галоген-C1-6-алкоксигрупи, галоген-C1-6-алкілу, C1-6-алкоксигрупи, C1-6-алкокси- C1-6алкілу, C2-6-алкініл-c1-6-алкоксигрупи, C2-6-алкінілу і C1-6-алкілу, iii) гетероарилу і iv) гетероарилу, що включає 1-4 замісники, індивідуально вибрані з ціаногрупи, ціано-C1-6алкілу, галогену, галоген-C1-6-алкоксигрупи, галоген-C1-6-алкілу, C1-6-алкоксигрупи, C1-6-алкоксиC1-6-алкілу, C2-6-алкініл-C1-6-алкоксигрупи, C2-6-алкінілу і C1-6-алкілу; 2 R вибирають з групи, що складається з i) водню, ii) C1-6-алкілу і 5 UA 113538 C2 5 iii) галогену; 3 R вибирають з групи, що складається з i) C1-6-алкілу і ii) галоген- C1-6-алкілу; 4 R позначає галоген-C1-6-алкіл; або її фармацевтично прийнятні солі. В окремому втіленні даного винаходу запропоновано сполуку формули Ia, H2N H N 1 R N 3 R O 10 15 20 25 2 R Ia де 1 R вибирають з групи, що складається з i) арилу, ii) арилу, що містить 1-2 замісники, індивідуально вибрані з ціаногрупи, ціано-C1-6-алкілу, галогену, галоген-C1-6-алкоксигрупи, галогенC1-6-алкілу, C1-6-алкоксигрупи, C1-6-алкокси-C1-6алкілу, C2-6-алкініл-C1-6-алкоксигрупи, C2-6-алкінілу і C1-6-алкілу, iii) гетероарилу і iv) гетероарилу, що містить 1-2 замісники, індивідуально вибрані з ціаногрупи, ціано C1-6алкілу, галогену, галоген-C1-6-алкоксигрупи, галоген-C1-6-алкілу, C1-6-алкоксигрупи, C1-6-алкоксиC1-6-алкілу, C2-6-алкініл-C1-6-алкоксигрупи, C2-6-алкінілу і C1-6-алкілу; 2 R вибирають з групи, що складається з i) водню, ii) C1-6-алкілу і iii) галогену; 3 R вибирають з групи, що складається з i) C1-6-алкілу і ii) галоген- C1-6-алкілу; 4 R позначає галоген-C1-6-алкіл; або її фармацевтично прийнятні солі. В окремому втіленні даного винаходу запропоновано сполуку формули Ic, H2N H N 1 R O 30 35 40 45 4 R O 4 R O N 3 R 2 R Ic де 1 R вибирають з групи, що складається з i) арилу, ii) арилу, що включає 1-4 замісники, індивідуально вибрані з ціаногрупи, ціано-C1-6-алкілу,, галогену, галоген-C1-6-алкоксигрупи, галоген-C1-6-алкілу, C1-6-алкоксигрупи, C1-6-алкокси-C1-6алкілу, C2-6-алкініл-C1-6-алкоксигрупи, C2-6-алкінілу і C1-6-алкілу, iii) гетероарилу і iv) гетероарилу, що включає 1-4 замісники, індивідуально вибрані з ціаногрупи, ціано-C1-6алкілу, галогену, галоген-C1-6-алкоксигрупи, галоген-C1-6-алкілу, C1-6-алкоксигрупи, C1-6-алкоксиC1-6-алкілу, C2-6-алкініл-C1-6-алкоксигрупи, C2-6-алкінілу і C1-6-алкілу; 2 R вибирають з групи, що складається з i) водню, ii) C1-6-алкілу і iii) галогену; 3 R вибирають з групи, що складається з i) C1-6-алкілу і ii) галоген-C1-6-алкілу; 6 UA 113538 C2 4 R позначає галоген-C1-6-алкіл; або її фармацевтично прийнятні солі. В окремому втіленні даного винаходу запропонован сполуку формули Id, H2N H N 1 R N 3 R O 5 10 15 20 2 R Id де 1 R вибирають з групи, що складається з i) арилу, ii) арилу, що включає 1-4 замісники, індивідуально вибрані з ціаногрупи, ціано-C1-6-алкілу, галогену, галоген-C1-6-алкоксигрупи, галоген-C1-6-алкілу, C1-6-алкоксигрупи, C1-6-алкокси- C1-6алкілу, C2-6-алкініл-C1-6-алкоксигрупи, C2-6-алкінілу і C1-6-алкілу; iii) гетероарилу і iv) гетероарилу, що включає 1-4 замісники, індивідуально вибрані з ціаногрупи, ціано-C1-6алкілу, галогену, галоген-C1-6-алкоксигрупи, галоген-C1-6-алкілу, C1-6-алкоксигрупи, C1-6-алкоксиC1-6-алкілу, C2-6-алкініл-C1-6-алкоксигрупи, C2-6-алкінілу і C1-6-алкілу; 2 R вибирають з групи, що складається з i) водню, ii) C1-6-алкілу і iii) галогену; 3 R вибирають з групи, що складається з i) C1-6-алкілу і ii) галоген- C1-6-алкілу; 4 R позначає галоген-C1-6-алкіл; або її фармацевтично прийнятні солі. В окремому втіленні даного винаходу запропоновано сполуку формули Ia-1, H2N H N 1 R O 25 30 35 40 4 R O CF3 O N 3 R F Ia-1 де 1 R вибирають з групи, що складається з i) арилу, ii) арилу, що містить 1-2 замісники, індивідуально вибрані з ціаногрупи, ціано-C1-6-алкілу, галогену, галоген-C1-6-алкоксигрупи, галоген-C1-6-алкілу, C1-6-алкоксигрупи, C1-6-алкокси-C1-6алкілу, C2-6-алкініл-C1-6-алкоксигрупи, C2-6-алкінілу і C1-6-алкілу, iii) гетероарилу і iv) гетероарилу, що містить 1-2 замісники, індивідуально вибрані з ціаногрупи, ціано-C1-6алкілу, галогену, галоген-C1-6-алкоксигрупи, галоген-C1-6-алкілу, C1-6-алкоксигрупи, C1-6-алкоксиC1-6-алкілу, C2-6-алкініл-C1-6-алкоксигрупи, C2-6-алкінілу і C1-6-алкілу; і 3 R вибирають з групи, що складається з i) C1-6-алкілу і ii) галоген- C1-6-алкілу, або її фармацевтично прийнятні солі. В окремому втіленні даного винаходу запропоновано сполуку формули Ia-1’, 7 UA 113538 C2 H2N H N 1 R O 5 10 15 20 25 30 35 40 45 50 O CF3 N F F Ia-1’ де 1 R позначає гетероарил, що містить 1-2 замісники, індивідуально вибрані з ціаногрупи і галогену, або її фармацевтично прийнятні солі. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 2 R позначає галоген. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 2 R позначає F. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 2 R позначає водень. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 2 R позначає C1-6-алкіл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 2 R позначає метил. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 3 R позначає галоген- C1-6-алкіл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 3 R позначає фтор-C1-6-алкіл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 3 R позначає фторметил. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 3 R позначає C1-6-алкіл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 3 R позначає метил. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 4 R позначає фтор-C1-6-алкіл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 4 R позначає трифторметил. 1 В окремому втіленні даного винаходу запропонован сполуку, розкриту в даному описі, де R позначає гетероарил, що містить 1-2 замісники, індивідуально вибрані з ціаногрупи, ціано-C1-6алкілу, галогену, галоген-C1-6-алкоксигрупи, галоген-C1-6-алкілу, C1-6-алкоксигрупи, C1-6-алкоксиC1-6-алкілу, C2-6-алкініл-C1-6-алкоксигрупи, C2-6-алкінілу і C1-6-алкілу. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає гетероарил, що містить 1-2 замісники, індивідуально вибрані з ціаногрупи, галогену, галоген-C1-6-алкоксигрупи, галоген-C1-6-алкілу, C1-6-алкоксигрупи, C2-6-алкініл-C1-6-алкоксигрупи і C1-6-алкілу. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає гетероарил, що містить 1-2 замісники, індивідуально вибрані з ціаногрупи, галогену, галоген-C1-6-алкоксигрупи і C1-6-алкоксигрупи. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає піридиніл або піразиніл, що містять 1-2 замісники, індивідуально вибрані з ціаногрупи, галогену, галоген-C1-6-алкоксигрупи і C1-6-алкоксигрупи. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає піридиніл, заміщений ціаногрупою. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає піридиніл, заміщений галогеном. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає піридиніл, заміщений галоген-C1-6-алкоксигрупою. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає піридиніл, заміщений C1-6-алкоксигрупою. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає піридиніл, заміщений ціаногрупою і C1-6-алкілом. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 8 UA 113538 C2 1 5 10 15 20 25 30 35 40 45 50 55 60 R позначає піридиніл, заміщений ціаногрупою і галогеном. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає піридиніл, заміщений галоген-C1-6-алкілом. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає піридиніл, заміщений C1-6-алкілом. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає піразиніл, заміщений C1-6-алкілом. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає піразиніл, заміщений галоген-C1-6-алкоксигрупою. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає піразиніл, заміщений галоген-C1-6-алкілом. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає піразиніл, заміщений C1-6-алкоксигрупою. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає піразиніл, заміщений C2-6-алкініл-C1-6-алкоксигрупою. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає оксазоліл, заміщений галоген-C1-6-алкілом. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає піразоліл, заміщений галоген-C1-6-алкіл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 1-(дифторметил)-1H-піразол-3-іл, 2-(фторметил)оксазол-4-іл, 3,5-дихлор-піридин-2іл, 3-хлор-5-ціанопіридин-2-іл, 3-метилпіразин-2-іл, 4-хлор-1-(дифторметил)-1H-піразол-3-іл, 5(2,2,2-трифторетокси)піразин-2-іл, 5-(2,2-дифторетокси)піразин-2-іл, 5-(бут-2-інілокси)піразин-2іл, 5-(дифторметокси)піразин-2-іл, 5-(дифторметил)піразин-2-іл, 5-(фторметокси)піразин-2-іл, 5(фторметил)піразин-2-іл, 5-хлорпіридин-2-іл, 5-ціано-3-метилпіридин-2-іл, 5-ціанопіридин-2-іл, 5дифторметоксипіразин-2-іл, 5-дифторметоксипіридин-2-іл, 5-дифторметилпіридин-2-іл, 5фторметоксипіридин-2-іл, 5-метоксипіразин-2-іл, 5-метоксипіридин-2-іл, 5-метилпіразин-2-іл, 5трифторетоксипіридин-2-іл, 5-трифторметоксипіразин-2-іл або 5-трифторметоксипіридин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-ціанопіридин-2-іл, 5-хлорпіридин-2-іл, 5-(2,2-дифторетокси)піразин-2-іл, 5-(2,2,2трифторетокси)піразин-2-іл або 5-метоксипіразин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 1-(дифторметил)-1H-піразол-3-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 2-(фторметил)оксазол-4-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 3,5-дихлорпіридин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 3-хлор-5-ціанопіридин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 3-метилпіразин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 4-хлор-1-(дифторметил)-1H-піразол-3-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-(бут-2-інілокси)піразин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-(дифторметокси)піразин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-(дифторметил)піразин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-(фторметокси)піразин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-(фторметил)піразин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-ціано-3-метилпіридин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-дифторметоксипіразин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-дифторметоксипіридин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 9 UA 113538 C2 1 5 10 15 20 25 30 35 40 45 50 55 60 R позначає 5-дифторметилпіридин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-фторметоксипіридин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-метоксипіридин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-метилпіразин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-трифторетоксипіридин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-трифторметоксипіразин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-трифторметоксипіридин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-ціанопіридин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-хлорпіридин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-(2,2-дифторетокси)піразин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-(2,2,2-трифторетокси)піразин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, де 1 R позначає 5-метоксипіразин-2-іл. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, вибрану з групи, що складається з наступних сполук: N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-ціанопіколінамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-хлорпіколінамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-ціанопіколінамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-хлорпіколінамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-метоксипіразин-2-карбоксамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(2,2-дифторетокси)піразин-2-карбоксамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(2,2,2-трифторетокси)піразин-2-карбоксамід, N-(3-((4S,6R)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-ціанопіколінамід, N-(3-((4S,6R)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-хлорпіколінамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-3,5-хлорпіколінамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(фторметокси)піколінамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-ціано-3-метилпіколінамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-3-хлор-5-ціанопіколінамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-метоксипіколінамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(дифторметокси)піколінамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(трифторметокси)піколінамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(дифторметил)піколінамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4 10 UA 113538 C2 5 10 15 20 25 30 35 40 45 50 55 60 фторфеніл)-5-(2,2,2-трифторетокси)піколінамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(фторметил)піразин-2-карбоксамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(дифторметил)піразин-2-карбоксамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-метилпіразин-2-карбоксамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(бут-2-інілокси)піразин-2-карбоксамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(фторметокси)піразин-2-карбоксамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(дифторметокси)піразин-2-карбоксамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-2-(фторметил)оксазол-4-карбоксамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-4-хлор-1-(дифторметил)-1H-піразол-3-карбоксамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-ціано-3-метилпіколінамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-3-хлор-5-ціанопіколінамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-3,5-дихлорпіколінамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-метоксипіколінамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(дифторметокси)піколінамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(трифторметокси)піколінамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(дифторметил)піколінамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(2,2,2-трифторетокси)піколінамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(фторметокси)піколінамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-метоксипіразин-2-карбоксамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(фторметил)піразин-2-карбоксамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(бут-2-інілокси)піразин-2-карбоксамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(дифторметокси)піразин-2-карбоксамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(2,2-дифторетокси)піразин-2-карбоксамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(2,2,2-трифторетокси)піразин-2-карбоксамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-метилпіразин-2-карбоксамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(фторметокси)піразин-2-карбоксамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-3-метилпіразин-2-карбоксамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(дифторметил)піразин-2-карбоксамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-4-хлор-1-(дифторметил)-1H-піразол-3-карбоксамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-2-(фторметил)оксазол-4-карбоксамід, N-(3-((4S,6R)-2-аміно-4-(дифторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4 11 UA 113538 C2 5 10 15 20 25 30 35 40 фторфеніл)-5-ціанопіколінамід і N-(3-((4S,6S)-2-аміно-4-(дифторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-ціанопіколінамід або її фармацевтично прийнятна сіль. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, вибрану з групи, що складається з наступних сполук: N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-ціанопіколінамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-хлорпіколінамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-ціанопіколінамід, N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-хлорпіколінамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-метоксипіразин-2-карбоксамід, N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(2,2-дифторетокси)піразин-2-карбоксамід і N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(2,2,2-трифторетокси)піразин-2-карбоксамід або її фармацевтично прийнятна сіль. В окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, яка позначає N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-ціанопіколінамід; в окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, яка позначає N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-хлорпіколінамід; в окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, яка позначає N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4іл)-4-фторфеніл)-5-ціанопіколінамід; в окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, яка позначає N-(3-((4S,6S)-2-аміно-4-(фторметил)-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4іл)-4-фторфеніл)-5-хлорпіколінамід; в окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, яка позначає N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-метоксипіразин-2-карбоксамід; в окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, яка позначає N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(2,2-дифторетокси)піразин-2-карбоксамід; і в окремому втіленні даного винаходу запропоновано сполуку, розкриту в даному описі, яка позначає N-(3-((4S,6S)-2-аміно-4-метил-6-(трифторметил)-5,6-дигідро-4H-1,3-оксазин-4-іл)-4фторфеніл)-5-(2,2,2-трифторетокси)піразин-2-карбоксамід. В окремому втіленні даного винаходу запропоновано спосіб, що включає введення в реакцію сполуки формули XI’ із сполукою формули XII’ з одержанням сполуки формули I. H2N 4 R O N H2N 1 3 R 50 XI' 1 2 OH O 2 R 45 R XII' 3 4 де R , R , R і R розкриті в даному описі. В окремому втіленні даного винаходу запропоновано сполуку формули I, розкриту в даному описі, у всіх випадках, коли вона одержана способом, визначеним вище. В окремому втіленні даного винаходу запропоновано сполуку формули I, розкриту в даному описі, для застосування як терапевтично активної речовини. В окремому втіленні даного винаходу запропоновано сполуку формули I, розкриту в даному 12 UA 113538 C2 5 10 15 20 25 30 35 40 45 50 55 60 описі, для застосування як інгібітора активності BACE1. В окремому втіленні даного винаходу запропоновано сполуку формули I, розкриту в даному описі, для застосування як терапевтично активної речовини для терапевтичного та/або профілактичного лікування захворювань і розладів, що характеризуються підвищеним рівнем βамілоїду та/або олігомерів β-амілоїду та/або β-амілоїдних бляшок та інших відкладень, або хвороби Альцгеймера. В окремому втіленні даного винаходу запропоновано сполуку формули I, розкриту в даному описі, для застосування як терапевтично активної речовини для терапевтичного та/або профілактичного лікування хвороби Альцгеймера. В окремому втіленні даного винаходу запропоновано сполуку формули I, розкриту в даному описі для застосування як терапевтично активної речовини для терапевтичного та/або профілактичного лікування аміотрофічного бічного склерозу (ALS), артеріального тромбозу, аутоімунних/запальних захворювань, раку, наприклад раку молочної залози, серцево-судинних захворювань, таких як інфаркт міокарда і інсульт, дерматоміозиту, синдрому Дауна, захворювань шлунково-кишкового тракту, мультиморфної гліобластоми, базедової хвороби, хвороби Гентінгтона, міозиту з включеними тільцями (IBM), запальних реакцій, саркоми Капоши, хвороби Костманна, еритематозного вовчаку, міофасциту макрофагового, ювенільного ідіопатичного артриту, гранулематозного артриту, злоякісної меланоми, множинної мієломи, ревматоїдного артриту, синдрому Шегрена, спіноцеребелярної атаксії 1, спіноцеребелярної атаксії 7, хвороби Уіппла або хвороби Вільсона. В окремому втіленні даного винаходу запропоновано фармацевтичну композицію, що включає сполуку формули I, розкриту в даному описі, і фармацевтично прийнятний носій та/або фармацевтично прийнятну допоміжну речовину. В окремому втіленні даного винаходу запропоновано застосування сполуки формули I, розкритої в даному описі, для виготовлення лікарського засобу для застосування в інгібуванні активності BACE1. В окремому втіленні даного винаходу запропоновано застосування сполуки формули I, розкритої в даному описі, для виготовлення лікарського засобу для терапевтичного та/або профілактичного лікування захворювань і розладів, що характеризуються підвищеним рівнем βамілоїду та/або олігомерів β-амілоїду та/або β-амілоїдних бляшок та інших відкладень, або хвороби Альцгеймера. В окремому втіленні даного винаходу запропоновано застосування сполуки формули I, розкритої в даному описі, для виготовлення лікарського засобу для терапевтичного та/або профілактичного лікування хвороби Альцгеймера. В окремому втіленні даного винаходу запропоновано застосування сполуки формули I, розкритої в даному описі, для виготовлення лікарського засобу для терапевтичного та/або профілактичного лікування аміотрофічного бічного склерозу (ALS), артеріального тромбозу, аутоімунних/запальних захворювань, раку, наприклад раку молочної залози, серцево-судинних захворювань, таких як інфаркт міокарда і інсульт, дерматоміозиту, синдрому Дауна, захворювань шлунково-кишкового тракту, мультиморфної гліобластоми, базедової хвороби, хвороби Гентінгтона, міозиту з включеними тільцями (IBM), запальних реакцій, саркоми Капоши, хвороби Костманна, еритематозного вовчаку, міофасциту макрофагового, ювенільного ідіопатичного артриту, гранулематозного артриту, злоякісної меланоми, множинної мієломи, ревматоїдного артриту, синдрому Шегрена, спіноцеребелярної атаксії 1, спіноцеребелярної атаксії 7, хвороби Уіппла або хвороби Вільсона. В окремому втіленні даного винаходу запропоновано застосування сполуки формули I, розкритої в даному описі, для виготовлення лікарського засобу для терапевтичного та/або профілактичного лікування хвороби Альцгеймера. В окремому втіленні даного винаходу запропоновано сполуку формули I, розкриту в даному описі, для застосування в інгібуванні активності BACE1. В окремому втіленні даного винаходу запропоновано сполуку формули I, розкриту в даному описі, для застосування в терапевтичному та/або профілактичному лікуванні захворювань і розладів, що характеризуються підвищеним рівнем β-амілоїду та/або олігомерів β-амілоїду та/або β-амілоїдних бляшок та інших відкладень, або хвороби Альцгеймера. В окремому втіленні даного винаходу запропоновано сполуку формули I, розкриту в даному описі, для застосування в терапевтичному та/або профілактичному лікуванні хвороби Альцгеймера. В окремому втіленні даного винаходу запропоновано сполуку формули I, розкриту в даному описі, для застосування в терапевтичному та/або профілактичному лікуванні аміотрофічного бічного склерозу (ALS), артеріального тромбозу, аутоімунних/запальних захворювань, раку, 13 UA 113538 C2 5 10 15 20 25 30 наприклад раку молочної залози, серцево-судинних захворювань, таких як інфаркт міокарда та інсульт, дерматоміозиту, синдрому Дауна, захворювань шлунково-кишкового тракту, мультиморфної гліобластоми, базедової хвороби, хвороби Гентінгтона, міозиту з включеними тільцями (IBM), запальних реакцій, саркоми Капоши, хвороби Костманна, еритематозного вовчаку, міофасциту макрофагового, ювенільного ідіопатичного артриту, гранулематозного артриту, злоякісної меланоми, множинної мієломи, ревматоїдного артриту, синдрому Шегрена, спіноцеребелярної атаксії 1, спіноцеребелярної атаксії 7, хвороби Уіппла або хвороби Вільсона. В окремому втіленні даного винаходу запропоновано спосіб для застосування в інгібуванні активності BACE1, зокрема для терапевтичного та/або профілактичного лікування захворювань і розладів, що характеризуються підвищеним рівнем β-амілоїду та/або олігомерів β-амілоїду та/або β-амілоїдних бляшок та інших відкладень, або хвороби Альцгеймера, що включає введення сполуки формули I, розкритої в даному описі, людині або тварині. В окремому втіленні даного винаходу запропоновано спосіб для застосування в терапевтичному та/або профілактичному лікуванні хвороби Альцгеймера, що включає введення сполуки формули I, розкритої в даному описі, людині або тварині. В окремому втіленні даного винаходу запропоновано спосіб для застосування в терапевтичному та/або профілактичному лікуванні аміотрофічного бічного склерозу (ALS), артеріального тромбозу, аутоімунних/запальних захворювань, раку, наприклад раку молочної залози, серцево-судинних захворювань, таких як інфаркт міокарда та інсульт, дерматоміозиту, синдрому Дауна, захворювань шлунково-кишкового тракту, мультиморфної гліобластоми, базедової хвороби, хвороби Гентінгтона, міозиту з включеними тільцями (IBM), запальних реакцій, саркоми Капоши, хвороби Костманна, еритематозного вовчаку, міофасциту макрофагового, ювенільного ідіопатичного артриту, гранулематозного артриту, злоякісної меланоми, множинної мієломи, ревматоїдного артриту, синдрому Шегрена, спіноцеребелярної атаксії 1, спіноцеребелярної атаксії 7, хвороби Уіппла або хвороби Вільсона, що включає введення сполуки формули I, розкритої в даному описі, людині або тварині. Крім того, даний винахід включає всі оптичні ізомери, тобто діастереомери, діастереомерні суміші, рацемічні суміші, всі їх відповідні енантіомери та/або таутомери, а також відповідні сольвати сполук формули I. Фахівцеві в даній області техніки відомо, що сполуки формули I можуть існувати в таутомерних формах HN H N 1 R O 35 40 45 50 4 R O HN 3 R 2 R Ie. Всі таутомерні форми охоплені даним винаходом. Сполуки формули I можуть містити один або більше асиметричних центрів і тому вони можуть існувати у вигляді рацематів, рацемічних сумішей, окремих енантіомерів, діастереомерних сумішей та індивідуальних діастереомеров. Залежно від природи різних замісників в молекулі, можлива наявність додаткових асиметричних центрів. Кожен такий асиметричний центр незалежно даватиме два оптичні ізомери, і мається на увазі, що всі можливі оптичні ізомери і діастереомери у вигляді сумішей, а також у вигляді чистих або частково очищених речовин, охоплені даним винаходом. Мається на увазі, що даний винахід охоплює всі подібні ізомерні форми таких споук. Незалежні синтези цих діастереомерів або їх хроматографічне розділення можна здійснити способами, відомими в даній області техніки, шляхом відповідної модифікації методології, розкритої в даному описі. Їх абсолютну стереохімію можна визначити за допомогою рентгеноструктурного аналізу кристалічних продуктів або кристалічних проміжних речовин, які по необхідності дериватизують за допомогою реагенту, що містить асиметричний центр з відомою абсолютною конфігурацією. За бажанням, рацемічні суміші сполук можна розділяти для того, щоб виділити індивідуальні енантіомери. Розділення можна проводити способами, які добре відомі в даній області техніки, такими як поєднання рацемічної суміші сполук з енантіомерно чистою сполукою, що приводить до суміші діастереомерів, з подальшим розділенням індивідуальних діастереомеров стандартними способами, такими як дробова кристалізація або хроматографія. Стереоізомери сполук формули I є сполуками формули Ia або сполуки формули Ib, зокрема, сполуками формули Ia, в яких залишки мають значення, розкриті в будь-якому з втілень. 14 UA 113538 C2 H2N H N 1 R 4 R O N H N 1 3 R O H2N 2 R R O 10 15 20 25 30 35 40 45 50 N 3 R 2 R Ia 5 4 R O Ib У тих втіленнях, де запропоновані оптично чисті енантіомери, термін "оптично чистий енантіомер" означає, що дана сполука містить > 90 мас.% бажаного ізомеру, зокрема > 95 мас.% бажаного ізомеру або, в окремому випадку > 99 мас.% бажаного ізомеру, при цьому зазначена маса виражена у відсотках від загальної маси ізомеру(ів) даної сполуки. Хірально чисті або хірально збагачені сполуки можна одержати хірально селективним синтезом або розділенням енантіомерів. Розділення енантіомерів можна проводити на стадії кінцевого продукту або, як варіант, на стадії відповідного проміжного продукту. Сполуки формули I можна одержати відповідно до наступних схем. Початкові речовини є у продажу або їх можна одержати відомими способами. Будь-які раніше певні залишки і змінні зберігають своє розкрите раніше значення, якщо не зазначено інше. Алкіл-2-хлор-2-(гідроксиіміно)ацетат вводять в реакцію з олефіном у присутності основи, такої як алкілумін, зокрема TEA (триетиламін), або карбонат лужного металу, зокрема NaHCO3 (гідрокарбонат натрію), в розчиннику, такому як хлоровані алкани, зокрема CH2Cl2 (дихлорметан), або ефір, зокрема AcOEt (етилацетат), з одержанням ефіру II. Ефір II відновлюють гідридом, зокрема NaBH4 (борогідридом натрію), в розчиннику, такому як спирт, зокрема EtOH (етанол), з одержанням спирту III. Нітросполуку вводять в реакцію з олефіном у присутності активуючого реагенту, такого як, наприклад, ізоціанат, зокрема фенілізоціанат, і каталітичної кількості основи, зокрема алкілуміну, в окремому випадку TEA, в розчиннику, такому як бензол або толуол, зокрема бензол, або алкіловий ефір, зокрема, діетиловий ефір, з одержанням дигідроізоксазолу IV, де 3 R позначає алкіл, зокрема метил. 3 Дигідроізоксазоли IV, де R позначає галогеналкіл, зокрема фторметил, можна одержати із спиртів III реакцією з фторуючим агентом, таким як, наприклад, трифторид морфоліносери, в інертному розчиннику, такому як галогеналкани, переважно дихлорметан, при температурі між 78 °C і кімнатною. Арилювання дигідроізоксазолу IV арилбромідом V з одержанням ізоксазолідину VI здійснюють за допомогою реакції арилгалогеніду, зокрема арилброміду, з алкіллітієвим реагентом, зокрема з n-BuLi, з одержанням ариллітієвих сполук, які можна вводити в реакцію з дигідроізоксазолом IV у присутності основи Люіса, переважно ефірату трифтористого бору, в суміші розчинників, що складається з ефіру, зокрема THF (тетрагідрофуран), і толуолу, при температурі від -100 °C до -20 °C, зокрема при -78 °C. Розділення рацемічного ізоксазолідину VI з одержанням хірального ізоксазолідину VII можна здійснити за допомогою хіральної високоефективної рідинної хроматографії (ВЕРХ) з використанням колонки Chiralpack AD або Reprosil NR, в суміші н-гептану і етанолу або ізопропанолу в якості елюенту. Гідрогеноліз хірального ізоксазолідину VII до аміноспирту VIII краще всього здійснювати шляхом гідрогенолізу з перенесенням водню, за допомогою паладієвого каталізатора, зокрема Pd на вугіллі, і джерела водню, наприклад солі мурашиної кислоти, зокрема форміату амонію, в протонному розчиннику, такому як спирт, зокрема, етанол. Оксазин IX можна одержати реакцією аміноспирту VIII бромціаном в розчиннику, такому як спирт, зокрема етанол, при підвищеній температурі. Як варіант, цю реакцію можна проводити в дві послідовні стадії з використанням бромціану і буфера, такого як, наприклад, ацетат натрію, у присутності розчинника, такого як, наприклад, CH3CN, з подальшою циклізацією проміжного продукту у присутності мінеральної кислоти, зокрема хлороводневої кислоти, в розчиннику, такому як ефір, зокрема 1,4-діоксан. Нітрацію оксазину IX з одержанням нітрооксазину X здійснюють стандартним способом з використанням чистої сірчаної кислоти і димлячої азотної кислоти без розчинника. Відновлення нітрогрупи в проміжному продукті X з одержанням аніліну XI можна здійснити гідруванням за допомогою каталізатора, такого як Pd на вугіллі, в протонних розчинниках, таких 15 UA 113538 C2 5 як спирти, зокрема етанол або метанол. Селективну амідну конденсацію аніліну XI і карбонової кислоти XII з одержанням аміду I можна здійснити за допомогою 4-(4,6-диметокси[1.3.5]триазин-2-іл)-4-метилморфолінію хлориду (DMTMM) гідрату як конденсуючого агента в розчиннику, такому як спирт, зокрема метанол. Схема 1: Синтез сполук формули Ia-1 CF3 OH N CF3 O CF3 O N N Cl EtOOC EtOOC HO III II Br CF3 O NO2 HN F N 3 R V F 3 R IV (R3 = Me, CH2F) H2N VI CF3 HO CF3 O CF3 O CF3 H2N N CF3 O HN 3 3 3 R R R F F F IX VIII H2N CF3 O H2N N 3 R X 20 1 R OH H2N O 3 R H2N F 15 CF3 O N O2N 10 VII CF3 O N XII 1 R H N 3 R F F O XI Ia-1 Сполуки формули Ia‘-1 можна одержати відповідно до наступної Схеми 2, як зазначено нижче. Сульфініліміни загальної формули XIV можна одержати за аналогією із способом, описаним в літературі (T.p. Tang & J.a. Ellman, J. Org. Chem. 1999, 64, 12), шляхом конденсації арилкетону XIII і сульфінаміду, наприклад алкілсульфінаміду, в окремому випадку (R)-третметилсульфінаміду або (S)-трет-метилсульфінаміду, у присутності кислоти Люіса, такої як, наприклад, алкоксид титану(IV), в окремому випадку етоксид титану(IV), в розчиннику, такому як ефір, наприклад діетиловий ефір або, в окремому випадку, тетрагідрофуран. Перетворення сульфініліміну XIV на сульфінамідний ефір XV протікає стереоселективно за рахунок хірально направляючої групи, як описано в літературі (Tang & Ellman). Сульфінілімін XIV можна вводити в реакцію Реформатського з енолятом цинку, що генерується з алкілацетату, заміщеного галогеном, наприклад з етилбромацетату, і активованому цинковому пилу, при температурі від кімнатної до підвищеної, зокрема від 23 до 60 °C, в розчиннику, такому як ефір, наприклад діетиловий ефір або, в окремому випадку, тетрагідрофуран, у присутності солі міді(I), переважно хлориду міді(I). Альдегіди формули XVI можна одержати відновленням етилового ефіру формули XV 16 UA 113538 C2 5 10 15 20 25 гідридом лужного металу, наприклад алюмогідридом літію, у присутності діетиламіну або дигідробіс(2-метоксиетокси)алюмінату натрію (Red-Al), переважно за допомогою гідриду діізометилалюмінію (DIBAH), в інертному розчиннику, такому як ефір, наприклад діетиловий ефір або, в окремому випадку, тетрагідрофуран, або в хлорованому розчиннику, такому як дихлорметан, при температурі між -78 °C і кімнатною. Спирти формули XVII можна одержати реакцією альдегідів формули XVI з трифторметилуючим агентом, переважно з трифторметилтриметилсиланом (реагент РуппертаПракаша), у присутності фториду тетраметиламонію в розчиннику, такому як ефір, наприклад діетиловий ефір або, в окремому випадку, тетрагідрофуран, при температурі між -10 °C і кімнатною. Гідроліз хірально направляючої групи в сульфінамідоспирті формули XVII з одержанням аміноспирту формули XVIII можна здійснити за допомогою мінеральної кислоти, наприклад сірчаної кислоти або, зокрема, хлороводневої кислоти, в розчиннику, такому як ефір, наприклад діетиловий ефір, тетрагідрофуран або, в окремому випадку, 1,4-діоксан. Амінооксазин формули XIX можна одержати реакцією аміноспирту формули XVIII з бромціаном в розчиннику, такому як спирт, зокрема етанол. Нітропохідну формули XX можна одержати нітрацією оксазину XIX стандартним способом за допомогою чистої сірчаної кислоти і димлячої азотної кислоти, без розчинника. Відновлення нітрогрупи в сполуці формули XX з одержанням анілінів формули XXI можна здійснити гідруванням за допомогою каталізатора, такого як паладій на вугіллі, в протонних розчинниках, таких як спирти, зокрема етанол або метанол. Селективну реакцію анілінів формули XXI з карбоновою кислотою формули XII з одержанням амідів формули Ia’-1 можна здійснити за допомогою 4-(4,6диметокси[1.3.5]триазин-2-іл)-4-метилморфолінію хлориду гідрату (DMTMM) як конденсуючий агент в розчиннику, такому як метанол, при температурі між 0 °C і кімнатною. Як варіант, 2,4,6® трипропіл-1,3,5,2,4,6-триоксатрифосфоринан-2,4,6-триоксид (T3P ) можна використовувати як конденсуючий агент в інертному розчиннику, такому як, наприклад, етилацетат, при температурі між 0 °C і кімнатною. 3‘ Схема 2: Синтез сполук формули Ia’-1 (де R = CH3, CH2F, CHF2) O N O tBu S O S tBu COOEt tBu F CF3 O N H2N O2N 3' R CF3 N H N 3' R XVII CF3 HO CF3 O H2N CF3 S F XVI O H2N tBu F XV XIV H2N R R F XIII 3' 3' R F CHO HN HN 3' 3' R O HO O S H2N N 3' 3' 3' R R R F F F F XXI XX XIX XVIII 1 R OH O H N 1 O 30 CF3 O H2N R XII N 3' R F Ia'-1 Відповідні фармацевтично прийнятні солі, утворені кислотами, можна одержати стандартними способами, відомими фахівцеві в даній області техніки, наприклад шляхом розчинення сполуки формули I у відповідному розчиннику, такому як, наприклад, діоксан або 17 UA 113538 C2 5 10 15 20 25 30 35 тетрагідрофуран, і додавання належної кількості відповідної кислоти. Такі продукти зазвичай можна виділити за допомогою фільтрації або хроматографії. Переведення сполуки формули I у фармацевтично прийнятну сіль, утворену основою, можна здійснити шляхом обробки зазначеної сполуки такою основою. Один з можливих способів одержання такої солі є, наприклад, додаванням 1/n еквівалентів основної солі, таких як, наприклад, M(OH)n, де M = катіон металу або амонію, а n = число гідроксидних аніонів, до розчину сполуки у відповідному розчиннику (наприклад, в етанолі, суміші етанол-вода, суміші тетрагідрофуран-вода), і видалення розчинника шляхом випаровування або ліофілізації. Зокрема, такі солі можуть бути гідрохлоридом, форміатом і трифторацетатом; у окремому випадку - гідрохлоридом. Якщо одержання сполук не описане в прикладах, то такі сполуку формули I, так само як і всі проміжні продукти, можна одержати аналогічними способами або способами, представленими в даному описі. Початкові речовини є у продажу, відомі в даній області техніки або можуть бути одержані способами, відомими в даній області техніки, або аналогічними їм. Слід розуміти, що сполуки загальної формули I за даним винаходом можна дериватизувати за функціональни\мих групами з одержанням похідних, які здатні перетворюватися назад в початкову сполуку in vivo. Фармакологічні тести Сполуки формули I та їх фармацевтично прийнятні солі мають цінні фармакологічні властивості. Виявили, що сполуки за даним винаходом пов'язані з інгібуванням активності BACE1. Ці сполуки були досліджені відповідно нижче описаного тесту. Клітинний аналіз зниження концентрації β-амілоїду Можна використовувати набір реагентів для аналізу Abeta 40 AlphaLISA. Клітини HEK293 APP висівалі на 96-лункових планшетах Microtiter в середовищі для культивування (середовище Iscove, з додаванням 10% (об./об.) фетальної сироватки корови, пеніцилін/стрептоміцин) приблизно до 80% злиття і вносили сполуки в 3-кратній концентрації в 1/3 об'єму середовища для культивування (кінцеву концентрацію DMSO витримували при 1% об./об.). Через 18-20 г інкубації при 37 °C і 5% CO2 в інкубаторі із зволоженням культуральні супернатанти збирали для визначення концентрацій Aβ 40 за допомогою набору реагентів Perkin-Elmer Human Amyloid beta 1-40 (високіої специфічності) (кат.№ AL275C). На планшетах Perkin-Elmer White Optiplate-384 (кат.№ 6007290) 2 мкл культуральних супернатантів об'єднували з 2 мкл 10-кратної суміші гранул AlphaLISA Anti-hAβAcceptor + Biotinylated Antibody Anti-Aβ 1-40 (анти-hAβ-акцептор + біотинільовані антитіла анти-Aβ50, мкг/мл / 5нМ). Через 1 г інкубації при кімнатній температурі додавали 16 мкл 1,25-кратного препарату Стрептавідин(SA)-донорних гранул (25 мкг/мл) та інкубували протягом 30 хв в темноті. Після цього проводили прочитування емісії при 615 нм на рідері EnVision-Alpha. Рівень Aβ 40 в культуральних супернатантах розраховували як процентну частку від максимального сигналу (клітини, оброблені 1% DMSO без інгібітора). Величини IC50 розраховували в програмному середовищі Excel XLfit. Приклад клітинна активність BACE1 Aβ40, IC50 [нМ] Структура H2N CF3 O N 1 NC H N N 2 F O H2N CF3 O N 2 Cl N H N O 5 F 18 UA 113538 C2 Приклад клітинна активність BACE1 Aβ40, IC50 [нМ] Структура H2N CF3 O N 3 H N N NC 13 F F O H2N CF3 O N 4 H N N Cl 22 F F O H2N CF3 O N 5 N O H N 5 N F O H2N F 6 N F H N N O 24 N F O H2 N F 7 CF3 O F F CF3 O N N O H N 15 N F O H2N CF3 O N 8 NC H N N 230 F O H2N CF3 O N 9 Cl N H N O 710 F 19 UA 113538 C2 Приклад клітинна активність BACE1 Aβ40, IC50 [нМ] Структура H2N CF3 O N 10 H N N Cl 6 F O Cl H2 N CF3 O F N 11 H N N O 4 F O H2N CF3 O N 12 H N N NC 3 F O H2N CF3 O N 13 H N N NC 13 F O Cl H2 N CF3 O N 14 H N N O 2 F O F 15 H2 N F O N N H N 1 F O F 16 H2 N F F O CF3 O CF3 O N N H N O 1 F 20 UA 113538 C2 Приклад H2 N CF3 O N F H N N 17 F 2 F O H2 N F 18 клітинна активність BACE1 Aβ40, IC50 [нМ] Структура F F CF3 O N H N N O 8 F O H2 N CF3 O N F H N N 19 6 N F O H2 N CF3 O N F H N N 20 F 5 N F O H2 N CF3 O N H N N 21 59 N F O H2N CF3 O N 22 N O H N 0,2 N F O H2 N F 23 CF3 O N N O H N N O 1 F 21 UA 113538 C2 Приклад клітинна активність BACE1 Aβ40, IC50 [нМ] Структура F 24 H2 N F CF3 O N H N N O 3 N F O H2 N F CF3 O N H N N 25 O 0,8 F O H2N F F 26 CF3 O N H N N N 1 F O Cl H2N CF3 O N 27 NC H N N F 2 F O H2N CF3 O N 28 NC H N N Cl F 11 F O H2N CF3 O N 29 Cl N Cl H N F 15 F O H2 N CF3 O N 30 O N H N O F F 22 11 UA 113538 C2 Приклад H2 N F F 31 N H N N O 32 H2 N CF3 O N H N N O 7 F F O H2 N CF3 O N F H N N 33 F F H2 N F F F 10 F O CF3 O N H N N O F F 71 F O H2 N 35 7 F F F F F CF3 O O 34 клітинна активність BACE1 Aβ40, IC50 [нМ] Структура CF3 O N H N N O F 19 F O H2 N CF3 O N 36 N O H N F N 31 F O H2 N CF3 O N F N 37 H N N O F F 23 53 UA 113538 C2 Приклад клітинна активність BACE1 Aβ40, IC50 [нМ] Структура H2N CF3 O N 38 H N N O F N F 39 F O H2 N F CF3 O N H N N O F O H2 N F CF3 O N F H N N O F N H2 N F F F 29 F O 41 0,4 F N 40 0,6 CF3 O N H N N O F N 17 F O H2 N CF3 O N H N N 42 N F O H2 N F 43 64 F CF3 O N N O H N F N 3 F O H2N CF3 O N N 44 H N N O F F 24 UA 113538 C2 Приклад клітинна активність BACE1 Aβ40, IC50 [нМ] Структура H2 N N F H N N 45 F F N H2N F 46 39 F O F CF3 O CF3 O N H N N N F F O Cl H2 N F 3 CF3 O N N 47 O H N 1 F F O H2N CF3 O N 48 NC N H N F 520 FF O H2N CF3 O N 49 NC N H N O F 82 FF Таблиця 1: значення IC50 у вибраних прикладах 5 10 15 Біологічні дані Аналіз P-gp (P-глікопротеїну) Клітинні лінії і везикули, використані для експериментів за транспортом Клітинна лінія LLC-PK1 (ATCC #CL-101) є лінією епітеліальних клітин нирок свині. Лінії клітин, трансфікованих MDR1 (білок множинної лікарської резистентності 1 людини), були надані доктором A. Schinkel (The Netherlands Cancer Institute, Амстердам, Нідерланди). Всі 2 клітинні лінії культивували на проникних вставках (Costar, площею 0,33 см , розмір пір 3,0 мкм, 2 низької щільності) при щільності 4,5·105 клітин/см . Транспортні вимірювання проводили на 4-й день після посіву. Щільність клітинного моношару контролювали за проникністю позаклітинного маркера lucifer yellow (10 мкм). Експерименти, в яких проникність маркера lucifer yellow складала вище 1%/г, були виключені. Експерименти за транспортом in vitro Двонаправлений трансцелюлярний транспорт з використанням клітин LLC-PK1 і L-MDR1 LLC-PK1, екзогенно експресуючих людський MDR1 Метод, використовуваний для експериментів за транспортом, проводили на автоматичній системі транспортування рідин TECAN. Коротко, середовище видаляли зі всіх відсіків, і 25 UA 113538 C2 5 10 15 20 25 30 35 40 45 50 55 середовище в приймальному відсіку замінювали культуральним середовищем. Трансцелюлярні транспортні вимірювання ініціювали додаванням субстрата разом з позаклітинним маркером lucifer yellow в подаючий відсік. Інгібітори додавали в обидва відсіки (1 мкм елакридар). Експерименти за транспортом здійснювали в обох напрямках: базолатерально-апікальному і апікально-базолатеральному, по 3 лунки на кожен напрям. Планшети інкубували при 37 °C і 5% CO2 в інкубаторі Liconic. Проби відбирали з подаючого і протилежного (приймального) відсіків через 2 години інкубації. Концентрації субстрата в обох відсіках визначали шляхом підрахунку сцинтиляцій (дигоксин) або за допомогою LC-MS/MS. Позаклітинний маркер (lucifer yellow) визначали кількісно на спектрофотометрі для прочитування планшетів Spectrafluor Plus при 430/535 нм (довжина хвилі збудження/випускання). У кожному експерименті використовували три різні вставки для кожної умови і розраховували середнє. Аналіз даних Двонаправлений трансцелюлярний транспорт з використанням клітин LLC-PK1 і L-MDR1 У разі трансцелюларного транспорту використовували наступне рівняння для оцінки даних: 1 dQ Papp * A * C0 dt де Papp, A, C0 і dQ/d позначають позірну проникність, площу поверхні фільтру, початкову концентрацію і кількість, перенесену за період часу, відповідно. Величини Papp розраховували на єдиний момент часу (2 г). PappBA Транспортні співвідношення ефлюкса (ER) розраховували таким чином: ER , Papp AB де PappBA позначає величину проникності в базолатерально-апікальному напрямку, а PappAB - величину проникності в апікально-базолатеральному напрямку. Papp не були скоректовані за потоком позаклітинного маркера lucifer yellow, який використовували для оцінки якості клітинних моношарів. Визначення кон'югатів глутатіону (GSH) Умови аналізу для визначення кон'югатів глутатіону відповідають способу, описаному в літературі (C.m.dieckhaus et al., Chem.Res.Toxicol. 2005, 18, 630-63). Вимірювання сили струму hERG Вимірювання сили струму hERG проводили в автоматизованій системі петч-кламп способом, описаним в літературі (R.e.martin et al., Bioorg.Med.Chem.Lett 19 (2009), 6106-6113). Експерименти in vivo. Інгібування Aβ40 в головному мозку мишей дикого типу. Самкам мишей C57Bl/6J вводили різні дози сполук, по 3-4 тварини на одну групу введення. Тестовану сполуку розчиняли в 5% EtOH, 10% солютол, і вводили через рот в дозі 10 мл/кг. Через 4 г тварин забивали і збирали мозок і плазму крові. Мозок розділяли на дві половини і негайно заморожували на сухому льоді. Мозок використовували для вимірювання Aβ40, а плазму використовували для визначення рівня дії сполуку. Використовували відомий з літератури спосіб визначення Aβ40, в лізатах мозку (Lanz, T.a.; Schachter, J.b. Demonstration of common artifact in immunosorbent assays of brain extracts: Development of solid-phase extraction protocol to enable measurement of amyloid-beta from wild-type rodent brain. J. Neurosci. Methods 2006, 157, 71-81). Мозкову тканину гомогенізували в 2% DEA буфері за допомогою пристрою Roche Magnalyser (20 сек, 4000 об/хв) і після цього центрифугували протягом 1 г при 100 000 g. Концентрацію DEA знижували до 0,2% в 50 мм NaCl і одну другу лізату DEA пропускали через планшет для екстракції Oasis Solid Phase (Waters; кат.№ 186000679), який було активовано за допомогою MeOH та урівноважено в dH2O (по 1 мл кожного). Після промивок в 10% і 30% MeOH (по 1 мл кожного) елюювали Аβ-пептиди в 0,8 мл 2% NH4OH в 90% MeOH. Елюат висушували в струмі азоту і висушений зразок перерозчиняли в 30 мкл буфера для аналізу AlphaLISA. Aβ40 визначали за допомогою аналізу AlphaLISA (Perkin Elmer). На білому 96-лунковому мікропланшеті з половинним об'ємом лунок (Perkin Elmer кат. № 6005561), змішували 20 мкл відновленого зразка з 5 мкл біотинильованого BAP-24 (специфічного до C-кінця Aβ40 (Brockhaus, M.; Grunberg, J.; Rohrig, S.; Loetscher, H.; Wittenburg, N.; Baumeister, R.; Jacobsen, H.; Haass, C. Caspase-mediated cleavage is not required for the activity of presenilins in amyloidogenesis і NOTCH signaling. Neuroreport 1998, 9, 1481-6), концентрація початкового розчину = 4,4 мг/мл, f.c. 5,5 мкг/мл) і 5 мкл гранул з акцептором 252Q6 (антитіла до 252Q6, Invitrogen AMB0062), заздалегідь кон'югованих з акцепторними гранулами AlphaLISA (Perkin Elmer кат.№ 6772002); кінцеве розведення 1:500). Цей мікс інкубували протягом 1 г при КТ в темноті. Потім вносили 20 мкл покритих стрептавідином донорних гранул (Streptavin-coated Donor Beads, Perkin Elmer кат.№ 6760002, кінцеве розведення 1:125) і цей підсумковий мікс інкубували в темноті ще протягом 30 хв при КТ, після чого вимірювали флюоресценцію по відн. 26 UA 113538 C2 5 10 15 20 25 30 35 40 45 50 55 од. (RFU) на рідері AlphaScreen Reader(Perkin Elmer Envision 2104). Кінетичний аналіз катепсину D і катепсину E з флюоресціюючим субстратом Загальний принцип аналізу Описані нижче методи флюоресцентного аналізу MR121 засновані на наступному явищі: MR121 утворює нефлюоресціюючий в основному стані комплекс з триптофаном. У розчині його формування відбувається при мілімолярних концентраціях триптофану. Цей механізм можна застосовувати для розробки загального біохімічного аналізу для протеаз. Пептидний субстрат мітять на N-кінці триптофаном, а на C-кінці - флюорофором MR121 (для катепсину D використовували 10-амінокислотний пептид WTSVLMAAPC-MR121; для катепсину E використовували MR121-CKLVFFAEDW). У відсутність протеазної активності ці субстрати залишаються інтактними, і флюоресценція MR121 знижується під дією високих локальних концентрацій Trp. Якщо субстрати розщеплюються під дією ферментів, то флюоресценція MR121 відновлюється. Процедура аналізу Кінетичний аналіз катепсину D і катепсину E з флюоресціюючим субстратом проводили при кімнатній температурі на 384-лункових мікропланшетах (чорні з прозорим плоским дном, планшети з незв'язуючою поверхнею виробництва Corning) в кінцевому об'ємі 51 мкл. Тестові сполуки послідовно розводили в DMSO (15 концентрацій, крок розведення 1/3), після чого змішували протягом 10 хв 1 мкл розведених сполук з 40 мкл катепсину D (з людської печінки, Calbiochem), розведеного в аналітичному буфері (100 мм ацетат натрію; 0,05% БСА; pH 5,5; кінцева концентрація: 200 нМ) або з 40 мкл рекомбінантним людським катепсином E (R&D Systems), розведенням в аналітичному буфері (100 мм ацетат натрію, 0,05% БСА, pH 4,5; кінцева концентрація: 0,01 нМ). Після внесення 10 мкл субстрата катепсину D WTSVLMAAPCMR121, розведеного в аналітичному буфері для катепсину D (кінцева концентрація: 300 нМ) або 10 мкл субстрата катепсину E MR121-CKLVFFAEDW, розведеного в аналітичному буфері для катепсину E (кінцева концентрація: 300 нМ), планшети інтенсивно струшували протягом 2 хв. Ензиматичну реакцію відстежували на спектрофотометрі для прочитування планшетів у видимій області (Perkin Elmer) (довжина хвилі збудження: 630 нм; випускання: 695 нм) протягом щонайменше 30 хв в режимі кінетичного вимірювання, детектуючи зростання флюоресценції MR121 в ході реакції. Розраховували нахил лінійної ділянки кінетичною кривою і визначали величини IC50 тестових сполук за допомогою 4-параметричного рівняння для побудови кривої. Аналіз інгібування CYP Інгібування цитохромів P450 (CYPs) 2C9, 2D6 і 3A4 оцінювали з використанням мікросом печінки людини і CYP-селективных субстратних метаболічних реакцій. Проводили інкубації в об'ємі 50 мкл, що містить (в кінцевому рахунку) 0,2 мг/мл пулованих мікросом печінки людини, 5 мкм субстрата (диклофенак для CYP2C9 [4’гідроксилази], декстрометорфан для CYP2D6 [Oдеметилази] або мідазолам для CYP3A4 [1’гідроксилази]), 0,25 мкл DMSO, що містить тестований інгібітор і НАДФH-регенеруючу систему. Тестові концентрації інгібітора, що становлять 50; 16,7; 5,6; 1,9; 0,6 і 0,2 мкм, оцінювали в моноплікатах. Заздалегідь нагрівали інкубований матеріал до 37 °C протягом 10 хв, після чого проводили ініціацію шляхом додавання НАДФH-регенеруючої системи. Інкубаційне середовище гасили через 5 хв (20 хв для декстрометорфану) додаванням 50 мкл холодного ацетонітирилу, що містить 20 нг/мл 4-OHдиклофенаку-13C6, 20 нг/мл декстрорфану-D3 і 20 нг/мл 1-OH-мідазоламу-D4. Інкубаційний матеріал після погашення реакції витримували при -20 °C протягом щонайменше 1 г, після чого центрифугували (20 000 x g, 20 хв). Супернатанти відокремлювали і розбавляли водою 1:1, після чого проводили аналіз із застосуванням інжектора проби RapidFIre і мас-спектрометра API4000. Площі піку для субстрата, метаболіту і стабільно-міченого стандарту метаболіту визначали за допомогою MS/MS. Відносини площин піків між метаболітом, що генерується в ході ензиматичної реакції, і внутрішнім стандартом використовували для подальших обчислень. Процентну частку активності контролю (DMSO) розраховували для кожного інкубованого матеріалу і оцінювали величини IC50 за нелінійною регресією. Сульфафеназол, хінідин або кетоконазол тестували в кожному експерименті інгібування CYP2C9, CYP2D6 або CYP3A4, відповідно, для контролю чутливості і відтворюваності аналізу. (Validated assays for human cytochrome P450 activities, R.l.walsky і R.s.obach, Drug Metabolism and disposition 32: 647-660, 2004; S.Fowler and H.Zhang, The AAPS Journal, Vol.10, No. 2, 410-424, 2008.) Результати 27 UA 113538 C2 1) Приклад P-gp люд. 1 2 3 11 22 35 36 46 1,90 1,82 1,61 2,30 2,63 1,50 0,71 1,23 2) GSH люд. NF NF NF NF NF NF NF NF hERG 75 84 39 26 26 7 8 3) Ефект in 4) vivo Катепсин E IC50 [мкМ] Катепсин D IC50 [мкМ] 95 93 88 87 83 74 88 61 >200 >200 >200 >200 >200 >200 >200 >200 >200 >200 >200 >200 178,69 >200 >200 >200 CYP IC50 [мкМ] 3A4 2D6 2C9 >50 28 >50 >50 3,9 >50 >50 >50 >50 >50 1,6 >50 >50 13,0 33,0 >50 5,2 33 >50 16,0 >50 >50 24,0 >50 Таблиця 2: Біологічні дані за вибраними прикладами 5 10 15 20 25 30 35 40 45 1) Співвідношення ефлюкса 2) NF = in vitro відсутність утворення адукта, по відношенню до контролю 3) Інгібування @ 10 мкМ 4) Процентна частка контролю @ 10 мг/кг p.o. Фармацевтичні композиції Сполуки формули I і фармацевтично прийнятні солі можна використовувати як терапевтично активні речовини, наприклад, у формі фармацевтичних препаратів. Такі фармацевтичні препарати можна вводити перорально, наприклад у формі пігулок, пігулок, покритих оболонкою, драже, твердих і м'яких желатинових капсул, розчинів, емульсій або суспензій. Крім того, введення можна здійснювати ректально, наприклад у формі супозиторіїв, або парентерально, наприклад у формі розчинів для ін'єкцій. Сполуки формули I та їх фармацевтично прийнятні солі можна процесувати спільно з фармацевтично інертними неорганічними або органічними носіями для одержання фармацевтичних препаратів. Як такі носії для пігулок, пігулок, покритих оболонкою, драже і твердих желатинових капсул можна використовувати, наприклад, лактозу, кукурудзяний крохмаль або його похідні, тальк, стеаринові кислоти або їх солі і т. п. Відповідними носіями для м'яких желатинових капсул є, наприклад, рослинні масла, віск, жири, напівтверді і рідкі поліоли і т. п. Проте, залежно від природи діючої речовини у разі м'яких желатинових капсул носії, як правило, не потрібні. Відповідними носіями для виготовлення розчинів і сиропів є, наприклад, вода, поліоли, гліцерин, рослинне масло і т. п. Відповідними носіями для супозиторіїв є, наприклад, природні або отведжені масла, віск, жири, напівтверді або рідкі поліоли і т. п. Крім того, такі фармацевтичні препарати можуть містити фармацевтично прийнятні допоміжні речовини, наприклад консерванти, солюбілізатори, стабілізатори, зволожуючі агенти, емульгатори, підсолоджувачі, барвники, ароматизатори, солі для варіювання осмотичного тиску, буфери, маскуючі агенти або антиоксиданти. Вони також можуть містити і інші терапевтично корисні речовини. Об'єктом даного винаходу також є лікарські засоби, що містять сполуку формули I або її фармацевтично прийнятну сіль і терапевтично інертний носій, а також спосіб їх виготовлення, що включає приведення одної або більше сполук формули I та/або їх фармацевтично прийнятних солей і, за бажанням, одної або більше інших терапевтично цінних речовин, в галенову лікарську форму спільно з одним або більше терапевтично інертним носієм. Дозування можна варіювати в широких межах, та його, зрозуміло, слід підбирати відповідно до індивідуальних вимог у кожному конкретному випадку. У разі перорального введення дозування для дорослих може варіюватися приблизно від 0,01 мг 1000 мг на добу сполуки загальної формули I або відповідної кількості її фармацевтично прийнятної солі. Добову дозу можна вводити у вигляді єдиної дози або роздільних доз, і, крім того, верхню межу можна перевищувати, якщо до цього є показання. Нижченаведені приклади є наочним представленням даного винаходу, але не обмежують його, а лише служать його ілюстрацією. Фармацевтичні препарати в цілях зручності містять приблизно 1-500 мг, зокрема, 1-100 мг сполуки формули I. Приклади композицій за винаходом представлені нижче. Приклад A Пігулки наступного складу виготовляють стандартним способом: 28
ДивитисяДодаткова інформація
Назва патенту англійськоюFluoromethyl-5,6-dihydro-4h-[1,3]oxazines
Автори англійськоюHilpert, Hans, Humm, Roland, Woltering, Thomas
Автори російськоюХильперт Ханс, Хумм Роланд, Волтэринг Томас
МПК / Мітки
МПК: A61K 31/5355, C07D 403/12, C07D 401/12, C07D 413/12, A61K 31/535
Мітки: фторметил-5,6-дигідро-4н-[1,3]оксазини
Код посилання
<a href="https://ua.patents.su/52-113538-ftormetil-56-digidro-4n-13oksazini.html" target="_blank" rel="follow" title="База патентів України">Фторметил-5,6-дигідро-4н-[1,3]оксазини</a>
Попередній патент: Водорозчинна гранульована препаративна форма 2,4-д солі та спосіб її отримання
Наступний патент: Спосіб одержання фармацевтичної композиції на основі модафінілу, одержувана фармацевтична композиція та її застосування
Випадковий патент: Спосіб одержання похідних тієно (3',4': 4,5) імідазо (2,1- b) тіазолу
























































