Спіро-[1,3]-оксазини та спіро-[1,4]-оксазепіни як інгібітори bace1 та (або) bace2
Номер патенту: 111847
Опубліковано: 24.06.2016
Автори: Востл Вольфганг, Пінар Еммануель, Наркізан Робер
Формула / Реферат
1. Сполука формули І
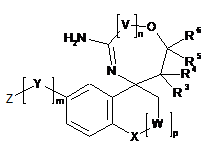 , I
, I
де
V означає CH2-;
W означає -CR2aR2b-;
X означає -CR1aR1b-, -O-, -S- або -SO2-;
Y - NH-CO-;
Z вибраний з групи, що складається з
і) 5-6-членного гетероарилу, що містить 1-2 гетероатоми N, заміщеного 1-2 замісниками, незалежно вибраними з R8,
іі) фенілу, заміщеного 1-2 замісниками, незалежно вибраними з R8;
R1a вибраний з групи, що складається з
і) водню,
іі) галогену, і
ііі) С1-6-алкілу;
R1b вибраний з групи, що складається з
і) водню,
іі) галогену, і
ііі) С1-6-алкілу;
R2a вибраний з групи, що складається з
і) водню, і
іі) С1-6-алкілу;
R2b вибраний з групи, що складається з
і) водню,
іі) фенілу, і
ііі) С1-6-алкілу;
або R2a та R2b разом з атомом вуглецю, до якого вони приєднані, утворюють 6-членний гетероцикліл, що містить 1 гетероатом О;
R3 означає галоген,
R4 означає галоген,
R5 означає водень,
R6 означає водень,
R8 вибраний з групи, що складається з
і) ціано,
іі) галогену,
ііі) галоген-С1-6-алкілу,
iv) С1-6-алкокси,
n означає 0 або 1;
m означає 0 або 1;
р означає 0 або 1;
або її фармацевтично прийнятні солі.
2. Сполука за п. 1, де
R2a та R2b разом з атомом вуглецю, до якого вони приєднані, утворюють тетрагідропіраніл.
3. Сполука за будь-яким з пп. 1-2, де n означає 0.
4. Сполука за будь-яким з пп. 1-3, де X означає -CR1aR1b-, і R1a та R1b обидва є воднем.
5. Сполука за будь-яким з пп. 1-4, де р означає 0.
6. Сполука за будь-яким з пп. 1-3, де X означає -О-.
7. Сполука за будь-яким з пп. 1-2 та 6, де р означає 1, W означає -CR2aR2b-, i R2a тa R2b обидва є воднем.
8. Сполука за будь-яким з пп. 1-7, де R3 означає F.
9. Сполука за будь-яким з пп. 1-8, де R4 означає F.
10. Сполука за будь-яким з пп. 1-9, де m означає 0.
11. Сполука за будь-яким з пп. 1-9, де m означає 1.
12. Сполука за будь-яким з пп. 1-11, де Z означає 5-6-членний гетероарил, що містить 1-2 гетероатоми N, заміщений галогеном або ціано.
13. Сполука за будь-яким з пп. 1-12, вибрана з групи, що складається з:
(R)-7-(5-хлорпіридин-3-іл)-5',5'-дифтор-3,4,5',6'-тетрагідро-2Н-спіро[нафталін-1,4'-[1,3]оксазин]-2'-аміну,
(2'R,4R)-6'-(5-xлopпipидин-3-iл)-5,5-дифтop-5,5",6,6"-тeтpaгiдpo-4"H-диcпipo[1,3-оксазин-4,4'-хромен-2',3"-піран]-2-аміну форміату,
(2RS,4R)-5',5'-дифтop-2-фeнiл-6-(пipимiдин-5-iл)-5',6'-дигiдpocпipo[xpoмaн-4,4'-[1,3]оксазин]-2'-аміну,
(2RS,4R)-6-(3,5-диxлopфeнiл)-5',5'-дифтop-2-фeнiл-5',6'-дигiдpocпipo[xpoмaн-4,4'-[1,3]оксазин]-2'-аміну,
(2RS,4R)-6-(3,5-диxлopфeнiл)-6',6'-дифтop-2-фeнiл-6',7'-дигiдpo-2'H-cпipo[xpoмaн-4,5'-[1,4]оксазепін]-3'-аміну,
(2RS,4R)-6-(5-xлopпipидин-3-iл)-5',5'-дифтop-2-фeнiл-5',6'-дигiдpocпipo[xpoмaн-4,4'-[1,3]оксазин]-2'-аміну,
(2RS,4R)-6-(5-xлopпipидин-3-iл)-6',6'-дифтop-2-фeнiл-6',7'-дигiдpo-2'H-cпіpo[xpoмaн-4,5'-[1,4]оксазепін]-3'-аміну,
(2RS,4R)-6',6'-дифтop-2-фeнiл-6-(пipимiдин-5-iл)-6',7'-дигiдpo-2'H-cпipo[xpoмaн-4,5'-[1,4]оксазепін]-3'-аміну,
(2'S,4R)-6'-(5-хлорпіридин-3-іл)-5,5-дифтор-5,5',6,6'-тетрагідро-4'Н-диспіро[1,3-оксазин-4,4'-хромен-2',3"-піран]-2-аміну форміату,
(R)-3-(2'-aмiнo-5',5'-дифтop-2,3,5',6'-тeтpaгiдpocпіpo[iндeн-1,4'-[1,3]oкcaзин]-6-іл)бензонітрилу,
(R)-4,4,5',5'-тeтpaфтop-7-(5-фтopпipидин-3-iл)-3,4,5',6'-тeтpaгiдpo-2H-cпipo[нaфтaлiн-1,4'-[1,3]оксазин]-2'-аміну,
(R)-5-(2'-аміно-4,4,5',5'-тетрафтор-3,4,5',6'-тетрагідро-2Н-спіро[нафталін-1,4'-[1,3]оксазин]-7-іл)нікотинонітрилу,
(R)-5-(2'-аміно-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-6-іл)нікотинонітрилу,
(R)-5-(2'-амiно-5',5'-дифтор-3,4,5',6'-тетрагідро-2Н-спіро[нафталін-1,4'-[1,3]оксазин]-7-іл)нікотинонітрилу,
(R)-5',5'-дифтор-6-(5-метоксипіридин-3-іл)-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-2'-аміну,
(R)-5',5'-дифтор-6-(піримідин-5-іл)-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-2'-аміну,
(R)-5',5'-дифтор-6-(піримідин-5-іл)-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-2'-аміну,
(R)-6-(2-хлорпіридин-4-іл)-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-2'-аміну,
(R)-6-(3,5-дихлорфеніл)-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-2'-аміну,
(R)-6-(3,5-дихлорфеніл)-5',5'-дифтор-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-2'-аміну,
(R)-6-(3,5-дихлорфеніл)-6',6'-дифтор-6',7'-дигідро-2'Н-спіро[хроман-4,5'-[1,4]оксазепін]-3'-аміну,
(R)-6-(5-хлорпіридин-3-іл)-5',5'-дифтор-2,2-диметил-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-2'-аміну,
(R)-6-(5-хлорпіридин-3-іл)-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-2'-аміну,
(R)-6'-(5-хлорпіридин-3-іл)-5,5-дифтор-5,6-дигідроспіро[[1,3]оксазин-4,4'-тіохроман]-2-аміну,
(R)-6-(5-хлорпіридин-3-іл)-5',5'-дифтор-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-2'-аміну,
(R)-6-(5-хлорпіридин-3-іл)-6',6'-дифтор-6',7'-дигідро-2'Н-спіро[хроман-4,5'-[1,4]оксазепін]-3'-аміну,
(R)-7-(5-хлорпіридин-3-іл)-4,4,5',5'-тетрафтор-3,4,5',6'-тетрагідро-2Н-спіро[нафталін-1,4'-[1,3]оксазин]-2'-аміну,
(R)-N-(2'-аміно-5',5'-дифтор-2,2-диметил-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6-іл)-5-хлорпіколінаміду,
(R)-N-(2'-аміно-5',5'-дифтор-2,2-диметил-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6-іл)-5-ціанопіколінаміду,
(R)-N-(2'-аміно-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-6-іл)-5-ціанопіколінаміду,
(R)-N-(2'-аміно-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-6-іл)-5-хлорпіколінаміду,
(R)-N-(2'-аміно-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-6-іл)-5-фторпіколінаміду,
(R)-N-(2'-аміно-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-6-іл)-5-(трифторметил)піколінаміду,
(R)-N-(2'-аміно-5',5'-дифтор-3,4,5',6'-тетрагідро-2Н-спіро[нафталін-1,4'-[1,3]оксазин]-7-іл)-5-хлорпіколінаміду,
(R)-N-(2'-аміно-5',5'-дифтор-3,4,5',6'-тетрагідро-2Н-спіро[нафталін-1,4'-[1,3]оксазин]-7-іл)-5-ціанопіколінаміду,
(R)-N-(2'-аміно-5',5'-дифтор-4,4-диметил-3,4,5',6'-тетрагідро-2Н-спіро[нафталін-1,4'-[1,3]оксазин]-7-іл)-5-ціанопіколінаміду,
(R)-N-(2-аміно-5,5-дифтор-5,6-дигідроспіро[[1,3]оксазин-4,4'-тіохроман]-6'-іл)-5-хлорпіколінаміду,
(R)-N-(2-аміно-5,5-дифтор-5,6-дигідроспіро[[1,3]оксазин-4,4'-тіохроман]-6'-іл)-5-ціанопіколінаміду,
(R)-N-(2'-аміно-5',5'-дифтор-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6-іл)-5-хлорпіколінаміду,
(R)-N-(2'-аміно-5',5'-дифтор-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6-іл)-5-ціанопіколінаміду,
(R)-N-(2'-аміно-5',5'-дифтор-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6-іл)-4-хлор-1Н-піразол-5-карбоксаміду,
(R)-N-(3'-аміно-6',6'-дифтор-3,4,6',7'-тетрагідро-2Н,2'Н-спіро[нафталін-1,5'-[1,4]оксазепін]-7-іл)-5-ціанопіколінаміду,
(R)-N-(3'-аміно-6',6'-дифтор-3,4,6',7'-тетрагідро-2Н,2'Н-спіро[нафталін-1,5'-[1,4]оксазепін]-7-іл)-5-хлорпіколінаміду,
(R)-N-(3'-аміно-6',6'-дифтор-6',7'-дигідро-2'Н-спіро[xроман-4,5'-[1,4]оксазепін]-6-іл)-5-ціанопіколінаміду,
(R)-N-(3'-аміно-6',6'-дифтор-6',7'-дигідро-2'Н-спіро[хроман-4,5'-[1,4]оксазепін]-6-іл)-5-хлорпіколінаміду,
(R)-N-(3'-амiно-6',6'-дифтор-6',7'-дигідро-2'Н-спіро[хроман-4,5'-[1,4]оксазепін]-6-іл)-3,5-дихлорпіколінаміду,
3-((2RS,4R)-2'-амiно-5',5'-дифтор-2-феніл-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6-іл)бензонітрилу,
3-((2RS,4R)-3'-аміно-6',6'-дифтор-2-феніл-6',7'-дигідро-2'Н-спіро[хроман-4,5'-[1,4]оксазепін]-6-іл)бензонітрилу,
3-[(2'R,4R)-2-аміно-5,5-дифтор-5,5",6,6"-тетрагідро-4"Н-диспіро[1,3-оксазин-4,4'-хромен-2',3"-піран]-6'-іл]бензонітрилу форміату,
5-((2RS,4R)-2'-аміно-5',5'-дифтор-2-феніл-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6-іл)нікотинонітрилу,
5-((2RS,4R)-3'-аміно-6',6'-дифтор-2-феніл-6',7'-дигідро-2'Н-спіро[хроман-4,5'-[1,4]оксазепін]-6-іл)нікотинонітрилу,
N-((2R aбo 2S,4R)-2'-аміно-5',5'-дифтор-2-феніл-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6-іл)-5-хлорпіколінаміду,
N-((2R aбo 2S,4R)-2'-аміно-5',5'-дифтор-2-феніл-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6-іл)-5-ціанопіколінаміду,
N-((2R aбo 2S,4R)-2'-аміно-5',5'-дифтор-2-феніл-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6-іл)-5-фторпіколінаміду,
N-((2R aбo 2S,4R)-2'-aмiнo-5',5'-дифтop-2-фeнiл-5',6'-дигiдpocпipo[xpoмaн-4,4'-[1,3]оксазин]-6-іл)-5-(трифторметил)піколінаміду,
N-((2RS,4R)-3'-aмiнo-6',6'-дифтop-2-фeнiл-6',7'-дигiдpo-2'H-cпipo[xpoмaн-4,5'-[1,4]оксазепін]-6-іл)-5-(трифторметил)піколінаміду,
N-((2RS,4R)-3'-aмiнo-6',6'-дифтop-2-фeнiл-6',7'-дигiдpo-2'H-cпіpo[xpoмaн-4,5'-[1,4]оксазепін]-6-іл)-5-ціанопіколінаміду,
N-[(2'R,4R)-2-aміно-5,5-дифтор-5,5",6,6"-тетрагідро-4"Н-диспіро[1,3-оксазин-4,4'-хромен-2',3"-піран]-6'-іл]-5-ціанопіридин-2-карбоксаміду,
N-[(4R)-2-aмiнo-5,5-дифтop-1',1'-діoкcидo-2',3',5,6-тeтpaгiдpocпipo[1,3-oкcaзин-4,4'-тіохромен]-6'-іл]-5-хлорпіридин-2-карбоксаміду і
N-[(4R)-2-aмiнo-5,5-дифтop-1',1'-дioкcидo-2',3',5,6-тeтpaгiдpocпipo[1,3-oкcaзин-4,4'-тіохромен]-6'-іл]-5-ціанопіридин-2-карбоксаміду,
або її фармацевтично прийнятні солі.
14. Сполука за будь-яким з пп. 1-13, вибрана з групи, що складається з:
(R)-N-(2'-aмiнo-5',5'-дифтop-2,3,5',6'-тeтpaгiдpocпipo[iндeн-1,4'-[1,3]oкcaзин]-6-iл)-5-ціанопіколінаміду,
(R)-6-(5-xлopпipидин-3-iл)-5',5'-дифтop-5',6'-дигiдpocпipo[xpoмaн-4,4'-[1,3]oкcaзин]-2'-аміну,
(R)-N-(2'-aмiнo-5',5'-дифтop-2,3,5',6'-тeтpaгiдpocпipo[iндeн-1,4'-[1,3]oкcaзин]-6-iл)-5-хлорпіколінаміду, і
(R)-N-(2'-aмiнo-5',5'-дифтop-2,3,5',6'-тeтpaгiдpocпipo[iндeн-1,4'-[1,3]oкcaзин]-6-iл)-5-фторпіколінаміду,
або її фармацевтично прийнятні солі.
15. Спосіб одержання сполук формули І за будь-яким з пп. 1-12, який включає взаємодію сполуки формули І' та карбонової кислоти формули Z-COOH в присутності конденсуючого агента 4-(4,6-диметокси[1.3.5]триазин-2-іл)-4-метилморфоліну хлоридгідрату (DMTMM) в розчиннику, такому як метанол
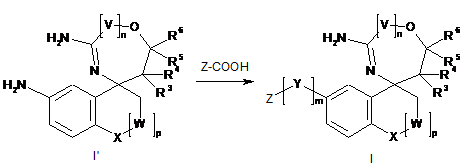 ,
,
де V, W, Y, Z, n, р, R1, R2, R3, R4, R5 та R6 є такими, як визначено в будь-якому з пп. 1-12, і m означає 1.
16. Сполука формули І за будь-яким з пп. 1-14 для застосування як терапевтично активної речовини.
17. Сполука формули І за будь-яким з пп. 1-14 для застосування як терапевтично активної речовини при терапевтичному та/або профілактичному лікуванні захворювань та порушень, які характеризуються підвищеними рівнями b-амілоїду та/або олігомерів b-амілоїду та/або b-амілоїдних бляшок та подальших відкладень або хвороби Альцгеймера.
18. Сполука формули І за будь-яким з пп. 1-14 для застосування як терапевтично активної речовини при терапевтичному та/або профілактичному лікуванні діабету або діабету 2 типу.
19. Фармацевтична композиція, що містить сполуку формули І за будь-яким з пп. 1-14 та фармацевтично прийнятний носій та/або фармацевтично прийнятну допоміжну речовину.
20. Застосування сполуки формули І за будь-яким з пп. 1-14 при виготовленні лікарського засобу для терапевтичного або профілактичного лікування хвороби Альцгеймера.
21. Застосування сполуки формули І за будь-яким з пп. 1-14 при виготовленні лікарського засобу для терапевтичного або профілактичного лікування діабету.
22. Спосіб терапевтичного та/або профілактичного лікування хвороби Альцгеймера, який включає введення сполуки формули І за будь-яким з пп. 1-14 людині або тварині.
23. Спосіб терапевтичного та/або профілактичного лікування діабету або діабету 2 типу, який включає введення сполуки формули І за будь-яким з пп. 1-14 людині або тварині.
Текст
Реферат: В даному винаході запропоновані спіро-[1,3]-оксазини та спіро-[1,4]-оксазепіни формули І V H2 N n O R 6 5 Y Z * R 4 R N R m X W 3 p ,I які виявляють інгібіторну активність по відношенню до ВАСЕ1 та/або ВАСЕ2, їх одержання, фармацевтичні композиції, їх що містять, та їх застосування як терапевтично активних речовин. Активні сполуки за даним винаходом корисні при терапевтичному або профілактичному лікуванні, наприклад, хвороби Альцгеймера та сахарного діабету 2 типу. UA 111847 C2 (12) UA 111847 C2 V 6 R O H N n 5 R 4 HR N Y 3 R m Z W p X UA 111847 C2 5 10 15 20 25 30 35 40 45 50 55 60 РІВЕНЬ ТЕХНІКИ Хвороба Альцгеймера (ХА) є нейродегенеративним захворюванням центральної нервової системи та є провідною причиною прогресуючого недоумства у населення літнього віку. Її клінічними симптомами є погіршення пам’яті, когнітивної діяльності, орієнтації у часі та локальної орієнтації, суджень та міркувань, а також тяжкі емоціональні порушення. Зараз немає способів лікування, які можуть запобігти захворюванню або його прогресуванню, або стабільно обертати його клінічні симптоми. ХА зробилася серйозною проблемою охорони здоров’я в усіх суспільствах з високою тривалістю життя, а також значним економічним тягарем для систем охорони здоров’я. ХА характеризується 2 основними патологіями в центральній нервовій системі (ЦНС) утворенням амілоїдних бляшок та нейрофібрилярних клубків (Hardy та співавт., The amyloid hypothesis of Alzheimer's disease: progress and problems on the road to therapeutics, Science. 2002 Jul 19;297(5580):353-6, Selkoe, Cell biology of the amyloid beta-protein precursor and the mechanism of Alzheimer's disease, Annu Rev Cell Biol. 1994;10:373-403). Обидві патології також часто спостерігаються у пацієнтів із синдромом Дауна (трисомія 21 хромосоми), при якому в більш ранньому віці також розвиваються симптоми, схожі з ХА. Нейрофібрилярні клубки є внутрішньоклітинними агрегатами зв’язаного з мікротрубочками тау білка (MAPT). Амілоїдні бляшки утворюються в міжклітинному просторі; їх головним компонентом є Aβ-пептиди. Вони є групою протеолітичних фрагментів, утворюваних з попередника білка β-амілоїду (APP) в результаті серії стадій протеолітичного розщеплення. Деякі форми APP були ідентифіковані, з них найчастіше зустрічаються білки довжиною 695, 751 та 770 амінокислот. Усі вони походять з одного гена внаслідок різного сплайсингу. Aβ-пептиди утворюються з одного домену білка APP, але вони відрізняються на їх N- та C-кінцях, довжина основних різновидів складає 40 та 42 амінокислоти. Існує декілька доказів, які явно підтверджують, що агреговані Aβ-пептиди є важливими молекулами в патогенезі ХА: 1) амілоїдні бляшки, утворені з Aβ-пептидів, є незмінною складовою патології ХА; 2) Aβ-пептиди токсичні для нейронів; 3) при спадковій хворобі Альцгеймера (FAD) мутації у зв’язаних із захворюванням генах APP, PSN1, PSN2 приводять до підвищеного рівня Aβ-пептидів та раннього амілоїдозу головного мозку; 4) у трансгенних мишей, експресуючих такі FAD-гени, розвивається патологія, яка має багато спільного із захворюванням людини. Aβ-Пептиди утворюються з APP шляхом послідовної дії двох протеолітичних ферментів, називаних β- та γ-секретазами. β-Секретаза спочатку розщеплює позаклітинний домен APP приблизно в районі 28 амінокислоти за межами трансмембранного домену (TM) з утворенням C-кінцевого фрагмента APP, що містить TM- та цитоплазматичний домен (CTFβ). CTFβ є субстратом для γ-секретази, яка розщеплює в декількох суміжних позиціях усередині TM-домену з утворенням Aβ-пептидів та цитоплазматичного фрагмента. γ-Секретаза є комплексом з принаймні 4 різних білків, її каталітична субодиниця дуже схожа на білок пресенілін (PSEN1, PSEN2). β-Секретаза (BACE1, Asp2; BACE позначає (β-сайт APP)-розщеплюючий фермент) є аспартилпротеазою, яка закріплена в мембрані за допомогою трансмембранного домену (Vassar та співавт., Betasecretase cleavage of Alzheimer's amyloid precursor protein by the transmembrane aspartic protease BACE, Science. 1999 Oct 22;286(5440):735). Вона експресується у множині тканин людського організму, однак її рівень є особливо високим в ЦНС. Генетичне видалення гена BACE1 у мишей ясно показує, що її активність є суттєвою для процесингу APP, який приводить до утворення Aβ-пептидів, без BACE1 Aβ-пептиди не продукуються (Luo та співавт., Mice deficient in BACE1, the Alzheimer's beta-secretase, have normal phenotype and abolished beta-amyloid generation, Nat Neurosci. 2001 Mar;4(3):231-2, Roberds та співавт., BACE knockout mice are healthy despite lacking the primary beta-secretase activity in brain: implications for Alzheimer's disease therapeutics, Hum Mol Genet. 2001 Jun 1;10(12):1317-24). Генетично модифіковані миші, які експресують людський ген APP та формують у великій кількості амілоїдні бляшки та патології, аналогічні захворюванню ХА при старінні, втрачають таку здатність при зниженні активності β-секретази шляхом видалення однієї з алелей гена BACE1 (McConlogue та співавт., Partial reduction of BACE1 has dramatic effects on Alzheimer plaque and synaptic pathology in APP Transgenic Mice. J Biol Chem. 2007 Sep 7;282(36):26326). Це, таким чином, дозволяє припустити, що інгібітори активності BACE1 можуть бути корисним засобом для лікування хвороби Альцгеймера (AD). Діабет 2 типу (T2D) є результатом резистентності до інсуліну та аномальної секреції інсуліну β-клітинами підшлункової залози, приводячи до зниженого контролю рівня глюкози в крові та гіперглікемії (M Prentki & CJ Nolan, “Islet beta-cell failure in type 2 diabetes.” J. Clin. Investig. 2006, 116(7), 1802-1812). Пацієнти з T2D мають підвищений ризик мікро- та макросудинних захворювань та ряду зв’язаних ускладнень, включаючи діабетичну нефропатію, ретинопатію та 1 UA 111847 C2 5 10 15 20 25 30 35 40 45 50 55 серцево-судинні захворювання. В 2000 р., за оцінками, від цього стану потерпали 171 мільйон осіб, з гаданим подвоєнням цієї цифри до 2030 р. (S Wild, G Roglic, A Green, R.Sicree & H King, “Global prevalence of diabetes”, Diabetes Care 2004, 27(5), 1047-1053), що робить це захворювання головною проблемою охорони здоров’я. Ріст розповсюдженості цукрового діабету 2 типу зв’язаний із сидячим способом життя та споживанням висококалорійної їжі населенням світу (P Zimmet, KGMM Alberti & J Shaw, “Global and societal implications of the diabetes epidemic” Nature 2001, 414, 782-787). Недостатність β-клітин і подальше різке зниження секреції інсуліну та гіперглікемія означають початок T2D. Більшість сучасних способів лікування не запобігає втраті маси βклітин, що характеризує явний T2D. Однак недавня розробка аналогів GLP-1, гастрину та інших агентів показує, що можна добитися збереження та проліферації β-клітин, що приводить до поліпшення толерантності до глюкози та більш повільного прогресування до явного T2D (LL Baggio & DJ Drucker, “Therapeutic approaches to preserve islet mass in type 2 diabetes”, Annu. Rev. Med. 2006, 57, 265-281). Tmem27 був ідентифікований як білок, що сприяє проліферації бета-клітин (P Akpinar, S Kuwajima, J Krützfeldt, M Stoffel, “Tmem27: A cleaved and shed plasma membrane protein that stimulates pancreatic β cell proliferation”, Cell Metab. 2005, 2, 385-397) та секреції інсуліну (K Fukui, Q Yang, Y Cao, N Takahashi та співавт., “The HNF-1 target Collectrin controls insulin exocytosis by SNARE complex formation”, Cell Metab. 2005, 2, 373-384). Tmem27 є 42 кДа мембранним глікопротеїном, який постійно від’єднується від поверхні β-клітин в результаті деградації повнорозмірного клітинного Tmem27. Надекспресія Tmem27 у трансгенних мишей збільшує масу β-клітин та поліпшує толерантність до глюкози у DIO моделі діабету з викликаним дієтою ожирінням. Крім того, міРНК-нокаут Tmem27 в аналізі проліферації β-клітин гризунів (наприклад, за допомогою INS1e-клітин) зменшує швидкість проліферації, вказуючи на роль Tmem27 в контролі маси β-клітин. В тому самому аналізі проліферації, інгібітори BACE2 також збільшували проліферацію. Тим не менш, інгібування BACE2 у поєднанні з Tmem27 міРНК-нокдауном приводило до низької швидкості проліферування. Таким чином, можна зробити висновок, що BACE2 є протеазою, яка відповідає за деградацію Tmem27. Крім того, in vitro, BACE2 розщеплює пептид на основі послідовності Tmem27. Тісно зв’язана протеаза BACE1 не розщеплює цей пептид, а селективне інгібування однієї лише BACE1 не дає збільшення проліферації β-клітин. Близький гомолог BACE2 є мембраннозв’язаною аспартилпротеазою та колокалізується з Tmem27 в β-клітинах підшлункової залози людини (G Finzi, F Franzi, C Placidi, F Acquati та співавт., “BACE2 is stored in secretory granules of mouse and rat pancreatic beta cells”, Ultrastruct Pathol. 2008, 32(6), 246-251). Відомо також, що вона здатна розкладати АРР (I Hussain, D Powell, D Howlett, G Chapman та співавт., “ASP1 (BACE2) cleaves the amyloid precursor protein at the βsecretase site” Mol Cell Neurosci. 2000, 16, 609-619), IL-1R2 (P Kuhn, E Marjaux, A Imhof, B De Strooper та співавт., “Regulated intramembrane proteolysis of the interleukin-1 receptor II by alpha-, beta-, and gamma-secretase” J. Biol. Chem. 2007, 282(16), 11982-11995) та ACE2. Здатність до деградації ACE2 вказує на можливу роль BACE2 в контролі гіпертензії. Тому інгібування BACE2 пропонується для лікування цукрового діабету 2 типу з потенціалом збереження та відновлення маси β-клітин та стимулювання секреції інсуліну в переддіабетичному стані та у хворих на цукровий діабет. Відповідно, задачею даного винаходу є створення селективних інгібіторів BACE2. Такі сполуки є корисними як терапевтично активні речовини, зокрема при лікуванні та/або профілактиці захворювань, зв’язаних з інгібуванням BACE2. Крім того, утворення або утворення та відкладення β-амілоїдних пептидів в, на або навколо неврологічної тканини (наприклад, мозку) інгібуються сполуками за даним винаходом, тобто інгібується Aβ-продукція з APP або фрагмента АРР. В даному винаході запропоновані нові сполуки формули I, їх одержання, лікарські засоби на основі сполуки відповідно до даного винаходу та їх виготовлення, а також застосування сполук формули I при лікуванні або профілактиці захворювань, таких як хвороба Альцгеймера та цукровий діабет 2 типу. Новісполуки формули I мають поліпшені фармакологічні властивості. Галузь, до якої належить винахід В даному винаході запропоновані спіро-[1,3]-оксазини та спіро-[1,4]-оксазепіни, які мають властивості інгібіторів BACE1 та/або BACE2, їх виготовлення, фармацевтичні композиції, що їх містять, та їх застосування як терапевтично активних речовин. Стислий опис винаходу В даному винаході запропоновані сполуки формули I, 60 2 UA 111847 C2 V H2N 4 R 3 R m X 5 10 15 20 25 30 35 40 45 50 5 R N Y Z 6 R O n W p I де замісники та змінні є такими, як описано нижче та в формулі винаходу, або їх фармацевтично прийнятні солі. Сполуки за даним винаходом виявляють інгібіторну активність по відношенню до Asp2 (βсекретаза, BACE1 або мемапсин-2) і, таким чином, можуть застосовуватися при лікуванні та/або профілактиці захворювань та порушень, які характеризуються підвищеними рівнями β-амілоїду та/або олігомерів β-амілоїдів та/або β-амілоїдних бляшок та додаткових відкладень, зокрема, хвороби Альцгеймера. Та/або сполуки за даним винаходом мають інгібіторну активність по відношенню до BACE2 і можуть, таким чином, застосовуватися в профілактичному та/або терапевтичному лікуванні захворювань та порушень, таких як діабет 2-го типу, та інших розладів метаболізму. Докладний опис винаходу В даному винаході запропоновані сполуки формули I та їх фармацевтично прийнятні солі, одержання вищевказаних сполук, лікарські засоби, що їх містять, та їх виготовлення, а також застосування вищевказаних сполук I при терапевтичному та/або профілактичному лікуванні захворювань та порушень, зв’язаних з інгібуванням активності BACE1 та/або BACE2, таких як хвороба Альцгеймера та цукровий діабет 2 типу. Крім того, утворення або утворення та відкладення β-амілоїдних бляшок в, на або навколо неврологічної тканини (наприклад, мозку) інгібуються сполуками за даним винаходом шляхом інгібування продукції Aβ з APP або фрагмента АРР. Наступні визначення загальних термінів, використовуваних в даному описі, є застосовними незалежно від того, чи використовуються терміни, про які йде мова, окремо або в комбінації з іншими групами. Якщо не вказане інше, наступні терміни, використовувані в даній заявці, включаючи опис та формулу винаходу, мають значення, наведені нижче. Слід відзначити, що при використанні в описі та формулі винаходу, що додається, форми однини включають посилання на множину, якщо з контексту явно не випливає інше. Термін "C1-6-алкіл", самостійно або в комбінації з іншими групами, позначає вуглеводневий радикал, який може бути лінійним чи розгалуженим, з однією чи декількома точками розгалужування, де алкільна група в основному містить від 1 до 6 атомів вуглецю, наприклад, метил (Me), етил (Et), пропіл, ізопропіл (i-пропіл), н-бутил, ізо-бутил (ізобутил), 2-бутил (вторбутил), т-бутил (трет-бутил), ізопентил, 2-етилпропіл, 1,2-диметилпропіл тощо. Термін "C1-3алкіл", самостійно або в комбінації з іншими групами, позначає вуглеводневий радикал, який може бути лінійним чи розгалуженим, де алкільна група містить від 1 до 3 атомів вуглецю. Конкретними прикладами «C1-6-алкілів» є "C1-3-алкіли". Конкретними прикладами є метил та етил. Найбільш конкретно - метил. Термін “ціано-C1-6-алкіл”, самостійно або в комбінації з іншими групами, позначає C1-6-алкіл, як тут визначено, який заміщений одним чи декількома ціано, зокрема, 1-5 ціано, більш конкретно, 1 ціано. Прикладами є ціанометил тощо. Термін "галоген-С1-6-алкіл", самостійно або в комбінації з іншими групами, стосується C 1-6алкілу, як визначено тут, який заміщений одним чи декількома галогенами, зокрема 1-5 галогенами, більш конкретно, 1-3 галогенами, ще більш конкретно, 1 галогеном або 3 галогенами. Термін "галоген-С1-3-алкіл", самостійно або в комбінації з іншими групами, стосується C1-3-алкілу, як визначено тут, який заміщений одним чи декількома галогенами, зокрема 1-5 галогенами, більш конкретно, 1-3 галогенами, ще більш конкретно, 1 галогеном або 3 галогенами. Конкретний галоген позначає фтор. Конкретний "галоген-C1-6-алкіл" позначає фтор-C1-6-алкіл, і конкретний "галоген-C1-3-алкіл" позначає фтор-C1-3-алкіл. Прикладами є дифторметил, хлорметил, фторметил тощо. Конкретним прикладом є трифторметил. Термін “C1-6-алкокси-C1-6-алкіл”, самостійно або в комбінації з іншими групами, стосується C 1 3 UA 111847 C2 який заміщений одним чи декількома C1-6-алкокси, як тут визначено. Прикладами є MeO-Me, 1MeO-Et, 2MeO-Et, 1MeO-2EtO-пропіл тощо. Термін “ціано”, самостійно або в комбінації з іншими групами, стосується N≡C-(CN). Термін “галоген", самостійно або в комбінації з іншими групами, позначає хлор (Cl), йод (I), фтор (F) та бром (Br). Конкретними “галогенами” є Cl та F. Конкретним ”галогеном” є F. Термін "гетероарил", самостійно або в комбінації з іншими групами, стосується ароматичної карбоциклічної групи, що має одне 4-8-членне кільце або декілька конденсованих кілець, що містять від 6 до 14, зокрема, від 6 до 10 кільцевих атомів, та містять 1, 2 або 3 гетероатоми, незалежно вибрані з N, O та S, зокрема N та О, у яких принаймні одне гетероциклічне кільце є ароматичним. Приклади "гетероарилу" включають бензофурил, бензимідазоліл, 1Нбензимідазоліл, бензоксазиніл, бензоксазоліл, бензотіазиніл, бензотіазоліл, бензотієніл, бензотриазоліл, фурил, імідазоліл, індазоліл, 1Н-індазоліл, індоліл, ізохінолініл, ізотіазоліл, ізоксазоліл, оксазоліл, піразиніл, піразоліл (піразил), 1H-піразоліл, піразоло[1,5-а]піридиніл, піридазиніл, піридиніл, піримідиніл, піроліл, хінолініл, тетразоліл, тіазоліл, тієніл, триазоліл, 6,7дигідро-5H-[1]піридиніл тощо. Конкретними "гетероарилами" є піридиніл, піримідиніл та 1Нпіразоліл. Конкретними групами є піридин-2-іл, піридин-3-іл, піридин-4-іл, піримідин-5-іл та 1Нпіразол-5-іл. Термін "арил" означає одновалентну ароматичну карбоциклічну моно- або бициклічну кільцеву систему, яка містить від 6 до 10 кільцевих атомів вуглецю. Приклади арильних груп включають феніл та нафтил. Конкретним “арилом” є феніл. Термін "гетероцикліл", самостійно або в комбінації з іншими групами, означає одновалентну насичену або частково ненасичену моно- або біциклічну кільцеву систему з 4-9 кільцевих атомів, яка містить 1, 2 або 3 кільцевих гетероатоми, вибраних із N, O та S, решта кольцевих атомів є вуглецем. Біциклічний означає такий, що складається з двох циклів, які мають два спільних кільцевих атоми, тобто місточок, що розділяє два кільця, є або одинарним зв’язком, або ланцюжком з одного чи двох кільцевих атомів. Прикладами моноциклічного насиченого гетероциклілу є азетидиніл, піролідиніл, тетрагідрофураніл, тетрагідротієніл, піразолідиніл, імідазолідиніл, оксазолідиніл, ізоксазолідиніл, тіазолідиніл, піперидиніл, тетрагідропіраніл, тетрагідротіопіраніл, піперазиніл, морфолініл, тіоморфолініл, 1,1-діоксотіоморфолін-4-іл, азепаніл, діазепаніл, гомопіперазиніл або оксазепаніл. Прикладами біциклічного насиченого гетероциклілу є 8-азабіцикло[3,2,1]октил, хінуклідиніл, 8-окса-3-азабіцикло[3,2,1]октил, 9азабіцикло[3,3,1]ноніл, 3-окса-9-азабіцикло[3,3,1]ноніл або 3-тіа-9-азабіцикло[3,3,1]ноніл. Прикладами частково ненасиченого гетероциклілу є дигідрофурил, імідазолініл, дигідрооксазоліл, тетрагідропіридиніл або дигідропіраніл. Конкретним "гетероциклілом" є тетрагідрофураніл. Термін "C1-6-алкокси", самостійно або в комбінації з іншими групами, означає -O-C1-6-алкіл, який може бути лінійним або розгалуженим, з однією чи декількома точками розгалуження, де алкільна група в основному містить від 1 до 6 атомів вуглецю, наприклад, метокси (OMe, MeO), етокси (OEt), пропокси, ізопропокси (і-пропокси), н-бутокси, і-бутокси (ізобутокси), 2-бутокси (втор-бутокси), т-бутокси (трет-бутокси), ізопентилокси (і-пентилокси) тощо. Конкретними "C1-6алкокси" є групи з від 1 до 4 атомами вуглецю. Конкретними прикладами є метокси та етокси. Термін "галоген-С1-6-алкокси", самостійно або в комбінації з іншими групами, стосується C1-6алкокси, як визначено тут, який заміщений одним чи декількома галогенами, зокрема фтором. Конкретним "галоген-C1-6-алкокси" є фтор-C1-6-алкокси. Конкретними групами є дифторметокси та трифторметокси. Термін "С2-6-алкініл", самостійно або в комбінації з іншими групами, означає одновалентну лінійну або розгалужену насичену вуглеводневу групу з 2-6 атомів вуглецю, зокрема 2-4 атомів вуглецю, яка містить один, два чи три потрійні зв’язки. Приклади C2-6-алкінілу включають етиніл, пропініл та н-бутиніл. Конкретними прикладами є етиніл та пропініл. Термін "фармацевтично прийнятні солі" стосується солей, які є придатними для використання при контакті з тканинами людини та тварин. Прикладами придатних солей з неорганічними та органічними кислотами є, без обмеження ними, оцтова кислота, лимонна кислота, мурашина кислота, фумарова кислота, соляна кислота, молочна кислота, малеїнова кислота, яблучна кислота, метансульфонова кислота, азотна кислота, фосфорна кислота, птолуолсульфонова кислота, бурштинова кислота, сірчана кислота, сірчана кислота, винна кислота, трифтороцтова кислота тощо. Конкретними прикладами є мурашина кислота, трифтороцтова кислота та соляна кислота. Зокрема, соляна кислота, трифтороцтова кислота та фумарова кислота. Терміни "фармацевтично прийнятний носій" та "фармацевтично прийнятні допоміжні речовини" стосуються носіїв та допоміжних речовин, таких як розріджувачі або наповнювачі, 6-алкілу, 5 10 15 20 25 30 35 40 45 50 55 60 4 UA 111847 C2 5 10 15 20 25 30 35 40 45 50 55 60 сумісні з іншими інгредієнтами композиції. Термін "фармацевтична композиція" охоплює продукт, що містить визначені інгредієнти в заздалегідь визначених кількостях або пропорціях, а також будь-який продукт, утворюваний, прямо чи опосередковано, з комбінації зазначених інгредієнтів в зазначених кількостях. Зокрема, він охоплює продукт, що містить один чи декілька активних інгредієнтів та, можливо, носій, що включає інертні інгредієнти, а також будь-який продукт, який прямо чи опосередковано утворюється, в результаті комбінації, комплексоутворювання або агрегації будь-яких двох чи декількох інгредієнтів або в результаті дисоціації одного чи декількох інгредієнтів, або в результаті інших типів реакцій або взаємодій одного чи декількох інгредієнтів. Термін "інгібітор" означає сполуку, яка конкурує з, знижує чи запобігає зв’язуванню конкретного ліганду з конкретним рецептором, або яка знижує чи запобігає інгібуванню функції конкретного білка. Термін "половина максимальної інгібуючої концентрації" (IC50) позначає концентрацію конкретної сполуки, необхідну для одержання 50%-ного інгібування біологічного процесу in vitro. Значення IC50 можуть бути перетворені на логарифмічні значення pIC50 (-log IC50), для яких більш високі значення вказують експоненціально більшу ефективність. Значення IC 50 не є абсолютним, але залежить від умов експерименту, наприклад, використовуваних концентрацій. Значення IC50 може бути перетворене на абсолютну константу інгібування (Ki) за рівнянням Ченга-Прусова (Biochem. Pharmacol. (1973) 22:3099). Термін "константа інгібування" (Ki) позначає абсолютну спорідненість зв’язування конкретного інгібітора з рецептором. Вона вимірюється за допомогою аналізу конкурентного зв’язування та дорівнює концентрації, при якій конкретний інгібітор буде зв’язувати 50% рецепторів за відсутності конкуруючого ліганду (наприклад, радіоактивного ліганду). Значення Ki можуть бути перетворені логарифмічно на значення pKI (-log Ki), для яких більш високі значення вказують експоненціально більшу ефективність. "Терапевтично ефективна кількість" означає кількість сполуки, яка, при введенні суб’єкту для лікування хворобливого стану, є достатньою для проведення такого лікування хворобливого стану. "Терапевтично ефективна кількість" буде варіюватися в залежності від сполуки, стану захворювання, яке лікують, тяжкості захворювання, яке лікують, віку та відносного стану здоровья суб’єкта, способу та форми введення, думки лікаря-куратора або ветеринара та інших факторів. Термін "як визначено тут" та "як описано тут", при посиланні на змінну, включає шляхом посилання широке визначення змінної, а також кращі, ще кращі та найкращі визначення, якщо такі є. Терміни "обробка", "контактування" та "взаємодія", по відношенню до хімічної реакції, означають додавання або змішування двох чи декількох реагентів при відповідних умовах для одержання зазначеного та/або бажаного продукту. Слід розуміти, що реакція, яка приводить до зазначеного та/або бажаного продукту, не обов’язково проводиться безпосередньо із комбінації двох реагентів, які були додані спочатку, тобто, можуть існувати одна чи декілька проміжних сполук, що утворюються в суміші, які в кінцевому підсумку приводять до утворення зазначеного та/або бажаного продукту. Термін "захисна група" позначає групу, яка селективно блокує реакційноздатну ділянку в багатофункціональній сполуці таким чином, що хімічна реакція може бути проведена селективно в іншій незахищеній реакційноздатній ділянці, в значенні, звичайно пов’язаному з нею в хімічному синтезі. Захисні групи можуть бути видалені на відповідній стадії. Типовими захисними групами є аміно-захисні групи, карбокси-захисні групи або гідрокси-захисні групи. 1 Термін "аміно-захисні групи" (також позначувані тут P ) позначає групи, призначені для захисту аміногрупи, та включає бензил, бензилоксикарбоніл (карбобензилокси, CBZ), 9флуоренілметилоксикарбоніл (Fmoc), п-метоксибензилоксикарбоніл, пнітробензилоксикарбоніл, трет-бутоксикарбоніл (ВОС), трифенілметил (Tr), 4монометокситритил (MMTr), 4,4-диметокситритил (DMTr), 4,4',4"-триметокситритил та трифторацетил. Інші приклади таких груп можна знайти у TW Greene та PGM Wuts, “Protective Groups in Organic Synthesis”, 2nd ed., John Wiley & Sons, Inc., New York, NY, 1991, chapter 7; E. Haslam, “Protective Groups in Organic Chemistry”, J. G. W. McOmie, Ed., Plenum Press, New York, NY, 1973, Chapter 5, та T.W. Greene, “Protective Groups in Organic Synthesis”, John Wiley та Sons, New York, NY, 1981. Термін "захищена аміногрупа" стосується аміногрупи, заміщеної за допомогою аміно-захисної групи. Конкретними амінозахисними групами є третбутоксикарбонільна група та диметокситритил. Термін "відхідна група" позначає групу зі значенням, звичайно пов’язаним з ним в хімії органічного синтезу, тобто атом або групу, які заміщаються в умовах реакції заміщення. 5 UA 111847 C2 5 10 15 Приклади відхідних груп включають галоген, зокрема бром, алкан- або ариленсульфонілокси, такі як метансульфонілокси, етансульфонілокси, тіометил, бензолсульфонілокси, тозилокси та тієнілокси, дигалофосфіноїлокси, можливо, заміщений бензилокси, ізопропілокси та ацилокси. Термін "ароматичний" означає звичайне розуміння ароматичності, як визначено в літературі, зокрема в IUPAC - Compendium of Chemical Terminology, 2nd, A. D. McNaught & A. Wilkinson (Eds). Blackwell Scientific Publications, Oxford (1997). Термін "фармацевтично прийнятний ексципієнт" означає будь-який інгредієнт, що не має терапевтичної активності та не є токсичним, такий як розпушувачі, зв’язуючі речовини, наповнювачі, розчинники, буфери, тонізуючі агенти, стабілізатори, антиоксиданти, поверхневоактивні речовини або любриканти, використовувані при розробці фармацевтичних продуктів. Кожного разу, коли в хімічній структурі присутній хіральний атом вуглецю, вважається, що усі стереоізомери, пов’язані з цим хіральним атомом вуглецю, охоплюються структурами. Винахід також стосується фармацевтичних композицій, способів застосування та способів одержання вищевказаних сполук. Усі окремі варіанти здійснення можуть бути скомбіновані. Одним з втілень винаходу є сполука формули I, V H2N 4 R 3 R m X 20 25 30 35 40 45 50 5 R N Y Z 6 R O n W p I де 7a 7b V позначає -CR R -; 2a 2b W позначає -CR R -; 1a 1b X позначає -CR R -, -O-, -S- або -SO2-; Y -NH-C=O-; Z вибраний з групи, що складається з i) гетероарилу, ii) гетероарилу, заміщеного 1-4 замісниками, незалежно вибраними з R8, iii) арилу, і iv) арилу, заміщеного 1-4 замісниками, незалежно вибраними з R8, 1a R вибраний з групи, що складається з i) водню, ii) галогену, і iii) C1-6-алкілу; 1b R вибраний з групи, що складається з i) водню, ii) галогену, і iii) C1-6-алкілу; 2a R вибраний з групи, що складається з i) водню, і ii) C1-6-алкілу; 2b R вибраний з групи, що складається з i) водню, ii) арилу, і iii) C1-6-алкілу; 2a 2b або R та R разом з атомом вуглецю, до якого вони приєднані, утворюють гетероцикліл; 3 R вибраний з групи, що складається з i) водню, і ii) галогену, 4 R вибраний з групи, що складається з i) водню, і 6 UA 111847 C2 5 10 15 20 25 30 35 40 45 50 55 60 ii) галогену, 5 R вибраний з групи, що складається з i) водню, і ii) C1-6-алкілу, 6 R вибраний з групи, що складається з i) водню, і ii) C1-6-алкілу, 7a R вибраний з групи, що складається з i) водню, і ii) C1-6-алкілу; 7b R вибраний з групи, що складається з i) водню, і ii) C1-6-алкілу; 8 R вибраний з групи, що складається з i) ціано, ii) ціано-C1-6-алкілу, iii) галогену, iv) галоген-C1-6-алкокси, v) галоген-C1-6-алкілу, vi) C1-6-алкокси, vii) C1-6-алкокси-C1-6-алкілу, viii) C2-6-алкінілу, і ix) C1-6-алкілу; n позначає 0 або 1; m позначає 0 або 1; p позначає 0 або 1; або її фармацевтично прийнятні солі. Одним з втілень є сполука, описана тут, у якій 7a 7b V позначає -CR R -; 2a 2b W позначає -CR R -; 1a 1b X позначає -CR R -, -O-, -S- або -SO2-; Y -NH-C=O-; Z вибраний з групи, що складається з i) гетероарилу, ii) гетероарилу, заміщеного 1-2 замісниками, незалежно вибраними з R8, і iii) арилу, заміщеного 1-2 замісниками, незалежно вибраними з R8, 1a R вибраний з групи, що складається з i) водню, ii) галогену, і iii) C1-6-алкілу; 1b R вибраний з групи, що складається з i) водню, ii) галогену, і iii) C1-6-алкілу; 2a R вибраний з групи, що складається з i) водню, і ii) C1-6-алкілу; 2b R вибраний з групи, що складається з i) водню, ii) фенілу, і iii) C1-6-алкілу; 2a 2b або R та R разом з атомом вуглецю, до якого вони приєднані, утворюють тетрагідропіраніл; 3 R позначає галоген; 4 R позначає галоген; 5 R позначає водень; 6 R позначає водень; 7a R позначає водень; 7b R позначає водень; 8 R вибраний з групи, що складається з 7 UA 111847 C2 5 10 15 20 25 30 35 40 45 50 55 60 i) ціано, ii) галогену, iii) галоген-C1-6-алкілу, і iv) C1-6-алкокси, n позначає 0 або 1; m позначає 0 або 1; p позначає 0 або 1; або її фармацевтично прийнятні солі. Одним з втілень є сполука, описана тут, у якій 7a 7b V позначає -CR R -; 2a 2b W позначає -CR R -; 1a 1b X позначає -CR R -; Y -NH-C=O-; Z вибраний з групи, що складається з i) гетероарилу, ii) гетероарилу, заміщеного 1-2 замісниками, незалежно вибраними з R8, і iii) арилу, заміщеного 1-2 замісниками, незалежно вибраними з R8, 1a R вибраний з групи, що складається з i) водню, ii) галогену, і iii) C1-6-алкілу; 1b R вибраний з групи, що складається з i) водню, ii) галогену, і iii) C1-6-алкілу; 2a R вибраний з групи, що складається з i) водню, і ii) C1-6-алкілу; 2b R вибраний з групи, що складається з i) водню, ii) фенілу, і iii) C1-6-алкілу; 3 R позначає галоген; 4 R позначає галоген; 5 R позначає водень; 6 R позначає водень; 7a R позначає водень; 7b R позначає водень; 8 R вибраний з групи, що складається з i) ціано, ii) галогену, і iii) галоген-C1-6-алкілу; n позначає 0 або 1; m позначає 0 або 1; p позначає 0 або 1; або її фармацевтично прийнятні солі. Одним з втілень є сполука, описана тут, у якій 1a 1b X позначає -CR R -; Y -NH-C=O-; 8 Z позначає гетероарил, заміщений R , 1a R позначає водень; 1b R позначає водень; 3 R позначає галоген; 4 R позначає галоген; 5 R позначає водень; 6 R позначає водень; 7a R позначає водень; 7b R позначає водень; 8 R вибраний з групи, що складається з i) ціано, і 8 UA 111847 C2 5 10 15 20 25 30 35 40 45 50 55 60 ii) галогену, і n позначає 0; m позначає 1; p позначає 0; або її фармацевтично прийнятні солі. Одним з втілень є сполука, як описано тут, де n позначає 0. Одним з втілень є сполука, як описано тут, де n позначає 1. Одним з втілень є сполука, як описано тут, де m позначає 0. Одним з втілень є сполука, як описано тут, де m позначає 1. Одним з втілень є сполука, як описано тут, де p позначає 0. Одним з втілень є сполука, як описано тут, де p позначає 1. 1a 1b 1a 1b Одним з втілень є сполука, як описано тут, де X позначає -CR R -, а R та R обидва є воднем. 1a 1b Одним з втілень є сполука, як описано тут, де X позначає -CR R -. 1a Одним з втілень є сполука, як описано тут, де R позначає водень. 1a Одним з втілень є сполука, як описано тут, де R позначає галоген. 1a Одним з втілень є сполука, як описано тут, де R позначає F. 1a Одним з втілень є сполука, як описано тут, де R позначає C1-6-алкіл. 1a Одним з втілень є сполука, як описано тут, де R позначає метил. 1b Одним з втілень є сполука, як описано тут, де R позначає водень. 1b Одним з втілень є сполука, як описано тут, де R позначає галоген. 1b Одним з втілень є сполука, як описано тут, де R позначає F. 1b Одним з втілень є сполука, як описано тут, де R позначає C1-6-алкіл. 1b Одним з втілень є сполука, як описано тут, де R позначає метил. 2a Одним з втілень є сполука, як описано тут, де R позначає C1-6-алкіл. 2a Одним з втілень є сполука, як описано тут, де R позначає метил. 2a Одним з втілень є сполука, як описано тут, де R позначає водень. 2b Одним з втілень є сполука, як описано тут, де R позначає C1-6-алкіл. 2b Одним з втілень є сполука, як описано тут, де R позначає метил. 2b Одним з втілень є сполука, як описано тут, де R позначає водень. 2b Одним з втілень є сполука, як описано тут, де R позначає арил. 2b Одним з втілень є сполука, як описано тут, де R позначає феніл. 2a 2b Одним з втілень є сполука, як описано тут, де R та R разом з атомом вуглецю, до якого вони приєднані, утворюють гетероцикліл. 2a 2b Одним з втілень є сполука, як описано тут, де R та R разом з атомом вуглецю, до якого вони приєднані, утворюють тетрагідропіраніл. Одним з втілень є сполука, як описано тут, де X позначає -O-. Одним з втілень є сполука, як описано тут, де X позначає -S-. Одним з втілень є сполука, як описано тут, де X позначає -SO2-. 2a 2b 2a Одним з втілень є сполука, як описано тут, де p позначає 1, W позначає -CR R -, а R та 2b R обидва є воднем. 7a 7b 7a 7b Одним з втілень є сполука, як описано тут, де V позначає -CR R -, а R та R обидва є воднем. 7a 7b Одним з втілень є сполука, як описано тут, де V позначає –CR R -. 7a Одним з втілень є сполука, як описано тут, де R позначає водень. 7b Одним з втілень є сполука, як описано тут, де R позначає водень. 2a 2b Одним з втілень є сполука, як описано тут, де W позначає –CR R -. 3 Одним з втілень є сполука, як описано тут, де R позначає галоген. 3 Одним з втілень є сполука, як описано тут, де R позначає F. 4 Одним з втілень є сполука, як описано тут, де R позначає галоген. 4 Одним з втілень є сполука, як описано тут, де R позначає F. 5 Одним з втілень є сполука, як описано тут, де R позначає водень. 6 Одним з втілень є сполука, як описано тут, де R позначає водень. Одним з втілень є сполука, як описано тут, де Y позначає -NH-C=O-. Одним з втілень є сполука, як описано тут, де Z позначає гетероарил, заміщений галогеном або ціано. Одним з втілень є сполука, як описано тут, де Z позначає 2-хлорпіридиніл, 3,5-дихлорфеніл, 3,5-дихлорпіридиніл, 3-ціанофеніл, 4-хлор-1H-піразоліл, 5-хлорпіридиніл, 5-хлорпіридиніл, 5ціанопіридиніл, 5-ціанопіридиніл, 5-фторпіридиніл, 5-фторпіридиніл, 5-метоксипіридиніл, 5трифторметилпіридиніл або піримідиніл. 9 UA 111847 C2 5 10 15 20 25 30 35 40 45 50 55 60 Одним з втілень є сполука, як описано тут, де Z позначає 2-хлорпіридин-4-іл, 3,5дихлорфеніл, 3,5-дихлорпіридин-2-іл, 3-ціанофеніл, 4-хлор-1H-піразол-5-іл, 5-хлорпіридин-2-іл, 5-хлорпіридин-3-іл, 5-ціанопіридин-2-іл, 5-ціанопіридин-3-іл, 5-фторпіридин-2-іл, 5-фторпіридин3-іл, 5-метоксипіридин-3-іл, 5-трифторметилпіридин-2-іл або піримідин-5-іл. Одним з втілень є сполука, як описано тут, де Z позначає 5-ціанопіридин-2-іл, 5хлорпіридин-2-іл, 5-хлорпіридин-3-іл або 5-фторпіридин-2-іл. Одним з втілень є сполука, як описано тут, де Z позначає гетероарил. Одним з втілень є сполука, як описано тут, де Z позначає піримідиніл. Одним з втілень є сполука, як описано тут, де Z позначає гетероарил, заміщений 1-2 8 замісниками, незалежно вибраними з R . Одним з втілень є сполука, як описано тут, де Z позначає 1H-піразоліл, піридиніл або піримідиніл. Одним з втілень є сполука, як описано тут, де Z позначає 1H-піразол-5-іл, піридин-2-іл, піридин-3-іл, піридин-4-іл або піримідин-5-іл. Одним з втілень є сполука, як описано тут, де Z позначає арил. Одним з втілень є сполука, як описано тут, де Z позначає арил, заміщений 1-4 замісниками, 8 незалежно вибраними з R . Одним з втілень є сполука, як описано тут, де Z позначає феніл, заміщений 1-2 замісниками, незалежно вибраними з хлору та ціано. 8 Одним з втілень є сполука, як описано тут, де R позначає ціано. 8 Одним з втілень є сполука, як описано тут, де R позначає галоген. 8 Одним з втілень є сполука, як описано тут, де R позначає хлор. 8 Одним з втілень є сполука, як описано тут, де R позначає фтор. 8 Одним з втілень є сполука, як описано тут, де R позначає галоген-C1-6-алкіл. 8 Одним з втілень є сполука, як описано тут, де R позначає трифторметил. 8 Одним з втілень є сполука, як описано тут, де R позначає C1-6-алкокси. 8 Одним з втілень є сполука, як описано тут, де R позначає метокси. Одним з втілень є сполука, як описано тут, вибрана з групи, що складається з: (R)-7-(5-хлорпіридин-3-іл)-5',5'-дифтор-3,4,5',6'-тетрагідро-2H-спіро[нафталін-1,4'[1,3]оксазин]-2'-аміну, (2'R,4R)-6'-(5-хлорпіридин-3-іл)-5,5-дифтор-5,5'',6,6''-тетрагідро-4''H-диспіро[1,3-оксазин-4,4'хромен-2',3''-піран]-2-аміну форміату, (2RS,4R)-5',5'-дифтор-2-феніл-6-(піримідин-5-іл)-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]2'-аміну, (2RS,4R)-6-(3,5-дихлорфеніл)-5',5'-дифтор-2-феніл-5',6'-дигідроспіро[хроман-4,4'[1,3]оксазин]-2'-аміну, (2RS,4R)-6-(3,5-дихлорфеніл)-6',6'-дифтор-2-феніл-6',7'-дигідро-2'H-спіро[хроман-4,5'[1,4]оксазепін]-3'-аміну, (2RS,4R)-6-(5-хлорпіридин-3-іл)-5',5'-дифтор-2-феніл-5',6'-дигідроспіро[хроман-4,4'[1,3]оксазин]-2'-аміну, (2RS,4R)-6-(5-хлорпіридин-3-іл)-6',6'-дифтор-2-феніл-6',7'-дигідро-2'H-спіро[хроман-4,5'[1,4]оксазепін]-3'-аміну, (2RS,4R)-6',6'-дифтор-2-феніл-6-(піримідин-5-іл)-6',7'-дигідро-2'H-спіро[хроман-4,5'[1,4]оксазепін]-3'-аміну, (2'S,4R)-6'-(5-хлорпіридин-3-іл)-5,5-дифтор-5,5'',6,6''-тетрагідро-4''H-диспіро[1,3-оксазин-4,4'хромен-2',3''-піран]-2-аміну форміату, (R)-3-(2'-аміно-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-6-іл)бензонітрилу, (R)-4,4,5',5'-тетрафтор-7-(5-фторпіридин-3-іл)-3,4,5',6'-тетрагідро-2H-спіро[нафталін-1,4'[1,3]оксазин]-2'-аміну, (R)-5-(2'-аміно-4,4,5',5'-тетрафтор-3,4,5',6'-тетрагідро-2H-спіро[нафталін-1,4'-[1,3]оксазин]-7іл)нікотинонітрилу, (R)-5-(2'-аміно-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-6-іл)нікотинонітрилу, (R)-5-(2'-аміно-5',5'-дифтор-3,4,5',6'-тетрагідро-2H-спіро[нафталін-1,4'-[1,3]оксазин]-7іл)нікотинонітрилу, (R)-5',5'-дифтор-6-(5-метоксипіридин-3-іл)-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-2'аміну, (R)-5',5'-дифтор-6-(піримідин-5-іл)-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-2'-аміну, (R)-5',5'-дифтор-6-(піримідин-5-іл)-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-2'-аміну, 10 UA 111847 C2 5 10 15 20 25 30 35 40 45 50 55 60 (R)-6-(2-хлорпіридин-4-іл)-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-2'аміну, (R)-6-(3,5-дихлорфеніл)-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-2'-аміну, (R)-6-(3,5-дихлорфеніл)-5',5'-дифтор-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-2'-аміну, (R)-6-(3,5-дихлорфеніл)-6',6'-дифтор-6',7'-дигідро-2'H-спіро[хроман-4,5'-[1,4]оксазепін]-3'аміну, (R)-6-(5-хлорпіридин-3-іл)-5',5'-дифтор-2,2-диметил-5',6'-дигідроспіро[хроман-4,4'[1,3]оксазин]-2'-аміну, (R)-6-(5-хлорпіридин-3-іл)-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-2'аміну, (R)-6'-(5-хлорпіридин-3-іл)-5,5-дифтор-5,6-дигідроспіро[[1,3]оксазин-4,4'-тіохроман]-2-аміну, (R)-6-(5-хлорпіридин-3-іл)-5',5'-дифтор-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-2'-аміну, (R)-6-(5-хлорпіридин-3-іл)-6',6'-дифтор-6',7'-дигідро-2'H-спіро[хроман-4,5'-[1,4]оксазепін]-3'аміну, (R)-7-(5-хлорпіридин-3-іл)-4,4,5',5'-тетрафтор-3,4,5',6'-тетрагідро-2H-спіро[нафталін-1,4'[1,3]оксазин]-2'-аміну, (R)-N-(2'-аміно-5',5'-дифтор-2,2-диметил-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6-іл)-5хлорпіколінаміду, (R)-N-(2'-аміно-5',5'-дифтор-2,2-диметил-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6-іл)-5ціанопіколінаміду, (R)-N-(2'-аміно-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-6-іл)-5ціанопіколінаміду, (R)-N-(2'-аміно-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-6-іл)-5хлорпіколінаміду, (R)-N-(2'-аміно-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-6-іл)-5фторпіколінаміду, (R)-N-(2'-аміно-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-6-іл)-5(трифторметил)піколінаміду, (R)-N-(2'-аміно-5',5'-дифтор-3,4,5',6'-тетрагідро-2H-спіро[нафталін-1,4'-[1,3]оксазин]-7-іл)-5хлорпіколінаміду, (R)-N-(2'-аміно-5',5'-дифтор-3,4,5',6'-тетрагідро-2H-спіро[нафталін-1,4'-[1,3]оксазин]-7-іл)-5ціанопіколінаміду, (R)-N-(2'-аміно-5',5'-дифтор-4,4-диметил-3,4,5',6'-тетрагідро-2H-спіро[нафталін-1,4'[1,3]оксазин]-7-іл)-5-ціанопіколінаміду, (R)-N-(2-аміно-5,5-дифтор-5,6-дигідроспіро[[1,3]оксазин-4,4'-тіохроман]-6'-іл)-5хлорпіколінаміду, (R)-N-(2-аміно-5,5-дифтор-5,6-дигідроспіро[[1,3]оксазин-4,4'-тіохроман]-6'-іл)-5ціанопіколінаміду, (R)-N-(2'-аміно-5',5'-дифтор-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6-іл)-5хлорпіколінаміду, (R)-N-(2'-аміно-5',5'-дифтор-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6-іл)-5ціанопіколінаміду, (R)-N-(2'-аміно-5',5'-дифтор-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6-іл)-4-хлор-1Hпіразол-5-карбоксаміду, (R)-N-(3'-аміно-6',6'-дифтор-3,4,6',7'-тетрагідро-2H,2'H-спіро[нафталін-1,5'-[1,4]оксазепін]-7іл)-5-ціанопіколінаміду, (R)-N-(3'-аміно-6',6'-дифтор-3,4,6',7'-тетрагідро-2H,2'H-спіро[нафталін-1,5'-[1,4]оксазепін]-7іл)-5-хлорпіколінаміду, (R)-N-(3'-аміно-6',6'-дифтор-6',7'-дигідро-2'H-спіро[хроман-4,5'-[1,4]оксазепін]-6-іл)-5ціанопіколінаміду, (R)-N-(3'-аміно-6',6'-дифтор-6',7'-дигідро-2'H-спіро[хроман-4,5'-[1,4]оксазепін]-6-іл)-5хлорпіколінаміду, (R)-N-(3'-аміно-6',6'-дифтор-6',7'-дигідро-2'H-спіро[хроман-4,5'-[1,4]оксазепін]-6-іл)-3,5дихлорпіколінаміду, 3-((2RS,4R)-2'-аміно-5',5'-дифтор-2-феніл-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6іл)бензонітрилу, 3-((2RS,4R)-3'-аміно-6',6'-дифтор-2-феніл-6',7'-дигідро-2'H-спіро[хроман-4,5'-[1,4]оксазепін]-6іл)бензонітрилу, 3-[(2'R,4R)-2-аміно-5,5-дифтор-5,5'',6,6''-тетрагідро-4''H-диспіро[1,3-оксазин-4,4'-хромен-2',3''піран]-6'-іл]бензонітрилу форміату, 11 UA 111847 C2 5 10 15 20 25 30 5-((2RS,4R)-2'-аміно-5',5'-дифтор-2-феніл-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6іл)нікотинонітрилу, 5-((2RS,4R)-3'-аміно-6',6'-дифтор-2-феніл-6',7'-дигідро-2'H-спіро[хроман-4,5'-[1,4]оксазепін]-6іл)нікотинонітрилу, N-((2R або 2S,4R)-2'-аміно-5',5'-дифтор-2-феніл-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6іл)-5-хлорпіколінаміду, N-((2R або 2S,4R)-2'-аміно-5',5'-дифтор-2-феніл-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6іл)-5-ціанопіколінаміду, N-((2R або 2S,4R)-2'-аміно-5',5'-дифтор-2-феніл-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6іл)-5-фторпіколінаміду, N-((2R або 2S,4R)-2'-аміно-5',5'-дифтор-2-феніл-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-6іл)-5-(трифторметил)піколінаміду, N-((2RS,4R)-3'-аміно-6',6'-дифтор-2-феніл-6',7'-дигідро-2'H-спіро[хроман-4,5'-[1,4]оксазепін]6-іл)-5-(трифторметил)піколінаміду, N-((2RS,4R)-3'-аміно-6',6'-дифтор-2-феніл-6',7'-дигідро-2'H-спіро[хроман-4,5'-[1,4]оксазепін]6-іл)-5-ціанопіколінаміду, N-[(2'R,4R)-2-аміно-5,5-дифтор-5,5'',6,6''-тетрагідро-4''H-диспіро[1,3-оксазин-4,4'-хромен2',3''-піран]-6'-іл]-5-ціанопіридин-2-карбоксаміду, N-[(4R)-2-аміно-5,5-дифтор-1',1'-діоксидо-2',3',5,6-тетрагідроспіро[1,3-оксазин-4,4'тіохромен]-6'-іл]-5-хлорпіридин-2-карбоксаміду, і N-[(4R)-2-аміно-5,5-дифтор-1',1'-діоксидо-2',3',5,6-тетрагідроспіро[1,3-оксазин-4,4'тіохромен]-6'-іл]-5-ціанопіридин-2-карбоксаміду, або її фармацевтично прийнятні солі. Одним з втілень є сполука, описана тут, вибрана з групи, що складається з: (R)-N-(2'-аміно-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-6-іл)-5ціанопіколінаміду, (R)-6-(5-хлорпіридин-3-іл)-5',5'-дифтор-5',6'-дигідроспіро[хроман-4,4'-[1,3]оксазин]-2'-аміну, (R)-N-(2'-аміно-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-6-іл)-5хлорпіколінаміду, і (R)-N-(2'-аміно-5',5'-дифтор-2,3,5',6'-тетрагідроспіро[інден-1,4'-[1,3]оксазин]-6-іл)-5фторпіколінаміду, або її фармацевтично прийнятні солі. В одному з втілень даного винаходу запропонований спосіб, описаний нижче: V 6 R O n H2N V 5 H2N R R Z-COOH 3 R X 45 3 R m W p X I' W p I 1 40 4 R N Y Z 35 5 R 4 N H2N 6 R O n 2 3 4 5 , 6 де V, W, Y, Z, n, p, R , R , R , R , R та R є такими, як описано тут, і m позначає 1. В одному з втілень даного винаходу запропонована сполука формули I, як описано одержана способом, визначеним вище. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, застосування як терапевтично активна речовина. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, застосування як інгібітор активності BACE1 та/або BACE2. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, застосування як інгібітор активності BACE1. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, застосування як інгібітор активності BACE2. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, 12 тут, для для для для для UA 111847 C2 5 10 15 20 25 30 35 40 45 50 55 60 застосування як інгібітор активності BACE1 та BACE2. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, для застосування як терапевтично активна речовина при терапевтичному та/або профілактичному лікуванні захворювань та порушень, які характеризуються підвищеними рівнями β-амілоїду та/або олігомерів β-амілоїду та/або β-амілоїдних бляшок та подальших відкладень або хвороби Альцгеймера. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, для застосування як терапевтично активна речовина при терапевтичному та/або профілактичному лікуванні хвороби Альцгеймера. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, для застосування як терапевтично активна речовина при терапевтичному та/або профілактичному лікуванні діабету або діабету 2 типу. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, для застосування як терапевтично активна речовина при терапевтичному та/або профілактичному лікуванні діабету. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, для застосування як терапевтично активна речовина при терапевтичному та/або профілактичному лікуванні діабету або діабету 2 типу. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, для застосування як терапевтично активна речовина при терапевтичному та/або профілактичному лікуванні хвороби Альцгеймера, діабету або діабету 2 типу. В одному з втілень даного винаходу запропонована фармацевтична композиція, що містить сполуку формули I, як описано тут, та фармацевтично прийнятний носій та/або фармацевтично прийнятна допоміжна речовина. В одному з втілень даного винаходу запропоноване застосування сполуки формули I, як описано тут, при виготовленні лікарського засобу для застосування при інгібуванні активності BACE1 та/або BACE2. В одному з втілень даного винаходу запропоноване застосування сполуки формули I, як описано тут, при виготовленні лікарського засобу для застосування при інгібуванні активності BACE1. В одному з втілень даного винаходу запропоноване застосування сполуки формули I, як описано тут, при виготовленні лікарського засобу для застосування при інгібуванні активності BACE2. В одному з втілень даного винаходу запропоноване застосування сполуки формули I, як описано тут, при виготовленні лікарського засобу для застосування при інгібуванні активності BACE1 та BACE2. В одному з втілень даного винаходу запропоноване застосування сполуки формули I, як описано тут, при виготовленні лікарського засобу для терапевтичного або профілактичного лікування захворювань та порушень, які характеризуються підвищеними рівнями β-амілоїду та/або β-амілоїдних олігомерів та/або β-амілоїдних бляшок та подальших відкладень або хвороби Альцгеймера. В одному з втілень даного винаходу запропоноване застосування сполуки формули I, як описано тут, при виготовленні лікарського засобу для терапевтичного або профілактичного лікування хвороби Альцгеймера. В одному з втілень даного винаходу запропоноване застосування сполуки формули I, як описано тут, при виготовленні лікарського засобу для терапевтичного або профілактичного лікування діабету або діабету 2 типу. В одному з втілень даного винаходу запропоноване застосування сполуки формули I, як описано тут, при виготовленні лікарського засобу для терапевтичного або профілактичного лікування діабету. В одному з втілень даного винаходу запропоноване застосування сполуки формули I, як описано тут, при виготовленні лікарського засобу для терапевтичного або профілактичного лікування діабету або діабету 2 типу. В одному з втілень даного винаходу запропоноване застосування сполуки формули I, як описано тут, при виготовленні лікарського засобу для терапевтичного або профілактичного лікування хвороби Альцгеймера, діабету або діабету 2 типу. В одному з втілень даного винаходу запропоноване застосування сполуки формули I, як описано тут, при виготовленні лікарського засобу для терапевтичного або профілактичного лікування хвороби Альцгеймера. В одному з втілень даного винаходу запропоноване застосування сполуки формули I, як 13 UA 111847 C2 5 10 15 20 25 30 35 40 45 50 55 описано тут, при виготовленні лікарського засобу для терапевтичного або профілактичного лікування діабету або діабету 2 типу. В одному з втілень даного винаходу запропоноване застосування сполуки формули I, як описано тут, при виготовленні лікарського засобу для терапевтичного або профілактичного лікування діабету. В одному з втілень даного винаходу запропоноване застосування сполуки формули I, як описано тут, при виготовленні лікарського засобу для терапевтичного або профілактичного лікування діабету 2 типу. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, для застосування при інгібуванні активності BACE1 та/або BACE2. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, для застосування при інгібуванні активності BACE1. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, для застосування при інгібуванні активності BACE2. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, для застосування при інгібуванні активності BACE1 та BACE2. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, для застосування при терапевтичному та/або профілактичному лікуванні захворювань та порушень, які характеризуються підвищеними рівнями β-амілоїду та/або β-амілоїдних олігомерів та/або βамілоїдних бляшок та подальших відкладень або хвороби Альцгеймера. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, для застосування при терапевтичному та/або профілактичному лікуванні хвороби Альцгеймера. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, для застосування при терапевтичному та/або профілактичному лікуванні діабету або діабету 2 типу. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, для застосування при терапевтичному та/або профілактичному лікуванні діабету. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, для застосування при терапевтичному та/або профілактичному лікуванні діабету або діабету 2 типу. В одному з втілень даного винаходу запропонована сполука формули I, як описано тут, для застосування при терапевтичному та/або профілактичному лікуванні хвороби Альцгеймера, діабету або діабету 2 типу. В одному з втілень даного винаходу запропонований спосіб застосування при інгібуванні активності BACE1 та/або BACE2, зокрема при терапевтичному або профілактичному лікуванні захворювань та порушень, які характеризуються підвищеними рівнями β-амілоїду та/або βамілоїдних олігомерів та/або β-амілоїдних бляшок та подальших відкладень, хвороби Альцгеймера, діабету або діабету 2 типу, при цьому спосіб включає введення сполуки формули I, як описано тут, людині або тварині. В одному з втілень даного винаходу запропонований спосіб застосування при терапевтичному та/або профілактичному лікуванні хвороби Альцгеймера, діабету або діабету 2 типу, при цьому спосіб включає введення сполуки формули I, як описано тут, людині або тварині. В одному з втілень даного винаходу запропонований спосіб застосування при терапевтичному та/або профілактичному лікуванні хвороби Альцгеймера, при цьому спосіб включає введення сполуки формули I, як описано тут, людині або тварині. В одному з втілень даного винаходу запропонований спосіб застосування при терапевтичному та/або профілактичному лікуванні діабету, при цьому спосіб включає введення сполуки формули I, як описано тут, людині або тварині. В одному з втілень даного винаходу запропонований спосіб застосування при терапевтичному та/або профілактичному лікуванні діабету 2 типу, при цьому спосіб включає введення сполуки формули I, як описано тут, людині або тварині. Крім того, винахід включає усі оптичні ізомери сполук формули I, тобто діастереоізомери, діастереомерні суміші, рацемічні суміші, усі їх відповідні енантіомери та/або таутомери, а також їх сольвати. Кваліфікований в рівні техніки фахівець зрозуміє, що сполуки формули I можуть існувати в таутомерній формі, наприклад, в такій таутомерній формі: 14 UA 111847 C2 V HN 4 R HN 3 R m X 5 10 15 20 5 R Y Z 6 R O n W p Id. Усі таутомерні форми включені до обсягу даного винаходу. Сполуки формули I можуть містити один чи декілька асиметричних центрів і, отже, можуть існувати у вигляді рацематів, рацемічних сумішей, окремих енантіомерів, діастереомерних сумішей та індивідуальних діастереомерів. В залежності від природи різних замісників в молекулі можуть бути присутніми додаткові асиметричні центри. Кожен такий асиметричний центр буде незалежно давати два оптичних ізомери, і вважається, що усі можливі оптичні ізомери та діастереомери в сумішах та у вигляді чистих або частково очищених сполук включені до обсягу даного винаходу. Даний винахід охоплює усі такі ізомерні форми цих сполук. Незалежні синтези цих діастереомерів або їх хроматографічне розділення можуть бути здійснені, як відомо в даній галузі техніки, шляхом відповідної модифікації методики, розкритої в даному описі. Їх абсолютна стереохімія може бути визначена за допомогою рентгенівської кристалографії кристалічних продуктів або кристалічних проміжних сполук, які, при необхідності, піддають дериватизації з реагентом, що містить асиметричний центр відомої абсолютної конфигурації. При необхідності, рацемічні суміші сполук можуть бути розділені з виділенням індивідуальних енантіомерів. Розділення може бути здійснене способами, добре відомими в даній галузі, такими як зв’язування рацемічної суміші сполук з енантіомерно чистою сполукою з утворенням діастереомерної суміші, з подальшим розділенням індивідуальних діастереомерів стандартними способами, такими як фракційна кристалізація або хроматографія. Конкретним прикладом ізомеру сполуки формули I є сполука формули Ia, де радикали мають значення, описані в будь-якому з варіантів здійснення. V H2N 5 R 4 R N Y Z 6 R O n 3 R m X W p Ia 25 30 35 40 У варіантах здійснення, де запропоновані оптично чисті енантіомери, оптично чистий енантіомер означає, що сполука містить >90% по масі бажаного ізомеру, зокрема >95% бажаного ізомеру по масі або, більш конкретно, >99% бажаного ізомеру по масі, зазначений масовий процент оснований на загальній вазі ізомеру (ізомерів) сполуки. Хірально чисті або хірально збагачені сполуки можуть бути одержані шляхом хірально селективного синтезу або шляхом розділення енантіомерів. Розділення енантіомерів може бути здійснене із кінцевого продукту або, альтернативно, із придатного проміжного продукту. Сполуки формули I можуть бути одержані згідно з такими схемами. Вихідні речовини є комерційно доступними або можуть бути одержані згідно з відомими способами. Будь-які раніше визначені радикали та змінні будуть й далі мати раніше визначені значення, якщо не зазначене інше. 1a 1b 1a 1b Сульфініліміни загальної формули A2, де X позначає -CR R (R , R є воднем, нижчим 2a 2b 2a 2b алкілом або фтором) та W позначає –CR R (p = 1, R , R є воднем), можуть бути одержані за аналогією з T.P. Tang & J.A. Ellman, J. Org. Chem. 1999, 64, 12, шляхом конденсації арилкетону A1 та сульфінаміду, наприклад, алкілсульфінаміду, більш конкретно, (R)-(+)-трет 15 UA 111847 C2 5 10 15 20 25 бутилсульфінаміду, в присутності кислоти Льюїса, такої як, наприклад, алкоксид титану(IV), більш конкретно, етоксид титану(IV) в розчиннику, такому як ефір, наприклад, діетиловий ефір чи, більш конкретно, тетрагідрофуран. Конверсія сульфініліміну A2 на ефір сульфінаміду A3 відбувається стереоселективно за допомогою хіральної напрямної замінної групи, як описано у Tang & Ellman. Сульфінілімін A2 може взаємодіяти в реакції Реформатського з енолятом цинку, одержаним з, наприклад, алкілбромдифторацетату, зокрема етилбромдифторацетату, та активованого цинкового порошку при температурі від кімнатної до підвищеної, зокрема при температурі від 23 до 60 °C в розчиннику, такому як ефір, наприклад, діетиловий ефір або, ще краще, тетрагідрофуран. Спирт формули A4 може бути одержаний відновленням етилового ефіру формули A3 з лужним гідридом, зокрема борогідридом літію або алюмогідридом літію, в розчиннику, такому як ефір, наприклад, діетиловий ефір або, ще краще, тетрагідрофуран. Гідроліз хіральної напрямної замінної групи в сульфінамідному спирті формули A4 з одержанням аміноспирту формули A5 може бути проведений з мінеральною кислотою, наприклад, сірчаною кислотою або, зокрема, соляною кислотою, в розчиннику, такому як ефір, наприклад, діетиловий ефір, тетрагідрофуран або, ще краще, 1,4-діоксан. Амінооксазин формули A6 може бути одержаний взаємодією аміноспирту формули A5 з бромціаном в розчиннику, такому як спирт, зокрема етанол. Відновлення похідних формули A6, де Q позначає нітрогрупу, з одержанням анілінів формули A7, може бути проведене шляхом гідрогенізації з використанням каталізатора, такого як паладій на вугіллі, в протонних розчинниках, таких як спирти, зокрема етанол або метанол. Схема A: Синтези сполук формул I.1 та I.2. Цільові аміни формули I.1 можуть бути одержані шляхом каталізованого паладієм кросa a зв’язування між сполуками формули A6 та похідними формули Z-R , де R є бороновою 16 UA 111847 C2 5 10 15 20 25 30 35 40 кислотою або ефіром, в умовах крос-сполучення Сузукі-Міяури, відомих кваліфікованим фахівцям. Цільові аміди формули I.2 можуть бути одержані шляхом селективного зв’язування анілінів формули A7 та карбонової кислоти формули Z-COOH з 4-(4,6-диметокси[1,3,5]триазин-2-іл)-4метилморфоліну хлориду гідратом (DMTMM) як конденсуючого агента в розчиннику, такому як метанол. Інший звичайний спосіб одержання анілінів формули A7 через N-захищені проміжні сполуки показаний на Схемі A.1. Захист аміногрупи у сполуках формули A6, де Q позначає бром, з одержанням арилбромідів формули A6.1, може бути виконаний за допомогою триарилметилхлоридів, таких як трифенілметилхлорид (Tr-Cl), п-метоксифенілдифенілметилхлорид (MMTr-Cl), ди-(пметоксифеніл)фенілметилхлорид (DMTr-Cl) або три-(п-метоксифеніл)метилхлорид (TMTr-Cl), зокрема DMTr-Cl, в лужних умовах, наприклад, в присутності аміну, такого як триетиламін або діізопропілетиламін, в хлорованому розчиннику, такому як дихлорметан або хлороформ, при температурах між 0 °C та кімнатною температурою. Арилброміди формули A6.1 можуть взаємодіяти з еквівалентами аміаку, такими як бензофенонімін, в присутності придатного каталізатора на основі перехідного металу, такого як біс(дибензиліденацетон)паладій(0) ((dba)2Pd) або трис(дибензиліденацетон)дипаладій(0) [(dba)3Pd2], та придатного ліганду, такого як рац-2,2'-біс(дифенілфосфіно)-1,1'-бінафтил (racBINAP), 2-біциклогексилфосфіно-2',4',6'-триізопропілбіфеніл (X-PHOS) або 2-ди-третбутилфосфіно-2',4',6'-триізопропілбіфеніл (t-Bu X-PHOS), в присутності основи, такої як третбутоксид натрію, фосфат калію або карбонат цезію, в придатному розчиннику, такому як толуол або 1,4-діоксан, в інертній атмосфері, такій як азотна чи аргонова, при температурах між 80 та 110 °C, з одержанням сполук формули A6.2. Депротекція обох аміногруп у сполуках формули A6.2 може здійснюватися за допомогою однореакторної процедури шляхом їх взаємодії спочатку із сильною органічною кислотою, такою як трифтороцтова кислота, в хлорованих розчинниках, таких як дихлорметан чи хлороформ, в безводних умовах при температурах між 0 °C та кімнатною температурою для відщеплення групи P1. Потім додавання води для розщеплення бензофеноніміну та взаємодія при кімнатній температурі приводить до діамінів формули A7. Схема A.1: Альтернативний синтез проміжних сполук анілінів формули A7. 2a 2b Сульфініліміни загальної формули B2, де X позначає O або S, і W позначає -CR R (p = 1, 2a 2b R , R є воднем, нижчим алкілом, фенілом або, узяті разом з атомом вуглецю, до якого вони приєднані, утворюють гетероцикліл), можуть утворювати гетероциклоалкіл), можуть бути одержані за аналогією з T.P. Tang & J.A. Ellman, J. Org. Chem. 1999, 64, 12, шляхом конденсації арилкетону B1 та сульфінаміду, наприклад, алкілсульфінаміду, більш конкретно, (R)-(+)-третбутилсульфінаміду, в присутності кислоти Льюїса, такої як, наприклад, алкоксид титану(IV), більш конкретно, етоксид титану(IV), в розчиннику, такому як ефір, наприклад, діетиловий ефір 17 UA 111847 C2 5 10 15 або, ще краще, тетрагідрофуран. Конверсія сульфініліміну B2 на сульфінамідний ефір B3 проводиться стереоселективно з використанням хіральної напрямної замінної групи, як описано у Tang & Ellman. Сульфінілімін B2 може взаємодіяти в реакції Реформатського з енолятом цинку, одержаним з, наприклад, алкілбромдифторацетату, зокрема етилбромдифторацетату, та активованого порошку цинку при температурі від кімнатної до підвищеної, зокрема від 23 до 60 °C, в розчиннику, такому як ефір, наприклад, діетиловий ефір або, ще краще, тетрагідрофуран. Спирт формули B4 може бути одержаний відновленням етилового ефіру формули B3 з лужним гідридом, зокрема борогідридом літію або алюмогідридом літію, в розчиннику, такому як ефір, наприклад, діетиловий ефір або, ще краще, тетрагідрофуран. Гідроліз хіральної напрямної замінної групи в сульфінамідному спирті формули B4 з одержанням аміноспирту формули B5 може бути проведений мінеральною кислотою, наприклад, сірчаною кислотою або, зокрема, соляною кислотою, в розчиннику, такому як ефір, наприклад, діетиловий ефір, тетрагідрофуран або, ще краще, 1,4-діоксан. Амінооксазин формули B6 може бути одержаний взаємодією аміноспирту формули B5 з бромціаном в розчиннику, такому як спирт, зокрема етанол. Відновлення похідних формули B6, де Q позначає нітрогрупу, з одержанням анілінів формули B7 може бути проведене гідруванням з використанням каталізатора, такого як паладій на вугіллі, в протонних розчинниках, таких як спирти, зокрема етанол або метанол. 20 25 Схема B: Синтези сполук формул I.3 та I.4. Цільові аміни формули I.3 можуть бути одержані шляхом каталізованого паладієм кросa a зв’язування між сполуками формули B6 та похідними формули Z-R , де R є бороновою кислотою або ефіром в умовах крос-сполучення Сузукі-Міяури, відомих кваліфікованому фахівцю. Цільові аміди формули I.4 можуть бути одержані селективним зв’язуванням анілінів 18 UA 111847 C2 5 10 15 20 25 30 35 формули B7 та карбонової кислоти формули Z-COOH з 4-(4,6-диметокси[1,3,5]триазин-2-іл)-4метилморфоліну хлориду гідратом (DMTMM) як конденсуючим агентом в розчиннику, такому як метанол. Цільові аміди формули I.3 або I.4, де X позначає SO 2, можуть бути одержані із сполук формули I.3 або I.4, де X позначає S, шляхом окиснення в інертному розчиннику при температурах між 0 °C та кімнатною температурою з використанням, наприклад, пероксомоносульфату калію як окисного агента. Альтернативно, аніліни формули B7 можуть бути одержані через N-захищені проміжні сполуки, як показано на Схемі B.1. Захист аміногрупи у сполуках формули A6, де Q позначає бром, з одержанням арилбромідів формули B6.1 може бути виконаний за допомогою триарилметилхлоридів, таких як трифенілметилхлорид (Tr-Cl), п-метоксифенілдифенілметилхлорид (MMTr-Cl), ди-(пметоксифеніл)фенілметилхлорид (DMTr-Cl) або три-(п-метоксифеніл)метилхлорид (TMTr-Cl), зокрема DMTr-Cl, в лужних умовах, наприклад, в присутності аміну, такого як триетиламін або діізопропілетиламін, в хлорованому розчиннику, такому як дихлорметан або хлороформ, при температурах між 0 °C та кімнатною температурою. Арилброміди формули B6.1 можуть взаємодіяти з еквівалентами аміаку, такими як бензофенонімін, в присутності придатного каталізатора на основі перехідного металу, такого як біс(дибензиліденацетон)паладій(0) ((dba)2Pd) або трис(дибензиліденацетон)дипаладій(0) [(dba)3Pd2], та придатного ліганду, такого як рац-2,2'-біс(дифенілфосфіно)-1,1'-бінафтил (racBINAP), 2-біциклогексилфосфіно-2',4',6'-триізопропілбіфеніл (X-PHOS) або 2-ди-третбутилфосфіно-2',4',6'-триізопропілбіфеніл (t-Bu X-PHOS), в присутності основи, такої як третбутоксид натрію, фосфат калію або карбонат цезію, в придатному розчиннику, такому як толуол або 1,4-діоксан, в інертній атмосфері, такій як азотна чи аргонова, при температурах між 80 та 110 °C, з одержанням сполук формули B6.2. Депротекція обох аміногруп у сполуках формули B6.2 може виконуватися за допомогою однореакторної процедури шляхом їх мвзаємодії спочатку з сильною органічною кислотою, такою як трифтороцтова кислота, в хлорованих розчинниках, таких як дихлорметан або хлороформ, в безводних умовах при температурах між 0 °C та кімнатною температурою, для 1 відщеплення групи P . Потім додавання води для розщеплення бензофеноніміну та взаємодія при кімнатній температурі приводить до діамінів формули B7. Схема B.1: Альтернативний синтез проміжних сполук анілінів формули B7. Алкілування спиртів формули A4 або B4 до нітрилів формули C1 може бути виконане з придатною слабкою основою, зокрема оксидом срібла(I) в розчиннику, такому як тетрагідрофуран або дихлорметан, ще краще, дихлорметан, в присутності алкілуючого 19 UA 111847 C2 5 10 15 каталізатора, такого як тетрабутиламонію йодид. Гідроліз хіральної напрямної замінної групи в нітрилах формули C1 з одержанням амінонітрилів формули C2 може бути проведений за допомогою мінеральної кислоти, наприклад, сірчаної кислоти і, зокрема, соляної кислоти в розчиннику, такому як ефір, наприклад, діетиловий ефір чи, краще, 1,4-діоксан. Амінооксазепіни формули C3 можуть бути одержані взаємодією амінонітрилів формули C2 та триметилалюмінію в розчиннику, такому як ксилол або толуол, зокрема толуол. Відновлення похідних формули C3, де Q позначає нітрогрупу, з одержанням анілінів формули C4, може бути проведене гідрогенізацією з використанням каталізатора, такого як паладій на вугіллі, в протонних розчинниках, таких як спирти, зокрема етанол або метанол. Схема C: Синтези сполук формул I.5 та I.6. Цільові аміни формули I.5 можуть бути одержані шляхом каталізованого паладієм кросa a зв’язування між сполуками формули C3 та похідними формули Z-R , де R позначає боронову 20 UA 111847 C2 5 10 15 20 25 30 35 40 45 50 55 60 кислоту або ефір, в умовах крос-сполучення Сузукі-Міяури, відомих кваліфікованому фахівцю. Цільові аміди формули I.6 можуть бути одержані селективним зв’язуванням анілінів формули C4 та карбонової кислоти формули Z-COOH з 4-(4,6-диметокси[1,3,5]триазин-2-іл)-4метилморфоліну хлориду гідратом (DMTMM) як конденсуючим агентом в розчиннику, такому як метанол. Відповідні фармацевтично прийнятні солі з кислотами можуть бути одержані стандартними способами, відомими фахівцю в даній галузі, наприклад, шляхом розчинення сполуки формули I в придатному розчиннику, таких як, наприклад, діоксан або тетрагідрофуран (ТГФ), та додавання придатної кількості відповідної кислоти. Продукти, як правило, можуть бути виділені фільтруванням, або за допомогою хроматографії. Конверсію сполуки формули I на фармацевтично прийнятну сіль з основою можна проводити шляхом обробки такої сполуки такою основою. Одним з можливих способів утворення такої солі є, наприклад, додавання 1/n еквівалентів основної солі, такої як, наприклад, M(OH) n, де М = катіон металу або амонію, і n = кількість гідроксид-аніонів, до розчину сполуки в придатному розчиннику (наприклад, етанол, суміш етанол-вода, суміш тетрагідрофуран-вода) та видалення розчинника шляхом випарювання або ліофілізації. Конкретними солями є гідрохлорид, форміат та трифторацетат. В тому ступені, в якому їх одержання не описане у прикладах, сполуки формули I, а також усі проміжні продукти можуть бути одержані згідно з аналогічними способами, або згідно зі способами, викладеними в даному документі. Вихідні матеріали є комерційно доступними, відомими в даній галузі або можуть бути одержані способами, відомими в даній галузі, чи за аналогією з ними. Слід розуміти, що сполуки загальної формули I за даним винаходом можуть бути дериватизовані по функціональних групах з утворенням похідних, здатних до зворотного перетворення на вихідну сполуку in vivo. Фармакологічні тести Сполуки формули I та їх фармацевтично прийнятні солі мають цінні фармакологічні властивості. Було знайдено, що сполуки за даним винаходом асоційовані з інгібуванням активності BACE1 та/або BACE2. Сполуки досліджували згідно з тестом, наведеним далі. Аналіз клітинного зниження Aβ: a) Клітини людини HEK293, які були стабільно трансфековані вектором, експресуючим cDNA гена APP дикого типу людини (APP695), використовували для визначення ефективності сполук в клітинному аналізі. Клітини засіяли на 96-лункові мікропланшети в клітинне середовище для культивування (середовище Іскова плюс 10% (об./об.) фетальної бичачої сироватки, глутамін, пеніцилін/стрептоміцин) до приблизно 80% конфлюентності та додали сполуки при 10× концентрації в 1/10 об’єму середовища без FCS, що містить 8% ДМСО (кінцева концентрація ДМСО зберігалася рівною 0,8% об./об.). Через 18-20 годин інкубації при 37 °C та 5% CO2 в зволожуваному інкубаторі культуральний супернатант зібрали для визначення концентрації Aβ40. 96-лункові ELISA планшети (наприклад, Nunc MaxiSorb) покрили моноклональними антитілами, які специфічно розпізнають C-кінець пептиду Aβ40 (Brockhaus та співавт., NeuroReport 9, 1481-1486; 1998). Після блокування сайтів неспецифічного зв’язування за допомогою, наприклад, 1% БСА, та промивання, культуральні супернатанти в придатному розведенні додавали до антитіл детекції Aβ, зв’язаних з пероксидазою хрону (наприклад, антитіло 4G8, Senetek, Maryland Heights, MO) та інкубували протягом 5-7 годин. Потім лунки мікропланшету інтенсивно промили ТРИС-буферизованим фізрозчином, що містить 0,05% Tween 20 та аналіз проявили тетраметилбензидином/H 2O2 в лимоннокислому буфері. Після зупинення реакції одним об’ємом 1 н. H2SO4 реакційну суміш вимірювали на ELISA ридері на довжині хвилі 450 нм. Концентрації Aβ в культуральних супернатантах обчислювали на основі стандартної кривої, одержаної з використанням відомих кількостей чистого Aβ пептиду. b) Альтернативно, можна використовувати аналіз Aβ40 AlphaLISA. Клітини HEK293 APP засіяли в 96-лункові мікропланшети в клітинне середовище для культивування (середовище Іскова плюс 10% (об./об.) фетальної бичачої сироватки, глутамін, пеніцилін/стрептоміцин) до приблизно 80% конфлюентності та додали сполуки при 3× концентрації в 1/3 об’єму культурального середовища (кінцева концентрація ДМСО зберігалася рівною 1 % об./об.). Через 18-20 годин інкубації при 37 °C та 5% CO2 в зволожуваному інкубаторі культуральний супернатант зібрали для визначення концентрації Aβ40 за допомогою набору Perkin-Elmer Human Amyloid beta 1-40 (високоспецифічний) (Cat# AL275C). В планшетах Perkin-Elmer White Optiplate-384 (Cat# 6007290) об’єднали 2 мкл культуральних супернатантів з 2 мкл суміші 10× AlphaLISA Anti-hAβ акцепторних бусин + біотиніловане антитіло Anti-Aβ 1-40 (50 мкг/мл / 5 нМ). Через 1 годину інкубації при кімнатній температурі додали 16 мкл 1,25× препарату донорні бусини-стрептавідин (SA) (25 мкг/ мл) та інкубували 30 21 UA 111847 C2 5 10 15 20 хв. в темряві. Емісію світла при 615 нм потім записували з використанням ридера EnVisionAlpha Reader. Рівні Aβ 40 в культуральних супернатантах обчислювалися як процент від максимального сигналу (клітини, оброблені 1% ДМСО без інгібітора). Значення IC50 обчислювали з використанням програмного забезпечення Excel XLfit. Аналіз інгібування BACE шляхом вимірювання розщеплення клітинного TMEM27: Аналіз використовує принцип інгібування розщеплення TMEM27 людини ендогенним клітинним BACE2 в клітинній лінії Ins1e щура та відокремлення від клітинної поверхні в культуральне середовище, з подальшою детекцією в аналізі ELISA. Інгібування BACE2 запобігає розщепленню та відокремленню у дозазалежний спосіб. Стабільна клітинна лінію “INS-TMEM27” є одержаною з INS1e клітинною лінією з індукованою експресією (з використанням системи TetOn) повнорозмірного hTMEM27 у доксициклін-залежний спосіб. Клітини протягом експерименту культивувалися в середовищі RPMI1640 + Glutamax (Invitrogen) пеніцилін/стрептоміцин, 10% фетальної бичачої сироватки, 100 мМ пірувату, 5 мМ бета-меркаптоетанолу, 100 мкг/мл G418 та 100 мкг/мл гігроміцину, і росли в прикріпленій культурі при 37 °C в звичайному клітинному CO2 інкубаторі. Клітини INS-TMEM27 засівали в 96-лункові планшети. Через 2 дні культивування додавали інгібітор BACE2 в діапазоні концентрацій, необхідних для аналізу та після ще 2 годин додали доксициклін до кінцевої концентрації 500 нг/мл. Клітини інкубували протягом додаткових 46 годин та зібрали супернатант для детекції відокремленого TMEM27. Аналіз ELISA (з використанням пари мишачих антитіл проти людського TMEM27, спрямованих проти позаклітинного домену TMEM27) використовували для детекції TMEM27 в культуральному середовищі. Значення EC50 для інгібування BACE2 обчислювали з використанням даних ELISA для кожної концентрації інгібітора та стандартного програмного забезпечення для апроксимації кривих, такого як XLFit для програми Excel. 25 Таблиця 1: a) b) Значення IC50 вибраних прикладів, та позначають, відповідно, використовуваний тип клітинного аналізу Приклад N 1 H2 N F F H2 N 0,080 F F 2,550 a) 0,543 a) 0,526 a) O N NC H2N O N 3 0,100 F F Cl N BACE2 кліт. акт. IC50, [мкМ] O N N 2 BACE1 кліт. акт. Aβ40 IC50, [мкМ] Структура Cl F F 22 UA 111847 C2 Таблиця 1: a) b) Значення IC50 вибраних прикладів, та позначають, відповідно, використовуваний тип клітинного аналізу Приклад N H2N F F F F H2N N H2N 7 Cl a) 2,730 a) F F N H2N 3,580 2,450 O N Cl 2,370 O Cl 9 a) F F H2N 8 N O N Cl a) 1,360 O N N F N H2N a) 2,770 F F NC N F F F 6 a) 5,690 F O N 5 BACE2 кліт. акт. IC50, [мкМ] O N 4 BACE1 кліт. акт. Aβ40 IC50, [мкМ] Структура F F 0,790 23 UA 111847 C2 Таблиця 1: a) b) Значення IC50 вибраних прикладів, та позначають, відповідно, використовуваний тип клітинного аналізу Приклад H2N 10 F F H2N NC H2N H N 12 3,380 a) b) a) a) 0,116 a) 13,034 a) a) O N N 0,960 F F NC Cl BACE2 кліт. акт. IC50, [мкМ] O N N 11 BACE1 кліт. акт. Aβ40 IC50, [мкМ] Структура O F F N 0,022 O NC H2N N H N 13 O F F 0,005 F F 1,110 F F N 0,510 O NC H2N N H N 14 O N O NC H2N N H N 15 O N O Cl H2N N H N 16 O F F N O 24 2,490 UA 111847 C2 Таблиця 1: a) b) Значення IC50 вибраних прикладів, та позначають, відповідно, використовуваний тип клітинного аналізу Приклад BACE1 кліт. акт. Aβ40 IC50, [мкМ] Структура H2N F3 C N H N 18 BACE2 кліт. акт. IC50, [мкМ] O F F N a) a) 0,124 a) 3,995 a) a) 0,926 a) 0,660 O H2N N 19 O F F Cl 0,380 F F N 2,020 O Cl H2N O N 20 Cl O H2N N 21 O F F N N N O H2N 5,140 O F F N 22 MeO 2,780 O N H2N O F F N 23 Cl 0,420 O 25 UA 111847 C2 Таблиця 1: a) b) Значення IC50 вибраних прикладів, та позначають, відповідно, використовуваний тип клітинного аналізу Приклад H2 N N BACE2 кліт. акт. IC50, [мкМ] O F F N 24 BACE1 кліт. акт. Aβ40 IC50, [мкМ] Структура NC a) a) a) a) a) 0,098 O H2N N O F F N N 25 1,580 O Cl H2N O F F N 26 Cl 2,868 O H2 N O F F N 27 NC 0,260 O N H2N O F F N 28 Cl 2,530 O 26 UA 111847 C2 Таблиця 1: a) b) Значення IC50 вибраних прикладів, та позначають, відповідно, використовуваний тип клітинного аналізу Приклад H2N N F F Cl H2N NC H2N H2N F F S H2N H N H N 34 O F F N a) 1,924 0,360 O O H2N N 0,986 0,676 O O NC a) O Cl 33 1,947 9,000 O N N a) F F Cl Cl b) O O 32 6,580 O N N b) F F O 31 O N N b) 4,430 O O 30 BACE2 кліт. акт. IC50, [мкМ] O N 29 BACE1 кліт. акт. Aβ40 IC50, [мкМ] Структура F F N O 27 0,080 UA 111847 C2 Таблиця 1: a) b) Значення IC50 вибраних прикладів, та позначають, відповідно, використовуваний тип клітинного аналізу Приклад BACE1 кліт. акт. Aβ40 IC50, [мкМ] Структура H2N H N N H N BACE2 кліт. акт. IC50, [мкМ] O F F N N H N a) O H2N a) Cl O a) Cl a) a) 35 1,250 O F F N 36 0,195 O NC O H2N N H N O F F N 37 0,070 O F O H2N N H N O F F N 38 0,510 O F3 C O H2N N H N O F F N 39 0,280 O O 28
ДивитисяДодаткова інформація
Назва патенту англійськоюSpiro-[1,3]-oxazines and spiro-[1,4]-oxazepines as bace1 and/or bace2 inhibitors
Автори англійськоюNarquizian, Robert, Pinard, Emmanuel, Wostl, Wolfgang
Автори російськоюНаркизан Робер, Пинар Эммануель, Востль Вольфганг
МПК / Мітки
МПК: C07D 498/10, A61P 25/28, A61K 31/537
Мітки: інгібітори, спіро-[1,3]-оксазини, або, bace1, спіро-[1,4]-оксазепіни, bace2
Код посилання
<a href="https://ua.patents.su/75-111847-spiro-13-oksazini-ta-spiro-14-oksazepini-yak-ingibitori-bace1-ta-abo-bace2.html" target="_blank" rel="follow" title="База патентів України">Спіро-[1,3]-оксазини та спіро-[1,4]-оксазепіни як інгібітори bace1 та (або) bace2</a>
Попередній патент: Теплоізольований пристрій для нагрівання курильного матеріалу
Наступний патент: Біговий протектор пневматичної шини для сільськогосподарського трактора
Випадковий патент: Спосіб обробки розплаву металу, що кристалізується