1-(арилсульфоніл)-4-(піперазин-1-іл)-1н-бензімідазоли як ліганди 5-гідрокситриптаміну-6
Номер патенту: 100192
Опубліковано: 26.11.2012
Автори: Хейдер Саймон Н., Андре Патрік М., Юн Хідонг, Робішо Альберт Дж.
Формула / Реферат
1. Сполука формули І:
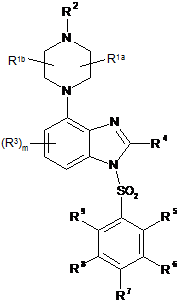 , I
, I
де
R1a та R1b , кожен незалежно, означають Н або С1-С6-алкіл, С2-С6-алкеніл або С2-С6-алкініл, кожен заміщений 0-4 замісниками, незалежно вибраними з групи, яка складається з наступних: С1-С4-алкіл, С3-С6-циклоалкіл, С3-С6-циклоалкеніл, С2-С6-алкеніл, С2-С6-алкініл, гало, нітро, ціано, гідрокси, -N(Ra)2, -C(O)Rb, -ОRс та -S(O)pRd;
альтернативно, R1a та R1b разом утворюють -(СН2)n-;
R2 означає Н, С1-С4-алкіл, -СНО або -С(О)(С1-С4-алкіл);
R3 незалежно означає у кожному випадку гало, нітро, ціано, гідрокси, -N(Ra)2, C1-C6-алкіл, С2-С6-алкеніл, С2-С6-алкініл, C1-C6-ацил або C1-C6-алкокси, де кожен C1-C6-алкіл, C1-C6-алкіл, С2-С6-алкеніл, C1-C6-ацил або C1-C6-алкокси заміщено 0-4 замісниками, незалежно вибраними з групи, яка складається з наступних: С1-С4-алкіл, С3-С6-циклоалкіл, С3-С6-циклоалкеніл, С2-С6-алкеніл, С2-С6-алкініл, гало, нітро, ціано, гідрокси, -N(Ra)2, -C(O)Rb, -ORc та -S(O)pRd;
R4 означає Н, гідрокси, C1-C6-алкіл, С2-С6-алкеніл, С2-С6-алкініл, C1-C6-ацил, С3-С6-циклоалкіл або С3-С6-циклоалкеніл, де кожен C1-C6-алкіл, С2-С6-алкеніл, С2-С6-алкініл, С1-С6-ацил, С3-С6-циклоалкіл або С3-С6-циклоалкеніл заміщено 0-4 замісниками, незалежно вибраними з групи, яка складається з наступних: С1-С4-алкіл, С3-С6-циклоалкіл, С3-С6-циклоалкеніл, гало, нітро, ціано, гідрокси, -N(Ra)2, -C(O)Rb, -ORc та -S(O)pRd;
R5, R6, R7, R8 та R9 кожен незалежно означає Н, гало, нітро, ціано, гідрокси, S(O)pRd, -N(Ra)2, C1-C6-алкіл, C1-C6-ацил, С1-С6-алкокси, С3-С6-циклоалкіл або С3-С6-циклоалкеніл, де кожен C1-C6-алкіл, C1-C6-ацил, C1-C6-алкокси, С3-С6-циклоалкіл або С3-С6-циклоалкеніл заміщено 0-4 замісниками, незалежно вибраними з групи, яка складається з наступних: С1-С4-алкіл, С3-С6-циклоалкіл, С3-С6-циклоалкеніл, С2-С6-алкеніл, С2-С6-алкініл, гало, нітро, ціано, гідрокси, -N(Ra)2, -C(O)Rb, -ОRс та -S(O)pRd;
альтернативно, один з R5 та R6 або R6 та R7 разом з атомами вуглецю, до яких вони приєднані, утворюють конденсований феніл, С3-С6-циклоалкіл або С3-С6-циклоалкеніл, заміщений 0-3 R10 групами;
R10 означає гало, нітро, ціано, гідрокси, S(O)pRd, -N(Ra)2, С1-С6-алкіл, C1-C6-ацил, C1-C6-алкокси, С3-С6-циклоалкіл або С3-С6-циклоалкеніл, де кожен C1-C6-алкіл, C1-C6-ацил, C1-C6-алкокси, С3-С6-циклоалкіл або С3-С6-циклоалкеніл заміщено 0-4 замісниками, незалежно вибраними з групи, яка складається з наступних: С1-С4-алкіл, С3-С6-циклоалкіл, С3-С6-циклоалкеніл, С2-С6-алкеніл, С2-С6-алкініл, гало, нітро, ціано, гідрокси, феніл, -N(Ra)2, -C(O)Rb, -ОRс та -S(O)pRd;
кожен Ra незалежно означає Н, -СНО, -С(О)(С1-С4-алкіл), -СО2(С1-С4-алкіл) або С1-С4-алкіл, необов'язково заміщений гало;
кожен Rb незалежно означає Н, -ОН, С1-С4-алкокси-, -NH2, -NН(С1-С4-алкіл), -N(С1-С4-алкіл)2 або С1-С4-алкіл, необов'язково заміщений гало;
кожен Rc незалежно означає Н, -С(О)(С1-С4-алкіл) або С1-С4-алкіл, необов'язково заміщений гало;
кожен Rd незалежно означає гідрокси або С1-С4-алкіл, необов'язково заміщений гало;
кожен р незалежно означає 0, 1 або 2,
m дорівнює 0, 1 або 2; та
n дорівнює 1 або 2; або її таутомер, стреоізомер або фармацевтична прийнятна сіль.
2. Сполука за п. 1, де R2 означає Н або С1-С4-алкіл.
3. Сполука за п. 1 або 2, де R2 означає Н.
4. Сполука за будь-яким з пп. 1-3, де R3 незалежно означає у кожному випадку гідрокси або гало.
5. Сполука за будь-яким з пп. 1-4, де m дорівнює 0.
6. Сполука за будь-яким з пп. 1-5, де R4 означає Н, гідрокси або С1-С6-алкіл.
7. Сполука за будь-яким з пп. 1-6, де R4 означає Н або С1-С4-алкіл.
8. Сполука за будь-яким з пп. 1-7, де R1a та R1b кожен незалежно означає Н або C1-C6-алкіл;
альтернативно, R1a та R1b разом утворюють -(СН2)n-.
9. Сполука за будь-яким з пп. 1-8, де R1a та R1b знаходяться у 3- та 5- положеннях піперазинового кільця формули І.
10. Сполука за будь-яким з пп. 1-9, де R1b означає Н або С1-С4-алкіл.
11. Сполука за п. 1, представлена 2-метил-1-(фенілсульфоніл)-4-піперазин-1-іл-1Н-бензімідазолом, або її таутомер, стреоізомер або фармацевтично прийнятна сіль.
12. Сполука за п. 1, представлена 2-метил-1-(фенілсульфоніл)-4-піперазиніл-1-іл-1Н-бензімідазолом.
13. Сполука за п. 1, представлена сукцинатом 2-метил-1-(фенілсульфоніл)-4-піперазиніл-1-іл-1Н-бензімідазолу.
14. Композиція, яка містить сполуку за будь-яким з пп. 1-13 та фармацевтично прийнятний носій.
15. Застосування сполуки за будь-яким з пп. 1-13 для одержання медикаменту для лікування розладу, пов'язаного з 5-НТ6.
16. Застосування за п. 15, де розлад, пов'язаний з 5-НТ6, є хворобою або розладом центральної нервової системи (ЦНС).
17. Застосування за п. 15 або 16, де розлад, пов'язаний з 5-НТ6, вибирають з наступних: психоз, тривога, депресія, епілепсія, синдром нав'язливих станів, мігрень, когнітивні розлади, розлади сну, розлади харчування, анорексія, ожиріння, булімія, компульсивне переїдання, напади паніки, розлади, що виникли внаслідок відмови від зловживання наркотиками, порушення когнітивних функцій, пов'язане з шизофренією, розлади шлунково-кишкового тракту, синдром подразненого кишечнику, розлади пам'яті, хвороба Альцгеймера, хвороба Паркінсона, хорея Хантінгтона, шизофренія, синдром дефіциту уваги та гіперактивності, нейродегенеративні хвороби, які характеризуються порушенням росту нейронів, та біль.
18. Застосування за п. 17, де розладом, пов'язаним з 5-НТ6, є когнітивна дисфункція, асоційована з хворобою Альцгеймера.
Текст
Реферат: Винахід стосується 1-(арилсульфоніл)-4-(піперазин-1-іл)-1Н-бензімідазолів формули І: UA 100192 C2 (12) 5 UA 100192 C2 R 2 N R1a R1b N N (R3) R m 4 N SO2 R 9 R 5 R 8 R 6 R 7 І або їх таутомеру, стреоізомера або фармацевтично прийнятної солі, де значення змінних є такими, як визначено у даному документі, композицій, які містять сполуки, та способів одержання та використання сполук. UA 100192 C2 5 10 15 20 25 30 35 40 45 50 55 60 Галузь винаходу Даний винахід стосується 1-(арилсульфоніл)-4-(піперазин-1-іл)-1H-бензімідазолів, фармацевтичних композицій, способів їх одержаних, їх застосування для модулювання активності 5-HT6 та способи лікування розладів центральної нервової системи (ЦНС). Передумови винаходу Рецептори серотоніну (5-гідрокситриптамін) (5-HT) грають вирішальну роль у багатьох фізіологічних та поведінкових функціях у людей та тварин. Ці функції опосередковуються через різноманітні 5-HT рецептори, розповсюджені по всьому тілу. Зараз відомо приблизно 15 різних клонованих підтипів рецепторів 5-HT людини, багато з яких грають чітко-визначену роль у людини. Нещодавно виявленим підтипом рецептора 5-HT є рецептор 5-HT6, вперше клонований з тканини пацюка у 1993 (Monsma, F. J.; Shen, Y.; Ward, R. P.; Hamblin, M. W. Molecular Pharmacology 1993, 43, 320-327) та після цього з тканини людини (Kohen, R.; Metcalf, M. A.; Khan, N.; Druck, T.; Huebner, K.; Sibley, D. R. Journal of Neurochemistry 1996, 66, 47-56). Рецептор є рецептором, зв‟язаним з G-білком (GPCR), позитивно зв‟язаним з аденілатциклазою (Ruat, M., Traiffort, E., Arrang, J-M., Tardivel-Lacombe, L., Diaz, L., Leurs, R., and Schwartz, J.-C., Biochemical Biophysical Research Communications 1993, 193, 268-276). Рецептор практично повністю знаходиться у центральній нервовій системі (ЦНС) пацюків та людини. Гібридизація іn situ 5-HT6 рецептора мозку пацюків, використовуючи мРНК, вказало на головну локалізацію у ділянках 5HT проекції, включаючи полосате тіло, прилегше ядро, нюховий бугорок та гіпокамп (Ward, R. P.; Hamblin, M. W.; Lachowicz, J. E.; Hoffman, B. J.; Sibley, D. R.; Dorsa, D. M. Neuroscience 1995, 64, 1105-1111). Існує значний потенціал терапевтичного застосування лігандів 5-HT6 у людей на основі прямого впливу та даних доступних наукових досліджень. Ці дослідження включають локалізацію рецептора, афінності лігандів з відомою in vivo активністю, та різноманітні дослідження на тваринах, здійснені до теперішнього часу. Одним потенційним застосуванням модуляторів рецептора 5-HT6 є покращення познавальної здатності та пам‟яті у людей, які страждають на захворювання, такі як хвороба Альцгеймера. Високі рівні рецептора, знайдені у важливих структурах переднього мозку, включаючи хвіст/путамен, гіпокамп, прилегше ядро та корку, передбачають роль рецептора у пам‟яті та пізнаванні, з огляду на те, що відомо, що ці ділянки відіграють життєву роль у пам‟яті (Gerard, C.; Martres, M.-P.; Lefevre, K.; Miquel, M.C.; Verge, D.; Lanfumey, R.; Doucet, E.; Hamon, M.; El Mestikawy, S. Brain Research, 1997, 746, 207-219). Здатність відомих лігандів рецептора 5HT6 покращувати холінергічну передачу також підтримує потенційне когнітивне застосування (Bentley, J. C.; Boursson, A.; Boess, F. G.; Kone, F. C.; Marsden, C. A.; Petit, N.; Sleight, A. J. British Journal of Pharmacology, 1999, 126(7), 1537-1542). За допомогою досліджень з‟ясували, що відомий селективний антагоніст 5-HT6 значно підвищує рівні глутамату та аспартату у лобній корі без підвищення рівнів норадреналіну, допаміну або 5-HT. Відомо, що таке селективне підвищення рівнів нейрохімікатів приймає участь у пам‟яті та когнітивних функціях, що вказує на роль 5-HT6 лігандів у когнітивних функціях (Dawson, L. A.; Nguyen, H. Q.; Li, P. British Journal of Pharmacology, 2000, 130(1), 23-26). Дослідження пам‟яті та утворення навичок на тваринах відомим селективним антагоністом 5-HT6 дало гарні результати (Rogers, D. C.; Hatcher, P. D.; Hagan, J. J. Society of Neuroscience, Abstracts 2000, 26, 680). Потенційним застосуванням лігандів 5-HT6, зокрема, антагоністів, є лікування розладів дефіциту уваги (ADD) та розладу уваги, та гіперактивності (ADHD) у дітей та дорослих. Ernst, M; Zametkin, A. J.; Matochik, J. H.; Jons, P. A.; Cohen, R. M. Journal of Neuroscience 1998, 18(15), 5901-5907). Ліганди 5-HT6 також проявляють потенціал щодо лікування шизофренії та депресії. Наприклад, клозапін (ефективний антипсихотичний лікарський засіб) має високу афінність до рецептора підтипу 5-HT6. Більш того, декілька клінічних антидепресантів також мають високу афінність до рецептора та діють як його антагоністи (Branchek, T. A.; Blackburn, T. P. Annual Reviews in Pharmacology and Toxicology 2000, 40, 319-334). Порушення когнітивної функції є ключовою характеристикою шизофренії, має багато проявів, включаючи фундаментальний дефект здатності пацієнта маніпулювати доступною інформацією. Weinberger et. al. International clinical psychopharmacology, 1997, 12, 38-40. Шизофренія характеризується значним когнітивним розладом, який залишається відносно стабільним, не зважаючи на коливання інших симптомів. Рівень диcфункції є значним показником при прогнозуванні тривалої непрацездатності. Гарний стан когнітивної функції залежить від здатності мозку визначати пріоритети завдань та переключатись з паралельної до поступової обробки даних при надмірному навантаженні. Це потребує роботи керівної пам‟яті. Нейровізуалізація та функціональний аналіз говорять про те, що така когнітивна функція 1 UA 100192 C2 5 10 15 20 25 30 35 40 45 50 55 60 залежить від неушкодженої передлобної активності. З‟являється все більше доказів щодо того, що антипсихотичні ліки з 5-гідрокситриптамін-блокуючою активністю (зокрема, 5-HT2a) краще впливають на когнітивну функцію у пацієнтів з шизофренією, ніж ліки з переважно дoпамін (D) 2блокуючою активністю (традиційні нейролептики). Відповідно, покращення або стабілізування когнітивної функції у пацієнтів з шизофренією внаслідок введення антипсихотичних ліків з 5гідрокситриптамін-блокуючою активністю приведе до покращення результатів лікування. Нейрокогнітивний дефіцит при шизофренії вважається окремою частиною захворювання, тобто, відносною незалежною від психотичних симптомів та більш пов‟язаною з функціями. Нейрокогнітивний дефіцит включає робочу пам‟ять, увагу/пильність, вербальне навчання та пам‟ять, візуальне навчання та пам‟ять, мислення та вирішення проблем, швидкість обробки та суспільне прийняття (Green MF, Nuechterlein KH, Gold JM, et al. “Approaching a consensus cognitive battery for clinical trials in шизофренія: the NIMH–MATRICS conference to select cognitive domains and test criteria”, Biol. Psychiatry 2004; 56:301–307). Також, нещодавні дослідження in vivo на пацюках вказують на те, що модулятори 5-HT6 можуть бути корисними при лікуванні розладів руху, включаючи епілепсію (Stean, T.; Routledge, C.; Upton, N. British Journal of Pharmacology 1999, 127 Proc. Supplement 131P and Routledge, C.; Bromidge, S. M.; Moss, S. F.; Price, G. W.; Hirst, W.; Newman, H.; Riley, G.; Gager, T.; Stean, T.; Upton, N.; Clarke, S. E.; Brown, A. M. British Journal of Pharmacology 2000, 130(7), 1606-1612). Всі вищенаведені дослідження вказують на те, що сполуки, які є модуляторами 5-HT6 рецептора, тобто, ліганди, можуть бути корисними при лікуванні наступних хвороб, включаючи: симптоми, асоційовані з хворобою Альцгеймера, такі як деменція, дефіцит пам‟яті, пізнання та навчання; розлади особистості, такі як шизофренія; розлади поведінки, наприклад, тривога, депресія та синдром нав‟язливих станів; лікування ADD та ADHD; розлади руху або моторики, такі як хвороба Паркінсона та епілепсія; хвороби, асоційовані з нейродегенерацією, такі як інсульт та травма голови; або абстиненція після завершення прийому лікарського засобу, включаючи звичку до нікотину, алкоголю, тощо. З огляду на те, що рецептори 5-HT6 розташовані практично повністю у мозку, модулювання рецепторів шляхом парентерального введення лікарських засобів, потребує щоб ліки перетнули гематоенцефалічний бар‟єр. Гематоенцефалічний бар‟єр складається з ендотеліальних клітин капілярів мозку з безперервними непроникними синапсами, що практично унеможливлює потрапляння сполук у мозок навколо клітин. J. Bryan, Pharmaceutical Journal, 273 (2004) 475-476. Замість цього, доступ у мозок обмежено пасивною дифузією або активним транспортом крізь th ендотеліальні клітини. G&G, Pharmaceutical Basis of Therapeutics, 10 Ed at page 10. Відповідно, біодоступні парентерально введені сполуки, які впливають на активність 5-HT6, повинні не тільки мати сприятливі профілі розчинності для вдалого потрапляння у кров‟яне русло, а ще їм потрібно перетнути гематоенцефалічний бар‟єр щоб потрапити до 5-HT6 рецепторів. Переважно, цей винахід стосується сполук, здатних модулювати активність рецептора 5-HT6, які є біодоступними. Нещодавні кліничні та докліничні дослідження лігандів 5-HT6 описані Rudy Schreiber, Andrew Sleight та Marie Woolley, “5-HT6 Receptors as Targets for the Treatment of Cognitive Deficits in Schizophrenia” у The Receptors Book The Serotonin Receptors, Humana Press, 2006, Pages 495515, Edited by Bryan L. Roth; Johnson CN, Ahmed M, Miller ND, "5-HT6 receptor antagonists: prospects for the treatment of cognitive disorders including dementia" Curr. Opin. Drug Discov. Devel. 11 (5): 642–54 (September 2008), Jorg Holenz, Petrus J. Pauwels, Jose Luis Dıaz, Ramon Merce, Xavier Codony, and Helmut Buschmann, “Medicinal chemistry strategies to 5-HT6 receptor ligands as potential cognitive enhancers and antiobesity agents”, Drug Discovery Today, 11 (7/8) April 2006, та Robin Emsley, “Drugs in development for the treatment of schizophrenia”, Expert Opinion on Investigational Drugs, 18 (8) 1103-1118, August 2009. Дев‟ять лігандів 5-HT6 пройшли клінічні дослідження на людині. Lu-AE-58054 від Lundbeck досліджували при шизофренокогнітивному розладі Фаза II, SAM-531 від Wyeth досліджували при хворобі Альцгеймера Фаза II, SYN-114 від Synosia Therapeutics досліджували при хворобі Альцгеймера Фаза I, PRX-07034 від EPIX Pharmaceuticals Inc, досліджували при шизофренії, хворобі Альцгеймера та ожирінні Фаза Ib, SUVN-502 від Suven Life Sciences Ltd. досліджували при хворобі Альцгеймера Фаза I, SB-742457 від GlaxoSmithKline досліджували при когнітивній диcфункції, асоційованій з хворобою Альцгеймера Фаза II, LY-483518 від Lilly, які надали ліцензію Saegis Pharmaceuticals (SGS- 518) досліджували при порушення когнітивних функцій, пов‟язаних з шизофренією Фаза IIa, SAX-187 від Wyeth у теперішній час досліджують при тривозі Фаза I, та SB-271046 від GlaxoSmithKline досліджували при хворобі Альцгеймера та шизофренії Фаза I, проте були зупинені (можливо через слабке проникнення крізь бар‟єр кровмозок). 2 UA 100192 C2 5 10 15 Структури 1-[(3-фторфеніл)сульфоніл]-4-(1-піперазиніл)-1H-бензімідазолу, 1-[(2фторфеніл)сульфоніл]-4-(1-піперазиніл)-1H-бензімідазолу, 1-[(3-хлорфеніл)сульфоніл]-4-(1піперазиніл)-1H-бензімідазолу, 1-(1-нафталінілсульфоніл)-4-(1-піперазиніл)-1H-бензімідазолу та 1-[(2,5-дихлорфеніл)сульфоніл]-4-(1-піперазиніл)-1H-бензімідазолу одержували від ChemZoo, Inc. of Winston-Salem, North Carolina у 2008 р. через базу даних ChemSpider. Однак, сполуки ніколи не пропонували до продажу. Не існує інформації щодо їх здатності зв‟язуватись з рецептором 5-HT6 або щодо їх фармакологічної дії або застосування цих сполук. Не існує інформації щодо їх одержання та способу їх одержання. Винахід стосується сполук придатних як терапевтичні агенти при лікуванні різноманітних станів, пов‟язаних з активністю рецептора 5-HT6, включаючи психоз (наприклад, шизофренію, тривогу або депресію), розлади руху (наприклад, хворобу Паркінсона), тривогу, депресію, залежність від лікарських засобів, синдром нав‟язливих станів, дефіцит уваги або будь-який стан, пов‟язаних з активністю рецептора 5-HT6. Ці та інші ознаки цього винаходу будуть більш очевидними після детального опису, наведеного нижче. Скорочений опис винаходу Даний винахід стосується потенційних антагоністів 5-HT6, представлених сполуками формули I: R1b R2 N R1a N N (R3)m R4 N SO2 R9 R5 R8 R6 R7 20 I де значення перемінних є таким як визначено нижче. Інший аспект винаходу стосується сполуки формули II: H N R1a N N R4 N SO2 R9 R5 R8 R6 R 25 7 II де значення перемінних є таким як визначено нижче. Інший аспект винаходу стосується сполуки формули III: 30 3 UA 100192 C2 H N R1a N N R4 N SO2 R9 R5 R8 R6 R7 III 5 де значення перемінних є таким як визначено нижче. Інший аспект винаходу стосується сполуки формули IV: H3 C H N R1a N N R4 N SO2 R9 R5 R8 R6 R 7 IV 10 15 де значення перемінних є таким як визначено нижче. У інших аспектах, винахід стосується композицій, які містять сполуку винаходу, та способів одержання сполук винаходу. У інших аспектах, винахід стосується способів модулювання 5-HT6 у суб‟єкта, та способів лікування розладів, пов‟язаних з 5-HT6 у ссавців, які цього потребують. Детальний опис винаходу У одному аспекті, винахід стосується сполуки формули I: R1b R2 N R1a N N (R3)m R4 N SO2 R9 R5 R8 R6 7 R I 20 де, 4 UA 100192 C2 1a 5 10 15 20 25 30 35 40 1b R та R кожен незалежно означає H або C1-C6-алкіл, C2-C6-алкеніл або C2-C6-алкініл, кожен заміщений 0-4 замісниками, незалежно вибраними з групи, яка складається з наступних: C1-C4-алкіл, C3-C6-циклоалкіл, C3-C6-циклоалкеніл, C2-C6-алкеніл, C2-C6-алкініл, гало, нітро, a b c d ціано, гідрокси, -N(R )2, -C(O)R , -OR , та -S(O)pR ; 1a 1b альтернативно, R та R разом утворюють -(CH2)n-; 2 R означає H, C1-C4-алкіл, -CHO або -C(O)(C1-C4-алкіл); 3 a R незалежно означає у кожному випадку гало, нітро, ціано, гідрокси, -N(R )2, C1-C6-алкіл, C2C6-алкеніл, C2-C6-алкініл, C1-C6-ацил або C1-C6-алкокси, де кожен C1-C6-алкіл, C1-C6-алкіл, C2C6-алкеніл, C1-C6-ацил або C1-C6-алкокси заміщено 0-4 замісниками, незалежно вибраними з групи, яка складається з наступних: C1-C4-алкіл, C3-C6-циклоалкіл, C3-C6-циклоалкеніл, C2-C6a b c d алкеніл, C2-C6-алкініл, гало, нітро, ціано, гідрокси, -N(R )2, -C(O)R , -OR та -S(O)pR ; 4 R означає H, гідрокси, C1-C6-алкіл, C2-C6-алкеніл, C2-C6-алкініл, C1-C6-ацил, C3-C6циклоалкіл або C3-C6-циклоалкеніл, де кожен C1-C6-алкіл, C2-C6-алкеніл, C2-C6-алкініл, C1-C6ацил, C3-C6-циклоалкіл або C3-C6-циклоалкеніл заміщено 0-4 замісниками, незалежно вибраними з групи, яка складається з наступних: C 1-C4-алкіл, C3-C6-циклоалкіл, C3-C6a b c d циклоалкеніл, гало, нітро, ціано, гідрокси, -N(R )2, -C(O)R , -OR та -S(O)pR ; 5 6 7 8 9 d a R , R , R , R та R кожен незалежно означає H, гало, нітро, ціано, гідрокси, S(O) pR , -N(R )2, C1-C6-алкіл, C1-C6-ацил, C1-C6-алкокси, C3-C6-циклоалкіл або C3-C6-циклоалкеніл, де кожен C1C6-алкіл, C1-C6-ацил, C1-C6-алкокси, C3-C6-циклоалкіл або C3-C6-циклоалкеніл заміщено 0-4 замісниками, незалежно вибраними з групи, яка складається з наступних: C 1-C4-алкіл, C3-C6a циклоалкіл, C3-C6-циклоалкеніл, C2-C6-алкеніл, C2-C6-алкініл, гало, нітро, ціано, гідрокси, -N(R )2, b c d -C(O)R , -OR та -S(O)pR ; 5 6 6 7 альтернативно, один з R та R або R та R разом з атомами вуглецю, до яких вони приєднані, утворюють конденсований феніл, C3-C6-циклоалкіл або C3-C6-циклоалкеніл, 10 заміщений 0-3 R групами; 10 d a R означає гало, нітро, ціано, гідрокси, S(O)pR , -N(R )2, C1-C6-алкіл, C1-C6-ацил, C1-C6алкокси, C3-C6-циклоалкіл або C3-C6-циклоалкеніл, де кожен C1-C6-алкіл, C1-C6-ацил, C1-C6алкокси, C3-C6-циклоалкіл або C3-C6-циклоалкеніл заміщено 0-4 замісниками, незалежно вибраними з групи, яка складається з наступних: C 1-C4-алкіл, C3-C6-циклоалкіл, C3-C6a b циклоалкеніл, C2-C6-алкеніл, C2-C6-алкініл, гало, нітро, ціано, гідрокси, феніл, -N(R )2, -C(O)R , c d OR , та -S(O)pR ; a кожен R незалежно означає H, -CHO, -C(O)(C1-C4-алкіл), -CO2(C1-C4-алкіл) або C1-C4-алкіл, необов‟язково заміщений гало; b кожен R незалежно означає H, -OH, C1-C4-алкокси-, -NH2, -NH(C1-C4-алкіл), -N(C1-C4-алкіл)2 або C1-C4-алкіл, необов‟язково заміщений гало; c кожен R незалежно означає H, -C(O)(C1-C4-алкіл) або C1-C4-алкіл, необов‟язково заміщений гало; d кожен R незалежно означає гідрокси або C1-C4-алкіл, необов‟язково заміщений гало; кожен p незалежно означає 0, 1 або 2, m дорівнює 0, 1 або 2; та n дорівнює 1 або 2; або їх таутомеру, стреоізомеру або фармацевтично прийнятної солі. Інший аспект винаходу стосується сполуки формули II: H N R1a N N R4 N SO2 R9 R5 R8 R6 R 45 7 II де перемінні є такими як описано для сполуки формули I. 5 UA 100192 C2 Інший аспект винаходу стосується сполуки формули III: H N R1a N N R4 N SO2 R9 R5 R8 R6 R7 III 5 де перемінні є такими як описано для сполуки формули I. Інший аспект винаходу стосується сполуки формули IV: H3 C H N R1a N N R4 N SO2 R9 R5 R8 R6 R 10 15 20 25 30 35 7 IV де перемінні є такими як описано для сполуки формули I. У одному варіанті здійснення: 1a 1b R та R кожен незалежно означає H або C1-C6-алкіл; 1a 1b альтернативно, R та R разом утворюють -(CH2)n-; 2 R означає H або C1-C4-алкіл; 3 R незалежно означає у кожному випадку гідроксил або гало; 4 R означає H, гідрокси або C1-C6-алкіл; 5 6 7 8 9 R , R , R , R та R кожен незалежно означає H, гало, гідрокси, C1-C6-алкіл або C1-C6алкокси, де кожен C1-C6-алкіл або C1-C6-алкокси заміщено 0-3 гало; 5 6 6 7 альтернативно, один з R та R або R та R разом з атомами вуглецю, до яких вони приєднані, утворюють конденсований феніл, C3-C6-циклоалкіл або C3-C6-циклоалкеніл, 10 заміщений 0-3 R групами; 10 кожен R незалежно означає гало, гідрокси, C1-C6-алкіл або C1-C6-алкокси, де кожен C1-C6алкіл або C1-C6-алкокси заміщено 0-3 гало; m дорівнює 0, 1 або 2; та n дорівнює 1 або 2. 2 У одному варіанті здійснення, R означає H або C1-C4-алкіл. 2 У одному варіанті здійснення, R означає H. 4 У одному варіанті здійснення, R означає C1-C6-алкіл. 4 У одному варіанті здійснення, R означає C1-C4-алкіл. 4 У одному варіанті здійснення, R означає метил, етил, пропіл або бутил. 4 У одному варіанті здійснення, R означає H. У одному варіанті здійснення, m дорівнює 0. 3 У одному варіанті здійснення, R означає гало. 6 UA 100192 C2 1a 5 10 15 20 25 30 35 40 45 50 55 60 1b У одному варіанті здійснення, R та R незалежно означає H або C1-C4-алкіл. 1a 1b У одному варіанті здійснення, R та R обидва означають H або –CH3. 1a 1b У одному варіанті здійснення, R та R обидва означають H. 1a 1b У одному варіанті здійснення, R означає H та R означає –CH3. 2 У одному варіанті здійснення, R означає H або C1-C4-алкіл. 5 У одному варіанті здійснення, R означає H або гало. 5 У одному варіанті здійснення, R означає хлор. 5 У одному варіанті здійснення, R означає C1-C4-алкокси, необов‟язково заміщений гало. 5 У одному варіанті здійснення, R означає C1-C4-алкіл, необов‟язково заміщений гало. 6 У одному варіанті здійснення, R означає H, гало, C1-C4-алкіл, необов‟язково заміщений гало або C1-C4-алкокси, необов‟язково заміщений гало. 6 У одному варіанті здійснення, R означає –OCF3. 5 6 7 8 9 У одному варіанті здійснення, один з R , R , R , R та R означає C1-C4-алкіл, необов‟язково 5 6 7 8 9 5 6 7 8 9 заміщений гало, один з R , R , R , R та R означає гало, та інші три з R , R , R , R та R означають H. 5 6 У одному варіанті здійснення, R означає C1-C4-алкіл, необов‟язково заміщений гало та R означає гало. 6 У одному варіанті здійснення, R означає фтор. 7 У одному варіанті здійснення, R означає H або гало. 7 У одному варіанті здійснення, R означає фтор. 7 У одному варіанті здійснення, R означає C1-C4-алкокси або C1-C4-алкіл, кожен необов‟язково заміщений гало. 5 6 7 8 9 5 6 У одному варіанті здійснення, один з R , R , R , R та R означає гало та інші чотири з R , R , 7 8 9 R , R та R є H. 5 6 7 8 9 5 6 7 8 У одному варіанті здійснення, два з R , R , R , R та R є гало та інші три з R , R , R , R та 9 R означають H. 5 6 7 8 9 У одному варіанті здійснення, один з R , R , R , R та R означає алкіл, необов‟язково 5 6 7 8 9 заміщений гало та інші чотири з R , R , R , R та R означають H. 5 6 У одному варіанті здійснення, R та R разом з атомами вуглецю, до яких вони приєднані, утворюють конденсований феніл, C3-C6-циклоалкіл або C3-C6-циклоалкеніл, кожен 10 необов‟язково заміщений R . 5 6 У одному варіанті здійснення, R та R разом з атомами вуглецю, до яких вони приєднані, утворюють конденсований феніл. 5 6 У одному варіанті здійснення, R та R означають H. 10 У одному варіанті здійснення, R означає гало. 6 7 У одному варіанті здійснення, R та R разом з атомами вуглецю, до яких вони приєднані, утворюють конденсований феніл, C1-C6-циклоалкіл або C1-C6-циклоалкеніл, необов‟язково заміщений гало. 6 7 У одному варіанті здійснення, R та R разом з атомами вуглецю, до яких вони приєднані, утворюють конденсований феніл. 6 8 9 У одному варіанті здійснення, R означає OC1-C4-алкіл, R означає C1-C4-алкіл, та R означає гало. 1a 1b 2 У іншому варіанті втілення, R та R означають H, R означає H або метил, m дорівнює 0, 4 5 6 7 8 9 R вибирають з групи, яка складається з H або C1-C6-алкілу; та R , R , R , R та R кожен означає H або гало. 4 У одному варіанті здійснення, R означає H. 6 У одному варіанті здійснення, R означає F. 7 8 9 У одному варіанті здійснення, R , R та R кожен означає H. 4 У одному варіанті здійснення, R означає метил. У одному варіанті здійснення, сполуки формули I виключають 1-[(3-фторфеніл)сульфоніл]-4(1-піперазиніл)-1H-бензімідазол, 1-[(2-фторфеніл)сульфоніл]-4-(1-піперазиніл)-1H-бензімідазол, 1-[(3-хлорфеніл)сульфоніл]-4-(1-піперазиніл)-1H-бензімідазол, 1-(1-нафталінілсульфоніл)-4-(1піперазиніл)-1H-бензімідазол та 1-[(2,5-дихлорфеніл)сульфоніл]-4-(1-піперазиніл)-1Hбензімідазол. Ілюстративні сполуки формули I включають: 4-(4-метилпіперазин-1-іл)-1-(нафталін-1-ілсульфоніл)-1H-бензо[d]імідазол; 1-(нафталін-1-ілсульфоніл)-4-(піперазин-1-іл)-1H-бензо[d]імідазол; 1-(фенілсульфоніл)-4-(піперазин-1-іл)-1H-бензо[d]імідазол; 2-метил-1-(1-нафтилсульфоніл)-4-піперазин-1-іл-1H-бензімідазол; 2-метил-1-(фенілсульфоніл)-4-піперазин-1-іл-1H-бензімідазол; 7 UA 100192 C2 5 10 15 20 25 30 35 40 45 50 55 60 2-етил-1-(фенілсульфоніл)-4-піперазин-1-іл-1H-бензімідазол; 4-(4-етилпіперазин-1-іл)-1-(фенілсульфоніл)-1H-бензімідазол; 2-бутил-1-(фенілсульфоніл)-4-піперазин-1-іл-1H-бензімідазол; 2-метил-4-(4-метилпіперазин-1-іл)-1-(1-нафтилсульфоніл)-1H-бензімідазол; 1-[(4-хлорфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(2-хлорфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 4-(4-метилпіперазин-1-іл)-1-(фенілсульфоніл)-1H-бензімідазол; 1-[(4-метоксифеніл)сульфоніл]-2-метил-4-піперазин-1-іл-1H-бензімідазол; 2-метил-4-піперазин-1-іл-1-{[3-(трифторметокси)феніл]сульфоніл}-1H-бензімідазол; 1-[(2-хлорфеніл)сульфоніл]-2-метил-4-піперазин-1-іл-1H-бензімідазол; 1-[(3-хлорфеніл)сульфоніл]-2-метил-4-піперазин-1-іл-1H-бензімідазол; 1-[(4-хлорфеніл)сульфоніл]-2-метил-4-піперазин-1-іл-1H-бензімідазол; 2-метил-1-[(3-метилфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(3-хлорфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(4-фторфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(2-фторфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(3-фторфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-(2-нафтилсульфоніл)-4-піперазин-1-іл-1H-бензімідазол; 1-[(4-метоксифеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 4-піперазин-1-іл-1-{[4-(трифторметокси)феніл]сульфоніл}-1H-бензімідазол; 1-[(3-фторфеніл)сульфоніл]-2-метил-4-піперазин-1-іл-1H-бензімідазол; 1-[(4-метилфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 4-піперазин-1-іл-1-{[3-(трифторметокси)феніл]сульфоніл}-1H-бензімідазол; 1-[(3-хлор-4-фторфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 2-метил-4-піперазин-1-іл-1-{[4-(трифторметокси)феніл]сульфоніл}-1H-бензімідазол; 2-метил-1-[(4-метилфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(2-фторфеніл)сульфоніл]-2-метил-4-піперазин-1-іл-1H-бензімідазол; 4-піперазин-1-іл-1-{[2-(трифторметокси)феніл]сульфоніл}-1H-бензімідазол; 1-[(3-метоксифеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(4-метил-1-нафтил)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(3-метилфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(3-хлор-2-метилфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(4-фторфеніл)сульфоніл]-2-метил-4-піперазин-1-іл-1H-бензімідазол; 1-[(2-метилфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 4-піперазин-1-іл-1-{[4-(трифторметил)феніл]сульфоніл}-1H-бензімідазол; 4-піперазин-1-іл-1-{[2-(трифторметил)феніл]сульфоніл}-1H-бензімідазол; 4-піперазин-1-іл-1-{[3-(трифторметил)феніл]сульфоніл}-1H-бензімідазол; 2-метил-1-(2-нафтилсульфоніл)-4-піперазин-1-іл-1H-бензімідазол; 1-[(2-метоксифеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(3-метоксифеніл)сульфоніл]-2-метил-4-піперазин-1-іл-1H-бензімідазол; 2-метил-4-піперазин-1-іл-1-{[2-(трифторметокси)феніл]сульфоніл}-1H-бензімідазол; 2-метил-1-[(2-метилфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 2-метил-4-піперазин-1-іл-1-{[2-(трифторметил)феніл]сульфоніл}-1H-бензімідазол; 2-метил-4-піперазин-1-іл-1-{[3-(трифторметил)феніл]сульфоніл}-1H-бензімідазол; 1-[(5-хлор-1-нафтил)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 2-метил-1-[(4-метил-1-нафтил)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(2-метоксифеніл)сульфоніл]-2-метил-4-піперазин-1-іл-1H-бензімідазол; 1-[(2-хлорфеніл)сульфоніл]-4-(3-метилпіперазин-1-іл)-1H-бензімідазол; 1-[(3-хлорфеніл)сульфоніл]-4-(3-метилпіперазин-1-іл)-1H-бензімідазол; 1-[(3-метилфеніл)сульфоніл]-4-(3-метилпіперазин-1-іл)-1H-бензімідазол; 1-[(2-метоксифеніл)сульфоніл]-4-(3-метилпіперазин-1-іл)-1H-бензімідазол; 4-(3-метилпіперазин-1-іл)-1-{[2-(трифторметокси)феніл]сульфоніл}-1H-бензімідазол; 1-[(3-хлор-2-метилфеніл)сульфоніл]-4-(3-метилпіперазин-1-іл)-1H-бензімідазол; 1-[(2-хлорфеніл)сульфоніл]-2-(1-метилетил)-4-піперазин-1-іл-1H-бензімідазол; 1-[(3-хлорфеніл)сульфоніл]-2-(1-метилетил)-4-піперазин-1-іл-1H-бензімідазол; 2-(1-метилетил)-1-(нафталін-1-ілсульфоніл)-4-піперазин-1-іл-1H-бензімідазол; 1-[(5-хлорнафталін-1-іл)сульфоніл]-2-(1-метилетил)-4-піперазин-1-іл-1H-бензімідазол; 2-(1-метилетил)-4-піперазин-1-іл-1-{[2-(трифторметокси)феніл]сульфоніл}-1H-бензімідазол; 2-(1-метилетил)-1-[(4-метилнафталін-1-іл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(5-хлор-2-метоксифеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 8 UA 100192 C2 5 10 15 20 25 30 35 40 45 50 55 60 1-[(5-бром-2-метоксифеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(2,5-диметоксифеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(2-метокси-5-метилфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(2-метокси-4-метилфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(2-хлор-6-метилфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-{[2-хлор-5-(трифторметил)феніл]сульфоніл}-4-піперазин-1-іл-1H-бензімідазол; 1-[(2-фтор-5-метилфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(2-фтор-3-метилфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(3-фтор-2-метоксифеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(2-хлорфеніл)сульфоніл]-4-[(3R)-3-метилпіперазин-1-іл]-1H-бензімідазол; 1-[(3-хлорфеніл)сульфоніл]-4-[(3R)-3-метилпіперазин-1-іл]-1H-бензімідазол; 1-[(3-хлор-2-метилфеніл)сульфоніл]-4-[(3R)-3-метилпіперазин-1-іл]-1H-бензімідазол; 4-[(3R)-3-метилпіперазин-1-іл]-1-(нафталін-1-ілсульфоніл)-1H-бензімідазол; 1-[(2-хлорфеніл)сульфоніл]-4-[(3S)-3-метилпіперазин-1-іл]-1H-бензімідазол; 1-[(3-хлорфеніл)сульфоніл]-4-[(3S)-3-метилпіперазин-1-іл]-1H-бензімідазол; 4-[(3S)-3-метилпіперазин-1-іл]-1-(нафталін-1-ілсульфоніл)-1H-бензімідазол; 1-[(3-хлор-2-метилфеніл)сульфоніл]-4-[(3S)-3-метилпіперазин-1-іл]-1H-бензімідазол; 1-[(2,3-дифторфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(2,5-дифторфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(2-хлор-5-фторфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(2,6-дихлорфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(3-фтор-2-метилфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(3-хлор-5-фторфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 1-[(2-етоксифеніл)сульфоніл]-2-метил-4-піперазин-1-іл-1H-бензімідазол; 1-[(5-хлор-2-метокси-4-метилфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол; 2-метил-4-(3-метилпіперазин-1-іл)-1-(фенілсульфоніл)-1H-бензімідазол; 2-метил-4-(3-метилпіперазин-1-іл)-1-(нафталін-1-ілсульфоніл)-1H-бензімідазол; 1-[(2-хлорфеніл)сульфоніл]-2-метил-4-(3-метилпіперазин-1-іл)-1H-бензімідазол; 1-[(3-фторфеніл)сульфоніл]-2-метил-4-(3-метилпіперазин-1-іл)-1H-бензімідазол; 1-[(3-хлор-2-метилфеніл)сульфоніл]-2-метил-4-(3-метилпіперазин-1-іл)-1H-бензімідазол; 4-[(3R,5S)-3,5-диметилпіперазин-1-іл]-2-метил-1-(фенілсульфоніл)-1H-бензімідазол; 4-[(3R,5S)-3,5-диметилпіперазин-1-іл]-2-метил-1-(нафталін-1-ілсульфоніл)-1H-бензімідазол; 1-[(2-хлорфеніл)сульфоніл]-4-[(3R,5S)-3,5-диметилпіперазин-1-іл]-2-метил-1H-бензімідазол; 4-[(3R,5S)-3,5-диметилпіперазин-1-іл]-1-[(3-фторфеніл)сульфоніл]-2-метил-1H-бензімідазол; 1-[(3-хлор-2-метилфеніл)сульфоніл]-4-[(3R,5S)-3,5-диметилпіперазин-1-іл]-2-метил-1Hбензімідазол; 6-фтор-1-(нафталін-1-ілсульфоніл)-4-піперазин-1-іл-1H-бензімідазол; 1-[(2-хлорфеніл)сульфоніл]-6-фтор-4-піперазин-1-іл-1H-бензімідазол; 6-фтор-1-(фенілсульфоніл)-4-піперазин-1-іл-1H-бензімідазол; 4-[(1S,4S)-2,5-діазабіцикло[2.2.1]гепт-2-ил]-1-(фенілсульфоніл)-1H-бензімідазол; 4-[(1S,4S)-2,5-діазабіцикло[2.2.1]гепт-2-ил]-1-(нафталін-1-ілсульфоніл)-1H-бензімідазол; 1-[(2-хлорфеніл)сульфоніл]-4-[(1S,4S)-2,5-діазабіцикло[2.2.1]гепт-2-ил]-1H-бензімідазол; 4-[(1S,4S)-2,5-діазабіцикло[2.2.1]гепт-2-ил]-1-[(3-фторфеніл)сульфоніл]-1H-бензімідазол; 1-[(3-хлор-2-метилфеніл)сульфоніл]-4-[(1S,4S)-2,5-діазабіцикло[2.2.1]гепт-2-ил]-1Hбензімідазол; 4-[(1S,4S)-2,5-діазабіцикло[2.2.1]гепт-2-ил]-2-метил-1-(фенілсульфоніл)-1H-бензімідазол; 4-[(1S,4S)-2,5-діазабіцикло[2.2.1]гепт-2-ил]-2-метил-1-(нафталін-1-ілсульфоніл)-1Hбензімідазол; 1-[(2-хлорфеніл)сульфоніл]-4-[(1S,4S)-2,5-діазабіцикло[2.2.1]гепт-2-ил]-2-метил-1Hбензімідазол; 4-[(1S,4S)-2,5-діазабіцикло[2.2.1]гепт-2-ил]-1-[(3-фторфеніл)сульфоніл]-2-метил-1Hбензімідазол; 1-[(3-хлор-2-метилфеніл)сульфоніл]-4-[(1S,4S)-2,5-діазабіцикло[2.2.1]гепт-2-ил]-2-метил-1Hбензімідазол; 2-метил-4-[(3R)-3-метилпіперазин-1-іл]-1-(фенілсульфоніл)-1H-бензімідазол; 2-метил-4-[(3R)-3-метилпіперазин-1-іл]-1-(1-нафтилсульфоніл)-1H-бензімідазол; 2-метил-4-[(3S)-3-метилпіперазин-1-іл]-1-(фенілсульфоніл)-1H-бензімідазол; 2-метил-4-[(3S)-3-метилпіперазин-1-іл]-1-(1-нафтилсульфоніл)-1H-бензімідазол; 4-(3-етилпіперазин-1-іл)-1-(1-нафтилсульфоніл)-1H-бензімідазол; 4-(3-етилпіперазин-1-іл)-1-(фенілсульфоніл)-1H-бензімідазол; 9 UA 100192 C2 5 10 15 20 25 30 35 40 4-(3-ізопропілпіперазин-1-іл)-1-(фенілсульфоніл)-1H-бензімідазол; 4-(3-ізопропілпіперазин-1-іл)-1-(1-нафтилсульфоніл)-1H-бензімідазол; 1-[(2-хлорфеніл)сульфоніл]-4-(3-ізопропілпіперазин-1-іл)-1H-бензімідазол; 4-(3-iзoбутилпіперазин-1-іл)-1-(фенілсульфоніл)-1H-бензімідазол; 4-(3-iзoбутилпіперазин-1-іл)-1-(1-нафтилсульфоніл)-1H-бензімідазол; 1-[(2-хлорфеніл)сульфоніл]-4-(3-iзoбутилпіперазин-1-іл)-1H-бензімідазол; 1-[(5-хлор-1-нафтил)сульфоніл]-2-метил-4-[(3S)-3-метилпіперазин-1-іл]-1H-бензімідазол; 1-[(5-хлор-1-нафтил)сульфоніл]-2-метил-4-[(3R)-3-метилпіперазин-1-іл]-1H-бензімідазол; 4-(3-метилпіперазин-1-іл)-1-(фенілсульфоніл)-1H-бензімідазол; та 4-(3-метилпіперазин-1-іл)-1-(1-нафтилсульфоніл)-1H-бензімідазол; або Їх таутомер, стреоізомер або фармацевтично прийнятну сіль. У інших аспектах, винахід стосується фармацевтичних композицій, які містять сполуки або фармацевтично прийнятні солі сполук будь-якої з формул I-IV та фармацевтично прийнятний носій. У інших аспектах, винахід стосується оральної лікарської форми, яка містить фармацевтично прийнятний носій придатний для орального введення та композицію. У інших аспектах, винахід стосується способу лікування 5-HT6-пов‟язаного розладу, який включає введення ссавцю, який цього потребує, сполуки будь-якої з формул I-IV у кількості, ефективній для лікування 5-HT6-пов‟язаного розладу. У інших аспектах, винахід стосується способу лікування хвороби або розладу центральної нервової системи (ЦНС), який включає введення суб‟єкту сполуки формул I-IV або їх таутомеру, стреоізомеру або фармацевтично прийнятної солі. У інших аспектах, хвороба або розлад центральної нервової системи (ЦНС) включає наступні хвороби: психоз, тривога, депресія, епілепсія синдром нав‟язливих станів, мігрень, когнітивні розлади, розлади сну, розлади харчування, анорексія, булімія, компульсивне переїдання, напади паніки, розлади, що виникли внаслідок відмови від зловживання лікарськими засобами, порушення когнітивних функцій пов‟язане з шизофренією, розлади шлунково-кишкового тракту, синдром подразненого кишечнику, розлади пам‟яті, когнітивна диcфункція, пов‟язана з хворобою Альцгеймера, хвороба Паркінсона, хорея Хантінгтона, шизофренія, синдром дефіциту уваги та гіперактивності, нейродегенеративні хвороби, які характеризуються порушенням росту нейронів, та біль. У іншому варіанті втілення, сполука будь-яких втілень даного винаходу існує у вигляді фармацевтично прийнятної солі. Зокрема, фармацевтично прийнятна сіль представлена гідрохлоридом (HCl). Інший варіант втілення винаходу стосується способу модулювання активності 5-HT6 рецептора у суб‟єкта, який включає введення суб‟єкту сполуки формул I-IV, де у суб‟єкта модулюється активність 5-HT6 рецептора. У інших аспектах, винахід стосується способу синтезу сполуки формули I, який включає: a) взаємодію сполуки формули IA: зі сполукою формули IB: де, 10 UA 100192 C2 2 X означає R або захисну групу; утворюючи сполук у формули IC: 5 10 15 20 25 IC; 1a 1b 2 9 де R , R та R -R є такими як визначено у формулі I; та 2 якщо X означає R , тоді отримують сполуку формули I; або якщо X означає захисну групу, спосіб додатково включає: b) зняття захисту зі сполуки формули IC одержуючи незахищену сполуку; 2 де якщо R означає H, тоді отримують сполуку формули I; або 2 якщо R не означає H, спосіб додатково включає: 2 2 c) взаємодію GA-R або GA=R з незахищеною сполукою; де GA означає активовану групу; де отримують сполуку формули I. У одному варіанті здійснення, взаємодію сполуки формули IA з IB здійснюють у апротонному розчиннику у присутності основи. У одному варіанті здійснення, основою є гідрид натрію (NaH). У одному варіанті здійснення, захисна група означає трет-бутоксикарбоніл (Boc), бензил, ацетил, p-метоксибензил (PMB) або бензилоксикарбоніл (Cbz). У одному варіанті здійснення, стадія зняття захисту включає взаємодію сполуки формули IC з трифтороцтовою кислотою (TFA). У одному варіанті здійснення, GA означає гало, тозилат, мезилат, трифлат або oксo. 2 У одному варіанті здійснення, GA означає оксо та стадія взаємодії GA=R з незахищеною сполукою включає відновлювальне амінування у присутності боронового відновлювального агента. У іншому аспекті винаходу, спосіб також включає одержання сполуки формули IB шляхом: a) взаємодії сполуки формули ID: 30 зі сполукою формули IE: 35 де, гало означає Cl, Br або I; та 11 UA 100192 C2 5 10 15 20 з одержанням сполуки формули IB. У одному варіанті здійснення, X означає захисну групу та стадію взаємодії сполуки формули ID зі сполукою формули IE здійснюють у присутності основи. У одному варіанті здійснення, основою є бікарбонат натрію (NaHCO 3) та стадію взаємодії o здійснюють при приблизно 100 C. У іншому аспекті винаходу, спосіб також включає одержання сполуки формули IB шляхом 4 взаємодії R -C(OEt)3 зі сполукою формули IF: IF з одержанням сполуки формули IB. 4 У одному варіанті здійснення, стадію взаємодії R -C(OEt)3 зі сполукою формули IF здійснюють у присутності монтморілоніту KSF та толуолу. У іншому аспекті винаходу, спосіб також включає одержання сполуки формули IF шляхом гідрування сполуки формули IG: де, Y означає N3 або NO2. У одному варіанті здійснення, стадію гідрування здійснюють у присутності H 2 та паладію на вугіллі (H2/Pd-C). У іншому аспекті винаходу, Y означає NO 2 та спосіб також включає одержання сполуки формули IG шляхом: (a) взаємодії 2,3-динітроаніліну з нітрітом натрію (NaNO 2), одержуючи (2,3динітрофеніл)діазоній; та (b) взаємодії (2,3-динітрофеніл)діазонію зі сполукою формули IH: 25 30 35 40 з одержанням сполуки формули IG. У одному варіанті здійснення, стадію взаємодії 2,3-динітроаніліну з нітрітом натрію (NaNO 2) здійснюють у присутності оцтової кислоти (AcOH) та броміду міді (CuBr). У одному варіанті здійснення, стадію взаємодії здійснюють у присутності 2,2'біс(дифенілфосфіно)-1,1'-бiнафтил (BINAP), тріс(дибензиліденацетон)дипаладію (Pd 2(dba)3), карбонат цезію (Cs2CO3) та толуол. У одному варіанті здійснення, 2,3-динітроанілін одержують шляхом взаємодії N-(3нітрофеніл)ацетаміду з азотною кислотою (HNO3) та сірчаною кислотою (H2SO4). У іншому аспекті винаходу, Y означає N3 та спосіб також включає одержання сполуки формули IG шляхом: (a) взаємодії азиду натрію з 1,3-дифтор-2-нітробензеном, одержуючи 1-азидо-3-фтор-2нітробензен; та (b) взаємодії 1-азидо-3-фтор-2-нітробензену зі сполукою формули IH: 12 UA 100192 C2 5 10 15 20 25 30 35 40 45 50 з одержанням сполуки формули IG. У одному варіанті здійснення, стадію взаємодії здійснюють у присутності N,Nдiізопропілетиламіну (DIPEA). У одному варіанті здійснення, будь-яку з вищевказаних стадій здійснюють у протонному розчиннику, апротонному розчиннику, полярному розчиннику, неполярному розчиннику, протонному полярному розчиннику, апротонному неполярному розчиннику або апротонному полярному розчиннику. У одному варіанті здійснення, будь-яка з вищевказаних стадій включає стадію очистки, яка включає щонайменше: фільтування, екстрагування, хроматографію, розтирання в порошок або перекристалізацію. У іншому варіанті втілення, aбудь-яка з вищевказаних стадій включає аналітичну стадію, яка включає рідинну хроматографію (РХ), масспектроскопію (MС), рідинну хроматографію/масспектроскопію (РХ/MС), газову хроматографію (ГХ), газову хроматографію/масспектроскопію (ГХ/MС), ядерномагнітний резонанс (ЯМР), тонко шарову хроматографію (TШХ), аналіз точки плавлення (ТП), оптичне обертання (OО) або елементарний аналіз. Представники "фармацевтично прийнятних солей" включають, проте не обмежуються, наприклад, водо-розчинними та водо-нерозчинними солями, такими як ацетат, алюміній, амсонат (4,4-діаміностілбен-2,2-дисульфонат), бензатин (N,N'-дибензилетилeндіамін), бензолсульфонат, бензоат, бікарбонат, вісмут, бісульфат, бітартрат, борат, бромід, бутират, кальцій, кальцію едетат, камсилат (камфорсульфонат), карбонат, хлорид, холін, цитрат, клавуларіат, диетаноламін, дигідрохлорид, дифосфат, едетат, едизілат (камфорсульфонат), езілат (етансульфонат), етилeндіамін, фумарат, глюцептат (глюкогептонат), глюконат, глюкуронат, глутамат, гексафторфосфат, гексилрезорцинат, гідрабамін (N,N'біс(дегідроабіетил)етилeндіамін), гідробромід, гідрохлорид, гідроксинафтоат, 1-гідрокси-2нафтоат, 3-гідрокси-2-нафтоат, йодид, ізотіонат (2-гідроксиетансульфонат), лактат, лактобіонат, лаурат, лаурилсульфат, літій, магній, малат, малеат, манделат, меглумін (1-деокси-1(метиламіно)-D-глюцитол), мезилат, метил бромід, метилнітрат, метилсульфат, мукат, напсилат, нітрат, N-метилглюкамін амонію, олеат, оксалат, палмітат, памоат (4,4'-метилeнбіс-3гідрокси-2-нафтоат або ембонат), пантотенат, фосфат, пікрат, полігалактуронат, калій, пропіонат, п-толуолсульфонат, саліцилат, натрій, стеарат, субацетат, сукцинат, сульфат, сульфосаліцилат, сурамат, танат, тартрат, теоклат (8-хлор-3,7-дигідро-1,3-диметил-1H-пурин2,6-діон), триетіодид, трометамін (2-аміно-2-(гідроксиметил)-1,3-пропандіол), валерат та цинк. Деякі сполуки даного винаходу містять один або кілька хіральних центрів, даний винахід включає кожен окремий енантіомер таких сполук, а також суміші енантіомерів. Коли сполуки даного винаходу містять кілька хіральних центрів, винахід включає кожну комбінацію, а також їх суміші. Всі хіральні, діастереомерні та рацемічні форми структури є включеними, доки не вказана конкретна стереохімія або ізомерна форма. У галузі добре відомо як одержати оптично активні форми, наприклад, шляхом розділення рацемічних форм або синтезу з оптично активних вихідних матеріалів. "Ефективна кількість" по відношенню до сполуки даного винаходу означає кількість, ефективну для інгібування mTOО або PI3K у суб‟єкта. Визначення термінів Наступні визначення приводяться стосовно сполук даного винаходу, доки не вказано протилежне. Взагалі, кількість атомів вуглецю у певній групі позначається як “C x-Cy”, де x та y є верхньою та нижньою границями, відповідно. Наприклад, група, позначена як “C 1-C6” містить від 1 дo 6 атомів вуглецю. Кількість вуглецю, вказана в позначенні, стосується вуглецю головного ланцюга та відгалужень, проте не включає атоми вуглецю замісників, таких як алкокси тощо. Доки не вказано протилежне, номенклатура чітко не названих замісників, починається зліва направо від термінальної частини функціональної групи до сусідньої функціональної групи у напрямку точки приєднання. Наприклад, замісник “арилалкілоксикарбоніл” стосується групи (C 6C14-арил)-(C1-C6-алкіл)-O-C(O)-. Зрозуміло, що вищенаведені визначення не включають 13 UA 100192 C2 5 10 15 20 25 30 35 40 45 50 55 неможливі варіанти заміщення (наприклад, метил заміщений 5 атомами фтору, дві гідроксильні групи на одному атомі вуглецю, гідроксильна група на не-aроматичному подвійному зв‟язку). Такі неможливі заміщення є добре відомими фахівцю у галузі. У кожній з нижченаведених груп, коли підгрупи позначаються з можливістю декількох варіантів, кожен варіант вибирають незалежно. Наприклад, у ди(C1-C6-алкіл)аміно-, наприклад, (C1-C6-алкіл)2N-, C1-C6-алкіли можуть бути однаковими або різними. “Активація" сполуки стосується взаємодії сполуки по реакційному центру з реагентом із введенням в цей центр активуючої групи, де активуюча сполука необов‟язково перетворюється на іншу активуючу сполуку за одну або кілька стадій. Приклади активації включають галогенування по вуглецю, після цього необов‟язково гідроборування, де галоген перетворюється на необов‟язково заміщений боран; тозилування, мезилування або трифлатування по кисню; та нітрування по вуглецю, після цього необов‟язково відновлення нітрогрупи до аміногрупи та перетворення аміногрупи на діазогрупу. “Активуюча група" є групою, яка при приєднанні до центру, збільшує реактивність при цьому центрі. Невичерпні приклади активуючої групи включають замісник, приєднаний до електрофільного центру та здатний до заміщення нуклеофільним реагентом; замісник, приєднаний до нуклеофільного центру та здатний до заміщення електрофільним реагентом; замісник здатний до заміщення радикалом; або замісник, приєднаний до центру, де після приєднання або втрати електрона, замісник здатний відділитись як аніон або катіон з утворенням радикалу при центрі. “Ацил-” стосується групи з нерозгалуженою, розгалуженою або циклічною конфігурацією або їх комбінації, приєднаною до батьківської структури через карбонільну функціональну групу. Такі групи можуть бути насиченими або ненасиченими, аліфатичними або ароматичними, та карбоциклічними або гетероциклічними. При підрахуванні кількості атомів вуглецю включають атом вуглецю карбонілу. Приклади C 1-C8-ацилу включають HC(O)-, ацетил-, бензоїл-, p-толуїл, нікотиноїл-, пропіоніл-, ізобутирил-, оксаліл-, тощо. Нижчий-ацил- стосується ацильних груп, які містять від 1 до 4 атомів вуглецю. Ацил може бути заміщеним або незаміщеним однією або кількома наступними групами: галоген, H2N-, (C1-C6-алкіл)аміно-, ди(C1-C6-алкіл)аміно-, (C1-C6алкіл)C(O)N(C1-C3алкіл)-, (C1-C6-алкіл)карбоніламідо-, HC(O)NH-, H2NC(O)-, (C1-C6алкіл)NHC(O)-, ди(C1-C6-алкіл)NC(O)-, -CN, гідроксил, C1-C6-алкокси-, C1-C6-алкіл-, HO2C-, (C1C6-алкокси)карбоніл-, C1-C8-ацил-, C6-C14-арил-, C1-C9-гетероарил- або C3-C8-циклоалкіл-. "Алкеніл-" стосується нерозгалуженого або розгалуженого ланцюга ненасиченого вуглеводню, який містить щонайменше один подвійний зв'язок. Де можливими є E- та/або Zізомери, термін “алкеніл” включає такі ізомери. Приклади C2-C6-алкенілу включають, проте не обмежуються наступними: етилeн, пропілен, 1-бутилeн, 2-бутилeн, iзoбутилeн, втор-бутилeн, 1пентен, 2-пентен, iзoпентен, пента-1,4-дiєн-1-іл, 1-гексен, 2-гексен, 3-гексен та iзoгексен. Алкеніл може бути заміщеним або незаміщеним однією або кількома наступними групами: галоген, H2N-, (C1-C6-алкіл)аміно-, ди(C1-C6-алкіл)аміно-, (C1-C6-алкіл)C(O)N(C1-C3алкіл)-, (C1-C6алкіл)карбоніламідо-, HC(O)NH-, H2NC(O)-, (C1-C6-алкіл)NHC(O)-, ди(C1-C6-алкіл)NC(O)-, -CN, гідроксил, C1-C6-алкокси-, C1-C6-алкіл-, HO2C-, (C1-C6-алкокси)карбоніл-, C1-C8-ацил-, C6-C14арил-, C1-C9-гетероарил- та C3-C8-циклоалкіл-. "Алкокси-” стосується групи R-O-, де R означає алкіл, як зазначено нижче. Приклади C 1-C6алкокси- включають, проте не обмежуються наступними: метокси, етокси, н-пропокси, 1пропокси, н-бутокси та т-бутокси. Алкокси може бути заміщеним або незаміщеним однією або кількома наступними групами: галоген, гідроксил, C 1-C6-алкокси-, H2N-, (C1-C6-алкіл)аміно-, ди(C1-C6-алкіл)аміно-, (C1-C6-алкіл)C(O)N(C1-C3алкіл)-, (C1-C6-алкіл)карбоніламідо-, HC(O)NH-, H2NC(O)-, (C1-C6-алкіл)NHC(O)-, ди(C1-C6-алкіл)NC(O)-, -CN, C1-C6-алкокси-, HO2C-, (C1-C6алкокси)карбоніл-, C1-C8-ацил-, C6-C14-арил-, C1-C9-гетероарил-, C3-C8-циклоалкіл-, C1-C6галоалкіл-, C1-C6аміноалкіл-, (C1-C6-алкіл)карбокси-, C1-C6-карбоніламідоалкіл- або O2N-;. “Алкіл-” стосується вуглеводневого ланцюгу з нерозгалуженим або розгалуженим ланцюгом, який містить певну кількість атомів вуглецю, наприклад, C l-Cl0-алкіл- може містити від 1 дo 10 (включно) атомів вуглецю. У відсутності будь-якого числового позначення, "алкіл" є ланцюгом (нерозгалуженим або розгалуженим), який містить від 1 дo 6 (включно) атомів вуглецю. Приклади C1-C6-алкілу включають, проте не обмежуються наступними: метил, етил, пропіл, бутил, пентил, гексил, ізопропіл, iзoбутил, втор-бутил, трет-бутил, ізопентил, неопентил та ізогексил. Алкіл може бути заміщеним або незаміщеним однією або кількома наступними групами: галоген, H2N-, (C1-C6-алкіл)аміно-, ди(C1-C6-алкіл)аміно-, (C1-C6-алкіл)C(O)N(C1C3алкіл)-, (C1-C6-алкіл)карбоніламідо-, HC(O)NH-, H2NC(O)-, (C1-C6-алкіл)NHC(O)-, ди(C1-C6алкіл)NC(O)-, -CN, гідроксил, C1-C6-алкокси-, C1-C6-алкіл-, HO2C-, (C1-C6-алкокси)карбоніл-, C1 14 UA 100192 C2 5 10 15 20 25 30 35 40 45 50 55 60 C8-ацил-, C6-C14-арил-, C1-C9-гетероарил-, C3-C8-циклоалкіл-, C1-C6-галоалкіл-, C1-C6аміноалкіл-, (C1-C6-алкіл)карбокси-, C1-C6-карбоніламідоалкіл- або O2N-. “Алкініл-" стосується нерозгалуженого або розгалуженого ланцюгу ненасиченого вуглеводню, який містить щонайменше один потрійний зв'язок. Приклади C2-C6-алкінілу включають, проте не обмежуються наступними: ацетилeн, пропін, 1-бутин, 2-бутин, ізобутин, втор-бутин, 1-пентин, 2-пентин, iзoпентин, пента-1,4-диін-1-іл, 1-гексин, 2-гексин, 3-гексин та iзoгексин. Алкініл може бути заміщеним або незаміщеним однією або кількома наступними групами: галоген, H2N-, (C1-C6-алкіл)аміно-, ди(C1-C6-алкіл)аміно-, (C1-C6-алкіл)C(O)N(C1C3алкіл)-, (C1-C6-алкіл)карбоніламідо-, HC(O)NH-, H2NC(O)-, (C1-C6-алкіл)NHC(O)-, ди(C1-C6алкіл)NC(O)-, -CN, гідроксил, C1-C6-алкокси-, C1-C6-алкіл-, HO2C-, (C1-C6-алкокси)карбоніл-, C1C8-ацил-, C6-C14-арил-, C1-C9-гетероарил- та C3-C8-циклоалкіл-. “Аміно” стосується групи H2N-. Арил стосується ароматичного вуглеводню. Приклади C 6-C14-арилу включають, проте не обмежуються наступними: феніл, 1-нафтил, 2-нафтил, 3-біфeн-1-іл, антрил, тетрагідронафтил, флуореніл, інданіл, бiфенілeніл та аценафтеніл. Арил може бути моно циклічним або поліциклічним, доки щонайменше одне кільце є ароматичним та місцем приєднання є атом вуглецю ароматичного кільця. Арил може бути заміщеним або незаміщеним однією або кількома наступними групами: C1-C6-алкіл-, галоген, галоалкіл-, гідроксил, гідроксил(C1-C6алкіл)-, H2N-, аміноалкіл-, ди(C1-C6-алкіл)аміно-, HO2C-, (C1-C6-алкокси)карбоніл-, (C1-C6алкіл)карбокси-, ди(C1-C6-алкіл)амідо-, H2NC(O)-, (C1-C6-алкіл)амідо- або O2N-. "(Арил)алкіл-" стосується алкілу, як вказано вище, де один або кілька атомів водню алкілу заміщено арилом як вказано вище. Залишки (C6-C14-арил)алкіл- включають: бензил, бензгідрил, 1-фенілетил, 2-фенілетил, 3-фенілпропіл, 2-фенілпропіл, 1-нафтилметил, 2-нафтилметил тощо. (Арил)алкіл- може бути заміщеним або незаміщеним однією або кількома наступними групами: галоген, H2N-, гідроксил, (C1-C6-алкіл)аміно-, ди(C1-C6-алкіл)аміно-, (C1-C6-алкіл)C(O)N(C1C3алкіл)-, (C1-C6-алкіл)карбоніламідо-, HC(O)NH-, H2NC(O)-, (C1-C6-алкіл)NHC(O)-, ди(C1-C6алкіл)NC(O)-, -CN, гідроксил, C1-C6-алкокси-, C1-C6-алкіл-, HO2C-, (C1-C6-алкокси)карбоніл-, C1C8-ацил-, C6-C14-арил-, C1-C9-гетероарил-, C3-C8-циклоалкіл-, C1-C6-галоалкіл-, C1-C6аміноалкіл-, (C1-C6-алкіл)карбокси-, C1-C6-карбоніламідоалкіл- або O2N-. “Хвороба ЦНС” або “розлад ЦНС” є хворобою або розладом, який уражує або починається у центральній нервовій системі, переважно хворобою, яка стосується активності 5-HT6 або на яку впливає модулювання 5-HT6. Певні хвороби ЦНС або розлади включають: психоз, тривога, депресія, епілепсія, мігрень, когнітивні розлади, розлади сну, розлади харчування, анорексія, булімія, компульсивне переїдання, напади паніки, розлади, що виникли внаслідок відмови від зловживання лікарськими засобами, порушення когнітивних функцій пов‟язане з шизофренією, розлади шлунково-кишкового тракту, синдром подразненого кишечнику, розлади пам‟яті, синдром нав‟язливих станів, когнітивна диcфункція, пов‟язана з хворобою Альцгеймера, ADD, ADHD, синдром неспокійних ніг (СВН), хвороба Паркінсона, хорея Хантінгтона, шизофренія, синдром дефіциту уваги та гіперактивності, нейродегенеративні хвороби, які характеризуються порушенням росту нейронів та біль. Терміни “хвороба ЦНС” або “розлад ЦНС”, використані у даному документі, також включають симптом іншої хвороби, такої як когнітивні розлади асоційовані з шизофренією. "Циклоалкіл-" стосується моноциклічного насиченого вуглеводневого кільця. Представники C3-C8-циклоалкілу- включають, проте не обмежуються наступними: циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил та циклооктил. Циклоалкіл- може бути незаміщеним або незалежно заміщеним однією або кількома наступними групами: галоген, H 2N-, (C1-C6алкіл)аміно-, ди(C1-C6-алкіл)аміно-, (C1-C6-алкіл)C(O)N(C1-C3алкіл)-, (C1-C6-алкіл)карбоніламідо-, HC(O)NH-, H2NC(O)-, (C1-C6-алкіл)NHC(O)-, ди(C1-C6-алкіл)NC(O)-, -CN, гідроксил, C1-C6алкокси-, C1-C6-алкіл-, HO2C-, (C1-C6-алкокси)карбоніл-, C1-C8-ацил-, C6-C14-арил-, C1-C9гетероарил- або C3-C8-циклоалкіл-, C1-C6-галоалкіл-, C1-C6аміноалкіл-, (C1-C6-алкіл)карбокси-, C1-C6-карбоніламідоалкіл- або O2N-. Окрім цього, кожен з двох атомів водню біля того ж атому вуглецю карбоциклічного кільця можуть бути заміщеними атомом кисню щоб утворити оксо (=O) замісник або два атоми водню можуть бути заміщені алкілендиокси групою, таким чином, що алкілендиокси група, разом з атомом вуглецю до якого вона приєднана, утворювала 5-7членний гетероцикл, який містить два атоми кисню. “Циклоалкеніл-” стосується не-ароматичних карбоциклічних кілець з одним або кількома С-С подвійними зв‟язками всередині кільцевої системи. “Циклоалкеніл” може мати одно або кілька кілець. Багато кільцеві структури можуть бути місткованими або конденсованими кільцевими структурами. Приклади C3-C10циклоалкенілу включають, проте не обмежуються наступними: циклопропеніл, циклобутеніл, циклопентеніл, циклогексеніл, 4,4a-окталін-3-іл та циклооктеніл. 15 UA 100192 C2 5 10 15 20 25 30 35 40 45 50 55 Циклоалкеніл може бути незаміщеним або незалежно заміщеним з однією або кількома наступними групами: галоген, H2N-, (C1-C6-алкіл)аміно-, ди(C1-C6-алкіл)аміно-, (C1-C6алкіл)C(O)N(C1-C3алкіл)-, (C1-C6-алкіл)карбоніламідо-, HC(O)NH-, H2NC(O)-, (C1-C6алкіл)NHC(O)-, ди(C1-C6-алкіл)NC(O)-, -CN, гідроксил, C1-C6-алкокси-, C1-C6-алкіл-, HO2C-, (C1C6-алкокси)карбоніл-, C1-C8-ацил-, C6-C14-арил-, C1-C9-гетероарил- або C3-C8-циклоалкіл-, C1-C6галоалкіл-, C1-C6аміноалкіл-, (C1-C6-алкіл)карбокси-, C1-C6-карбоніламідоалкіл- або O2N- Окрім цього, кожен з будь-яких двох атомів водню на одному й тому самому атомі вуглецю циклоалкенілу може бути заміщеним атомом кисню утворюючи оксо (=O) замісник або два атоми водню можуть бути заміщеними алкілeндиокси таким чином, що алкілeндиокси група разом з атомом вуглецю до якого вона приєднана, утворює 5-7-членний гетероцикл, який містить два атоми кисню. “Зняття захисту” стосується видалення захисної групи, таке як видалення бензилу або BOC групи, приєднаної до аміну. Зняття захисту здійснюють нагріванням та/або додаванням реагентів, здатних видаляти захисні групи. У бажаних варіантах здійснення, зняття захисту включає додавання кислоти, основи, відновлювального агента, окислювача, нагрівання або будь-яку їх комбінацію. Один бажаний варіант видалення BOC груп з аміно груп включає додавання до розчину HCl або TFA. Багато реакцій зняття захисту є добре відомими фахівцям та описані у Protective Groups in Organic Synthesis, Greene and Wuts, John Wiley & Sons, New rd York, NY, (3 Edition, 1999), вміст якого включено у даному документі за допомогою посилань. “Захисна група” або “Gp” по відношенню до аміногруп, гідроксильних груп та сульфгідрильних груп стосується таких форм цих групп, які є захищеними від небажаних реакцій захисними групами відомими фахівцям, такими як ті, що описані у Protective Groups in Organic Synthesis, Greene, T.W.; Wuts, P. G. M., John Wiley & Sons, New York, NY, (3rd Edition, 1999), вміст якого включено у даному документі за допомогою посилань, ці групи додають або видаляють за описаними тут способами. Приклади захищених гідроксильних груп включають, проте не обмежуються наступними: силілові етери, такі як отримані шляхом взаємодії гідроксильної групи з реагентом, таким як: т-бутилдиметил-хлорсилан, триметилхлорсилан, триізопропілхлорсилан, триетилхлорсилан; заміщені метиловий та етиловий етери, такі як: метоксиметиловий етер, метилтіометиловий етер, бензилoксиметиловий етер, тбутоксиметиловий етер, 2-метоксиетоксиметиловий етер, тетрагідропіраніловий етер, 1етоксиетил етер, аліловий етер, бензиловий етер, проте не обмежуюсь ними; естери, такі як: бензоїлформіат, форміат, ацетат, трихлорацетат та трифторацетат, проте не обмежуюсь ними. Приклади захищених аміно груп включають, проте не обмежуються наступними: аміди, такі як: формамід, ацетамід, трифторацетамід та бензамід; карбамати; наприклад Boc; іміди, такі як фталімід, Fmoc, Cbz, PMB, бензил та дитіосукцинімід; тощо. Приклади захищених або кепованих сульфгідрильних груп включають, проте не обмежуються наступними: тіоетери, такі як S-бензил тіoетер та S-4-піколіл тіoетер; заміщений S-метил похідні, такі як гемітіо, дитіо та амінотіо ацеталі; тощо. "Гало" або “галоген” стосується фтору, хлору, брому або йоду. "Галоалкіл-" стосується алкілу, як вказано вище, де один або кілька атомів водню заміщено F, -Cl, -Br або -I. Кожне заміщення вибирають незалежно. Зразкові приклади C1-C6-галоалкілу включають, проте не обмежуються наступними: -CH2F, -CCl3, -CF3, CH2CF3, -CH2Cl, -CH2CH2Br, CH2CH2I, -CH2CH2CH2F, -CH2CH2CH2Cl, -CH2CH2CH2CH2Br, -CH2CH2 CH2CH2I, CH2CH2CH2CH2CH2Br, -CH2CH2CH2CH2CH2I, -CH2CH(Br)CH3, -CH2CH(Cl)CH2CH3, -CH(F)CH2CH3 та -C(CH3)2(CH2Cl). “Гетероатом” стосується сірки, азоту або кисню. “Гідрокси” або “гідроксил” стосується групи HO-. “Модулювання активності рецептора 5-HT6” стосується впливу (наприклад, інгібування або стимулювання) або сигналювання, пов‟язаного з рецептором 5-HT6. Зокрема, інгібування 5-HT6 збільшує рівні ацетилхоліну та глутамату у мозку, у той час як агоністик рецептора 5-HT6 або стимулювання приводять до збільшення клітинного цAТФ. “Нітро” стосується групи O2N-. “Oксo” стосується атому (=O). Як активуюча група, „oксo‟ групи піддаються відновлювальному амінуванню нуклеофільними аміно групами з утворенням алкіламіно- або аміноалкіл- замісників. Бажано, стадію відновлювального амінування здійснюють у присутності борон-вмісного відновлювального агента. “Стереоізомер” або “стреоізомери” стосується сполук, які відрізняються хіральністю або зв‟язком між атомами у одному або кількох стереоцентрах. Стереoізомери включають енантіомери, діастереомери, а також цис-транс (E/Z) ізомери. 16 UA 100192 C2 5 10 15 20 25 30 35 40 45 50 55 60 "Суб‟єкт" або “пацієнт” означає ссавця, наприклад, людину, миша, пацюка, морську свинку, собаку, кішку, коня, корову, свиню або нелюдських приматів, таких як мавпа, шимпанзе, павіан або горила. “Таутомер” стосується перемінних форм сполуки, які відрізняються положення протону, таких як енол-кето або імін-єнамін таутомери. “Лікування” хвороби у суб‟єкта стосується: пригнічення хвороби або затримки її розвитку; полегшення симптомів хвороби; або регресії хвороби. Відповідно, “лікування хвороби Альцгеймера” як вказано у даному документі, включає полегшення симптомів хвороби Альцгеймера, полегшення деменції пов‟язаної з хворобою Альцгеймера або лікування когнітивної диcфункції, асоційованої з хворобою Альцгеймера. Окрім цього, “лікування шизофренії” включає полегшення або стабілізування когнітивної диcфункції та полегшення порушення когнітивних функцій, пов‟язане з шизофренією. Термін “необов‟язково заміщений”, доки не вказано протилежне, як вказано у даному документі, означає, що щонайменше один атом водню необов‟язково заміщеної групи заміщено галогеном, H2N-, (C1-C6-алкіл)аміно-, ди(C1-C6-алкіл)аміно-, (C1-C6-алкіл)C(O)N(C1-C3алкілом)-, (C1-C6-алкіл)карбоніламідо-, HC(O)NH-, H2NC(O)-, (C1-C6-алкіл)NHC(O)-, ди(C1-C6-алкіл)NC(O)-, CN, гідроксилом, C1-C6-алкокси-, C1-C6-алкілом-, HO2C-, (C1-C6-алкокси)карбонілом- , C1-C8ацилом-, C6-C14-арилом-, C1-C9-гетероарилом- або C3-C8-циклоалкілом-. Зрозуміло, що у всіх вищенаведених заміщених групах, полімери, що попадають під визначені замісники з додатковими замісниками, які є такими ж самими як і вони (наприклад, заміщений арил, який містить заміщену арильну групу як замісник, який є заміщеним заміщеним арилом, який також є заміщеним заміщеним арилом тощо) не є призначеними для включення у даний документ. У таких випадках, максимальна кількість замісників дорівнює трьом. Наприклад, серійні заміщення заміщених арильних груп двома іншими заміщеними арильними групами обмежено заміщений арил-(заміщений арил)-заміщений арил. Сполуки даного винаходу проявляють модулюючу активність 5-HT6 та тому можуть використовуватись для лікування пацієнтів, які страждають від хвороби центральної нервової системи (ЦНС) або розладу, яке включає введення суб‟єкту сполуки, описаної у даному документі, зокрема, сполуки формул I-IV. У іншому варіанті втілення, хвороба або розлад (ЦНС) означає наступні: психоз, тривога, депресія, епілепсія, синдром нав‟язливих станів, мігрень, когнітивні розлади, розлади сну, розлади харчування, анорексія, булімія, компульсивне переїдання, напади паніки, розлади, що виникли внаслідок відмови від зловживання лікарськими засобами, шизофренія, розлади шлунково-кишкового тракту, синдром подразненого кишечнику, розлади пам‟яті, когнітивна диcфункція, пов‟язана з хворобою Альцгеймера, хвороба Паркінсона, хорея Хантінгтона, шизофренія, синдром дефіциту уваги та гіперактивності, нейродегенеративні хвороби, які характеризуються порушенням росту нейронів або біль. Інший варіант втілення винаходу стосується способу покращення або стабілізування когнітивної функції у суб‟єкта, який включає введення суб‟єкту сполуки, описаної уданому документі, зокрема, сполуки формули I-IV або її таутомеру, стреоізомеру або фармацевтично прийнятної солі. У іншому варіанті втілення, когнітивну функцію стабілізують або покращують у пацієнта, який страждає від шизофренії. Для терапевтичного застосування, фармакологічно активні сполуки будь-якої з формул I-IV нормально вводяться у вигляді фармацевтичних композицій, які містять як необхідний активний інгредієнт щонайменше одну таку сполуку разом з твердим або рідким фармацевтично прийнятним носієм та, необов‟язково, з фармацевтично прийнятними ад‟ювантами та наповнювачами із застосуванням стандартних технік. Фармацевтичні композиції даного винаходу включають придатні лікарські форми для орального, парентерального (включаючи підшкірне, внутрішньом‟язове, інтрадермальне та внутрішньовенне) бронхіального або назального введення. Таким чином, у разі використання твердого носія, композицію можна формувати у таблетки, у порошкоподібній або гранулярній формі, поміщені у тверду желатинову капсулу саше або лозенгеру. Твердий носій може містити звичайні наповнювачі, такі як зв‟язувальні агенти, наповнювачі, лубриканти, які використовують у виготовленні таблеток, дезінтегрантів, змочувальних агентів тощо. У разі потреби, таблетка може мати плівкове покриття, нанесене за звичайними технологіями. У разі застосування рідкого наповнювача, лікарська форма може знаходитись у формі сиропу, емульсії, м‟якої желатинової капсули, стерильного середовища для ін‟єкцій, водної або неводної рідкої суспензії або може бути сухим продуктом для відновлення водою або іншим придатним середовищем перед застосуванням. Рідкі лікарські форми можуть містити звичайні добавки, такі як 17 UA 100192 C2 5 10 15 20 25 30 35 40 45 50 55 суспендувальні агенти, емульгатори, зволожувачі, неводні середовища (включаючи їстівні олії), консерванти, а також агенти для надання смаку та/або кольору. Для парентерального введення, середовище зазвичай містить стерильну воду, щонайменше більшу частину, хоча також можна використовувати сольові розчини, розчини глюкози тощо. Також застосовують ін‟єктивні суспензії, у цьому випадку використовують звичайні суспендувальні агенти. Звичайні консерванти, буферувальні агенти тощо також додають до парентеральних лікарських форм. Особливо придатним є введення сполуки будь-якої формули I-IV безпосередньо у парентеральній формі. Фармацевтичні композиції одержують за звичайними технологіями відповідно до бажаної лікарської форми, яка містить відповідну кількість активного інгредієнта, тобто, сполука за будь-якою з формул I-IV згідно з винаходом. Дивитись, наприклад, Remington: The Science and Practice of Pharmacy, 20th Edition. Baltimore, MD: Lippincott Williams & Wilkins, 2000. Дозування сполук за будь-якою з формул I-IV для отримання терапевтичного ефекта буде залежати не тільки від таких факторів, як вік, маса та стать пацієнта та шлях введення, а й від рівня активуючої активності калієвого каналу та сили дії застосованої сполуки на певний розлад або хворобу. Вважається, що лікування та доза певної сполуки може бути призначена у вигляді одиничної дозованої форми та фахівець у галузі під корегує одиничну дозовану форму відповідно до потрібного рівня активності. Рішення стосовно конкретної дози та частоти введення на добу приймається лікарем, та може змінуватись титруванням дози до певних умов цього винаходу з метою отримання бажаного терапевтичного впливу. Придатне дозування сполуки за будь-якою з формул I-IV або її фармацевтичної композиції для ссавця, включаючи людину, яка страждає або ймовірно страждає на будь-який стан, описаний у даному документі, є кількістю активного інгредієнта від приблизно 0,01 мг/кг дo 10 мг/кг маси тіла. Для парентерального введення, доза знаходиться в діапазоні від 0,1 мг/кг дo 1 мг/кг маси тіла для внутрішньовенного введення. Для орального введення, доза знаходиться в діапазоні від приблизно 0,1 мг/кг дo 5 мг/кг маси тіла. Активний інгредієнт бажано вводять у рівних дозах 1-4 рази на добу. Однак, зазвичай вводять невелику дозу, та її поступово збільшують до оптимальної для пацієнта, якого лікують. Однак, зрозуміло, що кількість фактично введеної сполуки визначається лікарем, зважаючи на відповідні обставини, включаючи стан, який потрібно лікувати, вибір введеної сполуки, вибраний шлях введення, вік, масу та відповідь пацієнта, та тяжкість симптомів пацієнта. Кількість сполуки даного винаходу або її фармацевтично прийнятної солі є кількістю, ефективною для модулювання активності рецептора 5-HT6 у суб‟єкта. Окрім цього, для ідентифікації діапазону оптимальної дози необов‟язково використовують in vitro або in vivo аналізи. Точна значення дози також залежить від шляху введення, стану, тяжкості стану, а також від різноманітних фізичних факторів пов‟язаних з пацієнтом, та визначається лікарем. Еквівалентні дози вводять протягом різних періодів часу, включаючи, проте не обмежуючись наступними: приблизно кожні 2 години, приблизно кожні 6 годин, приблизно кожні 8 годин, приблизно кожні 12 годин, приблизно кожні 24 години, приблизно кожні 36 годин, приблизно кожні 48 годин, приблизно кожні 72 години, приблизно кожен тиждень, приблизно кожні два тижні, приблизно кожні три тижні, приблизно кожен місяць, та приблизно кожні два місяці. Кількість та частота дозувань повного курсу лікування визначається лікарем. Ефективна кількість дози, описана у даному документі, стосується загально введеної кількості; тобто, у разі введення більше ніж однієї сполуки даного винаходу або її фармацевтично прийнятної солі, ефективна кількість дози відповідає загально введеної кількості. У одному варіанті здійснення, сполуку даного винаходу або її фармацевтично прийнятну сіль вводять одночасно з іншим терапевтичним агентом. У одному варіанті здійснення, вводять композицію, яка містить ефективну кількість сполуки даного винаходу або її фармацевтично прийнятну сіль та ефективну кількість іншого терапевтичного агента, у одній композиції. Ефективна кількість іншого терапевтичного агента є добре відомою фахівцям у галузі. Однак, середній фахівець у галузі може визначити діапазон ефективної кількості іншого терапевтичного агента. Сполука даного винаходу або її фармацевтично прийнятна сіль та інший терапевтичний агент можуть взаємодіяти адитивно, у одному варіанті здійснення, синергічно. У одному варіанті здійснення винаходу, коли тварині вводять інший терапевтичний агент, ефективна кількість сполуки даного винаходу або її фармацевтично прийнятної солі є меншою, ніж її ефективна кількість при відсутності іншого терапевтичного агента. У цьому випадку, без прив‟язки до теорії, вважається, що сполука даного винаходу або її фармацевтично прийнятна сіль та інший терапевтичний агент взаємодіють синергічно. 18 UA 100192 C2 5 У іншому аспекті винаходу, використовують набори, які включають одну або кілька сполук винаходу. Зразкові набори включають інгібітор 5-HT6 винаходу (наприклад, сполука формул IIV) та вкладиш або іншу позначку, включаючи шляхи лікування хвороб ЦНС шляхом введення ефективної кількість сполуки даного винаходу. Схема показана на Схемі 1 нижче, та Приготування після Схеми описують синтез сполук даного винаходу. Певні варіації описаних процедур, які є очевидними фахівцю у галузі, є включеними у рамки даного винаходу. Схема 1 GP R1b N Спосіб A R1a N NH2 NHAc a, b NO2 3 3 c, d (R )m (R )m NO2 NO2 (R3)m NO2 1 NO2 3 2 e GP Спосіб B 1b N R NO2 F (R3)m F f, g GP R1b N R1a R1a e N NO2 3 NH2 3 (R )m (R )m R1b N N H R1a i N 7 R2 R1b N GP R1b N R1a (R3)m 6 5 GP N 8 N R4 N SO 2 R9 R1a j, k N (R3)m R4 Спосіб C NH2 N3 4 h N R8 N N (R3)m I R5 R6 R4 N SO 2 R9 R5 R6 R8 7 R7 R i Спосіб D NH2 N 3 (R )m R1a 4 R 9 N N H N (R3)m R4 N H 10 10 15 l 2 R1b R N Схема 1 описує одержання сполуки формули I та її проміжних сполук. Реагенти у кожній стадії включають: a. HNO 3, H2SO4 b. NaOMe, MeOH c. NaNO2, AcOH, H2SO4, CuBr d. Boc-піперазин, BINAP, Pd2(dba)3, Cs2CO3, толуол. e. H2/Pd-C 10%, EtOH f. NaN3, 1 5 ДMСO g. Boc-піперазин, основа Хюніга, ДMСO h. R C(OEt)3, монтморілоніт KSF, толуол i. R , 19 UA 100192 C2 6 5 10 15 20 25 30 35 40 45 50 7 8 9 10 R , R , R , R або R -заміщений арил-SO2Cl, NaH, DMF j. TFA, CH2Cl2 (коли GP = Boc) k. 2 o R CHO, NaBH(OAc)3, 1,2-дихлоретан l. біс(2-хлоретил)-алкіламін, NaHCO3, 1-бутанол, 115 C. Сполуки 6 одержують або способом A або способом B. У прикладі способу A, N-(3нітрофеніл)ацетамід нітрували за процедурою, описаною у літературі, одержуючи 2,3динітроанілін (2). Після цього, сполуку 2 перетворювали на 2,3-динітробромбензол з нітритом натрію та бромідом міді. Останній проміжний продукт реагував з Boc-піперазином одержуючи бажаний продукт 3. Відновлення проміжного продукту 3 дало отримання відповідного аніліну 6. Альтернативно, сполуку 6 можна одержати за дві стадії, наприклад, з наявного у продажу 2,6дифторнітробензену. В результаті реакції сполуки 4 з азидом натрію та Boc-піперазином одержали проміжну сполуку 5. Наступне відновлення сполуки 5 привело до утворення сполуки 6. Ядро бензімідазолу 7 можна одержати при різних умовах, визначених у літературі, таких як нагрівання сполуки 6 у толуолі у присутності монтморілоніту KSF та триетилортоформіату. Проміжний сульфон 8 можна одержати реагуванням сполуки 7 з відповідним заміщеним арилсульфоном. Зняття захисту та наступне відновлювальне амінування сполуки 8 з відповідним альдегідом дало бажану сполуку формули I. Альтернативно, сполуки формули I можна одержати з проміжної сполуки 10, яку в свою чергу одержують взаємодією проміжної сполуки 9 з біс(2-хлоретил)алкіламіном. Фахівець у галузі розуміє, що Схема 1 може бути адаптована для одержання інших сполук формул I-IV та фармацевтично прийнятних солей сполук формул I-IV згідно з даним винаходом. Приклади У даному документі використані наступні абревіатури та вони мають наступні значення: ACN означає ацетонітрил, AcOH означає оцтову кислоту, BINAP означає 2,2′-біс(дифенілфосфіно)1,1′-бiнафталін та BOC означає т-бутоксикарбоніл. Celite є флюс-кальцинованою діатомовою землею. Celite є зареєстрованою торгівельною маркою фірми World Minerals Inc. DMF означає N,N-диметилформамід та ДMСO означає диметилсульфоксид. EDTA означає етилeндіамінтетраоцтової кислоти, EСI та EС обидва означають елетроспрей іонізацію, EtOAc 3 означає етилацетат, та EtOH означає етанол. [ H]-LSD означає мічений тритієм диетилaмід лізергінової кислоти, основа Хюніга означає дiізопропілетиламін, ВЕРХ означає високоефективну рідинну хроматографію, MeCN означає ацетонітрил, MeOH означає метанол та MС означає мас-спектрометрію. ЯМР означає ядерномагнітний резонанс, PBS означає фосфатний сольовий буфер (pH 7,4), TFA означає трифтороцтову кислоту, THF означає тетрагідрофуран, TШХ означає тонко-шарову хроматографію та TMС означає тетраметилсилан. PVT WGA SPA означає сцинтиляційний аналіз зближення полівінілтолуіден аглютинін зародків пшениці. Способи Синтезу 1 Кожен з наступних способів відповідає вищенаведеній Схемі 1, де R означає H, m дорівнює 0, та GP означає Boc. Сполуки та/або проміжні сполуки охарактеризовані за допомогою РХ масспектрометрії здійсненої на Agilent ВЕРХ та мас-спектрометрі Hewletт-Packard на колонці Onyx Monolithic C18 (100 X 3,0 мм): система розчинника: 10-100% ацетонітрил у воді, швидкість потоку: 1,8 мл/хв, діапазон молекулярної маси 200-700. Спектри ядерно-магнітного резонансу (ЯМР) сполук здійснювали приладом Varian NMR з частотою 400 MГц (Palo Alto, CA). Спектральною точкою відліку є або TMС або відомий хімічний зсув розчинника. Деякі зразки сполук аналізували при підвищених температурах (наприклад, 75 °C) для підвищення розчинності зразка. Потрібно розуміти, що органічні сполуки згідно з винаходом можуть проявляти таутомерію. З огляду на те, що хімічні структури у цьому описі можуть представляти тільки одну з можливих таутомерних форм, зрозуміло, що винахід включає будь-яку таутомерну форму намальованої структури. Спосіб A: Одержання 2,3-динітроаніліну (2) 2,3-динітроанілін одержують з N-(2,3-динітрофеніл)ацетаміду, який в свою чергу одержують з комерційного матеріалу 3-нітроацетаміду як описано на нижченаведеній схемі: 20 UA 100192 C2 NHAc NH 2 NHAc NO 2 NO 2 3-Нітроацетамід 5 10 15 20 NO 2 NO 2 NO 2 N-(2,3-динітрофеніл) ацетамід 2 2,3-динітроанілін A. N-(2,3-динітрофеніл)ацетамід: До перемішаної суміші концентрованої сірчаної кислоти (216 мл) та 90% азотної (що димить) o кислоти (216 мл) охолодженої до -3 C, додавали частинами 3-нітроацетанілід (12,0 г) протягом o 20 хв. Суміш перемішували протягом 30 хв. при –10 C. Після цього реакційну суміш нагрівали до кімнатної температури протягом 1 години та виливали на подрібнений лід (600 мл), одержуючи жовту тверду речовину. Отриманий осад збирали відсмоктуванням. Отриману тверду речовину розчиняли у киплячому етанолі (125 мл) та розчин залишали стояти протягом 2 годин. Отримані світло-жовті голки фільтрували, промивали етанолом та висушували повітрям, одержуючи бажаний продукт (3,1 г, 21%). Дивиться Arnold T. Nielsen, Ronald L. Atkins, William P. Norris, Clifford L. Coon, Michael E. Sitzmann J. Org. Chem.; 1980; 45(12); 2341-2347 (включено у даному документі за допомогою посилань). Хімічна формула: C8H7N3O5 Молекулярна маса: 225,16; MС (EС) m/z 226. B. 2,3-динітроанілін До розчину N-(2,3-динітрофеніл)ацетаміду (3,0 г) у метанолі (200 мл) додавали метоксид натрію (72 мг). Перемішаний розчин кип‟ятили зі зворотнім холодильником протягом 3 годин. До розчину (300 мл) додавали воду та збирали жовтий твердий оасад та висушували, одержуючи бажаний продукт (2,27 г, 93%). Хімічна формула:і C 6H5N3O4 Молекулярна маса: 183,12; MС (EС) m/z 184 Одержання трет-бутил 4-(2,3-динітрофеніл)піперазин-1-карбоксилату (3) Сполуку 3 одержували за нижченаведеною схемою: Boc N Br NH2 N NO2 NO2 NO2 NO2 NO2 NO2 3 2 25 30 35 40 45 1-бром-2,3-динітробензол Розчин 2,3-динітроаніліну (2,27 г, 12,4 ммоль) у 35 мл крижаної оцтової кислоти краплями додавали до перемішаного та охолодженого розчину нітриту натрію (0,95 г, 13,8 ммоль) у o концентрованій сірчаній кислоті (7 мл), доки температуру реакції підтримували на рівні 15-20 C. Отриманий розчин діазонію після цього додавали протягом 5 хв. до перемішаного розчину o броміду міді (1,85 г, 12,9 ммоль) у суміші HBr (48%) (10 мл) та води (10 мл), нагрітої при 75 C-80 o C. Після додавання, суміш охолоджували до кімнатної температури та додавали до води (500 мл). Світло-зелений порошок фільтрували з розчину та висушували у вакуумі при кімнатній температурі, одержуючи бажаний продукт 1-бром-2,3-динітробензол (3,0 г, 99%). Цей продукт використовували у наступній реакції без подальшої очистки. Дивитись, Donald L. Vivian J. Org. Chem. 1956, 21, 1188. Сполуку 3 Суміш 1-бром-2,3-динітробензолу (1,0 г, 4,05 ммоль), N-Boc-піперазину (0,90 г, 4,86 ммоль), карбонату цезію (1,58 г, 4,86 ммоль), BINAP (0,113 г, 0,182 ммоль) та тріс(дибензиліденацетон)дипаладію (0,111 г, 0,121 ммоль) у толуолі (12,0 мл) кип‟ятили зі зворотнім холодильником протягом 4 годин. Випаровували толуол та залишок розчиняли у дихлорметані (100 мл), промивали водою, висушували над сульфатом натрію, та фільтрували. Дихлорметан випаровували та залишок хроматографували на силікагелі використовуючи гексан/етилацетат (30-70% EtOAc), одержуючи бажаний продукт 3 (0,37 г, 26%). MС (EС) m/z 353. Дивитись, Shashank Shekhar, Per Ryberg, John F. Hartwig, Jinu S. Mathew, Donna G. 21 UA 100192 C2 Blackmond, Eric R. Strieter, and Stephen L. Buchwald J. Am. Chem. Soc. 2006 128, 3584-3591 (включено у даному документі за допомогою посилань). Одержання сполуки трет-бутил 4-(2,3-діамінофеніл)піперазин-1-карбоксилату (6) з сполуки (3) 5 Boc N N NH2 NH2 6 10 15 Спосіб A трет-бутил 4-(2,3-динітрофеніл)піперазин-1-карбоксилат (3) розчиняли у етанолі (8,0 мл) та до нього додавали 10% Pd-C (30 мг). Гідрування цієї суміші завершували на апараті Парра при 33 псі протягом ночі. Суміш фільтрували крізь CELITE™ та хроматографували на колонці з силікагелем, використовуючи дихлорметан та етилацетат (15-50% EtOAc) до виходу бажаного продукту у вигляді світло-коричневої аморфної твердої речовини (0,129 г, 79%); MС (EС) m/z 293 Одержання трет-бутил 4-(3-азидо-2-нітрофеніл)піперазин-1-карбоксилату (5) Boc N N NO2 5 N3 Сполуку 5 одержують з сполуки 4 за наступною схемою: 20 Boc N F F N NO 2 NO 2 NO 2 F N3 N3 5 1-Азидо-3-фтор2-нітробензол 4 Одержання 1-азидо-3-фтор-2-нітробензену: F NO2 25 N3 22 UA 100192 C2 5 10 15 До перемішаного розчину 2,6-дифторнітробензену (2,0 г, 12,6 ммоль) у ДMСO (6,0 мл) при кімнатній температурі, додавали азид натрію (0,82 г; 12,6 ммоль). Через 18 годин розчин виливали у 200 мл крижаної води. Осад, 1-азидо-3-фтор-2-нітробензену, збирали та 1 висушували у вакуумі (2,26 г; 99%); H ЯМР (CDCl3, 400 MГц) 7,00 (т, J=8,8 Гц, 1H); 7,07 (д, J=8,35 Гц, 1H); 7,47 (дт, J=8,35, 5,68 Гц, 1H). MС (EС) m/z 182,1 Одержання сполуки 5 До розчину 1-азидо-3-фтор-2-нітробензену (0,35 г; 1,9 ммоль) у ДMСO (2,0 мл) додавали o Boc-піперазин (0,40 мл; 1,2 екв.) та N-Boc-піперазин (1,2 екв.). Розчин нагрівали при 60 C протягом 6 годин. Після закінчення реакції, розчин виливали у воду (50 мл) та екстрагували етилацетатом. Органічний розчин висушували над Na2SO4, фільтрували, та випаровували при пониженому тиску. Залишок хроматографували на кремнеземі, використовуючи дихлорметан/метанол. Очищений продукт 5 кристалізували з диетилового етеру та гексану; MС (EС) m/z 348,2; Одержання сполуки трет-бутил 4-(2,3-діамінофеніл)піперазин-1-карбоксилату (6) з сполуки (5) (Спосіб B): Boc N N NH2 NH2 6 20 25 Сполуку 5 (2,43 г, 6,98 ммоль) суспендували у метанолі (100 мл) та додавали 10% Pd-C (0,37 г). Гідрування цієї суміші завершували на апараті Парра при 33 псі протягом 2 годин. Суміш фільтрували крізь Celite™ та хроматографували на колонці з силікагелем використовуючи дихлорметан та етилацетат (15-50% EtOAc) до виходу бажаного продукту у вигляді світло-коричневої аморфної твердої речовини (1,97 г, 97%); MС (EС) m/z 293. Методики одержання трет-бутил 4-(2-метил-1H-бензо[d]імідазол-4-іл)піперазину (7) з сполуки (6) (Спосіб C): Boc N N N R4 N H 7 30 До фенілeндiаміну (6) додають триетилортоформіат та толуол, після чого додають 17 мг монтморілоніту KSF. Суміш кип‟ятили зі зворотнім холодильником протягом ночі. Толуол випаровували та залишок хроматографували на кремнеземі, використовуючи звичайний етилацетат, одержуючи бажаний продукт (7). Загальна процедура одержання трет-бутил 4-(2-алкіл-1-арилсульфоніл)-1Hбензо[d]імідазол-4-іл)піперазину (8) з сполуки 7 35 23 UA 100192 C2 Boc N N N R4 N O R5 O S R9 8 5 10 R6 R8 R7 До суміші заміщеного або незаміщеного трет-бутил 4-(2-алкіл-1H-бензо[d]імідазол-4o іл)піперазину (7) у 5 мл DMF додавали гідрид натрію (2,0 екв.) при 0 C. Отриману суспензію перемішували при кімнатній температурі протягом 30 хв., після чого додавали заміщений або незаміщений арилсульфонілхлорид. Суміш перемішували при кімнатній температурі до завершення реакції як показано за допомогою РХ/MС. Розчин виливали у 100 мл H2O та отриману тверду речовину відділяли від розчину відсмоктуванням фільтруванням, та висушували у вакуумі. Методика одержання 2-алкіл-4-(4-алкілпіперазин-1-іл)-1-(арилсульфоніл)-1Hбензо[d]імідазолу (I) з сполуки 8: R2 N N N R4 N O R5 O S R9 R6 R8 15 20 25 30 35 R7 Сполуку 8 розчиняли у дихлорметані (CH2Cl2), після чого додавали у надлишку TFA. Суміш перемішували при кімнатній температурі до завершення реакції як показано за допомогою РХ/MС. Розчинник видаляли у вакуумі та суспендували у дихлорметані після чого додавали карбонат натрію калію. Реакційну суміш фільтрували крізь шар Celite™ та фільтрат 2 відновлювали у вакуумі, одержуючи бажану вільну основу. Де R не означає H, до суміші вільної основи у дихлоретані додавали альдегід (1,20 екв.), після чого додавали натрій триацетоксиборгідрид (1,6 екв.). Реакційну суміш перемішували протягом ночі, розчинник випаровували, та залишок очищали за допомогою флеш-хроматографії, використовуючи дихлорметан/метанол (5-20%). Методика одержання 2-алкіл-4-(4-алкілпіперазин-1-іл)-1-(арилсульфоніл)-1Hбензо[d]імідазолу (I) з сполуки (10) Спосіб D Сполуку формули I альтернативно одержують з проміжної сполуки 10 за загальною методикою, описаною для одержання сполуки 8. Методика одержання сполуки (10) Суміш 4-амінобензімідазолу, біс(хлоретил)алкіламіну перемішували у 25 мл 1-бутанолу з o бікарбонатом натрію (3,0 екв). Суміш кип‟ятили зі зворотнім холодильником (115 C олійна баня) протягом ночі. Суміш охолоджували, фільтрували крізь шар Celite™ та фільтрат концентрували у вакуумі. Неочищений залишок очищали на колонці з силікагелем до виходу бажаного продукту. Дивитись також методику синтезу наведену у: WO 2006/009734; Villemin et al., Synthetic Communications 1996 26 (15), 2895-2899; та Marcos et al., Tetrahedron 1991 47(35), 7459-64 (включено у даному документі за допомогою посилань). 24 UA 100192 C2 Кожен з наступних прикладів сполук одержували за вищенаведеною методикою. Приклад 1: 4-(4-метилпіперазин-1-іл)-1-(нафталін-1-ілсульфоніл)-1H-бензо[d]імідазол N N N N O O S 5 10 Цю сполуку одержували, як описано вище; MС (EС) m/z 407,15; 1H ЯМР (400 MГц, хлороформ-d) млн.ч. 2,44 (с, 3 H) 2,71 - 2,81 (м, 4 H) 3,51 - 3,59 (м, 4 H) 6,67 (дд, J=7,8, 1,3 Гц, 1 H) 7,15 – 7,25 (м, 1 H) 7,56 – 7,65 (м, 2 H) 7,65 – 7,70 (м, 1 H) 7,89 – 7,94 (м, 1 H) 8,12 - 8,17 (м, J=8,4 Гц, 1 H) 8,49 (дд, J=7,5, 1,3 Гц, 1 H) 8,54 (с, 1 H) 8,66 (дд, J=8,7, 0,8 Гц, 2 H). Приклад 2: 1-(нафталін-1-ілсульфоніл)-4-(піперазин-1-іл)-1H-бензо[d]імідазол H N N N N O O S 1 15 Цю сполуку одержували, як описано вище; MС (EС) m/z 393,13; H ЯМР (400 MГц, ДMСO-d6) млн.ч. 2,79 – 2,85 (м, 4 H); 3,29 – 3,33 (м, 4 H); 3,37 – 3,43 (м, 1 H); 6,61 (дд, J=7,8, 1,0 Гц, 1 H); 7,07 - 7,18 (м, 2 H); 7,66 - 7,72 (м, 1 H); 7,74 - 7,84 (м, 2 H); 8,13 (д, J=7,6 Гц, 1 H); 8,41 (д, J=8,5 Гц, 1 H); 8,64 (дд, J=8,5, 0,7 Гц, 1 H); 8,69 (дд, J=7,4, 1,1 Гц, 1 H); 9,08 (с, 1 H). Приклад 3: 1-(фенілсульфоніл)-4-(піперазин-1-іл)-1H-бензо[d]імідазол H N N N N O O S 20 1 25 Цю сполуку одержували, як описано вище: MС (EС) m/z 343,12; H ЯМР (400 MГц, ДMСO-d6) млн.ч. 3,24 - 3,31 (м, 4 H); 3,63 – 3,70 (м, 4 H); 6,81 (д, J=7,8 Гц, 1 H) 7,31 (т, J=8,1 Гц, 1 H) 7,42 (д, J=7,6 Гц, 1 H) 7,67 (т, J=7,8 Гц, 2 H) 7,78 (тт, J=7,5, 1,2 Гц, 1 H) 8,11 - 8,16 (м, 2 H) 8,77 (ш, с, 1 H) 8,79 (с, 1 H). 25 UA 100192 C2 Приклад 4: 2-метил-1-(1-нафтилсульфоніл)-4-піперазин-1-іл-1H-бензімідазол H N N N N O O S 5 Цю сполуку одержували, як описано вище: MС (EС) m/z 407,0; H ЯМР (400 MГц, ДMСO-d6) млн.ч. 2,69 (с, 3 H); 2,79 - 2,90 (м, 4 H); 3,33 - 3,49 (м, 4 H); 3,56 - 3,63 (м, 1 H); 6,67 (д, J=7,8 Гц, 1 H); 7,16 (т, J=7,9 Гц, 1 H); 7,26 (д, J=8,1 Гц, 1 H); 7,69 (дт, J=12,6, 6,6 Гц, 2 H); 7,76 (т, J=7,8 Гц, 1 H); 8,16 (д, J=7,1 Гц, 1 H); 8,24 (д, J=7,1 Гц, 1 H); 8,33 (д, J=7,8 Гц, 1 H); 8,41 (д, J=8,3 Гц, 1 H). Приклад 5: 2-метил-1-(фенілсульфоніл)-4-піперазин-1-іл-1H-бензімідазол 1 10 H N N N N O O S Цю сполуку одержували, як описано вище: MС (EС) m/z 357,0; H ЯМР (400 MГц, ДMСO-d6) млн.ч. 2,78 (с, 3 H); 2,81 - 2,86 (м, 4 H); 3,27 - 3,33 (м, 5 H); 6,67 (д, J=8,1 Гц, 1 H); 7,19 (т, J=8,2 Гц, 1 H); 7,39 (д, J=8,1 Гц, 1 H); 7,65 (т, J=7,9 Гц, 2 H); 7,77 (т, J=7,4 Гц, 1 H); 8,04 (д, J=7,6 Гц, 2 H). Приклад 6: 2-етил-1-(фенілсульфоніл)-4-піперазин-1-іл-1H-бензімідазол 1 15 H N N N N O O S 20 Цю сполуку одержували, як описано вище: MС (EС) m/z 371,1; H ЯМР (400 MГц, ДMСO-d6) млн.ч. 1,30 (т, J=7,3 Гц, 3 H); 2,78 - 2,84 (м, 4 H); 3,13 (к, J=7,3 Гц, 2 H); 3,22 - 3,31 (м, 5 H); 6,63 (д, J=7,3 Гц, 1 H); 7,14 (т, J=8,2 Гц, 1 H); 7,35 (дд, J=8,1, 0,7 Гц, 1 H); 7,56 - 7,62 (м, 2 H); 7,69 7,74 (м, 1 H); 7,94 - 7,97 (м, 2 H). Приклад 7: 4-(4-етилпіперазин-1-іл)-1-(фенілсульфоніл)-1H-бензімідазол 1 25 26 UA 100192 C2 N N N N O O S Цю сполуку одержували, як описано вище: MС (EС) m/z 371,1; H ЯМР (400 MГц, ДMСO-d6) млн.ч. 1,27 (т, J=7,3 Гц, 3 H); 3,09 - 3,25 (м, 5 H); 3,57 (д, J=11,0 Гц, 2 H); 4,34 (д, J=11,2 Гц, 2 H); 6,82 (д, J=7,6 Гц, 1 H); 7,31 (т, J=8,1 Гц, 1 H); 7,43 (д, J=7,8 Гц, 1 H); 7,67 (т, J=7,8 Гц, 2 H); 7,76 7,81 (м, 1 H); 8,12 - 8,16 (м, J=7,3 Гц, 2 H); 8,80 (с, 1 H); 10,22 (с, 1 H). Приклад 8: 2-бутил-1-(фенілсульфоніл)-4-піперазин-1-іл-1H-бензімідазол 1 5 H N N N N O O S 10 Цю сполуку одержували, як описано вище: MС (EС) m/z 399,1; H ЯМР (400 MГц, ДMСO-d6) млн.ч. 0,92 (т, J=7,4 Гц, 3 H); 1,36 – 1,48 (м, 2 H); 1,71 - 1,82 (м, 2 H); 2,81 - 2,87 (м, 2 H); 3,14 (т, J=7,4 Гц, 2 H); 3,21 - 3,26 (м, 2 H); 3,33 - 3,39 (м, 5 H); 6,67 (д, J=8,3 Гц, 1 H); 7,15 - 7,21 (м, 1 H); 7,36 - 7,41 (м, 1 H); 7,61 - 7,67 (м, J=7,8, 7,8 Гц, 2 H); 7,73 - 7,79 (м, 1 H); 7,96 - 8,00 (м, 2 H). Приклад 9: 2-метил-4-(4-метилпіперазин-1-іл)-1-(1-нафтилсульфоніл)-1H-бензімідазол 1 15 N N N N O O S Цю сполуку одержували, як описано вище: MС m/z 421,1; H ЯМР (400 MГц, ДMСO-d6) млн.ч. 2,21 (с, 3 H); 2,44 - 2,49 (м, 4 H); 2,69 (с, 3 H); 3,37 - 3,44 (м, 4 H); 6,69 (дд, J=8,1, 0,7 Гц, 1 H); 7,16 (т, J=8,1 Гц, 1 H); 7,27 (дд, J=8,3, 0,7 Гц, 1 H); 7,66 - 7,73 (м, 2 H); 7,74 - 7,79 (м, 1 H); 8,14 - 8,18 (м, 1 H); 8,25 (дд, J=7,6, 1,0 Гц, 1 H); 8,31 - 8,34 (м, J=7,8 Гц, 1 H); 8,41 (д, J=8,3 Гц, 1 H). Приклад 10: 1-[(4-хлорфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол 1 20 25 27 UA 100192 C2 H N N N N O O S Cl Цю сполуку одержували, як описано вище: MС (EС) m/z 377,1; H ЯМР (400 MГц, ДMСO-d6) млн.ч. 2,82 - 2,87 (м, 4 H); 3,33 - 3,37 (м, 5 H); 6,70 (дд, J=7,7, 1,1 Гц, 1 H); 7,25 (т, J=7,9 Гц, 1 H); 7,28 - 7,31 (м, 1 H); 7,74 (дт, J=9,2, 2,5 Гц, 2 H); 8,14 (дт, J=9,1, 2,5 Гц, 2 H); 8,70 (с, 1 H). Приклад 11: 1-[(2-хлорфеніл)сульфоніл]-4-піперазин-1-іл-1H-бензімідазол 1 5 H N N N N O O S 10 Cl Цю сполуку одержували, як описано вище: MС (EС) m/z 377,1; H ЯМР (400 MГц, ДMСO-d6) млн.ч. 2,84 - 2,90 (м, 4 H); 3,35 - 3,44 (м, 5 H); 6,69 (д, J=8,1 Гц, 1 H); 6,97 (д, J=8,1 Гц, 1 H); 7,17 (т, J=8,1 Гц, 1 H); 7,68 - 7,75 (м, 2 H); 7,77 - 7,84 (м, 1 H); 8,46 (дд, J=7,8, 1,2 Гц, 1 H); 8,75 (с, 1 H). Приклад 12: 4-(4-метилпіперазин-1-іл)-1-(фенілсульфоніл)-1H-бензімідазол 1 15 N N N N O O S 20 25 Цю сполуку одержували, як описано вище: MС (EС) m/z 357,1; 1H ЯМР (400 MГц, хлороформ-d) млн.ч. 2,37 (с, 3 H) 2,63 - 2,69 (м, 4 H) 3,50 - 3,57 (м, 4 H) 6,72 (дд, J=8,1, 0,9 Гц, 1 H) 7,24 - 7,30 (м, 1 H) 7,42 (дд, J=8,3, 0,9 Гц, 1 H) 7,47 - 7,54 (м, 2 H) 7,62 (тт, J=7,4, 1,2 Гц, 1 H) 7,95 - 8,00 (м, 2 H) 8,29 (с, 1 H) БІОЛОГІЧНІ ДОСЛІДЖЕННЯ: Афінність зв‟язування 5-HT6 CHO-Dukx-A2 клітини, які експресують 5-HT6 підтип рецептора серотоніну (клон 50-7), вирощені зрощеними групами по 10-клітин, розділяли та збирали у PBS буфері, який містив 5 28
ДивитисяДодаткова інформація
Назва патенту англійською1-(arylsulfonyl)-4-(piperazin-1-yl)-1h-benzimidazoles as 5-hydroxytryptamine-6 ligands
Автори англійськоюHaydar, Simon N., Andrae, Patrick M., Yun, Heedong, Robichaud, Albert J.
Назва патенту російською1-(арилсульфонил)-4-(пиперазин-1-ил)-1н-бензимидазолы как лиганды 5-гидрокситриптамина-6
Автори російськоюХейдер Саймон Н., Андре Патрик М., Юн Хидонг, Робишо Альберт Дж.
МПК / Мітки
МПК: C07D 403/04, A61K 31/496, C07D 235/22, C07D 487/08, A61P 25/00
Мітки: 5-гідрокситриптаміну-6, ліганди, 1-(арилсульфоніл)-4-(піперазин-1-іл)-1н-бензімідазоли
Код посилання
<a href="https://ua.patents.su/59-100192-1-arilsulfonil-4-piperazin-1-il-1n-benzimidazoli-yak-ligandi-5-gidroksitriptaminu-6.html" target="_blank" rel="follow" title="База патентів України">1-(арилсульфоніл)-4-(піперазин-1-іл)-1н-бензімідазоли як ліганди 5-гідрокситриптаміну-6</a>
Попередній патент: Спосіб охорони підготовчої виробки
Наступний патент: Спосіб оброблення вапняку відхідними конвертерними газами з одержанням м’якообпаленого вапна
Випадковий патент: Захисний футляр для принаймні двох кредитних карток або подібних виробів












