Заміщені похідні 3-сульфоніліндазолу як ліганди 5-гідрокситриптаміну-6
Номер патенту: 94053
Опубліковано: 11.04.2011
Автори: Ло Дженніфер Ребекка, Грінфілд Елікзандер Алексей, Лі Янфанг, Ліу Кевін, Макфарлейн Джералдін Рут, Гросану Крістіна, Елокдах Хассан Махмуд, Макдевітт Роберт Емметт, Бернотас Рональд Чарльз, Робішо Альберт Джин
Формула / Реферат
1. Сполука формули І
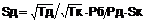 , (І)
, (І)
де
X є О, S, NR, CH2, CH2Y, CH2Z, CO, CONR або NRCO;
Y є О, S або NR;
Z є CO;
n є 0 або цілим числом 1, 2, 3,4, 5 або 6, якщо Х є СН2;
n є цілим числом 1, 2, 3, 4, 5 або 6, якщо X є CH2Z, CO або NRCO;
n є цілим числом 2, 3, 4, 5 або 6, якщо X є О, S, NR, CH2Y або CONR;
R є Н або необов'язково заміщеною алкільною групою;
R1 є Н або алкільною, циклоалкільною, арильною або гетероарильною групою, кожна з яких необов'язково є заміщеною;
R2 є необов'язково заміщеною алкільною, циклоалкільною, арильною або гетероарильною групою або необов'язково заміщеною 8-13-членною біциклічною або трициклічною кільцевою системою, яка має атом N у голові містка і необов'язково містить 1, 2 або 3 додаткові гетероатоми, вибрані з-поміж N, О або S;
R3 та R4 кожен незалежно є Н або необов'язково заміщеною алкільною групою;
R5 та R6 кожен незалежно є Н або алкільною, алкенільною, алкінільною, циклоалкільною, циклогетероалкільною, арильною або гетероарильною групою, кожна з яких необов'язково є заміщеною, або R5 та R6 можуть бути взяті разом з атомом, до якого вони приєднуються, для утворення необов'язково заміщеного 3-7-членного кільця, яке необов'язково містить додатковий гетероатом, вибраний з-поміж О, N або S;
R7 є галогеном, CN, OR8, CO2R9, CONR10R11 або алкільною, алкенільною, алкінільною, циклоалкільною, циклогетероалкільною, арильною або гетероарильною групою, кожна з яких є необов'язково заміщеною;
m є цілим числом 0, 1, 2 або 3;
R8 є Н, COR12 або алкільною, алкенільною, алкінільною, арильною або гетероарильною групою, кожна з яких необов'язково є заміщеною;
R9 є Н або С1-С6алкільною, арильною або гетероарильною групою, кожна з яких необов'язково є заміщеною;
R10 та R11 кожен незалежно є Н або необов'язково заміщеною алкільною групою; і
R12 є необов'язково заміщеною С1-С6алкільною, циклоалкільною, циклогетероалкільною, арильною або гетероарильною групою; або
її стереоізомер або фармацевтично прийнятна сіль.
2. Сполука за п. 1, яка відрізняється тим, що Х є О, NR aбo CH2.
3. Сполука за п. 2, яка відрізняється тим, що Х є О.
4. Сполука за будь-яким з пп. з 1 по 3, яка відрізняється тим, що n є 2 або 3.
5. Сполука за будь-яким з пп. з 1 по 4, яка відрізняється тим, що R2 є необов'язково заміщеною арильною або гетероарильною групою або необов'язково заміщеною 8-13-членною біциклічною або трициклічною кільцевою системою, яка має атом N у голові містка і необов'язково містить 1, 2 або 3 додаткові гетероатоми, вибрані з-поміж N, О або S.
6. Сполука за п. 5, яка відрізняється тим, що R2 є необов'язково заміщеною фенільною, нафтильною або імідазотіазолільною групою.
7. Сполука за будь-яким з пп. з 1 по 6, яка відрізняється тим, що R5 та R6 кожен незалежно є Н або С1-С4алкілом.
8. Сполука за будь-яким з пп. з 1 по 7, яка відрізняється тим, що R2 є нафтилом, і n є 3.
9. Сполука за п. 1, вибрана з групи, до якої, головним чином, належать:
N,N-диметил-3-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]окси}пропан-1-амін;
N-метил-Н-{2-[3-(фенілсульфоніл)-1Н-індазол-5-іл]етил}амін;
N,N-диметил-N-{2-[3-(фенілсульфоніл)-1Н-індазол-5-іл]етил}амін;
{2-[3-(фенілсульфоніл)-1H-індазол-7-іл]етил}амін;
N,N-диметил-N-{2-[3-(фенілсульфоніл)-1Н-індазол-7-іл]етил}амін;
N-{2-[3-(фенілсульфоніл)-1Н-індазол-7-іл]етил}циклопропанамін;
N,N-диметил-N-{3-[3-(фенілсульфоніл)-1Н-індазол-5-іл]пропіл}амін;
N-{3-[3-(фенілсульфоніл)-1Н-індазол-5-іл]пропіл}циклопропанамін;
{3-[3-(фенілсульфоніл)-1Н-індазол-5-іл]пропіл}амін;
{4-[3-(фенілсульфоніл)-1Н-індазол-5-іл]бутил}амін;
N-мeтил-N-{2-[3-(фенілсульфоніл)-1Н-індазол-7-іл]етил}амін;
N-[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]етан-1,2-діамін;
N,N-диметил-2-{[3-(фенілсульфоніл)-1Н-індазол-5-іл]оксі}етанамін;
3-(фенілсульфоніл)-5-(2-піперидин-1-ілетоксі)-1Н-індазол;
3-(1-нафтилсульфоніл)-5-(2-піролідин-1-ілетоксі)-1Н-індазол;
N,N-диметил-2-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етанамін;
N-(2-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етил)циклопентанамін;
5-(2-морфолін-4-ілетокси)-3-(1-нафтилсульфоніл)-1Н-індазол;
N-етил-N-метил-2-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етанамін;
N-(2-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етил)бутан-1-амін;
N1-[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]-бета-аланінамід;
N-етил-2-{[3-(фенілсульфоніл)-1Н-індазол-5-іл]оксі}етанамін;
N-(2-{[3-(фенілсульфоніл)-1Н-індазол-5-іл]оксі}етил)пропан-2-амін;
N-(2-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етил)пропан-2-амін;
N-етил-2-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етанамін;
N-метил-2-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етанамін;
1-метил-3-(1-нафтилсульфоніл)-7-(2-піперидин-1-ілетоксі)-1Н-індазол;
3-(1-нафтилсульфоніл)-5-(2-піперидин-1-ілетоксі)-1Н-індазол;
3-(2-аміноетил)-1-[(2,5-диметоксифеніл)сульфоніл]-1,3-дигідро-2Н-імідазо[4,5-b]піридин-2-он;
N,N-діетил-2-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етанамін;
N-(2-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етил)циклопропанамін;
1-(3-хлоробензил)-3-(1-нафтилсульфоніл)-7-(2-піперидин-1-ілетоксі)-1Н-індазол;
1-(3-хлоробензил)-3-(1-нафтилсульфоніл)-7-(2-піролідин-1-ілетоксі)-1Н-індазол;
(2S)-3-метил-N1-[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]бутано-1,2-діамін;
(2-{[1-(3-хлоробензил)-3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]оксі}етил)амін;
N-(2-{[3-(фенілсульфоніл)-1Н-індазол-5-іл]оксі}етил)циклопентанамін;
3-(фенілсульфоніл)-5-(2-піролідин-1-ілетоксі)-1Н-індазол;
N-метил-2-{[3-(фенілсульфоніл)-1Н-індазол-5-іл]оксі}етанамін;
N-метил-2-{[1-метил-3-(фенілсульфоніл)-1Н-індазол-7-іл]оксі}етанамін;
1-метил-3-(фенілсульфоніл)-7-(2-піролідин-1-ілетоксі)-1Н-індазол;
(2-{[1-(3-хлоробензил)-3-(фенілсульфоніл)-1Н-індазол-7-іл]оксі}етил)метиламін;
(2-{[1-(3-хлоробензил)-3-(фенілсульфоніл)-1Н-індазол-7-іл]оксі}етил)етиламін;
1-(3-хлоробензил)-3-(фенілсульфоніл)-7-(2-піролідин-1-ілетоксі)-1Н-індазол;
1-(3-хлоробензил)-5-метокси-3-(1-нафтилсульфоніл)-7-(2-піперидин-1-ілетоксі)-1Н-індазол;
N-метил-2-{[3-(фенілсульфоніл)-1Н-індазол-7-іл]оксі}етанамін;
(2-{[1-(3-хлоробензил)-3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]оксі}етил)етиламін;
(2-{[1-(3-хлоробензил)-3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]оксі}етил)метиламін;
N-етил-2-{[3-(фенілсульфоніл)-1Н-індазол-7-іл]оксі}етанамін;
N,N-діетил-2-{[3-(фенілсульфоніл)-1Н-індазол-7-іл]оксі}етанамін;
N-(2-{[3-(фенілсульфоніл)-1Н-індазол-7-іл]оксі}етил)бутан-1-амін;
3-(фенілсульфоніл)-7-(2-піролідин-1-ілетоксі)-1Н-індазол;
3-(фенілсульфоніл)-7-(2-піперидин-1-ілетоксі)-1Н-індазол;
N,N-діетил-2-{[1-метил-3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]оксі}етанамін;
1-метил-3-(1-нафтилсульфоніл)-7-(2-піролідин-1-ілетоксі)-1Н-індазол;
N-етил-2-{[1-метил-3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]оксі}етанамін;
3-(1-нафтилсульфоніл)-7-(2-піперидин-1-ілетоксі)-1Н-індазол;
3-(1-нафтилсульфоніл)-7-(2-піролідин-1-ілетоксі)-1Н-індазол;
N-етил-2-{[3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]оксі}етанамін;
(2-{[3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]оксі}етил)амін;
(2-{[1-(3-хлоробензил)-5-фторо-3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]оксі}етил)-диметиламін;
(2-{[1-бензил-3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етил)метиламін;
(2-{[1-бензил-3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етил)диметиламін;
(2-{[1-бензил-3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етил)етиламін;
N-метил-2-{[3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]оксі}етанамін;
N,N-диметил-2-{[3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]оксі}етанамін;
5-фторо-3-(1-нафтилсульфоніл)-7-(2-піролідин-1-ілетоксі)-1Н-індазол;
5-фторо-3-(1-нафтилсульфоніл)-7-(2-піперидин-1-ілетоксі)-1Н-індазол;
N,N-діетил-2-{[5-фторо-3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]оксі}етанамін;
(2-{[5-фторо-3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]оксі}етил)диметиламін;
N-етил-2-{[5-фторо-3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]оксі}етанамін;
(2-{[1-(3-хлоробензил)-3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етил)-диметиламін;
N-метил-3-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]окси}пропан-1-амін;
N-етил-N-метил-3-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]окси}пропан-1-амін;
3-(1-нафтилсульфоніл)-5-(3-піперидин-1-ілпропоксі)-1Н-індазол;
N,N-диметил-3-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]окси}пропан-1-амін;
N,N-діетил-3-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]окси}пропан-1-амін;
N-(3-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]окси}пропіл)бутан-1-амін;
3-(1-нафтилсульфоніл)-5-(3-піролідин-1-ілпропоксі)-1Н-індазол;
(2-{[5-метокси-3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]оксі}етил)метиламін;
(2-{[5-метокси-3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]оксі}етил)диметиламін;
5-метокси-3-(1-нафтилсульфоніл)-7-(2-піролідин-1-ілетоксі)-1Н-індазол;
5-метокси-3-(1-нафтилсульфоніл)-7-(2-піперидин-1-ілетоксі)-1Н-індазол;
(2-{[1-(3-хлоробензил)-3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етил)етиламін;
(3-{[1-(3-хлоробензил)-3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]оксі}пропіл)-діетиламін;
1-(3-хлоробензил)-3-(1-нафтилсульфоніл)-7-(3-піролідин-1-ілпропоксі)-1Н-індазол;
N-метил-3-{[3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]окси}пропан-1-амін;
N,N-дiетил-3-{[3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]окси}пропан-1-амін;
N-метил-2-{[1-метил-3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етанамін;
N,N-диметил-2-{[1-метил-3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етанамін;
N-етил-N-метил-2-{[1-метил-3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етанамін;
N-етил-2-{[1-метил-3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етанамін;
N,N-діетил-2-{[1-метил-3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етанамін;
N-(2-{[1-метил-3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етил)пропан-2-амін;
1-метил-3-(1-нафтилсульфоніл)-5-(2-піролідин-1-ілетоксі)-1Н-індазол;
{3-[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]пропіл}амін;
(2-{[1-метил-3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]оксі}етил)амін;
N-етил-3-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]окси}пропан-1-амін;
N-ізопропіл-3-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]окси}пропан-1-амін;
N-(3-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]окси}пропіл)циклопентанамін;
5-(3-морфолін-4-ілпропокси)-3-(1-нафтилсульфоніл)-1Н-індазол;
N-(3-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]окси}пропіл)циклопропанамін;
(3-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]окси}пропіл)амін;
N-метил-4-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]окси}бутан-1-амін;
N,N-диметил-4-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]окси}бутан-1-амін;
N-етил-4-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]окси}бутан-1-амін;
N,N-дieтил-4-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]окси}бутан-1-амін;
N-метил-4-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]окси}-N-пропілбутан-1-амін;
3-(1-нафтилсульфоніл)-5-(4-піролідин-1-ілбутоксі)-1Н-індазол;
3-(1-нафтилсульфоніл)-5-(4-піперидин-1-ілбутоксі)-1Н-індазол;
(4-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]окси}бутил)амін;
(2-{[5-фторо-3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]оксі}етил)метиламін;
5-[(4-метилпіперазин-1-іл)метил]-3-(1-нафтилсульфоніл)-1Н-індазол;
3-(1-нафтилсульфоніл)-5-(піперазин-1-ілметил)-1Н-індазол;
N-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]метил}етан-1,2-діамін;
N-метил-3-[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]пропан-1-амін;
N,N-диметил-4-[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]бутан-1-амін;
N,N-диметил-3-[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]пропан-1-амін;
N-етил-N-метил-3-[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]пропан-1-амін;
N-ізопропіл-3-[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]пропан-1-амін;
N-етил-N-метил-4-[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]бутан-1-амін;
(2-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етил)амін;
3-(1-нафтилсульфоніл)-5-(3-піролідин-1-ілпропіл)-1Н-індазол;
N-ізопропіл-4-[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]бутан-1-амін;
3-(1-нафтилсульфоніл)-5-(4-піролідин-1-ілбутил)-1Н-індазол;
N-етил-4-[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]бутан-1-амін;
5-[(3-метилпіперазин-1-іл)метил]-3-(1-нафтилсульфоніл)-1Н-індазол;
5-[(3,5-диметилпіперазин-1-іл)метил]-3-(1-нафтилсульфоніл)-1Н-індазол;
N-етил-3-[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]пропан-1-амін;
{4-[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]бутил}амін;
5-[1-(4-метилпіперазин-1-іл)етил]-3-(1-нафтилсульфоніл)-1Н-індазол;
N,N,N'-тpимeтил-N'-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]метил}етан-1,2-діамін;
N,N-диметил-2-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]метоксі}етанамін;
5-{[(3R)-3-метилпіперазин-1-іл]метил}-3-(1-нафтилсульфоніл)-1Н-індазол;
5-{[(3S)-3-метилпіперазин-1-іл]метил}-3-(1-нафтилсульфоніл)-1Н-індазол;
(3S)-N-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]метил}піролідин-3-амін;
(3R)-l-{[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]метил}піролідин-3-амін;
N-[2-(диметиламіно)етил]-3-(1-нафтилсульфоніл)-1Н-індазол-5-карбоксамід;
2-{[5-фторо-3-(фенілсульфоніл)-1Н-індазол-7-іл]оксі}етанамін;
N-[3-(1-нафтилсульфоніл)-1Н-індазол-6-іл]-бета-аланінамід;
N-[3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]-3-піперидин-1-ілпропанамід;
N3,N3-диметил-N-[3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]-бета-аланінамід;
2-{[3-(фенілсульфоніл)-1Н-індазол-7-іл]оксі}етанамін;
N-[3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]-бета-аланінамід;
N-[3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]етан-1,2-діамін;
N-[3-(1-нафтилсульфоніл)-1Н-індазол-6-іл]-3-піперидин-1-ілпропанамід;
N-[3-(1-нафтилсульфоніл)-1Н-індазол-6-іл]етан-1,2-діамін;
N3,N3-діетил-N-[3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]-бета-аланінамід;
N,N-диметил-2-{[3-(1-нафтилсульфоніл)-1Н-індазол-4-іл]оксі}етанамін;
3-(1-нафтилсульфоніл)-4-(2-піперидин-1-ілетоксі)-1Н-індазол;
3-(1-нафтилсульфоніл)-4-(2-піролідин-1-ілетоксі)-1Н-індазол;
2-{[3-(1-нафтилсульфоніл)-1Н-індазол-4-іл]оксі}етанамін;
N-метил-2-{[3-(1-нафтилсульфоніл)-1Н-індазол-6-іл]оксі}етанамін;
2-{[3-(1-нафтилсульфоніл)-1Н-індазол-6-іл]оксі}етанамін;
її стереоізомери та її фармацевтично прийнятні солі.
10. Спосіб лікування від порушення центральної нервової системи, яке є пов'язаним з 5-НТ6-рецептором або зазнає його впливу, у пацієнта, який цього потребує, включаючи введення вищезгаданому пацієнтові терапевтично ефективної кількості сполуки формули І за будь-яким з пп. з 1 по 9.
11. Спосіб за п. 10, який відрізняється тим, що вищезгадане порушення є порушенням когнітивної функції, порушенням розвитку або нейродегенеративним порушенням.
12. Спосіб за п. 11, який відрізняється тим, що вищезгадане порушення є порушенням когнітивної функції.
13. Спосіб за п. 11, який відрізняється тим, що вищезгадане порушення є вибраним з групи, яка складається з порушення здатності до навчання; дефіциту уваги; синдрому Дауна, синдрому ламкої хромосоми X або аутизму.
14. Спосіб за п. 11, який відрізняється тим, що вищезгадане порушення є інсультом або черепно-мозковою травмою.
15. Фармацевтична композиція, яка містить фармацевтично прийнятний носій та ефективну кількість сполуки формули І за будь-яким з пп. з 1 по 9.
16. Спосіб одержання сполуки формули І за будь-яким з пп. з 1 по 9, в якому здійснюють: реакцію сполуки формули II
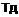 , (II)
, (II)
де X, R2, R3, R4, R5, R6, R7, m та n є такими, як описано вище для формули І;
з NaNO2 у присутності кислоти з одержанням сполуки формули І, де R1 є Н; і, необов'язково, реакцію вищезгаданої сполуки з R1-Hal, де Hal є Сl, Вr або І, і R1 є алкільною, циклоалкільною, арильною або гетероарильною групою, кожна з яких необов'язково є заміщеною.
Текст
1. Сполука формули І R6 C2 2 (19) 1 3 4. Сполука за будь-яким з пп. з 1 по 3, яка відрізняється тим, що n є 2 або 3. 5. Сполука за будь-яким з пп. з 1 по 4, яка відрізняється тим, що R2 є необов'язково заміщеною арильною або гетероарильною групою або необов'язково заміщеною 8-13-членною біциклічною або трициклічною кільцевою системою, яка має атом N у голові містка і необов'язково містить 1, 2 або 3 додаткові гетероатоми, вибрані з-поміж N, О або S. 6. Сполука за п. 5, яка відрізняється тим, що R2 є необов'язково заміщеною фенільною, нафтильною або імідазотіазолільною групою. 7. Сполука за будь-яким з пп. з 1 по 6, яка відрізняється тим, що R5 та R6 кожен незалежно є Н або С1-С4алкілом. 8. Сполука за будь-яким з пп. з 1 по 7, яка відрізняється тим, що R2 є нафтилом, і n є 3. 9. Сполука за п. 1, вибрана з групи, до якої, головним чином, належать: N,N-диметил-3-{[3-(1-нафтилсульфоніл)-1Ніндазол-5-іл]окси}пропан-1-амін; N-метил-Н-{2-[3-(фенілсульфоніл)-1Н-індазол-5іл]етил}амін; N,N-диметил-N-{2-[3-(фенілсульфоніл)-1Н-індазол5-іл]етил}амін; {2-[3-(фенілсульфоніл)-1H-індазол-7-іл]етил}амін; N,N-диметил-N-{2-[3-(фенілсульфоніл)-1Н-індазол7-іл]етил}амін; N-{2-[3-(фенілсульфоніл)-1Н-індазол-7іл]етил}циклопропанамін; N,N-диметил-N-{3-[3-(фенілсульфоніл)-1Н-індазол5-іл]пропіл}амін; N-{3-[3-(фенілсульфоніл)-1Н-індазол-5іл]пропіл}циклопропанамін; {3-[3-(фенілсульфоніл)-1Н-індазол-5іл]пропіл}амін; {4-[3-(фенілсульфоніл)-1Н-індазол-5-іл]бутил}амін; N-мeтил-N-{2-[3-(фенілсульфоніл)-1Н-індазол-7іл]етил}амін; N-[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]етан1,2-діамін; N,N-диметил-2-{[3-(фенілсульфоніл)-1Н-індазол-5іл]оксі}етанамін; 3-(фенілсульфоніл)-5-(2-піперидин-1-ілетоксі)-1Ніндазол; 3-(1-нафтилсульфоніл)-5-(2-піролідин-1-ілетоксі)1Н-індазол; N,N-диметил-2-{[3-(1-нафтилсульфоніл)-1Ніндазол-5-іл]оксі}етанамін; N-(2-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]оксі}етил)циклопентанамін; 5-(2-морфолін-4-ілетокси)-3-(1-нафтилсульфоніл)1Н-індазол; N-етил-N-метил-2-{[3-(1-нафтилсульфоніл)-1Ніндазол-5-іл]оксі}етанамін; N-(2-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]оксі}етил)бутан-1-амін; N1-[3-(1-нафтилсульфоніл)-1Н-індазол-5-іл]-бетааланінамід; N-етил-2-{[3-(фенілсульфоніл)-1Н-індазол-5іл]оксі}етанамін; N-(2-{[3-(фенілсульфоніл)-1Н-індазол-5іл]оксі}етил)пропан-2-амін; 94053 4 N-(2-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]оксі}етил)пропан-2-амін; N-етил-2-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]оксі}етанамін; N-метил-2-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]оксі}етанамін; 1-метил-3-(1-нафтилсульфоніл)-7-(2-піперидин-1ілетоксі)-1Н-індазол; 3-(1-нафтилсульфоніл)-5-(2-піперидин-1-ілетоксі)1Н-індазол; 3-(2-аміноетил)-1-[(2,5диметоксифеніл)сульфоніл]-1,3-дигідро-2Німідазо[4,5-b]піридин-2-он; N,N-діетил-2-{[3-(1-нафтилсульфоніл)-1Н-індазол5-іл]оксі}етанамін; N-(2-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]оксі}етил)циклопропанамін; 1-(3-хлоробензил)-3-(1-нафтилсульфоніл)-7-(2піперидин-1-ілетоксі)-1Н-індазол; 1-(3-хлоробензил)-3-(1-нафтилсульфоніл)-7-(2піролідин-1-ілетоксі)-1Н-індазол; (2S)-3-метил-N1-[3-(1-нафтилсульфоніл)-1Ніндазол-5-іл]бутано-1,2-діамін; (2-{[1-(3-хлоробензил)-3-(1-нафтилсульфоніл)-1Ніндазол-7-іл]оксі}етил)амін; N-(2-{[3-(фенілсульфоніл)-1Н-індазол-5іл]оксі}етил)циклопентанамін; 3-(фенілсульфоніл)-5-(2-піролідин-1-ілетоксі)-1Ніндазол; N-метил-2-{[3-(фенілсульфоніл)-1Н-індазол-5іл]оксі}етанамін; N-метил-2-{[1-метил-3-(фенілсульфоніл)-1Ніндазол-7-іл]оксі}етанамін; 1-метил-3-(фенілсульфоніл)-7-(2-піролідин-1ілетоксі)-1Н-індазол; (2-{[1-(3-хлоробензил)-3-(фенілсульфоніл)-1Ніндазол-7-іл]оксі}етил)метиламін; (2-{[1-(3-хлоробензил)-3-(фенілсульфоніл)-1Ніндазол-7-іл]оксі}етил)етиламін; 1-(3-хлоробензил)-3-(фенілсульфоніл)-7-(2піролідин-1-ілетоксі)-1Н-індазол; 1-(3-хлоробензил)-5-метокси-3-(1нафтилсульфоніл)-7-(2-піперидин-1-ілетоксі)-1Ніндазол; N-метил-2-{[3-(фенілсульфоніл)-1Н-індазол-7іл]оксі}етанамін; (2-{[1-(3-хлоробензил)-3-(1-нафтилсульфоніл)-1Ніндазол-7-іл]оксі}етил)етиламін; (2-{[1-(3-хлоробензил)-3-(1-нафтилсульфоніл)-1Ніндазол-7-іл]оксі}етил)метиламін; N-етил-2-{[3-(фенілсульфоніл)-1Н-індазол-7іл]оксі}етанамін; N,N-діетил-2-{[3-(фенілсульфоніл)-1Н-індазол-7іл]оксі}етанамін; N-(2-{[3-(фенілсульфоніл)-1Н-індазол-7іл]оксі}етил)бутан-1-амін; 3-(фенілсульфоніл)-7-(2-піролідин-1-ілетоксі)-1Ніндазол; 3-(фенілсульфоніл)-7-(2-піперидин-1-ілетоксі)-1Ніндазол; N,N-діетил-2-{[1-метил-3-(1-нафтилсульфоніл)-1Ніндазол-7-іл]оксі}етанамін; 1-метил-3-(1-нафтилсульфоніл)-7-(2-піролідин-1ілетоксі)-1Н-індазол; 5 N-етил-2-{[1-метил-3-(1-нафтилсульфоніл)-1Ніндазол-7-іл]оксі}етанамін; 3-(1-нафтилсульфоніл)-7-(2-піперидин-1-ілетоксі)1Н-індазол; 3-(1-нафтилсульфоніл)-7-(2-піролідин-1-ілетоксі)1Н-індазол; N-етил-2-{[3-(1-нафтилсульфоніл)-1Н-індазол-7іл]оксі}етанамін; (2-{[3-(1-нафтилсульфоніл)-1Н-індазол-7іл]оксі}етил)амін; (2-{[1-(3-хлоробензил)-5-фторо-3-(1нафтилсульфоніл)-1Н-індазол-7-іл]оксі}етил)диметиламін; (2-{[1-бензил-3-(1-нафтилсульфоніл)-1Н-індазол-5іл]оксі}етил)метиламін; (2-{[1-бензил-3-(1-нафтилсульфоніл)-1Н-індазол-5іл]оксі}етил)диметиламін; (2-{[1-бензил-3-(1-нафтилсульфоніл)-1Н-індазол-5іл]оксі}етил)етиламін; N-метил-2-{[3-(1-нафтилсульфоніл)-1Н-індазол-7іл]оксі}етанамін; N,N-диметил-2-{[3-(1-нафтилсульфоніл)-1Ніндазол-7-іл]оксі}етанамін; 5-фторо-3-(1-нафтилсульфоніл)-7-(2-піролідин-1ілетоксі)-1Н-індазол; 5-фторо-3-(1-нафтилсульфоніл)-7-(2-піперидин-1ілетоксі)-1Н-індазол; N,N-діетил-2-{[5-фторо-3-(1-нафтилсульфоніл)-1Ніндазол-7-іл]оксі}етанамін; (2-{[5-фторо-3-(1-нафтилсульфоніл)-1Н-індазол-7іл]оксі}етил)диметиламін; N-етил-2-{[5-фторо-3-(1-нафтилсульфоніл)-1Ніндазол-7-іл]оксі}етанамін; (2-{[1-(3-хлоробензил)-3-(1-нафтилсульфоніл)-1Ніндазол-5-іл]оксі}етил)-диметиламін; N-метил-3-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]окси}пропан-1-амін; N-етил-N-метил-3-{[3-(1-нафтилсульфоніл)-1Ніндазол-5-іл]окси}пропан-1-амін; 3-(1-нафтилсульфоніл)-5-(3-піперидин-1ілпропоксі)-1Н-індазол; N,N-диметил-3-{[3-(1-нафтилсульфоніл)-1Ніндазол-5-іл]окси}пропан-1-амін; N,N-діетил-3-{[3-(1-нафтилсульфоніл)-1Н-індазол5-іл]окси}пропан-1-амін; N-(3-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]окси}пропіл)бутан-1-амін; 3-(1-нафтилсульфоніл)-5-(3-піролідин-1ілпропоксі)-1Н-індазол; (2-{[5-метокси-3-(1-нафтилсульфоніл)-1Н-індазол7-іл]оксі}етил)метиламін; (2-{[5-метокси-3-(1-нафтилсульфоніл)-1Н-індазол7-іл]оксі}етил)диметиламін; 5-метокси-3-(1-нафтилсульфоніл)-7-(2-піролідин-1ілетоксі)-1Н-індазол; 5-метокси-3-(1-нафтилсульфоніл)-7-(2-піперидин1-ілетоксі)-1Н-індазол; (2-{[1-(3-хлоробензил)-3-(1-нафтилсульфоніл)-1Ніндазол-5-іл]оксі}етил)етиламін; (3-{[1-(3-хлоробензил)-3-(1-нафтилсульфоніл)-1Ніндазол-7-іл]оксі}пропіл)-діетиламін; 1-(3-хлоробензил)-3-(1-нафтилсульфоніл)-7-(3піролідин-1-ілпропоксі)-1Н-індазол; N-метил-3-{[3-(1-нафтилсульфоніл)-1Н-індазол-7іл]окси}пропан-1-амін; 94053 6 N,N-дiетил-3-{[3-(1-нафтилсульфоніл)-1Н-індазол7-іл]окси}пропан-1-амін; N-метил-2-{[1-метил-3-(1-нафтилсульфоніл)-1Ніндазол-5-іл]оксі}етанамін; N,N-диметил-2-{[1-метил-3-(1-нафтилсульфоніл)1Н-індазол-5-іл]оксі}етанамін; N-етил-N-метил-2-{[1-метил-3-(1нафтилсульфоніл)-1Н-індазол-5-іл]оксі}етанамін; N-етил-2-{[1-метил-3-(1-нафтилсульфоніл)-1Ніндазол-5-іл]оксі}етанамін; N,N-діетил-2-{[1-метил-3-(1-нафтилсульфоніл)-1Ніндазол-5-іл]оксі}етанамін; N-(2-{[1-метил-3-(1-нафтилсульфоніл)-1Н-індазол5-іл]оксі}етил)пропан-2-амін; 1-метил-3-(1-нафтилсульфоніл)-5-(2-піролідин-1ілетоксі)-1Н-індазол; {3-[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]пропіл}амін; (2-{[1-метил-3-(1-нафтилсульфоніл)-1Н-індазол-7іл]оксі}етил)амін; N-етил-3-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]окси}пропан-1-амін; N-ізопропіл-3-{[3-(1-нафтилсульфоніл)-1Н-індазол5-іл]окси}пропан-1-амін; N-(3-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]окси}пропіл)циклопентанамін; 5-(3-морфолін-4-ілпропокси)-3-(1нафтилсульфоніл)-1Н-індазол; N-(3-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]окси}пропіл)циклопропанамін; (3-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]окси}пропіл)амін; N-метил-4-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]окси}бутан-1-амін; N,N-диметил-4-{[3-(1-нафтилсульфоніл)-1Ніндазол-5-іл]окси}бутан-1-амін; N-етил-4-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]окси}бутан-1-амін; N,N-дieтил-4-{[3-(1-нафтилсульфоніл)-1Н-індазол5-іл]окси}бутан-1-амін; N-метил-4-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]окси}-N-пропілбутан-1-амін; 3-(1-нафтилсульфоніл)-5-(4-піролідин-1-ілбутоксі)1Н-індазол; 3-(1-нафтилсульфоніл)-5-(4-піперидин-1-ілбутоксі)1Н-індазол; (4-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]окси}бутил)амін; (2-{[5-фторо-3-(1-нафтилсульфоніл)-1Н-індазол-7іл]оксі}етил)метиламін; 5-[(4-метилпіперазин-1-іл)метил]-3-(1нафтилсульфоніл)-1Н-індазол; 3-(1-нафтилсульфоніл)-5-(піперазин-1-ілметил)1Н-індазол; N-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]метил}етан-1,2-діамін; N-метил-3-[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]пропан-1-амін; N,N-диметил-4-[3-(1-нафтилсульфоніл)-1Ніндазол-5-іл]бутан-1-амін; N,N-диметил-3-[3-(1-нафтилсульфоніл)-1Ніндазол-5-іл]пропан-1-амін; N-етил-N-метил-3-[3-(1-нафтилсульфоніл)-1Ніндазол-5-іл]пропан-1-амін; 7 N-ізопропіл-3-[3-(1-нафтилсульфоніл)-1Н-індазол5-іл]пропан-1-амін; N-етил-N-метил-4-[3-(1-нафтилсульфоніл)-1Ніндазол-5-іл]бутан-1-амін; (2-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]оксі}етил)амін; 3-(1-нафтилсульфоніл)-5-(3-піролідин-1-ілпропіл)1Н-індазол; N-ізопропіл-4-[3-(1-нафтилсульфоніл)-1Н-індазол5-іл]бутан-1-амін; 3-(1-нафтилсульфоніл)-5-(4-піролідин-1-ілбутил)1Н-індазол; N-етил-4-[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]бутан-1-амін; 5-[(3-метилпіперазин-1-іл)метил]-3-(1нафтилсульфоніл)-1Н-індазол; 5-[(3,5-диметилпіперазин-1-іл)метил]-3-(1нафтилсульфоніл)-1Н-індазол; N-етил-3-[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]пропан-1-амін; {4-[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]бутил}амін; 5-[1-(4-метилпіперазин-1-іл)етил]-3-(1нафтилсульфоніл)-1Н-індазол; N,N,N'-тpимeтил-N'-{[3-(1-нафтилсульфоніл)-1Ніндазол-5-іл]метил}етан-1,2-діамін; N,N-диметил-2-{[3-(1-нафтилсульфоніл)-1Ніндазол-5-іл]метоксі}етанамін; 5-{[(3R)-3-метилпіперазин-1-іл]метил}-3-(1нафтилсульфоніл)-1Н-індазол; 5-{[(3S)-3-метилпіперазин-1-іл]метил}-3-(1нафтилсульфоніл)-1Н-індазол; (3S)-N-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]метил}піролідин-3-амін; (3R)-l-{[3-(1-нафтилсульфоніл)-1Н-індазол-5іл]метил}піролідин-3-амін; N-[2-(диметиламіно)етил]-3-(1-нафтилсульфоніл)1Н-індазол-5-карбоксамід; 2-{[5-фторо-3-(фенілсульфоніл)-1Н-індазол-7іл]оксі}етанамін; N-[3-(1-нафтилсульфоніл)-1Н-індазол-6-іл]-бетааланінамід; N-[3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]-3піперидин-1-ілпропанамід; N3,N3-диметил-N-[3-(1-нафтилсульфоніл)-1Ніндазол-7-іл]-бета-аланінамід; 2-{[3-(фенілсульфоніл)-1Н-індазол-7іл]оксі}етанамін; N-[3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]-бетааланінамід; N-[3-(1-нафтилсульфоніл)-1Н-індазол-7-іл]етан1,2-діамін; N-[3-(1-нафтилсульфоніл)-1Н-індазол-6-іл]-3піперидин-1-ілпропанамід; N-[3-(1-нафтилсульфоніл)-1Н-індазол-6-іл]етан1,2-діамін; N3,N3-діетил-N-[3-(1-нафтилсульфоніл)-1Ніндазол-7-іл]-бета-аланінамід; 94053 8 N,N-диметил-2-{[3-(1-нафтилсульфоніл)-1Ніндазол-4-іл]оксі}етанамін; 3-(1-нафтилсульфоніл)-4-(2-піперидин-1-ілетоксі)1Н-індазол; 3-(1-нафтилсульфоніл)-4-(2-піролідин-1-ілетоксі)1Н-індазол; 2-{[3-(1-нафтилсульфоніл)-1Н-індазол-4іл]оксі}етанамін; N-метил-2-{[3-(1-нафтилсульфоніл)-1Н-індазол-6іл]оксі}етанамін; 2-{[3-(1-нафтилсульфоніл)-1Н-індазол-6іл]оксі}етанамін; її стереоізомери та її фармацевтично прийнятні солі. 10. Спосіб лікування від порушення центральної нервової системи, яке є пов'язаним з 5-НТ6рецептором або зазнає його впливу, у пацієнта, який цього потребує, включаючи введення вищезгаданому пацієнтові терапевтично ефективної кількості сполуки формули І за будь-яким з пп. з 1 по 9. 11. Спосіб за п. 10, який відрізняється тим, що вищезгадане порушення є порушенням когнітивної функції, порушенням розвитку або нейродегенеративним порушенням. 12. Спосіб за п. 11, який відрізняється тим, що вищезгадане порушення є порушенням когнітивної функції. 13. Спосіб за п. 11, який відрізняється тим, що вищезгадане порушення є вибраним з групи, яка складається з порушення здатності до навчання; дефіциту уваги; синдрому Дауна, синдрому ламкої хромосоми X або аутизму. 14. Спосіб за п. 11, який відрізняється тим, що вищезгадане порушення є інсультом або черепномозковою травмою. 15. Фармацевтична композиція, яка містить фармацевтично прийнятний носій та ефективну кількість сполуки формули І за будь-яким з пп. з 1 по 9. 16. Спосіб одержання сполуки формули І за будьяким з пп. з 1 по 9, в якому здійснюють: реакцію сполуки формули II R6 R5 N (CR3R4) X (R7)m SO2-R2 NH2 , (II) де X, R2, R3, R4, R5, R6, R7, m та n є такими, як описано вище для формули І; з NaNO2 у присутності кислоти з одержанням сполуки формули І, де R1 є Н; і, необов'язково, реакцію вищезгаданої сполуки з R1-Hal, де Hal є Сl, Вr або І, і R1 є алкільною, циклоалкільною, арильною або гетероарильною групою, кожна з яких необов'язково є заміщеною. 9 Рецептори серотоніну (5-гідрокситрипраміну) (5-HT) відіграють ключову роль у багатьох фізіологічних та поведінкових функціях у людей та тварин. Ці функції опосередковуються через різні 5HT-рецептори, розподілені по всьому організму. Нині є відомими приблизно п’ятнадцять різних підтипів людських 5-HT-рецепторів, які було клоновано, багато з яких мають добре визначену роль у людському організмі. Одним з останніх розпізнаних підтипів 5-HT-рецепторів є 5-HT6-рецептор, вперше клонований з тканини щура у 1993 р. (Monsma, F. J.; Shen, Y.; Ward, R. P.; Hamblin, M. W. Molecular Pharmacology 1993, 43, 320-327), а згодом з людської тканини (Kohen, R.; Metcalf, M. A.; Khan, N.; Druck, T.; Huebner, K.; Sibley, D. R. Journal of Neurochemistry 1996, 66, 47-56). Цей рецептор є з’єднаним з G-білком рецептором (GPCR), безпосередньо з’єднаним з аденілатциклазою (Ruat, M.; Traiffort, E.; Arrang, J-M.; TardivelLacombe, L.; Diaz, L.; Leurs, R.; Schwartz, J-C. Biochemical Biophysical Research Communications 1993, 193, 268-276). Цей рецептор міститься майже виключно у ділянках центральної нервової системи (CNS) як у щура, так і у людини. In situ дослідження гібридизації 5-HT6-рецептора у головному мозку щура з застосуванням мРНК вказують на основну локалізацію в ділянках виступу 5-HT, включаючи стріатум, прилеглому ядрі, нюховому туберкулі та гіпокампальному утворенні (Ward, R. P.; Hamblin, M. W.; Lachowicz, J. E.; Hoffman, B. J.; Sibley, D. R.; Dorsa, D. M. Neuroscience 1995, 64, 1105-1111). Існує багато можливостей терапевтичного застосування для 5-HT6 лігандів у людини на основі прямого впливу та наявних показань наукових досліджень. Ці дослідження забезпечували інформацію, включаючи інформацію про локалізацію рецептора, афінність лігандів з відомою in vivo активністю, та результати, отримані в результаті проведених на даний час досліджень на різних тваринах (Woolley, M. L.; Marsden, C. A.; Fone, K. C. F. Current Drug Targets: CNS & Neurological Disorders 2004, 3(1), 59-79). Одним з прикладів терапевтичного застосування модуляторів функції 5-HT6-рецептора є застосування для поліпшення когнітивної функції тапам’яті при хворобах людини, таких, як хвороба Альцгеймера. Високий рівень рецептора, виявлений у важливих структурах переднього мозку, включаючи хвостате ядро/шкаралупу, гіпокамп, прилегле ядро та кору, свідчить про роль рецептора для пам’яті та когнітивної функції, оскільки відомо, що ці ділянки відіграють життєво важливу роль для пам’яті (Gerard, C.; Martres, M.-P.; Lefevre, K.; Miquel, M.C.; Verge, D.; Lanfumey, R.; Doucet, E.; Hamon, M.; El Mestikawy, S. Brain Research, 1997, 746, 207-219). Здатність відомих лігандів 5-HT6-рецептора до підвищення холінергічної передачі також підтверджує доцільність їх застосування для підвищення когнітивної функції (Bentley, J. C.; Boursson, A.; Boess, F. G.; Kone, F. C.; Marsden, C. A.; Petit, N.; Sleight, A. J. British Journal of Pharmacology, 1999, 126(7), 1537-1542). Дослідження продемонстрували, що відомий селективний антагоніст 5-HT6 суттєво підвищує рівень 94053 10 глутамату та аспартату у лобовій корі без підвищення рівня норадреналіну, допаміну або 5-HT. Це вибіркове підвищення нейрохімічних чинників, які є пов’язаними з пам’яттю та когнітивною функцією, свідчить про роль лігандів 5-HT6, яку вони відіграють для когнітивної функції (Dawson, L. A.; Nguyen, H. Q.; Li, P. British Journal of Pharmacology, 2000, 130(1), 23-26). Проведені на тваринах дослідження пам’яті та навчання з відомим селективним антагоністом 5-HT6 виявили позитивний вплив (Rogers, D. C.; Hatcher, P. D.; Hagan, J. J. Society of Neuroscience, Abstracts 2000, 26, 680). Останні дослідження підтвердили ці дані на кількох додаткових тваринних моделях у дослідженні когнітивної функції та пам’яті, включаючи модель розпізнавання нового об’єкта (King, M. V.; Sleight, A. J.; Wooley, M. L.; Topham, I. A.; Marsden, C. A.; Fone, K. C. F. Neuropharmacology 2004, 47(2), 195-204 та Wooley, M. L.; Marsden, C. A.; Sleight, A. J.; Fone, K. C. F. Psychopharmacology, 2003, 170(4), 358-367) та модель водного лабіринту (Rogers, D. C.; Hagan, J. J. Psychopharmacology, 2001, 158(2), 114-119 та Foley, A. G.; Murphy, K. J.; Hirst, W. D.; Gallagher, H. C.; Hagan, J. J.; Upton, N.; Walsh, F. S.; Regan, C. M. Neuropsychopharmacology 2004, 29(1), 93-100). Подібне терапевтичне застосування лігандів 5HT6 є пов’язаним з лікуванням від дефіциту уваги (ADD, також відомого як пов’язаний з гіперактивністю дефіцит уваги або ADHD) у дітей та дорослих. Оскільки антагоністи 5-HT6 підвищують активність нігростріатарного шляху допаміну, і оскільки ADHD є пов’язаним з відхиленнями у хвостатому ядрі (Ernst, M; Zametkin, A. J.; Matochik, J. H.; Jons, P. A.; Cohen, R. M. Journal of Neuroscience 1998, 18(15), 5901-5907), антагоністи 5-HT6 зменшують дефіцит уваги. Ранні дослідження з вивченням афінності різних лігандів ЦНС з відомим терапевтичним застосуванням або значною структурною подібністю до відомих медикаментів передбачають застосування лігандів 5-HT6 у лікуванні від шизофренії та депресії. Наприклад, клозапін (ефективний клінічний антипсихотичний засіб) має високу афінність до підтипу 5-HT6-рецептора. Крім того, кілька клінічних антидепресантів також мають високу афінність до рецептора і діють як антагоністи в цьому місці (Branchek, T. A.; Blackburn, T. P. Annual Reviews in Pharmacology and Toxicology 2000, 40, 319-334). Крім того, кілька in vivo досліджень на щурах свідчать, що модулятори 5-HT6 є корисними для лікування від порушень рухів, включаючи епілепсію (Stean, T.; Routledge, C.; Upton, N. British Journal of Pharmacology 1999, 127 Proc. Supplement 131P та Routledge, C.; Bromidge, S. M.; Moss, S. F.; Price, G. W.; Hirst, W.; Newman, H.; Riley, G.; Gager, T.; Stean, T.; Upton, N.; Clarke, S. E.; Brown, A. M. British Journal of Pharmacology 2000, 130(7), 1606-1612). Таким чином, мета даного винаходу полягає у забезпеченні сполук, які можуть застосовуватись як терапевтичні засоби для лікування від різних порушень центральної нервової системи, які є пов’язаними з 5-HT6-рецептором або зазнають його впливу. 11 94053 Інша мета даного винаходу полягає у забезпеченні терапевтичних способів та фармацевтичних композицій, які можуть застосовуватись для лікування від порушень центральної нервової системи, які є пов’язаними з 5-HT6-рецептором або зазнають його впливу. Особливістю цього винаходу є те, що запропоновані сполуки також можуть застосовуватись для подальшого дослідження та пояснення 5-HT6рецептора. Даний винахід забезпечує сполуку 3сульфоніліндазолу формули I R5 R6 N (CR3R4)n X SO2-R2 N N (R7)m R1 (I) де X є O, S, NR, CH2, CH2Y, CH2Z, CO, CONR або NRCO; Y є O, S або NR; Z є CO; n є 0 або цілим числом 1, 2, 3, 4, 5 або 6, якщо×є CH2; n є цілим числом 1, 2, 3, 4, 5 або 6, якщо×є CH2Z, CO або NRCO; n є цілим числом 2, 3, 4, 5 або 6, якщо×є O, S, NR, CH2Y або CONR; R є H або необов’язково заміщеною алкільною групою; R1 є H або алкільною, циклоалкільною, арильною або гетероарильною групою, кожна з яких необов’язково є заміщеною; R2 є необов’язково заміщеною алкільною, циклоалкільною, арильною або гетероарильною групою або необов’язково заміщеною 8-13-членною біциклічною або трициклічною кільцевою системою, яка має атом N у голові містка і необов’язково містить 1, 2 або 3 додаткові гетероатоми, вибрані з-поміж N, O або S; R3 та R4 кожен незалежно є H або необов’язково заміщеною алкільною групою; R5 та R6 кожен незалежно є H або алкільною, алкенільною, алкінільною, циклоалкільною, циклогетероалкільною, арильною або гетероарильною групою, кожна з яких необов’язково є заміщеною, або R5 та R6 можуть бути взяті разом з атомом, до якого вони приєднуються, для утворення необов’язково заміщеного 3-7-членного кільця, яке необов’язково містить додатковий гетероатом, вибраний з-поміж O, N або S; R7 є H, галогеном, CN, OR8, CO2R9, CONR10R11 або алкільною, алкенільною, алкінільною, циклоалкільною, циклогетероалкільною, арильною або гетероарильною групою, кожна з яких є необов’язково заміщеною; m є цілим числом 1, 2 або 3; R8 є H, COR12 або алкільною, алкенільною, алкінільною, арильною або гетероарильною групою, 12 кожна з яких необов’язково є заміщеною; R9 є H або C1-C6алкільною, арильною або гетероарильною групою, кожна з яких необов’язково є заміщеною; R10 та R11 кожен незалежно є H або необов’язково заміщеною алкільною групою; і R12 є необов’язково заміщеною C 1C6алкільною, циклоалкільною, циклогетероалкільною, арильною або гетероарильною групою; або її стереоізомер або фармацевтично прийнятну сіль. Даний винахід також забезпечує способи та композиції, які можуть застосовуватися для терапевтичного лікування порушень центральної нервової системи, які є пов’язаними з 5-HT6рецептором або зазнають його впливу. Рецептор 5-гідрокситрипраміну-6 (5-HT6) було розпізнано шляхом молекулярного клонування. Його здатність до зв’язування з багатьма терапевтичними сполуками, які застосовують у психіатрії, у поєднанні з цікавим розподілом у головному мозку, стимулює значну зацікавленість у нових сполуках, здатних взаємодіяти з вищезгаданим рецептором і справляти вплив на нього. Докладаються значні зусилля для розуміння ролі 5-HT6рецептора у психіатрії, когнітивній дисфункції, моторній функції та регуляції моторики, пам’яті, настрої і т.ін. Для цього старанно відшукували сполуки, які демонструють афінність зв’язування з 5HT6-рецептором, як для сприяння дослідженню 5HT6-рецептора, так і як потенційні терапевтичні засоби у лікуванні порушень центральної нервової системи. Див., наприклад, C. Reavill and D. C. Rogers, Current Opinion in Investigational Drugs, 2001, 2(1):104-109, Pharma Press Ltd and Woolley, M. L.; Marsden, C. A.; Fone, K. C. F. Current Drug Targets: CNS & Neurological Disorders 2004, 3(1), 59-79. Несподівано було виявлено, що сполуки 3сульфоніліндазолу формули I демонструють афінність 5-HT6-рецептора разом зі значною селективністю підтипу рецептора. Вигідним є те, що вищезгадані сполуки формули I є ефективними терапевтичними засобами для лікування від порушень центральної нервової системи (ЦНС), які є пов’язаними з 5-HT6-рецептором або зазнають його впливу. Відповідно, даний винахід забезпечує сполуку 3-сульфоніліндазолу формули I R5 R6 N (CR3R4)n X SO2-R2 N N (R7)m R1 (I) де X є O, S, NR, CH2, CH2Y, CH2Z, CO, CONR або NRCO; Y є O, S або NR; Z є CO; n є 0 або цілим числом 1, 2, 3, 4, 5 або 6, як 13 що×є CH2; n є цілим числом 1, 2, 3, 4, 5 або 6, якщо×є CH2Z, CO або NRCO; n є цілим числом 2, 3, 4, 5 або 6, якщо×є O, S, NR, CH2Y або CONR; R є H або необов’язково заміщеною алкільною групою; R1 є H або алкільною, циклоалкільною, арильною або гетероарильною групою, кожна з яких необов’язково є заміщеною; R2 є необов’язково заміщеною алкільною, циклоалкільною, арильною або гетероарильною групою або необов’язково заміщеною 8-13-членною біциклічною або трициклічною кільцевою системою, яка має атом N у голові містка і необов’язково містить 1, 2 або 3 додаткові гетероатоми, вибрані з-поміж N, O або S; R3 та R4 кожен незалежно є H або необов’язково заміщеною алкільною групою; R5 та R6 кожен незалежно є H або алкільною, алкенільною, алкінільною, циклоалкільною, циклогетероалкільною, арильною або гетероарильною групою, кожна з яких необов’язково є заміщеною, або R5 та R6 можуть бути взяті разом з атомом, до якого вони приєднуються, для утворення необов’язково заміщеного 3-7-членного кільця, яке необов’язково містить додатковий гетероатом, вибраний з-поміж O, N або S; R7 є H, галогеном, CN, OR8, CO2R9, CONR10R11 або алкільною, алкенільною, алкінільною, циклоалкільною, циклогетероалкільною, арильною або гетероарильною групою, кожна з яких є необов’язково заміщеною; m є цілим числом 1, 2 або 3; R8 є H, COR12 або алкільною, алкенільною, алкінільною, арильною або гетероарильною групою, кожна з яких необов’язково є заміщеною; R9 є H або C1-C6алкільною, арильною або гетероарильною групою, кожна з яких необов’язково є заміщеною; R10 та R11 кожен незалежно є H або необов’язково заміщеною алкільною групою; і R12 є необов’язково заміщеною C 1C6алкільною, циклоалкільною, циклогетероалкільною, арильною або гетероарильною групою; або її стереоізомер або фармацевтично прийнятну сіль. Слід розуміти, що формула винаходу охоплює всі можливі стереоізомери та проліки. Крім того, якщо не зазначено іншого, кожна алкільна, алкенільна, алкінільна, циклоалкільна, циклогетероалкільна, арильна або гетероарильна група передбачається як необов’язково заміщена. Необов’язково заміщений компонент може бути заміщений одним або кількома замісниками. Групи замісників, які необов’язково є присутніми, можуть бути однією або кількома з тих, які зазвичай застосовують для розробки фармацевтичних сполук або модифікації таких сполук для впливу на їхню структуру/активність, тривалість, абсорбцію, стійкість або іншу вигідну властивість. Конкретними прикладами таких замісників є атоми галогенів, нітро, ціано, тіоціанато, ціанато, гідроксильні, алкільні, галоалкільні, алкокси, галоалкокси, аміно, алкіламіно, діалкіламіно, формільні, алкоксикар 94053 14 бонільні, карбоксильні, алканоїльні, алкілтіо, алкілсульфінільні, алкілсульфонільні, карбамоїльні, алкіламідо, фенільні, фенокси, бензильні, бензилокси, гетероциклільні або циклоалкільні групи, в оптимальному варіанті - атоми галогенів або нижчі алкільні або алкокси групи. Якщо не зазначено іншого, зазвичай можуть бути присутні 0-4 замісники. Якщо будь-який з вищезазначених замісників являє собою або містить алкільну замісну групу, вона може бути лінійною або розгалуженою і може містити до 12 атомів вуглецю, в оптимальному варіанті до 6 атомів вуглецю, у ще кращому варіанті - до 4 атомів вуглецю. У даному описі термін "алкіл" включає як (C1C10) лінійний, так і (C3-C12) розгалужений (якщо не визначено іншого) моновалентний насичений вуглеводневий компонент. Прикладами насичених вуглеводневих алкільних компонентів, крім інших, є хімічні групи, такі, як метил, етил, n-пропіл, ізопропіл, n-бутил, трет-бутил, ізобутил, втор-бутил; вищі гомологи, такі, як n-пентил, n-гексил і т.ін. Визначення “алкіл” включає алкільні групи, які є необов’язково заміщеними. Придатними алкільними заміщеннями, крім інших, є CN, OH, NR10R11, галоген, феніл, карбамоїл, карбоніл, алкокси або арилокси. Вжитий авторами термін "галоалкіл" означає CnH2n+1 групу, яка має від одного до 2n+1 атомів галогенів, які можуть бути однаковими або різними. Прикладами галоалкільних груп є CF3, CH2Cl, C2H3BrCl, C3H5F2 або інші подібні групи. Термін “галоген” у даному описі означає фтор, хлор, бром та йод. Термін “алкеніл” у даному описі стосується (C2-C8) лінійного або (C3-C10) розгалуженого моновалентного вуглеводневого компонента, який містить принаймні один подвійний зв’язок. Такі вуглеводневі алкенільні компоненти можуть бути моноабо поліненасиченими і можуть існувати в E або Z конфігураціях. Передбачається, що сполуки згідно з цим винаходом включають усі можливі E та Z конфігурації. Прикладами моно- або поліненасичених вуглеводневих алкенільних компонентів, крім інших, є хімічні групи, такі, як вініл, 2-пропеніл, ізопропеніл, кротил, 2-ізопентеніл, бутадієніл, 2(бутадієніл), 2,4-пентадієніл, 3-(1,4-пентадієніл) та їх вищі гомологи, ізомери і т.ін. Термін “циклоалкіл” у даному описі стосується моноциклічного, біциклічного, трициклічного, злитого, місткового або спіро-моновалентного насиченого вуглеводневого компонента з 3-10 атомів вуглецю, якщо не зазначено іншого, причому атоми вуглецю розташовуються всередині або ззовні кільцевої системи. Будь-яка прийнятна позиція в кільці циклоалкільного компонента може бути ковалентно зв’язана з визначеною хімічною структурою. Прикладами циклоалкільних компонентів, крім інших, є хімічні групи, такі, як циклопропіл, циклопропілметил, циклобутил, циклопентил, циклогексил, циклогексилметил, циклогексилетил, циклогептил, норборніл, адамантил, спіро[4.5]деканіл, та їх гомологи, ізомери і т.ін. Вжитий авторами термін "циклогетероалкіл" означає C5-C7циклоалкільну кільцеву систему, яка містить 1, 2 або 3 гетероатоми, які можуть бути 15 94053 однаковими або різними, вибрані з-поміж N, O або S, і необов’язково містить один подвійний зв’язок. Прикладами циклогетероалкільних кільцевих систем, які охоплюються зазначеним авторами терміном, є нижчезазначені кільця, в яких X1 є NR', O або S, і R є H або необов’язковим замісником, як визначено нижче. N X1 X1 NR' X1 X1 X1 X1 X1 X1 X1 N X1 X1 X1 NR' N R' Термін "арил" у даному описі стосується ароматичного карбоциклічного компонента, що має до 20 атомів вуглецю, який може бути одним кільцем (моноциклічним) або кількома кільцями (біциклічним, до трьох кілець), злитими або ковалентно зв’язаними. Будь-яка прийнятна позиція в кільці арильного компонента може бути ковалентно зв’язаною з визначеною хімічною структурою. Прикладами арильних компонентів, крім інших, є хімічні групи, такі, як феніл, 1-нафтил, 2-нафтил, біфеніл, антрил, фенантрил, флуореніл, інданіл, біфеніленіл, аценафтеніл, аценафтиленіл і т.ін. Вжитий авторами термін "гетероарил" означає ароматичну гетероциклічну кільцеву систему, яка N N N N N N N N N N N N N N N W N W N W N N N N N N N N N N N N N Сполуки згідно з цим винаходом обмежуються тими, які є реально можливими з хімічної точки зору і стійкими. Таким чином, комбінація замісників або змінних у вищеописаних сполуках допускається лише у разі, якщо така комбінація в результаті W N N N N N N N N N N W N N W N N N W N W N N N N N N N N N N N N N W N W W N N W N N N N N N N N N W N N W N N N N N W N N N N N N N N N N N N N N N N N N може бути одним кільцем (моноциклічною) або кількома кільцями (біциклічною, до трьох кілець), злитими або ковалентно зв’язаними. В оптимальному варіанті гетероарил є 5-6-членним кільцем. Кільця можуть містити від одного до чотирьох гетероатомів, вибраних з-поміж азоту, кисню та сірки, причому атом(и) азоту або сірки необов’язково є окисненими, або атом(и) азоту є необов’язково кватернізованими. Будь-яка прийнятна позиція в кільці гетероарильного компонента може бути ковалентно зв’язана з визначеною хімічною структурою. Прикладами гетероарильних компонентів, крім інших, є гетероцикли, такі, як фуран, тіофен, пірол, піразол, імідазол, оксазол, ізоксазол, тіазол, ізотіазол, оксадіазол, триазол, піридин, піримідин, піразин, піридазин, бензімідазол, бензоксазол, бензізоксазол, бензoтіазол, бензoфуран, бензoтіофен, тіантрен, дибензoфуран, дибензoтіофен, індол, індазол, хінолін, ізохінолін, хіназолін, хіноксалін, пурин і т.ін. Прикладами 8-13-членних біциклічних або трициклічних кільцевих систем, які мають атом N у голові містка і необов’язково містять 1, 2 або 3 додаткові гетероатоми, вибрані з-поміж N, O або S, які охоплюються зазначеним авторами терміном, є нижчезазначені кільцеві системи, в яких W є NR', O або S; і R' є H або необов’язковим замісником, як описано нижче: N N N N W N 16 N N забезпечує стійку або реально можливу з хімічної точки зору сполуку. Якщо не зазначено іншого, описані авторами структури також включають усі стереохімічні форми структури; тобто, R та S конфігурації для кож 17 ного асиметричного центра. Таким чином, окремі стереохімічні ізомери, а також енантіомерні та діастереомерні суміші представлених сполук охоплюються обсягом винаходу. Якщо не зазначено іншого, описані авторами структури також включають сполуки, які відрізняються лише за наявністю одного або кількох ізотопно збагачених атомів. Наприклад, сполуки, які мають представлену структуру, за винятком заміни водню на дейтерій або тритій або заміни вуглецю на 13C- або 14Cзбагачений вуглець, охоплюються обсягом даного винаходу. Сполуки згідно з даним винаходом можуть бути перетворені на солі, зокрема, фармацевтично прийнятні солі, з застосуванням визнаних процедур. Прийнятними солями з основами є, наприклад, солі металів, такі, як солі лужних металів або лужноземельних металів, наприклад, солі натрію, калію або магнію, або солі з аміаком або органічним аміном, таким, як морфолін, тіоморфолін, піперидин, піролідин, моно-, ди- або три- нижчий алкіламін, наприклад етил-трет-бутил-, діетил-, діізопропіл-, триетил-, трибутил- або диметилпропіламін, або моно-, ди-, або тригідрокси нижчим алкіламіном, наприклад, моно-, ди- або триетаноламіном. Крім того, можуть утворюватися внутрішні солі. Також включаються солі, які є не придатними для фармацевтичного застосування, але можуть застосовуватися, наприклад, для виділення або очищення вільних сполук або їхні фармацевтично прийнятних солей. Термін "фармацевтично прийнятна сіль" у даному описі стосується солей, які походять від органічних або неорганічних кислот, таких, як, наприклад, оцтова, пропіонова, молочна, лимонна, винна, бурштинова, фумарова, малеїнова, малонова, мигдалева, яблучна, фталева, хлористоводнева, бромистоводнева, фосфорна, азотна, сірчана, метансульфонова, нафталінсульфонова, бензолсульфонова, толуолсульфонова, камфорсульфонова, та подібні відомі прийнятні кислоти, якщо сполука згідно з цим винаходом містить основний компонент. Також можуть утворюватися солі з органічних та неорганічних основ, в оптимальному варіанті - солі лужних металів, наприклад, натрію, літію або калію, коли сполука згідно з цим винаходом містить карбоксилатний або фенольний компонент або інший подібний компонент, здатний утворювати основні адиційні солі. Сполуки згідно з винаходом включають естери, карбамати або інші традиційні форми проліків, які в цілому є функціональними похідними сполук згідно з винаходом і легко перетворюються на активний компонент згідно з винаходом in vivo. Відповідно, спосіб згідно з винаходом охоплює лікування різних описаних вище станів з застосуванням сполуки формули I або сполуки, яка конкретно не описується, але після введення перетворюється на сполуку формули I in vivo. Також включаються метаболіти сполук згідно з даним винаходом, визначені як активні різновиди, які виробляються після введення цих сполук у біологічну систему. Оптимальними сполуками згідно з винаходом є сполуки формули I, в яких×є O, NR або CH2. 94053 18 Іншою групою оптимальних сполук є сполуки формули I, в яких n є 2 або 3. Також перевагу віддають сполукам формули I, в яких R2 є необов’язково заміщеною арильною або гетероарильною групою або необов’язково заміщеною 8-13-членною біциклічною або трициклічною кільцевою системою, яка має атом N у голові містка і необов’язково містить 1, 2 або 3 додаткові гетероатоми, вибрані з-поміж N, O або S. Ще кращими сполуками згідно з винаходом є сполуки формули I, в яких×є O, і R5 та R6 кожен незалежно є H або C1-C4 алкілом. Іншою групою ще кращих сполук є сполуки формули I, в яких×є O, і n є 3. Ще однією групою ще кращих сполук є сполуки формули I, у яких×є O; n є 3, і R2 є нафтилом. До оптимальних сполук згідно з винаходом належать: N, N-Диметил-3-{[3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]окси}пропан-1-амін; N-Метил-N-{2-[3-(фенілсульфоніл)-1H-індазол5-іл]етил}амін; N,N-Диметил-N-{2-[3-(фенілсульфоніл)-1Hіндазол-5-іл]етил}амін; {2-[3-(Фенілсульфоніл)-1H-індазол-7іл]етил}амін; N,N-Диметил-N-{2-[3-(фенілсульфоніл)-1Hіндазол-7-іл]етил}амін; N-{2-[3-(Фенілсульфоніл)-1H-індазол-7іл]етил}циклопропанамін; N,N-Диметил-N-{3-[3-(фенілсульфоніл)-1Hіндазол-5-іл]пропіл}амін; N-{3-[3-(Фенілсульфоніл)-1H-індазол-5іл]пропіл}циклопропанамін; {3-[3-(Фенілсульфоніл)-1H-індазол-5іл]пропіл}амін; {4-[3-(Фенілсульфоніл)-1H-індазол-5іл]бутил}амін; N-Метил-N-{2-[3-(фенілсульфоніл)-1H-індазол7-іл]етил}амін; N-[3-(1-Нафтилсульфоніл)-1H-індазол-5іл]етан-1,2-діамін; N,N-Диметил-2-{[3-(фенілсульфоніл)-1Hіндазол-5-іл]окси}етанамін; 3-(Фенілсульфоніл)-5-(2-піперидин-1-ілетокси)1H-індазол; 3-(1-Нафтилсульфоніл)-5-(2-піролідин-1ілетокси)-1H-індазол; N,N-Диметил-2-{[3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]окси}етанамін; N-(2-{[3-(1-Нафтилсульфоніл)-1H-індазол-5іл]окси}етил)циклопентанамін; 5-(2-Морфолін-4-ілетокси)-3-(1нафтилсульфоніл)-1H-індазол; N-Етил-N-метил-2-{[3-(1-нафтилсульфоніл)1H-індазол-5-іл]окси}етанамін; N-(2-{[3-(1-Нафтилсульфоніл)-1H-індазол-5іл]окси}етил)бутан-1-амін; N~1~-[3-(1-Нафтилсульфоніл)-1H-індазол-5іл]-бета-аланінамід; N-Етил-2-{[3-(фенілсульфоніл)-1H-індазол-5іл]окси}етанамін; N-(2-{[3-(Фенілсульфоніл)-1H-індазол-5іл]окси}етил)пропан-2-амін; N-(2-{[3-(1-Нафтилсульфоніл)-1H-індазол-5 19 іл]окси}етил)пропан-2-амін; N-Етил-2-{[3-(1-нафтилсульфоніл)-1H-індазол5-іл]окси}етанамін; N-Метил-2-{[3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]окси}етанамін; 1-Метил-3-(1-нафтилсульфоніл)-7-(2піперидин-1-ілетокси)-1H-індазол; 3-(1-Нафтилсульфоніл)-5-(2-піперидин-1ілетокси)-1H-індазол; 3-(2-Аміноетил)-1-[(2,5диметоксифеніл)сульфоніл]-1,3-дигідро-2Hімідазо[4,5-b]піридин-2-он; N,N-Діетил-2-{[3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]окси}етанамін; N-(2-{[3-(1-Нафтилсульфоніл)-1H-індазол-5іл]окси}етил)циклопропанамін; 1-(3-Хлоробензил)-3-(1-нафтилсульфоніл)-7(2-піперидин-1-ілетокси)-1H-індазол; 1-(3-Хлоробензил)-3-(1-нафтилсульфоніл)-7(2-піролідин-1-ілетокси)-1H-індазол; (2S)-3-Метил-N~1~-[3-(1-нафтилсульфоніл)1H-індазол-5-іл]бутанe-1,2-діамін; (2-{[1-(3-Хлоробензил)-3-(1-нафтилсульфоніл)1H-індазол-7-іл]окси}етил)амін; N-(2-{[3-(Фенілсульфоніл)-1H-індазол-5іл]окси}етил)циклопентанамін; 3-(Фенілсульфоніл)-5-(2-піролідин-1-ілетокси)1H-індазол; N-Метил-2-{[3-(фенілсульфоніл)-1H-індазол-5іл]окси}етанамін; N-Метил-2-{[1-метил-3-(фенілсульфоніл)-1Hіндазол-7-іл]окси}етанамін; 1-Метил-3-(фенілсульфоніл)-7-(2-піролідин-1ілетокси)-1H-індазол; (2-{[1-(3-Хлоробензил)-3-(фенілсульфоніл)-1Hіндазол-7-іл]окси}етил)метиламін; (2-{[1-(3-Хлоробензил)-3-(фенілсульфоніл)-1Hіндазол-7-іл]окси}етил)етиламін; 1-(3-Хлоробензил)-3-(фенілсульфоніл)-7-(2піролідин-1-ілетокси)-1H-індазол; 1-(3-Хлоробензил)-5-метокси-3-(1нафтилсульфоніл)-7-(2-піперидин-1-ілетокси)-1Hіндазол; N-Метил-2-{[3-(фенілсульфоніл)-1H-індазол-7іл]окси}етанамін; (2-{[1-(3-Хлоробензил)-3-(1-нафтилсульфоніл)1H-індазол-7-іл]окси}етил)етиламін; (2-{[1-(3-Хлоробензил)-3-(1-нафтилсульфоніл)1H-індазол-7-іл]окси}етил)метиламін; N-Етил-2-{[3-(фенілсульфоніл)-1H-індазол-7іл]окси}етанамін; N,N-Діетил-2-{[3-(фенілсульфоніл)-1H-індазол7-іл]окси}етанамін; N-(2-{[3-(Фенілсульфоніл)-1H-індазол-7іл]окси}етил)бутан-1-амін; 3-(Фенілсульфоніл)-7-(2-піролідин-1-ілетокси)1H-індазол; 3-(Фенілсульфоніл)-7-(2-піперидин-1-ілетокси)1H-індазол; N,N-Діетил-2-{[1-метил-3-(1нафтилсульфоніл)-1H-індазол-7-іл]окси}етанамін; 1-Метил-3-(1-нафтилсульфоніл)-7-(2піролідин-1-ілетокси)-1H-індазол; N-Етил-2-{[1-метил-3-(1-нафтилсульфоніл)-1Hіндазол-7-іл]окси}етанамін; 94053 20 3-(1-Нафтилсульфоніл)-7-(2-піперидин-1ілетокси)-1H-індазол; 3-(1-Нафтилсульфоніл)-7-(2-піролідин-1ілетокси)-1H-індазол; N-Етил-2-{[3-(1-нафтилсульфоніл)-1H-індазол7-іл]окси}етанамін; (2-{[3-(1-Нафтилсульфоніл)-1H-індазол-7іл]окси}етил)амін; (2-{[1-(3-Хлоробензил)-5-фторо-3-(1нафтилсульфоніл)-1H-індазол-7-іл]окси}етил)диметиламін; (2-{[1-Бензил-3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]окси}етил)метиламін; (2-{[1-Бензил-3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]окси}етил)диметиламін; (2-{[1-Бензил-3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]окси}етил)етиламін; N-Метил-2-{[3-(1-нафтилсульфоніл)-1Hіндазол-7-іл]окси}етанамін; N,N-Диметил-2-{[3-(1-нафтилсульфоніл)-1Hіндазол-7-іл]окси}етанамін; 5-Фторо-3-(1-нафтилсульфоніл)-7-(2піролідин-1-ілетокси)-1H-індазол; 5-Фторо-3-(1-нафтилсульфоніл)-7-(2піперидин-1-ілетокси)-1H-індазол; N,N-Діетил-2-{[5-фторо-3-(1нафтилсульфоніл)-1H-індазол-7-іл]окси}етанамін; (2-{[5-Фторо-3-(1-нафтилсульфоніл)-1Hіндазол-7-іл]окси}етил)диметиламін; N-Етил-2-{[5-фторо-3-(1-нафтилсульфоніл)1H-індазол-7-іл]окси}етанамін; (2-{[1-(3-Хлоробензил)-3-(1-нафтилсульфоніл)1H-індазол-5-іл]окси}етил)-диметиламін; N-Метил-3-{[3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]окси}пропан-1-амін; N-Етил-N-метил-3-{[3-(1-нафтилсульфоніл)1H-індазол-5-іл]окси}пропан-1-амін; 3-(1-Нафтилсульфоніл)-5-(3-піперидин-1ілпропокси)-1H-індазол; N,N-Диметил-3-{[3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]окси}пропан-1-амін; N,N-Діетил-3-{[3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]окси}пропан-1-амін; N-(3-{[3-(1-Нафтилсульфоніл)-1H-індазол-5іл]окси}пропіл)бутан-1-амін; 3-(1-Нафтилсульфоніл)-5-(3-піролідин-1ілпропокси)-1H-індазол; (2-{[5-Метокси-3-(1-нафтилсульфоніл)-1Hіндазол-7-іл]окси}етил)метиламін; (2-{[5-Метокси-3-(1-нафтилсульфоніл)-1Hіндазол-7-іл]окси}етил)диметиламін; 5-Метокси-3-(1-нафтилсульфоніл)-7-(2піролідин-1-ілетокси)-1H-індазол; 5-Метокси-3-(1-нафтилсульфоніл)-7-(2піперидин-1-ілетокси)-1H-індазол; (2-{[1-(3-Хлоробензил)-3-(1-нафтилсульфоніл)1H-індазол-5-іл]окси}етил)етиламін; (3-{[1-(3-Хлоробензил)-3-(1-нафтилсульфоніл)1H-індазол-7-іл]окси}пропіл)-діетиламін; 1-(3-Хлоробензил)-3-(1-нафтилсульфоніл)-7(3-піролідин-1-ілпропокси)-1H-індазол; N-Метил-3-{[3-(1-нафтилсульфоніл)-1Hіндазол-7-іл]окси}пропан-1-амін; N,N-Діетил-3-{[3-(1-нафтилсульфоніл)-1Hіндазол-7-іл]окси}пропан-1-амін; 21 N-Метил-2-{[1-метил-3-(1-нафтилсульфоніл)1H-індазол-5-іл]окси}етанамін; N,N-Диметил-2-{[1-метил-3-(1нафтилсульфоніл)-1H-індазол-5-іл]окси}етанамін; N-Етил-N-метил-2-{[1-метил-3-(1нафтилсульфоніл)-1H-індазол-5-іл]окси}етан-амін; N-Етил-2-{[1-метил-3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]окси}етанамін; N,N-Діетил-2-{[1-метил-3-(1нафтилсульфоніл)-1H-індазол-5-іл]окси}етанамін; N-(2-{[1-Метил-3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]окси}етил)пропан-2-амін; 1-Метил-3-(1-нафтилсульфоніл)-5-(2піролідин-1-ілетокси)-1H-індазол; {3-[3-(1-Нафтилсульфоніл)-1H-індазол-5іл]пропіл}амін; (2-{[1-Метил-3-(1-нафтилсульфоніл)-1Hіндазол-7-іл]окси}етил)амін; N-Етил-3-{[3-(1-нафтилсульфоніл)-1H-індазол5-іл]окси}пропан-1-амін; N-Ізопропіл-3-{[3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]окси}пропан-1-амін; N-(3-{[3-(1-Нафтилсульфоніл)-1H-індазол-5іл]окси}пропіл)циклопентанамін; 5-(3-Морфолін-4-ілпропокси)-3-(1нафтилсульфоніл)-1H-індазол; N-(3-{[3-(1-Нафтилсульфоніл)-1H-індазол-5іл]окси}пропіл)циклопропанамін; (3-{[3-(1-Нафтилсульфоніл)-1H-індазол-5іл]окси}пропіл)амін; N-Метил-4-{[3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]окси}бутан-1-амін N,N-Диметил-4-{[3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]окси}бутан-1-амін; N-Етил-4-{[3-(1-нафтилсульфоніл)-1H-індазол5-іл]окси}бутан-1-амін; N,N-Діетил-4-{[3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]окси}бутан-1-амін; N-Метил-4-{[3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]окси}-N-пропілбутан-1-амін; 3-(1-Нафтилсульфоніл)-5-(4-піролідин-1ілбутокси)-1H-індазол; 3-(1-Нафтилсульфоніл)-5-(4-піперидин-1ілбутокси)-1H-індазол; (4-{[3-(1-Нафтилсульфоніл)-1H-індазол-5іл]окси}бутил)амін; (2-{[5-Фторо-3-(1-нафтилсульфоніл)-1Hіндазол-7-іл]окси}етил)метиламін; 5-[(4-Метилпіперазин-1-іл)метил]-3-(1нафтилсульфоніл)-1H-індазол; 3-(1-Нафтилсульфоніл)-5-(піперазин-1ілметил)-1H-індазол; N-{[3-(1-Нафтилсульфоніл)-1H-індазол-5іл]метил}етан-1,2-діамін; N-Метил-3-[3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]пропан-1-амін; N,N-Диметил-4-[3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]бутан-1-амін; N,N-Диметил-3-[3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]пропан-1-амін; N-Етил-N-метил-3-[3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]пропан-1-амін; N-Ізопропіл-3-[3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]пропан-1-амін; N-Етил-N-метил-4-[3-(1-нафтилсульфоніл)-1H 94053 22 індазол-5-іл]бутан-1-амін; (2-{[3-(1-Нафтилсульфоніл)-1H-індазол-5іл]окси}етил)амін; 3-(1-Нафтилсульфоніл)-5-(3-піролідин-1ілпропіл)-1H-індазол; N-Ізопропіл-4-[3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]бутан-1-амін; 3-(1-Нафтилсульфоніл)-5-(4-піролідин-1ілбутил)-1H-індазол; N-Етил-4-[3-(1-нафтилсульфоніл)-1H-індазол5-іл]бутан-1-амін; 5-[(3-Метилпіперазин-1-іл)метил]-3-(1нафтилсульфоніл)-1H-індазол; 5-[(3,5-Диметилпіперазин-1-іл)метил]-3-(1нафтилсульфоніл)-1H-індазол; N-Етил-3-[3-(1-нафтилсульфоніл)-1H-індазол5-іл]пропан-1-амін; {4-[3-(1-Нафтилсульфоніл)-1H-індазол-5іл]бутил}амін; 5-[1-(4-Метилпіперазин-1-іл)етил]-3-(1нафтилсульфоніл)-1H-індазол; N,N,N'-Триметил-N'-{[3-(1-нафтилсульфоніл)1H-індазол-5-іл]метил}етан-1,2-діамін; N,N-Диметил-2-{[3-(1-нафтилсульфоніл)-1Hіндазол-5-іл]метокси}етанамін; 5-{[(3R)-3-Метилпіперазин-1-іл]метил}-3-(1нафтилсульфоніл)-1H-індазол; 5-{[(3S)-3-Метилпіперазин-1-іл]метил}-3-(1нафтилсульфоніл)-1H-індазол; (3S)-N-{[3-(1-Нафтилсульфоніл)-1H-індазол-5іл]метил}піролідин-3-амін; (3R)-1-{[3-(1-Нафтилсульфоніл)-1H-індазол-5іл]метил}піролідин-3-амін; N-[2-(Диметиламіно)етил]-3-(1нафтилсульфоніл)-1H-індазол-5-карбоксамід; 2-{[5-Фторо-3-(фенілсульфоніл)-1H-індазол-7іл]окси}етанамін; N-[3-(1-Нафтилсульфоніл)-1H-індазол-6-іл]бета-аланінамід; N-[3-(1-Нафтилсульфоніл)-1H-індазол-7-іл]-3піперидин-1-ілпропанамід; N~3~,N~3~-Диметил-N-[3-(1нафтилсульфоніл)-1H-індазол-7-іл]-бетааланінамід; 2-{[3-(Фенілсульфоніл)-1H-індазол-7іл]окси}етанамін; N-[3-(1-Нафтилсульфоніл)-1H-індазол-7-іл]бета-аланінамід; N-[3-(1-Нафтилсульфоніл)-1H-індазол-7іл]етан-1,2-діамін; N-[3-(1-Нафтилсульфоніл)-1H-індазол-6-іл]-3піперидин-1-ілпропанамід; N-[3-(1-Нафтилсульфоніл)-1H-індазол-6іл]етан-1,2-діамін; N3,N3-діетил-N-[3-(1-нафтилсульфоніл)-1Hіндазол-7-іл]-бета-аланінамід; N,N-Диметил-2-{[3-(1-нафтилсульфоніл)-1Hіндазол-4-іл]окси}етанамін; 3-(1-Нафтилсульфоніл)-4-(2-піперидин-1ілетокси)-1H-індазол; 3-(1-Нафтилсульфоніл)-4-(2-піролідин-1ілетокси)-1H-індазол; 2-{[3-(1-Нафтилсульфоніл)-1H-індазол-4іл]окси}етанамін; N-Метил-2-{[3-(1-нафтилсульфоніл)-1H 23 94053 індазол-6-іл]окси}етанамін; 2-{[3-(1-Нафтилсульфоніл)-1H-індазол-6іл]окси}етанамін; їх стереоізомери; або їх фармацевтично прийнятні солі. В одному варіанті втілення×є O. В одному варіанті втілення n є 3. В одному варіанті втілення R2 є необов’язково заміщеною фенільною, нафтильною або імідазотіазолільною групою. У ще одному варіанті втілення R2 є нафтилом. В одному варіанті втілення R1 є H або необов’язково заміщеним алкілом. У ще одному варіанті втіленняM є 0 або 1. У ще одному варіанті втіленняM є 0. В одному варіанті втілення R5 та R6 кожен незалежно є H або C1-C4 алкілом. Сполуки згідно з винаходом можуть бути одержані з застосуванням традиційних синтетичних способів і, у разі потреби, стандартних способів виділення та відокремлення. На представлених нижче Схемах з I по VII Z представляє групу (CR3R4)n, в якій R3, R4 та n є такими, як визначено вище для формули I. Сполуки формули I, де×є O (Ia), можуть бути 24 одержані, як пояснюється нижче на Схемі I, де хлорометилсульфон 2 є або таким, що виробляється серійно, або може бути легко одержаний з застосуванням способів, як описано у публікації M. Makosza and J. Golinski in J. Org. Chem.,1984, 49, 1488-1494; або публікації Antane, S.; Bernotas, R., Li, Y.; McDevitt, R.; Yan, Y. Synthetic Communications 2004, 34(13), 2443-2449, або іншими відомими способами. Реакція сульфонілхлориду 1 з сульфітом натрію в основних умовах з наступною реакцією з хлоро-бромо-метаном забезпечує хлорометилсульфон 2. Реакція 2 з фторонітробензолом 3 в основних умовах забезпечує бензилсульфонільну похідну 4. Сполуку 4 піддають реакції з діолом, HO-(CR3R4)n-OH, в основних умовах для утворення 5. Тозилування з наступною гідрогенізацією 5 забезпечує анілін 6. Сполуку 6 піддають реакції з нітритом натрію у присутності кислоти для утворення індазолу 7. Алкілування індазолу 7 забезпечує алкіловану тозилатну сполуку 8. Заміщення тозильних груп будь-якої зі сполук 7 або 8 відповідним аміном після цього забезпечує потрібну сполуку формули Ia. Реакцію показано на Схемі I, де Ts представляє pтолуолсульфоніл, і Hal представляє Cl, Br або I. Схема I (R7)m 1) Na2SO3, NaHCO3 R2 SO2Cl 1 2) Bu4NBr, BrCH2Cl NO2 F R2-SO2CH2Cl 3 2 t-BuOK, THF HO-(CR3R4)n-OH Z O O S R2 O 2) NO2 (R7)m 1) 4 H2/10% Pd/C NH2 (R7)m 6 O O S R2 O NaNO2/HCl (R7)m O O S R2 TsO Z O TsCl, Et3N 5 TsO Z NO2 (R7)m t-BuOK HO F O O S R2 O O S R2 TsO Z O R1-Hal N N H N N R1 (R7)m 7 8 HNR5R6 R5 N HNR5R6 O O S R2 Z O R6 N N H (R7)m (Ia) Подібним чином сполуки формули I, де×є O, і R5 та R6 є H (Ib), або сполуки формули Ia можуть бути одержані шляхом реакції нітробензольної похідної 9 з хлорометилсульфоном 2 з наступною гідрогенізацією для утворення аніліну 10. Анілін 10 перетворюють на індазольну похідну 11, як описано вище на Схемі I. Алкілування або захист інда R5 N O O S R2 Z O R6 N N R1 (R7)m (Ia) золу 11 забезпечує сполуку 12. Реакція 12 з азидом натрію з наступним відновленням азидо-групи забезпечує потрібний первинний амін Ib. В альтернативному варіанті реакція 11 або 12 з аміном, HNR5R6, забезпечує сполуку Ia. Реакцію показано на Схемі II, де Hal представляє Cl, Br або I. 25 94053 26 Схема II Cl Z 1) R2SO2CH2Cl O NO2 (R7)m 2) H2, Pd/C NaNO2/HCl NH2 (R7)m 9 Cl O O S R2 Cl Z O 2 10 O O S R2 O Z N N H (R7)m O O S R2 Cl Z O R1-Hal N N R1 (R7)m 11 1) NaN3 H2N 2) [H] (Ib) HNR5R6 HNR5R6 R5 O O S R2 Z O N R6 O O S R2 R6 N Z O N N H (R7)m N N R1 (R7)m 12 R5 O O S R2 Z O N N R1 (R7)m (Ia) (Ia) В альтернативному варіанті сполуки формули Ia можуть бути одержані шляхом реакції аміноспирту 14 або з фторонітробензолом 13 в основних умовах, або з нітрофенолом 15 в умовах Міцунобу для утворення сполуки 16. Сполуку 16 піддають реакції з хлоросульфоном 2 з наступною гідрогенізацією для утворення аніліну 17. Наступне утворення потрібних індазолів формули Ia здійснюють, як описано вище на Схемах I та II. Реакцію показано на Схемі III, де Hal представляє Cl, Br або I. Схема III R5 F R5R6N-(CR3R4)n-OH 14 t-BuOK NO2 (R7)m R6 N R5R6N-(CR3R4)n-OH O Z NO2 (R7)m DEAD, PPh3 1) Z O (R7)m R2-SO2CH2Cl O O S R2 2) 2 H2/10% Pd/C NH2 17 NaNO2/HCl Na2CO3 R5 R6 N Z O (R7)m R5 O O S R2 N N H (Ia) R6 R1-Hal NO2 (R7)m 15 16 13 R6 R5 N OH 14 N Z O (R7)m O O S R2 N N R1 (Ia) 27 94053 Сполуки формули I, де×є NR, і R та R1 є H (Ib), або×є NRCO, і R та R1 є H (Ic), можуть бути одержані шляхом реакції нітроіндазолу 18 з йодом для утворення відповідного 3-йодоіндазолу 19; з’єднання 19 з тіолом 20 з наступним окисненням відповідним окисником, таким, як mхлоропербензойна кислота (mCPBA), для утворення сульфону 21; відновлення нітро-групи 21 за 28 допомогою Sn/HCl або SnCl2/HCl для утворення відповідного аміну 22; і реакції 22 з аміноальдегідом 23 в умовах відновного амінування для утворення потрібної сполуки формули Ib або з’єднання 22 з амінокислотою 24 для одержання потрібної сполуки формули Ic. Реакції показано нижче на Схемі IV, де Ac представляє COCH3. Схема IV I I2, KOH N O2N (R7)m 20 N O2N N H N H (R7)m SO2-R2 1) R2SH, CuI 2) mCPBA, Sn, HCl or SnCl2, EtOH 21 R5 R6 N Z CHO O 2 O S R N H (R7)m O O S R2 R5 Z R6 N 23 N H2N N H (R7)m 19 18 N O2N HN N NaBH(OAc)3, N H (R7)m 22 (Ib) R5 R6 N Z CO2H 24 R5 R6 N O Z NH O O S R2 N N H (R7)m (Ic) Сполуки формули I, де×є CH2, і R5 та R6 є відмінними від H (Id), можуть бути одержані шляхом реакції нітробензольної сполуки 25 з хлорометилсульфонільною сполукою 2 для утворення проміжної сполуки 26; відновлення нітро-групи сполуки 26 до відповідного аміну та нітрозування вищезгада ного аміну, як описано на Схемах II та III, для утворення потрібної сполуки формули Id, де R1 є H, та, необов’язково, алкілування вищезгаданої сполуки для одержання потрібної сполуки формули Id, де R1 є відмінним від H. Реакції показано нижче на Схемі V, де Hal представляє Cl, Br або I. Схема V R6 R5 R5 N (CR3R4)n H2C R2SO2CH2Cl 2 (CR3R4)n 1) Sn/HCl H2C SO2R2 2) NaNO2, HCl NO2 NO2 (R7)m 26 (R7)m 25 R5 R6 N R6 N R5 (CR3R4)n SO2-R2 H2C N (R7)m R1-Hal R6 N (CR3R4)n SO2-R2 H2C N N H N (R7)m (Id) R1 (Id) N N (CR3R4)n H2C R2SO2CH2Cl 2 R5 1) Sn/HCl SO2R2 2) NaNO2, HCl NO2 NO2 (R7)m 94053 26 (R7)m 25 29 (CR3R4)n H2C 30 R6 N R5 (CR3R4)n SO2-R2 H2C R1-Hal N (R7)m R6 N (CR3R4)n SO2-R2 H2C N N H N (R7)m (Id) Сполуки формули Id, де R5 є H (Ie), можуть бути одержані у подібний спосіб шляхом захисту сполуки 27 відповідною захисною групою, такою, як t-бутилоксикарбоніл (BOC), етилоксикарбоніл, метилоксикарбоніл, бензил (Bn), фталімід, флуоренілметилкарбоніл (Fmoc), ацетил, бензоїл і т.ін., для утворення захищеного аміну 28; реакції сполу R1 (Id) ки 28 з хлорометилсульфонілом 2, з наступним відновленням та нітрозуванням, як показано вище на Схемі V, для утворення захищеної сполуки 29 та депротекції для одержання потрібної сполуки формули Ie. Реакцію показано нижче на Схемі VI, де Hal представляє Cl, Br або I. Схема VI Сполуки формули Id також можуть бути одержані шляхом з’єднання сполуки 31 з алкіном 32 з застосуванням умов Соногашири для утворення сполуки 33; відновлення 33 до повністю насиченого аміну 34; реакцію 34 з NaNO2 для утворення індазолу 35 та перетворення гідроксильної групи на відщеплювану групу та заміщення відщеплюваної групи аміном, HNR5R6, необов’язкового алкілування утвореного в результаті продукту для одержання потрібної сполуки формули Id. Реакції показано нижче на Схемі VII, де TsCl представляє тозилхлорид, і Hal представляє Cl, Br або I. 31 94053 32 Схема VII HO (R4R3C)n-1 OH OH Br (CR3R4)n (CR3R4)n-1 SO2-R2 SO2-R2 32 NO2 (R7)m Pd, DMF H2, Pd/C SO2-R2 NO2 (R7)m 31 H2C NH2 (R7)m 33 34 R5 OH R6 (CR3R4)n NaNO2/HCl H2C R5 N (CR3R4)n SO2-R2 1) TsCl H2C N H (R7)m (CR3R4)n SO2-R2 N N 2) HNR5R6 N H (R7)m R6 N H2C SO2-R2 R1-Hal N N (R7)m R1 35 (Id) Вигідним є те, що сполуки формули I згідно з винаходом можуть застосовуватися для лікування порушень ЦНС, які є пов’язаними з 5-HT6рецептором або зазнають його впливу, включаючи порушення моторної функції, порушення настрою, особистості, поведінкові, психіатричні, когнітивні, нейродегенеративні або інші подібні порушення, наприклад, хворобу Альцгеймера, хворобу Паркінсона, дефіцит уваги, страхи, епілепсію, депресію, обсесивно-компульсивне порушення, порушення сну, нейродегенеративні порушення (такі, як черепно-мозкова травма або інсульт), порушення харчової поведінки (такі, як анорексія або булімія), шизофренію, втрату пам’яті, порушення, пов’язані з відвиканням від наркотичної або нікотинової залежності або інші подібні порушення, або певні порушення шлунково-кишкового тракту, такі, як синдром подразненого кишечника. Відповідно, даний винахід забезпечує спосіб лікування від порушення центральної нервової системи, яке є пов’язаним з 5-HT6-рецептором або зазнає його впливу, у пацієнта, який цього потребує, включаючи забезпечення для вищезгаданого пацієнта терапевтично ефективної кількості сполуки формули I, як описано вище. Сполуки можуть забезпечуватися шляхом перорального або парентерального введення або в будь-який традиційний спосіб, який є ефективним способом введення терапевтичного агента пацієнтові, який цього потребує. Термін “забезпечення”, вжитий авторами по відношенню до забезпечення сполуки або речовини, яка охоплюється винаходом, означає або безпосереднє введення такої сполуки або речовини, або введення проліків, похідної або аналога, які утворюють рівноцінну кількість сполуки або речовини в організмі. Спосіб згідно з винаходом включає: спосіб лікування від шизофренії; спосіб лікування від хвороби, пов’язаної з дефіцитом пам’яті, когнітивної функції та/або здатності до навчання, або когнітивного порушення, такого, як хвороба Альцгеймера або дефіцит уваги; спосіб лікування від порушень (Id) розвитку, таких, як шизофренія; синдром Дауна, синдром ламкої хромосоми X, аутизм і т.ін.; спосіб лікування від поведінкових порушень, наприклад, страху, депресії або обсесивно-компульсивного порушення; спосіб лікування від рухових або моторних порушень, таких, як хвороба Паркінсона або епілепсія; спосіб лікування від нейродегенеративного порушення, такого, як інсульт або черепно-мозкова травма або відвикання від наркотичної залежності, включаючи залежність від нікотину, алкоголю або інших речовин, що викликають звикання, або будь-якої іншої хвороби або порушення ЦНС, пов’язаних з 5-HT6-рецептором. В одному варіанті втілення даний винахід забезпечує спосіб лікування від дефіциту уваги (ADD, також відомого як пов’язаний з гіперактивністю дефіцит уваги або ADHD) у дітей та дорослих. Відповідно, в цьому варіанті втілення даний винахід забезпечує спосіб лікування від дефіциту уваги у педіатричних пацієнтів. Даний винахід таким чином забезпечує спосіб лікування від кожного з описаних вище станів у пацієнта, в оптимальному варіанті - у людини, вищезгаданий спосіб включає забезпечення для вищезгаданого пацієнта терапевтично ефективної кількості сполуки формули I, як описано вище. Сполуки можуть доставлятися шляхом перорального або парентерального введення або у будьякий традиційний спосіб, який є ефективним способом введення терапевтичного агента пацієнтові, який цього потребує. Терапевтично ефективна кількість, яка забезпечується при лікуванні конкретного порушення ЦНС, може бути різною, залежно від конкретного(их) стану(ів), який(і) підлягає(ють) лікуванню, розміру, віку та характеру реакції пацієнта, тяжкості порушення, рішення лікаря, який здійснює лікування, і т.ін. Як правило, ефективна кількість для щоденного перорального введення може становити приблизно від 0,01 до 1,000мг/кг, в оптимальному варіанті - приблизно від 0,5 до 500мг/кг, а ефективна кількість для парентерального введен 33 ня може становити приблизно від 0,1 до 100мг/кг, в оптимальному варіанті - приблизно від 0,5 до 50мг/кг. На практиці сполуки згідно з винаходом забезпечуються шляхом введення сполуки або її прекурсора у твердій або рідкій формі, окремо або у комбінації з одним або кількома традиційними фармацевтичними носіями або наповнювачами. Відповідно, даний винахід забезпечує фармацевтичну композицію, яка включає фармацевтично прийнятний носій та ефективну кількість сполуки формули I, як описано вище. В одному варіанті втілення винахід стосується композицій, які включають принаймні одну сполуку формули I або її фармацевтично прийнятну сіль та один або кілька фармацевтично прийнятних носіїв, наповнювачів або розріджувачів. До таких композицій належать фармацевтичні композиції для лікування або контролювання хвороб або станів центральної нервової системи. У деяких варіантах втілення композиції включають суміші однієї або кількох сполук формули I. У деяких варіантах втілення винахід стосується композицій, які включають принаймні одну сполуку формули I або її фармацевтично прийнятну сіль та один або кілька фармацевтично прийнятних носіїв, наповнювачів або розріджувачів. Такі композиції одержують згідно з прийнятними фармацевтичними процедурами. Фармацевтично прийнятними носіями є носії, які є сумісними з іншими інгредієнтами у композиції і є біологічно прийнятними. Сполуки формули I можуть вводитись перорально або парентерально, окремо або у комбінації з традиційними фармацевтичними носіями. Придатні тверді носії можуть включати одну або кілька речовин, які також можуть діяти як ароматизатори, мастила, солюбілізатори, суспендуючі агенти, наповнювачі, суперпластифікатори, компресійні засоби, зв’язувальні речовини, дезінтегратори таблеток або інкапсулюючі матеріали. У порошках носій може бути тонко диспергованою твердою речовиною у суміші з тонко диспергованим активним інгредієнтом. У таблетках активний інгредієнт змішують з носієм, який має необхідні компресійні властивості, у відповідних пропорціях і пресують у потрібній формі та розмірі. Порошки та таблетки в оптимальному варіанті містять до 99% активного інгредієнта. До придатних твердих носіїв належать, наприклад, фосфат кальцію, стеарат магнію, тальк, цукри, лактоза, декстрин, крохмаль, желатин, целюлоза, метилцелюлоза, натрій карбоксиметилцелюлоза, полівінілпіролідин, низькоплавкі воски та іонообмінні смоли. У деяких варіантах втілення сполука формули I передбачається у композиції таблетки, яка розпадається перорально, придатній для введення педіатричним пацієнтам. Рідкі носії застосовують для приготування розчинів, суспензій, емульсій, сиропів та еліксирів. Активний інгредієнт може бути розчинений або суспендований у фармацевтично прийнятному рідкому носії, такому, як вода, органічний розчинник, їх суміш або фармацевтично прийнятна олія або жир. Рідкий носій може містити інші прийнятні 94053 34 фармацевтичні домішки, такі, як, наприклад, солюбілізатори, емульгатори, буфери, консерванти, підсолоджувачі, ароматизатори, суспендуючі агенти, загусники, барвники, регулятори в’язкості, стабілізатори або осморегулятори. Прикладами рідких носіїв, придатних для перорального та парентерального введення, є вода (зокрема, з вмістом вищезгаданих домішок, наприклад, похідних целюлози, в оптимальному варіанті - розчин натрій карбоксиметилцелюлози), спирти (включаючи одноатомні спирти та багатоатомні спирти, наприклад, гліколі) та їхні похідні, та олії (наприклад, фракціонована кокосова олія та арахісова олія). Для парентерального введення носій також може бути олійним естером, таким, як етилолеат або ізопропіл міристат. Стерильні рідкі носії застосовують у стерильних рідких композиціях для парентерального введення. Рідким носієм для аерозольних композицій може бути галогенований вуглеводень або інший фармацевтично прийнятний газ-витискувач. У деяких варіантах втілення забезпечується рідка фармацевтична композиція, причому вищезгадана композиція є придатною для введення педіатричним пацієнтам. В інших варіантах втілення рідкою композицією є сироп або суспензія. Рідкі фармацевтичні композиції, які є стерильними розчинами або суспензіями, вводять, наприклад, шляхом внутрішньом’язової, внутрішньочеревинної або підшкірної ін’єкції. Стерильні розчини також можуть вводитися внутрішньовенно. Композиції для перорального введення можуть бути в рідкій або твердій формі. Сполуки формули I можуть вводитись ректально або вагінально у формі традиційного супозиторію. Для введення шляхом інтраназальної або внутрішньобронхіальної інгаляції або вдування, сполуки формули I можуть бути рецептовані у водний або частково водний розчин, який може застосовуватись у формі аерозолю. Сполуки формули I також можуть вводитися крізьшкірно через застосування крізьшкірного пластиру, який містить активну сполуку та носій, який є інертним для активної сполуки, є нетоксичним для шкіри і забезпечує доставлення агента для системної абсорбції в систему кровообігу крізь шкіру. Носій може набувати різних форм, таких, як креми та мазі, пасти, гелі та оклюзійні засоби. Креми та мазі можуть бути в’язкими рідкими або напівтвердими емульсіями типу “олія у воді” або “вода в олії”. Також можуть бути застосовані пасти, які складаються з абсорбційних порошків, диспергованих у вазеліні або гідрофільному вазеліні, що містить активний інгредієнт. Можуть застосовуватися різні герметичні засоби для вивільнення активного інгредієнта у кровотік, такі, як напівпроникна мембрана, яка вкриває вмістище, яке містить активний інгредієнт з носієм або без нього, або матрикс, який містить активний інгредієнт. Інші оклюзійні засоби є відомими з літератури. В оптимальному варіанті фармацевтична композиція має форму дозованої одиниці, наприклад, таблеток, капсул, порошків, розчинів, суспензій, емульсій, гранул або супозиторіїв. У такій формі композиція розділяється на одиничні дози, які міс 35 94053 тять належну кількість активного інгредієнта; окремі дозовані форми можуть бути розфасованими композиціями, наприклад, порошками у пакетах, флаконами, ампулами, попередньо заповненими шприцами або саше, які містять рідини. Форма дозованої одиниці може бути, наприклад, самою капсулою або таблеткою, або може бути відповідною кількістю будь-яких подібних композицій у формі упаковки. Терапевтично ефективна кількість сполуки формули I, яку вводять пацієнтові, може бути різною, залежно від того, що вводиться, мети введення, такої, як профілактика або терапія, стану пацієнта, способу введення і т.ін. при терапевтичному застосуванні сполуки формули I вводять пацієнтові, який страждає від стану, у кількості, достатній для лікування або принаймні часткового лікування від симптомів стану та його ускладнень. Достатня для цього кількість є "терапевтично ефективною кількістю", як описано авторами вище. Доза, яка має бути застосована для лікування конкретного випадку, може суб’єктивно визначатися лікарем. До задіяних змінних належать конкретний стан і розмір, вік та характер реакції пацієнта. Лікування від наркотичної або алкогольної залежності так само вимагає дотримання суб’єктивно визначеного введення медикаменту під наглядом лікаря. Зазвичай початкова доза становить приблизно 5 мг на день з поступовим підвищенням денної дози до приблизно 150 мг на день для забезпечення потрібного рівня дозування у пацієнта. У деяких варіантах втілення даний винахід стосується проліків сполук формули I. Термін “проліки” у даному описі означає сполуку, яка може бути перетворена in vivo метаболічними засобами (наприклад, шляхом гідролізу) на сполуку формули I. Спеціалістам у даній галузі є відомими різні форми проліків, такі, як обговорюються, наприклад, у публікаціях Bundgaard, (ed.), Design of Prodrugs, Elsevier (1985); Widder, et al. (ed.), Methods in Enzymology, vol. 4, Academic Press (1985); Krogsgaard-Larsen, et al., (ed). “Design and Application of Prodrugs, Textbook of Drug Design and Development, Chapter 5, 113-191 (1991), Bundgaard, et al., Journal of Drug Delivery Reviews, 8:1-38(1992), Bundgaard, J. of Pharmaceutical Sciences, 77:285 et seq. (1988); and Higuchi and Stella (eds.) Prodrugs as Novel Drug Delivery Systems, American Chemical Society (1975). Для більш чіткого розуміння і для більш чіткого 36 пояснення винаходу нижче представлено його конкретні приклади. Представлені нижче приклади подаються лише для пояснення і не можуть розглядатись як такі, що якимось чином обмежують обсяг винаходу та його основні принципи. Терміни H ЯМР, MS та HPLC означають мас-спектр, високоефективну рідинну хроматографію та протонний ядерний магнітний резонанс, відповідно. Терміни THF, DMF та DMSO означають тетрагідрофуран, диметилформамід та диметилсульфоксид, відповідно. Колонкову хроматографію в усіх випадках здійснювали з застосуванням як підкладки SiO2. Якщо не зазначено іншого, всі частини є масовими частинами. Приклад 1 [2-(3-Бензолсульфоніл-1H-індазол-5-ілокси)етил]-диметил-амін Етап 1 Cl F + F O S O KOtBu/THF NO2 NO2 O S O 2-Бензолсульфонілметил-4-фторо-1-нітробензол: До розчину хлорометилфенілсульфону (10,51г, 55,13ммоль) у THF (110мл) додавали 5,9мл (56ммоль) 1-фторо-4-нітробензолу. Реакційну суміш охолоджували до 0°C і по краплях додавали 1,0M трет-бутоксиду калію у THF (145мл, 145ммоль). Реакційну суміш перемішували в атмосфері азоту при навколишній температурі протягом однієї години. Після цього додавали оцтову кислоту (9мл, 160ммоль). Реакційну суміш піддавали випарюванню розчинника і розподіляли між сольовим розчином та етилацетатом. Органічну фазу після цього висушували безводним сульфатом магнію, фільтрували й концентрували. Залишок перемішували в діетиловому етері, фільтрували й висушували у вакуумі при 73°C протягом 12 годин. Одержували 2-бензолсульфонілметил-4фторо-1-нітробензол у вигляді твердої речовини світлого буро-жовтого кольору (10.24г, 62.8%): Т.пл.: 169-171°C; Мас-спектр (-EI, [M-H]-) m/z 294. 1 H ЯМР (500MГц, DMSO-d6): δ8,10-8,14 (m, 1H), 7,70-7,75 (m, 1H), 7,56-7,63 (m, 4H), 7,45-7,50 (m, 1H), 7,20 (dd, 1H, J=9,27Гц та 2,81Гц), 5,12 ppm (s, 2H). Елементний аналіз для C13H10FNO4S: Розраховано: C, 52.88; H, 3.41; N, 4.74; Виявлено: C, 52,63; H, 3,14; N, 4,66; Етап 2 HO F NO2 O S O + HO OH 2-(3-Бензолсульфонілметил-4-нітро-фенокси)етанол Суміш 2-бензолсульфонілметил-4-фторо-1нітробензол (10,2г, 34,7ммоль), етиленгліколь (80мл, 1,4моль) та 1M трет-бутоксиду калію у THF (78мл, 78ммоль) у THF (50мл) піддавали дефлегмації в атмосфері азоту протягом 30 хвилин. Після O KOtBu/THF O S O NO2 охолодження приблизно до навколишньої температури реакційну суміш піддавали випарюванню розчинника. До залишку додавали воду і виливали його у 2,0N хлористоводневої кислоту та лід. Потім суміш екстрагували етилацетатом і промивали водою та сольовим розчином. Органічну фазу висушували безводним сульфатом магнію, фільтру 37 94053 вали, концентрували і висушували у вакуумі при 74°C протягом 20 хвилин. Одержували 2-(3бензолсульфонілметил-4-нітро-фенокси)-етанол у вигляді темно-бурої смоли (11,7г, 100%-й вихід); 1 Мас-спектр (-EI, [M-H] ) m/z 336. H ЯМР (500MГц, DMSO-d6): δ8,01 (d, 1H, J=9,15Гц), 7,67-7,73 (m, 38 1H), 7,54-7,63 (m, 4H), 7,10 (dd, 1H, J=9,51Гц та 2,93Гц), 6,85 (d, 1H, J=2,81Гц), 5,12 (s, 2H), 4,884,90 (m, 1H), 3,93-3,96 (m, 2H), 3,65 ppm (d, 2H, J=4,51Гц). Елементний аналіз для C15H15NO6S: Розрах.: C, 53,41; H, 4,48; N, 4.15; Виявлено: C, 53,47; H, 4,69; N, 4,04; Етап 3 хроматографії з 100% хлороформом та 5% метанолом у хлороформі. Висушували у вакуумі при 65°C протягом 20 хвилин для одержання 2-(3бензолсульфонілметил-4-нітро-фенокси)етилового естеру толуол-4-сульфонової кислоти у вигляді жовтої твердої речовини (8,1г, 69%); Мас-спектр (-EI, [M-H]-) m/z 490. 1H ЯМР (300MГц, DMSO-d6): δ7,99 (d, 1H, J=9,02Гц), 7,67-7,75 (m, 3H), 7,54-7,62 (m, 4H), 7,43 (d, 2H, J=7,93Гц), 7,00 (dd, 1H, J=9,15Гц та 2,80Гц), 6,78 (d, 1H, J=2,81Гц), 5,09 (s, 2H), 4,29-4,31 (m, 2H), 4,134,15 (m, 2H), 2,37 ppm (s, 3H). Елементний аналіз для C22H21NO8S 0,40моль H2O: Розраховано: C, 52,98; H, 4.41; N, 2,81; Виявлено: C, 52,67; H, 4,26; N, 2,61. 2-(3-бензолсульфонілметил-4-нітрофенокси)-етиловий естер толуол-4-сульфонової кислоти Суміш 2-(3-бензолсульфонілметил-4-нітрофенокси)-етанолу (8,2г, 24ммоль), pтолуолсульфонілхлориду (9,39г, 49,3ммоль) та триетиламіну (19мл, 140ммоль) у метиленхлориді (85мл) перемішували при навколишній температурі в атмосфері азоту протягом 4,5 години. Потім її піддавали випарюванню розчинника і розподіляли між метиленхлоридом та водним бікарбонатом натрію. Органічну фазу після цього промивали сольовим розчином, висушували безводним сульфатом магнію, фільтрували, концентрували і висушували у вакуумі при 63°C протягом 30 хвилин. Залишок очищали шляхом флешЕтап 4 TosO TosO O THF/EtOH 10 % Pd/C O O O S O S O NO2 NH2 2-(4-аміно-3-бензолсульфонілметилфенокси)-етиловий естер толуол-4-сульфонової кислоти Розчин 2-(3-бензолсульфонілметил-4-нітрофенокси)-етилового естеру толуол-4сульфонової кислоти (13,1г, 26,7ммоль) у THF (350мл) та етанолі (250мл) додавали до 10% паладію на вугіллі (5,8г) і гідрогенізували на апараті Парра протягом однієї години (початковий тиск 30-40 psi). Суміш фільтрували над целітом, концентрували й висушували у вакуумі при 80°C протягом 30 хвилин для одержання 2-(4-аміно-3 бензолсульфонілметил-фенокси)-етилового естеру толуол-4-сульфонової кислоти у вигляді світло-жовтої твердої речовини (11,7г, 95,1%): Т.пл.: 144-6°C; Мас-спектр (+EI, [M+H]+) m/z 462. 1 H ЯМР (500MГц, DMSO-d6): δ7,72-7,75 (m, 4H), 7,63-7,66 (m, 1H), 7,52-7,56 (m, 2H), 7,44 (d, 2H, J=8,05Гц), 6,52 (d, 2H, J=1,58Гц), 6,29-6,30 (m, 1H), 4,65 (s, 2H), 4,46 (s, 2H), 4,16-4,18 (m, 2H), 3,79-3,82 (m, 2H), 2,38 ppm (s, 3H). Елементний аналіз для C22H23NO6S: Розраховано: C, 57,25; H, 5,02; N, 3,03; Виявлено: C, 57,60; H, 4,98; N, 3,10. Етап 5 TosO O O S O EtOH/HCl NaNO2 NH2 2-(3-бензолсульфоніл-1H-індазол-5-ілокси)етиловий естер толуол-4-сульфонової кислоти До суміші 2-(4-аміно-3бензолсульфонілметил-фенокси)-етилового естеру толуол-4-сульфонової кислоти (11,7г, O S O O O O S O N N H 25,3ммоль) в етанолі (350мл) та 1,0 N хлористоводневій кислоті (425мл) по краплях додавали нітрит натрію (2,67г, 38,7ммоль) у воді (50мл). Після перемішування при навколишній температурі протягом 1,5 години, додавали твердий кар 39 94053 бонат натрію до основного рівня pH. Реакційну суміш перемішували протягом додаткових 2 годин. Після цього її піддавали випарюванню розчинника і екстрагували теплим етилацетатом. Органічну фазу промивали водою та сольовим розчином, висушували безводним сульфатом магнію, фільтрували й концентрували. Залишок очищали шляхом флеш-хроматографії з 2% метанолом у хлороформі для одержання 2-(3 40 бензолсульфоніл-1H-індазол-5-ілокси)-етилового естеру толуол-4-сульфонової кислоти у вигляді оранжевої твердої речовини (9,54г, 79,5%): Т.пл.: 174-7°C; Мас-спектр (-EI, [M-H]-) m/z 471, 1H ЯМР (500MГц, DMSO-d6): δ14,11 (s, 1H), 7,96-7,98 (m, 2H), 7,74-7,77 (m, 2H), 7,62-7,66 (m, 1H), 7,53-7,59 (m, 3H), 7,39 (d, 2H, J=8,05Гц), 7,24 (d, 1H, J=2,32Гц), 6,97-7,00 (m, 1H), 4,35-4,37 (m, 2H), 4,21-4,23 (m, 2H), 2,33 ppm (s, 3H). Етап 6 O S O O O S O O THF/Me2NH N N O S O O N N H N H [2-(3-Бензолсульфоніл-1H-індазол-5-ілокси)етил]-диметил-амін Розчин 2-(3-бензолсульфоніл-1H-індазол-5ілокси)-етилового естеру (0,341г, 0,722ммоль) толуол-4-сульфонової кислоти у 2,0N диметиламіну у THF (9мл, 18ммоль) перемішували при 70°C протягом 6 годин у герметично закритій пробірці. Після певного охолодження реакційну суміш піддавали випарюванню розчинника і розподіляли між етилацетатом та водним розчином бікарбонату натрію. Органічну фазу промивали водою та сольовим розчином. Висушували безводним сульфатом магнію, фільтрували й концентрували. Залишок розподіляли між етилацетатом/водним розчином карбонату калію. Органічну фазу промивали водою та сольовим розчином, висушували безводним сульфатом магнію, фільтрували й концентрували. В результаті одержували [2-(3-бензолсульфоніл-1H-індазол-5-ілокси)етил]-диметиламін у вигляді світлої жовто-бурої твердої речовини (0,167г, 67,1%). Сполуку розчиняли в метанолі і додавали етерний гідрохлорид. Після концентрування та висушування in vacuo протягом 12 годин при 70°C одержували гідрохлорид у вигляді світло-оранжевої твердої речовини (94,0 мг); Мас-спектр (+EI, [M+H]+) m/z 346. 1 H ЯМР (500MГц, DMSO-d6): δ14,22 (s, 1H), 10,00 (br, 1H), 7,97-7,99 (m, 2H), 7,56-7,68 (m, 4H), 7,42 (d, 1H, J=2,20Гц), 7,17-7,20 (m, 1H), 4,39-4,42 (m, 2H), 3,52-3,53 (m, 2H), 2,84 ppm (s, 6H). Приклад 2 O O S O O O S O EtMeNH, THF N O O S O N N N H [2-(3-Бензолсульфоніл-1H-індазол-5-ілокси)етил]-етил-метил-амін Розчин 2-(3-бензолсульфоніл-1H-індазол-5ілокси)-етилового естеру толуол-4-сульфонової кислоти (0,364г, 0,770ммоль) та Nетилметиламіну (0,95мл, 11ммоль) у THF (8мл) перемішували протягом 6 годин при 70°C у герметично закритій пробірці. Після певного охолодження до навколишньої температури реакційну суміш піддавали випарюванню розчинника і розподіляли між етилацетатом та водним розчином бікарбонату натрію. Органічну фазу промивали водою та сольовим розчином, висушували безводним сульфатом магнію, фільтрували й концентрували. Після висушування у вакуумі при на N H вколишній температурі протягом 1,5 години утворену в результаті темно-жовту тверду речовину (0,249г, 89,9%), [2-(3-бензолсульфоніл-1Hіндазол-5-ілокси)-етил]-етил-метил-амін, розчиняли у метанолі та метиленхлориді й додавали етерний гідрохлорид. Концентрування та висушування при 80°C протягом 12 годин забезпечували на виході гідрохлорид у вигляді світло-оранжевої твердої речовини (0,253г); Мас-спектр (+EI, [M+H]+) m/z 360, 1H ЯМР (500MГц, DMSO-d6): δ14,23 (s, 1H), 9,95 (br, s, 1H), 7,97-7,99 (m, 2H), 7,56-7,68 (m, 4H), 7,42 (d, 1H, J=2,32Гц), 7,19 (dd, 1H, J=9,15Гц та 2,32Гц), 4,41-4,43 (m, 2H), 3,553,60 (m, 1H), 3,43-3,49 (m, 1H), 3,11-3,17 (m, 1H), 2,82 (d, 3H, J=4,63Гц), 1,22-1,25 ppm (m, 3H). 41 94053 42 Приклад 3 O O S O O O S O NH N O O S O N N N H N H THF 3-Бензолсульфоніл-5-(2-піперидин-1-ілетокси)-1H-індазол Розчин 2-(3-бензолсульфоніл-1H-індазол-5ілокси)-етилового естеру толуол-4-сульфонової кислоти (0,386г, 0,817ммоль) та піперидину (1,0мл, 10ммоль) у THF (8мл) перемішували при 70°C протягом 6 годин у герметично закритій пробірці. Після певного охолодження до навколишньої температури реакційну суміш піддавали випарюванню розчинника і розподіляли між етилацетатом та водним розчином бікарбонату натрію. Органічну фазу промивали водою та сольовим розчином. Висушували безводним сульфатом магнію, фільтрували й концентрували. Висушування у вакуумі при 80°C протягом 20 в результаті забезпечувало 3-бензолсульфоніл5-(2-піперидин-1-іл-етокси)-1H-індазол у вигляді світло-жовтої твердої речовини (0,275г, 87,3%). Його розчиняли у метанолі і додавали етерний гідрохлорид. Цю суміш концентрували й висушували у вакуумі при 70°C протягом приблизно 12 годин для одержання на виході гідрохлориду у вигляді жовтої твердої речовини (0,268г): Т.пл.: 249-250°C; Мас-спектр (+EI, [M+H]+) m/z 386, 1H ЯМР (500MГц, DMSO-d6): δ14,24 (s, 1H), 10,0210,03 (br, 1H), 7,97-7,99 (m, 2H), 7,56-7,68 (m, 4H), 7,41 (d, 1H, J=2,32Гц), 7,18 (dd, 1H, J=9,15Гц та 2,33Гц), 4,44-4,46 (m, 2H), 3,48-3,51 (m, 4H), 2,943,04 (m, 2H), 1,65-1,77 (m, 5H), 1,31-1,42 ppm (m, 1H). Елементний аналіз для C20H23N3O3 S.1,00моль HCl · 0,15моль H2O: Розрах.: C, 56,57; H, 5,77; N, 9,90; Виявлено: C, 56,34; H, 5,88; N, 9,57. Приклад 4 O O S O O O S O EtNH2/THF N H N O O S O N N H N H [2-(3-Бензолсульфоніл-1H-індазол-5-ілокси)етил]-етил-амін Розчин 2-(3-бензолсульфоніл-1H-індазол-5ілокси)-етилового естеру толуол-4-сульфонової кислоти (0,361г, 0,764ммоль) у 2,0 N етиламіну у THF (9мл, 18ммоль) перемішували при 70°C протягом 6 годин у герметично закритій пробірці. Після певного охолодження реакційну суміш піддавали випарюванню розчинника і розподіляли між етилацетатом та водним розчином бікарбонату натрію. Органічну фазу після цього промивали водою та сольовим розчином, висушували безводним сульфатом магнію, фільтрували й концентрували. Залишок очищали шляхом флешхроматографії з застосуванням 10% метанолу в хлороформі. Після висушування у вакуумі при 68°C протягом 20 хвилин одержували [2-(3бензолсульфоніл-1H-індазол-5-ілокси)-етил]етил-амін у вигляді світло-бурої смоли (0,116г, 43,9%). Його розчиняли у хлороформі та метанолі і додавали етерний гідрохлорид. Концентрування та висушування при 74°C протягом 13,5 години in vacuo забезпечували на виході гідрохлорид у вигляді темно-жовтої твердої речовини (0,113г): Т.пл.: 248-50°C (dec). Мас-спектр (+EI, [M+H]+) m/z 346. 1H ЯМР (500MГц, DMSO-d6): δ14,23 (s, 1H), 8,81 (br, 2H), 7,96-7,98 (m, 2H), 7,56-7,68 (m, 4H), 7,40 (d, 1H, J=2,07Гц), 7,19 (dd, 1H, J=9,15Гц та 2,32Гц), 4,31 (t, 2H, J=5,00Гц), 3,35 (br, 2H), 3,00-3,05 (m, 2H), 1,18-1,22 ppm (m, 3H). Приклад 5 O O S O O O S O Et2NH, THF N O O S O N N N H [2-(3-Бензолсульфоніл-1H-індазол-5-ілокси)етил]-діетил-амін Розчин 2-(3-бензолсульфоніл-1H-індазол-5ілокси)-етилового естеру толуол-4-сульфонової кислоти (0,420г, 0,889ммоль) та діетиламіну (1,0мл, 9,7ммоль) у THF (8мл) перемішували при N H 70°C протягом 6 годин у герметично закритій пробірці. Додавали додатковий діетиламін (1,0мл, 9,7ммоль) і реакційну суміш перемішували при 80°C у герметично закритій пробірці протягом 6 годин. Після певного охолодження реакційну суміш піддавали випарюванню розчинника і 43 94053 розподіляли між етилацетатом та водним розчином бікарбонату натрію. Органічну фазу після цього промивали водою та сольовим розчином, висушували безводним сульфатом магнію, фільтрували й концентрували. Залишок очищали шляхом флеш-хроматографії з застосуванням 7,5% метанолу в хлороформі. Після висушування у вакуумі при 80°C протягом 20 хвилин одержували [2-(3-бензолсульфоніл-1H-індазол-5-ілокси)етил]-діетил-амін у вигляді блідо-жовтої твердої речовини (0,155г, 46,6%). Його розчиняли у метанолі та хлороформі й додавали етерний гідрох 44 лорид. Суміш концентрували й висушували у вакуумі при 74°C протягом 13,5 години для одержання на виході гідрохлориду у вигляді світлооранжевої твердої речовини (0,163г); Мас-спектр + 1 (+EI, [M+H] ) m/z 374. H ЯМР (500MГц, DMSOd6): δ14,24 (s, 1H), 9,94 (br, 1H), 7,96-7,99 (m, 2H), 7,56-7,68 (m, 4H), 7,41 (d, 1H, J=2,20Гц), 7,16-7,19 (m, 1H), 4,40-4,43 (m, 2H), 3,52 (br, 2H), 3,19-3,23 (m, 4H), 1,23 ppm (t, 6H, J=7,20Гц). Елементний аналіз для C19H23N3O3S .1,00моль HCl · 0,20моль H2O: Розраховано: C, 55,18; H, 5,95; N, 10,16; Виявлено: C, 54,85; H, 5,85; N, 10,02. Приклад 6 O O S O O O S O iPrNH2, THF N H N O S O O N N H [2-(3-Бензолсульфоніл-1H-індазол-5-ілокси)етил]-ізопропіл-амін Розчин 2-(3-бензолсульфоніл-1H-індазол-5ілокси)-етилового естеру толуол-4-сульфонової кислоти (0,378г, 0,800ммоль) та ізопропіламіну (1,0мл, 12ммоль) у THF (8мл) перемішували при 70°C протягом 6 годин у герметично закритій пробірці. Додавали додатковий ізопропіламін (1,0мл, 12ммоль) і реакційну суміш перемішували при 80°C протягом 6 годин у герметично закритій пробірці. Після певного охолодження реакційну суміш піддавали випарюванню розчинника і розподіляли між етилацетатом та водним розчином бікарбонату натрію. Органічну фазу після цього промивали водою та сольовим розчином, висушували безводним сульфатом магнію, фільтрували й концентрували. Залишок очищали шляхом флеш-хроматографії з застосуванням 10% метанолу в хлороформі. Після висушування у вакуумі N H при 80°C протягом 30 хвилин одержували [2-(3бензолсульфоніл-1H-індазол-5-ілокси)-етил]ізопропіл-амін у вигляді блідо-жовтої твердої речовини (0,110г, 38,2%). Його розчиняли у метанолі та хлороформі й додавали етерний гідрохлорид. Суміш концентрували й висушували у вакуумі при 74°C протягом 13,5 години для одержання на виході гідрохлориду у вигляді кремової твердої речовини (0,117г): Т.пл.: 275-7°C (dec); Мас-спектр (+EI, [M+H]+) m/z 360. 1H ЯМР (500MГц, DMSO-d6): δ14,22 (br, 1H), 8,75 (br, 2H), 7,96-7,98 (m, 2H), 7,56-7,68 (m, 4H), 7,41 (d, 1H, J=2,08Гц), 7,19 (dd, 1H, J=9,15Гц та 2,32Гц), 4,304,33 (m, 2H), 3,34-3,40 (m, 3H), 1,25 ppm (d, 6H, J=6,59Гц). Елементний аналіз для C18H21N3O3S.1,00моль HCl · 0,10моль H2O: Розраховано: C, 54,36; H, 5,36; N, 10,57; Виявлено: C, 54,02; H, 5,42; N, 10,22. Приклад 7 O S O O O O S O N N H [2-(3-Бензолсульфоніл-1H-індазол-5-ілокси)етил]-бутил-амін Розчин 2-(3-бензолсульфоніл-1H-індазол-5ілокси)-етилового естеру толуол-4-сульфонової кислоти (0,348г, 0,736ммоль) та n-бутиламіну (1,0мл, 10ммоль) у THF (8мл) перемішували при 70°C протягом 6 годин у герметично закритій пробірці. Після певного охолодження реакційну суміш піддавали випарюванню розчинника і розподіляли між етилацетатом та водним розчином бікарбонату натрію. Органічну фазу після цього промивали водою та сольовим розчином, висушували безводним сульфатом магнію, фільтрували й концентрували. Залишок очищали шляхом флеш-хроматографії з застосуванням 7,5-10% THF,BuNH2 N H O O S O N N H метанолу в хлороформі. Після висушування у вакуумі при 55°C протягом 40 хвилин одержували [2-(3-бензолсульфоніл-1H-індазол-5-ілокси)етил]-бутил-аміну у вигляді світло-бежевої напівтвердої речовини (0,105г, 38,2%). Його розчиняли у хлороформі й додавали етерний гідрохлорид. Утворену в результаті тверду речовину фільтрували і висушували у вакуумі при 75°C протягом 16,5 години для одержання на виході гідрохлориду у вигляді білої твердої речовини (0,0813г): Т.пл.: 271-3°C dec; Мас-спектр (+EI, [M+H]+) m/z 374, 1H ЯМР (300MГц, DMSO-d6): δ14,27-14,35 (br, 1H), 8,98-9,00 (br, 2H), 8,03-8,06 (m, 2H), 7,627,76 (m, 4H), 7,46 (d, 1H, J=2,19Гц) 7,25 (dd, 1H, J=9,15Гц та 2,29Гц), 4,38-4,41 (m, 2H), 3,41-3,44 45 94053 (m, 2H), 3,03 (t, 2H, J=7,87Гц), 1,62-1,72 (m, 2H), 1,33-1,45 (m, 2H), 0,94 ppm (t, 3H, J=7,32Гц). Елементний аналіз для C19H23N3O3S .1,00моль HCl · 46 0,05моль H2O: Розраховано: C, 55,55; H, 5,91; N, 10,23; Виявлено: C, 55,23; H, 5,87; N, 10,09. Приклад 8 O O S O O S O O EtMeNH, THF O N H N N H O S O N N H флеш-хроматографії з застосуванням 5% метанолу в хлороформі. Після висушування у вакуумі при температурі 55°C протягом 25 хвилин одержували [2-(3-бензолсульфоніл-1H-індазол-5ілокси)-етил]-циклопропіл-амін у вигляді світложовтої піни (0,127г, 50,0%). Його розчиняли у хлороформі й додавали етерний гідрохлорид. Суміш концентрували й висушували у вакуумі при 75°C протягом 16,5 години для одержання на виході гідрохлориду у вигляді темно-жовтої твердої речовини (0,131г): Т.пл.: 184-5°C dec.; Масспектр (+EI, [M+H]+) m/z 358. 1H ЯМР (300MГц, DMSO-d6): δ14,33 (s, 1H), 9,33 (br, 2H), 8,03-8,06 (m, 2H), 7,60-7,76 (m, 4H), 7,47 (d, 1H, J=2,11Гц), 7,25 (dd, 1H, J=9,15Гц та 2,38Гц), 4,40-4,43 (m, 2H), 3,49-3,52 (m, 2H), 2,81-2,88 (m, 1H), 1,62-1,72 (m, 2H), 0,92-0,97 (m, 2H), 0,77-0,87 ppm (m, 2H). [2-(3-Бензолсульфоніл-1H-індазол-5-ілокси)етил]-циклопропіл-амін Розчин 2-(3-бензолсульфоніл-1H-індазол-5ілокси)-етилового естеру толуол-4-сульфонової кислоти (0,336г, 0,711ммоль) та циклопропіламіну (1,0мл, 14ммоль) у THF (8мл) перемішували при 70°C протягом 6 годин у герметично закритій пробірці. Додавали додатковий циклопропіламін (1,0мл, 14ммоль) і реакційну суміш перемішували протягом 6 годин при 80°C у герметично закритій пробірці. Після певного охолодження реакційну суміш піддавали випарюванню розчинника і розподіляли між етилацетатом та водним розчином бікарбонату натрію. Органічну фазу після цього промивали водою та сольовим розчином, висушували безводним сульфатом магнію, фільтрували й концентрували. Залишок очищали шляхом Приклад 9 O S O O O O S O NH2 THF N H N O S O O N N H N H піролідин-1-іл-етокси)-1H-індазол у вигляді жовтої піни (0,137г, 48,8%). Його розчиняли у метанолі та хлороформі й додавали етерний гідрохлорид. Суміш концентрували й висушували у вакуумі при 75°C протягом 16,5 години для одержання на виході гідрохлориду у вигляді білої твердої речовини (0,0956г): Т.пл.: 255-8°C(dec.); Мас-спектр (+EI, [M+H]+) m/z 386. 1H ЯМР (300MГц, DMSOd6): δ14,31-14,41 (br, 1H), 9,13-9,14 (br, 2H), 8,038,06 (m, 2H), 7,62-7,76 (m, 4H), 7,46 (d, 1H, J=2,10Гц) 7,25 (dd, 1H, J=9,15Гц та 2,29Гц), 4,394,42 (m, 2H), 3,58-3,63 (m, 1H), 3,41 (s, 2H), 1,992,05 (m, 2H), 1,67-1,82 (m, 4H), 1,53-1,62 ppm (m, 2H). Елементний аналіз для C20H23N3O3S . 1,00моль HCl·0,50моль H2O: Розраховано: C, 55,74; H, 5,85; N, 9,75; Виявлено: C, 55,39; H, 5,74; N, 9,62. 3-Бензолсульфоніл-5-(2-піролідин-1-ілетокси)-1H-індазол Розчин 2-(3-бензолсульфоніл-1H-індазол-5ілокси)-етилового естеру толуол-4-сульфонової кислоти (0,345г, 0,730ммоль) та циклопентиламіну (1,0мл, 10ммоль) у THF (8мл) перемішували у герметично закритій пробірці при 70°C протягом 6 годин і при 80°C протягом 6 годин. Після певного охолодження реакційну суміш піддавали випарюванню розчинника і розподіляли між етилацетатом та водним розчином бікарбонату натрію. Органічну фазу після цього промивали водою та сольовим розчином, висушували безводним сульфатом магнію, фільтрували й концентрували. Залишок очищали шляхом флеш-хроматографії з застосуванням 7,5% метанолу в хлороформі. Після висушування у вакуумі при 57°C протягом 25 хвилин одержували 3-бензолсульфоніл-5-(2Приклад 10 O O S O O O S O N N H H N O THF N O O O S O N N H 47 94053 48 при 57°C протягом 20 хвилин одержували 3бензолсульфоніл-5-(2-морфолін-4-іл-етокси)-1Hіндазол у вигляді кремової піни (0,0443г, 15,1%). Його розчиняли у метанолі та хлороформі й додавали етерний гідрохлорид. Суміш концентрували й висушували у вакуумі при 75°C протягом 16,5 години для одержання на виході гідрохлориду у вигляді світло-оранжевої твердої речовини (0,0411г). Мас-спектр (+EI, [M+H]+) m/z 388. 1H ЯМР (300MГц, DMSO-d6): δ14,31 (s, 1H), 10,82-88 (br, 1H), 8,03-8,07 (m, 2H), 7,62-7,76 (m, 4H), 7,49 (d, 1H, J=2,10Гц), 7,26 (dd, 1H, J=9,14Гц та 2,28Гц), 4,54 (s, 2H), 4,02 (d, 2H, J=11,71Гц), 3,803,87 (m, 2H), 3,51-3,73 (m, 4H), 3,19-3,31 ppm (m, 2H). 3-Бензолсульфоніл-5-(2-морфолін-4-ілетокси)-1H-індазол Розчин 2-(3-бензолсульфоніл-1H-індазол-5ілокси)-етилового естеру толуол-4-сульфонової кислоти (0,359г, 0,760ммоль) та морфоліну (1,0мл, 11ммоль) у THF (8мл) перемішували при 70°C протягом 6 годин у герметично закритій пробірці. Після певного охолодження реакційну суміш піддавали випарюванню розчинника і розподіляли між етилацетатом та водним розчином бікарбонату натрію. Органічну фазу після цього промивали водою та сольовим розчином, висушували безводним сульфатом магнію, фільтрували й концентрували. Залишок очищали шляхом флеш-хроматографії з застосуванням 5% метанолу в хлороформі. Після висушування у вакуумі Приклад 11 O O S O O S O O N N H N N H O S O O N N H THF 3-Бензолсульфоніл-5-(2-піролідин-1-ілетокси)-1H-індазол Розчин 2-(3-бензолсульфоніл-1H-індазол-5ілокси)-етилового естеру толуол-4-сульфонової кислоти (0,347г, 0,734ммоль) та піролідин (1,0мл, 12ммоль) у THF (8мл) перемішували при 70°C у герметично закритій пробірці протягом 6 годин. Після певного охолодження реакційну суміш піддавали випарюванню розчинника і розподіляли між етилацетатом та водним розчином бікарбонату натрію. Органічну фазу після цього промивали водою та сольовим розчином, висушували безводним сульфатом магнію, фільтрували й концентрували. Залишок очищали шляхом флешхроматографії з застосуванням 7,5% метанолу в хлороформі. Після висушування при 55°C in vacuo одержували 3-бензолсульфоніл-5-(2піролідин-1-іл-етокси)-1H-індазол у вигляді блідожовтої твердої речовини (0,0595г, 21,8%). Його розчиняли у метанолі та хлороформі й додавали етерний гідрохлорид. Суміш концентрували й висушували у вакуумі при 75°C протягом 16,5 години для одержання на виході гідрохлориду у вигляді жовтоїпіни (0,0598г). Мас-спектр (+EI, [M+H]+) m/z 372. 1H ЯМР (300MГц, DMSO-d6): δ14,30 (s, 1H), 10,35 (br, 1H), 8,05 (d, 2H, J=7,04Гц), 7,63-7,75 (m, 4H), 7,48 (d, 1H, J=1,83Гц) 7,25-7,29 (m, 1H), 4,45-4,48 (m, 2H), 3,66 (s, br, 4H), 3,18-3,19 (m, 2H), 1,94-2,06 ppm (m, 4H). Приклад 12 O O S O O O S O N N H [2-(3-Бензолсульфоніл-1H-індазол-5-ілокси)етил]-метил-амін Розчин 2-(3-бензолсульфоніл-1H-індазол-5ілокси)-етилового естеру толуол-4-сульфонової кислоти (0,340г, 0,720ммоль) у 2,0M метиламіну у THF (8мл, 16ммоль) перемішували при 70°C у герметично закритій пробірці протягом приблизно 15,5 години. Після певного охолодження реакційну суміш піддавали випарюванню розчинника і розподіляли між хлороформом та водним розчином бікарбонату натрію. Органічну фазу після цього промивали сольовим розчином, висушували безводним сульфатом магнію, фільтрували й концентрували. Залишок очищали шляхом флеш MeNH2/THF N H O O S O N N H хроматографії з застосуванням 10% метанолу в хлороформі та 1,0% гідроксиду амонію/10% метанолу в хлороформі. Після висушування при 57°C in vacuo протягом 20 хвилин одержували [2(3-бензолсульфоніл-1H-індазол-5-ілокси)-етил]метил-амін у вигляді світло-жовтої напівтвердої речовини (0,0461г, 19,4%). Його розчиняли у метанолі та хлороформі й додавали етерний гідрохлорид. Суміш концентрували й висушували у вакуумі при 73°C протягом 20 годин для одержання на виході гідрохлориду у вигляді жовтобурої піни (0,0422г). Мас-спектр (+EI, [M+H]+) m/z 332. 1H ЯМР (500MГц, DMSO-d6): δ14,24 (s, 1H), 49 94053 8,89 (s, 2H), 7,96-7,99 (m, 2H), 7,53-7,68 (m, 4H), 7,40 (d, 1H, J=2,19Гц), 7,25 (dd, 1H, J=9,15Гц та 50 2,32Гц), 4,30-4,32 (m, 2H), 3,33-3,35 (m, 2H), 2,602,63 ppm (m, 3H). Приклад 13 O S O O O O S O NH3, THF H2N N O N N H N H 2-(3-Бензолсульфоніл-1H-індазол-5-ілокси)етиламін У п’яти різних реакціях рідкий аміак (приблизно 10мл) додавали до -78°C розчину 2-(3бензолсульфоніл-1H-індазол-5-ілокси)-етилового естеру толуол-4-сульфонової кислоти (1,72г, 3,63ммоль) у THF (48мл). Його зазвичай залишали нагріватися до навколишньої температури. Нагрівали у герметично закритій пробірці протягом приблизно 16-35 годин при 70-100°C. Після охолодження приблизно до навколишньої температури комбіновану реакційну суміш виливали у надлишкову кількість розчину бікарбонату натрію і екстрагували хлороформом або метиленхлоридом. Органічну фазу промивали сольовим розчином, висушували безводним сульфатом магнію, фільтрували й концентрували. Залишок очищали шляхом флеш-хроматографії з 0,75% гідроксиду амонію/7,5% метанолу в хлороформі. Залишок піддавали подальшому очищенню шляхом HPLC з використанням 30-80% (хлороформу/метанолу(8:2)/TEA) у гептані/TEA. Концентрування й висушування забезпечували на виході 2(3-бензолсульфоніл-1H-індазол-5-ілокси)етиламін у вигляді білої твердої речовини, до якої додавали метанол та етерний гідрохлорид. Концентрування та висушування протягом 30 годин у вакуумі при 83°C забезпечували на виході гідрохлорид у вигляді твердої речовини кремового кольору (0,0951г, 7,4%): Т.пл.: >300°C; Мас-спектр (-EI, [M-H]-) m/z 316. 1H ЯМР (500MГц, DMSO-d6): δ14,24(s, 1H), 8,09 (br,s, 3H), 7,96-7,98 (m, 2H), 7,56-7,68 (m, 4H), 7,39 (d, 1H, J=2,20Гц), 7,17 (dd, 1H, J=9,15Гц та 2,32Гц), 4,22-4,25 (m, 2H), 3,203,24 ppm (m, 2H). Елементний аналіз для C15H15N3O3S .1,00моль HCl·0,85моль H2O: Розраховано: C, 48,81; H, 4,83; N, 11,38; Виявлено: C, O S O 48,65; H, 4,77; N, 11,00. Приклад 14 Диметил-{3-[3-(нафталін-1-сульфоніл)-1Hіндазол-5-ілокси]-пропіл}-амін Етап 1 Cl Cl O S O O S O 1. Na2SO3, NaHCO3, H2O 2. ClCH2Br, Bu4NBr 1-Хлорометансульфоніл-нафталін Суміш 1-нафталінсульфонілхлориду (20,2г, 89,1ммоль), сульфіту натрію (22,5г, 178ммоль) та бікарбонату натрію (15,1г, 180ммоль) у воді (125мл) перемішували при 100°C протягом однієї години. Після охолодження до навколишньої температури протягом 40 хвилин додавали бромохлорометан (90мл, 1,4моль) та тетрабутиламонійбромід (2,87г, 8,91ммоль). Реакційну суміш після цього перемішували при 75°C протягом 14,5 години. Після охолодження до навколишньої температури шари реакційної суміші розділяли і органічну фазу концентрували. Залишок очищали шляхом флеш-хроматографії з 100% етилацетатом. Після концентрування додавали гексан для сприяння затвердненню і суміш знову концентрували. Висушування при 80°C in vacuo протягом 20 хвилин забезпечувало на виході 1хлорометансульфоніл-нафталін у вигляді блідожовтої твердої речовини (19,0г, 88,8%). MP 1035°C. Мас-спектр (+EI, M+) m/z 240. 1H ЯМР (500MГц, DMSO-d6): δ8,64-5 (m, 1H), 8,41 (d, 1H, J=8,23Гц), 8,27 (dd, 1H, J=7,33Гц та 1,22Гц), 8,168,18 (m, 1H), 7,71-7,81 (m, 3H), 5,40 ppm, (s, 2H), Елементний аналіз для C11H9ClO2S: Розраховано: C, 54,89; H, 3,77; N, 0,00; Виявлено: C, 54,98; H, 3,81; N, 0,00. Етап 2 Cl F + O S O NO2 1-(5-Фторо-2-нітро-фенілметансульфоніл)нафталін До охолодженої суміші 1хлорометансульфоніл-нафталіну (19,7г, 81,8ммоль) та 1-фторо-4-нітробензолу (8,7мл, 82ммоль) у сухому THF (197мл) по краплях додавали 1,0M t-бутоксиду калію у THF (205мл, 205ммоль). Реакційну суміш перемішували при F KOtBu/THF NO2 O S O навколишній температурі в атмосфері азоту протягом 1,5 години. Після цього додавали кристалічну оцтову кислоту (16мл, 280ммоль). Після перемішування при навколишній температурі протягом 1 години 40 хвилин реакційну суміш концентрували й розподіляли між теплим етилацетатом та сольовим розчином. Органічну фазу висушували безводним сульфатом магнію, філь 51 94053 52 1 трували й концентрували. Твердий залишок перемішували в етері, фільтрували й висушували при 82°C in vacuo протягом 1 години. На виході одержували 1-(5-фторо-2-нітрофенілметансульфоніл)-нафталін у вигляді бурої/рудуватої твердої речовини (19,9г, 70,6%): Т.пл.: 155-160°C; Мас-спектр (-EI, [M-H]-) m/z 344. H ЯМР (300MГц, DMSO-d6): δ8,50-8,52 (m, 1H), 8,33 (d, 1H, J=8,30Гц), 8,06-8,14 (m, 2H), 7,97 (dd, 1H, J=7,32Гц та 1,22Гц), 7,62-7,74 (m, 3H), 7,447,48 (m, 1H), 7,23-7,26 (m, 1H), 5,23 ppm (s, 2H). Елементний аналіз для C17H12 FNO4S: Розраховано: C, 59,12; H, 3,50; N, 4,06; Виявлено: C, 58,77; H, 3,30; N, 3,92. Етап 3: F NO2 HO O S O + HO OH O KOtBu/THF NO2 3-[3-(Нафталін-1-сульфонілметил)-4-нітрофенокси]-пропан-1-ол До суміші 1-(5-фторо-2-нітрофенілметансульфоніл)-нафталіну (19,9г, 57,6ммоль) та 1,3-пропандіолу (49мл, 680ммоль) у сухому THF (17мл) по краплях додавали 1,0M трет-бутоксиду калію у THF (123мл, 123ммоль). Реакційну суміш піддавали дефлегмації в атмосфері азоту протягом 1 години. Давали охолонути до навколишньої температури. До реакційної суміші додавали воду і виливали у суміші льоду та 2,0N хлористоводневої кислоти. Після цього екстрагували етилацетатом. Органічну фазу промивали сольовим розчином, висушували безводним сульфатом магнію, фільтрували й концентрува O S O ли. Залишок очищали шляхом флешхроматографії з застосуванням 60% етилацетату в гексані та 100% етилацетату. В результаті одержували жовту тверду речовину (12,9г, 55,8%-й вихід), 3-[3-(нафталін-1-сульфонілметил)-4-нітрофенокси]-пропан-1-ол: Т.пл.: 134-5°C; Мас-спектр (-EI, [M-H]-) m/z 400. 1H ЯМР (500MГц, DMSO-d6): δ8,50-8,53 (m, 1H), 8,31 (d, 1H, J=8,17Гц), 8,108,12 (m, 1H), 7,95-7,99 (m, 2H), 7,61-7,71 (m, 3H), 7,06 (dd, 1H, J=9,15Гц та 2,80Гц), 6,78 (d, 1H, J=2,81Гц), 5,23 (s, 2H), 4,52-4,55 (m, 1H), 3,913,94 (m, 2H), 3,43-3,47 (m, 2H), 1,71- 1,78 ppm (m, 2H). Елементний аналіз для C20H19NO6S: Розрах.: C, 59,84; H, 4,77; N, 3,49; Виявл.: C, 59,78; H, 4,41; N, 3,43. Етап 4 3-[3-(нафталін-1-сульфонілметил)-4-нітрофенокси]-пропіловий естер толуол-4сульфонової кислоти Розчин 3-[3-(нафталін-1-сульфонілметил)-4нітро-фенокси]-пропан-1-олу (12,9г, 32,1ммоль), p-толуолсульфонілхлориду (24,6г, 129ммоль) та триетиламіну (37мл, 270ммоль) у метиленхлориді (300мл) перемішували при навколишній температурі в атмосфері азоту. Через 2 години додавали другу частину p-толуолсульфонілхлориду (12,1г, 63,5ммоль). Реакційну суміш перемішували ще протягом 2 годин, а потім концентрували. Залишок розподіляли між метиленхлоридом та водним розчином бікарбонату натрію. Органічну фазу промивали сольовим розчином, висушували безводним сульфатом магнію, фільтрували й концентрували. Залишок очищали шляхом флеш хроматографії з 20-50% етилацетатом у гексані, 100% етилацетатом, а потім 100% метиленхлоридом (через обмежену розчинність). У вигляді жовтої твердої речовини (13,0г, 73,0%) одержували 2-[3-(нафталін-1-сульфонілметил)-4-нітрофенокси]-пропіловий естер толуол-4сульфонової кислоти: Т.пл.: 162-4°C; Мас-спектр (-EI, [M-H]-) m/z 554. 1H ЯМР (500MГц, DMSO-d6): δ8,52-8,54 (m, 1H), 8,31 (d, 1H, J=8,18Гц), 8,098,11 (m, 1H), 7,97-8,00 (m, 2H), 7,62-7,73 (m, 5H), 7,35 (d, 2H, J=7,93Гц), 6,92 (dd, 1H, J=9,15Гц та 2,81Гц), 6,73 (d, 1H, J=2,80Гц), 5,22 (s, 2H), 4,09 (t, 2H, J=5,98Гц), 3,79-3,82 (m, 2H), 2,29 (s, 3H), 1,911,97 ppm (m, 2H). Елементний аналіз для C27H25NO8S2: Розраховано: C, 58,37; H, 4,54; N, 2,52; Виявлено: C, 58,13; H, 4,43; N, 2,41. Етап 5 TosO O THF/EtOH 10 % Pd/C O TosO O O S O NO2 S O NH2 53 94053 54 vacuo протягом 20 хвилин для одержання на виході 3-[4-аміно-3-(нафталін-1-сульфонілметил)фенокси]-пропілового естеру толуол-4сульфонової кислоти у вигляді буро-зеленої напівтвердої речовини (0,627г, 84,4%). Мас-спектр (+EI, [M+H]+) m/z 526. 1H ЯМР (500MГц, DMSOd6): δ8,61 (d, 1H, J=8,42Гц), 8,25 (d, 1H, J=8,17Гц), 8,02-8,07 (m, 2H), 7,59-7,72 (m, 5H), 7,39 (d, 2H, J=7,93Гц), 6,56 (d, 1H, J=8,17Гц), 6,44-6,47 (m, 1H), 6,01 (d, 1H, J=2,81Гц), 4,62 (s, 2H), 3,984,01(m, 2H), 3,36-3,39 (m, 2H), 2,35 (s, 3H), 1,711,79 ppm (m, 2H). 3-[4-аміно-3-(нафталін-1-сульфонілметил)фенокси]-пропіловий естер толуол-4сульфонової кислоти Етанол (30мл) та 10% паладій на вугіллі (0,439г) додавали до гарячого розчину 2-[3(нафталін-1-сульфонілметил)-4-нітро-фенокси]пропілового естеру толуол-4-сульфонової кислоти (0,785г, 1,41ммоль) у гарячому безводному THF (40мл). Реакційну суміш гідрогенізували на апараті Парра протягом 2 годин (початковий тиск 43 psi). Потім реакційну суміш фільтрували над целітом і концентрували. Висушували при 75°C in Етап 6 O TosO O iPrOH/HCl NaNO2 S O O O S O NH2 3-[3-(нафталін-1-сульфоніл)-1H-індазол-5ілокси]-пропіловий естер толуол-4-сульфонової кислоти Ізопропанол (205мл) та 1,0N хлористоводневу кислоту (200мл) додавали до 3-[4-аміно-3(нафталін-1-сульфонілметил)-фенокси]пропілового естеру толуол-4-сульфонової кислоти (8,1г, 15ммоль). Реакційну суміш нагрівали через обмежену розчинність. Після цього додавали нітрит натрію (1,6г, 2,3ммоль) у воді (22мл). Для підвищення розчинності до реакційної суміші ще додавали ізопропанол (100мл). Після перемішування при навколишній температурі протягом 1 години додавали карбонат натрію до основного рівня pH. Цю реакційну суміш після цього перемішували при навколишній температурі протягом 30 хвилин. Після концентрування залишок розподіляли між етилацетатом та водою. Органічну фазу після цього промивали сольовим розчином, O O S O N N H висушували безводним сульфатом магнію, фільтрували й концентрували. Залишок очищали шляхом флеш-хроматографії з застосуванням 50% етилацетату в гексані. У вигляді світлобурштинової напівтвердої речовини (3,3г, 41%) одержували 3-[3-(нафталін-1-сульфоніл)-1Hіндазол-5-ілокси]-пропіловий естер толуол-4сульфонової кислоти. Мас-спектр (-EI, [M-H]-) m/z 535. 1H ЯМР (500MГц, DMSO-d6): δ14,08(s, 1H), 8,78 (d, 1H, J=8,78Гц), 8,55 (dd, 1H, J=7,44Гц та 1,22Гц), 8,28 (d, 1H, J=8,17Гц), 8,02-8,04 (m, 1H), 7,73-7,77 (m, 1H), 7,55-7,65 (m, 4H), 7,48 (d, 1H, J=9,15Гц), 7,03-7,06 (m, 3H), 6,88-6,91 (m, 1H), 4,17 (t, 2H, J=5,98Гц), 3,85-3,88 (m, 2H), 2,00-2,03 (m, 2H), 1,97 ppm (s, 3H). Елементний аналіз для C27H24N2O6S2. 0,10моль H2O: Розраховано: C, 60,23; H, 4,53; N, 5,20; Виявл.: C, 59,92; H, 4,30; N, 5,17. Етап 7 O O S O O O S O MeNH2/THF N O O S O N N H Диметил-{3-[3-(нафталін-1-сульфоніл)-1Hіндазол-5-ілокси]-пропіл}-амін Розчин 3-[3-(нафталін-1-сульфоніл)-1Hіндазол-5-ілокси]-пропілового естеру толуол-4сульфонової кислоти (1,02г, 1,89ммоль) у 2,0M диметиламіну у THF (20мл, 40ммоль) перемішували протягом 16 годин при 70°C у герметично закритій пробірці. Після охолодження до навколишньої температури реакційну суміш концентрували і розподіляли між хлороформом та водним розчином бікарбонату натрію. Органічну фазу промивали сольовим розчином, висушували безводним сульфатом магнію, фільтрували й концентрували. Залишок очищали шляхом флешхроматографії з застосуванням 0,5% гідроксиду амонію/5,0% метанолу в хлороформі. Одержува N N H ли диметил-{3-[3-(нафталін-1-сульфоніл)-1Hіндазол-5-ілокси]-пропіл}-амін у вигляді світложовтої твердої речовини (0,453г, 58,5%). Потім до цієї сполуки додавали метанол та етерний гідрохлорид. Одержаний в результаті розчин концентрували й висушували протягом 14 годин при 84°C in vacuo. Одержували диметил-{3-[3-(нафталін-1сульфоніл)-1H-індазол-5-ілокси]-пропіл}амінгідрохлорид у вигляді дуже світлої жовтої твердої речовини (0,455г): Т.пл.: 264-5°C; Масспектр (-EI, [M-H]-) m/z 408. 1H ЯМР (500MГц, DMSO-d6): δ14,17(s, 1H), 10,19 (s, 1H), 8,75 (d, 1H, J=8,67Гц), 8,53 (dd, 1H, J=7,44Гц та 1,22Гц), 8,27 (d, 1H, J=8,30Гц), 8,02-8,04 (m, 1H), 7,71-7,75 (m, 1H), 7,54- 7,65 (m, 3H), 7,29 (d, 1H, J=2,08Гц), 7,07-7,10 (m, 1H), 4,07-4,10 (m, 2H), 3,19-3,23 (m, 55 94053 2H), 2,76 (s, 6H), 2,11-2,18 ppm (m, 2H). Елементний аналіз для C22H23N3O3S · 1,00моль HCl: Роз 56 раховано: C, 59,25; H, 5,42; N, 9,42; Виявлено: C, 58,97; H, 5,58; N, 9,23. Приклад 15 O O S O O O S O MeNH2/THF H N O O S O N N N H N H Метил-{3-[3-(нафталін-1-сульфоніл)-1Hіндазол-5-ілокси]-пропіл}-амін Розчин 3-[3-(нафталін-1-сульфоніл)-1Hіндазол-5-ілокси]-пропілового естеру толуол-4сульфонової кислоти (0,422г, 0,786ммоль) у 2,0M метиламіну у THF (8,0мл, 16ммоль) перемішували протягом 15 годин при 70°C у герметично закритій пробірці. Після охолодження до навколишньої температури реакційну суміш концентрували й розподіляли між етилацетатом та водним розчином бікарбонату натрію. Органічну фазу промивали сольовим розчином. Водні фази екстрагували хлороформом і обидві органічні фази комбінували й висушували безводним сульфатом магнію, фільтрували й концентрували. Залишок очищали шляхом флеш-хроматографії з застосуванням 0,75% гідроксиду амонію/7,5% метанолу в хлороформі. Метил-{3-[3-(нафталін-1-сульфоніл) 1H-індазол-5-ілокси]-пропіл}-амін одержували у вигляді світло-жовтої піни (0,209г, 67,2%). До сполуки додавали метанол та етерний гідрохлорид. Одержаний в результаті розчин концентрували і висушували протягом 14 годин при 84°C in vacuo. Гідрохлорид одержували у вигляді світложовтої піни (0,217г). Мас-спектр (-EI, [M-H]-) m/z 394, 1H ЯМР (500MГц, DMSO-d6): δ14,16 (s, 1H), 8,74-8,76 (m, 1H), 8,67 (s, br, 2H), 8,52 (dd, 1H, J=7,44Гц та 1,22Гц), 8,27 (d, 1H, J=8,30Гц), 8,028,05 (m, 1H), 7,70-7,75 (m, 1H), 7,54-7,65 (m, 3H), 7,29 (d, 1H, J=2,19Гц), 7,08-7,11 (m, 1H), 4,09 (t, 2H, J=5,98Гц), 3,05 (s, br, 2H), 2,55 (s, 3H), 2,052,11 ppm (m, 2H). Елементний аналіз для C21H21N3O3S ·1,00моль HCl·0,45моль H2O: Розраховано: C, 57,32; H, 5,25; N, 9,55; Виявлено: C, 57,64; H, 5,33; N, 9,39. Приклад 16 O O S O O S O O EtNH2/THF H N O O S O N N N H N H Етил-{3-[3-(нафталін-1-сульфоніл)-1Hіндазол-5-ілокси]-пропіл}-амін Розчин 3-[3-(нафталін-1-сульфоніл)-1Hіндазол-5-ілокси]-пропілового естеру толуол-4сульфонової кислоти (0,080мг, 0,15ммоль) у 10мл 2,0M етиламіну/THF (20ммоль) перемішували при 90°C протягом приблизно 2 годин у герметично закритій пробірці. Після охолодження до навколишньої температури реакційну суміш піддавали випарюванню розчинника. Розчиняли в етилацетаті і двічі промивали водним розчином бікарбонату натрію. Органічну фазу висушували над безводним сульфатом магнію, фільтрували й концентрували. Залишок очищали шляхом флешхроматографії з застосуванням 0,75% гідроксиду амонію/7,5% метанолу в хлороформі. Висушування при 66°C in vacuo протягом 20 хвилин забезпечувало на виході етил-{3-[3-(нафталін-1 сульфоніл)-1H-індазол-5-ілокси]-пропіл}-амін у вигляді світло-жовтої піни (43,0мг, 70,0%). Його розчиняли у метанолі й додавали етерний гідрохлорид. Концентрування й висушування у вакуумі при 83°C протягом 16 годин забезпечували гідрохлорид у вигляді блідо-жовтої напівтвердої речовини (41,7мг, 62,3%). Мас-спектр (+EI, [M+H]+) m/z 410; 1H ЯМР (500MГц, DMSO-d6): δ14,14-14,18 (br, 1H), 8,74-8,76 (m, 1H), 8,56-8,72 (br, 2H), 8,52 (dd, 1h, J=7,44Гц та 1,22Гц), 8,27 (d, 1H, J=8,29Гц), 8,03-8,05 (m, 1H), 7,71- 7,75 (m, 1H), 7,54-7,65 (m, 3H), 7,29 (d, 1H, J=2,08Гц), 7,07-7,10 (m, 1H), 4,09-4,12 (m, 2H), 3,03-3,07 (m, 2H), 2,902,97 (m, 2H), 2,05-2,12 (m, 2H), 1,15-1,19 ppm (m, 3H). Елементний аналіз для C22H23N3O3S . 1,00моль HCl·1.20моль H2O: Розраховано: C, 56,51; H, 5,69; N, 8,99; Виявлено: C, 56,20; H, 5,36; N, 8,81. Приклад 17 O O S O O O S O EtMeNH/THF N O O S O N N N H N H 57 94053 Етил-метил-{3-[3-(нафталін-1-сульфоніл)-1Hіндазол-5-ілокси]-пропіл}-амін Розчин 3-[3-(нафталін-1-сульфоніл)-1Hіндазол-5-ілокси]-пропілового естеру толуол-4сульфонової кислоти (0,080мг, 0,15ммоль) та метилетиламіну (0,45-0.75ммоль) перемішували при 90°C протягом приблизно 2 годин у герметично закритій пробірці. Після охолодження до навколишньої температури реакційну суміш піддавали випарюванню розчинника. Розчиняли в етилацетаті і двічі промивали водним розчином бікарбонату натрію. Органічну фазу висушували над безводним сульфатом магнію, фільтрували й концентрували. Залишок розчиняли у метанолі і додавали етерний гідрохлорид. Після цього суміш концентрували й висушували протягом 29 58 80°C in vacuo. Етил-метил-{3-[3-(нафталін-1сульфоніл)-1H-індазол-5-ілокси]-пропіл}амінгідрохлорид одержували у вигляді жовтобурої напівтвердої речовини (53,2мг, 77,1%); + 1 Мас-спектр (+EI, [M+H] ) m/z 424. H ЯМР (500MГц, DMSO-d6): δ14,14-14,17 (br, 1H), 9,719,77 (br, 1H), 8,74-8,76 (m, 1H), 8,52 (dd, 1H, J=7,44Гц та 1,22Гц), 8,27 (d, 1H, J=8,30Гц), 8,038,05 (m, 1H), 7,70-7,74 (m, 1H), 7,56-7,64 (m, 3H), 7,29 (d, 1H, J=2,19Гц), 7,08-7,10 (m, 1H), 4,08-4,11 (m, 2H), 3,04-3,25 (m, 2H), 2,72 (s, 3H), 1,18-1,21 ppm (m, 3H). Елементний аналіз для C23H25N3O3S ·1,00моль HCl·0,90моль H2O: Розраховано: C, 58,01; H, 5,88; N, 8,82; Виявлено: C, 58,37; H, 5,55; N, 8,50. Приклад 18 O O S O O O S O Et2NH/THF N O O S O N N N H N H Діетил-{3-[3-(нафталін-1-сульфоніл)-1Hіндазол-5-ілокси]-пропіл}-амін Розчин 3-[3-(нафталін-1-сульфоніл)-1Hіндазол-5-ілокси]-пропілового естеру толуол-4сульфонової кислоти (0,080мг, 0,15ммоль) та діетиламіну (0,45-0.75ммоль) у THF (10мл) перемішували при 90°C протягом приблизно 2 годин у герметично закритій пробірці. Після охолодження до навколишньої температури реакційну суміш піддавали випарюванню розчинника. Розчиняли в етилацетаті і двічі промивали водним розчином бікарбонату натрію. Органічну фазу висушували над безводним сульфатом магнію, фільтрували й концентрували. Залишок розчиняли у метанолі та хлороформі й додавали етерний гідрохлорид. Суміш концентрували й висушували у вакуумі при 80°C протягом 17 годин. Діетил-{3-[3-(нафталін-1сульфоніл)-1H-індазол-5-ілокси]-пропіл}-амін гідрохлорид одержували у вигляді жовто-бурої піни (69,9мг, 98,3%); Мас-спектр (+EI, [M+H]+) m/z 438. 1 H ЯМР (500MГц, DMSO-d6): δ14,13-14,11 (br, 1H), 9,59-9,63 (br, 1H), 8,75 (d, 1H, J=8,42Гц), 8,51 (dd, 1H, J=7,44Гц та 1,10Гц), 8,27 (d, 1H, J=8,29Гц), 8,03-8,05 (m, 1H), 7,70-7,74 (m, 1H), 7,52-7,64 (m, 3H), 7,05-7,11 (m, 2H), 4,10 (t, 2H, J=5,98Гц), 3,113,25 (m, 6H), 2,09-2,24 (m, 2H), 1,18 ppm (t, 6H, J=7,20Гц). Приклад 19 O O S O O O S O BuNH2/THF H N O O S O N N H Бутил-{3-[3-(нафталін-1-сульфоніл)-1Hіндазол-5-ілокси]-пропіл}-амін Розчин 3-[3-(нафталін-1-сульфоніл)-1Hіндазол-5-ілокси]-пропілового естеру толуол-4сульфонової кислоти (0,080мг, 0,15ммоль) та бутиламіну (0,45-0,75ммоль) у THF (10мл) перемішували при 90°C протягом приблизно 2 годин у герметично закритій пробірці. Після охолодження до навколишньої температури реакційну суміш піддавали випарюванню розчинника. Розчиняли в етилацетаті і двічі промивали водним розчином бікарбонату натрію. Органічну фазу висушували над безводним сульфатом магнію, фільтрували й концентрували. Залишок розчиняли у метанолі і N N H додавали етерний гідрохлорид. Концентрування й висушування у вакуумі при 80°C протягом 17 годин забезпечували бутил-{3-[3-(нафталін-1сульфоніл)-1H-індазол-5-ілокси]-пропіл}-амін гідрохлорид у вигляді світло-оранжевої напівтвердої речовини (43,3мг, 60,9%); Мас-спектр (+EI, [M+H]+) m/z 438. 1H ЯМР (500MГц, DMSO-d6): δ13,8-14,2 (br, 1H), 8,75 (d, 1H, J=8,66Гц), 8,508,52 (m, 1H), 8,27 (d, 1H, J=8,30Гц), 8,03-8,05 (m, 1H), 7,71-7,75 (m, 1H), 7,54-7,64 (m, 3H), 7,29 (d, 1H, J=2,07Гц), 7,07-7,10 (m, 1H), 4,08-4,11 (m, 2H), 3,04- 3,08 (m, 2H), 2,86-2,90 (m, 2H), 2,06-2,13 (m, 2H), 1,52-1,59 (m, 2H), 1,26-1,33 (m, 4H), 0,880,84 ppm (m, 3H). 59 94053 60 Приклад 20 O O S O O S O O N H N NH2 O O S O N THF N H N H Циклопропіл-{3-[3-(нафталін-1-сульфоніл)1H-індазол-5-ілокси]-пропіл}-амін Розчин 3-[3-(нафталін-1-сульфоніл)-1Hіндазол-5-ілокси]-пропілового естеру толуол-4сульфонової кислоти (0,080мг, 0,15ммоль) та циклопропіламіну (0,45-0.75ммоль) у THF (10мл) перемішували при 90°C протягом приблизно 2 годин у герметично закритій пробірці. Після охолодження до навколишньої температури реакційну суміш піддавали випарюванню розчинника. Розчиняли в етилацетаті і двічі промивали водним розчином бікарбонату натрію. Органічну фазу висушували над безводним сульфатом магнію, фільтрували й концентрували. Залишок двічі очищали шляхом флеш-хроматографії з застосуванням 0,75% гідроксиду амонію/7,5% метанолу в хлороформі та 0,5% гідроксиду амонію/5,0% метанолу в хлороформі для одержання циклопро піл-{3-[3-(нафталін-1-сульфоніл)-1H-індазол-5ілокси]-пропіл}-аміну у вигляді прозорої жовтої плівки (51,0мг, 80,7%). Цю сполуку розчиняли у метанолі і додавали етерний гідрохлорид. Концентрування й висушування in vacuo протягом 24 годин при 83°C забезпечували гідрохлорид у вигляді жовтої піни (48,9мг, 71,2%); Мас-спектр (+EI, [M+H]+) m/z 422. 1H ЯМР (500MГц, DMSO-d6): δ14,15 (s, 1H), 9,01 (s, 2H), 8,74-8,76 (m, 1H), 8,518,53 (m, 1H), 8,27 (d, 1H, J=8,29Гц), 8,02-8,05 (m, 1H), 7,71-7,75 (m, 1H), 7,51- 7,65 (m, 3H), 7,29 (d, 1H, J=2,19Гц), 7,08-7,11 (m, 1H), 4,11 (t, 2H, J=6,10Гц), 3,11-3,20 (br, s, 2H), 2,65-2,75 (m, 1H), 2,08-2,15 (m, 2H), 0,83-0,87 (m, 2H), 0,70-0,77 ppm (m, 2H). Елементний аналіз для C23H23N3O3S ·1,00моль HCl·0,70моль H2O: Розраховано: C, 58,70; H, 5,44; N, 8,93; Виявлено: C, 58,70; H, 5,09; N, 8,68. Приклад 21 O O S O O O S O N NH2 H N O S O O N THF N H N H Циклопентил-{3-[3-(нафталін-1-сульфоніл)1H-індазол-5-ілокси]-пропіл}-амін Розчин 3-[3-(нафталін-1-сульфоніл)-1Hіндазол-5-ілокси]-пропілового естеру толуол-4сульфонової кислоти (0,080мг, 0,15ммоль) та циклопентиламіну (0,45-0,75ммоль) у THF (10мл) перемішували при 90°C протягом 2 годин у герметично закритій пробірці. Після охолодження до навколишньої температури реакційну суміш піддавали випарюванню розчинника. Розподіляли в етилацетаті і двічі промивали водним розчином бікарбонату натрію. Органічну фазу висушували над безводним сульфатом магнію, фільтрували й концентрували. Залишок очищали шляхом флешхроматографії з застосуванням 0.75% гідроксиду амонію/7,5% метанолу в хлороформі для одержання циклопентил-{3-[3-(нафталін-1-сульфоніл) 1H-індазол-5-ілокси]-пропіл}-аміну у вигляді бежевої піни (70,6мг, 100%). Цю сполуку розчиняли у метанолі і додавали етерний гідрохлорид. Концентрування й висушування in vacuo протягом 12,5 години при 83°C забезпечували гідрохлорид у вигляді світло-бурої піни (69,7мг, 95,6%); Масспектр (+EI, [M+H]+) m/z 450. 1H ЯМР (500MГц, DMSO-d6): δ14,15-14,21 (br, 1H), 8,70-8,83 (m, 3H), 8,51-8,53 (m, 1H), 8,27 (d, 1H, J=8,30Гц), 8,03-8,05 (m, 1H), 7,71-7,75 (m, 1H), 7,54-7,65 (m, 3H), 7,30 (d, 1H, J=2,20Гц), 7,09 (dd, 1H, J=9,15Гц та 2,31Гц), 4,11 (t, 2H, J=6,10Гц), 3,43- 3,49 (m, 1H), 3,06 (br, s, 2H), 2,05-2,14 (m, 2H), 1,88-1,96 (m, 2H), 1,43-1,71 ppm (m, 6H). Елементний аналіз для C25H27N3O3S ·1,00моль HCl·0,75моль H2O: Розраховано: C, 60,11; H, 5,95; N, 8,41; Виявлено: C, 59,71; H, 5,83; N, 8,25. Приклад 22 O O S O O O S O N N H Ізопропіл-{3-[3-(нафталін-1-сульфоніл)-1Hіндазол-5-ілокси]-пропіл}-амін Розчин 3-[3-(нафталін-1-сульфоніл)-1Hіндазол-5-ілокси]-пропілового естеру толуол-4 NH2 THF H N O O S O N N H сульфонової кислоти (0,080мг, 0,15ммоль) та ізопропіламіну (0,45-0,75ммоль) у THF (10мл) перемішували при 90°C протягом приблизно 2 годин у герметично закритій пробірці. Після охо
ДивитисяДодаткова інформація
Назва патенту англійськоюSubstituted-3-sulfonylindazole derivatives as 5-hydroxytryptamine-6 ligands
Автори англійськоюElokdah Hassan Mahmoud, Greenfield Alexander Alexei, Liu Kevin, Mcdevitt Robert Emmett, Mcfarlane Geraldine Ruth, Grosanu Cristina, Lo Jennifer Rebecca, Li Yanfang, Robichaud Albert Jean, Bernotas Ronald Charles
Назва патенту російськоюЗамещенные производные 3-сульфонилиндазола в качестве лигандов гидрокситриптамина-6
Автори російськоюЭлокдах Хассан Махмуд, Гринфилд Эликзандер Алексей, Лиу Кевин, Макдевитт Роберт Эмметт, Макфарлейн Джералдин Рут, Гросану Кристина, Ло Дженнифер Ребекка, Ли Янфанг, Робишо Альберт Джин, Бернотас Рональд Чарльз
МПК / Мітки
МПК: C07D 413/12, C07D 403/12, C07D 401/12, C07D 231/56
Мітки: похідні, ліганди, заміщені, 5-гідрокситриптаміну-6, 3-сульфоніліндазолу
Код посилання
<a href="https://ua.patents.su/90-94053-zamishheni-pokhidni-3-sulfonilindazolu-yak-ligandi-5-gidroksitriptaminu-6.html" target="_blank" rel="follow" title="База патентів України">Заміщені похідні 3-сульфоніліндазолу як ліганди 5-гідрокситриптаміну-6</a>
Попередній патент: Похідні піридазину
Наступний патент: Похідні нітрокатехолу як комт-інгібітори
Випадковий патент: Багатошаровий пакувальний матеріал












