Сполука n-пара-бромфеніл-3-(уридин-5′-аміно)-сукцинімід, яка має потенційну фізіологічну активність
Формула / Реферат
Сполука N-пара-бромфеніл-3-(уридин-5'-аміно)-сукцинімід, яка має потенційну фізіологічну активність, загальної формули:
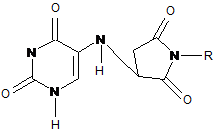 .
.
Текст
Реферат: Сполука N-пара-бромфеніл-3-(уридин-5'-аміно)-сукцинімід активність. має потенційну фізіологічну UA 76762 U (54) СПОЛУКА N-ПАРА-БРОМФЕНІЛ-3-(УРИДИН-5'-АМІНО)-СУКЦИНІМІД, ЯКА МАЄ ПОТЕНЦІЙНУ ФІЗІОЛОГІЧНУ АКТИВНІСТЬ UA 76762 U UA 76762 U 5 10 15 20 25 30 Корисна модель належить до медицини, а саме до нейрофармакології. Сполука N-пара-бромфеніл-3-(уридин-5'-аміно)-сукцинімід (далі, сполука), належить до середньотоксичних та протисудомної активності не проявляє, але потенціює судомні ефекти у лабораторних тварин, які виникають в наслідок дії коразолу. Велика кількість похідних малеїнімідів на даний момент є відомими лікарськими засобами, що активно застосовуються в медицині завдяки їх високій фізіологічній активності [1, 2, 3]. Етосуксімід слугує препаратом першого ряду при малих та моноклонічних приступах епілепсії. Має захисну дію при міоклонічних нападах генералізованої епілепсії, у тому числі і при вроджених формах, якщо вони не пов'язані зі структурними аномаліями мозку. При інших формах епілепсії препарат не ефективний. Окрім цього, препарат має іще й анальгізуючу дію, при невралгії трійчастого нерву, але цією ефективністю він поступається карбамазепіну. Для усіх препаратів цієї групи характерні такі побічні прояви: порушення функції ШКТ (біль, розлади травлення), ЦНС (у вигляді дискенизії), алергічні реакції з еозинофілією та іншими порушеннями крові, а також червоний вовчак. Препарати цієї групи пригнічують моторні центри кори великого мозку і підвищують судомний поріг. Впливу на концентрацію ГАМК в мозку вони в терапевтичних дозах не мають [3]. Іміди бурштинової кислоти (2,5-піролідиндіони) здатні відновлювати обмінні процеси в центрах кори головного мозку і особливо в підкоркових ядрах, нормалізувати їх функції. Тому ці препарати часто використовують з вальпроатом натрію, для підвищення ефективності останнього. Необхідно зазначити, що сумісне використання цих двох препаратів призводить до збільшення рівня сукцимідів у крові. Останнім часом окрім антиконвульсивної дії у імідів ненасичених карбонових кислот було виявлено психотропну активність (слабкий стимулюючий ефект), α-заміщені амінокротонові ефіри характеризуються слабким ефектом типу антидепресантів [4]. Описано [5], що N-алкілмалеїніміди можуть виконувати роль інгібіторів нітрифікації амонійних сполук із сечі, а N-етилмалеїніміди мають потенційну здатність контролювати процес розвитку зубного карієсу [6]. N(арил/алкіл)-малеїніміди були отримані в реакції малеїнового ангідриду і N(арил/алкіл)-амінів. Була досліджена їх антимікробна активність. N(арил/алкіл)-малеїніміди проявляли антибактеріальну активність по відношенню до грампозитивних бактерій таких як: Bacillus subtilis і Staphylococcus aureus. Майже всі виявляли антибактеріальну активність до грамнегативних бактерій таких як: Kscherichia colі, але були неактивні до Pseudomonas acriginosa. Всі N-(арил/алкіл)-малеїніміди проявляли активність до дріжджових і міцелійних грибів [7]. Антиалергічна дія та імунотерапевтична активність описана для похідних малеїнімідів -біс(індоліл)малеїнімідів [8, 9]: R4 O N O R3 R5 R6 N R2 35 R1 . Протимікробна дія знайдена у N-(діалкілфеніл)-малеїнімідів та N[-(аріл/алкіл)-малеїнімідів [7, 10]. Авторами роботи [11] описана фізіологічна дія похідних малеїнімідів – 1,3-діоксо-4фенілпіроло-(3,4-е)карбазолів загальної формули: O H N O R N H 40 як кардіоваскулярних агентів. Крім того, деякі з них потенціюють інгібіторів протеїнкінази. В роботах [12, 13] представлено нові похідні малеїнімідів, які мають противиразкову та антиішемічну активність: 1 UA 76762 U O [ SOD ] N S W COOH O 2 5 10 15 20 25 30 35 . Раніше нами були отримані інші нові гетероциклічні похідні малеїнімідів з потенційними фізіологічними властивостями шляхом нуклеофільного приєднання по подвійному зв'язку [14, 15]. Структурні аналоги вищевказаного продукту реакції між N-пара-бромфенілмалеїнімідом та 5-аміноурацилом з потенційними фізіологічними властивостями на сьогодні не відомі (літературний опис відсутній). В основу корисної моделі поставлено задачу, що полягає у дослідженні токсичності сполуки N-пара-бромфеніл-3-(уридин-5'-аміно)-сукцинімід (далі сполука) під час вивчення її протисудомної активності після підшкірного введення до організму лабораторних тварин коразолу. Сполука, яка має потенційну фізіологічну активність, отримана шляхом взаємодії Nпapa-бромфенілмалеїніміду та 5-аміноурацилу у молярному співвідношенні 1:1. Реакції проводилися у системі розчинників (вода - ізопропіловий спирт, 1:1,5) при постійному нагріванні та перемішуванні реакційної суміші 12-14 год. для забезпечення отримання сполуки, яка має потенційну фізіологічну активність. Експерименти щодо вивчення токсичності сполуки під час вивчення її протисудомної активності проведені на білих нелінійних мишах з масою тіла 222 г. Кількість лабораторних тварин - 6. Сполука, розчинена у фізіологічному розчині, вводилася одноразово, підшкірно. Сполука у вигляді фізіологічного розчину вводилася за 30 хвилин до введення коразолу. Критерієм оцінки токсичності вважався відсоток загибелі лабораторних тварин, критерієм протисудомної активності - відсоток гальмування судомних ефектів у лабораторних тварин після введення коразолу. Вивчення параметрів токсичності проводилось у дослідах на білих нелінійних мишах. Результати досліду обраховувались у альтернативній формі на 14 добу після введення. Статистична обробка проведена по В.Б. Прозоровскому та ін. [16]. Експерименти показали, що сполука належить до середньотоксичних сполук, ЛД 50 її становить 708 (620-800) мг/кг (див.таблицю). У 83-100 % лабораторних тварин розвивалися судомні ефекти після введення фізіологічного розчину досліджуваної сполука, а потім через 30 хв. - коразолу, що свідчить про відсутність у неї протисудомної активності. При введенні фізіологічного розчину досліджуваної сполуки до організму лабораторних тварин зареєстровано відсоток загибелі тварин - 17 %. Таким чином, можна зробити висновок, що сполука належить до середньотоксичних та не проявляє протисудомну активність, а навпаки, потенціює судомну дію коразолу. Однак, сполука може бути перспективною як потенційно фізіологічно активна з метою подальшого вивчення її можливих фізіологічних властивостей. У таблиці наведено параметри токсичності та фізіологічної активності сполуки N-парабромфеніл-3 -(уридин-5'-аміно)-сукцинімід, загального формули: ФОРМУЛА КОРИСНОЇ МОДЕЛІ 40 Сполука N-пара-бромфеніл-3-(уридин-5'-аміно)-сукцинімід, яка має потенційну фізіологічну активність, загальної формули: O O N N N R H O N H O . 2 UA 76762 U O O N N N R H O N O H Таблиця Назва сполуки Шлях введення Кількість лабораторних тварин (білі нелінійні миші) ЛД50 (миші, мг/кг) Протисудомна активність N-пара-бром-феніл-3 (уридин-5'-аміно)сукцинімід підшкірно 6 708 (620-800) Відсутня. Потенціює судомні ефекти Таким чином, сполука, що заявляється належить до середньотоксичних, ЛД 50 її становить 708 (620-800) мг/кг та не проявляє протисудомну активність, а навпаки, потенціює судомні ефекти, які виникають після введення коразолу. Однак, сполука може бути перспективною як потенційно фізіологічно активна для подальшого вивчення її можливих фізіологічних властивостей. Вивчення токсичності під час дослідження протисудомної активності сполуки N-парабромфеніл-3-(уридин-5'-аміно)-сукцинімід проводилося у відділі нейрофармакології Інституту фармакології та токсикології НАМИ України. Джерела інформації: 1. Фармакотерапия эпилепсии у детей и клиническая фармакология противоэпилептических средств. - Л.-1988.-20с. 2. Эди М.Ж. Противосудорожная терапия / М.Ж. Эди, Д.Х.Тайрер. - М.: Медицина, 1983.-С.143163. 3. Машковський М.Д. Лекарственные средства / М.Д. Машковський. - М.: Новая волна, 2006.1200 с. 4. Лулукян К.К. О влиянии N-заместителей в малеимидах на направление реакции с енаминами / К.К. Лулукян, Р.Т. Григорян, С.Г. Агбалян / Арм. хим. журн.-1982. - Т. 35, № 12. - С. 780-785. 5. Shimizu Toshio. Five-membered ring heterocyclic compounds / Toshio Shimizu // Chem. Abstr.2008. - Vol. 104. - P. 448. 6. Watanabe S. Antimicrobial activity of some N-(arylalkyl)-maleimides / S. Watanabe, Y. Igarashi, K. Yagami // Chem. Abstr.-1992. - Vol. 116. - P. 190904g. 7. Watanabe S. Biological activities of N-(alkylphenyl)-maleimides / S. Watanabe, Y. Igarashi, K. Yagami et al. // Chem. Abstr.-1992. - Vol. 116. - P. 190904g. 8. Schultz M. Preparation of 4-(3-indolyl)maleimides as antiallergics and immunotherapeutic agents / M. Schultz, C. Tsaklakidis, R. Haag et al. // Chem. Abstr.-1991.-Vol. 115.-P. 848. 9. Tsaklakidis С Preparation of bis(indolyl)maleimides and analogs as antiallergics and for use in immune diseases / С Tsaklakidis, M. Schultz, R. Haag et al. // Chem. Abstr. - 1991.-Vol. 115.-P. 931. 10. Wolfbeis O. Heterocyclicles reagents / O. Wolfbeis, S. Liebigs // Ann. Chem.-1982. -Vol. 25, N1.P. 182-189. 11. Kleinschorth J. Preparation of l, 3-dioxo-4-phenylpyrrolo[3,4-c]carbozoles and analogs as cardiovascular agents / J. Kleinschorth, J. Hartenstein et al. // Chem. Abstr.-1990. -Vol. 113.-P. 191154η. 12. Massayasu I. Preparation of N-carboxyalkylsuccinimide derivatives of superoxide dismutase for pharmaceutical use /1. Massayasu, J. Ebashi, T. Tkigawo // Chem. Abstr. - 1993.-Vol. 118.-P. 55129. 13. Ebata I. Preparation of maleimide long-chain carboxylic acids /1. Ebata, T. Takigawa et al. // Chem. Abstr.-1993. - Vol. 118. - P. 254741c. 14. Ошовский Г.В., Толмачев Φ.Φ., Меркулов А.С, Пинчук A.M. Тиадиазолилфосфины с азотсодержащими заместителями.// ХГС - 1997.- № 10, С. 1422-1424. 3 UA 76762 U 15. Вельчинська О.В., Кузьменко І.Й., Драпайло А.Б. Синтез нових похідних заміщених малеїнімідів як потенційних фізіологічно активних агентів. Тези. доп. XVIII-оїУкр.конф.з орг.хімії. 1998. Дніпропетровськ, с.369. 16. Прозоровский В.Б. Экспресс метод определения средней эффективности дозы и ее ошибки / В.Б. Прозоровский, В.П. Прозоровский, В.М. Демченко // Фармакол. и токсикол.-1978. - Т. 41, № 4. - С. 407-509. Комп’ютерна верстка Г. Паяльніков Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 4
ДивитисяДодаткова інформація
Назва патенту англійськоюCompound n-para-bromophenyl-3-(uridine-5'-amino)-succinimide having potential physiological activity
Автори англійськоюVelchynska Olena Vasylivna
Назва патенту російськоюСоединение n-пара-бромфенил-3-(уридин-5'-амино)-сукцинимид, которое имеет потенциальную физиологическую активность
Автори російськоюВельчинская Елена Васильевна
МПК / Мітки
МПК: C07C 21/185, C07C 21/18, C07D 239/553, A61K 33/16
Мітки: фізіологічну, сполука, n-пара-бромфеніл-3-(уридин-5'-аміно)-сукцинімід, активність, яка, потенційну, має
Код посилання
<a href="https://ua.patents.su/6-76762-spoluka-n-para-bromfenil-3-uridin-5-amino-sukcinimid-yaka-maeh-potencijjnu-fiziologichnu-aktivnist.html" target="_blank" rel="follow" title="База патентів України">Сполука n-пара-бромфеніл-3-(уридин-5′-аміно)-сукцинімід, яка має потенційну фізіологічну активність</a>
Попередній патент: Сполука n-бензил-3-[5′-(2”-амінотіадіазоліл)дифенілфосфіно]-сукцинімід, яка має потенційну фізіологічну активність
Наступний патент: Спосіб визначення стану гематотестикулярного бар’єру
Випадковий патент: Спосіб рекультивації териконів










