Сполуки n-пара-бромфеніл-3-(уридин-5′-аміно)-сукцинімід та n-пара-бромфеніл-3-(уридин-6′-аміно)-сукцинімід з потенційними фізіологічними властивостями
Номер патенту: 18096
Опубліковано: 16.10.2006
Формула / Реферат
Сполуки N-пара-бромфеніл-3-(уридин-5’-аміно)-сукцинімід та N-пара-бромфеніл-3-(уридин- 6’-аміно)-сукцинімід загальної формули:
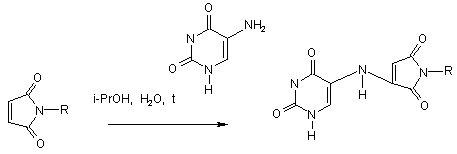 I, II,
I, II,
де R=пара-BrPh,
з потенційними фізіологічними властивостями.
Текст
Сполуки N-пара-бромфеніл-3-(уридин-5’аміно)-сукцинімід та N-пара-бромфеніл-3-(уридин6’-аміно)-сукцинімід загальної формули: 2 3 O O S + 18096 h, ацетон O O S NH NH O O який вступає в реакції заміщення по атому водню при гетеро атомі азоту: Схема 3. O O O O NH + HN S N Br(CH2)4Br R O N S N O O O N R N - вмісні гетероциклічні сполуки менш нуклеофільні, у порівнянні з аліфатичними та ароматичними амінами, але їх нуклеофільність достатня для здійснення реакції Міхаеля [4]. Встановлено, що N-(R-аніліно) малеїніміди при кип’ятінні в спирті з морфоліном, піролідином і піперидином утворюють 3-морфоліл-, 3-піролідилі 3-піперидилпохідні сукциніміду. R1 O N O HN R!H + O C6H4 O N HN C6H4 R R При взаємодії N-заміщених імідів малеїнової кислоти з піперазином у розчинах абсолютного спирту або толуолу утворюються диіміди алкіленбіс-аспарагінової кислоти. Таким чином навіть при проведенні реакції в абсолютному спирті відбувається розкриття імідного ядра. Раніше нами були отримані інші нові гетероциклічні похідні малеїнімідів шляхом нуклеофільного приєднання по подвійному зв’язку [5, 6]. Структурні аналоги продуктів реакції між Nпара-бромфенілмалеїніміду та 5-(6)аміноурацилами з потенційними фізіологічними властивостями насьогодні не відомі (літературний опис відсутній). В основу корисної моделі поставлено хімічну будову молекули сполук N-пара-бромфеніл-3(уридин-5’-аміно)-сукциніміду та N-парабромфеніл-3-(уридин-6’-аміно)-сукциніміду (далі, сполуки І, II) з потенційними фізіологічними властивостями шляхом взаємодії N-парабромфенілмалеїніміду та 5-(6)-аміноурацилами у молярному співвідношенні 1:1. Реакції проводилися у системі розчинників (вода - ізопропіловий спирт, 1:1,5) при постійному нагріванні та перемішуванні реакційної суміші 1214 години з метою забезпечення отримання сполук (І, II) з потенційними фізіологічними властивостями. O NH2 N O O O O N O R i-PrOH, H2O, t 4 O O N N N H O H N H N R O I, II де R=пара-BrPh Варіювання умов проведення реакцій та внесення змін до методики синтезу, а саме: заміна вказаної системи розчинників на систему (вода етиловий спирт, 1:1,5), промивання кінцевих продуктів реакцій під час фільтрування в вакуумі сухим гексаном без перекристалізації дозволили збільшити практичний вихід сполук (І, II) до 50%. Таким чином, можна зробити висновок, що сполуки (І, II) з потенційними фізіологічними властивостями можуть бути перспективними у розробці нових лікарських засобів з проти судомною активністю, з анксіолітичним типом дії; що впливають на постсинаптичні рецептори, психотропних агентів та з іншими типами дії. Методика синтезу N-пара-бромфеніл-3(уридин-5’-аміно)-сукциніміду (І). До гарячого розчину 0,5г N-парабромфенілмалеїніміду (0,0019моль) в 50мл ізопропілового спирту додають по краплях розчин 0,3г (0,002моль) 5-аміноурацилу в 450мл суміші вода ізопропіловий спирт (1:1,5), перемішують реакційну суміш при кипінні 14 годин, при цьому її забарвлення стає світло-коричневим та випадає осад світло-гірчичного кольору. Залишають реакційну суміш охолоджуватися при кімнатній температурі, фільтрують. Осад промивають сухим гексаном, сушать на повітрі. Практичний вихід 0,39г (44%). Т. топл. 270-275 С. C14H11N4O4Br. Методика синтезу N-пара-бромфеніл-3(уридин-6’-аміно)-сукциніміду (ІI). До гарячого розчину 0,5г N-парабромфенілмалеїніміду (0,0019моль) в 50мл ізопропілового спирту додають по краплях розчин 0,3г (0,002моль) 6-аміноурацилу в 450мл суміші вода ізопропіловий спирт (1:1,5), перемішують реакційну суміш при кипінні 14 годин, при цьому її забарвлення стає світло-коричневим та випадає осад темно-гірчичного кольору. Залишають реакційну суміш охолоджуватися при кімнатній температурі, фільтрують. Осад промивають сухим гексаном, сушать на повітрі. Практичний вихід 0,445г (50%). Т. топл. 273-276 С. C14H11N4O4Br. Індивідуальність сполук (І, II) контролювали методом тонкошарової хроматографії, склад підтверджували даними елементного аналізу. УФ - спектри сполук (І, II) записували на спектрофотометрі Mel Temp II (USA). ІЧ - спектри записували на спектрофотометрі UR-20 (виробник «Charles Ceise Неnа», Germany). Спектри ПМР сполук (І, II) записували на приладах „Bruker WP-200” (виробник „Bruker”, Switzerland), „Varian T-60” (виробник „Varian”, USA) з робочою частотою 200-132МГц у виді розчинів ДМСО-D6 (внутрішні стандарти ТМС та ГМДС). ТШХ виконували на пластинах Silufol-254. ГРХ визначали на газорідинному хроматографі «Perkin Еlmer» з УФ-детектором (виробник «Perkin», Germany). Хроматограма, ІЧ-, ПМР - спектри сполук (І, II) ідентифікували у порівнянні з хроматограмами, УФ-, ІЧ-, ПМР - спектрами вихідних сполук. Синтезовані сполуки (І, II) - це кристалічний порошки від світло- до темно-гірчичного кольору, ізолюються без кристалізації, з метою очистки 5 18096 6 промиваються сухим гексаном. результаті високої інтенсивності смугу зв’язку С-Вr Дані елементного аналізу на С, Н, N сполук (І, при 505-550см-1, хоча цінність даної ідентифікації II) відповідають розрахованим значенням. обмежена, оскільки присутність брому в молекулах УФ - спектри сполук (І, II) характеризуються задоводиться за допомогою якісних реакцій. Співвідношення інтегральних інтенсивностей гальним показником - наявністю mах, положення сигналів в ПМР - спектрах сполук (І, II) підтверджує яких коливаються в широкому інтервалі від 218 до відсутність протонів первинної групи (-NH2) при 267нм у зв’язку із спряженням фрагменту молеку6,14м.д. в молекулі, спостерігається сигнал у вили заміщеного урацилу з додатковими хромофогляді синглету при 5,098-5,196м.д. протону вторами -N-фенілзаміщеним циклом малеїніміду з ринної групи (-NH-). Сигнали протонів при N (1) та групами С=O та вторинною аміногрупою. N (3) молекул урацилу ідентифікуються в області IЧ - спектри сполук (І, II) смуги NH спостері10,307 та 11,247м.д. у вигляді синглетів (креслен1 гаються в області 1450, 1490, 1540см- . Валентні ня). коливання групи (С=О) проявляються високоінтенВіднесення сигналів в УФ -, IЧ-, ПМР-спектрах, -1 сивним максимумом в області 1660-1750см та є дані елементного аналізу сполук (І, II) наведено в найбільш характеристичними, оскільки інші сигнатаблиці . ли в цій області практично відсутні. Крім того, в низькочастотній області спектрів легко визначити в Таблиця 1 Віднесення сигналів в УФ -, IЧ-, ПМР-спектрах, дані елементного аналізу сполук (І, II). УФ-спектр ІЧ-спектр (KBr), max, EtOH, см-1, нм 43,85 3,2 13,82 44,23 3,18 14,7 218, 252, 267 505-550 (-Br),600-900 (C-H, Ph), 1490 (-NH-), 1660,1710, 1750 (C=О) 43,85 3,2 13,82 44,23 3,18 14,7 218, 252, 267 505-550 (-Br), 600-900 (C-H, Ph), 1490 (-NH-), 1660, 1710, 1750 (C=О) Спо- Знайдено, у% Знайдено, у % лука СНN СНN І II Таким чином, можна зробити висновок, що сполуки (І, II) з потенційними фізіологічними властивостями можуть бути перспективними у розробці нових лікарських засобів з проти судомною активністю, з анксіолітичним типом дії; що впливають на постсинаптичні рецептори, психотропних агентів та з іншими типами дії. Завданням корисної моделі є опис хімічної будови нових сполук: N-пара-бромфеніл-3-(уридин5’-аміно)-сукцинімід та N-пара-бромфеніл-3(уридин-6’-аміно)- сукцинімід, які можуть бути фізіологічно активними за рахунок наявності в будові фрагменту молекули циклічного іміду. Література: 1. Magid Abou - Gharbia, Usha R. Patel and all. //J. Med. Chem.- 1988. -Vol.31, №7. -P.1382-1385. 2. Richards M.N. (Merrel D., Res. Inst. 67084, Спектр ПМР (ДМСО-D6), , м.д. (J, Гц) 2,716,3.180 (с., с., -СН2-, 2Н), 4,509 (с., HCN, 1Н), 5,106 (д., N Н, 1Н), 6,66 (с., С(5)Н, 1Н), 7,259, 7,723 (с., с., Ph, 4Н), 10,307 (с., N(3)H, 1H), 11,247 (с., N(1)H, 1Н) 2,716, 3,180 (с., с., -СН2-, 2Н), 4,509 (с., HCN, 1Н), 5,106 (д., NH, 1Н), 6,78 (с., С(6)Н, 1Н), 7,260, 7,725 (с., с., Ph, 4H), 10,310 (с., N(3)H, 1H), 11,249 (с., Strasbourg, Fr.) //J. Pharmacol. Exp. Ther. -1990. 255(1). -P.83-89. 3. Amagat P. //Traite de Chemie Organique. 1941. -Vol.13. -P.502-521. 4. Лулукян К.К., Агбалян С. Г. //Армянский химический журнал. -1987. -т.40, №5. -С.296-312. 5. Вельчинская Е.В., Кузьменко И.Й., Кулик Л.С. Синтез новых производных замещенных урацилов и пиримидинов. //Химикофармацевтический журнал. Росс. Федерация. 1999.- №3.- С.40-42. 6. Вельчинська О.В., Кузьменко І.Й., Драпайло А.Б. Синтез нових похідних заміщених малеїнімідів як потенційних фізіологічно активних агентів. Тези. доп. XVIII-ої Укр. конф. з орг. хімії. 1998. Дніпропетровськ, с.369. 7 Комп’ютерна верстка Л.Литвиненко 18096 8 Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюCompounds of n-para-bromphenyl-3-(uridine-5'-amino)-succinimide and n-para-bromphenyl-3-(uridine- 6'-amino)-succinimide with potential physiological properties
Автори англійськоюHubskyi Yurii Ivanovych, Velchynska Olena Vasylivna
Назва патенту російськоюСоединения n-пара-бромфенил-3-(уридин-5'-амино)-сукцинимид и n-пара-бромфенил-3-(уридин- 6'-амино)-сукцинимид с потенциальными физиологическими свойствами
Автори російськоюГубский Юрий Иванович, Вельчинская Елена Васильевна
МПК / Мітки
МПК: A61K 33/16, C07C 21/00, C07D 239/553
Мітки: потенційними, фізіологічними, n-пара-бромфеніл-3-(уридин-5'-аміно)-сукцинімід, сполуки, властивостями, n-пара-бромфеніл-3-(уридин-6'-аміно)-сукцинімід
Код посилання
<a href="https://ua.patents.su/4-18096-spoluki-n-para-bromfenil-3-uridin-5-amino-sukcinimid-ta-n-para-bromfenil-3-uridin-6-amino-sukcinimid-z-potencijjnimi-fiziologichnimi-vlastivostyami.html" target="_blank" rel="follow" title="База патентів України">Сполуки n-пара-бромфеніл-3-(уридин-5′-аміно)-сукцинімід та n-пара-бромфеніл-3-(уридин-6′-аміно)-сукцинімід з потенційними фізіологічними властивостями</a>
Попередній патент: Фільтр для очищання газу
Наступний патент: Спосіб отримання речовин з потенційними фізіологічними властивостями
Випадковий патент: Спосіб спалювання природного газу








